Développement de produit dans un contexte règlementaire global

Aptean Food and Beverage PLM Lascom Edition
Introduction
Quel que soit le pays, le cadre réglementaire de l’industrie agroalimentaire ne cesse de se rigidifier et de se renforcer. Les ingrédients, labels, allégations, certifications d’origine ou encore le packaging sont de plus en plus contrôlés. Même si les industriels font preuve de volonté pour aider le consommateur à faire des choix plus éclairés, ils restent confrontés aux différences de réglementations qui peuvent s’opérer d’un territoire à un autre. Un défi qui peut rapidement se transformer en point de blocage.

L’hétérogénéité et l’évolution dans le temps des lois ont des conséquences propres sur chaque étape du processus de développement produit et donc auprès de chaque département de l’entreprise, du Marketing à la Qualité. Et la non conformité d’un produit peut être très coûteuse pour l’entreprise, que ce soit en termes financier ou d’image.
Il est ainsi crucial pour les acteurs de l’agroalimentaire de gérer efficacement l’information produit pour disposer d’une vue complète du processus de développement et détecter au plus tôt les jalons critiques à la mise en conformité. Pour cela, 4 « best practices » 1) Avoir une connaissance des règles de commercialisation 2) Sélectionner la bonne information 3) Se conformer à la réglementation via une approche « by design » 4) Collaborer efficacement avec l’ensemble des parties prenantes externes.
2Livre Blanc | Le Développement Produit dans un Environnement Règlementaire Global
Un Cadre de plus en plus Réglementé
1. Substance réglementées (ingrédients et additifs)
L’ autorisation d’un ingrédient ou d’un additif est strictement connectée à l’appellation du produit fini. Afin d’assurer la conformité vis à vis de la réglementation en vigueur, les étapes suivantes sont recommandées :
› Définir la catégorie de produit;
› Évaluer si tous les ingrédients, y compris les additifs, sont autorisés dans cette catégorie spécifique;
› Appliquer les restrictions, telles que les concentrations maximales.
Les tolérances et limites pour les additifs potentiels et pour les ingrédients peuvent être différentes pour chaque pays où le produit est commercialisé. Il est donc obligatoire pour une entreprise de connaître toutes les contraintes réglementaires associées.
Au sein de l’ UE l’autorisation des additifs est cadrée par le Règlement (UE) 1333/2008. Les ingrédients autorisés sont définis par les législations verticales spécifiques aux catégories de produit. Les produits alimentaires tels que le chocolat, les confitures, les jus de fruits et les conserves de thon sont couvertes par la réglementation de l’UE ou par des directives définissant la composition du produit. Pour les autres catégories de produit, les législations des différents pays s’appliquent.
Les exigences législatives sur les additifs alimentaires sont différentes aux USA et au Canada. Pour l’autorisation des ingrédients des standards fédéraux définissent l’appellation officielle et la composition spécifique de certains produits alimentaires.
Proposition 65 en Californie (CA PROP 65)
La CA PROP 65 est une loi californienne visant à protéger les citoyens contre une liste de produits chimiques connus pour causer des cancers, malformations congénitales et autres troubles reproductifs. Le programme est géré par l’ « Office of Environmental Health Hazard Assessment » (OEHHA) de l’Agence de protection de l’environnement de Californie (CalEPA). L’OEHHA détermine si les produits chimiques remplissent les critères pour être ajouté à la liste CA PROP 65 et gère les exigences sur l’étiquetage, la prévention et le risque d’exposition pour les substances visant à intégrer le marché californien. Cela n’interdit pas la mise en vente de produits contenant des substances dangereuses à tous niveaux. Afin d’aider les professionnels à déterminer si un avertissement est nécessaire ou si les rejets de produits chimiques dans les sources d’eau potable sont interdits, l’OEHHA a développé un « niveau de sécurité » pour plusieurs produits de la CA PROP 65 : « Pas de risque significatif » pour les produits cancérigènes et « Dose Maximale Admissible » pour les produits causant des malformations congénitales ou autres troubles reproductifs selon le degré d’exposition, les sanctions pour le non respect de la CA PROP 65 peuvent atteindre 2,500 $ par infraction et par jour.
3Livre Blanc | Le Développement Produit dans un Environnement Règlementaire Global
10 mg/l
Dioxide de souffre Légumes surgelés
Lactosérum Chocolat
50 mg/kg
Bonnes Pratiques de Fabrication Champignons surgelés: 90 ppm
Chocolat au lait Autorisé, pas de limite, doit être ≤ 14% d’extrait sec pour le lait entier partiellement ou complètement déshydraté, le lait demi ou entièrement écrémé, la crème partiellement ou complètement déshydratée, beurre ou la matière grasse de lait.
Chocolat blanc doit être ≤ 5% (du poids)
Chocolat au lait doit être ≥ 5 % (du poids)
Réglisse Confiseries contenant de l’acide lycyrrhizinique ou son sel d’ammonium
S’il y a un ajout de plante de réglisse Glycyrrhiza glabra ≥ 4 g/kg une mention doit être ajoutée après la liste des ingrédients ou après l’appellation du produit « contient de la réglisse les personnes souffrant d’hypertension devraient éviter la consommation excessive ».
Niveau maximum (% glycyrrhizine): 1,1 pour les chewinggums, 16 pour les bonbons durs et 3,1 pour les bonbons mous. La FDA recommande d’éviter de manger trop de réglisse noire d’un coup; pour information, la réglisse noire peut interagir avec les médicaments, les infusions et compléments alimentaires.
Pas d’avertissement ou de limite pour les aliments, uniquement pour les produits de santé mises en garde, avertissements et contre indications sont donnés pour les femmes enceintes (ex dysfonctionnements rénaux augmentation de la pression sanguine)
4Livre Blanc | Le Développement
Produit dans un Environnement
Règlementaire Global
Exemples de limites réglementaires pour des substances spécifiques dans les denrées alimentaires
Substance Produit EU USA Canada
E160 B Annatto Produits laitiers fermentés aromatisés
Bonnes Pratiques de Fabrication Bonnes Pratiques de Fabrication
Substance EU USA Canada
Produits sans gluten Gluten < 20 ppm Gluten < 20 ppm Gluten < 20 ppm
Produits bio ≥ 95% d’ingrédients bio.
Exceptions : ajout d’eau et de sel.
≥ 95% d’ingrédients bio.
Exceptions : ajout d’eau et de sel.
≥ 95% d’ingrédients bio.
Exceptions : ajout d’eau et de sel.
Produit contenant des OGM
Déclaration obligatoire pour tout ingrédient génétiquement modifié Exceptions : Produits contenant ≤ 0, 9 d’OGM / ingrédient composant le produit, présence accidentelle ou techniquement inévitable.
Législation fédérale pas de déclaration obligatoire si l’ingrédient est génétiquement modifié. Peut varier selon la règlementation de l’Etat.
Pas de déclaration obligatoire si l’ingrédient est génétiquement modifié.
5Livre Blanc | Le Développement Produit
dans
un Environnement Règlementaire Global
Exemples d’exigences réglementaires pour des ingrédients dans des denrées alimentaires spécifiques
2. Étiquetage
› En Europe l’étiquetage alimentaire est régi par le Règlement (UE) 1169/2011, couvrant l’ensemble des catégories de produits alimentaires pré emballés et introduisant de nouvelles exigences spécifiques aux allergènes et aux nanomatériaux ainsi qu’aux obligations d’étiquetage nutritionnel. Des informations complémentaires pour des produits spécifiques (ex: aliment bio, huile d’olive) peuvent être définies dans d’autres textes réglementaires horizontaux et verticaux. Quelques législations nationales sont la transposition des directives de l’UE cependant, chaque pays peut avoir une réglementation spécifique, des exigences de conformité du produit jusqu’aux règles d’étiquetage. A l’heure actuelle, le fromage n’est pas régi par une réglementation commune de l’UE l’analyse de la présence de gras sur les matières sèches n’est obligatoire que dans quelques pays.
› Une entrée réussie sur le marché des USA exige une connaissance approfondie et complète de la réglementation fédérale ainsi que de celle de chaque. Etat Les agences fédérales sont essentielles pour le contrôle de la réglementation l’US Department of Agriculture, Food Safety Inspection Service (FSIS) contrôle la viande, la volaille et les ovo produits tandis que la Food Drug Administration (FDA) est responsable des 75 80 restant de l’approvisionnement alimentaire des USA, incluant les établissements de transformation alimentaire nationaux étranger. Les agence des Etats ont un rôle de supervision au niveau local sur les entreprises de transformation alimentaire en collaboration avec les agences fédérales. Concernant l’étiquetage alimentaire et nutritionnel, les additifs alimentaires et les normes produits, presque toutes les exigences sont couvertes par la loi fédérale via le Code of Federal Regulation (CFR) Titre 21 «Aliments et Médicaments», Partie 101 «Etiquetage alimentaire». Cela couvre plusieurs sujets tel que les informations nutritionnelles sur l’étiquetage, section 9 dans laquelle les nouvelles exigences de déclaration nutritionnelle « Nutrition Facts » sont définies. CFR partie 101 couvre aussi les additifs alimentaires et l’information nutritionnelle dans les restaurants dans d’autres sections dédiées.
› Au Canada le CFIA (Agence d’Inspection Alimentaire Canadienne) est l’autorité administrative responsable de la sécurité des denrées alimentaires, des animaux, et des plantes et met en oeuvre les programmes fédéraux. Santé Canada (le département d’inspection de la CFIA), définit les politiques, les règlements et les normes pour l’étiquetage alimentaire et nutritionnel, les additifs alimentaires, la publicité et les normes produits sous la loi des aliments et médicaments Food and Drug Act. Cela inclut notamment les exigences de déclaration des allergènes dans la liste des ingrédients la table des informations nutritionnelles pour aider à une alimentation équilibrée et un auto contrôle de sa santé ainsi que les instructions pour l’utilisation, la consommation, le stockage en toute sécurité. De nouvelles réglementations sont attendues pour 2021. Les colorants alimentaires seront déclarés par leurs noms communs plutôt que le terme générique «couleur», la liste des ingrédients et des allergènes sera simplifiée et un étiquetage sur la face avant du contenant sera développé.

6Livre Blanc | Le Développement Produit dans un Environnement Règlementaire Global
Comparaison des exigences relatives à l’étiquetage
Substance EU USA Canada
Chartre graphique pour la lisibilité
› 1, 2 mm mini pour les phrases obligatoires
› 0, 9 mm si la plus petite surface d’étiquetage est < 80 cm² <80 cm2
› Les déclarations de quantité doivent avoir une hauteur minimale en fonction du poids net du produit
› 1, 6 mm mini pour les phrases obligatoires
› Nom du produit et quantité doivent être accentués avec des dimensions spécifiques
› 1, 6 mm mini pour les phrases obligatoires
› Les déclarations de quantité ont une dimension spécifique selon la surface d’affichage principale
Dénomination commerciale et quantité
Le nom du produit et les quantités doivent être écrits sur la même surface (pas forcément la principale).
Le nom du produit et les quantités doivent être reportés et présentés aux clients, soit à l’avant du paquet.
Le nom du produit et les quantités doivent être reportés et présentés aux clients, soit à l’avant du paquet.
Comment indiquer les allergènes
14 allergènes dont la déclaration est obligatoire doivent être écrits de manière accentuée (ex: en gras), afin de clairement les identifier parmi les autres ingrédients.
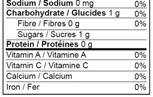

8 allergènes doivent être mentionnés avec le nom de la source alimentaire en gras et dans des « » après l’ingrédient; ou avec la mention « contient » derrière l’ingrédient (de la même taille). Ex: Lactosérum (Lait) dans la liste d’ingrédients ou « contient du lait » à la fin.
18 aliments sources d’allergènes et 5 aliments sources de gluten doivent être déclarés dans la liste des ingrédients ou avec la mention « contient » à la fin de liste des ingrédients.

Ex: « Contient du blé »
Exigence pour la contamination croisée avec les allergènes
Dates minimales de durabilité
Non définie, même dans le Règlement «UE » 1169/2011
Obligatoire avec une formulation stricte.
Quelques exceptions (ex: vinaigre, bonbons, sel, sucre)
Non définie
La contamination croisée des ingrédients peut être indiquée avec la mention : « Peut contenir »
Aucune obligation, sauf pour les préparations pour nourrissons
Obligatoire pour les produits pré emballés avec une durée de conservation ≤ 90 jours, déclaration dans les deux langues officielles avec des formats différents.
Information nutritionnelle

7Livre Blanc | Le Développement
Produit dans un Environnement
Règlementaire Global
Le système d’étiquetage nutritionnel sur la face avant de l’emballage (Front Of Pack) a été développé dans différents pays, dans l’optique d’augmenter la transparence et d’aider les consommateurs à faire le choix en étant informés Ils peuvent être volontaires ou obligatoires.
Le système Nutri Score en France
L’étiquetage (FOP) volontaire inclut généralement les informations concernant le sucre, les matières grasses et le sel contenu dans 100g ou par portion ainsi que le système de notation (ex: étoiles, couleur, code, lettres) indiquant si les quantités sont élevées ou non et/ou sur la qualité globale d’un point de vue nutritionnel du produit. Alors que des plans nationaux ont été utilisés depuis des années dans des pays tels que le Royaume Uni, l’Australie, et les pays Scandinaves un nouveau système vient d’être adopté en France. Le Journal Officiel de la République Française a publié le 31 octobre 2017 le déploiement du Système Nutri Score comme cela était recommandé pas le gouvernement français via l’article L 3232 8 et R 3232 7 du Code la Santé Publique. Ce nouveau système d’étiquetage consiste en un marqueur graphique synthétisant le score nutritionnel du produit en 5 classes sur une échelle de 5 couleurs (du vert foncé au rouge), associé à une série de lettres allant de A (« meilleure qualité nutritionnelle ») jusqu’à E (« mauvaise qualité nutritionnelle »). Ce système a été adopté après un processus de consultation dont il ressort qu’il s’agit du système d’étiquetage le « plus compréhensible ». La charte graphique du système Nutri Score et ses caractéristiques sont fournies en annexe à la demande. Toute entreprise éligible et désirant utiliser le Nutri Score doit faire part de ses intentions à l’organisation française de santé publique.
Déclaration nutritionnelle au Mexique
Exigences pour l’étiquetage dématérialisé en Europe
En raison de la croissance du e-commerce, le règlement européen (UE) 1169/2011 stipule que toutes les informations obligatoires sur les produits alimentaires pré emballés destinés à la vente à distance doivent être fournies avant que le consommateur décide d’acheter l’article. Les consommateurs doivent recevoir les informations nécessaires pour faire des choix éclairés, comme c’est le cas dans un supermarché. Ces informations doivent être précises et fournies en temps réel, introduisant ainsi des défis d’échange électronique entre les opérateurs alimentaires (en partie entre les fabricants et les distributeurs). La compatibilité des systèmes d’information sur les produits et la gestion des modifications de recettes font partie des principaux défis.
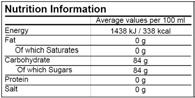
L’étiquetage sur la face principale (FOP) peut aussi être obligatoire. Par exemple, au Mexique un label nutritionnel, obligatoire pour les déclarations de sucre, de sodium, de matières grasses et la valeur énergétique (Kcal) contenus par portion est en vigueur depuis l’amendement sur la réglementation de l’étiquetage nutritionnel en 2014. La déclaration des nutriments et de la valeur énergétique doit être effectuée correctement et dans le bon sens, de gauche à droite. Certains produits sont exemptés des exigences du FOP herbes, épices, arômes, extraits de café, café en grains, café moulu, café décaféiné, café soluble ou non, tisanes, thés caféinés ou non, thés instantanés ou non avec additifs, vinaigres fermentés ou similaires, produits en vrac. Le FOP peut être complété avec une « estampille nutritionnelle » volontaire basée sur un profil nutritionnel strict développé par l’Alliance Internationale des Aliments et Boissons (International Food & Beverage Alliance (IFBA)).
8Livre Blanc | Le Développement Produit
dans
un Environnement Règlementaire Global
3. Allégations Nutritionnelles et de Santé
Une allégation nutritionnelle est une indication faisant référence à la teneur en un ou plusieurs nutriments dans un produit alimentaire. Les allégations nutritionnelles autorisées sont généralement énumérées dans les réglementations pertinentes et ne nécessitent aucune procédure d’approbation spécifique. Les allégations nutritionnelles et de santé diffèrent considérablement en termes de formulation et de conditions d’utilisation selon le pays de commercialisation.
Dans les pays de l’UE, les conditions d’utilisation des allégations dépendent de la teneur en nutriments dans 100 g ou 100 ml d’aliments.
Aux États Unis et au Canada, ils dépendent de la teneur en nutriments par portion du produit.
Exemples d’allegations sur le calcium
Substance EU USA Canada
Libellé de l’allégation
Condition d’utilisation
“Source de calcium” “Bonne source de calcium”
Le produit doit contenir ≥ 15% pour 100g ou 100ml (ou par emballage s’il ne contient qu’une seule portion) de la quantité journalière recommandée en calcium.
Le produit doit contenir entre 10 et 19 % de la quantité journalière recommandée en calcium selon le panier moyen.
“Contient du calcium”
Le produit doit contenir au moins 5% de la quantité journalière recommandée en calcium par portion.
Une allégation de santé désigne toute indication établissant ou suggérant l’existence d’une relation entre une catégorie d’aliments, un produit alimentaire ou l’un de ses constituants et la santé humaine. Les allégations de santé sont soumises à des exigences d’approbation différentes selon le pays de commercialisation et le type d’indication (il peut s’agir notamment d’une allégation de structure fonction, d’une allégation liée à un risque de maladie ou d’une nouvelle allégation fondée sur des preuves scientifiques). Certaines d’entre elles nécessitent une approbation avant leur commercialisation, tandis que d’autres sont répertoriées dans les réglementations pertinentes et peuvent être généralement utilisées si les conditions d’utilisation sont remplies.
9Livre Blanc | Le Développement Produit dans un Environnement Règlementaire Global
Libellé de l’allégation
Chewing gum sans sucre Édulcorants glucidiques non cariogènes (xylitol, mannitol, maltitol de sorbitol, isomalt lactitol hydrolysats d’amidon hydrogénés, sirops de glucose hydrogénés et érythritol isolé ou combiné), D tagatose isomaltulose sucralose.
Le chewing gum sans sucre contribue au maintien de la minéralisation des dents.
La consommation fréquente d’aliments riches en sucres et en féculents comme collations entre les repas peut favoriser la carie dentaire. L’alcool de sucre utilisé pour sucrer cet aliment peut réduire le risque de carie dentaire.
La mastication de 2.7g de chewing gum sans sucre, 3 fois par jour après les repas, contribue à réduire le risque de caries dentaires.
Condition d’utilisation
Les chewing gums doivent respecter la législation concernant les allégations nutritionnelles « sans sucre »
Les aliments doivent contenir 1 des édulcorants glucidiques non cariogènes mentionnés, sans niveau minimum requis.
Chewing gum sans sucre
› contient ≥ 0,8 g d’édulcorant à l’alcool de sucre par portion et montant de référence
› répondent aux conditions pour “sans sucre” et contiennent ≤ 0,25 % d’amidon, dextrines, mono --, di et oligosaccharides ou glucides fermentescibles combinés.
Informations additionnelles requises
Oui : le consommateur doit être informé que l’effet bénéfique est obtenu en mâchant 2 à 3 g de chewing gum sans sucre pendant 20 minutes au moins trois fois par jour après les repas.
Non Oui : la teneur totale en alcools de sucre doit être déclarée dans le tableau de la valeur nutritive en grammes par portion.
10Livre Blanc | Le Développement
Produit dans un Environnement
Règlementaire Global
Substance EU USA Canada
Produit sujet à la déclaration nutritionnelle
Chewing-gum sans sucre
Exemple d’allegation sur la reduction d’apparition de caries
4. Origine des ingrédients
La Commission Européenne a récemment lancé une consultation publique sur une proposition de règlement visant à établir des méthodes d’application de l’article 26.3 du règlement (UE) 1169/2011. Plus précisément, cette réglementation définirait des règles pour indiquer le pays ou le lieu d’origine de l’ingrédient principal d’un produit si celui-ci diffère de l’origine revendiquée de l’aliment principal. Les parties intéressées pouvaient envoyer leurs commentaires avant le 1 er février 2018. Après la consultation, la réglementation sera votée par un comité comprenant chaque Etat membre. Le règlement devrait entrer en vigueur trois jours après la date de sa publication dans le Journal officiel de l’UE et s’appliquera à compter du 1 er avril 2019. Les aliments mis sur le marché ou étiquetés avant la date d’application peuvent être commercialisés jusqu’à épuisement des stocks. Selon le projet de règlement, l’origine peut être exprimée avec les zones géographiques suivantes.
› “UE”, “non-UE” ou “UE et non-UE”;
› État(s) membre(s) ou pays tiers;
› Région ou toute autre zone géographique à l’intérieur d’un Etat membre ou d’un pays tiers, qui soit clairement compréhensible par les consommateurs moyens;
› Le pays d’origine ou le lieu de provenance conformément aux dispositions spécifiques de l’UE applicables à l’ingrédient ou aux ingrédients primaires en tant que tels (par exemple, le niveau de précision établi pour la viande bovine).
Alternativement, les opérateurs alimentaires peuvent apposer sur l’étiquette une indication telle que :”X [X ingrédient principal] ne provient pas (du pays d’origine ou du lieu d’origine de l’aliment)” ou d’une formulation similaire qui peut encore avoir même sens pour le consommateur.
L’origine de l’ingrédient primaire doit être exprimée avec une taille de police non inférieure à la taille minimale requise par l’article 13 2 du règlement (UE) 1169 /011 (1, 2 mm) et, en tout cas, dans le même champ de vision où l’indication sur le pays ou le lieu d’origine de la nourriture est écrite. En outre, si elle est exprimée par écrit, elle ne doit pas être inférieure à 75% de la hauteur de l’indication du pays ou du lieu d’origine de l’aliment.
Au niveau européen, des réglementations sur les pays d’origine sont déjà en vigueur pour la viande, le miel, l’huile d’olive, le vin, le poisson et les aliments biologiques.
Partant des exigences du règlement (UE) 1169/2011 et en attendant les règlements d’application de la Commission européenne sur l’origine des ingrédients, le gouvernement italien a publié plusieurs lois réglementant l’étiquetage du pays d’origine de certains produits finis (lait, pâtes, riz, tomates et vin) ainsi que les ingrédients qu’ils peuvent contenir.
Un décret français (2016-1137) établissant des indications d’étiquetage obligatoire pour les aliments pré emballés a été publié le 21 août 2016. Seules les denrées alimentaires destinées aux consommateurs finaux fabriquées et commercialisées en France sont concernées. Les aliments pré-emballés fabriqués dans d’autres pays (y compris les États membres de l’UE) et les produits avec Indication Géographique Protégée sont hors de portée. Les produits visés sont le lait, le lait utilisé comme ingrédient dans les produits laitiers (yaourts beurre, fromage) et la viande (bœuf, porc, mouton, chèvre, volaille) utilisée comme ingrédient dans les aliments transformés. Pour la viande, le pays de naissance, d’élevage et d’abattage d’animaux doit être libellé avec une formulation spécifique selon que la viande a un seul pays d’origine ou plus (“origine UE”, “origine non-UE”). Pour le lait, le pays de collecte, d’emballage ou de transformation doit être spécifié. Cette information est indiquée dans la liste des ingrédients juste après l’ingrédient correspondant ou avec une note à la fin de la liste des ingrédients. L’arrêté du 28 septembre 2016 relatif au décret 2016/1137 définit un seuil spécifique pour le lait et la viande utilisés en tant qu’ingrédient 50% et 8% respectivement - au dessus duquel l’indication de leur origine est obligatoire. La traçabilité des produits durera cinq ans et certaines pénalités financières sont définies en cas de non respect des dispositions.
11Livre Blanc | Le Développement Produit dans un Environnement Règlementaire Global
5. Eco concept des emballages
L’étiquetage des denrées alimentaires n’est pas seulement régi par les législations du secteur alimentaire, il peut également être couvert par les réglementations sur les emballages et leur recyclage.

En Europe la directive sur les emballages 94/62/CE du 31 décembre 1994 met en place un cadre réglementaire qui a été révisé en 2004. Il fixe des objectifs que les pays doivent respecter en matière de stratégie et de législation. En conséquence, les textes réglementaires peuvent être très différents d’un pays à l’autre.
En Allemagne la base juridique est l’ordonnance de 1991 sur les emballages, qui vise à éviter, réduire, réutiliser et/ou à recycler les déchets d’emballages et, par conséquent, à les renvoyer dans la boucle de production.
Le 1 er janvier 2019 une nouvelle loi allemande sur les emballages entrera en vigueur avec des exigences supplémentaires en matière de gestion écologique des déchets.
Différents types d’emballages sont considérés :
› emballage de vente
› suremballages
› emballage de transport
› emballage de boisson
› emballage réutilisable
Il définit les principes suivants :
› Les déchets d’emballage doivent être évités
› Si les déchets d’emballage ne peuvent être évités, la réutilisation et le recyclage doivent être prioritaires par rapport à la récupération d’énergie,
› L’élimination des déchets compatible avec le bien être public doit être mise en place
Par conséquent, les fabricants doivent obligatoirement mettre en place un système de collecte et d’élimination des emballages à usage unique mis sur le marché pour les “consommateurs privés”. Pour les emballages à usage unique, un système de consigne doit être mis en place. De plus, des symboles et logos spécifiques doivent être ajoutés sur l ’emballage afin de permettre le remboursement.
12Livre Blanc | Le Développement Produit dans un Environnement Règlementaire Global
En France, le logo Triman doit être visible sur tous les produits recyclables collectés séparément et soumis à un principe de responsabilité élargie du producteur après utilisation. Si ce n’est pas possible, il doit être ajouté à l’emballage, à la notice ou à tout autre moyen, même si un produit est vendu en ligne. Cette exigence résulte du décret d’application 2014-1577 du 1 er janvier 2015 et fait l’objet d’un dépôt. La généralisation de cette signalisation est progressivement mise en place. L’utilisation du logo Triman et des signes associés est gratuite et autorisée par l’ADEME à des fins d’information. En fait, il vise à aider les consommateurs à identifier clairement et sans ambiguïté les produits recyclables, collectés séparément et soumis au principe de responsabilité élargie des producteurs après utilisation. Le logo Triman ne remplace pas le « Point Vert » ou l’”Info Tri”.
Eco-Emballages et Adelphe sont deux organismes reconnus par l’Etat qui ont pour mission d’organiser, de superviser et de soutenir le recyclage des emballages ménagers en France. Les industriels qui soutiennent et cotisent aux systèmes EcoEmballages ou Adelphe doivent imprimer un Point Vert sur tous les emballages qu’ils mettent sur le marché français. Ainsi, la présence du Point Vert sur un emballage ne signifie pas nécessairement qu’il sera recyclé. Cela signifie seulement que le fabricant doit contribuer financièrement au tri et au retraitement des emballages de ses produits. Le point vert “info tri” complète et donne plus de sens au point vert en fournissant aux consommateurs des informations supplémentaires il spécifie pour chaque emballage s’il doit être jeté ou recyclé et comment.

13Livre Blanc | Le Développement Produit dans un Environnement Règlementaire Global
6. Matériaux au contact des aliments
Les matériaux en contact avec les denrées alimentaires (Food Contact Material FCM) sont des matériaux qui sont ou sont destinés à être en contact avec des aliments pendant leur production, leur stockage, leur préparation et leur service, tels que emballages alimentaires, ustensiles de cuisine et récipients. Ainsi, ils peuvent avoir un impact sur la sécurité sanitaire et la qualité des aliments tout au long de la chaîne d’approvisionnement alimentaire. Les FCM couvrent un large éventail de matériaux différents tels que le plastique, le verre papier et le métal, mais également les adhésifs, les encres d’impression et les revêtements utilisés dans la finition des produits finis.
Pour assurer la sécurité des FCM, une série d’exigences légales et de contrôles sont en place dans l’Union européenne. La réglementation de la Commission (CE) 1935/2004 est la législation cadre européenne pour les FCM. Elle énonce les principes généraux de sécurité et d’inertie. L’article 3 stipule que les substances présentes dans les FCM ne doivent pas migrer dans les aliments à des concentrations susceptibles de nuire à la santé humaine ou impliquer un changement inacceptable de la composition alimentaire ou une détérioration de ses propriétés organoleptiques.
Le règlement établit également des exigences générales pour la fabrication des FCM en tant qu’obligation de respecter les bonnes pratiques de fabrication (BPF) établies dans le règlement (CE) n°2023/2006 de la Commission, ainsi que des exigences spécifiques pour le processus d’autorisation. Il doit être démontré que les FCM sont conformes aux règles grâce à des tests appropriés et sont soumis à la déclaration de conformité (DoC). Un matériau ou un article est considéré comme “sûr” lorsqu’il respecte des limites de migration spécifiques ou d’autres restrictions réglementaires. Lorsqu’une telle limite n’est pas établie, l’évaluation toxicologique effectuée par l’EFSA est considérée comme la référence. Pour les substances non évaluées, le fabricant a la responsabilité de démontrer la sécurité du produit.
Concernant les matériaux et objets en matière plastique le règlement (UE) 10/2011 est le plus complet et le plus efficace avec des mesures spécifiques pour les plastiques, les procédés de recyclage des pellicules en cellulose régénérée, les céramiques et les matériaux et emballages actifs et intelligents. En l’absence de mesures spécifiques de l’UE, les États membres peuvent maintenir ou adopter leurs propres dispositions nationales conformes aux règles du traité.

14Livre Blanc | Le Développement Produit dans un Environnement Règlementaire Global
Aux États Unis et au Canada, l’approche des FCM est différente, notamment en ce qui concerne les définitions, les lois et les organismes officiels impliqués dans les processus d’évaluation et d’autorisation des risques.
EU USA Canada
Acteurs principaux
Evaluation des risques par l’EFSA et management des risques par la commission européenne.
Autorisation
Dossier pour les substances à autoriser.
Evaluation et management des risques par la FDA.
Soumission volontaire à la Direction générale des produits de santé et des aliments (HPFB) pour une évaluation précise de la salubrité des produits chimiques.
Les FCM sont considérés comme des additifs indirects des produits chimiques pouvant être transférés dans les aliments via l’emballage ou via le matériel de traitement.
Le FCM est uniquement un emballage alimentaire et des matériaux qui entrent en contact avec des aliments pendant la production et la transformation, mais pas d’autres produits de consommation tels que des ustensiles de cuisine, etc.
Cadre réglementaire
Le règlement de la commission (CE) 1935/2004 est la référence. Les exigences sont basées sur la migration.
Le règlement de référence est le Code Federal Regulation (CFR), titre 21. Un avis de contact alimentaire est nécessaire à la conformité. Les exigences sont basées sur l’exposition. Le seuil réglementaire (ToR) est défini.
La section 23 du Règlement sur les aliments et médicaments constitue le cadre principal. Elle contient l’admission et la non admission, les limites des substances.
15Livre Blanc | Le Développement Produit dans un Environnement Règlementaire Global
Quels sont les nouveaux challenges ?
Les étiquettes doivent respecter des législations de plus en plus complexes dans le monde entier. L’un des principaux défis des entreprises du secteur alimentaire est d’étiqueter correctement et complètement les produits conformément aux lois locales, nationales et internationales applicables. Un aspect important à prendre en compte lors de l’exportation vers un pays étranger est qu’une simple traduction littéraire d’étiquettes, même si elle est effectuée par un interlocuteur natif, n’est pas toujours suffisante. Une formulation spécifique obligatoire peut ne pas figurer dans la traduction et peut différer même dans la même langue. Le libellé de la «date limite» en français canadien («Meilleur avant») est différent de celui de la France («à consommer de préférence avant»). De plus, les spécificités culturelles et linguistiques doivent être prises en compte, notamment pour rendre le consommateur confiant dans le produit.
Même dans le cas de réglementations communes, chaque pays a sa propre interprétation selon le niveau de tolérance sensibilité locale sur des sujets spécifiques.
Par exemple, en Italie les autorités et les organismes de contrôle examineront des informations telles que le pays d’origine (label “made in Italy”). Cela est dû à la grande quantité de produits alimentaires domestiques. En revanche, leur approche est moins dure pour les produits provenant d’autres pays de l’UE.
Dans de nombreux pays des directives spécifiques, telles que définies par les organismes nationaux ou des associations professionnelles, s’appliquent à diverses catégories de produits alimentaires en plus des règlements officiels. Ces directives d’étiquetage concernent non seulement la composition du produit, mais aussi le côté “marketing” en termes de noms et d’images apparaissant sur l’emballage. A titre d’exemple, l’impression d’une fleur de vanille sur un emballage de glace n’est autorisée que pour les produits fabriqués avec des arômes naturels.

Livre Blanc | Le Développement Produit dans un Environnement Règlementaire Global
1. Conformité des produits quelque soit le pays : du marketing à la production
2. Risques associés aux non conformités
Une non conformité peut provenir de différents aspects d’un produit tels que :
› sa composition il peut contenir des ingrédients ou des additifs interdits;
› l’hygiène : des contaminants peuvent être présents à des niveaux plus élevés que ceux autorisés;

› des problèmes d’étiquetage des informations obligatoires peuvent manquer, les textes marketing peuvent induire en erreur. Si la non conformité est détectée, elle entraîne différents types de sanctions notamment des rappels de produits, des sanctions pénales et des coûts financiers. Chaque pays a son propre cadre juridique en matière de sanctions.
Cependant, il est difficile de prévoir quels sont les risques associés. En fait, de nombreux facteurs tels que la taille de l’industriel du distributeur, l’exposition du produit au marché et l’interprétation par les autorités locales doivent être pris en compte pour une non conformité liée aux problèmes de marketing.
RASFF Allergen Notifications
2017 Statistics & Trends
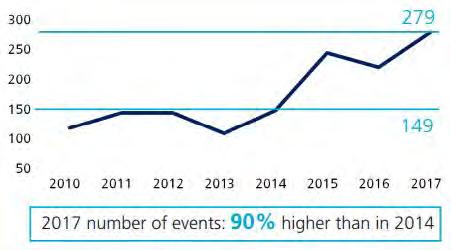
La présence d’un allergène non déclaré dans un produit alimentaire constitue un grave danger pour la sécurité des aliments et comporte un risque élevé pour le consommateur final. Si cela se produit en Europe, une procédure de retrait conforme à les principes du règlement (CE) 178/2002 doit être immédiatement initiée, associée à des coûts énormes (plusieurs millions) et à des dommages sur l’image de marque. Néanmoins, les allergènes non déclarés restent une cause majeure de rappels de produits alimentaires dans le monde, avec une tendance à la hausse au cours des dernières années. Leur présence est en grande partie à due à la contamination croisée dans des les usines et de la chaîne d’approvisionnement, ou à des erreurs d’étiquetage (étiquette erronée ou déclaration d’allergènes erronée). Les rappels liés aux allergènes peuvent également être causés par la fraude alimentaire. En Europe, une augmentation de 26% des notifications dues aux allergènes a été observée en 2017 selon la base de données RASFF (Rapid Alert System for Food and Feed) gérée par la Commission européenne. Au total, 279 notifications ont été faites par les États membres européens. Cependant, ce nombre ne reflète pas correctement le nombre réel d’alertes aux allergènes dans les pays européens. La plupart des rappels d’allergènes ne sont pas liés à des situations transfrontalières et ne sont donc pas signalés dans le système RASFF.
L’un des points difficiles pour l’industrie alimentaire est la gestion de l’étiquetage des denrées alimentaires en raison de petits ajustements de recettes tels que la substitution d’une matière première par changement de fournisseur. Si l’introduction d’un nouvel allergène doit de toute évidence être déclarée et nécessite le passage à un nouveau conditionnement, le changement des éléments nutritionnels n’entraîne pas nécessairement un changement immédiat des illustrations de l’étiquette. Les opérateurs alimentaires doivent savoir à quel point les autorités locales sont tolérantes pour prendre une décision appropriée concernant les stocks d’étiquettes. Par conséquent, l’anticipation, la prévoyance et une bonne connaissance des règles locales et de leur interprétation sont essentielles pour minimiser les risques et les coûts.
17Livre Blanc | Le Développement Produit dans un Environnement Règlementaire Global
Mérieux NutriSciences analysis
Les bonnes pratiques
1. Se fier à un réseau international d’Experts réglementaires
Il est clair que la conformité des produits nécessite une connaissance approfondie des règles locales et de leur interprétation, ainsi que la capacité de toujours être au courant de ces règles afin d’anticiper l’application de tout changement éventuel.
En règle générale, les petites entreprises ne disposant pas d’un service juridique dédié sont confrontées à des problèmes de conformité et de réglementation et doivent s’appuyer sur des spécialistes externes ou des conseils fournis par les syndicats professionnels. Mais même pour les moyennes et grandes entreprises qui exportent des produits vers un grand nombre de pays, la surveillance de ces pays sans aucune personne basée dans la région est un gros challenge.
› Comment être au courant en temps réel de nouvelles réglementations ?
› Comment connaître l’interprétation et les tolérances des autorités locales, ainsi que des organisations professionnelles ?
› Comment être au courant des discussions en cours ?
Quelle que soit la situation, le recours à des experts en réglementation locale est essentiel pour répondre aux questions clés et garantir la conformité des produits.
L’accès à un réseau de spécialistes de la réglementation alimentaire répartis dans les pays où les produits sont commercialisés, constitue un élément clé de la stratégie des entreprises du secteur alimentaire. C’est le meilleur moyen de maximiser la conformité des produits et des étiquettes tout en minimisant les risques associés.
De plus, l’utilisation d’outils spécifiques dédiés pour faciliter le suivi dans le pays et être alerté en cas d’impact sur les nouvelles règles est appropriée pour gagner en efficacité et en réactivité. Plus besoin de passer du temps à identifier les bonnes sources et à surveiller les sites Web connexes. Au lieu de cela, le temps est consacré à l’application des règles appropriées avec le soutien d’experts, ce qui optimise la conformité du produit et permet de répondre aux objectifs marketing et aux attentes des consommateurs.
18Livre Blanc | Le Développement Produit dans un Environnement Règlementaire Global
Iintroduire Un Produit Sur Le Marché
Comment adapter l’étiquetagede mon produit à ce pays ?
Comment connaitre les nouvelles réglementations ?
Comment savoir si une modification de la règlementation impacte mon produit ?
Quels sont les règles pour ce produit sur ce marché ?
Est ce que mon produit et ses ingrédients respectent les règles locales de ce pays ?
Comment intégrer une nouvelle réglementation et consolider les règles existantes ?
Comment connaitre l’interprétation locale des textes ?
2. Une source unique de l’information dans un contexte réglementaire complexe
L’information joue un rôle crucial dans l’entreprise et doit être disponible au bon endroit et au bon moment pour le bon interlocuteur. Mais pour gérer un volume de données toujours croissant, il est indispensable d’établir des procédures claires et partagées. Les équipes R&D doivent par exemple savoir comment renseigner et traiter les données générées à chaque création ou modification de recette simulation de coûts, quantification des ingrédients, valeurs nutritionnelles, BOM (Bill of Materials, etc.).
En effet, ces données sont vouées à être exploitées ultérieurement, notamment par les services Qualité et Réglementaire. Si l’entreprise ne dispose d’aucun outil ou processus dédié à la gestion de cette information, les équipes peuvent perdre un temps considérable à parcourir la base de données pour récupérer la bonne information au lieu de se concentrer sur leur coeur de métier, comme la mise en conformité du produit. Il faut recentrer les équipes sur des tâches à valeur ajoutée. On comprend facilement que gérer efficacement l’ensemble de l’information produit peut être un challenge à part entière. Mais grâce aux quelques étapes suivantes, c’est possible.
1. Centraliser et organiser l’ensemble de l’information produit
L’information produit comprend les données quantitatives et qualitatives, les contraintes définies, les spécifications techniques, les certifications obtenues et tous les autres documents relatifs au développement du produit, au suivi de la qualité et à la gestion de la conformité réglementaire. Toute cette information doit donc être unifiée et consolidée au sein d’un unique référentiel afin de pouvoir rapidement trouver et communiquer la bonne information au bon moment et à la bonne personne.
2. Structurer les données et documents au cours du cycle de vie produit
De l’idée du produit jusqu’à la dernière étape de son cycle de vie, la moindre action sur le moindre élément du produit peut avoir des conséquences sur tout le reste la chaîne. Par exemple, remplacer une matière première par une autre, qui introduirait un nouvel allergène, impactera tous les produits finis utilisant cette matière première. Cela demande donc d’intégrer cette donnée et de la suivre tout au long du processus.
Pour comprendre ces nombreuses interactions et disposer en permanence des spécifications exactes des éléments du produit, il est nécessaire de rassembler et structurer les données et documents de manière cohérente.
3. Générer automatiquement des documents
Se conformer à la réglementation est un processus long, rigoureux et clairement défini par les organismes de certification. L’entreprise doit fournir de nombreuses informations, structurées selon un modèle établi par ces organismes déclarations d’ingrédients, étiquetage des valeurs nutritionnelles, fiche produit. Pour que cela ne devienne pas un frein au time to market il faut se doter d’un outil qui rassemble l’information puis l’exploite pour générer automatiquement les documents nécessaires, en accord avec les modèles prédéfinis.
19Livre Blanc | Le Développement Produit dans un Environnement Règlementaire Global
3. Conformité “by design” : continuité de l’information de la matière première au produit fini
Lancer sur le marché un produit non conforme à la législation peut porter un coup dur au portefeuille de l’entreprise et à sa réputation. Du Marketing au Sourcing en passant par la R&D, tous les services de l’entreprise impliqués dans le développement produit sont donc concernés par les questions réglementaires.
Pour assurer cette conformité, chaque équipe doit pouvoir s’appuyer sur la version la plus récente et la plus précise de chaque information. Disposer de processus clairement définis permet aux différents services de ne pas perdre de temps à demander et à vérifier de l’information, et de se concentrer sur leur coeur de métier. Les services Réglementaire et Qualité peuvent ainsi devenir plus proactifs en anticipant les nouvelles réglementations ou en prévoyant des plans d’actions en cas de non conformité avérée.
Le travail des équipes R&D, Réglementaire et Qualité illustre ce défi. La première doit être force de propositions sur les formulations tout en respectant des contraintes à la fois internes (cahier des charges marketing) et externes (liste des ingrédients interdits dans le pays).
En parallèle, l’équipe Réglementaire doit pouvoir suivre de façon fiable les essais de la R&D pour détecter une non conformité dès qu’elle se présente, sans attendre la version finale du produit.
De plus, un produit destiné à l’export doit dès le départ être pensé et développé dans une optique internationale pour intégrer en amont les réglementations spécifiques aux pays les réseaux de fournisseurs, la traduction des informations...
Chaque service de l’entreprise est concerné par un lot spécifique d’étapes du développement produit. Mais ces étapes sont interdépendantes et suppriment, créent, modifient et réutilisent de l’information.
Il est donc essentiel d’instaurer une collaboration forte entre ces équipes afin de garantir la continuité de l’information.
Mais cet enjeu ne s’arrête pas à la validation du produit fini, il se poursuit lors des phases de production et de commercialisation. Les outils de l’entreprise oeuvrent en définitive tous au même objectif : supporter la réussite des produits et projets initiés. Du PLM pour l’innovation au PIM pour la diffusion en passant par l’ERP pour la production, de nombreux outils applicatifs complémentaires existent pour garantir l’exactitude et la complétude de l’information, qui est en permanence réutilisée et enrichie. C’est en définitive le fait de disposer d’un référentiel unique et structuré de l’information qui permet aux visiteurs de votre plateforme e-commerce de trouver un produit qui correspond effectivement à sa description.
20Livre Blanc | Le Développement Produit dans un Environnement Règlementaire Global
4. Conformité par collaboration : faciliter la communication avec les parties prenantes externes
Renforcer la communication et la collaboration avec les partenaires de l’entreprise (fournisseurs, experts réglementaires, laboratoires de test, agences de création…) est un autre moyen d’optimiser la mise en conformité.
Lors d’un appel d’offre, les fournisseurs doivent soumettre différentes propositions en respectant à la fois les délais et le cahier des charges du client. Ils ne peuvent pas se permettre de perdre du temps à rechercher l’information voire à la demander à leurs propres fournisseurs. Encore une fois, l’information doit être centralisée et structurée.
Si le portefeuille produits n’est pas à jour, impossible pour le fournisseur de savoir s’il a déjà à disposition un produit répondant aux besoins du client. Et dans le cas où un nouveau produit doit être développé, il est indispensable de pouvoir rechercher, identifier et tracer les matières premières qui correspondent aux besoins client, comme, par exemple, celles sans allergènes.
› Comment garantir une information précise et en temps réel
» La première étape est de réunir l’ensemble de l’information et des documents détenus par les parties prenantes externes
» Les informations de même nature doivent être structurées et traitées de la même manière. Par exemple, les fiches de matières premières envoyées par vos fournisseurs devront suivre le même format
» Il faut tenir à jour le référentiel de l’information afin d’accélérer toute recherche et d’en assurer la précision
› Comment renforcer la conformité de votre produit
» Pour un suivi qualité efficace, un plan de contrôle détaillé présentant les différents tests à réaliser doit être établi avant d’entamer le développement du produit. Les processus et workflows internes ainsi que le portail destiné aux parties prenantes externes garantissent la rigueur des tâches menées
» Pour s’assurer de la sécurité et de la conformité d’un produit, s’entourer d’experts réglementaires est le meilleur moyen pour les équipes de se concentrer sur leur métier
» S’équiper de solutions IT permet de suivre facilement les échantillons et résultats, d’automatiser certaines actions comme la génération de documents et de lier de façon fiable et durable tous les résultats au produit fini
21Livre Blanc | Le Développement Produit dans un Environnement Règlementaire Global
› Comment faciliter les échanges avec vos fournisseurs et partenaires
» La première étape est de structurer de façon cohérente les informations similaires reçues et envoyées aux parties prenantes externes

» Chaque fois qu’un fournisseur renseigne une nouvelle information comme un changement de prix, une mise à jour de certification ou le remplacement d’une matière première, votre base de données doit impérativement intégrer cette modification. Pour cela, créez, utilisez et partagez avec vos fournisseurs et partenaires vos propres modèles. Installez un portail fournisseurs ces derniers peuvent ainsi renseigner leurs informations en accord avec vos contraintes et modalités d’usage. Ils sont ainsi responsabilisés quant à l’exactitude et la complétude des informations et gagnent en proactivité dans la relation que vous entretenez avec eux. Ces processus peuvent être également implémentés pour le développement du packaging afin d’assurer que toutes les caractéristiques requises ont bien été respectées, telles que les dimensions et compositions
Une collaboration à tous les niveaux est indispensable pour garantir la conformité du produit
Vous pouvez ensuite transposer cette méthode à d’autres problématiques comme la gestion du packaging et de la chaîne graphique. Effectivement, le service Marketing gère le développement des artworks éventuellement avec des agences de création externes, mais ce sont la Qualité et le Réglementaire qui valident les propositions finales. Disposer d’une plateforme commune d’échanges accélère la création et la validation de tous les éléments graphiques. Les équipes Marketing, Packaging et les La agences de création devraient également avoir accès aux instructions réglementaires dès le début de la création.
22Livre Blanc | Le Développement Produit
dans
un Environnement Règlementaire Global
ConclusionLes industriels agroalimentaires font face à d’importantes contraintes réglementaires quand ils lancent leurs produits. Des ingrédients aux labels en passant par le packaging, c’est un challenge de se mettre en conformité et de se tenir à jour des différentes lois, directives et restrictions. De nouveaux facteurs comme le besoin de traçabilité et de transparence accentuent ce défi et augmentent l’importance d’ avoir les bons processus, workflows et supports en place. La globalisation met en avant le besoin de disposer d’une compréhension complète des règles locales.

Ainsi, pour assurer un développement de produit efficace et un time to market compétitif, il est essentiel de s’inscrire au plus tôt dans le cadre réglementaire du marché adressé. Cela requiert une information structurée et continue des fournisseurs aux consommateurs, et une collaboration efficace permise par des processus optimaux. Ces processus ne vont pas simplement faciliter chaque étape du développement produit, mais aussi supporter l’ensemble du cycle de vie produit.
La conformité « by design » est la méthodologie optimale pour être en conformité réglementaire. Le levier d’agilité est l’expertise de pair à pair de l’écosystème réglementaire. Cela peut aussi être qualifié d’ intelligence collective avec le partage et l’utilisation des connaissances et compétences des experts. L’intelligence collective est la capacité à collaborer et partager l’expertise et la connaissance entre toutes les parties prenantes (ex. : experts réglementaires, fournisseurs de solutions IT, services de l’entreprise…) pour faciliter le développement produit et accélérer son lancement sur le marché.
Êtes-vous prêt à
A propos d’Aptean
Aptean est un leader mondial des progiciels métiers. Nos solutions ERP et de gestion de la supply chain sont spécialement conçues pour répondre aux besoins des manufacturiers et distributeurs de plus de 20 industries, alors que nos solutions de conformité adressent des marchés spécifiques comme les sciences du vivant et la finance. Les solutions Aptean sont utilisées par plus de 6.000 clients à travers le monde. Avec des options de déploiement on-premise ou cloud, les produits et services Aptean aident les entreprises de toutes tailles à croître et réussir.
For more information, visit www.aptean.com.
Copyright @ Aptean 2021. All rights reserved.
en savoir plus? Prêt à savoir plus sur Aptean PLM Lascom Edition ? Contactez nous sur info@aptean.com ou visiter www.aptean.com.
















