
135 minute read
Christopher A. Dalus, Wolfgang Domej
from Jahrbuch 2016
by bigdetail
❙ Christopher A. Dalus, Wolfgang Domej ❙
Bergsport nach Gelenkersatz
Mountain sports after joint replacement
SUMMARY
With increasing numbers of modern hip and knee prostheses being implanted, even in younger persons, patients expect excellent functionality and restoration of their former physical activity level. In spite of the obvious health benefits of sports, many patients lack the confidence to take up an alpine sport again. Returning to sports after joint replacement is an important issue, particularly for those who practice disciplines as mountaineering, climbing or skiing, which often are an important part of their personal identity. Many questions may arise in the context of knee and hip replacement such as patterns of strain occurring during mountaineering that are to be avoided or completely excluded. Orthopedic risks related to alpine sports shall be evaluated and further, which precautions should be taken to decrease orthopedic risks, and whether there are any recommendations on how to increase the feeling of safety and self-confidence that will make it easier to return to these sports. Today, hip-resurfacing and unicompartmental knee arthroplasty (UKA) show satisfactory results. Good preoperative physical fitness and postoperative rehabilitation will contribute to the success of joint replacement surgery and good functionality. It is essential to reestablish coordination and range of motion immediately after joint replacement surgery. Strength and endurance should be restored within 3 – 6 months. The postoperative training program should be individually tailored and adapted to the particular sports discipline, taking the patient’s former level of activity and proficiency into account. When stability, security of movement and good technique have been achieved postoperatively, a patient may practice many of the alpine disciplines, but it is not recommended to start with a new sport immediately after joint replacement surgery.
115
The recent relevant literature was reviewed systematically. Further, two mountaineers report their practical experience with artificial knee joints, and an orthopedic surgeon involved in sports gives recommendations for optimal behavior in the postoperative period. Keywords: mountaineering, total hip arthroplasty (THA), hip-resurfacing, total knee arthroplasty (TKA), unicompartmental knee arthroplasty (UKA)
ZUSAMMENFASSUNG
Zunehmend werden heute auch bei jüngeren Patienten Hüft- und Kniegelenkprothesen implantiert. Moderner Gelenkersatz führt zu hoher Erwartungshaltung bezüglich Funktionalität und Wiedererlangung eines vormaligen Aktivitätsgrades. Trotz positiver Gesundheitseffekte durch sportliche Betätigung mangelt es vielen Prothesenträgern an ausreichendem Selbstvertrauen, um ihren Alpinsport wieder auszuüben. Dabei wäre die sportliche Wiedereingliederung nach Gelenkersatz von ganz besonderer Bedeutung, vor allem wenn es sich dabei um Alpinsportarten handelt, da für Alpinsportler die Ausübung von Bergsteigen, Klettern und Schifahren oftmals Teil ihrer persönlichen Identität ist. Etliche Fragen ergeben sich im Zusammenhang mit einem Knie- oder Hüftgelenkersatz wie etwa nach speziellen Belastungsmustern im Alpinsport, die bei Prothesenträgern vermieden oder gänzlich ausgeschlossen werden sollten, oder auch Fragen nach den orthopädischen Risiken, die speziell auf Ausübung des Alpinsports fokussiert sind. Weiter soll auf Vorsichtsmaßnahmen eingegangen werden, die Risiken minimieren und Empfehlungen abgegeben werden, die auch das Sicherheits- und Selbstwertgefühl alpinistischer Wiedereinsteiger erhöhen. Heute führen Hüftoberflächenersatzoperationen und unikondyläre Knieprothesen in der Regel zu erstaunlich guten Ergebnissen. Der Erfolg des Gelenkersatzes und die zufriedenstellende Funktionalität stehen immer in engem Verhältnis zum präoperativen Fitnessgrad und einer effizienten Rehabilitation. Bewegungskoordination und -umfang sollten unmittelbar nach der chirurgischen Intervention wiederhergestellt werden. Ein Aufbau von Kraft und Ausdauer ist ab dem 3.-6. postoperativen Monat sinnvoll. Übungen dazu sollten sich an den Bedürfnissen sowie der angestrebten Bergsportdisziplin orientieren. Präoperative Erfahrungswerte in einer Alpinsportart zählen dabei zu den wesentlichsten Faktoren eines Trainingsplanes und Trainingszieles. Bei angepasster Technik, wiedererlangter Stabilität und Bewegungssicherheit ist mit einem künstlichen Gelenk auch nahezu jede Alpinsportart wieder möglich; da-
116
von abgesehen, sollte postoperativ mit keiner neuen Alpinsportdisziplin mehr begonnen werden. Eine systematische Literaturübersicht wurde zu dieser Thematik durchgeführt. Zusätzlich geben zwei Alpinsten Auskunft über praktische Erfahrungen mit ihrem neuen Kniegelenk und ein Sportorthopäde gibt Empfehlungen für postoperative Verhaltensmaßnahmen. Schlüsselwörter: Bergsteigen, Hüftgelenkersatz (HTEP), Hüftoberflächenersatz Kniegelenkersatz (TKA), unikondyläre Knieprothese (KTEP)
EINLEITUNG
Endoprothetische Eingriffe an Knie oder Hüfte gehören heute zu den häufigsten Operationen im orthopädischen und unfallchirurgischen Bereich. Bereits im Oktober 2007 wurde die Implantation einer Hüftendoprothese in der Fachzeitschrift „The Lancet“ als Jahrhundertoperation gefeiert (1). Endoprothesen können durch altersbedingt-degenerative oder traumatische Ursachen erforderlich werden (2). Grundlegend werden bei derartigen Eingriffen die artikulierenden Gelenkpartner durch künstliche Oberflächen aus Metall, Polyethylen oder Keramik ersetzt, die der Anatomie nachempfunden sind. Wie weitreichend ein Gelenk dabei reseziert und neu aufgebaut werden muss, hängt vom Ausmaß der Schädigung und von der Stabilität des umliegenden Knochengewebes ab. Am Beispiel der Hüftprothese kann dabei nur der Femurkopf mit einer Metalloberfläche beschichtet werden (Hüftoberflächenersatz). Alternativ kann eine komplett neue Hüftgelenkpfanne eingefräst werden, die mit einem Ersatz des Femurhalses kombiniert wird. Dieser sogenannte Schaft wird im proximalen Femur verankert und mit einem Keramik-, Metall- oder Polyethylenkopf (PE-Kopf) zur Artikulation mit der neuen Pfanne versehen (klassische HTEP). Am häufigsten wird eine Indikation zur HTEP bei primär idiopathischer sowie sekundärer Koxarthrose im Rahmen verschiedener Grunderkrankungen (wie z.B. juveniler Hüftdysplasie) gestellt. Auch die Hüftkopfnekrose bei Alkohol- und Steroidabusus sowie Diabetes mellitus gilt als Indikation für die klassische HTEP. Der Indikation zur Knietotalendoprothese (KTEP) liegt meist eine über Jahre und Jahrzente vorbestehende Fehlstellung der Tragachse im Knie zugrunde (Varus- bzw. Valgusgonarthrose). Bei Knieendoprothesen handelt es sich in der Regel um einen Oberflächenersatz durch ein Femurschild, das mit einem an der proximalen Tibia befestigten sogenannten Tibiaplateau und der Patella interagiert. Zwischen diesen
117
beiden Bauteilen liegt bei der konventionellen KTEP noch ein Polyethylen-Inlay (PE-Inlay), das ein abriebfreies Gleiten der ersetzten Gelenkoberflächen ermöglicht und die Gelenkführung vermittelt. Bei ausgeprägter Arthrose des patellofemoralen Gleitlagers kann auch ein Ersatz der Gleitfläche an der Patella mittels einer PE-Beschichtung angedacht werden. Doch gibt es auch hier eine weniger invasive Prothesenvariante, bei der nur das mediale oder laterale Kompartiment des Kniegelenks mit Metalloberflächen und einem PE-Inlay versehen wird (unikondyläre Knieprothese bzw. „Hemischlittenprothese“). In der Revisions- und Tumorchirurgie wird allerdings auch ein Ersatz des gesamten distalen Femurs bis hin zu einem Femur-Totalersatz durchgeführt. Die Entscheidung, welche Prothesenbauform gewählt wird, hängt dabei von Kli-
Abb. 2: KTEP-Träger beim mit Trekkingstöcken unterstützten Abstieg (mit freundlicher Genehmigung des Patienten)

Abb. 1: Optimale Knie-TEP Versorgung rechts; radiologische Saumbildung zementbedingt (mit freundlicher Genehmigung von Univ.-Doz. Dr. G. Gruber, Univ.-Klinik für Orthopädie Graz) Abb. 3: Konventionelle KTEP (GMKprimary): Femurschild in Artikulation mit PE belegtem Tibiaplateau (mit freundlicher Genehmigung der Firma Vivamed, Salzburg)
118
nik, radiologischem Befund und dem Patientenwunsch nach postoperativer Belastbarkeit ab. Das Ziel dieser, doch sehr großen, Eingriffe ist die Wiederherstellung alltagstauglicher und schmerzfreier Bewegungsabläufe. Traditionell waren derartige Operationen einem älteren vielfach körperlich inaktiven Patientenkollektiv vorbehalten. Für diese Patienten stand die Wiederherstellung der Lebensqualität im Vordergrund ohne auf sportliche Aktivität zu fokussieren. Der Entschluss zur Endoprothese sollte jedoch immer erst als „ultima ratio“ nach Ausschöpfung aller konservativen Therapiemaßnahmen fallen. Mit der sportlichen Belastung einer Endoprothese geht immer die Angst vor einer Prothesendislokation, -lockerung oder -infektion einher. Den „worst case“ stellt ein Bruch von Prothesenkomponenten bzw. der knöchernen Einbettung (periprothetische Fraktur) dar. Prothesendislokationen treten zu 90% im Rahmen von Alltagsbewegungen während der ersten drei postoperativen Monate auf (3, 4). Eine HTEP hat aufgrund des erhöhten Bewegungsumfanges ein erhöhtes Dislokationsrisiko gegenüber der KTEP. HTEP-dislokationen kommen in 3-5% aller HTEPs vor und machen 20% der Revisionsoperationen an der künstlichen Hüfte aus (3). Die gefürchtetste Spätkomplikation und zugleich der häufigste Revisionsgrund sind aseptische Prothesenlockerungen. Pathogenetisch ist dafür ein verstärkter Abrieb von Knochenzement bzw. von Prothesenmaterial verantwortlich. Oftmals ziehen diese nicht resorbierbaren Abriebpartikel entzündliche Reaktionen im Prothesenbett nach sich. Periprothetische Entzündungsreaktionen können zu osteolytischen, granulomatösen oder zystischen Veränderungen sowie einer Hemmung der Osteoblastenaktivtät führen, wodurch die ossäre Integrität des Implantats gestört wird.
METHODIK
Die Literaturrecherche erfolgte in PubMed. Der Suchaufbau umfasste die Kombination von endoprothetischen Operationstechniken und Endoprothesen (z.B. KTEP „OR“ HTEP „AND“ mountainieering) mit verschiedenen Formen des Alpinsports. Zur Illustration fanden Einzelfallinterviews mit Alpinisten (<80 Jahre) statt, die ein künstliches Gelenk erhalten hatten. Bedingung für die Auswahl der Einzelfälle war das Vorliegen einer Primärimplantation, die zum Befragungszeitpunkt länger als sechs Monate zurückliegen musste. Zur möglichst vergleichbaren Befragung der betroffenen Alpinsportler wurde ein fünfteiliger Fragebogen entworfen. Im ersten Teil wurden Daten zur Person des Bergsportlers sowie der Operation und der Prothese erhoben. In einem
119
zweiten Teil wurde das Aktivitätsniveau zum aktuellen Zeitpunkt erhoben. Der UCLA-Aktivitätsscore (University of California, Los Angeles) erschien dafür am geeignetsten (5). Der dritte Teil betraf Patienten mit Knieendoprothesen. Als Scoring System diente hier sowohl der zweiteilige „Knee-Society-Score“ (Knee-Score/ Function-Score) sowie der kniespezifische „WOMAC-Score“ (Western Ontario and McMaster Universities Arthritis Index) (6, 7). Der vierte Teil bildete das Hüftäquivalent zu Teil drei, wobei der „Harris-Hip-“ (8) und der hüftspezifische „WOMAC-Score“ zur Anwendung kamen (7). Diese breite Auswahl an standardisierten Scores misst sowohl den Bewegungsumfang im operierten Gelenk wie auch die Sicherheit im Alltag. Zur Auswertung aller Scores wurde die Website www.orthopedicscores.com herangezogen (9). Im Anschluss daran wurden spezifische Fragen zum Thema Alpinsport gestellt z.B. eine Frage nach den praktizierten Bergsportdisziplinen und der Intensität. Als Vorlage hierzu diente ein Fragebogen, der im Jahre 1999 im Jahrbuch der österreichischen Gesellschaft für Höhen- und Alpinmedizin publiziert wurde (10). Im Wesentlichen wurde der Fragebogen übernommen und durch einige weitere Antwortmöglichkeiten ergänzt.
ERGEBNISSE
Aus der Literaturrecherche ergaben sich 1936 Artikel, von denen 110 für diese Übersichtsarbeit relevant erschienen. Davon waren 28 Publikationen weder in Deutsch noch Englisch verfügbar. Während der Volltextsichtung der verbleibenden 82 Artikel zeigte sich in 22 Publikationen trotz thematischen Bezuges keine Aktualität. Insgesamt verblieben nach der Volltextanalyse 52 PubMed-Beiträge zur Auswertung; es ergab sich daraus nachfolgender Konsens: In den vergangenen zehn Jahren war in Deutschland und den USA ein drastischer Anstieg an elektiv und primär implantierten Hüft- und Kniegelenkprothesen (HTEP/KTEP) zu verzeichnen. In Deutschland zeigte sich für die HTEP zwischen 2005 und 2011 eine um 11% gesteigerte Eingriffszahl. In den USA fiel dieser Anstieg mit 28% im selben Zeitraum noch deutlicher aus. Ebenso nahmen im selben Zeitraum die KTEPs in beiden Ländern mit einem Zuwachs an Eingriffen von 22% (D) bzw. 30% (USA) deutlich zu (11). Schätzungen zufolge wird die Nachfrage nach HTEP-Implantationen bis 2030 um 175%, nach KTEP um 675% zunehmen (12). Auch die Inzidenz beider Gelenkersatzoperationen nahm in der Altersgruppe der 50-60-Jährigen innerhalb des vergangenen halben Jahrzehntes um 50% zu (3). Die damit immer jünger
120
werdende Zielgruppe erfordert heute eine differenziertere Herangehensweise an das präoperative Assessment und an die postoperative Betreuung. Viele Alpinisten, die sich einem Gelenksersatz unterziehen mussten, hatten vor der Operation bereits den expliziten Wunsch nach einem Wiedereinstieg in den Alpinsport und knapp 20% aller Probanden einer Beobachtungsgruppe führten an, den Gelenkersatz mit dem Ziel geplant zu haben, danach wieder schmerzfrei ihren gewohnten Sportarten nachkommen zu können (13). Der Erfolg der Endoprothetik und damit das „grüne Licht“ zur erneuten Aktivität ist auf der einen Seite stark von neuen Materialien sowie der Implantationstechnik abhängig. Auf der anderen Seite sind zufriedenstellende Ergebnisse auch in hohem Maße an eine optimale postoperative Begleitung und regelmäßige Bewegung gebunden. Beide Elemente dienen der muskulären Stabilisierung und kardiovaskulären Leistungsverbesserung. Sobald die muskuläre Stabilisierung des Gelenkersatzes erreicht ist, ergibt sich für den Prothesenträger (HTEP & KTEP) ein geringeres Dislokationsrisiko des operierten Gelenks und damit die Möglichkeit einer lebenslangen Fortführung sportlicher Aktivitäten. Mit der Verbesserung von Koordination und Gleichgewicht wird zugleich das Sturzrisiko verringert. Darüber hinaus verbessert sich die Propriozeption, sodass Über- und Fehlbelastungen eher vermieden werden können. Nicht zuletzt wirkt sich regelmäßiges sportliches Training auch positiv auf die Psyche des Prothesenträgers aus, das Selbstvertrauen steigt und ängstliche Verstimmungszustände werden sukzessive abgebaut (4). Moderate sportliche Aktivität ruft zusätzlich verschiedenste anti-inflammatorische Effekte hervor und übt auf diesem Wege einen Benefit auf die postoperative Geweberegeneration aus (14). Zusätzlich verringert ein aktiver Lebensstil das Risiko periprothetischer Komplikationen durch eine Reduktion des Körpergewichtes. Bereits im Jahre 1990 fanden sich dazu in der Zeitschrift des American College of Sports Medicine Empfehlungen für Prothesenträger (15):so wurden Trainingseinheiten in der Dauer von 20–60 Minuten, 3-5mal/Woche für den Erhalt kardiovaskulärer bzw. muskulärer Leistungsfähigkeit als zielführend erachtet. Im Zusammenhang mit alpinen Sportarten wurde vor allem das Wandern empfohlen (15). Auch technisch korrektes Schifahren stellt keine außergewöhnliche Gelenkbelastung dar (16). Demgegenüber stehen die Angst vor verstärktem Abrieb von Prothesenbauteilen sowie ein erhöhtes Sturz- und Dislokationsrisiko im Rahmen von unvorhergesehenen Bewegungen. Früher wurde langfristige sportliche Belastung der Endoprothese verdächtigt, einen verstärkten Verschleiß der Prothesenbauteile nach sich zu ziehen. Neue Erkenntnisse deuten jedoch darauf hin, dass Abrieb eher als Indikator einer Überbelastung der Prothese durch fehlerhafte
121
Bewegungsmuster anzusehen ist (17). Es muss in diesem Zusammenhang jedoch auch betont werden, dass die Prothesenbelastung differenziert zu sehen ist und von der jeweiligen alpinsportlichen Disziplin abhängt. Der Beanspruchungsgrad kann von sehr hoch wie beim Klettern und Höhenbergsteigen bis zu moderat beim Bergwandern, Mountainbiking oder bei der Begehung einfacher Klettersteige reichen. Auf jeden Fall problematisch im Sinne der Gelenkbelastung sind Kampf- sowie Ballsportarten anzusehen. Auch das Körpergewicht, eine korrekte Implantation und das Prothesenmaterial sind wesentliche Faktoren für die Haltbarkeit. Die zunehmende Anwendung von Polyethylen auf künstlichen Gelenkflächen lässt prospektiv eine lange Lebensdauer erwarten (18). Das Sturzrisiko im Rahmen von alpinistischer Aktivität kann durch die Auswahl der geeigneten Bergsportdisziplin aber auch durch den Einsatz entsprechend längenadaptierter Trekking- und Wanderstöcke minimiert werden (10). Weiter wird berichtet, dass selbst ein Sturz direkt auf das künstliche Gelenk bei guter muskulärer Stabilität selten zu Schäden an Prothese bzw. ihrer Verankerung führt (19). In Bezug auf die Hüftgelenkprothesen verspricht der minimal invasive Hüft-Oberflächenersatz bei stabiler Knochenmatrix die besten Ergebnisse (20). Präzise Positionierung des Implantats und Bewegungsschulung minimieren die Abriebeffekte bei allen Formen der HTEP. Sollte es dennoch zu einer aseptischen Lockerung durch den Abrieb kommen, bietet sich im Anschluss an einen Oberflächenersatz immer noch eine einfache Erweiterung zu einer traditionellen HTEP, da die physiologische Architektur des Knochens durch den Oberflächenersatz kaum gestört wird (3). Trotz dieser theoretisch idealen Prothesenarchitektur wechseln viele Probanden postoperativ die Bergsportdisziplin. Dabei erfuhr Wandern einen postoperativen Zulauf von 10%. Der Schilanglauf nahm um +6% zu, Alpinschifahren dagegen nahm um –17% ab. Die stärkste postoperative Abnahme betrifft das Bergsteigen und Klettern. Die postoperative Abnahme in diesen Disziplinen betrug trotz Hüftoberflächenersatz -33% (21). Der wahre Grund dieses Rückganges dürfte in der Sorge vor einer Beschädigung des Kunstgelenkes liegen, womit ein gewisses Vermeidungsverhalten plausibel wird (21). Patientinnen und Patienten mit klassischer HTEP dagegen zeigten präoperativ in 36% sportliche Aktivität, postoperativ in 52%. Auch wird von HTEP-Trägern (im Vergleich zu KTEP-Trägern) Sport öfter und in längeren Einheiten ausgeübt (22-24). Insbesondere das Wandern, Radfahren und Schifahren (Alpinstil/Schitouren) erfreuen sich bei dieser Gruppe großer Beliebtheit (25).
122
Knieprothesenträger dagegen führen vermehrt Schmerzen durch ihr neues Gelenk als Begründung für ihren sportlichen Rückzug an (23). Die Anzahl aktiv Sporttreibender ging von präoperativ 42% auf 34% postoperativ zurück (24). Eine Ausnahme bilden dabei die Träger unikondylärer Knieprothesen mit einer Sport-Wiedereinstiegsrate innerhalb der ersten postoperativen 18 Monate von 97% (18,24-27). Da diese Form der Knieprothese durch ihre Spezifität eine sehr geringe Indikationsbreite aufweist, wird sie sehr selten eingesetzt. Bezüglich der Revisionsrate wird die unikondyläre Prothese von jener der KTEP in neueren Studien unterboten (28). Somit bleibt eine Versorgung mittels unikondylärer Prothese eher Sonderfällen vorbehalten. Der operative Zugangsweg dürfte sowohl für HTEP wie auch KTEP bezüglich des postoperativen Outcome überbewertet werden. Rehabilitation und physikalische Therapie haben auf jeden Fall die größere Bedeutung (4,29,30). Bei der Befragung zweier Alpinisten mit künstlichem Knie- bzw. Hüftgelenk zeichnete sich besonders die Bedeutung der präoperativen Muskelstabilität sowie Konsequenz im Rahmen der Rehabilitation für ein hohes postoperatives Aktivitätsniveau ab. In der Literatur wird für sportliche Prothesenträger ein durchschnittliches UCLA-Aktivitätslevel von 7 beschrieben (31). Dieser Wert konnte von beiden Alpinisten mit 10 überboten werden, was einem Maximum an Aktivität mit Prothese entspricht. Für junge, präoperativ aktive Patienten mit KTEP findet sich in der Literatur ein postoperativer Knee-Society-Score von 94 Punkten für den Bewegungsumfang sowie 89 Punkte für die Funktion (31,32). Patient A (aktiver Alpinist/ KTEP) konnte diese Werte mit einer Prothesenstandzeit von 4 Jahren mit 93 und 90 Punkten bestätigen. Es liegt nahe, dass diese Werte vor allem durch präoperative Fitness, sowie regelmäßiges Training mit dem künstlichen Gelenk erreicht werden konnten. Den postulierten WOMAC-Score in Höhe von 33 Punkten (31) konnte er mit 98 Punkten deutlich überbieten. Dieses Ergebnis zeigt, dass alpinistisches Training einen unbeschwerten Alltag mit einer Prothese wie mit einem physiologischen Gelenk ermöglichen kann. Ganz außergewöhnlich zeigten sich die Ergebnisse im Harris-Hip-Score, sowie WOMAC-Score für Patient B (Alpinist/ HTEP bds.). Mit einer Prothesenstandzeit von 18 und 7 Jahren konnte er in beiden Scores jeweils das Maximum von 100 Punkten erzielen. Beide Interviewpartner gaben an, mit ihrer Prothese wieder viele Tage in den Bergen zu verbringen ohne dabei Einschränkungen in der Bandbreite ihrer ausgeübten Bergsportdisziplinen hinnehmen zu müssen. Patient A berichtete sogar über eine Besteigung der Zugspitze mit dem neuen Kniegelenk. Patient B
123
konnte mit zwei künstlichen Hüftgelenken bereits nach 6 Wochen den 1.722 m hohen Wallberg am Tegernsee besteigen. Ein Jahr postoperativ absolvierte er einen Sprint-Triathlon (500 m Schwimmen, 20 km Mountainbike, 5 km Laufen) ohne Probleme. Als Erfolgsgeheimnis gaben beide ihren präoperativen Trainingszustand sowie ihre Eigeninitiative und Motivation in der Nachbehandlung an. Auch die Einhaltung von Regenerationsphasen wurde von beiden als wesentlich erachtet.
DISKUSSION
Es sollte berücksichtigt werden, dass die Follow-up Untersuchungen wie sie beschrieben wurden oft unterschiedlich lange (1-5 Jahre) nach dem Eingriff durchgeführt wurden (23, 24). Weiter zeigten sich unterschiedliche Beobachtungszeiträume. Wie viele Patientinnen oder Patienten ihre alpinsportliche Aktivität allein auf Grund ihrer Altersprogression niedergelegt haben, konnte nicht untersucht werden. Ebenso ist die Validität der üblicherweise verwendeten Fragebögen zu hinterfragen. Harris-Hip, WOMAC, Knee-Society und UCLA-Score stellen zwar etablierte, standardisierte orthopädische Evaluationen dar (5-7), doch Alpinsport kommt darin nicht vor. Damit sind obige Scoring-Systeme für die Erforschung der Belastungsfähigkeit einer Endoprothese im Alpinsport nur bedingt geeignet. Der Bedarf nach einem für den Bergsport adaptierten Scoring-Systems wird daraus deutlich. In weiterer Folge wäre die Untersuchung größerer Kollektive von alpinsportlichen Endoprothesenträgern mit einem adaptierten Scoring-System bei verbesserter Kontrolle von Störvariablen wünschenswert. Die Patientenzufriedenheit nach einem Gelenkersatz und die damit verbundene individuelle Lebensqualität können mit den gängigen Gelenk- und Aktivitäts-Scores nur grob objektiviert werden. Ein gutes Scoring Ergebnis muss nicht obligat mit dem erforderlichen Selbstbewusstsein verbunden sein, sportlichen bzw. alpinistischen Herausforderungen wieder gewachsen zu sein (16). Es ist für einen Prothesenträger nicht unbedingt zufriedenstellend, allein schmerzfrei zu sein, um in den Supermarkt zu gehen, wenn das künstliche Gelenk als Hindernis für Alpinsportarten angesehen wird. Als Grundtenor des Experteninterviews mit einem der führenden Orthopäden zeigte sich, dass die Entscheidung zur Endoprothese immer erst fallen sollte, wenn die Lebensqualität dramatisch eingeschränkt ist. Beschönigende Einzelfallberichte sollten dabei mit Vorsicht registriert werden. Wenn die Pro-
124
thesenkomponenten stabil verankert sind und gute Beweglichkeit sowie Achsverhältnisse bestehen, sollte in Bezug auf alpinsportliche Aktivität kaum eine Einschränkung bestehen.
Tab. 1: Empfohlene Alpinsportarten nach HTEP und KTEP (33)
Alpinistische Disziplin
Radfahren Langlauf Alpinschilauf Wandern Klettern
Hoher Empfehlungsgrad
HTEP, KTEP HTEP, KTEP
Mittlerer Empfehlungsgrad
HTEP, KTEP HTEP, KTEP HTEP, KTEP
Beim Aufbautraining macht wie so oft in der Medizin die Dosis das Gift. Ein individueller Trainingsplan, angepasst an die postoperative Situation sowie die sportlich/technischen Fähigkeiten, ist der Schlüssel zur Zufriedenheit mit dem künstlichen Gelenk. Nach dem Motto „zu Tode gefürchtet ist auch gestorben“ vermerkten Dietl und Haid im Jahrbuch Beitrag „Bergsport mit künstlichem Hüftgelenk“ kritisch: Die Empfehlung zur Belastungseinschränkung seitens des Operateurs scheint oft übertrieben und erfolgt häufig vor dem Hintergrund einer Absicherung gegen postoperative Schäden an der Prothese (10). Damit wird nämlich erreicht, dass der Patient bzgl. seiner Sportausübung verunsichert wird. Eine übertriebene Vorsicht ist kontraproduktiv und mindert die Lebensqualität des Prothesenträgers. Trotzdem sollten Kontraindikationen für den Wiedereinstieg in den Alpinsport berücksichtigt werden; zu solchen zählen Gelenkinfektionen, Implantatlockerungen, muskuläre Insuffizienz, höhergradige Gelenkinstabilität oder Revisionsendoprothesen.
Postoperative Verhaltensempfehlungen für Alpinsport:
Regelmäßige körperliche Aktivität verbessert die Muskelkraft und Ausdauer und senkt das Dislokationsrisiko signifikant. Auch Koordination, Propriozeption und Körperempfindung werden durch sportliche Betätigung gefördert (4). Diesen Aspekten entgegen steht die Angst, durch Abrieb eine aseptische Prothesenlockerung zu riskieren. Ebenso gefürchtet sind Dislokation, Implan-
125
tatbruch und periprothetische Frakturen. Der Abrieb minimiert sich durch einen guten technischen Bewegungsablauf und die Verwendung moderner Prothesenmaterialien (18). Ein Implantatbruch kommt bei modernen Prothesenbauformen sehr selten vor (13). Prothesenhaltbarkeitszeiten von über 28 Jahren sind heute bei gelenkschonender Sportausübung absolut möglich. Bei starker Gelenkbelastung werden immer noch durchschnittlich 15 Jahre guter funktioneller Haltbarkeit prognostiziert (3). Die Gefahr einer periprothetischen Fraktur beim Sport besteht allerdings immer. Das Risiko kann durch ausreichende muskuläre Stabilität und Balance verringert werden. Der Benefit sportlicher Aktivität mit einem künstlichen Gelenk ist somit unumstritten. Die individuelle Bedürfnisgerechtigkeit der therapeutischen Empfehlungen ist Grundvoraussetzung für den Erfolg; gerade Bergsportarten, die für die Partizipierenden oftmals eher Teil ihrer Identität denn reines „Workout“ darstellen, sollten nicht aus reiner Übervorsicht unterbunden werden. Präoperativ ist ein regelmäßiges Training der gelenkstabilisierenden Muskulatur wie durch Radfahren oder auch am Heimtrainer sinnvoll (10,21,34,35). Postoperativ sollte so bald als möglich mit einem zweiphasigen Aufbautraining begonnen werden (10,21,36). Als Ziel der ersten Phase sollten volles Koordinationsvermögen und ein ausreichender Bewegungsumfang stehen (36). In der zweiten Phase sollte in die Verbesserung von Kraft und Ausdauer investiert werden (36); auch in dieser Phase sind klinische Kontrolluntersuchungen im Abstand von 3-6 Monaten postoperativ vorzusehen, um die korrekte Implantatposition, eine regelrechte Osseointegration, die Beweglichkeit und das Gangbild als Grundvoraussetzungen in Hinblick auf die Sportausübung zu reevaluieren (37). Die angestrebte Alpindisziplin sollte hinsichtlich Risiko und Erfahrung diskutiert werden (10,19). Das Risiko einer Gelenkkomplikation ist bei erfahrenen Bergsteigern weit geringer (36). Eine während der Belastung neu auftretende Schmerzsymptomatik kann jederzeit einen Hinweis auf einen erhöhten Prothesenverschleiß darstellen und sollte einer Abklärung zugeführt werden (32). Zudem sollten während der gesamten Wiederaufbauphase die Trainingspläne laufend und individuell angepasst werden (10). Eine Anpassung nach Umfang und Intensität kann bei entsprechender Bewältigung zeitnahe erfolgen, jedoch nicht um jeden Preis. Es sollte beim Patienten Verständnis dafür geschaffen werden, dass eine Gelenkendoprothese zwar hoch belastbar ist, der Aufbau der erforderlichen muskulären Stabilität jedoch Zeit beansprucht (38). Für den Volkssport Schifahren gibt die Literatur die ausführlichsten Empfehlungen. 63% der Prothesenträger mit einem Hüft-Oberflächenersatz sind
126
bereits 33 Wochen postoperativ wieder auf Alpinschi aktiv. Die meisten Probanden in dieser Gruppe konnten bereits wieder nach 22 Wochen dem Langlaufsport nachgehen (39). Der Schilanglauf verzeichnete postoperativ sogar einen Zulauf von 6% (21). Beim Alpinschifahren werden gut präparierte nicht kupierte Pisten mit weitem Kurvenradius empfohlen (34,40). Bei Beachtung dieser Empfehlungen lässt sich die Gelenkbelastung nach HTEP um zwei Drittel reduzieren. Auch die Erfahrung des Einzelnen spielt hier wieder eine große Rolle. So ist beispielsweise ein routinierter Alpinschifahrer postoperativ imstande, die am Knie mit bis zu 10-fachem Körpergewicht wirksamen Kräfte auf das 4-fache Körpergewicht zu reduzieren (41). Für Schibergsteiger mit Endoprothese sind kurze, drehfreudige Freeride-Schi zu empfehlen. Das Schifahren im Alpinstil, sowie Tourengehen und Langlaufen sind also mit HTEP und KTEP und bei guter Technik durchaus wieder möglich (42). Zwei bis drei Trainingseinheiten pro Woche am Hang zeigten bereits positive Effekte auf die körperliche Fitness (16) und eine deutliche Reduktion des Sturzrisikos (42,43). Wanderungen in einfachem Terrain können in den ersten Wochen nach dem Eingriff durchaus bewältigt werden. Hohe Belastungen wie beispielsweise Sprünge sollten jedoch in den ersten Monaten vermieden werden (33,36). Postoperativ ergibt sich für leichtes Wandern ein Zulauf von 10% gegenüber der präoperativen Situation (21). Bergauf können im Knie Belastungen bis zum 5-fachen des Körpergewichts auftreten, bergab sogar bis zum 8-fachen. Das entspricht einer tibiofemoralen Belastung wie bei langsamem Laufen (15). Diese Krafteinwirkungen treten bei Flexionswinkeln von 40°-60° auf, wobei viele Implantatmodelle in diesem Bereich eine schlechte Kraftübertragung aufweisen; dadurch können 40% bis 70% der gesamten Kontaktfläche überbelastet sein, was eine zusätzliche Materialabnützung bedeuten kann (15). Die Verwendung von Teleskopstöcken beim Bergabgehen ist daher besonders für KTEP-Träger sehr zu empfehlen. Die am Knie wirkenden Kräfte können durch diese Maßnahme um 20% reduziert werden (15); Belastungen am Hüftgelenk verhalten sich ähnlich. Zudem sollte das Rucksackgewicht gering gehalten werden (15). Werden diese Empfehlungen berücksichtigt, können Spaziergänge in einfachem Gelände unmittelbar postoperativ bewältigt werden. Bei guter Vorerfahrung und umsichtiger Belastung sollte Wanderungen mit künstlichem Knie- bzw. Hüftgelenk nichts entgegenstehen. Mountainbiking ist ideal, um schnell wieder an die Berge zu kommen. Die Zahl der Biker erhöhte sich nach einem Hüft-Oberflächenersatz um 3% (44). Im Vergleich zu einfachem Gehen reduziert Radfahren die tibiofemoralen
127
Kompressionskräfte deutlich; damit ist auch weniger Prothesenverschleiß zu erwarten. Eine korrekte Einstellung der Sattelhöhe ist dabei unbedingt erforderlich; der Sattel sollte so hoch wie möglich gestellt werden (15,34,35). Eine leichte Übersetzung führt zusätzlich zu einer Reduktion der Druckbelastung im Kniegelenk (10). Die Verwendung eines Mountainbikes mit elektrischer Unterstützung ist für die erste postoperative Zeit anzudenken; für eine Empfehlung fehlt jedoch noch ausreichende Evidenz. An der Kletterwand können Schnellkraft sowie Kraftausdauer, Koordination und Propriozeption trainiert werden (45). Starke Krafteinwirkungen im Rahmen von hohen Stürzen sollten vermieden werden. In diesem Zusammenhang ist eine enge Routenabsicherung sowie Klettern im Nachstieg empfehlenswert (10,36). Training an der Kletterwand (therapeutisches Klettern) hat sich als erfolgversprechend erwiesen, nicht nur für Bergsportler. Griffe und Tritte einer Kletterwand können dabei variiert und an individuelle Bedürfnisse angepasst werden (45). Die Erfahrung hat gezeigt, dass die Ausübung einer alpinsportlichen Disziplin, die vor der Prothesenimplantation beherrscht wurde, auch postoperativ wieder möglich ist. Die technische Beherrschung der sportartspezifischen Bewegungsabläufe sollte bereits präoperativ gegeben sein, um postoperativ erneute Ausübung sicher zu ermöglichen. Die Gelenkbelastung wird durch mangelnde Technik wesentlich vergrößert (15,36). Als Konsequenz wird vom Erlernen einer neuen Disziplin nach Prothesenimplantation abgeraten (19). Engmaschige Funktionskontrollen und eine gute Kommunikation mit dem betreuenden Orthopäden verbessern das Langzeitergebnis. Es ist zu empfehlen, bereits vor dem Gelenkersatz die postoperativen Erwartungen mit dem orthopädischen Betreuerteam zu besprechen. Ein hoher Fitnessgrad sowie präoperatives kardiovaskuläres Training und Aufbau der gelenkstabilisierenden Muskulatur durch Bergaufgehen, Bergradfahren oder auch mittels Physiotherapie verbessern den postoperativen Outcome deutlich (10). Informationen über Rehabilitationsmöglichkeiten sollen frühzeitig eingeholt und die Planung der Nachbehandlung bereits vor dem operativen Eingriff begonnen werden. Lagegefühl und Koordination können postoperativ bereits im Bett trainiert werden. Sportarttypische Bewegungsabläufe können ebenso in das Physiotherapieprogramm integriert werden (43). Mit zunehmender Belastbarkeit sollten auch Schnellkraft und Kraftausdauer optimiert werden, etwa durch leichte Mountainbike-Touren. Besonderes Augenmerk sollte dem Aufwärmen und Dehnen gewidmet werden. Die Ausrüstung sollte dem Kunstgelenk Rechnung tragen, etwa durch den Umstieg auf einen kürzeren Freeride-Ski. Zudem kann
128
beim Tourengehen und Mountainbiking ein Hüftschutz sinnvoll sein. Auch auf Berg- und Trekkingschuhe mit gut dämpfenden Sohlen sowie einen nicht zu schweren Rucksack sollte geachtet werden. Vernünftiges Verhalten von Seiten des Alpinsportlers ist die Grundvoraussetzung für jegliche alpine Aktivität, denn alle Bergsportarten können potentiell gefährlich sein, wenn sie ohne gute Abschätzung situationsbedingter Risiken ausgeübt werden. Der Prothesenträger sollte versuchen, ein Gefühl für potentiell schädigende Belastungen und Bewegungsvorgänge zu entwickeln und Sprünge, Stürze sowie extreme Verdrehungen des ersetzten Gelenks vermeiden. Ein sicheres und sturzfreies Gehen, Klettern und Skilaufen sollte angestrebt werden. Die sportlichen Herausforderungen sollten postoperativ stets eine Stufe niedriger als vor der Operation gewählt werden. Bei sorgfältiger Vorbereitung und Achtsamkeit kann das Risiko der Prothesenschädigung bei nahezu allen Formen des Alpinsports gering gehalten werden (36). Damit kann bewusst ausgeübter Bergsport auch mit künstlichem Gelenk ganz wesentlich zur Lebensqualität beitragen.
LITERATUR
(1)
(2)
(3)
(4)
(5)
(6)
(7) Learmonth I.D., Young C., Rorabeck C. The operation of the century: total hip replacement. The Lancet 2007; 370(9597): 1508–1519. Claes L. Herausgeber. AE-Manual der Endoprothetik:Hüfte und Hüftrevision. Springer Verlag, Heidelberg 2012: 91-123. Meira E.P., Zeni J. Sports participation following total hip arthroplasty. Int J Sports Phys Ther 2014; 9(6): 839–850. Golant A., Christoforou D.C., Slover J.D., Zuckerman J.D. Athletic participation after hip and knee arthroplasty. Bull NYU Hosp Jt Dis 2010; 68(2): 76–83. Naal F.D., Impellizzeri F.M., Leunig M. Which is the Best Activity Rating Scale for Patients Undergoing Total Joint Arthroplasty? Clin Orthop 2009; 467(4): 958–965. Dinjens R.N., Senden R., Heyligers I.C., Grimm B. Clinimetric quality of the new 2011 Knee Society score: high validity, low completion rate. The Knee 2014; 21(3): 647–654. Giesinger J.M., Hamilton D.F., Jost B., Behrend H., Giesinger K. WOMAC, EQ-5D and Knee Society Score Thresholds for Treatment Success After Total Knee Arthroplasty. J Arthroplasty 2015; 30(12): 2154–2158.
129
(8) Nilsdotter A., Bremander A. Measures of hip function and symptoms: Harris Hip
Score (HHS), Hip Disability and Osteoarthritis Outcome Score (HOOS), Oxford Hip
Score (OHS), Lequesne Index of Severity for Osteoarthritis of the Hip (LISOH), and
American Academy of Orthopedic Surgeons (AAOS) Hip and Knee Questionnaire.
Arthritis Care Res 2011; 63 Suppl 11: 200-207. (9) Orthopaedic Scores Home Page [Internet]. [zitiert 22. August 2016]. Verfügbar unter: http://www.orthopaedicscore.com/ (10) Dietl W., Haid C. Bergsport mit künstlichem Hüftgelenk. In: Jenny E., Flora G., Berghold F., Straub G. (Hrsg). Jahrbuch 1999 der Österreichischen Gesellschaft für Alpin- und Höhenmedizin, Raggl digital graphic + print GmbH, Innsbruck, 1999; 73-84. (11) Wengler A., Nimptsch U., Mansky T. Hip and knee replacement in Germany and the
USA: analysis of individual inpatient data from German and US hospitals for the years 2005 to 2011. Dtsch Ärztebl Int. 9 2014; 111(23–24): 407–416. (12) Kurtz S.M., Ong K.L., Lau E., Bozic K.J. Impact of the economic downturn on total joint replacement demand in the United States: updated projections to 2021. J Bone
Joint Surg Am 2014; 96(8): 624–630. (13) Bloomfield M.R., Hozack W.J. Total hip and knee replacement in the mature athlete.
Sports Health 2014; 6(1): 78–80. (14) Szostak J., Laurant P. The forgotten face of regular physical exercise: a „natural“ anti-atherogenic activity. Clin Sci (Lond). 2011; 121(3): 91–106. (15) Kuster M.S., Spalinger E., Blanksby B.A., Gächter A. Endurance sports after total knee replacement: a biomechanical investigation. Med Sci Sports Exerc 2000; 32(4): 721–724. (16) Amesberger G., Müller E., Würth S. Alpine Skiing With total knee ArthroPlasty (AS-
WAP): physical self-concept, pain, and life satisfaction. Scand J Med Sci Sports 2015; 25 Suppl 2: 82–89. (17) Schmalzried T.P., Shepherd E.F., Dorey F.J., Jackson W.O., dela Rosa M. et al. The John
Charnley Award. Wear is a function of use, not time. Clin Orthop 2000; (381): 36–46. (18) Selvarajah E., Hooper G., Grabowski K., Frampton C., Woodfield T.B..F, Inglis G. The rates of wear of X3 highly cross-linked polyethylene at five years when coupled with a 36 mm diameter ceramic femoral head in young patients. Bone Jt J 2015; 97–B(11): 1470–1474. (19) Niederle P., Knahr K. Sporting activities following total hip and knee arthroplasty.
Wien Med Wochenschr 2007; 157(1–2): 2–6. (20) Hallert O., Li Y., Brismar H., Lindgren U. The direct anterior approach: initial experience of a minimally invasive technique for total hip arthroplasty. J Orthop Surg 2012; 7: 17.
130
(21) Naal F.-D., Maffiuletti N.A., Munzinger U., Hersche O. Sports after hip resurfacing arthroplasty. Am J Sports Med 2007; 35(5): 705–711. (22) Bourne R.B., Chesworth B., Davis A., Mahomed N., Charron K. Comparing patient outcomes after THA and TKA: is there a difference? Clin Orthop 2010; 468(2): 542–546. (23) Huch K., Müller K. a. C., Stürmer T., Brenner H., Puhl W., Günther K.-P. Sports activities 5 years after total knee or hip arthroplasty: the Ulm Osteoarthritis Study. Ann
Rheum Dis 2005; 64(12): 1715–1720. (24) Williams D.H., Greidanus N.V., Masri B.A., Duncan C.P., Garbuz D.S. Predictors of participation in sports after hip and knee arthroplasty. Clin Orthop 2012; 470(2): 555–561. (25) Hopper G.P., Leach W.J. Participation in sporting activities following knee replacement: total versus unicompartmental. Knee Surg Sports Traumatol Arthrosc Off J ESS-
KA 2008; 16(10): 973–979. (26) Fisher N., Agarwal M., Reuben S.F., Johnson D.S., Turner P.G. Sporting and physical activity following Oxford medial unicompartmental knee arthroplasty. The Knee 2006; 13(4): 296–300. (27) Pietschmann M.F., Wohlleb L., Weber P., Schmidutz F., Ficklscherer A. et al. Sports activities after medial unicompartmental knee arthroplasty Oxford III-what can we expect? Int Orthop 2013; 37(1): 31–37. (28) Wiik A.V., Manning V., Strachan R.K., Amis A.A., Cobb J.P. Unicompartmental knee arthroplasty enables near normal gait at higher speeds, unlike total knee arthroplasty.
J Arthroplasty 2013; 28(9 Suppl): 176–178. (29) Queen R.M., Appleton J.S., Butler R.J., Newman E.T., Kelley S.S. et al. Total hip arthroplasty surgical approach does not alter postoperative gait mechanics one year after surgery. PM R 2014; 6(3): 221–226 (30) Varela-Egocheaga J.R., Suárez-Suárez M.A., Fernández-Villán M., González-Sastre
V., Varela-Gómez J.R., Murcia-Mazón A. Minimally invasive hip surgery: the approach did not make the difference. Eur J Orthop Surg Traumatol Orthopédie Traumatol 2013; 23(1): 47–52. (31) Meftah M., Ranawat A.S., Sood A.B., Rodriguez J.A., Ranawat C.S. All-polyethylene tibial implant in young, active patients a concise follow-up, 10 to 18 years. J Arthroplasty 2012; 27(1): 10–14. (32) Mont M.A., Marker D.R., Seyler T.M., Jones L.C., Kolisek .FR., Hungerford D.S.
High-impact sports after total knee arthroplasty. J Arthroplasty 2008; 23(6 Suppl 1): 80–84. (33) Clifford P.E., Mallon W.J. Sports after total joint replacement. Clin Sports Med 2005; 24(1): 175–186.
131
(34) Breugem S.J.M., Haverkamp D., Sierevelt I.N., Stibbe A.B.O., Blankevoort L., van Dijk
C.N. The important predictors of cycling use in three groups of knee patients. Disabil
Rehabil 2011; 33(19–20): 1925–1929. (35) Swanson E.A., Schmalzried T.P., Dorey F.J. Activity recommendations after total hip and knee arthroplasty: a survey of the American Association for Hip and Knee Surgeons. J Arthroplasty 2009; 24(6 Suppl): 120–126. (36) Peters P. Mountain sports and total hip arthroplasty: a case report and review of mountaineering with total hip arthroplasty. Wilderness Environ Med 2003; 14(2): 106–111. (37) Berghold .F, Brugger H., Burtscher M., Domej W., Durrer B., Fischer R.et al (Hrsg.).
Alpin- und Höhenmedizin, Springer Verlag, Wien 2015: 73–74. (38) Bradbury N., Borton D., Spoo G., Cross M.J. Participation in sports after total knee replacement. Am J Sports Med 1998; 26(4): 530–535. (39) Banerjee M., Bouillon B., Banerjee C., Bäthis H., Lefering R., et al. Sports activity after total hip resurfacing. Am J Sports Med 2010; 38(6): 1229–1236. (40) Gschwend N., Frei T., Morscher E., Nigg B., Loehr J. Alpine and cross-country skiing after total hip replacement: 2 cohorts of 50 patients each, one active, the other inactive in skiing, followed for 5-10 years. Acta Orthop Scand 2000; 71(3): 243–249. (41) Kuster M.S. Exercise recommendations after total joint replacement: a review of the current literature and proposal of scientifically based guidelines. Sports Med Auckl
NZ. 2002; 32(7): 433–445. (42) Pötzelsberger B., Stöggl T., Scheiber P., Lindinger S.J., Seifert J. et al. Alpine Skiing
With total knee ArthroPlasty (ASWAP): symmetric loading during skiing. Scand J
Med Sci Sports 2015; 25 Suppl 2: 60–66. (43) Rieder F., Kösters A., Wiesinger H.-P., Dorn U., Hofstaedter T. et al. Alpine Skiing
With total knee ArthroPlasty (ASWAP): muscular adaptations. Scand J Med Sci Sports 2015; 25 Suppl 2: 26–32. (44) Banerjee M., Bouillon B., Banerjee C., Bäthis H., Lefering R. et al. Sports activity after total hip resurfacing. Am J Sports Med 2010; 38(6): 1229–1236. (45) Lazik D., Bernstädt W., Kittel R., Luther S. Herausgeber. Therapeutisches Klettern.
Thieme Verlag Stuttgart 2008.
132
❙ Lukas Höllrigl, Jörg Fessler, Martin Burtscher ❙
Auswirkungen einer mehrtägigen Nitratsupplementierung auf die Ausdauerleistungsfähigkeit in akuter Hypoxie
Effects of nitrate supplementation on endurance performance under acute hypoxic conditions
SUMMARY
Various studies have examined the effects of nitrate supplementation on performance capacity over the past years. A great number of studies found an improved economy of locomotion, an increased continuous performance limit, and an improvement in peak power output (PPO). Especially under hypoxic conditions an increased plasma nitrite reservoir and the connected NO availability seem to have a positive effect. This hypoxia can be caused by high intense exercise and by exposure in high altitudes. There is a lack of evidence because only few studies have examined the effects of an NO supplement under normobaric or hypobaric hypoxia so far. This study was designed as a double-blind placebo controlled crossover trial. 10 female and 15 male physically active subjects (maximal oxygen uptake 49.9 ml/ min/kg) participated in the study. Over a period of three weeks the participants performed an incremental exercise test in normoxia followed by two time-trials (16.1 km) on a cycle ergometer under normobaric hypoxia. Five days before each time-trial the subjects started supplementing the 400 mg NO3 - in form of (sodium nitrate) capsules or the placebo which appeared to be the same. The study showed no significant improvement of the mean power during the time-trial caused by sodium nitrate. Likewise, the cardiorespiratory values and blood lactate showed no difference between the two different supplementations. The same applied to the received perception of exertion of the participants.
133
The present study showed no considerable effects caused by sodium nitrate. However, consulting other recent studies a high potential of an additional nitrate supplementation under hypoxic conditions may be effective. Therefore, further studies are necessary. The different results may be caused by the type of subject, including age, diet, different levels of hypoxia, health and fitness status, intensity and duration of the workload. Keywords: high altitude, nutrition, endurance sports
ZUSAMMENFASSUNG
Unzählige Studien befassten sich während der letzten Jahre mit den Auswirkungen einer Nitratsupplementierung auf die sportliche Leistungsfähigkeit. Eine große Anzahl von Untersuchungen konnte eine verbesserte Bewegungsökonomie, eine erhöhte Dauerleistungsfähigkeit als auch eine verbesserte maximale Leistungsfähigkeit feststellen. Besonders unter hypoxischen Bedingungen scheinen sich das erhöhte Plasmanitritreservoir und die damit verbundene NO-Verfügbarkeit positiv auszuwirken. Diese Hypoxie kann sowohl durch intensive Belastung als auch durch Aufenthalte in großer Höhe hervorgerufen werden. Die bis dato in deren Anzahl spärlich durchgeführten Studien in normobarer als auch in hypobarer Hypoxie lassen jedoch kein klares Bild auf die Effekte einer Nitratgabe unter diesen Bedingungen zu. Ziel dieser Arbeit war es daher, herauszufinden, ob durch eine mehrtägige Supplementierung mit Nitrat eine verbesserte Leistungsfähigkeit in akuter normobarer Hypoxie hervorgerufen werden kann. Die vorliegende Arbeit wurde als doppelblinde, placebo-kontrollierte Crossoverstudie durchgeführt. An der Untersuchung nahmen 10 weibliche und 15 männliche aktive ProbandInnen teil (maximale Sauerstoffaufnahme 49,9 ml/ min/kg). Während eines Zeitraums von drei Wochen wurde eine Spiroergometrie in Normoxie, gefolgt von zwei Zeitfahren (16,1 km) am Fahrradergometer in normobarer Hypoxie durchgeführt. Fünf Tage vor dem jeweiligen Zeitfahren nahmen die ProbandInnen täglich 400 mg NO3 , in Form einer Natriumnitrat-Kapseloder ein Placebo zu sich. Durch die Supplementierung konnte keine signifikante Veränderung der Leistungsfähigkeit beim Zeitfahren festgestellt werden. Auch bezüglich der erhobenen kardiorespiratorischen Parameter und des Blutlaktats war kein Unterschied zwischen der jeweiligen Supplementierung festzustellen. Selbiges galt für das erhobene subjektive Belastungsempfinden der Teilnehmer. In der vorliegenden Untersuchung konnten zwar keine nennenswerten Effekte, die durch das Natriumnitrat hervorgerufen werden, festgestellt werden, ande-
134
re Arbeiten können allerdings dennoch wirksame Effekte einer Nitratsupplementierung aufzeigen. Um diese Differenzen aus dem Weg zu räumen, sind in Zukunft weitere Erhebungen nötig. Eine mögliche Erklärung für diese unterschiedlichen Ergebnisse könnte eine differenziert ausgeprägte Reaktion der ProbandInnen auf das Supplement sein. Zudem bedarf es weiterer Forschung hinsichtlich der Auswirkungen des Nitrats auf unterschiedliche Personengruppen und Altersklassen, Ernährungsformen, Gesundheits- und Fitnessstatus sowie Intensität und Dauer der Belastung und Hypoxie. Schlüsselwörter: Höhe, Ernährung, Ausdauersport
EINLEITUNG
Grundsätzlich wird Nitrat bereits mit der natürlichen Ernährung zugeführt. Vor allem im Trinkwasser und in verschiedenen Gemüsesorten ist Nitrat enthalten. Speziell Salate wie Rucola, Feld- und Kopfsalat aber auch Spinat sowie Rote Beete weisen hier den größten Anteil an Nitrat auf. Auch die verwendeten Düngemittel beim Gemüseanbau lassen den Nitratgehalt in den Pflanzen variieren. Generell beträgt die Aufnahme aus natürlichen Ressourcen 50–160 mg pro Tag (2). Sehr viele aktuelle Arbeiten beschäftigen sich mit einer möglichen Leistungssteigerung in Bezug auf die Ausdauerleistungsfähigkeit, hervorgerufen durch eine zusätzliche Zufuhr von Nitrat. Diese Idee entstand durch die Entdeckung des sauerstoffunabhängigen Nitrat-Nitrit-NO-Kreislaufes, denn vorher ging man davon aus, dass NO lediglich unter Einbezug von Sauerstoff aus der Aminosäure L-Arginin synthetisiert werden kann. Wäre dies der Fall, könnte eine zusätzliche Nitrat-Zufuhr (NO3 -) zu keiner Erhöhung der NO-Verfügbarkeit führen. 2007 untersuchten Larsen et al. (3) erstmalig die Auswirkungen von Nitrat auf die Leistungsfähigkeit in Normoxie und stellte eine Senkung des Ruheblutdruckes sowie eine verbesserte Bewegungsökonomie fest. Andere Arbeiten stellten weitere positive Effekte wie eine erhöhte Dauerleistungsfähigkeit als auch vereinzelt eine erhöhte maximale Leistungsfähigkeit fest (1,4). Die Autoren dieser Arbeiten begründen dies mit einer möglichen Vasodilatation und dem damit verbesserten Blutfluss, einer verbesserten Effizienz der Mitochondrien (5) und mit einer gesteigerten Muskelkontraktilität. Immer häufiger werden sportliche Höchstleistungen, im Speziellen Ausdauerleistungen bis in große Höhen, von Athleten gefordert und von diesen auch gemeistert. Dies ist vor allem beim Skibergsteigen, Trail- u. Ultrarunning und
135
bei einigen Radsport-Veranstaltungen der Fall. Aber auch im modernen Spitzenalpinismus wird eine hoch ausgeprägte Ausdauerleistungsfähigkeit vom Bergsportler gefordert (Abb. 1), dies gilt quasi als Grundvoraussetzung für eine „Speed-Begehung“ (6).
Abb. 1: Skibergsteiger auf alpiner Trainingstour (Waze Spitze 3533 m, Pitztal, Tirol)

Einige Forschungsergebnisse aus der Vergangenheit weisen nun auf eine besondere Wirksamkeit einer Nitratsupplementierung in Hypoxie hin. So berichten Maher et al. (7) und Millar et al. (8) von einer gesteigerten Reduktion von Nitrit (NO2) zu Stickstoffmonoxid in Hypoxie (NO), dies kann durch eine Hemmung des Sauerstoffabhängigen L-Arginin-NOS Syntheseweges (Abb. 2) begründet werden. Des Weiteren weisen Höhenbewohner höhere NO3 --und NO2-Reservoirs auf (9). Im Vergleich dazu produzieren Flachländer in Hypoxie weniger NO (10). Nun kann also vermutet werden, dass eine Nitratzufuhr zu einer Erhöhung der Stickstoffmonoxid-Verfügbarkeit führen kann.
136
Einige andere Arbeiten konnten auch bereits verschiedenste positive Effekte feststellen. Beispielsweise konnte häufig eine verbesserte Bewegungsökonomie festgestellt werden (11). Aber auch andere Parameter wie die arterielle und muskuläre Sauerstoffsättigung oder die Zeit bis zur Erschöpfung zeigten signifikante Verbesserungen (12–14).

Abb. 2: Die beiden Schenkel der NO-Synthese. Einmal über die externe Zufuhr (links) und über die im Körper stattfindende Synthese aus L-Arginin und O2 (rechts). Des Weiteren sind die möglichen physiologischen Auswirkungen und deren Einfluss auf diverse leistungsbestimmende Größen dargestellt (8,9).
137
METHODIK
Die Untersuchung wurde als randomisierte, doppelblinde, placebo-kontrollierte Cross-Over-Studie durchgeführt. Die Verblindung der Präparate wurde von einer externen Person vorgenommen. Die Randomisierung der Reihenfolge wurde mittels Los gewährleistet. Von jedem Teilnehmer waren ein Vortest sowie zwei Haupttests zu absolvieren. Als Vortest wurde eine Spiroergometrie durchgeführt. Das Protokoll startete bei einer Last von 50 Watt und wurde alle 60 Sekunden um 25 Watt gesteigert (50-25-60). Vor jeder Messung erfolgte eine Eichung der Gas- und Volumensensoren. Bei dem Test war die Trittfrequenz für die Teilnehmer frei wählbar, da mit einem drehzahlunabhängigen Ergometer gearbeitet wurde. Die Werte wurden über 30 Sekunden gemittelt und anschließend tabellarisch ausgegeben. Die Maximalwerte wurden anschließend manuell aus den Tabellen entnommen. Die Haupttests wurden in Form eines Zeitfahrens auf demselben Fahrradergometer durchgeführt. Diese wurden in normobarer Hypoxie (3.500 m) über eine Distanz von 16,1 km (10 Meilen) absolviert. Die Probanden regulierten die Leistung über die gewählte Trittfrequenz und konnten das Drehmoment selbst justieren. Ziel war es, eine möglichst hohe Durchschnittsleistung über die 16,1 Kilometer zu erzielen. Das Drehmoment am Start des Zeitfahrens wurde für die Probanden so eingestellt, dass sie bei einer Trittfrequenz von 90 U/min eine Leistung erreichten, die 60% der maximalen Leistung im Vortest entsprach. Während des Zeitfahrens wurden Laktatproben bei fünf, zehn und fünfzehn Kilometern entnommen und Spirometriedaten aufgezeichnet. Die muskuläre sowie die zerebrale Sauerstoffsättigung wurden mittels Nahinfrarotspektroskopie (NIRS) aufgezeichnet, wobei der Gewebeoxygenierungsindex (TOI) und der normalisierte Gewebehämoglobinindex (nTHI) zur Auswertung herangezogen wurden. Der schematische Studienablauf ist in Abbildung 3 dargestellt.
Abb. 3: Schematisch dargestellter Verlauf der Studie im Crossover Design. Die Gruppenzuteilung erfolgte randomisiert.

138
PROBANDEN
Neun weibliche und vierzehn männliche Personen absolvierten die komplette Studie und wurden somit zur Auswertung herangezogen. Die Teilnehmer waren im Mittel 28,4 ± 6,3 Jahre alt. Das Gewicht der weiblichen Probanden lag im Mittel bei 62,2 kg, das der männlichen bei 73,4 kg. Die Maximalwerte aus dem Vortest sind in Tabelle 1 dargestellt.
Tab. 1: Leistungsparameter der Probanden (n=23) aus dem Vortest (Spiroergometrie)
Maximale Herzfrequenz [bpm] Maximale Ventilation [l/min] Minimale Sauerstoffsättigung [%] Maximale Atemfrequenz [1/min] Maximale Sauerstoffaufnahme [ml/min] Maximale Kohlendioxidabgabe [ml/min] Rel. max. Sauerstoffaufnahme [ml/min/kg] Respiratorischer Quotient bei Ausbelastung Atemäquivalent für O2 Maximale Leistung [Watt]
Mittelwert
183 147 92 58 3415 4424 49,9 1,3 43 334
Standardabweichungen 10 31 4 9 701 927 7,1 0,1 6 64
STATISTIK
Die Rohdaten der Spiroergometrie und der Infrarotspektroskopie wurden in Excel aufbereitet und synchronisiert. Um unterschiedliche Verläufe über die Zeitfahren ersichtlich zu machen, wurden diese in vier Splits zu je vier Kilometern geteilt. Die Mittelwerte aus den gesamten Zeitfahren bzw. aus den einzelnen Splits wurden nun in SPSS (IBM - Armonk, New York, USA) übertragen und zur weiteren Auswertung herangezogen. Die schließende Statistik erfolgte in SPSS. Um Veränderungen der Ruhewerte und der Gesamtdurchschnitte aufzuzeigen, wurden ANOVAs für wiederholte Messungen durchgeführt (zwei Messzeitpunkte eines Faktors). Hierbei wurde die Variable, welche die Supplementierungsreihenfolge beschreibt, als Zwischensubjektfaktor einge-
139
setzt. So konnte ein eventueller Lerneffekt festgestellt werden. Während des Zeitfahrens wurden Durchschnitte aller gemessenen Werte für Teilabschnitte zu je vier Kilometern berechnet. Für diese gemittelten Teilabschnitte sowie für die Laktatwerte wurden ebenfalls einfaktorielle ANOVAs für wiederholte Messungen berechnet, wobei auch hier die Reihenfolge der Supplementierung als Zwischensubjekteffekt miteinbezogen wurde. Zusätzlich wurde auch der Verlauf der einzelnen Parameter über die Zeitfahren mittels ANOVA mit Messwiederholungen berechnet (zwei Faktoren). P-Werte < 0,05 wurden als statistisch signifikant angesehen.
ERGEBNISSE
Ruhewerte
Nach Betreten des Hypoxiebereiches wurden unmittelbar die Ruheparameter bestimmt. Hierbei lag die arterielle Sauerstoffsättigung unter Nitratsupplementierung um zwei Prozent höher als unter Placeboeinfluss (86 vs. 84%) (F(1,21)=4,07; p=0,056; η2=0,163). Der Ruhelaktatwert war unter Nitrateinnahme signifikant um 0,22mmol/l erhöht (F(1,19)=6,47; p=0,02; η2=0,254).
Werte während der Belastung
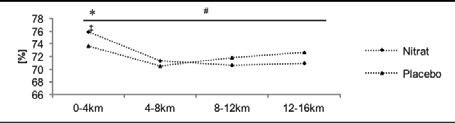
Die Laktatwerte zeigten wie in Abbildung 4 zu sehen nur nach zehn Kilometern eine signifikante Veränderung, hier war der Wert unter Nitrat höher als jener unter Placebo (10,7 vs. 9,16 mmol/l F(1,12)=8,14; p=0,01; η2=0,311).

140
Abb. 4: Verläufe der Laktatkonzentration während des Zeitfahrens über 16,1 km. Gemessen nach 5, 10 und 15 Kilometern. * signifikante Veränderung der Werte bei der Messung nach 10 km (p=0,01).
Für die Verläufe insgesamt gesehen konnte keine signifikante Veränderung festgestellt werden. Auch die mittlere Herzfrequenz sowie die durchschnittliche Leistung während der gesamten Belastung als auch innerhalb der Splits veränderten sich durch das Supplement nicht. Die Sauerstoffaufnahme sowie die Kohlendioxydabgabe haben sich wie in Tabelle 2 ersichtlich nicht verändert. Auch der respiratorische Quotient zeigte dadurch natürlich keine Veränderung. Im Verlauf der Sauerstoffsättigung zeigte sich eine Veränderung verursacht durch das Nitrat-Supplement. Auch die Sättigung während der ersten vier Kilometer des Zeitfahrens war unter Nitrateinfluss signifikant erhöht (Abb. 5).
Tab. 2: Durchschnittliche Sauerstoffaufnahme (VO2), Kohlendioxidabgabe (VCO2) und respiratorischer Quotient (RER) während des Zeitfahrens.
VO2
[ml/min]
VCO2
[ml/min]
RER Supplement
Nitrat Placebo Nitrat Placebo Nitrat Placebo
Mittelwert
2574 2458 2572 2501 0,988 1,004
Standardabweichung
651 567 682 625 0,051 0,07
p
0,208
η2
0,087
0,411 0,038
0,287 0,059
Abb. 5: Verläufe der Sauerstoffsättigung während der Split-Zeiten der Messung. ‡ Statistisch signifikanter Unterschied, verursacht durch die Reihenfolge der
Supplementierung * statistisch signifikante Veränderung während des einzelnen Splits (p<0,001). # Veränderung des Gesamtverlaufes verursacht durch das Supplement (p<0,05).
141
DISKUSSION
Generell lag die mittlere Leistung während des Zeitfahrens in etwa bei 55% der maximalen Leistung aus dem Stufentest in Normoxie. Wie Bourdillon et al. (12) konnte auch in dieser Studie während des Zeitfahrens keine Veränderung der gemittelten Leistung, hervorgerufen durch das Nitratsupplement, festgestellt werden. Im Gegensatz dazu konnten Muggeridge et al. (13) eine Verbesserung im Zeitfahren über 16,1 Kilometer um 2,9% feststellen. Hierbei muss festgehalten werden, dass sich bei Muggeridge et al. (13) die Probanden auf einer simulierten Höhe von in etwa 2.500 m (15% FiO2) belasteten und einmalig 5 mmol Nitrat supplementierten. Bourdillon et al. (12) hingegen führten die Zeitfahren bei 11% FiO2 durch und verabreichte eine Dosis von 0,1 mmol/kg über drei Tage. Von Wylie et al. (15) konnte in Normoxie festgestellt werden, dass es in Bezug auf die Leistung eine Verbindung zwischen der Nitratdosierung und der Wirksamkeit gibt (16). Diese „dose-response“-Verbindung bezüglich einer möglichen Leistungssteigerung wurde in der vorliegenden Arbeit nicht untersucht, könnte aber weitere Aufschlüsse bezüglich der Wirksamkeit geben. In anderen Arbeiten wird auch häufig von Respondern und Nonrespondern gegenüber der Wirksamkeit der Nitratsupplementierung berichtet (17). Auch dies bezieht sich lediglich auf die Leistungsfähigkeit unter normoxischen Bedingungen. Während des gesamten Zeitfahrens war die arterielle Sauerstoffsättigung nicht signifikant erhöht. Die verbesserten Sättigungswerte in Berichten aus der Literatur ergeben sich allerdings unter submaximalen Bedingungen (11). Hier könnte vermutet werden, dass unter einer längeren und dadurch submaximalen Belastung eine Verbesserung in Bezug auf die Sättigung möglich wäre. Auch der signifikant erhöhte Wert zu Beginn des Zeitfahrens deckt sich mit Ergebnissen in bisherigen Arbeiten (13). Eine verbesserte Sättigung könnte durch eine mögliche Verminderung der pulmonalen Hypertonie (Euler Liljestrand Mechanismus) begründet werden. Die Sauerstoffaufnahme war bei gleicher Leistung praktisch unverändert, dies war bei gleichbleibender Ökonomie zu erwarten. Andere Autoren stellten aber vor allem eine verbesserte Ökonomie als Hauptergebnis dar, dies geschah allerdings meist bei submaximalen Belastungen (11,14,18–21). Diese Verbesserung wird von den Autoren meist auf eine effizientere Wirkungsweise der Mitochondrien zurückgeführt. Die Laktatwerte deuten tendenziell auf einen vermehrt anaerob arbeitenden Stoffwechsel hin. Gegensätzlich dazu konnten in anderen Studien verminderte Laktatwerte festgestellt werden (22).
142
SCHLUSSFOLGERUNGEN
Die vermutete Verbesserung bezüglich der Ökonomie konnte unter der gegebenen Belastung nicht bestätigt werden. Möglicherweise wäre dies bei einer längeren, submaximalen Belastung der Fall. Die größten Tendenzen haben sich im Bereich der Sauerstoffsättigung gezeigt, hier sind unterschiedliche Dosierungen und Supplementierungsstrategien genauer zu untersuchen. Des Weiteren bleibt natürlich auch jene Vermutung im Raum stehen, dass Personen unterschiedlich auf das Nitrat reagieren und so von Respondern und Nonrespondern gesprochen werden könnte.
DANKSAGUNG
Dieses Projekt fand im Rahmen einer Masterarbeit am Institut für Sportwissenschaft der Universität Innsbruck statt und wurde von der Österreichischen Gesellschaft für Alpin- und Höhenmedizin finanziell unterstützt.
143
LITERATUR
(1) Jones A.M. Dietary nitrate supplementation and exercise performance. Sports Med 2014; 44 Suppl 1: 35–45. doi:10.1007/s40279-014-0149-y. (2) Martin H. Vom Saulus zum Paulus? UGB-Forum 2008; 2008: 245–247. (3) Larsen F.J., Weitzberg E., Lundberg J.O., Ekblom B. Effects of dietary nitrate on oxygen cost during exercise. Acta Physiol (Oxf) 2007; 191: 59–66. (4) Hoon M.W., Jones A.M., Johnson N.A., Blackwell J.R., Broad E.M., Lundy B. et al. The effect of variable doses of inorganic nitrate-rich beetroot juice on simulated 2,000-m rowing performance in trained athletes. Int J Sports Physiol Perform 2014; 9: 615–620. (5) Zafeiridis A. The Effects of Dietary Nitrate (Beetroot Juice) Supplementation on Exercise Performance: A Review. AJSS 2014; 2: 97. (6) House S., Johnston S. Training for the new alpinism: A manual for the climber as athlete. 1st ed. Ventura CA: Patagonia Books; 2014. (7) Maher A.R., Milsom A.B., Gunaruwan P, Abozguia K, Ahmed I, Weaver R.A., et al.
Hypoxic modulation of exogenous nitrite-induced vasodilation in humans. Circulation 2008; 117: 670–677. (8) Millar T.M., Kanczler J.M., Bodamyali T, Blake D.R., Stevens C.R. Xanthine oxidase is a peroxynitrite synthase: newly identified roles for a very old enzyme. Redox Rep 2002; 7: 65–70. (9) Erzurum S.C., Ghosh S., Janocha A.J., Xu W., Bauer S., Bryan N.S. et al. Higher blood flow and circulating NO products offset high-altitude hypoxia among Tibetans. Proc
Natl Acad Sci U S A 2007; 104: 17593–17598. (10) Lundberg J.O., Weitzberg E., Gladwin M.T. The nitrate-nitrite-nitric oxide pathway in physiology and therapeutics. Nat Rev Drug Discov 2008; 7: 156–167. (11) Masschelein E., van Thienen R., Wang X., van Schepdael A., Thomis M., Hespel P.
Dietary nitrate improves muscle but not cerebral oxygenation status during exercise in hypoxia. J Appl Physiol 2012; 113: 736–745. (12) Bourdillon N., Fan J.L., Uva B., Muller H., Meyer P., Kayser B. Effect of oral nitrate supplementation on pulmonary hemodynamics during exercise and time trial performance in normoxia and hypoxia: a randomized controlled trial. Frontiers in Physiology 2015; 6: 288. (13) Muggeridge D.J., Howe C.C.F., Spendiff O., Pedlar C., James P.E., Easton C. A single dose of beetroot juice enhances cycling performance in simulated altitude. Med Sci
Sports Exerc 2014; 46: 143–150. (14) Vanhatalo A., Fulford J., Bailey S.J., Blackwell J.R., Winyard P.G., Jones A.M. Dietary nitrate reduces muscle metabolic perturbation and improves exercise tolerance in hypoxia. J Physiol (Lond) 2011; 589: 5517–5528.
144
(15) Wylie L.J., Mohr M., Krustrup P., Jackman S.R., Ermιdis G., Kelly J. et al. Dietary nitrate supplementation improves team sport-specific intense intermittent exercise performance. Eur J Appl Physiol 2013; 113: 1673–1684. (16) Affourtit C., Bailey S.J., Jones A.M., Smallwood M.J., Winyard P.G. On the mechanism by which dietary nitrate improves human skeletal muscle function. Frontiers in Physiology 2015; 6: 211. (17) Boorsma R.K., Whitfield J., Spriet L.L. Beetroot juice supplementation does not improve performance of elite 1500-m runners. Med Sci Sports Exerc 2014; 46: 2326–2334. (18) Bailey S.J., Winyard P., Vanhatalo A., Blackwell J.R., Dimenna F.J., Wilkerson D.P. et al. Dietary nitrate supplementation reduces the O2 cost of low-intensity exercise and enhances tolerance to high-intensity exercise in humans. J Appl Physiol 2009; 107: 1144–1155. (19) Cermak N.M., Gibala M.J., van Loon, Luc J.C. Nitrate supplementation’s improvement of 10-km time-trial performance in trained cyclists. Int J Sport Nutr Exerc Metab 2012; 22: 64–71. (20) Larsen F.J., Schiffer T.A., Borniquel S., Sahlin K., Ekblom B., Lundberg J.O., Weitzberg
E. Dietary inorganic nitrate improves mitochondrial efficiency in humans. Cell Metab 2011; 13: 149–159. (21) Muggeridge D.J., Howe C.C.F., Spendiff O., Pedlar C., James P.E., Easton C. The effects of a single dose of concentrated beetroot juice on performance in trained flatwater kayakers. Int J Sport Nutr Exerc Metab 2013; 23: 498–506. (22) Carriker C.R., Mermier C.M., McLain T.A., Johnson K.E., Beltz N.M., Vaughan R.A., et al. Effect of Acute Dietary Nitrate Consumption on Oxygen Consumption During
Submaximal Exercise in Hypobaric Hypoxia. Int J Sport Nutr Exerc Metab 2015.
145
❙ David Morawetz, Arnold Koller, Wolfgang Schobersberger ❙
Die exzentrische Beanspruchung im Alpinsport – Effekte-Vorbereitung-Anpassung
Eccentric loading in mountain sport activities – Effects-Preparation-Adaptation
SUMMARY
This paper discusses the importance of eccentric muscle contraction in mountain sport activities. Physical stress is common in alpine terrain, but especially eccentric loading dominates in this kind of sports. Downhill running/walking, trailrunning or ski descents are predominately characterized by eccentric muscle contractions. Unaccustomed eccentric exercise leads to intensity-dependent muscle damage, strength loss and muscle soreness. The muscle forces produced during these lengthening contractions can be extremely high, despite the low energetic cost. Using the “repeated bout effect” in training, muscle soreness can be prevented or weakened. The systematic use of eccentric training modalities decreases the risk of injury, enhance performance and can be used in competitive or recreational sports. Keywords: eccentric contractions, mountain sport activities, repeated bout effect, injury prevention, metabolism
ZUSAMMENFASSUNG
Dieser Beitrag soll die Bedeutung der exzentrischen Muskelarbeit im Alpinsport und somit im alpinen Gelände aufzeigen. Trotz der allgemeinen physischen Belastung bei Bergsportaktivitäten wird der exzentrischen Belastung ein dominierender Stellenwert eingeräumt. Beim Bergabgehen/laufen, beim Trailrunning oder beim Skifahren arbeitet die Muskulatur des menschlichen Organismus in einer exzentrischen Arbeitsweise. Diese oft ungewohnten Belastungen können intensitätsabhängig in weiterer Folge zu Muskelkater und
147
lang andauernden Kraftverlusten führen. Aber die Exzentrik zeichnet sich nicht nur durch negative Effekte aus: Die metabolische Effizienz dieser Form der Muskelarbeit und die hohen Kraftzuwachsraten durch exzentrisches Training beleuchten die attraktive Seite. Mittels der Ausnützung des „Repeated Bout Effects“ können Muskelkatersymptome weitgehend verhindert oder abgeschwächt werden. Schlussfolgernd wirkt der systematische Einsatz exzentrischer Trainingsformen leistungssteigernd, verletzungspräventiv und kann sowohl im Leistungssport als auch im Breitensport eingesetzt werden. Schlüsselwörter: exzentrische Muskelarbeit, Alpinsport, Repeated Bout Effekt, Verletzungsprävention, Metabolismus
EINLEITUNG
Der Alpinsport in Österreich findet in all seinen Facetten in den letzten Jahren starken Andrang von inländischen als auch ausländischen Touristen (1). Besonders der Sommer eignet sich für lange Tagestouren oder auch mehrtägige Wanderungen und Gebirgsüberschreitungen. Die alpine Umwelt stellt jedoch hohe Anforderungen an den menschlichen Organismus. Neben den leistungsbestimmenden Faktoren wie der allgemeinen Ausdauer des Herz-Kreislaufsystems, der Kraftausdauer der Beinmuskulatur sowie der Trittsicherheit (Gleichgewicht), beeinflussen auch die Umweltfaktoren (Wetter, Wegbeschaffenheit, Höhenlage, etc.) unsere Tage in den Bergen maßgeblich (2,3). Denn ein schlecht trainierter Organismus endet meist früher als später mit einem erhöhten Verletzungsrisiko, in Erschöpfung und Ermüdung. Hingegen werden bei Personen mit einer hohen Dauerleistungsgrenze (wiederum abhängig von einer hohen VO2max) und einer guten Bewegungsökonomie, die denselben Randbedingungen ausgesetzt sind, Erschöpfung und Ermüdung später relevant werden (2,4,5). Ein Faktor, der trotz allem im Bergsport wenig Beachtung findet und vielleicht auch als Besonderheit angesehen werden darf, ist die exzentrische Belastung. Doch was wird unter exzentrischer Belastung im Alpinsport verstanden? Das Ziel dieses Artikels ist es, die exzentrische Arbeitsweise der Muskulatur genauer zu erläutern und dabei die gewünschten und auch nicht gewünschten Effekte, die in alpiner Umgebung auftreten können, zu beschreiben. Fakt ist jedoch, dass exzentrische Belastungen zu langanhaltenden Kraftverlusten und Ermüdung führen (6). Ob dies möglicherweise sogar einen Risikofaktor für Verletzungen darstellt, wird im weiteren Verlauf dieses Beitrags versucht, zu klären. Praxisrelevante Hinweise zur Vorbeugung und
148
weitgehenden Verhinderung von exzentrischer Ermüdung werden am Ende des Artikels dargelegt.
DIE EXZENTRISCHE ARBEITSWEISE UND IHRE EFFEKTE

Im alpinen Umfeld arbeitet die Muskulatur des menschlichen Organismus dann exzentrisch, wenn es darum geht, das eigene Körpergewicht kontrolliert in der Vertikalen abzubremsen und sich gleichzeitig horizontal fortzubewegen. Mit Beispielen belegt bedeutet dies: beim Bergabgehen, beim Bergablaufen, beim Alpinskilauf oder während der Abfahrt von Skitouren. Bei der exzentrischen Arbeitsweise ist nun die dem Muskel entgegengesetzte Last größer als die Kraft, welche der Muskel selbst aufbringt und so kommt es zu einer Dehnung des Muskel-Sehnensystems: Muskelansatz und -ursprung entfernen sich voneinander. Man kann dies auch als eine Verlängerung oder Streckung des Muskels bezeichnen. Dabei kann die Größe der entgegengesetzten Last das isometrische Kraftmaximum um bis zu 40% übersteigen (7–9). Wird nun dem Muskel eine Last entgegengesetzt, so wird Energie frei, die entweder als Wärme abtransportiert oder als elastische Energie gespeichert wird. Die Abgabe von Wärme ist beim Abwärtsgehen eines steilen Hanges der hauptsächliche Effekt der bewegten Muskulatur, die somit nur absorbierend funktioniert. Denn beispielsweise absorbiert eine 70kg schwere Person, die 500 Höhenmeter (Hm) absteigt ~350 kJ an Energie, die ausreicht die Körpertemperatur stark zu heben (10).
Abb. 1: Flugphase im Bergablauf. Die Beinmuskulatur des Bergläufers erfährt durch die kurze Impactdauer eine starke exzentrische Belastung.
149
© David Morawetz
Energie, welche der Muskel hingegen aufnimmt und folglich speichert (im Muskel-Sehnenkomplex), spielt in der Fortbewegung eine große Rolle, da sie in der darauffolgenden Muskelaktion freigesetzt wird und diese positiv unterstützt. Jener Ablauf wird in der Literatur auch als Dehnungs-Verkürzungszyklus (DVZ) beschrieben (10–12). Vereinfacht ausgedrückt: Eine Kombination aus einer kurzen exzentrischen und darauf folgenden konzentrischen Muskelarbeit stellt die klassische Form des Dehnungs-Verkürzungszyklus dar. Während der exzentrischen Phase wird die freigesetzte Energie im Muskel-Sehnen-System gespeichert und unterstützt nachstehend die konzentrische Bewegung.
(a) Voraktivierung
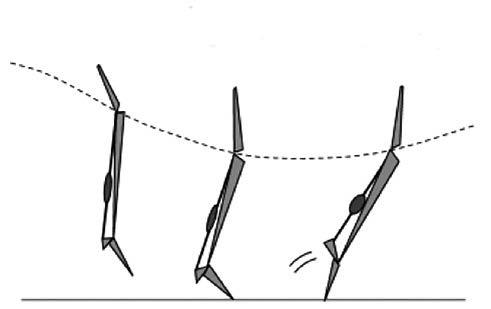
(b) Dehnung
(c) Verkürzung
Abb. 2: Dehnungs-Verkürzungs-Zyklus einer Lauf-/Sprungbewegung mit a) Voraktivierungsphase, b) Dehnungsphase und c) konzentrischer Phase (mod. Komi, 2000.)
Anhand der Impactdauer wird grundsätzlich zwischen langem und kurzem DVZ unterschieden. Als Beispiel für einen langen DVZ kann die Sportart Skifahren herangezogen werden. Diese Bewegung ist gekennzeichnet durch eine eher langsamere geschmeidigere Dehnungsphase, die sich folglich auch minder schädigend auf die Muskulatur auswirkt. Während hingegen ein kurzer DVZ (50–120 ms), wie er beim Laufen auftritt, eine intensivere Belastung für die Muskulatur darstellt und daraus resultierend längere Regenerationszeiten verlangt (11,12).
150
Bezüglich der neuralen Ansteuerung kann festgehalten werden, dass die exzentrische Kontraktion im Vergleich zur konzentrischen oder isometrischen Arbeitsweise in ihrer Stärke und ihrem Umfang deutlich vermindert ist. Darüber hinaus konnte festgestellt werden, dass es durch das kurzzeitige Überschreiten der Belastungstoleranz zu einem stärkeren Einsatz der hochschwelligen motorischen Einheiten (bei FT-Fasern) kommt (13,14). Durch die geringere Innervation der Muskelfasern zeigt sich unter anderem daraus resultierend eine sehr hohe metabolische Effizienz. Vergleiche bei maximalen Kraftausdauertests zwischen den unterschiedlichen Arbeitsweisen der Muskulatur wiesen darauf hin, dass der geringe metabolische Aufwand durch höhere erreichte Kraftwerte, durch eine langsamere Ermüdung und durch niedrigere Laktatwerte bei exzentrischer Arbeitsweise bestätigt wird. Bei Gegenüberstellungen von konzentrischen und exzentrischen Wiederholungszahlen konnte ferner bestätigt werden, dass exzentrisch sogar bis zum Siebenfachen mehr Wiederholungen ausgeführt werden konnten. Diese Ermüdungsresistenz soll die metabolische Effizienz deutlich unterstreichen (15–17). Ein weiterer Effekt, der bedingt durch die oft ungewohnte exzentrische Arbeitsweise der Muskulatur auftritt, sind Muskelkatersymptome. Diese treten durch Muskelschädigungen auf. Grundsätzlich betreffen diese Schädigungen die Sarkomere im Muskel, wobei auch noch andere Strukturen involviert sind. Da nicht alle Sarkomere gleich stark gebaut sind und sich so unterschiedlich resistent gegen Dehnung verhalten, kommt es zuerst zu Rupturen an den schwächeren Sarkomeren, bis schlussendlich auch die stärkeren überdehnt werden. Die Schädigung der muskulären Struktur kann sich darüber hinaus ausbreiten und so angrenzende Bereiche, wie die Membran des sarkoplasmatischen Retikulums, die transversalen Tubuli oder das Sarkolemm schädigen (18). Gleichzeitig werden jedoch auch Reparaturmechanismen ausgelöst, die die zerstörten Muskelstrukturen reparieren. Diese Rupturen an den Sarkomeren führen zu einer Abnahme der Muskelkraft, zu einer verringerten Bewegungsamplitude (Range of Motion (ROM)) sowie zu Muskelschmerzen in Bewegung oder bei Berührung. Zusätzlich ist es Faktum, dass je größer die Bewegungsamplitude, je höher die Geschwindigkeit und je mehr Last bewegt wird, desto stärker fallen die Muskelschädigungen aus (6,7,19,20). Werden jedoch wiederholt exzentrische Belastungen in einer Muskelgruppe gesetzt, so gibt es einen gewissen Schutzeffekt („Repeated Bout Effect“), der die nachfolgenden Symptome abgeschwächt auftreten lässt. Anders ausgedrückt bedeutet dies, dass ein einmaliger exzentrischer Belastungsreiz (z.B. an der Beinmuskulatur) Schutz vor vergleichbaren Mikroläsionen bei nachfolgenden Trainingseinheiten (an der Beinmuskulatur) bietet. Bei den nachfolgenden
151
Belastungen zeigten sich dahingehend auch zusätzlich geringere Kraftabfälle und schnellere Erholungszeiten nach der Belastung. Um einen Schutzeffekt zu gewährleisten, muss jedoch die Initialbelastung nahezu maximal intensiv sein. Denn auch nach wochenlangem submaximalem Training (50% des 1-Repetiton-Maximum) entwickelt sich kein Schutzeffekt für ein darauffolgendes maximal intensives exzentrisches Training (21,22). Die Aufrechterhaltung dieses Schutzeffektes wird in vielen Studien mit einer Dauer bis zu mehreren Wochen bestätigt (23,24). Nosaka et al. konnten 2001 zeigen, dass dieser Schutzmechanismus bis mindestens 6 Monate nach der ersten exzentrischen Belastung aufrechterhalten werden kann, dass jedoch nach 9 und 12 Monaten dieser Schutzeffekt nicht mehr gegeben ist. Anzumerken ist jedoch noch, dass mit zunehmender Zeitdauer zwischen den exzentrischen Belastungen der Schutzmechanismus immer stärker abnimmt. Ein weiterer Punkt, welcher zu beachten ist, sind Entzündungsreaktionen, die durch die Muskelschädigung hervorgerufen werden. Dabei weisen große Muskelgruppen (z.B. Beinmuskulatur beim Bergablaufen), die an der Bewegungsausführung beteiligt waren, eine stärkere Immunantwort auf als isoliert exzentrisch bewegte Muskelgruppen (z.B. Ellbogenbeuger). Somit haben exzentrische Belastungen, bei denen große Muskelgruppen involviert sind, einen weitaus stärkeren Stimulus auf Entzündungsreaktionen. Bei wiederholter Belastung zeigte sich unter anderem eine deutlich abgeschwächte Ausschüttung von Stresshormonen und Zytokinen (19). Aber auch die Enzymkonzentration der Kreatinkinase (CK), der Laktatdehydrogenase (LDH) und des sauerstofftransportierenden Muskelproteins Myoglobin (Mb) nimmt durch die exzentrische Belastung bedingte Muskelschädigung und dem konsekutiven Membranleck im Plasma zu (25–27). Abbildung 3 gibt einen schematischen Überblick über die durch Belastung induzierten Muskelschäden hervorgerufenen Entzündungsreaktionen und die anschließenden Regenerationsprozesse. Kurz zusammengefasst zeigt sich nach exzentrischer Belastung eine rapide Mobilisation der Neutrophilen, die anschließend in das geschädigte Muskelgewebe eindringen. Des Weiteren werden natürliche Killerzellen und Lymphozyten mobilisiert und entzündungshemmende Zytokine in den Blutkreislauf freigesetzt. Innerhalb eines Tages werden die Neutophilen im geschädigten Muskelgewebe von Markophagen ersetzt und proinflammatorische Zytokine im Muskel produziert. Diese Entzündungsreaktionen sind bedeutsam in der Regulation der Akutphase-Antwort sowie für die Beseitigung von zerstörten Muskelgewebsfragmenten. Über einen Zeitraum von Tagen bis hin zu Wochen kommt es somit zur Regeneration der Muskelfasern (19).
152
Abb. 3: Durch Bewegung induzierte Muskelschädigung mit resultierenden Entzündungsprozessen und dem anschließenden Regenerationsprozess. (PMN-Leukozyten, Mb-Myoglobin, CK-Kreatinkinase, ROS- Reaktive Sauerstoffspezies) (19).

DAS ALPINE UMFELD UND DIE EXZENTRISCHE BELASTUNG
Wie bereits erwähnt zeichnen sich die exzentrischen Belastungen durch eine Vielzahl von Effekten aus, die sich positiv und teilweise auch negativ auf den menschlichen Organismus auswirken. Und so erscheint es besonders in den verschiedenen Bergsportdisziplinen (Wandern, Bergsteigen, Trailrunning, Skifahren und Skitourengehen) durchaus sinnvoll, diese Effekte miteinzubeziehen beziehungsweise sie weitgehend zu verhindern. Da zum einen ältere Personen eine geringere Muskelkraft in der Knie- und Hüftmuskulatur aufweisen, resultiert daraus eine geringere Gelenksstabilität (insbesondere des Kniegelenks), die ein erhöhtes Risiko für Verletzungen darstellt (28). Aber zum anderen kann auch zusätzliches Gewicht, wie es beim Tragen von Rucksäcken der Fall ist, die Gelenksstabilität des Knies negativ beeinflussen (29). Nun dominiert die exzentrische Muskelarbeit besonders beim Bergabgehen und stärker noch beim Bergablaufen und führt infolgedessen zu zusätzlichen Kraftverlusten in den beanspruchten Muskelgruppen, die bis zu mehreren Tagen anhalten können (27,30). Ob jedoch die durch exzentrische Belastung induzierten Kraftverluste auch für Verletzungen verantwortlich
153
© David Morawetz Abb. 4: Akkumulierende exzentrische Belastung durch Bergabgehen mit schwerem Rucksack bei einer mehrtägigen Trekkingtour im indischen Himalaya.

sind, kann nach aktuellem Stand der Literatur nicht eindeutig bestätigt werden (31). Dahingehend behaupten Vogt und Hoppeler (2014), dass besonders exzentrisches Training durch den Muskelmassenzuwachs helfen kann Verletzungen vorzubeugen. La Stayo et al. (2003) schreiben ferner, dass exzentrisches Training (8–11 Wochen mit je 2–3 Einheiten/Woche) verletzungsprophylaktisch auf das Muskel-Sehnensystem wirkt und beziffern den hohen Kraftzuwachs mit 40% bei jungen Personen und bis zu 120% bei älteren Menschen. Wobei ebenso beachtet werden sollte, dass eine chronische exzentrische Belastung zu einer Erhöhung der Steifheit des Muskel-Sehnen-Komplexes führt und somit eine verbesserte Gelenksstabilität erreicht wird (32). Die nachstehende Abbildung 5 soll beispielhaft die Trainingseffekte eines rein exzentrischen oder rein konzentrischen Trainings über 8 Wochen darlegen. Die signifikanten Steigerungen durch die exzentrische Trainingsmodalität zu den Ausgangswerten (100%) und im Vergleich zu den durch konzentrisches Training erreichten Werten unterstreichen sehr deutlich die hohen Effekte. Dahingehend wäre es daher besonders vor intensiven langen Touren oder bevor der Urlaub in der alpinen Bergwelt verbracht wird anzudenken, ob aufgrund dieser Faktoren ein exzentrisches Training absolviert wird. Somit könnte
154
% der Vortrainingswerte

Isometrische Kraft Muskelfaserquerschnitt Hüpffrequenz
Abb. 5: Effekte eines 8-wöchigen Trainings (rein konzentrisch oder rein exzentrisch). Der Muskelfaserquerschnitt, die isometrische Maximalkraft und die Hüpffrequenz steigerten sich signifikant verglichen zu den Ausganswerten und zu den Werten des konzentrischen Trainings. Die gesteigerte Hüpffrequenz spiegelt die erhöhte Steifheit der Sehnen wieder (10).
die Muskulatur bestmöglich auf die folgenden Belastungen vorbereitet werden. Bleibt jedoch nicht die Zeit für ein mehrwöchiges Vorbereiten, so kann immer noch der „Repeated Bout Effect“ ausgenützt werden. Infolgedessen könnten Muskelfaserschädigungen und die Schmerzproblematik des Muskelkaters weitgehend verhindert werden (22). Denn obwohl laut Mc Hugh (2001) die Initialbelastung maximal intensiv sein sollte um einen hinreichenden Schutz vor weiteren Muskelfaserschädigungen durch Folgebelastungen zu bieten, zeigten nach neuesten Untersuchungen Maeo et al. (2015) schon durch eine submaximale exzentrische Einheit im Bergabgehen Adaptionen der Muskelfasern. Durch 20-minütiges Bergabgehen (submaximale exzentrische Einheit) ein bis vier Wochen vor einer darauffolgenden submaximalen 40-minütigen Einheit konnten die Muskelkatersymptome zwar nicht gänzlich verhindert werden, aber im Gegensatz zu der Kontrollgruppe, welche keine Vorbelastung hatte, signifikant verringert werden. Darüber hinaus sollte noch festgehalten werden, dass Muskelkater nicht die exzentrischen Trainingsreize fördert (33). Dies verdeutlicht den Stellenwert der dosierten Vorbereitung durch entsprechendes exzentrisches Training, um die Muskelkatersymptome möglichst gering zu halten.
155
Der Vollständigkeit wegen ist an dieser Stelle noch anzumerken, dass entleerte Muskelglykogenspeicher (z.B. durch Aufstiege) keinen Einfluss auf den Schweregrad des Muskelkaters haben (34, 35). Vermindert ist hingegen die Glykogen-Resyntheserate nach exzentrischer Muskelarbeit verglichen zu einer rein konzentrischen Belastung. Dies ist möglicherweise beding durch die Muskelfaserschädigung (36). Aktuell zeigten Philippe et al. (2016), dass es durch nicht-muskelfaserschädigende exzentrische Belastungen zu keiner Beeinträchtigung des Glukose-Metabolismus kommt, sondern sich die Glukosetoleranz sogar kurzfristig optimiert (37). Für den Alpinsport ist dies besonders für mehrtägige Touren mit hoher exzentrischer Belastung von Bedeutung. Denn da auch durch eine ausreichende Bereitstellung an Glukose die Syntheserate nicht gesteigert werden kann, kann somit der spezifischen Vorbereitung (Muskelkaterabschwächung/-vermeidung) ein hoher Stellenwert zugeschrieben werden. Alternativ gesehen wirkt ein Regenerationstag, um die Syntheserate zu erhöhen und somit durch volle Glykogenspeicher die vollständige Leistungsfähigkeit zu erreichen (36). Doch die gesundheitlichen Effekte und die metabolischen Verbesserungen, die wir über die exzentrische Beanspruchung in der alpinen Umgebung erfahren sind bei weitem nicht zu vernachlässigen. Eine kurzzeitige Steigerung (bis 48h) des Ruheenergiebedarfs (REB) um 9% scheint eine sehr beachtliche Reaktion zu sein. Doch insbesondere bei adipösen Personen (BMI >24,9) nahm der REB um bis zu 25% zu (38). Langzeiteffekte, die durch eine einmal wöchentliche 30-minütige exzentrische Einheit über die Dauer von 2 Monaten aufgedeckt wurden, konnten den Ruheenergiebedarf immer noch um 5% für 48h nach der Belastung erhöhen (39). Es scheint jedoch, dass belastungsinduzierte Muskelfaserschädigungen, mit den darauffolgenden Entzündungsprozessen und der erhöhten Muskel-Protein-Synthese, möglicherweise für die Erhöhung des Ruheenergiebedarfs verantwortlich sind (40). Chronische exzentrische Belastungen wie bei längeren Berg- und Trekkingtouren zeichnen sich auch in einer Verbesserung des Lipidstoffwechsels (z.B: Senkung des LDL, höhere Fettstoffwechselraten) und in einer erhöhten Insulinsensitivität aus (38, 39). Auch in Bezug auf die Glukosetoleranz konnten durch chronische exzentrische Belastungen Erfolge erreicht werden (41). Denn eine signifikant verbesserte Glukosetoleranz (6,2%, p=0,023) konnten Drexel et al. (2008) durch 2-monatiges Bergabgehen feststellen. So kommt es trotz der Anwendung unterschiedlicher Trainingsprotokolle bei exzentrischem Ausdauertraining zu einer eindeutig stärkeren Verbesserung der Glukosetoleranz sowie des Lipidstoffwechsel verglichen zu konzentri-
156
Abb. 6: Blutzuckerspiegel nach 75g oral verabreichter Glukose. Gepunktete Linie: nach 8-wöchigem exzentrischem Training (Bergabgehen). Strichlierte Linie: nach 8-wöchigem konzentrischem Training (bergaufgehen). Durchgehende Linie: vor den beiden verschiedenen Trainingsmodalitäten (41).
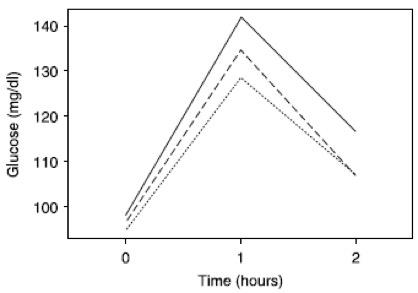
schem Training. Zwangsläufig heißt dies aber nicht, dass beispielsweise in einer Stunde bergabgehend dadurch auch mehr Energie verbrannt wird als in einer Stunde bergaufgehend. Dies bedeutet lediglich, dass pro kcal, die verstoffwechselt wird, sich das LDL-Cholesterol um beinahe das 3-fache stärker reduziert (0,0982 mg/dl/kcal exzentrisch vs. 0,0346 mg/dl/kcal konzentrisch). Auch die Glukosetoleranz profitiert pro aufgewendeter kcal um das 4-fache (0,1123 mg/ dl/kcal exzentrisch vs. 0,0245 mg/dl/kcal konzentrisch) durch das exzentrische Ausdauertraining (42). Relativ (pro kcal) gesehen sind somit die Effekte des exzentrischen Ausdauertrainings ökonomischer und die Adaptionen durch exzentrisches Ausdauertraining angesichts des Energiestoffwechsels scheinen jenen des konzentrischen Ausdauertrainings überlegen zu sein. Obwohl nun die Forschergruppe um Zeppetzauer et al. (2013) metabolisch sehr vorteilhafte Effekte zeigten, sollte wie schon erwähnt, beachtet werden, dass der Gesamtenergieverbrauch der exzentrischen Arbeitsweise immer noch niedriger liegt als jener der konzentrischen. Nach derzeitigem Wissensstand scheint es aber, dass akute exzentrische Belastungen (ohne Muskelkater!) weniger positive Effekte auf die Glukosetoleranz zeigen als eine vergleichbare konzentrische Belastung. Hingegen beeinflusst ein mehrwöchiges exzentrisches Training die Glukosetoleranz verglichen zum konzentrischen Training wiederum stärker
157
(37, 41). Dahingehend können durch die geringere kardiovaskuläre Belastung und die metabolischen Vorteile eines exzentrischen Ausdauertrainings vor allem Herzpatienten, Diabetiker (Typ II) und adipöse Personengruppen profitieren (38,41,42). In den allermeisten Alpinsportdisziplinen dominiert zu einem beachtlichen Teil die exzentrische Muskelarbeit. Die Literatur zeigte, dass besonders ungewohnte exzentrische Belastungen zu hohen Kraftverlusten und Muskelkater führen. Kontrovers wird jedoch diskutiert, ob daraus ein Verletzungsrisiko resultiert. Übereinstimmend kann hingegen behauptet werden, dass eine entsprechende Vorbereitung, vom mehrwöchigen Training bis hin zu einer einzigen intensiven exzentrischen Einheit, die Muskulatur für die spezifischen Belastungen im Alpinsport weitgehend adaptiert. Kontrovers wird hingegen die Verbesserung der Glukosetoleranz diskutiert. Hier scheinen die Muskelfaserschädigung oder der Trainingsumfang (akute vs. chronische Belastung) beeinflussend auf die Effekte zu sein. Schlussfolgernd lässt sich zusammenfassen, dass durch die verschiedenen Alpinsportdisziplinen auch die Risikofaktoren eines metabolischen Syndroms gesenkt werden können.
DANKSAGUNG
David Morawetz wurde durch den Forschungsförderungsfond der ÖGAHM dankenswerterweise unterstützt.
158
LITERATUR
(1) Helmenstein C., Kleissner A., Moser B. Der Bergsport in Österreich. SportsEconAustria: Institut für Sportökonomie 2007: 1–81. (2) Krenn M., Domej W., Schwaberger G. Performance testing in mountaineering. Wien
Med Wochenschr 2005; 155: 193–198. doi:10.1007/s10354-005-0169-1. (3) Hochholzer T., Burtscher M., editor. Trekking und Expeditionsbergsteigen. Ein medizinischer Ratgeber. 1st ed. Köngen: Panico Alpinverlag; 2011. (4) Schenk K., Faulhaber M., Gatterer H., Burtscher M., Ferrari M. Ski mountaineering competition: fit for it? Clin J Sport Med 2011; 21: 114–118. doi:10.1097/JSM.0b013e31820f903e. (5) Weineck J. Optimales Training: Leistungsphysiologische Trainingslehre unter besonderer Berücksichtigung des Kinder- und Jugendtrainings. 16th ed. Balingen: Spitta; 2010. (6) Proske U., Allen TJ. Damage to Skeletal Muscle from Eccentric Exercise. Exercise and
Sport Sciences Reviews 2005; 33: 98–104. doi:10.1097/00003677-200504000-00007. (7) Herzog W. Mechanisms of enhanced force production in lengthening (eccentric) muscle contractions. J Appl Physiol (1985) 2014; 116: 1407–1417. doi:10.1152/japplphysiol.00069.2013. (8) Colliander E.B., Tesch P.A. Effects of eccentric and concentric muscle actions in resistance training. Acta Physiol Scand 1990; 140: 31–39. doi:10.1111/j.1748-1716.1990. tb08973.x. (9) Dudley G.A., Tesch P.A., Miller B.J., Buchanan P. Importance of eccentric actions in performance adaptations to resistance training. Aviat Space Environ Med 1991; 62: 543–550. (10) Lindstedt S.L., LaStayo P.C., Reich T.E. When active muscles lengthen: properties and consequences of eccentric contractions. News Physiol Sci 2001; 16: 256–261. (11) Komi P.V. Stretch-shortening cycle: a powerful model to study normal and fatigued muscle. J Biomech 2000; 33: 1197–1206. (12) Nicol C., Avela J., Komi P.V. The stretch-shortening cycle: A model to study naturally occurring neuromuscular fatigue. Sports Med 2006; 36: 977–999. (13) Enoka R.M. Eccentric contractions require unique activation strategies by the nervous system. J Appl Physiol (1985) 1996; 81: 2339–2346. (14) Duchateau J., Baudry S. Insights into the neural control of eccentric contractions. J
Appl Physiol (1985) 2014; 116: 1418–1425. doi:10.1152/japplphysiol.00002.2013. (15) Flanagan S.D., Mills M.D., Sterczala A.J., Mala J., Comstock B.A. et al. The relationship between muscle action and repetition maximum on the squat and bench press in men and women. J Strength Cond Res 2014; 28: 2437–2442. doi:10.1519/
JSC.0000000000000337. (16) Horstmann T., Mayer F., Maschmann J., Niess A., Roecker K., Dickhuth H.H. Meta-
159
bolic reaction after concentric and eccentric endurance-exercise of the knee and ankle.
Med Sci Sports Exerc 2001; 33: 791–795. (17) Ryschon T.W., Fowler M.D., Wysong R.E., Anthony A., Balaban R.S. Efficiency of human skeletal muscle in vivo: comparison of isometric, concentric, and eccentric muscle action. J Appl Physiol (1985) 1997; 83: 867–874. (18) Sorichter S., Puschendorf B., Mair J. Skeletal muscle injury induced by eccentric muscle action: muscle proteins as markers of muscle fiber injury. Exerc Immunol Rev 1999; 5: 5–21. (19) Peake J., Nosaka K., Suzuki K. Characterization of inflammatory responses to eccentric exercise in humans. Exerc Immunol Rev 2005; 11: 64–85. (20) Vogt M., Hoppeler H. Eccentric exercise: mechanisms and effects when used as training regime or training adjunct. J Appl Physiol (1985) 2014; 116: 1446–1454. doi:10.1152/ japplphysiol.00146.2013. (21) McHugh M.P. Recent advances in the understanding of the repeated bout effect: The protective effect against muscle damage from a single bout of eccentric exercise. Scand
J Med Sci Sports 2003; 13: 88–97. doi:10.1034/j.1600-0838.2003.02477.x. (22) Nosaka K., Newton M. Repeated eccentric exercise bouts do not exacerbate muscle damage and repair. J Strength Cond Res 2002; 16: 117–122. (23) Clarkson P.M., Nosaka K., Braun B. Muscle function after exercise-induced muscle damage and rapid adaptation. Med Sci Sports Exerc 1992; 24: 512–520. (24) McHugh M.P., Connolly D.A., Eston R.G., Gleim G.W. Exercise-induced muscle damage and potential mechanisms for the repeated bout effect. Sports Med 1999; 27: 157–170. (25) Hasenoehrl T., Wessner B., Tschan H., Vidotto C., Crevenna R., Csapo R. Eccentric resistance training intensity may affect the severity of exercise induced muscle damage.
J Sports Med Phys Fitness 2016 May 11. (26) Fredsted A., Clausen T., Overgaard K. Effects of step exercise on muscle damage and muscle Ca2+ content in men and women. J Strength Cond Res 2008; 22: 1136–1146. (27) Mastaloudis A., Traber M.G., Carstensen K., Widrick J.J. Antioxidants Did Not Prevent Muscle Damage in Response to an Ultramarathon Run. Medicine & Science in
Sports & Exercise 2006; 38: 72–80. doi:10.1249/01.mss.0000188579.36272.f6. (28) Wang LI. The kinetics and stiffness characteristics of the lower extremity in older adults during vertical jumping. J Sports Sci Med 2008; 7: 379–386. (29) Stastny P., Lehnert M., Zaatar A., Svoboda Z., Xaverova Z., Jelen K. Knee joint muscles neuromuscular activity during load-carrying walking. Neuro Endocrinol Lett 2014; 35: 633–639. (30) Chen T.C., Nosaka K., Lin M.J., Chen H.L., Wu C.J. Changes in running economy at different intensities following downhill running. J Sports Sci 2009; 27: 1137–1144. doi:10.1080/02640410903062027.
160
(31) Debenham J., Travers M., Gibson W., Campbell A., Allison G. Eccentric Fatigue Modulates Stretch-shortening Cycle Effectiveness--A Possible Role in Lower Limb Overuse
Injuries. Int J Sports Med 2016; 37: 50–55. doi:10.1055/s-0035-1549923. (32) La Stayo P.C., Woolf J.M., Lewek M.D., Snyder-Mackler L., Reich T., Lindstedt S.L. Eccentric muscle contractions: their contribution to injury, prevention, rehabilitation, and sport. J Orthop Sports Phys Ther 2003; 33: 557–571. doi:10.2519/jospt.2003.33.10.557. (33) Chen T.C., Tseng W.C., Huang G.L., Chen H.L., Tseng K.W., Nosaka K. Low-intensity eccentric contractions attenuate muscle damage induced by subsequent maximal eccentric exercise of the knee extensors in the elderly. Eur J Appl Physiol 2013; 113: 1005–1015. doi:10.1007/s00421-012-2517-3. (34) Nelson M.R., Conlee R.K., Parcell A.C. Inadequate carbohydrate intake following prolonged exercise does not increase muscle soreness after 15 minutes of downhill running. Int J Sport Nutr Exerc Metab 2004; 14: 171–184. (35) Close G.L., Ashton T., Cable T., Doran D., Noyes C., McArdle F., MacLaren D.P.M.
Effects of dietary carbohydrate on delayed onset muscle soreness and reactive oxygen species after contraction induced muscle damage. Br J Sports Med 2005; 39: 948–953. doi:10.1136/bjsm.2005.019844. (36) Zehnder M., Muelli M., Buchli R., Kuehne G., Boutellier U. Further glycogen decrease during early recovery after eccentric exercise despite a high carbohydrate intake. Eur J
Nutr 2004; 43: 148–159. doi:10.1007/s00394-004-0453-7. (37) Philippe M., Krusmann P.J., Mersa L., Eder E.M. et al. Acute effects of concentric and eccentric exercise on glucose metabolism and interleukin-6 concentration in healthy males. Biol Sport 2016; 33: 153–158. doi:10.5604/20831862.1198634. (38) Paschalis V., Nikolaidis M.G., Giakas G., Theodorou A.A., Sakellariou G.K. et al.
Beneficial changes in energy expenditure and lipid profile after eccentric exercise in overweight and lean women. Scand J Med Sci Sports 2010; 20: e103-111. doi:10.1111/ j.1600-0838.2009.00920.x. (39) Paschalis V., Nikolaidis M.G., Theodorou A.A., Panayiotou G., Fatouros I.G. et al. A weekly bout of eccentric exercise is sufficient to induce health-promoting effects. Med
Sci Sports Exerc 2011; 43: 64–73. doi:10.1249/MSS.0b013e3181e91d90. (40) Penailillo L., Blazevich A., Nosaka K. Energy expenditure and substrate oxidation during and after eccentric cycling. Eur J Appl Physiol 2014; 114: 805–814. doi:10.1007/ s00421-013-2816-3. (41) Drexel H., Saely C.H., Langer P., Loruenser G., Marte T. et al. Metabolic and anti-inflammatory benefits of eccentric endurance exercise – a pilot study. Eur J Clin Invest 2008; 38: 218–226. doi:10.1111/j.1365-2362.2008.01937.x. (42) Zeppetzauer M., Drexel H., Vonbank A., Rein P., Aczel S., Saely C.H. Eccentric endurance exercise economically improves metabolic and inflammatory risk factors. Eur J
Prev Cardiol 2013; 20: 577–584. doi:10.1177/2047487312444236.
161
❙ Elena Pocecco, Hannes Gatterer, Martin Niedermeier, Maike Huth, Tobias Dünnwald, Verena Menz, Martin Burtscher, Martin Faulhaber ❙
Wiederholte 1-stündige Hypoxieexpositionen zur Vorakklimatisation bei AMS-anfälligen Personen
Repeated 1-hour hypoxia exposures for pre-acclimatization of AMS-susceptible individuals
SUMMARY
The present study investigated effects of pre-acclimatization applying 7 repeated 1-hour exposures to normobaric hypoxia (4500 m) on prevalence and severity of acute mountain sickness (AMS) during a subsequent high-altitude exposure (3650 m) in AMS-susceptible individuals. The study was designed as a randomized controlled trial (double-blinded) including 32 healthy male and female persons with known AMS susceptibility. Participants completed seven passive 1-hour sessions in a normobaric hypoxic room. Participants of the hypoxia group were exposed to 4500 m whereas participants of the control group were exposed to ambient altitude (590 m). After finishing the pre-acclimatization program participants travelled by bus and cog railway to the Jungfraujoch (Switzerland) and hiked (about 1 hour) to the Mönchsjochhut (3650 m), where the 45-hour lasting high-altitude exposure took place. AMS symptoms and physiological parameters were repeatedly determined. There was no significant difference in incidence and severity of AMS between the hypoxia and the control group during the high-altitude exposure. 59% of the hypoxia group and 67% of the control group suffered from AMS at 1 or more times during the high-altitude exposure. Resting ventilation at high altitude tended to be higher in the hypoxia compared to the control group (P = 0.06). No significant between-group differences for arterial oxygen saturation and for the other physiological parameters were detected.
163
Pre-acclimatization using 7 repeated 1-hour exposures to 4500 m normobaric hypoxia did not prevent AMS development during a subsequent exposure to real high altitude in AMS susceptible persons. Keywords: Intermittent hypoxia, randomized controlled trial, pre-acclimatization, high-altitude disease, mountaineering
ZUSAMMENFASSUNG
Die vorliegende Studie untersuchte die Effekte einer Vorakklimatisation, bestehend aus 7 Einheiten zu je 1 Stunde in normobarer Hypoxie (4.500 m), auf die Prävalenz und den Schweregrad der akuten Bergkrankheit (AMS) während eines nachfolgenden Höhenaufenthalts in natürlicher Höhe (3.650 m) bei AMS-anfälligen Personen. Es handelte sich um eine randomisiert kontrollierte Doppelblindstudie, die 32 gesunde männliche und weibliche Teilnehmer mit bekannter AMS-Anfälligkeit inkludierte. Alle Probanden absolvierten 7 einstündige passive Sitzungen in einer normobaren Hypoxiekammer, wobei die Hypoxiegruppe einer simulierten Höhe von 4.500 m und die Kontrollgruppe einer Umgebungshöhe von 590 m ausgesetzt waren. Nach Abschluss des Vorakklimatisationsprogramms wurden die Probanden per Bus und Zahnradbahn aufs Jungfraujoch (Schweiz) transportiert und wanderten ca. 1 Stunde weiter zur Mönchsjochhütte (3.650 m), wo sie 45 Stunden verbrachten. Dabei wurden wiederholt AMS-Symptome sowie physiologische Parameter ermittelt. Es gab keinen signifikanten Unterschied in Inzidenz und Schweregrad der akuten Bergkrankheit zwischen den Gruppen während des Höhenaufenthalts. Insgesamt litten 59% der Probanden der Hypoxiegruppe und 67% der Kontrollgruppe unter AMS an einem bzw. mehreren Zeitpunkten des Höhenaufenthalts. Die Ruheventilation in der Höhe war in der Hypoxiegruppe tendenziell höher als in der Kontrollgruppe (P = 0,06). Während des Höhenaufenthalts gab es keine signifikanten Unterschiede zwischen den Gruppen in Bezug auf die arterielle Sauerstoffsättigung und die weiteren erfassten physiologischen Parameter. Eine Vorakklimatisation, bestehend aus 7 Einheiten zu je 1 Stunde normobarer Hypoxie entsprechend 4.500 m Höhe, konnte während eines darauffolgenden realen Höhenaufenthalts der Entwicklung der AMS bei AMS-anfälligen Personen nicht vorbeugen. Schlüsselwörter: intermittierende Hypoxie, Randomisiert kontrollierte Studie, Prä-Akklimatisation, Höhenkrankheit, Bergsteigen
164
EINLEITUNG
Weltweit steigt das Interesse an Berg- und Trekkingtouren bis in große und sogar extreme Höhen. (1,2). Ein akuter Höhenaufenthalt führt aber zwangsläufig zu einer verminderten Ausdauerleistungsfähigkeit (3) und auch das Risiko für Höhenerkrankungen, von denen die akute Bergkrankheit (AMS) die häufigste Form darstellt, nimmt mit zunehmender Höhe zu (4). AMS ist in den meisten Fällen selbstlimitierend und die Symptome verschwinden häufig nach Stunden bis Tagen - adäquates Verhalten der betroffenen Person vorausgesetzt. Allerdings können auch schwere Formen der Höhenerkrankungen wie ein Höhenlungenödem oder ein Höhenhirnödem folgen (5). Die Symptome der AMS (z.B. Kopfschmerzen, Erbrechen, Schwindel) sind für Bergsteiger insofern relevant, dass sie die Gipfelchancen reduzieren, aber vor allem das Unfallrisiko durch die Beeinträchtigung der Betroffenen erhöhen (6,7). Die AMS-Inzidenz liegt zwischen 9 und 63% in Abhängigkeit von der absoluten Höhe, der Aufstiegsgeschwindigkeit, dem Ausmaß der körperlichen Beanspruchung, dem Akklimatisationsgrad und der individuellen Anfälligkeit (8–10). Obwohl die Reproduzierbarkeit der AMS-Anfälligkeit kontrovers diskutiert wird (11), stellt sie doch einen unabhängigen Risikofaktor für die Entwicklung einer AMS dar und in der Praxis trifft man regelmäßig auf Personen, welche eindeutig von wiederholten AMS-Symptomen bereits in Höhen um 3.000 m berichten. Die generellen Empfehlungen für eine wirkungsvolle AMS-Prävention beinhalten eine ausreichend langsame Steigerung der Schlafhöhe (12). Geografische Gegebenheiten und/oder straffe Zeitpläne bei vielen Hoch- und Trekkingtouren (z.B. Mont Blanc, Kilimandscharo) sind Gründe, weshalb diese Akklimatisationsregeln oftmals nicht befolgt werden. Hier sind speziell AMS-anfällige Teilnehmer einem besonderen AMS-Risiko ausgesetzt. Wiederholte Hypoxieexpositionen, wie zum Beispiel wiederholte Nächtigungen in simulierter Höhe, dürften einen Vorakklimatisationseffekt haben (13,14). Für die Praxis sind natürlich möglichst zeiteffektive Vorakklimatisationsstrategien interessant. Tatsächlich haben mehrere Studien eine zumindest teilweise AMS-Prävention durch wiederholte Hypoxieexpositionen von 4 oder weniger Stunden pro Exposition gezeigt (6,15,16). Eine Laborstudie in normobarer Hypoxie hat sogar eine AMS-Prophylaxe durch 7 wiederholte 1-stündige passive Hypoxiesitzungen gezeigt (17). Dieses Vorakklimatisationsprotokoll stellt eine wenig zeitintensive Art der Höhenvorbereitung dar. Allerdings ist eine Übertragbarkeit dieser Ergebnisse auf eine Exposition unter natürlichen Höhenbedingungen und auf eine spezielle Zielgruppe (AMS-Anfällige) nicht
165
ohne weiteres gerechtfertigt (18). Daher war es das Ziel dieser Untersuchung, an AMS-anfälligen Personen die Effekte dieses Vorakklimatisationsprotokolls auf die AMS-Entwicklung bei einem nachfolgenden Aufenthalt in natürlicher Höhe zu überprüfen.
METHODIK
Probanden
An der Studie nahmen gesunde Personen (18–60 Jahre), die mittels öffentlicher Ausschreibung rekrutiert wurden, teil. Sie mussten in den vergangenen Jahren mindestens 2-mal AMS-Symptome bei einem Höhenaufenthalt erfahren haben. Interessenten wurden zu einem Vortest-Termin eingeladen, an dem der Gesundheitszustand sowie mögliche Ausschlusskriterien ermittelt wurden. Des Weiteren wurden soziodemografische, anthropometrische und höhenanamnestische Daten erhoben. Die AMS-Anfälligkeit wurde nach der Methode von Schneider et al. (10) erhoben. Die Teilnehmer wurden gefragt, wie oft die 5 AMS-Symptomkomplexe (Kopfschmerzen, Magen-Darm-Symptome, Müdigkeit/Abgeschlagenheit, Schwindel/Benommenheit, Schlafstörungen) während früheren Höhenaufenthalten vorkamen (nie = 0, selten = 1, häufig = 2 bzw. regelmäßig = 3). Kriterium, um jemanden als AMS-anfällig zu bezeichnen, war das häufige bzw. regelmäßige Auftreten von Kopfschmerzen (Bewertung ≥2) sowie ein Gesamtscore von ≥4. Ausschlusskriterien waren chronische bzw. akute Krankheiten, regelmäßiges Rauchen von mehr als 5 Zigaretten pro Tag, regelmäßige Medikamenteneinnahme, Schwangerschaft bzw. Stillzeit, gewöhnlicher Wohnort >1.500 m, mindestens eine Übernachtung auf Höhen >2.500 m in den vergangenen 4 Wochen. Insgesamt wurden 33 Personen mit AMS-Anfälligkeit und ohne Ausschlusskriterien für die Studie rekrutiert. Das schriftliche Einverständnis wurde nach Aufklärung über das Untersuchungsverfahren und über die mit der Studie verbundenen Risiken eingeholt. Die Studie wurde vom institutsinternen Reviewboard (Institut für Sportwissenschaft der Universität Innsbruck) für unbedenklich erklärt. Eine Probandin, die sich am ersten Tag des Höhenaufenthalts verletzte und den Höhenaufenthalt zur medizinischen Abklärung unterbrechen musste, wurde nicht in die Auswertungen inkludiert. Die Charakteristika der 32 Probanden sind in Tabelle 1 beschrieben.
166
Tab. 1: Probandencharakteristika der Hypoxie- (n = 17) und der Kontrollgruppe (n = 15). Werte sind Mittelwerte ± Standardabweichung oder absolute (relative) Häufigkeiten. Die Anfälligkeit für eine akute Bergkrankheit wurde in Anlehnung an die Vorgehensweise von Schneider et al. (10) ermittelt. Keine signifikanten Unterschiede zwischen den Gruppen.
Hypoxiegruppe Kontrollgruppe
Frauen, n (%) 9 (53) 8 (53) Alter (Jahre) 38,0 ± 11,7 38,0 ± 11,8 Körpergröße (cm) 174 ± 7 177 ± 11 Körpergewicht (kg) 70 ± 11 71 ± 12 Wohnorthöhe (m) 653 ± 108 622 ± 122 AMS-Anfälligkeit (Score-Punkte) 7,5 ± 2,0 7,5 ± 1,9
Studiendesign
Das Projekt wurde als randomisierte und kontrollierte Doppelblindstudie konzipiert. Aufgrund von Dauer und Zeitverlauf der Messungen während des Höhenaufenthalts wurden 2 aufeinanderfolgende Blöcke (September/Oktober 2013 und Mai 2014) geplant, auf die die Studienteilnehmer gleichmäßig verteilt wurden. Nach den Vortests fand am Institut für Sportwissenschaft der Universität Innsbruck (590 m) die Messung der Ruheparameter (arterielle Sauerstoffsättigung, hämatologische und ventilatorische Parameter) in Normoxie statt. Anschließend wurden die Probanden von einer Person, welche nicht in die weiteren Erhebungen involviert war, zur Hypoxie- bzw. Kontrollgruppe zugeteilt. Die Gruppenzuteilung war randomisiert (stratifiziert nach Alter, Geschlecht und AMS-Anfälligkeit) und verblindet für Studienteilnehmer sowie Personen, die bei Tests bzw. Auswertungen involviert waren. Die Gruppenzuteilung wurde für jeden Studienblock separat durchgeführt. Das Vorakklimatisationsprogramm wurde in 2 normobaren Hypoxiekammern (LowOxygen, Deutschland and Höhenbalance, Deutschland) am Institut für Sportwissenschaft der Universität Innsbruck (590 m) durchgeführt. Das Protokoll sah einen Aufenthalt in der Kammer von einer Stunde pro Tag an 7 aufeinanderfolgenden Tagen vor. Diese Anzahl und Dauer der Sitzungen in der Höhenkammer war für alle Studienteilnehmer gleich, unabhängig von der Gruppenzuteilung. Allerdings befand sich während der Sitzungen die Hypoxiegruppe auf einer simulierten Höhe von 4.500 m (inspiratorische Sauerstoffkonzentration (FIO2) 12,6%) während die Kontrollgruppe normoxische Luft
167
(FIO2 20,9%) atmete. Die arterielle Sauerstoffsättigung (SpO2) (Pulsox-3i, Konica Minolta, Osaka, Japan) wurde nach circa 30 Minuten bei jeder Sitzung ermittelt. Das Vorakklimatisationsprogramm wurde von Mitarbeitern organisiert und durchgeführt, die in weiterer Folge weder an Messungen noch an der Auswertung der Daten beteiligt waren. Am Tag nach der letzten Sitzung in der Höhenkammer wurden die Teilnehmer per Bus nach Interlaken (Schweiz, 570 m) transportiert und übernachteten in einer Jugendherberge. Am nächsten Morgen wurden die Ausgangswerte der AMS-Symptomatik erhoben. Danach fuhren die Studienteilnehmer mittels Zahnradbahn zum Jungfraujoch (3.450 m) und wanderten ca. 1 Stunde lang über einen markierten und präparierten Gletscherweg bis zur Mönchsjochhütte (3.650 m), wo der 45-stündige Höhenaufenthalt stattfand. Am ersten Tag des Höhenaufenthalts erfolgte zwischen den Messzeitpunkten eine theoretische und praktische alpintechnische Einführung durch staatlich geprüfte Bergführer (in der Hütte bzw. im direkten Umfeld der Hütte). Am zweiten Tag wurde eine ca. 3-stündige Tour unter Leitung der Bergführer unternommen. Die Probanden wurden angewiesen, eine moderate Belastungsintensität bei der Bergtour zu wählen, entsprechend einem subjektiven Belastungsempfinden von ≤13 auf der Borg-RPE-Skala (19), da hohe Belastungsintensitäten die AMS provozieren können (4). Die Ernährung war während des Höhenaufenthalts standardisiert und Wasser stand den Studienteilnehmern ad libidum zur Verfügung. Diese wurden darauf hingewiesen, regelmäßig zu trinken, allerdings waren keine alkoholischen Getränke zugelassen, da geringe Flüssigkeitszunahme und Alkoholkonsum die Entwicklung von AMS fördern (9). Ein Höhenmediziner stand während des gesamten Höhenaufenthalts zur Verfügung. Bei AMS-Symptomatik und mindestens mäßigen Kopfschmerzen wurden die Krankheitserscheinungen auf Wunsch der Einzelnen mit NSAIDs (z.B. Ibuprofen) behandelt. Die AMS-Symptomatik und die Ruheparameter wurden während des Höhenaufenthalts wiederholt erfasst (siehe nachfolgender Abschnitt). Nach Beendigung der letzten Messungen erfolgten der Abstieg und die Heimreise. Hauptzielparameter waren AMS-Inzidenz und Schweregrad der AMS-Symptomatik während des Höhenaufenthalts.
Messungen
Symptomatik der akuten Bergkrankheit (AMS-Symptomatik) Die Inzidenz und der Schweregrad der AMS wurden mittels Lake Louise Score (LLS) erhoben (20). Der LLS beinhaltete die 5 AMS-Symptomkomplexe Kopfschmerzen, Übelkeit/Erbrechen, Müdigkeit/Abgeschlagenheit, Schwindel/Be-
168
nommenheit und Schlafstörungen, wobei jeder auf einer Skala von 0 (nicht vorhanden) bis 3 (stark) beurteilt wurde. Das Vorliegen einer AMS wurde beim Vorhandensein von Kopfschmerzen (Bewertung ≥2) und einem zweiten Symptom bei einem Gesamtscore von ≥4 definiert (17). Die Beurteilung von AMS wurde in Interlaken (570 m) morgens vor dem Aufstieg (Ausgangswerte) und nach 6, 9, 21, 30 und 45 Stunden Höhenaufenthalt durchgeführt.
Ruheparameter: Arterielle Sauerstoffsättigung, hämatologische und ventilatorische Parameter Die SpO2 wurde mittels Fingerpulsoxymeter (Pulsox-3i, Konica Minolta, Osaka, Japan) über 4 Minuten gemessen, wobei der Mittelwert der letzten 2 Minuten für die Auswertungen herangezogen wurde. Kapillarblutproben vom hyperämisierten Ohrläppchen wurden für die Blutgasanalyse (ABL80 FLEX Co-Ox, Radiometer, Dänemark) und die Bestimmung der Blutlaktatkonzentrationen (Biosen C-line, EKF, Deutschland) verwendet. Die ventilatorischen Parameter wurden über 3 Minuten erfasst (MetaLyzer 3B, Cortex, Deutschland) und die Mittelwerte flossen in die Auswertungen ein. Alle Ruheparameter wurden im Rahmen der Tests in Innsbruck vor der Vorakklimatisation (Ausgangswerte) und während des Höhenaufenthaltes (SpO2 nach 6, 21, and 45 Stunden, hämatologische Parameter nach 6 und 45 Stunden, ventilatorische Parameters nach 21 Stunden) gemessen.
Statistik
Die statistische Analyse erfolgte mittels SPSS (Version 21, IBM, Österreich). Die Ergebnisse sind als Häufigkeiten (AMS Inzidenz) beziehungsweise Mittelwerte ± Standardabweichung dargestellt. Häufigkeitsvergleiche erfolgten mittels Chi-Quadrat-Test. Zur Analyse von Zeit und Gruppen-Zeit-Interaktionen wurde eine ANOVA mit Messwiederholungen (Gruppe x Zeit) anwendet. Das Signifikanzniveau wurde bei einem P-Wert <0,05 festgelegt (zweiseitig).
ERGEBNISSE
Vorakklimatisationsprogramm
Alle Studienteilnehmer absolvierten das Vorakklimatisierungsprogramm wie geplant und vertrugen die Exposition ohne negative Auswirkungen. Die durchschnittliche SpO2 über alle 7 Sitzungen war in der Hypoxie- erwartungsgemäß niedriger als in der Kontrollgruppe (78,9 ±5,3% versus 97,2±0,5%, P
169
<0,01 für ANOVA Gruppeneffekt). Es gab jedoch weder einen signifikanten Zeiteffekt (P = 0,36) noch eine Gruppen-Zeit-Interaktion (P = 0,41) für die SpO2 während des Vorakklimatisationsprogramms (Abb. 1).
Arterielle Sauerstoffsättigung (%) 100
95
90
85
80
75
70
65
1 2 3 4 5
Vorakklimatisationssitzung 6 7
Abb. 1: Verlauf der arteriellen Sauerstoffsättigung während der 7 Vorakklimatisationssitzungen für die Hypoxie- (blau) und die Kontrollgruppe (rot). Werte sind Mittelwerte ± Standardabweichung.
Inzidenz und Schweregrad der akuten Bergkrankheit (AMS)
Die Inzidenz von AMS erreichte ihren Höhepunkt morgens nach der ersten Nacht in der Höhe (nach 21 Stunden) mit 53% sowohl in der Hypoxie- als auch in der Kontrollgruppe. Die AMS-inzidenz unterschied sich nicht signifikant zwischen den Gruppen sowohl in Bezug auf die Basalwerte als auch während der Messungen in der Höhe. Insgesamt lag bei 59% der Probanden in der Hypoxiegruppe sowie 67% in der Kontrollgruppe AMS an einem bzw. mehreren Messzeitpunkten des Höhenaufenthalts vor (P = 0,65 zwischen den Gruppen). Der Verlauf der AMS-Symptomatik in der Hypoxie- und in der Kontrollgruppe ist in Abbildung 2 dargestellt. Es gab signifikante Zeiteffekte (p <0,01), allerdings keine Gruppen-Zeit-Interaktionen (P = 0,75) für den Schweregrad von AMS. Außerdem zeigten sich keine signifikanten Gruppen-Zeit-Interakti-
170
onen für den AMS-Schweregrad bei getrennter Analyse von Geschlechtern (P = 0,36 für Frauen bzw. P = 0,50 für Männer) sowie Altersgruppen (P = 0,94 für Personen <40 Jahre bzw. P = 0,61 für Personen ≥40 Jahre).
8
Lake Louise Score 6
4
2
0
Baseline 6 Stunden 9 Stunden 21 Stunden 30 Stunden 45 Stunden
Abb. 2: Verlauf der Symptomatik der akuten Bergkrankheit (Lake-Louise-Score) in der Hypoxie- (blau) und in der Kontrollgruppe (rot) vor (Baseline) und nach 6, 9, 21, 30 und 45 Stunden Höhenaufenthalt. Werte sind Mittelwerte ± Standardabweichung. Keine signifikante Interaktion zwischen den Gruppen.
Ruheparameter: Arterielle Sauerstoffsättigung, hämatologische und ventilatorische Parameter
Die SpO2 sowie die hämatologischen und ventilatorischen Parameter sind in Tabelle 2 dargestellt. Die SpO2 zeigte erwartungsgemäß signifikante Zeiteffekte aber keine Gruppeninteraktion. Auch bei den hämatologischen Parametern ergaben sich signifikante Effekte über die Messzeitpunkte ohne signifikante Interaktionen. Die ventilatorischen Parameter (Atemfrequenz, Atemminutenvolumen und ventilatorische Äquivalente) zeigten signifikante Veränderungen über die Messzeitpunkte. Es konnten aber auch hier keine signifikanten Interaktionen zwischen den beiden Gruppen gezeigt werden. Es ergab sich lediglich eine Tendenz zur einem stärkeren Anstieg des Atemminutenvolumens in der Höhe in der Hypoxiegruppe (P = 0,06 für die Interaktion).
171
Tab. 2: Arterielle Sauerstoffsättigung und hämatologische Parameter der Hypoxiegruppe (HG) und der Kontrollgruppe (KG) in Tallage vor Präakklimatisation (Baseline) und während der Höhenexposition. Werte sind Mittelwerte ± Standardabweichung. P-Werte beziehen sich auf Zeiteffekte (Zeit) und Gruppe-Zeit-Interaktionen (Interaktion) in der ANOVA für Messwiederholungen. SpO2 = Arterielle Sauerstoffsättigung (Pulsoxymetrie), La = Blutlaktatkonzentration, pCO2 = Kohlendioxidpartialdruck, pO2 = Sauerstoffpartialdruck, Hb = Hämoglobinkonzentration, HCO3 = Bikarbonatkonzentration, AF = Atemfrequenz, AMV = Atemminutenvolumen, VE/VO2 = Atemäquivalent für Sauerstoff, VE/VCO2 = Atemäquivalent für Kohlendioxid.
SpO2 (%)
La (mmol/L)
pCO2 (mmHg)
pO2 (mmHg)
Hb (mg/dL)
HCO3 (mmol/L)
AF (1/min)
AMV (L/min)
VE/VO2
VE/VCO2 HG KG HG KG HG KG HG KG HG KG HG KG HG KG HG KG HG KG HG KG
Baseline
97,3 ± 0,9 97,0 ± 0,9 1,03 ± 0,67 1,05 ± 0,33 32,8 ± 3,7 32,8 ± 3,5 83,0 ± 7,5 82,3 ± 7,0 16,0 ± 1,0 16,2 ± 2,5 21,5 ± 2,5 21,1 ± 2,8 11,5 ± 2,8 11,9 ± 2,5 9,7 ± 1,9 9,7 ± 2,6 27,9 ± 3,0 28,1 ± 5,7 30,8 ± 3,1 31,1 ± 3,3
Messzeitpunkte Höhenexposition Nach 6 Nach 21 Nach 45 Stunden Stunden Stunden
89,5 ± 4,1 90,6 ± 2,3 90,6 ± 2,2 89,0 ± 4,5 90,0 ± 3,2 90,6 ± 2,5 0,80 ± 0,46 --- 1,60 ± 0,55 0,94 ± 0,54 --- 1,85 ± 0,43 30,0 ± 3,1 --- 27,1 ± 2,1 31,1 ± 4,4 --- 28,4 ± 2,3 49,9 ± 3,9 --- 54,5 ± 3,6 48,9 ± 4,7 --- 52,9 ± 3,6 15,6 ± 1,0 --- 16,5 ± 1,1 15,6 ± 1,3 --- 16,6 ± 1,7 21,2 ± 1,8 --- 18,8 ± 1,9 21,6 ± 2,8 --- 19,2 ± 1,5 --- 13,9 ± 4,0 ----- 12,7 ± 2,9 ----- 11,7 ± 2,8 ----- 10,0 ± 2,5 ----- 34,5 ± 7,4 ----- 33,0 ± 5,2 ----- 36,3 ± 4,6 ----- 35,2 ± 3,5 ---
P-Wert Zeit Interaktion
<0,01 0,87
<0,01 0,67
<0,01
<0,01
<0,01
<0,01
<0,01
0,01 0,48
0,86
0,92
0,51
0,16
0,06
<0,01
<0,01 0,38
0,35
172
DISKUSSION
Das Hauptergebnis der vorliegenden Studie ist, dass das verwendete Vorakklimatisierungsprotokoll in normobarer Hypoxie keine signifikanten Effekte auf Inzidenz und Schweregrad der AMS bei einem unmittelbar folgenden Höhenaufenthalt hatte. Die Ruheventilation zeigte einen tendenziellen Anstieg von Tallage zu Höhenlage, der in der Hypoxiegruppe höher als in der Kontrollgruppe war. Diese Tendenz könnte moderate ventilatorische Anpassungen infolge des Vorakklimatisierungsprogramms widerspiegeln. Allerdings zeigten alle anderen physiologischen Parameter den typischen Verlauf, der bei einem kontinuierlichen Höhenaufenthalt zu erkennen ist - ohne Unterschiede zwischen Hypoxie- und Kontrollgruppe. Die vorliegenden Ergebnisse unterscheiden sich von jenen einer früheren Laborstudie, die in normobarer Hypoxie durchgeführt wurde. Wille et al. (17) setzten 26 Männer für 8 Stunden einer Hypoxie aus, die einer Höhe von ca. 5.300 m entsprach, vor und nach einer Vorakklimatisation mit genau demselben Protokoll, wie es in der vorliegenden Studie verwendet wurde. Die Autoren konnten einen signifikant verringerten AMS-Schweregrad in der Hypoxie- verglichen zur Placebogruppe feststellen (17). Die unterschiedlichen Ergebnisse können nicht durch die längere Hypoxieexposition in der vorliegenden Studie erklärt werden, da der zeitliche Verlauf der AMS-Symptome in den beiden Gruppen mehr oder weniger deckungsgleich war. Dennoch könnten zwei methodische Unterschiede zwischen der Studie von Wille et al. (17) und unserer die verschiedenen Effekte desselben Vorakklimatisierungsprogramms bewirkt haben. Erstens, die Effekte auf die AMS-Prävention wurden während einer Exposition in natürlicher Höhe nach einem Aufstieg mit der Bahn gefolgt von einer Wanderung von ca. 1 Stunde ermittelt. Da natürliche Höhenexpositionen mit zusätzlichen Faktoren verbunden sind, die die AMS-Entwicklung begünstigen können (z.B. Hypobarie (21)), könnte angenommen werden, dass die milden Anpassungen nicht ausreichend waren, um der AMS wirkungsvoll vorzubeugen, wenn diese zusätzlichen Stressoren vorhanden waren. Diese Annahme wird von den Erkenntnissen von Fulco et al. (22) unterstützt, die anhand der Ergebnisse ihrer Studien zum Fazit kamen, dass eine Vorakklimatisierung in normobarer Hypoxie nicht so effektiv wie in hypobarer Hypoxie ist. Schommer et al. (16) konnten hingegen durchaus relevante positive Effekte durch eine Vorakklimatisation in normobarer Hypoxie (insgesamt ca. 15 Stunden Hypoxieexposition) zeigen. Obwohl das getestete Protokoll nach einem Aufstieg auf 4.559 m keine AMS-Prophylaxe ergab, war die AMS-Inzidenz
173
markant niedriger in der Hypoxiegruppe im Vergleich zur Kontrollgruppe nach Ankunft (11% bzw. 47%) und nach der ersten Nacht (6% bzw. 47%) auf einer Höhe von 3.611 m (16). Momentan bleibt unklar, ob die höhere „absolute Dosis an Hypoxie“ der Grund dafür ist, dass die teilweise präventiven Effekte auf AMS in der Studie von Schommer et al. (16) gezeigt werden konnten. Zweitens inkludierte die vorliegende Studie eine spezifische Population von AMS-empfindlichen Probanden, also Personen, die von wiederholten AMS-Symptomen bei früheren Höhenaufenthalten berichteten. In der Praxis stellen genau diese Personen die Zielgruppe für zielgerichtete Interventionen gegen AMS dar. Allerdings könnte es sein, dass die beobachtete Unwirksamkeit der Vorakklimatisation gerade auf die selektierte Population zurückzuführen ist. Auch diese Erklärung bleibt auf Basis des momentanen Wissensstandes letztendlich ohne wissenschaftlichen Nachweis, da ein direkter Vergleich mit nicht AMS-anfälligen Probanden noch nicht durchgeführt wurde. Die vorliegende Studie weist einige Limitationen auf. Aus praktischer Sicht dürfte interessant sein, dass die Verblindung während des Vorakklimatisierungsprogramms nicht erfolgreich war. Nach Beendigung des Projekts tippten 81% der Studienteilnehmer auf die richtige Gruppenzugehörigkeit. Dies zeigt, wie schwierig es ist, Hypoxieexpositionen auch ohne körperliche Belastung in einem Studiensetting zu verblinden. Der dadurch möglicherweise entstandene Placeboeffekt hätte aber eher zu einer Überschätzung des AMS-Präventionseffekts geführt. Des Weiteren basierte die Beurteilung der AMS-Empfindlichkeit der Studienteilnehmer auf Berichten von AMS-Symptomen während Höhenexpositionen, die teilweise mehrere Jahre zurücklagen. Aufgrund fehler- oder lückenhafter Informationen könnte die Einschätzung der AMS-Empfindlichkeit bei manchen Probanden zu einer Unter- oder Überbewertung geführt haben. Eine Vorakklimatisation, die 7 einstündige passive Expositionen in normobarer Hypoxie (entsprechend 4.500 m) umfasst, dürfte bei AMS-anfälligen Personen keine signifikanten und relevanten Auswirkungen auf die AMS-Entwicklung bei einem unmittelbar folgenden Höhenaufenthalt haben. Daher scheint das getestete Vorakklimatisationsprogramm nicht geeignet, um AMS-anfällige Personen auf einen Aufenthalt im Hochgebirge vorzubereiten. Nichtdestotrotz bleibt ungeklärt, ob andere Vorakklimatisationsstrategien (wie z.B. Intervallhypoxie-Programme (23)) in der Vorbereitung AMS-anfälliger Personen erfolgreich sein könnten. Hier wäre es in Zukunft wichtig, systematische Vergleiche zwischen unterschiedlichen Vorakklimatisationsprotokollen anhand kontrollierter Studiendesigns durchzuführen.
174
Die vorliegende Arbeit wurde mit einem umfangreicheren Parametersatz in der Zeitschrift Medicine & Science in Sports and Exercise publiziert (Faulhaber M, Pocecco E, Gatterer H, Niedermeier M, Huth M, Dünnwald T, Menz V, Bernardi L, Burtscher M. Seven Passive 1-h Hypoxia Exposures Do Not Prevent AMS in Susceptible Individuals. Med Sci Sports Exerc 2016, Epub ahead of print).
DANKSAGUNG
Die Studie wurde vom Jubiläumsfonds der Österreichischen Nationalbank gefördert (Projektnummer: 15370).
LITERATUR
(1) Burtscher M., Bachmann O., Hatzl T., Hotter B., Likar R., et al. Cardiopulmonary and metabolic responses in healthy elderly humans during a 1-week hiking programme at high altitude. Eur J Appl Physiol 2001; 84: 379–386. (2) Gaillard S., Dellasanta P., Loutan L., Kayser B. Awareness, prevalence, medication use and risk factors of acute mountain sickness in tourists trekking around the Annapurnas in Nepal: A 12-year follow-up. High Alt Med Biol 2004; 5: 410–419. (3) Burtscher M., Faulhaber M., Flatz M., Likar R., Nachbauer W. Effects of short-term acclimatisation to altitude (3200 m) on aerobic and anaerobic exercise performance.
Int J Sports Med 2006; 27: 629–635. (4) Netzer N., Strohl K., Faulhaber M., Gatterer H., Burtscher M. Hypoxia-related altitude illnesses. Travel Med 2013; 20: 247–255. (5) Hackett P.H., Roach R.C. High-altitude illness. N Engl J Med 2001; 345: 107–114. (6) Beidleman B.A., Muza S.R., Fulco C.S., Cymerman A., Ditzler D. et al. Intermittent altitude exposures reduce acute mountain sickness at 4300 m. Clin Sci 2004; 106: 321–328. (7) Shukitt-Hale B., Banderet L.E., Lieberman H.R. Relationships between symptoms, moods, performance, and acute mountain sickness at 4,700 meters. Aviat Space Environ Med 1991; 62: 865–869. (8) Maggiorini M., Buhler B., Walter M., Oelz O. Prevalence of acute mountain sickness in the Swiss Alps. Br Med J 1990; 301: 853–855. (9) Mairer K., Wille M., Bucher T., Burtscher M. Prevalence of acute mountain sickness in the Eastern Alps. High Alt Med Biol 2009; 10: 239–245.
175
(10) Schneider M., Bernasch D., Weymann J., Holle R., Bärtsch P. Acute mountain sickness: influence of susceptibility, preexposure, and ascent rate. Med Sci Sports Exerc 2002; 34: 1886–1891. (11) MacInnis M.J., Lohse K.R., Strong J.K., Koehle M.S. Is previous history a reliable predictor for acute mountain sickness susceptibility? A meta-analysis of diagnostic accuracy. Br J Sports Med 2015; 49: 69–75. (12) Küpper T.E., Schöffl V. Preacclimatization in hypoxic chambers for high altitude sojourns. Sleep Breath 2010; 14: 187–191. (13) Dehnert C., Böhm A., Menold E., Grigoriev I., Bärtsch P. Simulated altitude during the night reduces severity of acute mountain sickness. Med Sci Sports Exerc 2009; 41: 175. (14) Fulco C.S., Muza S.R., Beidleman B.A., Demes R., Staab J.E., et al. Effect of repeated normobaric hypoxia exposures during sleep on acute mountain sickness, exercise performance, and sleep during exposure to terrestrial altitude. Am J Physiol Regul Integr
Comp Physiol 2011; 300: R428–436. (15) Burtscher M., Brandstätter E., Gatterer H. Preacclimatization in simulated altitudes.
Sleep Breath 2008; 12: 109–114. (16) Schommer K., Wiesegart N., Menold E., Haas U., Lahr K., et al. Training in normobaric hypoxia and its effects on acute mountain sickness after rapid ascent to 4559 m.
High Alt Med Biol 2010; 11: 19–25. (17) Wille M., Gatterer H., Mairer K., Philippe M., Schwarzenbacher H., et al. Short-term intermittent hypoxia reduces the severity of acute mountain sickness. Scand J Med Sci
Sports 2012; 22: e79–e85. (18) Millet G.P., Faiss R., Pialoux V. Point: Hypobaric hypoxia induces different physiological responses from normobaric hypoxia. J Appl Physiol 2012; 112: 1783–1784. (19) Borg G. Psychophysical bases of perceived exertion. Med Sci Sports Exerc 1982; 14: 377–381. (20) Roach R.C., Bärtsch P., Hackett P.H., Oelz O. The Lake Louise acute mountain sickness scoring system. In: Sutton JR, Houston CS, Coates G, editors. Hypoxia and Molecular
Medicine. Queen City Printers, Burlington, 1993: 272–274. (21) Roach R.C., Loeppky J.A., Icenogle M.V. Acute mountain sickness: increased severity during simulated altitude compared with normobaric hypoxia. J Appl Physiol 1996; 81: 1908–1910. (22) Fulco C.S., Beidleman B.A., Muza S.R. Effectiveness of preacclimatization strategies for high-altitude exposure. Exerc Sport Sci Rev 2013; 41: 55–63. (23) Bernardi L., Passino C., Serebrovskaya Z., Serebrovskaya T., Appenzeller O. Respiratory and cardiovascular adaptations to progressive hypoxia: effect of interval hypoxic training. Eur Heart J 2001; 22: 879–886.
176
❙ Wolfgang Domej, Peter Rohrer ❙
Immunstimulation gegen aktinische Keratosen
Immune stimulation against actinic keratoses
SUMMARY
Actinic keratoses (AKs) are erythematous or flesh coloured plaques or papules with localized hyperkeratosis and a sandpaper-like surface. AKs represent an extremely common dermatologic problem. Over the years, mountaineers are likely to develop such flat actinic keratoses on their weather-beaten faces, mainly on the skin of the forehead, temples, neck and nose, but also on the dorsal surfaces of the hands and forearms. Besides the negative cosmetic aspects the premalignant character of AKs should be mentioned. Imiquimod (IMQ) is an effective immunostimulating agent („immune response modifier“). Topical application promotes healing of such lesions within several weeks by initiating a targeted inflammatory reaction. The agent binds Toll-like-receptors (TLR) of immuno-competent cells of the skin, releasing proinflammatoric cytokines like TNF or IL-1 that stimulate other inflammatory cells to infiltrate neoplastic cell clones and bring about apoptosis. This topical therapeutic method is an excellent alternative to other established procedures like cryosurgery (liquid nitrogen), ablative methods (curettage, dermabrasion) and electro-cauterisation or laser. In the setting of a topical field treatment, IMQ allows AKs to heal without significant scarring and/or systemic side effects. Keywords: Imiquimod (IMQ), aktinic keratoses (AKs), solar keratoses, skin neoplasms, field directed therapy
ZUSAMMENFASSUNG
Aktinische Keratosen (AKs) imponieren als erythematöse bis fleischfarbene Plaques oder Papeln mit umschriebenen Hyperkeratosen und fühlbar sandpapierartiger Oberfläche; AKs stellen ein extrem häufiges dermatologisches Problem dar. Im Laufe von Jahren entwickeln viele Alpinsportler in ihrer vom
177
Wetter gegerbten Gesichtshaut flächige AKs, die sich vor allem an lichtexponierten Stellen wie Stirn-, Schläfen- und Nasenregion, Lippen, aber auch an Handrücken und Unterarmen manifestieren. Abgesehen von ihrem negativen kosmetischen Aspekt sollte ihr präkanzeröser Charakter nie außer Acht gelassen werden. Imiquimod (IMQ) ist ein lokal wirksamer Immunstimulator („immune response modifier“), dessen Anwendung zu einer gezielten inflammatorischen Reaktion führt. Die Substanz bindet speziell an Toll-like-Rezeptoren (TLR) immunkompetenter Zellen (Makrophagen, dentritische Zellen) in der Haut, wodurch proinflammatorische Zytokine wie TNF oder IL-1 zur Freisetzung kommen. Letztere stimulieren ihrerseits inflammatorische Zellen zur Infiltration der tumorösen Zellverbände, die dadurch zur Apoptose gebracht werden. Diese Feldbehandlung der AKs durch IMQ stellt eine ausgezeichnete Alternative zu anderen gängigen Verfahren wie Kryotherapie (Flüssigstickstoff), ablativen Methoden (Curretage, Dermabrasion) bzw. Elektrokauterisation oder Laser dar. IMQ ermöglicht eine Abheilung von AKs ohne wesentliche Narbenbildungen oder systemische Nebenwirkungen. Schlüsselwörter: Imiquimod (IMQ), aktinische Keratosen (AKs), solare Keratosen, Hauttumore, Feldtherapie
EINLEITUNG
Schätzungen zufolge sind mehr als 100 Millionen Menschen im EU-Raum von einer oder mehreren aktinischen Keratosen (AKs) betroffen (1, 2). Im Jahre 2004 wurde die Prävalenz für AKs in den USA auf nahezu 40 Millionen geschätzt. AKs werden in mehr als 10% aller dermatologischen Ambulanzvisiten festgestellt (1). Obwohl man sich bisher noch auf keine allgemein gültige Definition der AKs einigen konnte (3), bestehen AKs aus dysplastisch veränderten Keratinozyten beschränkt auf die Epidermis und stellen damit ein in-situ-Plattenepithelkarzinom der Haut oder anders ausgedrückt eine oberflächliche Variante des „non-melaoma skin cancer/NMSC“ dar (4). AKs sind erste Manifestationen dysplastischer Zellveränderungen, die im weiteren Verlauf zu Spontanremission, zu Chronizität oder zu maligner Transformation (squamous cell carcinoma, SCC) führen. Das dysplastische Epithel einer AK und eines SCC weisen sehr ähnliche Merkmale auf; man könnte sagen AKs und SCC repräsentieren ein und denselben Krankheitsprozess in jeweils unterschiedlichen Entwicklungsstadien (5). Die histologische Untersuchung ist
178
die Methode der Wahl bei allen unklaren Hautläsionen, bei makroskopisch eindeutigen AKs jedoch nicht zwingend erforderlich. AKs finden sich bei fast jedem zweiten Menschen über 70 Jahre; sie können sich unbehandelt zum NMSC weiterentwickeln (6, 7). Die Spontanremissionsrate bewegt sich bei AKs im Bereiche von 50%, es kommt allerdings häufig zum Wiederauftreten bereits rückgebildeter aktinischer Läsionen (3). AKs erhöhen das Risiko für sämtliche Karzinome der Haut um das 6-Fache; sie sind Folge der kumulativen Einwirkung der UV-Strahlung des Sonnenlichtes (812). Einer Metaanalyse zufolge ergab sich für Personen in „Outdoor-Berufen“ ein signifikant höheres Risiko für AKs/PE-Karzinome im Vergleich zu Berufen im Innenbereich (13). Nach Jahren der solaren Exposition können AK-Läsionen auch bei „Outdoor-Sportlern“ wie etwa Alpinisten beobachtet werden. Häufigkeitsangaben in Bezug auf dieses spezielle Kollektiv sind derzeit nicht verfügbar. Schätzungen zufolge entwickeln 10-15% aller Patienten mit AKs und etwa 30% mit zusätzlicher wie immer gearteter Immunsuppression nach Jahren ein infiltrativ wachsendes SCC (14). Es besteht ein wesentlich deutlicherer Zusammenhang zwischen UV-Exposition und der Entwicklung von AKs/ Hautkarzinomen als zwischen UV-Exposition und der Entwicklung eines malignen Melanoms (MM). AKs treten häufig multifokal als rauhe sandpapierartig tastbare Erhabenheiten an stark lichtexponierten Stellen in Erscheinung, insbesondere im Bereiche des Kopfes (Glatze, Kopfhaut, Schläfen-, Stirn-, Nasenregion, Lippen), seltener auch an Extremitäten (Unterarme, Handrücken). Oftmals sind AKs auch leichter zu ertasten als zu sehen; sie sind größenmäßig variabel, wobei der Durchmesser von wenigen Millimetern bis >2 cm reichen kann (15, 16). In den meisten Fällen bleibt die Symptomatik diskret und umfasst bestenfalls leichten Juckreiz und eine gewisse Druckempfindlichkeit, die meisten Patienten mit AKs bleiben dauerhaft asymptomatisch. Therapieziel bei AKs ist die Abheilung aktinischer Läsionen durch die Zerstörung mutierter Keratinozyten sowie deren zahlenmäßige Reduzierung. Die Behandlungsmethode sollte möglichst von minimaler Schmerzentwicklung bzw. Vernarbung begleitet sein und eine niedrige Rezidivrate aufweisen (14, 17). Eine Reihe mehr oder weniger nachhaltiger Therapieoptionen wie chirurgische Exzision, Curettage, Laser- und Kryobehandlung (18-20) oder rein topische Verfahren mit Imiquimod (IMQ), photodynamischer Therapie mit Aminolävulinsäure als Photosensibilisator, Cox-1/2-Inhibitoren oder Peeling mit 5-Fluorouracil (5-FU) stehen heute zur Verfügung (21, 22) (Tab. 1). Dabei ist nicht jede Methode für jeden Patienten bzw. jede Läsion geeignet. Die Wahl der individuell besten Behandlungsmethode richtet sich nach der Anzahl,
179
Größe, Lokalisation sowie dem Wachstumsverhalten einzelner Läsionen; auch Alter, Lifestyle und frühere Behandlungsergebnisse können bei der Auswahl eine Rolle spielen. Bei eindeutigen AKs kann die Lokalbehandlung durch den Hausarzt durchgeführt und kontrolliert werden. Erst wenn sich auf die Lokalbehandlung hin keine Befundbesserung einstellt oder der Charakter der flächig-aktinischen Keratose (Feldkanzerisierung) in einen knotig infiltrativen übergeht, sollte nicht gezögert werden, den Dermatologen zu konsultieren.
Tab. 1: Therapeutische Möglichkeiten bei aktinischen Keratosen
Chirurgische Therapie
Medikamentöse Lokaltherapie
Photodynamische Therapie
Exzision, Dermabrasion, Kryotherapie (Flüssigstickstoff)
5-Fluorouracil (Actikerall®, Verrumal® , Efudix®) (zytotoxisch) Imiquimod (Aldara®, Zyclara®)(immunmodulatorisch) Diclofenac + Hyaluronsäure (Solaraze Gel®)(antiphlogistisch) 5-Aminolävulinsäure (Levulan®, Metvix®)
Limitierungen in der Behandlung bestehen vor allem in einer eingeschränkten Patiententoleranz, wenn es um die Behandlung von Hautarealen geht, die kosmetisch mit einer bestimmten Behandlungsmethode schwer in Einklang zu bringen sind. Die Rezidivraten nach erfolgter Therapie variieren von Methode zu Methode; oftmals ist ein AK-Rezidiv Folge einer unvollständig entfernten klinisch sichtbaren Läsion oder von subklinischen, nicht detektierten AKs, die als solche nicht erkennbar waren. Wegen der für AKs typischen Feldkanzerisierung sollten bei multiplen Läsionen medikamentöse Cremen/Salben immer flächenhaft aufgetragen werden (Feldtherapie), um auch maskierte Herde zu erfassen (24, 23). Zur Zeit existiert noch kein Konsens über die wirksamste Behandlungsform. Der Antimetabolit 5-Fluorouracil hat sich in der Lokaltherapie von AKs bewährt, IMQ sowie photodynamische Therapieverfahren sind wahrscheinlich jene Methoden mit den besten kosmetischen Ergebnissen (3).
180
Abb. 1: Schematischer Wirkmechanismus von IMQ bei AK: gestufter zytokingesteuerter Ablauf bis zur Apoptose (Fortbildungsveranstaltung „Spezielle Therapien in der Dermatologie, Salzburg, 25. März 2011)

Imiquimod (IMQ)
IMQ stimuliert durch die Bindung am Toll-like-Rezeptor 7 (TLR 7) an der Oberfläche von Immunzellen (Monozyten/Makrophagen) die angeborene respektive zellvermittelte Immunität. Über die Aktivierung dendritischer Zellen und stimulierte Zytokinausschüttung (IFN-a, IL-1, TNF-a) wird in der Folge die Apoptose dysplastischer Keratinozyten eingeleitet (Abb. 1). Auf Basis der antiviralen, antitumorösen und immunregulatorischen Effekte und seltenen Nebenwirkungen ist IMQ für eine Lokaltherapie prädestiniert (25). Der Wirkstoff ist in Form von Cremen (3%/5%) verfügbar (Aldara®, Zyclara®). Topisches IMQ stellt auf Grund seines stimulierenden Einflusses auf angeborene und adaptive Immunreaktionen („immune response modifier“) sowie den damit verbundenen immunregulatorischen Eigenschaften eine ausgezeichnete Therapieoption für eine Reihe benigner und maligner Hautläsionen (AKs, superfizielles Basalzell-Karzinom/sBCC) dar (25). Die Mechanismen der Hautpenetration von IMQ wurden erst kürzlich beschrieben (26). IMQ wurde von der FDA neben der Behandlung von AKs und sBCC auch zur Behandlung anogenitaler Warzen zugelassen. Als topische Behandlungsform von AK stellt IMQ eine schmerzlose alternative Methode etwa zu chirurgischen Verfahren
181
dar und kann vom betroffenen Patienten nach entsprechender Verschreibung leicht selbst angewandt werden (Tab. 1). Ein prospektiv sorgfältig durchgeführter Sonnenschutz sollte dabei obligat sein (27), wobei die Protektion mit hochfaktoriellen Sonnenschutzmitteln unumstritten ist. Allerdings sind Präparate, in die DNA-ReparatuAbb. 2: Imiquimod (Aldara®) zur Lokalthera- renzyme (Endonuklease T4N5) pie von AKs in Form einer 5%-Creme implementiert sind, umstritten. Alpinsportler sollten sich selbst von Zeit zu Zeit kritisch in Bezug auf AK-verdächtige Hautveränderungen an den prädisponierten Stellen überprüfen. Es ist vor allem der erhöhte UV-Anteil in der Höhe, der sich kumulativ an nicht bedeckten Hautstellen abbildet.

Praktische Anwendung von IMQ
Zur Selbstbehandlung von AKs sollte IMQ flächenwirksam als 5% Creme dreimal/Woche appliziert werden (Abb. 2, 3). Klinische sowie subklinische Läsionen werden damit innerhalb von vier Wochen (12-14 Anwendungen) demaskiert, indem sie in Form entzündlicher Lokalreaktionen deutlich werden (Abb. 3). Diese gezielte Provokation einer inflammatorischen Therapieantwort ist zugleich Zeichen eines guten Ansprechens und Indikator der nachfolgenden Abheilung. Die inflammierten meist hochgeröteten Läsionen verschwinden innerhalb von 2-3 Monaten ohne Residuen zu hinterlassen (Abb. 3 a-d). Vergleichsstudien belegen, dass bei AKs unter IMQ die Heilungsraten nach einem Jahr deutlich höher liegen als vergleichsweise nach einer topischen Applikation von 5-FU oder nach Kryotherapie. Als Nebenwirkungen können sehr selten Geschmacksstörungen auftreten, da die parakrine Transmission des Wirkstoffes offensichtlich das Potential hat, von den Geschmacksknospen ausgehende afferente Signale zu modifizieren (28). IMQ kann auch mit anderen Therapien kombiniert werden; so kann beispielsweise ein Zyklus photodynamischer Therapie der Behandlung mit IMQ vorangestellt werden oder IMQ folgt auf eine initiale Kryotherapie (29). Zudem kommt IMQ auch bei sBCC mit Clearance-Raten bis über 80% sowie bei aktinischer Cheilitis (Carcinoma-in-situ der Lippe) ebenfalls mit hoher Heilungsrate zur Anwendung. Im Falle von AKs
182
sowie histologisch verifizierten sBCC gibt es auch klinische Erfahrungen mit einer Lokalbehandlung mit Ingenolmebutate-Gel (IGM) (Picato Gel® 150 µg/g; 500 µg/g) (30, 31). Die Substanz wird aus Teilen der Pflanze Euphorbia peplus (Gartenwolfsmilch) extrahiert; der größte Vorteil von IGM ist, dass bereits eine Anwendung über einen Zeitraum von 2-3 Tagen ausreichend ist. IGM erwies sich bei einer Gruppe von sieben Patienten, die eine chirurgische Sanierung abgelehnt hatten, als sehr wirksam (32). Nach Gelapplikation sollte die behandelte Fläche 6 Stunden lang nicht mit Wasser in Berührung kommen, das Präparat sollte unbedingt bei 2-8°C gelagert werden. Bei fortgeschrittenen Basalzellkarzinomen (Basaliomen/BCC) hat sich eine perorale Behandlung mit Vismodegib (Erivedge Kpsl.®) als wirkungsvolle Therapieoption jener Lokalisationen herausgestellt, die chirurgischen Verfahren schwer zugänglich sind. Vismodegib hat sich selbst bei fortgeschrittenen potentiell entstellenden BCC als hochwirksam erwiesen (33) und vermag das Tumorwachstum, das von Hedgehog-Mutationen ausgeht (>90% aller BCC mit dieser Genmutation), zu hemmen.


Abb. 3a-d: Multiple AKs im Bereiche der Stirne. IMQ-Behandlung im Verlauf von 14 Wochen (vor Behandlung, dann nach 2, 6, 14 Wochen)

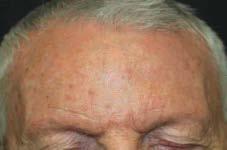
183
DANKSAGUNG
Wir danken der Firma MEDA Pharma GmbH, insbesondere Herrn Heinrich Hirschmugl und Frau Natascha Müllner, MSC, für die Bereitstellung des Bildmaterials.
LITERATUR
(1) Bickers D.R., Lim H.W., Margolis D., Weinstock M.A., Goodman C. et al. The burden of skin diseases: 2004 a joint project of the American Academy of Dermatology Association and the Society for Investigative Dermatology. J Am Acad Dermatol 2006; 55(3): 490–500. (2) Rosen T., Lebwohl M.G. Prevalence and awareness of actinic keratosis: barriers and opportunities. J Am Dermatol 2013; 68: 2–9. (3) Siegel J.A., Korgavkar K., Weinstock M.A. Current perspective on actinic keratosis: a review. Br J Dermatol 2016. Epub ahead of print. (4) Röweret-Huber J., Patel M.J., Forschner T., Vinciullo C., Francis D. et al. Actinic keratosis is an early in situ squamous cell carcinoma: a proposal for reclassification. Br J
Dermatol 2007; 156(3): 8–12. (5) Cockerell C.J. Histopathology of incipient intraepidermal squamous cell carcinoma („actinic keratosis“). J Am Acad Dermatol 2000; 42(1Pt2): 11–17. (6) Marks R., Rennie G., Selwood T.S. Malignant transformation of solar keratoses to squamous cell carcinoma. Lancet 1988; 1(8589): 795–797. (7) Chen G.J., Feldman S.R., Williford P.M., Hester E.J., Kiang S.H. et al. Clinical diagnosis of actinic keratosis identifies an elderly population at high risk of developing skin cancer. Dermatol Surg 2005; 31(1): 43–47. (8) Bauer A. Skin cancer as occupational disease. Hautarzt 2016. Epub ahead of print. (9) Trakatelli M., Barkitzi K., Apap C., Majewski S., De Vries E. EPIDERM Group. Skin cancer risk in outdoor workers: a European multicenter case control study. J Eur Acad
Dermatol Venereol 2016; Suppl 3: 5–11. (10) Ruppert L., Ofenloch R., Surber C., Diepgen T. Occupational risk factors for skin cancer and the availability of sun protection measures at German outdoor workplaces. Int
Arch Occup Environ Health 2016; 89(6): 1009–1015. (11) Berman B., Cockerell C.J. Pathobiology of actinic keratosis: ultraviolet-dependent keratinocyte proliferation. Am J Acad Dermatol 2013; 68(1Suppl1): 10–19. (12) Frost C., Williams G., Green A. High incidence and regression rates of solar keratoses in a Queensland community. J Invest Dermatol 2000; 115(2): 273–277.
184
(13) Fartasch M., Diepgen T.L., Schmitt J., Drexler H. The relationship between occupational sun exposure an non-melanoma skin cancer: clinical basics, epidemiology, occupational disease evaluation, and prevention. Dtsch Ärztebl Int 2012; 109(43): 715–720. (14) Stockfleth E. Topical management of actinic keratosis and field cancerisation. G Ital
Dermatol Venereol 2009, 144(4): 459–462. (15) Moy R.L. Clinical presentation of actinic keratoses and squamous cell carcinoma. J
Am Acad Dermatol 2000; 42(1Pt2): 8–10. (16) Filosa A., Filosa G.G. Actinic keratosis and squamous cell carcinoma: clinical and pathological features. Ital Dermatol Venereol 2015;150(4): 379–384. (17) Pickert A. Treatment of actinic keratoses. Cutis 2012; 90(1): 1–3. (18) Coleman W.P. 3rd, Yarborough J.M., Mandy S.H. Dermabrasion for prophylaxis and treat-ment of actinic keratoses. Dermatol Surg 1996; 22(1): 17–22. (19) Thai K.E., Fergin O., Freeman M., Vinciullo C., Francis D. et al. A prospective study of the use of cryosurgery for the treatment of actinic keratoses. Int J Dermatol 2004; 43(9): 687–692. (20) Kuflik E.G. Cryosurgery updated. J Am Acad Dermatol 1994; 31(6): 925–944. (21) Savoia P., Cremona O., Fava P. New Perspectives in the pharmacological treatment of non-melanoma skin cancer. Curr Drug Targets 2016; 17(3): 353–374. (22) Vegter S., Tolley K. A network meta-analysis of the relative efficacy of treatments for actinic keratosis of the face or scalp in Europe. PLOS ONE 2014; 9(6): e96829. (23) Goldenberg G., Perl M. Actinic keratosis: update on field therapy. J Clin Aesthet Dermatol 2014; 7(10): 28–31. (24) Kopera D., Kerl H. Visualization and treatment of subclinical actinic keratosis with topical imiquimod 5% cream: an observational study. BioMed Res Int 2014; 2014: 135916. doi: 10.1155/2014/135916 (25) Hanna E., Abadi R., Abbas O. Imiquimod in dermatology: an overview. Int J Dermatol 2016; 55(8): 831–844. (26) Telo I., Pescina S., Padula C., Santi P., Nicoli S. Mechanisms of imiquimod skin penetration. Int J Pharm 2016; 511(1): 516–523. (27) Naylor M.F., Boyd A., Smith D.W., Cameron G.S., Hubbard D., Neldner K.H. High sun protection factor sunscreens in the suppression of actinic neoplasia. Arch Dermatol 1995; 131(2): 170–175. (28) Huang A.Y., Wu S.Y. The effect of imiquimod on taste bud calcium transients and transmitter secretion. Br J Pharmacol 2016; 173(21): 3132–3133. (29) Jorizzo J.L., Markowitz O., Lebwohl M.G., Bourcier M., Kulp J. et al. A randomized, double-blinded, placebo-controlled, multicenter, efficacy and safety study of 3,75%
185
imiquimod cream following cryosurgery for the treatment of actinic keratoses. J
Drugs Dermatol 2010; 9(9): 1101–1108. (30) Martin G., Swanson N. Clinical findings using ingenol mebutate gel to treat actinic keratoses. J Am Acad Dermatol 2013; 68(1Suppl1): 39–48. (31) U.S. Food and Drug Administration. DDA Drug Safety Communication: FDA warns of severe adverse events with application of Picato (ingenol mebutate) gel for skin condition; http://www.fda.gov/Drugs/DrugSafety/ucm459142.htm. (32) Bettencourt M.S. Treatment of superficial basal cell carcinoma with ingenol mebutate gel, 0,05%. Clin Cosmet Investig Dermatol 2016; 9: 205–209. (33) Sligh J.E. Jr. New therapeutic options for actinic keratosis and basal cell carcinoma.
Semin Cutan Med Surg 2014; 33(4Suppl): 76–80.
186
❙ Luca Moroder, Peter Mair ❙
Lawinenverschüttung – Grenzen der Laienreanimation nach Kameradenrettung
Limitations of bystander CPR after avalanche burial
SUMMARY
Bystander CPR can increase the survival rate of avalanche victims with cardiac arrest up to 22%. After avalanche burial, due to limited patient access and atypical body position, resuscitation efforts often cannot be performed strictly following standard algorithms and efficiency of bystander CPR may be limited. In the guidelines released by the European Resuscitation Council (ERC) there is no defined algorithm for basic life support resuscitation of avalanche victims in atypical body position or with a difficult rescue/extricating situation. Aim of this paper was to try to establish evidence-based recommendations for bystander CPR of patients in difficult rescue scenarios after avalanche burial, based on published evidence from scientific papers and reports. We carried out a electronical (Medline) and a manual literature review using the key words “resuscitation of avalanche victims”, “asphyxial cardiac arrest”, “resuscitation with difficult patient access” and “resuscitation in atypical body position”. Literature review revealed only reports including data with low or very low evidence level. Establishing free airways to allow spontaneous respiration or to start mouth to mouth ventilation is the intervention of upmost priority in the management of a patient rescued with no signs of life after avalanche burial. According to the ERC algorithm, patients with asphyxial cardiac arrest should receive 5 initial rescue breathings. If spontaneous respiration does not start, CPR including chest compressions is required. However, in many cases a getting free and unhindered access to the patient’s chest for external compression can be very time consuming or the patient is found in an atypical body position. There is no scientific evidence if in this particular circumstance a “ventilation-only-CPR” or intermittent ventilation during extrication efforts
187
can improve the chance of survival as compared to the interruption of resuscitation measures during extrication. In case of a victim position making standard rescuer position impossible (e.g. face down position, restricted patient access from the side), alternative techniques of external chest compression (e.g. over-head-position, chest compression from behind) should be considered. If several bystanders are present at scene, resuscitation efforts and extrication efforts can be performed simultaneously. Problems and limitations of basic life support resuscitation in the particular scenario of an avalanche accident should be taught and discussed during first-aid-courses for skiers. More research data are needed to optimize bystander CPR after comrade rescue in order to improve survival rates of avalanche victims. Keywords: cardiac arrest, cardiopulmonary resuscitation, avalanche, algorithm
ZUSAMMENFASSUNG
Laienreanimation am Lawinenfeld erhöht die Überlebenschancen für Lawinenopfer mit Herz- Kreislaufstillstand auf bis zu 22%. Durch die besonderen Umstände dieses Notfalls kann eine optimale, den Leitlinien entsprechende, Laienreanimation nach Lawinenverschüttung allerdings oft deutlich erschwert oder sogar unmöglich sein. In den Leitlinien des European Resuscitation Council (ERC) zur Wiederbelebung existieren keine definierten Algorithmen zum Vorgehen bei Patienten mit Herz- Kreislaufstillstand bei atypischer Körperposition oder bei erschwertem Patientenzugang. Ziel der vorliegenden Arbeit war, mit Hilfe bisher publizierter Erfahrungen evidenzbasierte Behandlungsempfehlungen für Laienhelfer für die Versorgung von Lawinenopfern mit Herz- Kreislaufstillstand in einer die Reanimation erschwerenden Auffindungsposition zu erstellen. Mittels elektronischer (Medline) und anschließender händischer Literatursuche wurden Publikationen zu den Themen „Reanimation beim Lawinenunfall“, „Reanimation bei Asphyxie“, „Reanimation bei eingeschränktem Patientenzugang“ und „Reanimation in atypischer Körperposition“ gesucht und auf relevante Informationen für die Erstellung der Behandlungsempfehlungen zur Laienreanimation nach Lawinenverschüttung hin untersucht. Insgesamt wurden nur wenige Publikationen zu den genannten Themen gefunden und alle enthielten ausschließlich Daten auf niedrigem oder sehr niedrigem Evidenzniveau. Auf Basis der gefundenen Evidenz hat die Freilegung der Atemwege, um eine Spontanatmung oder eine eventuell erforderliche Beatmung möglichst rasch zu ermöglichen, absolute Priorität. Auch bei guter Patientenzugänglichkeit müssen vor Beginn einer Herzdruckmassage bei allen
188
Patienten ohne Lebenszeichen, fünf Initialbeatmungen durchgeführt werden, da sie vermutlich einen hypoxisch bedingten Herz- Kreislaufstillstand erlitten haben. Setzt nach 5 initialen Beatmungen keine Spontanatmung ein, wird der sofortige Beginn einer Herzdruckmassage allgemein empfohlen. Bei Lawinenverschüttung wird die Freilegung des Brustkorbes zur Durchführung der Herzdruckmassage oft sehr viel Zeit benötigen bzw. befindet sich der Patient nach Freilegung des Brustkorbes häufig nicht in Rückenlage. Ob im Falle einer oft zeitraubenden Freilegung des Brustkorbs das Fortführen der Reanimation mit alleiniger Beatmung oder eine intermittierende Beatmung während der Freilegung des Opfers die Überlebenswahrscheinlichkeit im Vergleich zu einer Reanimationsunterbrechung erhöhen, ist nach heutiger Datenlage unklar. Bei ungünstiger Lage des Opfers (nur Zugang von oben/unten, Bauchlage) können auch atypische Positionen des Retters zur Durchführung der Herzdruckmassage in Erwägung gezogen werden (Über-Kopf-Position, Grätschstellung, Kompression des Brustkorbs von dorsal). Sind mehrere Ersthelfer vor Ort kann eine koordinierte Arbeitsteilung reanimationsfreie Intervalle kurz halten. In Erste-Hilfe-Kursen für Schneesportler sollten die Probleme und Limitationen der Reanimation am Lawinenfeld angesprochen und mögliche Lösungsansätze diskutiert werden, sowie auf die große Bedeutung freier Atemwege und eine sofortige Beatmung hingewiesen werden. Untersuchungen zur Optimierung der Laienreanimation am Lawinenkegel wären ein wichtige Aufgabe für die alpine Notfallmedizin und könnten die Überlebenschancen Lawinenverschütteter deutlich verbessern. Schlüsselwörter: Kreislaufstillstand, Kardiopulmonale Reanimation, Lawine, Algorithmus
EINLEITUNG
Durchschnittlich sterben in Nordamerika und Europa jährlich etwa 146 Menschen durch Lawinenunfälle (1). Die Sterblichkeit bei Lawinenopfern liegt in Abhängigkeit von der vorgefundenen Verschüttungssituation im Schnitt bei 23%. Verschüttungsgrad, Verschüttungsdauer, Verschüttungstiefe, Vorhandensein einer Atemhöhle sowie Begleitverletzungen spielen eine entscheidende Rolle für das Überleben nach Verschüttung in den Schneemassen einer Lawine (1). Asphyxie ist zu 70–80% für den Tod nach Lawinenunfällen ursächlich, während tödliche Traumata in 10–30% verantwortlich sind (2). Die schwere akzi-
189
dentelle Hypothermie spielt als Todesursache erst bei langer Verschüttungsdauer eine Rolle (2). Die Verschüttungsdauer ist ein ganz entscheidender Faktor für das Überleben von Lawinenopfern. Die Überlebenswahrscheinlichkeit bei einer Verschüttungsdauer bis zu 18 Minuten liegt laut der von Brugger et al. 1996 publizierten Überlebenskurve ganzverschütteter Lawinenopfer immerhin noch bei etwa 90% (3). Dies unterstreicht die enorme Wichtigkeit der Kameradenrettung und Laienreanimation in den ersten Minuten nach Lawinenabgang.
Grundlagen des asphyxiebedingten Herz-Kreislaufstillstand
Die Pathophysiologie eines Herz-Kreislaufstillstands im Rahmen eines Lawinenunfalls mit Kameradenrettung und kurzer Verschüttungszeit ist jener beim Ertrinken und Erhängen sehr ähnlich. In allen Fällen ist meist eine Asphyxie Ursache für den Herz-Kreislaufstillstand. So führt die plötzlich auftretende, rasch voranschreitende und nicht sofort reversible Hypoxie zu einer Bewusstseinseintrübung bzw. einem Bewusstseinsverlust innerhalb von etwa 1–2 Minuten. In weiterer Folge entwickelt sich ein immer größeres Sauerstoffdefizit mit metabolischer Azidose und gleichzeitiger Hyperkapnie, welche innerhalb von 3–10 Minuten über eine zentrale Atemlähmung zum Herz-Kreislaufstillstand, und in der weiteren Folge unbehandelt zum Tod führen. Aus dieser Pathophysiologie resultiert nur ein sehr kurzer, 1 bis 2 minütiger Zeitraum zwischen Eintritt eines Kreislaufstillstandes und dem Auftreten irreversibler Schäden im Gehirn (4, 5). Aus diesem Grund ist für das Überleben von Patienten mit Asphyxie bedingtem Herz-Kreislaufstillstand, z.B. Lawinenopfern, die sofortige Durchführung von kombinierten Reanimationsmaßnahmen (Thoraxkompressionen und Beatmung) von enormer Wichtigkeit. Es konnte in Studien wiederholt gezeigt werden, dass die kombinierte Form der Reanimationsmaßnahmen mit gleichzeitiger Beatmung der sogenannten „compression only“ Reanimation bei Patienten mit asphyktischem Herz-Kreislaufstillstand überlegen ist. Im Herbst 2015 hat das European Resuscitation Council (ERC) seine neuen Leitlinien für Reanimation vorgestellt und publiziert (6). Wie auch in den Jahren zuvor wurde für einen durch Asphyxie bedingten Herz-Kreislaufstillstand ein eigener Algorithmus erarbeitet. Dieser sieht 5 Initialbeatmungen vor Beginn der kombinierten Reanimationsmaßnahmen, mit 30 Thoraxkompressionen und 2 Beatmungen im Wechsel, vor (6). Allerdings kann dieser Algorithmus des ERC im Rahmen eines Lawinenunfalls häufig nur beschränkt umgesetzt werden, meist nur dann, wenn der Brustkorb bei Rückenlage des
190
Patienten sehr rasch und vollständig von den Schneemassen befreit werden kann. Ist der Brustkorb eines Patienten nicht oder nur zum Teil für eine Reanimation freigelegt oder ist das Opfer in Bauch- oder Seitenlage verschüttet, wird der sofortige Beginn der in den ERC Leitlinien geforderten Herzdruckmassage schwierig. In der Regel würde dann eine den Leitlinien entsprechende Reanimation das komplette Ausgraben des Lawinenopfers mit Bergung an die Oberfläche erfordern, was andererseits zu einer inakzeptabel langen Reanimationsunterbrechung von mehreren Minuten führen würde. Für diese in der Praxis beim Lawinenunfall häufige und relevante Situation existieren bis heute keine Handlungsempfehlungen.
Das reanimationspflichtige Lawinenopfer nach Kameradenrettung
Untersuchungen der letzten Jahre haben gezeigt, dass Reanimationsmaßnahmen durch Ersthelfer das Überleben und den Outcome von Lawinenopfern maßgeblich positiv beeinflussen können, vor allem dann wenn diese sofort und richtig durchgeführt werden (7). Die richtige Durchführung von leitliniengerechten Reanimationsmaßnahmen muss durch Kurse und regelmäßiges Training erlernt werden; allerdings werden in heute üblichen Kursen die lebensrettenden Sofortmaßnahmen fast immer in einem „normalen“ Umfeld gelehrt, d.h. mit einem Patienten in Rückenlage ohne erschwerende äußere Einflüsse. Beim Lawinenunfall wird sich die Situation allerdings ganz anders darstellen. So liegen beispielsweise reanimationspflichtige Personen noch zum Teil oder gar zur Gänze in den Schneemassen und müssen erst so befreit werden, dass Reanimationsmaßnahmen sinnvoll möglich sind. Bei Kursen für Wintersportler sollte dies immer beachtet werden. Hilfreich wären an dieser Stelle spezifisch auf diese Situation zugeschnittene, adaptierte Algorithmen, nach denen der Laienhelfer am Lawinenfeld vorgehen könnte. Derartige Algorithmen für den Ersthelfer am Lawinenfeld existieren allerdings noch nicht. Mit dieser Thematik wollen wir uns im Folgenden auseinandersetzen und versuchen, einen Vorschlag für, so weit wie möglich, evidenzbasierte Behandlungsempfehlungen zur Erstversorgung reanimationspflichtiger Lawinenopfer durch Laienhelfer nach erfolgreicher Kameradenrettung zu erstellen. Basis dieser Empfehlungen sind eine elektronische (Medline) und anschließend händische Literatursuche in relevanten Publikationen zu den Problemfeldern „Reanimation beim Lawinenunfall“, „Reanimation bei Asphyxie“, „Reanimation bei eingeschränktem Patientenzugang“ und „Reanimation in atypischer Körperposition“.
191
1. Beatmung
Nach einem Lawinenabgang soll unmittelbar mit der Suche nach Verschütteten begonnen und gleichzeitig ein Notruf abgesetzt werden. Wird ein Verschütteter lokalisiert, so soll dieser möglichst rasch soweit freigelegt werden, dass Mund bzw. Nase schneefrei sind und das Gesicht des Opfers für den Retter frei zugänglich ist. Anschließend wird nach Lebenszeichen wie zum Beispiel Husten, Schlucken, Seufzen oder Spontanatmung gesucht. Das Opfer wird auch gemäß den ERC-Leitlinien berührt und laut angesprochen, um eine entsprechende Reaktion auszulösen. Reagiert der Patient darauf, soll dieser weiterhin engmaschig kontrolliert, betreut, und Kopf sowie Oberkörper der Situation entsprechend vorsichtig weiter ausgegraben werden. Soweit noch nicht erfolgt, sollte spätestens jetzt ein Notruf durch den Ersthelfer selbst oder durch zufällig anwesende Personen abgesetzt werden. Reagiert das Opfer nicht, muss unverzüglich das Vorhandensein von Atemaktivität kontrolliert werden. Im Falle einer Lawinenverschüttung müssen dazu der Kopf und obere Brustkorb soweit freigelegt werden, sodass ein adäquates Atemwegsmanagement möglich ist. Darunter versteht man eine problemlos durchführbare, vorsichtige Überstreckung des Kopfes, eine ungehinderte Öffnung des Mundes zum Entfernen von Schneeresten sowie im besten Fall eine gute Sicht auf den Brustkorb des Patienten. Im Anschluss wird der Kopf des Patienten leicht nach hinten überstreckt und der Mund geöffnet, gefolgt von der Kontrolle der Atmung für 10 Sekunden und zwar nach dem „Sehen- Hören- Fühlen“-Prinzip. Da häufig der Brustkorb noch von Schneeresten bedeckt ist und somit das Sichtbarwerden von Atembewegungen erschwert ist, wird die Atmung durch Hören des Atemzugs an Mund oder Nase des Patienten wahrgenommen und durch Fühlen der Atemzug an der Wange gespürt. Zwei mögliche Vorgehensweisen können anschließend entsprechend den erhobenen Befunden notwendig werden:
a) Atmet der Patient, so sollen durch vorsichtige Überstreckung des Kopfes die Atemwege des Patienten weiterhin offen gehalten werden. Der Patient wird engmaschig kontrolliert, d.h. die Vitalfunktionen Bewusstsein und Atmung werden in regelmäßigen, kurzen Abständen neu evaluiert. Falls noch nicht erfolgt, sollte spätestens jetzt ein Notruf abgesetzt werden. In weiterer Folge
192
Abb. 1: Vorschlag zur Versorgung von Lawinenverschütteten ohne Lebenszeichen – Beatmung
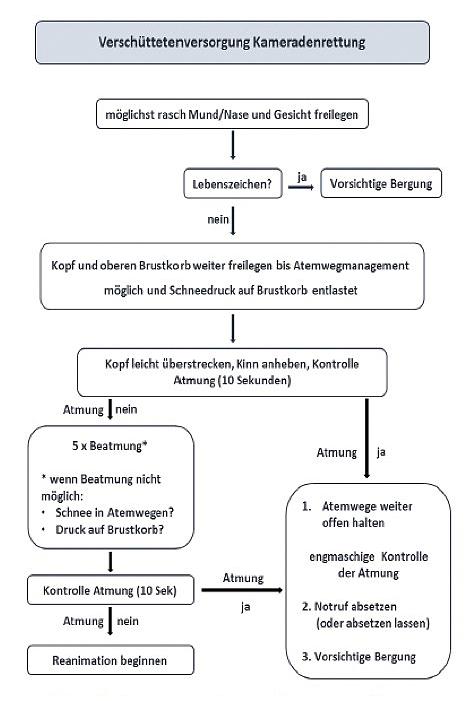
193
wird der Oberkörper des Patienten vorsichtig von den restlichen Schneemassen freigelegt. Nach Freilegen der Atemwege wird der Patient auf Grund seiner suffizienten Spontanatmung in aller Regel rasch aufklaren und das Bewusstsein wiedererlangen.
b) Atmet der Patient nicht, wird der Patient zunächst 5 Mal mittels Mund-zuMund- oder mittels Mund-zu-Nase-Methode beatmet. Ist dies nicht möglich, so müssen neben einer zu geringen Überstreckung des Kopfes oder einer inkorrekt durchgeführten Technik zur Beatmung zwei weitere, lawinenspezifische Ursachen in Betracht gezogen werden: einerseits können die Atemwege weiterhin durch Schnee verlegt sein, anderseits können Schneemassen den Thorax soweit komprimieren, dass eine suffiziente Beatmung nicht möglich ist. Diese Ursachen müssen in Folge so rasch als möglich behoben werden und der Patient neuerlich 5 Mal beatmet werden. Bis heute ist nicht untersucht, wie und ob überhaupt Mund-zu-Mund- oder Mund-zu-Nase-Beatmung durch einen Laien auf beengtem Raum oder in atypischer Körperposition möglich und erlernbar ist. Daten dazu wären aber essentiell, um evidenzbasierte Empfehlungen zu erstellen hinsichtlich des Ausmaßes der notwendigen Freilegung von Kopf und Oberkörper des Verschütteten zur effektiven Beatmung und Reanimation. Tritt nach den 5 Beatmungen Atemaktivität ein, so soll wie in Punkt a) beschrieben vorgegangen werden. Setzt nach den 5 Beatmungen keine Spontanatmung ein, wird die Situation sehr komplex.
2. Herzdruckmassage
Setzt nach 5 initialen Beatmungen keine Spontanatmung ein, sollte entsprechend den ERC-Richtlinien zur Reanimation bei Asphyxie unverzüglich mit kombinierten Herz-Wiederbelebungsmaßnahmen, also Herzdruckmassage und Beatmung, begonnen werden. In der Realität wird das Lawinenopfer oft nicht sofort und problemlos soweit freigelegt werden können, dass eine Herzdruckmassage unter Standardbedingungen möglich ist. Außerdem sind Laien selten auf diese Situation vorbereitet, da in Kursen zur Reanimation bzw. zu medizinischen Notfällen in der Regel mit ausreichend Platzangebot mit einer
194
Abb. 2: Vorschlag zur Versorgung von Lawinenverschütteten mit Herz-Kreislaufstillstand – Herzdruckmassage

seitlichen Standardposition an einem am Rücken liegenden Patienten geübt wird. In einer kürzlich publizierten Untersuchung wurden die unterschiedlichen Auffindungspositionen verschütteter Lawinenopfer beschrieben. Insgesamt wurden 159 Patienten hinsichtlich Körperlage und Kopfposition unter-
195
sucht. Die Bauchlage war mit 45% die häufigste Auffindungssituation, gefolgt von der Rückenlage mit etwa 24%. In 16% der Fälle wurden die Patienten stehend oder sitzend vorgefunden, 15% wurden in Seitenlage verschüttet. Die meisten Patienten lagen mit dem Kopf talwärts gerichtet (65%), in 24% der Fälle war der Kopf bergwärts und in 11% auf gleichem Niveau wie der restliche Körper ausgerichtet (8). Es gibt bis heute kaum Daten zum „Wie“ einer Herzdruckmassage bei räumlicher Enge, bei beschränktem Patientenzugang oder atypischer Körperposition. Damit ist es derzeit nicht möglich, für diese Situation klare, einfache und für Laien auch schulbare Algorithmen zu erstellen. Auch sind alle dahingehend angestellten Überlegungen auf sehr wenig und schwacher Evidenz basierend. Klar ist allerdings, dass im Falle der Notwendigkeit einer Herzdruckmassage ein differenzierteres Vorgehen am Lawinenfeld bereits durch den Laienhelfer erforderlich sein wird. Primär entscheidend ist, innerhalb welcher Zeitspanne der Patient vermutlich soweit freigelegt werden kann, dass eine Herzdruckmassage sinnvoll durchgeführt werden kann. Ist die Freilegung des Patienten sofort möglich, beispielsweise bei lockeren Schneeverhältnissen, so wird man sich für das weitere Ausgraben des Opfers entscheiden. Ob dieses durch zwischengeschaltete Beatmungszyklen unterbrochen werden soll oder nicht, ist heute unklar. Dauert das Freilegen des Opfers für eine suffiziente Herzdruckmassage voraussichtlich länger, stellt sich die Frage, ob ein reanimationsfreies Intervall dieser Dauer akzeptiert werden darf. Alternativ könnte man das Fortführen der Beatmungen als einzige Reanimationsmaßnahme überlegen, unter der Annahme, dass dem Fehlen von Lebenszeichen eine kardiale Restaktivität zu Grunde liegt, die sich nach Durchbrechen der Hypoxie spontan normalisiert. Tierexperimentelle Daten legen nahe, dass eine Beatmung alleine bei asphyxiebedingtem Kreislaufstillstand einen besseren Outcome ermöglicht als keine Reanimationsmaßnahmen. Wie bereits beschrieben ist das rasche Freimachen der Atemwege und Beginn der Beatmung von oberster Priorität und möglicherweise in der meist vorliegenden sehr frühen Phase der Asphyxie entscheidender für das Überleben des Patienten als Herzdruckmassage. Sind mehrere Helfer vor Ort, so können alle beschriebenen Maßnahmen natürlich parallel erfolgen: So kann beispielsweise die Beatmung durch einen Helfer so lange weitergeführt werden, bis durch den zweiten Helfer der Brustkorb freigelegt worden ist und eine kombinierte Reanimation möglich ist. Zusammenfassend zeigen alle Überlegungen die dringende Notwendigkeit für weitere Untersuchungen zur Durchführung einer Herzdruckmassage in der speziellen Situation einer Lawinenverschüttung auf.
196
Publikationen in der Literatur legen nahe, dass in speziellen Situationen unkonventionelle Positionen zur Durchführung der Herzdruckmassage erfolgreich sein können, zum Beispiel eine „Über-Kopf-Position“, eine „Grätschstellung“ (Abb. 2) oder eine von dorsal durchgeführte Kompression des Thorax. Bei der „Über-Kopf-Position“ positioniert sich der Ersthelfer in kniender Position über den Kopf des Patienten und führt von hier aus die Herzdruckmassage durch; analog dazu kann sich der Ersthelfer in der sog. „Grätschstellung“ vom Becken aus über den Patienten stellen und von hier aus die Herzdruckmassage durchführen. Einzelerfahrungen zeigen, dass diese atypischen Formen der Wiederbelebung durchaus suffiziente Blutflüsse generieren können. Im Extremfall kann eine Durchführung der Herzdruckmassage sogar in Bauchlage erwogen werden; dass dies – zumindest im innerklinischen Setting – erfolgreich sein kann, zeigen publizierte Fallberichte eindrücklich (9). Bevor diese alternativen Methoden der Reanimation in Kursen für Wintersportler geschult werden, sind sicher weitere Untersuchungen notwendig.
SCHLUSSFOLGERUNGEN
Ein Kreislaufstillstand nach Lawinenverschüttung und Kameradenrettung ist typischerweise durch Asphyxie bedingt und die damit verbundene extrem kurze Zeitspanne für eine erfolgreiche Reanimation mit neurologischer Erholung erfordert ein sofortiges und richtiges Handeln des Laienretters. Durch atypische Körperposition und beschränkten Patientenzugang kann Laienreanimation nach Lawinenverschüttung allerdings deutlich erschwert sein und viele der auftretenden Probleme und Limitationen werden in den ERC-Leitlinien zur Wiederbelebung nicht abgehandelt. Das rasche Freimachen der Atemwege und Beginn der Beatmung haben oberste Priorität und können nach klaren, auch auf Evidenz basierenden, Empfehlungen durchgeführt werden. Kombinierte Reanimation mit Beatmung und Herzdruckmassage ist meist nur mit viel Improvisation möglich, dazu häufig erst verzögert oder abweichend vom Standardverfahren. Alternative Formen der Herzdruckmassage könnten in der Laienreanimation nach Lawinenverschüttung eine Rolle spielen, sind aber derzeit noch zu wenig untersucht.
197
LITERATURNACHWEIS
(1) Brugger H., Durrer B., Adler- Kastner L., Falk M., Tschirky F. Field management of avalanche victims. Resuscitation 2001 Oct; 51(1): 7–15. (2) Hohlrieder M., Brugger H., Schubert HM., Pavlic M., Ellerton J., Mair P. Pattern and severity of injury in avalanche victims. High Alt Med Biol 2007; 8(1): 56–61. (3) Brugger H., Paal P., Bojd J. Prehospital resuscitation of the buried avalanche victim.
High Alt Med Biol 2011; 12(3): 199–205. (4) Safar P., Paradis N.A., Weil M.H. Asphyxial cardiac arrest. In: Paradis NH, Halperin HR., Kern KB, Wenzel V., Chamberlain DA, editors. Cardiac arrest – the science and practice of resuscitation medicine. 2nd. Ed. Cambridge University Press 2007; 969–993. (5) Farmery A.D., Roe P.G. A model to describe the rate of oxyhaemoglobin desaturation during apnoea. Br. J. Anaesth 1996; 79: 284–291. (6) ERC- Leitlinien zur Reanimation 2015, Kapitel 2 Basismaßnahmen zur Wiederbelebung Erwachsener und Verwendung automatisierter externer Defibrillatoren, Kapitel 3 Erweiterte Reanimationsmaßnahmen für Erwachsene („adult advanced life support“), Kapitel 4 Kreislaufstillstand in besonderen Situationen. (7) Moroder L., Mair B., Brugger H., Voelckel W., Mair P. Outcome of avalanche victims with out- of- hospital cardiac arrest. Resuscitation 2015 Apr; 89: 114–118. (8) Kornhall D.K., Logan S., Dolven T. Body Positioning of Buried Avalanche Victims.
Wilderness Environ Med 2016 Jun; 27(2): 321–325. (9) Haffner E., Sostarich A.M., Fösel T. Erfolgreiche kardiopulmonale Reanimation in
Bauchlage. Anaesthesist 2010; 59: 1099–1101.
198
❙ Simon Woyke, Mathias Ströhle, Hans Ebner, Peter Paal ❙
Flugunfälle im alpinen Gelände Österreichs von 2006 bis 2015
Flight accidents in alpine terrain of Austria from 2006 to 2015
SUMMARY
About 3,000 accidents per year happen in alpine terrain in Tyrol, Austria. There are no incidences of alpine accidents. This study assessed injury patterns resulting from aviation accidents in alpine terrain, and also explored risk factors as well as prevention and prehospital emergency care. Personal patient data of University Innsbruck Trust got assigned retrospectively to anonymized data of alpine police in the period from 01/01/2006 to 31/12/2015. Information concerning the accident´s sequence of events could be matched with medical data and get analyzed. Trends in causal correlations were deduced from frequency distributions and comparative calculations. This study included 126 persons, which have been injured in an aviation accident in alpine terrain in Austria and were subsequently treated at the University Innsbruck Hospital. Information concerning pre-clinical care, clinical care and diagnoses have been classified from medical records. Additionally, an accident statistics including 2,037 persons, that were injured in an aviation accident in Austria, was created from a data base of the Austrian Alpine Police. Areas with an increased number of aviation accident events could be detected within Tyrol. The vast majority were paragliders, followed by hang-gliders. According to police data most persons were seriously injured and were rescued by helicopter. National Advisory Committee for Aeronautics (NACA) Score 4 (serious injury, life-threatening condition possible) was scored most frequently by the emergency doctor. Especially fractures of the thoracic and the lumbar spine (69 of 125*; 55.2%) stand out. Other common injuries were head injuries (24 of 125*; 19.2%), pelvic injuries (22 of 125*; 17.2%), injuries of the limbs (especially ankle injuries (17 of 125*; 13.6%)) and injuries of the spinal cord (12 of 125*; 9.6%). According to the Abbreviated Injury Score (AIS) the areas head and neck were often injured severely to critically (AIS 4–6), areas chest,
199
abdomen and pelvic were mostly injured seriously to severely (AIS 3–4). Causes of death were head injuries (twice), respiratory failure (once) and haemorrhagic shock (once). *In one person diagnoses could not be detected. Serious injuries and multiple trauma were common, especially injuries of the thoracic and lumbar spine, in part with persisting neurological deficits caused by spinal cord, and ankle injuries. Existing protection systems should be improved. Adequate immobilization and analgesia is essential during pre-hospital emergency care to prevent further injuries and pain. Keywords: alpine terrain, aviation accidents, cardiac arrest, electricity, hanggliding accidents, injury, lightning, paragliding accidents, wounds
ZUSAMMENFASSUNG
Jährlich ereignen sich in Tirol etwa 3.000 Unfälle im alpinen Gelände. Inzidenzen zu Unfällen im alpinen Gelände gibt es nicht. Welche Verletzungsmuster z.B. aus Flugunfällen im alpinen Gelände resultieren, welche Risikofaktoren eine Rolle spielen und inwieweit die Prävention und das präklinische Management optimiert werden können, sollte in dieser Studie untersucht werden. Den von der Österreichischen Alpinpolizei anonymisierten Daten im Zeitraum von 01.01.2006 bis 31.12.2015 wurden retrospektiv personenbezogene Patientendaten der Universitätsklinik Innsbruck zugeordnet. So konnten Informationen zum Unfallhergang mit medizinischen Daten zusammengeführt und ausgewertet werden. Auf Basis von Häufigkeitsverteilungen und Vergleichsrechnungen wurden Tendenzen zu kausalen Zusammenhängen abgeleitet. 126 Personen, die sich im Rahmen eines Flugunfalls im alpinen Gelände in Österreich verletzten und anschließend in der Universitätsklinik Innsbruck behandelt wurden, wurden in diese Studie eingeschlossen. Informationen zur präklinischen und innerklinischen Versorgung und den Diagnosen wurden aus Arztbriefen klassifiziert. Aus der Datenbank der Alpinpolizei wurde eine Unfallstatistik mit 2.037 durch einen Flugunfall in Österreich verletzten Personen erstellt. Der Großteil waren Paragleiter, gefolgt von Drachenpiloten. Die meisten Personen waren nach Polizeiangaben schwer verletzt und wurden mit dem Helikopter gerettet. Am häufigsten wurde vom Notarzt der NACA-Wert 4 vergeben (schwer bis lebensbedrohlich verletzt). Besonders imponierten Frakturen im Bereich der Brust- und/oder der Lendenwirbelsäule (69 von 125*; 55,2%). Des Weiteren traten Schädelhirntraumata (24 von 125*; 19,2%), Beckenverletzungen (22 von 125*; 17,2%), Extremitäten Verletzungen (v.a. Sprunggelenksverletzungen (17 von 125*; 13,6%)) und Verletzungen des Rückenmarks (12 von 125*; 9,6%) auf. Die Region Kopf und Hals war gemäß
200
Abbreviated Injury Score (AIS) oft sehr schwer bis kritisch verletzt (AIS 4–6), Brust, Bauch und Beckengürtel zumeist schwer bis sehr schwer verletzt (AIS 3–4). Todesursachen waren Schädelhirntraumata (zweimal), Atemversagen (einmal) und hämorrhagischer Schock (einmal). *Bei einer Person konnten die Diagnosen nicht eruiert werden. Schwere Verletzungen und Polytraumata, insbesondere Verletzungen der Brust- und Lendenwirbelsäule, teils mit persistierenden neurologischen Rückenmarksverletzungen, und Sprunggelenksverletzungen waren häufig. Bestehende Protektorsysteme sollten verbessert werden. Adäquate Schienung und Analgesie sind in der Notfallversorgung zur Vermeidung weiterer Verletzungen und Schmerzen unabdingbar. Schlüsselwörter: Alpines Gelände, Blitzschlag, Flugunfälle, Hängegleiterunfälle, Herzstillstand, Paragleiterunfälle, Strom, Verletzung, Wunden
EINLEITUNG
Unfälle im alpinen Gelände
Große Flächen Österreichs sind Gebirge, entlegene Talschaften und unwegsames Gelände. Durch den zunehmenden Bergtourismus nehmen Unfälle in diesen oft schwer zugänglichen Gebieten zu und machen somit einen beträchtlichen Teil der gesamten Unfälle aus. Am Beispiel Tirols lässt sich dies in Zahlen fassen: Die Alpinpolizei verzeichnete in Tirol in einem Zeitraum von 12 Monaten (November 2009 bis Oktober 2010) 2.992 verletzte Personen und 108 Tote (1). Im Gegensatz dazu ereigneten sich nach Angaben der Statistik Austria 2010 in Tirol 3.543 Straßenverkehrsunfälle mit 4.649 Verletzten und 39 Toten (2). Vergleicht man diese Zahlen, so erkennt man, dass der Straßenverkehr zwar jährlich mehr Verletzte fordert, die Zahl der tödlich Verunglückten im alpinen Raum allerdings höher liegt. Während es zu Unfällen im Straßenverkehr eine große Anzahl an Studien und Statistiken gibt, sind im alpinen Gelände die Epidemiologie von Unfällen und die spezifischen Verletzungsmuster weitestgehend unbekannt. Ebenso sind Präventionsmaßnahmen nur unzureichend untersucht.
Flugsport als Extremsport
Bereits 2004 beschrieben Watson und Pulford, dass Extremsportarten wie Klettern, Tauchen, Fallschirmspringen, Kitesurfen oder Paragleiten größeren Zulauf bekommen (3). Doch gelten die in dieser Arbeit behandelten Flugs-
201
portarten tatsächlich noch als Extremsportarten? Schließlich hat sich in Sachen Sicherheit in den letzten Jahrzehnten einiges verbessert. So machen Helme, hohes Schuhwerk, diverse Protektoren und Rettungsschirme Sportarten wie das Paragleiten sicherer. In den 70er und 80er Jahren des 20. Jahrhunderts galt Paragleiten noch als Extremsport. Die Schirme waren noch nicht ausgereift und es gab weniger Sicherheitsvorkehrungen. Heute wehren sich Paragleiter dagegen, das „normale“ Paragleiten als Extremsport zu bezeichnen. Lediglich spezielle Varianten des Paragleitens werden noch als Extremsportart eingestuft, wie z.B. Acro-Paragleiten oder Speedflying. Beim Acro-Paragleiten z.B. fliegt der Pilot akrobatische Kunststücke und gefährliche Manöver. Beim Speedflying werden bewusst kleinere Schirme benutzt, um höhere Geschwindigkeiten zu erreichen. Gestartet wird meistens auf Skiern. Bohnsack und Schröter zeigten 2005 in einer Studie, dass „die tatsächliche Verletzungshäufigkeit und die Quote tödlicher Unfälle beim Gleitschirmfliegen nicht höher sind als bei anderen Luftsportarten oder beim Motorradfahren“ (4).
Zielsetzung
Es sind keine Daten zur Inzidenz von Flugsportunfällen und Analysen zu typischen Verletzungsmustern im alpinen Raum Österreichs vorhanden. Ziel dieser Studie war es deshalb, mittels vorhandener Daten des Österreichischen Kuratoriums für Alpine Sicherheit, die von der österreichischen Alpinpolizei gesammelt werden, und der Universitätsklinik Innsbruck, einen Einblick in Kasuistik und Verletzungsmuster zu erlangen. Ein sekundäres Ziel war es, mögliche Risikofaktoren zu bestimmen und somit eine Verbesserung in der Unfallprävention und der Notfallversorgung zu ermöglichen.
METHODIK
Studiendesign
Es handelt sich bei dieser Arbeit um eine retrospektive Studie. Primär wurden die Daten der alpinpolizeilichen Erhebungen bei Flugunfällen im alpinen Gelände mit Patientendaten der Universitätsklinik Innsbruck abgeglichen. Polizeiangaben zum Unfallhergang und klinische Angaben zu den Diagnosen und zum Outcome ermöglichen einen annähernd vollständigen Überblick über Flugunfälle. In dieser Studie wurden nur Patientenfälle analysiert, deren klinische Daten im Klinischen Informationssystem (KIS) der Universitätsklinik Innsbruck identifiziert werden konnten. Diese Daten wurden mit der Daten-
202
bank des Österreichischen Kuratoriums für Alpine Sicherheit zusammengeführt. Die Patientenfälle der Universitätsklinik Innsbruck werden nachfolgend „Innsbrucker Patienten“ genannt. Es konnten 126 Innsbrucker Patienten ausgewertet werden. Zusätzlich wurden in einer Unfallstatistik alle Flugunfälle, die in der Datenbank der Alpinpolizei in den letzten 10 Jahren erfasst wurden, ausgewertet. Die Daten des Österreichischen Kuratoriums für Alpine Sicherheit umfassen im Zeitraum vom 01.01.2006 bis 31.12.2015 Informationen zu 2.037 Personen.
ERGEBNISSE UND DISKUSSION





Auswertung zum Unfallhergang
Bei den Innsbrucker Patienten sind Männer überproportional vertreten. Unter den 126 Personen sind lediglich 20 (15,9%) weiblich. Bei den gesamten Flugunfällen zeigt sich dieser Unterschied noch deutlicher: Nur 13,2% der 2.037 Personen sind weiblich. Abbildung 1 zeigt die Altersverteilung, vergleichend werden die Innsbrucker Patienten mit allen Flugunfällen dargestellt.
Abb. 1: Altersverteilung der Personen, die einen Flugunfall im alpinen Gelände in Österreich erlitten haben (Angaben in Prozent)




203
In dieser Auswertung konnte nicht erfasst werden, welchen Flugausbildungs- und Flugerfahrungsstand die Personen zum Zeitpunkt des Flugunfalls hatten, aus der Literatur geht jedoch hervor, dass vor allem unerfahrene Piloten und sehr erfahrene Piloten, die möglicherweise besonders riskante Manöver fliegen, gefährdet sind. Sowohl bei den gesamten Flugunfällen, als auch bei den Innsbrucker Patienten war Wind die häufigste Unfallursache. Materialversagen war nur äußerst selten die Unfallursache und bestätigt die Qualität der Materialprüfung durch Hersteller und Verbände. Die große Mehrheit der Studien beschreibt Pilotenfehler als häufigste Unfallursache (4-11). Wichtig erscheint es in einem vom Tourismus geprägten Land wie Österreich zu erfassen, welchen Anteil Touristen unter den Flugunfallopfern ausmachen. Vor allem die Flugsportarten Drachen und Paragleiten erfordern geeignete Startflächen auf Anhöhen oder einen Windenschlepp. Daher werden diese Sportarten besonders in den Bergen praktiziert und Piloten aus dem Flachland kommen gerne zum Fliegen in die Berge Tirols. Unter den Innsbrucker Patienten sind 46,8% Österreicher und 42,1% Deutsche. Weitere Personen sind Niederländer, Italiener, Schweizer, Tschechen. Auch ein Chilene und ein Däne befinden sich unter den Verletzten. Unter allen von der Alpinpolizei erfassten Flugunfällen sind die Nationalitäten noch breiter gestreut; die erfassten Personen kommen aus 31 verschiedenen Ländern. Abbildung 2 zeigt in welchen Bundesländern sich die gesamten Flugunfälle ereigneten.







Abb. 2: Bundesländer, in denen sich die Flugunfälle ereigneten



204
Bei den Innsbrucker Patienten verletzten sich geografisch bedingt nahezu alle Personen in Tirol und einige im Bundesland Salzburg. Es konnte in dieser Gruppe gezeigt werden, dass sich die meisten Unfälle in Gegenden ereigneten, in denen es viele Flugplätze und Flugschulen gibt. Als „Hot-Spots“ für Unfälle in Tirol können deshalb die Regionen Innsbruck/Schwaz und Kufstein/Kitzbühel angesehen werden. Das Paragleiten stellt bei den Innsbrucker Patienten mit 105 Personen (83,3%) mit Abstand die größte Gruppe dar. Acht Personen (6,3%) verunglückten mit einem Drachen, drei Personen (2,4%) mit einem Helikopter und jeweils eine Person (0,8%) mit einem Segelflugzeug beziehungsweise einem Motorflugzeug. In den übrigen Fällen wurde die Art des Fluggeräts nicht vermerkt. Unter allen von der Alpinpolizei erfassten Flugunfällen zeigt sich mit 84% Paragleitern und 6,8% Drachenfliegern eine ähnliche Verteilung. Wie in Abbildung 3 dargestellt wird, erfolgte die Rettung der Innsbrucker Patienten verglichen mit allen Flugunfällen deutlich häufiger mit dem Helikopter (69% vs. 42,4%). Verglichen mit den Innsbrucker Patienten wurden unter den gesamten Flugunfällen die Personen häufiger terrestrisch gerettet (28,9% vs. 13,5%) oder aber es war keine Rettung notwendig (14,4% vs. 4%). Dass unter den gesamten Flugunfällen im Vergleich zu den Innsbrucker Patienten mehrfach keine Rettung notwendig war, lässt sich dadurch erklären, dass die Alpinpolizei auch Personen erfasst, welche unverletzt sind und daher keine ärztliche Behandlung benötigen. Vergleicht man die luftgebundenen Rettungen, so fällt


Abb. 3: Rettung der Personen, die einen Flugunfall im alpinen Gelände Österreichs erlitten haben (Angaben in Prozent)



205
auf, dass bei den Innsbrucker Patienten deutlich mehr Personen mit dem Helikopter gerettet wurden. Das könnte einerseits verletzungsbedingt sein, aber auch eine Folge der hohen Notarzthelikopterdichte in Tirol, die bereits 2012 vom Rechnungshof wegen mangelnder Wirtschaftlichkeit kritisiert wurde (12). Die Universitätsklinik Innsbruck ist ein Krankenhaus der Maximalversorgung, komplexe Verletzungen und Erkrankungen können dort erfolgreich behandelt werden. Kann ein Patient am Unfallort nicht ausreichend stabilisiert werden oder wird die Verletzungsschwere vor Ort unterschätzt, erfolgt eine Erstversorgung in einem peripheren Krankenhaus und anschließend ein Sekundärtransport an die Universitätsklinik.
Medizinische Auswertung
Die folgende Auswertung bezieht sich ausschließlich auf die Innsbrucker Patienten. Anhand des NACA-Scores (National Advisory Committee for Aeronautics) bewertet der Notarzt vor Ort die Schwere der Verletzungen (NACA 0 = keine Verletzung bis NACA 7 = tödliche Verletzung). Bei den Innsbrucker Patienten wurden ausschließlich NACA-Werte größer als 3 vergeben, was Verletzungen entspricht, die notärztlicher Versorgung bedürfen und in einer Klinik behandelt werden müssen. In vielen Fällen wurden die Verletzungen als schwerwiegend bis lebensbedrohlich eingestuft. Das heißt, dass sich Personen bei Flugunfällen meist schwere bis schwerste Verletzungen zuziehen. Dieses Ergebnis wird in aktuellen Studien bestätigt. Die meisten Personen wurden im Schockraum erstversorgt und stabilisiert, was ebenso für schwerwiegende Verletzungen spricht. Standardmäßig wird im Innsbrucker Schockraum ein „Schockraum-CT“ durchgeführt, welches den gesamten Körperstamm, den Hals und den Kopf abbildet und somit hilft, sämtliche potentiell lebensbedrohliche Verletzungen rasch zu erkennen (13). Röntgenuntersuchungen wurden vor allem bei Personen, die nicht im Schockraum behandelt wurden, durchgeführt. Diese Personen waren erwartungsgemäß weniger schwer verletzt. Im Folgenden werden Verletzungsmuster abgebildet, die bei Flugunfällen besonderes häufig auftreten. Abbildung 4 stellt Körperregionen dar, welche häufig verletzt wurden. Hier sind nur absolute Zahlenwerte angegeben, die sich auf 125 Personen beziehen, da bei einer Person die endgültigen Diagnosen nicht erhoben werden konnten. Die hellblauen Balken der Frakturen im Bereich der Wirbelsäule (d.h. Halswirbel-, Brustwirbel-, Lendenwirbelsäule) und bei den Beckenverletzungen entsprechen dem Anteil der Wirbelsäulenverletzungen, die mit einem neuro-
206
logischen Defizit (z.B. Lähmung oder Gefühlausfall) einhergegangen sind. Am Beispiel der Lendenwirbelkörperfrakturen bedeutet das, dass sich 50 Personen der 125 Personen mit bekannter Diagnose mindestens einen Lendenwirbelkörper gebrochen haben, wobei bei acht Personen diese Lendenwirbelkörperfraktur mit einem neurologischen Defizit einherging. Unter dem Begriff Becken werden hier alle Frakturen des Beckenrings, des Kreuzbeins und der Oberschenkelknochen zusammengefasst. Der hellblaue Bereich des Balkens für das Bein entspricht dem Anteil der Sprunggelenksverletzungen bezogen auf sämtliche Verletzungen des Beins.






Abb. 4: Verletzte Körperregion (HWS = Halswirbelsäule, BWS = Brustwirbelsäule, LWS = Lendenwirbelsäule, n* = Anteil der Verletzungen mit neurologischen Ausfällen, bzw. Anteil der Sprunggelenksverletzungen bei den Beinverletzungen)




Abbildung 5 stellt auf der linken Seite die verletzte AIS (Abbreviated Injury Scale) Körperregion und auf der rechten Seite die Körperregion nach eigener Einteilung dar. Die Häufigkeiten wurden für beide Einteilungen getrennt berechnet. Es kann mehr als eine Körperregion verletzt worden sein, somit ergeben die Prozentangaben in beiden Einteilungen mehr als 100%. Die Darstellung zeigt nicht den Verletzungsgrad an. Es haben sich demnach knapp ein
207
Abb. 5: Links: Anteil der Personen, die mindestens eine Verletzung in der genannten AIS Region aufwiesen; Rechts: Verletzte Körperregion (BWS = Brustwirbelsäule, HWS = Halswirbelsäule, LWS = Lendenwirbelsäule, RM = Rückenmarksverletzung) (14)







Viertel eine Fraktur in der Brustwirbelsäule und noch mehr eine Fraktur in der Lendenwirbelsäule zugezogen. 55,2% aller Personen zogen sich eine Fraktur in der Brustwirbelsäule und/oder in der Lendenwirbelsäule zu. 17 der 39 Verletzungen der unteren Extremität waren Sprunggelenksverletzungen. Die Abbreviated Injury Scale (AIS) dient der Einteilung und der Bewertung der Schwere einer erlittenen Verletzung in einer Körperregion. Der AIS wird für jeweils sechs Körperregionen einzeln errechnet. Es wird jeweils die schwerste Verletzung der Körperregion von 1 (unverletzt) bis 6 (maximal/tödlich) eingeteilt. Diese Bewertung wurde nachträglich anhand der Entlassungsdiagnosen durchgeführt.



208
In Abbildung 6 wird die Bewertung der Körperregionen Kopf und Hals, Gesicht, Brust, Bauch und Beckenorgane, Extremitäten und Beckenring und äußere Verletzungen gezeigt. So lassen sich Rückschlüsse auf die meistbelasteten Körperregionen ziehen.




Abb. 6: Abbreviated Injury Scale (AIS) der verschiedenen Körperregionen (Angaben in absoluten Zahlen)




Die Region Kopf und Hals fällt dadurch auf, dass besonders schwere Verletzungen (AIS = 4 bis 6) vorkommen, allerdings mittelschwere Verletzungen (AIS = 2 bis 3) relativ selten sind. Schwerstverletzte Personen wiesen bei Kopf und Hals oft schwerste Verletzungen auf. Brust- und Bauchverletzungen scheinen beide sehr häufig zu sein, fast die Hälfte der Personen hat hier mindestens eine Verletzung. Gehäuft wurden die Verletzungen hier mit 2 oder 3 gestuft, wobei die Bauch- und Beckenorganverletzungen an der Verletzungsschwere ein wenig überwiegen. In diese Kategorien fallen die Brustwirbelsäulen- und Lendenwirbelsäulenverletzungen, jedoch wurden auch innere Organe teils schwer verletzt. Bei den Becken- und Extremitätenverletzungen dominieren

209
AIS-Werte von 1 und 2, was unkomplizierten Frakturen der Extremitäten entspricht. Die hohen AIS-Werte dieser Körperregion spiegeln Verletzungen des Beckenrings wieder. Gesichtsverletzungen und äußere Verletzungen scheinen keine große Rolle zu spielen. Allerdings ist hier anzumerken, dass gerade Hautverletzungen, wie Abschürfungen, Quetschungen und Blutergüsse, oft nicht erfasst werden oder in Entlassungsdiagnosen eine untergeordnete Rolle spielen, aber in dieser Studie deshalb möglicherweise unterrepräsentiert sind. Da bei einer Bewertung durch die AIS leichtere Verletzungen unberücksichtigt bleiben, wenn in derselben Region eine schwere Verletzung vorliegt, wurden in dieser Studie Verletzungen der Extremitäten zusätzlich zu der Kategorie Arm, Bein, Beckenring Verletzungen als eigene Kategorie gewertet. Da Verletzungen der Extremitäten selten als lebensbedrohlich bewertet werden, wurden hier nur AIS-Werte von 1 bis 3 vergeben, allerdings zogen sich 45,2% aller Personen Brüche an Armen und Beinen zu. Extremitätenverletzungen waren vor allem bei den Flugsportlern zu sehen, die ohne eine schützende Kabine fliegen. Paragleiter und Drachenflieger brachen sich in vielen Fällen die Arme, noch öfter die Beine. Besonders Frakturen in der Sprunggelenksregion waren deutlich gehäuft. Paragleiter fliegen in der Regel sitzend. Im Falle eines Absturzes prallt der Pilot mit dem Gesäß voran am Boden auf. Bei einem solchen Unfallmechanismus können Frakturen des Beckenrings entstehen, die Wirbelsäule wird besonders im Bereich der Lendenwirbelsäule und Brustwirbelsäule gestaucht. Ein solcher Unfallmechanismus spiegelt sich in unseren Untersuchungen wieder; LWS-Verletzungen waren mit 44,2% und Beckenverletzungen mit 18,3% besonders häufig. Bereits Schulze et al. konnten in ihrer Studie zeigen, dass 59% der Paragleiter auf dem Gesäß oder Rücken landeten, 22% auf der Seite und 19% mit ausgestreckten Beinen, was diese Verteilung erklären könnte (6). Karl Slezak vom Referat für Sicherheit und Technik des deutschen Hängegleiter Verbandes interviewte 72 Personen, die sich im Rahmen eines Flugunfalls eine Rückenverletzung zugezogen hatten. Es wurde festgestellt, dass in mehr als 40% der Fälle die Person wie oben erklärt zuerst mit dem Gesäß bzw. sitzend aufgeprallt ist. Etwas mehr als die andere Hälfte prallte anders auf. Es wird sogar von weiteren Überschlägen nach dem Aufprall berichtet (15). Per Erlass des Bundesministeriums für Verkehr, der obersten Zivilluftfahrtbehörde, müssen Paragleiter und Drachenpiloten einen Helm tragen und bei Höhenflügen ein Rettungssystem mitführen (16). Außerdem ist vorgeschrieben, dass im Gurtzeug ein Rückenschutz in Form eines Protektors oder Airbags eingearbeitet sein muss (16). Da in dieser Studie nicht dezidiert erfasst wurde, ob und welche Protektorsysteme verwen-
210
det wurden, wird davon ausgegangen, dass alle in Österreich zugelassenen Fluggeräte und der Großteil der nicht-österreichischen Fluggeräte den gesetzlichen Vorgaben entsprochen haben und daher über ein Rückenprotektorsystem verfügten. Dennoch zeigt diese Studie, dass es bei Paragleitern vor allem zu Verletzungen der Wirbelsäule im Bereich des thorakolumbalen Übergangs kommt und Sprunggelenksverletzungen sehr häufig sind. Entgegen anderen Studien gibt es in unserer Stichprobe aber auch eine nennenswerte Anzahl an Kopfverletzungen. Drachenpiloten fliegen liegend, der Unfallmechanismus unterscheidet sich also grundlegend. Bei den Drachenpiloten wurden in 37,5% der Fälle (8 Personen der Innsbrucker Patienten) Schädelhirntraumata (Kopfverletzungen) diagnostiziert, außerdem sind bei vier der acht Personen Frakturen der Brustwirbelsäule festgestellt worden, zwei davon mit Nervenschäden. Man würde vermehrt Halswirbelsäulenverletzungen erwarten, was diese Studie aber nicht bestätigte. Gut die Hälfte der Personen wurde chirurgisch versorgt, meist zur Reposition und Fixierung von Frakturen. Viele Personen wurden entweder mit Schienung, Gips, externem Fixateur oder Extension immobilisiert bzw. operiert und immobilisiert. Dies spiegelt die hohe Zahl an Frakturen im Rahmen des Unfalls wieder. Zumeist war ein stationärer Aufenthalt erforderlich, Intensivaufenthalte waren bei jedem fünften Flugunfallopfer erforderlich. An der Zahl der Intensivaufenthalte kann auch die hohe Anzahl von Schwerstverletzten erkannt werden. Jene Personen, die keiner Behandlung bedurften, waren gehäuft solche, die durch die Alpinpolizei als unverletzt eingestuft wurden, keiner Rettung bedurften oder nur zur Abklärung von geringen Verletzungen selbstständig in die Innsbrucker Notaufnahme kamen. Dass bei Krankenhausentlassung mehr als die Hälfte der Personen noch Schmerzen hatte und Analgetika einnahm ist wohl der Tatsache geschuldet, dass die Verletzungen noch nicht vollständig abgeheilt waren. Beachtlich ist, dass 15,5% am Entlassungstag an einer Lähmung litten. Die Lähmungen umfassten einzelne Nerven, Nervenbündel bis hin zu einer kompletten Querschnittlähmung. Aufgrund der geringen Datenmenge zur Nervenfunktion nach sechs Monaten konnte keine valide Auswertung über bleibende Langzeitschäden durchgeführt werden. Dennoch soll erwähnt sein, dass bei mindestens fünf Personen noch nach Monaten Schmerzen bestanden haben und mindestens vier Personen gelähmt waren. Vier Personen überlebten den Flugunfall trotz Maximalversorgung nicht, alle vier Personen wurden in Innsbruck obduziert. Zwei Personen verstarben an schweren Schädelhirntraumata, eine Person an Atemversagen und eine Per-
211
son an hämorrhagischem Schock. Die tödlichen Verletzungen traten alle im Rahmen eines Polytraumas auf. Bei drei der vier Toten wurden die tödlichen Verletzungen bereits im Schockraum festgestellt. Eine Person verstarb nach der Notoperation. Unter den Innsbrucker Patienten sind im Vergleich zu allen Flugunfällen weniger tödlich verletzte Personen (3,2% vs. 5,3%). Das lässt sich damit erklären, dass in diese Studie nur jene Personen aufgenommen und ausgewertet wurden, welche an der Universitätsklinik Innsbruck behandelt wurden. Es ist durchaus denkbar, dass bei einigen Flugunfallopfern aufgrund gravierender Verletzungen bereits am Unfallort der Tod festgestellt wurde.
LIMITATIONEN
Aus der großen Datenbank des Österreichischen Kuratoriums für Alpine Sicherheit (2.037 Personen) im Zeitraum von 01.01.2006 bis 31.12.2015 konnten nur 126 Personen hinsichtlich einer klinischen Behandlung an der Universitätsklinik Innsbruck untersucht werden. Die anderen Patienten wurden in anderen Krankenhäusern Tirols und außerhalb Tirols behandelt, die Daten dieser anderen Patienten waren für diese Studie nicht zugänglich. Im Vergleich der Innsbrucker Patienten zu allen von der Alpinpolizei erfassten Flugunfällen zeigt sich, dass diese Stichprobe als repräsentativ für die Gesamtheit der Flugunfälle im alpinen Gelände angesehen werden darf, da sich die Personenmerkmale beider Gruppen nicht wesentlich unterscheiden. Diese Studie ist retrospektiv. Es konnten nicht alle Variablen bei jeder Person erhoben werden, weil im Krankenhaus Information System (KIS) nicht alle Angaben vorlagen. Welche Flugsportart die höchste Gefahr in sich birgt, konnte in dieser Studie nicht geklärt werden, da kein Vergleich mit Flugstunden in den einzelnen Flugsportarten möglich war. Möglicherweise werden in dieser Studie schwere Unfälle betont dargestellt, da vor allem Schwerverletzte an der Universitätsklinik Innsbruck und leichter Verletzte in peripheren Krankenhäusern behandelt werden.
DANKSAGUNG
Wir danken der österreichischen Alpinpolizei für die Sammlung der präklinischen Daten und dem Österreichischen Kuratorium für Alpine Sicherheit für die Bereitstellung der Daten.
212
LITERATUR
(1) Bilek H., Ebner H., Lehner G. Analyse: Berg Sommer 2011. 1. Ausgabe. Ort: Innsbruck. Hrsg: Österreichisches Konservatorium für alpine Sicherheit. S. 11. (2) Statistik Austria. Statistik der Straßenverkehrsunfälle [Internet]. 2015 [zitiert am 15.03.2016].Verfügbar unter: http://www.statistik.at/wcm/idc/idcplg?IdcService=-
GET_PDF_FILE&RevisionSelectionMethod=LatestReleased&dDocName=069550. (3) Watson A.E., Pulford B.D. Personality differences in high risk sports amateurs and instructors. Percept Mot Skills 2004; 99(1): 83–94. (4) Bohnsack M., Schroter E. Injury patterns and typical stress situations in paragliding.
Orthopade 2005; 34(5): 411–418. (5) Schulze W., Richter J., Schulze B., Esenwein S.A., Buttner-Janz K. Injury prophylaxis in paragliding. Br J Sports Med 2002; 36(5): 365–369. (6) Schulze W., Hesse B., Blatter G., Schmidtler B., Muhr G. Verletzungsmuster und -prophylaxe beim Gleitschirmfliegen. Sportverl Sportschad 2000(14): 41–49. (7) Krissoff W.B. Follow-up on hang gliding injuries in Colorado. Am J Sports Med 1976; 4(5): 222–229. (8) Fasching G., Schippinger G., Pretscher R. Paragliding accidents in remote areas. Wilderness Environ Med 1997; 8(3): 129–133. (9) Lautenschlager S., Karli U., Matter P. Paragliding accidents-a prospective analysis in
Swiss mountain regions. Z Unfallchir Versicherungsmed 1993; Suppl 1: 55–65. (10) Tongue J R. Hang gliding injuries in California. Journal Trauma 1977; 17(12): 898–902. (11) Slezak K. Unfallstatistik 2002 Gleitschirm [Internet]. Ohne Datum [zitiert am 15.03.2016]. Verfügbar unter: http://www.dhv.de/web/fileadmin/user_upload/monatsordner/2004-06/Ausbildung/Unfallstatistik_2002_Gleitschirm.pdf (12) Österreichischer Rechnungshof. Bericht des Rechnungshofes [Internet]. 2012 [zitiert am 16.03.2016]. S. 8-129. Verfügbar unter: https://www.google.at/url?sa=t&rct=j&q=&esrc=s&source=web&cd=2&ved=0ahUKEwiNh87y68XLAh-
VGWRQKHeqRBFMQFggpMAE&url=http %3A %2F %2Fwww.rechnungshof. gv.at%2Ffileadmin%2Fdownloads%2F_jahre%2F2012%2Fberichte%2Fteilberichte%2Fbund%2FBund_2012_02%2FBund_2012_02_1.pdf&usg=AFQjCNGhHhyXkjzvhlCcqL9S1SjVL1jiJA&cad=rja. (13) Rieger M., Czermak B., El Attal R., Sumann G., Jaschke W., Freund M. Initial clinical experience with a 64-MDCT whole-body scanner in an emergency department: better time management and diagnostic quality? J Trauma 2009; 66(3): 648–657.
213
(14) Akademie Cellsymbiosistherapie. Anamnese-Fragebogen [Internet]. Ohne Datum [zitiert am 23.03.2016]. Verfügbar unter: https://www.google.at/url?sa=i&rct=j&q=&esrc=s&source=images&cd=&cad=rja&uact=8&ved=0ahUKEwjD18-c0tbLAhV-
BohQKHe-RASYQ5TUICQ&url=http%3A%2F%2Fduesseldorf-naturheilpraxis. de%2Fapp%2Fdownload%2F5781424735%2FAnamnesebogen_DE_01-2014_interaktiv.pdf&bvm=bv.117218890,d.bGs&psig=AFQjCNFhydTSQtQv8U9XG5jHWvZgI_uy1Q&ust=1458816774607774. (15) Slezak K. Auswertung Pilotenumfrage zum Rückenschutz [Internet]. 2011 [zitiert am 16.03.2016]. Verfügbar unter: http://www.dhv.de/web/fileadmin/user_upload/files/2011/sicherheit/Bericht_Auswertung_Fragebogen_Rueckenschutz.pdf. (16) Österreichisches Bundesministerium für Verkehr/Oberste Zivilfahrtbehörde. Erlaß des Bundesministeriums für Verkehr/Oberste Zivilfahrtbehörde über «Hängegleiter» und «Paragleiter» [Internet]. 1997 [zitiert am 16.03.2016]. Verfügbar unter: http:// www.flugschulen.at/down/erlass.html.
214
DANK DEN FÖRDERNDEN MITGLIEDERN
CHEMOMEDICA
ÖSTERREICHISCHER ALPENVEREIN


