
CHUYÊN ĐỀ ÔN THI LỚP 12 MÔN HÓA HỌC Ths Nguyễn Thanh Tú eBook Collection CHUYÊN ĐỀ ĐẦY ĐỦ ÔN THI LỚP 12 MÔN HÓA HỌC - 8 CHƯƠNG - LÍ THUYẾT TRỌNG TÂM - CÁC DẠNG BÀI TẬP - BÀI TẬP TỰ LUYỆN CƠ BẢN NÂNG CAO WORD VERSION | 2022 EDITION ORDER NOW / CHUYỂN GIAO QUA EMAIL TAILIEUCHUANTHAMKHAO@GMAIL COM Hỗ trợ trực tuyến Fb www.facebook.com/DayKemQuyNhon Mobi/Zalo 0905779594 Tài liệu chuẩn tham khảo Phát triển kênh bởi Ths Nguyễn Thanh Tú Đơn vị tài trợ / phát hành / chia sẻ học thuật : Nguyen Thanh Tu Group vectorstock com/28062440
CHƯƠNG 1: ESTE - LIPIT
BÀI 1: ESTE
Mục tiêu
Kiến thức
+Nêu được khái niệm, cách đọc tên,tính chất vật lí, phương pháp điều chế và ứng dụng của este.
Kĩ năng
+ Viết được công thức cấu tạo các đồng phâneste.
+ Viết được phương trìnhhóa học của phản ứng thủy phânestetrongcácmôi trường.
+ Giải được bài tập về các phản ứng đốt cháy, điều chế và thủy phâneste.
I. LÍ THUYẾT TRỌNG TÂM
1.
Khái niệm
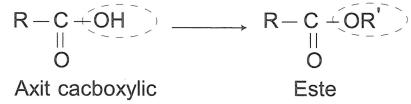
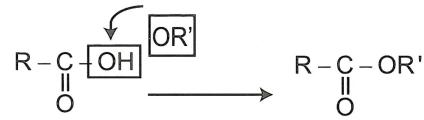
Khithay thế nhómOHtrongaxitcacboxylic bằng nhómORtathu được este.
Ví dụ:Este: .325 CHCOOCH
Trong đó: R,R’có thể thuộc loại: no(không chứa liên kết pi);khôngno (chứa liên kết linh động) hoặc thơm (chứa vòngbenzen).
Nếu RvàR’ đều no:esteno.
Nếu R hoặc R’khôngno:estekhông no. Nếu R hoặc R’ thơm: este thơm.
Ví dụ: 3HCOOCH 325 CHCOOCH Esteno 2 3CHCHCOOCH 25 2CHCOOCHCH 2 2CHCHCOOCHCH


Estekhôngno
Este thơm
NhómCOO được xemlànhóm chức của este. Chú ý:
Este đơn chức: có1nhómCOO. Công thức tổng quát của esteno, đơn chức, mạch hở: m2m1p2p1 CHCOOCHm0;p1 Hay n2n2 CHOnmp12 Este đa chức: có2nhómCOO trở lên.
DẠYKÈMQUYNHƠN
Trang1
OFFICIAL
2. Danh pháp
Tên este RCOOR’ = Tên gốc R’ + Tên gốc axit RCOO
Tên một số gốc hiđrocacbon thường gặp: Phân loại Gốc hiđrocacbon Tên gọi 3CH metyl 25CH etyl 322 CHCHCH propyl 37CH 32 CHCH isopropyl 3222 CHCHCHCH butyl
No 3222 CHCHCHCH isoamyl 2 CHCH vinyl Không no 2 2CHCHCH anlyl phenyl Thơm benzyl


Chú ý: Một số este thường gặp: Công thức cấu tạo Tên gọi 3HCOOCH metylfomat 25HCOOCH etylfomat 223 HCOOCHCHCH propylfomat 32HCOOCHCH isopropyl fomat 33 CHCOOCH metylaxetat
OFFICIAL
DẠYKÈMQUYNHƠN
Trang2
Tên một số gốc axit tương ứng thường gặp: Gốc axit
Công thức Tên gọi HCOO
3 CHCOO
25 CHCOO
322 CHCHCHCOO
2 CHCHCOO
232 CHCCHCOO
3. Tính chất vật lí
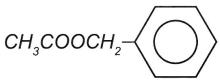
325 CHCOOCH etylaxetat 32232CHCOOCHCHCHCH isoamylaxetat 3 2CHCOOCHCH vinylaxetat 2 3CHCHCOOCH
metylacrylat 23 3CHCCHCOOCH metyl metacrylat benzylaxetat
Phân loại
fomat
axetat
propionat No
butirat
acrylat Khôngno
metacrylat Thơm benzoat
Đặc điểm: phản ứng thuận nghịch. Ví dụ: t 3 252 3 25 H CHCOOCHHOCHCOOHCHOH
b. Phản ứng thủy phân este trong môi trường bazơ (phản ứng xà phòng hóa)
RCOOR'NaOHRCOONaR'OH
Ví dụ: Este Mùi 3HCOOCH Táochín 25HCOOCH Đào chín 325 CHCOOCH Bơ 32232CHCOOCHCHCHCH Chuối chín 2525 CHCOOCH 3725 CHCOOCH Dứa Hoanhài 4. Tính chất hóa học a. Phản ứng thủy phân este trong môi trường axit CHCHCOOCHHCHCHCOOCH CHCHCOOCHBrCHBrCHBrCOOCH
t 2 32 32 3 Ni 2
t 2H RCOOR'HORCOOHR'OH e. Phản ứng cháy Cáceste dễ cháyvà phản ứng tỏa nhiệt. Ví dụ: t 3 252 22 CHCOOCH5O4CO4HO 5. Điều chế Este của ancol được điều chế bằng phản ứng estehóa giữa axitcacboxylicvàancol: 24 HSO,Æ c 2 t RCOOHR'OH RCOOR'HO đ Ví dụ: 24 HSO,Æ c 3 25 3 252 t CHCOOHCHOH CHCOOCHHO đ
DẠYKÈMQUYNHƠN
Trang3
OFFICIAL
Trạng thái ở điều kiện thường: chất lỏng hoặc rắn. Nhiệt độ nóng chảy và nhiệt độ sôi: Thấp hơn so với ancolvàaxitcacboxyliccó số nguyên tử cacbonvà số nhóm chức tương đương. Tính tan: không tan trong nước, tan nhiều trong các dungmôi hữu cơ. Mùi thơm: Nhiều estecómùi thơm của hoa quả chín. 32 2 3
t
Đặc điểm: phản ứng một chiều. Ví dụ: t 3 25 3 25 CHCOOCHNaOHCHCOONaCHOH
c. Phản ứng cộng và phản ứng trùng hợp của este không no Cácestekhôngnocó thể thamgia phản ứng cộng (xúctác, ), cộng (dung dịch) t, cộng HX(X 2 Ht 2Br là gốc axit)và phản ứng trùng hợp. Ví dụ:
6. Ứng dụng
Một số estedùnglàmdungmôi để tách, chiết chất hữu cơ (etylaxetat),pha sơn (butylaxetat),…
Một số este được dùng điều chế polime để sản xuất chất dẻo như poli (vinyl axetat), poli (metyl metacrylat),…
Một số este có mùi thơm, không độc, được dùng làm chất tạo hương trong công nghiệp thực phẩm (benzylfomat,etylfomat,…), mỹ phẩm (linalylaxetat,geranylaxetat,…),…
SƠ ĐỒ HỆ THỐNG HÓA ESTE
1. Khái niệm:
Khi thay thế nhóm OH của axit cacboxylic bằng nhóm OR’ ta được este. Công thức tổng quát: Este no, đơn chức, mạch hở: .n2n2 CHOn2
2. Danh pháp:
Tên gốc R’+Tên gốc axitRCOO (đuôi at). Ví dụ: :etylaxeatat; :metylfomat. 3 25CHCOOCH 3HCOOCH
3. Tính chất vật lí:
OFFICIAL
Cácestelà chất lỏng khôngmàu (một số estecó khối lượng phân tử lớn ở trạng thái rắn như sápong, mỡ động vật,…), dễ bay hơi, íttantrong nước. Cáceste thường cómùi thơm đặc trưng của hoa,tráicâychín.
Nhiệt độ sôi thấp hơn axit tương ứng dokhôngcóliên kết H giữa cácphân tử.
4. Tính chất hóa học: Phản ứng thủy phân: Môi trường axit: H,t RCOOR'HOHRCOOHR'OH
Đặc điểm: Phản ứng thuận nghịch (hai chiều).
Môi trường kiềm: 2 HO,t RCOOR'NaOHRCOONaR'OH Đặc điểm: Phản ứng một chiều. Phản ứng còn được gọi là phản ứng xàphònghóa. 5. Điều chế: Phương phápchung: phản ứng estehóa: 24 HSO,Æ
DẠYKÈMQUYNHƠN
Trang4
c 2 t RCOOHR'OH RCOOR'HO đ 6. Ứng dụng: Estecó khả năng hòatan tốt nhiều chất nên
dùnglàmdungmôi
số polime của este
Một số este
được
để tách, chiết chất hữu cơ,… Một
được dùng để sản xuất chất dẻo.
có mùi thơm của hoa quả, không độc dược dùng trong công nghiệp thực phẩm (bánh kẹo, nước giải khát)và mĩ phẩm (xàphòng, nước hoa,…).
II. CÁC DẠNG BÀI TẬP
Dạng 1: Lí thuyết trọng tâm
Kiểu hỏi 1: Khái niệm – Cấu tạo – Danh pháp Ví dụ mẫu
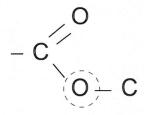
Ví dụ 1: Hợp chất nàosau đây thuộc loại este?
A. B. 3 25CHOOCCOOCH 3HCOOCH C. D. 25 CHCOOH 33CHOCH
Hướng dẫn giải
KhithaynhómOH của axitcacboxylic bằng nhómORta được este. Hợp chất thuộc loại este 3 25CHOOCCOOCH
Chọn A.
Chú ý: Nguyên tử oxi(khôngcóliên kết đôi xungquanh)trongnhóm chức este phải liên kết với nguyên tử cacbon: Ví dụ 2: Công thức chung của esteno, đơn chức, mạch hở là:
OFFICIAL
A. B. C. D. n2n2 CHOn2 n2n42 CHOn4 n2n22 CHOn2 n2n42 CHOn4
Hướng dẫn giải
Công thức chung của esteno, đơn chức, mạch hở là: n2n2 CHOn2 Chọn A.
dụ
thức cấu
Hướng dẫn giải Xlàeste đơn chức vàlàeste của axitaxeticnênXcó dạng 3 CHCOOR'
MàXcócông thức phân tử là nênR’là . 362CHO 3CH
DẠYKÈMQUYNHƠN
Trang5
Ví
3: Công
tạo của vinylpropionatlà: A. B. 2 37CHCHCOOCH 25 2CHCOOCHCH C. D. 2 25CHCHCOOCH
37 2CHCOOCHCH Hướng dẫn giải Công thức của gốc vinyllà 2CHCH Công thức của gốc axitpropionatlà 25 CHCOO Công thức cấu tạo của estelà . 25 2CHCOOCHCH
Chọn B. Ví dụ 4: Chất Xcócông thức phân tử làeste của axitaxetic.Công thức cấu tạo của Xlà: 362CHO A. B. C. D. 25 CHCOOH 24 HOCHCHO 3 3CHCOOCH 25HCOOCH
Vậy công thức cấu tạo của Xlà . 3 3CHCOOCH
Chọn C.
Kiểu hỏi 2: Đồng phân
Ví dụ mẫu
Ví dụ 1: Số đồng phân thuộc loại este ứng với công thức phân tử là: 482CHO A. 2. B. 3. C. 4. D. 5.
Hướng dẫn giải
Các đồng phâneste ứng với công thức phân tử là: 482CHO
HCOOCHCHCH HCOOCHCH CHCOOCH CHCOOCH
Có4 đồng phân. Chọn C.
Ví dụ 2: Choeste mạch hở tác dụng với dung dịch NaOH,thu được sản phẩm có phản ứng 462XCHO

tráng bạc. Số công thức cấu tạo phù hợp của Xlà: A. 2. B. 3. C. 4. D. 5. Hướng dẫn giải
TH1:Este của axitfomic. t HCOORNaOHHCOONaROH
Muối HCOONacónhóm chức nêncó phản ứng tráng bạc. CHO TH2:Este bị thủy phânsinhra anđehit.
DẠYKÈMQUYNHƠN
Trang6
OFFICIAL
223
25
32 3
25 3
t 12
RCOOCHCRRNaOHRCOONaRRCHCHO ( và là gốc hiđrocacbon hoặc hiđro). 1R2R Như vậy, có4công thức cấu tạo
là: 2 2 2 3 2 3 2 HCOOCHCHCH HCOOCHCHCH HCOOCCHCH CHCOOCHCH Chọn C. ® Chú ý: Ban đầu: t 12 21 RCOOCHCRRNaOHRCOONaRRCCHOH Chất kém bền (do nhóm OH liên kết với nguyên tử cacbon có liên kết 21 RRCCHOH
21
phù hợp
với nguyên tử cacbonkhác)và bị chuyển vị thành anđehit: 21 21 RRCCHOHRRCHCHO
Ví dụ 3: Số este ứng với công thức phân tử khi bị thủy phânthu được anđehit là: 582CHO A. 6. B. 7. C. 4. D. 5.
Hướng dẫn giải
Các đồng phâneste ứng với công thức phân tử khi bị thủy phânthu được anđehit là: 582CHO (có đồng phânhình học) 23HCOOCHCHCHCH
đồng phânhình học)
CHCOOCHCH
Như vậy, có6 chất (6este)khi bị thủy phânsinhra anđehit. Chọn A.
Chú ý: Với estecó1liên kết trongphân tử thì nếu: CC
Đề bài hỏi số đồng phânthì phải tính cả đồng phânhình học.
Đề bài hỏi số đồng phân cấu tạo thì không tính đồng phânhình học.
Trong đó, điều kiện để có đồng phânhình học:
Ví dụ 4: Số đồng phân thuộc loại este chứa vòngbenzen ứng với công thức phân tử là:882CHO
A. 6. B. 3. C. 4. D. 5.


Hướng dẫn giải
Cáccông thức cấu tạo phù hợp là: Haycông thức viết gọn là:
DẠYKÈMQUYNHƠN
Trang7
OFFICIAL
33HCOOCHCCHCH (có
3 3CHCOOCHCHCH 25 2
Chọn A. ®
Kiểu hỏi 3: Tính chất hóa học Ví dụ mẫu
Ví dụ 1: Chất nàosau đây có phản ứng tráng bạc?
A. B. C. D. 3 3CHCOOCH 3 25CHCOOCH 3HCOOCH 3 CHCOOH
Hướng dẫn giải
Các hợp chất có phản ứng tráng bạc là: anđehit, axitfomic(HCOOH), muối của axitfomic,estecó dạng HCOOR’.
Chất có phản ứng tráng bạc là .3HCOOCH
Chọn C. ®
Ví dụ 2: Sản phẩm của phản ứng thủy phânmetylacrylattrongdung dịch NaOH gồm: A. và . B. và . 2 CHCHCOONa 3 CHOH 3 CHCOONa 2 CHCHOH C. và . D. và . 3 CHCOONa 3 CHCHO 2 CHCHCOOH 3 CHOH Hướng dẫn giải Phương trìnhhóa học: t 2 3 2 3 CHCHCOOCHNaOHCHCHCOONaCHOH Chọn A. ® Ví dụ 1: Estenàosau đây khitác dụng với dung dịch NaOH đun nóng,thu được hỗn hợp sản phẩm gồm và ? 3 CHCOONa 3 CHCHO A. B. 2 3CHCHCOOCH 3 2CHCOOCHCH C. . D. . 2HCOOCHCH 3 3CHCOOCHCHCH Hướng dẫn giải Khi thủy phân este thu được sản phẩm chứa anđehit axetic thì este đó có đầu ancol là gốc 3 CHCHO vinyl,có dạng: 2RCOOCHCH Mà sản phẩm muối là . 3 CHCOONa Công thức estelà
DẠYKÈMQUYNHƠN OFFICIAL Trang8
643 643 643 2653 6565 3 HCOOCHCHo;HCOOCHCHm;HCOOCHCHp; HCOOCHCH;CHCOOCH;CHCOOCH
®
. 3 2CHCOOCHCH
Chọn B.
Ví dụ 4: Estenàosau đây phản ứng với NaOHtrongdung dịch theo tỉ lệ mol1:2? A. Phenylaxetat. B. Anlylfomat. C. Benzylaxetat. D. Vinylfomat. Hướng dẫn giải Este đơn chức mà phản ứng với NaOHtheo tỉ lệ mol1:2thì chỉ có thể làestecó dạng (este 65RCOOCH của phenol).
Phương trìnhhóa học: 65 65 2 RCOOCH2NaOHRCOONaCHONaHO
Chọn A. ®
Chú ý: (phenyl axetat) là este của phenol, khi bị thủy phân trong môi trường bazơ thu 3 65CHCOOCH
được hai muối và nước.
Kiểu hỏi 4: Tính chất vật lí - Ứng dụng – Điều chế Ví dụ mẫu
Ví dụ 1: Trong số các chất dưới đây, chất có nhiệt độ sôicao nhất là: A. . B. . C. . D. 25 CHOH 3HCOOCH 3 CHCOOH 3 CHCHO
Hướng dẫn giải
Do ảnh hưởng của liên kết hiđro nên nhiệt độ sôi của este, anđehit < ancol < axit có phân tử khối tương đương.
Nếu cùng loại hợp chất thì nhiệt độ sôi tăng theo chiều tăng của phân tử khối (M).
Trong bốn chất, axitaxetic có nhiệt độ sôicao nhất. 3 CHCOOH
Chọn C.
Ví dụ 2: Chất nàosau đây là chất lỏng ở điều kiện thường? A. Etylaxetat. B. Anđehit fomic. C. Natriaxetat. D. Phenol. Hướng dẫn giải Chất Etylaxetat 3 25CHCOOCH
Anđehit fomic HCHO
Natriaxetat 3 CHCOONa
Phenol 65 CHOH Trạng thái (ở điều kiện thường) lỏng khí rắn rắn Chọn A. ® Ví dụ 3: Khicho chất Xvào nước thu được hỗn hợp bị táchthànhhai lớp. Chất Xlà: A. etylaxetat. B. axitaxetic. C. axitfomic. D. ancoletylic. Hướng dẫn giải Axitcacboxylicvàancolcó số nguyên tử cacbon từ 1C đến 3Ctan tốt trong nước. Este nhẹ hơn nước, khôngtantrong nước. Khi cho este ở thể lỏng vào nước thì hỗn hợp sẽ bị tách thành hai lớp. Trong đó, lớp chất lỏng phía trênlàeste; lớp chất lỏng phía dưới là nước. Chọn A. ® Ví dụ 4: Este được điều chế trực tiếp từ phản ứng giữa hai chất là: 3 25CHCOOCH
DẠYKÈMQUYNHƠN
Trang9
OFFICIAL
A. và . B. và . 3 CHCOOH25 CHOH 25 CHCOOH 3 CHOH C. và . D. và . HCOOH37 CHOH 3 CHCOOH 3 CHOH
Hướng dẫn giải
Este được điều chế trực tiếp từ phản ứng giữa và . 3 25CHCOOCH 3 CHCOOH25 CHOH Phương trìnhhóa học:
Chọn A. ® Ví dụ 5: Phát biểu nàosau đây là sai?
A. Benzylaxetatcómùi thơm của hoanhài.
B. Isoamylaxetatcómùi thơm của chuối chín.
C. Cáceste rất íttantrong nước.
D. Một số este được dùnglàm chất dẻo.
Hướng dẫn giải
A đúng vìestecómùi thơm của hoanhàilàbenzylaxetat.
B đúng vìestecómùi thơm của chuối chínlàisoamylaxetat.
C đúng vì khả năng tạo liên kết hiđro giữa cácphân tử este với cácphân tử nước rất kémnêncáceste rất íttantrong nước.
D sai vì không có este nào được dùng làm chất dẻo mà chỉ có một số polime của este được dùng để sản xuất chất dẻo.
Chọn D. ®
Kiểu hỏi 5: Lí thuyết tổng hợp Ví dụ mẫu
Ví dụ 1: Tiến hànhthí nghiệm điều chế etylaxetattheocác bước sau đây: Bước 1: Cho1ml ,1ml vàvài giọt dung dịch đặc vào ống nghiệm. 25 CHOH 3 CHCOOH 24HSO
Bước 2: Lắc đều ống nghiệm, đun cách thủy (trong nồi nước nóng) khoảng 5–6phút ở .6570C Bước 3: Làm lạnh, sau đó rót2mldung dịch NaClbãohòavào ống nghiệm. Phát biểu nàosau đây sai?
A. đặc cóvaitrò vừa làm chất xúctác vừa làm tăng hiệu suất tạo sản phẩm. 24HSO
B. Mục đích chính của việc thêmdung dịch NaClbãohòalà để tránhphân hủy sản phẩm.
C. Sau bước 2,trong ống nghiệm vẫn còn và . 25 CHOH 3 CHCOOH
D. Sau bước 3, chất lỏng trong ống nghiệm táchthànhhai lớp. Hướng dẫn giải Phương trìnhhóa học: .
đặc làm xúc tác và hút nước nên làm chuyển dịch cân bằng theo chiều thuận Tăng hiệu suất 24HSO phản ứng.
DẠYKÈMQUYNHƠN
Trang10
OFFICIAL
c
đ
24 HSO,Æ
3 25 3 252 t CHCOOHCHOH CHCOOCHHO
c
CHCOOHCHOH CHCOOCHHO
đ
24 HSO,Æ
3 25 3 252 t
Dung dịch NaClbãohòachovàolàm tăng khối lượng riêng của dung dịch và tăng tínhion của lớp nước nên làm giảm độ tan của este sẽ đẩy este tạo thành lên trên, dung dịch NaCl bão hòa dưới (có hòa tan ancolvàaxit dư). Như vậy, hỗn hợp bị táchthànhhai lớp.
Khilàm lạnh thì phản ứng sẽ dừng lại. Phản ứng thuận nghịch nênaxitvàancol đều dư. Chọn B. ®
Biết Xcócông thức phân tử và chứa hai chức este; đều cóhainguyên tử cacbontrong 6104CHO 12X,X phân tử và khối lượng mol của nhỏ hơn khối lượng mol của .2X
Phát biểu nàosau đây sai?
A. Phân tử khối của là60. 4X
B. là hợp chất hữu cơ tạp chức. 5X
C. là anđehit axetic. 6X
D. Phân tử cóhainguyên tử oxi. 2X
Hướng dẫn giải Phương trìnhhóa học:
DẠYKÈMQUYNHƠN
Trang11
OFFICIAL
123 1 4 t 2 5 3
aX2NaOHXXXbXHClXNaCl cXHClXNaCldXCuOXCuHO
Ví dụ 3: Cho sơ đồ phản ứng theo đúng tỉ lệ mol
6 2
t 3 2 25 3 2 25 1 2 3 3 3 1 4 2 2 2 5 t 25 3 2 3 6 aCHCOOCHCOOCH2NaOHCHCOONaHOCHCOONaCHOH X X X X bCHCOONaHClCHCOOHNaCl X X cHOCHCOONaHClHOCHCOOHNaCl X X dCHOHCuOCHCHOCuHO X X Do đó, A,B,C đúng, Dsai. Chọn D. ® Bài tập tự luyện dạng 1 Câu 1: Chocác chất cócông thức cấu tạo sau đây: 32 3 3 3 25 3 3 23 22 3 25 33 1CHCHCOOCH;2CHOOCCH; 3HCOOCH; 4CHCOOH; 5CHOCOCH;6HOOCCHCHOH; 7CHOOCCOOCH;8CHCOCH
Số chất thuộc loại estelà:
A. 3. B. 4. C. 5. D. 6. Câu 2: Etylpropionatlàestecómùi thơm của dứa. Công thức của etylpropionatlà:
A. B. C. D. 25HCOOCH 25 25CHCOOCH 25 3CHCOOCH 3 3CHCOOCH
Câu 3: Chất lỏng cócông thức cótên gọi là: 3 2CHCOOCHCH
A. vinylaxetat. B. metylaxetat. C. etylaxetat. D. metylpropionat.
Câu 4: EsteXtác dụng với dung dịch NaOHthu được natrifomat.Công thức cấu tạo của esteXlà:
A. B. C. D. 25 25CHCOOCH 3 25CHCOOCH 3 3CHCOOCH 3HCOOCH Câu 5: Estenàosau đây tác dụng với NaOHthu được ancoletylic?
A. B. C. D. 3 25CHCOOCH 3 37CHCOOCH 25 3CHCOOCH 3HCOOCH Câu 6: XàphònghóaesteXtrongdung dịch NaOH,thu được và .Công 2 CHCHCOONa 33CHCOCH thức cấu tạo của Xlà: A. B. 3 3 2CHCHCHCOOCHCH
C. D. 2 3CHCHCOOCHCHCH
25 2CHCOOCHCH
OFFICIAL
2 3 2CHCHCOOCCHCH
Câu 7: Thủy phân este X trong dung dịch axit loãng, thu được axit oxalic và ancol etylic. Công 24HSO thức của Xlà: A. . B. . 25 25CHOOCCOOCH 3 22 3CHCOOCHCHOOCCH C. D. 25 25CHCOOCOOCH 3 22 25CHCOOCHCHCOOCH Câu 8: Dãynàosau đây sắp xếp các chất theo thứ tự tăng dần nhiệt độ sôi? A. . B. . 37 25 3 3CHOHCHCOOHCHCOOCH 25 37 3 3CHCOOHCHOHCHCOOCH C. . D. . 3 325 37 CHCOOCHCHCOOHCHOH 3 337 25 CHCOOCHCHOHCHCOOH Câu 9: Este E (đơn chức, mạch hở), phân tử có chứa hai liên kết pi . Công thức phân tử của E có dạng: A. B. C. D. n2n2CHO n2n42 CHO n2n22 CHO n2n24 CHO Câu 10: Este X (mạch hở, được tạo thành từ một axit cacboxylic và một ancol) có công thức phân tử là Số công thức cấu tạo phù hợp của Xlà: 464CHO A. 1. B. 4. C. 2. D. 3. Câu 11: Thủy phâneste thu được anđehit. Số công thức cấu tạo phù hợp của Xlà: 582XCHO A. 6. B. 3. C. 4. D. 5. Câu 12: Estenàosau đây cóphân tử khối là88?
A. Etylaxetat. B. Metylfomat. C. Vinylfomat. D. Metylaxetat. Câu 13: Trongthành phần của dầu gội đầu thường có một số este.Vaitrò của cácestenàylà A. tạo màu sắc hấp dẫn. B. làm giảm thành phần của dầu gội. C. tăng khả năng làm sạch của dầu gội. D. tạo hương thơm mát, dễ chịu. Câu 14: Chất X có công thức phân tử . Khi X tác dụng với dung dịch NaOH sinh ra chất Y có 462CHO công thức . Chất Xcótên gọi là: 332 CHONa
DẠYKÈMQUYNHƠN
Trang12
A. metylacrylat. B. metylmetacrylat. C. metylaxetat. D. etylacrylat. Câu 15: Choeste tác dụng với NaOHtheo tỉ lệ mol tương ứng là1:2,thu được một muối 6104XCHO và một ancol. Biết Xkhôngcó phản ứng tráng bạc. Số công thức cấu tạo phù hợp với Xlà: A. 6. B. 5. C. 4. D. 3. Câu 16: Hợp chất X có công thức phân tử Đun nóng a mol X trong dung dịch NaOH vừa đủ, 462CHO thu được dung dịch Y.ChoYtác dụng với dung dịch trong ,thu được 4amol bạc. Biết các 3AgNO 3NH phản ứng xảy rahoàntoàn.Công thức cấu tạo của Xlà A. B. 2 2HCOOCHCHCH 3 2HCOOCCHCH C. . D. . 3HCOOCHCHCH 3 2CHCOOCHCH
OFFICIAL
Câu 17: Thủy phân hoàn toàn este trong dung dịch NaOH, thu được hai sản phẩm đều có 582XCHO phản ứng tráng bạc. Số công thức cấu tạo phù hợp của Xlà: A. 2. B. 3. C. 4. D. 5. Câu 18: Este phản ứng với NaOHtheo tỉ lệ mol tương ứng bằng 1:2. Số công thức cấu tạo 882XCHO phù hợp của Xlà: A. 3. B. 4. C. 2. D. 5. Câu 19: Este không tác dụng với chất (hoặc dung dịch) nàosau đây? 2 3CHCHCOOCH
A. Dung dịch NaOH (đun nóng). B. (xúctácNi, đun nóng). 2H
C. Kim loại Na (điều kiện thường). D. (xúctác loãng, đun nóng). 2 HO 24HSO
Câu 20: Cho các este: etyl fomat, vinyl axetat, metyl benzoat, phenyl axetat. Số este phản ứng được với dung dịch NaOH (đun nóng)sinhraancollà: A. 1. B. 2. C. 3. D. 4. Bài tập nâng cao Câu 21: Estehai chức, mạch hở Xcócông thức phân tử vàkhôngthamgia phản ứng tráng bạc. 684CHO X được tạo thành từ ancolYvàaxitcacboxylicZ.Ykhông phản ứng với ở điều kiện thường; 2 CuOH khi đun Y với đặc ở không tạo raanken.Phát biểu nàosau
DẠYKÈMQUYNHƠN
Trang13
đây đúng? 24
A. TrongXcóbanhóm .3CH B. Chất Zkhônglàm mất màudung dịch bromtrongdungmôi .4CCl C. Chất Ylàancoletylic. D. Phân tử chất Zcó số nguyên tử cacbon bằng số nguyên tử oxi. Câu 22: Este X có công thức phân tử . Xà phòng hóa hoàn toàn X bằng dung dịch NaOH, thu 6104CHO được ba chất hữu cơ Y, Z, T . Biết Y tác dụng với tạo
ZTMM
NungnóngZ với hỗn hợp rắn gồm
thức
năng
HSO170C
dung dịch màu xanh lam.
2 CuOH
NaOHvàCaO,thu được .Phát biểu nàosau đây sai? 4CH A. Xcóhaicông
cấu tạo phù hợp. B. Ycó mạch cacbonphânnhánh. C. Tcó khả
thamgia phản ứng tráng bạc. D. Zkhônglàm mất màudung dịch brom.
Câu 23: Chất X có công thức phân tử . Cho 1 mol X phản ứng hết với dung dịch NaOH, thu 684CHO được chất Y và 2 mol chất Z. Đun Z với dung dịch đặc, thu được đimetyl ete. Chất Y phản ứng 24HSO với dung dịch HCl,thu được chất Tcó mạch cacbonkhôngphânnhánh.Phát biểu nàosau đây sai?
A. Chất Tkhôngcó đồng phânhình học.
B. Chất X phản ứng với theo tỉ lệ mol1:1. 2 HNi,t
C. Chất Ycócông thức .4242 CHONa
D. Chất Zkhônglàm mất màudung dịch bromtrongdungmôi .4CCl
Câu 24: Hợp chất hữu cơ mạch hở tác dụng với lượng dư dung dịch NaOH đun nóng thu 8125XCHO được glixerolvà hỗn hợp hai muối cacboxylatYvàZ .Hai chất Y,Z đều khôngcó phản ứng YZMM tráng bạc. Phát biểu nàosau đây đúng?
A. Axitcacboxylic của muối Zcó đồng phânhình học.
B. Tên gọi của Zlànatriacrylat.
C. Cóhaicông thức cấu tạo thỏa mãntính chất của X.
OFFICIAL
D. Phân tử X chỉ chứa một loại nhóm chức. Câu 25: Hợp chất hữu cơ mạch hở tác dụng với lượng dư dung dịch NaOH đun nóng,thu 8125XCHO được glixerol và hai muối của axit cacboxylic Y và Z. Axit Z có đồng phân hình học. Phát biểu nào sau đây đúng?
A. Cóhaicông thức cấu tạo thỏa mãntính chất của X.
B. Ycó phản ứng tráng bạc.
C. Phân tử X chỉ chứa một loại nhóm chức.
D. Phân tử khối của Zlà94.
Câu 26: Cho1mol chất X(, chứa vòngbenzen)tác dụng hết với NaOH dư, thu được 2mol chất 984CHO Y, 1 mol chất Z và 1 mol . Chất Z tác dụng với dung dịch loãng thu được chất hữu cơ T. 2 HO 24HSO Phát biểu nàosau đây sai?
A. Chất Ttác dụng với NaOHtheo tỉ lệ mol1:2.
B. Chất Ycó phản ứng tráng bạc.
C. Phân tử chất Zcóhainguyên tử oxi.
D. Chất Xtác dụng với NaOHtheo tỉ lệ mol1:3.
DẠYKÈMQUYNHƠN
Trang14
Câu
sơ đồ chuyển hóasau(theo
mol): t 123 124 424 t 224 524 3 6 2 aX2NaOHXXXb2XHSO2XNaSO c2XHSO2XNaSOdXCuOXCuHO Biết Xcóhainhómeste,cócông thức phân tử làcác chất hữu cơ khácnhau( tác 464345 CHO;X,X,X 3X dụng được với Na).Phát biểu nàosau đây đúng? A. hòatan được . B. Chất Xthamgia phản ứng tráng bạc. 3X 2 CuOH C. Hai chất và đều cóhainguyên tử oxi. D. Phân tử bị oxihóa bởi tạo ra . 4X 5X 6X 3X Câu 28: Chocác sơ đồ phản ứng theo đúng tỉ lệ mol:
27: Cho
đúng tỉ lệ
Biết chứa hai chức este; các phân tử có cùng số nguyên tử cacbon. Phát biểu 6104XCHO 345X,X,X nàosau đây sai?
A. Nhiệt độ nóng chảy của và đều cao hơn . 4X 5X 3X
B. Các chất đều tan tốt trong nước. 345X,X,X
C. Chất bị khử bởi dung dịch trong ,thu được kết tủa Ag. 6X 3AgNO 3NH
D. Dung dịch nước của và đều tác dụng với 4X 5X 3CaCO Câu 29: Chất X có công thức phân tử . Cho 1 mol X phản ứng hết với dung dịch NaOH, thu 684CHO được chất Y và 2 mol chất Z. Đun Z với dung dịch đặc, thu được đimetyl ete. Chất Y phản ứng 24HSO với dung dịch loãng (dư), thu được chất T. Cho T phản ứng với HBr, thu được hai sản phẩm là 24HSO đồng phân cấu tạo của nhau.Phát biểu nàosau đây đúng?
A. Chất Tkhôngcó đồng phânhình học.
B. Chất X phản ứng với theo tỉ lệ mol1:3. 2 HNi,t
C. Chất Ycócông thức .4442 CHONa
D. Chất Zlàm mất màu nước brom. Câu 30: Tiến hànhcácthí nghiệm theocác bước sau:
Bước 1: Chovàohai ống nghiệm mỗi ống 2mletylaxetat.
Bước 2: Thêm 2 ml dung dịch 20% vào ống thứ nhất; 4 ml dung dịch NaOH 30% vào ống thứ 24HSO hai.
Bước 3: Lắc đều cả hai ống nghiệm, ngâmtrong nước nóng, để nguội.
Chocácphát biểu sau:
(a)Sau bước 2, chất lỏng trong cả hai ống nghiệm đều phânthànhhai lớp. (b)Sau bước 2, chất lỏng trong cả hai ống nghiệm đều đồng nhất.
(c)Sau bước 3, ở hai ống nghiệm đều thu được sản phẩm giống nhau. (d) Ở bước 3,có thể thay việc ngâmtrong nước nóng bằng cách đun nóng nhẹ. Số phát biểu đúng là: A. 1. B. 3. C. 4. D. 2. Dạng
DẠYKÈMQUYNHƠN OFFICIAL Trang15 t 123 124244 224245
3 6
X2NaOHXXX 2XHSONaSO2X
XCuOXCuOHO
t
2
2XHSONaSO2X
2: Phản ứng thủy phân thông thường Bài toán 1: Xác định lượng chất trong phản ứng Phương pháp giải Ví dụ: Xà phòng hóa 5,28 gam etyl axetat bằng 250 ml dung dịch
sau
thu
NaOH 0,2M. Cô cạn dung dịch
phản ứng,
được chất rắn khancó khối lượng là:
A. 4,98gam. B. 4,10gam. C. 4,92gam. D. 4,52gam. Hướng dẫn giải
Bước 1: Quy đổi số liệu đề bàira số mol. 325 CHCOOCH NaOH n0,06mol;n0,05mol
Bước 2: Viết phương trình phản ứng xà phònghóa. Phương trìnhhóa học: 3 25 3 25 CHCOOCHNaOHCHCOONaCHOH 0,060,05 mol Bước 3: Tínhtheo phương trìnhhóa học. Chú ý 1: Đối với bài chất hết, chất dư thì: Nếu NaOH hết: chÊtr¾nkhanmuèimm
Nếu NaOH dư: chÊtr¾nkhanmuèiNaOHd mmm Chú ý 2: Ngoài ra, ta có thể áp dụng định luật bảo toàn khối lượng. estepNaOHchÊtr¾nancol mmmm
Ta thấy: phản ứng hết, 0,060,05NaOH 11 dư, tínhtoántheo số molNaOH. 3 25CHCOOCH Theo phương trình: . 3 CHCOONaNaOH nn0,05mol
DoNaOH hết nên khối lượng chất rắn khanlà: 3 crCHCOONa mm0,05.824,1gam
được
DẠYKÈMQUYNHƠN
Trang16
OFFICIAL
CHCOOCHNaOHCHCOONaCHOH
0,1 mol 3 muèiCHCOONa mm0,1.828,2gam Chọn D. Ví dụ 2: Xàphòng hóa3,52 gametylaxetat bằng 225ml dung dịch NaOH 0,2M.Cô cạn dung dịch sau phản ứng, thu được chất rắn khancó khối lượng là A. 3,69gam. B. 3,28gam. C. 5,32gam. D. 3,48gam. Hướng dẫn giải 325 CHCOOCH NaOH n0,04mol;n0,045mol
Chọn B. Ví dụ mẫu Ví dụ 1: Xàphònghóahoàntoàn7,4gammetylaxetat bằng dung dịch NaOH dư, thu
mgam muối. Giá trị của mlà: A. 11,0. B. 9,6. C. 6,8. D. 8,2. Hướng dẫn giải Theo đề bài: . 33CHCOOCH 7,4 n70,1mol 4
Phương trìnhhóa học: t 3 3 3 3
0,1
Phương trìnhhóa học: t 3 25 3 25 CHCOOCHNaOHCHCOONaCHOH 0,040,045 mol
n0,0450,040,005mol m0,005.400,2gam MM74 14,8 nn 70,2mol 4
CHCOONaNaOHpCHCOOCH CHCOONa 25 33 25 33
Bảo toàn khối lượng: estepNaOHchÊtr¾nancol chÊtr¾n
Khối lượng chất rắn khanlà: . 3 CHCOONaNaOHd mmm3,280,23,48gam Cách 2: Theo phương trình: . 25 325 CHOHCHCOOCH nn0,04mol Phương trìnhhóa học: t 25 25 t 3 3 3 3
HCOOCHNaOHHCOONaCHOH CHCOOCHNaOHCHCOONaCHOH
mmmm 3,520,04540m0,0446m3,48gam Theo phương trình: 3 33NaOHHCOOCHCHCOOCH NaOH
Chọn D. ® Chú ý: Khicô cạn thìNaOH tồn tại ở dạng rắn. Ví dụ 3: Xàphònghóahoàntoàn14,8gam hỗn hợp haiestelà và bằng một 25HCOOCH 3 3CHCOOCH lượng dung dịch NaOH vừa đủ, đun nóng. Khối lượng NaOH cần dùnglà: A. 4,0gam. B. 12,0gam. C. 16,0gam. D. 8,0gam. Hướng dẫn giải
thấy:
nnn0,2mol m0,2.408gam Chọn D. ® Chú ý: Khibài tập cho hỗn hợp các chất, ta cố gắng tìm điểm chung của các chất đó để giải quyết bài tập đơn giản hơn. Bài toán 2: Xác định công thức của este Phương pháp giải Ví dụ: Khi cho este X đơn chức tác dụng vừa đủ với NaOH thu được 9,52 gam natri fomat và 8,4
DẠYKÈMQUYNHƠN OFFICIAL Trang17
Nhận thấy: hết, NaOH dư, tínhtoántheo số mol . 3 250,040,045CHCOOCH 11 3 25CHCOOCH Chất rắn gồm: NaOH dư và . 3 CHCOONa Cách 1: Theo phương trình:
3 3 5 3 Ta
nnn0,04mol m0,04.823,28gam Tacó: NaOHd NaOHd HCOOCHCHCOOCH HCOOCHCHCOOCH
Viết phương trình phản ứng xà phòng hóa, từ đó tính theo phương trình hóa học hoặc áp dụng định luật bảo toàn khối lượng để tìm khối lượng của chất chưa biết.
Dựa vào biểu thức: .Mm n
Tìm được phân tử khối của este, suy ra được công thức phân tử của este.
Tìm được khối lượng mol muối của axit tạo este, suyra được công thức của muối.
Tìm được khối lượng của ancol tạo este, suy ra được công thức của ancol.
Từ đó xác định được công thức phân tử, công thức cấu tạo của este hoặc của hỗn hợp haieste. Chú ý: Đối với các hỗn hợp ta đặt công thức chung và tính được khối lượng mol trung bình Suy ra được công thức của một hoặc hai chất.
gamancol.Xlà:
A. metylfomat. B. etylfomat. C. propylfomat. D. butylfomat.
Hướng dẫn giải
HCOONa n0,14mol
Phương trìnhhóa học: HCOOR'NaOHHCOONaR'OH 0,140,14mol
DẠYKÈMQUYNHƠN
Trang18
OFFICIAL
ancol R' 37M8,460M43CH 0,14
1: Xà phòng hóa hoàn toàn m gam este X
chức
150
12,3gam
Yvà6,9gamancolZ.Công
A. B. C. D. 3HCOOCH 3 3CHCOOCH 25HCOOCH 3 25CHCOOCH Hướng dẫn giải NaOH n0,15mol Phương trìnhhóa học: t HCOOR'NaOHHCOONaR'OH 0,150,150,15mol Tacó: RCOONa R 3 R' 25 R'OH M12,382M82442315CH 0,15 6,9 M461729CH M 46 0,15 Vậy công thức cấu tạo của Xlà: . 3 25CHCOOCH Chọn D. ®
Tacó:
Công thức của Xlà (propylfomat). 37HCOOCH Chọn C. ® Ví dụ mẫu Ví dụ
đơn
cần vừa đủ
ml dung dịch NaOH 1M, thu được
muối
thức cấu tạo của Xlà:
A.
ý: Esteno đơn chức mạch hở cócông thức phân tử tổng quátlà: n2n2 CHOn2 Nênluôncó: M14n32 Ví dụ 3: Xàphònghóahoàntoàn20,8gam hỗn hợp X gồm haieste đơn chức bằng dung dịch NaOH,thu được 20,4gam một muối và12,4gam hỗn hợp haiancol đồng đẳng kế tiếp. Công thức của haiestetrong Xlà: A. và . B. và . 25HCOOCH 37HCOOCH 3 3CHCOOCH 25 3CHCOOCH C. và . D. và . 3HCOOCH
DẠYKÈMQUYNHƠN OFFICIAL Trang19
X X X
Tacó: X
14 Công
X
25HCOOCH
Hướng dẫn giải Bảo toàn khối lượng: XNaOHmuoiancol NaOH NaOH NaOH mmmm 20,8m20,412,4 m20,412,420,812gamn0,3mol Gọi công thức chung của haiestelà .RCOOR' Phương trìnhhóa học: t RCOOR'NaOHRCOONaR'OH 0,30,30,3mol Tacó: RCOONa R R' R'OH M20,468M6844231 0,3 M41,331724,33M12,441,33 0,3 Vậy RlàH,R’là và . 3CH 25CH Công thức của haiestetrongXlà và . 3HCOOCH 25HCOOCH
Ví dụ 2: Xlàesteno, đơn chức, mạch hở. Cho9,00gamXtác dụng vừa đủ với 200mldung dịch NaOH 0,75M đun nóng.Công thức cấu tạo thu gọn của Xlà: A. . B. . C. . D. . 3HCOOCH 3 3CHCOOCH 25HCOOCH 3 25CHCOOCH Hướng dẫn giải Theo đề bài: NaOH n0,75.0,20,15mol Phương trìnhhóa học: RCOOR'NaOHRCOONaR'OH 0,150,15 mol
Mm960 n0,15
Gọi công thức phân tử của Xlà .n2n2 CHOn2
6032M14n32n 2
thức cấu tạo của
chỉ có thể là .3HCOOCH Chọn
® Chú
3 3CHCOOCH 3 25CHCOOCH
Chọn C. ®
Bài tập tự luyện dạng 2 Bài tập cơ bản
Câu 1: Thủy phânhoàntoàn4,4gametylaxetat cần vừa đủ Vmldung dịch NaOH0,5M đun nóng.Giá trị của Vlà: A. 50. B. 200. C. 150. D. 100. Câu 2: Xà phòng hóa hoàn toàn 2,96 gam bằng một lượng dung dịch KOH đun nóng, vừa 25HCOOCH đủ. Cô cạn dung dịch sau phản ứng, thu được mgam muối khan.Giá trị của mlà
A. 5,20. B. 2,72. C. 4,48. D. 3,36. Câu 3: Xàphònghóahoàntoàn14,8gam hỗn hợp gồm metylaxetatvàetylfomat cần vừa đủ Vmldung dịch KOH1M.Giá trị của Vlà
A. 400. B. 200. C. 150. D. 175. Câu 4: Xàphònghóahoàntoànm1 gam hỗn hợp gồm và bằng lượng vừa đủ 3 3CHCOOCH 3HCOOCH
200mldung dịch NaOH1M.Sau phản ứng xảy rahoàntoàn,thu được mgamancol.Giá trị của m2 là:
OFFICIAL
A. 12,3. B. 6,4. C. 3,2. D. 9,2. Câu 5: Để xà phòng hóa 17,4 gam một este no đơn chức, mạch hở cần dùng 300 ml dung dịch NaOH 0,5M.Este đó cócông thức phân tử là:
A. B. C. D. 482CHO 362CHO 5102CHO 6122CHO
Câu 6: Thủy phân 13,2 gam etyl axetat bằng 300 ml dung dịch NaOH 0,2M. Sau khi phản ứng xảy ra hoàntoàn,cô cạn dung dịch, thu được mgam chất rắn khan.Giá trị của mlà A. 12,30. B. 12,84. C. 15,60. D. 4,92. Câu 7: Cho8,8gamesteXcócông thức phân tử tác dụng với dung dịch chứa 0,15molNaOH. 482CHO Cô cạn dung dịch sau phản ứng thu được 11,6gam chất rắn khan.Công thức cấu tạo của Xlà
A. . B. . 223 HCOOCHCHCH 25 3CHCOOCH C. D. 23 3CHCOOCH 3 25CHCOOCH Câu 8: Xàphònghóahoàntoàn41,2gam hỗn hợp X gồm haieste đơn chức bằng dung dịch NaOH,thu được 45,2 gam hỗn hợp hai muối của hai axit cacboxylic đồng đẳng kế tiếp và 16 gam một ancol. Công thức của haiestetrongXlà:
A. và . B. và . 3 25CHCOOCH 25 25CHCOOCH 3 3CHCOOCH 25 3CHCOOCH C. và . D. và . 25HCOOCH 3 25CHCOOCH 3 3CHCOOCH 3HCOOCH Câu 9: Xàphònghóahoàntoàn13,2gam hỗn hợp X gồm haiesteno, đơn chức, mạch hở (là đồng phân của nhau, đều không tham gia phản ứng tráng bạc) cần vừa đủ 0,15 mol NaOH. Công thức của hai este trongXlà: A. và . B. và . 3 25CHCOOCH 37HCOOCH 25 25CHCOOCH 37 3CHCOOCH C. và . D. và .
3
CHCOOCH 25 3CHCOOCH 3 25CHCOOCH Câu 10: Este X được tạo thành từ etylen glicol với hai axit cacboxylic đồng đẳng kế tiếp (một axit có phản ứng tráng bạc). Biết rằng, mgamXtác dụng vừa đủ với 0,125molKOH.Giá trị của mlà: A. 7,25. B. 8,75. C. 7,75. D. 8,25.
DẠYKÈMQUYNHƠN
Trang20
49HCOOCH
37
Câu 11: Hóa hơi hoàntoàn2,2gamesteX mạch hở, thu được thể tích bằng thể tích của 0,8gamkhíoxi (đo ở cùng điều kiện). Mặt khác, thủy phânhoàntoàn22gamX bằng dung dịch NaOH dư, thu được 20,5 gam muối. Công thức cấu tạo của Xlà:
A. B. C. D. 25 3CHCOOCH 3 25CHCOOCH 25 25CHCOOCH 37HCOOCH
Câu 12: Để phản ứng hết với một lượng hỗn hợp gồm hai chất hữu cơ đơn chức XvàY cần ( )XYMM < vừa đủ 300mldung dịch NaOH1M,thu được 24,6gam muối của một axit hữu cơ vàmgam một ancol. Đốt cháyhoàntoàn lượng ancoltrên,thu được 4,48lít (đktc) và5,4gam . Chất Ylà: 2 HO
A. B. C. D. 3 25CHCOOCH 3 3CHCOOCH 23 3CHCOOCH 25 25CHCOOCH Câu 13: Cho 0,03 mol este no, mạch hở X tác dụng vừa đủ với 50 ml dung dịch NaOH 1,2M, thu được 4,44gam một muối của axitcacboxylic đa chức và1,92gam một ancol đơn chức. Công thức của Xlà
A. . B. 22 HCOOCHCHOOCH 3 2 3CHCOOCHCOOCH
C. D. 3 22 3CHOOCCHCHCOOCH 3 2 3CHOOCCHCOOCH
OFFICIAL
Bài tập nâng cao Câu 14: Cho4,4gamestecócông thức phân tử tác dụng với dung dịch NaOH vừa đủ, thu được 482CHO mgamancolY. Đun Y với dung dịch đặc ở nhiệt độ thích hợp, thu được chất hữu cơ Z,có tỉ khối 24HSO hơi so với Y bằng 1,7. Biết các phản ứng xảy rahoàntoàn.Giá trị của mlà
A. 3,00. B. 2,55. C. 2,30. D. 1,60. Câu 15: Chất hữu cơ X mạch hở, có công thức phân tử , không tham gia phản ứng tráng bạc. 464CHO Cho a mol X phản ứng với dung dịch KOH dư, thu được ancol Y và m gam một muối. Đốt cháy hoàn toànY,thu được 0,2mol và0,3mol .Giá trị của avàm lần lượt là 2CO 2 HO
A. 0,05và8,4. B. 0,1và13,4. C. 0,2và12,8. D. 0,1và16,6. Câu 16: Thủy phân9,25gamhaiestecócùngcông thức phân tử bằng dung dịch NaOH vừa đủ. 362CHO Cô cạn dung dịch sau phản ứng thu được hỗn hợp ancolYvàmgam chất rắn Z. Đun nóngY với 24HSO đặc ở ,thu được 3,575gam hỗn hợp cácete.Giá trị của mlà 135C A. 10,0. B. 9,55. C. 10,55. D. 8,55. Câu 17: Este đơn chức Xcó tỉ khối so với Helà25.Cho20gamXtác dụng với 300mldung dịch KOH 1M đun nóng.Cô cạn dung dịch sau phản ứng thu được 28gam chất rắn. Công thức cấu tạo của Xlà
DẠYKÈMQUYNHƠN
Trang21
.
3 3CHCOOCHCHCH
CHCHCOOCHCH
2 2 3CHCHCHCOOCH 25 2CHCOOCHCH
Thủy phân hoàn toàn hỗn hợp gồm
cấu tạo của nhau cần vừa đủ 100mldung dịch NaOH1M,thu được 7,85gam hỗn hợp muối của haiaxitlà đồng đẳng kế tiếp và4,95gamhaiancol bậc I.Công
khối
A. B. 25 3 3 HCOOCH,45%;CHCOOCH,55%. 37 3 25 HCOOCH,75%;CHCOOCH,25%. C. D. 37 3 25 HCOOCH,25%;CHCOOCH,75% 25 3 3 HCOOCH,55%;CHCOOCH,45% Câu 19:
vừa
với
A.
B. .
2 23
C. D.
Câu 18:
hai este đơn chức X, Y là đồng phân
thức cấu tạo và phần trăm
lượng của haiestelà
Cho18,48gam hỗn hợp E gồm một este đơn chức, mạch hở và một estehai chức, mạch hở tác dụng
đủ
130mldung dịch NaOH2M,thu được hỗn hợp X gồm haiancolnovà hỗn hợp Y chứa hai muối của haiaxitcacboxylic. Đốt cháyhoàntoànX,thu được 0,32mol và0,48mol . Khối 2CO 2 HO lượng muối có khối lượng mol lớn hơn trongYlà
A. 6,80gam. B. 8,20gam. C. 4,92gam. D. 13,12gam. Câu 20: Thủy phân 17,2 gam este đơn chức A trong 50 gam dung dịch NaOH 28% thu được dung dịch X. Cô cạn dung dịch X thu được chất rắn Y và 42,4 gam ancol Z. Cho toàn bộ chất lỏng Z tác dụng với một lượng Na dư thu được 24,64lít (đktc). Đun toàn bộ chất rắn Y với CaOthu được mgam chất khí. 2H Các phản ứng xảy rahoàntoàn.Giá trị của mlà: A. 5,60. B. 4,20. C. 6,00. D. 4,50. Dạng 3: Phản ứng este hóa Bài toán 1: Tính hiệu suất phản ứng este hóa Phương pháp giải
Ví dụ: Cho 45 gam axit axetic phản ứng với 69 gam etanol (có đặc làm xúc tác) đun nóng, thu được 24HSO 41,25gameste. Hiệu suất của phản ứng estehóalà A. 31,25%. B. 40,00%. C. 50,00%. D. 62,50%. Hướng dẫn giải
OFFICIAL
n0,75mol;n1,5mol
trìnhhóa học:
Ta thấy: Hiệu suất tínhtheoaxit. 0,751,5 11 Bước 2: Tính (tính theo phương estelýthuyÕ t n trìnhhóa học).
Bước 1: Xác định hiệu suất tínhtheo chất nào (nếu đề bàicho số liệu của hai chất thamgia).
m n H 100% 100% m n Chú ý: và đề bàicho.
Theo phương trình: 325 3 325
n n0,75mol m 0,75.8866gam
CHCOOCHltCHCOOH CHCOOCHlt
thùctÕn thùctÕm Hiệu suất của phản ứng estehóalà: estethùctÕ estelýthuyÕ t m 41,25 H 100%100%62,5% m 66
DẠYKÈMQUYNHƠN
Trang22
3 25 CHCOOH CHOH
đ
Phương
24 HSO,Æ c 3 25 3 252 t CHCOOHCHOH CHCOOCHHO
Ví dụ mẫu Ví dụ 1: Đun 3,0 gam với dư (xúc tác đặc), thu được 2,2 gam 3 CHCOOH 25 CHOH 24HSO . Hiệu suất của phản ứng estehóalà: 3 25CHCOOCH A. 50,00%. B. 25,00%. C. 36,67%. D.
Bước 3: Tính hiệu suất. estethùctÕ estethùctÕ estelýthuyÕ t estelýthuyÕ t Hướng dẫn giải Do dư nên hiệu suất phản ứng estehóatínhtheoaxit. 25 CHOH 3 325 CHCOOH CHCOOCH n0,05mol;n0,025mol
Chọn D.
20,75%.
Phương trìnhhóa học: 24 HSO,Æ c 3 25 3 252 CHCOOHCHOH CHCOOCHHO đ
Theo phương trình: 325 3 325
n n0,05mol m 0,05884,4gam
CHCOOCHtheolýthuyÕtCHCOOH CHCOOCHtheolýthuyÕ t
Hiệu suất của phản ứng estehóatrênlà: thùctÕ lýthuyÕ t
m 2,2 H100%100%50% m 4,4 Chọn A. ® Ví dụ 2: Cho 75 gam axit axetic phản ứng với 46 gam ancol etylic (có mặt đặc xúc tác, đun 24HSO nóng),thu được 0,6moletylaxetat. Hiệu suất của phản ứng estehóalà: A. 40%. B. 48%. C. 60%. D. 52%. Hướng dẫn giải
của phản ứng estehóalà: thùctÕ lýthuyÕ t
n 0,6 H.100%.100%60% n 1
Ví dụ: Thực hiện phản ứng estehóamgam 3 CHCOOH bằng thu được 0,02 mol este. Biết hiệu suất 25 CHOH phản ứng được tínhtheoaxit .Giá trị của mlà: H80% A. 2,00. B. 0,72. C. 1,20. D. 1,50. Hướng dẫn giải Phương trìnhhóa học:
24 HSO,Æ c 3 25 3 252 CHCOOHCHOH
DẠYKÈMQUYNHƠN OFFICIAL Trang23
3 25 CHCOOH CHOH n1,25mol;n1mol Phương trìnhhóa học: 24 HSO,Æ c 3 25 3 252 CHCOOHCHOH CHCOOCHHO 1,251 mol đ Ta thấy: Hiệu suất tínhtheo . 1,251 11 25 CHOH Theo phương trình: 325 25 CHCOOCHtheolýthuyÕtCHOH n n1mol Hiệu suất
CHCOOCHHO đ Bước 1: Tínhtoántheo hiệu suất 100%. Coi thì
3 CHCOOHeste
3 CHCOOH
Bước 2: Tínhtoántheoyêu
thì
3
Chọn C. ® Bài toán 2: Tính toán lượng chất khi biết hiệu suất phản ứng Phương pháp giải Với những bài tập cho sẵn hiệu suất ta có thể làmnhanh như sau: đ
. H100%
nn0,02mol
m0,02601,2gam
cầu. Với
H80%
CHCOOHbanÇum 1,2:80%1,5gam
Chọn B. ® Bài tập tự luyện dạng 3 Bài tập cơ bản Câu 1: Đun nóng24gamaxitaxetic với lượng dư ancoletylic(xúctác đặc), thu được 26,4gam 24HSO este. Hiệu suất của phản ứng estehóalà A. 44%. B. 55%. C. 60%. D. 75%. Câu 2: Cho 45 gam axit axetic phản ứng với 69 gam ancol etylic (xúc tác đặc), đun nóng, thu 24HSO được 41,25gametylaxetat. Hiệu suất của phản ứng estehóalà
A. 62,50%. B. 50,00%. C. 40,00%. D. 31,25%. Câu 3: Đun m gam axit axetic với m gam etanol (có đặc làm xúc tác) đến khi phản ứng đạt tới 24HSO trạng tháicân bằng, thu được mgameste. Hiệu suất của phản ứng estehóalà A. 50,00%. B. 62,50%. C. 68,18%. D. 75,00%. Câu 4: Đun nóng6gamaxitaxetic với lượng dư ancoletylic(xúctác đặc), thu được mgameste. 24HSO Biết hiệu suất của phản ứng estehóa bằng 40%.Giá trị của mlà
A. 3,52. B. 5,28. C. 8,80. D. 2,96. Câu 5: Đun nóng4,5gamaxitaxetic với 2,3gamancoletylic(xúctác đặc), thu được mgameste. 24HSO Biết hiệu suất của phản ứng estehóa bằng 55%.Giá trị của mlà
A. 1,98. B. 2,42. C. 4,40. D. 6,6. Câu 6: Đun nóng 4,5 gam axit axetic với m gam ancol etylic (xúc tác đặc), thu được 3,432 gam 24HSO este. Biết hiệu suất của phản ứng estehóa bằng 65%.Giá trị của mlà:
DẠYKÈMQUYNHƠN OFFICIAL Trang24
đ đ
đ Ta
3
Coi
.
325 3 325 CHCOOCHCHCOOH CHCOOCH
đ
chÊtÇuchÊtÇukhiH100% s¶nphÈms¶nphÈmkhiH100% mm :H% mm .H%
Chọn D. ® Ví dụ mẫu Ví dụ 1: Đun nóng 6,0 gam với 6,0 gam (có làm xúc tác, hiệu suất phản 3 CHCOOH 25 CHOH 24HSO ứng estehóa bằng 50%). Khối lượng este tạo thànhlà A. 6,0gam. B. 4,4gam. C. 8,8gam. D. 5,2gam. Hướng dẫn giải 3 25 CHCOOH CHOH n0,1mol;n0,13mol
Phương trìnhhóa học: 24 HSO,Æ c 3 25 3 252 CHCOOHCHOH CHCOOCHHO 0,10,13 mol
thấy: Tínhtoántheo số mol . 0,10,13 11
CHCOOH
thì
H100%
nn0,1molm0,1888,8gam
Với thì H50%
estethuîc m8,850%4,gam 4
A. 1,794. B. 1,166. C. 2,760. D. 5,106. Câu 7: Đun nóng267gamaxitaxetic với 391,6gamancolisoamylic có 3 22 2 CHCHCHCHOH24HSO đặc, biết hiệu suất phản ứng đạt 68%. Khối lượng isoamylaxetat (dầu chuối) thu được là A. 412,896gam. B. 393,380gam. C. 516,120gam. D. 359,080gam. Bài tập nâng cao Câu 8: Cho0,1molaxit đơn chức X phản ứng với 0,15molancol đơn chức Ythu được 4,5gameste với hiệu suất 75%.Tên gọi của estelà
A. metylfomat. B. metylaxetat. C. etylaxetat. D. metylpropionat. Câu 9: Hỗn hợp X gồm axit HCOOH và axit (tỉ lệ mol 1 : 1). Lấy 5,3 gam hỗn hợp X cho 3 CHCOOH tác dụng với 5,75 gam (có xúc tác đặc) thu được m gam hỗn hợp este (hiệu suất các 25 CHOH 24HSO phản ứng estehóa đều bằng 80%).Giá trị của mlà
OFFICIAL
A. 10,12. B. 8,10. C. 6,48. D. 16,20. Câu 10: Chia11,52gam hỗn hợp X gồm axitaxeticvàancoletylicthànhhai phần bằng nhau.Cho phần một tác dụng với Na dư, thu được 1,232lít (đktc). Đun phần hai với đặc, thu được mgameste 2H 24HSO với hiệu suất 80%.Giá trị của mlà
A. 4,224. B. 5,280. C. 3,520. D. 4,400. Dạng 4: Phản ứng thủy phân của este đặc biệt Phương pháp giải Một số loại este đặc biệt: este của phenol;estekhi bị thủy phânsinhra sản phẩm có phản ứng tráng bạc; este tạo bởi cácaxitcacboxylicvàancol nhỏ nhất trongdãy đồng đẳng;…
Viết sơ đồ phản ứng (thường không cần phải cân bằng phương trìnhhóa học).
Viết sơ đồ dạng nhóm chức phản ứng, chẳng hạn:
Khaithác tất
DẠYKÈMQUYNHƠN
Trang25
64 64 2 2 COONaOHCOONaOH COOCHR2NaOHCOONaRCHONaHO 2OH2Na2ONaH
cả các dữ kiện đề cho
luật bảo toànnguyên tố, định luật bảo toàn khối lượng. Ví dụ mẫu Ví dụ 1: Cho 7,2 gam vinyl fomat tác dụng vừa đủ với dung dịch KOH thu được hỗn hợp X. Cho hỗn hợp Xtác dụng với dung dịch trong dư thu được agamAg.Giá trị của alà 3AgNO 3NH A. 21,6. B. 10,8. C. 43,2. D. 16,2. Hướng dẫn giải vinylfomat n0,1mol Phương trìnhhóa học: 2 3 HCOOCHCHKOHHCOOKCHCHO 0,1 0,10,1mol
như: cấu trúc mạch cacbon; giới hạn phân tử khối; đặc điểm của sản phẩm tạo thành;… Vận dụng linh hoạt định
n0,12mol 9,6m8012%9,6gamn40,24mol 0
Ta thấy: esteNaOH n:n1,2:0,241:2
EsteElàeste của phenol .
Cách 1: Tacó: 65 muèikhanHCOONaCHONa xmmm0,12.680,12.11622,08gam
DẠYKÈMQUYNHƠN OFFICIAL Trang26
Hỗn hợp X gồm HCOOK(0,1mol) và (0,1mol). 3 CHCHO 3 Ag
HCOOK2Ag 0,10,2mol CHCHO2Ag 0,10,2mol am0,410843,2gam
23,5294% khối lượng. Cho0,1molX phản ứng với dung dịch NaOH vừa đủ, thu được 19,8gam muối. Nhận xétnàosau đây về Xlà đúng? A. Số công thức cấu tạo phù hợp của Xlà4. B. Xtan tốt trong nước. C. TrongXcónhóm 2CH D. X được điều chế trực tiếp từ một axitcacboxylicvà một ancol. Hướng dẫn giải Xlàeste đơn chức nêntrongphân tử có2nguyên tử. Tacó: O X 32%m23,5294%M 136 23,5294%
Chọn C. ® Ví dụ 2: Đun nóng14,64gamesteEcócông thức phân tử cần dùng vừa đủ 80gamdung dịch 762CHO NaOH12%.Cô cạn dung dịch được xgam muối khan.Giá trị của xlà A. 22,08. B. 28,08. C. 24,24. D. 25,82. Hướng dẫn giải Theo đề bài: 762CHO NaOH NaOH
65RCOOCH MàEcócông thức phân tử Công thức của esteElà . 762CHO 65HCOOCH Phương trìnhhóa học: 65 65 2 HCOOCH2NaOHHCOONaCHONaHO 0,120,240,120,12mol
Cách 2: Dựa vào số mol ,áp dụng định luật bảo toàn khối lượng: 2 HO 2 muèikhanENaOHHO xmmmm14,649,60,121822,08gam
Chọn A. ® Ví dụ 3: EsteX đơn chức, trongXnguyên tử oxi chiếm
Công thức phân tử của Xlà 882CHO
TH1:Xkhông phải làeste của phenol. Phương trìnhhóa học: RCOOR'NaOHRCOONaR'OH 0,1 0,1 mol RCOONa M198
(khôngcóestenào thỏa mãn). R M131
TH2:Xlàeste của phenol. Công thức Xlà hoặc 3 65CHCOOCH 643HCOOCHCH
A đúng vìcó4 đồng phân cấu tạo phù hợp với Xlà và 3 65CHCOOCH 643 HCOOCHCHo,p,m
BsaivìXlàestenêníttantrong nước. Csaivì cả 4 đồng phân của X đều khôngcónhóm . 2CH DsaivìXlàeste của phenolnênkhông được điều chế trực tiếp từ một axitcacboxylicvà một ancol. Chọn A. ® Ví dụ 4: Đốt cháy hoàn toàn m gam hỗn hợp E gồm hai este mạch hở X và Y (đều tạo ra từ axit cacboxylicvàancol, ),thu được 4,48lítkhí (đktc). ChomgamEtác dụng vừa đủ XY MM150 2CO với dung dịch NaOH, thu được 1 muối F và 3,14 gam hỗn hợp ancol Z. Cho toàn bộ Z tác dụng với Na dư, thu được 1,12lítkhí (đktc). Phần trăm khối lượng của XtrongElà 2H A. 29,63%. B. 62,28%. C. 40,40%. D. 30,30%. Hướng dẫn giải
DẠYKÈMQUYNHƠN
Trang27
OFFICIAL
2 CZ CF 2 2 CE CF CECFCZ CZ 2OH2Na2ONaH ZNa 0,1 0,05mol n0,1mol COONaOHCOONaOH ENaOH 0,1 0,10,1mol n0,1mol EOCOn0,2mol 0,2mol n0,1mol nnn n0,1mol * Từ Số nguyên tử cacbontrongancol bằng số nhómOH. CZOHZnn Cácancol thỏa mãntính chất trênlà 3242353 CHOH,CHOH,CHOH, Lại có: Estecó tối đa hai chức este. Y M150 Vậy chỉ cóhaiancol thỏa mãn: . 3242CHOH,CHOH
%m40,40%
tập tự luyện dạng 4 Bài tập cơ bản Câu 1: Thủy phânhoàntoàn8,6gamvinylaxetat rồi chotoàn bộ sản phẩm tác dụng với lượng dư dung dịch trong .Saukhicác phản ứng xảy rahoàntoàn,thu được mgamAg.Giá trị của mlà 3AgNO 3NH
A. 32,4. B. 21,6. C. 43,2. D. 86,4. Câu 2: Thủy phânhoàntoàn14,4gamvinylfomattrongdung dịch KOH dư thu được dung dịch X.Cho Xtác dụng với dư thu được mgamAg.Giá trị của mlà 33AgNO/NH
A. 86,4. B. 21,6. C. 32,4. D. 43,2. Câu 3: Đun nóng13,6gamphenylaxetat với 250mldung dịch NaOH1M.Saukhi phản ứng xảy rahoàn toàn,cô cạn dung dịch được mgam chất rắn khan.Giá trị của mlà
A. 8,2. B. 21,6. C. 19,8. D. 21,8. Câu 4: Cho 5,16 gam một este đơn chức mạch hở X phản ứng hoàn toàn với lượng dư trong 3AgNO thìthu được 12,96gamAg. Biết . Số đồng phân cấu tạo phù hợp của Xlà 3NH X M150
A. 4. B. 2. C. 5. D. 3. Câu 5: Cho 4,48 gam hỗn hợp etyl axetat và phenyl axetat (có tỉ lệ mol 1 :1) tác dụng hết với 800 ml dung dịch NaOH0,1Mthu được dung dịch X.Cô cạn dung dịch Xthu được mgam chất rắn khan.Giá trị của mlà
A. 5,60. B. 4,88. C. 3,28. D. 6,40. Bài tập nâng cao Câu 6: Hỗn hợp haiesteXvàYlà hợp chất thơm cócùngcông thức phân tử là .Cho4,08gam882CHO hỗn hợp trên phản ứng vừa đủ dung dịch chứa 1,6gamNaOH,thu được dung dịch Z chứa ba chất hữu cơ. Khối lượng muối cótrongdung dịch Zlà A. 3,34gam. B. 5,50gam. C. 4,96gam. D. 5,32gam. Câu 7: Hỗn hợp X gồm phenyl axetat, metyl benzoat, benzyl fomat và etyl phenyl oxalat. Thủy phân hoàn toàn 36,9 gam X trong dung dịch NaOH (dư, đun nóng), có 0,4 mol NaOH phản ứng, thu được m gam hỗn hợp muối và10,9gam hỗn hợp Y gồm cácancol.Chotoàn bộ Ytác dụng với Na dư, thu được 2,24lítkhí (đktc). Giá trị của mlà 2H A. 40,2. B. 49,3. C. 42,0. D. 38,4.
DẠYKÈMQUYNHƠN OFFICIAL Trang28 * Từ F chỉ có nguyên tử cacbon
F là CFCCOONa nn0,1mol
thuộc nhóm chức COONa
HCOONa hoặc Axit tạo estelàHCOOH hoặc . 2 COONa 2 COOH Este mạch hở chỉ cóaxitHCOOH thỏa mãn. Vậy Xlà (xmol);ylà (ymol). 3HCOOCH 224HCOOCH Tacó hệ phương trình: x2y0,1x0,04 32x62y3,14y0,03
X
Chọn C. ® Bài
Câu 8: Hai este X, Y có cùng công thức phân tử và chứa vòng benzen trong phân tử. Cho 6,8 882CHO gam hỗn hợp gồm X và Y tác dụng với dung dịch NaOH dư, đun nóng, lượng NaOH phản ứng tối đa là 0,06mol,thu được dung dịch Z chứa 4,7gamba muối. Khối lượng muối của axitcacboxyliccóphân tử khối lớn hơn trongZlà
A. 0,82gam. B. 0,68gam. C. 2,72gam. D. 3,40gam. Câu 9: Thủy phânhoàntoàn10,32gameste đơn chức Xtrongdung dịch NaOH dư, rồi chotoàn bộ sản phẩm tác dụng với lượng dư dung dịch trong . Sau khi các phản ứng xảy ra hoàn toàn thu 3AgNO 3NH được 51,84gamAg.Phát biểu nàosau đây sai?
A. Xcó đồng phânhình học cis–trans.
B. Có thể điều chế X bằng phản ứng estehóa giữa axitfomicvàancolanlylic.
C. Xcó thể làm mất màu nước brom.
D. Trongphân tử Xcó6nguyên tử hiđro. Câu 10: Hỗn hợp E gồm bốn este đều cócông thức vàcóvòngbenzen.ChomgamEtác dụng 882CHO tối đa với 200mldung dịch NaOH1M (đun nóng)thu được hỗn hợp X gồm cácancolvà20,5gam hỗn hợp muối. Chotoàn bộ Xvàobình đựng Na dư, saukhi phản ứng kết thúc, khối lượng chất rắn trongbình tăng 6,9gamso với ban đầu. Giá trị của mlà A. 16,32. B. 8,16. C. 20,40. D. 13,60. Dạng 5: Phản ứng đốt cháy
OFFICIAL
Bài toán 1: Xác định lượng chất trong phản ứng Phương pháp giải * Đốt cháyestetaluôncó: Ví dụ: Đốt cháyhoàntoàn hỗn hợp X gồm haieste no, đơn chức mạch hở thu được 3,6gam vàV 2 HO lítkhí (đktc). Giá trị của Vlà 2CO
A. 2,24. B. 3,36. C. 1,12. D. 4,48. Hướng dẫn giải 2 HO n0,2mol Đối với este no, đơn chức, mạch hở: 2 2 COHOk1:nn
DẠYKÈMQUYNHƠN
Trang29
2 2 esteCOHOk2:nnn *Áp dụng các định luật bảo
2 2 2
Đối với este không no, đơn chức, một liên kết đôi hoặc este no, hai chức, mạch hở CC
toàn: bảo toànnguyên tố, bảo toàn khối lượng,… Bảo toànnguyên tố:
COHOOOeste n2nn2n Đốt cháy este no, đơn chức, mạch hở ta có: 2 2HOCO nn0,2mol V0,222,44,48lÝ t
Chọn D. ®
toán đốt cháy hợp chất hữu cơ. Khi dẫn sản phẩm cháy qua dung dịch kiềm: + Nếu dư: . 2 2 BaOH/CaOH 2COnn
khối lượng dung dịch tăng. dungdÞchthayæ i m 0
Khối lượng dung dịch giảm. dungdÞchthayæ i m 0
dụ mẫu Ví dụ 1: Đốt cháyhoàntoàn một esteno, đơn chức mạch hở rồi dẫn sản phẩm cháyquabình đựng KOH dư, thấy khối lượng bình tăng lên9,3gam. Số mol và sinhra lần lượt là 2CO 2 HO
A. 0,10molvà0,10mol. B. 0,15molvà0,15mol. C. 0,25molvà0,25mol. D. 0,05molvà0,25mol. Hướng dẫn giải Đốt cháyhoàntoànesteno, đơn chức, mạch hở thu được: . 2 2HOCO nnamol Dẫn sản phẩm cháyquabình đựng KOH dư, thấy khối lượng bình tăng lên9,3gam:
DẠYKÈMQUYNHƠN OFFICIAL Trang30
Este đơn chức: . esteOeste 1 nn 2 Bảo toàn khối lượng: 2 2 2 esteCOH esteOpCOHO mmmm mmmm Chú ý: Bài toán phụ với các bài
+ 2 2 binhtngCOHOmmm + 2 2 dungdÞchthayæiCOHO m mmm đ
đ
đ Ví
binht O ng
2CO 2 HO Chọn B. ® Ví dụ 2: Đốt cháy hoàn toàn hỗn hợp X (gồm và cần 3 2323 3CHCOOCH;CHCOOCH 3335CHCOOCH 17,808 lít (đktc) thu được 30,36 gam và 10,26 gam . Lượng X trên phản ứng tối đa với a 2O 2CO 2 HO molNaOH.Giá trị của alà A. 0,18. B. 0,16. C. 0,12. D. 0,20. Hướng dẫn giải 2 2 2 O CO HO n0,795mol;n0,69mol;n0,57mol Tacó: t 2 22 XOCOHO Bảo toànnguyên tố O: . 2 2 2 OCOHOOX OX OX n2n2nnn20,79520,690,57n0,36mol
2 2COH
9,3 mmm44a18a62a9,3gama0,15 62
Vậy số mol và sinhra lần lượt là0,15molvà0,15mol.
Chọn A. ®
dụ 3: Hỗn hợp X gồm esteno, đơn chức, mạch hở Yvàesteno,hai chức, mạch hở Z. Đốt cháyhoàn toàn10,48gamX,thu được 0,37mol và0,3mol . Phần trăm khối lượng YtrongXlà 2CO 2 HO A. 21,18%. B. 48,00%. C. 19,80%. D. 39,60%.
A. ® Bài toán 2: Xác định công thức của este Phương pháp giải Ví dụ: Đốt cháy hoàn toàn 6,0 gam một este no, đơn chức, mạch hở thu được 4,48lít (ở đktc). 2CO Công thức phân tử của estelà A. B. 242CHO 482CHO C. . D. . 5102CHO 362CHO Hướng dẫn giải
DẠYKÈMQUYNHƠN OFFICIAL Trang31
OX 1
2 2
Op
Bảo
tố O: 2 2 2 OCOHOOX OX OX n2n2nnn2.0,352.0,370,3n0,34mol Công thức phân tử của Y dạng: ,công thức phân tử của Z dạng: có số n2n2 CHOn2 p2p24 CHOn4 mol lần lượt làa,bmol. Tacó: .2a4b0,34 Lại có: . 2 2 Z COHO Y 0,3440,07nbnn0,370,30,07molna20,03mol Bảo toànnguyên tố C: . n3 0,03n0,07p0,373n7p37p4 Vậy Ylà (0,03mol)vàZlà
Dựa vào
Ví
Tacó: .
NaOHCOO
nnn0,18mol 2
Ví
Hướng dẫn giải Bảo toàn khối lượng: 2 2 2
esteOpCOHO
Op mmmm 10,4832n440,37180,3n0,35mol
toànnguyên
(0,07mol). 362CHO 464CHO . Y %0,03.74 m1.100%21,18% 0,48
Chọn
2CO n0,2mol
phương trìnhhóa học:
dụ: Este no, đơn chức, mạch hở có công thức tổng quát .n2n2 CHOn2
Gọi công thức của estelà .n2n2 CHOn2 Phương trìnhhóa học:
Tacó phương trình: 60,2n2 14n32n
Công thức phân tử của estelà .242CHO Chọn A. ®

Chú ý: Để giải phương trình một ẩn tacó thể nhập: Rồi bấm “SHIFT + CALC” rồi bấm dấu “=” để ra được kết quả: Vậy hay X2 n2 Ví dụ mẫu Ví dụ 1: Đốt cháyhoàntoàn0,05mol một esteno, mạch hở, đơn chức X rồi dẫn sản phẩm cháyquabình

DẠYKÈMQUYNHƠN OFFICIAL Trang32 t n2n2 2 22 C3n2HOOnCOnHO 2 t n2n2 2 22 C3n2HOOnCOnHO 2 6
Bảo toànnguyên tố: Số nguyên tử 2CO este n C n Số nguyên tử 2 HO este 2n H n Số nguyên tử 2 2 2OesteCOHOO este este n2nn2n O n n
đựng
A. . B. . C. . D. . 242CHO 362CHO 5102CHO 482CHO Hướng dẫn giải 3CaCO n0,2mol Gọi công thức phân tử của estelà: n2n2 CHOn2 Phương trìnhhóa học: t n2n2 2 22 2 32 2 C3n2HOOnCOnHO1 2 COCaOHCaCOHO2 Theo(2): . 2 2 3 CO COCaCO este n0,2nn0,2moln 4 n0,05 Vậy công thức phân tử của Xlà: .482CHO Chọn D. ® Ví dụ 2: Đốt cháy hoàn toàn 13,12 gam hỗn hợp X gồm hai este là đồng đẳng kế tiếp, thu được 21,12 gamkhí và8,64gam nước. Công thức phân tử của haiestetrongXlà 2CO
0,2mol 14n32
nước vôitrong dư thu được 20gam kết tủa. Công thức phân tử của Xlà
A. và . B. và . 242CHO362CHO 342CHO 462CHO C. và . D. và . 362CHO 482CHO 482CHO 582CHO
Hướng dẫn giải 2 2 CO HO n0,48mol;n0,48mol
Ta thấy: Haiestelàno, đơn chức, mạch hở. 2 2 COHOnn Gọi công thức chung của haiestelà: .n2 2n CHOn2 X 13,12 n mol 14n32 Phương trìnhhóa học: t 2 2 22 n2n C3n2HOOnCOnHO 2 13,12 0,48mol 14n32
Tacó phương trình: . 13,120,48n2,4 14n32n
Vậy công thức phân tử của haiestelà và 242CHO362CHO Chọn A. ® Bài tập tự luyện dạng 5 Bài tập cơ bản Câu 1: Đốt cháyhoàntoànesteno, đơn chức, mạch hở thu được 4,4gam vàymol .Giá trị của 2CO 2 HO ylà: A. 0,2. B. 0,1. C. 1,8. D. 0,5. Câu 2: Đốt cháyhoàntoànmgam hỗn hợp haiesteno, đơn chức, mạch hở cần dùng30,24lít (đktc), 2O sau phản ứng thu được 48,4gamkhí .Giá trị của mlà 2CO A. 68,2. B. 25,0. C. 9,8. D. 43,0. Câu 3: Hỗn hợp X gồm ba chất cócông thức là . Đốt cháyhoàntoàn một lượng 22242482 CHO,CHO,CHO hỗn hợp X,thu được 0,8mol vàmgam .Giá trị của mlà 2 HO 2CO A. 17,92. B. 70,40. C. 35,20. D. 17,60. Câu 4: Đốt cháyhoàntoàn0,15molestethu được 19,8gam và0,45mol .Công thức phân tử 2CO 2 HO estelà
A. B. C. D. 5102CHO 362CHO 482CHO 242CHO Câu 5: Đốt cháyhoàntoàn0,1mol một esteX (chứa C,H,O) đơn chức, mạch hở cần dùng vừa đủ Vlít khí (ở đktc) thu được 6,72lítkhí (ở đktc) và3,6gam .Giá trị của Vlà 2O 2CO 2 HO
A. 26,88. B. 4,48. C. 6,72. D. 13,44. Câu 6: Đun nóng m gam etyl axetat trong dung dịch NaOH dư thu được 8,2 gam muối. Mặt khác, đốt cháyhoàntoàn lượng estetrên bằng dư thu được baonhiêumol ? 2O 2CO
DẠYKÈMQUYNHƠN OFFICIAL Trang33
A. 0,1mol. B. 0,2mol. C. 0,3mol. D. 0,4mol. Câu 7: Đun nóng este X đơn chức mạch hở với NaOH thu được muối và ancol. Đốt cháy hoàn toàn 0,1 molXthu được 8,96lít (đktc). Xkhôngcó phản ứng tráng gương. Công thức cấu tạo của Xlà 2CO
A. B. 2 2HCOOCHCHCH 3 2 2CHCOOCHCHCH C. . D. . 2 3CHCHCOOCH
3 2CHCOOCHCH
Câu 8: Đốt cháyhoàntoàn7,8gamesteXthu được 11,44gam và4,68gam .Công thức phân 2CO 2 HO tử của estelà
A. . B. . C. . D. . 484CHO 482CHO 242CHO 362CHO Câu 9: Đốt cháyhoàntoàn3,7gamesteno, đơn chức, mạch hở Xthu được 3,36lít (đktc). Số đồng 2CO phân cấu tạo của esteXlà
A. 1. B. 4. C. 3. D. 2. Câu 10: Đốt cháyhoàntoàn14,3gamesteX cần vừa đủ 18,2lít (đktc), thu được và có số 2O 2CO 2 HO mol bằng nhau.Cho14,3gamX phản ứng vừa đủ với Vmldung dịch NaOH0,5M.Giá trị của Vlà
A. 162,5. B. 487,5. C. 325,0. D. 650,0. Câu 11: Đốt cháyhoàntoàn2,2gamesteXthu được gồm 0,1mol và0,1mol . Mặt khác,cho 2CO 2 HO 2,2gamXtác dụng hết với dung dịch NaOH,thu được 2,4gam muối. Tên gọi của Xlà
A. etylpropionat. B. metylpropionat. C. isopropylaxetat. D. etylaxetat. Câu 12: Hỗn hợp X gồm etylaxetat,vinylaxetatvàmetylfomat. Thủy phân hoàntoàn20,0 gamX cần dùng vừa đủ 200 ml dung dịch NaOH 1,5M. Mặt khác đốt cháy hoàn toàn 20,0 gam X thu được V lít (đktc) và12,6gam .Giá trị của Vlà 2CO 2 HO
A. 14,56. B. 17,92. C. 16,80. D. 22,40. Câu 13: Hỗn hợp X gồm hai este no, đơn chức, mạch hở được tạo thành từ một axit và hai ancol đồng đẳng kế tiếp. Đốt cháyhoàntoàn9,7gamX,thu được 15,4gam . Phần trăm khối lượng estecóphân 2CO tử khối nhỏ hơn trongXlà
A. 38,14%. B. 61,86%. C. 62,99%. D. 37,01%. Câu 14: Đốt cháy hoàn toàn hỗn hợp gồm các este no, đơn chức, mạch hở. Hấp thụ toàn bộ sản phẩm cháyvàobình đựng dung dịch dư, thu được mgam kết tủa vàdung dịch sau phản ứng có khối 2 CaOH lượng giảm 1,33gamso với dung dịch ban đầu. Giá trị của mlà 2 CaOH A. 3,5. B. 2,8. C. 3,8. D. 4,2. Câu 15: Đốt cháyhoàntoàn3,08gam hỗn hợp X gồm vinylaxetat,metylaxetatvàetylfomat,thu được 2,16gam . Phần trăm số mol của vinylaxetattrongXlà 2 HO A. 25%. B. 72%. C. 28%. D. 75%. Câu 16: Đốt cháyhoàntoàn2,5gam hỗn hợp X gồm haieste cần vừa đủ 0,135mol ,thu được 2O 2CO và0,11mol . Mặt khác, nếu choXtác dụng với dung dịch NaOHthìthu được một muối và hỗn hợp 2 HO haiancol đồng đẳng kế tiếp. Công thức phân tử của haiestetrongXlà A. và . B. và . 242CHO362CHO 362CHO 462CHO C. và . D. và . 362CHO 482CHO 482CHO 5102CHO
DẠYKÈMQUYNHƠN
Trang34
OFFICIAL
Câu 17: Hỗn hợp X gồm một este no, đơn chức mạch hở và một este no, hai chức mạch hở. Đốt cháy hoàntoàn10,48gamX,thu được 16,28gam và5,4gam . Phần trăm khối lượng của este đơn 2CO 2 HO chức trongXlà
A. 21,18%. B. 48,00%. C. 19,80%. D. 39,60%. Câu 18: Hỗn hợp T gồm hai este mạch hở được tạo thành từ cùng một ancol đơn chức và hai axit cacboxylic no, đơn chức là đồng đẳng kế tiếp. Đốt cháy hoàn toàn 2,86 gam T cần vừa đủ 3,696 lít khí (đktc), thu được 1,98gam .Tên gọi của haiestetrongTlà 2O 2 HO
A. metylaxetatvàmetylpropionat. B. etylaxetatvàetylpropionat. C. metylacrylatvàmetylmetacrylat. D. anlylfomatvàanlylaxetat.
Câu 19: Hỗn hợp G gồm axit acrylic, axit metacrylic, vinyl axetat và metyl metacrylat. Đốt cháy hoàn toàn1,72gamG cần vừa đủ amolkhí ,thu được và3,52gam .Giá trị của alà 2O 2 HO 2CO
OFFICIAL
A. 0,09. B. 0,10. C. 0,08. D. 0,12. Câu 20: Hỗn hợp X gồm hai este là đồng phân cấu tạo. Đốt cháy hoàn toàn m gam X cần dùng 7,84 lít khí (đktc), thu được 13,2gam và5,4gam .Công thức cấu tạo haiestetrongXlà 2O 2CO 2 HO A. . B. . 3 2525 3CHCOOCH,CHCOOCH 33 2HCOOCHCHCH,CHCOOCHCH C. D. 253 3HCOOCH,CHCOOCH 2 22 3HCOOCHCHCH,CHCHCOOCH Câu 21: Đốt cháyhoàntoàn hỗn hợp X gồm một ancolvà một este (đều đơn chức, mạch hở) cần vừa đủ 3,808lítkhí (đktc), thu được 6,16gam và3,6gam .Têm gọi của estetrongXlà 2O 2CO 2 HO
A. metylfomat. B. vinylfomat. C. etylaxetat. D. metylacrylat. Câu 22: Hai este X và Y đều mạch hở, tạo bởi cùng một ancol và hai axit cacboxylic kế tiếp trong dãy đồng đẳng. Đốt cháy hoàn toàn m gam hỗn hợp gồm X và Y cần dùng 3,36 lít khí (đktc), thu được 2O 5,72gam và1,8gam .Công thức cấu tạo của Xlà 2CO 2 HO A. B. C. D. 3 3CHCOOCH 25HCOOCH 3 35CHCOOCH 23 3CHCOOCH
Câu 23: Đốt cháy hoàn toàn 12,3 gam hỗn hợp X gồm một ancol đơn chức và một este no, đơn chức, mạch hở, thu được 8,96lítkhí (đktc) và9,9gam . Mặt khác, đun nóng12,3gamX với 200ml 2CO 2 HO dung dịch NaOH1,2M rồi cô cạn dung dịch, thu được mgam chất rắn khan.Giá trị của mlà A. 8,5. B. 13,1. C. 16,4. D. 17,8. Câu 24: Đun nóng21,9gameste đơn chức X với lượng dư dung dịch NaOHthìcó tối đa 12gamNaOH phản ứng. Mặt khác, đốt cháyhoàntoànmgamXtrên cần dùng vừa đủ 42,56lít (đktc). Giá trị của m 2O là
A. 26,28. B. 43,80. C. 58,40. D. 29,20. Câu 25: Chomgam hỗn hợp X gồm hai chất hữu cơ no, đơn chức, mạch hở tác dụng vừa đủ với 100ml dung
DẠYKÈMQUYNHƠN
Trang35
tổng khối lượng và
2CO 2 HO A. và . B. và . 3 CHCOOH 3 25CHCOOCH 37 CHCOOH 3HCOOCH C. và . D. và . 25 CHCOOH25 3CHCOOCH HCOOH 25HCOOCH Bài tập nâng cao
dịch NaOH0,2M,thu được một muối và0,0075mol một ancol. Nếu đốt cháyhoàntoànmgamX thìthu được
là3,41gam. Hỗn hợp X gồm
Câu 26: Hỗn hợp X gồm baeste đơn chức, tạo thành từ ancolmetylic với baaxitcacboxylic;trong đó, có haiaxitnolà đồng đẳng kế tiếp nhauvà một axitkhôngno (chứa hailiên kết trongphân tử). Đốt cháy hoàntoàn5,6gamX,thu được 9,68gam và3,6gam . Phần trăm khối lượng của estekhôngno 2CO 2 HO
trongXlà
A. 35,71%. B. 38,76%. C. 30,71%. D. 46,07%.
Câu 27: Đốt cháyhoàntoànmgam một este cần 3,78lít (đktc). Dẫn toàn bộ sản phẩm cháyvàobình 2O đựng dung dịch ,thu được 7,5gam kết tủa vàdung dịch Ycó khối lượng tăng 1,125gamso với 2 CaOH dung dịch ban đầu. Đun nóngY,thuthêm3,75gam kết tủa nữa. Biết các phản ứng xảy rahoàn 2 CaOH toàn.Giá trị của mlà A. 3,225. B. 2,825. C. 2,450. D. 2,575. Câu 28: Đốt cháyhoàntoàn một este đơn chức mạch hở X(phân tử có số liên kết nhỏ hơn 3)thu được thể tíchkhí bằng 6/7 thể tíchkhí đã phản ứng (cáckhí đo ở cùng điều kiện). ChomgamXtác 2CO 2O dụng hoàn toàn với 200 ml dung dịch KOH 0,7M thu được dung dịch Y. Cô cạn Y thu được 12,88 gam chất rắn khan.Giá trị của mlà
OFFICIAL
A. 10,56. B. 7,20. C. 8,88. D. 6,66. Câu 29: ChoElàesteno,hai chức, mạch hở; Tlàeste đơn chức, mạch hở, chứa hailiên kết trongphân tử. Đốt cháyhoàntoàn0,1mol hỗn hợp gồm EvàT cần vừa đủ 0,42mol ,thu được và0,32mol 2O 2CO
Biết E được tạo thành từ axitcacboxylicvàancol. Số nguyên tử cacbontrongEvàT lần lượt là 2 HO
A. 5và3. B. 4và4. C. 4và5. D. 5và4. Câu 30: Hỗn hợp E gồm haieste đơn chức, là đồng phân cấu tạo của nhauvà đều chứa vòngbenzen. Đốt cháyhoàntoànmgamE cần vừa đủ 8,064lítkhí (đktc), thu được 14,08gam và2,88gam . 2O 2CO 2 HO Mặt khác,chomgamE phản ứng tối đa với dung dịch chứa 2,4gamNaOH,thu được dung dịch T chứa hai muối. Khối lượng muối của axitcacboxylictrongTlà
A. 1,64gam. B. 2,72gam. C. 3,28gam. D. 2,46gam. Dạng 6: Bài tập tổng hợp
Phương pháp giải Vận dụng linh hoạt định luật bảo toànnguyên tố, định luật bảo toàn khối lượng. Nên giải theo phương phápquy đổi: Quy về chất nhỏ nhất vànhóm . 2CH Ví dụ mẫu Ví dụ 1: Chocác chất hữu cơ mạch hở: Xlàaxitkhôngnocóhailiên kết trongphân tử, Ylàaxitno đơn chức, Zlàancolnohai chức,
DẠYKÈMQUYNHƠN
Trang36
X,Y với
vàT,thu được 0,1 mol và0,07mol .Cho6,9gamM phản ứng vừa đủ với dung dịch
2CO 2 HO cô
A.
Tlàeste của
Z. Đốt cháyhoàntoànagam hỗn hợp M gồm X
NaOH,
cạn dung dịch sau phản ứng thu được hỗn hợp muối khanE. Đốt cháyhoàntoànE,thu được ;23NaCO 0,195 mol và 0,135 mol . Phần trăm khối lượng của T trong M có giá trị gần nhất với giá trị 2CO 2 HO nàosau đây?
68,7. B. 68,1. C. 52,3. D. 51,3. Hướng dẫn giải
chức làeste của axitmetacrylicvàhaiestehai chức là đồng phân của nhau. Đốt cháyhoàntoàn12,22 gam E bằng , thu được 0,37 mol . Mặt khác, cho 0,36 mol E phản ứng vừa đủ với 234 ml dung 2O 2 HO dịch NaOH 2,5M, thu được hỗn hợp X gồm các muối của các axit cacboxylic không no, có cùng số nguyên tử cacbon trong phân tử; hai ancol không no, đơn chức có khối lượng gam và một ancol no, 1m đơn chức có khối lượng gam. Tỉ lệ cógiá trị gần nhất với giá trị nàosau đây? 2m 12m:m
DẠYKÈMQUYNHƠN OFFICIAL Trang37 Tacócácquátrình: 2 2 2 XT 2 O BTKL BTO ag 2 O n2n22 2 O NaOH 23 6,9g 2 m2m42 n2n0,03MXCO:0,1 a2,3gam THO:0,07 n0,105 CHO2:x ACOONa2 CO M E NaCO HO CHO3:y BCOONa1 Tacó: 2CO nnxmy0,3x0,03n3 xy0,06 y0,03m7 14.0,330x60y6,9nm10 23 23 24 3 X:CHCOOH T:CHCOOCHOOCCH68,7% Chọn A. ® Ví dụ 2: Hỗn hợp E gồm baeste mạch hở, đều có bốn liên kết pi trongphân tử, trong đó có một este đơn
A.
B.
C.
Hướng dẫn giải 12,22gamE gồm: 2 3 2 782 2 2 38104 2 CHCCHCOOCHCCHCHO,amol; CHCHCHOOCCHCHCOOCHCHO,bmol; vµCHcmol Tacó: 2 E HO m124a170b14c12,22gam124a170b14c12,22* n4a5bc0,37mol4a5bc0,37** Lại có:0,36molE cần 0,585molNaOH. E NaOH nab0,365a3b*** na2b0,585 Từ (*),(**)và(***)suyra (khôngcó ghépvào). a0,03;b0,05;c0 2CH Hỗn hợp E gồm: và 2 3 2 CHCCHCOOCHCCH0,03mol (hai đồng phânhình học của nhau, tổng 0,05mol). 2 2 3CHCHCHOOCCHCHCOOCH Tacó: gamhaiancollà (0,03mol)và (0,05mol). 1m 2 HCCCHOH 2 2 CHCHCHOH . 1 m4,58gam
2,7.
1,1.
4,7. D. 2,9.
Tacó: gam một ancolnolà0,05mol tương ứng . 2m 3 CHOH 2 m1,6gam Vậy 12 m:m4,58:1,62,8625
Chọn D. ® Bài tập tự luyện dạng 6 Bài tập nâng cao Câu 1: Cho X, Y là hai axit cacboxylic đơn chức ; T là este ba chức, mạch hở được tạo bởi XYMM X, Y với glixerol. Cho 23,06 gam hỗn hợp E gồm X, Y, T và glixerol (với số mol của X bằng 8 lần số mol của T)tác dụng vừa đủ với 200mldung dịch NaOH2M,thu được hỗn hợp F gồm hai muối có tỉ lệ mol1:3và3,68gamglixerol. Đốt cháyhoàntoànF cần vừa đủ 0,45mol ,thu được và 2O 232 NaCO,HO 0,4mol . Phần trăm khối lượng của TtrongEcógiá trị gần nhất với giá trị nàosau đây? 2CO A. 29. B. 35. C. 26. D. 25. Câu 2: Hỗn hợp E chứa ba este đều mạch hở, trong phân tử chỉ chứa một loại nhóm chức gồm este X ,esteY vàesteZ . Đun nóng0,4molE với dung dịch NaOH vừa x2x2CHO y2y22 CHO z2z24 CHO đủ, thu được 25,7gam hỗn hợp gồm baancolcùngdãy đồng đẳng và49,1gam hỗn hợp T gồm ba muối. Đốt cháytoàn bộ T cần dùng0,275mol ,thu được và0,49mol hỗn hợp gồm và . 2O 23NaCO 2CO 2 HO Phần trăm khối lượng của Ytrong hỗn hợp Elà
A. 8,35%. B. 9,47%. C. 7,87%. D. 8,94%. Câu 3: Hỗn hợp E gồm X,Ylàhaiaxit đồng đẳng kế tiếp; Z,Tlàhaieste (đều hai chức, mạch hở, Yvà Zlà đồng phân của nhau, ). Đốt cháyhoàntoàn12,84gamE cần vừa đủ 0,37mol ,thu TZ MM14 2O được và . Mặt khác, cho 12,84 gam E phản ứng vừa đủ với 220 ml dung dịch NaOH 1M. Cô 2CO 2 HO cạn dung dịch sau phản ứng thu được hỗn hợp muối khanG của cácaxitcacboxylicvà2,8gam hỗn hợp baancolcócùng số mol. Khối lượng muối của axitcóphân tử khối lớn nhất trongGlà
A. 3,24gam. B. 2,68gam. C. 6,48gam. D. 4,86gam. Câu 4: Hợp chất hữu cơ X (chứa C,H,O) chỉ có một loại nhóm chức. Cho0,15molX phản ứng vừa đủ với 180gamdung dịch NaOH,thu được dung dịch Y.Làmbay hơi Y, chỉ thu được 164,7gam hơi nước và 44,4 gam hỗn hợp chất rắn khan Z. Đốt cháy hoàn toàn Z, thu được 23,85 gam ; 56,1 gam 23NaCO và 14,85 gam . Mặt khác, Z phản ứng với dung dịch loãng (dư) thu được hai axit 2CO 2 HO 24HSO cacboxylic đơn chức và hợp chất T (chứa C,H,Ovà ). Số nguyên tử HtrongT bằng T M126 A. 8. B. 6. C. 12. D. 10. Câu 5: Hợp chất hữu cơ X chứa C, H, O thuộc loại hợp chất no, mạch hở và chứa hai loại nhóm chức (khôngcó chức ete). Thủy phânXtrongmôi trường axitvô cơ loãng,thu được ba chất hữu cơ Y,Z,T(Y và Z thuộc loại hợp chất đơn chức, có cùng số nguyên tử cacbon trong phân tử và đều tác dụng với Na giải phóng ). Nếu đốt cháyhoàntoànYthìthu được và có số mol bằng nhau. Nếu đốt cháy 2H 2CO 2 HO hoàntoànZthìthu được và có tỉ lệ mol tương ứng bằng 2:3.Cho0,52gamT phản ứng hết 2CO 2 HO với dung dịch dư trong , thu được 1,08 gam Ag và chất hữu cơ . Phát 3AgNO 3NH ET EMM50 biểu nàosau đây sai? A. Tổng số nguyên tử Ctrongcácphân tử X,Y,ZvàT bằng 14. B. Tỉ lệ số nguyên tử H giữa YvàT bằng 1:1.
DẠYKÈMQUYNHƠN
Trang38
OFFICIAL
C. Ở
nhiệt độ thường, chất Yhòatan được . 2 CuOH
D. Chất Tcó mạch cacbonphânnhánh. ĐÁP ÁN
Dạng 1: Lí thuyết trọng tâm
1 – C 2 – B 3 – A 4 – D 5 – A 6 – D 7 – A 8 – D 9 – C 10 – C 11 – C 12 – A 13 – D 14 – A 15 – C 16 – C 17 – A 18 – B 19 – C 20 – B 21 – D 22 – B 23 – A 24 – B 25 – B 26 – A 27 – B 28 – C 29 – A 30 – D
Câu 1: Đáp án C
Các chất thuộc loại estelà hợp chất hữu cơ cónhóm chức COO. Các chất thuộc estelà:(1),(2),(3),(5),(7).
Câu 8: Đáp án D
Nhiệt độ sôi của este<ancol<axitcócùng số nguyên tử C. Nhiệt độ sôi: . 3 337 25 CHCOOCHCHOHCHCOOH
Câu 10: Đáp án C
Có2công thức phù hợp là: và . 2 2
COOCH |COOCH
HCOOCH H|COOCH 3 3
HCOOCHCHCHCH HCOOCHCCH
CHCOOCHCHCH CHCOOCHCH
là . 2 CHCHCOONaX
DẠYKÈMQUYNHƠN
Trang39
OFFICIAL
C|H
Câu 11: Đáp án C Có4công thức thỏa mãnlà: 23 3 3 3 2 25 2
Câu 14: Đáp án A Ylà
2 3CHCHCOOCH
Câu 15: Đáp án C Có4công thức phù hợp là: ; ;; 25 25 COOCH | COOCH 2 3 2 3 CHCOOCH | CHCOOCH
3 32CHCHCOOCH 3 2 3 2 CHCOOCH | CHCOOCH Câu 16: Đáp án C Tacó: Xlàestekhôngno,có một liên kết đôi k2 CC Thủy phân a mol X, sản phẩm thu được tác dụng với trong , thu được 4a mol Ag Hai 3AgNO 3NH sản phẩm thủy phân đều tráng bạc Chỉ có thỏa mãn. 3HCOOCHCHCH Câu 17: Đáp án A
HCOOCHCCH
EsteX đơn chức phản ứng với NaOHtheo tỉ lệ 1:2 Xlàeste của phenol.
Có4công thức phù hợp là: (3 đồng phâno,m,p) 643 3 65
Câu 19: Đáp án C
HCOOCHCH CHCOOCH
Este bị thủy phântrongmôi trường axitvà kiềm nên phản ứng được với dung dịch NaOHvà . 2 HO
Este làestekhôngnonên phản ứng được với (xúctácNi, đun nóng). 2 3CHCHCOOCH 2H
Estekhông phản ứng được với kim loại Na.
Câu 20: Đáp án B
Cáceste phản ứng với dung dịch NaOH (đun nóng)sinhraancollà:etylfomat,metylbenzoat. Câu 21: Đáp án D
Estehai chức X được tạo thành từ axitcacboxylicZvàancolY,Zkhôngcó phản ứng tráng bạc nênXcó dạng 1 22RCOOR
Độ bất bãohòa .Trong đó có ở nhómCOOnên trong gốc hiđrocacbon. k3 2 1 Đun ancolY với đặc ở không tạo raankennênYlà . 24 HSO170C 3 CHOH Xlà Zlà . 3 3
CHCOOCH || CHCOOCH HOOCCHCHCOOH
DẠYKÈMQUYNHƠN
Trang40
OFFICIAL
Có2công thức phù hợp là: và 23HCOOCHCHCHCH 3 3C|H
Câu 18: Đáp án B
dụng với tạo dung dịch màuxanhlam Ylàancol đa chức cócácnhómOH liền kề. 2 CuOH Xlàestehai chức tạo bởi 2axitno(Z,T)và1ancolnohai chức (Y). Xcó thể là hoặc . 3 2 3 CHCOOCH | HCOOCHCH 2 3 3 HCOOCH | CHCOOCHCH Ylà ;TlàHCOONa;Zlà . 2 3CHCHCH || OHOH 3 CHCOONa A,C,D đúng.
AsaivìtrongXcó2nhóm .3CH BsaivìZcólàm mất màudung dịch bromtrong .4CCl CsaivìYlàancolmetylic. D đúng. Câu 22: Đáp án B Độ bất bãohòa: . X k2 Tacó: nênZlà CaOt 4ZNaOHCH
3 CHCOONa Ytác
BsaivìYcó mạch Ckhôngphânnhánh. Câu 23: Đáp án A Đun Z với dung dịch đặc, thu được đimetyl ete Zlà . 24HSO 3 CHOH TkhôngphânnhánhnênYlà muối của axitcacboxylic mạch khôngphânnhánh. YHCl Tacó: làestehai chức tạo bởi axitkhôngno(1liên kết đôi )và . X k3X CC 3 CHOH
đúng.
24: Đáp
phânhình học.
Ylà ;Zlà .
CHCOONa 2 CHCHCOONa
Asaivì muối khôngcó đồng phânhình học. 2 CHCHCOONa B đúng. Csaivìcó3công thức thỏa mãnXlà:
DẠYKÈMQUYNHƠN OFFICIAL Trang41
CHCOOCH || CHCOOCH
Xlà ;Ylà ;Tlà . 3 3
CHCOONa || CHCOONa CHCOOH || CHCOOH
CHCOOCHCOOCHOH
; ; 3 2 2 2 CHCOOCH | CHCHCOOCH C|HOH 2 2 3 2 CHCHCOOCH C|HCOOCH C|HOH 2 2 3 2 CHCHCOOCH | CHOH C| HCOOCH
X
chức tạo
X k3X CC Xlà 3 35 HCOOCHCHCHCOOCHOH Ylà ;Zlà . HCOONa 3 CHCHCHCOONa
thức thỏa
; ; 2 3 2 HCOOCH | CHCHCHCOOCH C|HOH 3 2 2 CHCHCHCOOCH H|COOCH C|HOH 3 2 2 CHCHCHCOOCH C|HOH H|COOCH
chứa hai loại nhóm
. Z
AsaivìTcó đồng
B,C,D
Câu
án B Y,Zkhôngcó phản ứng tráng bạc Y,Zcó dạng . RCOONaRH làestehai chức tạo bởi glixerolvà1axitno+1axitkhôngno(có1liên kết đôi ). X k3X CC Xlà .
3 23 35
3
Dsaivìphân tử
chứa hai loại nhóm chức làestevàancol. Câu 25: Đáp án B làestehai
bởi glixerolvà1axitno+1axitkhôngno(có1liên kết đôi ).
Asaivìcó3công
mãnXlà:
B đúng. CsaivìX
chức làestevàancol. Dsaivì
M108
Câu 26: Đáp án A
làestehai chức chứa vòngbenzen. X k6X 2 XNaOHd2molY1molZ1molHO
Ylà muối cacboxylat;Z thuộc dãy đồng đẳng phenol. Xlà ;YlàHCOONa;Zlà ;Tlà . 64 2
HCOOCH | HCOOCH 642 NaOCHCHOH 642 HOCHCHOH
AsaivìT phản ứng với NaOHtheo tỉ lệ 1:1. B,C,D đúng. Câu 27: Đáp án B làestehai chức no tạo bởi (cónhóm chức axit)vàancol . X k2X 12X,X 3X Xlà . 2 3HCOOCHCOOCH có thể làHCOONa, 12X,X 2 33 HOCHCOONa;XlµCHOH . 45 2 6 X,XcãthÓlµHCOOH,HOCHCOOH;XlµHCHO
Asaivì khônghòatan được . 3 CHOH 2 CuOH
B đúng. Csai hoặc có thể có3oxi. 4X 5X
Dsaivì bị khử bởi tạo ra . 6X 2H 3X
Câu 28: Đáp án C cócùng số nguyên tử cacbon cócùng số nguyên tử cacbon. 345X,X,X 312X,X,X
làestehai chức no tạo bởi (cónhóm chức axit)vàancol . X k2X 12X,X 3X Xlàcó thể là . 3 2 25CHCOOCHCOOCH có thể là . 12X,X 3 2 325 CHCOONa,HOCHCOONa;XlµCHOH 45 3 2 33 X,XcãthÓlµCHCOOH,HOCHCOOH;XlµCHCHO
đúng.
bị oxihóa bởi thu
DẠYKÈMQUYNHƠN
Trang42
OFFICIAL
X
3
T
ứng với
Ycó
tạo
Xlà ;Ylà ;Tlà
2 32CHCCOOCH 2 2 CHCCOONa
A,B,D
Csaivì
được kết tủa Ag. 6X 33AgNO/NH Câu 29: Đáp án A Zlà . 3 CHOH làestehai chức tạo bởi vàaxitYkhôngno (chứa 1liên kết đôi ).
k3X
CHOH CC
phản
HBr, thu được hai sản phẩm là đồng phần cấu tạo của nhau T có cấu tạo không đối xứng.
cấu
không đối xứng.
.
2 2 CHCCOOH
A đúng.
BsaivìX phản ứng với theo tỉ lệ 1:1. 2 HNi,t Csaivìcông thức phân tử của Ylà .4242 CHONa
Dsaivì khônglàm mất màu nước brom. 3 ZCHOH
Câu 30: Đáp án D Ở hai ống nghiệm đều xảy ra phản ứng thủy phân . 3 25CHCOOCH Ống thứ nhất: . 24 HSO,t 3 252 3 25 CHCOOCHHOCHCOOHCHOH Ống thứ hai: . t 3 25 3 25 CHCOOCHNaOHCHCOONaCHOH
(a) đúng vìestekhôngtantrong vàNaOHnên ở hai ống nghiệm đều phânthànhhai lớp. 24HSO (b)sai. (c)saivì ống thứ nhất thu được axitvàancol, ống thứ haithu được muối vàancol. (d) đúng. Có2phát biểu đúng.
DẠYKÈMQUYNHƠN
Trang43
OFFICIAL
1 – D 2 – D 3 – B 4 – B 5 – D 6 – D 7 – B 8 – B 9 – D 10 – D 11 – B 12 – A 13 – D 14 – A 15 – D 16 – B 17 – D 18 – C 19
D 20
B Câu 3: Đáp án B 33 25CHCOOCHHCOOCH hh KOHhh KOH MM74n0,2mol 0,2nn0,2molV 0,2lÝt200ml 1 Câu 4: Đáp án B NaOH n0,2mol Phương trìnhhóa học: 3 3 3 3 3 3 CHCOOCHNaOHCHCOONaCHOH HCOOCHNaOHHCOONaCHOH Tacó: . 3 CHOHNaOH 2 nn0,2molm0,2.326,4gam Câu 5: Đáp án D NaOH n0,15mol Esteno, đơn chức, mạch hở: esteNaOH este nn0,15molM116 Gọi công thức phân tử của estelà . n2n2 11632CHOn2n 6 14 Vậy estecócông thức phân tử là: .6122CHO Câu 6: Đáp án D 325 CHCOOCH NaOH n0,15mol;n0,06mol Ta thấy: hết, dư, chất rắn là muối . 325 CHCOOCHNaOH nnNaOH 3 25CHCOOCH 3 CHCOONa
Dạng 2: Phản ứng thủy phân thông thường
–
–
Tacó: 3 3
nn0,06mol m82.n82.0,064,92gam
CHCOONaNaOH chÊtr¾nkhan CHCOONa
Câu 7: Đáp án B X n0,1mol Esteno, đơn chức, mạch hở loại C. X k1
Bảo toàn khối lượng: XNaOHchÊtr¾nancolancol mmmmm3,2gam
Tacó: Ancollà . ancolX ancol nn0,1molM32 3 CHOH Công thức cấu tạo của Xlà . 25 3CHCOOCH
Câu 8: Đáp án B
Bảo toàn khối lượng: XNaOHmuoiancolNaOH mmmmn0,5mol Este đơn chức: ancolhhmuèiX nnn0,5mol Ancollà . ancol M32 3 CHOH Hai muối là và . hhmuèi M90,4 3 CHCOONa25 CHCOONa
Vậy công thức của haiestelà và . 3 3CHCOOCH 25 3CHCOOCH
HCOOCH | CHCOOCH KOH X n n0,0625mol 2
m0,06251328,25gam
Trang44
DẠYKÈMQUYNHƠN OFFICIAL
X
Câu 9: Đáp án D Este đơn chức XNaOH X 482nn0,15molM88CHO Công thức của haiestelà và . 25 3CHCOOCH 3 25CHCOOCH Câu 10: Đáp án D Xlà với . 2 3 2 tạo của Xlà . 3 25CHCOOCH Câu 12: Đáp án A 1 muối +1ancol Xlàaxit,Ylàeste tạo bởi axitXvàancol đơn chức. X,YNaOH Xét phản ứng đốt cháyancol: 2 2 CO HO n0,2mol;n0,3mol Nhận thấy Ancolno, đơn chức, mạch hở. 2 2 COHOnn Tacó: Ancollà . 2 2ancolHOCO nnn0,1molSèC2 25 CHOH
Câu 11: Đáp án B Dựa vào đáp án,Xlàesteno, đơn chức, mạch hở. Tacó: Công thức phân tử của Xlà . 2XO
nn0,025molM88
482CHO Xét phản ứng thủy phân: .
muèiX muèi 3 nn0,25molM82CHCOONa
Vậy công thức cấu
Xét phản ứng . muèiNaOH muèi 3 X,YNaOH:nn0,3molM82CHCOONa
Ylà . 3 25CHCOOCH Câu 13: Đáp án D Tacó làestehai chức. NaOH X n0,062X n0,03 Doancolthu được axit đa chức vàancol đơn chức nênAkhông thỏa mãn. Tacó: . ancolNaOH muèi nn0,06mol;n0,03mol
M32AncollµCHOH. M148MuèilµCHCOONa
ancol 3 muèi 2 2
Vậy công thức của Xlà . 3 2 3CHOOCCHCOOCH Câu 14: Đáp án A este n0,05mol Estecó dạng esteno, đơn chức, mạch hở . n2n2CHO Yeste nn0,05mol
Nhận thấy: Zlàete. Z/Y d1,7 Sơ đồ phản ứng: 2 2YEteZHO Tacó: . 2 ZHOY 1 nnn0,025mol 2 Bảo toàn khối lượng: . 2 YZHO Y Y Y mmm0,05M0,0251,7M0,02518M60 .m0,05603gam
Câu 15: Đáp án D Nhận thấy: Ancolno, đơn chức, mạch hở. 2 2 COHOnn Tacó Ancollà . 2 2ancolHOCO nnn0,1molSèC2 25 CHOH Công thức cấu tạo của Xlà . 25 ancol HOOCCOOCHan0,1mol
DẠYKÈMQUYNHƠN OFFICIAL Trang45
Muối thu được là . 2 COOK:0,1molm0,116616,6gam Câu 16: Đáp án B Estecó dạng Esteno, đơn chức, mạch hở n2n2CHO Yeste nn0,125mol Xét phản ứng tạo ete: 2 2YEteHO Tacó: . 2 HOY 1 nn0,0625mol 2 Bảo toàn khối lượng: . 2 YeteHOY mmmm3,5750,0625.184,7gam Xét phản ứng thủy phân: . NaOHeste nn0,125mol Bảo toàn khối lượng: esteNaOHYZZ mmmmm9,250,125404,79,55gam
Câu 17: Đáp án D Gọi công thức của XlàRCOOR’. KOH n0,3mol Tacó: . X X M25.4100n0,2mol
Ta thấy Este hết, KOH dư. XKOHX nn2n Trong phản ứng: . KOHpmuèieste KOHd nnn0,2moln0,30,20,1mol
Công thức của estelà . 25 2CHCOOCHCH
DẠYKÈMQUYNHƠN OFFICIAL Trang46
Tacó: . chÊtr¾nmuèiKOHdmuèi mmmm280,1.5622,4gam
RCOOK R 25 R' 23M22,4112M29CHM100294427CH 0,2
Câu
este
trình: .xy0,1x0,025 68x82x7,85y0,075 Haiestelà (0,025mol)và (0,075mol). 37HCOOCH 3 25CHCOOCH 37 325 HCOOCH CHCOOCH 0,02588%m 100%25% 8,8 %m100%25%75% Câu 19: Đáp án D Xét phản ứng đốt cháyX: . ancol n0,480,320,16mol Nhận thấy X gồm một ancol đơn chức (A)và một ancolhai chức (B). 2 CONaOHnn AB A AB B nn0,16n0,06mol n2n0,26n0,1mol Tacó: Số .Cx2 Nếu X gồm (0,06mol)và (0,1mol). 3 CHOH 2 ROH Số Ctrong bằng: (không thỏa mãn). 2 ROH0,320,0612,6 0,1 X gồm (0,06mol)và (0,1mol). 25 CHOH 242CHOH Xét phản ứng : ENaOH
18: Đáp án C Bảo toàn khối lượng: estemuèiancolNaOH mmmm8,8gam
Este đơn chức nêntacó: estemuèiancolNaOH
nnnn0,1molM88
Công thức phân tử của haiesteXvàY đều là .
482CHO Tacó: . muèi M7,8578,5 0,1
Hai muối của haiaxit đồng đẳng kế tiếp làHCOONa(xmol)và (ymol).
3 CHCOONa Tacó hệ phương
DoY chứa hai muối nêncó2 trường hợp: TH1: không thỏa mãn. 2312 1 2 115 RR3R10R125R;R1 3
TH2: thỏa mãn. 1213 1 33 RR8R5R125R15CH;R1H
Chất lỏng Z gồm R’OHvà nên: . 2 HO ancol m42,4366,4gam
0,06R730,1RR11618,48 3R5R5R125 24CH m0,15284,2gam Dạng 3: Phản ứng este hóa 1 – D 2 – A 3 – C 4 – A 5 – B 6 – C 7 – B 8 – A 9 – C 10 - C Câu 3: Đáp án C Tacó: Hiệu suất phản ứng tínhtheoaxit. 3 65 CHCOOH CHOH m m n n 60 46 Hmm8:100%68,18% 860 Câu 6: Đáp án C 3 325 CHCOOH CHCOOCH n0,075mol;n0,039mol Nhận thấy: Hiệu suất tínhtheoancol. 3 3 CHCOOHlt CHCOOHtt 0,039 n 00,06n0,075 ,65
DẠYKÈMQUYNHƠN OFFICIAL Trang47
Y gồm HCOONa(0,1mol)và (0,16mol). 3 CHCOONa . 3 CHCOONa m0,168213,12gam Câu 20: Đáp án B 2 2 NaOH HO H n0,35mol;n2mol;n1,1mol Phương
R'OH
DoE gồm cáceste mạch hở nênY gồm hai muối của axit đơn chức. E gồm 1 25 2 24 3 RCOOCH0,06molvµRCOOCHOOCR0,1mol Tacó: 1 23 123 gồm ,NaOH dư . 2 CHCHCOONa0,2mol 0,350,20,15mol Phương trìnhhóa học: t,CaO 2 2223 CHCHCOONaNaOHCHCHNaCO 0,20,15 0,15 mol
trìnhhóa học: RCOOR'NaOHRCOONaR'OH
Tacó: . 2 2 R'OHHOHR'OH
R' 3nn2nn2.1,120,2molM32M15CH
Alàeste đơn chức nên . Aancol A 23nn0,2molM86R86441527CH
Vậy Acócông thức . 2 3CHCHCOOCH
Chất rắn Ythu được
M4,560 0,075 MM16
nn.80%0,04mol H80% nn.80%0,04mol
DẠYKÈMQUYNHƠN OFFICIAL Trang48
đ RCOOR' RR'
. 25 25 CHOH CHOH n0,06molm2,76gam
Câu 8: Đáp án A Gọi công thức của XvàY lần lượt mmmm0,04.740,04.886,48gam Câu 10: Đáp án C Gọi số mol và ở mỗi phần lần lượt làx,ymol. 3 CHCOOH25 CHOH 60x46y5,76* Cho phần một tác dụng với Na dư: . 2H n0,055mol Theo phương trình: . 3 25 2CHCOOHCHOHH nn2n2.0,0550,11mol xy0,11** Từ (*)và(**)suyra: .x0,05;y0,06 Đun phần hai với đặc: 24HSO Ta thấy: Hiệu suất tínhtheo . 3 25 CHCOOHCHOHnn 3 CHCOOH Tacó: . 325 CHCOOCH H80%n0,0580%0,04mol . 325 CHCOOCH mm0,04883,52gam
làRCOOHvàR’OH.
Ta thấy: Hiệu suất phản ứng tínhtheoX. XYnn Do Xp H75%n0,175%0,075mol Phương trìnhhóa học: 24 HSO,Æ c 2 t RCOOHR'OH RCOOR'HO 0,075 0,075mol
RlàHvàR’là Công thức của estelà (metylfomat).
3CH 3HCOOCH Câu 9: Đáp án C 25 CHOH 5,75 n40,125mol 6
Gọi số mol của HCOOHvà làx(mol). 3 CHCOOH Tacó: . 3 XHCOOHCHCOOH mmm46x60x5,3x0,05mol Vì số molancol lớn hơn số molaxitnêntính khối lượng
estetheo số mol của axit. Tacó: 25 325 3
HCOOCHHCOOH CHCOOCHCHCOOH
. 25 325 esteHCOOCHCHCOOCH
Dạng 4: Phản ứng thủy phân của este đặc biệt 1 – B 2 – A 3 – D 4 – D 5 – D 6 – A 7 – A 8 – A 9 – B 10 - C Câu 1: Đáp án B 3 2CHCOOCHCHn 0,1mol
DẠYKÈMQUYNHƠN OFFICIAL Trang49
Nhận
este hết, NaOH dư,
12 Theo
. 2
Bảo toàn khối lượng: 2 chÊtr¾nkhanesteKOHHO mmmm13,60,25400,11821,8gam Câu 4: Đáp án D Ag n0,12mol X phản ứng với dung dịch trong thu được AgnênXcó dạng HCOOR’. 3AgNO 3NH Tacó: . HCOOR'Ag HCOOR' R' 35 1 5,16nn0,06molM 86M41CH 2 0,06 Vậy công thức cấu tạo có thể có của Xlà: 3 2 2 3 2HCOOCHCHCH;HCOOCHCHCH;HCOOCCHCH
Sơ đồ phản ứng: 33AgNO/NH OH,t 3 2 3 CHCOOHCH CHCHO 2Ag 0,1 0,2mol . Ag m0,210821,6gam Câu 2: Đáp án A . vinylfomat n0,2mol Phương trìnhhóa học: 2 3 HCOOCHCHNaOHHCOONaCHCHO 0,2 0,20,2mol KhichoXtác dụng với :33AgNO/NH 3 HCOONa2Ag 0,20,4mol CHCHO2Ag 0,20,4mol . Ag m0,8.10886,4gam Câu 3: Đáp án D Tacó: . 365 CHCOOCH NaOH n0,1mol;n0,25mol Phương trìnhhóa học: 3 65 3 65 2 CHCOOCH2NaOHCHCOOKCHOKHO 0,10,25 mol
thấy:
tínhtoántheo số moleste. 0,10,25
phương trình:
HOeste nn0,1mol
DẠYKÈMQUYNHƠN OFFICIAL Trang50
Câu
hh NaOH
ứng
NaOH hh 1n2 n
265
HCOOCHCH2NaOHHCOONaCHCHONaHO x 2xxx mol HCOOCHCHNaOHHCOONaCHCHOH y yy mol Tacó hệ phương trình: .xy0,03x0,01 2xy0,04y0,02 364 muèiHCOONaCHCHONa mmm3,34gam Câu 7: Đáp án A Quy đổi hỗn hợp X gồm hai este có công thức là và (etyl phenyl oxalat được 1 RCOOR'2 65RCOOCH quy đổi thànhhaieste đơn chức có dạng như trên). Phương trìnhhóa học: 1 1 2 65 2 65 2 RCOOR'NaOHRCOONaR'OH1 RCOOCH2NaOHRCOONaCHONaHO2 Y gồm cácancol đơn chức 2R'OHH NaOH1 2,24 n2n.20,2moln0,2mol 22,4 2 NaOHbNaOH2 NaOH1 HO2NaOH2 11 nnn0,40,20,2molnn0,20,1mol 22 đ Bảo toàn khối lượng có: 2 XNaOHmuoiancolHO mmmmm m36,90,44010,90,11840,2gam
Câu 5: Đáp án D 325 365 CHCOOCHCHCOOCH NaOH nn0,02mol;n0,10,80,08mol
Ta thấy: NaOH dư, este hết. 325 365 NaOHCHCOOCHCHCOOCH nn2n Phương trìnhhóa học:
3 25 3 25 3 65 3 65 2 CHCOOCHNaOHCHCOONaCHOH1 0,02 0,02mol CHCOOCH2NaOHCHCOONaCHONaHO2 0,02 0,02mol
Bảo toàn khối lượng: .
25 2 chÊtr¾nkhanesteNaOHCHOHHO mmmmm4,480,08.400,02.460,02.186,4gam
6: Đáp án A
n0,03mol;n0,04mol
Khi cho hỗn hợp hai este X và Y phản ứng vừa đủ với dung dịch NaOH thu được dung dịch Z chứa ba chất hữu cơ và X,Ykhông thể cùng phản
với NaOHtheo tỉ lệ mol1:2vàX,Ycó
cùng gốc axit. Công thức phân tử của haiesteXvàYlà (xmol)và (ymol). 643HCOOCHCH 265HCOOCHCH Phương trìnhhóa học: 643 364 2
652
Câu 9: Đáp án B
TH3: X có dạng phản ứng với NaOH thu được muối HCOONa và anđehit HCOOCHCHR'
A đúng vìXcó đồng phânhình học cis–trans. BsaivìXkhông thể điều chế bằng phản ứng estehóa giữa axitfomicvàancolanlylic. C đúng vìXcóliên kết nênlàm mất màudung dịch nước brom. CC D đúng vìcông thức phân tử của Xlà ,trongphân tử có6nguyên tử hiđro.
DẠYKÈMQUYNHƠN OFFICIAL Trang51
XY X
XY Y
.
Tacó: . HCOOR'HCOONaAg HCOOR' 1 nnn0,24molM43Lo¹i 2 TH2: X có dạng phản ứng với NaOH thu được muối RCOONa và anđehit RCOOCHCHR' . 2 R'CHCHO
Câu 8: Đáp án A X hoặc Ylàeste của phenol. Giả sử Ylàeste của phenol. XY NaOHn0,05moln
Mặt khác,Z chứa ba muối Công thức haiestelà và .
265 HCOOCHCHX 3 65 CHCOOCHY Tacó: . 3
CHCOONa
nn0,05n0,04m0,01820,82gamn2n0,06n0,01
Ag n0,48mol
TH1:Xcó dạng HCOOR’ phản ứng với NaOHthu được muối HCOONavàancolR’OH.
Tacó: . 2 RCOOCHCHR'R'CHCHOAg RCOOCHCHR' 1 n nn0,24molM 43Lo¹i 2
. 2 R'CHCHO Tacó: . RCOOCHCHR'Ag RCOOCHCHR' 1 n n0,12molM 86 4
Vậy Xlà .3HCOOCHCHCH
Câu 10: Đáp án C Gọi số molcáceste của phenolvàcáceste
NaOH n2ab0,21 Vìcáceste đều đơn chức nên . 2 ancolestecñaancol H nnbmoln0,5bmol Tacó: . 2 binhtngancolHancol mmmm6,9bgam Lại có: . 2 HOestecñaphenol nnamol Bảo toàn khối lượng: 2 ENaOHancolmuèiHO mmmmm136ab0,2406,9b20,518a2 Từ (1)và(2)suyra . a0,05mol;b0,1mol m0,10,0513620,4gam Dạng 5: Phản ứng đốt cháy
462CHO
của ancoltrong hỗn hợp E lần lượt làavàbmol.
Câu 1: Đáp án B
Esteno, đơn chức, mạch hở: 2 2 COHO 4,4 ynn0,1mol 44
Câu 2: Đáp án B . 2 2 O CO n1,35mol;n1,1mol
Haiesteno, đơn chức, mạch hở nên: 2 2 COHO nn1,1mol Bảo toàn khối lượng: 2 2 2COHOO mmmm25gam
Câu 3: Đáp án C Hỗn hợp ba chất đều có dạng: . 2 2 n2n2COHO CHOnn0,8mol . 2CO mm0,8.4435,2gam
Câu 4: Đáp án B Esteno, đơn chức, mạch hở . 2 2 COHO nn0,45mol n2n2 CHOn2
DẠYKÈMQUYNHƠN OFFICIAL Trang52
–
–
–
– C
1– B 2 – B 3 – C 4 – B 5
C 6
D 7 – C 8 – C 9
D 10
11 – B 12 – C 13 – B 14 – A 15 – A 16 – C 17 – A 18 – D 19 – A 20 – C 21 – A 22 – D 23 – B 24 – D 25 – A 26 – C 27 – A 28 – C 29 – A 30 - B
X
Bảo toànnguyên tố O: . 2 2 2 2OCOHOOOX n2n2nnn0,3mol .V0,322,46,72lÝ t Câu 6: Đáp án D . 3 325 CHCOONa CHCOOCH n0,1moln0,1mol Bảo toànnguyên tố C: 2 482COCHO n4n0,4mol Câu 7: Đáp án C Thủy phânXthu được muối vàancol Loại D. Xkhôngcó phản ứng tráng gương Loại A. Số Xlà . C0,44 0,1 2 3CHCHCOOCH
Số nguyên tử C0,453 0,15
Công thức phân tử estelà . 362CHO Câu 5: Đáp án C 2 2 CO HO n0,3mol;n0,2mol
EsteX đơn chức nên .
OX n2n0,2mol
Câu 8: Đáp án C
làesteno, đơn chức, mạch hở 2 2 CO HO n0,26mol;n0,26molX n2n2 CHOn2
Bảo toàn khối lượng: 2 2 2 2 OCOHOX O mmmm11,444,687,88,32gamn0,26mol
Bảo toànnguyên tố O: . X OX OX 1 n0,2620,260,2620,26molnn0,13mol 2 Công thức phân tử của Xlà . X M7,860 0,13 242CHO Câu 9: Đáp án D 2CO n0,15mol Gọi công thức phân tử của Xlà .n2n2 CHOn2 . X 3,7 n 14n32
Bảo toànnguyên tố C: 2 COX 3,7 nnnn10,15n3 4n32
Vậy công thức phân tử của Xlà .362CHO Có2 đồng phân cấu tạo là . 253 3HCOOCH;CHCOOCH
Câu 10: Đáp án C 2O n0,8125mol
Gọi số mol và số mol bằng xmol. 2CO 2 HO
toàn khối lượng:
62x14,30,81253240,3x0,65mol
DẠYKÈMQUYNHƠN OFFICIAL Trang53
1 0,1625
0,325lÝ
0,5 Câu 11: Đáp án B Xlàesteno, đơn chức, mạch hở 2 2 COHO nn0,1mol n2n2 CHOn2 Bảo toàn khối lượng: 2 2 2 2 OCOHOX O mmmm4gamn0,125mol Bảo toànnguyên tố O: 2 2 2COHOOOX n2nn2n0,05mol Tacó Xmuèi X muèi OX 1 nnn0,025molM88;M96 2 Muối là Xlà :metylpropionat. 25 CHCOONa 25 3CHCOOCH Câu 12: Đáp án C 2 NaOH HO n0,3mol;n0,7mol
Bảo
.
Bảo toànnguyên tố O: . 2 2 2COHOOOX n2nn2n0,325mol Tacó:
NaOHCOOOX
nnn0,1625molV
t325ml 2
DẠYKÈMQUYNHƠN OFFICIAL Trang54 Khi
. COONaOH COOOX
2
Bảo
X
Bảo
2 2 CO CO CX 9
12 Câu
B Gọi công thức của haiestelà 2CO n0,35mol n2 2n CHOn2 Bảo
tố C: . 2CO X X n0,35 n M27,7n14n3227,7nn2,34 nn Haiestelà (amol)và
3HCOOCH 25HCOOCH Tacó: . 3HCOOCH 60a74b9,7a0,1%0,160 m 100%61,86%
9,7 Câu
A Cácesteno,
chức, mạch hở Saukhi đốt thu được: 2 2 2 COHO CO nnxmolnnxmol Tacó: . 2 2 dungdÞchgi¶m COHO m mmm1,33100x62x1,33x0,035mol
Câu
. 2 HO
X
. 3 234623 3362 25362 CHCOOCHCHO;CHCOOCHCHO;HCOOCHCHO Coi
X gồm (xmol)và (ymol). 462CHO 362CHO 86x74y3,08* Bảo toànnguyên tố H: 2 462 362HOCHOCHO n3n3n0,12xy0,04** Từ (*)và(**)suyra: .x0,01;y0,03 . vinylaxetat %0,01 n .100%25% 0,04 Câu 16: Đáp án C Bảo toàn khối lượng: . 2 2 2 2 COXOHO CO mmmm4,84gamn0,11mol Nhận thấy Esteno, đơn chức, mạch hở Loại B. 2 2 COHOnn n2n2CHO Bảo toànnguyên tố O: 2 2 2COHOO X OX OX 1 n2nn2n0,06molnn0,03mol 2 Số Công thức phân tử của haiestelà và . C0,113,67 0,03 362CHO 482CHO
thủy phânXtrongNaOH:
nn0,3moln2n0,6mol
Bảo toànnguyên tố H: .
HOHX n2n1,4mol
toàn khối lượng: .
CX OXHX mmmm200,6.161,4.19gam
toànnguyên tố C: .
nn0,75molVV16,8lÝ t
13: Đáp án
toànnguyên
(bmol).
2a3b0,35b0,05
14: Đáp án
đơn
m0,0351003,5gam
15: Đáp án A
n0,12mol
Hỗn hợp
gồm
hỗn hợp
Câu 17: Đáp án A 2 2 CO HO n0,37mol;n0,3mol Tacó: . 2 2 este2chøcCOHO nnn0,07mol
Bảo toàn khối lượng: 2 2 2 2 OCOHOX O mmmm11,2gamn0,35mol Bảo toànnguyên tố O: 2 2 2COHOO este®¬nchøc OX 0,340,074n2nn2n0,34moln 20,03mol
Gọi X gồm (0,03mol)và (0,07mol). n2n2CHO m2m24 CHO Tacó: thỏa mãn. 0,03n0,07m0,373n7m37n3;m4 Haiestelà (0,03mol)và .
Nhận thấy Tkhông gồm cácesteno Loại A,B. 2 2 COHOnn
T được tạo thành từ ancolvàaxitcacboxylicno, đơn chức Loại C. Câu 19: Đáp án A Nhận thấy: các chất trongG đều có Gọi công thức chung của hỗn hợp Glà k2 n2n22 CHO Phương trìnhhóa học: . t n2n22 2 2 2 3n1 CHOOnCOn1HO 2
DẠYKÈMQUYNHƠN OFFICIAL Trang55
362
362CHO %0,0374 m1100%21,18% 0,48 Câu
2 2 HO O
Bảo
2 2 2 2
CO
2 2HOO 22a nnmol 33 Bảo
lượng: . 2 2 2 GOCOHO 2a mmmm1,7232a3,52.18a0,09mol 3 Câu 20:
án C 2 2 2 CO HO O n0,3mol;n0,3mol;n0,35mol Nhận thấy: X gồm esteno, đơn chức, mạch hở Loại B,D. 2 2 COHOnn n2n2CHO Bảo toànnguyên tố O: 2 2 2COHOO X OX OX 1 n2nn2n0,2molnn0,1mol 2 Số Công thức phân tử của Xlà . X C0,33 0,1 362CHO Công thức cấu tạo của Xlà và . 25HCOOCH 3 3CHCOOCH Câu 21: Đáp án A
CHO
464 CHO0,07mol
18: Đáp án D
n0,11mol;n0,165mol
toàn khối lượng:
COXOHO
mmmm6,16gamn0,14mol
toàn khối
Đáp
n0,14mol;n0,2mol;n0,17mol
2 2 2 CO HO O
Nhận thấy X gồm ancolno, đơn chức, mạch hở (amol)vàeste 2 2 COHOnn n2n22 CHO
Bảo toànnguyên tố O: 2 2 2COHOOOX n2nn2n0,14mola2b0,l41
Bảo toànnguyên tố C: namb0,142
Từ (1)và(2)suyra: X gồm và (metylfomat). n1;m2 3 CHOH 3HCOOCH
Câu 22: Đáp án D 2 2 2 CO HO O n0,13mol;n0,1mol;n0,15mol
DẠYKÈMQUYNHƠN OFFICIAL Trang56
m2m22k2 CHO (bmol).
2 2 2
X OX OX 1
2
Xcó4CvàYcó5C
2
2 2
Bảo
2 2 2 2
Bảo
2 2 2COHOO este OX 0,40,15n2nn2n0,4moln20,125mol Gọi số Ccótrongancolvàeste lần lượt làuvàv. Ta có: thỏa mãn Ancol là , este là 0,15u0,125v0,4u1;v2 3 CHOH 3 HCOOCH0,125mol Xét : Chất rắn khan gồm HCOONa(0,125mol)vàNaOH dư XNaOH 0,240,1250,115mol m0,125680,1154013,1gam Câu 24: Đáp án D 2 NaOH O n0,3mol;n1,9mol TH1:X phản ứng với NaOHtheo tỉ lệ 1:1 (không thỏa mãn). XNaOH X nn0,3molM73 TH2:X phản ứng với NaOHtheo tỉ lệ 1:2 là . XNaOH X 1 nn0,15molM146X 2 962CHO Phương trìnhhóa học: t 962 2 22 CHO9,5O9CO3HO 0,21,9 mol
Nhận thấy: X,Ylàcácestekhôngno Loại A,B. 2 2 COHOnn Theo đáp án,XvàY đều làeste đơn chức. Bảo toànnguyên tố O:
COHOO
n2nn2n0,06molnn0,03mol
Số
Loại C. C0,134,33 0,03
Câu 23: Đáp án B
2 CO HO NaOH n0,4mol;n0,55mol;n0,24mol
Tacó:
ancolHOCO nnn0,15mol
toàn khối lượng:
OCOHOX O mmmm15,2gamn0,475mol
toànnguyên tố O:
Câu 25: Đáp án A NaOH n0,02mol
Xtác dụng với NaOH X gồm 1axitvà1estevà . ancol n0,0075mol
DẠYKÈMQUYNHƠN OFFICIAL Trang57
este
Haiestenolà ;estekhôngnolà
33 3HCOOCH;CHCOOCH
2 3CHCHCOOCH 0,0286 %m 5100%30,71% ,6 Câu 27: Đáp án A Xét phản ứng sản phẩm cháy+ : 2 CaOH 2 3 3 O CaCO CaCO1 n0,16875mol;n0,075mol;n0,0375mol Tacó: 2 3 3 COCaCO1CaCO2 nn2n0,15mol 2 2 2 3 dungdÞchtngCOHO HO CaCO1 mmmm1,125m2,025gam Xét phản ứng đốt cháyeste: Bảo toàn khối lượng: . 2 2 2esteCOHOO mmmm3,225gam Câu 28: Đáp án C Xét phản ứng đốt cháyX: Gọi công thức của Xlà . * n2n22k2 CHOn,k3
m0,214629,2gam
axit n0,0075mol;n0,0125mol
Tacó: 2 2 2 2 2 2 COHO COHO COHO nn nn0,055mol 44n18n3,41
Gọi số C của axitvàestetrongX lần lượt làavàb . a1;b2 thỏa mãn. 0,0125a0,0075b0,0555a3b22a2;b4
Vậy axitlà ;estelà . 3 CHCOOH 3 25CHCOOCH Câu 26: Đáp án C 2 2 2 2 CO HO estekh«ngnoCOHO n0,22mol;n0,2molnnn0,02mol
Bảo toàn khối lượng: 2 2 2 2 OCOHOX O mmmm7,68gamn0,24mol Bảo toànnguyên tố O: 2 2 2COHOO X OX OX 1 n2nn2n0,16molnn0,08mol 2
Gọi số Ctronghaiestenovàestekhôngno lần lượt làuvàv . u2;v4 Tacó là nghiệm duy nhất thỏa mãn. 0,06u0,02v0,223uv11u7/3;v4
.
2 3 CHCHCOOCH0,02mol
DẠYKÈMQUYNHƠN OFFICIAL Trang58
3n1k
Tacó:
R83x560,14x12,88R27x5,04 Do là . 5,04 x0,14R2736R9R 0,14 3 CHx0,12 Xlà . 3 3 CHCOOCH0,12molm0,12748,88gam Câu 29: Đáp án A Gọi công thức của EvàT lần lượt là . n2n24 m2m22 CHOn4;CHOm3 Gọi số mol của EvàT lần lượt
.ab0,1a0,06 4a2b0,32b0,04 Bảo toànnguyên tố C: là nghiệm duy nhất. 0,06n0,04m0,423n2m21n5,m3 Câu 30: Đáp án B Khi đốt mgamE: Bảo toànnguyên tố O: 2 2 2COHOO E OX OX 1 n2nn2n0,08molnn0,04mol 2 Có , vậy công thức phân tử của haiestetrongElà 2 2 COHO EE n2n :8:8 nn 882 CHO1 Theo đề bàithìkhichoEtác dụng với NaOHthu được dung dịch T chứa hai muối (2). Từ các dữ kiện (1)và(2)suyrahaiestelà và . 265 HCOOCHCHA 643 HCOOCHCHB Xét hỗn hợp muối Ttacó: ABE A ABNaOHB nnnn0,02mol n2nnn0,02mol . HCOONa m0,04.682,72gam Dạng 6: Bài tập tổng hợp
Phương trìnhhóa học: . t n2n22k2 2 2 2
CHO OnCOn1kHO 2
Theo phương trình: .3n62n3k3 n1k7 2
Nếu (thỏa mãn) Xlà . k1n3 362CHO Nếu (không thỏa mãn). k2n4,5 Xét phản ứng KOH XKOH:n0,14mol
Gọi công thức của estelàRCOOR’(xmol) .R15 Chất rắn khan gồm RCOOK(xmol)vàKOH dư
0,14xmol
.
làavàbmol. Tacó: . 2 2 2ETCOHOCO nnnn0,42mol
Bảo toànnguyên tố O: . 2 2 2COHOOOX n2nn2n0,32mol
Tacó hệ phương trình:
DẠYKÈMQUYNHƠN OFFICIAL Trang59 1 – C 2 – A 3 – C 4 – A 5 - D Câu 1: Đáp án C . 2 23 22 0,4molRCOONa0,45molO0,2molNaCO0,4molCOHO Tacó: Số F chứa muối HCOONa. trungb×nhhçnhîpF 0,20,4 C 01,5 ,4 Bảo toànnguyên tố oxi: 2 HO n0,3mol Bảo toàn khối lượng: F m29,8gam Tỉ lệ hai muối trong F là 1 : 3 nên nếu có 0,1 mol HCOONa số (không muèicßnl¹i C0,60,11,67 0,3 thỏa mãn). Do đó, có0,3molHCOONa số ; số muèicßnl¹i C0,60,33 0,1 muèicßnl¹i H0,60,33 0,1 Mà nênXlàHCOOHvàYlà (axitacrylic). XYMM 23 CHCOOH Tacóquátrình: 3532 23,06gam 23 0,4mol 0,04mol 29,8gam X HCOONa Y E: NaOH CHOHHO CHCOONa T Glixerol Bảo toàn khối lượng: . 2 2 HO HO m5,58gamn0,31mol . 2 axit®¬nchøcHO nn0,31mol Từ 0,4mol muối T 0,09 n0,03mol 3 Theo giả thiết nên có trongT. XTn8n XtrongE n0,24mol 0,30,240,06mol T chứa 2nhómHCOO,1nhóm . 23 23 35 2 CHCOOT:HCOOCHCOOCH T %0,03202 m2100%26,28% 3,06 Câu 2: Đáp án A Quy đổi muối gồm: xmolHCOONa;ymol ;zmol vàamol . 23 CHCOONa2 COONa 2CH Tacó hệ 4 ẩn: Tổng số molcác muối: xyz0,41 Tổng số mol và 2 HO 2 CO:x4yz2a0,492 Tổng khối lượng muối T: 68x94y134z14a49,13 Số mol cần để đốt là: 2O 0,5x3y0,5z1,5a0,2754
DẠYKÈMQUYNHƠN OFFICIAL Trang60
có số . E3,9 C4 Nếu YvàZ đều <4CthìZlà là ,công thức cấu tạo là . 22 HCOOCHT 464CHO 32COOCH Nhận thấy không tạo được ba ancol không thỏa mãn Y và Z phải có số ENaOH 4CX .C4 Để thỏa mãncác dữ kiện đề bàithìXlà ;Ylà ;Zlà 2 2 CHCOOH 24 2 CHCOOH224HCOOCH ;Tlà . 3 25CHOOCCOOCH Để baancolcó số mol bằng nhauthì T Z X Y n0,02mol;n0,02mol;n0,03mol;n0,04mol YNa m6,48gam Câu 4: Đáp án A Bảo toànNa: . 23NaOHNaCO NaOH 23,85 n2n20,45molm0,454018,0gam 106 Trong180gamdung dịch NaOHcó18gamNaOHvà162gam . 2 HO Tacóquátrình: . 2+O bayh¬i xyz 2 2322 44,4gam 2 164,7gam 56,1gam14,85gam23,85gam 0,15mol 18gamNaOHXCHO YHOZNaCOCOHO 162gamHO Sơ đồ viết lại: 2+O bayh¬i xyz 2 23 22 44,4gam 18,0gam 2,7gam 56,1gam14,85gam23,85mol 0,15mol0,45mol 0,15mol 1,275mol0,825mol0,225mol XCHONaOHYHOZNaCOCOHO Bảo toàn khối lượng:
Giải hệ ta được: .x0,05;y0,03;z0,32;a0 ancol n0,72mol Quy đổi ancol gồm 0,72mol và0,19mol . Thấy 3 CHOH 2 CH0,190,05.20,03.3 E gồm 0,05mol và0,03mol và0,32mol . 37HCOOCH 23 49CHCOOCH 32COOCH . Y %m8,35% Câu 3: Đáp án C 2 2 E O CO HO n0,11moln0,44moln0,43mol;n0,32mol
Ta thấy: X,Y,Z,T đều no,hai chức. 2 2 ECOHOnnn Số Ctrungbình của có chất
m44,42,71829,1gam 1,5 n0,2251,2751,5molx10 0,15 1,5 n0,1520,82520,451,5moly10 0,15 29,11,5.121,5 0,6 n 0,6molz416 0,15
Vậy công thức phân tử là .10104 CHO X bị thủy phân thu được muối của hai axit cacboxylic; thủy phân X có tạo thành; 0,15 mol X tác 2 HO dụng 0,45molNaOH (tỉ lệ 1:3) Xlàestehai chức, trong đó có một nhóm chức este của phenol:
Công thức phân tử của Tlà 782CHO
Câu 5: Đáp án D
Từ phản ứng thủy phân X chứa chức este; Y là axit no mạch hở hoặc ancol đơn chức, mạch hở, có một liên kết đôi: hoặc . n2n2CHO n2n CHOn2
Zlàancolno, đơn chức, mạch hở, có số Ctrongphân tử bằng: . 2 n2 32
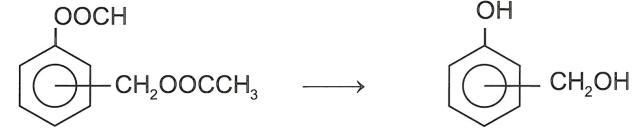
Vậy Zlà: . 25 CHOH
YcóCTPT (Ycócùng số nguyên tử C với Z; loại vìkhông tồn tại 242CHO 24 CHO 2 CHCHOH vàXno).
Công thức cấu
DẠYKÈMQUYNHƠN OFFICIAL Trang61 X CX HX OX
Xcó chức este,khi thủy phân tạo ra và . 3 CHCOOH25 CHOH T phải cónhómCOOHvàOH. Ag T T n0,01 0,52 n 0,005molM 104 22 0,005 Gọi công thức T: a HORCHOCOOH17aR30a1,R13CH Vậy Tcócông thức cấu tạo: Mạch cacbonkhôngphânnhánh. HOOCCHOHCHO Công thức phân tử của Xlà . 25 3 CHOOCCHOOCCHCHO
tạo của Ylà (phản ứng với ở nhiệt độ thường). 3 CHCOOH 2 CuOH Khi1nhóm thìphân tử khối tăng 33,mà . 4CHOCOONH 335033,2 Vậy trongTngoài1nhómCHOcòncó1nhómCOOH.
Mục tiêu
Kiến thức
+Nêu được khá niệm lipit, chất béovàphân loại lipit.
+Trìnhbày được khái niệm chất béo,tính chất vật lí,tính chất hóa học (tính chất chung của este và phản ứng hiđro hóa chất béo lỏng), ứng dụng của chất béo.
+Trìnhbày được phương pháp điều chế, ứng dụng của chất béo.
+ Chỉ ra được cách chuyển hóa chất béo lỏng thành chất béo rắn, phản ứng oxihóa chất béo bởi oxikhôngkhí. Kĩ năng
+ Viết các phương trìnhhóa học minh họa tính chất hóa học và điều chế của chất béo.
+Phân biệt được dầu ăn và mỡ bôi trơn về thành phần hóa học.
+ Giải được các bài tập có liên quan dựa trên phương trình hóa học và định luật bảo toàn như: tính khối lượng các chất trong phản ứng xàphònghóa, phản ứng thủy phân…
+ Biết cách sử dụng, bảo quản được một số loại chất béoantoàn, hiệu quả.
DẠYKÈMQUYNHƠN
Trang1
OFFICIAL
BÀI 2: CHẤT BÉO
I. LÍ THUYẾT TRỌNG TÂM
1. Khái niệm
* Axit béo là axit đơn chức có mạch cacbon dài, không phânnhánh (số nguyên tử C chẵn, khoảng 12–24C).
* Chất béo là trieste của glixerol với axit béo gọi chung làtriglixerithaytriaxylglixerol. Công thức cấu tạo chung: 1 2 2 3 2
RCOOCH | RCOOCH | RCOOCH
Trong đó, là các gốc hiđrocacbon có thể 123 R,R,R giống hoặc khácnhau.
2. Tính chất vật lí
* Chất béo không tan trong nước, nhẹ hơn nước, tan nhiều trongdungmôi hữu cơ như benzen,clorofom…
* Ở nhiệt độ thường chất béo tồn tại ở trạng thái lỏng hoặc rắn
Chất béono: chất rắn Chất béokhôngno: thường là chất lỏng. 3. Tính chất hóa học * Phản ứng thủy phântrongmôi trường axit:
OFFICIAL
DẠYKÈMQUYNHƠN
Trang2
*
lâungày bị hôi. 4. Ứng dụng Ví
Ví
2
2 CHCOOCH |
|
Viết
Tripanmitin: 1531335CHCOOCH Triolein: 1733335CHCOOCH Ví
Ví
Ví
1531335 CHCOOCH3NaOH 1531 3533CHCOONaCHOH Ví dụ: Ni,t 17333352 1735335 CHCOOCH3H CHCOOCH Chú ý: Không nên sử dụng dầu mỡ đã để
t,H 3352 353 (RCOO)CH3HO3RCOOHCH(OH) * Phản ứng xàphònghóa: t 335 353 (RCOO)CH3NaOH3RCOONaCH(OH)
Phản ứng hiđro hóa (đối với chất béo lỏng): Estekhôngno+H2 → Esteno * Phản ứng oxihóa: Nối đôi ở gốc axitbéokhôngno bị oxihóa chậm
CC trongkhôngkhíthànhpeoxit, chất này bị phân hủy thành anđehit cómùikhó chịu → Nguyênnhân của hiện tượng dầu, mỡ để
dụ: Axit panmitic: 1531 CHCOOH Axit stearic: 1735 CHCOOH Axit oleic: 1733 CHCOOH
dụ: Tristearin: 1735
1735 1735
CHCOOCH
CHCOOCH
gọn: 1733335CHCOOCH
dụ: Tristearin, tripanmitin
dụ: Triolein.
dụ:
lâu ngày.
-Là thức ăn quan trọng của con người.
- Nguyên liệu để tổng hợp một số chất cần thiết cho cơ thể.
- Điều chế xàphòngvàglixerol.
- Sản xuất thực phẩm khác:mì sợi, đồ hộp.
Chú ý: Dầu mỡ sau khi rán có thể dùng để tái chế thành nhiên liệu.
DẠYKÈMQUYNHƠN OFFICIAL
Trang3
Lipit
Lipit là những hợp chất hữu cơ có trong tế bào sống, không tan trong nước nhưng tan trong dung môi hữu cơ không phân cực.
Lipit gồm: chất béo, sáp, steroit, photpholipit,…
Axit béo Chất béo
Axit béo là các axit đơn chức có mạch cacbon dài không phân nhánh.
Chất béo là trieste của glixerol với axit béo, gọi chung là triglixerit hay triaxylglixerol.
Axit béo và chất béo thường gặp
C15H31COOH: Axit panmitic(C15H31COO)3C3H5: Tripanmitin C17H35COOH: Axit stearic(C17H35COO)3C3H5: Tristearin
C17H33COOH: Axit oleic(C17H33COO)3C3H5: Triolein C17H31COOH: Axit linoleic
Nhẹ hơn nước, không tan trong nước, tan trong các dung môi hữu cơ như benzen, ete,…
Chất béo no là chất rắn Chất béo không no thường là chất lỏng.
Trong môi trường axit (xảy ra ở dạ dày)
môi trường kiềm (dùng để sản xuất xà phòng)
DẠYKÈMQUYNHƠN
Trang4 SƠ ĐỒ HỆ THỐNG HÓA
OFFICIAL
H,t 352 35 3 3 RCOOCH3HO3RCOOHCHOH Trong
t 35 35 3 3 RCOOCH3NaOH3RCOONaCHOH Chất béo không no Chất béo no Ni,t 2H Ví dụ: Triolein Tristearin Ni,t 23H Phản ứng thủy phân Phản ứng cộng hiđro TÍNH CHẤT HÓA HỌC TÍNH CHẤT VẬT LÍ KHÁI NIỆM CHẤT BÉO
II. CÁC DẠNG BÀI TẬP
Dạng 1: Lí thuyết trọng tâm
Kiểu hỏi 1: Khái niệm Ví dụ mẫu
Ví dụ 1: Trongcác hợp chất sau, hợp chất nàolà chất béo?
A. (C2H3COO)3C3H5 B. (C17H31COO)3C3H5 C. (C2H5COO)3C3H5 D. (C6H5COO)3C3H5
Hướng dẫn giải
Chất béolàtrieste của glixerol(C2H5(OH)3)vàaxitbéo(axitbéolàaxit đơn chức có mạch cacbondài từ 12C–24C,khôngphânnhánh).
→ Hợp chất là chất béo:(C17H31COO)3C3H5
→ Chọn B.
Ví dụ 2: Tên hợp chất cócông thức cấu tạo (C17H33COO)3C3H5 là
A. triolein B. tristearin C. trilinolein D. tripanmitin
OFFICIAL
Hướng dẫn giải
Têneste tạo nên từ ba gốc axit giống nhau=tri+tênaxit tương ứng (thay thế đuôi “ic”thành“in”).
Tên của axitbéo tương ứng C17H33COOHlàaxitoleic.
→ Tên chất béolàtriolein
→ Chọn A. Ví dụ 3: Khi thủy phân hoàn toàn một triglixerit X trong môi trường axit thu được hỗn hợp sản phẩm gồm glixerol,axitstearicvàaxitpanmitic. số công thức cấu tạo của X thỏa mãntính chất trênlà A. 6 B. 8 C. 2 D. 4 Hướng dẫn giải Khi thủy phân một triglixeritXtrongmôi trường axitthu được haiaxitbéonênestecó
DẠYKÈMQUYNHƠN
Trang5
dạng: 2RR và . R2R ; ; ; 2 2 RCOOCH | RCOOCH | RCOOCH 2 2 RCOOCH | RCOOCH | RCOOCH 2 2 RCOOCH | RCOOCH | RCOOCH 2 2 RCOOCH | RCOOCH | RCOOCH → Chọn D. Chú ý: Khi thủy phân hoàn toàn chất béo (triglixerit) thu được hai axit béo thì số công thức cấu tạo thỏa mãn luôn là 4. Kiểu hỏi 2: Tính chất vật lí Ví dụ mẫu Ví dụ 1: Ở nhiệt độ thường, chất nàosau đây là ở trạng thái rắn? A. CH3COOC2H5 B. (C17H33COO)3C3H5 C. (C17H35COO)3H3H5 D. (C17H31COO)3C3H5 Hướng dẫn giải
AsaivìlàCH3COOC2H5 là chất lỏng ở nhiệt độ thường.
B, D sai vì (C17H33COO)3C3H5 và (C17H31COO)3C3H5 là chất béo không no nên là chất lỏng ở nhiệt độ thường.
C đúng vì(C17H35COO)3C3H5 là chất béononênlà chất rắn ở nhiệt độ thường
→ Chọn C
Ví dụ 2: Chocácphát biểu sau:
(1) Chất béo thuộc loại este
(2) Chất béokhôngtantrong nước và nhẹ hơn nước
(3)Khi đun chất béo lỏng với H2 dư cóNixúctácthìthu được chất béo rắn
(4) Chất béo lỏng làcáctriglixerit chứa gốc axitkhôngno
Cácphát biểu đúng là:
A. (1),(4) B. (1),(2),(4) C. (1),(3),(4) D. (1),(2),(3),(4)
Hướng
dẫn giải
(1) đúng vì chất béolàtrieste của glixerol với axitbéo
OFFICIAL
(2) đúng vì các chất béo không tạo liên kết hiđro với nước và phân tử cồng kềnh nên không tan trong nước và nhẹ hơn nước
(3) đúng vì chất béo lỏng là chất béocó gốc axitkhôngno,khitác dụng với hiđro cóNixúctácthu được chất béocó gốc axitnovàlà chất béo rắn
(4) đúng vìkhitrongphân tử có gốc axitkhôngno, chất béo ở trạng thái lỏng
→ Chọn D.
Kiểu hỏi 3: Tính chất hóa học Ví dụ mẫu
Ví dụ 1: Tính chất nàosau đây không phải của triolein?
A. Là chất lỏng ở điều kiện thường
B. Tác dụng với Cu(OH)2 ở điều kiện thường, tạo radung dịch xanhlam
C. Thủy phânhoàntoàntrongdung dịch NaOH,thu được xàphòng
D. Tác dụng với H2 dư (xúctácNi, đun nóng) tạo ratristearin
Hướng dẫn giải
A đúng vìtrongphân tử chức gốc axitkhôngno,nêntrioleinlà chất lỏng ở điều kiện thường
Bsaivìtrioleinlàestenênkhôngcó phản ứng với Cu(OH)2 C đúng vìtrioleinlà chất béo,khi thủy phânhoàntoàntrongNaOHthu được muối natri của axitbéo(xà phòng)
đúng vìtacó phương trìnhhóa học:
DẠYKÈMQUYNHƠN
Trang6
Ni,t 1733 352 1735 35 3 3 CHCOOCH3HCHCOOCH Triolein Tristearin → Chọn B Ví dụ 2: Chocácphát biểu sau (a) Chất béocòn được gọi làtriglixerithaytriaxylglixerol (b) Chất béo nhẹ hơn nước, khôngtantrong nước nhưng tan nhiều trongcácdungmôi hữu cơ
D
(c) Phản ứng thủy phân chất béotrongmôi trường axitlà phản ứng thuận nghịch
(d)Tristearin,trioleincócông thức lần lượt là(C17H33COO)3C3H5,(C17H35COO)3C3H5
(e)Trioleincó khả năng thamgia phản ứng cộng hiđro khi đun nóngcóxúctácNi
(g) Chất béo bị thủy phânkhi đun nóngtrongdung dịch kiềm
Số phát biểu đúng là A. 3 B. 5 C. 4 D. 6
Hướng dẫn giải
(a),(c),(e)và(g) đúng. (b)saivì chất béo chỉ tan nhiều trongdungmôikhôngphân cực (d)saivìtristearin,trioleincócông thức lần lượt là(C17H35COO)3C3H5 và(C17H33COO)3C3H5 → Chọn C Kiểu hỏi 4: Ứng dụng Ví dụ mẫu Ví dụ 1: Chất béo là thức ăn quan trọng của con người, là nguồn cung cấp dinh dưỡng và năng lượng đáng kể cho cơ thể hoạt động. Ngoàira, một lượng lớn chất béo được dùngtrongcông nghiệp để sản xuất A. glucozơ vàancoletylic B. xàphòngvàancoletylic C. glucozơ vàglixerol D. xàphòngvàglixerol Hướng dẫn giải Khi xà phòng hóa chất béo người ta thu được xà phòng và glixerol. Dựa vào tính chất này người ta sản xuất xàphòngvàglixerol từ chất béo. → Chọn D. Bài tập tự luyện dạng 1
OFFICIAL
Câu 1: Chất béolàtrieste của axitbéo với chất nàosau đây?
A. Etanol B. Etylenglicol C. Glixerol D. Metanol Câu 2: Axitnàosau đây không phải làaxit tạo ra chất béo? A. Axitoleic B. Axitacrylic C. Axitstearic D. Axitpanmitic Câu 3: Trongcác hợp chất sau, hợp chất nàolà chất béo? A. (C17H35COO)3C3H5 B. (C17H35COO)2C2H4 C. (CH3COO)3C3H5 D. (C2H5COO)2C3H5 Câu 4: Tên hợp chất cócông thức cấu tạo (C17H33COO)3C3H5 là A. triolein B. tristearin C. trilinolein D. tripanmitin Câu 5: Đun nóngtristearintrongdung dịch NaOH
DẠYKÈMQUYNHƠN
Trang7
dư thu được glixerolvà A. C17H35COONa B. C17H33COONa C. C15H31COONa D. C17H31COONa Câu 6: Khi thủy phânhoàntoàntripanmitintrongmôi trường kiềm (NaOH)tathu được sản phẩm là A. C17H35COOHvàglixerol B. C15H31COONavàglixerol C. C15H31COOHvàglixerol D. C17H35COONavàglixerol Câu 7: Ở nhiệt độ thường, chất nàosau đây tồn tại ở trạng thái rắn? A. Etylaxetat B. Triolein C. Tristearin D. Trilinolein Câu 8: Phát biểu nàosau đây sai?
A. Muốn chuyển chất béo từ thể lỏng sang thể rắn, người ta tiến hành đun chất béo với H2 (xúctácNi)
B. Tên gọi của chất béocócông thức (C15H31COO)3C3H5 làtriolein
C. Chất béokhôngtan được trong nước
D. Khi đun nóng chất béo với dung dịch NaOH hoặc KOHta được muối dùnglàmxàphòng.
Câu 9: Phát biểu nàosau đây sai?
A. Chất béokhôngtantrong nước, nhẹ hơn nước nhưng tan nhiều trongdungmôi hữu cơ
B. Chất béo lỏng có phản ứng cộng H2
C. Trongcông nghiệp, một lượng lớn chất béodùng để điều chế xàphòngvàglixerol
D. Chất béo rắn được tạo nên từ các gốc axitbéokhôngno
Câu 10: Khi thủy phân hoàn toàn một triglixerit X trong môi trường axit thu được hỗn hợp sản phẩm gồm glixerol,axitpanmiticvàaxitoleic, số công thức cấu tạo của X thỏa mãntính chất trênlà
A. 6 B. 8 C. 2 D. 4 Câu 11: Phát biểu nàosau đây sai?
A. Khi thủy phân chất béoluônthu được etylenglicol
OFFICIAL
B. Hiđro hóahoàntoàntriolein hoặc trilinolein đều thu được tristearin
C. Dầu mỡ động thực vật bị ôithiudo nối đôi C=C ở gốc axitkhôngno của chất béo bị oxihóa chậm bởi oxikhôngkhí tạo thànhpeoxit, chất này bị phân hủy thànhcác sản phẩm cómùikhó chịu
D. Chất béo nhẹ hơn nước vàkhôngtantrong nước.
Câu 12: Phát biểu nàosau đây sai?
A. Nhiệt độ nóng chảy của tristearincao hơn của triolein
B. Chất béolàthành phần chính của dầu mỡ động, thực vật
C. Trongphân tử trilinoleincó9liên kết
D. Thủy phânhoàntoàn1mol chất béothu được 3molglixerol
Câu 13: Cho các chất sau: triolein, tristearin, tripanmitin, vinyl axetat, metyl axetat. Số chất tham gia phản ứng cộng H2 (Ni,t°)là
A. 2 B. 3 C. 4 D. 1
Bài tập nâng cao
Câu 14: Thủy phân một triglixeritX bằng dung dịch NaOH,thu được hỗn hợp muối gồm natrioleat,natri stearat(có tỉ lệ mol tương ứng là1:2)vàglixerol. Số công thức cấu tạo phù hợp của Xlà A. 2 B. 1 C. 3 D. 4
DẠYKÈMQUYNHƠN
Trang8
Phản ứng thủy phân Bài toán 1: Xác định lượng chất trong phản ứng Phương pháp giải Phương trìnhhóa học dạng tổng quát: Ví dụ: Xà phòng hóa hoàn toàn m gam triglixerit X bằng lượng vừa đủ
Dạng 2:
NaOH thu được 0,5molglixerolvà459gam muối khan. Giá trị của mlà A. 443 B. 442 C. 444 D. 445
Chọn D
dụ mẫu
dụ 1: Xàphònghóahoàntoàn một lượng triglixerit cần Vmldung dịch NaOH1Mthu được 9,2gam glixerol.Giá trị của Vlà A. 100 B. 150 C. 200 D. 300 Hướng dẫn giải
glixerol n0,1mol Xàphònghóa chất béo:
DẠYKÈMQUYNHƠN OFFICIAL Trang9 1 1 2 35 2 353 3 3 RCOO \ RCOONa RCOOCH3NaOHRCOONaCHOH RCOONa / RCOO Phương trìnhhóa học dạng rút gọn: 35 35 3 3 RCOOCH3NaOH3RCOONaCHOH - Nhận xét: chaátbeùoglixerolNaOH NaOHmuoáiglixerolchaátbeù o 1 nnn 3 nn3n3n - Bảo toàn khối lượng: chaátbeùoNaOHmuoáiglixerolmmmm Chú ý: Công thức của glixerollàC3H5(OH)3 (M=92) Hướng dẫn giải Tacó: glixerol m0,59246gam Nhận xét: NaOHglixerol n3n30,51,5mol NaOH m1,54060gam Bảo toàn khối
353 chaá
chaátbeù
chaátbeù o m 4594660 445gam →
NaOH
muoá
1735 xaøphoøngCHCOONamm 0,330691,8gam Phương trình hóa học: (C17H35COOC3H5)3 + 3NaOH → 3C17H35COONa + C3H5(OH)3 Ví dụ 3: Xàphònghóahoàntoàn17,24gam chất béo cần vừa đủ 0,06molNaOH.Cô cạn dung dịch sau phản ứng thu được muối có khối lượng là
lượng:
tbeùoNaOHxaøphoøngCHOHmmmm
o m6045946
Ví
Ví
333NaOHCHOH n3n3.0,10,3mol
V0,30,3lít300ml 1 → Chọn D Ví dụ 2: Xàphònghóahoàntoàn một lượng tristearintrongNaOH,sau phản ứng hoàntoànthu được 9,2 gamglixerol. Khối lượng muối thu được là A. 91,8gam B. 61,2gam C. 30,6gam D. 122,4gam Hướng dẫn giải
glixerol n0,1mol Xàphònghóatristearin:
iglixerol n3n30,10,3mol
A. 16,68gam B. 17,80gam C. 18,24gam D. 18,38gam Hướng dẫn giải Tacó: NaOH m0,06.402,4gam Xàphònghoàntoàn chất béo: 353 NaOH CHOH 1 n3n0,02mol glixerol m0,02.921,84gam Bảo toàn khối lượng:
DẠYKÈMQUYNHƠN OFFICIAL Trang10
→
→
Ví
2:
chất
thu được glixerol và hỗn hợp hai muối C17H35COONa,C15H31COONacó khối lượng hơn kémnhau1,817 lần. Trongphân tử Xcó A. 2 gốc C15H31COO B. 3 gốc C17H35COO C. 2 gốc C17H35COO D. 3 gốc C15H31COO Hướng dẫn giải Khi thủy phân chất béoXtrongdung dịch NaOH,thu được glixerolvà hỗn hợp hai muối C17H35COONa, C15H31COONanênXcó chứa hai gốc axitC15H31COOvàC17H35COO. TH1:X chứa hai gốc C17H35COOvà một gốc C15H31COO. Gọi số molC17H35COONalà2molthì số molC17H35COONalà1mol. 1735 1531 CHCOONa CHCOONa m 23062,2 m 278
353 chaátbeùoNaOHxaøphoøngCHOHmmmm
xaøphoøng 17,242,4m1,84 xaøphoøng m17,8gam
→ Chọn B Bài toán 2: Xác định công thức chất béo Ví dụ mẫu Ví dụ 1: Thủy phân hoàn toàn m gam triglixerit X trong dung dịch NaOH. Sau phản ứng thu được glixerolvà15,2gamnatrioleatvà30,6gamnatristearat.Phân tử khối của Xlà A. 886 B. 888 C. 890 D. 884 Hướng dẫn giải Theo đề bài: 1733 CHCOONanatrioleat nn0,05mol 1735 CHCOONanatristearatn n0,1mol Tacó: NaOH 1733 1735 353XCHCOONa2CHCOONaCHOH → Trongphân tử Xcó một gốc axitC17H33COOvàhai gốc axitC17H35COO.
Công thức phân tử của Xlà:(C17H33COO)(C17H35COO)2C3H5 Xcóphân tử khối là: X M888
Chọn B
dụ
Khi thủy phân
béo X trong dung dịch NaOH,
→ Loại
TH2:X chứa hai gốc C15H31COOvà một gốc C17H35COO. Gọi số molC15H31COONalà2molthì số molC17H35COONalà1mol
→ Thỏa mãn. Vậy trongphân tử X chứa 2 gốc C15H31COO
→ Chọn A
Bài tập tự luyện dạng 2
Câu 1: Xà phòng hóa hoàn toàn 178 gam tristearin trong dung dịch KOH, thu được m gam kali stearat. Giá trị của mlà
A. 200,8 B. 183,6 C. 211,6 D. 193,2
Câu 2: Xàphònghoáhoàntoàn89gam chất béoX bằng dung dịch NaOHthu được 9,2gamglixerolvà mgamxàphòng.Giá trị của mlà
A. 91,8 B. 83,8 C. 79,8 D. 98,2
Câu 3: Xàphònghóahoàntoàn17,24gam một triglixerit cần vừa đủ 0,06molNaOH.Cô cạn dung dịch sau phản ứng thu được khối lượng xàphònglà
A. 16,68gam B. 18,24gam C. 18,38gam D. 17,80gam Câu 4: Một loại chất béo có chứa 89% tristearin và 11% axit stearic (theo khối lượng). Xà phòng hóa hoàntoàn100gam chất béo đó bằng dung dịch NaOH (phản ứng vừa đủ), sau phản ứng thu được mgam xàphòng.Giá trị của mlà
A. 124,56 B. 102,25 C. 108,48 D. 103,65 Câu 5: Thủy phân hoàn toàn m gam chất béo X bằng 250 ml dung dịch KOH 1,5M, đun nóng (lượng KOH được lấy dư 25%so với lượng cần phản ứng). Cô cạn dung dịch sau phản ứng thu được 100,2gam hỗn hợp chất rắn khan gồm hai chất. Tên gọi của Xlà A. trilinolein B. tristearin C. triolein D. tripanmitin
DẠYKÈMQUYNHƠN
Trang11
OFFICIAL
1531 1735 CHCOONa CHCOONa m 22781,817 m 306
Dạng 3: Phản ứng oxi hóa – khử Bài toán 1: Phản ứng với H2/Br2 Phương pháp giải Ví
→
CC
dụ: Hiđro hóa hoàn toàn 26,52 gam triolein cần vừa đủ VlítkhíH2 (đktc). Giá trị của Vlà A. 0,672 B. 4,032 C. 2,016 D. 1,792 Hướng dẫn giải Axit oleic có 1 liên kết
Triolein có 3 liên
CC kết nên phản ứng với H2 theo tỉ lệ 1:3
Ví dụ: Đốt cháy hoàn toàn 1 mol triglixerit X, thu được lượng CO2 vàH2O hơn kémnhau5mol. Mặt khác,choamolXtác dụng tối đa với 600mldung dịch Br2 1M.Giá trị của alà A. 0,20 B. 0,12 C. 0,10 D. 0,15 Hướng dẫn giải Tacó: → k=6 2 2 COHO chaátbeù o nnk1n Chất béo tham gia phản ứng cộng dung dịch Br2 theo tỉ lệ 1:3(vìk=6nên chất béonàycóbaliên kết trongnhómCOOvàbaliên kết ). CC → Chất béo phản ứng với Br2 theo tỉ lệ 1:3. Theo đề bài: 2Br n0,6.10,6mol chaátbeù o 0,6 an30,2mol → Chọn A
DẠYKÈMQUYNHƠN OFFICIAL Trang12 Chất
(với
)
CC
n
2
2
→
Ví
Ví
1:
A.
B.
Hướng
1735335CHCOOCHn
Axitoleiccó1liên
→ Trioleincó3liên
phản ứng với H2 theo tỉ lệ 1:3 CC CC Phương trìnhhóa học: 1733 3531735 35 3 3 CHCOOCH3HCHCOOCH 0,1 0,1mol 1733335trioleinCHCOOCHmm 0,1.88488,4gam →
B Bài
* Công
khi đốt cháy chất béo với 2 2 COHO chaátbeù o nnk1n kn3 Do trong este có 3 liên kết trong nhóm COO và nliên kết nên độ bất bãohòa: . CC kn3 Áp dụng các định luật bảo toàn:
béo không no phản ứng với H2/Br2 theo tỉ lệ
nlà số liên kết
1:n
1733335CHCOOCH
0,03mol
Tacó:
Htriloein n3n0,09mol
H V0,09.22,42,016lít
Chọn C.
dụ mẫu
dụ
Hiđro hoáhoàntoànmgamtrioleinthìthu được 89gamtristearin.Giá trị mlà
84,8
88,4 C. 48,8 D. 88,9
dẫn giải
0,1mol
kết
kết nên
Chọn
toán 2: Phản ứng đốt cháy Phương pháp giải
thức
V0,78.22,417,472lít
Chọn A Ví dụ 2: Đốt cháyhoàntoàn1mol chất béotrungtính,thu được lượng CO2 vàH2O hơn kémnhau6mol. Mặt khácamol chất béotrêntác dụng tối đa với 600mldung dịch Br2 1M.Giá trị của alà A. 0,30 B. 0,18 C. 0,20 D. 0,15
DẠYKÈMQUYNHƠN OFFICIAL Trang13 Bảo
2
Tacó: Thuûyphaâ n 1733 1531 1735 X CHCOOHCHCOOCHCOOH → Công
của Xlà(C17H33COO)(C15H31COO)(C17H35COO)C3H5 → Công
tử của XlàC55H104O6 X
t
Tacó: 2 2 COHO chaátbeù o
phản ứng cộng
kết trongnhómCOOvà bốn liên kết ). CC → Chất béo phản ứng với Br2 theo tỉ lệ 1:4 Theo đề bài: 2Br n0,6.10,6mol chaátbeù o 0,6 an40,15mol → Chọn D. Ví dụ 3: Đốt cháy hoàn toàn m gam một triglixerit X cần dùng 1,61 mol O2, thu được 1,14 mol CO2 và 1,06molH2O.Cho26,58gamXtác dụng vừa đủ với dung dịch NaOHthì khối lượng muối tạo thànhlà A. 18,28gam B. 25,02gam C. 27,42gam D. 27,14gam Hướng dẫn giải Xét phản ứng đốt cháymgamX:
toàn khối lượng:
2 2 chaátbeùoOCOHOmmmm Bảo toànnguyên tố O(do chất béoluôn chứa 6O)
2 2 2 OOCOHO6n2n2nn Ví dụ mẫu Ví dụ 1: Khi thủy phân hoàn toàn một triglixerit X, thu được các axit béo gồm axit oleic, axit panmitic, axitstearic. Thể tíchkhíO2 (đktc) cần dùng vừa đủ để đốt cháyhoàntoàn8,6gamXlà A. 17,472lít B. 16,128lít C. 20,160lít D. 15,680lít Hướng dẫn giải
thức
thức phân
8,6 n0,01mol 860 Phương trìnhhóa học:
551046 2 2 2 CHO78O55CO52HO
0,010,78 mol
2O
→
Hướng dẫn giải
nnk1nk7 Chất béothamgia
dung dịch Br2 theo tỉ lệ 1:4(vìk=7nên chất béonàycóbaliên
với dung dịch KOH dư, đun nóng,thu được agam muối. Giá trị của alà A. 45,6 B. 45,9 C. 48,3 D. 48,0 Câu 3: Đốt cháy hoàn toàn 1 mol triglixerit X, thu được lượng CO2 và H2O hơn kém nhau 7 mol. Mặt khác,choamolXtác dụng tối đá với 600mldung dịch Br2 1M.Giá trị của alà A. 0,20 B. 0,12 C. 0,10 D. 0,15
DẠYKÈMQUYNHƠN OFFICIAL Trang14 Chất béoXluôncó6nguyên tử Onên bảo toànnguyên tố Otacó 2 2 2 XOCOHO6n2n2nn X 6n21,611,1421,06 X 6n0,12 Xn 0,02 Bảo toàn khối lượng: 2 2 2 XOCOHO mmmm X m1,61321,14441,0618 X m17,72gam Tacó: X M17,72886 0,02 Xét phản ứng thủy phânXtrongmôi trường kiềm: Theo đề bài: X 26,58 n80,03mol 66 Phương trìnhhóa học: 35 35 3 3 RCOOCH3NaOH3RCOONaCHOH 0,030,09 0,03mol Bảo toàn khối lượng: 353 XNaOHmuoáiCHOHmmmm muoá i 26,580,0940m0,0392 muoá i 26,583,6m2,76 muoá im 27,42gam → Chọn C. Bài tập tự luyện dạng 3 Bài tập cơ bản Câu 1: Hiđro hóahoàntoàn17,68gamtriolein cần vừa đủ VlítkhíH2 (đktc). Giá trị của Vlà A. 1,344 B. 0,448 C. 2,688 D. 4,032 Câu 2: Cho mgam triolein tác dụng hoàn toàn với H2 dư thu được (m+ 0,3) gam chất X. Nếu chotoàn bộ Xtác dụng hết
Câu 4: Thuỷ phântriglixeritXtrongNaOH người tathu được hỗn hợp hai muối gồm natrioleatvànatri stearattheo tỉ lệ mol lần lượt là2:1.Khi đốt cháyamolXthu được bmolCO2 vàcmolH2O.Liên hệ giữa a,b,clà
A. b–c=5a B. b–c=3a C. b–c=4a D. b–c=2a Câu 5: Đốt cháy 34,32 gam chất béo X bằng lượng oxi vừa đủ, thu được 96,8 gam CO2 và 36,72 gam nước. Mặt khác0,12molXlàm mất màu tối đa Vmldung dịch Br2 1M.Giá trị của Vlà
A. 120ml B. 360ml C. 240ml D. 480ml
Câu 6: Đốt cháy hoàn toàn a gam triglixerit X cần vừa đủ 3,2 mol O2, thu được 2,28 mol CO2 và 2,08 molH2O. Mặt khác,choagamXvào500mlNaOH0,3M,sau phản ứng cô cạn dung dịch thu được chất rắn chứa mgam muối khan.Giá trị của mlà
A. 43,14 B. 37,68 C. 37,12 D. 36,48 Câu 7: Đốt cháy hoàn toàn a gam triglixeritx cần vừa đủ 4,83 mol O2, thu được 3,42 mol CO2 và 3,18 mol H2O. Mặt khác, cho a gam X phản ứng vừa đủ với dung dịch NaOH, thu được b gam muối. Giá trị của blà
A. 53,16 B. 57,12 C. 60,36 D. 54,84
OFFICIAL
Câu 8: : Đốt cháyhoàntoànmgam một triglixeritX cần vừa đủ 0,77molO2,sinhra0,5molH2O. Nếu thủy phânhoàntoànmgamXtrongdung dịch KOH đun nóngthu được dung dịch chứa 9,32gam muối. Mặt khácamolXlàm mất màu vừa đủ 0,12molbromtrongdung dịch. Giá trị của alà
A. 0,03 B. 0,04 C. 0,02 D. 0,01 Câu 9: Đốt cháyhoàntoànmgam một chất béotriglixerit cần 1,61molO2,sinhra1,14molCO2 và1,06 molH2O.Cho7,088gam chất béotác dụng vừa đủ với dung dịch NaOHthì khối lượng muối tạo thànhlà
A. 7,612gam B. 7,512gam C. 7,412gam D. 7,312gam
Bài tập nâng cao
Câu 10: Xlà một trieste mạch hở được tạo bởi glixerol với cácaxit đơn chức. Đốt cháyhoàntoànamol Xthu được bmolCO2 vàcmolH2O, (biết rằng b–c=6a). Biết amolXtác dụng vừa đủ với dung dịch chứa 12,8gambromthu được 18,12gam sản phẩm hữu cơ. ChoamolXtác dụng với dung dịch NaOH vừa đủ thìthu được mgam muối. Giá trị của m gần nhất với giá trị nàosau đây
DẠYKÈMQUYNHƠN
Trang15
A. 6 B. 5 C. 8 D. 7 ĐÁP ÁN Dạng 1: Lí tuyết trọng tâm 1-C 2-B 3-A 4-A 5-A 6-B 7-C 8-B 9-D 10-D 11-A 12-D 13-A 14-A Câu 8: A,C,D đúng. Bsaivì(C15H31COO)3C3H5 cótên gọi làtripamitin Câu 9: A,B,C đúng. Dsaivì chất béo rắn được tạo nên từ các gốc
Câu 10:
axitbéono
Thủy phânhoàntoànXtrongmôi trường axitthu được hỗn hợp sản phẩm gồm glixerol,axitpanmiticvà axitoleic → Xlàtrieste được tạo nên từ glixerolvàaxitpanmiticvàaxitoleic. Cáccông thức cấu tạo của X viết gọn là: PPO;POP;OOP;OPO
Câu 11: Asaivìkhi thủy phân chất béoluônthu được glixerol B,C,D đúng
Câu 12: A đúng vìtrioleincóliên kết nên nhiệt độ nóng chảy nhỏ hơn của tristearin CC B đúng C đúng vì gốc axitlinoleiccó Ba gốc axitcó vàcó3liên kết trong3nhómCOO. Vậy
phương trìnhhóa học:
35 35 3 3
1 1 mol
Thủy phânhoàntoàn1mol chất béothu được 1molglixerol Câu 13: Các chất thamgia phản ứng cộng làtriolein,vinylaxetat. o 2 HNi,t Câu 14: Thủy phânXthu được hai muối natrioleatvànatristeratcó tỉ lệ mollà1:2 → Xcó1 gốc oleicvà2 gốc stearic → Công thức của X thỏa mãn viết gọn là: OSS;SOS Dạng 2: Phản ứng thủy phân 1-D 2-A 3-D 4-D 5-C Câu 1:
DẠYKÈMQUYNHƠN
Trang16
OFFICIAL
1735 1735
CHCOOKCHCOOCH
1735 CHCOOK m0,6322193,2gam Câu 2: Xàphònghóahoàntoàn chất béo: 353NaOHCHOH 9,2 n3n3.0,3mol 92 Bảo toàn khối lượng: 353 xaøphoøngchaátbeùoNaOHCHOH mmmm91,8gam Câu 3: Xàphònghóahoàntoàn chất béo: 353 NaOH CHOH 1 n3n0,02mol Bảo toàn khối lượng: 353 xaøphoøngchaátbeùoNaOHCHOH mmmm17,8gam Câu 4: tristearin axitstearic m10089%89gam;m10011%11gam
CC2 CC6 trongphân tử trilinoleincó9liên kết Dsaivì
RCOOCH3NaOH3RCOONaCHOH
→
stearin n0,2mol Xàphònghóahoàntoàn chất béo:
335
n3n 3.0,20,6mol
DẠYKÈMQUYNHƠN OFFICIAL Trang17 1735 1735335 CHCOOH CHCOOCHn 0,1mol;n0,0387mol Phương trìnhhóa học: 1735 35 1735 35 3 3 CHCOOCH3NaOH3CHCOONaCHOH 0,1 0,3 mol 1735 1735 2 CHCOOHNaOHCHCOONaHO 0,0387 0,0387 mol 1735 CHCOONan 0,30,03870,3387mol m0,3387.306103,65gam Câu 5: 353 KOH KOHpö X KOHpö CHOH 1n0,375moln0,3molnn3n0,1mol Bảo toàn khối lượng: 353 Xchaátraé n KOH X CHOH mmmm88,4M884 → Công thức của Xlà(C17H33COO)3C3H5:triolein Dạng 3: Phản ứng oxi hóa – khử 1-A 2-C 3-B 4-C 5-C 6-D 7-D 8-B 9-D 10-A Câu 1: triolein n0,02mol 2 2 Htriolein H n3n0,06molV0,0622,41,344lít Câu 2: Bảo toàn khối lượng: 2 2 H H m0,3gamn0,15mol Trioleintác dụng với H2 theo tỉ lệ lên 2trioleinH 1 1:3:nn0,05mol 3 Phương trìnhhóa học: 1735 35 1735 35 3 3 CHCOOCHKOH3CHCOOKCHOH 0,05 0,15 mol a0,1532248,3gam Câu 3: Tacó: Số liên kết 2 2 COHO X nnk1nk8 CC COO 835 2Br 0,6 n5aa0,12mol 5 Câu 4: Theo đề bài,X gồm 2 gốc C17H33COOvà1 gốc C17H35COO. → Tổng số liên kết COOCC 325 Tacó: 2 2 COHO X nnk1nbc4a
Câu 5:
Xét phản ứng đốt cháy34,32gam chất béo:
n2,2mol;n2,04mol
Bảo toàn khối lượng: 2 2 O O m96,836,7234,3299,2gamn3,1mol Bảo toànnguyên tố O: 2 2 2 XOCOHOX 6n2n2nnn0,04mol Tacó: 2 2 COHO chaátbeù o nnk1nk5 → Chất béothamgia phản ứng cộng dung dịch Br2 theo tỉ lệ 1:2(vì nên chất béonàycóbaliên k5 kết trongnhómCOOvàhailiên kết ). CC Khicho0,12mol chất béotác dụng với dung dịch Br2:
Câu 6: Xét phản ứng đốt cháyagamX: Bảo toànnguyên tố O:
DẠYKÈMQUYNHƠN
Trang18
OFFICIAL
2 2 CO HO
2Br 0,24 n2.0,120,24molV0,24lít240ml 1
1733 35 1733 35 3 3 CHCOOCH3NaOH3CHCOONaCHOH 0,040,150,12mol 1733 CHCOONamm 0,12.30436,48gam Câu 7: Xét phản ứng đốt cháyX: Bảo toàn khối lượng: 2 2 2XCOHOO mmmm53,16gam Bảo toànnguyên tố O: 2 2 2COHOO X OX OX 1 n2nn2n0,36nn0,06mol 6 Xét phản ứng : XNaOH 353 NaOHX XCHOH n3n0,18mol;nn0,06mol Bảo toàn khối lượng: 353XNaOHCHOH bmmm54,84gam Câu 8: Gọi số mol của X ứng với mgamlàxmol. Xét 353 KOH CHOH XKOH:n3xmol;nxmol Bảo toàn khối lượng: 353 muoá i KOHCHOH mmmm9,3276xgam
2 2 2 XOCOHOX 6n2n2nnn0,04mol Bảo toàn khối lượng:
2 2 2 XOCOHO X mmmma35,36gamM884 → Xlà(C17H33COO)3C3H5. ChoagamXvào500mlNaOH0,3M:
NaOH n0,15mol Phương trìnhhóa học:
toànnguyên
DẠYKÈMQUYNHƠN OFFICIAL Trang19
2 2 2 XOCOHOX
Bảo
2 2 2
X
353 XNaOHmuoá i muoá i CHOH mmmmm7,312gam Câu 10: Có: COOCCbc6ak734 Cứ amolXtác dụng vừa đủ với 4amol 2X Brn0,08:40,02mol Bảo toàn khối lượng: X m18,120,081605,32gam Tacó: NaOH n0,0230,06mol 353 NaOH CHOH 1 n3n0,02mol Bảo toàn khối lượng: m5,320,06.400,02.925,88gam6gam
Xét phản ứng đốt cháyX: Bảo
tố O: 2 2 2 OHOOX CO n2nn n 0,523xmol 2 Bảo toàn khối lượng: 2 2 2 OCOHOmmmm 9,3276x0,77.320,523x.440,5.18x0,01mol
2 2 2 COHO CO X nn n0,55molk 16 n → Số liên kết 2Br CC COO n 633a0,04mol 3 Câu 9: Xét phản ứng đốt cháymgam chất béo: Bảo toànnguyên tố O:
6n2n2nnn0,02mol
toàn khối lượng:
XOCOHOX
mmmmm17,72gamM886 Xétcho7,088gam chất béotác dụng vừa đủ với dung dịch NaOH: X n0,008mol Phương trìnhhóa học:
35 35 3 3 RCOOCH3NaOH3RCOONaCHOH
0,0080,024 0,008mol Bảo toàn khối lượng:
CHƯƠNG 2: CACBOHIĐRAT
BÀI 3: CACBOHIĐRAT
Mục tiêu
Kiến thức
+Phát biểu được khái niệm vàphân loại cacbohiđrat.
+Trìnhbày được công thức cấu tạo, tính chất vật lí (trạng thái,màu,mùi, nhiệt độ nóng chảy, độ tan), ứng dụng của glucozơ.
+Trình bày được tính chất hóa học của glucozơ: tính chất của ancol đa chức, anđehit đơn chức; phản ứng lênmen rượu.
+ Chỉ ra được công thức phân tử, đặc điểm cấu tạo, tính chất vật lí, ứng dụng của saccarozơ, xenlulozơ vàtinh bột.
+Phân tích được tính chất hóa học của saccarozơ, tinh bột và xenlulozơ: tính chất chung (thủy phân), tính chất riêng (phản ứng của hồ tinh bột với iot, phản ứng của xenlulozơ với axit HNO3).
Kĩ năng
+ Viết được các phương trìnhhóa học minh họa tính chất hóa học của các chất.
+Phân biệt glucozơ vàglixerol, glucozơ và fructozơ bằng phương pháphóa học.
+Phân biệt được saccarozơ, tinh bột, xenlulozơ với các chất khác.
+ Giải được cácbài tập hóa học cóliênquan dựa trên phương trìnhhóa học vàcác định luật bảo toàn như: tính khối lượng của glucozơ trong phản ứng, hiệu suất phản ứng, độ rượu…
DẠYKÈMQUYNHƠN
Trang1
OFFICIAL
I. LÍ THUYẾT TRỌNG TÂM
Cacbohiđrat là những hợp chất hữu cơ tạp chức, có công thức chunglà . n2mCHO Phân loại:
Monosaccarit là nhóm cacbohiđrat đơn giản nhất, không thủy phân được.
Ví dụ: Glucozơ, fructozơ.
Ví dụ: Saccarozơ, mantozơ.
Đisaccarit là nhóm cacbohiđrat mà khi thủy phân mỗi phân tử sinhrahaiphân tử monosaccarit.
Ví dụ: Tinh bột, xenlulozơ.
Polisaccaritlànhóm cacbohiđrat phức tạp, khi thủy phân đến cùng mỗi phân tử sinhra nhiều phân tử monosaccarit.
A. Monosaccarit: C6H12O6
1. Glucozơ
a. Tính chất vật lí và trạng thái tự nhiên Chất rắn, dạng kết tinh,khôngmàu,có vị ngọt.
b. Tính chất hóa học Làm mất màudung dịch brom. Phản ứng với Cu(OH)2: 2C6H12O6 +Cu(OH)2 → (C6H11O6)2Cu+2H2O (xanh lam) Khử bằng hiđro: C6H12O6 +H2 C6H14O6 Ni,t Phản ứng tráng bạc: 1C6H12O6 2Ag 33AgNO/NH Phản ứng lênmen: C6H12O6 2C2H5OH+2CO2 ↑ enzim 3035C c. Điều chế, ứng dụng Điều chế trongcông nghiệp: Thủy phântinh bột (xúctácHClloãng hoặc enzim). Thủy phân xenlulozơ (xúctácH2SO4 đặc). Ứng dụng: Là chất dinh dưỡng, thuốc tăng lực cho trẻ em và người ốm.
Dùng để tráng gương, tráng ruột phích. Là sản phẩm trunggianchoquátrình sản xuất ancoletylic.
2. Fructozơ
a. Tính chất vật lí và trạng thái tự nhiên
OFFICIAL
Glucozơ đặc biệt có nhiều trong quả nho chín nên được gọi là đường nho. Công thức cấu tạo Mạch hở: 2 CHCHCHCHCHCHO |||||
OHOHOHOHOH
Mạch vòng (α-glucozơ và β-glucozơ) là dạng tồn tại chủ yếu.
Fructozơ có nhiều trong mật ong.
DẠYKÈMQUYNHƠN
Trang2
Chất kết tinh,khôngmàu, dễ tantrong nước, có vị ngọt.
b. Tính chất hóa học Phản ứng với Cu(OH)2: C6H12O6 +Cu(OH)2 → (C6H11O6)2Cu+2H2O (xanh lam) Khử bằng hiđro: C6H12O6 +H2 C6H14O6 Ni,t Phản ứng tráng bạc: 1C6H12O6 2Ag 33AgNO/NH Khônglàm mất màu nước brom. B. Đisaccarit (Saccarozơ: C12H22O11)
a. Tính chất vật lí và trạng thái tự nhiên Chất rắn kết tinh,khôngmàu,khôngmùi,có vị ngọt.
b. Tính chất hóa học Phản ứng thủy phân: C12H22O11 +H2O C6H12O6 +C6H12O6 H,t Saccarozơ Glucozơ Fructozơ Phản ứng với Cu(OH)2: 2C12H22O11 +Cu(OH)2 → (C12H21O11)Cu+2H2O (xanh lam) c. Sản xuất và ứng dụng Sản xuất: Từ câymía, củ cải đường hoặc hoa thốt nốt. Ứng dụng: Là thực phẩm quan trọng của con người. Pha chế thuốc. Là nguyên liệu để thủy phân thành glucozơ và fructozơ dùngtrong kĩ thuật tráng gương, tráng ruột phích.
C. Polisaccarit: (C6H10O5)n
Công thức cấu tạo (fructozơ là đồng phân cấu tạo của glucozơ). Mạch hở: 2 2CHCHCHCHCHCH |||||||
OHOHOHOHOOH Mạch vòng (α-fructozơ và β-fructozơ) là dạng tồn tại chủ yếu.
Chú ý: Trong môi trường bazơ: Fructozơ Glucozơ OH
Nên fructozơ cũng tham gia phản ứng tráng bạc.
Chú ý: Dùng nước brom để phân biệt glucozơ và fructozơ.
Saccarozơ có nhiều nhất trong cây mía, củ cải đường và hoa thốt nốt, còn có tên là đường mía, đường củ cải,… Saccarozơ được cấu tạo từ một gốc glucozơ và một gốc fructozơ liên kết với nhau qua nguyên tử oxi nên khi thủy phân trong môi trường axit thu được glucozơ và fructozơ.
Chú ý: Saccarozơ không làm mất màu dung dịch nước brom và không tham gia phản ứng tráng bạc.
1. Tinh bột
a. Tính chất vật lí, cấu trúc phân tử
Chất rắn vô định hình, màu trắng, không tan trong nước lạnh, trong nước nóng bị trương lên tạo thành dung dịch
DẠYKÈMQUYNHƠN
Trang3
OFFICIAL
keo gọi là hồ tinh bột. Cóhai dạng: Amilozơ: khôngphânnhánh, chứa liên kết α-1,4-glicozit. Amilopectin:phânnhánh, chứa liên kết α-1,4-glicozit và α1,6-glicozit.
b. Tính chất hóa học Phản ứng thủy phân: (C6H10O5) +nH2O nC6H12O6 n H,t Phản ứng màu với iot: Hồ tinh bột Xanh tím Mất màu iot t denguoi Xanhtím
c. Tổng hợp, ứng dụng Tổng hợp: Tinh bột được tạo thànhtrongcâyxanh nhờ quá trìnhquang hợp, theo sơ đồ phản ứng: CO2 C6H12O6 (C6H10O5) 2 HO,as chatdiepluc n
Ứng dụng: Chất dinh dưỡng cơ bản của con người và động vật. Sản xuất bánh kẹo, glucozơ và hồ dán.
2. Xenlulozơ
a. Tính chất vật lí và trạng thái tự nhiên Chất rắn dạng sợi, màu trắng, khôngmùi vị. Khôngtantrong nước và nhiều dungmôi hữu cơ, nhưng lại tantrong nước Svayde(Cu(OH)2/NH3) Có nhiều trongbông, gỗ… b. Tính chất hóa học
Tinh bột được tạo thành từ các gốc glucozơ nên khi thủy phân hoàn toàn tạo glucozơ.
Chú ý: Khi cho tinh bột vào dung dịch iot tạo thành hợp chất bọc có màu xanh tím.
Tương tự như tinh bột, xenlulozơ thủy phân cũng tạo glucozơ.
Chú ý: Xenlulozơ trinitrat được ứng dụng vào làm thuốc súng không khói.
DẠYKÈMQUYNHƠN
Trang4
OFFICIAL
+nH
O nC
6 n H,t
: [C
3] +3nHNO3 n 24 HSOdac,t dac [C
2)3] +3nH2O n
Phản ứng thủy phân: (C6H10O5)
2
6H12O
Phản ứng với HNO3
6H7O2(OH)
6H7O2(ONO
Xenlulozơ trinitrat c. Ứng dụng Nguyên liệu chứa xenlulozơ được sử dụng trực tiếp hoặc chế biến thành giấy. Lànguyên liệu để sản xuất tơ nhân tạo: tơ visco, tơ axetat,
chế tạo thuốc súngkhôngkhóivà chế tạo phim ảnh. SƠ ĐỒ HỆ THỐNG HÓA
Dạng mạch vòng (α-glucozơ và β-glucozơ) là dạng tồn tại chủ yếu.
Chất kết tinh không màu, dễ tan trong nước, vị ngọt nhưng không ngọt bằng đường mía. Có nhiều trong quả nho chín, mật ong (30%), máu (0,1%).
Tính chất của ancol đa chức dkthuong 6126 6116 2 2 2 2CHOCuOHCHOCu2HO
xanh lam
Phản ứng tráng gương (tráng bạc) 33AgNO/NH Glucozo2Ag
Phản ứng làm mất màu dung dịch nước brom 22 GlucozoBrHOAxitgluconic2HBr
Phản ứng lên men rượu enzim 6126 25 2 3035C CHO2CHOH2CO
Trongcông nghiệp Hhoacenzim 61052 6126 n CHOnHOnCHO
Thuốc tăng lực, tráng gương, tráng ruột phích. Mạch hở: 6 54321 2 2 CHOHCHOHCHOHCHOHCOCHOH
Chất kết tinh,khôngmàu, dễ tantrong nước, vị ngọt hơn đường mía. Có nhiều trong dứa, xoài, mật ong(40%). OH GlucozoFructozo → Ngoài tính chất của ancol đa chức, fructozơ còn có phản ứng tráng gương. Chú ý: Fructozơ không phản ứng với dung dịch nước brom nên dùng dung dịch brom để phân biệt glucozơ và frutozơ. Ni,t 61262 6146
Cấu tạo phân tử
Tính chất vật lí
Tính chất hóa học Điều chế Ứng dụng Cấu tạo phân tử
MONOSACCARIT (không thủy phân được)
Tính chất vật lí
Fructozơ
Tính chất hóa học
DẠYKÈMQUYNHƠN
Trang5
OFFICIAL
Mạch hở: 2 CHCHCHCHCHCHO ||||| OHOHOHOHOH
CHOHCHO Glucozơ/Fructozơ Sobitol
Glucozơ
Saccarozơ
Cấu tạo phân tử
Tính chất vật lí Tính chất hóa học
DISACCARIT
(Thủy phân tạo ra 2 phân tử monosaccarit)
POLISACCARIT
(Thủy phân hoàn toàn tạo ra nhiều phân tử monosaccarit)
Cấu tạo phân tử
Tính chất vật lí Tính chất hóa học
Saccarozơ được cấu tạo từ một gốc glucozơ và một gốc fructozơ liên kết quanguyên tử O.
Chất kết tinhkhôngmàu, dễ tantrong nước, vị ngọt. Tính chất của ancol đa chức:
xanh lam Phản ứng thủy phân: Hhoacenzim SaccarozoGlucozoFructozo
Không có phản ứng tráng bạc.
CACBOHIĐRAT n2mCHO
Amilozơ: khôngphânnhánh, chứa liên kết α-1,4-glicozit. Amilopectin: phân nhánh, chứa liên kết α-1,4-glicozit và α-1,6-glicozit.
Tinh bột là chất rắn, vô định hình,màu trắng. Hồ tinh bột Xanh tím Mất màu iot t Xanhtím denguoi Phản ứng thủy phân Hhoacenzim 61052 6126 n CHOnHOnCHO
DẠYKÈMQUYNHƠN
Trang6
OFFICIAL
122211 122111 2 2 2 2CHOCuOHCHOCu2HO
Phản ứng quang hợp ở cây xanh anhsangmattroi 22 61052dieplucclorophin n 6nCO5nHO CHO6nO Tinh bột Xenlulozơ Tính chất vật lí Tính chất hóa học Xenlulozơ là chất rắn, dạng sợi, màu trắng. Xenlulozơ tác dụng với 3HNO 24 HSOdac,t 672 3dac 3n CHOOH3nHNO 672232 n CHOONO3nHO Xenlulozơ trinitrat Xenlulozơ trinitrat được dùng làm thuốc súng không khói. Phản ứng thủy phân: Hhoacenzim 61052 6126 n CHOnHOnCHO
II. CÁC DẠNG BÀI TẬP
Dạng 1: Lí thuyết trọng tâm Ví dụ mẫu
Ví dụ 1: Trongphân tử các cacbohiđrat luôncó
A. nhóm chức xeton.
C. nhóm chức ancol.
Hướng dẫn giải
B. nhóm chức axit.
D. nhóm chức anđehit.
Trongphân tử của cacbohiđrat luôncónhóm chức ancol.
→ Chọn C.
Ví dụ 2: Các chất nào sau đây đều có phản ứng thủy phân trong môi trường axit?
A. Tinh bột, xenlulozơ, saccarozơ.
B. Tinh bột, saccarozơ, fructozơ.
C. Tinh bột, xenlulozơ, fructozơ.
D. Tinh bột, xenlulozơ, glucozơ.
Hướng dẫn giải
Glucozơ và fructozơ làmonosaccaritnênkhông bị thủy phân.
→ Loại B,C,D. Saccarozơ là đisaccarit, tinh bột và xenlulozơ là polisaccarit đều bị thủy phântrongmôi trường axit.
→ Chọn A.
Ví dụ 3: Để phân biệt glucozơ và fructozơ, người tadùng thuốc thử nào sau đây?
A. AgNO3/NH3 B. Nước Br2 C. Cu(OH)2 D. H2/Ni, . t
Hướng dẫn giải
A sai vì cả glucozơ và fructozơ đều phản ứng được với AgNO3/NH3 tạo ra chất rắn Ag.
B đúng vì glucozơ chứa nhóm chức anđehit (CHO)nêncó khả năng làm mất màu nước Br2 còn fructozơ thìkhông. Csaivì cả glucozơ và fructozơ có nhiều nhómOH liền kề nên đều phản ứng với Cu(OH)2 tạo phức màuxanhlam. D sai vì cả glucozơ và fructozơ đều là hợp chất cacbonyl (nhóm chức andehitCHOvàxetonC=O)nên đều phản ứng được với H2 → Chọn B. Ví dụ 4: Phát biểu nàosau đây là sai? A. Xenlulozơ là chất rắn khôngmàu,khôngmùi,khôngtantrong nước.
Glucozơ và fructozơ có 5 nhóm OH (dùng phản ứng este hóa với anhiđrit axetic (CH3CO)2O để chứng minh), saccarozơ có 8 nhóm OH, mỗi mắt xích của xenlulozơ có 3 nhóm OH.
DẠYKÈMQUYNHƠN
Trang7
OFFICIAL
B. Saccarozơ dùng để pha chế thuốc.
C. Tinh bột và xenlulozơ không phải là đồng phân của nhau.
D. Để chứng minh glucozơ có5nhómOH, người tadùng phản ứng với (CH3CO)2O.
Hướng dẫn giải
A sai vì xenlulozơ là chất rắn màu trắng, không mùi, không tan trong nước.
B đúng vì ứng dụng của saccarozơ trongcông nghiệp dược phẩm làdùng để pha chế thuốc.
C đúng vì tinh bột và xenlulozơ có công thức phân tử là (C6H10O5)n nhưng không phải là đồng phândo hệ số nkhácnhau.
D đúng vì để chứng minh glucozơ có 5 nhóm OH, người ta dùng phản ứng với anhiđrit axetic(CH3CO)2O tạo este.
OFFICIAL
→ Chọn A.
Ví dụ 5: Cho các chất: dung dịch saccarozơ, glixerol, ancol etylic, etyl axetat. Số chất phản ứng với Cu(OH)2 ở điều kiện thường là
A. 1 B. 2 C. 3 D. 4
Hướng dẫn giải
Các chất phản ứng với Cu(OH)2 ở điều kiện thường là các chất có nhiều hơn OH kề nhau hoặc axit.
→ Các chất phản ứng với Cu(OH)2 ở điều kiện thường trongdãytrênlà: saccarozơ, glixerol.
→ Chọn B.
Ví dụ 6: Trong các chất sau: benzen, axetilen, glucozơ, axit fomic, anđehit axetic,etilen, saccarozơ, fructozơ, metylfomat. Số chất tác dụng được với dung dịch AgNO3 trongNH3 để tạo ra kết tủa Aglà A. 7 B. 5 C. 6 D. 4
Hướng dẫn giải Các chất tác dụng được với dung dịch AgNO3 trongNH3 để tạo ra kết tủa Aglà: glucozơ, axitfomic, anđehit axetic, fructozơ, metylfomat.
→ Chọn B.
Chú ý: Các chất tác dụng được với dung dịch AgNO3 trong NH3 là: Các anđehit. Axit fomic (HCOOH). Muối của axit fomic. Este của axit fomic ( ). HCOOR Glucozơ, fructozơ. Ank-1-in (nhưng không phải phản ứng tráng bạc nên không tạo ra kết tủa Ag).
Ví dụ 7: Chocácphát biểu sau:
DẠYKÈMQUYNHƠN
Trang8
(1)Amilopectincó cấu trúc mạch phânnhánh.
(2) Thủy phân saccarozơ trong môi trường axit thu được hai phân tử glucozơ.
(3) Fructozơ phản ứng được với AgNO3/NH3 do phân tử chứa nhóm CHO. Số phát biểu đúng là:
A. 0 B. 1 C. 2 D. 3 Hướng dẫn giải
(1) đúng vìamilopectincó cấu trúc mạch phânnhánhcòn amilozơ có cấu trúc mạch khôngphânnhánh.
(2)saivì saccarozơ được cấu tạo bởi một phân tử glucozơ và một phân tử fructozơ nênkhi thủy phânthu được một phân tử glucozơ và một phân tử fructozơ.
OFFICIAL
(3) sai vì fructozơ không có nhóm anđehit CHO nhưng vẫn phản ứng tráng gương được vì trong môi trường bazơ (OH) fructozơ chuyển hóa thành glucozơ.
→ Chọn B. Bài tập tự luyện dạng 1 Bài tập cơ bản
Câu 1: Chất nàosau đây làpolisaccarit?
A. Glucozơ. B. Fructozơ. C. Tinh bột. D. Saccarozơ. Câu 2: Glucozơ cócông thức phân tử là
A. C6H10O5 B. C12H22O11 C. C6H12O6 D. C5H10O5 Câu 3: “Đường mía”là thương phẩm có chứa chất nào dưới đây?
A. Glucozơ. B. Tinh bột. C. Fructozơ. D. Saccarozơ. Câu 4: Chất nàosau đây là đồng phân của glucozơ?
A. Xenlulozơ. B. Fructozơ. C. Saccarozơ. D. Tinh bột. Câu 5: Trong công nghiệp, để sản xuất gương soi và ruột phích, người ta cho dung dịch AgNO3 trong NH3 tác dụng với chất nàosau đây?
A. Saccarozơ. B. Axetilen. C. Andehitfomic. D. Glucozơ. Câu 6: Số nhóm hiđroxit (OH)trongphân tử glucozơ là
A. 5 B. 6 C. 3 D. 4 Câu 7: Ở nhiệt độ thường, nhỏ vài giọt dung dịch iotvàolát cắt củ khoailang thấy xuất hiện màu A. đỏ. B. xanhtím. C. nâu đỏ. D. hồng.
Câu 8: Saccarozơ không thamgia phản ứng nàosau đây?
A. Thủy phân với xúctácenzim. B. Thủy phân nhờ xúctácaxit.
C. Phản ứng với Cu(OH)2 tạo dung dịch xanhlam.
DẠYKÈMQUYNHƠN
Trang9
D. Tráng bạc.
Câu 9: Khi bị ốm, mất sức hoặc saucácca phẫu thuật, nhiều người bệnh thường được truyền dịch để
thể sớm hồi phục. Chất trong dịch truyền cótác dụng trênlà
A. axitaxetic. B. glucozơ. C. saccarozơ. D. ancoletylic.
Câu 10: Fructozơ không phản ứng với
A. nước brom. B. dung dịch AgNO3/NH3
C. H2/Ni (đun nóng). D. Cu(OH)2.
Câu 11: Glucozơ không cótính chất nào?
A. Tính chất của nhóm anđehit.
B. Thamgia phản ứng thủy phân.
C. Tính chất của ancol đa chức. D. Lênmen tạo ancoletylic.
Câu 12: Phát biểu nàosau đây là sai?
A. Glucozơ và fructozơ đều có phản ứng tráng bạc.
B. Glucozơ và fructozơ là đồng phân cấu tạo của nhau.
C. Saccarozơ bị thủy phântrongmôi trường axitkhi đun nóng.
D. Choiotvào hồ tinh bột xuất hiện màutím đặc trưng.
Câu 13: Ứng dụng nàosau đây không phải của glucozơ?
A. Sản xuất rượu etylic.
C. Nhiên liệu cho động cơ đốt trong.
Câu 14: Phát biểu nàosau đây đúng?
OFFICIAL
B. Tráng gương, tráng ruột phích.
D. Thuốc tăng lực trongy tế.
A. Dung dịch saccarozơ phản ứng với Cu(OH)2 tạo dung dịch màuxanhlam.
B. Xenlulozơ bị thủy phântrongdung dịch kiềm đun nóng.
C. Glucozơ bị thủy phântrongmôi trường axit.
D. Tinh bột có phản ứng tráng bạc.
Câu 15: Dãy gồm các chất đều bị thủy phântrongdung dịch H2SO4 đun nónglà:
A. Glucozơ, saccarozơ và fructozơ.
B. Fructozơ, saccarozơ vàtinh bột.
D. Saccarozơ, tinh bột và xenlulozơ. Câu 16: Cho các tính chất sau: (1) dạng sợi; (2) tan trong nước; (3) tan trong dung dịch Svayde; (4) tác dụng với dung dịch HNO3 /H2SO4 ;(5)tráng bạc; (6) thủy phân. Xenlulozơ cócáctính chất là: dd
C. Glucozơ, tinh bột và xenlulozơ.
A. (1),(3),(4),(5). B. (1),(3),(4),(6). C. (2),(3),(4),(6). D. (1),(2),(3),(6). Câu 17: Chocácdãy chất: tinh bột, xenlulozơ, glucozơ, fructozơ, saccarozơ. Số chất trongdãy thuộc loại monosaccaritlà
A. 2. B. 4. C. 3. D. 1. Câu 18: Dãy gồm cácdung dịch đều tác dụng với Cu(OH)2 là:
A. Glucozơ, glixerol,natriaxetat. B. Glucozơ, glixerol,axitaxetic. C. Glucozơ, anđehit fomic,kaliaxetat. D. Glucozơ, glixerol,ancoletylic. Câu 19: Thủy phânhoàntoàntinh bột trongdung dịch axitvô cơ loãngthu được chất X.ChoX phản ứng với khíH2 (Ni, )thu được hợp chất hữu cơ Y.Các chất X,Y lần lượt là: t
A. Glucozơ, sobitol. B. Glucozơ, fructozơ. C. Glucozơ, etanol. D. Glucozơ, saccarozơ.
Câu 20: Chocácphát biểu sau: (1) Fructozơ và glucozơ đều có khả năng thamgia phản ứng tráng bạc.
DẠYKÈMQUYNHƠN
Trang10
cơ
(2) Saccarozơ vàtinh bột đều không bị thủy phânkhicóaxitH2SO4 (loãng)làmxúctác.
(3)Tinh bột được tạo thànhtrongcâyxanh nhờ quátrìnhquang hợp.
(4) Xenlulozơ và saccarozơ đều thuộc loại đisaccarit.
Phát biểu đúng là
A. (2)và(4). B. (1)và(3). C. (3)và(4). D. (1)và(2).
Câu 21: Đặc điểm giống nhau giữa glucozơ và saccarozơ là
A. đều thamgia phản ứng tráng gương.
B. đều hòatanCu(OH)2 ở nhiệt độ thường chodung dịch màuxanhlam.
C. đều có phản ứng thủy phântrongmôi trường axit.
D. đều được sử dụng trongy học làm “huyết thanh ngọt”.
Bài tập nâng cao
Câu 22: Cacbohiđrat Xcó đặc điểm:
Bị thủy phântrongmôi trường axit.
Thuộc loại polisaccarit.
Phân tử gồm nhiều gốc β-glucozơ.
Cacbohiđrat Xlà
OFFICIAL
A. glucozơ. B. saccarozơ. C. xenlulozơ. D. tinh bột.
Câu 23: Chocácphát biểu sau:
(a) Thủy phânhoàntoàn saccarozơ vàtinh bột đều chỉ thu được glucozơ.
(b) Saccarozơ và xenlulozơ đều thuộc loại đisaccarit.
(c) Người tadùngdung dịch brom để phân biệt glucozơ và fructozơ.
(d) Glucozơ khử hiđro thu được axitgluconic.
(e) Xenlulozơ axetatlà thuốc súngkhôngkhói.
(f) Mỗi mắt xíchtrongphân tử xenlulozơ cóbanhómOH.
Số phát biểu sai là
A. 1 B. 2 C. 3 D. 4
Câu 24: Chocácphát biểu sau:
(a)Công thức hóa học của xenlulozơ là[C6H7O2(OH)3]. n
(b) Amilozơ được tạo thành từ các gốc α-glucozơ liên kết với nhau bằng liên kết α-1,4-glicozit.
(c)Phân tử saccarozơ được cấu tạo bởi hai gốc glucozơ.
(d)Tinh bột và xenlulozơ làhai đồng phân của nhau.
Số phát biểu đúng là
A. 3 B. 2 C. 1 D. 4
Câu 25: Chocácphát biểu sau:
(a) Hiđro hóahoàntoàn glucozơ tạo raaxitgluconic.
(b) Phản ứng thủy phân xenlulozơ xảy ra được trong dạ dày của động vật ăn cỏ.
(c) Xenlulozơ trinitratlànguyên liệu để sản xuất tơ nhân tạo.
(d) Xenlulozơ bị hóa đen trongH2SO4 đặc.
(e)Trongcông nghiệp dược phẩm, saccarozơ được dùng để pha chế thuốc.
DẠYKÈMQUYNHƠN
Trang11
Trongcácphát biểu trên, số phát biểu đúng là
A. 3 B. 2 C. 4 D. 5
Dạng 2: Phản ứng oxi hóa – khử
Bài toán 1: Phản ứng tráng bạc
Phương pháp giải Phản ứng tráng gương: Glucozơ +2AgNO3 +3NH3 +H2O → Amonigluconat+2Ag+2NH4NO3 Fructozơ +2AgNO3 +3NH3 +H2O → Amonigluconat+2Ag+2NH4NO3
Ví dụ: Đun nóng dung dịch chứa 18 gam glucozơ với lượng vừa đủ dung dịch bạc nitrat trong amoniac đến phản ứng hoàn toàn. Khối lượng bạc đã sinhralà A. 10,8gam. B. 43,2gam. C. 21,6gam. D. 32,4gam. Hướng dẫn giải glucozo n0,1mol Tacó: Glucozơ 2Ag 33AgNO/NH 0,1 → 0,2 mol Ag m21,6gam → Chọn C. Ví dụ mẫu Ví dụ 1: Cho 500 ml dung dịch glucozơ phản ứng hoàn toàn với lượng dư dung dịch AgNO3 trong NH3, thu được 21,6 gam Ag. Nồng độ của dung dịch glucozơ đã dùnglà A. 0,02M B. 0,20M C. 0,10M D. 0,01M Hướng dẫn giải Ag n0,2mol Tacó: Glucozơ 2Ag 33AgNO/NH 0,1 0,2 mol Nồng độ của dung
Nhận xét: 1Glucozơ/Fructozơ → 2Ag
OFFICIAL
DẠYKÈMQUYNHƠN
Trang12
dịch glucozơ đã dùnglà: M C0,10,2M 0,5 → Chọn B. Ví dụ 2: Đun nóng m gam glucozơ với lượng AgNO3 trong NH3 dư thu được 54gamAg. Biết hiệu suất của phản ứng là75%.Giá trị của mlà A. 45,00. B. 33,75. C. 67,50. D. 60,00. Hướng dẫn giải Ag n0,5mol Chú ý:
Tương tự như các bài
toán hiệu suất. Các bạn xem lại phương pháp ở Chương 1 – Bài 1 – Dạng 3. Bài toán 2: Phản ứng đốt cháy Phương pháp giải
Phản ứng đốt cháy Phương trìnhhóa học: t n2 2 22 m CHOnOnCOmHO Nhận xét: 22 OCOnn Cách 1: Bảo toàn khối lượng:
cacbohidratOCOHO mmmm
một
CO HO
Với thì H75% glucozo mm45:75%60gam n6 n5
DẠYKÈMQUYNHƠN OFFICIAL Trang13
2 22
Đốt cháy
số cacbohiđrat: Với Cacbohiđrat là glucozơ hoặc 2 2 CO HO n 1 n fructozơ.
2 2 CO HO n12 n11
Nếu : Glucozơ 2Ag H100% 33AgNO/NH 0,25 0,5 mol glucozo m0,25.18045gam 2 2
→ Chọn D.
Cách 2: 2 cacbohidratCHOmmm
Với Cacbohiđrat là saccarozơ.
Với Cacbohiđrat là tinh bột hoặc
xenlulozơ.
Ví dụ: Đốt cháy hoàn toàn m gam hỗn hợp gồm tinh bột, glucozơ và saccarozơ cần 5,376 lít O2 (đktc), thu được 3,96gam nước. Giá trị của mlà A. 4,68. B. 6,84. C. 8,64. D. 6,48. Hướng dẫn giải 2 2 O HO n0,24mol;n0,22mol
Đốt cháy cacbohiđrat luôncó: 22 COO nn0,24mol
Bảo toàn khối lượng: 2 22 OCOHOmmmm m0,24320,24440,2218
m10,563,967,68 m6,84gam Cách 2: Tacó: 2 cacbohidratCHOmmm 0,24.123,966,84gam → Chọn B.
Ví dụ mẫu
Ví dụ 1: Đốt cháyhoàntoànagam một cacbohiđrat X cần dùngVlítO2 thu được 13,44 lít CO2 và 10,8 gam H2O. Biết , các khí X 170M190 đo ở đktc. Xcócông thức phân tử là A. . B. C6H12O6. C. C3H5(OH)3. D. C2H4(OH)2. 6105nCHO Hướng dẫn giải 2 2 CO HO n0,6mol;n0,6mol
Gọi công thức phân tử đơn giản nhất của Xlà . n2mCHO
CO HO nn0,61 mn0,6
COO nn0,4mol
DẠYKÈMQUYNHƠN
Trang14
OFFICIAL
22
Ta có: Công thức phân tử đơn giản nhất của X là 2 2 CO2 +Ba(OH)2 → BaCO3 +H2O 0,4 → 0,4 mol 3BaCO mm0,419778,8gam → Chọn D. Bài tập tự luyện dạng 2 Bài tập cơ bản Câu 1: Cho9,0gam
CH2O. → Công thức phân tử của Xlà . 2xCHO Tacó: 17030x190 5,6x6,3 x6 Vậy công thức phân tử của XlàC6H12O6. → Chọn B. Ví dụ 2: Đốt cháyhoàntoàn cacbohiđrat X cần 8,96lítkhíO2 (đktc) thu được CO2 và H2O. Hấp thụ hoàn toàn sản phẩm cháy bằng dung dịch Ba(OH)2 dư thu được mgam kết tủa. Giá trị của mlà A. 19,7 B. 39,4 C. 59,1 D. 78,8 Hướng dẫn giải 2O n0,4mol Đốt cháy cacbohiđrat luôncó:
Sản phẩm cháy được hấp thụ hoàntoàn bằng dung dịch Ba(OH)2 dư:
glucozơ phản ứng hoàntoàn với lượng dư dung dịch AgNO3 trongNH3 (đun nóng), thu được mgamAg.Giá trị của mlà A. 16,2. B. 10,8. C. 5,4. D. 21,6.
Câu 2: Đun nóng75gamdung dịch glucozơ với dung dịch AgNO3 trong dư NH3 thu được 10,8gam chất rắn. Nồng độ phần trăm của glucozơ là
A. 11%. B. 24%. C. 22%. D. 12%.
Câu 3: Hỗn hợp M gồm glucozơ và saccarozơ. Đốt cháy hoàn toàn một lượng M cần dùng vừa đủ 0,4 molO2,thu được H2OvàVlítkhíCO2 (đktc). Giá trị của Vlà
A. 6,72. B. 8,96. C. 10,08. D. 111,20. Câu 4: Cho250mldung dịch glucozơ phản ứng hoàntoàn với lượng dư dung dịch AgNO3 trongNH3 thu được 5,4gamAg. Nồng độ mol của dung dịch glucozơ đã dùnglà A. 0,10M B. 0,20M C. 0,50M D. 0,25M Câu 5: Đun nóng m gam glucozơ với lượng dư dung dịch AgNO3 trong dư NH3 thu được 54 gam Ag. Biết hiệu suất phản ứng là75%.Giá trị của mlà
A. 45,00. B. 33,75. C. 67,50. D. 60,00. Câu 6: Đốt cháyhoàntoànmgam hỗn hợp gồm xenlulozơ, tinh bột, glucozơ và saccarozơ cần 2,52lítO2 (đktc), thu được 1,8gam nước. Giá trị của mlà
OFFICIAL
A. 3,06. B. 5,25. C. 3,15. D. 6,02. Câu 7: Người ta thường dùng glucozơ để tráng ruột phích. Trung bình phải cần dùng 0,72 gam glucozơ cho một ruột phích, biết hiệu suất của toànquátrìnhlà80%. Khối lượng bạc cótrong ruột phíchlà
A. 0,8640gam B. 0,6912gam C. 1,0800gam D. 0,9000gam Câu 8: Cho dung dịch chứa m gam hỗn hợp gồm glucozơ và fructozơ tác dụng với lượng dư dung dịch AgNO3/NH3, đun nóngthu được 38,88gamAg.Giá trị của mlà
A. 48,6. B. 32,4. C. 64,8. D. 16,2. Câu 9: Đốt cháy hoàn toàn một lượng hỗn hợp X chứa glucozơ, fructozơ, saccarozơ cần dùng vừa đủ 37,632 lít khí O2 (đktc) thu được CO2 và H2O. Cho toàn bộ sản phẩm cháy qua dung dịch Ba(OH)2 dư thấy cómgam kết tủa xuất hiện. Giá trị của mlà
A. 330,96. B. 165,48. C. 197,00. D. 220,64. Câu 10: Hòatan6,12gam hỗn hợp X gồm glucozơ và saccarozơ vào nước được dung dịch Y.Chodung dịch Y tác dụng với lượng dư dung dịch AgNO3/NH3 thu được 3,24 gam Ag. Phần trăm khối lượng saccarozơ cótrong hỗn hợp Xlà
A. 44,1%. B. 55,9%. C. 70,6%. D. 35,3%. Bài tập nâng cao Câu 11: Chiamgam hỗn hợp gồm glucozơ và fructozơ thànhhai phần bằng nhau: Phần một: Chotác dụng với lượng dư dung dịch AgNO3/NH3 thu được 86,4gamAg. Phần hai:Làm mất màu vừa hết dung dịch chứa 35,2gamBr2 Thành phần phần trăm khối lượng fructozơ trong hỗn hợp ban đầu là
A. 32,4%. B. 55,0%. C. 16,2%. D. 45,0%. Câu 12: Đốt cháy hoàn toàn a gam cacbohiđrat X cần 6,72 lít khí O2, sau phản ứng thu được CO2 và H2O. Hấp thụ hết sản phẩm cháy bằng dung dịch nước vôitrong dư, thấy khối lượng dung dịch nước vôi trong giảm 11,4gam.X thuộc loại
A. polisaccarit. B. monosaccarit. C. trisaccarit. D. đisaccarit.
DẠYKÈMQUYNHƠN
Trang15
Câu 13: Đốt cháyhoàntoànmgam hỗn hợp X gồm xenlulozơ, glucozơ, saccarozơ bằng oxi.Toàn bộ sản phẩm cháy hấp thụ hết vàobình đựng dung dịch Ca(OH)2 dư, thấy xuất hiện gam kết tủa và m185,6 khối lượng bình tăng gam.Giá trị của mlà m83,2
A. 74,4. B. 80,3. C. 51,2. D. 102,4. Dạng 3: Phản ứng thủy phân Bài toán 1: Thủy phân saccarozơ Phương pháp giải
Ví dụ: Thủy phân hoàn toàn 1 mol saccarozơ thu được sản phẩm là
OFFICIAL
Thủy phân saccarozơ: C12H22O11 +H2OC6H12O6 +C6H12O6 H Glucozơ Fructozơ Chú ý: Khi thủy phân saccarozơ thu được sản phẩm chứa glucozơ và fructozơ, sau đó cho sản phẩm phản ứng với AgNO3 trong NH3: Agsaccarozon4n
A. 180gam glucozơ và180gam fructozơ. B. 360gam glucozơ. C. 360gam glucozơ và360gam fructozơ. D. 360gam fructozơ. Hướng dẫn giải Quátrình phản ứng: C12H22O11 +H2O Glucozơ + Fructozơ H 1 1 1 mol glucozofructozo mm1.180180gam → Chọn A.
Ví dụ mẫu Ví dụ 1: Thủy phânhoàntoàn0,01mol saccarozơ trongmôi trường axit, với hiệu suất là 60%, thu được dung dịch X. Trung hòa dung dịch X thu được dung dịch Y, đem toàn bộ dung dịch Ytác dụng với lượng dư dung dịch
DẠYKÈMQUYNHƠN
Trang16
A.
giải Nếu H=100%:Quátrình phản ứng: C12H22O11 +H2O Glucozơ + Fructozơ 4Ag H 33AgNO/NH 0,01 0,01 0,01 0,04 mol Ag m0,04.1084,32gam Với H=60% Ag m4,3260%2,592gam → Chọn B. Bài toán 2: Thủy phân xenlulozơ/tinh bột Phương pháp giải
AgNO3/NH3 thu được mgamAg.Giá trị của mlà
6,480. B. 2,592. C. 0,648. D. 1,296. Hướng dẫn
Thủy phântinh bột/xenlulozơ: (C6H10O5) +nH2O nC6H12O6 n H Glucozơ Coi ,tacó sơ đồ: n1 (C6H10O5) → C6H12O6 162 180 gam Ta cần ghi nhớ tỉ lệ về khối lượng trên.
Ví dụ: Cho 32,4 gam xenlulozơ đem thủy phân trong môi trường axit thu được 27 gam glucozơ. Hiệu suất của quátrình thủy phânlà
A. 50%. B. 75%. C. 80%. D. 40%. Hướng dẫn giải Coin=1,tacó sơ đồ: (C6H10O5) → C6H12O6 162 180 gam 32,4 → gam 32,4.18036 162
H=75%thì glucozothuduoc m360.75%270gam
→ Chọn D. Bài tập tự luyện dạng 3 Bài tập cơ bản Câu 1: Thủy phânhoàntoàn1kg saccarozơ thu được A. 1kg glucozơ và1kg fructozơ. B. 0,5kg glucozơ và0,5kg fructozơ. C. 1kg glucozơ. D. 0,526kg glucozơ và0,526kg fructozơ. Câu 2: Thủy phân hoàn toàn3,42 gam saccarozơ thu được dung dịch X. Cho toàn bộ dung dịch X phản ứng hết với dung dịch AgNO3/NH3 dư, đun nóng,thu được mgamAg.Giá trị của mlà A. 43,20. B. 4,32. C. 21,60. D. 2,16. Câu 3: Thủy phân202,5gamtinh bột với hiệu suất phản ứng là75%, khối lượng glucozơ thu được là
DẠYKÈMQUYNHƠN OFFICIAL Trang17
glucozotheothucte glucozotheolythuyet m H 100% m 27 100%75% 36
→ Chọn B. Ví dụ mẫu Ví dụ 1: Thủy phân324gamtinh bột với hiệu suất của phản ứng là75%, khối lượng glucozơ thu được là A. 250gam. B. 360gam. C. 300gam. D. 270gam. Hướng dẫn giải Nếu H=100%,tacó sơ đồ: (C6H10O5) → C6H12O6 162 180 gam 324 → gam 324180 360 162
Với
A. 225,00gam. B. 300,00gam. C. 168,75gam. D. 480,00gam. Câu 4: Cho32,4gam xenlulozơ đem thủy phântrongmôi trường axitthu được 28,8gam glucozơ. Hiệu suất của quátrình thủy phânlà
A. 50%. B. 75%. C. 80%. D. 40%. Câu 5: Thủy phânhoàntoàn8,55gam saccarozơ trongmôi trường axitthu được dung dịch X. Đun nóng dung dịch X với dung dịch AgNO3/NH3 dư thu được mgam chất rắn. Giá trị của mlà
A. 10,8. B. 5,4. C. 21,6. D. 16,2. Câu 6: Đem saccarozơ thủy phântrongmôi trường axitthu được 72gam glucozơ. Khối lượng saccarozơ đã đem thủy phânlà (biết hiệu suất của quátrình thủy phânlà80%)
A. 117,00gam. B. 136,80gam. C. 109,44gam. D. 171,00gam. Câu 7: Thủy phânhoàntoàn405gamtinh bột trongmôi trường axitthu được mgam glucozơ. Biết hiệu suất của quátrình thủy phânlà75%.Giá trị của mlà
OFFICIAL
A. 675,0. B. 450,0. C. 337,5. D. 600,0. Câu 8: Thủy phân hoàn toàn 150 gam dung dịch saccarozơ 10,26% trong môi trường axit vừa đủ ta thu được dung dịch X. Cho X tác dụng hoàn toàn với dung dịch AgNO3 trong NH3 thì khối lượng Ag thu được là
A. 36,94gam. B. 19,44gam. C. 15,50gam. D. 9,72gam. Câu 9: Lấy mgam saccarozơ đem thủy phântrongmôi trường axit,sau đó cho sản phẩm thủy phânvào dung dịch AgNO3/NH3 dư thu được 2,7gam chất rắn. Giá trị của mlà
A. 6,4500. B. 4,2750. C. 2,1375. D. 1,2825. Câu 10: Thủy phân 6,84 gam saccarozơ trong môi trường axit (hiệu suất phản ứng là 80%), thu được dung dịch X. Cho toàn bộ dung dịch X phản ứng hết với lượng dư dung dịch AgNO3 trong NH3, đun nóng,thu được mgamAg.Giá trị của mlà
A. 6,912. B. 3,456. C. 34,560. D. 69,120. Câu 11: Thủy phânmgamtinh bột trongmôi trường axit (giả sử sự thủy phân chỉ tạo glucozơ). Sau phản ứng, đem trung hòaaxit bằng kiềm rồi thực hiện phản ứng tráng bạc thu được m gam Ag. Hiệu suất của phản ứng thủy phântinh bột là
A. 66,67%. B. 80,00%. C. 75,00%. D. 50,00%.
Câu 12: Tiến hành thủy phânmgam gạo chứa 80%tinh bột, rồi lấy toàn bộ sản phẩm thu được thực hiện phản ứng với AgNO3/NH3 thì được 5,4 gam kết tủa. Biết hiệu suất của toàn bộ quá trình là 50%. Giá trị của mlà
A. 1,620. B. 6,480. C. 10,125. D. 2,350. Bài tập nâng cao
Câu 13: Thủy phânhoàntoàn8,55gam saccarozơ rồi chia sản phẩm thànhhai phần: Phần một: Chotác dụng với lượng dư dung dịch AgNO3/NH3 thìthu được xgam kết tủa. Phần hai:Chotác dụng với dung dịch nước brom dư thìcóygambromthamgia phản ứng. Giá trị của x,y lần lượt là A. 5,40và2,00. B. 2,16và3,20. C. 2,16và3,20. D. 4,32và3,20. Câu 14: Cho m gam hỗn hợp X gồm tinh bột và glucozơ tác dụng với dung dịch AgNO3 trong NH3 dư, đun nóng,thu được 21,6gamAg. Mặt khác, thủy phânhoàntoànXtrongmôi trường axit,thu được dung dịch Y.Dung dịch Ylàm mất màu vừa hết dung dịch chứa 32gamBr2.Giá trị của mlà
DẠYKÈMQUYNHƠN
Trang18
lượng
thì
khối lượng.
Lên men 108 gam glucozơ thu được khối
ancoletyliclàbaonhiêu?
27,6gam. B. 55,2gam.
36,8gam. D. 57,5gam.
dẫn giải
n0,6mol
A. 33,3. B. 34,2. C. 50,4. D. 17,1. Câu 15: Hỗn hợp X gồm glucozơ và saccarozơ. Thủy phânhoàntoàn7,02gamXtrongmôi trường axit, thu được dung dịch Y. Trung hòa axit trong dung dịch Y, sau đó cho thêm lượng dư AgNO3 trong dung dịch NH3, đun nóng,thu được 8,64gamAg.Thành phần phần trăm theo khối lượng của glucozơ trongX là A. 51,28%. B. 48,70%. C. 81,19%. D. 18,81%. Dạng 4: Tổng hợp ancol etylic Bài toán 1: Phản ứng lên men ancol Phương pháp giải Phản ứng lênmen rượu: C6H12O6 2C2H5OH+2CO2 menruou
có thể
DẠYKÈMQUYNHƠN
Trang19
OFFICIAL
3
CO2 +Ca(OH)2 → CaCO3 +H2
du
0,15
Nếu H=100%,tacó: 6126 2
2 glucozo
Với H=75%thì glucozobandau
180 96 88 gam Nhận xét: 25 2 CHOHCOglucozo nn2n Chú ý: Với các bài khối
lớn
ta
sử dụng tỉ lệ
Ví dụ:
lượng
A.
C.
Hướng
glucozo
Phương trìnhhóa học: C6H12O6 2C2H5OH+2CO2 menruou Tacó: 25 CHOHglucozo n2n20,61,2mol 25 CHOH m1,2.4655,2gam → Chọn B. Ví dụ mẫu Ví dụ 1: Lên men m gam glucozơ thu được khí X. Dẫn khí X vào bình đựng nước vôitrong dư thu được 15gam kết tủa. Hiệu suất quátrìnhlên menlà75%.Giá trị của mlà A. 18,0. B. 36,0. C. 20,5. D. 27,0. Hướng dẫn giải
CaCO n0,15mol
Phương trìnhhóa học:
O
0,15
mol
CHOCO 1 nn0,075mol
m0,07518013,5gam
mm13,5:75%18gam
Các em hãy quay lại bài toán về phản ứng đốt cháy (Chương 1 – Bài 1 – Dạng 5) để ghi nhớ bài toán phụ khi cho CO2 tác dụng dung dịch kiềm.
dụ mẫu Ví dụ 1: Thủy phân hoàn toàn m gam tinh bột, thu lấy toàn bộ lượng glucozơ đem lênmenthànhancoletylic với hiệu suất 50%,thu được Vlít (đktc) khí CO2 Hấp thụ hết lượng CO2 trên vào nước vôi trong dư thu được 40gam kết tủa. Giá trị của mlà A. 72,0. B. 32,4. C. 36,0. D. 64,8. Hướng dẫn giải
DẠYKÈMQUYNHƠN OFFICIAL Trang20 → Chọn A.
25 2 CHOHCOtinhbot/xenlulozo
25
ruou ddruou CHOHHO VV D.100
VVV
sơ
(C6H10O5) → C6H12O6 → 2C2H5OH+2CO2 0,2 0,4 mol tinhbot m0,2.16232,4gam Với
tinhbot m32,4:50%64,8gam →
m
Bài toán 2: Tổng hợp ancol etylic từ tinh bột/xenlulozơ Phương pháp giải
Tổng hợp ancoletylic từ tinh bột/xenlulozơ Tinh bột/xenlulozơ Glucozơ 2C2H5OH+2CO2 H
enzim,3035C Coin=1,tacó sơ đồ: (C6H10O5) → C6H12O6 → 2C2H5OH+2CO2 162 180 96 88 gam Nhận xét:
nn2n
Chú ý: Với cácbài khối lượng lớn thìta cần sử dụng tỉ lệ khối lượng.
Độ rượu:
25 2 CHOH
.100
Ví
3 3 CaCO CaCO mm40gamn0,4mol
Hấp thụ CO2 vào nước vôitrong dư: 2 3COCaCO nn0,4mol Nếu H=100%: Coin=1,tacó
đồ:
H=50%:
Chọn D. Ví dụ 2: Từ
gam tinh bột điều chế được 575 ml dung dịch rượu 10
(khối lượng riêng của ancoletylicnguyên chất là0,8g/ml) với hiệu suất cả quátrìnhlà75%.Giá trị của mlà A. 135,00. B. 75,94. C. 108,00. D. 60,75. Hướng dẫn giải
tập
Chú ý: Nhân hiệu suất của cả hai quá trình hoặc tính hiệu suất của cả quá trình: 12 HH%H%100
DẠYKÈMQUYNHƠN
Trang21
OFFICIAL
Tacó: 25 25 CHOH CHOH V575.10%57,5mlm57,5.0,846gam
Bài tập tự luyện dạng 4 Bài
cơ bản
glucozơ
ancoletylic tạo ralà A. 9,20gam. B. 18,40gam.
2: Cho11,25gam glucozơ lênmen rượu
A. 70%. B. 75%.
3:
glucozơ
nước
Nếu H=100%: Coin=1,tacó sơ đồ: (C6H10O5) → C6H12O6 → 2C2H5OH+2CO2 162 92 gam 46 gam 46162 81 92 Với H=75%nên tinhbot m81:75%108gam → Chọn C. Ví dụ 3: Đem thủy phân rồi lên men 1 tấn gạo (chứa 80% tinh bột) thu được m tấn ancol etylic. Biết hiệu suất của mỗi quá trình là 75%, giá trị của mlà A. 0,425. B. 0,345. C. 0,256. D. 0,613. Hướng dẫn giải tấn tinhbottronggao m1.80%0,8 Nếu H=100%: Coin=1,tacó sơ đồ: (C6H10O5) → C6H12O6 → 2C2H5OH+2CO2 162 92 gam 0,8 → tấn 0,892 162 tấn 25 CHOH 0,892 m 162 Với hiệu suất mỗi quátrìnhlà75%: tấn 25 CHOHthuduoc 0,8.92 mm .75%.75%0,256 162 dư thu
→ Chọn C.
Câu 1: Cho 18 gam
lên men thành ancol etylic, biết hiệu suất quá trình lên mên đạt 60%. Khối lượng
C. 5,52gam. D. 15,30gam. Câu
thoátra2,24lítCO2 (đktc). Hiệu suất của quátrìnhlênmen là
C. 80%. D. 85%. Câu
Chomgam
lênmenthành rượu etylic với hiệu suất 80%. Hấp thụ hoàntoànkhíCO2 sinh ravào
vôitrong
được 20gam kết tủa. Giá trị của mlà
A. 28,8. B. 14,4. C. 18,0. D. 22,5. Câu 4: Thực hiện lên men ancol từ glucozơ (H = 80%) được etanol và khí CO2 Dẫn khí thu được vào dung dịch nước vôitrong dư thu được 40gam kết tủa. Khối lượng glucozơ ban đầu là
A. 45,0gam. B. 36,0gam. C. 28,8gam. D. 43,2gam. Câu 5: Cho360gam glucozơ lênmen tạo thành rượu etylic.Khísinhra được dẫn vào nước vôitrong dư thu được mgam kết tủa. Biết hiệu suất của quátrìnhlênmen đạt 80%.Giá trị của mlà
A. 400. B. 320. C. 200. D. 160. Câu 6: Tiến hành lên men m gam tinh bột (hiệu suất toàn quá trình đạt 81%) rồi hấp thụ toàn bộ lượng CO2 sinhravào nước vôitrong dư được 70gam kết tủa. Giá trị của mlà
A. 90. B. 150. C. 120. D. 70.
Câu 7: Dùng m kg tinh bột để điều chế 2 lít dung dịch ancol etylic (khối lượng riêng của C2H5OH 46 nguyên chất là0,8g/ml). Biết hiệu suất cả quátrìnhlà80%.Giá trị của mlà
A. 3,60. B. 1,44. C. 2,88. D. 1,62.
OFFICIAL
Câu 8: Lênmen60gam glucozơ, lượng khíCO2 sinhra hấp thụ hết vào nước vôitrongthu được 12gam kết tủa và khối lượng dung dịch sau phản ứng tăng lên 10 gam với khối lượng nước vôi trong ban đầu. Hiệu suất phản ứng lênmenlà
A. 75,0%. B. 60,0%. C. 54,0%. D. 67,5%. Câu 9: Tráng bạc hoàn toàn m gam glucozơ thu được 43,2 gam Ag. Nếu lên men hoàn toàn m gam glucozơ rồi chokhíCO2 thu được hấp thụ vào nước vôitrong dư. Khối lượng kết tủa thu được là
A. 40gam. B. 80gam. C. 60gam. D. 20gam. Câu 10: Lênmenmgam glucozơ (hiệu suất quátrìnhlênmenlà90%),thu được etanolvàkhíCO2. Hấp thụ hết lượng khí CO2 sinh ra bằng nước vôi trong, thu được 10 gam kết tủa và khối lượng dung dịch giảm so với ban đầu là3,4gam.Giá trị của mlà
A. 15. B. 14. C. 13. D. 12. Câu 11: Ancoletylic được điều chế từ tinh bột bằng phương pháplênmen với hiệu suất toàn bộ quátrình là90%. Hấp thụ toàn bộ lượng CO2 sinhrakhilênmenmgamtinh bột vào nước vôitrongthu được 330 gam kết tủa vàdung dịch X. Biết khối lượng X giảm đi so với khối lượng nước vôitrongban đầu là132 gam.Giá trị của mlà
A. 324,0. B. 405,0. C. 364,5. D. 328,1. Câu 12: Lên men 162 gam bột nếp (chứa 80% tinh bột). Hiệu suất quá trình lên men là 55%. Lượng ancoletylicthu được đem phaloãngthànhVlít rượu etylic . Biết khối lượng riêng của ancolnguyên 23 chất là0,8g/ml.Giá trị của Vlà
A. 220,000. B. 275,000. C. 0,220. D. 0,275. Bài tập nâng cao
Câu 13: Một loại mùn cưa có chứa 60% xenlulozơ. Dùng 1kg mùn cưa trên có thể sản xuất được bao nhiêulít cồn 70o? (Biết hiệu suất của quátrìnhlà70%; khối lượng riêng của C2H5OHnguyên chất là0,8 g/ml).
A. 0,426lít. B. 0,543lít. C. 0,298lít. D. 0,298lít. Câu 14: Lên men m gam tinh bột thành ancol etylic với hiệu suất của cả quá trình là 75%. Lượng CO2 sinh ra được hấp thụ hoàn toànvào dung dịch Ca(OH)2, thu được 50 gam kết tủa và dung dịch X.Thêm dung dịch NaOH1MvàoX,thu được kết tủa. Để lượng kết tủa thu được là lớn nhất thì cần tối thiểu 100 mldung dịch NaOH.Giá trị của mlà
DẠYKÈMQUYNHƠN
Trang22
A. 72,0. B. 64,8. C. 75,6. D. 90,0. Câu 15: Thực hiện phản ứng lênmen rượu từ 2,025kgkhoai chứa 80%tinh bột (còn lại là tạp chất trơ). Cho toàn bộ lượng CO2 hấp thụ hoàn toàn vào dung dịch Ca(OH)2 thu được 450 gam kết tủa, đun nóng dung dịch lại thu được 200gam kết tủa nữa. Hiệu suất của phản ứng lênmenlà
A. 85,5%. B. 42,5%. C. 37,5%. D. 30,3%.
Dạng 5: Tổng hợp xenlulozơ trinitrat Phương pháp giải Điều chế xenlulozơ trinitrat:
H=100%,tacó phương trình:
DẠYKÈMQUYNHƠN
Trang23
OFFICIAL
672 36722 2 3 3 n n CHOOH3nHNOCHOONO3nHO 162189 297
24dac HSO,t
2 3 3 n n CHOOH3nHNOCHOONO3nHO
xuất 297 gam xenlulozơ trinitrat nếu hiệu suất đạt 65%là A. 434,5ml. B. 303,6ml. C. 324,0ml. D. 336,0ml. Hướng dẫn giải Nếu H=100%,tacó phương trình: 24dac HSO,t 672 3 6722 2 3 3 n n CHOOH3nHNOCHOONO3nHO 189 297 gam Với H=65%thì 3HNO m189:65%290,77gam 3ddHNO m290,77:63%461,54gam
54 gam Chú ý: Ta thường sử dụng tỉ lệ về khối lượng. Ví dụ mẫu Ví dụ 1: Xenlulozơ trinitrat được điều chế giữa axit nitric với xenlulozơ (hiệu suất phản ứng là 60% tính theo xenlulozơ). Nếu dùng 2 tấn xenlulozơ thì khối lượng xenlulozơ trinitrat điều chế được là A. 2,97 tấn. B. 3,67 tấn. C. 1,10 tấn. D. 2,20 tấn. Hướng dẫn giải Nếu
672 3 6722
162 297 gam 2 ? tấn tấn xenlulozotrinitrat 2.297 m 3,67 162
Với H=60%thì tấn xenlulozotrinitrat m3,67.60%2,2
→ Chọn D. Ví dụ 2: Thể tích axit nitric 63% có d = 1,52 g/ml cần để sản
Vm461,54303,6ml d1,52
→ Chọn B.
Bài tập tự luyện dạng 5 Bài tập cơ bản
Câu 1: Đun nóng 121,5 gam xenlulozơ với dung dịch HNO3 đặc trong H2SO4 đặc, dư, thu được m gam xenlulozơ trinitrat.Giá trị của mlà
A. 222,75. B. 186,75. C. 176,25. D. 129,75. Câu 2: Cho 340,2 kg xenlulozơ tác dụng dung dịch HNO3 đặc dư. Biết hiệu suất là 80%. Khối lượng xenlulozơ trinitratthu được là
A. 504,90kg. B. 501,93kg. C. 498,96kg. D. 493,02kg. Câu 3: Từ 16,2 tấn xenlulozơ người ta sản xuất được m tấn xenlulozơ trinitrat (biết hiệu suất phản ứng tínhtheo xenlulozơ là90%).Giá trị của mlà
A. 26,73. B. 33,00. C. 25,46. D. 29,70. Bài tập nâng cao
Câu 4: Thể tích dung dịch HNO3 67,5% (khối lượng riêng là 1,5 g/ml) cần dùng để tác dụng với xenlulozơ tạo thành178,2kg xenlulozơ trinitratlà (biết khối lượng HNO3 bị hao hụt là20%)
A. 98lít. B. 140lít. C. 162lít. D. 110lít. Câu 5: Chia một lượng xenlulozơ thành hai phần bằng nhau. Cho phần một tác dụng với một lượng dư dung dịch hỗn hợp HNO3/H2SO4 đun nóng, thu được 35,64 kg xenlulozơ trinitrat với hiệu suất 75%. Thủy phân phần hai với hiệu suất 80%, trung hòa dung dịch sau thủy phân rồi cho toàn bộ lượng sản phẩm sinh ra tác dụng với một lượng H2 dư (Ni, ) đến khi phản ứng xảy ra hoàn toàn thu được m kg t sobitol.Giá trị của mlà
A. 29,120. B. 17,472. C. 23,296. D. 21,840.
DẠYKÈMQUYNHƠN
Trang24
OFFICIAL
3ddHNO
Dạng 1: Lí thuyết trọng tâm
1 - C 2 - C 3 - D 4 - B 5 - D 6 - A 7 - B 8 - D 9 - B 10 - A
11 - B 12 - D 13 - C 14 - A 15 - D 16 - B 17 - A 18 - B 19 - A 20 - B
21 - B 22 - C 23 - D 24 - B 25 - A
Câu 10:
Fructozơ không chứa nhómanđehit(CHO)nênkhông phản ứng được với nước brom → A đúng.
Fructozơ cónhómhiđroxyl(OH) kề nhaunên phản ứng được với dung dịch Cu(OH)2 tạo phức màuxanh lam → Bsai.
Fructozơ bị chuyển hóa thành glucozơ trong môi trường bazơ nên phản ứng được với AgNO3/NH3 thu được kết tủa bạc → Csai.
Fructozơ là hợp chất cacbonyl (nhóm chức C = O) nên phản ứng được với H2/Ni (đun nóng) thu được sobitol → Dsai.
Câu 11:
Cấu tạo của glucozơ có chứa nhóm chức anđehit và 5 nhóm OH nên glucozơ có tính chất của nhóm anđehitvà của ancol đa chức → A,Bsai.
Glucozơ làmonosaccaritnênkhôngthamgia phản ứng thủy phân → B đúng. Khicóenzimxúctác, glucozơ trongdung dịch lênmen tạo ancoletylicvàkhícacbonic → Dsai.
Câu 12: A,B,C đúng.
Dsaivìchoiotvào hồ tinh bột thì xuất hiện màuxanhtím đặc trưng.
Câu 13: A đúng.
Bsaivì saccarozơ, tinh bột hay xenlulozơ chỉ bị thủy phântrongmôi trường axit. Csaivì glucozơ làmonosaccaritnênkhông bị thủy phântrongmôi trường axit. Dsaivìtinh bột khôngcónhómCHOnênkhôngcó phản ứng tráng bạc.
Câu 17:
Monosaccarit gồm glucozơ và fructozơ. Đisaccarit gồm saccarozơ. Polisaccarit gồm tinh bột và xenlulozơ. → Có2 chất trongdãy thuộc loại monosaccarit.
Câu 18: Dãy gồm cácdung dịch đều tác dụng với Cu(OH)2 là: Glucozơ, glixerol,axitaxetic.
Câu 19: Phương trìnhhóa học: (C6H10O5)+nH2O nC6H12O6 n H,t (X: Glucozơ)
DẠYKÈMQUYNHƠN
Trang25 ĐÁP ÁN
OFFICIAL
(X) (Y:Sobitol)
Câu 20: Cácphát biểu đúng là(1)và(3).
Câu 21:
Asaivì chỉ có glucozơ thamgia phản ứng tráng gương.
B đúng vì glucozơ và saccarozơ đều có các nhóm OH kề nhau nên đều hòa tan Cu(OH)2 ở nhiệt độ thường chodung dịch màuxanhlam. Csaivì glucozơ khôngcó phản ứng thủy phântrongmôi trường axit. Dsaivì chỉ có glucozơ mới được sử dụng trongy học làm “huyết thanh ngọt”.
Câu 22:
X bị thủy phântrongmôi trường axit → Loại A.
X thuộc loại polisaccarit → Loại B. Phân tử X gồm nhiều gốc β-glucozơ nênXlà xenlulozơ → Loại D,C đúng.
Câu 23: (a)saivìkhi thủy phânhoàntoàn saccarozơ ngoài glucozơ cònthu được fructozơ. (b)saivì xenlulozơ thuộc loại polisaccarit. (d)saivì hiđro khử glucozơ thu được sobitol. (e)saivì thuốc súngkhôngkhóilà xenlulozơ trinitrat.
Câu 24: (a),(b) đúng. (c)saivìphân tử saccarozơ được cấu tạo bởi một gốc glucozơ và một gốc fructozơ. (d)saivìtinh bột và xenlulozơ không phải là đồngphân của nhau. → Có2phát biểu đúng.
Câu 25:
(a)saivì hiđro hóahoàntoàn glucozơ tạo rasobitol. (b) đúng. (c)saivì xenlulozơ trinitratlà thuốc súngkhôngkhói.
(d) đúng vìH2SO4 cótínhháo nước, làm đường hóathan. (e) đúng.
DẠYKÈMQUYNHƠN
Trang26 C6H12O6 +H2 C6H14O6 Ni,t
OFFICIAL
Dạng 2: Phản ứng oxi hóa – khử 1 - B 2 - D 3 - B 4 - A 5 - D 6 - C 7 - B 8 - B 9 - A 10 - B 11 - D 12 - B 13 - A Câu 1: glucozo Ag Ag n0,05moln20,050,1molmm0,110810,8gam Câu 2: Ag glucozoAg 1 n0,1molnn0,05mol 2 C0,05180%100%12% 75
Câu 3: Đốt cháy cacbohiđrat luôncó: lít 22 2 COO CO nn0,4molV0,4.22,48,96
Câu 4: Ag n0,05mol
Tacó: glucozoAg 1 nn0,025mol 2 M C0,0250,1M 0,25
Câu 5: Ag n0,5mol
Nếu H=100%: glucozoAg glucozo 1 nn0,25molm0,25.18045gam 2
Với H=75%thì m45:75%60gam
6: 2 2 O HO n0,1125mol;n0,1mol
Đốt cháy hỗn hợp các cacbohiđrat luôncó: 22 COO nn0,1125mol Bảo toàn khối lượng: 22 2COHOO mmmm0,1125440,1180,1125323,15gam
Câu 7: glucozo n0,004mol Nếu H=100%: Agglucozo Ag n2n0,008molm0,008.1080,864gam
Với H=80%thì Ag m0,864.80%0,6912gam Câu 8: Tacó: Glucozơ → 2Ag Fructozơ → 2Ag Lại có: Ag glucozofructozoAg 1 n0,36molnn0,18mol 2 m0,1818032,4gam Câu 9: Đốt cháy hỗn hợp
DẠYKÈMQUYNHƠN
Trang27
OFFICIAL
Câu
X gồm các cacbohiđrat: 22
Chotoàn
sản phẩm cháyquadung dịch
3BaCO mm1,68.197330,96gam Câu
Ag n0,03mol Do chỉ có glucozơ thamgia phản ứng tráng bạc, nêntacó: glucozoAg 1
2 glucozo m2,7gam saccarozo m6,122,73,42gam saccarozo %3,42m.100%55,9% 6,12
COO nn1,68mol
bộ
Ba(OH)2 dư: 32 BaCOCO nn1,68mol
10:
nn0,015mol
Câu 11: Phần hai: 2glucozoBr nn0,22mol Phần một: glucozofructozoAg 1 nnn0,4 2 fructozo n0,40,220,18mol fructozo %0,18.180 m .100%45% 0,18.1800,22.180
Câu 12: Đốt cháy cacbohiđrat: 22 COO nn0,3mol Hấp thụ hết sản phẩm cháy bằng dung dịch Ca(OH)2 dư thấy khối lượng nước vôitrong giảm 11,4gam: 32 3 CaCOCO CaCO nn0,3molm0,310030gam
DẠYKÈMQUYNHƠN OFFICIAL Trang28
2
2
2 2
Bảo
2 22 OCOHOX
22 COO 83,2 nn2,6mol 32 Lại có: 32 CaCOCO nn2,6mol 3CaCO m260gamm74,4gam Dạng 3: Phản ứng thủy phân 1 - D 2 - B 3 - C 4 - C 5 - A 6 - D 7 - C 8 - B 9 - C 10 - A 11 - C 12 - C 13 - A 14 - B 15 - A Câu 1: Tacó sơ đồ: Saccarozơ Glucozơ + Fructozơ H 342 180 180 gam 1 → x x kg 1180 x0,526kg 342 Câu 2: saccarozo n0,01mol Tacó sơ đồ: Saccarozơ Glucozơ + Fructozơ 4Ag H 33AgNO/NH
3 22 22 ddgiamCaCOCOHOCOHO mmmmmm18,6gam
HO m5,4gam
HO n0,3mol
Ta thấy: X thuộc loại monosaccarit.
CO HO n0,31 n0,3
Câu 13: Tacó: 22 binhtangCOHO mmmm83,2gam
toàn khối lượng:
mmmmm83,2m83,2gam
DẠYKÈMQUYNHƠN OFFICIAL Trang29
đồ:
Glucozơ +
H 342
72.342 136,8 180 Với
saccarozo
Câu
Nếu
bột Glucozơ H Cứ: 162 180gam Nên 405 xgam 405180 x450gam 162 Với H=75%: glucozo m45075%337,5gam
Agsaccarozo n4n4.0,010,04mol Ag mm0,041084,32gam Câu 3: Nếu H=100%,tacó sơ đồ: (C6H10O5) → C6H12O6 162 180gam 202,5 → gam 202,5.180225 162 Với H=75%thì glucozothuduoc m225.75%168,75gam Câu 4: Coin=1,tacó sơ đồ: (C6H10O5) → C6H12O6 162 180gam 32,4 → gam 32,4.18036 162 H28,8.100%80% 36 Câu 5: saccarozo n0,025mol Tacó sơ đồ: Saccarozơ Glucozơ + Fructozơ 4Ag H 33AgNO/NH Agsac n4n0,1mol Ag m10,8gam Câu 6: Nếu H=100%,tacó sơ
Saccarozơ
Fructozơ
180gam 72gam
H=80%nên:
m136,880%171gam
7:
H=100%:Tinh
Câu 8: saccarozo saccarozo m15,39gamn0,045mol Tacó sơ đồ: Saccarozơ Glucozơ + Fructozơ 4Ag H 33AgNO/NH Agsaccarozo n4n0,18mol Ag m0,18.10819,44gam
Câu 9: Ag n0,025mol Tacó sơ đồ: Saccarozơ Glucozơ + Fructozơ 4Ag H 33AgNO/NH saccarozoAg 1 nn0,00625mol 4 m0,006253422,1375gam
Câu 10: saccarozo n0,02mol Tacó sơ đồ: Saccarozơ Glucozơ + Fructozơ 4Ag H 33AgNO/NH Nếu H= 100%: Agsaccarozo Ag n4n40,020,08molm0,081088,64gam
DẠYKÈMQUYNHƠN OFFICIAL Trang30
m.108gam 813 m H.100%75% 4m 3 Câu 12: Ag n0,05mol Nếu
tinhbotglucozoAg 1 nnn0,025mol 2 tinhbot m0,0251624,05gam Với H=50%: tinhbot m4,05:50%8,1gam gao m8,1:80%10,125gam Câu 13: nsaccarozơ ở mỗi phần glucozofructozo 0,0125molnn0,0125mol Phần một: Agglucozofructozo n2n2n0,05molx0,051085,4gam Phần hai: 2 Brglucozo nn0,0125moly0,0125.1602gam Câu 14: ChomgamXtác dụng với dung dịch AgNO3 trongNH3: Ag n0,2mol
Với H=80%thì m8,64.80%6,912gam
Câu 11: Coin=1,tacó sơ đồ: (C6H10O5) → C6H12O6 → 2Ag → mol m 162 2mm 16281
Agtheolythuyet m4m
H=100%:
glucozoAg 1 nn0,1mol 2
Thủy phânhoàntoànXtrongmôi trường axit: Gọi số moltinh bột trongmgamXlàamol. Tacó sơ đồ: Tinh bột Glucozơ H,t glucozo na0,1mol Lại có: 2glucozoBr nn0,2mola0,1mol m0,1.1800,1.16234,2gam Câu 15: Gọi số mol của saccarozơ và glucozơ trong hỗn hợp X lần lượt làx,ymol. (*) 342x180y7,02 Tacóquátrình: Saccarozơ Glucozơ
DẠYKÈMQUYNHƠN OFFICIAL Trang31
+
4Ag 2
33
x → 4xmol Glucozơ
33
y →
4x2y0,08y0,02 glucozo %0,02180 m 100%51,28% 7,02 Dạng 4: Tổng hợp ancol etylic 1 - C 2 - C 3 - D 4 - A 5 - B 6 - D 7 - D 8 - A 9 - A 10 - A 11 - B 12 - C 13 - A 14 - C 15 – B Câu 1: glucozo n0,1mol Nếu H=100%: C6H12O6 2C2H5OH+2CO2 menruou 0,1 → 0,2mol 25 CHOH m0,2469,2gam Với H=60%: ancoletylic m9,2.60%5,52gam Câu 2: 2 2 CO glucozoltCO 1 n0,1molnn0,05mol 2 glucozolt glucozottt Hm0,05180100%100%80% m 11,25 Câu 3:
Fructozơ
HO,t
AgNO/NH
2Ag
AgNO/NH
2ymol Theo đề bài: (**) Ag n0,08mol4x2y0,08
Từ (*)và(**)tacó hệ phương trình: 342x180y7,02x0,01
Nếu H=100%,tacó: 3 2 CaCO CO n0,2moln0,2mol 2glucozoCO 1 nn0,1mol 2 glucozo m0,118018gam
Với H=80%: glucozo m18:80%22,5gam Câu 4: 3 2 CaCO CO n0,4moln0,4mol
Phương trìnhhóa học: C6H12O6 2C2H5OH+2CO2 menruou 0,2 0,4mol Nếu H=100%thì glucozo m0,2.18036gam Với H=80%thì glucozobandau m36:80%45gam Câu 5: glucozo n2mol Nếu H=100%,tacó phương trình: C6H12O6 2C2H5OH+2CO2 lenmen 2 → 4mol Với H=80%thì 2 COthuduoc n480%3,2mol Phương trìnhhóa học: CO2 +Ca(OH)2 → CaCO3 +H2O 3,2 → 3,2mol 3CaCO mm3,2.100320gam
DẠYKÈMQUYNHƠN
Trang32
OFFICIAL
Nếu
2tinhbotCO tinhbot 1 nn0,35molm0,35.16256,7gam 2
Câu 7: 25 25 CHOH CHOH 46 V20,92litm0,9210000,8736gam 100 Nếu
sơ đồ: (C6H10O5) C6H12O6 2C2H5OH+2CO2 2 HO,t t 162 92gam 736gam 736.162 1296 92 Với
Câu 8:
Câu 6: 3 2 CaCO CO n0,7moln0,7mol
H=100%:
Với H=81%: m56,7:81%70gam
H=100%vàcoin=1,tacó
H=80%thì m1296:80%1620gam1,62kg
DẠYKÈMQUYNHƠN OFFICIAL Trang33
Nếu
sơ đồ: (C6H10O5) C6H12O6 2C2H5OH+2CO2 2 HO,t t 16288gam 198gam 198.162 364,5 88 Với hiệu suất của quátrìnhlà90%thì tinhbotbandau mm364,5:90%405gam Câu
tinhbot
Nếu
sơ đồ
Tacó: 2 2 2 ddtangCO CO CO mmmm22gamn0,5mol glucozopu n0,25mol glucozopu m0,2518045gam 45 H100%75% 60 Câu 9: Ag n0,4mol Tacó: Glucozơ 2Ag 33AgNO/NH 0,2 0,4mol Lại có: C6H12O6 2C2H5OH+2CO2 menruou 0,2 → 0,4mol CO2 +Ca(OH)2 → CaCO3 +H2O 0,4 → 0,4mol 3CaCO mm0,4.10040gam Câu 10: KhichoCO2 vào nước vôitrong: 2dungdichgiamkettuaCO mmm3,4gam 2CO n0,15mol Nếu H=100%,tacó: 2glucozoCO 1 nn0,075mol 2 glucozo m0,07518013,5gam
Với H=90%: glucozo m13,5:90%15gam
Câu 11: Khi hấp thụ CO2 và nước vôitrong: 32 dungdichgiamCaCOCO mmm
2CO m330132198gam
H=100%vàcoin=1,tacó
12:
m16280%129,6gam
H=100%vàcoin=1,tacó
DẠYKÈMQUYNHƠN OFFICIAL Trang34 (C6H10O5) C6H12O6 2C2H5OH+2CO2 2 HO,t t
25 25
→
→
→
25
25
VV:70%:70%0,426lit 0,8 Câu
Nếu H=100%: Phương trìnhhóa học CO2 +Ca(OH)2 → CaCO3 +H2O 0,5 0,5mol 2CO2 +Ca(OH)2 → Ca(HCO3)2 x → 0,5xmol Ca(HCO3)2 +NaOH → CaCO3 +NaHCO3 +H2O 0,1 0,1mol 0,5x0,1x0,2 2CO n0,7mol 2tinhbotglucozoCO 1 nnn0,35mol 2 tinhbot m0,3516256,7gam Với H=75%tacó: m56,7:75%75,6gam Câu 15: Khi đun nóngdung dịch tạo thêm kết tủa → Chứng tỏ cóCa(HCO3)2.
16292gam 129,6 gam 129,6.9273,6 162
Với H=55%thì: 25 CHOHthuduoc m73,655%40,48gam
CHOH ddCHOH23 40,48 100 V 50,6mlV50,6.220ml0,22lit 0,8 23
Câu 13: xenlulozo m1.600,6kg
Nếu H=100%,coin=1tacó sơ đồ: (C6H10O5)
C6H12O6
2C2H5OH+2CO2 162 92gam 0,6
kg 0,692 162 Với H=70%nên 25 CHOH 0,692 m70%0,2385kg 162
CHOH V0,2385lit 0,8
ddruouCHOH 0,2385
14:
DẠYKÈMQUYNHƠN OFFICIAL Trang35 Phương trìnhhóa
Ca(HCO3)2 CaCO3 +CO2 +H2O t 22mol Bảo toànnguyên tố C: 2 3 32COCaCOCaHCO nn2n4,5228,5mol 2CO m374gam Coin=1,tacó sơ đồ: (C6H10O5) C6H12O6 2C2H5OH+2CO2 2 HO,t t 162 88gam 374gam 374162 688,5 88 Mà: tinhbotthucte m2,025.80%1,62kg1620gam H688,5.100%42,5% 1620 Dạng 5: Tổng hợp xenlulozơ trinitrat 1 - A 2 - C 3 - A 4 - B 5 - C Câu
Phương trìnhhóa học: [C6H7O2(OH)3] +3nHNO3 [C6H7O2(ONO2)3] +3nH2O n 24dac HSO,t n 162297gam 121,50 → gam 121,5.297222,75 162 Câu 2: Nếu H=100%,tacó phương trình: [C6H7O2(OH)3] +3nHNO3 [C6H7O2(ONO2)3] +3nH2O n 24dac HSO,t n 162297gam 340,20 → kg 340,2.297623,70 162 Với H=80%thì xenlulozotrinitrat m623,780%498,96kg Câu 3: Nếu H=100%,tacó phương trình: [C6H7O2(OH)3] +3nHNO3 [C6H7O2(ONO2)3] +3nH2O n 24dac HSO,t n 162297gam 16,20 → tấn 16,2.29729,70 162 Với H=90%thì tấn xenlulozotrinitrat m29,7.90%26,73
học:
1:
OFFICIAL Trang36
DẠYKÈMQUYNHƠN
Câu 4: Nếu H=100%,tacó phương trình: [C6H7O2(OH)3] +3nHNO3 [C6H7O2(ONO2)3] +3nH2O n 24dac HSO,t n 189297gam 178,2kg 178,2.189113,4 297 Với thì H100%20%80% 3HNO n113,4:80%141,75kg 3HNO Vm141,7594,5lit D1,5 3 ddHNO67,5% V94,5:67,5%140lit
Câu 5: Phần một: Phương trìnhhóa học: C6H7O2(OH)3 +3HNO3 C6H7O2(ONO2)3 +3H3O 24dacHSO 162 297gam 35,64kg 35,6416219,44 297 Với H=75%: xenlulozo m19,44:75%25,92kg Phần hai: Coin=1,tacó sơ đồ: C6H10O5 → C6H12O6 → C6H14O6 162 182gam 25,92 → 29,12kg Với H=80%: sobitol m29,12.80%23,296kg
BÀI 4: AMIN
Mục tiêu
Kiến thức
+ Biết được khái niệm, phân loại, gọi tênamin.
+Trìnhbày được tính chất điển hình của amin.
Kĩ năng
+ Nhận dạng các hợp chất của amin.
+ Viết được các phương trìnhhóa học của amin.
+Quansát,phântích được cácthí nghiệm chứng minhtính chất của amin.
+Làm được một số bài tập liênquan đến amin, muối amoni.
Trang1
DẠYKÈMQUYNHƠN OFFICIAL
CHƯƠNG 3: AMIN – AMINO AXIT – PEPTIT - PROTEIN
I. LÍ THUYẾT TRỌNG TÂM
1. Khái niệm phân loại, đồng phân
a. Khái niệm
Khithay thế nguyên tử Htrongphân tử NH3 bằng gốc hiđrocacbon tathu được amin.
Trong đó: Công thức phân tử của amin no, đơn chức, mạch hở là .n2n3 CHNn1
b. Phân loại
•Theo bậc của amin: Bậc amin là số nguyên tử H trong NH3 bị thay thế bởi gốc hiđrocacbon. → Như vậy cóamin bậc I, bậc IIvà bậc III.
•Theo gốc hiđrocacbon: Aminbéo:Khicócác gốc hiđrocacbon no.
Amin thơm: Khinguyên tử Nliên kết trực tiếp với vòng thơm.
•Theo số chức: Amin đơn chức: 252CHNH
Aminhai chức: 222CHNH c. Đồng phân
•Aminno, đơn chức, mạch hở thường có đồng phân n2n3 CHN về mạch cacbon, vị trínhóm chức và bậc amin.
Ví dụ: Amin đơn giản nhất là: . 32CHNH
Ví dụ: Về bậc amin:
Amin bậc I: 32CHNH
OFFICIAL
Amin bậc II: 3 3CHNHCH
Amin bậc III: 33 CHN
Ví dụ: Về amin béo, amin thơm: Amin béo: C2H5NH2
Amin thơm: C6H5NH2; CH3C6H4NH2
Ví dụ: Đồng phân của C4H11N. Mạch cacbon và vị trí nhóm chức: 32222 CHCHCHCHNH 3 22 3
CHCHCHNH | CH 32 2 3
CHCHCHNH | CH 3 3 2 3
CH | CHCNH | CH
DẠYKÈMQUYNHƠN
Trang2
CHCHNHCH
CHNCHCH | CH Chú ý: Công thức kinh nghiệm để tính số đồng phân của amin no, đơn chức, mạch hở: là: là . n2n3 CHN n12 n5 Ví dụ: 1234 3 23 2
CHCHCHCH | NH Tên amin là: Butan-2-amin. Ví dụ: 3 23 3
CHNCHCH | CH Tên amin là: N, N-đimetyletanamin. Ví dụ: : 25 3CHNHCH Etylmetylamin
DẠYKÈMQUYNHƠN OFFICIAL Trang3
c. Tên riêng Anilin:C6H5NH2 (C6H5 là gốc phenyl) d. Bảng tên một số amin quen thuộc CTCT Tênthay thế Tên gốc chức CH3NH2 Metanamin Metylamin (CH3)2NH N-metylmetanamin Đimetylamin (CH3)3N N, N-đimetylmetanamin Trimetylamin C2H5NH2 Etanamin Etylamin (C2H5)2NH N-etyletanamin Đietylamin C6H5NH2 Benzenamin Phenylamin NH2[CH2]6NH2 Hexan-1,6-điamin Hexametylenđiamin 2. Tính chất vật lí
2. Danh pháp a. Tên thay thế •Amin bậc Icócách đọc tương tự với ancol: Tên=Tên hiđrocacbon-(số chỉ vị trínhómNH2)-amin •Amin bậc IIvà bậc III: b. Tên gốc chức (thường dùng) Tên=Têncác gốc hiđrocacbon +amin
3
|
32
3
Bậc amin: 322 3CHCHCHNHCH 3 3
CH
23CHCHNHCHCH 3 23
Bốn amin ở trạng thái khí điều kiện thường, mùi khai, khó chịu, tan nhiều trong nước là metylamin (CH3NH2), đimetylamin ((CH3)2NH),trimetylamin((CH3)3N),etylamin(C2H5NH2).
Khi khối lượng mol tăng: nhiệt độ sôi tăng, độ tan trong nước giảm.
Cácamin thơm đều là chất lỏng hoặc chất rắn, dễ bị oxihóatrong khôngkhí chuyển thànhmàu đen.
Cácamin đều độc.
3. Tính chất hóa học
a. Tính bazơ
Nhận xétchung: về cấu tạo, amincónguyên tử N như trongphân tử NH3,do vậy, amincótính bazơ tương tự NH3
• Phản ứng với nước: Cácaminno, đơn chức, mạch hở bậc I, bậc II đều làm quỳ tím ẩm chuyển xanh.
Anilin và các amin thơm khác phản ứng rất kém với nước và chúngkhônglàm quỳ tím ẩm chuyển màu.
Sosánh lực bazơ giữa cácamin: (CH3)2NH>C2H5NH2 >CH3NH2 >C6H5NH2
• Phản ứng với axit:Cácamin dễ dàng phản ứng với cácdung dịch axit mạnh tạo thành muối amoni(tan tốt trong nước).
Ví dụ: CH3NH2 +HOH CH3NH3 + +OH

Thí nghiệm 1: Nhỏ vài giọt anilin vào ống nghiệm đựng nước, anilin không tan, lắng xuống đáy.
b. Phản ứng thế ở nhân thơm của anilin
Trong phân tử anilin, nhóm NH2 ảnh hưởng đến vòng benzen tương tự sự ảnh hưởng của nhómOHtrongphenol. Cặp e của N,Oliên hợp vàovòng thơm đến các vị tríoctovàpara.
Thí nghiệm 2: Nhỏ vài giọt anilin vào ống nghiệm đựng dung dịch HCl, thấy anilin tan, tạo dung dịch không màu: C6H5NH2 + HCl → [C6H5NH3]+Cl

(phenylamoni clorua)
Thí nghiệm: Nhỏ vài giọt nước brom vào ống nghiệm chứa anilin thấy xuất hiện kết tủa trắng:
DẠYKÈMQUYNHƠN
Trang4
OFFICIAL
Chú ý: Phản ứng với brom tạo kết tủa trắng dùng để nhận biết anilin SƠ ĐỒ HỆ
THỐNG HÓA
AMIN
KHÁI NIỆM, PHÂN LOẠI
Khái niệm: Khithay thế một hay nhiều nguyên tử HtrongNH3 bằng các gốc hiđrocacbon thu được amin Phân loại:
Amin bậc I: 2RNH
Amin bậc II: 1 2RNHR
RNR | R
Amin bậc III: 13 2
TÍNH CHẤT VẬT LÝ
OFFICIAL
Metylamin, đimetylamin, trimetylamin và etylamin là những chất khí, mùi khai, khó chịu, tan tốt trong nước, độc.
Anilinlà chất lỏng, íttantrong nước.
TÍNH CHẤT HÓA HỌC Tính bazơ yếu 22 3 RNHHORNHOH
Sosánhtính bazơ (CH3)2NH>C2H5NH2 >CH3NH2 >NH3 >C6H5NH2 (anilin) Tính chất đặc biệt của anilin: sự ảnh hưởng qua lại của –NH2 vàC6H5 Tính bazơ rất yếu: khônglàm đổi màu quỳ
DẠYKÈMQUYNHƠN
Trang5
2 3 RNHHClRNHCl
tím ẩm 65226232 dd CHNH3BrCHBrNH3HBr II. CÁC DẠNG BÀI TẬP Dạng 1: Lí thuyết trọng tâm Kiểu hỏi 1: Khái niệm, phân loại Ví dụ mẫu Ví dụ 1: Chất nàosau đây làamin bậc một? A. CH3NHCH3. B. (CH3)3N. C. CH3NH2. D. CH3CH2NHCH3. Hướng dẫn giải Bậc aminlà số nguyên tử H bị thay thế trongNH3 bởi gốc hiđrocacbon. CH3NHCH3:amin bậc hai; (CH3)3N:amin bậc ba;
CH3NH2:amin bậc một; CH3CH2NHCH3:amin bậc hai.
→ Chọn C.
Kiểu hỏi 2: Danh pháp Ví dụ mẫu
Ví dụ 1: Chất nàosau đây làtrimetylamin?
A. CH3NHCH3 B. (CH3)3N. C. CH3NH2 D. CH3CH2NHCH3 Hướng dẫn giải
Tênaminlàtrimetylamin → Chất được tạo thành từ ba gốc hiđrocacbon giống nhaulà gốc metyl(CH3).
→ Công thức aminlà(CH3)3N.
→ Chọn B.
Chú ý: Nếu amin được tạo từ nhiều gốc hiđrocacbon giống nhau thì ta thêm tiền tố tương ứng. Ví dụ: 2 là đi; 3 là tri; ... Nếu amin được tạo từ nhiều gốc hiđrocacbon khác nhau thì ta gọi tên gốc hiđrocacbon theo thứ tự bảng chữ cái. Kiểu hỏi 3: Đồng phân Phương pháp giải Công thức phân tử của amin: .xyt CHN
OFFICIAL
Số đồng phân cấu tạo của amincócùng công thức phân tử C4H11Nlà A. 8. B. 5. C. 4. D. 3. Hướng dẫn giải Độ bất bãohòak: k4.221110 2
→ Aminno, đơn chức, mạch hở. Amin bậc I: ,CCCC CCC | C
Dấu “↓” chỉ vị trí đặt nhómNH2 để tạo amin bậc I. → Có4 đồng phânamin bậc I. Amin bậc hai: Số C RR43122 → Cóba đồng phânamin bậc II.
DẠYKÈMQUYNHƠN
Trang6
để xác
amin. k2x2yt0 2 Chú ý: Aminno, đơn chức, mạch hở cócông thức tổng quátlà . n2n3 CHN n1 Bước 2: Viết đồng phân • Amin bậc I: Viết mạch cacbon rồi đặt nhóm NH2. •Amin bậc II: Viết tương tự ete. Số C = Số C của amin RR
Bước 1: Tính độ bất bão hòa k:
định loại
Ví dụ:
→ Xác định Rvà (với R, có thể là1,2...) R R
•Amin bậc III: Viết tương tự este. Số C = Số C của amin RRR
Chú ý: Tacó thể sử dụng công thức tínhnhanh số
đồng phânaminno, đơn chức, mạch hở: n1 2n5
CH3CH2CH2–NH–CH3
CH3CH(CH3)–NH–CH3 C2H5–NH–C2H5
Amin bậc ba: Số C RRR4211 → Có một đồng phânamin bậc III. 25 3 3
CHNCH | CH
Vậy có8 đồng phânamin. → Chọn A. Ví dụ mẫu Ví dụ 1: Số đồng phânamin bậc một, chứa vòngbenzen,cócùngcông thức phân tử C7H9Nlà A. 3. B. 5. C. 2. D. 4. Hướng dẫn giải Amin bậc một: (–NH2) ; ; ; 3642 oCHCHNH 3642 mCHCHNH 3642 pCHCHNH6522 CHCHNH Vậy có4 đồng phânamin bậc một, chứa vòngbenzen,cócócùngcông thức phân tử C7H9N.
→ Chọn D.
Kiểu hỏi 4: Tính chất vật lý Ví dụ mẫu
Ví dụ 1: Aminnàosau đây là chất khí ở điều kiện thường?
A. Metylamin. B. Butylamin. C. Phenylamin. D. Propylamin. Hướng dẫn giải
Có bốn aminlà chất khí ở điều kiện thường là:metylamin; đimetylamin; trimetylamin;etylamin.
→ Chọn A.
Ví dụ 2: Phát biểu nàosau đây sai?
A. Cácaminkhícómùi tương tự amoniac, độc.
B. Anilinlà chất lỏng, khótantrong nước, màu đen.
C. Độ tan của amin giảm dần khi số nguyên tử cacbontrongphân tử tăng.
D. Metylamin,etylamin, đimetylamin, trimetylaminlà những chất khí, dễ tantrong nước.
Hướng dẫn giải
A đúng vìcácaminkhícómùikhaikhó chịu tương tự amoniacvà độc.
Bsaivìanilinlà chất lỏng nhưng khôngmàuvàíttantrong nước. Khi để lâutrongkhôngkhí bị oxihóa bởi oxikhôngkhínên chuyển thànhmàu đen.
DẠYKÈMQUYNHƠN
Trang7
OFFICIAL
C đúng vì độ tan của amin giảm dần theo chiều tăng của phân tử khối haykhi số nguyên tử cacbontrong phân tử tăng.
D đúng vìmetylamin,etylamin, đimetylamin, trimetylaminlà những chất khí,tan nhiều trong nước.
→ Chọn B. Kiểu hỏi 5: So sánh tính bazơ giữa các amin
Phương pháp giải Quy tắc sosánhtính bazơ giữa cácamin
•Aminno đơn, bậc II>aminno, đơn, bậc I(cùng số C).
Ví dụ: (CH3)2N>C2H5NH2
• Amin no, đơn, bậc I có gốc ankyl càng lớn, lực bazơ càng mạnh:
Ví dụ: C2H5NH2 >CH3NH2
Tổng quát: Amin thơm bậc II<amin thơm bậc I<NH3 <amin no bậc I<aminno bậc II<NaOH
Ví dụ mẫu
Ví dụ: Trongcác chất sau, chất nàosau đây có lực bazơ lớn nhất?
A. Etylamin. B. Phenylamin. C. Amoniac. D. Metylamin. Hướng dẫn giải Theoquy tắc tacó: Phenylamin < amoniac < metylamin < etylamin Vậy chất có lực bazơ lớn nhất làetylamin. → Chọn A.
OFFICIAL
Ví dụ 1: Chodãycác chất: C6H5NH2 (1),C2H5NH2 (2),(C6H5)2NH(3),(C2H5)2NH(4),NH3 (5)(C6H5 là gốc phenyl).Dãycác chất sắp xếp theo thứ tự lực bazơ giảm dần là: A. (4),(1),(5),(2),(3). B. (3),(1),(5),(2),(4). C. (4),(2),(3),(1),(5). D. (4),(2),(5),(1),(3). Hướng dẫn giải
Tacó:C6H5NH2 (1):Amin thơm bậc I; C2H5NH2 (2):Aminno, bậc I; (C6H5)2NH(3):Amin thơm bậc II; (C2H5)2NH(4):Aminno, bậc II. Nêncó:(C
DẠYKÈMQUYNHƠN
Trang8
2H5)2NH>C2H5NH2 >NH3 >C6H5NH2
→ Thứ tự lực bazơ giảm dần:
→ Chọn D. Bài tập tự luyện dạng 1 Bài tập cơ bản Câu 1: Chất nàosau đây làamin bậc ba? A. (CH3)3N. B. CH3–NH2. C. C2H5–NH2 D. CH3–NH–CH3 Câu 2: Chất nàosau đây làamin bậc hai? A. H2N–CH2–NH2. B. (CH3)2CH–NH2. C. CH3–NH–CH3 D. (CH3)3N. Câu 3: Ancolvàaminnàosau đây cùng bậc? A. (C6H5)2NHvàC6H5CH2OH. B. C6H5NHCH3 vàC6H5CH(OH)CH3. C. (CH3)3COHvà(CH3)3CNH2 D. (CH3)2CHOHvà(CH3)2CHNH2 Câu 4: Amin ứng với công thức C6H5NH2 (C6H5:phenyl)cótên gọi là
>(C6H5)2NH.
(4),(2),(5),(1),(3).
A. anilin. B. benzylamin. C. etylamin. D. alanin.
Câu 5: Aminnàosau đây là chất lỏng ở điều kiện thường?
A. Anilin. B. Metylamin. C. Đimetylamin. D. Etylamin.
Câu 6: Cóbaonhiêuamin bậc balà đồng phân cấu tạo của nhau ứng với công thức phân tử C5H13N?
A. 3. B. 2. C. 5. D. 4.
Câu 7: Số amin bậc một cócùngcông thức phân tử C3H9Nlà
A. 3. B. 1. C. 2. D. 4.
Câu 8: Số amin thơm bậc một ứng với công thức phân tử C7H9Nlà A. 3. B. 2. C. 5. D. 4. Câu 9: số đồng phân cấu tạo của amin bậc một cócùngcông thức phân tử C4H11Nlà A. 4. B. 2. C. 5. D. 3 Câu 10: Dãy gồm các chất được sắp xếp theo thứ tự tăng dần lực bazơ từ tráisang phải là:
A. Phenylamin,amoniac,etylamin. B. Etylamin,amoniac,phenylamin. C. Etylamin,phenylamin,amoniac. D. Phenylamin,etylamin,amoniac.
OFFICIAL
Câu 11: Cho dãy các chất: C6H5NH2 (1), C2H5NH2 (2), (C2H5)2NH (3), NH3 (4) (C6H5 - là gốc phenyl). Dãycác chất sắp xếp theo thứ tự lực bazơ giảm dần là: A. (1),(4),(2),(3). B. (3),(1),(4),(2). C. (3),(2),(1),(4). D. (3),(2),(4),(1).
Câu 12: CH3NH2 vàC6H5NH2 đều phản ứng với
A. dung dịch NaNO3 B. dung dịch Br2/CCl4 C. dung dịch NaOH. D. dung dịch HCl.
Câu 13: Trong số cácphát biểu sau:
(1)Metylaminkhônglàm đổi màu quỳ tím.
(2)Anilin để lâungàytrongkhôngkhí dễ bị oxihóa chuyển sangmàu đen.
(3)Danhpháp gốc chức của C2H5NH2 làetylamin.
(4)CH3NH2,C2H5NH2,CH3NHCH3,(CH3)3Nlàcác chất lỏng, mùikhaikhó chịu, tan nhiều trong nước. Số phát biểu đúng là A. 1. B. 2. C. 3. D. 4. Bài tập nâng cao
Câu 14: Chocác chất: (a)C6H5NH2;(b)CH3NH2;(c)CH3–C6H4–NH2;(d)O2N–C6H4–NH2. Trật tự giảm dần tính bazơ của các chất trênlà: A. (a),(b),(d),(e). B. (b),(c),(d),(a). C. (a),(b),(c),(d). D. (b),(c),(a),(d). Câu 15: Chodung dịch metylamin dư lần lượt vàocácdung dịch riêng biệt sau:AlCl
DẠYKÈMQUYNHƠN
Trang9
3,FeCl3,Cu(NO3)2, HCl,Na2SO4.Saukhicác phản ứng kết thúc, số kết tủa thu được là A. 2. B. 4. C. 1. D. 3. Dạng 2: Phản ứng với axit Phương pháp giải Amintác dụng với HCl 2 3 a a RNHaHClRNHCl Với alà số nhóm chức amin. Ví dụ: Cho20gam hỗn hợp gồm haiaminno, đơn chức, mạch hở tác dụng vừa đủ với Vmldung dịch
Nhận xét: (với alà số nhómNH2) HClaminna.n
Chú ý: Amin đơn chức: HClaminnn
Bước 1: Sử dụng bảo toàn khối lượng aminaxitmuoá immm Bước 2: Tìmcácthông số mà đề bàiyêu cầu.
HCl 1M, thu được dung dịch chứa 31,68 gam hỗn hợp muối. Giá trị của Vlà A. 320. B. 50. C. 200. D. 100. Hướng dẫn giải Bảo toàn khối lượng: HClmuoáiamin mmm31,682011,68gam HCl m0,32mol V0,32lit320ml → Chọn A. Ví dụ mẫu Ví dụ 1: Cho 2,0 gam hỗn hợp X gồm metylamin, đimetylamin phản ứng vừa đủ với 0,05 mol HCl, thu được mgam muối. Giá trị của mlà A. 3,425. B. 4,725. C. 2,550. D. 3,825. Hướng dẫn giải Bảo toàn khối lượng: muoáiaminaxitmmm 20,0536,53,825gam → Chọn D. Ví dụ 2: Cho10gamamin đơn chức X phản ứng hoàntoàn với HCI (dư), thu được 15gam muối, số đồng phân cấu tạo của Xlà
A. 4. B. 8. C. 5. D. 7. Hướng dẫn giải
toàn khối lượng:
DẠYKÈMQUYNHƠN
Trang10
OFFICIAL
Bảo
HCl 510 nmol 36,573 Amin đơn chức: aminHCl 10 nnmol 73 amin 10 M73 10 73 Vậy công thức phân tử của aminlàC4H11N. Số đồng phân cấu tạo của X: 413 228 → Chọn B. Chú ý: Sử dụng công thức tính nhanh số đồng
HClmuoáiamin mmm15105gam
phân amin.
Ví dụ 3: Cho2,1gam hỗn hợp X gồm haiaminno, đơn chức, mạch hở kế tiếp nhautrongdãy đồng đẳng phản ứng hết với dung dịch HCl dư, thu được 3,925gam hỗn hợp muối. Công thức của haiamintrong hỗn hợp Xlà A. C3H7NH2 vàC4H9NH2 B. CH3NH2 vàC2H5NH2 C. CH3NH2 và(CH3)3N. D. C2H5NH2 vàC3H7NH2. Hướng dẫn giải
DẠYKÈMQUYNHƠN OFFICIAL Trang11
M2,142 0,05 Gọi công thức
của
.n2n3 CHNn1
n1,8
Gọi
. 2n RNHn1 Phương trìnhhóa học: 2 3 n n RNHnHClRNHCl ← 0,12mol 0,12 n Tacó: 0,12R16n4,44 n R 21 n Nếu (loại) n1R21 Nếu (thỏa mãn) n2R42 → Chọn D Bài tập tự luyện dạng 2 Bài tập cơ bản
Bảo toàn khối lượng:
HClmuoáiX3 m , m 9252,11mm ,825ga
HCl n0,05mol Amin đơn chức: aminHCl nn0,05mol
chung
hỗn hợp haiamintrongXlà
42143
14
→ Công thức của haiamintrong hỗn hợp XlàCH3NH2 vàC2H5NH2 → Chọn B. Ví dụ 4: Để phản ứng hoàntoàn với 4,44gam một amin (bậc một, mạch cacbonkhôngphânnhánh) bằng dung dịch HCl, tạo ra8,82gam muối. Amincócông thức là A. H2NCH2CH2CH2CH2NH2 B. CH3CH2CH2NH2 C. H2NCH2CH2NH2. D. H2NCH2CH2CH2NH2. Hướng dẫn giải
công thức của aminlà
Câu 1: Cho2,0gam hỗn hợp X gồm metylamin, đimetylamin phản ứng vừa đủ với 0,05molHCl,thu được mgam muối. Giá trị của mlà
A. 3,825. B. 4,725. C. 2,550. D. 3,475. Câu 2: Cho4,5gamaminX(no, đơn chức, mạch hở) tác dụng hết với dung dịch HCl dư, thu được 8,15 gam muối. Số nguyên tử hiđro trongphân tử Xlà
A. 7. B. 4. C. 5. D. 2. Câu 3: Để phản ứng hết với 25gamdung dịch của một amin đơn chức X nồng độ 12,4% cần dùng100ml dung dịch HCl1M.Công thức phân tử của Xlà
A. C2H7N. B. C3H7N. C. C3H5N. D. CH5N. Câu 4: Cho5,9gamamin đơn chức Xtác dụng vừa đủ với dung dịch HCl,saukhi phản ứng xảy rahoàn toànthu được dung dịch Y.Làmbay hơi dung dịch Y được 9,55gam muối khan. Số công thức cấu tạo ứng với công thức phân tử của Xlà
A. 5. B. 4. C. 2. D. 3. Bài tập nâng cao
OFFICIAL
Câu 5: Cho hoàn toàn 8,88 gam một amin (bậc một, mạch cacbon không phân nhánh) phản ứng hết với HCl, tạo ra17,64gam muối. Amincócông thức là A. H2NCH2CH2CH2CH2NH2. B. CH3CH2CH2NH2. C. H2NCH2CH2NH2 D. H2NCH2CH2CH2NH2 Dạng 3: Phản ứng đốt cháy – Kết hợp giữa phản ứng cháy và phản ứng với axit
Phương pháp giải
Chúýtrongbài tập về phản ứng cháy: •Cách đặt công thức chung của amin: Aminno, đơn chức, mạch hở: .n2n3 CHNn1 Aminno,hai chức, mạch hở: .n2n42 CHNn2
Ví dụ: Hỗn hợp E gồm baaminno, đơn chức. Đốt cháy hoàn toàn m gam E bằng O2, thu được CO2, H2O và 0,672 lít khí N2 (đktc). Mặt khác, để tác dụng với mgamE cần vừa đủ Vmldung dịch HCl 1M.Giá trị của Vlà A. 45. B. 60. C. 15. D. 30. Hướng dẫn giải
DẠYKÈMQUYNHƠN
Trang12
• Nhận xét: HClphaûnöùngvôùiaminNtrongamin n n
Tacó: HClphaûnöùngvôùiaminNtrongamin n n0,06mol V0,060,06lit60ml 1 → Chọn B. Ví dụ mẫu Ví dụ 1: Đốt cháyhoàntoàn một aminno, đơn chức, mạch hở Xthu được hơi nước,
lítN2 (các thể tíchkhí đều đo ở
tử
của Xlà
2N n0,03mol
Bảo toànnguyên tố N: 2NtrongaminN n2n0,06mol
4,48lítCO2 và1,12
đktc). Phân
khối
A. 45. B. 59. C. 31. D. 43. Hướng dẫn giải ; 2CO n0,2mol 2N n0,05mol
Gọi công thức phân tử của Xlà .n2n3 CHNn1 Phương trìnhhóa học: t n2n3 2 2 2 2 6n3 CHNOnCOn1,5HO0,5N 4 0,20,05mol Tacó phương trình: 0,20,05n2 n0,5 Vậy công thức của XlàC2H7N . M45 → Chọn A. Ví dụ 2: Đốt cháyhoàntoàn0,1mol một aminno, mạch hở X bằng oxi vừa đủ, thu được 0,5mol hỗn hợp Y gồm khívà hơi. Cho4,6gamXtác dụng với dung dịch HCl (dư), số molHCl phản ứng là A. 0,1mol. B. 0,4mol. C. 0,3mol. D. 0,2mol. Hướng dẫn giải Gọi công thức phân tử của Xlà n2n2kk CHNn1,k1 Bảo toànnguyên tố C,H,N:
DẠYKÈMQUYNHƠN OFFICIAL Trang13
2 HO X
n
2 2 NX k
2 Tacó: 222 COHON nnn0,1.nn10,5k0,5k0,1.2nk1mol Theo đề bài: 222 COHON nnn0,5mol 0,12nk10,5 2nk15 2nk4 ;n1k2 Vậy XlàCH2(NH2)2 (0,1mol) Bảo toànnguyên tố N: NtrongaminX n2n0,2mol Cho4,6gamXtác dụng với dung dịch HCl (dư): HClphaûnöùngvôùiaminNtrongamin n n0,2mol → Chọn D. Bài tập tự luyện dạng 3 Bài tập cơ bản
2 COX nnn0,1nmol
2n2k
n0,1n10,5kmol
nn0,1.0,5kmol
Câu 1: Đốt cháyhoàntoàn6,2gammetylamin(CH3NH2),thu được sản phẩm có chứa VlítkhíN2 (đktc). Giá trị của Vlà
A. 3,36. B. 2,24. C. 4,48. D. 1,12.
Câu 2: Đốt cháyhoàntoànhaiaminno, đơn chức bậc một đồng đẳng kế tiếp thu được: . 22 COHO n:n1:2
Công thức phân tử của haiaminlà:
A. CH3NH2,C2H5NH2 B. C2H5NH2,C3H7NH2 C. C4H9NH2,C5H11NH2. D. C2H7NH2,C4H9NH2.
Câu 3: Đốt cháyhoàntoànaminX(no, đơn chức, mạch hở), thu được 0,4molCO2 và0,05molN2.Công thức phân tử của Xlà
OFFICIAL
A. C2H7N. B. C4H11N. C. C2H5N. D. C4H9N. Câu 4: Đốt cháyhoàntoàn một aminX đơn chức bậc một trongkhíoxi dư, thu được khíN2;13,44lítkhí CO2 (đktc) và18,9gamH2O. Số công thức cấu tạo của Xlà A. 3. B. 1. C. 2. D. 4. Câu 5: Đốt cháyhoàntoànamin đơn chức X bằng O2 thu được 0,05molN2;0,3molCO2 và6,3gamH2O. Công thức phân tử của Xlà A. C4H9N. B. C2H7N. C. C3H7N. D. C3H9N. Câu 6: Đốt cháyhoàntoàn6,2gam một amin bậc một, no, đơn chức, mạch hở cần dùng10,08lítkhíO2 (đktc). Công thức của aminlà
A. C2H5NH2. B. CH3NH2. C. C3H7NH2. D. C4H9NH2. Câu 7: Đốt cháyhoàntoànhaiaminno, đơn chức đồng đẳng kế tiếp cần 2,24lítO2 thu được 1,12lítCO2 (cáckhí đều đo ở điều kiện tiêu chuẩn). Công thức của haiaminlà:
A. C3H7NH2,C4H9NH2
B. C2H5NH2,C3H7NH2 C. C4H9NH2,C5H11NH2. D. CH3NH2,C2H5NH2. Câu 8: Khi đốt cháyhoàntoàn một amin đơn chức X,thu được 8,4lítkhíCO2;1,4lítkhíN2 (các thể tích khí đo ở đktc) và10,125gamH2O.Công thức phân tử của Xlà
A. C3H7N. B. C2H7N. C. C3H9N. D. C4H9N. Câu 9: AminXcócông thức phân tử trùng với công thức đơn giản nhất. Đốt cháyhoàntoàn một lượng X cần dùng vừa đủ 0,475molO2,thu được 0,05molN2 và19,5gam hỗn hợp gồm CO2 vàH2O.Công thức phân tử của Xlà
A. C3H7N. B. C3H9N. C. C2H7N. D. C4H11N. Câu 10: Đốt cháy hoàn toàn m gam hỗn hợp ba amin X, Y, Z bằng một lượng không khí vừa đủ (trong khôngkhí1/5 thể tíchlàoxi,còn lại là nitơ) thu được 26,4gamCO2;18,9gamH2Ovà104,16lítkhíN2 (ở đktc). Giá trị của mlà
A. 13,5. B. 16,4. C. 15,0. D. 12,0. Câu 11: Đốt cháy4,56gam hỗn hợp E chứa metylamin, đimetylamin, trimetylamin cần dùng0,36molO2. Mặt khác, lấy 4,56gamEtác dụng với dung dịch HClloãng dư thì khối lượng muối thu được là A. 9,67gam. B. 8,94gam. C. 8,21gam. D. 8,82gam. Bài tập nâng cao
Câu 12: Đốt cháyhoàntoàn0,1mol một aminno, mạch hở X bằng oxi vừa đủ, thu được 0,5mol hỗn hợp Y gồm khívà hơi. Cho4,6gamXtác dụng với dung dịch HCl (dư), số molHCl phản ứng là
A. 0,1mol. B. 0,2mol. C. 0,4mol. D. 0,3mol.
DẠYKÈMQUYNHƠN
Trang14
Câu 13: Hỗn hợp M gồm một esteno, đơn chức, mạch hở vàhaiaminno, đơn chức, mạch hở XvàYlà đồng đẳng kế tiếp (). Đốt cháyhoàntoàn một lượng Mthu được N2;5,04gamH2Ovà3,584lít XYMM CO2 (đktc). Khối lượng molphân tử của chất Xlà
A. 59. B. 31. C. 45. D. 73.
Câu 14: Đốt cháy hoàn toàn m gam một amin X đơn chức bằng lượng không khí vừa đủ thu được 17,6 gamCO2;12,6gamH2Ovà69,44lítN2 (đktc). Giả thiết khôngkhí chỉ gồm N2 vàO2 trong đó oxi chiếm 20% thể tíchkhôngkhí.Xcócông thức là
A. C2H5NH2. B. C3H7NH2. C. CH3NH2. D. C4H9NH2. Câu 15: Đốt cháyhoàntoàn50ml hỗn hợp khíX gồm trimetylaminvàhai hiđrocacbon đồng đẳng kế tiếp bằng một lượng oxi vừa đủ, thu được 375ml hỗn hợp Y gồm khívà hơi. Dẫn toàn bộ Y đi quadung dịch H2SO4 đặc (dư), thể tíchkhícòn lại là175ml.Các thể tíchkhívà hơi đo ở cùng điều kiện. Hai hiđrocacbon đó là A. C2H4 vàC3H6. B. C3H6 vàC4H8. C. C3H8 vàC4H10. D. C2H6 vàC3H3. Dạng 4: Phản ứng của anilin với brom Phương pháp giải Phương trìnhhóa học: C6H5NH2 +3Br2 → Br3C6H2NH2 +3HBr Tínhtheo phương trìnhhóa học.
OFFICIAL
Ví dụ: Cho nước brom dư tác dụng với dung dịch chứa 0,02 mol anilin thu được m gam kết tủa. Giá trị của mlà A. 6,6. B. 6,8. C. 7,2. D. 7,6. Hướng dẫn giải Phương trìnhhóa học: C6H5NH2 +3Br2 → Br3C6H2NH2 +3HBr 0,02 → 0,02mol 3622 BrCHNH m0,023306,6m ga m
DẠYKÈMQUYNHƠN
Trang15
→ Chọn
Ví dụ mẫu Ví dụ 1: Để tác dụng hoàntoàn với dung dịch chứa molanilin cần vừa đủ Vmldung dịch brom 31,5.10 0,01M.Giá trị của Vlà A. 450. B. 300. C. 250. D. 200. Hướng dẫn giải Phương trìnhhóa học: C6H5NH2 +3Br2 → Br3C6H2NH2 +3HBr → mol 31,5.10 34,5.10 3 V4,5.100,45lit450ml 0,01 → Chọn A.
A.
132,00.
Biết ,giáH80%
206,25. D. 257,81.
H80%
Câu 1: Dung dịch chứa amiligamanilinlàm mất màu vừa hết 60ml nước brom0,01M.Giá trị của alà A. 55,8. B. 27,9. C. 18,6. D. 11,6. Câu 2: Cho27,9gamanilintác dụng với dung dịch brom, phản ứng xảy rahoàntoàn tạo 49,5gam kết tủa. Khối lượng bromtrongdung dịch bromban đầu là A. 72gam. B. 24gam. C. 48gam. D. 14gam. Câu 3: Cho nước brom đến dư vào dung dịch anilin, thu được 165 gam kết tủa 2,4,6-tribromanilin. Biết , khối lượng anilincótrongdung dịch ban đầu là
A. 42,600gam. B. 37,200gam. C. 58,125gam. D. 46,500gam.
DẠYKÈMQUYNHƠN OFFICIAL Trang16
Ví dụ 2: Chobromvào58,125gamanilin,thu được mgam kết tủa 2,4,6-tribromanilin.
trị của mlà A. 165,00. B.
C.
Hướng dẫn giải 652 CHNHanilin nn0,625mol Nếu ,tacó phương trìnhhóa học: H100% C6H5NH2 +3Br2 → Br3C6H2NH2 +3HBr 0,625 → 0,625mol 2623HNC2,4,6tribroma B nili Hr n mm0,625330206,25gam
Với thì H80% 2,4,6tribromanilin m206,2580%165gam → Chọn A. Bài tập tự luyện dạng 4
Dạng 1: Lí thuyết trọng tâm 1-A 2-C 3-B 4-A 5-A 6-A 7-C 8-D 9-A 10-A 11-D 12-D 13-B 14-D 15-A
Câu 6:
Với công thức có2 đồng phân(do gốc C3H7 có2 đồng phân cấu tạo). 37 3 3
CH | CHNCH
CH | CHNCH
Với công thức có1 đồng phân. 25 325
→ Có3 đồng phânamin bậc ba ứng với công thức phân tử C5H13N.
Câu 7: Amin bậc một có dạng C3H7NH2 có2 đồng phân(do gốc C3H7 có2 đồng phân cấu tạo).
Câu 8: Số amin thơm bậc một ứng với công thức phần tử C7H9Nlà4.
C6H5CH2NH2;o–CH3–C6H4NH2,p–CH3–C6H4NH2,m–CH3–C6H4NH2
Câu 9: Amin bậc một có dạng C4H9NH2 có4 đồng phân(do gốc có4 đồng phân cấu tạo).
Câu 11: Thứ tự sosánh lực bazơ: Amin thơm bậc II<amin thơm bậc I<NH3 <aminno bậc I<aminno bậc II<NaOH → Sắp xếp các chất theo thứ tự lực bazơ giảm dần là:(C2H5)2NH(3)>C2H5NH2 (2)>NH3 (4)>C6H5NH2 (1).
Câu 12: CH3NH2 vàC6H5NH2 đều làaminnêncótính bazơ, phản ứng được với dung dịch axitHCl. Câu 13:
(1)saivìmetylaminlàm quỳ tím chuyển xanh. (2),(3) đúng. (4)saivìCH3NH2,C2H5NH2,CH3NHCH3,(CH3)3Nlàcác chất khí.
Câu 14:
NhómCH3 lànhóm đẩy electron,nhómnày đẩy electron về phíanhómNH2 làm tăng mật độ electron trênnhómNH2,làm tăng tính bazơ.
NhómC6H5,NO2 lànhómhútelectron,nhómnàyhútelectron của nhómNH2 làm giảm mật độ electron trênnhómNH2,làm giảm tính bazơ.
Chất (c) do có nhóm CH3 đẩy e về vòng làm giảm khả năng hút e của nhóm C6H4 nên có tính bazơ mạnh hơn chất (a).
Chất (d)cónhómNO2 húte mạnh làm tăng khả năng húte của nhómNH2,cànglàm giảm tính bazơ.
Câu 15:
Chometylamin dư lần lượt vàocácdung dịch:
AlCl3 tạo kết tủa trắng keo.
FeCl3 tạo kết tủa màunâu đỏ.
Cu(NO3)2 tạo kết tủa màuxanhlam,sau đó kết tủa tan tạo dung dịch phức.
HClvàNa2SO4 không tạo kết tủa.
Dạng 2: Phản ứng với axit
DẠYKÈMQUYNHƠN
Trang17 ĐÁP
OFFICIAL
ÁN
1-A 2-A 3-D 4-B 5-D
Câu 1: Bảo toàn khối lượng: muoáiaminHCl20,0536,53,825gammmm
Câu 2:
Bảo toàn khối lượng:
HClmuoáiamin8,154,53,65gammmm HCl n0,1mol Amin đơn chức: aminHCl nn0,1mol XlàC2H5NH2 → Số nguyên tử hiđro trongphân tử Xlà7. amin M4,545 0,1 Câu 3: aminX m25.12,4%3,1gam
Amin đơn chức: aminHCl nn0,1mol X M3,131 0,1 → Công thức phân tử của XlàCH3NH2. Câu 4: Bảo toàn khối lượng: HClmuoáiamin9,555,93,65gammmm mHCl =mnuối -mamin HCl n0,1mol Amin đơn chức: aminHCl nn0,1mol Công thức phân tử của XlàC3H9N. X M5,959 0,1 Số công thức cấu tạo ứng với công thức phân tử của Xlà4. C3H7NH2 (2 đồng
DẠYKÈMQUYNHƠN OFFICIAL Trang18
phân),CH3–NH–C2H5,(CH3)3N. Câu 5: Bảo toàn khối lượng: HClmuoáiamin m m mm8,76ga HCl n0,24mol Nếu aminlà đơn chức: aminHCl nn0,24mol (Khôngcócông thức aminnào thỏa mãn) amin M8,8837 0,24 Nếu aminlàhai chức: aminHCl 1 nn0,12mol 2 amin M8,8874 0,12 → Công thức của aminlàH2NCH2CH2CH2NH2. Dạng 3: Phản ứng đốt cháy – Kết hợp giữa phản ứng cháy và phản ứng với axit
DẠYKÈMQUYNHƠN OFFICIAL Trang19
2
X
→
1,050,6nn1,5nn 0,3mol 1,5 Số nguyên tử C 2CO amin n0,62 n0,3 → Công thức phân tử của XlàC2H7N. MàXlàamin bậc một nênXcócông thức cấu tạo làC2H5–NH2. Câu 5: 2 HO n0,35mol Amin đơn chức: 2XN n2n0,1mol Số nguyên tử C 2CO X n 3 n Số nguyên tử H 2 HO X 2n2.0,357 n0,1 → Công thức phân tử của XlàC3H7N. Câu 6: 2O n0,45mol
1-B 2-A 3-B 4-B 5-C 6-B 7-D 8-C 9-A 10-A 11-B 12-B 13-B 14-A 15-B Câu 1: 2N n0,1mol Metylaminlàamin đơn chức: 2 32NCHNH 1 nn0,1mol 2 2N V0,1.22,42,24lit
Câu 2: Gọi công thức chung của haiaminlà .n2n3 CHNn1 Quátrình: 2 O,t n2n3 2 2 2n3 CHnCOHO 2 12mol Tacó phương trình: n2n3 n1,5 12 → HaiaminlàCH3NH2 vàC2H5NH2. Câu 3: Gọi công thức phân tử của Xlà .n2n3 CHNn1 Tacó: 2XN n2n0,1mol
CO
n n4 n
Công thức phân tử của XlàC4H11N. Câu 4: ; 2CO n0,6mol
2 HO n1,05mol Tacó: 2 2 HOCOaminamin
Gọi công thức phân tử của aminno, đơn chức, mạch hở Xlà .n2n3 CHNn1 Phương trìnhhóa học: t n2n3 2 2 22 6n3 2n31 CHNOnCOHON 4 22
0,45mol 6,2 14n17
Tacó phương trình: Công thức phân tử aminlàCH3NH2. 6,20,45n1 16n3 4n17 4
Gọi công thức phân tử chung của haiaminno, đơn chức, mạch hở
DẠYKÈMQUYNHƠN OFFICIAL Trang20
Xlà .n2n3 CHNn1 Phương trìnhhóa học: t n2n3 2 2 22 6n3 2n31 CHNOnCOHON 4 22 0,10,05mol Tacó phương trình: 6n3n n1,5 4.0,10,05 →
2
2
2
Bảo
C,H: Số nguyên tử C 2CO amin n0,3753 n0,125 Số nguyên tử H 2 HO amin 2n2.0,56259 n0,125 Công thức phân tử của XlàC3H9N. Câu 9: Gọi số molCO2 vàH2O lần lượt làa,bmol. 44a18b19,5 * Bảo toànnguyên tố O: 2ab20,4750,95 ** Từ và suyra: ; ***a0,3 b0,35 Tacó: 2NN X n2n0,1mol Bảo toànnguyên tố C,Htacó: 2 2 CCO HHO N nn0,3mol n2n0,7mol n0,1mol → Công thức đơn giản nhất của XlàC3H7N.
Câu 7: ; 2O n0,1mol 2CO n0,05mol
Công thức của haiaminlàCH3NH2 vàC2H5NH2. Câu 8: ; ;
CO n0,375mol
N n0,0625mol
HO n0,5625mol
Amin đơn chức: 2amimN n2n0,125mol
toànnguyên tố
DẠYKÈMQUYNHƠN OFFICIAL Trang21 →
3
7
Câu
2
2
2
Bảo
2
2 2 NO kk
Bảo
2 22 2 2ONCOHON kk mmmmmm m1,125324,52826,418,94,6528 m13,5gam Câu 11: Gọi công thức tổng quát của Elà .n2n3 CHNn1 Phương
t n2n3 2 2 22 6n3 2n31 CHNOnCOHON 4 22 0,36mol 4,56
Tacó:
4
đều làamin đơn chức nên EHCl 4,56 nn 0,12mol 141,517 Bảo toàn khối lượng: muoá i m4,560,12.36,58,94gam Câu 12: Gọi công thức tổng quát của Xlà n2n2t CHNn1,t1 Sơ đồ phản ứng: 2 O,t n2n2tt 2 2 2CHNnCOn10,5tHO0,5tN 0,1 →0,1n→ → 0,05tmol 0,1n0,10,05t Tacó: ,0,2n0,1t0,10,52nt4n1 t2 → Công thức của XlàCH2(NH2)2. Cho4,6gamXtác dụng với dung dịch HCI: X HClX n0,1moln2n0,2mol Câu 13: Đốt cháyesteno, đơn chức, mạch hở: 22 COHOnn 2 2HOCO amin M nn n 0,08moln 1,5 Tacó: Số nguyên tử C M MMamin Cn0,160,162 nnn Mà số nguyên tử C của este → Số nguyên tử 2 X,Y C2 → XlàCH3NH2 M31
Công thức phân tử của XlàC
H
N.
10: ;;
CO n0,6mol
HO n1,05mol
N n4,65mol
toànnguyên tố O: 22
COHO O 2nn n 1,125mol 2
n4n4,5mol
toàn khối lượng trong phản ứng đốt cháy:
trìnhhóa học:
14n17
4,560,366n1,51n3 4n17
CócácamintrongE
DẠYKÈMQUYNHƠN OFFICIAL Trang22
Câu 14: ;; 2CO n0,4mol 2 HO n0,7mol 2N n3,1mol
H5NH2. Câu 15: ; 2 HO V375175200ml 22 CON VV175mol Tỉ lệ về thể tíchchínhlà tỉ lệ về số mol: Số nguyên tử 2 HO X 2V2.200 H 8 V50 DoC3H9Ncó số nên hiđrocacbon có số . H8 H8 1 Tacó: 2 39 2 N CO CHN V50mlV25mlV150ml → Số nguyên tử 2CO X V150 C 3 V50 DoC3H9Ncó số nên hiđrocacbon có số H3 C3 2 Chỉ đáp ánB thoả mãn và . 1 2 Dạng 4: Phản ứng của anilin với brom 1-C 2-A 3-C Câu 1: 2 2 652 Br Br CHNH n n0,0006moln0,0002mola0,0186gam18,6mg 3 Câu 2: ; anilin n0,3mol 2623 HNCHBr n0,15mol Ta thấy Anilin dư, Br2 hết. 2623652 HNCHBrCHNHnn Tacó: 22623 BrHNCHBr n3n30,150,45mol 2Br m0,45.16072gam Câu 3: 2623H2,4,6tribromanil B in HNCr nn0,5mol
Bảo toànnguyên tố O: 2 22 OCOHO2n2nn 2O 2.0,40,7 n 0,75mol 2 2 2 NtrongkhoângkhíO n 4n3mol 2 Nsinhratrongpön 3,130,1mol Amin đơn chức: 2aminN n2n0,2mol Bảo toànnguyên tố C,H: Số nguyên tử C 2CO amin n0,42 n0,2 Số nguyên tử H 2 HO amin 2n2.0,77 n0,2 Công thức phân tử của XlàC2H7NhayC2
DẠYKÈMQUYNHƠN OFFICIAL Trang23 Nếu , phương trìnhhóa học: H100% C6H5NH2 +3Br2 H2NC6H2Br3 +3HBr 0,5 ←
652CHNH
Với
0,5mol
mm0,5.9346,5gam
tacó: H80%
anilin m46,5:80%58,125gam
BÀI 5: AMINO AXIT
Mục tiêu
Kiến thức
+Nêu được khái niệm, tính chất vật lí,tính chất hóa học của aminoaxit.
+ Đọc được têncácaminoaxitvà một số tênthông thường của một số aminoaxit thường gặp.
+Trìnhbày được tính chất hóa học, viết được các phương trìnhhóa học tương ứng với tính chất.
+Phát biểu được các ứng dụng của aminoaxittrong thực tế.
Kĩ năng
+ Sosánh được pH của cácdung dịch aminoaxitkhácnhau.
+ Giải được cácbài tập liênquan.
I. LÍ THUYẾT TRỌNG TÂM
Aminoaxitlà loại hợp chất hữu cơ tạp chức, phân tử chứa đồng thời nhóm amino (NH2) và nhóm cacboxyl (COOH). Cácaminoaxitcótên gọi xuất phát từ tênaxit tương ứng (tên hệ thống hoặc tên thường), khi đó cóthêm tiếp ngữ amino trước tên axit và số hoặc chữ cái chỉ nhóm amino (tùy vào đó là tên hệ thống haybán hệ thống). Ngoàira -aminoaxitthiênnhiêncòn cótênriêng(tên thường).
OFFICIAL
DẠYKÈMQUYNHƠN
Trang1
Tênthay thế Tênbán hệ thống
PTK 2 2 CHCOOH | NH Axit2-aminoetanoic Axitaminoaxetic glyxin Gly 75 3 2 CHCHCOOH | NH Axit 2-aminopropanoic Axit -aminopropionic alanin Ala 89 3 32 CHCHCHCOOH || CHNH Axit 2-amino-3-metylbutanoic Axit -aminoisovaleric valin Val 117 224 2 HNCHCHCOOH | NH Axit 2,6-điaminohexanoic Axit , điaminocaproic lysin Lys 146 22 2 HOOCCHCHCOOH | NH Axit 2-aminopentanđioic Axit -aminoglutaric axit glutamic Glu 147 2. Cấu tạo phân tử, tính chất vật lí
Ví dụ: 22 NHCHCOOH Chú ý: Vị trí nhóm amino (NH3): 654321 CCCCCCCOOH Một số các -aminoaxit thường dùng: Công thức
Tên thường Kí hiệu
Hainhóm chức trongaminoaxit tương tác với nhau tạo raion lưỡng cực: 2 3 HNRCOOHHNRCOO (dạng phân tử)(dạng ion lưỡng cực) Ở nhiệt độ thường, aminoaxitlà chất rắn kết tinh, không màu, vị ngọt, dễ tan trong nước và có nhiệt độ nóng chảy cao.
3. Tính chất hóa học
a. Tính lưỡng tính
Aminoaxit vừa tác dụng được với axit, vừa tác dụng được với bazơ.
Nhóm NH2: Có tính bazơ.
Nhóm COOH: Có tính axit. Tác dụng với axit: 2 3 HNRCOOHHClClHNRCOOH
Chú ý: Muối sau phản ứng của amino axit tác dụng với HCl có thể tiếp tục phản ứng với NaOH: 3 2 2 ClHNRCOOH2NaOHHNRCOONaNaCl2HO Tác dụng với bazơ: 2 2 2 HNRCOOHNaOHHNRCOONaHO Chú ý: Muối sau phản ứng của amino axit tác dụng với NaOH có thể tiếp tục phản ứng với HCl: 2 3 HNRCOONa2HClClHNRCOOHNaCl b. Tính axit – bazơ
Xétaminoaxitcócông thức tổng quát: 2b a HNRCOOH:
Aminoaxitcó: Làm quỳ tím chuyển màu hồng. ab Aminoaxitcó: Làm quỳ tímkhông đổi màu. ab
Aminoaxitcó: Làm quỳ tím chuyển màuxanh. ab Ví dụ: Axit glutamic làm quỳ tím chuyển màu hồng. Glyxin, alanin, valin không làm đổi màu quỳ tím. Lysin làm quỳ tím chuyển màu xanh. c. Phản ứng este hóa (của nhóm COOH) Tương tự axitcacboxylic,aminoaxit phản ứng với ancolkhicó mặt axitvô cơ mạnh:
DẠYKÈMQUYNHƠN
Trang2
OFFICIAL
xt 2 2 2 HNRCOOHROHHNRCOORHO
t 22 2 2 5 5n nHNCHCOOHNHCHCOnHO
d. Phản ứng trùng ngưng Một số -, -aminoaxitthamgia phản ứng trùng ngưng tạo poliamit.
axit -aminocaproic policaproamit(nilon-6)

Chú ý: Nhóm NH2 của phân tử này phản ứng tách nước với nhóm COOH của phân tử kia.
4. Ứng dụng
Cácaminoaxitthiênnhiên (hầu hết làcác -aminoaxit)là những hợp chất cơ sở để kiến tạo nêncác loại protein của cơ thể sống.
Muối mononatri của axitglutamicdùnglàm bột ngọt (mìchính).
Axitglutamiclà thuốc hỗ trợ thần kinh,methioninlà thuốc bổ gan.
Axit6-aminohexanoic(-aminocaproic)và7-aminoheptanoic( aminoenantoic)lànguyên liệu sản xuất tơ nilon-6vànilon-7.
DẠYKÈMQUYNHƠN
OFFICIAL
Trang3
KHÁI NIỆM
Amino axit là loại hợp chất hữu cơ tạp chức trong phân tử chứa đồng thời nhóm amino (NH2) và nhóm cacboxyl (COOH).
HNCHCOOHHNCHCOO
TÍNH CHẤT VẬT LÍ
Aminoaxitlà những hợp chất có cấu tạo ion lưỡng cực nên ở điều kiện thường chúnglà chất rắn kết tinh, tương đối dễ tan trong nước vàcó nhiệt độ nóng chảy cao.
AMINO AXIT
TÍNH CHẤT HÓA HỌC
Tính lưỡng tính 22 32 HNCHCOOHHClClHNCHCOOH 22 22 2 HNCHCOOHNaOHHNCHCOONaHO
Tính axit – bazơ của dung dịch amino axit Xétaminoaxitcócông thức: 2b a HNRCOOH
Nếu Quỳ tím chuyển xanh. ab Nếu Quỳ tímkhông đổi màu. ab Nếu Quỳ tím chuyển đỏ. ab
este hóa (của nhóm COOH)
ỨNG DỤNG
Các amino axit thiên nhiên (hầu hết là các -amino axit) là những hợp chất cơ sở để kiến tạo nên các loại protein của cơ thể sống.
Muối mononatri của axit glutamic dùng làm mì chính.
Axit glutamic là thuốc hỗ trợ thần kinh, methionin là thuốc bổ gan.
Axit 6-aminohexanoic (-aminocaproic) và 7-aminoheptanoic ( -aminoenantoic) là nguyên liệu sản xuất tơ nilon-6 và nilon-7.
DẠYKÈMQUYNHƠN
Trang4 SƠ ĐỒ HỆ THỐNG
OFFICIAL
HÓA
22 32
Phản ứng
HClkhí 22 25 22 252 HNCHCOOHCHOHHNCHCOOCHHO Phản ứng trùng ngưng t 22 2 2 5 5n nHNCHCOOHNHCHCOnHO axit -aminocaproic policaproamit(nilon-6)
II. CÁC DẠNG BÀI TẬP
Dạng 1: Lí thuyết trọng tâm
Kiểu hỏi 1: Khái niệm và cấu tạo phân tử Ví dụ mẫu
Ví dụ 1: Aminoaxitlà hợp chất hữu cơ trongphân tử có chứa
A. nhómaminovànhómcacboxyl.
B. một nhómaminovà một nhómcacbonyl. C. nhómamino. D. nhómcacboxyl.
Hướng dẫn giải
Amino axit là hợp chất hữu cơ tạp chức trong phân tử có chứa nhóm amino (NH2) và nhóm cacboxyl (COOH).
Chọn A. Ví dụ 2: Công thức cấu tạo nàosau đây tương ứng với -aminoaxit?
A. B. 3 2 CHCHNHCOONa 2 22 HNCHCHCOOH C. D. 3 2 CHCHNHCOOH 2 2 3 HNCHCHCHCOOH Hướng dẫn giải Các -aminoaxitlàaminoaxitcónhómcacboxylCOOHvànhómaminoNH2 cùng gắn vào một cacbon haynhómaminoNH2 được gắn vàoC vị trí số 2. Chọn C. Ví dụ 3: Chất rắn Xkhôngmàu, dễ tantrong nước, kết tinh ở điều kiện thường. Xlà chất nàosau đây?
A. C6H5NH2. B. C2H5OH. C. H2NCH2COOH. D. CH3NH2. Hướng dẫn giải
Aminoaxitlà những hợp chất có cấu tạo ion lưỡng cực nên ở điều kiện thường chúnglà chất rắn kết tinh, dễ tantrong nước.
H2NCH2COOHlà chất rắn khôngmàu, dễ tantrong nước, kết tinh ở điều kiện thường. Chọn C. Kiểu hỏi 2: Danh pháp Phương pháp giải Trong dạng bài
DẠYKÈMQUYNHƠN
Trang5
OFFICIAL
này, chủ yếu câu hỏi liên quan đến
chắc tên
Ví
A.
6
5
2.
tên thường gọi của -amino axit thiên nhiên. Học
sinh nắm
thường của năm -aminoaxitnày.
Ngoàira, cũng cần biết cách gọi tên hệ thống vàbán hệ thống của cácaminoaxit.
dụ: Alanincócông thức là
C
H
NH
B. CH3CH(NH2)COOH. C. H2NCH2COOH. D. H2NCH2CH2COOH. Hướng dẫn giải
Alaninlàtên thường gọi của một trong những -aminoaxit thường gặp cócông thức là: CH3CH(NH2)COOH . M89
Chọn B.
Ví dụ mẫu
Ví dụ 1: Tên gọi nàosau đây không phù hợp với hợp chất NH2CH(CH3)COOH?
A. Axit2-aminopropanoic.
B. Alanin. C. Axit -aminopropionic.
D. Axit -aminoisopropionic.
Hướng dẫn giải
Hợp chất NH2CH(CH3)COOHcótênlà:
1.Tênthay thế: Axit2-aminopropanoic.
2.Tênbán hệ thống: Axit -aminopropionic.
3.Tên thường: Alanin. Khôngcótênlàaxit -aminoisopropionic. Chọn D.
Kiểu hỏi 3: Đồng phân
Phương pháp giải
OFFICIAL
Dạng câu hỏi này thường chỉ hỏi các amino axit no, mạch hở, có một nhóm NH2 và một nhóm COOH.
Công thức chunglà: n2n12 CHON
Cóhai loại đồng phân cấu tạo: Do mạch cacbon. Do vị trínhómNH2
Ví dụ: Số đồng phân cấu tạo aminoaxitcócông thức phân tử C4H9O2Nlà A. 2. B. 4. C. 5. D. 3. Hướng dẫn giải
DẠYKÈMQUYNHƠN
Trang6
lượt vào
trí2,3,4
32CCCOOH | C Đặt nhómNH2 lần lượt vào
trí2,3
Mạch Ckhôngphânnhánh: 432 CCCCOOH Đặt nhómNH2 lần
vị
3 đồng phân.
Mạch Cphânnhánh:
vị
2 đồng phân.
Vậy có5 đồng phânaminoaxitcócông thức phân tử C4H9O2N. Chọn C.
Ví dụ mẫu Ví dụ 1: Số đồng phân cấu tạo -aminoaxit ứng với công thức phân tử C4H9O2Nlà
A. 3. B. 4. C. 2. D. 6. Hướng dẫn giải Mạch cacbon: CCCCOOH;CCCOOH | C Các đồng phân -aminoaxit ứng với công thức phân tử C4H9O2Nlà: ; 32 2 CHCHCHNHCOOH3 32 CHCCHNHCOOH Chọn C. Chú ý: Đồng phân -amino axit thì điền nhóm amino (NH2) vào cacbon ở vị trí số 2. Kiểu hỏi 4: Tính chất vật lí Ví dụ mẫu Ví dụ: Trongcác chất sau, chất nàocó nhiệt độ nóng chảy cao nhất? A. Glyxin. B. Axitaxetic. C. Ancoletylic. D. Etanal. Hướng dẫn giải Glyxinlàaminoaxitcó tương tác tĩnh điện do tồn tại ở dạng nên nhiệt độ nóng chảy cao 32 HNCHCOO nhất. Chọn A. Chú ý: Amino axit là chất rắn, kết tinh, tan tốt trong nước, có nhiệt độ nóng chảy cao. So về nhiệt độ nóng chảy thì: Amino axit > Axit cacboxylic tương ứng. Kiểu hỏi 5: Môi trường dung dịch amino axit, so sánh pH các dung dịch, nhận biết Phương pháp giải Với (H2N)bR(COOH)a. Nếu: pHdung dịch <7. ab Làm quỳ tím chuyển màu hồng. Nếu: pHdung dịch ab 7
Làm quỳ tímkhông đổi màu. Nếu pHdung dịch >7. ab
Làm quỳ tím chuyển màuxanh. Ví dụ: Chocác chất sau:lysin,axitglutamic,valin,glyxin,alanin,trimetylamin,anilin. Số chất làm quỳ tím chuyển màu hồng, màuxanhvàkhông đổi màu lần lượt là: A. 1,2,4. B. 3,1,3. C. 2,2,3. D. 2,1,4. Hướng dẫn giải
Lysinlàaminoaxitcó số nhómCOOH< số nhómNH2 Làm quỳ tím chuyển màuxanh.
Axitglutamiclàaminoaxitcó số nhómCOOH> số nhómNH2 Làm quỳ tím chuyển màu hồng.
DẠYKÈMQUYNHƠN
Trang7
OFFICIAL
Valin,glyxin,alaninlàaminoaxitcó số nhómCOOH= số nhómNH2 Không đổi màu quỳ tím.
Trymetylamincótính bazơ Làm quỳ tím chuyển màuxanh.
Anilinlàamincótính bazơ yếu Khônglàm đổi màu quỳ tím. Có1 chất làm quỳ tím chuyển màu hồng; có2 chất làm quỳ tímsangmàuxanh;có4 chất khônglàm đổi màu quỳ tím.
Chọn A.
Ví dụ mẫu
Ví dụ 1: Cho các dung dịch loãng có cùng nồng độ sau: alanin (1); lysin (2); axit glutamic (3); HCl (4). Dung dịch cópH nhỏ nhất là
A. (1). B. (2). C. (3). D. (4). Hướng dẫn giải
OFFICIAL
AxitglutamicvàHCl đều cópH<7. TuynhiênHCllàaxit mạnh nêncógiá trị pH nhỏ hơn. Chọn D. Ví dụ 2: Để phân biết cácdung dịch riêng biệt, khôngmàusau:alanin,axitaxetic,etylamin,anilin bằng phương pháphóa học có thể dùngcác thuốc thử là:
A. Nước brom,Cu(OH)2.
B. Dung dịch Na2CO3,dung dịch AgNO3/NH3
C. Quỳ tím,Cu(OH)2.
D. Quỳ tím, nước brom.
Hướng dẫn giải
nhận biết:
DẠYKÈMQUYNHƠN
Trang8
6: Tính chất hóa học Ví dụ mẫu Ví dụ 1: Cho dãy các chất: H2NCH2COOH, C6H5NH2, C2H5NH2, CH3COONH4 Số chất trong dãy vừa tác dụng với dung dịch NaOH vừa tác dụng với dung dịch HCllà A. 2. B. 4. C. 3. D. 1. Hướng dẫn giải Các chất thỏa mãnlà:H2NCH2COOH,CH3COONH4 Phương trìnhhóa học: 22 22 2 HNCHCOOHNaOHHNCHCOONaHO 3 4 3 32 CHCOONHNaOHCHCOONaNHHO
Bảng
Anilin Axitaxetic Etylamin Alanin Quỳ tím Không đổi màu Chuyển đỏ Chuyển xanh Không đổi màu Nước brom Kết tủa trắng X X Không hiện tượng Chọn D. Kiểu hỏi
Chọn A. Ví dụ 2: Cho sơ đồ chuyển hóasau: Chất Ylà chất nàosau đây?
A. H2NCH2CH2COOH. B. CH3CH(NH3Cl)COONa. C. CH3CH(NH3Cl)COOH. D. CH3CH(NH2)COONa. Hướng dẫn giải Phương trìnhhóa học
Chọn D.
Kiểu hỏi 7: Ứng dụng, câu hỏi thực tiễn Ví dụ mẫu Ví dụ 1: Chất nàosau đây được sử dụng làm bột ngọt (mìchính)?
A. Muối mononatriglutamat B. Muối đinatri glutamat. C. Axitglutamic. D. Axitaxetic. Hướng dẫn giải Muối mononatri của axitglutamic(mononatriglutamat) được dùnglàmgia vị thức ăn. Chọn A. Bài tập tự luyện dạng 1 Bài tập cơ bản
Câu 1: Hợp chất nào dưới đây thuộc loại aminoaxit? A. H2NCH2COOH. B. CH3COOC2H5. C. C2H5NH2. D. HCOONH4. Câu 2: Dung dịch chứa chất nàosau đây làm quỳ tím đổi thànhmàuxanh? A. Glyxin. B. Lysin. C. Alanin. D. Axitglutamic. Câu 3: Công thức chung của aminoaxitno, mạch hở có một nhómNH2 và một nhómCOOHlà A. B. C. D.
DẠYKÈMQUYNHƠN OFFICIAL Trang9 22 32 2 HNCHCOOHHClClHNCHCOOHHO 3 4 3 42 CHCOONHHClCHCOOHNHClHO
HCl NaOH AlaninXY
3 2 3 3 CHCHNHCOOHHClCHCHNHClCOOH (Alanin)(X) 3 3 3 2 2 CHCHNHClCOOH2NaOHCHCHNHCOONaNaClHO (X)(Y)
n2n32 CHNOn2. n2n12 CHNOn2. n2n324 CHNOn3. n2n12 CHNOn2. Câu 4: Chất nàosau đây vừa phản ứng với dung dịch NaOH vừa phản ứng với dung dịch HCl? A. Anilin. B. Alanin. C. Metylamin. D. Axitaxetic. Câu 5: Dung dịch chất nàosau đây đổi màu quỳ tím chuyển sangxanh? A. Axit-2,6-điaminohexanoic. B. Axitaxetic. C. Axitglutamic. D. Alanin. Câu 6: Cho các chất: H2NCH2COOH, C2H5COOH, CH3NH2 và CH3(CH2)3NH2 Số chất làm đổi màu quỳ tím ẩm là
A. 1. B. 2. C. 4. D. 3. Câu 7: Chocác chất sau:H2NCH2COOH;CH3CH(NH2)COOH;HOOCCH2CH2CH(NH2)COOH; H2N(CH2)4CH(NH2)COOH. Số chất làm quỳ tím ẩm chuyển màulà
A. 1. B. 2. C. 3. D. 4. Câu 8: Cho ba dung dịch có cùng nồng độ mol: (1) H2NCH2COOH, (2) CH3COOH, (3) CH3CH2NH2. Dãy sắp xếp theo thứ tự pH tăng dần là:
A. (3),(1),(2). B. (1),(2),(3). C. (2),(3),(1). D. (2),(1),(3). Câu 9: Dung dịch chất nàosau đây làm quỳ tím chuyển thànhmàu hồng?
A. Axitaminoaxetic. B. Axit -aminopropionic. C. Axit -aminoglutaric. D. Axit -điaminocaproic. , Câu 10: Dung dịch nàosau đây làmchophenolphtalein đổi màu?
A. Glyxin. B. Metylamin. C. Axitaxetic. D. Alanin. Câu 11: Dung dịch chất nàosau đây không làm quỳ tím chuyển màu?
A. Axitglutamic. B. Alanin. C. Metylamin. D. Lysin. Câu 12: Dung dịch chứa chất nàosau đây làm quỳ tím đổi thànhmàuxanh?
A. Alanin. B. Glyxin. C. Lysin. D. Valin. Câu 13: Chodãycác chất: H2NCH2COOH,C2H5NH2,CH3NH2,CH3COOH. Số chất trongdãy phản ứng với HCltrongdung dịch là
A. 4. B. 1. C. 2. D. 3. Câu 14: Hai chất nàosau đây đều tác dụng được với dung dịch NaOHloãng?
A. CH3NH3ClvàCH3NH2. B. CH3NH3ClvàH2NCH2COONa.
C. CH3NH2 vàH2NCH2COOH.
Câu 15: Phát biểu nàosau đây sai?
D. ClH3NCH2COOC2H5 vàH2NCH3COOC2H5
A. Trongdung dịch, aminoaxit tồn tại ở dạng ion lưỡng cực.
B. Cácaminoaxitlà chất rắn, kết tinh.
C. Tất cả cácaminoaxittrongphân tử chỉ gồm một nhómNH2 và một nhómCOOH.
D. Hợp chất aminoaxitcótính lưỡng tính.
Câu 16: Phát biểu nàosau đây sai?
A. Trongphân tử -aminoaxit chỉ có một nhómNH2.
B. Aminoaxitlà hợp chất hữu cơ tạp chức.
C. Aminoaxitlà những chất rắn, kết tinh,tan tốt trong nước vàcó vị ngọt.
D. Nhóm chức COOHtrongaminoaxitcó phản ứng estehóa với ancol.
Câu 17: Ứng dụng nàosau đây của aminoaxitlà sai?
A. Axitglutamiclà thuốc bổ thần kinh,methioninlà thuốc bổ gan.
B. Muối đinatri glutamatlàgia vị cho thức ăn (gọi là bột ngọt haymìchính).
C. Aminoaxitthiênnhiên (hầu hết là -aminoaxit)là cơ sở kiến tạo proteintrong cơ thể sống.
D. Cácaminoaxit(nhómNH2 ở vị số 6,7…)lànguyên liệu sản xuất tơ nilon.
Câu 18: Phát biểu nàosau đây sai?
A. Dung dịch lysinlàm quỳ tím chuyển màuxanh.
DẠYKÈMQUYNHƠN
Trang10
OFFICIAL
B. Aminoaxitlà hợp chất hữu cơ tạp chức.
C. Dung dịch glyxinkhônglàm đổi màuphenolphtalein.
D. Anilintác dụng với nước brom tạo thành kết tủa vàng.
Câu 19: Phát biểu nàosau đây là đúng?
A. Axitglutamiclàthành phần chính của bột ngọt.
B. Aminoaxit thuộc loại hợp chất hữu cơ tạp chức.
C. Cácaminoaxitthiênnhiên hầu hết làcác -aminoaxit.
D. Ở nhiệt độ thường, cácaminoaxit đều là những chất lỏng.
Câu 20: Ứng với công thức phân tử C2H7O2N có bao nhiêu chất vừa phản ứng được với dung dịch NaOH, vừa phản ứng được với dung dịch HCl?
A. 4. B. 2. C. 1. D. 3. Câu 21: Số đồng phânaminoaxit ứng với công thức C3H7O2Nlà
A. 4. B. 1. C. 2. D. 3. Bài tập nâng cao
OFFICIAL
Câu 22: Hai hợp chất hữu cơ XvàYcócùngcông thức phân tử làC3H7O2N, đều là chất rắn ở điều kiện thường. Chất X phản ứng với dung dịch NaOH, giải phóng khí. Chất Y có phản ứng trùng ngưng. Các chất XvàY lần lượt là: A. vinylamonifomatvàamoniacrylat. B. axit2-aminopropionicvàaxit3-aminopropionic. C. axit2-aminopropionicvàamoniacrylat. D. amoniacrylatvàaxit2-aminopropionic. Câu 23: Cho sơ đồ phản ứng trongdung dịch: Biết các phản ứng xảy rahoàn
NaOH GlyxinXY toàn;X,Ylàcác chất hữu cơ vàNaOHdùng dư. Công thức phân tử của Ylà A. C2H4O2NNa. B. C2H5O2NNaCl. C. C3H6O2NNa. D. C2H6O2NCl. Câu 24: Chất Xcócông thức phân tử C4H9O2N. Biết:
YHCldöZNaCl Công thức cấu tạo của XvàZ lần lượt là A. H2NCH2CH2COOCH3 vàCH3CH(NH3Cl)COOH. B. CH3CH(NH2)COOCH3 vàCH3CH(NH3Cl)COOH. C. CH3CH(NH2)COOCH3 vàCH3CH(NH2)COOH.
DẠYKÈMQUYNHƠN
Trang11
D. H2NCH2COOC2H5 vàCIH3NCH2COOH. Câu 25: Cho sơ đồ chuyển hóa: 3 25 CHOH/HCl,t CHOH/HCl,t NaOHdö,t Axitglutamic Y Z T Biết Y,Z,Tlàcác chất hữu cơ chứa nitơ. Công thức phân tử của YvàT lần lượt là A. C6H12O4NClvàC5H7O4Na2N. B. C6H12O4NvàC5H7O4Na2N. C. C7H14O4NClvàC5H7O4Na2N. D. C7H15O4NClvàC5H8O4Na2NCl. Dạng 2: Tính lưỡng tính của amino axit Bài toán 1: Amino axit tác dụng với axit Phương pháp giải
HCl
4 XNaOHYCHO
n NHbnb.n n
Hướng
DẠYKÈMQUYNHƠN OFFICIAL Trang12
Aminoaxittác dụng với axit, phương trìnhhóa học: 2 3 b a b a HNRCOOHbHClClHNRCOOH dẫn giải Tacó: muoáiX HCl mm n30,1mol 6,5 Aminoaxitcó một nhómNH2: aaHCl nn0,1mol aa M10,3103 0,1 Công thức của Xcó dạng H2NRCOOH (C3H6) R M103164542 MàXlà -aminoaxitnêncông thức cấu tạo thu gọn của Xcó thể làCH3CH2CH(NH2)COOH. Chọn D. Bài toán 2: Amino axit tác dụng với bazơ Phương pháp giải
Số nhómamino HCl 2 HClaa aa
Bảo toàn khối lượng: aaHClmuoá immm muoáiaa HCl mm n 36,5 Ví dụ: Cho dung dịch chứa 14,6 gam lysin tác dụng với lượng dư 2 2 2 4 HNCHCHNHCOOH dung dịch HCl,thu được dung dịch chứa mgam muối. Giá trị của mlà A. 21,90. B. 18,25. C. 16,43. D. 10,95. Hướng dẫn giải lysin n0,1mol Lysincó2nhómNH2: HCllysin n2n0,2mols Bảo toàn khối lượng: muoáilysinHCl mmm14,60,236,521,9gam
Chọn A. Ví dụ mẫu Ví dụ 1: Xlà một -aminoaxit chỉ chứa một nhómNH2 và một nhómCOOH.Cho10,3gamXtác dụng với dung dịch HCl dư thu được 13,95gam muối. Công thức cấu tạo thu gọn của Xlà A. CH3CH(NH2)COOH. B. NH2CH2COOH. C. NH2CH2CH2COOH. D. CH3CH2CH(NH2)COOH.
2 2 2 b a b
n COOH:ana.n n Nhận xét: 2 HONaOHCOOH nnn Bảo toàn khối lượng: 2 aaNaOHmuoáiHOmmmm
alanin n0,06mol Alaninlàaminoaxitcó1nhómCOOH: 2 HOKOHaa nnn0,06mol Bảo toàn khối lượng: 2 alaninKOHmuoáikaliHOmmmm
DẠYKÈMQUYNHƠN OFFICIAL Trang13
muoá
Aminoaxittác muoáikali m7,62gam Chọn A. Ví dụ 2: Trong phân tử amino axit X có một nhóm amino và một nhóm cacboxyl. Cho 15 gam X tác dụng vừa đủ với dung dịch NaOH, cô cạn dung dịch sau phản ứng thu được 19,4 gam muối khan. Công thức của Xlà A. H2NC4H8COOH. B. H2NC3H6COOH. C. H2NC2H4COOH. D. H2NCH2COOH. Hướng dẫn giải
dụng với bazơ, phương trìnhhóa học:
a HNRCOOHaNaOHHNRCOONaaHO Số nhómcacboxyl NaOH NaOHaa aa
muoáiaa NaOH mm n 22 Ví dụ: Để phản ứng hoàn toàn với dung dịch chứa 7,5 gam glyxin (H2NCH2COOH) cần vừa đủ V ml dung dịch NaOH1M.Giá trị Vlà A. 50. B. 200. C. 100. D. 150. Hướng dẫn giải glyxin n0,1mol Glyxincó một nhómCOOH: NaOHglyxin nn0,1mol NaOH V0,1lít100ml Chọn C. Ví dụ mẫu Ví dụ 1: Cho5,34gamalanintác dụng vừa đủ với dung dịch KOHthìthu được mgam muối kali.Giá trị của mlà A. 7,62. B. 7,53. C. 6,66. D. 7,74. Hướng dẫn giải
ikali 5,340,0656m0,0618
Tacó: muoáiX NaOH mm19,415 n 0,2mol2222
DoXcó một nhómCOOHnên: aaNaOH nn0,2mol X M1575 0,2
Gọi công thức của XlàH2NRCOOOH. (CH2) R M75164514
Công thức của XlàH2NCH2COOH. Chọn D. Ví dụ 3: Cứ 0,01 mol amino axit A phản ứng vừa đủ với 40 ml dung dịch NaOH 0,25M. Mặt khác, 1,5gamaminoaxitA phản ứng vừa đủ với 80mldung dịch NaOH0,25M. Khối lượng phân tử của Alà A. 150. B. 75. C. 105. D. 89. Hướng dẫn giải
0,01molaminoaxitA phản ứng với NaOH: NaOH n0,01mol
Ta thấy: NaOHaa nn0,01mol
AminoaxitAcó một nhómCOOH. Cho1,5gamaminoaxitA phản ứng NaOH: NaOH n0,02mols AminoaxitAcó một nhómNaOH: aaNaOH nn0,02mol
A M1,575 0,02 Chọn B. Bài toán 3: Amino axit tác dụng với axit hoặc amino axit tác dụng với bazơ
Phương pháp giải
Kết hợp và vận dụng linh hoạt hai phương pháp giải của bàitoán1vàbàitoán2. Ví dụ mẫu
dụ 1: Cho0,01molaminoaxitXtác
DẠYKÈMQUYNHƠN
Trang14
OFFICIAL
Xtác
vừa đủ với
A.
B.
C.
Hướng dẫn giải Cho0,01molaminoaxitXtác dụng với HCl: HCl n0,02mol Số mol HCl 2 aa Nn0,02 H 2 n0,01 Cho0,02molaminoaxitXtác dụng với NaOH: NaOH NaOH m108%0,8gamn0,02mol
Ví
dụng vừa đủ với 200mldung dịch HCl0,1M. Mặt khác0,02mol
dụng
10gamdung dịch NaOH8%thu được 2,8gam muối khan.Phân tử khối của Xlà
118.
146.
147. D. 117.
công
Xlà(H
NaOH mm8,88m n mol 2222 DoX chỉ chứa một nhómNH2, một nhómCOOHnên: XHClNaOHnnn Tacó phương trình: 10,04m8,88m
DẠYKÈMQUYNHƠN OFFICIAL Trang15
m7,12gam36,522 Thay ta được: m7,12, X n0,08mol X M7,1289 0,08 Công thức của XlàH2NC2H4COOH. Chọn A. Chú ý: Ngoài cách giải bên các em có thể sử dụng phương pháp tăng giảm khối lượng. 1 mol X phản ứng với HCl và NaOH thì khối lượng muối clorua nhiều hơn khối lượng muối natri là: 36,52214,5gam X 10,048,88 n 14,5 0,08mol X M8,882289 0,08
Số nhóm NaOH aa Cn0,02 OOH 1 n0,02 Gọi
thức
2N)2RCOOH. Tacó: 2 HONaOH nn0,02mol Bảo toàn khối lượng: 2 aaNaOHmuoáiHOmmmm aa m0,02.402,80,02.18 aa m2,36gam aa M2,36118 0,02 Chọn A. Ví dụ 2: AminoaxitX chứa một nhómaminovà một nhómcacboxyl.ChomgamXtác dụng vừa đủ với NaOH,thu được 8,88gam muối. Mặt khác,chomgamXtác dụng vừa đủ với HCl,thu được 10,04gam muối. Công thức của Xlà A. H2NC2H4COOH. B. H2NC3H4COOH. C. H2NC3H6COOH. D. H2NCH2COOH. Hướng dẫn giải Tacó: muoáiX HCl mm10,04m n mol 36,536,5
muoáiX
Bài tập tự luyện dạng 2
Bài tập cơ bản
Câu 1: Để phản ứng hoàn toàn với dung dịch chứa 3,75 gam glyxin cần vừa đủ V ml dung dịch NaOH 1M.Giá trị của Vlà
A. 200. B. 150. C. 50. D. 100.
Câu 2: Cho2,67gamalanin phản ứng hết với dung dịch NaOH. Khối lượng muối thu được là
A. 4,44gam. B. 3,33gam. C. 11,00gam. D. 2,88gam.
Câu 3: Chomgam hỗn hợp X gồm glyxin,valinvàaxitglutamictác dụng vừa đủ với 400mldung dịch HCl1Mthu được 52gam hỗn hợp muối. Giá trị của mlà
A. 66,6. B. 37,8. C. 66,2. D. 37,4. Câu 4: Cho 96 gam hỗn hợp gồm valin và glyxin (tỉ lệ mol 1 : 1) tác dụng hoàn toàn với dung dịch NaOH dư, thu được dung dịch Y chứa mgam muối. Giá trị của mlà
A. 107. B. 201. C. 118. D. 181. Câu 5: Cho 0,1 mol -amino axit A có dạng H2NRCOOH phản ứng hết với HCl tạo thành 11,15 gam muối. Alà chất nàosau đây?
A. Glyxin. B. Alanin. C. Lysin. D. Valin. Câu 6: Cho m gam H2NCH2COOH phản ứng hết với dung dịch KOH, thu được dung dịch chứa 28,25 gam muối. Giá trị của mlà
A. 37,50. B. 28,25. C. 21,75. D. 18,75. Câu 7: Cho0,01mol -aminoaxitXtác dụng vừa đủ với 80mldung dịch HCl0,125M;sau đó đem cô cạn dung dịch thìthu được 1,815gam muối. Phân tử khối của Xlà A. 187. B. 145. C. 195. D. 147. Câu 8: Xlà một aminoaxitno chỉ chứa 1nhómNH2 và một nhómCOOH.Cho0,89gamXtác dụng với HCl vừa đủ tạo ra1,255gam muối. Công thức cấu tạo của Xlàcông thức nàosau đây? A. B. 3 2 CHCHNHCOOH 3 2 2 CHCHNHCHCOOH C. D. 2 2 HNCHCOOH 37 2 CHCHNHCOOH Câu 9: Cho hỗn hợp X chứa 17,80 gam alanin và 15 gam glyxin tác dụng với 500 ml dung dịch NaOH 1M.Khi phản ứng xảy rahoàntoàn,cô cạn dung dịch, thu được mgam chất rắn khan.Giá trị của mlà A. 22,2. B. 19,4. C. 45,6. D. 41,6. Câu 10:
nhómCOOHvàhainhómNH2.Cho0,1molXtác dụng hết với 270ml dung dịch NaOH0,5Mcô cạn thu được 15,4gam chất rắn. Công thức phân tử có thể có của Xlà
A. C4H10N2O2. B. C5H12N2O2. C. C5H10NO2. D. C3H9NO4. Câu 11: Cứ 0,01 mol amino axit A phản ứng vừa đủ với 80 ml dung dịch NaOH 0,25M. Mặt khác, 4,41gamaminoaxitA phản ứng vừa đủ với 240mldung dịch NaOH0,25M. Khối lượng phân tử của Alà A. 75. B. 147. C. 117. D. 89. Câu 12: Cho0,02molaminoaxitXtác dụng vừa đủ với 200mldung dịch HCl0,1Mthu được 3,67gam muối khan. Mặt khác,0,02molXtác dụng vừa đủ với 40gamdung dịch NaOH4%.Công thức của Xlà A. H2NC2H3(COOH)2 B. H2NC3H5(COOH)2 C. (H2N)2C3H5COOH. D. H2NC3H6COOH.
DẠYKÈMQUYNHƠN
Trang16 Chọn A.
OFFICIAL
AminoaxitX chứa một
Câu 13: Cho 17,64 gam X có công thức tác dụng với 200 ml dung 2 2 2 HOOCCHCHNHCOOH dịch gồm NaOH1MvàKOH1M.Cô cạn dung dịch sau phản ứng thu được mgam chất rắn. Giá trị của mlà
A. 24,74gam. B. 35,72gam. C. 29,32gam. D. 32,52gam. Câu 14: Amino axit X trong phân tử chỉ chứa hai loại nhóm chức. Cho 0,1 mol X tác dụng vừa đủ với 0,2molNaOH,thu được 17,7gam muối. Số nguyên tử hiđro trongphân tử Xlà
A. 9. B. 6. C. 7. D. 8.
Câu 15: Hỗn hợp X gồm glyxin, alanin, axit glutamic (trong đó nguyên tố oxi chiếm 41,2% về khối lượng). ChomgamXtác dụng với dung dịch NaOH dư, thu được 20,532gam muối. Giá trị của mlà
A. 16,0. B. 13,8. C. 13,1. D. 12,0.
Câu 16: Cho 0,1 mol amino axit X tác dụng vừa đủ với 200 ml dung dịch KOH 1M, sau phản ứng thu được dung dịch chứa 20,9gam muối. Số nguyên tử hiđro cótrongXlà
A. 9. B. 11. C. 7. D. 8. Bài tập nâng cao
OFFICIAL
Câu 17: AminoaxitX chứa một nhómaminovà một nhómcacboxyl.ChomgamXtác dụng vừa đủ với NaOH, thu được 7,76 gam muối. Mặt khác, cho m gam X tác dụng vừa đủ với HCl, thu được 8,92 gam muối. Công thức của Xlà
A. B. 224 HNCHCOOH 234 HNCHCOOH C. D. 236 HNCHCOOH 2 2 HNCHCOOH
Câu 18: Cho 0,01 mol -amino axit X tác dụng vừa đủ với 200 ml dung dịch KOH 0,1M hay 100 ml dung dịch HCl0,1M. Nếu cho0,03molXtác dụng với 40gamdung dịch NaOH7,05%cô cạn dung dịch sau phản ứng, thu được 6,15gam chất rắn. Công thức của Xlà
A. (H2N)2C3H5COOH. B. H2NC4H7(COOH)2. C. H2NC2H3(COOH)2. D. H2NC3H5(COOH)2. Câu 19: Cho100mldung dịch aminoaxitX0,2Mtác dụng vừa đủ với 80mldung dịch HCl0,5M, đun nóng.Sau phản ứng, cô cạn cẩn thận dung dịch được 4,34gam muối khan.Công thức phân tử của Xlà A. C6H14O2N2 B. C6H13O2N2 C. C5H9O4N. D. C6H12O2N2 Câu 20: Hỗn hợp X gồm alaninvàaxitglutamic.ChomgamXtác dụng hoàntoàn với dung dịch NaOH (dư), thu được dung dịch Y chứa gam muối. Mặt khác, nếu chomgamXtác dụng hoàntoàn m30,8 với dung dịch HCl,thu được dung dịch
DẠYKÈMQUYNHƠN
Trang17
Z chứa gam
Giá
A. 112,2. B. 165,6. C. 123,8. D. 171,0. Dạng 3: Phản ứng nối tiếp Bài toán 1: Amino axit tác dụng với axit tạo dung dịch X. Cho X tác dụng tiếp với dung dịch bazơ Phương pháp giải Xétaminoaxitcócông thức tổng quátlà 2b a HNRCOOH HCl NaOH 1 2 aaXY Coi(1)không xảy ra,dung dịch X gồm aminoaxitvàHCltác dụng với NaOH.
muối.
trị của mlà
m36,5
lượng:
Ngoài viết phương trìnhphân tử thìcó thể viết phương trìnhion 2 HOHHO
Ví dụ: Cho0,2molglyxinvào175mldung dịch HCl2M,thu được dung dịch X.Chodung dịch NaOH dư vàoX.Saukhicác phản ứng xảy rahoàntoàn, số molNaOHthamgia phản ứng là A. 0,50mol. B. 0,65mol. C. 0,35mol. D. 0,55mol. Hướng dẫn giải glyxin HCl n0,2mol;n0,35mol Coidung dịch X chứa glyxin(0,2mol)vàHCl(0,35mol)tác dụng với NaOH. Phương trìnhhóa học: 2GlyNaOHMuoáiHO mol 0,20,2 2 HClNaOHNaClHO mol 0,350,35 NaOHpö n0,20,350,55mol Chọn D. Ví dụ mẫu Ví dụ 1: Cho 13,23 gam axit glutamic phản ứng với 200 ml dung dịch HCl 1M, thu được dung dịch X. Cho 400 ml dung dịch NaOH 1M vào X, thu được dung dịch Y. Cô cạn dung dịch Y, thu được m gam chất rắn khan. Biết các phản ứng xảy rahoàntoàn.Giá trị của mlà A. 29,69. B. 17,19. C. 31,31. D. 28,89. Hướng dẫn giải Cách 1: axitglutamic HCl NaOH n0,09mol;n0,2mol;n0,4mol
DẠYKÈMQUYNHƠN OFFICIAL Trang18
2AaaNaOHMuoáiaHO 2 HClNaOHNaClHO Tacó: 2 NaOHpöaaHCl HONaOH nann nn Bảo toàn khối
2 aaNaOHHCl HO muoáichaátraé n mmmm m Chú ý:
Coidung dịch X gồm axitglutamic(0,09mol)vàHCl(0,2mol)tác dụng với NaOH. Phương trìnhhóa học: 2Glu2NaOHMuoái2HO mol 0,090,18 0,18
2 HClNaOHNaClHO mol 0,20,2 0,2 NaOH dư và mol 2 HONaOHpö nn0,180,20,38 Bảo toàn khối lượng: 2 GluNaOHHClchaátraénHOmmmmm chaátraé n 13,230,4400,236,5m0,3818 chaátraénkhan m29,69gam Cách 2: HaxitglutamicHCl n2nn0,38mol Phương trìnhion: 2 HOHHO mol 0,380,380,38 Bảo toàn khối lượng: chaátraé n 13,230,4400,236,5m0,3818 chaátraé n m29,69gam Chọn A. Chú ý: Xét chất dư, chất hết để xem số mol H2O tính theo chất nào. Ví dụ 2: Cho0,01molaminoaxitY phản ứng vừa đủ với dung dịch chứa 0,01molHClthu được dung dịch chứa chất Z. Chất Z phản ứng vừa đủ với dung dịch chứa 0,02molNaOH.Công thức Ycó dạng A. (H2N)2R(COOH)2. B. H2NRCOOH. C. (H2N)2RCOOH. D. H2NR(COOH)2 Hướng dẫn giải
DẠYKÈMQUYNHƠN OFFICIAL Trang19
HCl 2 Y Nn0,01 H 1 n0,01
Z chứa aminoaxitY(0,01mol)vàHCl(0,01mol).
trìnhhóa học: 2YNaOHMuoáiHO mol 0,010,01 2 HClNaOHNaClHO mol 0,010,01 Vậy Ycó một nhómCOOH. Công thức Ycó dạng: H2NRCOOH. Chọn B. Ví dụ 3: Cho0,3mol hỗn hợp X gồm H2NC3H5(COOH)2 (axitglutamic)và(H2N)2C5H9COOH(lysin)và 400 ml dung dịch HCl 1M, thu được dung dịch Y. Biết Y phản ứng với vừa hết với 800 ml dung dịch NaOH1M. Số mollysintrong hỗn hợp Xlà
Số nhóm
Coidung dịch
Phương
A. 0,20mol. B. 0,25mol. C. 0,10mol. D. 0,15mol. Hướng dẫn giải HCl NaOH n0,4mol;n0,8mol
Gọi số mol của axitglutamicvàlysintrong hỗn hợp X lần lượt làx,ymol. (*) xy0,3 Coidung dịch Y chứa axitglutamic(xmol),lysin(ymol)vàHCl(0,4mol)tác dụng với NaOH. Phương trìnhhóa học: 2Glu2NaOHMuoái2HO mol x2x 2LysNaOHMuoáiHO mol yy 2 HClNaOHNaClHO mol 0,40,4 Tacó: NaOH n2xy0,40,8mol 2xy0,4** Từ (*)và(**)tacó hệ phương trình: xy0,3x0,1 2xy0,4y0,2
DẠYKÈMQUYNHƠN OFFICIAL Trang20
Bài
2: Amino
Phương pháp giải Xétaminoaxitcócông thức tổng quátlà 2b a HNRCOOH NaOH HCl 1 2 aaXY Coi(1)không xảy ra,dung dịch X gồm aminoaxitvàNaOHtác dụng với HCl. Muối AabHCl 2 NaOHHClNaClHO Tacó: 2 HClpöaaNaOH HONaOH nbnn nn Bảo toàn khối lượng: 2 aaNaOHHCl HO muoáichaátraé n mmmm m Ví dụ: Cho0,15molalaninvào300mldung dịch NaOH1M,thu được dung dịch X.ChoXtác dụng vừa đủ với dung dịch HCl,thu được dung dịch Y.Cô cạn Y,thu được mgam chất rắn khan.Giá trị của mlà
Vậy số mollysintrong hỗn hợp là0,2mol. Chọn A.
toán
axit tác dụng với dung dịch bazơ tạo dung dịch X. Cho X tác dụng tiếp với axit
A. 30,900. B. 17,550. C. 18,825. D. 36,375. Hướng dẫn giải alanin NaOH n0,15mol;n0,3mol Coidung dịch Y gồm Ala(0,15mol)vàNaOH(0,3mol). Phương trìnhhóa học: AlaHClMuoá i mol 0,150,15 2 NaOHHClNaClHO mol 0,30,3 0,3 HCl n0,150,30,45mol Bảo toàn khối lượng: 2 alaninNaOHHClchaátraénkhanHOmmmmm
nkhan m36,375
gam
Chọn D. Ví dụ mẫu Ví dụ 1: Cho13,35gam hỗn hợp X gồm NH2CH2CH2COOHvàCH3CH(NH2)COOHtác dụng với Vml dung dịch NaOH1Mthu được dung dịch Y. Biết dung dịch Ytác dụng vừa đủ với 250mldung dịch HCl 1M.Giá trị của Vlà A. 100. B. 150. C. 200. D. 250. Hướng dẫn giải X HCl n0,15mol;n0,25mol
DẠYKÈMQUYNHƠN OFFICIAL Trang21
i mol 0,150,15 2 NaOHHClNaClHO mol xx Tacó: 0,15x0,25x0,1 lít=100ml V0,1 Chọn A. Bài tập tự luyện dạng 3 Câu 1: Cho0,15molaxitglutamicvào175mldung dịch HCl2M,thu được dung dịch
NaOH dư vàoX.Saukhicác phản ứng
ứng
chaátraé
Coidung dịch Y gồm aminoX(0,15mol)vàNaOH(xmol). Phương trìnhhóa học: YHClMuoá
X.Chodung dịch
xảy rahoàntoàn, số molNaOHthamgia phản
là
A. 0,50mol. B. 0,65mol. C. 0,35mol. D. 0,55mol. Câu 2: Cho15,00gamglyxinvào300mldung dịch HCl,thu được dung dịch X.ChoXtác dụng vừa đủ với 250 ml dung dịch KOH 2M, thu được dung dịch Y. Cô cạn dung dịch Y thu được m gam chất rắn khan.Giá trị của mlà
A. 53,95. B. 22,35. C. 44,95. D. 22,60. Câu 3: Cho2,67gam một aminoaxitX (chứa một nhómCOOH)vào100mlHCl0,2M,thu được dung dịch Y. Biết Y phản ứng vừa đủ với 200mlKOH0,25M. Số đồng phân cấu tạo của Xlà
A. 1. B. 3. C. 2. D. 4. Câu 4: Cho một lượng -aminoaxitvào cốc đựng 100mldung dịch HCl2M.Dung dịch sau phản ứng tác dụng vừa đủ với 0,45molNaOH.Cô cạn dung dịch sau phản ứng thu được 46,45gam muối khan.Tên gọi của Xlà
A. valin. B. axitglutamic. C. glyxin. D. alanin. Câu 5: Cho0,2molaminoaxitX (mạch hở) vào200mldung dịch HCl1M,thu được dung dịch Y.Cho Y phản ứng vừa đủ với 400 ml dung dịch NaOH 1M, sau khi phản ứng xảy ra hoàn toàn thu được 33,9gam muối. Khối lượng của chất Xlà
OFFICIAL
A. 23,4gam. B. 15,0gam. C. 17,8gam. D. 20,6gam. Câu 6: Cho 15,94 gam hỗn hợp gồm alanin và axit glutamic tác dụng vừa đủ với 200 ml dung dịch NaOH 1M thu được dung dịch X. Cho 450 ml dung dịch HCl 0,8M vào dung dịch X, cô cạn dung dịch sau phản ứng thu được mgam rắn khan.Giá trị của mlà A. 32,75. B. 23,48. C. 27,64. D. 33,91. Câu 7: Xlà -aminoaxittrongphân tử chứa 1nhómNH2 và1nhómCOOH. Lấy 0,01molXtác dụng vừa đủ với dung dịch HCl0,1Mthu được dung dịch Y.Cho400mldung dịch KOH0,1MvàoY,cô cạn dung dịch sau phản ứng, thu được 2,995gam rắn khan.Công thức cấu tạo của Xlà
A. B. 2 22 HNCHCHCOOH 3 2 2 CHCHCHNHCOOH C. D. 2 2 HNCHCOOH. 3 22 CHCHNHCOOH. Bài tập nâng cao Câu 8: Cho 21 gam hỗn hợp gồm glyxin và axit axetic tác dụng vừa đủ với dung dịch KOH, thu được dung dịch X chứa 32,4gam muối. ChoXtác dụng với dung dịch HCl dư chứa mgam muối. Giá trị của m là
A. 44,65. B. 50,65. C. 22,30. D. 22,35. Câu 9: Amino axit X có công thức (H2N)2C3H5COOH. Cho 0,02 mol X tác dụng với 200 ml dung dịch hỗn hợp H2SO4 0,1MvàHCl0,3M,thu được dung dịch Y.ChoY phản ứng vừa đủ với 400mldung dịch NaOH0,1MvàKOH0,2Mthu được dung dịch chứa mgam muối. Giá trị của mlà
A. 10,43. B. 6,38. C. 10,45. D. 8,09. Câu 10: Hỗn hợp X gồm glyxin,valin,lysinvàaxitglutamic(trongX tỉ lệ khối lượng của nitơ vàoxilà 7 : 15). Cho 7,42 gam X tác dụng vừa đủ với dung dịch HCl, thu được dung dịch Y. Dung dịch Y tác dụng vừa đủ dung dịch chứa 0,08 mol NaOH và 0,075 mol KOH, cô cạn dung dịch sau phản ứng, thu được mgam muối khan.Giá trị của mlà
A. 14,76. B. 14,95. C. 15,46. D. 15,25.
Dạng 4: Phản ứng cháy của amino axit
DẠYKÈMQUYNHƠN
Trang22
Bài toán 1: Xác định lượng chất trong phản ứng Phương pháp giải
Đốt cháyaminoaxitno, mạch hở, phân tử chỉ chứa một nhómNH2 và một nhómCOOH:
Chú ý: Aminoaxitcó số nhómNH2 lớn hơn hoặc bằng số nhómCOOH. 2 2HOCOnn Ví dụ: Đốt cháyhoàntoànmgamaminoaxitno, mạch hở Xsinhra2molCO2 và2,5molH2Ovàamol khíN2.Giá trị của alà (biết X chỉ chứa một nhómNH2 và một nhómCOOH) A. 0,25. B. 0,50. C. 0,75. D. 1,00. Hướng dẫn giải Đốt cháyaminoaxitno, mạch hở có một nhómNH2 và một nhómCOOH: 2 2 HOCOaaaa 2,52 nn0,5nn1mol 0,5 Bảo toànnguyên tố N: 2 Naa 11 nn.10,5mol 22 Chọn B. Ví dụ mẫu Ví dụ 1: Đốt cháyhoàntoànmgamaminoaxitno, mạch hở Bsinhra3molCO2 và3,5molH2Ovà một lượng khíN2.Giá trị của mlà (biết B chỉ chứa một nhómNH2 và một nhómCOOH) A. 75. B. 89. C. 117. D. 146. Hướng
DẠYKÈMQUYNHƠN OFFICIAL Trang23
t
aa
dẫn giải Aminoaxitno, mạch hở có1nhómNH2 và1nhómCOOH: 2 2 HOCOaaaa 3,53 nn0,5nn1mol 0,5 B chỉ chứa 1nhómNH2 và1nhómCOOHnên: NB OB n1mol;n212mol Bảo toànnguyên tố C,H: 2 2 CO HO CB HB nn3mol;n2n23,57mol Bảo toàn khối lượng: BCHON mmmmm
n2n12 2 2 2 2 6n3 2n11 CHONOnCOHON 4 22
Nhận xét: 2 2 2 N aa HOCO
1 nn 2 nn0,5n
Đốt cháy một aminoaxit bất kì: t xyzt 2 22 2 4xy2z yt CHON OxCOHON 4 22
89gam Chọn B.
Bài toán 2: Xác định công thức của amino axit
Phương pháp giải Đốt cháyaminoaxitno, mạch hở, phân tử chỉ chứa một nhómNH2 và một nhómCOOH: t n2n12 2 2 22 6n3 2n11 CHONOnCOHON 4 22
Ngoàita,tacó thể áp dụng các định luật bảo toàn:
Bảo toànnguyên tố C,H,N: Số nguyên tử nguyên tố 2CO aa
n C n
2n H n Số nguyên tử nguyên tố 2N aa
Số nguyên tử nguyên tố 2 HO aa
2n N n
toàn khối lượng:
2)
1 nn;n2n 2 Ví dụ: Đốt cháyhoàntoànxmolaminoaxitAcó1nhómCOOHthu được 2xmolCO2 và0,5xmolN2. Công thức Cn2x2 nx Số nguyên tử nguyên tử. 2N aa
cấu tạo của N2n20,5x1 nx Vậy Acó thể là:H2NCH2COOH. Chọn A. Ví dụ mẫu Ví dụ 1: Đót cháyhoàntoànaminoaxitXlà đồng đẳng của axitaminoaxeticthu được CO2 vàH2Otheo tỉ lệ mol6:7.Công thức cấu tạo có thể có của Xlà
COOH. D. H2NCH(COOH)2.
DẠYKÈMQUYNHƠN OFFICIAL Trang24 31271216114
Bảo
aaCHO mmmm 2 22 2aaOCOHON mmmmm
Alà A. H2NCH2COOH. B. H2N(CH2)2COOH. C. H2N(CH
3
Chú ý: Nếu aminoaxit chỉ chứa một nhómNH2, một nhómCOOH: 2 NaaOaa aa Hướng dẫn giải Bảo toànnguyên tố C,N: Số nguyên tử nguyên tử 2CO aa
)COOH.
Chọn A. Ví dụ 2: Một -amino axit no, mạch hở X có công thức tổng quát NH2RCOOH. Đốt cháy hoàn toàn a molXthu được 6,72lítCO2 (đktc) và6,75gamH2O.Công thức cấu tạo của Xlà A. CH2NH2COOH. B. CH2NH2CH2COOH. C. CH3CH(NH2)COOH. D. Cả BvàC. Hướng dẫn giải
Xlà -aminoaxitno, mạch hở
t n2n12 2 2 2 N 6n3 2n11 CHONOnCOHOn 4 22 Cn0,32 n0,15 Số nguyên tử 2 HO aa
mol 67 Tacó phương trình: 67n3 n2n1 2 MàXlà -aminoaxitnêncông thức cấu tạo của Xlà:CH3CH(NH2 H2n20,3755 n0,15 Vậy công thức của XlàC2H5O2NhayCH2NH2COOH. Chọn A. Bài tập tự luyện dạng 4 Bài tập cơ bản Câu 1: Đốt cháyhoàntoànamolaminoaxitAthu được 2amolCO2 và0,5amolN2.Công thức cấu tạo của Alà A. H2NCH2COOH. B. H2N(CH2)2COOH. C. H2N(CH2)3COOH. D. H2NCH(COOH)2.
DẠYKÈMQUYNHƠN OFFICIAL Trang25
2 2
A. CH3CH(NH2)COOH. B. CH3CH2CH(NH2)COOH. C. H2NCH2CH2COOH. D. CH3CH(NH2)CH2COOH. Hướng dẫn giải Amino axit X là đồng đẳng của axit aminoaxetic nên nó là -amino axit có công thức là: n2n12 CHON n2 Phương trìnhhóa học: 2 có một nhómNH2 và một nhómCOOHnên: mol 2 2HOCO aaaa 0,3750,3nn0,5nn00,15 ,5 Bảo toànnguyên tố C,H: Số nguyên tử 2CO aa
CO HO n0,3mol;n0,375mol
Câu 2: Đốt cháyhoàntoàn75gamaminoaxitno, mạch hở Xsinhra2molCO2,2,5molH2Ovàamol khíN2 Biết X chỉ chứa một nhómNH2 và một nhómCOOH.Giá trị của alà
A. 0,25. B. 0,50. C. 0,75. D. 1,00. Câu 3: Đốt cháyhoàntoàn một -aminoaxitthu được CO2 vàH2Otheo tỉ lệ 8:9.Công thức cấu tạo có thể có của Xlà
A. CH3CH(NH2)COOH. B. CH3CH2CH(NH2)COOH. C. H2N(CH2)3COOH. D. CH3(CH2)3CH(NH2)COOH. Câu 4: Đốt cháyhoàntoàn12,36gamaminoaxitXcócông thức dạng ,thu được a 2xy t HNCHCOOH mol CO2 và b mol H2O . Mặt khác, cho 0,2 mol X vào 1 lít dung dịch hỗn hợp KOH 0,4M và ba NaOH 0,3M, thu được dung dịch Y. Thêm dung dịch HCl vào Y, thu được dung dịch chứa 75,25 gam muối. Giá trị của blà
A. 0,54. B. 0,42. C. 0,48. D. 0,30. Câu 5: Đốt cháy amino axit X no, mạch hở, chứa một nhóm amino và một nhóm cacboxyl bằng một lượng không khí vừa đủ (80% N2 và 20% O2 về thể tích), thu được hỗn hợp khí và hơi có tỉ khối so với H2 là14,317.Công thức của Xlà
OFFICIAL
A. C3H7O2N. B. C4H9O2N. C. C2H5O2N. D. C5H11O2N. Câu 6: Đốt cháyhoàntoàn0,5mol hỗn hợp X gồm một aminoaxitY(có một nhómamino)và một axit cacboxylic no Z (đơn chức, mạch hở), thu được 26,88 lít CO2 (đktc) và 23,4 gam H2O. Mặt khác, 0,45 molX phản ứng vừa đủ với lượng dung dịch chứa mgamHCl.Giá trị của mlà A. 10,95. B. 6,39. C. 6,57. D. 4,38. Câu 7: Hỗn hợp A gồm amino axit X có dạng NH2CnH2nCOOH và 0,02 mol Y có công thức (NH2)2C5H9COOH. Cho A vào dung dịch chứa 0,11 mol HCl, thu được dung dịch B. Dung dịch B phản ứng vừa đủ với dung dịch gồm 0,12molNaOHvà0,04molKOH,thu được dung dịch chứa 14,605gam muối. Đốt cháyhoàntoànAthu được amolCO2.Giá trị của alà A. 0,21. B. 0,24. C. 0,27. D. 0,18. Bài tập nâng cao
Câu 8: Cho m gam hỗn hợp X gồm glyxin, alanin và valin phản ứng với 100 ml dung dịch HCl 1M thu được dung dịch Y. Để phản ứng hết với các chất trong dung dịch Y cần 380 ml dung dịch KOH 0,5M. Mặt khác, đốt cháy hoàn toàn m gam hỗn hợp X rồi cho sản phầm cháy vào bình đựng dung dịch Ba(OH)2 dư, sau phản ứng khối lượng dung dịch trongbình giảm 43,74gam.Giá trị của mlà A. 7,57. B. 8,85. C. 7,75. D. 5,48. Câu 9: Amino axit X có công thức dạng NH2CxHy(COOH)n Đốt cháy m gam X bằng oxi dư thu được N2, 1,12 lít CO2 (đktc) và 0,99 gam nước. Cho 29,25 gam X vào V lít dung dịch H2SO4 0,1M thu được dung dịch Y.Y phản ứng vừa đủ với 100mldung dịch hỗn hợp NaOH2MvàKOH2,5Mthu được dung dịch chứa agam muối. Biết phản ứng xảy rahoàntoàn.Giá trị của alà A. 52,95. B. 42,45. C. 62,55. D. 70,11. Câu 10: Hỗn hợp X gồm haiaminoaxitno (chỉ chứa nhómCOOHvàNH2 trongphân tử) trong đó tỉ lệ Để tác dụng vừa đủ với 3,83gam hỗn hợp X cần 30mldung dịch HCl1M. Mặt khác, ON m:m80:21 đốt cháy hoàn toàn 3,83 gam hỗn hợp X cần 3,192 lít khí oxi (đktc). Dẫn toàn bộ sản phẩm cháy gồm CO2,H2O,N2 vàodung dịch nước vôitrong dư thì khối lượng kết tủa thu được là
A. 15gam. B. 13gam. C. 10gam. D. 20gam.
DẠYKÈMQUYNHƠN
Trang26
Đáp án và lời giải
Dạng 1: Lí thuyết trọng tâm 1 – A 2 – B 3 – B 4 – B 5 – A 6 – D 7 – B 8 – D 9 – C 10 – C 11 – B 12 – C 13 – D 14 – D 15 – C 16 – A 17 – B 18 – D 19 – B 20 – B 21 – C 22 – D 23 – A 24 – B 25 – A
Câu 5: Axit-2,6-điaminohexanoic có số nhóm > số nhóm 2 NH2 COOH1 Làm đổi màu quỳ tím chuyển sangmàuxanh.
Câu 6: Có3 chất làm đổi màu quỳ tím ẩm: C2H5COOHlàm đổi màu quỳ tím chuyển sangmàu đỏ. CH3NH2 vàCH3(CH2)3NH2 làm đổi màu quỳ tím chuyển sangmàuxanh. Câu 7: Có2 chất làm đổi màu quỳ tím ẩm là:HOOCCH2CH2CH(NH2)COOHvà H2N(CH2)4CH(NH2)COOH.
Câu 8: Dãy xếp theo thứ tự pH tăng dần là:CH3COOH(2),H2NCH2COOH(1),CH3CH2NH2 (3). Câu 13: Có3 chất phản ứng được với dung dịch HCllà:H2NCH2COOH,C2H5NH2,CH3NH2 Câu 14: Hai chất đều tác dụng được với dung dịch NaOH loãng là: ClH3NCH2COOC2H5 và H2NCH2COOC2H5 Phương trìnhhóa học: 32 25 22 25 2 ClHNCHCOOCH2NaOHHNCHCOONaNaClCHOHHO 22 25 22 25 HNCHCOOCHNaOHHNCHCOONaCHOH
Câu 15: C sai vì không phải amino axit nào trong phân tử cũng chỉ gồm một nhóm NH2 và một nhóm COOH. Câu 16: Asaivìví dụ lysinlà -aminoaxit nhưng trongphân tử cóhainhómNH2
Câu 17: Bsaido muối mononatriglutamat mới làgia vị cho thức ăn (gọi là bột ngọt haymìchính).
Câu 18:
A đúng vìlysincó số nhóm số nhómCOOHnênlàm quỳ tím chuyển màuxanh. 2NH
B đúng vì amino axit là hợp chất hữu cơ tạp chức, phân tử chứa đồng thời nhóm amino (NH2) và nhóm cacboxyl(COOH).
C đúng vìglyxincó số nhómNH2 = số nhómCOOHnênkhônglàm đổi màuphenolphtalein.
Dsaivìanilintác dụng với brom tạo thành kết tủa trắng.
Câu 19: Asaivìthành phần chính của bột ngọt là muối mononatriglutamat.
B đúng.
DẠYKÈMQUYNHƠN
Trang27
OFFICIAL
Csaivìcácaminoaxitthiênnhiên hầu hết làcác -aminoaxit.
Dsaivì ở nhiệt độ thường, cácaminoaxit đều là những chất rắn.
Câu 20: Các chất thỏa mãnlà:CH3COONH4 vàHCOONH3CH3
Câu 21: Mạch cacbon: CCCOOH Các đồng phânaminoaxit tương ứng với công thức phân tử C3H7O2Nlà:
3 2 22 2 CHCHNHCOOH;CHNHCHCOOH Câu 22: Xcócông thức phân tử làC3H7O2N, phản ứng với dung dịch NaOH, giải phóngkhí. Ycócông thức phân tử làC3H7O2Ncó phản ứng trùng ngưng (aminoaxit). Chỉ có đáp ánD thỏa mãn:XlàamoniacrylatvàYlàaxit2-aminopropionic. Câu 23: Phương trìnhhóa học:
DẠYKÈMQUYNHƠN
Trang28
OFFICIAL
HNCHCOOHHClClHNCHCOOH X 32 22 2 ClHNCHCOOH2NaOHHNCHCOONaNaCl2HO Y
3 2 3 3 2 4 CHCHNHCOOCHNaOHCHCHNHCOONaCHO 3 2 3 3 CHCHNHCOONaHCl(dö)CHCHNHClCOOHNaCl Câu 25: Sơ đồ chuyển hóa: 3 25 CHOH/HCl,t CHOH/HCl,t NaOHdö,t Axitglutamic Y Z T Phương trìnhhóa học: 3 CHOH/HCl,t 352 3 353 2 HOOCCHNHCOOH CHOOCCHNHClCOOHHO Y 25 CHOH/HCl,t 3 353 3 353 252 CHOOCCHNHClCOOH CHOOCCHNHClCOOCHHO Z NaOHdö,t 3 353 25 352 3 25 2 CHOOCCHNHClCOOCH NaOOCCHNHCOONaCHOHCHOHNaClHO
22 32
Công thức phân tử của YlàC2H4O2NNa. Câu 24:
Dạng 2: Tính lưỡng tính của amino axit 1 – C 2 – B 3 – D 4 – C 5 – A 6 – D 7 – B 8 – A 9 – C 10 – A 11 – B 12 – B 13 – D 14 – C 15 – A 16 – C 17 – D 18 – D 19 – D 20 – A
Câu 1: glyxin n0,05mol
Glyxincó một nhómCOOH: NaOHglyxin nn0,05mol V0,05lít50ml
Câu 2: alanin n0,03mol Alanincó một nhómCOOH: 2 HONaOHalanin nnn0,03mol
Bảo toàn khối lượng: 2 muoáialaninNaOHHO mmmm2,670,03223,33gam
Câu 3: HCl n0,4mol
Bảo toàn khối lượng: muoáiHCl mmm520,136,537,4gam Câu 4: valinglyxin nn0,5mol
Valinvàglyxin đều có một nhómCOOH: 2 NaOHHOvalinglyxin nnnn0,50,51mol
Bảo toàn khối lượng: 2 hoãnhôïpNaOHmuoáiHOmmmm muoá i mm96140118118gam
DẠYKÈMQUYNHƠN OFFICIAL Trang29 T
mmm11,150,136,57,5mol A M75 Alàglyxin. Câu 6: Phương trìnhhóa học: 22 22 2 HNCHCOOHKOHHNCHCOOKHO Theo đề bài: muoá i 28,25 n10,25mol 13 Theo phương trình: 22 HNCHCOOHmuoá i n n0,25mol m0,257518,75gam Câu 7: HCl HCl n0,01molm0,365gam Bảo toàn khối lượng: XmuoáiHCl mmm1,8150,3651,45gam
Câu 5: Alà một nhómNH2: HClA nn0,1mol
Bảo toàn khối lượng: AmuoáiHCl
X M1,45145 0,01 Câu 8: Bảo toàn khối lượng: HClmuoáiX mmm0,365gam HCl n0,01mol Xcó một nhómNH2: XHCl nn0,01mol X M0,8989 0,01 Công thức của Xlà 3 2 CHCHNHCOOH. Câu 9: alanin glyxin NaOH n0,2mol;n0,2mol;n0,5mol Doalaninvàglyxin đều có một nhómCOOH: 2 HONaOHpöalaninglyxin nnnn0,4mol Bảo toàn khối lượng: 2 glyxinalaninNaOHchaátraénkhanHOmmmmm chaátraénkhan m17,8150,5.400,4.1845,6gam Câu 10: NaOH n0,135mol AminoaxitXcó một nhómCOOH: 2 HONaOHpöX nnn0,1mol Bảo toàn khối lượng: 2 XNaOHchaá
DẠYKÈMQUYNHƠN OFFICIAL Trang30
X
X M11,8118 0,1 Công thức phân tử có thể có của XlàC4H10N2O2. Câu
phản ứng với NaOH: NaOH n0,02mol AminoaxitAcó2nhómCOOH. Cho4,41gamaminoaxitA phản ứng NaOH: NaOH n0,06mol AminoaxitAcó2nhómCOOH: aminoaxit NaOH n0,5n0,03mol A M4,41147 0,03 Câu 12: HCl NaOH NaOH n0,02mol;m40.4%1,6gamn0,04mol Số nhóm HCl 2 X Nn0,02 H 1 n0,02
traénkhanHOmmmm
m15,40,1180,1354011,8gam
11: 0,01molaminoaxitA
DẠYKÈMQUYNHƠN OFFICIAL Trang31
X
R
chaátraé n m17,640,2400,2560,241832,52gam Câu 14: Tacó: TrongXcó2nhómCOOH. NaOH X n 2 n Lại có: Công thức của Xlà: X M17,70,222133 0,1 223 2 HNCHCOOH TrongXcó7nguyên tử H. Câu 15: O O 0,412mm0,412.mgamn10,02575mmol 6 Tacó: 2 NaOHHOCOOH 0,02575m nnn 2 Bảo toàn khối lượng: 2 XNaOHmuoáiHOmmmm 0,02575mm22.220,532 m16 Câu 16: KOH n0,2mol Số nhóm COOH2 Công thức của Xcó dạng (H2N)xR(COOH)2 Tacó: 2 HOKOH nn0,2mol Bảo toàn khối lượng: 2 XmuoáiHOKOH mmmm20,90,2.180,2.5613,3gam
Số nhóm
NaOH X Cn0,04 OOH 2 n0,02 Công thức Xcó dạng H2NR(COOH)2. Bảo toàn khối lượng cho phản ứng của X với HCl: XmuoáiX mmm3,670,0236,52,94gam
M2,94147 0,02
35M1471645.241CH
Công thức của XlàH2NC3H5(COOH)2 Câu 13: X NaOH KOH n0,12mol;n0,2mol;n0,2mol
Tacó: 2 HOX n2n0,24mol
Bảo toàn khối lượng: 2 XNaOHKOHchaátraénHOmmmmm
X M133 Công thức của Xlà:H2NC2H3(COOH)2 Số nguyên tử hiđro của Xlà7. Câu 17: Theo đề bài: muoáiX X mm8,92m n mol 36,526,5
muoáiX X mm7,76m n mol 2222
Tacó phương trình: 8,92m7,76mm6gam36,522 Thay ,ta được: m6 X n0,08mol X M675 0,08
Công thức của Xlà . 2 2 HNCHCOOH Câu 18: KOH HCl n0,02mol;n0,01mol
DẠYKÈMQUYNHƠN OFFICIAL Trang32
n NH1 n
NaOH
2
Bảo toàn khối lượng: 2 XNaOHchaátraénHOmmmm X m6,150,06.182,824,41gam X M147 R 35M41CH Công thức của XlàH2NC3H5(COOH)2. Câu 19: X HCl n0,02mol;n0,04mol Số nhómNH2 trong X2 Công thức Xcó dạng 22 a HNRCOOH. Bảo toàn khối lượng: XmuoáiHCl mmm4,340,0436,52,88gam X M144 R45a112
Số nhóm Số nhóm KOH X n COOH2; n HCl 2 X
Công thức Xcó dạng H2NR(COOH)2.
Nếu cho0,03molXtác dụng với NaOH:
NaOH m407,05%2,82gamn0,0705mol
XcóhainhómCOOH:
HONaOHpöX nn2n0,06mol
Công thức của Xlà(H2N)2C5H7COOH. Công thức phân tử của XlàC6H12O2N2 Câu 20: Gọi số molalaninvàaxitglutamictrongX lần lượt làx,ymol. ChomgamXtác dụng hoàntoàn với dung dịch NaOH dư: Tacó: muoáiX NaOH mmm30,8m n 1,4mol 22 22
Doalanincó1nhómCOOHvàaxitglutamiccó2nhómCOOHnên: (*) NaOHAlaGlu nn2nx2y1,4 ChomgamXtác dụng hoàntoàn với dung dịch HCl: Tacó: muoáiX HCl mmm36,5m n 1mol 36,536,5
DẠYKÈMQUYNHƠN OFFICIAL Trang33
57a1,R67CH
m0,6890,4147111,2gam Dạng 3: Phản ứng nối tiếp 1 – B 2 – C 3 – C 4 – A 5 – C 6 – A 7 – C 8 – A 9 – A 10 – B Câu 1: NaOHHClaxitglutamic nn2n0,350,15.20,65mol
2GlyKOHMuoáiHO mol
0,2 2 HClKOHKClHO
khối lượng: 2 GlyHClKOHmuoá
Doalanincó1nhómNH2 vàaxitglutamiccó1nhómNH2 nên: (**) HClAlaGlu nnnxy1 Từ (*)và(**)suyra: x0,6;y0,4
Câu 2: glyxin KOH n0,2mol;n0,5mol
Coidung dịch X gồm glyxin(0,2mol)vàHCl. Phương trìnhhóa học:
0,20,2
mol 0,30,30,3 Bảo toàn
iHOmmmmm
m150,3.36,50,5.560,5.1844,95gam
Câu 3: HCl KOH n0,02mol;n0,05mol
Coidung dịch Y gồm X(amol)vàHCl(0,02mol). Phương trìnhhóa học:
2XKOHMuoáiHO mol aa 2 HClKOHKClHO mol 0,020,02 Tacó: a0,020,05a0,03 X M89 Xcócáccông thức là: 2 22 HNCHCHCOOH; 3 2 CHCHNHCOOH Câu 4: HCl NaOH n0,2mol;n0,45mol Coidung dịch gồm X(xmol)vàHCl(0,2mol)tác dụng với 0,45molNaOH. Tacó: 2 HONaOH nn0,45mol Bảo toàn khối lượng: 2 XHClNaOHmuoáiHOmmmmm X m46,450,45180,45400,236,529,25gam Giả sử Xcó1nhómCOOHtacó phương trìnhhóa học: 2XNaOHMuoáiHO mol xx 2 HClNaOHNaClHO mol 0,20,2 Tacó: x0,20,45x0,25mol X M117 -aminoaxitXlàvalin.
DẠYKÈMQUYNHƠN OFFICIAL Trang34
iHOmmmmm X m33,90,4.180,4.400,2.36,517,8gam Câu
NaOH HCl n0,2mol;n0,36mol Gọi
mol của alaninvàaxitglutamic
(*)
Coi
gồm
(**)
Câu 5: HCl NaOH n0,2mol;n0,4mol
Coidung dịch Y gồm X(0,2mol)vàHCl(0,2mol)tác dụng với NaOH. Tacó: 2 HOXHCl nnn0,4mol Bảo toàn khối lượng: 2 XNaOHHClmuoá
6:
số
lần lượt làx,ymol.
89x147y15,94
hỗn hợp
alanin(xmol);axitglutamic(ymol)tác dụng vừa đủ với 0,2molNaOH.
x2y0,2
Từ (*)và(**)suyra: x0,08;y0,06 Coidung dịch X gồm alanin(0,08mol);axitglutamic(0,06mol)và0,2molNaOHtác dụng với HCl. Phương trìnhhóa học: AlaHClMuoá i GluHClMuoá i 2 NaOHHClNaClHO Tacó: HClphaûnöùngalagluNaOH nnnn0,080,060,20,34 HCl dư vào 2 HONaOH nn0,2mol Bảo toàn khối lượng: 2 alagluNaOHHClpömuoáiHOmmmmmm raénkhanmuoá i mm15,940,34.36,50,2.400,2.1832,75gam
DẠYKÈMQUYNHƠN OFFICIAL Trang35
Câu 7: Xcó1nhómNH2: HClX nn0,01mol Coidung
Phương
2
mol 0,010,01 0,01 2 HClKOHNaClHO mol 0,010,010,01 dư và KOHbanñaà u n0,04molKOH 2 HOKOHpö nn0,02mol Bảo toàn khối lượng: 2 XKOHHClchaátraénHOmmmmm X m0,04560,0136,52,9950,0218 X m0,75gam X M0,7575 0,01 Công thức của Xlà: 2 2 HNCHCOOH Câu 8: Gọi số molglyxinvàaxitaxetic lần lượt làx,ymol (*) 75x60y21 Tacó: KOH 32,421 n50,3mol 618 (**) ab0,3 Từ (*)và(**)suyra: mol a0,2;b0,1
dịch Y gồm X(0,01mol)vàHCl(0,01mol).
trìnhhóa học:
XKOHMuoáiHO
DẠYKÈMQUYNHƠN OFFICIAL Trang36
2
Coidung
Y gồm
Phương
2XCOOHNaOH&KOHMuoáiHO mol 7,5x 7,5x 7,5x 2HClNaOH&KOHMuoáiHO mol 8x8x 8x Tacó: NaOHKOH nn0,155molx0,01 2 HO HCl n15,5x0,155mol n0,08mol Bảo toàn khối lượng: 2 XHClNaOHKOHmuoáiHOmmmmmm muoá i m7,420,08.36,50,08.400,075.560,155.1814,95gam Dạng 4: Phản ứng cháy của amino axit 1 – A 2 – B 3 – B 4 – A 5 – B 6 – C 7 – C 8 – C 9 – A 10 – B
Tacóquátrình: KOH HCl 22 22 32 3 3 NHCHCOOH:0,2molXNHCHCOOKClNHCHCOOH:0,2mol CHCOOH:0,1mol CHCOOK KCl:0,3mol
m0,2.111,50,3.74,544,65gam
Câu 9: 24HSO HCl NaOH KOH n0,02mol;n0,06mol;n0,04mol;n0,08mol H OH n0,1mol;n0,12mol Coidung dịch Y chứa X(0,02mol);H+ (0,1mol). 2 OHpöHOXH nnnn0,020,10,12mol Bảo toàn khối lượng: 2 XaxitddkieàmmuoáiHOmmmmm muoá i m0,02.1180,02.980,06.36,50,04.400,08.560,12.1810,43gam Câu 10: OH n0,155mol Tacó: N N O O mn78 m15n15 Gọi số mol của NvàOtrongX lần lượt là8x,15xmol.
NHN COOHO 1 nn8xmol;nn7,5xmol 2
Xtác dụng vừa đủ với HCl: 2HClNH nn8xmol
dịch
XvàHCl(8xmol).
trìnhhóa học:
tử.
AlàH
DẠYKÈMQUYNHƠN OFFICIAL Trang37
2 t
2 2 2
22
cấu tạo của Xlà:CH3CH2CH(NH2)COOH. Câu 4: X chỉ có thể cho1nhómNH2 và1nhómCOOH. 2 2HOCOnn Công thức của Xcó dạng: H2NRCOOH. KOH NaOH n0,4mol,n0,3mol Coidung dịch Y gồm X,NaOH(0,03mol),KOH(0,4mol).Tacó: 2 2 XHClMuoá i KOHHClKClHO NaOHHClNaClHO 2 HClXNaOHKOH HONaOHKOH nnnn0,9mol nnn0,7mol Bảo toàn khối lượng: 2 XNaOHKOHHClmuoáiHOmmmmmm X X m75,250,7180,3400,4560,936,520,6gamM103R42
Câu 1: Số nguyên tử nguyên tử Acó1nhómNH2 2N A 2n N1 n Số nguyên tử nguyên
2CO A Cn2a2 na Công thức cấu tạo của
2NCH2COOH. Câu 2: Công thức phân tử của Xlà n2n12 CHONn2 2 2 2 HOCO XX N X 1 nn0,5nn1molnn0,5mol 2 Câu 3: Các đáp án đều là các amino axit no, có 1 nhóm COOH và 1 nhóm NH2 nên có công thức là: .n2n12 CHONn2
Phương trìnhhóa học:
n2n12
N 6n3 2n11 CHONOnCOHOn 4
mol 89 Tacó phương trình: 89n4 n2n1 2
MàXlà -aminoaxitnêncông thức
t n2n12 2 2 2 N 6n3 2n11 CHONOnCOHOn 4 22 mol 16n3nn0,50,5 4 Tacó: 2 2NkkO n4n6n3mol
DẠYKÈMQUYNHƠN OFFICIAL Trang38
2 2HOCO Y nn n00,2mol ,5 Z
Y Z n0,22 n0,33 Khicho0,45molX phản ứng với HCl: Y 0,45.2 n50,18mol Chỉ
phản ứng được
Công thức của XlàH2NC3H6COOH. Đốt cháy12,36gamXcó 2 Ot 492 2 CHON4,5HO mol 0,120,54 Câu 5: Gọi công thức phân tử của Xlà n2n12 CHONn2 Phương trìnhhóa học: 2
Sau phản ứng cóCO2 (nmol);H2O(mol);N2 (mol) n0,5 0,56n36n2,5 Tỉ khối hỗn hợp khívà hơi so với H2 và14,317nêntacó: 44n18n0,5286n2,5 28,634 nn0,56n2,5
n4 Vậy công thức của XlàC4H9O2N. Câu 6: 2 2 CO HO n1,2mol;n1,3mol
Đốt cháyaxitcacboxylicno, đơn chức mạch hở Zluônthu được 2 2 COHO nn. Đốt cháyaminoaxitYcó một nhómNH2 thu được 2 2 COHOnn Aminoaxitno, mạch hở, có một nhómNH2 và một nhómCOOH.
n0,50,20,3mol
cóYtrongX
với HCl. MàYcó một nhómNH2: HClY nn0,18mol
gam m0,18.36,56,57
Câu 7: Coidung dịch B gồm X(xmol),Y(0,02mol)vàHCl(0,11mol).
OH n0,16mol. Phương trìnhhóa học: 2XOHMuoáiHO mol xx x 2YOHMuoáiHO mol 0,020,020,02 2 HOHHO mol 0,110,110,11 Tacó: 2 HOOH x0,020,110,16x0,03;nn0,16mol Bảo toàn khối lượng: 2 XYNaOHKOHHClmuoáiHOmmmmmmm X m14,6050,16180,1136,50,12400,04560,021463,51gam
DẠYKÈMQUYNHƠN OFFICIAL Trang39
mol 0,10,1 x0,10,19x0,09 Đốt cháyhoàntoànmgam hỗn hợp X: Gọi số molCO2 làamol.X gồm cácaminoaxitcó1nhómCOOHvà1nhómNH2 nên 2 2 2 HOCO XHO nn0,5nna0,045mol Tacó: 3 2BaCOCO nnamol Khối lượng dung dịch trongbình giảm 43,74gam: 3 2 2 BaCOCOHO mmm43,74gam 197a44a18a0,8143,74 a0,33
X M3,51117 0,03 Công thức của XlàH2NC4H8COOH. Đốt cháyhoàntoànA: 2 COXY an5n6n5.0,036.0,020,27mol Câu 8:Coidung dịch Y gồm X(xmol)vàHCl(0,1mol). Tacó: KOH n0,19mol Phương trìnhhóa học: 2XKOHMuoáiHO mol xx 2 HClKOHKClHO
DẠYKÈMQUYNHƠN OFFICIAL Trang40
2 2
Số
2
X
2 HO X 2n H11 n Vậy công thức của XlàH2NC4H8COOH. X NaOH KOH OH n0,25mol;n0,2mol;n0,25moln0,45mol Coidung dịch Y gồm H2NC4H8COOH(0,25mol)vàH2SO4 Phương trìnhhóa học: 248 248 2 HNCHCOOHOHHNCHCOOHO mol 0,250,25 0,25 2 HOHHO mol 0,20,20,2 24 HSOH 1 nn0,1mol 2 Bảo toàn khối lượng: 24 2 XNaOHKOHHSOmuoáiHOmmmmmm a29,250,2.400,25.560,1.980,45.1852,95gam Câu 10: Tacó: O O N N mn8010 m21n3 Gọi số molO,NtrongX lần lượt là10x,3xmol. 2 COOHO NHN 1 nn5xmol 2 nn3xmol Xtác dụng vừa đủ với 0,03molHCl: 2 NHHCl nn0,03molx0,01mol
2 2 CCO HHO NX OX nn0,33mol n2n0,75mol nn0,09mol n2n0,18mol Bảo toànnguyên tố C,H,N,O: m0,33120,750,18160,09148,85gam Câu 9: 2 2 CO HO n0,05mol;n0,055mol
Ta thấy: Aminoaxitno, mạch hở, chỉ có thể có một nhómNH2 và một nhómCOOH. 2 2HOCOnn
HOCO X nn n00,01mol ,5
nguyên tử Số nguyên tử
CO
n C5; n
OFFICIAL Trang41
2
X OX
DẠYKÈMQUYNHƠN
Tacó
NNH
nn0,03mol n0,1mol
CH mm1,81gam Gọi số molCO2 vàH2O lần lượt làx,ymol. Bảo toànnguyên tố C,H: 2 2 CCO HHO nnxmol;n2n2ymol (*) 12x2y1,81 Lại có: 2O n0,1425mol Bảo toànnguyên tố O: 2 2 2 OCOHOOX n2n2nn (**) 2xy0,385 Từ (*)và(**)suyra: x0,13;y0,125 Dẫn sản phẩm cháyquadung dịch nước vôitrong dư: 3 2CaCOCO keáttuû a nn0,13molm13gam
BÀI 6: PEPTIT - PROTEIN
Mục tiêu
Kiến thức
+Nêu được khái niệm, định nghĩa, đặc điểm cấu tạo phân tử của proteinvàpeptit.
+Trìnhbày được tính chất hoá học của peptit (phản ứng thuỷ phân).
+ Chỉ ra được vaitrò của protein đối với sự sống.
+Trình bày được tính chất của protein (sự đông tụ, phản ứng thuỷ phân, phản ứng màu của protein với Cu(OH)2). Kĩ năng
+ Viết được các phương trìnhhoá học minh hoạ tính chất hoá học của peptitvàprotein.
+ Phân biệt được dung dịch protein với chất lỏng khác.
+ Giải được bài tập hoá học có liên quan dựa theo phương trình hoá học và các định luật bảo toàn.
I. LÍ THUYẾT TRỌNG TÂM
A. PEPTIT
1. Khái niệm
a. Khái niệm
Peptitlà những hợp chất chứa từ 2 đến 50 gốc -aminoaxitliên kết với nhau bằng liên kết peptit. Liên kết peptitlàliên kết giữa hai đơn vị -aminoaxit. CONH
CNH =
Nhóm giữa hai đơn vị -aminoaxit được gọi lànhómpeptit. O
b. Phân loại
Oligopeptit chứa từ 2 đến 10 gốc -aminoaxit.
Đipeptit: chứa 2 gốc -aminoaxit.
Tripeptit: chứa 3 gốc -aminoaxit.
Tetrapeptit: chứa 4 gốc -aminoaxit.
Polipeptit chứa từ 11 đến 50 gốc -aminoaxit.
c. Danh pháp
gốc
DẠYKÈMQUYNHƠN
Trang1
OFFICIAL
Ví dụ: 22 3 aminoaxitñaàuN aminoaxitñaàuC HNCHCONHCH(CH)COOH
Glyxylalanin. Viết
.
Tên
axyl của -aminoaxit đầu N+Tên gốc -aminoaxit đầu C.
Tên gọi:
tắt: Gly-Ala. Chú ý: -amino axit đầu N còn nhóm NH2
-amino axit đầu C còn nhóm COOH.
2. Tính chất hoá học
Phản ứng thuỷ phân:
Phản ứng thuỷ phânhoàntoàn:
Peptit -aminoaxit HhoaëcOH
Phản ứng thuỷ phânkhônghoàntoàn:
Peptit Peptit ngắn hơn
Phản ứng màubiure:
Trong môi trường kiềm, peptit từ hai liên kết peptit trở lên tác dụng với Cu(OH)2 cho hợp chất màu tím đặc trưng.
Chú ý: Đipeptit chỉ có một liên kết peptit nên không có phản ứng màu biure. Dùng để nhận biết đipeptit với các peptit khác.
B. PROTEIN
1. Khái niệm
a. Khái niệm
Proteinlà những polipeptitcaophân tử cóphân tử khối từ vài chục nghìn đến vài triệu.
b. Phân loại
Protein đơn giản: khi thuỷ phân chỉ cho hỗn hợp các -aminoaxit.
Ví dụ: Anbumin trong lòng trắng trứng,…
Protein phức tạp: tạo thànhprotein đơn giản cộng với thành phần “phiprotein”.
Ví dụ: Lipoprotein chứa trong chất béo…
2. Tính chất vật lí
Nhiều protein Dung dịch keo Đông tụ. 2 HO ot
Ví dụ: Lòng trắng trứng hoà tan trong nước, khi đun sôi sẽ đông tụ lại. Protein Đông tụ hoặc kết tủa.
ô/muoá i 3. Tính chất hoá học
Phản ứng thuỷ phân: tương tự peptit.
Phản ứng màubiurecho hợp chất cómàutím đặc trưng. Chú ý: Đây là phản ứng dùng để nhận biết protein. 4. Vai trò của protein đối với sự sống
Proteinlà cơ sở tạo nên sự sống.
Proteinlàthành phần chínhtrong thức ăn của người và động vật.
DẠYKÈMQUYNHƠN
Trang2
OFFICIAL
chieä u
HhoaëcOH Enzimñaë
axit/baz
Peptit là những hợp chất chứa từ 2 đến 50 gốc -
aminoaxitliên kết với nhau bằng liên kết peptit. Liên kết peptit
HOÁ
Oligopeptit chứa từ 2 đến 10 gốc -aminoaxit.
Đipeptit chứa 2 gốc -aminoaxit.
Tripeptit chứa 3 gốc -aminoaxit.
Tetrapeptit chứa 4 gốc -aminoaxit.
Polipeptit chứa từ 11 đến 50 gốc -aminoaxit.
KHÁI NIỆM
PHÂN LOẠI
PHÂN
DẠYKÈMQUYNHƠN OFFICIAL Trang3 SƠ ĐỒ HỆ THỐNG
H2
O
PEPTIT
NCC H R1 O NCC OH
H H R2 Aminoaxit đầu N Aminoaxit đầu C
DANH PHÁP TÍNH CHẤT HOÁ HỌC n
m
n m Ví dụ: Gọi tên của đipeptit 22 3 Glyxyl Alanin HNCHCONHCH(CH)COOH Cách1:glyxylalanin Cách2:Gly-Ala Phản ứng thuỷ phân Peptit -aminoaxit HhoaëcOH Peptit Peptit ngắn hơn H Enzim hoaëcOH ñaëchieä u Phản ứng màu biure Từ tripeptit trở lên có phản ứng với
2 tạo
ĐỒNG
loại -aminoaxit n!phân tử n-peptit
loại -aminoaxit phân tử n-peptit
Cu(OH)
phức màutím đặc trưng.
PROTEIN
KHÁI NIỆM
Protein là những polipeptit cao phân tử có phân tử khối từ vài chục nghìn đến vài triệu.
Protein đơn giản: khi thuỷ phân chỉ cho hỗn hợp các -aminoaxit. Ví dụ: anbumin của lòng trắng trứng fibroin của tơ tằm
PHÂN LOẠI
Protein phức tạp: tạo thành từ protein đơn giản cộng với thành phần “phiprotein”. Nhiều protein Dung dịch keo 2 HO ot Đông tụ
TÍNH CHẤT VẬT LÝ
Protein axit/bazô/muoá i Ñoângtuï Keáttuû a
TÍNH CHẤT HOÁ HỌC
Phản ứng thuỷ phân Proteincó phản ứng thuỷ phân tương tự peptit.
Phản ứng màu biure Protein có phản ứng màu biure với Cu(OH)2 Dùng để nhận biết protein.
DẠYKÈMQUYNHƠN
Trang4 II. CÁC DẠNG
OFFICIAL
BÀI TẬP
Dạng 1: Lí thuyết trọng tâm Ví dụ mẫu
Ví dụ 1: Số gốc -aminoaxittrongphân tử tripeptit mạch hở là
A. 4. B. 2. C. 3. D. 5.
Hướng dẫn giải
Đipeptit được tạo thành từ 2 gốc -aminoaxit.
Tripeptit được tạo thành từ 3 gốc -aminoaxit.
Tetrapeptit được tạo thành từ 4 gốc -aminoaxit.
Pentapeptit được tạo thành từ 5 gốc -aminoaxit. Chọn C.
Chú ý: Giả sử peptit được tạo thành từ n gốc -amino axit thì số liên kết peptit (NH – CO) là: n – 1
Ví dụ 2: Thuốc thử dùng để phân biệt Gly-Ala-GlyvàGly-Alalà
OFFICIAL
A. dung dịch NaCl. B. dung dịch NaOH. C. dung dịch HCl. D. Cu(OH)2 trongmôi trường kiềm. Hướng dẫn giải
Thuốc thử dùng để phân biệt Gly-Ala-GlyvàGly-AlalàCu(OH)2 trongmôi trường kiềm: Gly-Ala-Glylàtripeptitnêncó phản ứng màubiure với Cu(OH)2 tạo phức màutím. Gly-Alakhôngcó hiện tượng gìvì đipeptit khôngcó phản ứng màubiure với Cu(OH)2 Chọn D. Ví dụ 3: Đipeptit Xcócông thức: H2NCH2CONHCH(CH3)COOH.Tên gọi của Xlà
A. alanylglixyl. B. alanylglixin. C. glyxylalanin. D. glyxylalanyl. Hướng dẫn giải
Tacó: 22 3
C.
hoặc Gly-Ala.
dụ 4: Số tripeptit mạch hở khi thuỷ phânhoàntoànthu được ba loại -aminoaxit:Gly,Ala,Vallà
DẠYKÈMQUYNHƠN
Trang5
Glyxyl alanin HNCHCONHCH(CH)COOH
Xcótênlàglyxylalanin
Chọn
Ví
A. 2. B. 3. C. 4. D. 6. Hướng dẫn giải Cách 1: Liệt kê Khi thuỷ phânhoàntoàntripeptitthu được ba loại -aminoaxitnêntripeptit phải được tạo thành từ ba
loại -aminoaxit:Gly,Ala,Val.
G-A-V;G-V-A;A-G-V;A-V-G;V-A-G;V-G-A Cách 2: Sử dụng công thức tínhnhanh Tripeptit phải được tạo thành từ ba loại -aminoaxit:Gly,Ala,Valnên số tripeptit thoả mãnlà:
3!=6. Chọn D.
Ví dụ 5: Thuỷ phân không hoàn toàn tetrapeptit X ngoài các -amino axit còn thu được các đipeptit: Gly-Ala;Phe-Val;Ala-Phe. Cấu tạo đúng của Xlà
A. Ala-Val-Phe-Gly.
B. Val-Phe-Gly-Ala. C. Gly-Ala-Phe-Val. D. Gly-Ala-Val-Phe. Hướng dẫn giải Ghép mạch peptittacó: Gly-Ala Ala-Phe Phe-Val Gly-Ala-Phe-Val Chọn C.
Ví dụ 6: Phát biểu nàosau đây đúng?
A. Cácpeptitmàphân tử chứa từ 11 đến 50 gốc aminoaxit được gọi làpolipeptit.
B. Cácprotein đều là chất rắn, nhiệt độ nóng chảy caovà dễ tantrong nước.
C. Trongphân tử peptit mạch hở phân tử chứa hai gốc -aminoaxit được gọi là đipeptit.
D. Trongphân tử peptit mạch hở phân tử chứa hailiên kết peptitCO–NH được gọi là đipeptit. Hướng dẫn giải
Asaivìpolipeptit gồm cácpeptitcó từ 11 đến 50 gốc -aminoaxit.
Bsaivìprotein được chialàmhai loại là dạng proteinhình sợi vàproteinhình cầu.
Proteinhình sợi hoàntoànkhôngtantrong nước.
Proteinhình cầu tantrong nước tạo thànhdung dịch keo. C đúng vì đipeptit được tạo nên từ hai gốc -aminoaxit.
Dsaivìtrongphân tử peptit mạch hở phân tử chứa hailiên kết peptitCO–NH được gọi làtripeptit. Chọn C.
Ví dụ 7: Tiến hànhcácthí nghiệm sau với dung dịch X chứa lòng trắng trứng:
Thí nghiệm 1: Đun sôidung dịch X.
Thí nghiệm 2:Chodung dịch HClvàodung dịch X, đun nóng.
Thí nghiệm 3:Chodung dịch CuSO4 vàodung dịch X,sau đó nhỏ vài giọt dung dịch NaOHvào.
Thí nghiệm 4:Chodung dịch NaOHvàodung dịch X, đun nóng.
Thí nghiệm 5:Chodung dịch AgNO3 trongNH3 vàodung dịch X, đun nóng.
Số thí nghiệm có xảy ra phản ứng hoá học là
A. 3. B. 5. C. 2. D. 4.
Hướng dẫn giải
Lòng trắng trứng chínhlàprotein(polipeptit)nên thể hiện đầy đủ tính chất của polipeptit. Cácthí nghiệm có xảy ra phản ứng hoá học là:
Thí nghiệm 2vìlà phản ứng thuỷ phântrongmôi trường axit.
Thí nghiệm 3vìlà phản ứng màubiure.
Thí nghiệm 4vìlà phản ứng thuỷ phântrongmôi trường kiềm.
DẠYKÈMQUYNHƠN
Trang6
OFFICIAL
Chọn A.
Bài tập tự luyện dạng 1
Bài tập cơ bản
Câu 1: Hợp chất nàosau đây thuộc loại đipeptit?
A. H2N–CH2 –CO–NH–CH2 –CO–NH–CH2 –COOH.
B. H2N–CH2 –CH2 –CO–NH–CH2 –COOH.
C. H[HN–CH2 –CH2 –CO]2OH.
D. H2N–CH2 –CO–NH–CH(CH3)–COOH.
Câu 2: Tripeptitlà hợp chất
A. có3liên kết peptitmàphân tử có2 gốc -aminoaxit.
B. có3liên kết peptitmàphân tử có2 gốc -aminoaxit.
C. có2liên kết peptitmàphân tử có3 gốc -aminoaxit.
D. có2liên kết peptitmàphân tử có3 gốc -aminoaxit.
OFFICIAL
Câu 3: Protein phản ứng với Cu(OH)2/OH tạo sản phẩm cómàu đặc trưng là
A. màu đỏ. B. màudacam. C. màuvàng. D. màutím.
Câu 4: Để nhận biết Gly-AlavàGly-Gly-Gly-Alatronghai lọ riêng biệt, thuốc thử cần dùnglà
A. Cu(OH)2/OH B. NaCl. C. HCl. D. NaOH. Câu 5: Khi nấu canhcuathì thấy các mảng “riêucua” nổi lênlàdo
A. sự đông tụ của proteindo nhiệt độ. B. sự đông tụ của lipit. C. phản ứng màu của protein. D. phản ứng thuỷ phân của protein.
Câu 6: Dung dịch chất nàosau đây có phản ứng màubiure?
A. Triolein. B. Gly-Ala. C. Glyxin. D. Anbumin. Câu 7: Từ glyxin(Gly)vàalanin(Ala)có thể tạo rabaonhiêu đipeptit?
A. 1. B. 2. C. 3. D. 4. Câu 8: Phát biểu nàosau đây sai?
A. Peptit bị thuỷ phântrongmôi trường axitvà kiềm.
B. Glyxin(H2NCH2COOH) phản ứng được với dung dịch NaOH. C. Metylaminlàmxanh quỳ tím ẩm.
D. TripeptithoàtanCu(OH)2 tạo dung dịch màuxanh. Câu 9: Protein là cơ sở tạo nên sự sống vì hai thành phần chính của tế bào là nhân và nguyên sinh chất đều hình thành từ protein. Protein cũng là hợp chất chính trong thức ăn của con người. Trong phân tử proteincác gốc -aminoaxit gắn với nhau bằng liên kết
A. peptit. B. hiđro. C. amit. D. glicozit.
Câu 10: Phát biểu nàosau đây sai?
A. TripeptitGly-Ala-Glycó phản ứng màubiure với Cu(OH)2/OH
B. Protein đơn giản được tạo thành từ các gốc -aminoaxit.
C. Tất cả cácpeptit đều có khả năng thamgia phản ứng thuỷ phân.
D. Trongphân tử đipeptit mạch hở cóhailiên kết peptit.
Câu 11: Khinói về peptitvàprotein,phát biểu nàosau đây là sai?
DẠYKÈMQUYNHƠN
Trang7
A. Liên kết của nhómCO với nhómNH giữa hai đơn vị -aminoaxit được gọi làliên kết peptit.
B. Tất cả cácprotein đều tantrong nước tạo thànhdung dịch keo.
C. Proteincó phản ứng màubiure với Cu(OH)2
D. Thuỷ phânhoàntoànprotein đơn giản bằng enzimthu được các -aminoaxit.
Câu 12: PeptitXcócông thức Pro-Pro-Gly-Arg-Phe-Ser-Phe-Pro.Khi thuỷ phânkhônghoàntoànXthu được tối đa baonhiêu loại peptitcóaminoaxit đầu Nlàphenylalanin(Phe)?
A. 4. B. 6. C. 5. D. 3.
Câu 13: Cho các chất sau: xenlulozơ, axit aminoaxetic, Ala-Gly-Glu, etyl propionat. Số chất phản ứng với dung dịch NaOH (đun nóng)là
A. 4. B. 2. C. 1. D. 3. Câu 14: Tiến hànhthí nghiệm với các chất X,Y,Z,T. Kết quả được ghi ở bảng sau: Mẫu thử Thí nghiệm Hiện tượng
X Tác dụng với Cu(OH)2 trongmôi trường kiềm
Y Đun nóng với dung dịch NaOH (loãng, dư), để nguội. Thêm tiếp vài giọt dung dịch CuSO4
Z Đun nóng với dung dịch NaOH loãng (vừa đủ). Thêm tiếp dung dịch AgNO3 trongNH3, đun nóng
Tạo dung dịch màutím
OFFICIAL
Tạo dung dịch màuxanhlam
Tạo kết tủa Ag
T Tác dụng với dung dịch I2 loãng Cómàuxanhtím Các chất X,Y,Z,T lần lượt là:
A. Lòng trắng trứng, triolein,vinylaxetat, hồ tinh bột.
B. Lòng trắng trứng, triolein, hồ tinh bột, vinylaxetat.
C. Vinylaxetat,lòng trắng trứng, triolein, hồ tinh bột.
D. Triolein,vinylaxetat, hồ tinh bột, lòng trắng trứng.
Câu 15: Đun nóng chất H2N–CH2 –CHNH–CH(CH3)–CONH–CH2 –COOHtrongdung dịch HCl dư, saukhicác phản ứng kết thúcthu được sản phẩm là:
A. ClH3N–CH2 –COOH,ClH3N–CH2 –CH2 –COOH. B. H2N–CH2 –COOH,H2N–CH2 –CH2 –COOH. C. ClH3N–CH2 –COOH,ClH3N–CH(CH3)–COOH. D. H2N–CH2 –COOH,H2N–CH(CH3)–COOH. Câu 16: Thuỷ phân hoàn toàn một tetrapeptit X thu được 1 mol glyxin, 2 mol alanin, 1 mol valin. Số đồng phân cấu tạo của peptitXlà A. 8. B. 10. C. 12. D. 18. Câu 17: Cho các chất: glyxin; axit glutamic; ClH3NCH2COOH; Gly-Ala. Số chất tác dụng được với NaOHtrongdung dịch theo tỉ lệ tương ứng 1:2là A. 1. B. 2. C. 3. D. 4. Bài tập nâng cao
DẠYKÈMQUYNHƠN
Trang8
Câu 18: Công thức phân tử của peptit mạch hở có 4 liên kết peptit được tạo thành từ -amino axit no, mạch hở, có một nhómaminovà một nhómcacboxylcó dạng
A. B. C. D. n2n365 CHON n2n254 CHON n2n665 CHON n2n654 CHON Câu 19: Thuỷ phânkhônghoàntoànpeptitcócông thức hoá học: H2N–CH(CH3)–CONH–CH2 –CONH–CH2 –CONH–CH2 –CONH–CH(CH3)–COOH. Sản phẩm thu được có tối đa baonhiêupeptitcó phản ứng màubiure? A. 5. B. 3. C. 4. D. 10.
Câu 20: Chocácphát biểu sau:
(a)Trong một phân tử tetrapeptit mạch hở có4liên kết peptit.
(b)Dung dịch lysinlàmxanh quỳ tím.
(c)Anilintác dụng với nước brom tạo thành kết tủa trắng.
(d)PeptitGly-Alacó phản ứng màubiure với Cu(OH)2
(e) Thuỷ phânhoàntoànprotein đơn giản thu được các -aminoaxit. (f)Các hợp chất peptitkém bền trongmôi trường bazơ nhưng bền trongmôi trường axit. Số phát biểu đúng là
OFFICIAL
A. 5. B. 4. C. 3. D. 2. Dạng 2: Phản ứng thuỷ phân
Bài toán 1: Thuỷ phân hoàn toàn Phương pháp giải Chú ý: peptit MM18n1 aminoaxit
Phản ứng thuỷ phânhoàntoàn:Peptit được tạo nên từ ncác -aminoaxit
DẠYKÈMQUYNHƠN
Trang9
oxt,t n 2 An1HOnaminoaxit Bảo
peptit mmm nöôùcaminoaxit Môi
axit: Muối n 2 An1HOnHCl Nhận xét: 2 peptitHOHCl nnnnmuoá i Bảo toàn khối lượng: peptit HCl mmmm nöôù c muoá i Môi trường kiềm (NaOH/KOH): Ví dụ: Muối +H2O n AnNaOH Nhận xét: 2 peptitHO NaOH peptit nn nnn.n pömuoá i
Môi trường trungtính:
toàn khối lượng:
trường
Bảo toàn khối lượng: 2 peptitNaOH HOmmmm pömuoá i Nếu NaOH dư: 2 peptit HO NaOH mmmm chaátraénkhan banñaà u Ví dụ: Thuỷ phân hoàn toàn m gam đipeptit Gly-Ala (mạch hở) bằng dung dịch HCl vừa đủ thu được dung dịch X.Cô cạn toàn bộ dung dịch Xthu được 4,74gam muối khan.Giá trị của mlà A. 2,92. B. 2,72. C. 3,28. D. 2,44. Hướng dẫn giải Gọi số mol của đipeptit Gly-Alalàxmol. Phương trìnhhoá học: Muối 2 2 A2HClHO x 2x x mol Bảo toàn khối lượng: 2 peptitHClHO mmmmmuoá
146x2x36,518x4,74 4,74 x0,02 237
m0,02.1462,92gam Chọn A. Ví dụ mẫu Ví dụ 1: Thuỷ phân1250gamproteinXthu được 425gamalanin. Nếu phân tử khối trungbình của Xlà 100000 đvC thì số mắt xíchtrungbìnhalanincótrongphân tử Xlà A. 453. B. 382. C. 328. D. 479. Hướng dẫn giải protein alanin 1250 425 n 0,0125mol;n4,78mol 100000 89 Số mắt xíchalanincótrongphân tử Xlà: 4,78382 0,0125
DẠYKÈMQUYNHƠN OFFICIAL Trang10
Chọn B. Ví dụ 2: Thuỷ phân73,8gam một peptit chỉ thu được 90gamglyxin(Gly).Peptitban
là A. đipeptit. B. tripeptit.
Hướng dẫn giải Gly n1,2mol Khi thuỷ phânpeptit chỉ thu được glyxinnênpeptitcó
Glyn Bảo toàn khối lượng: 2 HO
2 HO n0,9mol
i
đầu
C. tetrapeptit. D. pentapeptit.
dạng:
m9073,816,2gam
Phương trìnhhoá học: n 2 Glyn1HOnGly 0,9 1,2 mol
Tacó phương trình: 0,91,2n4 n1n
Vậy peptitban đầu làtetrapeptit. Chọn C. Ví dụ 3: Thuỷ phân14,6gamGly-Alatrongdung dịch NaOH dư thu được mgam muối. Giá trị của mlà A. 20,6. B. 18,6. C. 22,6. D. 20,8. Hướng dẫn giải Tacó: peptit M75891.18146 peptit n0,1mol Phương trìnhhoá học: Muối +H2O 2 A2NaOH 0,1 0,2 0,1 mol Bảo toàn khối lượng: 2 peptitNaOH HOmmmm muoá i 14,60,240m0,118 muoá i m14,681,820,8gam muoá i Chọn D. Ví dụ 4: Cho3,96gamGly-Gly phản ứng hoàntoàn với 150mldung dịch KOH0,5M.Cô cạn dung dịch sau phản ứng, thu được mgam chất rắn khan.Giá trị của mlà A. 6,42. B. 7,08. C. 8,16. D. 7,62. Hướng
DẠYKÈMQUYNHƠN
Trang11
OFFICIAL
dẫn giải Tacó: GlyGly M75218132 GlyGly n0,03mol Lại có: KOH n0,075mol Phương trìnhhoá học: Muối +H2O 2 A2KOH 0,03 0,075 0,03 mol KOH dư, bảo toàn khối lượng: 2 peptit HO KOH mmmm chaátraénkhan banñaà u m3,960,075.560,03.187,62gam chaátraénkhan Chọn D.
Ví dụ 5: X là tetrapeptit Gly-Val-Ala-Val, Y là tripeptit Val-Ala-Val. Đun nóng 14,055 gam hỗn hợp X vàY bằng dung dịch NaOH vừa đủ, saukhi phản ứng kết thúcthu được dung dịch Z.Cô cạn dung dịch Z thu được 19,445gam muối. Phần trăm khối lượng của Xtrong hỗn hợp là A. 48,95%. B. 61,19%. C. 38,81%. D. 51,05%.
dẫn giải
M75117289318344;M117289218287
DẠYKÈMQUYNHƠN
Trang12
OFFICIAL
X %0,02344
14,055 Chọn A. Bài toán 2: Thuỷ phân không hoàn toàn Phương pháp giải Thuỷ phânkhônghoàntoàn: Peptit Peptit xuùctaù c hoaëcenzim ngaénhôn aminoaxit Bảo toàn gốc: n ncaùcgoáctrongcaùcchaátsauphaûnöùng goáctrongchaátñaà u Ví dụ: Thuỷ phân hết hỗn hợp gồm mgamtetrapeptitAla-Gly-Ala-Gly mạch hở thu được hỗn hợp gồm 21,7gamAla-Gly-Ala;agamGly;14,6gamAla-Gly.Giá trị của mlà A. 42,16. B. 43,80. C. 34,80. D. 41,10. Hướng dẫn giải AlaGlyAla 21,7 n 0,1mol 217
Hướng
Tacó: X Y
Gọi số mol của XvàYtrong14,055gam hỗn hợp lần lượt làx,ymol. 344x287y14,055* Phương trìnhhoá học: Muối +H2O 4 A4NaOH x 4x x mol Muối +H2O 3 A3NaOH y 3y y mol 2 NaOH HO n4x3ymol;nxymol Bảo toàn khối lượng: 2 NaOH HOmmmm hoãnhôïp muoá i 14,0554x3y4019,445xy18 142x102y5,39** Từ (*)và(**)suyra: x0,02;y0,025
Phần trăm khối lượng của Xtrong hỗn hợp là:
m100%48,95%
AlaGly 14,6 n0,1mol 146
Quátrình thuỷ phân: Ala-Gly-Ala-Gly Ala-Gly-Ala+Gly+Ala-Gly Bảo toàn gốc Ala: AlaGlyAlaGlyAlaGlyAlaAlaGly 2n2nn AlaGlyAlaGly 2n20,10,1 AlaGlyAlaGly n0,15mol Tacó: M89.275.23.18274 m0,15.27441,1gam Chọn D. Ví dụ mẫu Ví dụ 1: Thuỷ phân hết mgampentapeptitAla-Ala-Ala-Ala-Ala (mạch hở) thu được hỗn hợp gồm 21,36 gamAla,32gamAla-Alavà27,72gamAla-Ala-Ala.Giá trị của mlà A. 75,50. B. 74,60. C. 90,60. D. 111,74. Hướng dẫn giải Ala AlaAla AlaAlaAla n0,24mol;n0,2mol;n0,12mol Gọi số mol của pentapeptitlàxmol. Quátrình thuỷ phân:Ala-Ala-Ala-Ala-Ala Ala+Ala-Ala+Ala-Ala-Ala x 0,24 0,2 0,12 mol Bảo toàn gốc Ala: 5x0,240,220,123 x0,2 Tacó: M5.894.18373
pentapeptit m0,2.37374,6gam
Chọn B.
Bài tập tự luyện dạng 2 Bài tập cơ bản Câu 1: Thuỷ phânhoàntoàn65gampeptitXthu được 22,25gamalaninvà56,25gamglyxin.Xlà A. đipeptit. B. tripeptit. C. tetrapeptit. D. pentapeptit. Câu 2: Cho một peptitX được tạo nên bởi n gốc alanincó khối lượng phân tử là302 đvC. PeptitX thuộc loại A. pentapeptit. B. đipeptit. C. tetrapeptit. D. tripeptit. Câu 3: Khi thuỷ phân500gam một polipeptitthu được 170gamalanin. Nếu polipeptit đó có khối lượng phân tử là50000 đvC thìcóbaonhiêu mắt xích của alanin?
A. 175. B. 170. C. 191. D. 210. Câu 4: Thuỷ phân hoàn toàn 14,6 gam Gly-Ala trong dung dịch HCl dư, thu được m gam muối. Giá trị của mlà
DẠYKÈMQUYNHƠN OFFICIAL Trang13
A. 11,15. B. 12,55. C. 18,60. D. 23,70.
Câu 5: Thuỷ phân hoàn toàn 13,02 gam tripeptit Ala-Gly-Ala cần dùng hết V ml dung dịch NaOH 2M. Giá trị của Vlà
A. 120. B. 60. C. 30. D. 90.
Câu 6: Xlàtetrapeptit:Ala-Gly-Ala-Val. Thuỷ phânhoàntoàn0,1molXtrongNaOH vừa đủ thu được muối natri của alanin,glyxin,valin. Số mol mỗi muối lần lượt là:
A. 0,1mol;0,1mol;0,2mol. B. 0,2mol;0,1mol;0,2mol. C. 0,2mol;0,1mol;0,1mol. D. 0,1mol;0,1mol;0,1mol.
Câu 7: Thuỷ phân hoàn toàn 6,04 gam Gly-Ala-Val-Gly bằng dung dịch HCl dư, thu được dung dịch Y chứa mgam muối. Giá trị của mlà
A. 10,04. B. 9,67. C. 8,96. D. 26,29. Câu 8: Cho3,96gamGly-Gly phản ứng hoàntoàn với 150mldung dịch KOH0,5M.Cô cạn dung dịch sau phản ứng, thu được mgam chất rắn khan.Giá trị của mlà
OFFICIAL
A. 6,42. B. 7,08. C. 8,16. D. 7,62. Câu 9: Cho X là hexapeptit Ala-Gly-Ala-Val-Gly-Val và Y là tetrapeptit Gly-Ala-Gly-Val. Thuỷ phân hoàntoànmgam hỗn hợp gồm XvàYthu được baaminoaxit,trong đó có30gamglyxinvà28,48gam alanin.Giá trị của mlà
A. 77,6. B. 73,4. C. 80,8. D. 87,4. Câu 10: Cho 0,1 mol Ala-Gly tác dụng hết với 300 ml dung dịch KOH 1M. Cô cạn dung dịch sau phản ứng được mgam chất rắn. Giá trị của mlà
A. 29,6. B. 24,0. C. 22,3. D. 31,4. Câu 11: Thuỷ phân hết m gam tetrapeptit Gly-Gly-Gly-Gly (mạch hở) thu được hỗn hợp gồm 24 gam Gly,26,4gamGly-Glyvà22,68gamGly-Gly-Gly.Giá trị của mlà
A. 66,42. B. 66,44. C. 81,54. D. 81,81. Câu 12: Thuỷ phân hoàn toàn 8,6 gam một peptit X, thu được hỗn hợp sản phẩm gồm 4,5 gam glyxin; 3,56 gam alanin và 2,34 gam valin. Thuỷ phân không hoàn toàn X thu được tripeptit Ala-Val-Gly và đipeptit Gly-Ala,khôngthu được đipeptit Ala-Gly.Công thức cấu tạo của Xlà
A. Ala-Val-Gly-Ala-Val-Gly.
B. Gly-Ala-Val-Gly-Ala-Gly. C. Gly-Ala-Val-Gly-Gly-Ala. D. Gly-Ala-Gly-Val-Gly-Ala. Câu 13: Cho 36,3 gam hỗn hợp X gồm hai peptit: Ala-Gly và Ala-Gly-Ala tác dụng hết với dung dịch HCl dư thu được 59,95gam muối. Phần trăm số mol của Ala-GlytrongXlà A. 75,0%. B. 50,0%. C. 80,0%. D. 41,8%. Câu 14: Thuỷ phân một lượng pentapeptit mạch hở X chỉ thu được 3,045 gam Ala-Gly-Gly; 3,48 gam Gly-Val;7,5gamGly;2,34gamVal;xmolVal-AlavàymolAla. Biết Xcócông thức Ala-Gly-Gly-ValAla. Tỉ lệ x:ylà
A. 7:20. B. 2:5. C. 6:1. D. 11:16. Câu 15: Thuỷ phânhoàntoànmgam hỗn hợp oligopeptit gồm Ala-Val-Ala-Gly-AlavàVal-Gly-Glythu được agamAla;37,5gamGlyvà35,1gamVal.Giá trị của m,a lần lượt là
DẠYKÈMQUYNHƠN
Trang14
A. 92,1và26,7. B. 99,3và30,9. C. 84,9và26,7. D. 90,3và30,9. Câu 16: Thuỷ phânhoàntoàn6,04gamtetrapeptit mạch hở X (được tạo nên từ hai -aminoaxitcócông
thức dạng H2NCxHyCOOH) bằng dung dịch NaOH dư thu được 8,88 gam muối. Mặt khác, thuỷ phân hoàntoàn6,04gamX bằng dung dịch HCl dư thu được mgam muối. Giá trị của mlà
A. 7,12. B. 9,25. C. 10,04. D. 4,08. Câu 17: X là hỗn hợp chứa hai peptit mạch hở. Lấy m gam X cho vào dung dịch chứa NaOH dư đun nóng.Saukhicác phản ứng xảy rahoàntoàn thấy có0,1molNaOHthamgia phản ứng vàthu được (m+ 3,46) gam hỗn hợp hai muối của Ala và Gly. Biết phần trăm khối lượng của nguyên tố oxi trong X là 29,379%.Giá trị của mlà
OFFICIAL
A. 8,16. B. 7,28. C. 6,82. D. 7,08. Bài tập nâng cao Câu 18: Hỗn hợp A gồm bapeptit mạch hở X,Y,Zcó tỉ lệ mol tương ứng là2:3:4. Thuỷ phânhoàn toàn m gam A thu được hỗn hợp sản phẩm gồm 21,75 gam glyxin và 16,02 gam alanin. Biết số liên kết peptittrongphân tử X nhiều hơn trongZvà tổng số liên kết peptittrongbaphân tử X,Y,Z nhỏ hơn 17. Giá trị của mlà
A. 30,93. B. 30,57. C. 30,21. D. 31,29. Câu 19: X là một pentapeptit cấu tạo từ một amino axit mạch hở Y có một nhóm COOH và một nhóm NH2. Y có tổng phần trăm khối lượng oxi và nitơ là 51,685%. Khi thuỷ phân hết m gam X trong môi trường axit thu được 30,2 gam tetrapeptit; 30,03 tripeptit; 25,6 gam đipeptit và 88,11 gam Y. Giá trị của mlà
A. 149,2. B. 167,85. C. 156,66. D. 141,74. Câu 20: Hỗn hợp E gồm tripeptitXvàtetrapeptitY đều mạch hở. Thuỷ phânhoàntoàn0,2molEtrong dung dịch NaOH dư, thu được 76,25gam hỗn hợp muối của alaninvàglyxin. Mặt khác, thuỷ phânhoàn toàn 0,2 mol E trong dung dịch HCl dư, thu được 87,125 gam muối. Thành phần phần trăm theo khối lượng của Xtrong hỗn hợp E gần nhất với giá trị nào?
DẠYKÈMQUYNHƠN
Trang15
A. 27%. B. 31%. C. 35%. D. 22%. Dạng 3: Phản ứng đốt cháy Phương pháp giải Đốt cháypeptit được tạo nên bởi -aminoaxitno, mạch hở, phân tử chỉ chứa một nhómNH2 và một nhómCOOH: Công thức có dạng: a2an2nn1CHNO Nhận xét: 2 22 HOCONpeptit ONpeptit nnnn nnn Quy đổi peptitthành hỗn hợp gồm CHON,CH2,H2O.
Trong đó: 2
nn.n nn
CHONpeptit HOpeptit
n n Ngoàiracó thể áp dụng định luật bảo toànnguyên tố, bảo toàn khối lượng. Ví dụ: Tripeptit mạch hở X được tạo nên từ một -aminoaxitno, mạch hở, phân tử chỉ chứa một nhóm NH2 và một nhóm COOH. Đốt cháy hoàn toàn 0,1 mol X, thu được tổng khối lượng CO2 và H2O bằng 54,9gam.Công thức phân tử của Xlà A. C9H17N3O4. B. C6H11N3O4. C. C6H15N3O6. D. C9H21N3O6. Hướng dẫn giải Công thức của Xcó dạng: hay a2a3234 CHNO a2a134 CHNO. Bảo toànnguyên tố C,H: 2CO n0,1amol 2 HO 2a1 n0,1.0,1a0,05mol 2 Tổng khối lượng CO2 vàH2O bằng 54,9gam,tacó: 440,1a180,1a0,0554,9 a9 Vậy công thức phân tử của XlàC9H17N3O4. Chọn A. Ví dụ mẫu Ví dụ 1: Oligopeptitmạchhở X đượctạonêntừ các -aminoaxit đềucócôngthứcdạngH2NCnHmCOOH. Đốt cháyhoàntoàn0,05molX cần dùng vừa đủ 1,875molO2, chỉ thu được N2;1,5molCO2 và1,3mol H2O. Mặt khác, thuỷ phânhoàntoàn0,025molX bằng 400mldung dịch NaOH1M, đun nóng,thu được dung dịch Y.Cô cạn cẩn thận toàn bộ dung dịch Ythu được mgam chất rắn khan. Số liên kết peptittrong Xvàgiá trị của m lần lượt là A. 9và27,75. B. 10và27,75. C. 9và33,75. D. 10và33,75. Hướng dẫn giải Gọi nlà số mắt xíchtrongoligopeptitX. CHON:xmol CH:ymol 1,5molCO1,3molHON HO:0,05mol
Quy đổi Bảo toànnguyên tố C: xy1,5* Bảo toànnguyên tố H: x2y0,05.21,3.2x2y2,5** Từ (*)và(**)suyra: x0,5;y1
DẠYKÈMQUYNHƠN
Trang16
OFFICIAL
Nhận xét: Số mắt xích=n= CHON peptit X gồm CHON(xmol);CH2 (ymol)vàH2O(0,05mol). X:An o 2 1,875molO,t 2 2 22 2
m0,25.830,5.1440.0,1533,75gam
Chọn C.
Ví dụ 2: Hỗn hợp E gồm bapeptit mạch hở: đipeptit X,tripeptitY,tetrapeptitZcó tỉ lệ mol tương ứng là 2:1:1.Cho một lượng E phản ứng hoàntoàn với dung dịch NaOH dư, thu được 0,25mol muối glyxin; 0,2 mol muối alanin và 0,1 mol muối của valin. Mặt khác, đốt cháy hoàn toàn m gam E, thu được tổng khối lượng của CO2 vàH2Olà39,14gam.Giá trị của mlà
A. 16,78. B. 25,08. C. 20,17. D. 22,64. Hướng dẫn giải Gọi công thức của cácpeptitX,Y,Z lần lượt làA2,B3,C4 với số mol tương ứng là2a,a,amol. Xét phản ứng thuỷ phân Bảo toàn gốc -aminoaxitcó: 22a3a4a0,250,20,1
DẠYKÈMQUYNHƠN OFFICIAL Trang17
Tacó: Số mắt xích= CHON X n0,510 n0,05 X được tạo thành từ 10 -aminoaxit Số liên kết peptittrongXlà9. Tacó: NaOHCHON nn0,25mol NaOHd n0,40,250,15mol ö
Mặt khác: 22 2 6,4molNaOH 2 d 2 2 CHONNa:0,25mol CHON:0,25mol CH:0,5mol CH:0,5mol NaOH:0,15mol HO:0,025mol HO:0,025mol ö
mol Muối +H2O 3
0,05 0,15 0,05 mol Muối +H2O 4 C4NaOH 0,05 0,2 0,05 mol 2 NaOH HO n0,55mol,n0,2mol Thu được 0,25 mol muối glyxin (M = 97); 0,2 mol muối alanin (M = 111); 0,1 mol muối valin (M = 139). m0,25970,11110,113960,35gam muoá i Bảo toàn khối lượng: 2 ENaOH HOmmmm muoá i E m0,554060,350,218 =41,95gam E m60,350,2.180,55.40 Nếu đốt cháy41,95gamE:
a0,05 Phương trìnhhoá học: Muối +H2O 2 A2NaOH
0,1 0,2 0,1
B3NaOH
Bảo toànnguyên tố C: 2COCGlyAlaVal E nn2n3n5n1,6mol
Bảo toànnguyên tố N: 2 NGlyAlaVal N nnnn0,55moln0,275mol
CácpeptittrongE đều tạo từ các -aminoaxitno, chứa một nhómCOOHvà một nhómNH2 Tacó: 2 22 HOCONE nnnn1,60,2750,21,525mol Tổng khối lượng CO2 vàH2O bằng: 1,6.441,525.1897,85gam Khi đốt cháymgamEthu được 22 COHO mm39,14gam Tacó:41,95gamE 97,85gamCO2 vàH2O ot mgamE 39,14gamCO2 vàH2O ot 39,14 m41,9516,78gam 97,85 Chọn A. Ví dụ 3: Đun nóng 0,14 mol hỗn hợp A gồm hai peptit X (CxHyOzN4) và Y (CnHmO7Nt) với dung dịch NaOH vừa đủ chỉ thu được dung dịch chứa 0,28 mol muối của glyxin và 0,4 mol muối của alanin. Mặt khác đốt cháymgamAtrongO2 vừa đủ thu được hỗn hợp CO2,H2OvàN2,trong đó tổng khối lượng của CO2 và nước là63,312gam.Giá trị m gần nhất với
A. 28. B. 34. C. 32. D. 18. Hướng dẫn giải Đun nóngA với dung dịch NaOH vừa đủ: Quy đổi A gồm CHON(xmol),CH2 (ymol)vàH2O(0,14mol). Tacó:
DẠYKÈMQUYNHƠN
Trang18
OFFICIAL
Bảo
2
A
Nếu đốt cháy0,14molA: Tacó: 2 2 2 2 2 CHON0,68molCO CH1,08molHO NHO0,14mol Bảo toànnguyên tố C: 2CO n0,681,081,76mol Bảo toànnguyên tố H: 2 HO 0,681,08.20,14.2 n 1,56mol 2 Tổng khối lượng CO2 vàH2Olà: 1,76441,5618105,52gam Đốt cháymgamAthu được tổng khối lượng của CO2 và nước là63,312gamnêntacó: 46,8863,312 m128,128gam 05,52
N242 aOH 2 362 CHONNa0,28molCHON(xmol) CHymolCHONNa0,4mol
toànnguyên tố N: x0,280,40,68mol
Bảo toànnguyên tố C:
CH n0,2820,430,681,08mol
m0,68.431,08.140,14.1846,88gam
Chọn A.
Bài tập tự luyện dạng 3
Bài tập cơ bản
Câu 1: Peptit X mạch hở được tạo bởi glyxin và alanin. Đốt cháy hoàn toàn 0,1 mol X bằng lượng oxi vừa đủ, sản phẩm cháy gồm CO2,N2 và1,15molH2O. Số liên kết peptitcótrongXlà A. 3. B. 4. C. 5. D. 2.
Câu 2: Peptit X có mạch hở được tạo thành từ các aminoaxit chỉ chứa một nhóm NH2 và một nhóm
m4 m3
COOH.Trongphân tử có tỉ lệ khối lượng Số liên kết peptittrongphân tử Xlà O N
OFFICIAL
A. 3. B. 4. C. 5. D. 6. Bài tập nâng cao Câu 3: Cho hỗn hợp X gồm các peptit mạch hở, đều được tạo thành từ các amino axit có dạng H2NCnHmCOOH. Đun nóng 4,63 gam X với dung dịch KOH dư, thu được dung dịch chứa 8,19 gam muối. Nếu đốt cháyhoàntoàn4,63gamX cần 4,2lítO2 (đktc). Dẫn toàn bộ sản phẩm cháy(CO2,H2O, N2)vàodung dịch Ba(OH)2 dư, sau phản ứng thu được mgam kết tủa. Giá trị của m gần nhất với giá trị nàosau đây?
A. 30. B. 28. C. 35. D. 32. Câu 4: Đun nóng 0,4 mol hỗn hợp E gồm đipeptit X, tripeptit Z đều mạch hở bằng lượng vừa đủ dung dịch NaOHthu được dung dịch chứa 0,5mol muối của glyxin;0,4mol muối của alaninvà0,2mol muối của valin. Mặt khác, đốt cháy m gam E trong oxi vừa đủ thu được hỗn hợp CO2; H2O và N2. Trong đó tổng khối lượng của CO2 vàH2Olà78,28gam.Giá trị của m gần nhất với
A. 55,6. B. 45,1. C. 43,2. D. 33,5. Câu 5: Hỗn hợp P gồm haipeptit mạch hở: X(CnHmN7O8)vàY(CxHyN4O5). Đốt cháyhoàntoàn13,29 gam hỗn hợp P cần dùng vừa đủ 13,104lítkhíO2 (đktc) thu được khíCO2,H2Ovà2,24lítkhíN2 Thuỷ phân hoàn toàn 13,29 gam P trong dung dịch NaOH dư thu được m1 gam muối glyxin và m2 gam muối của alanin.Giá trị của m1 là
A. 10,67. B. 10,44. C. 8,73. D. 12,61. Câu 6: Cho m gam hỗn hợp A gồm đipeptit X, tripeptit Y, tetrapeptit Z và pentapeptit T (đều mạch hở) tác dụng với dung dịch NaOH vừa đủ, thu được hỗn hợp B gồm các muối của Gly, Ala, Val. Đốt cháy hoàntoànB bằng lượng oxi vừa đủ, thu lấy toàn bộ khívà hơi đem hấp thụ vàobình đựng nước vôitrong dư, thấy khối lượng bình tăng 13,23gamvàcó0,84lítkhí (đktc) thoátra. Mặt khác, đốt cháyhoàntoàn mgamA,thu được 4,095gam nước. Giá trị của m gần nhất với giá trị nàosau đây? A. 6,0. B. 6,6. C. 7,0. D. 7,5. Câu 7: Hỗn hợp X gồm các peptit mạch hở và các amino axit (các amino axit tự do và amino axit tạo peptit đều có dạng H2NCnH2nCOOH). Thuỷ phânhoàntoànmgamXtrongdung dịch NaOH, đun nóng, thấy có1,0molNaOH đã phản ứng vàsau phản ứng thu được 118gam hỗn hợp muối. Mặt khác, đốt cháy
DẠYKÈMQUYNHƠN
Trang19
hoàntoànmgamX bằng oxi,sau đó cho sản phẩm cháy hấp thụ hết bởi nước vôitrong dư, thu được kết tủa và khối lượng dung dịch nước vôitrong giảm 137,5gam.Giá trị của mlà
A. 82,5. B. 74,8. C. 78,0. D. 81,6. Câu 8: Chia m gam hỗn hợp T gồm các peptit mạch hở thành hai phần bằng nhau. Đốt cháy hoàn toàn phần một, thu được N2,CO2 và7,02gamH2O. Thuỷ phânhoàntoàn phần hai,thu được hỗn hợp X gồm alanin, glyxin, valin. Cho X vào 200 ml dung dịch NaOH 0,5M và KOH 0,6M, thu được dung dịch Y chứa 20,66gam chất tan. Để tác dụng vừa đủ với Y cần 360mldung dịch HCl1M. Biết các phản ứng xảy rahoàntoàn.Giá trị của mlà
A. 21,32. B. 24,20. C. 24,92. D. 19,88. Dạng 4: Các hợp chất chứa N khác
Phương pháp giải Chất hữu cơ chứa Ntác dụng với NaOHcó thể là:
Aminoaxit:H2N–R–COOH
OFFICIAL
Peptit:H2N–R–CONH–R–CO–…–NH–R–COOH
Este của aminoaxit:H2N–R–COOR’(ví dụ: H2N–R–COOCH3)
Muối amoni:RCOONH3R’(ví dụ: HCOONH3CH3)
Muối nitrat hoặc cacbonat: Nếu hợp chất hữu cơ có dạng CxHyO3N2 thì: 33 323 233 333
DẠYKÈMQUYNHƠN
Trang20
oC)thu được chất rắn B,khíClàm xanh quỳ tím ẩm. Đun B với NaOH rắn được CH4.Công thức cấu tạo của Xlà A. C2H5COONH4. B. CH3COONH3CH3. C. H2NCH2COOCH3. D. HCOONH3C2H5. Hướng dẫn giải Đun B với NaOH rắn thu được CH4 Công thức của BlàCH3COONa. oCaO,t 3 423 CHCOONaNaOHCHNaCO Cấu tạo của X chỉ có thể làCH3COONH3CH3. Phương trìnhhoá học: o tC 333 3 322 CHCOONHCHNaOHCHCOONaCHNHHO (X) (B) (C)
RNHNO k0(RNH)CO HNRNHHCO k1RNHCONHR amonivoøng
Nếu hợp chất hữu cơ có dạng CxHyO3NthìRNH3HCO3 Chú ý: Ở điều kiện thường, khílàmxanh quỳ tím ẩm thường làNH3 và bốn aminCH3NH2,C2H5NH2, (CH3)2NH,(CH3)3N. Ví dụ mẫu Ví dụ 1: Chất Xcócông thức C3H9O2N.ChoXtác dụng với NaOH(t
KhíClàmetylaminnênlàmxanh quỳ tím ẩm. Chọn B. Ví dụ 2: Một chất hữu cơ Xcócông thức phân tử C2H8O3N2 Lấy mgamXcho phản ứng hết với 200ml dung dịch NaOH1M.Cô cạn dung dịch sau phản ứng thu được 14,75gam chất rắn gồm các chất vô cơ. Giá trị của mlà A. 18,8. B. 9,4. C. 4,7. D. 16,2. Hướng dẫn giải Xtác dụng với NaOH tạo ra chất vô cơ nênXcócông thức C2H5NH3NO3 (xmol). Phương trìnhhoá học:
Chọn D.
Ví dụ 3: Hỗn hợp X gồm hai chất có công thức phân tử là C3H12N2O3 và C2H8N2O3. Cho 3,40 gam X phản ứng vừa đủ với dung dịch NaOH đun nóng, thu được dung dịch Y chỉ gồm các chất vô cơ và 0,04 mol hỗn hợp hai chất hữu cơ đơn chức (đều làmxanh giấy quỳ tím ẩm). Cô cạn Ythu được mgam muối khan.Giá trị của mlà A. 3,36. B. 3,12. C. 2,97. D. 2,76. Hướng dẫn giải X phản ứng với NaOH đun nóng, thu được dung dịch Y chỉ gồm các chất vô cơ và hỗn hợp hai chất đơn chức (đều làmxanh quỳ tím ẩm) nêncông thức cấu tạo của X lần lượt là:(CH3NH3)2CO
DẠYKÈMQUYNHƠN OFFICIAL Trang21
2533 32522 CHNHNONaOHNaNOCHNHHO X x x
Tacó: 3 NaNONaOHmmmdö chaátraénvoâcô
3 (amol)và C2H5NH3NO3 (bmol). 124a108b3,4* Phương trìnhhoá học: 333 23322 2 CHNHCO2NaOHNaCO2CHNH2HO a a 2a mol 2533 32522 CHNHNONaOHNaNOCHNHHO b b b mol 2ab0,04** Từ (*)và(**)suyra: a0,01;b0,02 Muối khansau phản ứng gồm 0,01molNa2CO3 và0,02molNaNO3 gam m0,01.1060,02.852,76 Chọn D.
mol
14,7585x40.0,2x
x0,15
gam m0,15.10816,2
Bài tập tự luyện dạng 4 Bài tập cơ bản Câu 1: A là hợp chất có công thức phân tử CH6O3N2. Cho A tác dụng với NaOH thì thu được khí B và các chất vô cơ. Công thức khíBlà
A. CO. B. CH3NH2. C. NH3. D. CO2. Câu 2: Ứng với công thức phân tử C2H7O2N số chất vừa phản ứng được với dung dịch NaOH, vừa phản ứng được với dung dịch HCllà
A. 4. B. 2. C. 1. D. 3. Câu 3: Cho các chất sau: ClH3NCH2COOH; CH3COOH, CH3CH2NH2; CH3COOH3NCH3; C6H5NH2; H2NCH2COOCH3. Số chất vừa tác dụng với NaOH, vừa tác dụng với HCllà
A. 4. B. 3. C. 2, D. 5. Câu 4: Cho chất hữu cơ X có công thức phân tử C2H7O3N tác dụng với dung dịch NaOH dư, thu được chất hữu cơ đơn chức Yvàcác chất vô cơ. Khối lượng phân tử theo đvC của Ylà
OFFICIAL
A. 68. B. 45. C. 46. D. 31. Câu 5: Cho muối X có công thức phân tử C3H12N2O3. Cho X tác dụng hết với dung dịch NaOH đun nóng, sau phản ứng thu được hỗn hợp khí Z có khả năng làm quỳ ẩm hoá xanh và muối axit vô cơ. Số công thức cấu tạo của X thoả mãn điều kiện trênlà
A. 3. B. 2. C. 5. D. 4. Câu 6: Cho 0,1 mol chất X có công thức là C2H12O4N2S tác dụng với dung dịch chứa 0,35 mol NaOH đun nóngthu được chất khílàmxanh giấy quỳ ẩm vàdung dịch Y.Cô cạn dung dịch Y,thu được mgam chất rắn khan.Giá trị của mlà
A. 16,0. B. 20,2. C. 26,4. D. 28,2. Câu 7: Chất Acócông thức phân tử làC2H7O2N.Cho7,7gamAtác dụng với 200mldung dịch NaOH 1Mthu được dung dịch XvàkhíY, tỉ khối của Yso với H2 nhỏ hơn 10.Cô cạn dung dịch Xthu được m gam chất rắn. Giá trị của mlà
A. 12,20. B. 14,60. C. 18,45. D. 10,70. Câu 8: Hỗn hợp X gồm chất Y (C2H10O3N2) và chất Z (C2H7O2N). Cho 14,85 gam X phản ứng vừa đủ với dung dịch NaOH và đun nóng, thu được dung dịch M và 5,6 lít (đktc) hỗn hợp T gồm hai khí (đều làmxanh quỳ tím ẩm). Cô cạn toàn bộ dung dịch Mthu được mgam muối khan.Giá trị lớn nhất của mlà A. 11,8. B. 12,5. C. 14,7. D. 10,6. Bài tập nâng cao Câu 9: Hỗn hợp E gồm muối vô cơ X (CH8N2O3) và đipeptit Y (C4H8N2O3). Cho E tác
DẠYKÈMQUYNHƠN
Trang22
NaOH đun nóng,thu được khíZ.ChoEtác
cơ Q.Phát biểu nàosau đây sai? A. Chất YlàH2NCH2CONHCH2COOH. B. Chất QlàH2NCH2COOH. C. Chất ZlàNH3 và chất TlàCO2 D. Chất
2CO3
dụng với dung dịch
dụng với dung dịch HCl dư, thu được khíTvà chất hữu
Xlà(NH4)
Câu 10: Cho hỗn hợp X gồm muối A(C5H16O3N2)vàB(C4H12O4N2)tác dụng với một lượng dung dịch NaOH vừa đủ, đun nóng đến khi phản ứng xảy rahoàntoàn rồi cô cạn thu được mgam hỗn hợp Y gồm hai muối DvàE(MD <ME)và4,48lít hỗn hợp Z gồm haiaminno, đơn chức đồng đằng kế tiếp có tỉ khối hơi đối với H2 là18,3. Khối lượng của muối Etrong hỗn hợp Ylà A. 3,18gam. B. 8,04gam. C. 4,24gam. D. 5,36gam.
ĐÁP ÁN BÀI TẬP
Dạng 1: Lí thuyết trọng tâm
1 - D 2 - D 3 - D 4 - A 5 - A 6 - D 7 - D 8 - D 9 - A 10 - D 11 - B 12 - A 13 - D 14 - A 15 - C 16 - C 17 - C 18 - A 19 - A 20 - C Câu 1:
OFFICIAL
Đipeptit được tạo thành từ 2 -aminoaxit bằng 1liên kết peptit. Alàtripeptit. B,Ckhông phải làpeptitdocó gốc không phải là -aminoaxit. Dlà đipeptit. Câu 2: Tripeptitlà hợp chất màphân tử có3 gốc -aminoaxitvà số liên kết peptit:3–1=2. Câu 4: Thuốc thử dùng để phân biệt Gly-AlavàGly-Gly-Gly-AlaCu(OH)2 trongmôi trường kiềm: +Gly-Gly-Gly-Alalàtetrapeptitnêncó phản ứng màubiure với Cu(OH)2 tạo phức màutím. +Gly-Alakhôngcó hiện tượng gìvì đipeptit khôngcó phản ứng màubiure với Cu(OH)2/OH Câu 6:
Anbumincótronglòng trắng trứng, là một loại proteinnêncó phản ứng màubiure. Câu 7: Từ glyxin(Gly)vàalanin(Ala)có thể tạo ra số đipeptit là:22 =4hay: Gly-Gly;Ala-Ala,Gly-Ala,Ala-Gly Câu 8:
A,B,C đúng. TripeptithoàtanCu(OH)2 (phản ứng màubiure) tạo phức màutím. Câu 10:
A,B,C đúng. Dsaivìtrongphân tử đipeptit có2 gốc -aminoaxitvàcó2–1=1liên kết peptit. Câu 11: A,C,D đúng. Bsaivìkhông phải tất cả proteintantrong nước đều tạo dung dịch keo. Câu 12: Khi thuỷ phânkhônghoàntoànXthu được cácpeptitcóaminoaxit đầu Nlàphenylalanin(Phe)là: Phe-Ser;Phe-Ser-Phe;Phe-Ser-Phe-Pro;Phe-Pro Câu 13:
DẠYKÈMQUYNHƠN
Trang23
Xenlulozơ làpolisaccaritkhôngcó phản ứng với NaOH đun nóng. Axit aminoaxetic là amino axit, Ala-Gly-Glu là peptit, etyl propionat là este nên đều có phản ứng với dung dịch NaOH đun nóng. Câu 14: Xtác dụng được với Cu(OH)2 trongmôi trường kiềm tạo dụng dịch màutím Xlàlòng trắng trứng. Loại C,D. Z đun nóng với dung dịch NaOHloãng (vừa đủ) rồi thêm tiếp dung dịch AgNO3 trongNH3, đun nóng tạo kết tủa AgnênZlàvinylaxetat.
Vậy Xlàlòng trắng trứng, Ylàtriolein,Zlàvinylaxetat,Tlà hồ tinh bột. Câu 15: Phương trìnhhoá học: 22 3 2 232 3 3 HNCHCONHCH(CH)CONHCHCOOH3HCl2HO2ClHNCHCOOHClHNCH(CH)COOH
Câu 16: Xlà một tetrapeptit được tạo từ 1Gly+3Ala+1Val. Số đồng phân cấu tạo của peptitXlà: 4! 12 2 Câu 17: Tacó: 2352 235 22 NHCH(COOH)2NaOHNHCH(COONa)2HO
Gly-Alalà đipeptit nêntác dụng với NaOHtheo tỉ lệ mol1:2 Câu 18: Xét chất đại diện làGly-Gly-Gly-Gly-Gly, chất nàycócông thức phân tử làC10H17O6N5. Đáp ánAphù hợp với công thức phân tử.
Câu 19: PeptitXcó thể viết lại dưới dạng: A-B-B-B-A
Peptit có phản ứng màu biure phải là peptit từ tripeptit trở đi nên các peptit thu được có phản ứng màu biurelà:A-B-B;B-B-B;B-B-A;B-B-B-A;A-B-B-B
Câu 20:
(a)saivìtrong một phân tử tetrapeptit mạch hở có:4–1=3liên kết peptit. (b) đúng vìlysincó số nhómNH2 > số nhómCOOHnênlàmxanh quỳ tím. (c) đúng vìanilintác dụng với nước brom tạo thành2,4,4-tribromanilin (kết tủa trắng). (d)saivì đipeptit khôngcó phản ứng màubiure với Cu(OH)2 (e) đúng vìproteinlàpolipeptit, thuỷ phânhoàntoànthu được các -aminoaxit. (f)saivìcác hợp chất peptitkém bền trong cả môi trường axit lẫn bazơ. Dạng 2: Phản ứng thuỷ phân
DẠYKÈMQUYNHƠN OFFICIAL Trang24
33
3 2 3 3 CHCOOCHCHNaOHCHCOONaCHCHO
AgNO/NH 3 CHCHO2Ag
32 22 2 ClHNCHCOOH2NaOHHNCHCOONaNaCl2HO
1 - C 2 - C 3 - C 4 - D 5 - D 6 -
7 -
8 - D 9 - C 10 -
11 - A 12 - C 13 - B 14 - A 15 - C 16 -
17 -
18
19
C
A
A
C
D
- A
- C 20 - D
Câu 1:
Gọi công thức của XlàaGly-bAla. Phương trìnhhoá học: oH,t 2 22 32 aGlybAlaab1HOaHNCHCOOHbCHCH(NH)COOH Ala Gly a0,753n0,25mol;n0,75mol 1 b0,251
Bảo toàn khối lượng: 2 2 HOGlyAlaX HO a0,75mmmm13,5gamn0,75mol 12 ab10,75
Từ (1)và(2)suyra: a3,b1 Xlàtetrapeptit. Câu 2: Công thức peptitX:Alan. Số liên kết peptit:n–1 Tacó: Mn89n118302n4 PeptitX thuộc loại tetrapeptit. Câu 3: Tacó: Ala polipeptit 170 500n1,91mol;n 0,01mol 89 50000 0,01molpolipeptit chứa 1,91molalanin 1molpolipeptit chứa 191molalaninhay1polipeptit chứa 191 mắt xíchalanin. Câu 4: peptit M146n0,1mol Phương trìnhhoá học: Muối 2 2 A2HClHO 0,1 0,2 0,1 mol Bảo toàn khối lượng:
DẠYKÈMQUYNHƠN
Trang25
OFFICIAL
i m14,60,236,50,11823,7gam muoá i Câu
AlaGlyAla n0,06mol
+H2O 3
0,06 0,18 mol =90ml V0,180,09lít 2 Câu 7: GlyAlaValGly n0,02mol Phương trìnhhoá
42 X3HO4HCl 0,02
mol Bảo toàn
2
Câu
GlyGly KOH n0,03mol;n0,075mol
2 peptitHClHO mmmmmuoá
5:
Phương trìnhhoá học: Muối
A3NaOH
học: Muối
0,06 0,08
khối lượng:
YGlyAlaValGlyHClHO mmmm10,04gam
8:
Phương trìnhhoá học: Muối +H2O GlyGly2KOH 0,03 0,075 0,03 mol Bảo toàn khối lượng: 2 peptitKOHHO mmmm3,960,075.560,03.187,62gam chaátraé n
Câu 9: Ala Gly n0,32mol;n0,4mol
Gọi số mol của XvàY lần lượt làavàbmol. Tacó: 2ab0,32a0,12mol 2a2b0,4b0,08mol
Câu 10: KOH n0,3mol
Phương trìnhhoá học: Muối +H2O 2 A2KOH 0,1 0,3 0,1 mol Bảo toàn khối lượng: 2 peptitKOHHO mmmm0,1.1460,3.560,1.1829,6gam chaátraé n
Câu 11: Gly GlyGly GlyGlyGly n0,32mol;n0,2mol;n0,12mol Gọi số mol của Gly-Gly-Gly-Glylàxmol. Bảo toàn gốc Gly: 4x0,320,220,123 x0,27 m0,27.24666,42 Câu 12: Gly Ala Val n0,06mol;n0,04mol;n0,02mol
Thuỷ phân không hoàn toàn X thu được tripeptit Ala-Val-Gly và đipeptit Gly-Ala, không thu được đipeptit Ala-Glynêncông thức cấu tạo của Xlà:Gly-Ala-Val-Gly-Gly-Ala. Câu 13: Gọi
DẠYKÈMQUYNHƠN OFFICIAL Trang26
m0,12.4720,08.30280,8gam
Phương trìnhhoá học: Muối 2 2 A2HClHO x 2x x mol Muối 3 2 A3HCl2HO y 3y 2y mol Bảo toàn khối lượng: 2 HClHO mm59,9536,323,65gam 91x145,5y23,65** Từ (*)và(**)suyra: xy0,1 Phần trăm số mol của Ala-GlytrongXlà: 0,1.100%50% 0,10,1 Câu 14:
số mol của Ala-GlyvàAla-Gly-Ala lần lượt làx,ymol.
146x217y36,3*
Thuỷ phânXthu được: Ala-Gly-Gly (0,015 mol); Gly-Val (0,02 mol); Val-Ala (x mol); Gly (0,1 mol); Val (0,02 mol); Ala (y mol). Công thức pentapeptitXcó dạng Ala-Gly-Gly-Val-Ala.
Bảo toàn gốc Gly: X GlyX n2.0,0150,020,10,15moln0,075mol
Bảo toàn gốc Val: 0,02x0,020,075x0,035mol
Bảo toàn gốc Ala: 0,015xy20,075y0,150,0150,0350,1mol
Tỉ lệ: x:y=0,035:0,1=7:20
Câu 15: Gly Val n0,5mol;n0,3mol Gọi số molAla-Val-Ala-Gly-AlavàVal-Gly-Gly lần lượt làx,ymol. Bảo toàn gốc -aminoaxittacó: Ala-Val-Ala-Gly-Ala 3Ala+Gly+Val x 3x x x mol
Val-Gly-Gly 2Gly+Val y 2y y mol Tacó hệ phương trình: x2y0,5x0,1 xy0,3y0,2
m0,1.3870,2.23184,9gam
x30,18926,7gam
Câu 16: Gọi số mol của Xlàxmol. Phương trìnhhoá học: Muối +H2O 4 A4NaOH x 4x x mol Bảo toàn khối lượng: 6,04404x8,8818x x0,02mol Phương trìnhhoá học: Muối 4 2 A4HCl3HO 0,02 0,08 0,06 mol Bảo toàn khối lượng: m6,040,0836,50,061810,04gam muoá i
DẠYKÈMQUYNHƠN
Trang27
OFFICIAL
2 2 HO HO mm0,140m3,460,54gamn0,03mol Tacó: NaOH COO nn0,1moln0,2mol Otrongmuoá i trongmuoá i Bảo toànnguyên tố O: 2 OXONaOH OHO O nnnn trongmuoá i OX n0,20,030,10,13mol X m0,1316:29,379%7,08gam Câu 18:
Câu 17: Bảo toàn khối lượng:
Tổng số mắt xích= Ala Gly n0,18mol;n0,29molGly:Ala29:18 * 2918k47kkN. Gọi số gốc aminoaxittrongX,Y,Z lần lượt làa,b,c 2a3b4c47 Bảo toànnguyên tố N: 2a3b4cx0,47molx1 Quátrình phản ứng: Aminoaxit 2 Xa1HO Aminoaxit 2 Yb1HO Aminoaxit 2 Zc1HO Tacó: 2
Câu 20: Gọi số mol của XvàY lần lượt làx,ymol.
DẠYKÈMQUYNHƠN OFFICIAL Trang28
xy0,2* Thuỷ phânhoàntoàn0,2molEtrongdung dịch NaOH dư: Muối +H2O 3 A3NaOH x 3x x mol Muối +H2O 4 A4NaOH y 4y y mol Bảo toàn khối lượng: E m76,25102x142ygam Thuỷ phânhoàntoàn0,2molEtrongdung dịch HCl dư: Muối 3 2 A3HCl2HO x 3x 2x mol Muối 4 2 A4HCl3HO y 4y 3y mol Bảo toàn khối lượng: E m87,125145,5x200ygam Tacó phương trình: 76,25102x142y87,125145,5x200y 43,5x58y10,875**
HO n2xa13xb14xc1
2ax3bx4cx9x0,479.0,010,38mol
Bảo toàn khối lượng: 2 A HO mmm21,7516,020,38.1830,93gam aminoaxit
Câu 19: Gọi công thức của Ylà n2n12 CHNOn2 Tacó: Công thức của XlàC3H7NO2 (Ala). ON 46 %m100%51,685n3 14n47
tetrapeptit tripeptit Y n0,1mol;n0,13mol;n0,16mol;n0,99mol. ñipeptit Bảo toànnhómAla: pentapeptit 0,1.40,13.30,16.20,99 n 0,42mol 5
m0,42373156,66gam
Từ (*)và(**)suyra: x0,05;y0,15
E gồm: Xlà(Gly)n(Ala)3-n vàYlà(Gly)m(Ala)4-m. Gly n0,5mol0,05n0,15m0,5n3m10
(thoả mãn) n1;m3
Công thức của XlàGly(Ala)2 vàYlà(Gly)3Ala. X %m21,76%22%
Dạng 3: Phản ứng đốt cháy 1 - B 2 - C 3 - D 4 - D 5 - A 6 - A 7 - A 8 - A
Câu 1:
Gọi công thức peptitlà(Gly)x(Ala)y Tacó:(Gly)x(Ala)y =xGly+yAla–(x–y–1)H2O Glyxincó5H,alanincó7H: Số Htrongpeptit=5x+7y–2.(x–y–1)=3x+5y+2
Bảo toànnguyên tố H: 0,1.3x5y21,15.2 3x5y21
(thoả mãn) x2;y3 Số liên kết peptittrongXlà:2+3–1=4.
Câu 2:
m16k144 k6 m314k3 CHONxmolCHONKxmol CHymolCHymol 99x14y8,19** Đốt cháyX: o o
43x14y18z4,63*
t 2 22 2 t 22 22
Vậy trongXcó5liên kết peptit. Câu 3: Quy đổi X gồm CHON(xmol),CH2 (ymol)vàH2O(zmol). CHON0,75OCO0,5HO0,5N CH1,5OCOHO 0,75x1,5y0,1875*** Từ (*),(**)và(***)suyra: x0,07;y0,09;z0,02 Bảo toànnguyên tố C: 2CO nxy0,16mol 3BaCO mm0,16.19731,52gam Câu 4: Đun nóng0,4molE: Quy đổi E gồm CHON(xmol),CH2 (ymol)vàH2O(0,4mol).
DẠYKÈMQUYNHƠN
Trang29
OFFICIAL
Gọi công thức tổng quát của peptit được tạo từ k mắt xíchlà:CnH2n+2 – kOk+1Nk Tacó: O N Đun nóngX với KOH dư: 22KOH 2 2
toànnguyên tố
toànnguyên tố
nx0,5.10,4.10,2.11,1mol
Tổng khối lượng CO2 vàH2Olà: 3,2443,0518195,7gam
DẠYKÈMQUYNHƠN OFFICIAL Trang30
2 2 O N
Sơ
2 2 0,585molO 2 2 2 2 CHON0,2molCO0,2ymol CHymol HO0,1yzmol HOzmol N0,1mol Bảo
khối
22 COHO mm13,290,585320,12829,21gam 440,2y180,1yz29,21** Từ (*)và(**)suyra: y0,29;z0,035 Thuỷ phânhoàntoàn13,29gamPtrongdung dịch NaOH dư: Tacó: N242 aOH 2 362 CHON0,2molCHONNaamol CH0,29molCHONNabmol Bảo toànC,Ntacó hệ phương trình: ab0,2a0,11 2a3b0,49b0,09 1 m0,11.9710,67gam Câu 6: Quy đổi hỗn hợp A gồm CHON(amol),CH2 (bmol)vàH2O(cmol). Tacó sơ đồ: 2 23 22 O2 NaOH 2 2 2 2 2 NaCO:0,5amol CHON:amol CHONNa:amolCO:0,5abmolCH:bmolB CH:bmol HO:abmol HO:cmol N:0,5a0,0375a0,075 Tacó: m44.0,5.0,075b18.0,075b13,23b0,165 bìnhtaêng
Bảo
N: CHON
Bảo
C: 2CH ny0,520,430,251,12,1mol E m1,1.432,1.140,4.1883,9gam Nếu đốt cháy0,4molE: 2 2 2 2 2 CHON1,1molCO3,2mol CH2,1molHO3,05mol NHO0,4mol
Đốt cháymgamEthu được tổng khối lượng CO2 vàH2Olà78,28gam 83,978,28 m133,56gam 95,7
Câu 5: Quy đổi hỗn hợp P gồm CHON(xmol),CH2 (ymol),H2O(zmol). 43x14y18z13,29*
Đốt cháy13,29gam hỗn hợp P:
n0,585mol;n0,1mol
Bảo toànnguyên tố N: x2.0,10,2mol**
đồ:
toàn
lượng:
DẠYKÈMQUYNHƠN OFFICIAL Trang31 Bảo
Câu 7: Quy
Sơ đồ: 221molNaOH 2 2 CHON1molCHONNa1mol CH CH 2 2 CH CH m11818335gamn2,5mol Khi đốt cháyhoàntoàn hỗn hợp Xthìtacó: 2 1molNaOH 2 2 2 2 CHON1molCO CH2,5molHO N HOxmol Bảo toànnguyên tố C: 2CO n3,5mol Bảo toànnguyên tố H: 2 HO n3xmol Khi
32 3 CaCOCO CaCO
3 22 2 ddCaCOCOHO HO
giaûm 2 HO
n2 2n1 CHONn2. Coidung dịch Y gồm X(Ala,Gly,Val),NaOH,KOHtác dụng vừa đủ với 0,36molHCl. XNaOHKOHHClX nnnnn0,360,10,120,14mol Tacó:0,14molX(Ala,Gly,Val) 0,1molNaOH 20,12molKOHYHO 2 HOX nn0,14mol Bảo toàn khối lượng: 2 XNaOHKOH HOmmmmm chaátraé n X X m20,660,14180,1400,125612,46gamM89n3 Công thức phân tử của XlàC3H7NO2 (0,14mol). *Xét phần (1): 2 HO H1 n0,39moln0,78mol Bảo toànnguyên tố C: 2 COC1CX nnn0,14.30,42mol
toànnguyên tố H: 0,5.0,0750,165c0,2275c0,025
m0,075.430,165.140,025.185,985gam6gam
đổi hỗn hợp XthànhCHON,CH2,H2O(xmol). Tacó: CHONNaOH nn1mol
sục sản phẩm cháyvàodung dịch Ca(OH)2 dư:
nn3,5molm350gam
mmmm137,5gamm58,5gam
n3,25mol
x0,25mol
X m1.432,5.140,25.1882,5gam Câu 8: * Xét phần (2) Trong X đều là các -amino axit chứa một nhóm COOH và một nhóm NH2 nên có công thức phân tử chunglà
Bảo toànnguyên tố N: 2N N1NX N1 1 nn0,14.10,14molnn0,07mol 2
T được tạo từ các -aminoaxitnêncó: 2 22 HOCONTT nnnnn0,390,420,070,04mol TO1N1 nnn0,140,040,18mol Bảo toàn khối lượng: TCHON mmmmm20,42120,780,18160,141421,32gam Dạng 4: Các hợp chất chứa N khác 1 - D 2 - B 3 - C 4 - D 5 - B 6 - B 7 - A 8 - C 9 - B 10 - B Câu 1: AlàCH3NH3NO3. Phương trìnhhoá học: 333 3232 CHNHNONaOHCHNHNaNOHO Câu 2: Các chất thoả mãn:CH3COONH4 vàHCOONH3CH3 Câu 3: Có hai chất vừa tác dụng được với NaOH, vừa tác dụng được với HCl là CH3COOH3NCH3; H2NCH2COOCH3 Câu 4: X tác dụng với NaOH thu được chất hữu cơ Y và chất vô cơ, mà X có công thức phân tử dạng CnH2n+3O3N.SuyraXcócông thức cấu tạo CH3NH3HCO3 Phương trìnhhoá học: 333 32232 CHNHHCO2NaOHCHNHNaCO2HO (Y) Vậy Y M31 Câu 5: Cáccông thức cấu tạo thoả mãn điều kiện trênlà:C2H5NH3CO3NH4 và(CH3)2NH2CO3NH4 Câu 6: Công thức của Xlà(CH3NH3)2SO4 Phương trìnhhoá học: 3324 24322 (CHNH)SO2NaOHNaSO2CHNH2HO
DẠYKÈMQUYNHƠN OFFICIAL Trang32
0,1 0,2 0,1
Na
SO
Dung dịch Y gồm
2
4 (0,1mol);NaOH dư (0,15mol). m0,1.1420,15.4020,2gam
Câu 7: VìMY <20nênYlàNH3 Acó cấu tạo làCH3COONH4.
A NaOH n0,1mol;n0,2mol
Phương trìnhhoá học: 34 3 32 CHCOONHNaOHCHCOONaNHHO
0,1 0,1 0,1 mol X gồm NaOH(0,1mol)vàCH3COONa(0,1mol). m12,2gam raé n Câu 8: YlàCH3NH3 –CO3 –NH4 (ymol);ZlàHCOONH3CH3 hoặc CH3COONH4 (zmol). Tacó: 110y77z14,85y0,1 2yz0,25z0,05
Na2CO
COONH
Na2CO
(0,1mol)vàHCOONa(0,05mol)
đáp án.
(0,1mol)vàCH3COONa(0,05mol)
C.
DẠYKÈMQUYNHƠN OFFICIAL Trang33
2H5NH2
E
xy0,2* Tacó: 31x45y0,2.36,67,32** Từ (*)và(**)suyra: x0,12;y0,08 Ylà(C2H5NH3)2CO3 vàZlà(COOH3NCH3)2. Phương trìnhhoá học: 25323 232522 (CHNH)CO2NaOHNaCO2CHNH2HO 0,04 0,08 0,04 0,08 mol 332 2322 (COOHNCH)2NaOH(COONa)2CHNH2HO 0,06 0,12 0,06 0,12 mol Elà(COONa)2 DEMM E m0,06.1348,04gam
TH1:ZlàHCOONH3CH3 M gồm
3
khôngcó
m0,1.1060,05.6814gam TH2:ZlàCH3
4 M gồm
3
Chọn
m0,1.1060,05.8214,7gam Câu 9: Xlà(NH4)2CO3.YlàH2NCH2 –CONH–CH2COOH. Phương trìnhhoá học: 423 2332 (NH)CO2NaOHNaCO2NHHO (Z) 22 2 22 2 HNCHCONHCHCOOH2NaOH2HNCHCOONaHO 423 422 (NH)CO2HCl2NHClCOHO (T) 22 2 2 32 HNCHCONHCHCOOH2HClHO2ClHNCHCOOH (Q) Vậy BsaivìQlàClH3NCH2COOH. Câu 10: HaiaminlàCH3NH2 (xmol)vàC
(ymol).
M36,6
CHƯƠNG 4: POLIME
BÀI 7: POLIME
Mục tiêu
Kiến thức
+Trình bày được khái niệm, đặc điểm cấu tạo, tính chất vật lí (trạng thái, nhiệt độ nóng chảy, tính cơ học) của polime.
+Nêu được ứng dụng và một số phương pháp tổng hợp polime(trùng hợp, trùng ngưng).
+ Chỉ ra được khái niệm, thành phần chính, sản xuất và ứng dụng của: chất dẻo, tơ, caosu. Kĩ năng
+ Từ monome viết được công thức cấu tạo của polimevà ngược lại.
+ Viết được phương trìnhhóa học tổng hợp cácpolime, chất dẻo, tơ, caosuthông dụng.
+Phân biệt được polimethiênnhiên với polime tổng hợp hoặc nhân tạo.
+ Biết cách sử dụng và bảo quản được một số vật liệu polime trong đời sống. Giải được một số bài tập cóliênquan.
OFFICIAL
DẠYKÈMQUYNHƠN
Trang1
I. LÍ THUYẾT TRỌNG TÂM
A. ĐẠI CƯƠNG POLIME
1. Khái niệm
a. Khái niệm
Polimelà những hợp chất có phân tử khối rất lớn do nhiều đơn vị cơ sở (mắt xích) liên kết với nhau tạo nên.
Ví dụ: 22n (CHCH)
Hệ số nlà hệ số polimehóa( hoặc độ polimehóa).
b. Danh pháp
Tên của monome chỉ gồm một cụm từ: Tênpolime=Poli+tênmonome
Ví dụ: :Polietilen.22n (CHCH)
Tên của monome gồm hai cụm từ trở lên: Tênpolime=Poli+(tênmonome)
Ví dụ: :Poli(vinylclorua). 2 n(CHCHCl)
c. Phân loại Dựa vào nguồn gốc: Polimethiênnhiên:có sẵn trong tự nhiên.
Ví dụ: Xenlulozơ, tinh bột...
Polime tổng hợp: docon người tổng hợp.
Ví dụ: Polietilen, polibutađien,...
Polimebán tổng hợp: polimethiênnhiên được chế biến một phần.
Ví dụ: tơ visco, tơ axetat,...
Dựa vào đặc điểm cấu trúc:
Polime mạch khônggian.
Ví dụ: cao su lưu hóa, nhựa bakelit.
Polime mạch phânnhánh.
Ví dụ: aminlopectin, glicogen.
Polime mạch khôngphânnhánh.
Ví dụ: PE, PVC, amilozơ...
Dựa vào phương pháp tổng hợp:
Polimetrùng hợp.
Ví dụ: PE, PVC, cao su buna,...
Polimetrùng ngưng.
Ví dụ: tơ nilon-6, tơ lapsan,...
OFFICIAL
DẠYKÈMQUYNHƠN
Trang2
2. Tính chất vật lí
Hầu hết cácpolime đều là chất rắn, khôngbay hơi, khôngcó nhiệt độ nóng chảy xác định.
Đa số polimekhôngtantrongcácdungmôithông thường, một số tan được trongdungmôithích hợp tạo dung dịch nhớt.
Nhiều polimecótính dẻo, một số cótính đàn hồi, một số có thể kéothành sợi dai, bền...
3. Phương pháp điều chế
a. Phản ứng trùng hợp
Trùng hợp làquátrình kết hợp nhiều phân tử nhỏ (monome) giống hoặc tương tự nhauthànhphân tử lớn (polime).
Điều kiện về cấu tạo của monome:Cóliên kết bội hoặc cóvòngkém bền có thể mở ra.
Ví dụ: 222 CHCH;CHCHCl
b. Phản ứng trùng ngưng
Là quá trình kết hợp nhiều phân tử nhỏ (monome) thành phân tử lớn (polime) đồng thời giải phóng những phân tử nhỏ khác(...). 2 HO
OFFICIAL
Điều kiện về cấu tạo của monome:cóít nhất hainhóm chức có khả năng phản ứng.
Ví dụ: 2 2 CHOHCHCOOH
4. Ứng dụng
Làmcác loại vật liệu polime phục vụ cho sản xuất và đời sống.
B. VẬT LIỆU POLIME
1. Chất dẻo
a. Khái niệm
Chất dẻo là những vật liệu polimecótính dẻo.
b. Một số polime được dùng làm chất dẻo
Polietilen(PE): 22n (CHCH)
Chất dẻo mềm, nóng chảy ở trên110°C,cótính trơ.
Được dùnglàmmàng mỏng, vật liệu cách điện, bình chứa.
Poli(vinylclorua): 2 n(CHCHCl)
Chất rắn vô định hình,cách điện tốt, bền với axit.
Được dùnglàm vật liệu cách điện, ống dẫn nước, vải che mưa.
CHOOC | (CHC) | CH
Poli(metylmetacrylat): 3 2n 3
Chất rắn trong suốt, choánhsáng truyền tốt.
Được dùng để chế tạo thủy tinh hữu cơ plexiglas.
Poli(phenol-fomanđehit) (PPF):
DẠYKÈMQUYNHƠN
Trang3
Cóba dạng: nhựa novolac, nhựa rezol, nhựa rezit.
Được dùng để sản xuất bột ép, sơn.
2. Tơ
a. Khái niệm
Tơ là những vật liệu polimehình sợi dàivà mảnh với độ bền nhất định.
Phân loại:
Tơ thiênnhiên:có sẵn trongthiênnhiên.
Ví dụ: bông, len, tơ tằm...
Tơ hóa học: chế tạo thành phương pháphóa học.
+ Tơ tổng hợp: chế tạo từ cácpolime tổng hợp.
Ví dụ: tơ nilon, tơ capron... + Tơ bán tổng hợp (tơ nhân tạo): xuất phát từ polimethiênnhiên nhưng chế biến bằng phương pháphóa học.
OFFICIAL
Ví dụ: tơ visco, tơ xenluzơ axetat,... b. Một số loại tơ thường gặp Tơ nilon-6,6 Trùng ngưng hexametylenđiamin vàaxit ađipic:
Được dùng để dệt vải may mặc, bện dâycáp,dâydù, đan lưới. Tơ nitron(olon):Trùng hợp vinylxianua(hayacrilonitrin):
để dệt vải may quần áo ấm, hoặc bện thành sợi “len” đan áorét. 3. Cao su
DẠYKÈMQUYNHƠN
Trang4
t 2 2 2 2 2 2 n 2 6 6 4 nHNCHNHnHOOCCHCOOH(NHCHNHCOCHCO)2nHO (T¬nilon6,6)
t,p,xt 2 2 nnCHCHCN(CHCH) | CN T¬nitron Được dùng
a. Khái niệm Caosulà vật liệu polimecótính đàn hồi. Phân loại: Caosuthiênnhiên lấy từ mủ câycaosu. 2 3 2n(CHCCHCHCH) Caosu tổng hợp: vật liệu polime tương tự caosuthiênnhiên, thường được điều chế từ ankađien bằng phản ứng trùng hợp. b. Một số cao su tổng hợp
Caosubuna
buta1,3®ien caosubuna
Caosubunacótính đàn hồi và độ bền kémcaosuthiênnhiên.
Caosubuna-Svàcaosubuna-N
®ångtrïnghîp Buta1,3®ien+stiren CaosubunaS
®ångtrïnghîp Buta1,3®ien+acrilonitrin CaosubunaN
Caosubuna-Scótính đàn hồi cao. Caosubuna-Ncótính chống dầu khácao. SƠ ĐỒ HỆ THỐNG HÓA
Chú ý: Nếu tên của monome gồm hai cụm từ trở lênthìtên đó được đặt trong dấu ngoặc đơn. Ví dụ: 22n (CHCH):polietilen
2 n (CHCH):polivinylclorua | Cl 3. Tính chất vật lý Hầu hết polimelà chất rắn, khôngbay hơi, khôngcó nhiệt độ nóng chảy xác định, đa số polimekhông tantrongdungmôithông thường. Nhiều polimecótính dẻo, một số polimecótính đàn hồi, một số cótínhdai, bền, có thể kéothành sợi.
4. Phân loại
Dựa vào cấu trúc
Mạch phânnhánh
Ví dụ: amilopectin, glicogen.
Mạch khôngphânnhánh
Ví dụ: PE, PVC, amilozơ...
Mạch mạng khônggian
Ví dụ: cao su lưu hóa, nhựa bakelit.
Dựa vào nguồn gốc
Polimethiênnhiên
DẠYKÈMQUYNHƠN OFFICIAL Trang5 Na,t,p 2
2 2n
2
nCHCHCHCH(CHCHCHCH)
1.
t,xt,P 22
M¾
nCHCH(CHCH)HÖsèpolimehãa Monome
2.
ĐẠI CƯƠNG POLIME
Khái niệm
22n
txÝch
Polime
Danh pháp Tênpolime=Poli+tênmonome
Ví dụ: xenlulozơ, tinh bột... Polimenhân tạo (bán tổng hợp)
Ví dụ: tơ visco, tơ axetat...
Polime tổng hợp
Ví dụ: polietilen, polibutanđien...
5. Điều chế
Phản ứng trùng hợp Trùng hợp làquátrình kết hợp nhiều phân tử nhỏ (monome) giống hoặc tương tự nhauthànhphân tử lớn (polime).
Ví dụ:
t,xt,P 2 2 nnCHCH(CHCH) | | Cl Cl
Phản ứng trùng ngưng Làquátrình kết hợp nhiều phân tử nhỏ (monome)thànhphân tử lớn (polime) đồng thời giải phóng những phân tử nhỏ khác 2 HO
Ví dụ: trïngngngAxitaminocaproic t¬nilon6
VẬT LIỆU POLIME
1. Chất dẻo
Polietilen(PE) :Là chất dẻo mềm, nóng chảy trên ,cótính trơ. 22n (CHCH) 110C Ứng dụng: làmmàng mỏng, bình chứa,...
Poli(vinylclorua)(PVC) :Là chất rắn vô định hình,cách điện tốt, bền với axit. 2 n(CHCH) | Cl Ứng dụng : vật liệu cách điện, ống dẫn nước,...
CH | (CHC) | COOCH qua tốt gần 90%nêndùng chế tạo thủy tinh hữu cơ plexiglas. Teflon,poli(tetrafloetilen) :Làpolime nhiệt dẻo, cótính bền cao với cácdungmôi 22n (CFCF) vàhóa chất nêndùng để làm vỏ cách điện, chất chống dínhtráng phủ lên chảo, nồi,...
Caosuthiênnhiên(poliisopren)
DẠYKÈMQUYNHƠN
Trang6
OFFICIAL
Poli(metylmetacrylat)(PMMA) :Là chất rắn trong suốt, choánhsáng truyền 3 2n 3
Poli(phenol– fomanđehit) (PPF): Gồm 3 dạng: nhựa novolac, nhựa rezol, nhựa rezit. Nhựa novolacdùng sản xuất bột ép, sơn. 2. Cao su
2 2 3 n CHCCHCH | CH Lấy từ mủ
câycaosu.
Cótính đàn hồi, không dẫn điện và nhiệt, không thấm khívà nước, khôngtantrong nước, etanol, axeton,... nhưng tantrong xăng, benzen.
Caosu tổng hợp:
o Caosubuna: :Caosubunacótính đàn hồi, nhưng độ bền kém 2 2n(CHCHCHCH) caosuthiênnhiên.
o Caosubuna–N:cótính chống dầu khácao.
o Caosubuna–S:cótính đàn hồi cao
3. Tơ
Tơ thiênnhiên:Bông,len, tơ tằm
Tơ hóa học
o Tơ tổng hợp
Tơ nilon-6,6(poli(hexametylen ađipamit)): 2 2 n 6 4 (NHCHNHCOCHCO)
Cótínhdai, bền, mềm mại, ống mượt, ít thấm nước, giặt maukhô,kém bền với nhiệt, với axitvà kiềm, dùng để dệt vải may mặc, vải lót săm lốp xe, bện dâycáp, đan lưới,...
Tơ nitron (tơ olon) :Cótínhdai, bền với nhiệt và giữ nhiệt tốt nên 2 n(CHCH) | CN
thường dùng để dệt vải may quần áo ấm hoặc bện thành sợi “len” đan áorét. Tơ lapsan(poli(etylenterephtalat)) 64 24n (COCHCOOCHO) Bền về mặt cơ học, bền với nhiệt, axit, kiềm hơn nilon,dùng để dệt vải may mặc o Tơ bán tổng hợp: (tổng hợp từ xenlulozơ)
DẠYKÈMQUYNHƠN
Trang7
OFFICIAL
Tơ axetat Tơ visco II. CÁC DẠNG BÀI TẬP Dạng 1: Lí thuyết trọng tâm Ví dụ mẫu Ví dụ 1: Quátrình kết hợp nhiều phân tử nhỏ (monome)thànhphân tử lớn (polime) đồng thời giải phóng những phân tử nhỏ khác(ví dụ ) được gọi là phản ứng 2 HO A. trùng hợp. B. thủy phân. C. trùng ngưng. D.
Hướng dẫn giải: Polime thường được điều chế theohai
phản ứng
Trùng hợp là quá trình kết
xàphònghóa.
loại
làtrùng hợp vàtrùng ngưng.
hợp nhiều phân tử nhỏ (monome) giống nhau hay tương tự nhau thành phân tử lớn (polime).
Trùng ngưng làquátrình kết hợp nhiều phân tử nhỏ (monome)thànhphân tử lớn (polime) đồng thời giải phóng những phân tử nhỏ khác(ví dụ ). 2 HO
Chọn C.
Ví dụ 2: Tên gọi của polimecócông thức là 22n (CHCH)
A. poli(vinylclorua). B. polietilen. C. poli(metylmetacrylat). D. polistiren. Hướng dẫn giải
Tacó:Tênpolime=Poli+Tên của monome Polime được tổng hợp từ etilennênpolimecótênlàpolietilen. 22n (CHCH)
Chọn B.
Ví dụ 3: Trongcácpolimesau,polimenàocó cấu trúc mạng khônggian?
OFFICIAL
A. Amilopectin. B. Xenlulozơ. C. Amilozơ. D. Caosu lưu hóa. Hướng dẫn giải
Cấu trúc mạch thường gặp: Cấu trúcphânnhánh:Amilopectin,glicogen. Cấu trúckhônggian:Caosu lưu hóa, nhựa bakelit. Cấu trúc mạch khôngphânnhánh:Cácpolimecòn lại.
Chọn D.
Ví dụ 4: Cho các polime: cao su buna, amilopectin, xenlulozơ, cao su cloropren, tơ nilon-7, teflon, số polimethiênnhiênlà
A. 1. B. 2. C. 3. D. 4.
Hướng dẫn giải Nguồn gốc của cácpolime thường gặp: Polimethiênnhiên:tinh bột (amilozơ, amilopectin),len, tơ tằm, bông... Polimenhân tạo (bán tổng hợp): tơ visco, tơ axetat, xenlulozơ trinitrat. Polime tổng hợp: hầu hết cácpolimecòn lại như nilon-6.
Trongdãycóhaipolimethiênnhiênlà:amilopectinvà xenlulozơ.
Chọn B.
Ví dụ 5: Trong số các loại tơ sau: tơ nitron; tơ visco; tơ nilon-6,6; tơ lapsan.Cóbaonhiêu loại tơ thuộc tơ nhân tạo (tơ bán tổng hợp)?
3. B. 2. C. 1. D. 4. Hướng dẫn giải Tơ hóa học được chiathànhnhóm: Tơ nhân tạo (tơ bán tổng hợp) thường gặp là: tơ visco, tơ xenlulozơ axetat... Tơ tổng hợp thường gặp là:nitron,nilon-6,nilon-6,6, tơ nilon-7...
DẠYKÈMQUYNHƠN
Trang8
A.
Trongdãycó một tơ nhân tạo (tơ bán tổng hợp) là tơ visco. Chọn C. Ví dụ 6: Cho các chất: cao su buna, poli(metyl metacrylat), tơ olon, tơ nilon-6,6 và polietilen. Số chất được tạo thành từ phản ứng trùng hợp là A. 5. B. 2. C. 4. D. 3. Hướng dẫn giải
Caosubunalà sản phẩm khitrùng hợp buta-1,3-đien.
Poli(metylmetacrylat)là sản phẩm khitrùng hợp metylmetacrylat.
Tơ olon (tơ nitron)là sản phẩm khitrùng hợp vinylxianua(hayacrilonitrin).
nilon-6,6là sản phẩm khitrùng ngưng hexametylenđiamin vàaxit ađipic.
Polietilen(PE)là sản phẩm khitrùng hợp etilen.
xt,t,p 22 22n nCHCH(CHCH)
Trong dãy có 4 chất được tạo thành từ phản ứng trùng hợp: cao su buna, poli(metyl metacrylat), tơ olon,polietilen. Chọn C. Ví dụ 7: Caosubuna-Svàcaosubuna-Nlà sản phẩm đồng trùng hợp của buta-1,3-đien lần lượt với hai chất là
A. stirenvàamoniac.
B. lưu huỳnh vàvinylclorua. C. lưu huỳnh vàvinylxianua. D. stirenvàacrilonitrin.
Hướng dẫn giải
Khi đồng trùng hợp buta-1,3-đien với stiren()cóxúctácNathu được caosubuna-S. 65 2CHCHCH
Khi đồng trùng hợp buta-1,3-đien với acrilonitrin()cóxúctácNathu được caosubuna- 2 CHCHCN N.
Chọn D. Bài tập tự luyện dạng 1
Bài tập cơ bản
DẠYKÈMQUYNHƠN OFFICIAL Trang9
t,p 2 2 2 2nnCHCHCHCH(CHCHCHCH)
3 t,p,xt 2 3 2n 3 3 CHOOC | nCHCCOOCH(CHC) | | CH CH
t,p,xt 2 2 nnCHCHCN(CHCH) | CN Tơ
t 2 2 2 2 2 2 n 2 6 6 4 nHNCHNHnHOOCCHCOOH(NHCHNHCOCHCO)2nHO
Câu 1: Chất nàosau đây khônglàpolime?
A. Tinh bột. B. Thủy tinh hữu cơ. C. Isopren. D. Tơ nilon-6,6.
Câu 2: Loại vật liệu polimenàosau đây có chứa nguyên tố nitơ?
A. Caosubuna. B. Nhựa poli(vinylclorua).
C. Tơ visco. D. Tơ nilon-6,6.
Câu 3: Tơ được sản xuất từ xenlulozơ là
A. tơ nilon-6,6. B. tơ visco. C. tơ tằm. D. tơ capron.
Câu 4: Tơ visco thuộc loại polime?
A. Bán tổng hợp. B. Thiênnhiên. C. Tổng hợp. D. Trùng hợp. Câu 5: Loại tơ nàosau đây được điều chế bằng phản ứng trùng hợp?
A. Tơ nitron. B. Tơ visco. C. Tơ nilon–6,6. D. Tơ xenlulozơ axetat. Câu 6: Poli(vinylclorua)(PVC) được điều chế từ phản ứng trùng hợp chất nàosau đây?
A. . B. . C. . D. . 22CHCH 2 CHCHCl CHClCHCl 25 CHCl Câu 7: PolimethiênnhiênX được sinhratrongquátrìnhquang hợp của câyxanh, ở nhiệt độ thường, X tạo với dung dịch iot hợp chất cómàuxanhtím.PolimeXlà
OFFICIAL
A. tinh bột. B. xenlulozơ. C. saccarozơ. D. glicogen. Câu 8: Tơ thuộc loại tơ poliamitlà
A. tơ lapsan. B. tơ axetat. C. Poli(vinylclorua). D. Poli(metylmetacrylat). Câu 9: Polimenàosau đây không được dùnglàm chất dẻo?
A. Poliacrilonitrin. B. Polietilen. C. Poli(vinylclorua). D. Poli(metylmetacrylat). Câu 10: Tơ tằm thuộc loại
A. polime tổng hợp. B. polimebán tổng hợp. C. polimethiênnhiên. D. polime đồng trùng hợp. Câu 11: Polimedùng để chế tạo thủy tinh hữu cơ (plexiglas) được điều chế bằng phản ứng trùng hợp chất nàosau đây?
A. B. 65 2CHCHCH 3 2CHCOOCHCH C. D. 2 3 3CHCCHCOOCH 2 3CHCHCOOCH Câu 12: Chocácpolimesau: tơ enang; sợi bông;len; tơ tằm; tơ visco; tơ nitron; tơ axetat; tơ lapsan. Số polimecó nguồn gốc từ xenlulozơ là A. 1. B. 2. C. 3. D. 4. Câu 13: Tơ nitrondai bền với nhiệt, giữ nhiệt tốt, thường được dùng để dệt vải vàmay quần áo ấm. Hợp chất nàosau đây tạo thànhpolimedùng
DẠYKÈMQUYNHƠN
Trang10
để sản xuất tơ nitron? A. . B. . 2 25 HNCHCOOH 2 3CHCHCH C. . D. . 2 CHCHCN 2 262HNCHNH Câu 14: Tơ capronvànilon-6,6 thuộc loại A. poliamit. B. polipeptit. C. polieste. D. vinylic. Câu 15: Tơ nilon-6,6là sản phẩm của phản ứng trùng ngưng giữa A. và . 24 HOOCCHCOOH2 242HNCHNH B. và 242HOOCCHNH 2 26 HNCHCOOH
C. và 26 HOOCCHCOOH2 262HNCHNH
D. và 24 HOOCCHCOOH2 262HNCHNH
Câu 16: Cho các polime: poli(vinyl clorua), xenlulozơ, amilozơ, amilopectin. Có bao nhiêu polime có cấu trúc mạnh thẳng?
A. 1. B. 2. C. 3. D. 4. Câu 17: Trong các polime sau: polietilen, tơ nitron, xenlulozơ, poli(vinyl clorua), tơ nilon-6,6. Có bao nhiêupolimelà sản phẩm của phản ứng trùng hợp?
A. 5. B. 2. C. 3. D. 4. Câu 18: Phát biểu nàosau đây đúng?
A. Trùng ngưng vinylcloruathu được poli(vinylclorua).
B. Tơ visco, tơ xenlulozơ axetat thuộc loại tơ tổng hợp.
C. Tơ nilon-6,6 được điều chế từ hexametylenđiamin vàaxitaxetic.
D. Sợi bông, tơ tằm làpolimethiênnhiên.
Câu 19: Cho các polime: poli(vinyl clorua), xenlulozơ, policaproamit, polistiren, xenlulozơ triaxetat, nilon-6,6. Số polime tổng hợp là
A. 5. B. 2. C. 3. D. 4. Câu 20: Phát biểu nàosau đây sai?
A. Polimelà hợp chất cóphân tử khối lớn do nhiều mắt xíchliên kết với nhau tạo nên.
B. Điều kiện cần về cấu tạo của monomethamgia phản ứng trùng hợp làtrongphân tử phải cóliên kết bội hoặc vòngkém bền.
C. Hệ số ntrongcông thức polime gọi là hệ số trùng hợp.
D. Polime tổng hợp được tạo thành nhờ phản ứng trùng hợp hoặc phản ứng trùng ngưng.
Câu 21: Phát biểu nào dưới đây sai?
A. Tơ viscolà tơ thiênnhiênvì xuất xứ từ sợi xenlulozơ.
B. Tơ nilon-6,6là tơ tổng hợp.
C. Tơ hóa học gồm hai loại là tơ nhân tạo và tơ tổng hợp.
D. Tơ tằm là tơ thiênnhiên.
Câu 22: Trong các polime sau: (1) poli(metyl metacrylat); (2) polistiren; (3) nilon-7; (4) poli(etylenterephtalat);(5)nilon-6,6;(6)poli(vinylaxetat),cácpolimelà sản phẩm của phản ứng trùng ngưng là: A. (1),(3),(6). B. (3),(4),(5). C. (1),(2),(3). D. (1),(3),(5).
Câu 23: Phát biểu nàosau đây đúng?
A. Caosu lưu hoá,amilopectinlà những polimecó cấu trúc mạng khônggian.
B. Tơ poliamitkém bền về mặt hoá học làdocácnhómpeptit-CO-NH- dễ bị thuỷ phântrongmôi trường axitvàmôi trường kiềm.
C. Tơ nitron, tơ nilon-6,6,poli(metylmetacrylat) đều được điều chế bằng phương pháptrùng hợp.
D. Tơ visco, tơ nilon-6,6, tơ enang, tơ axetat đều thuộc loại tơ nhân tạo.
Bài tập nâng cao
Câu 24: Chocácpolimesau:
(1)Poliacrilonitrin;
(2)Policaproamit;
DẠYKÈMQUYNHƠN
Trang11
OFFICIAL
(3)Poli(metylmetacrylat); (4) Poli(ure-formanđehit); (5)Poli(etylen-terephatalat); (6)Poli(hexametylen ađipamit); (7) Tơ tằm; (8) Tơ axetat. Số polimecó thể dùnglàm tơ hóa học là A. 5. B. 4. C. 6. D. 7. Câu 25: Chocác sơ đồ phản ứng sau:
Phân tử khối của là 6X A. 194. B. 136. C. 202. D. 184. Dạng 2: Xác định cấu tạo polime và điều chế polime Bài toán 1: Xác định số mắt xích Phương pháp giải Số mắt xích= hệ số polimehóa(n) = số phân tử monome polime 23 m¾txÝch monome
M 610n M
Chú ý: Số mắt xích phải là số tự nhiên, nếu là số thập phân phải làmtròn. Ví dụ: Khối lượng trung bình của xenlulozơ trong sợi bông là 4 860 000 đvC. Số gốc glucozơ có trong loại xenlulozơ nêutrênlà A. 25000. B. 30000. C. 28000. D. 35000. Hướng dẫn giải Công thức của xenlulozơ là 6105nCHO Số gốc cótrong loại xenlulozơ nêutrên
DẠYKÈMQUYNHƠN OFFICIAL Trang12
xt,t
t 8144 122 XCHO2NaOHXXHO 124 324 XHSOXNaSO
53 2 nXnXPolihexametylena®ipamit2nHO
24 HSO,t 23 62 2XX X2HO
polime monome M4860000 n
M162
thu được một loại polime X dùng để điều chế
TrongXcó chứa 66,67%clotheo khối
tử clo?
.
30000
Chọn B. Ví dụ mẫu Ví dụ 1: Tiến hành clo hóa poli(vinyl clorua)
tơ clorin.
lượng. Trungbìnhcóbaonhiêu mắt xíchPVC phản ứng được với một phân
A. 1. B. 2. C. 3. D. 4. Hướng dẫn giải Gọi nlà số mắt xíchPVC phản ứng với một phân tử clo.
DẠYKÈMQUYNHƠN OFFICIAL Trang13
Gọi
2 2 2
m CHCHCHCHCHCHCH Số liên kết trongpolime Xn Tacó: 2 Brx nn.n 02,8296n ,010854n104m 0,5832n1,1232m2,8296n 1,1232m2,2464n n1,12321 m2,24642 Chọn B. Bài toán 2: Điều chế polime Phương pháp giải Ghi nhớ cácquátrình điều chế polime. Sử dụng tỉ lệ khối lượng vàcông thức tính hiệu suất. Ví dụ: Từ 4 tấn etilencó chứa 30% tạp chất có thể điều chế được baonhiêu tấn polietilen(PE), biết hiệu suất phản ứng là90%? A. 2,55 tấn. B. 2,80 tấn. C. 2,52 tấn. D. 3,60 tấn.
Phương trìnhhóa học: 23 2 2n3n1n1 n CHClClCHClHCl X TrongX chứa 66,67%clotheo khối lượng nêntacó: Cl %35,5.n1 m 100%66,77% 62,5n34,5 n2 Chọn B. Nhận xét: Phản ứng clo hóa PVC: 23 2 2311 nnn n CHClClCHClHCl Phản ứng tạo ra cao su lưu hóa:582 n CHS 58222 nn CHSH Ví dụ 2: Tiến hành phản ứng đồng trùng hợp giữa stirenvà buta-1,3-đien (butađien), thu được polimeX. Cứ 2,8296 gam X phản ứng vừa hết với 1,728 gam . Tỉ lệ số mắt xích (butađien : stiren) trong loại 2Br polimetrênlà A. 1:1. B. 1:2. C. 2:3. D. 1:3. Hướng dẫn giải 2Br n0,0108mol
công thức polimecó dạng: .
65 n
Hướng dẫn giải tấn 24CH n470%2,8 Nếu nên tấn H100% 24polietilenCH mm2,8 Với nên tấn H90% polietilenthu®îcm 2,8.90%2,52
Chọn C. Ví dụ mẫu Ví dụ 1: Poli(vinylclorua) được điều chế từ khíthiênnhiên(metan chiếm 90%)theo sơ đồ chuyển hóavà hiệu suất mỗi giai đoạn như sau: 1 2 3 H15% H95% H90% 4 22 23 CH CH CHClPVC
Muốn tổng hợp 1 tấn PVCthì cần baonhiêu khíthiênnhiên (đktc)? 3m A. 5589. B. 5883. C. 5589. D. 6210. Hướng dẫn giải Tacóquátrình: 422 2 2 n2nCHnCHnCHCHCl(CHCHCl) Nếu , cứ: 32 62,5 tấn H100% Suyra: 1 tấn 1.320,512 62,5 Hiệu suất baquátrình: nên: 1 2 3 H15%,H95%,H90%
3 CH CH 3992 m0,512:15%:95%:90%3,992tÊn=3992kgV:22,45588,8m 16
4 4
Trongkhíthiênnhiên,metan chiếm 90%: 3 khÝthiªnnhiªn V5588,8:90%6210m Chọn D. Bài tập tự luyện dạng 2 Câu 1: Phân tử khối trungbình của một loại PE bằng 398300. Hệ số polimehóa của loại PE đó là A. 14225. B. 6373. C. 4737. D. 2122. Câu 2: Trùng hợp m tấn etilen thu được 1 tấn polietilen (PE) với hiệu suất phản ứng bằng 80%. Giá trị của mlà
A. 1,80. B. 0,80. C. 2,00. D. 1,25. Câu 3: Khối lượng của một đoạn mạch tơ nilon-6,6 là 25538 đvC. số lượng mắt xích trong đoạn mạch nilon-6,6nêutrênlà
A. 152. B. 114. C. 121. D. 113. Câu 4: Từ 250kgmetylmetacrylatcó thể điều chế baonhiêukg thủy tinh hữu cơ với hiệu suất 90%?
A. 250kg. B. 235kg. C. 225kg. D. 278kg. Câu 5: Khối lượng của một đoạn mạch tơ nilon-6,6 là 25538 đvC và của một đoạn mạch tơ capron là 17176 đvC. Số lượng mắt xíchtrong đoạn mạch nilon-6,6vàcapronnêutrên lần lượt là
A. 113và152. B. 121và114. C. 121và152. D. 113và114.
DẠYKÈMQUYNHƠN OFFICIAL Trang14
Câu 6: Một loại caosu chứa 2%S về khối lượng. Hỏi cứ baonhiêu mắt xíchisoprenthìcó một cầu nối đisunfua -S-S-?
A. 46. B. 64. C. 80. D. 40. Câu 7: Thủy phân4,3gampoli(vinylaxetat)trongmôi trường kiềm thu được 2,62gampolime. Hiệu suất của phản ứng thủy phânlà
A. 60%. B. 80%. C. 75%. D. 85%.
OFFICIAL
Câu 8: Clo hoá PVC thu được một polime chứa 63,96% clo về khối lượng, trung bình một phân tử clo phản ứng với n mắt xíchtrong mạch PVC.Giá trị của nlà A. 2. B. 4. C. 5. D. 3. Câu 9: Cứ 5,669 gam cao su buna-S phản ứng vừa hết với 3,462 gam trong . Tỉ lệ mắt xích 2Br 4CCl butađien vàstirentrongcaosubuna-Slà A. B. C. D. 2 3 1 2 1 3 3 5 Câu 10: Khi tiến hành đồng trùng hợp buta-1,3-đien vàacrilonitrinthu được một loại caosubuna-N chứa 8,69% nitơ. Tỉ lệ số mol buta-1,3-đien vàacrilonitrintrongcaosulà A. 1:2. B. 1:1. C. 2:1. D. 3:1. Câu 11: Để điều chế caosubuna từ tinh bột người ta tiến hànhtheo sơ đồ sau: Tinh bột Glucozơ Ancoletylic Buta-1,3-đien Caosubuna
Từ 10 tấn khoai chứa 80%tinh bột điều chế được baonhiêu tấn caosubuna? H60% A. 3,1 tấn. B. 2,0 tấn. C. 2,5 tấn. D. 1,6 tấn. Câu 12: Để điều chế caosubuna người tacó thể thực hiện theocác sơ đồ biến hóasau:
25 CHOHButa1,3®ienCaosubuna Khối lượng ancoletylic cần lấy để có thể điều chế được 54gamcaosubunatheo sơ đồ trênlà A. 92gam. B. 230gam. C. 115gam. D. 184gam. Bài tập nâng cao Câu 13: Danhân tạo (PVC) được điều chế từ khíthiênnhiên . Nếu hiệu suất của toàn bộ quátrình 4CH là20%thì để điều chế 1 tấn PVC phải cần thể tíchkhíthiênnhiên(xemkhíthiênnhiên chứa 85%metan) là
A. 4216,47 . B. 4321,70 . C. 3584,00 . D. 3543,88 . 3m 3m 3m 3m Câu 14: Khi cho một loại cao su buna – S tác dụng với brom (trong ), người ta thấy cứ 1,05 gam 4CCl caosu đó có thể tác dụng hết với 0,8gambrom. Tỉ lệ số mắt xích butađien vàstirentrong loại caosutrên là
A. 3:2. B. 2:3. C. 2:1. D. 1:2. Câu 15: Có10,5gampropilen đem polimehóathu được sản phẩm chứa phân tử polime, phần 208,82710 propilen không tham gia polime hóa có thể làm mất màu 79 gam dung dịch 6%. Phân tử khối 4KMnO trungbình của polipropilen vừa thu được là(Cho )23 A N6,02.10
A. 4200. B. 6300. C. 7560. D. 5873.
DẠYKÈMQUYNHƠN
Trang15
H50% H80%
Câu 16: Khi đốt cháy một polimesinhra từ phản ứng đồng trùng hợp isopren với acrilonitrin bằng lượng oxi vừa đủ thu được hỗn hợp khí chứa 58,33% về thể tích. Tỉ lệ mắt xích isopren với acrilonitrin 2CO trongpolimetrênlà A. 2:1. B. 1:3. C. 3:2. D. 1:2.
ĐÁP ÁN
Dạng 1: Lí thuyết trọng tâm
1–C 2–D 3–B 4–A 5–A 6–B 7–A 8–D 9–A 10–C 11–C 12–C 13–C 14–A 15–D 16–C 17–C 18–D 19–D 20–C 21–A 22–B 23–B 24–A 25–C
Câu 6: Poli(vinylclorua)(PVC) được điều chế từ phản ứng trùng hợp của monome tương ứng làvinylclorua,có công thức là: . 2 CHCHCl
OFFICIAL
Câu 7: Xlàtinh bột dotinh bột làpolimethiênnhiênvà được sinhratrongquátrìnhquang hợp của câyxanhvà tạo với dung dịch iot hợp chất cómàuxanhtím.
Câu 9: Các polime như: polietilen, poli(vinyl clorua), poli(metyl metacrylat) được dùng làm chất dẻo. Poliacrilonitrin được dùnglàm tơ nitron (tơ olon).
Câu 11:
Polime dùng để chế tạo thủy tinh hữu cơ (plexiglas) được điều chế bằng phản ứng trùng hợp metyl metacrylat,cócông thức là: . 2 3 3CHCCHCOOCH
Câu 12: Polimecó nguồn gốc từ xenlulozơ là: sợi bông, tơ visco, tơ axetat.
Câu 13: Trùng hợp vinylxianuathu được sản phẩm hữu cơ được dùng để chế tạo tơ nitron (tơ tổng hợp). Câu 16: Cácpolimecó cấu trúc mạch thẳng là:poli(vinylclorua), xenlulozơ, amilozơ.
Câu 17: Cácpolimelà sản phẩm của phản ứng trùng hợp là:polietilen, tơ nitron,poli(vinylclorua).
Câu 18: Asaivìkhitrùng hợp vinylclorua mới thu được poli(vinylclorua).
Bsaivì tơ viscovà tơ xenlulozơ axetat đều thuộc loại tơ bán tổng hợp. Csaivì tơ nilon-6,6 được điều chế từ hexametylenđiamin vàaxit ađipic. D đúng.
Câu 19:
DẠYKÈMQUYNHƠN
Trang16
Cácpolime tổng hợp là:poli(vinylclorua),policaproamit,polistiren,nilon-6,6.
Câu 20:
Csaivìn được gọi là hệ số polimehóahay độ polimehóa.
Câu 21:
Asaivì tơ viscolà tơ nhân tạo.
Câu 23:
Asaivìcaosu lưu hóalàpolimecó cấu trúckhônggian, nhưng amilopectinlàpolimecó cấu trúc mạch phânnhánh. B đúng.
Csaivì tơ nilon-6,6 được điều chế bằng phương pháptrùng ngưng. Dsaivì tơ nllon-6,6, tơ enanglà tơ tổng hợp.
Câu 24: Tơ hoá học là tơ được chế tạo bằng phương pháphoá học gồm tơ tổng hợp và tơ bán tổng hợp. Số polimecó thể dùnglàm tơ hóa học là(1): tơ olon,(2): tơ capron,(5): tơ lapsan,(6): tơ nilon6,6,(8): tơ axetat. Câu 25: Tacó: là . 3X48 2 CHCOOH là . X 25 48 CHOOCCHCOOH là . 2X 25 CHOH là . 6X 48 252CHCOOCH
OFFICIAL
DẠYKÈMQUYNHƠN
Trang17
Dạng 2: Xác định cấu tạo polime và điều chế polime 1–A 2–D 3–C 4–C 5–A 6–A 7–B 8–D 9–B 10–C 11–D 12–B 13–A 14–B 15–D 16–B Câu 1: Hệ số polime của loại PE đó: .39830014225 28 Câu 2: Trong phản ứng trùng hợp: tấn monomepolime mm1 tấn etilenbandau m1:80%1,25 Câu 3: Số mắt xích polime monome M27346 n 121 M226 Câu 4:
6X M202
Câu 5: Tơ nilon-6,6: 2 2n 6 4 (NHCHNHCOCHCO)M 25538226n25538n113 Tơ capron: 2n 5 (NHCHCO)M 17176113n17176n152
Câu 6: Công thức isoprenlà: .58CH Phương trìnhhóa học: 582 5n8n222 n CHSCHSH Caosu chứa 2%S về khối lượng: 5n8n22 CHS 322100%2%n46 68n2322
trìnhhóa
Gọi số moipoli(vinylaxetat) phản ứng làamol. Bảo toàn khối lượng: 4,3an402,62an82 an0,04 Han860,0486100%100%80% 4,3 4,3
DẠYKÈMQUYNHƠN OFFICIAL Trang18
kg thñytinhh÷uc¬m 25090%225
223
ClnCHClCHClHCl Tacó: Cl 35,5n1 %m 100%63,96%n3 122n3n135,5n1 Câu 9: Gọi nlà số mắt xích butađien, mlà số mắt xíchstiren. Công thức của caosubuna-Slà 466523 n m CHCHCH Phương trìnhhóa học: 466523 2 4626523 n m n m CHCHCHnBrCHBrCHCH 54n104m160n gam 5,6693,462 gam 54n104m3,4625,669160nn:m1:2 Câu 10: Phương trìnhhóa học:
Câu 7: Phương
học: 3 PolivinylaxetatnNaOHPolimenCHCOONa a an aanmol
Câu 8: Phương trìnhhóa học:
2n3n1n1
DẠYKÈMQUYNHƠN OFFICIAL Trang19 2 2 2 2 2a2 bnnaCHCHCHCHnbCHCHCN(CHCHCHCH)(CHCHCN) CaosubunaN Tacó: N %14b m5.100%8,96%a:b2:1 4a53b Câu 11: tấn tinhbét m1080%8 Tacó: 6126 610525 6105 46 46 6126CHOCHOCHOHCHOCHCHCHO nn,n2n2nnn Bảo toàn khối lượng: tấn 46 CHcaosubuna 8 mm 3 Mà tấn caosubuna 8H60%m360%1,6 Câu 12: Bảo toàn khối lượng: 46 CHcaosubuna 46 mm54gamCH1mol Mà 25 CHOH 1 2 H50%;H80%n2.1:50%:80%5mol 25 CHOH m5.46230gam Câu 13: Sơ đồ điều chế: 4 22 2 2 n2CHCHCHCHCl(CHCHCl) Tacó: lít 4 4 6 CHPVCCH 10 n2nV2.:20%.22,43584000 62,5 33584m 3 khÝthiªnnhiªn V3584:85%4216,47m Câu 14: Gọi nlà số mắt xíchbutadien,mlà số mắt xíchstiren. Công thức của caosubuna-Slà . 486523 n m CHCHCH Phương trìnhhóa học: 466523 2 4626523 n m n m CHCHCHnBrCHBrCHCH 54n104m160n gam 1,05 0,8 gam 54n104m0,81,05.160n n:m2:3 Câu 15: Số molpolime 20 3 23 8,827.101,466.10mol 6,02.10 4 4 KMnO KMnO m79,6%4,74gamn0,03mol Phương trìnhhóa học:
DẠYKÈMQUYNHƠN OFFICIAL Trang20 3 2 42 3 2 2 3CHCHCH2KMnO4HO3CHCHOHCHOH2MnO2KOH 0,0450,03 propilend m0,045.421,89gam polime m10,51,898,61gam Phân tử khối trungbình của polipropilen vừa thu được là 3 8,615873 1.466.10 Câu 16: Sơ đồ: 2 t 5833 2 2 a b 2 CO:5a3bmol CHCHNOHO:4a1,5bmol N:0,5bmol Tacó: 2CO 5a3b %V 100%58,33% 5a3b4a1,5b0,5b 3aba:b1:3




















