# 077 ΜΑΡ-ΑΠΡ 2023
# 035
ΙΑΝ-ΦΕΒ 2016
ΡΕΠΟΡΤΑΖ
ΠΡΟΦΙΛ
Τα 10 πιο σημαντικά νέα φάρμακα του 2023
ΠΡΟΦΙΛ
Ο πιο καλός ο διοικητής ΣΥΝΕΝΤΕΥΞΗ
Ο πιο καλός ο διοικητής
ΡΕΠΟΡΤΑΖ
Πασχάλης Αποστολίδης
Ένα καλύτερο μέλλον για τις κλινικές μελέτες στην Ελλάδα
ΣΥΝΕΝΤΕΥΞΗ Πασχάλης Αποστολίδης
ΡΕΠΟΡΤΑΖ
4ο Clinical Research Conference
ΡΕΠΟΡΤΑΖ
ΡΕΠΟΡΤΑΖ
Think Tank για κλινικές µελέτες
4ο Clinical Research Conference

Think Tank για κλινικές µελέτες

www.virus.com.gr
ISSN: 2241-0961
www.virus.com.gr
ISSN: 2241-0961
Επιτέλους στην Ελλάδα συγκροτημένο σύστημα Νοσοκομειακής Φροντίδας στο Σπίτι Αφιέρωμα
# 035 ΙΑΝ-ΦΕΒ 2016
Αιματολογία


● Πυρετός;
● Πονόδοντος;
● Συμπτώματα κρυολογήματος και γρίπης;
● Πονόλαιμος;
● Ημικρανία;
● Πονοκέφαλος;
● Πόνοι περιόδου;
● Οσφυαλγία;
● Πόνος σε μυς ή αρθρώσεις;
13 φορές


την ημέρα
Εάν το 1 δισκίο δεν ελέγξει τα συμπτώματα, μπορείτε να πάρετε 2 δισκία έως και 3 φορές την ημέρα.
ΚΑΙ ΠΡΟΝΟΙΑΣ ΚΑΙ Ο ΕΘΝΙΚΟΣ ΟΡΓΑΝΙΣΜΟΣ ΦΑΡΜΑΚΩΝ ΣΥΝΙΣΤΟΥΝ: ΔΙΑΒΑΣΤΕ ΠΡΟΣΕΚΤΙΚΑ ΤΙΣ ΟΔΗΓΙΕΣ ΧΡΗΣΗΣ - ΣΥΜΒΟΥΛΕΥΤΕΙΤΕ ΤΟ ΓΙΑΤΡΟ Ή ΤΟ ΦΑΡΜΑΚΟΠΟΙΟ ΣΑΣ. Αντενδείκνυται σε σοβαρή ηπατική, νεφρική ή καρδιακή ανεπάρκεια, αλλεργία στα ΜΣΑΦ και άτομα κάτω των 18 ετών. Απαιτείται προσοχή σε ασθενείς με άσθμα. Για χρήση έως 3 συνεχόμενες ημέρες.
Μέγιστη δόση έως 6 δισκία σε 24 ώρες (6 ώρες απόσταση ανάμεσα στις δόσεις). Να φυλάσσεται μακριά από παιδιά.
1 ➤
συστατικά
200 mg ΠΑΡΑΚΕΤΑΜΟΛΗ 500 mg Οιδίποδος 1-3 & Παράδρομος Αττικής Οδού 33-35, 15238 Χαλάνδρι Τηλ.: 2107488821, Fax: 2107488827 info@winmedica.gr, www.winmedica.gr
πόνο ➤ πυρετό ➤ φλεγμονή
ΑΠΕΛΕΥΘΕΡΩΝΕΙ από γρήγορα και με διάρκεια! 2δραστικά
ΙΒΟΥΠΡΟΦΑΙΝΗ
IBUTOMOL ADV 11/2021
ΥΠΟΥΡΓΕΙΟ
ΤΟ
ΥΓΕΙΑΣ
6 Ρεπορτάζ
Τα 10 πιο σημαντικά νέα φάρμακα του 2023


14 Ρεπορτάζ
Ένα καλύτερο μέλλον για τις κλινικές
μελέτες στην Ελλάδα
16 Ρεπορτάζ
Επιτέλους στην Ελλάδα συγκροτημένο
σύστημα Νοσοκομειακής Φροντίδας
στο Σπίτι
19 ΑΦΙΕΡΩΜΑ ΑΙΜΑΤΟΛΟΓΙΑ
20 Έρευνα
Η ανταπόκριση της ανοσοθεραπείας στο προχωρημένο μελάνωμα
22 Έρευνα
Θεραπείες CAR-T: Βελτιώνουν την ποιότητα ζωής
24 Ρεπορτάζ
Δευτεροπαθής οξεία μυελογενής
λευχαιμία: Μπορεί να προληφθεί;
26 Ρεπορτάζ
Θετική εξέλιξη στην οξεία
λεμφοβλαστική λευχαιμία Β
28 Ρεπορτάζ
Λευχαιμίες: Ελπίδες από νέες
θεραπείες
31 Ρεπορτάζ
Σπάνια, αλλά αντιμετωπίσιμη
κληρονομική πάθηση
32 Ρεπορτάζ
«Κλειδί» οι μεταλλάξεις στα επιθετικά
λεμφώματα
34 Έρευνα
Μελάνωμα: Ανοσοθεραπεία πριν από το χειρουργείο

Κωνσταντίνος Ουζούνης CEO, ethosGROUP ouzounis.k@ethosmedia.eu
Νατάσσα Λαζαράκου ΣΥΜΒΟΥΛΟΣ ΔΙΟΙΚΗΣΗΣ lazarakou.n@ethosmedia.eu
Αιμίλιος Νεγκής ΔΙΕΥΘΥΝΤΗΣ ΣΥΝΤΑΞΗΣ negis.e@ethosmedia.eu

#077
ΜΑΡ-ΑΠΡ 2023
2023
Μαρία Αλιμπέρτη
ΣΥΝΤΑΚΤΡΙΑ alimperti.m@ethosmedia.eu
Χρήστος Χαραλαμπάκης KEY ACCOUNT MANAGER charalampakis.c@ethosmedia.eu
Αμαλία Λούβαρη
ΕΠΙΜΕΛΕΙΑ - ΔΙΟΡΘΩΣΗ louvari.a@ethosmedia.eu
2 /
Μάρτιος-Απρίλιος
ΠΕΡ ΟΜΕΝΑ
14 06 42
16
Γιούλη Μουτεβελή ΔΙΟΙΚΗΤΙΚΗ ΥΠΟΣΤΗΡΙΞΗ mouteveli.g@ethosmedia.eu
Λωρέττα Μπούρα ΥΠΕΥΘΥΝΗ ΣΥΝΔΡΟΜΩΝ boura.l@ethosmedia.eu
Μαρία Ανδριώτη ΛΟΓΙΣΤΗΡΙΟ andrioti.m@ethosmedia.eu
36 Ρεπορτάζ
Αιμορροφιλία:
Το χρονικό της γονιδιακής θεραπείας
38 Έρευνα
Η χρήση αντιβιοτικών αυξάνει
τον κίνδυνο υποτροπής
του καρκίνου
42 Άρθρο
Εξελίξεις στο λέμφωμα Hodgkin
46 Άρθρο
Εξελίξεις στη Μακροσφαιριναιμία Waldenström
50 Άρθρο
Εξελίξεις στο πολλαπλό μυέλωμα και στην AL Αμυλοείδωση
Πόπη Καλογιάννη ΔΗΜΙΟΥΡΓΙΚΟ popikalogianni@gmail.com
Photopress/ Θ&Α Αναγνωστόπουλοι Shutterstock ΦΩΤΟΓΡΑΦΙΑ

Pressious Αρβανιτίδης Α.Β.Ε.Ε. ΕΚΤΥΠΩΣΗ - ΒΙΒΛΙΟΔΕΣΙΑ
56 Άρθρο Εξελίξεις στα νεοπλάσματα της μυελικής σειράς
62 Ρεπορτάζ
Το luspatercept, πλέον, και στην Ευρώπη για την αντιμετώπιση της αναιμίας
64 Άρθρο
Παχυσαρκία: «Μεταβολική βόμβα» που απειλεί την υγεία της κοινωνίας μας
70 Ρεπορτάζ
9 συστάσεις για τη δευτερογενή χρήση δεδομένων υγείας

78 Ρεπορτάζ
Εξαιρετικά ανήσυχοι οι Έλληνες για τα προσωπικά δεδομένα
Λυσικράτους 64, 176 74 Καλλιθέα
T: +30 210 998 4950
E: phb-press@ethosmedia.eu
www.virus.com.gr • www.phb.com.gr
ΓΕΜΗ: 00044774007000
• www.ethosmedia.eu
• www.ethosevents.eu
• www.banks.com.gr
• www.insuranceworld.gr
ISSN: 2241-0961

3
�Απαγορεύεται αυστηρά η αναδημοσίευση φωτογραφιών και ύλης, ή μέρος αυτής, και η καθ’ οιονδήποτε τρόπο εκμετάλλευσή τους, χωρίς την έγγραφη άδεια του εκδότη
ιδιοκτησία
64 50 70
Χρειάζονται τολμηρές και ριζικές
αλλαγές στον τρόπο οργάνωσης, διοίκησης και χρηματοδότησης των υπηρεσιών υγείας.
Δεν είναι μόνο θέμα χρημάτων
στην Υγεία
Οι προεκλογικές εξαγγελίες των τριών μεγαλύτερων κομμάτων στην Υγεία
έχουν αρκετές διαφορές, αλλά και ορισμένα κοινά σημεία. Όλοι υπόσχονται
περισσότερες προσλήψεις και αύξηση των δαπανών σε βάθος τετραετίας.
Δεν θα σχολιάσω το γεγονός αν τα δημοσιονομικά επιτρέψουν αύξηση των
δημόσιων δαπανών για την Υγεία κατά 1%-2% μέχρι το 2027. Μακάρι να ήταν
τόσο απλά τα πράγματα. Δηλαδή να αρκούσε απλώς η αύξηση των πόρων.
Δυστυχώς, τα προβλήματα στο σύστημα υγείας είναι πιο δομικά, όπως έχουν
δείξει όλες οι μελέτες Ελλήνων και ξένων ειδικών. Χρειάζονται τολμηρές και
ριζικές αλλαγές στον τρόπο οργάνωσης, διοίκησης και χρηματοδότησης των
υπηρεσιών υγείας.
Άλλωστε, και πριν το 2010, η Ελλάδα δαπανούσε περίπου 7 δισ. ευρώ
επιπλέον για την Υγεία, χωρίς φυσικά να είμαστε ικανοποιημένοι από την
ποιότητα και την ποσότητα των παρεχόμενων υπηρεσιών. Και τότε είχαμε

ράντζα στις εφημερίες και ελλείψεις προσωπικού, ειδικά σε νησιωτικές και απομακρυσμένες περιοχές. Η μεταρρύθμιση του ΕΣΥ χρειάζεται διακομματική στήριξη και συναίνεση.
Είναι φανερό ότι αν υπάρξει συνεργασία για τον σχηματισμό κυβέρνησης
μεταξύ ΝΔ-ΠΑΣΟΚ ή ΣΥΡΙΖΑ-ΠΑΣΟΚ, τότε θα έχουμε αυξημένες πιθανότητες
να υπάρξει συντονισμένη προσπάθεια αναδιοργάνωσης του ΕΣΥ.
Από την άλλη, μια μονοκομματική κυβέρνηση –όπως αυτή στην οποία στοχεύει η ΝΔ– θα έχει μικρότερο πολιτικό κεφάλαιο για να φέρει εις πέρας το δύσκολο εγχείρημα. Γι’ αυτό, ακόμη κι αν ο Κυριάκος Μητσοτάκης πετύχει
να λάβει αυτοδυναμία, οφείλει να επιδιώξει τη συνεργασία με το ΠΑΣΟΚ στην υλοποίηση των αλλαγών στην Υγεία. Διαφορετικά, πολύ φοβάμαι ότι οι πιθανότητες επιτυχίας θα είναι λίγες…
Αιμίλιος Νεγκής
EDITΟRIAL
editorial
4 / Μάρτιος-Απρίλιος 2023
5
Ετήσια έκθεση της Evaluate Vantage
Το δυναμικό
πωλήσεων για το 2023 εκτιμάται
σε 17,5 δισ. δολάρια

του 2023
Eλπίδες γεννούν οι εγκρίσεις νέων φαρμάκων για τους ασθενείς, αλλά η επιφυλακτικότητα των εγκριτικών αρχών έχει μεταφραστεί σε ένα πολύ μικρότερο εκτιμώμενο σύνολο για το δυναμικό πωλήσεων του top 10 σε σύγκριση με πέρσι. Το 2022, το δυναμικό των εκτιμώμενων πωλήσεων για τα 10 κορυφαία φάρμακα από την ετήσια
έκθεση της Evaluate Vantage ανήλθε σε 26,9 δισ. δολ., ενώ για το 2023 είναι μόλις 17,5 δισ. δολάρια Στο «ομιχλώδες» τοπίο για το Αλτσχάιμερ, το Leqembi της Eisai λειτουργεί με παρόμοιο τρόπο με το donanemab, που δημιούργησε σχεδόν σκάνδαλο για τον FDA πέρσι, «φέρνει λίγο ήλιο», σύμφωνα με όσα δημοσιεύει το Fiercepharma.
6 / Μάρτιος-Απρίλιος 2023
Τα
πιο
νέα
10
σημαντικά
φάρμακα
ΡΕΠΟΡΤΑΖ
Στον ορίζοντα υπάρχουν αρκετές πρώτες
εγκρίσεις, μεταξύ άλλων για τη θεραπεία της Apellis για τη γεωγραφική α -
τροφία (GA) και ένα εμβόλιο κατά του
αναπνευστικού συγκυτιακού ιού που
έρχεται από την GSK, προστατεύοντας

από έναν κοινό ιό του κρυολογήματος, που μπορεί να αποβεί μοιραίος για τους
πολύ ηλικιωμένους και τους πολύ νέους, καθώς και μια πειραματική γονιδιακή
θεραπεία της Sarepta/Roche για τη
μυϊκή δυστροφία Duchenne (DMD), μια γενετική πάθηση που πλήττει τα νεαρά αγόρια και εξασθενεί σοβαρά τους μύες τους, αποβιώνοντας, τελικά, μοιραία, πριν από τη μέση ηλικία. Ωστόσο, οι εκπληκτικές καινοτομίες σε αυτόν τον κατάλογο δεν σημαίνει ότι θα φέρουν και την πρωτιά στη φαρμακοβιομηχανία, λόγω των υψηλών κινδύνων όσον αφορά τη ρύθμιση και την αποζημίωση, καθώς και άγνωστα στοιχεία όσον αφορά τη μακροπρόθεσμη ασφάλεια και αποτελεσματικότητα. 1
Eisai και Biogen με το lecanemab για το Αλτσχάιμερ

Στις εκτιμήσεις της ετήσιας έκθεσης της
Evaluate Vantage όσον αφορά τις μελλοντικές δυνατότητες πωλήσεων περιλαμβάνεται μια θεραπεία για τη νόσο του Αλτσχάιμερ. Στην κορυφή βλέπει η Evaluate την Eisai και την Biogen με το lecanemab για τη νόσο Αλτσχάιμερ, που εγκρίθηκε τον Ιανουάριο ως Leqembi, με εκτιμώμενες πωλήσεις 3 δισ. δολ. έως το 2028. Ωστόσο, θα πρέπει να κρατούν «μικρό καλάθι», όπως έδειξε η πορεία
του Aduhelm, το οποίο είχε προδιαγραφεί ως ένα σημαντικό blockbuster, αλ -
λά, αμέσως μετά την έγκρισή του, οι δημιουργοί του φαρμάκου Biogen και Eisai
είδαν μια εμπορική αποτυχία. Η υψηλή
τιμή του, σε συνδυασμό με την αμφισβη-
τούμενη ασφάλεια και αποτελεσματικότητά του, ήταν απλά πολύ μεγάλη για να την αντέξει η αγορά, παρά το γεγονός ότι ήταν το πρώτο νέο φάρμακο για τη νόσο Αλτσχάιμερ εδώ και περισσότερα από 15 χρόνια.
2
Sarepta και Roche με το SRP-9001 για τη Δυστροφία Duchenne, DMD
Είναι δεύτερο σε αυτόν τον κατάλογο, με εκτιμώμενες πωλήσεις ύψους 2,2 δισ. δολ. το 2028. Η Evaluate Vantage προειδοποιεί ότι η εμπορική επιτυχία του SRP-9001 των Sarepta και Roche στις ΗΠΑ δεν είναι καθόλου εγγυημένη (Hailshadow/iStock/ Getty Images Plus).
Το SRP-9001 λειτουργεί ως γονιδιακή θεραπεία και έχει σχεδιαστεί για να παραδίδει το γονίδιο που κωδικοποιεί τη μικροδυστροφίνη στον μυϊκό ιστό, ώστε να προτρέπει την παραγωγή της πρωτεΐνης μικροδυστροφίνης. Οι ασθενείς με DMD έχουν μια μετάλλαξη στο γονίδιο DMD και δεν μπορούν να παράγουν την πρωτεΐνη από μόνοι τους, οδηγώντας σε προοδευτική απώλεια της μυϊκής δύναμης.
Οι προβλέψεις είναι δύσκολες, λόγω του περιορισμένου αριθμού ληπτών, του νέου θεραπευτικού τομέα και του κόστους. Ερωτήματα υπάρχουν, επίσης, σχετικά με την ασφάλεια, ένα ζήτημα που έχει καταδιώξει τις γονιδιακές θεραπείες στο παρελθόν, καθώς και τη μακροπρόθεσμη αποτελεσματικότητά της. Η Sarepta εξακολουθεί να προχωράει, καθώς έλαβε ταχεία επανεξέταση από τον FDA πέρσι, με ημερομηνία του Prescription Drug User Fee Act την 29η
7
αν
να παραταθεί ή θα μπορούσε ακόμη και να εγκριθεί νωρίτερα.
Μαΐου,
και αυτή θα μπορούσε
Το lecanemab, για
τη νόσο Αλτσχάιμερ, εκτιμάται ότι θα
φτάσει σε πωλήσεις τα 3 δισ. δολ. έως το 2028.
Η Apellis Pharmaceutical υπολογίζει ότι θα μπορούσε να έχει πωλήσεις ύψους 2,2 δισ. δολ. μέχρι το 2028.

Όσο για τη χρηματοδότηση, ο διευθύνων σύμβουλος της βιοφαρμακευτικής εταιρείας, Doug Ingram, δήλωσε σε συνέντευξή του στο Fierce Biotech τον Νοέμβριο, ότι η εταιρεία συγκέντρωσε περισσότερα από 1 δισ. δολ. κατά τη διάρκεια του τρίτου τριμήνου, «για να διασφαλίσουμε ότι διαθέτουμε τους απαραίτητους πόρους για την πλήρη προετοιμασία και την επιτυχή κυκλοφορία του SRP-9001». 3
Apellis για την ατροφία
Με δεδομένο το ότι υπάρχει περίπου 1 εκατομμύριο Αμερικανών που ζει με ατροφία, η Apellis Pharmaceutical εκτιμάται ότι θα μπορούσε να έχει πωλήσεις ύψους 2,2 δισ. δολ. μέχρι το 2028. Η Apellis ελπίζει ότι η βελτιωμένη εκδοχή της πεγκετακοπλάνης, του δραστικού συστατικού του φαρμάκου Empaveli της φαρμακευτικής εταιρείας για σπάνιες ασθένειες, μπορεί να περάσει τη γραμμή
τερματισμού του FDA φέτος και να γίνει το πρώτο νέο φάρμακο για τη γεωγραφική ατροφία (ΓΑ). Εφόσον αυτό συμβεί, θα αποτελέσει έγκριση-σταθμό, αφού δεν υπάρχουν εγκεκριμένες από τον FDA θεραπείες για την πάθηση αυτή, μια προχωρημένη μορφή εκφύλισης της ωχράς κηλίδας που σχετίζεται με την ηλικία και οδηγεί, τελικά, σε απώλεια όρασης και τύφλωση στους ηλικιωμένους. Ωστόσο, οι αναλυτές της Evaluate σημειώνουν ότι εξακολουθεί να υπάρχει μεγάλος κίνδυνος εδώ για την Apellis, όχι μόνο από προηγούμενες αποτυχίες στον κλάδο, αλλά και από εσωτερικά ζητήματα. Ακόμη, υπάρχει αβεβαιότητα όσον αφορά τα κλινικά δεδομένα του φαρμάκου, καθώς έχουμε δεδομένα μόνο από μία από τις δύο δοκιμές Φάσης ΙΙΙ της εταιρείας. Επίσης, η οφθαλμολογική επιτροπή του FDA δεν έχει ακόμη επαναλάβει τις ακροάσεις της επιτροπής της στον απόηχο του Covid-19.

4Lilly με το Donanemab
για το Αλτσχάιμερ
Το φάρμακο αυτό βρισκόταν, στην πραγματικότητα, και στη λίστα με τα 10 κορυφαία φάρμακα της Evaluate για το 2022. Από πέρσι είχαν δοθεί προβλέψεις για το φάρμακο της Eli Lilly donanemab με εκτιμώμενες πωλήσεις το 2026 αξίας… 6 δισ. δολαρίων! Ωστόσο, δεν έλαβε έγκριση και επιστρέφει και πάλι στη φετινή λίστα, καταλαμβάνοντας την τέταρτη θέση, αλλά με σημαντικά χαμηλότερες εκτιμήσεις
8 ΡΕΠΟΡΤΑΖ / Μάρτιος-Απρίλιος 2023
για τις πωλήσεις, μόλις 1,9 δισ. δολ. έως
το 2028. Σημειώνεται ότι ο FDA απέρριψε την έγκριση ταχείας παρακολούθησης
της Lilly για το donanemab, λέγοντας ότι χρειάζονται περισσότερα δεδομένα και

ότι η εταιρεία θα πρέπει να υποβάλει αίτηση για παραδοσιακή επανεξέταση, κάτι
που θα μεταθέσει το όποιο «ναι» του FDA για το επόμενο έτος. Η Lilly αποφάσισε να κρατήσει τα «πυρά» της στην αναζήτηση έγκρισης για το φάρμακο, που ήρθε μετά την εμπορική αποτυχία του φαρμάκου Aduhelm της Eisai και της Biogen για τη νόσο Αλτσχάιμερ, και η ρυθμιστική διαμάχη γύρω από αυτό προκάλεσε σαφώς μια παύση.
5
Εμβόλιο για τον ιό RSV
Η GSK ελπίζει να λάβει φέτος την πρώτη

έγκριση για ένα εμβόλιο για τον αναπνευστικό συγκυτιακό ιό (RSV), το οποίο θα μπορούσε να αποφέρει πωλήσεις blockbuster για τη μεγάλη φαρμακευτική εταιρεία του Ηνωμένου Βασιλείου. Η GSK θα αντιμετωπίσει σχεδόν αμέσως μια βασική «μάχη» στις ΗΠΑ με την Pfizer για μερίδιο αγοράς, η οποία παρασκευάζει το δικό της αντίπαλο εμβόλιο RSV, με αμφότερα
να μπορούν ενδεχομένως να εγκριθούν τον Μάιο. Το RSVPreF3 OA, εμβόλιο για ηλικιωμένους ενήλικες για τον αναπνευστικό συγκυτιακό ιό, εκτιμάται ότι μπορεί να φθάσει σε πωλήσεις το 2028 το 1,8 δισ. δολάρια. Έως τώρα, έχουν γίνει αρκετές απόπειρες για ένα εμβόλιο, αλλά ο δρόμος ήταν γεμάτος με πισωγυρίσματα και αποτυχίες. Η GSK ελπίζει σε μια απόφαση του FDA μέχρι τις 3 Μαΐου. Το εμβόλιό της πέτυχε τον στόχο σε μια δοκιμή Φάσης ΙΙΙ σε ενήλικες μεγαλύτερης ηλικίας το περασμένο καλοκαίρι, η οποία έδειξε ότι το ερευνητικό της εμβόλιο παρήγαγε στατιστικά σημαντική και κλινικά σημαντική μείωση των περιπτώσεων νόσου του κατώτερου αναπνευστικού συστήματος που προκαλείται από τον RSV σε ενήλικες ηλικίας 60 ετών και άνω. Η GSK ήλπιζε να αναπτύξει ένα εμβόλιο τόσο για τα βρέφη όσο και για τα άτομα ηλικίας 60 ετών και άνω, αλλά μια ανησυχία για την ασφάλεια στη δοκιμή του εμβολίου για τις μητέρες κατέστρεψε τα σχέδια για τα πρώτα.
6
Το epcoritamab της AbbVie
για τον καρκίνο
Το epcoritamab της AbbVie και της Genmab θα εισέλθει σε μια αγορά που «θερμαίνεται» για τα διειδικά αντισώματα με στόχο τον καρκίνο. Η «μάχη» των διειδικών για την αγορά των CD20 διειδικών λεμφωμάτων μαίνεται, εδώ και καιρό, κάπως αθόρυβα. Η ημερομηνία για ένα Prescription Drug User Fee Act ορίστηκε στις 21 Μαΐου. Το διειδικό αντίσωμα CD3xCD20 φαίνεται ότι είναι έτοιμο να ανταγωνιστεί το Lunsumio της Roche, το
ενήλικες για τον αναπνευστικό
συγκυτιακό ιό, εκτιμάται ότι μπορεί
να έχει το 2028
πωλήσεις
1,8
9
Το RSVPreF3 OA, εμβόλιο για ηλικιωμένους
αξίας
δισ. δολαρίων.
πρώτο στην κατηγορία του, μαζί με ένα υποψήφιο της Regeneron, το odronextamab. Οι θεραπείες λειτουργούν με τη σύνδεση με το CD20 στα κακοήθη Βκύτταρα και το CD3 στα Τ-κύτταρα για τη θανάτωση των καρκινικών κυττάρων, προσφέροντας αποτελεσματικότητα όπως οι CAR-T, χωρίς την πολυπλοκότητα των κυτταρικών θεραπειών. Αν εγκριθεί, το epcoritamab μπορεί να ξεχωρίσει ως
το πρώτο υποδόριο διειδικό αντίσωμα που θα εγκριθεί στην αγορά του λεμφώματος μεγάλων Β-κυττάρων. Τον περασμένο Ιούνιο, οι εταίροι αποκάλυψαν ελπιδοφόρα αποτελέσματα από μια δοκιμή Φάσης ΙΙ στο λέμφωμα. Το epcoritamab απέδειξε ποσοστό αντικειμενικής ανταπόκρισης 63% και ποσοστό πλήρους ανταπόκρισης 39%, με διάμεση διάρκεια της ανταπόκρισης τους 12 μήνες. Σχεδόν το 90% των ατόμων με πλήρη ανταπόκριση δεν είχαν υποτροπιάσει έως τους 9 μήνες, το οποίο σημαίνει ότι η ομάδα αυτή δεν είχε ακόμη φτάσει τη διάμεση διάρκεια της ανταπόκρισης. Όσον αφορά την ασφάλεια, το 2,5% των συμμετεχόντων υπέστησαν σύνδρομο απελευθέρωσης κυτταροκινών βαθμού 3, με διάμεση έναρξη 20 ώρες μετά την υποδόρια ένεση και διάμεσο χρόνο υποχώρησης 48 ώρες. Τώρα, οι εταιρείες δοκιμάζουν την υποδόρια epcoritamab σε διάφορους τύπους λεμφώματος. Στο ASH 2022, οι δύο ανακοίνωσαν τα πρώτα αποτελέσματα για έναν συνδυασμό epcoritamab συν Rituxan και Revlimid της Bristol Myers Squibb σε νεοδιαγνωσθέν οζώδες λέμφωμα, ο οποίος απέδειξε πο-
σοστό ανταπόκρισης 90%. Το odronextamab της Regeneron επιδιώκει επίσης αυτήν την ένδειξη, έχοντας συγκεντρώσει ποσοστό αντικειμενικής ανταπόκρισης
82% σε δοκιμή Φάσης ΙΙ. Ωστόσο, οι μελέτες της Regeneron έχουν αμαυρωθεί από ανεπιθύμητες ενέργειες που σχετίζονται με τη θεραπεία, θανάτους και εγκαταλείψεις. Όσον αφορά τις προσφορές
της AbbVie και της Genmab, οι δύο εταιρείες υπέβαλαν αιτήσεις στον Ευρωπαϊκό Οργανισμό Φαρμάκων τον Οκτώβριο για τη χρήση των θεραπειών σε υποτροπιάζον ή ανθεκτικό διάχυτο λέμφωμα μεγάλων κυττάρων Β, μετά από δύο ή περισσότερες σειρές συστηματικής θεραπείας.

Zuranolone της Sage
Therapeutics για την κατάθλιψη
Η ζουρανολόνη έχει στόχο την κατάθλιψη εν γένει και την κατάθλιψη μετά τον τοκετό. Η αγορά ψυχικής υγείας είναι, ιστορικά, γεμάτη κενά στις θεραπευτικές επιλογές. Από τότε που οι εκλεκτικοί αναστολείς επαναπρόσληψης σεροτονίνης (SSRIs) εμφανίστηκαν στην αγορά, τη δεκαετία του ’90, οι εγκρίσεις για καινοτόμες θεραπείες ήταν ελάχιστες και πολύ σπάνιες, αφήνοντας μια μεγάλη ανεκπλήρωτη ανάγκη για τους ασθενείς με καταθλιπτικές διαταραχές. Εφόσον λάβουν έγκριση

10 ΡΕΠΟΡΤΑΖ / Μάρτιος-Απρίλιος 2023
7
Το Zuranolone της Sage Therapeutics
για την κατάθλιψη θα μπορούσε να
αποφέρει έως
το 2028 1,5 δισ. δολάρια.
οι Biogen και Sage Therapeutics, η ζουρανολόνη θα αποτελέσει μια πρωτοποριακή επιλογή για δύο υποεξυπηρετούμενες αγορές. Εκτιμάται ότι θα μπορούσε να αποφέρει έως το 2028 1,5 δισ. δολάρια. Πρόκειται για από του στόματος φάρμακο και θα χορηγείται σε θεραπεία δύο εβδομάδων, μία φορά την ημέρα. Στοχεύοντας στον υποδοχέα GABA-A, το φάρμακο θα αλλάζει το «παιχνίδι», αντιμετωπίζοντας ένα καταθλιπτικό επεισόδιο
με μια σύντομη πορεία «κατά περίπτωση».
Σε μια δοκιμή Φάσης ΙΙΙ της ζουρανολόνης στη ΜΔΣ πέτυχε τον κύριο στόχο της, δηλαδή τη βελτίωση των συμπτωμάτων της κατάθλιψης σε σχέση με το εικονικό
φάρμακο, έχασε όμως ορισμένα δευτερεύοντα τελικά σημεία και οι επιδράσεις του φαρμάκου άρχισαν να μειώνονται γύρω στην 42η ημέρα. Όμως το φάρμακο απέδειξε αναμφίβολα την αξία του στην PPD σε μια δοκιμή Φάσης ΙΙΙ, ξεπερνώντας το εικονικό φάρμακο σε μια κλίμακα κατάθλιψης σε τέσσερα διαφορετικά χρονικά σημεία.
Mirikizumab της Lilly
για κολίτιδα του έλκους και
νόσο του Crohn
ψήφιο είναι επίσης το Entyvio της Takeda μαζί με το Skyrizi και το Tremfya. Ωστόσο, αν εγκριθεί πρώτο ως αναστολέας της IL23, θα συμβάλει στην καθιέρωση της Eli Lilly ως βασικού «παίκτη» στην αγορά UC. Επειδή πολλοί ασθενείς χάνουν την ανταπόκριση στα βιολογικά φάρμακα, το mirikizumab θα μπορούσε να καλύψει ένα θεραπευτικό κενό. Επίσης, ως εναλλακτικός μηχανισμός δράσης του, θα μπορούσε να είναι η απάντηση για ασθενείς που έχουν δυσανεξία ή αντοχή σε αναστολείς του TNF, όπως το Humira της AbbVie ή το Enbrel της Amgen.
Etrasimod της Pfizer

για την κολίτιδα
Με την εξαγορά της Arena Pharmaceuticals έναντι 6,7 δισ. δολ. η Pfizer απέκτησε το υποψήφιο φάρμακο για την ελκώδη κολίτιδα (UC) etrasimod, το οποίο πέτυχε σε ένα ζευγάρι δοκιμών Φάσης ΙΙΙ, υποδηλώνοντας ότι ο επιλεκτικός διαμορφωτής της 1-φωσφορικής σφιγγοσίνης (S1P-1) έχει δυνατότητες για να καταστεί blockbuster, με εκτιμώμενες πωλήσεις έως το 2028 1,2 δισ. δολάρια. Τον Δεκέμβριο του 2022, ο FDA αποδέχθηκε
κολίτιδα (UC)
etrasimod, το οποίο
έχει δυνατότητες
να καταστεί blockbuster, με εκτιμώμενες
Σε μια δοκιμή Φάσης ΙΙΙ, πριν από τρία χρόνια, η mirikizumab, δοκιμάστηκε και
για την ψωρίαση πλάκας και στοχεύει στην υπομονάδα p19 της IL-23. Η μιρικιζουμά-
μπη έχει την ευκαιρία να κάνει θραύση
ως πρώτη στην κατηγορία της θεραπεί -
ας στην UC και τρίτη στην κατηγορία της στη νόσο του Crohn. Εκτιμάται ότι θα φέρει στα ταμεία της εταιρείας έως το 2028 1,2 δισ. δολάρια.
Για την αντιμετώπιση της συγκεκριμένης νόσου η Lilly δίνει «αγώνα δρόμου», με περισσότερους από 12 υποψηφίους, που βρίσκονται τώρα σε δοκιμές Φάσης ΙΙβ ή Φάσης ΙΙΙ, πολλοί από τους οποίους έχουν υποσχόμενους νέους μηχανισμούς δράσης
και νέες οδούς χορήγησης, σύμφωνα με την εταιρεία αναλύσεων GlobalData. Το mirikizumab εκτιμάται ότι θα εγκριθεί πρώτο και θα ανταγωνιστεί τις δυνατότητες του obefazimod της Abivax και του cobitolimod της InDex Pharmaceuticals. Υπο-
την αίτηση της Pfizer για νέο φάρμακο, θέτοντάς τη σε τροχιά έγκρισης το δεύτερο εξάμηνο του 2023. Οι ρυθμιστικές αρχές στην Ευρώπη έκαναν το ίδιο, με την απόφαση να αναμένεται το πρώτο εξάμηνο του 2024. Οι αποδοχές βασίστηκαν σε δεδομένα από τις μελέτες ELEVATE UC 12 και ELEVATE UC 52, οι οποίες έδειξαν ποσοστά κλινικής ύφεσης 25% και 32% στις 12 και 52 εβδομάδες, αντίστοιχα, σε ασθενείς με μέτρια έως σοβαρή UC, σε σύγκριση με ποσοστά 15% την Εβδομάδα 12 και 6,7% την Εβδομά-

11
8
9
Η Pfizer απέκτησε το υποψήφιο φάρμακο
για την ελκώδη
πωλήσεις έως το 2028 1,2 δισ. δολάρια.
Η απόκτηση της
σοτατερσέπτης ήταν
ο κύριος στόχος
της συμφωνίας
ύψους 11,5 δισ.
δολ. της Merck για
την εξαγορά της Acceleron το 2021,
η οποία μπορεί να
διασφαλίσει έως το 2028 πωλήσεις 1 δισ. δολαρίων.
δα 52 σε ασθενείς που έλαβαν εικονικό φάρμακο. Ακόμη επιτεύχθηκαν στατιστικά σημαντικές βελτιώσεις στα δευτερεύοντα καταληκτικά σημεία, συμπεριλαμβανομένης της ενδοσκοπικής βελτίωσης, της συμπτωματικής ύφεσης και της επούλωσης του βλεννογόνου στις εβδομάδες 12 και 52, καθώς και της ύφεσης χωρίς κορτικοστεροειδή και της παρατεταμένης κλινικής ύφεσης την εβδομάδα 52.
Θα μπορούσε να είναι η αρχή για μια άπαξ ημερησίως χορηγούμενη θεραπεία ανοσοφλεγμονωδών νόσων, ενδεχόμενο που βρίσκεται επίσης υπό διερεύνηση για τη γυροειδή αλωπεκία, την ατοπική δερματίτιδα, τη νόσο του Crohn και την ηωσινοφιλική οισοφαγίτιδα. Ο πρωταρχικός ανταγωνισμός της etrasimod στην UC φαίνεται να είναι το φάρμακο S1P Zeposia της Bristol Myers Squibb, το οποίο εγκρίθηκε για την UC τον Μάιο του 2021 και διερευνάται στις ίδιες ενδείξεις με την etrasimod. 10
Sotatercept των Acceleron
και Merck για την πνευμονική αρτηριακή υπέρταση Η απόκτηση της σοτατερσέπτης ήταν ο κύριος στόχος της συμφωνίας ύψους 11,5 δισ. δολ. της Merck για την εξαγορά της Acceleron το 2021. Θεωρήθηκε μάλιστα ότι μπορεί να αποτελέσει την αναγκαία επανάσταση για τη διαμόρφωση της νόσου στην πνευμονική αρτηριακή υπέρταση (ΠΑΥ). Σύμφωνα με την ετήσια

έκθεση, μπορεί να διασφαλίσει πωλήσεις έως το 2028 1 δισ. δολαρίων. Η sotatercept, μια πρωτεΐνη σύντηξης πρώτη στην κατηγορία της, αποτέλεσε στόχο της Merck στην προσπάθειά της να διαφοροποιηθεί από την ανοσο-ογκολογία και τη θεραπεία σούπερ σταρ για τον καρκίνο Keytruda. Τα θετικά κορυφαία στοιχεία που δημοσιεύθηκαν από μια δοκιμή Φάσης ΙΙΙ τον Οκτώβριο του 2022 ώθησαν τους αναλυτές στο να προσδιορίσουν τότε τις μέγιστες πωλήσεις της sotatercept στα 2 δισ. δολάρια.
Η σοτατερσέπτη είναι μια πρόσθετη θεραπεία στην καθιερωμένη θεραπεία. Με τον νέο μηχανισμό δράσης του, που στοχεύει στη σηματοδότηση του BMPR-II, το sotatercept θα μπορούσε ενδεχομένως να αντιμετωπίσει την υποκείμενη αιτία της ΠΑΥ, σε αντίθεση με τις τρέχουσες θεραπείες που στοχεύουν απλώς στα συμπτώματα μέσω της διαστολής των αιμοφόρων αγγείων. Ενώ οι τρέχουσες θεραπείες προσφέρουν ανακούφιση, δεν είναι θεραπευτικές. Η αξία του sotatercept ενισχύεται επίσης από το γεγονός ότι χορηγείται με ένεση κάτω από το δέρμα. Στην καταχωριστική μελέτη STELLAR με 324 ασθενείς, εκείνοι που έλαβαν σοτατερσέπτη παρουσίασαν βελτίωση στη δοκιμασία περπατήματος έξι λεπτών σε σχέση με εκείνους που έλαβαν εικονικό φάρμακο σε 24 εβδομάδες. Οι ασθενείς με σοτατερσέπτη είδαν επίσης στατιστικά σημαντικές βελτιώσεις σε οκτώ από τις εννέα δευτερογενείς μετρήσεις. Η Merck αναμένει να καταθέσει αίτηση για έγκριση στις αρχές του 2023.•••
12 ΡΕΠΟΡΤΑΖ / Μάρτιος-Απρίλιος 2023
Oπήχης ανέβηκε για τον αριθμό των φαρμακευτικών επενδύσεων στη χώρα, αφού, πλέον, φθάνουν τις 53 και ξεπερνούν σε αξία τα 519 εκατ. ευρώ για το 2023.
Ο κλάδος φαίνεται ότι διανύει εποχή «παχιών αγελάδων», καθώς από το 2022 τα αιτήματα για κλινικές μελέτες που κατατέθηκαν στον ΕΟΦ αυξήθηκαν. Συγκεκριμένα, υποβλήθηκαν 262 αιτήματα για ερευνητικά πρωτόκολλα φαρμάκων και ιατροτεχνολογικών προϊόντων, ενώ μια χρονιά πριν σχεδόν 100 λιγότερα.
Ο γενικός γραμματέας Υπηρεσιών Υγείας, Ιωάννης Κωτσιόπουλος, πολλάκις σε δηλώσεις του, έχει επισημάνει την εκρίζωση των εμποδίων αλλά και την πολιτική μέριμνας για την προώθηση της έρευνας στον φαρμακευτικό κλάδο. «Ούριο άνεμο» φαίνεται πως έφερε στον τομέα της έρευνας το επενδυτικό clawback και δημιουργήθηκε κλίμα αισιοδοξίας για την ανάπτυξη της καινοτομίας στη χώρα μας. Απώτερος σκοπός είναι να επωφεληθούν, το συντομότερο δυνατό, οι ασθενείς από νέα φάρμακα και ιατροτεχνολογικά προϊόντα, ιδίως εκείνοι με σοβαρά και απειλητικά για τη ζωή τους νοσήματα. Μέσα από την καινοτομία οι ασθενείς μπορούν να εξασφαλίσουν καλύτερη θεραπεία και αναβαθμισμένη ποιότητα ζωής. Μάλιστα, η θετική πτυχή που προέκυψε από την πανδημία ήταν η κατάδειξη της σημασίας της έρευνας, με χαρακτηριστικό παράδειγμα την άμεση ανάπτυξη εμβολίων, χάρη στις κλινικές μελέτες, που αποσκοπούσαν στην αντιμετώπιση του θανατηφόρου ιού.
Ο ρόλος του επενδυτικού clawback

Στα βήματα προόδου συνέβαλαν, σύμφωνα με τον κ. Κωτσιόπουλο, οι ευοίωνες συνθήκες που καλλιεργήθηκαν μέσα από δράσεις και κινήσεις της ηγεσίας. Προτεραιότητα, κατά τον σχεδιασμό του υπουργείου, δόθηκε στην προσέλκυση κλινικών μελετών στη χώρα μας. Στο πνεύμα αυτό, δημιουργήθηκε το επενδυτικό clawback, με τον συμψηφισμού αυτόματων επιστροφών και δαπανών για την έρευνα και την καινοτομία, όπως είναι οι κλινικές μελέτες.
Αναλυτικά, κατά την τελευταία διετία, οι αιτήσεις φακέλων για διεξαγωγή κλινικών μελετών αυξήθηκαν κατά 70%. Ειδικότερα, οι αιτήσεις για τη διεξαγωγή κλινικών μελετών στην Ελλάδα που δέχθηκε ο ΕΟΦ την προηγούμενη χρονιά έφθασαν τις 262 μελέτες για φάρμακα και ιατροτεχνολογικά προϊόντα.
Σημειώνεται πως, μία χρονιά πριν, το 2019, τα αιτήματα ήταν 154. Συνεπώς, με την άνθηση του κλάδου στη χώρα ευνοούνται τόσο οι ασθενείς όσο και η επιστήμη, αλλά και ο τομέας της οικονομίας.
Οι δε πόροι που εξασφαλίζονται επιστρέφουν στον φαρμακευτικό κλάδο, ενώ βοηθούν το επιστημονικό κεφάλαιο της χώρας να παραμείνει στην Ελλάδα, να αναπτυχθεί και να διακριθεί.
Συνολικά κατά την τελευταία τριετία, εκτιμάται ότι τα χρήματα που κατευθύνθηκαν στις κλινικές μελέτες σχεδόν διπλασιάστηκαν.
14 / Μάρτιος-Απρίλιος 2023
Ένα καλύτερο μέλλον
για τις κλινικές
μελέτες στην Ελλάδα
Ο ρόλος του επενδυτικού clawback και ποια άλλα μέτρα συνέβαλαν
ΡΕΠΟΡΤΑΖ
Αύξηση των επενδύσεων την τελευταία τριετία
Μέτρα με θετικό πρόσημο
Στην «ανθοφορία» συνέβαλε και η νομοθετική ρύθμιση (ν. 4950/2022) για τη χρόνια στρέβλωση στα νοσοκομεία του ΕΣΥ, η οποία αφορά σε έσοδα από τη διεξαγωγή βιοϊατρικής έρευνας. Με τη ρύθμι-
ση οι υγειονομικές μονάδες διαθέτουν τα έσοδα που διασφαλίζουν σε νέο ιατροτεχνολογικό εξοπλισμό ή στη βελτίωση των υποδομών τους. Επίσης, το Υπουργείο Υγείας μερίμνησε ώστε να δημιουργηθεί ένα εθνικό οικοσύστημα με μια εξειδικευμένη ομάδα εργασίας για τη βιοϊατρική έρευνα και τις κλινικές μελέτες. Στόχος
ήταν η αναβάθμιση διεξαγωγής των κλινικών μελετών, υλοποιώντας συνέργειες από όλο το φάσμα των εμπλεκομένων, από τις φαρμακευτικές επιχειρήσεις μέχρι


τους συλλόγους ασθενών.
Ο γενικός γραμματέας Υπηρεσιών Υγείας δίνει έμφαση τόσο στην άρση των εμποδίων όσο και στη δημιουργία κέντρων καινοτομίας, όπως αυτού της Pfizer στη συμπρωτεύουσα. Σε τέτοιες ερευνητικές «κυψέλες» υλοποιούνται σημαντικές συνεργασίες και δίνονται επαγγελματικές ευκαιρίες
σε νέες επιστήμονες.
Ο κ. Κωτσιόπουλος συμμετείχε σε συνάντηση εργασίας με περισσότερους από 70 συμμετέχοντες από τον χώρο των κλινικών μελετών στην Ελλάδα. Μετά από «ζυμώσεις», ετοίμασαν δράσεις και κατέληξαν σε πορίσματα σχετικά με την καλυτέρευση των σχετικών διεργασιών, και οι προσπάθειες αναβάθμισης «είδαν» αποτελέσματα. Άξια λόγου είναι και η παρέμβαση που προέκυψε με το άρθρο 83 του ν.4051 (ΦΕΚ 87/Α’/8-4-2023) για τη σύσταση Αυτοτελών Τμημάτων Κλινικών Μελετών στα νοσοκομεία του ΕΣΥ. Επιπλέον, έχει σχεδιαστεί
να διεξαχθούν εκπαιδευτικές δράσεις για όσους λαμβάνουν μέρος σε κλινικές μελέτες, ώστε να διασφαλιστούν προηγμένες πληροφορίες. Έχει ακόμη δρομολογηθεί η ανάπτυξη ενός οικοσυστήματος από νοσοκομεία «πιλότου» στην κλινική έρευνα, ως άξονα για την προτυποποίηση των σχετικών διαδικασιών. Επίσης, το επόμενο διάστημα, θα ολοκληρωθεί το «Εθνικό Μητρώο Βιοϊατρικής Έρευνας», ώστε να καταρτιστεί ένα ενιαίο ψηφιακό περιβάλλον, που θα αποτελέσει κοινό πεδίο τόσο για τους ερευνητές όσο και για τους πολίτες. Επιδίωξη είναι να προσφερθεί ορθή πληροφόρηση, αποβλέποντας στην προώθηση της Βιοϊατρικής Έρευνας στη χώρα. Επομένως, σύμφωνα με τον σχεδιασμό, θα εφαρμοστεί μια πρωτοπόρα στρατηγική για το σύστημα υγείας, θέτοντας έναν ασθενοκεντρικό πυρήνα και ως στόχευση την προσφορά ποιοτικών και αποδοτικών υπηρεσιών στους πολίτες.•••
15
Τα χρήματα που κατευθύνθηκαν στις κλινικές μελέτες σχεδόν διπλασιάστηκαν.
8 Μονάδες πανελλαδικά για την κατ’ οίκον περίθαλψη
Φροντίδα θα παρέχεται σε ένα πλαίσιο
εξειδικευμένης ασθενοκεντρικής προσέγγισης.
Kαινοτόμο σύστημα φροντίδας κατ’ οίκον θα αποκτήσει η χώρα μας, καθώς, με απόφαση του αναπληρωτή υπουργού Οικονομικών, επιδοτείται το έργο με τίτλο «Δημιουργία συστήματος Νοσοκομειακής Φροντίδας στο Σπίτι (ΝΟΣΠΙ)», το εντάσσεται στο Ταμείο Ανάκαμψης και Ανθεκτικότητας. Η δαπάνη υπολογίζεται σε 14.722.272 ευρώ, την ευθύνη των έργων έχει το Υπουργείο Υγείας και φορέας υλοποίησης έχει οριστεί ο Οργανισμός Διασφάλισης της Ποιότητας στην Υγεία. Ακόμη, προβλέπεται η συγκρότηση ομάδας ειδικών εμπειρογνωμόνων για την επιστημονική υποστήριξη και επιμέλεια του έργου. Στην προσπάθεια αυτή σύμμαχοι θα είναι η ιατροτεχνολογική πρόοδος, η ψηφιακή τεχνολογία και η ανάπτυξη εφαρμογών και συστημάτων εξ αποστάσεως παρακολούθησης των ασθενών, που εκτιμάται ότι θα ευνοήσουν την ασφαλή εφαρμογή της Νοσοκομειακής Φροντίδας στο Σπίτι με υψηλά πρότυπα ασφάλειας.
Με στόχο την κατ’ οίκον περίθαλψη, προβλέπεται έως το 2025 η ίδρυση 8 στελεχωμένων και λειτουργικών μονάδων που παρέχουν κατ’ οίκον περίθαλψη. Εξ αυτών δύο θα λειτουργήσουν στην Αθήνα, μία στη Θεσσαλονίκη, μία στην Αλεξανδρούπολη, μία στην Πάτρα, μία στα Ιωάννινα, μία στο Ηράκλειο και μία στη Λάρισα. Στον σχεδιασμό περιλαμβάνεται η ολοκλήρωση των ακόλουθων υποέργων:
α. έρευνας σχετικά με την «αξιολόγηση της τρέχουσας κατάστασης και των αναγκών», β. εφαρμογής τηλεϊατρικής: εγκατάσταση και θέση σε λειτουργία συσκευών και εξοπλισμού για πιλοτικό κέντρο κατ’ οίκον περίθαλψης, συμπεριλαμβανομένης της κατάρτισης, γ. εθνικού μητρώου ασθενών που νοσηλεύονται κατ’ οίκον, δ. κριτηρίων αξιολόγησης και βασικών δεικτών επιδόσεων (ΒΔΕ).
Η ιδιαιτερότητα των ασθενών
Σύμφωνα με τα στοιχεία που έχουν προκύψει από έρευνες για τους ασθενείς με σύνθετα προβλήματα υγείας –τα οποία συνήθως απαιτούν υποστήριξη ενός ή περισσότερων
οργάνων με τη βοήθεια της ιατρικής τεχνολογίας–, αυτοί αποτελούν μια ξεχωριστή ομάδα, που απαιτεί υπηρεσίες υγείας σε νοσοκομειακό επίπεδο και επίπεδο κοινότητας πέρα από αυτές που απαιτούνται συνήθως για μια χρόνια πάθηση. Εξαιτίας της βαρύτητας και της κλινικής πολυπλοκότητας που εμφανίζουν, η φροντίδα τους θα πρέπει να παρέχεται σε ένα πλαίσιο εξειδικευμένης ασθενοκεντρικής προσέγγισης, ώστε να επιτευχθεί η αποτελεσματική διαχείριση των συμπτωμάτων τους, να ικανοποιηθούν οι ανάγκες τους και να αποκτήσουν μια σχετική λειτουργικότητα στην καθημερινότητα, αποβλέποντας στη βελτίωση της ποιότητας ζωής τους.
16 / Μάρτιος-Απρίλιος 2023
Επιτέλους στην Ελλάδα
συγκροτημένο σύστημα
Φροντίδας στο Σπίτι Σχεδιάζεται
Νοσοκομειακής
σύστημα εξ αποστάσεως παρακολούθησης των ασθενών
ΡΕΠΟΡΤΑΖ
Μέχρι τώρα, στην Ελλάδα, η πλειοψηφία αυτών των περιπτώσεων γίνεται αποδέκτης φροντίδας για παρατεταμένο και επαναλαμβανόμενο χρόνο (συχνές εισαγωγές και επανεισαγωγές) σε νοσοκομειακό

επίπεδο, γεγονός που προκαλεί σημαντικές επιπτώσεις στην υγεία τους, στην ευημερία των οικογενειών καθώς και στο σύστημα υγειονομικής περίθαλψης. Συνεπώς, το έργο Νοσοκομειακής Φροντίδας στο Σπίτι αποσκοπεί στην ανάπτυξη υπηρεσιών παροχής Νοσοκομειακής Φροντίδας στο Σπίτι (ΝΟΣΠΙ) για την αναβάθμιση της ποιότητας ζωής των ασθενών και των οικογενειών τους, τη μείωση του κόστους φροντίδας και την αποσυμφόρηση των τριτοβάθμιων κέντρων παροχής φροντίδας. Όραμα είναι η διασφάλιση της παροχής ασφαλούς, μακροχρόνιας, ολιστικής, εξατομικευμένης φροντίδας
στους ασθενείς που πληρούν τα κριτήρια ένταξης στο πρόγραμμα.
Τα οφέλη από την εφαρμογή
Κέρδη όμως αναμένεται να διασφαλιστούν
και σε κρατικό επίπεδο, καθώς αναμένεται
να μειωθούν ο μέσος χρόνος νοσηλείας και οι επανεισαγωγές ασθενών με σύν-
θετα χρόνια νοσήματα, που χρήζουν υποστήριξης ενός ή περισσότερων συστημάτων. Ως αποτέλεσμα, θα ελευθερωθούν κλίνες και πόροι σε νοσοκομειακό επίπεδο, ενώ προβλέπεται ότι θα υπάρξει μείωση και των δεικτών λοίμωξης, καθώς θα μειωθεί ο βαθμός έκθεσης των ασθενών σε πολυανθεκτικά στελέχη και ο κίνδυνος ενδονοσοκομειακής μετάδοσης. Παράλληλα, θα είναι πιο εύκολη η παρακολούθηση της συμμόρφωσης των ασθενών στη μακροχρόνια θεραπεία. Θετικές θα είναι οι επιπτώσεις και στη μείωση του άμεσου και έμμεσου κόστους φροντίδας τόσο για τα συστήματα υγείας όσο και για τους ασθενείς και τις οικογένειές τους. Απαραίτητη προϋπόθεση για την επίτευξη των παραπάνω στόχων είναι η οργάνωση της βέλτιστης κατ’ οίκον ιατρονοσηλευτικής φροντίδας τους, με αυστηρές συνθήκες ασφάλειας, που για να επιτευχθεί απαιτείται ένα καλά οργανωμένο δίκτυο υποστήριξης από εξειδικευμένο προσωπικό. Στο πλαίσιο του έργου, θα πραγματοποιηθεί μελέτη της υφιστάμενης κατάστασης και εκτίμησης των αναγκών μέσω έρευνας για τη διερεύνηση «καλών πρακτικών» ί-

17
Θα ελευθερωθούν
κλίνες και πόροι σε νοσοκομειακό
επίπεδο, ενώ προβλέπεται ότι θα υπάρξει μείωση και των δεικτών λοίμωξης.
Δράσεις ενημέρωσης
και ευαισθητοποίησης
καθώς και υποστήριξης της
διαχείρισης της
αλλαγής εντός των νοσοκομείων και φορέων για την
εξασφάλιση της
βιωσιμότητας του προγράμματος.
δρυσης κέντρων φροντίδας στο σπίτι για παιδιά, εφήβους και ενήλικες, σε άλλες χώρες. Επίσης, θα υπάρξει καταγραφή
των αναγκών και της υφιστάμενης κατάστασης στην Ελλάδα στον τομέα της υγειονομικής περίθαλψης στο σπίτι.
Εκτός από τον καθορισμό των 8 κέντρων αναφοράς που θα υποστηρίζουν τη λειτουργία των προγραμμάτων παροχής Νοσοκομειακής Φροντίδας στο Σπίτι, θα οριστούν οι προϋποθέσεις ασφαλούς λειτουργίας. Ακόμη, θα γίνει ανασκόπηση της εθνικής και διεθνούς εμπειρίας (καλές πρακτικές) και αποτύπωση της παρούσας κατάστασης για παιδιά, εφήβους και ενήλικες.
Στο πλαίσιο της προετοιμασίας, θα καθοριστεί ο πληθυσμός-στόχος, όπως και τα κριτήρια δυνητικής επιλεξιμότητας για παιδιά, εφήβους και ενήλικες. Επιπλέον, προβλέπεται η καταγραφή των αναγκών ασθενών και οικογενειών/φροντιστών και η αναλυτική περιγραφή του μοντέλου λειτουργίας ΝΟΣΠΙ με συγκρότηση ομάδας εμπειρογνωμόνων κ.ά. Επίσης, ο καθορισμός των κριτηρίων ένταξης/αποκλεισμού
από το πρόγραμμα με συγκρότηση ομάδας εμπειρογνωμόνων, η καταγραφή απαιτήσεων πληροφοριακής οργάνωσης και διαλειτουργικότητας κ.ά.
Τροποποίηση του υπάρχοντος θεσμικού
πλαισίου
Για την υλοποίηση του έργου θα πραγματοποιηθεί η ανάλυση και η προσαρμογή του υπάρχοντος θεσμικού πλαισίου για τη λειτουργία του ΝΟΣΠΙ. Το αρμόδιο επιτελείο θα προβεί σε ανασκόπηση του υπάρχοντος θεσμικού πλαισίου και θα αναπτύξει προτεινόμενο νομοθετικό πλαίσιο λειτουργίας του ΝΟΣΠΙ. Ακόμη, προβλέπεται η θεσμοθέτηση νοσηλευτικής εξειδίκευσης στην παροχή Νοσοκομειακής Φροντίδας στο Σπίτι, ενώ θα διερευνηθεί το θεσμικό πλαίσιο για τις ιατρικές αρμοδιότητες στην παροχή Νοσοκομειακής Φροντίδας στο Σπίτι και το πλαίσιο για τη διατήρηση των ομάδων ΝΟΣΠΙ και μετά το πέρας του προγράμματος.
στο σπίτι ασθενών ΝΟΣΠΙ. Με το σκεπτικό αυτό τίθενται οι βασικές παράμετροι παρακολούθησης του πληροφοριακού συστήματος, το οποίο θα λειτουργεί και ως μητρώο ασθενών των ωφελουμένων. Πέρα από τα δημογραφικά στοιχεία, θα αναφέρονται η διάγνωση του νοσήματος, τα στοιχεία της θεραπείας, η πορεία της νόσου, τα φάρμακα και ο τεχνολογικός εξοπλισμός κ.ά.
Σημειώνεται ότι θα παρέχεται δυνατότητα πρόσβασης στο προσωπικό ΝΟΣΠΙ τόσο από το νοσοκομείο όσο και από το σπίτι του ασθενούς και θα υποστηρίζεται η εξ αποστάσεως παρακολούθηση των ασθενών μέσω εμφυτεύσιμων ή φορητών συσκευών καταγραφής.
Άξιο αναφοράς είναι το γεγονός πως το πληροφοριακό σύστημα θα παρέχει τη δυνατότητα διαλειτουργικότητας με τα τοπικά πληροφοριακά συστήματα του Κέντρου Αναφοράς, εφόσον απαιτείται. Θα έχει επίσης τη δυνατότητα διαλειτουργικότητας με όλες τις συσχετιζόμενες υπηρεσίες (ΕΟΠΥΥ, ΗΔΙΚΑ, ΚΑ, eΔΑΠΥ, ΣΗΠ, ΕΟΦ, ΑΗΦΥ κ.λπ.).
Σε μια συγκρατημένη προσπάθεια, προβλέπεται και η ανάπτυξη πλαισίου για τη Διασφάλιση της Ποιότητας των παρεχόμενων υπηρεσιών, στο πλαίσιο της εφαρμογής του προγράμματος, με βασικούς δείκτες απόδοσης. Ακόμη σχεδιάστηκε η εκπαίδευση και η κατάρτιση του προσωπικού των κέντρων με διασύνδεση με ανάλογα κέντρα του εξωτερικού και εκπαιδευτικές επισκέψεις σε κέντρα του εξωτερικού, με σκοπό τη μεταφορά γνώσης και καλών πρακτικών.
Σχετικά με την πρόσληψη του προσωπικού, θα δημιουργηθεί μια επιτροπή αξιολόγησης από τον ΟΔΙΠΥ η οποία θα επιλέγει το κατάλληλο προσωπικό λαμβάνοντας υπόψη την εμπειρία του υποψηφίου, την ακαταλληλότητα κ.λπ.
Απαραίτητη κρίνεται η ανάπτυξη ενός πληροφοριακού συστήματος εξ αποστάσεως παρακολούθησης των ασθενών.
Επιδίωξη είναι η στήριξη της φροντίδας
Αξιοσημείωτο είναι το ότι έχουν προβλεφθεί και δράσεις ενημέρωσης και ευαισθητοποίησης καθώς και υποστήριξης της διαχείρισης της αλλαγής εντός των νοσοκομείων και των φορέων, με άξονα την εξασφάλιση της βιωσιμότητας του προγράμματος, λαμβάνοντας υπόψη τη γραφειοκρατικής δομή, την επικρατούσας πρακτική, τον φόβο της αλλαγής, τους περιορισμούς της νομοθεσίας κ.ά. Στόχος είναι η ολοκληρωμένη πληροφόρηση για τη σημασία του προγράμματος ΝΟΣΠΙ τόσο στην επιστημονική κοινότητα όσο και στον γενικό πληθυσμό σε θέματα που αφορούν τη νοσοκομειακή φροντίδα.•••
18 ΡΕΠΟΡΤΑΖ / Μάρτιος-Απρίλιος 2023
Σύστημα εξ αποστάσεως
παρακολούθησης των ασθενών
20
Έρευνα
Η ανταπόκριση
της ανοσοθεραπείας στο προχωρημένο
μελάνωμα
28 Ρεπορτάζ
Λευχαιμίες: Ελπίδες από νέες θεραπείες
32
Ρεπορτάζ
«Κλειδί» οι μεταλλάξεις
στα επιθετικά
λεμφώματα
42 Άρθρο
Εξελίξεις στο λέμφωμα Hodgkin
αφιέρωμα
αιματολογία
Τι δείχνει
Τα τελευταία
χρόνια, έχουν αναπτυχθεί και χρησιμοποιούνται
νέες ανοσοθεραπείες, που ονομάζονται αναστολείς σημείου ελέγχου PD-1.
Ηανταπόκριση της ανοσοθεραπείας σε ασθενείς με προχωρημένο μελάνωμα εξαρτάται από προηγούμενες θεραπείες, όπως δείχνει νέα μελέτη, που δημοσιεύτηκε πρόσφατα στο Cancer Cell. Ειδικότερα, ερευνητές από το UCLA Jonsson Comprehensive Cancer Center διαπίστωσαν ότι η ανταπόκριση σε έναν τύπο νέων ανοσοθεραπειών, που ονομάζονται αναστολείς σημείου ελέγχου PD-1, σε ασθενείς με προχωρημένο μελάνωμα εξαρτώνται από το αν είχαν λάβει προηγουμένως άλλη ανοσοθεραπεία –αποκλεισμό CTLA-4– καθώς και από άλλους παράγοντες.
Τα ευρήματά τους βασίζονται στην ανάλυση επτά συνόλων δεδομένων, που δημιουργήθηκαν την τελευταία δεκαετία, τα οποία περιελάμβαναν αποτελέσματα βιοψιών όγκου από περισσότερους από 500 ασθενείς.
Οι αναστολείς PD-1
Το ανθρώπινο ανοσοποιητικό σύστημα αποτελείται, εκτός των άλλων, και από Τ-κύτταρα, που συμβάλλουν στην καταπολέμηση των ασθενειών. Τα Τ-κύτταρα βοηθούν τον οργανισμό στην καταπολέμηση των λοιμώξεων και άλλων ασθενειών, όπως ο καρκίνος. Ωστόσο, τα καρκινικά κύτταρα έχουν την ικανότητα να ξεφεύγουν των Τ-κυττάρων, εκφράζοντας μια πρωτεΐνη που λέγεται PD-L1, η οποία λειτουργεί ως «στοπ» και αδρανοποιεί τα Τ-κύτταρα.
Μια νέα προσέγγιση, λοιπόν, για την καταπολέμηση του καρκίνου είναι η καταστολή της πρωτεΐνης PD-L1, μέσω της οποίας τα καρκινικά κύτταρα παύουν να αδρανοποιούν τα Τ-κύτταρα μέσω των υποδοχέων PD-1 και B7.1. Προς την κατεύθυνση αυτή, τα τελευταία χρόνια, έχουν αναπτυχθεί και χρησιμοποιούνται νέες ανοσοθεραπείες που έχουν αυτόν ακριβώς τον σκοπό και ονομάζονται αναστολείς σημείου ελέγχου PD-1.
Όταν ένας ασθενής διαγνωστεί με προχωρημένο μελάνωμα, συνήθως αντιμετωπίζεται με ανοσοθεραπείες, όπως αναστολείς PD-1 ή αναστολείς CTLA-4, σε συνδυασμό ή με μονοθεραπεία. Μπλοκάροντας διαφορετικές πρωτεΐνες που μειώνουν την αποτελεσματικότητα των Τ-κυττάρων, αυτοί οι αναστολείς του σημείου ελέγχου ενισχύουν την ανοσοαπόκριση του οργανισμού στον καρκίνο.
Τι λένε οι ερευνητές
«Στο μεγάλο μας σύνολο δεδομένων, οι εξετάσεις που έχουν χρησιμοποιηθεί για την πρόβλεψη της ανταπόκρισης στη θεραπεία με αναστολείς σημείων ελέγχου PD-1 –που ονομάζονται βιοδείκτες– σχετίζονται με την παρουσία ορισμένων τύπων ανοσοκυττάρων στον όγκο και το γενετικό προφίλ των ίδιων των όγκων, που τροποποιήθηκαν από το ιστορικό θεραπείας ενός ασθενούς» δήλωσε η επικεφαλής συγγραφέας Katie Campbell, μεταδιδακτορική υπότροφος στην Αιματολογία/Ογκολογία στο UCLA
20 / Μάρτιος-Απρίλιος 2023 ΕΡΕΥΝΑ
Η
ανταπόκριση της ανοσοθεραπείας στο προχωρημένο μελάνωμα
μελέτη σε 500 ασθενείς Εξαρτάται από προηγούμενες θεραπείες, σύμφωνα με νέα μελέτη
Jonsson Comprehensive Cancer Center. «Ως μεταφραστικοί επιστήμονες, όταν εργαζόμαστε με κλινικούς γιατρούς, ένας από τους στόχους είναι να σκεφτούμε πώς μπορούν να χρησιμοποιηθούν οι βιοδείκτες για να ενημερώσουν το κλινικό όφελος. Αν μπορούμε να προβλέψουμε ποιοι ασθενείς ανταποκρίνονται ή δεν πρόκειται


να ανταποκριθούν στη θεραπεία από τη
μελέτη των βιοψιών τους, αυτό μπορεί να αρχίσει να ορίζει πιο στρατηγικά ποιες θεραπείες ή συνδυασμοί θεραπειών πρέπει να χρησιμοποιούνται και πότε» σημειώνει. «Δεδομένου ότι το τρέχον παράδειγμα θεραπείας για το μελάνωμα περιλαμβάνει συνδυασμούς ή διαδοχική χρήση θεραπειών σημείων ελέγχου του ανοσοποιητικού, η μελέτη μας αναδεικνύει πώς αυτές οι θεραπείες μπορούν να συνεργαστούν για την αποτελεσματική θεραπεία του μελανώματος. Υπογραμμίζει επίσης τη σημασία του ιστορικού προηγούμενης θεραπείας ενός ασθενούς ως τροποποιητικού παράγοντα που πρέπει να λαμβάνεται υπόψη κατά τον σχεδιασμό μιας στρατηγικής θεραπείας» τονίζει ο δρ Antoni Ribas, ανώτερος συγγραφέας, διευθυντής του προγράμματος Ανοσολογίας στο UCLA Jonsson Comprehensive Cancer Center.
της μελέτης
Αν και η ανοσοθεραπεία γίνεται ολοένα
και πιο συχνή στη θεραπεία καρκίνων τελικού σταδίου, οι περισσότερες μελέτες για βιοδείκτες και παράγοντες που καθορίζουν την αποτελεσματικότητα βασίζονται σε μικρές σειρές δειγμάτων. Ως εκ τούτου, η διεπιστημονική και πολυκεντρική ερευνητική ομάδα ξεκίνησε να συγκεντρώνει έναν μεγάλο σύνολο όγκων και κλινικών δεδο-
μένων από ασθενείς με μελάνωμα, για να εντοπίσει βασικούς παράγοντες που σχετίζονται με την ανταπόκριση στη θεραπεία. «Η συνεκτική επεξεργασία συνόλων κλινικών δεδομένων απαιτεί συνεργασία μεταξύ ειδικών με γνώσεις στην επιστήμη των υπολογιστών, τη Στατιστική, τη Βιολογία, την Ανοσοθεραπεία, την Πληροφορική και τη Μεταφραστική και Κλινική Ιατρική. Αναλάβαμε αυτό το έργο για να δημιουργήσουμε έναν πόρο για άλλους ερευνητές, με στόχο τον στατιστικό προσδιορισμό με σημαντικές συσχετίσεις των αποκρίσεων μελανώματος στη θεραπεία με αναστολείς του PD-1» αναφέρει η Campbell. «Καθώς κάναμε τις αναλύσεις, οι μεγαλύτερες διαφορές παρατηρήθηκαν όταν λάβαμε υπόψη την προηγούμενη θεραπεία ενός ασθενούς με αναστολείς του CTLA-4» πρόσθεσε. «Το πλαίσιο στο οποίο συλλέγεται μια βιοψία πρέπει να εξεταστεί για να καθοριστεί καλύτερα ο τρόπος με τον οποίο θα πρέπει να εφαρμόζονται οι βιοδείκτες στο κλινικό περιβάλλον». Οι ερευνητές λένε ότι, επεξεργαζόμενοι τα δεδομένα αλληλουχίας DNA και RNA από εκατοντάδες ασθενείς, μπόρεσαν να βγάλουν συμπεράσματα για ορισμένες από τις μεγάλες διαφορές που υπάρχουν μεταξύ ασθενών, όγκων και ιστορικών θεραπείας. Εξέτασαν, επίσης, κλινικά δημογραφικά στοιχεία που μπορεί να είναι σημαντικά για την κατανόηση του γιατί ένας ασθενής ανταποκρίθηκε ή δεν ανταποκρίθηκε στη θεραπεία με αναστολείς PD-1. Αν και τα αποτελέσματα δεν εξηγούν συγκεκριμένα το πώς ή το πότε πρέπει να εφαρμοστούν κλινικά οι πληροφορίες του βιοδείκτη, παρέχουν μια βάση και έναν «οδικό χάρτη».•••
Οι ερευνητές, επεξεργαζόμενοι
τα δεδομένα
αλληλουχίας
DNA και RNA
από εκατοντάδες
ασθενείς, μπόρεσαν
να βγάλουν
συμπεράσματα
για ορισμένες
από τις μεγάλες
διαφορές που
υπάρχουν μεταξύ
ασθενών, όγκων
και ιστορικών
θεραπείας.
21 ΑΦΙΕΡΩΜΑ ΑΙΜΑΤΟΛΟΓΙΑ
Η σημασία
Το 76% των
ασθενών πέτυχε
ύφεση και το
33% εμφάνισε σύνδρομο
νευροτοξικότητας, μια κοινή
παρενέργεια της
θεραπείας με
CAR-T.
Συνολικά το 76% των ασθενών πέτυχαν ύφεση της νόσου!
CAR-T:
Το 20% υποφέρει από επίμονα σωματικά
Oι νέες θεραπείες τύπου CAR-Τ βελτιώνουν σημαντικά την ποιότητα ζωής των ασθενών με αιματολογικούς καρκίνους, σύμφωνα
με νέα μελέτη που δημοσιεύτηκε στο Blood Advances. Ωστόσο, ένας στους πέντε ασθενείς αντιμετωπίζει επίμονα συμπτώματα
έως και 6 μήνες μετά τη θεραπεία, που μειώνουν την ποιότητα ζωής του.
Οι θεραπείες CAR-T έχουν μεταμορφώσει τη θεραπεία ορισμένων μορφών καρκίνου, ωστόσο λίγες μελέτες έχουν διερευνήσει τον αντίκτυπο των θεραπειών αυτών στην ποιότητα ζωής του ασθενούς –μια πτυχή της φροντίδας που συχνά πλήττεται από τη λήψη των παραδοσιακών θεραπειών, όπως η χημειοθεραπεία.
Οι θεραπείες CAR-T βασίζονται στον επαναπρογραμματισμό του ανοσοποιητικού συστήματος, ώστε να επιτίθεται στα καρκινικά κύτταρα. Είναι ένας τύπος γονιδιακής ή κυτταρικής θεραπείας. Προς το παρόν, χρησιμοποιείται για τη θεραπεία καρκίνων του αίματος, όμως αποτελεί μια πολλά υποσχόμενη μέθοδο, με πιθανές μελλοντικές χρήσεις και σε άλλους τύπους καρκίνου.
«Η τεχνολογία CAR-T έφερε επανάσταση στη θεραπεία ασθενών με υποτροπιάζοντες και ανθεκτικούς καρκίνους του αίματος. Ωστόσο, παραμένει μια θεραπεία με μοναδικές τοξικότητες, συμπεριλαμβανομένου του συνδρόμου απελευθέρωσης κυτοκίνης, μια δυνητικά απειλητική για τη ζωή πάθηση, που μπορεί να προκαλέσει πυρετό, έμετο, δύσπνοια, πόνο και υπότα-
ση, καθώς και νευρολογικές τοξικότητες. Και αυτές οι επιπλοκές μπορεί να επιβαρύνουν τους ασθενείς. Δεδομένης της σχετικά νέας εξέλιξης των θεραπειών CAR-T, υπάρχουν λίγες μελέτες που έχουν εξετάσει τα αποτελέσματα στην ποιότητα ζωής σε όσους λαμβάνουν αυτές τις θεραπείες» αναφέρει ο Connor Johnson, ογκολόγος στο Γενικό Νοσοκομείο της Μασαχουσέτης και επικεφαλής της μελέτης.
Η μελέτη
Για τη διεξαγωγή αυτής της μελέτης οι ερευνητές ενέταξαν 103 ασθενείς ηλικίας 23-90 ετών με διάγνωση καρκίνου του αίματος από τον Απρίλιο του 2019 έως τον Νοέμβριο του 2021. Από αυτούς τους ασθενείς το 71% διαγνώστηκε με λέμφωμα, το 28% με μυέλωμα και το 1% με οξύ Β-κύτταρο λεμφοβλαστική λευχαιμία.
Στους ασθενείς που ήταν κατάλληλοι να λάβουν θεραπεία CAR-T χορηγήθηκε πιο συχνά tisagenlecleucel (34%), lisocabtagene maraleucel (16%), axicabtagene ciloleucel (13%) και idecabtaene vicleucel (12%).
Οι ερευνητές χορήγησαν αυτοαναφερόμενα ερωτηματολόγια που μετρούσαν μεταβλητές ποιότητας ζωής σε χρονικά διαστήματα μεταξύ των οποίων πριν από την έγχυση κυττάρων CAR-T και μία εβδομάδα, έναν μήνα, τρεις μήνες και έξι μήνες μετά την έγχυση κυττάρων CAR-T. Η ποιότητα ζωής μετρήθηκε χρησιμοποιώντας ένα ερωτηματολόγιο 27 στοιχείων, γνωστό ως Functional Assessment of Cancer Therapy-General (FACT-G), το
22 / Μάρτιος-Απρίλιος 2023 ΕΡΕΥΝΑ
Θεραπείες
Βελτιώνουν την ποιότητα ζωής
και ψυχολογικά
συμπτώματα
οποίο μετρά τους παράγοντες ποιότητας ζωής χρησιμοποιώντας τέσσερις διαφορετικές υποκλίμακες (σωματική, λειτουργική, συναισθηματική και κοινωνική) σε
όλα τα χρονικά σημεία. Η ψυχολογική δυσφορία μετρήθηκε χρησιμοποιώντας την Κλίμακα Hospital Anxiety and Depression Scale (HADS).
Τέλος, τα μείζονα καταθλιπτικά συμπτώματα μετρήθηκαν επίσης χρησιμοποιώντας
το PHQ-9 και τα συμπτώματα της διαταραχής μετατραυματικού στρες μετρήθηκαν χρησιμοποιώντας τη λίστα ελέγχου μετατραυματικού στρες. Οι ερευνητές κατέγραψαν επίσης σωματικά συμπτώματα χρησιμοποιώντας το Edmonton Symptom Assessment System, το οποίο αξιολόγησε τον πόνο, την κόπωση, την υπνηλία, τη ναυτία, την όρεξη, τη δύσπνοια, την αϋπνία, τη δυσκολία στην κατάποση και την ευεξία σε διάστημα 24 ωρών. Συνολικά, το 76% των ασθενών πέτυχε ύφεση και το 33% εμφάνισε σύνδρομο νευροτοξικότητας, μια κοινή παρενέργεια της θεραπείας με CAR-T. Αξίζει να σημειωθεί
ότι το 38% των ασθενών δεν επέζησε κατά τη διάρκεια της παρακολούθησης
για τη μελέτη.
Οι ερευνητές ενδιαφέρθηκαν, συγκεκριμένα, να κατανοήσουν πώς η CAR-T θεραπεία επηρέασε την ποιότητα ζωής των ασθενών. Διαπίστωσαν ότι για τα περισσό-
τερα άτομα η ποιότητα ζωής αρχικά μειώθηκε την πρώτη εβδομάδα μετά τη χορήγηση της θεραπείας (μειώνοντας από
μια μέση τιμή αναφοράς 77,9 σε 70,1), μια περίοδο στην οποία τα συμπτώματα που σχετίζονται με τη θεραπεία είναι συνήθως στο αποκορύφωμά τους και στη συνέχεια αυξήθηκε σημαντικά (σε διάμεσο 83,7) έξι μήνες μετά την έγχυση. Ομοίως, βρήκαν βελτιώσεις στο βάρος των σωματικών συμπτωμάτων, καθώς και στα συμπτώματα άγχους. Ενώ οι περισσότεροι συμμετέχοντες στη μελέτη παρουσίασαν τελικά βελτίωση στην ποιότητα ζωής τους, περίπου το 20% των ασθενών παρουσίασαν επίμονα σωματικά και ψυχολογικά συμπτώματα, τα οποία κατά καιρούς ήταν επιζήμια για την ποιότητα ζωής τους. Ο δρ Johnson εξηγεί ότι είναι σημαντικό να αναγνωρίσουμε το βάρος που επιφέρει η θεραπεία με CAR-T σε ορισμένους ασθενείς, για να μεγιστοποιηθεί η αποτελεσματικότητα αυτών των θεραπειών και να βελτιωθεί η φροντίδα για όλα τα άτομα που ζουν με αιματολογικές κακοήθειες.
«Εδώ δείχνουμε σημαντικές βελτιώσεις στην
σημειώθηκαν
στην ποιότητα
ζωής σε ασθενείς
ποιότητα ζωής σε ασθενείς με μια σειρά από διαγνώσεις καρκίνου του αίματος που λαμβάνουν μια ποικιλία θεραπειών CART» λέει ο δρ Johnson. «Ωστόσο, εντοπίζουμε επίσης ένα ξεχωριστό υποσύνολο ασθενών που έχουν επίμονη σωματική και ψυχολογική επιβάρυνση, ακόμη και στο εξάμηνο μετά τη χορήγηση της θεραπείας. Ελπίζω ότι αυτά τα ευρήματα οδηγούν σε πρόσθετες παρεμβάσεις με στόχο τη βελτίωση της συνολικής τροχιάς ποιότητας ζωής όλων των ασθενών».•••
23 ΑΦΙΕΡΩΜΑ ΑΙΜΑΤΟΛΟΓΙΑ
Σημαντικές βελτιώσεις
με μια σειρά από
διαγνώσεις καρκίνου του αίματος που λαμβάνουν μια ποικιλία θεραπειών CAR-T.
Σχεδόν κάθε
ασθενής που
αναπτύσσει οξεία
λευχαιμία μετά
από ιστορικό
μυελοϋπερπλαστικών
νεοπλασμάτων θα
πεθάνει από τη νόσο.
Nέα μελέτη προτείνει μια καινούργια στρατηγική για την πρόληψη της εξέλιξης της χρόνιας λευχαιμίας σε επιθετική νόσο. Η μελέτη δημοσιεύθηκε πρόσφατα στο περιοδικό Nature Cancer και αναδεικνύει νέους στόχους για φαρμακευτική θεραπεία. Ένας τύπος χρόνιας λευχαιμίας μπορεί να σιγοβράζει για πολλά χρόνια. Μερικοί ασθενείς μπορεί να χρειαστούν θεραπεία για τη διαχείριση αυτών των τύπων καρκίνου του αίματος –που ονομάζονται μυελοϋπερπλαστικά νεοπλάσματα (MPN)– ενώ άλλοι μπορεί να περάσουν από μεγάλες περιόδους άγρυπνης αναμονής.
Αλλά για ένα μικρό ποσοστό ασθενών η πιο αργή νόσος μπορεί να μετατραπεί σε επιθετικό καρκίνο, που ονομάζεται δευτεροπαθής οξεία μυελογενής λευχαιμία, που έχει λίγες αποτελεσματικές θεραπευτικές επιλογές. Πολύ λίγες πληροφορίες
είναι γνωστές για το πώς λαμβάνει χώρα αυτή η μεταμόρφωση και αν μπορεί να προληφθεί.
Όμως, τώρα, οι ερευνητές της Ιατρικής Σχολής του Πανεπιστημίου της Ουάσιγκτον εντόπισαν ένα σημαντικό σημείο στη μετάβαση από τη χρόνια στην επιθετική λευχαιμία. Έδειξαν ότι η παρεμπόδιση ενός βασικού μορίου στην οδό μετάβασης αποτρέπει αυτήν την επικίνδυνη εξέλιξη της νόσου σε ποντίκια με μοντέλα της νόσου και σε ποντίκια με όγκους που ελήφθησαν από ανθρώπους ασθενείς.
Η δευτεροπαθής οξεία μυελογενής λευχαι-
μία έχει δυσοίωνη πρόγνωση. Σχεδόν κάθε ασθενής που αναπτύσσει οξεία λευχαιμία μετά από ιστορικό μυελοϋπερπλαστικών νεοπλασμάτων θα πεθάνει από τη νόσο. Ως εκ τούτου, κύριος στόχος της έρευνάς μας είναι να κατανοήσουμε καλύτερα αυτή τη μετατροπή από χρόνια σε επιθετική νόσο και να αναπτύξουμε καλύτερες θεραπείες και, ελπίζουμε, στρατηγικές πρόληψης για αυτούς τους ασθενείς» τονίζει ο Stephen T. Oh, αναπληρωτής καθηγητής Ιατρικής στο Τμήμα Αιματολογίας της Ιατρικής Σχολής του Πανεπιστημίου της Ουάσιγκτον στο Σεντ Λούις.
Η μελέτη αναδεικνύει το γεγονός ότι η αναστολή ενός μορίου που ονομάζεται DUSP6 βοηθά να ξεπεραστεί η αντίσταση που αναπτύσσουν συχνά αυτοί οι καρκίνοι στους αναστολείς JAK2, τη θεραπεία που χρησιμοποιείται συνήθως για την αντιμετώπισή τους. Οι αναστολείς JAK2 είναι μια αντιφλεγμονώδης θεραπεία που χρησιμοποιείται επίσης για τη θεραπεία της ρευματοειδούς αρθρίτιδας.
«Αυτοί οι ασθενείς συνήθως αντιμετωπίζονται με αναστολείς JAK2, αλλά η ασθένειά τους εξελίσσεται, παρά αυτήν τη θεραπεία, επομένως προσπαθούμε επίσης να προσδιορίσουμε πώς η νόσος μπορεί
να επιδεινωθεί ακόμη και στο πλαίσιο της αναστολής JAK2» αναφέρει ο Oh.
Οι ερευνητές πραγματοποίησαν μια έρευνα σε βάθος στη γενετική αυτών των όγκων, τόσο κατά τη διάρκεια της αργής χρόνιας φάσης όσο και μετά τη μετατρο-
24 / Μάρτιος-Απρίλιος 2023 ΡΕΠΟΡΤΑΖ
Δευτεροπαθής
Πώς η χρόνια λευχαιμία εξελίσσεται σε επιθετική νόσο Σημαντική ανακάλυψη από Αμερικανούς ερευνητές για νέους στόχους θεραπείας
οξεία μυελογενής
λευχαιμία: Μπορεί να προληφθεί;
πή της νόσου στην επιθετική μορφή, ενώ οι ασθενείς έπαιρναν αναστολείς JAK2. Το γονίδιο DUSP6 ξεχώρισε ως εξαιρετικά εκφρασμένο στους 40 ασθενείς των οποίων οι όγκοι αναλύθηκαν σε αυτήν τη μελέτη.
Η χρήση γενετικών τεχνικών για τη διαγραφή του γονιδίου DUSP6 απέτρεψε τη μετάβαση σε επιθετική ασθένεια σε ποντίκια με μοντέλα αυτού του καρκίνου. Οι ερευνητές δοκίμασαν επίσης μια ένωση φαρμάκου που αναστέλλει το DUSP6 και διαπίστωσαν ότι η ένωση –διαθέσιμη μόνο για έρευνα σε ζώα– σταμάτησε την εξέλιξη της χρόνιας νόσου στην επιθετική νόσο σε δύο διαφορετικά μοντέλα ποντικών και σε ποντίκια με ανθρώπινους όγκους που ελήφθησαν από ασθενείς. Η μείωση των επιπέδων DUSP6, τόσο γενετικά όσο και με ένα φάρμακο, μείωσε επίσης τη φλεγμονή σε αυτά τα μοντέλα.
Δεδομένου του ότι το φάρμακο που αναστέλλει το DUSP6 δεν είναι διαθέσιμο για κλινικές δοκιμές σε ανθρώπους, ο Oh και οι συνεργάτες του ενδιαφέρονται να μελετήσουν θεραπείες που αναστέλλουν ένα
άλλο μόριο που ανακάλυψαν ότι ενεργοποιείται από το DUSP6 και που έδειξαν ότι απαιτείται επίσης για τη διαιώνιση των αρνητικών επιπτώσεων του DUSP6.
Υπάρχουν φάρμακα σε κλινικές δοκιμές
που αναστέλλουν αυτό το μόριο, που είναι γνωστό ως RSK1. Η ομάδα του Oh ενδιαφέρεται να διερευνήσει αυτά τα φάρμακα για τη δυνατότητά τους να μπλοκάρουν την επικίνδυνη μετάβαση από χρόνια σε
επιθετική νόσο και να αντιμετωπίσουν την αντίσταση στην αναστολή του JAK2. «Μια μελλοντική κλινική δοκιμή θα μπορούσε να περιλαμβάνει ασθενείς με μυελοπολλαπλασιαστικό νεόπλασμα που λαμβάνουν αναστολείς JAK2 και, παρ’ όλα αυτά, έχουν σημάδια επιδείνωσης της νόσου τους» τονίζει ο Oh. «Σε εκείνο το σημείο, θα μπορούσαμε να προσθέσουμε τον τύπο του αναστολέα RSK που βρίσκεται τώρα σε δοκιμές στη θεραπεία τους, για να δούμε αν αυτό βοηθά στην παρεμπόδιση της εξέλιξης της νόσου σε επιθετική δευτεροπαθή οξεία μυελογενή λευχαιμία. Ένας πρόσφατα αναπτυγμένος αναστολέας RKS βρίσκεται σε κλινικές δοκιμές φάσης Ι για ασθενείς με καρκίνο του μαστού, επομένως ελπίζουμε ότι η δουλειά μας παρέχει μια πολλά υποσχόμενη βάση για την ανάπτυξη μιας νέας στρατηγικής θεραπείας για ασθενείς με αυτόν τον χρόνιο καρκίνο του αίματος».•••
Η χρήση γενετικών τεχνικών για τη διαγραφή
του γονιδίου DUSP6 απέτρεψε τη μετάβαση
σε επιθετική ασθένεια σε ποντίκια με μοντέλα
αυτού του καρκίνου.
25 ΑΦΙΕΡΩΜΑ ΑΙΜΑΤΟΛΟΓΙΑ
Σημαντική πρόοδος σημειώθηκε στη θεραπεία ενηλίκων ασθενών με νεοδιαγνωσθείσα οξεία λεμφοβλαστική λευχαιμία (ΟΛΛ) Β-κυττάρων. Νέα μελέτη έδειξε ότι η προσθήκη ανοσοθεραπείας με blinatumomab βελτιώνει σημαντικά την αποτελεσματικότητα της θεραπευτικής αντιμετώπισης. H οξεία λεμφοβλαστική λευχαιμία έχει δύο τύπους: την οξεία λεμφοκυτταρική λευχαιμία Β-κυττάρων και την οξεία λεμφοκυτταρική λευχαιμία Τ-κυττάρων. Οι περισσότε-
ροι τύποι μπορούν να αντιμετωπιστούν με καλές πιθανότητες ύφεσης στα παιδιά. Οι ενήλικες δεν έχουν τόσο υψηλές πιθανότητες ύφεσης, αλλά οι πιθανότητες θεραπείας βελτιώνονται σταδιακά με την πάροδο των ετών.
Σύμφωνα με την Αμερικανική Αντικαρκινική Εταιρεία, μεταξύ 80% και 90% των ενηλίκων με οξεία λεμφοκυτταρική λευχαιμία θα εισέλθουν σε ύφεση. Ωστόσο, περίπου οι μισοί εξ αυτών θα παρατηρήσουν τη λευχαιμία να επιστρέφει. Η συνολική πιθανότητα ίασης για τους ενήλικες με οξεία λεμφοκυτταρική λευχαιμία είναι 40%. Ένας ενήλικας θεωρείται ότι έχει ιαθεί αν είναι σε ύφεση για 5 χρόνια. Το blinatumomab είναι ένα αντίσωμα ειδικά σχεδιασμένο για να προσκολλάται σε μια πρωτεΐνη (CD19) που υπάρχει στα Β-κύτταρα, μεταξύ άλλων και στα κύτταρα της ΟΛΛ. Επίσης, προσκολλάται σε μια πρωτεΐνη (CD3) που υπάρχει στα Τ-κύτταρα (έναν άλλο τύπο λευκών αιμοσφαιρίων). Συνεπώς, δρα ως «συνεκτικός κρίκος» συνδέοντας τα Τ-κύτταρα με τα Β-κύτταρα και προκαλώντας την απελευθέρωση ουσιών από τα Τ-κύτταρα, οι οποίες εξουδετερώνουν τελικά τα καρκινικά Β-κύτταρα.
Η νέα μελέτη είναι μια τυχαιοποιημένη μελέτη φάσης ΙΙΙ (ονομάζεται E1910), η οποία αξιολόγησε την ανοσοθεραπεία με blinatumomab σε ασθενείς με καλή πρόγνωση μετά από έναν αρχικό γύρο χημειοθεραπείας. Μετά από περίπου 3,5 χρόνια παρακολούθησης, το 83% των ασθενών που έλαβαν χημειοθεραπεία συν blinatumomab ήταν ζωντανοί έναντι 65%
26 / Μάρτιος-Απρίλιος 2023 ΡΕΠΟΡΤΑΖ
Θετική
λεμφοβλαστική λευχαιμία Β Σήμερα, οι ενήλικες δεν έχουν τόσο υψηλές πιθανότητες ύφεσης Η προσθήκη ανοσοθεραπείας μπορεί να βελτιώσει την αποτελεσματικότητα της θεραπείας
εξέλιξη στην οξεία
όσων έλαβαν μόνο χημειοθεραπεία.
Η προσθήκη του blinatumomab στη χημειοθεραπεία αντιπροσωπεύει έναν νέο πρότυπο φροντίδας για ασθενείς με νεοδιαγνωσθείσα οξεία λεμφοβλαστική λευχαιμία τύπου Β, οι οποίοι βρίσκονται σε ύφεση και δεν έχουν μετρήσιμη υπολειπόμενη νόσο μετά από αρχική χημειοθεραπεία εισαγωγής» σημειώνει ο δρ Mark R. Litzow, καθηγητής Ιατρικής στη Mayo Clinic της Μινεσότα.
Η μελέτη E1910 σχεδιάστηκε και διεξήχθη ανεξάρτητα από τη βιομηχανία με δημόσια χρηματοδότηση. Η ομάδα έρευνας για τον καρκίνο ECOG-ACRIN ηγήθηκε της δοκιμής με χρηματοδότηση από το Εθνικό Ινστιτούτο Καρκίνου (NCI), μέρος των Εθνικών Ινστιτούτων Υγείας των ΗΠΑ. Στη δοκιμή συμμετείχαν και άλλες ομάδες δικτύου που χρηματοδοτούνται από το NCI. «Αυτή είναι η πρώτη τυχαιοποιημένη δοκιμή που αποδεικνύει ότι είμαστε σε θέση να βελτιώσουμε την επιβίωση όλων των ασθενών που βρίσκονται σε πλήρη ύφεση και καθιερώνει την προσθήκη της ανοσοθεραπείας με blinatumomab στην τυπική χημειοθεραπεία ως το νέο πρότυπο φροντίδας» συμπληρώνει η Selina M. Luger, πρόεδρος της Επιτροπής Λευχαιμίας της ECOG ACRIN και καθηγήτρια Ιατρικής στο Πανεπιστήμιο της Πενσυλβάνια.
Η μελέτη
Συνολικά, σε 77 ιατρικά κέντρα σε ΗΠΑ, Καναδά και Ισραήλ συμμετείχαν 488 ασθενείς με νεοδιαγνωσθείσα ALL σειράς Β μεταξύ του Δεκεμβρίου 2013 και του Οκτωβρίου 2019. Οι ασθενείς με ανωμαλία του γονιδίου BCR::ABL1 δεν ήταν επιλέξιμοι. Η διάμεση ηλικία ήταν 51 έτη (εύρος 30-70).
Η καθιερωμένη θεραπεία της ΟΛΛ είναι περίπλοκη, με πολλαπλούς κύκλους συνδυασμών χημειοθεραπείας. Η επισκόπηση θεραπείας E1910 έχει ως εξής:
Βήμα 1: Όλοι οι συμμετέχοντες έλαβαν 2,5 μήνες συνδυασμένης χημειοθεραπείας, συμπεριλαμβανομένης της pegaspargase για άτομα κάτω των 55 ετών. Οι ασθενείς που βρέθηκαν θετικοί στο αντιγόνο Β-λεμφοκυττάρων CD20 έλαβαν επίσης rituximab. Στο τέλος, 395 ασθενείς (81%) βρίσκονταν σε ύφεση και 333 προχώρησαν στο Βήμα 2. Οι υπόλοιποι αποχώρησαν από τη μελέτη.
Βήμα 2-Εντατικοποίηση: Οι ασθενείς έλαβαν μια σειρά θεραπείας για να
σταματήσει η ανάπτυξη λευχαιμίας στο κεντρικό νευρικό σύστημα, μια κοινή εστία υποτροπής αν δεν προληφθεί. Στη συνέχεια, όλοι οι ασθενείς εξετάστηκαν κεντρικά για υπολειπόμενη νόσο (MRD).
Ενώ η αρχική αξιολόγηση ήταν στην κοόρτη με αρνητικό MRD-, οι ασθενείς
με θετικό MRD+ συνέχισαν τη δοκιμή.
Βήμα 3-Πειραματικό: 286 ασθενείς (224 MRD- και 62 MRD+) τυχαιοποιήθηκαν/για να λάβουν 4 κύκλους χημειοθεραπείας με ή χωρίς blinatumomab.
Αυτό χορηγήθηκε με συνεχή ενδοφλέβια έγχυση για 4 εβδομάδες για καθέναν από τους 4 κύκλους όπου χορηγήθηκε. Το 72% των ασθενών έλαβαν blinatumomab με εγχύσεις 72 και 96 ωρών, οι οποίες ξεπέρασαν τα ζητήματα σκοπιμότητας για τη διεξαγωγή της δοκιμής. Μετά την έγκριση της FDA για το blinatumomab για ασθενείς με MRD+ τον Μάρτιο του 2018, οι συμμετέχοντες στο MRD+ κατατάχθηκαν στο σκέλος του blinatumomab. Οι ασθενείς με αρνητικό MRD συνέχισαν να τυχαιοποιούνται.
Βήμα 4-Συντήρηση: Οι ασθενείς έλαβαν θεραπεία με POMP (Purinethol + Oncovin® + μεθοτρεξάτη + πρεδνιζόνη) για περίπου δύο χρόνια, που χορηγείται συνήθως για να διατηρηθούν όλοι
σε ύφεση και να αυξηθεί η πιθανότητα επίτευξης ίασης.
Μια προγραμματισμένη ενδιάμεση ανάλυση έδειξε ότι μεταξύ των 224 ασθενών με αρνητικό MRD υπήρξαν 56 θάνατοι: 17 στο σκέλος της χημειοθεραπείας και της blinatumomab και 39 στο σκέλος της χημειοθεραπείας ελέγχου. Η διάμεση παρακολούθηση ήταν 43 μήνες. Η διάμεση συνολική επιβίωση δεν επιτεύχθηκε στο σκέλος της χημειοθεραπείας και του blinatumomab έναντι σχεδόν 6 ετών (71,4 μήνες) στο σκέλος ελέγχου. Η δοκιμή συνεχίζει να ακολουθεί τους συμμετέχοντες. Η μελέτη δεν βρήκε νέες ανησυχίες για την ασφάλεια που να σχετίζονται με τη χρήση χημειοθεραπείας και blinatumomab και χρησιμοποίησε εγχύσεις 72 και 96 ωρών στο 72% των ασθενών. Αυτοί οι χρόνοι έγχυσης αποδείχθηκαν απαραίτητοι για την εφικτή διεξαγωγή της δοκιμής. Οι ερευνητές σχεδιάζουν να αναλύσουν περαιτέρω τα δεδομένα για να προσδιορίσουν αν συγκεκριμένες υποομάδες ασθενών είναι πιο πιθανό να ωφεληθούν από την blinatumomab από άλλες.•••
Μεταξύ 80%
και 90% των
ενηλίκων με οξεία
λεμφοκυτταρική
λευχαιμία θα
εισέλθουν σε ύφεση.
Η μελέτη δεν βρήκε
νέες ανησυχίες
για την ασφάλεια
που να σχετίζονται
με τη χρήση
χημειοθεραπείας
και blinatumomab.
27 ΑΦΙΕΡΩΜΑ ΑΙΜΑΤΟΛΟΓΙΑ
Ενθαρρυντικά
είναι τα ποσοστά ανταπόκρισης σε ηλικιωμένους ή
ασθενείς υψηλού
κινδύνου, καθώς η νεοδιαγνωσθείσα
κοόρτη είχε 80%
συνολικό ποσοστό ανταπόκρισης.
Νέες κλινικές μελέτες παρουσιάζουν θετικές εξελίξεις
Ποια στοχευμένα φάρμακα & συνδυασμοί
υπόσχονται
Στην τελευταία ετήσια συνάντηση της Αμερικανικής Εταιρείας Αιματολογίας (ASH), που πραγματοποιήθηκε τον Δεκέμβριο του 2022, παρουσιάστηκαν ελπιδοφόρα νέα
από τρεις κλινικές δοκιμές για την προώθηση της χρήσης στοχευμένων θεραπειών και νέων συνδυασμών σε πολλαπλούς τύπους λευχαιμίας. Ειδικότερα, οι κλινικές δοκιμές αφορούν
την οξεία μυελογενή λευχαιμία υψηλού κινδύνου, την πρόσφατα διαγνωσμένη οξεία μυελογενή λευχαιμία (AML) τόσο σε ηλικιωμένους όσο και σε νεότερους ασθενείς και μια μορφή της οξείας λεμφοβλαστικής λευχαιμίας που ονομάζεται «Φιλαδέλφεια θετική» (Ph + ALL).
Τριπλή θεραπεία
Περίπου το 50%-55% των ασθενών με ΟΜΛ θεωρούνται μεγάλοι σε ηλικία ή ακατάλληλοι για εντατική χημειοθεραπεία. Η θεραπεία πρώτης γραμμής με azacitidine-venetoclax επιτυγχάνει ποσοστά ανταπόκρισης 65%-70% σε ασθενείς που διαγνώστηκαν πρόσφατα, αλλά οι περισσότεροι ασθενείς υποτροπιάζουν και όσοι έχουν μεταλλάξεις TP53 συνεχίζουν να έχουν κακή έκβαση, με διάμεση επιβίωση μικρότερη από έξι μήνες! Συνεπώς, υπάρχει μεγάλη ανάγκη βελτίωσης της θεραπείας. Σε μια δοκιμή Φάσης Ib/II, δοκιμάστηκε ένα τριπλό σχήμα με την προσθήκη της ουσίας magrolimab στον καθιερωμένο συνδυασμό azacitidinevenetoclax. Οι ερευνητές παρατήρησαν ενθαρρυντικά ποσοστά ανταπόκρισης σε
ηλικιωμένους ή ασθενείς υψηλού κινδύνου, καθώς η νεοδιαγνωσθείσα κοόρτη είχε 80% συνολικό ποσοστό ανταπόκρισης (ORR).
«Είμαστε ενθαρρυμένοι από τα πολλά υποσχόμενα στοιχεία αυτής της θεραπείας. Θα συνεχίσουμε να επεκτείνουμε τη δοκιμή για να συμπεριλάβουμε περισσότερους ασθενείς και έχουμε ξεκινήσει μια διεθνή τυχαιοποιημένη μελέτη Φάσης ΙΙΙ που αξιολογεί τη θεραπεία με τριπλή έναντι της διπλής με azacitidine-venetoclax. Αν η μελέτη είναι θετική, θα μπορούσε να δημιουργήσει ένα νέο πρότυπο πρώτης γραμμής φροντίδας για αυτούς τους ασθενείς» ανέφερε ο Naval Daver, αναπληρωτής καθηγητής Αιματολογίας.
Το magrolimab είναι ένα αντίσωμα κατά του CD47 που δρα για να μπλοκάρει το σήμα «μη με φας» που εκφράζουν τα λευχαιμικά κύτταρα λευχαιμίας. Σε μια προηγούμενη δοκιμή, έδειξε αποτελεσματικότητα με την αζακιτιδίνη στη νεοδιαγνωσθείσα ΟΜΛ, με ένα ιδιαίτερα ενθαρρυντικό σήμα ανταπόκρισης και επιβίωσης στην πρώτη γραμμή σε ασθενείς ΟΜΛ που φέρουν μεταλλάξεις TP53.
Στην τρέχουσα δοκιμή συμμετείχαν 74 ασθενείς σε δύο ομάδες. Στην πρώτη ομάδα συμμετείχαν 45 ασθενείς πρώτης γραμμής ηλικίας 75 ετών και άνω με τεκμηριωμένες συννοσηρότητες που τους καθιστούσαν μη κατάλληλους για εντατική θεραπεία ή με δυσμενείς παράγοντες κινδύνου και/ή μετάλλαξη TP53, ανεξαρτήτως ηλικίας. Αυτή η κοόρτη περιλάμβανε 27 ασθενείς με μετάλλαξη TP53 και 14 χωρίς. Στη δεύτε-
28 / Μάρτιος-Απρίλιος 2023 ΡΕΠΟΡΤΑΖ
Λευχαιμίες:
Ελπίδες από νέες
θεραπείες
καλύτερα αποτελέσματα
ρη ομάδα συμμετείχαν 29 ασθενείς με υποτροπιάζουσα/ανθεκτική νόσο.
Όλοι οι ασθενείς που έλαβαν τουλάχιστον
μία δόση από οποιοδήποτε από τα τρία φάρμακα της μελέτης συμπεριλήφθηκαν
για ανταπόκριση και ανεπιθύμητες ενέργειες. Δεκαοκτώ ασθενείς εμφάνισαν αναιμία μεγαλύτερη του βαθμού 3 και οι πιο συχνές μη αιματολογικές ανεπιθύμητες ενέργειες ήταν η εμπύρετη ουδετεροπενία, η πνευμονία, η υπερχολερυθριναιμία, η τρανσαμινίτιδα, η αύξηση της κρεατίνης
και η υποκαλιαιμία.
Στη νεοδιαγνωσθείσα κοόρτη, το ποσοστό ανταπόκρισης σε ασθενείς με και χωρίς
μεταλλάξεις TP53 ήταν 74% και 93%, αντίστοιχα. Το διάμεσο ποσοστό συνολικής
επιβίωσης OS δεν είχε ακόμη επιτευχθεί
για καμία από τις ομάδες ασθενών. Οι ανταποκρίσεις σε ασθενείς με υποτροπιάζουσα/ανθεκτική νόσο με προηγούμενη
θεραπεία με venetoclax ήταν μέτριες και
η κοόρτη έκλεισε λόγω ματαιότητας. Ασθενείς με υποτροπιάζουσα/ανθεκτική νόσο
χωρίς έκθεση στο venetoclax εξακολουθούν να εγγράφονται. Η μελέτη χρηματοδοτήθηκε από την Gilead, που έχει αναπτύξει το magrolimab.
Συνδυασμός ponatinibblinatumomab
Οι ασθενείς με οξεία λεμφοβλαστική λευ-
χαιμία «Φιλαδέλφεια θετική» (Ph + ALL) έχουν ιστορικά χαμηλά ποσοστά επιβίωσης.
Οι ερευνητές ανακάλυψαν ότι η προσθήκη αναστολέων κινάσης τυροσίνης (TKIs), όπως το ponatinib, στη χημειοθεραπεία
μπορεί να βελτιώσει δραστικά την επιβίωση.
Το ponatinib ανήκει σε μια ομάδα φαρμάκων που ονομάζονται αναστολείς τυροσινικής κινάσης. Αυτές οι ενώσεις αναστέλλουν ένζυμα που είναι γνωστά ως τυροσινικές κινάσες. Το ponatinib δρα αναστέλλοντας την τυροσινική κινάση Bcr-Abl. Το ένζυμο αυτό βρίσκεται στην επιφάνεια των λευχαιμικών κυττάρων και συμμετέχει στην ενεργοποίηση της ανεξέλεγκτης διαίρεσης των κυττάρων. Το ponatinib αναστέλλει τη δράση της Bcr-Abl και συμβάλλει με αυτόν τον τρόπο στον έλεγχο της ανάπτυξης και εξάπλωσης των λευχαιμικών κυττάρων. Σύμφωνα με αποτελέσματα κλινικής δοκιμής Φάσης ΙΙ, το θεραπευτικό σχήμα ponatinib και blinatumomab χωρίς χημειοθεραπεία πέτυχε υψηλά ποσοστά ανταπόκρισης και μείωσε την ανάγκη για αλλογενή μεταμόσχευση βλαστοκυττάρων. «Παραδοσιακά, η νόσος ανταποκρίνεται ελάχιστα στην τυπική χημειοθεραπεία και είναι υψηλού κινδύνου για υποτροπή, επομένως αυτά τα αποτελέσματα επιβίωσης και η μειωμένη ανάγκη για μεταμόσχευση βλαστοκυττάρων είναι πολύ ενθαρρυντικά» είπε ο Nicholas Short, επίκουρος καθηγητής Αιματολογίας. «Αυτό το σχήμα όχι μόνο φαίνεται να είναι μια ασφαλής και αποτελεσματική επιλογή χωρίς χημειοθεραπεία, αλλά δείχνει επίσης να ξεπερνά την ιστορική ανάγκη για μεταμόσχευση σε αυτούς τους ασθενείς».

Στη δοκιμή συμμετείχαν 40 ασθενείς με νεοδιαγνωσθείσα (Ph + ALL). Ασθενείς με μη ελεγχόμενη καρδιαγγειακή νόσο ή κλινικά σημαντικές συννοσηρότητες του κεντρικού νευρικού συστήματος αποκλείστηκαν από τη μελέτη. Η μέση ηλικία των
Το 96% των ασθενών ανταποκρίθηκαν
29 ΑΦΙΕΡΩΜΑ ΑΙΜΑΤΟΛΟΓΙΑ
στη θεραπεία
μετρήσιμη
και το 90% δεν είχαν
ασθένεια σε δείγμα μυελού των οστών.
συμμετεχόντων ήταν τα 56 έτη. Από τους ασθενείς που ήταν αξιολογήσιμοι για αιματολογική απόκριση το 96% είχαν πλήρη ύφεση. Μεταξύ των 38 ασθενών που ήταν αξιολογήσιμοι για πλήρη μοριακή απόκριση (CMR), το 68% πέτυχαν CMR μετά από έναν κύκλο θεραπείας και το 87% πέτυχαν CMR κατά τη διάρκεια της δοκιμαστικής περιόδου.
Οι μοριακές αποκρίσεις ήταν γρήγορες, με την πλειονότητα των ασθενών να επιτυγχάνουν CMR στο περιφερικό αίμα εντός δύο εβδομάδων από τη θεραπεία. Μόνο ένας ασθενής υποβλήθηκε σε μεταμόσχευση βλαστοκυττάρων σε πρώτη ύφεση. Σε μια διάμεση παρακολούθηση 15 μηνών, η συνολική επιβίωση χωρίς συμβάματα και η εκτιμώμενη συνολική επιβίωση ήταν 95%. Αυτά τα ενθαρρυντικά αποτελέσματα παρατηρήθηκαν παρά το πολύ χαμηλό ποσοστό μεταμόσχευσης στη μελέτη. Η θεραπεία ήταν καλά ανεκτή και οι περισσότερες τοξικότητες ήταν βαθμού 1-2 και συμβατές με γνωστές παρενέργειες των δύο παραγόντων.
Να σημειώσουμε ότι, σύμφωνα με τον ΕΜΑ, το ponatinib μπορεί να προκαλέσει θρόμβους ή απόφραξη των αρτηριών και των φλεβών. Συνεπώς, οι ασθενείς πρέπει
να υποβάλλονται σε εξετάσεις για την κατάσταση της καρδιάς και την κυκλοφορία του αίματός τους τόσο πριν από την έναρξη όσο και κατά τη διάρκεια της θεραπείας και σε περίπτωση που διαπιστωθούν προβλήματα, να λαμβάνουν την κατάλληλη θεραπεία. Αν ο ασθενής εμφανίσει ορισμένες ανεπιθύμητες ενέργειες, ενδέχεται να πρέπει να μειωθεί η δόση ή να διακοπεί η θεραπεία, ενώ σε περίπτωση απόφραξης αρτηρίας ή φλέβας, η θεραπεία πρέπει να διακοπεί αμέσως.
Συνδυασμός venetoclax με CLIA
Τα τελευταία αποτελέσματα μιας μελέτης Φάσης ΙΙ που αξιολογούσε την προσθήκη του venetoclax στην εντατική χημειοθεραπεία με cladribine, idarubicin και cytarabine (CLIA) ως θεραπεία πρώτης γραμμής κατέδειξαν υψηλά ποσοστά ελέγχου της νόσου και υφέσεις σε νεότερους ασθενείς με πρόσφατα διαγνωσμένη ΟΜΛ και υψηλού κινδύνου μυελοδυσπλαστικό σύνδρομο (MDS). Στη μελέτη, το 96% των ασθενών ανταποκρίθηκαν στη θεραπεία και το 90% δεν είχαν μετρήσιμη ασθένεια σε δείγμα μυελού των οστών.
«Το Venetoclax ήταν μια σημαντική ανακάλυψη για ασθενείς με AML που δεν είναι κατάλληλοι για εντατική θεραπεία. Αυτά τα δεδομένα συνεχίζουν να καταδεικνύουν το όφελος από τη συμπερίληψη του venetoclax
στο θεραπευτικό σχήμα CLIA» δήλωσε ο δρ Patrick Reville από το MD Anderson Cancer Cente. «Αυτό το σχήμα οδηγεί σε άνευ προηγουμένου ανταπόκριση και μετρήσιμα ποσοστά εναπομένουσας αρνητικότητας της νόσου. Καθώς συνεχίζουμε να ακολουθούμε τους συμμετέχοντες, ενθαρρυνόμαστε από τα μακροπρόθεσμα αποτελέσματα και την επιβίωσή τους».

Στην κλινική δοκιμή ενός σκέλους συμμετείχαν 67 ασθενείς με μέση ηλικία τα 48 έτη. Εξήντα ασθενείς είχαν ΟΜΛ και τέσσερις ασθενείς είχαν MDS υψηλού κινδύνου. Επιπλέον, τρεις ασθενείς είχαν οξεία λευχαιμία μικτού φαινότυπου (MPAL). Το σύνθετο ποσοστό πλήρους ανταπόκρισης ήταν 96% σε όλους τους ασθενείς και 100% για ασθενείς με MDS και MPAL με μυελογενή κυρίαρχο κλώνο. Οι περισσότεροι ασθενείς έλαβαν μεταμόσχευση αλλογενών βλαστοκυττάρων, συμπεριλαμβανομένου του 70% όσων ανταποκρίθηκαν στη θεραπεία. Είναι ενθαρρυντικό το ότι, στους 12 μήνες, το εκτιμώμενο ποσοστό επιβίωσης χωρίς συμβάν είναι 70% και το εκτιμώμενο συνολικό ποσοστό επιβίωσης είναι 86%. Το 74% των ασθενών που ανταποκρίνονται εκτιμάται ότι έχουν συνεχή ανταπόκριση στους 12 μήνες.
Η πιο συχνή μη αιματολογική ανεπιθύμητη ενέργεια που παρουσίασαν οι συμμετέχοντες ήταν η εμπύρετη ουδετεροπενία, η οποία αντιμετωπίστηκε. Οι ερευνητές συνεχίζουν να παρακολουθούν τους ασθενείς και να μελετούν αυτό το θεραπευτικό σχήμα ως μια ασφαλή και αποτελεσματική στρατηγική θεραπείας εισαγωγής για αυτόν τον πληθυσμό ασθενών.•••
30 / Μάρτιος-Απρίλιος 2023
ΡΕΠΟΡΤΑΖ
Sobi :Το Liberate Life στηρίζει τους ασθενείς
Σπάνια, αλλά
Στην Ελλάδα ζουν 1.016 άτομα με αιμορροφιλία Α και Β
Hαιμορροφιλία είναι μια σπάνια
κληρονομική διαταραχή στην πήξη του αίματος. Οφείλεται σε
έλλειψη του παράγοντα VIII (αιμορροφιλία Α) ή του παράγοντα IX (αιμορροφιλία Β), μια κατηγορία πρωτεϊνών με σημαντικό ρόλο στον έλεγχο των αιμορραγιών. Χωρίς την κατάλληλη θεραπευτική
αντιμετώπιση, η πάθηση αυτή οδηγεί συχνά σε αιμορραγία στις αρθρώσεις, τους
μύες, τον εγκέφαλο και σε άλλα εσωτερικά όργανα. Επίσης, μπορεί να προκαλέσει έντονο πόνο, βλάβη των αρθρώσεων
και να οδηγήσει ακόμα και σε αναπηρία.
Η ασθένεια εμφανίζεται από τη γέννηση
του ατόμου, κυρίως σε άνδρες, και διαρκεί για όλη τους τη ζωή, ενώ η βαρύτητά
της εξαρτάται από το ποσοστό έλλειψης
της αντίστοιχης πρωτεΐνης.
Η παγκόσμια συχνότητα εμφάνισης της αιμορροφιλίας Α είναι περίπου 21 περιπτώσεις ανά 100.000 γεννήσεις, ενώ η αιμορροφιλία Β αφορά 4 περιπτώσεις ανά 100.000 γεννήσεις. Εκτιμάται ότι, σήμερα, 450.000 άτομα παγκοσμίως πάσχουν από αιμορροφιλία ενώ στην Ελλάδα υπολογίζεται ότι ζουν 1.016 άτομα με αιμορροφιλία Α και Β.
Πλέον, καινοτόμες θεραπείες προσφέρουν στους ασθενείς τη δυνατότητα να ζήσουν μια ζωή με όσο το δυνατόν λιγότερους περιορισμούς. Στόχος της θεραπείας είναι η πρόληψη και αντιμετώπιση των αιμορραγιών και των επιπλοκών τους.
Liberate Life: Για μια ζωή
πέρα από την αιμορροφιλία
Η φαρμακευτική εταιρεία εξειδικευμένης φροντίδας Sobi, έχοντας ως στόχο να κάνει καλύτερη τη ζωή των ατόμων με αι-
μορροφιλία, έκανε πράξη ένα σημαντικό όραμα: Το Liberate Life δημιουργήθηκε με στόχο να στηρίξει τα άτομα που ζουν με αιμορροφιλία και να τα βοηθήσει να διεκδικήσουν τα όνειρά τους και μια ζωή χωρίς περιορισμούς. Ο ιστότοπος liberatelife.gr παροτρύνει όλους όσους ζουν με αιμορροφιλία να απολαμβάνουν την κάθε τους στιγμή και να αξιοποιούν τις ευκαιρίες που ανοίγονται μπροστά τους «χωρίς δεύτερες σκέψεις». Θέλοντας επίσης να μας δώσει περισσότερη έμπνευση, μας συστήνει τους Liberators, τους ανθρώπους της «διπλανής πόρτας» που ζουν με αιμορροφιλία, αλλά καταφέρνουν καθημερινά να ξεπερνούν τις δυσκολίες και να διεκδικούν μια καλύτερη ζωή, απαλλαγμένη από τα «Πρόσεχε» και τα «Μη».
Γιατί, τελικά, είναι εφικτό να ζεις μια ζωή πέρα από την αιμορροφιλία!•••
31 ΑΦΙΕΡΩΜΑ ΑΙΜΑΤΟΛΟΓΙΑ
αντιμετωπίσιμη κληρονομική πάθηση
Η παγκόσμια συχνότητα εμφάνισης της
αιμορροφιλίας Α
είναι περίπου 21 περιπτώσεις ανά 100.000 γεννήσεις.
Το BTG1 λειτουργεί
ως φύλακας για
να διασφαλίσει
ότι μόνο μερικά
επιλεγμένα
Β-κύτταρα
επιβιώνουν
από αυτήν την ανταγωνιστική
διαδικασία φυσικής επιλογής.
Το 40% των ασθενών με διάχυτο λέμφωμα μεγάλων Β-κυττάρων
δεν ανταποκρίνονται στη θεραπεία
Ερευνητές
Tο «κλειδί» για την κατανόηση του τρόπου με τον οποίο εμφανίζονται τα πιο επιθετικά λεμφώματα και αντιστέκονται στις τρέχουσες θεραπείες μπορεί να βρίσκεται σε μεταλλάξεις που διαταράσσουν μια κρίσιμη διαδικασία φυσικής επιλογής μεταξύ των Β-κυττάρων που παράγουν αντισώματα. Αυτό τουλάχιστον προκύπτει από μια σημαντική προκλινική μελέτη, με επικεφαλής ερευνητές της Ιατρικής Σχολής Weill Cornell, που δημοσιεύθηκε πρόσφατα στο περιοδικό Science.
Το διάχυτο λέμφωμα μεγάλων Β-κυττάρων (DLBCL) είναι ο πιο κοινός τύπος λεμφώματος non-Hodgkin, με τουλάχιστον το 40% των περιπτώσεων να μην ανταποκρίνεται στη θεραπεία. Οι ασθενείς με μεταλλάξεις στο γονίδιο 1 (BTG1) της μετατόπισης των Β-κυττάρων, οι οποίες εντοπίζονται κυρίως στα λεμφώματα των Β-κυττάρων, έχουν ιδιαίτερα κακή έκβαση.
Η νέα μελέτη, λοιπόν, καταδεικνύει ότι το BTG1 δρα ως ένα σημαντικό «εξελικτικό» σημείο ελέγχου των Β-κυττάρων που διέπει τη διαδικασία φυσικής επιλογής των Β-κυττάρων, δήλωσε ο κύριος ερευνητής
της μελέτης, δρ Ari M. Melnick, καθηγητής Αιματολογίας/Ογκολογίας.
Για τη δημιουργία ισχυρών αντισωμάτων έναντι νέων μολυσματικών παραγόντων, όπως ο Covid-19, τα Β-κύτταρα περνούν από μια κυκλική διαδικασία ανάπτυξης, γονιδιακή μετάλλαξη αντισωμάτων και εξαιρετικά γρήγορη κυτταρική διαίρεση.
Χιλιάδες από αυτά τα μεταλλαγμένα Β-
κύτταρα ανταγωνίζονται σθεναρά για πρόσβαση σε πολύ μικρότερο αριθμό ανοσοκυττάρων Τ. Αυτά τα Τ-κύτταρα επιλέγουν μόνο λίγα Β-κύτταρα για επιβίωση, με βάση την ικανότητά τους να δεσμεύουν αντιγόνα, τα ξένα σωματίδια σε ιούς και άλλους μικροοργανισμούς που πυροδοτούν μια ανοσολογική απόκριση.
«Αυτός ο έντονος ανταγωνισμός μεταξύ μεμονωμένων κυττάρων Β είναι διαφορετικός από την πιο αλτρουιστική και συνεργατική κυτταρική συμπεριφορά που συναντάμε σε όλους τους άλλους ιστούς στον άνθρωπο και μοιάζει περισσότερο με τον τρόπο με τον οποίο οι μονοκύτταροι οργανισμοί ανταγωνίζονται μεταξύ τους» εξηγεί ο δρ Melnick.
Η αλληλεπίδραση με τα Τ-κύτταρα απαιτείται για την επιβίωση των Β-κυττάρων επειδή ενεργοποιεί την παροδική έκφραση ενός ισχυρού ρυθμιστή κυτταρικής ανάπτυξης που ονομάζεται MYC, ο οποίος τροφοδοτεί τον μεταβολισμό των κυττάρων για να δημιουργήσει τα δομικά στοιχεία που απαιτούνται για τις επόμενες «εκρήξεις» κυτταρικής διαίρεσης. Το BTG1 λειτουργεί ως φύλακας για να διασφαλίσει ότι μόνο μερικά επιλεγμένα Βκύτταρα επιβιώνουν από αυτήν την ανταγωνιστική διαδικασία φυσικής επιλογής, ενώ παράλληλα περιορίζει τον ανταγωνισμό, αποτρέποντας την ακατάλληλη λειτουργία του MYC. Για να επιτευχθεί αυτή
η ευαίσθητη ισορροπία το BTG1 ελέγχει τον ρυθμό έκφρασης της πρωτεΐνης MYC στα Β-κύτταρα.
32 / Μάρτιος-Απρίλιος 2023 ΡΕΠΟΡΤΑΖ
«Κλειδί»
οι
μεταλλάξεις στα
επιθετικά λεμφώματα
βρήκαν την εξήγηση στο πώς εμφανίζονται τα πιο επιθετικά λεμφώματα
Οι μεταλλάξεις BTG1 συμβαίνουν στο 70%
της πιο επιθετικής μορφής DLBCL και
προκαλούν αυτήν τη διαδικασία ώστε να
πηγαίνει στραβά, επιτρέποντας πιο γρή-
γορη επαγωγή της έκφρασης της πρωτεΐ-
νης MYC στα Β κύτταρα. «Το αποτέλεσμα

είναι μικροσκοπικό από μοριακή άποψη»
λέει ο Melnick. «Αυξάνεται κατά προσέγγιση 10% στον ρυθμό παραγωγής πρωτεΐνης MYC».
Ωστόσο, αυτό το μικρό αποτέλεσμα επιτρέπει στα μεταλλαγμένα Β-λεμφοκύττα-
ρα BTG1 να ξεφύγουν και να αναλάβουν
την ανοσολογική απόκριση ανταγωνιζόμενα τα υγιή Β-κύτταρα κατά τη διάρκεια της φυσικής επιλογής που καθοδηγείται από Τ-κύτταρα. Αυτό το αποτέλεσμα επιτρέπει στα Β-κύτταρα να υποστούν περισσότερους κύκλους μετάλλαξης, γεγονός που τα θέτει σε κίνδυνο να καταστρέψουν άλλα γονίδια και τελικά να γίνουν καρκινικά. «Σε αυτήν τη μελέτη, η μετάλλαξη BTG1 επιτάχυνε τον σχηματισμό λεμφώματος και οδήγησε σε εξαιρετικά επιθετικούς καρκίνους που εξαπλώθηκαν σε όλο το σώμα στα ποντίκια, κάτι που θυμίζει αυτό που συμβαίνει στους ασθενείς» δήλωσε η δρ Coraline Mlynarczyk, η πρώτη συγγραφέας της εργασίας και ερευνήτρια στο εργαστήριο του Melnick. «Ως εκ τούτου, αυτό το μικροσκοπικό αποτέλεσμα 10%, με την πάροδο του χρόνου, οδηγεί σε εξαιρετικά επιθετικές ασθένειες». Η μελέτη δείχνει επίσης πόσο ευαίσθητη
είναι η εξέλιξη σε μικρές επιπτώσεις που μπορούν να αυξήσουν δραματικά την ικανότητα των κυττάρων στο πλαίσιο του ανταγωνισμού. Επιπλέον, μια τέτοια αλλαγή της φυσικής επιλογής των Β-κυττάρων είναι εντυπωσιακά παρόμοια με τη διαδικασία του υπερ-ανταγωνισμού στα αναπτυσσόμενα όργανα σε έμβρυα εντόμων και ζώων. Και εκεί, μικρές διαφορές στην έκφραση MYC επιτρέπουν στα υπερ-ανταγωνιστικά κύτταρα να αναλάβουν πλήρως τον σχηματισμό νέων ιστών. «Τα λεμφώματα είναι περίεργοι και ολέθριοι όγκοι, γιατί προέρχονται από το ανοσοποιητικό σύστημα, το οποίο υποτίθεται ότι μας προστατεύει από τον καρκίνο» σημειώνει ο Melnick. «Δεδομένου ότι, επί του παρόντος, δεν έχουμε θεραπείες που να λειτουργούν για αυτούς τους ασθενείς, η κατανόηση των διαδικασιών που εμπλέκονται στην ανάπτυξη των χειρότερων και πιο θανατηφόρων μορφών DLBCL είναι το πρώτο βήμα προς την παρέμβαση».
είναι το λέμφωμα
Το λεμφικό σύστημα αποτελεί μέρος του ανοσοποιητικού συστήματος του οργανισμού, είναι η φυσική άμυνα έναντι των λοιμώξεων. Ένα δίκτυο μικρών αγγείων
στούν μόνο με απεικονιστικές εξετάσεις. Τα λεμφοκύτταρα διαιρούνται συνεχώς προκειμένου να παράγουν νέα κύτταρα. Όταν αντιμετωπίζετε μια λοίμωξη, ο οργανισμός σας φτιάχνει πολλά νέα λεμφοκύτταρα πολύ γρήγορα. Παράγονται διάφοροι τύποι λεμφοκυττάρων, αλλά μόνο εκείνα τα λεμφοκύτταρα που βοηΤι
θούν στην αντιμετώπιση της λοίμωξης είναι χρήσιμα για το ανοσοποιητικό σύστημα. Λεμφοκύτταρα που δεν στοχεύουν τη λοίμωξη συνήθως πεθαίνουν και μόνο τα χρήσιμα λεμφοκύτταρα επιβιώνουν. Αυτή η διαδικασία ελέγχεται αυστηρά από τον οργανισμό σας. Το λέμφωμα μπορεί να αναπτυχθεί όταν αυτό το αυστηρά ελεγχόμενο σύστημα διαταράσσεται. Γενετικές μεταβολές στα κύτταρα μπορεί να οδηγήσουν σε λανθασμένη ανταπόκριση στα σήματα του οργανισμού. Τα κύτταρα αυτά μπορεί να διαιρούνται χωρίς να υπάρχει λόγος ή μπορεί να μην πεθαίνουν, ενώ θα έπρεπε. Αυτή η διαταραχή του ελέγχου επιτρέπει στα παθολογικά λεμφοκύτταρα να αθροιστούν και δημιουργούν έτσι έναν όγκο. Ο όγκος αυτός ονομάζεται λέμφωμα.•••
33 ΑΦΙΕΡΩΜΑ ΑΙΜΑΤΟΛΟΓΙΑ
στα κύτταρα μπορεί να οδηγήσουν σε λανθασμένη
σήματα του οργανισμού.
Γενετικές μεταβολές
ανταπόκριση στα
που ονομάζονται λεμφαγγεία και πολλές ομάδες λεμφαδένων ανευρίσκονται σε όλο το σώμα. Το λεμφικό σύστημα περιλαμβάνει επίσης όργανα που αποτελούν μέρος του ανοσοποιητικού συστήματος, όπως ο σπλήνας και ο θύμος. Η κατηγορία των λευκών αιμοσφαιρίων που ονομάζονται λεμφοκύτταρα βοηθούν τον οργανισμό να καταπολεμήσει τις λοιμώξεις και βρίσκονται συγκεντρωμένα στους λεμφαδένες. Μερικές ομάδες λεμφαδένων είναι εύκολα ψηλαφητοί, ειδικά στον λαιμό, στις μασχάλες και τους βουβώνες. Άλλοι βρίσκονται βαθύτερα στο σώμα και μπορούν να εντοπι-
Hέναρξη της ανοσοθεραπείας πριν από τη χειρουργική επέμβαση βελτιώνει τις προοπτικές για ασθενείς με μελάνωμα υψηλού κινδύνου, σύμφωνα με νέα μελέτη, που δημοσιεύτηκε στο New England Journal of Medicine
Ειδικότερα, ασθενείς με μελάνωμα σταδίου III-IV που έλαβαν το ανοσοθεραπευτικό φάρμακο pembrolizumab τόσο πριν όσο και μετά τη χειρουργική επέμβαση είχαν σημαντικά χαμηλότερο κίνδυνο επανεμφάνισης του καρκίνου σε σχέση με τους ασθενείς που έλαβαν το φάρμακο μόνο μετά τη χειρουργική επέμβαση. Πρόκειται για μια ερευνητική μελέτη με επικεφαλής το SWOG Cancer Research Network, μια ομάδα κλινικών δοκιμών καρκίνου που χρηματοδοτείται από το Εθνικό Ινστιτούτο Καρκίνου (NCI). Τα ευρήματα παρουσιάστηκαν αρχικά σε Προεδρικό Συμπόσιο στο Συνέδριο της Ευρωπαϊκής
Εταιρείας Ιατρικής Ογκολογίας (ESMO) 2022 (Abstract LBA6).
Η μελέτη, γνωστή ως S1801, διενεργήθηκε
από ομάδα επιστημόνων με επικεφαλής
τον Sapna Patel, πρόεδρο της επιτροπής μελανώματος SWOG και αναπληρωτή καθηγητή Ιατρικής Ογκολογίας του Μελανώματος στο Κέντρο Καρκίνου MD Anderson του Πανεπιστημίου του Τέξας.
«Δεν είναι μόνο αυτό που δίνεις, είναι και πότε το δίνεις. Η μελέτη S1801 καταδεικνύει ότι η ίδια θεραπεία που δίνουμε σήμερα μετά το χειρουργείο, αν δοθεί πριν από τη χειρουργική επέμβαση, μπορεί να δημιουργήσει καλύτερα αποτελέσματα. Σε αυτήν την περίπτωση, χρησιμοποιήσαμε τον αναστολέα του ανοσοποιητικού σημείου ελέγχου pembrolizumab και διαπιστώσαμε ότι η έναρξη της θεραπείας πριν αφαιρεθεί το μελάνωμα οδηγεί σε μεγαλύτερη ανταπόκριση από το να δώσεις το φάρμακο μετά την επέμβαση» δηλώνει ο Patel.
Το pembrolizumab είναι μονοκλωνικό αντίσωμα, ένας τύπος πρωτεΐνης που έχει σχεδιαστεί έτσι ώστε να αναγνωρίζει και να αποκλείει έναν υποδοχέα («στόχο») που ονομάζεται PD-1. Ορισμένες μορφές καρκίνου μπορούν να παράγουν μια πρωτεΐνη (PD-L1), η οποία, σε συνδυασμό με τον υποδοχέα PD-1, αδρανοποιεί τη δραστηριότητα ορισμένων κυττάρων του ανοσοποιητικού συστήματος (της φυσικής άμυνας του οργανισμού) και με αυτόν τον τρόπο τα εμποδίζει να επιτεθούν στον καρκίνο. Αναστέλλοντας τον υποδοχέα PD-1, η πεμπρολιζουμάμπη σταματά την αδρανοποίηση των εν λόγω ανοσοποιητικών κυττάρων
34 / Μάρτιος-Απρίλιος 2023 ΕΡΕΥΝΑ
Τι έδειξε νέα μελέτη για το
Ασθενείς με μελάνωμα σταδίου III-IV που έλαβαν το ανοσοθεραπευτικό φάρμακο pembrolizumab τόσο πριν όσο και μετά τη χειρουργική επέμβαση είχαν σημαντικά χαμηλότερο κίνδυνο επανεμφάνισης του καρκίνου.
Μελάνωμα: Ανοσοθεραπεία
πριν από το χειρουργείο
pembrolizumab Βελτιώνει τις προοπτικές σε ασθενείς υψηλού κινδύνου
από τον καρκίνο και, συνεπώς, ενισχύει την ικανότητα του ανοσοποιητικού συστήματος να εξουδετερώνει τα καρκινικά κύτταρα. Οι ερευνητές υπέθεσαν ότι θα υπήρχε μεγαλύτερη αντικαρκινική ανοσολογική απόκριση και μεγαλύτερη ανοσολογική μνήμη αν το pembrolizumab χορηγούνταν
ενώ ο όγκος του μελανώματος ήταν ακόμα στο σώμα, σε αντίθεση με το να δοθεί μετά την αφαίρεση αυτού του όγκου, όταν το ανοσοποιητικό σύστημα θα ανταποκρι -
νόταν κυρίως σε μικρομεταστατικά καρκινικά κύτταρα.
Για να ελέγξουν αυτήν την υπόθεση οι ερευνητές ενέγραψαν 345 συμμετέχοντες με μελάνωμα σταδίου IIIB έως και σταδίου IV
που κρίθηκε χειρουργήσιμο. Οι συμμετέχοντες ηλικίας 18-90 ετών τυχαιοποιήθηκαν για να λάβουν είτε εκ των προτέρων χειρουργική επέμβαση, ακολουθούμενη από 200 mg pembrolizumab κάθε τρεις εβδομάδες (μόνο επικουρικό) για συνολικά
18 δόσεις, είτε 200 mg pembrolizumab
κάθε τρεις εβδομάδες σε τρεις δόσεις πριν
από το χειρουργείο και στη συνέχεια 15 επιπλέον δόσεις μετά την επέμβαση.
Το κύριο καταληκτικό σημείο που μετρήθηκε ήταν η διάρκεια της επιβίωσης χωρίς συμβάντα που ορίστηκε ως ο χρόνος από την τυχαιοποίηση έως την εμφάνιση ενός από τα ακόλουθα: εξέλιξη της νόσου ή τοξικότητα που οδήγησε στη μη λήψη χειρουργείου, αποτυχία έναρξης επικουρικής θεραπείας εντός 84 ημερών από τη χειρουργική επέμβαση, υποτροπή μελανώματος μετά από χειρουργική επέμβαση ή θάνατος από οποιαδήποτε αιτία. Με διάμεση παρακολούθηση 14,7 μη-
νών, η επιβίωση χωρίς συμβάματα ήταν σημαντικά μεγαλύτερη στο σκέλος της θεραπείας πριν από το χειρουργείο, που αντιστοιχεί σε 42% χαμηλότερο ποσοστό συμβάντων.
Οι ερευνητές διαπίστωσαν ότι το όφελος ήταν συνεπές σε μια σειρά παραγόντων, όπως η ηλικία του ασθενούς, το φύλο και το στάδιο της νόσου. Διαπίστωσαν επίσης ότι τα ποσοστά ανεπιθύμητων ενεργειών (παρενέργειες) ήταν παρόμοια και στα δύο σκέλη της μελέτης και ότι η χορήγηση pembrolizumab πριν από το χειρουργείο δεν οδήγησε σε αύξηση των ανεπιθύμητων ενεργειών που σχετίζονται με τη χειρουργική επέμβαση. «Με βάση αυτά τα ευρήματα, οι ασθενείς με μελάνωμα υψηλού κινδύνου θα πρέπει να ξεκινήσουν ανοσοθεραπεία πριν από τη χειρουργική επέμβαση για να δημιουργήσουν μια ανοσολογική απόκριση, ενώ το μεγαλύτερο μέρος του μελανώματος και τα αντικαρκινικά Τ κύτταρα είναι άθικτα» κατέληξε ο Patel.•••
35 ΑΦΙΕΡΩΜΑ ΑΙΜΑΤΟΛΟΓΙΑ Με
η
μεγαλύτερη στο σκέλος της
πριν
που
σε 42%
διάμεση παρακολούθηση 14,7 μηνών,
επιβίωση χωρίς συμβάματα ήταν σημαντικά
θεραπείας
από το χειρουργείο,
αντιστοιχεί
χαμηλότερο ποσοστό συμβάντων.
Η CSL Behring
επενδύει στην
έρευνα και την
ανάπτυξη έχοντας
ήδη πολυετή
εμπειρία και εξειδίκευση στις
αιμορραγικές διαταραχές.
CSL Behring
Η εξατομικευμένη αντιμετώπιση ικανοποιεί
και ακάλυπτες ανάγκες
Eλπίδα προσφέρουν οι γονιδιακές θεραπείες για την ορθότερη διαχείριση της αιμορροφιλίας. Η εξατομικευμένη προσέγγιση που ακολουθείται στις μέρες μας ικανοποιεί ακάλυπτες ανάγκες των ασθενών.
Η κατάκτηση της γνώσης
Πριν από περισσότερα από 100 χρόνια, οι επιστήμονες άρχισαν να «ξεκλειδώνουν»
τα μυστήρια των γονιδίων και των κληρονομικών χαρακτηριστικών. Ήταν τότε που, μαζί με την επακόλουθη ανακάλυψη της δομής του DNA στη δεκαετία του 1950, επιβεβαιώθηκε ότι το γονίδιο (ένα τμήμα της αλληλουχίας του DNA) ήταν υπεύθυνο για την κωδικοποίηση ενός μορίου (πρωτεΐνης) με συγκεκριμένη κυτταρική λειτουργία, μεταφέροντας έτσι τη γενετική πληροφορία στους απογόνους.
Ωστόσο, το γενετικό υλικό μπορεί να υποστεί αλλαγές (μεταλλάξεις) που εμποδίζουν την παραγωγή πλήρως λειτουργικών πρωτεΐνών και ευθύνονται για πολλές κληρονομικές ασθένειες. Η γονιδιακή θεραπεία
είναι μια καινοτόμος θεραπεία που στοχεύει στην αντιμετώπιση αυτών των υποκείμενων γενετικών μεταλλάξεων, με στόχο την καλύτερη διαχείριση ή τη θεραπεία μιας πάθησης.
Οι πρώτες απόπειρες γονιδιακής θεραπείας για μια μεταβολική νόσο άρχισαν το 1970. Ενώ η προσπάθεια για μια αποτελεσματική θεραπεία απέτυχε τότε, με το πέρασμα των χρόνων τόσο οι ερευνητές όσο και οι ρυθμιστικές αρχές που είναι υπεύθυνες για τη διασφάλιση της αποτελεσματικότητας και της ασφάλειας των φαρμακευτικών προϊόντων και θεραπειών απέκτησαν πολύτιμες γνώσεις και εμπειρία. Σήμερα, χρειάζονται περίπου 6-12 χρόνια φαρμακευτικής έρευνας σε εργαστή-
ρια και προσεκτικά σχεδιασμένες και ελεγχόμενες κλινικές δοκιμές, με τελική αξιολόγηση από τις αρμόδιες ρυθμιστικές αρχές για να λάβει έγκριση μια γονιδιακή θεραπεία, ενώ τις τελευταίες δεκαετίες έχουν αρχίσει περισσότερες από 2.500 κλινικές μελέτες γονιδιακής θεραπείας για ποικίλες νόσους.
CSL Behring:
Σύμμαχος των ασθενών
Η θεραπευτική αντιμετώπιση των ασθενειών είναι, πλέον, εξατομικευμένη για κάθε ασθενή, συμπεριλαμβανομένης της αιμορροφιλίας. Παράλληλα όμως, με την ήδη υπάρχουσα εξέλιξη των θεραπειών στην αιμορροφιλία, εξακολουθεί να υπάρχει η επιθυμία για νέες θεραπευτικές επιλογές, όπως η γονιδιακή θεραπεία, οι οποίες θα ανταποκρίνονται στις ανεκπλήρωτες ανάγκες των αιμορροφιλικών ασθενών, όπως είναι η μείωση ή εξάλειψη της ανάγκης για τακτική θεραπεία προφύλαξης, παράλληλα με μακροχρόνιο έλεγχο των αιμορραγιών, με σημαντική βελτίωση της ποιότητας ζωής τους.
Στην CSL Behring, η συνεχής επένδυση στην έρευνα και την ανάπτυξη, σε συνδυασμό με την πολυετή εμπειρία και εξειδίκευσή μας στις αιμορραγικές διαταραχές, είναι ο οδηγός στη διερεύνηση των θεραπευτικών επιλογών για την αντιμετώπιση της αιμορροφιλίας, προσβλέποντας σε μια νέα προοπτική στη διαχείριση της νόσου. Με την επένδυση στην ανάπτυξη καινοτόμων θεραπειών, η CSL Behring ανανεώνει συνεχώς τη μακροχρόνια δέσμευσή της προς την κοινότητα των ασθενών με αιμορροφιλία, συνεχίζοντας ως σταθερός σύμμαχός τους στη διεκδίκηση μιας ζωής ελεύθερης από τους περιορισμούς που μπορεί να επιφέρει η νόσος.•••
36 / Μάρτιος-Απρίλιος 2023 ???
Αιμορροφιλία: To χρονικό της γονιδιακής θεραπείας
Στη CSL Behring ωθούμαστε από την υπόσχεσή μας να σώζουμε ζωές
Ανταποκρινόμαστε στις ανάγκες των ασθενών χρησιμοποιώντας τις πιο εξελιγμένες τεχνολογίες
για την ανάπτυξη και διάθεση καινοτόμων βιοθεραπειών για την αντιμετώπιση σπάνιων
και απειλητικών για τη ζωή παθήσεων, όπως:
• οι αιμορραγικές διαταραχές
• οι ανοσοανεπάρκειες
• το κληρονομικό αγγειοοίδημα
• η κληρονομική μορφή χρόνιας αποφρακτικής πνευμονοπάθειας
We are unlocking the lifesaving potential of biotherapies www.cslbehring.gr
37 ΑΦΙΕΡΩΜΑ ΑΙΜΑΤΟΛΟΓΙΑ Βοηθήστε να γίνουν τα φάρμακα πιο ασφαλή και Αναφέρετε ΟΛΕΣ τις ανεπιθύμητες ενέργειες για ΟΛΑ τα φάρμακα Συμπληρώνοντας την «ΚΙΤΡΙΝΗ ΚΑΡΤΑ» CSL/AD/01/0223/GR CSL Behring Eλλάς ΕΠΕ Χατζηγιάννη Μέξη 5, Αθήνα 11528 Τηλέφωνο Φαρμακοεπαγρύπνησης: 210 6527444 Για ιατρική ενημέρωση: 210 7255660
Oι ασθενείς με καρκίνο του μαστού που χρησιμοποιούν αντιβιοτικά είναι πιο πιθανό να εμφανίσουν υποτροπή ή θάνατο.
Αυτό έδειξε μια σημαντική μελέτη που δημοσιεύτηκε πρόσφατα στο Nature Communications.
Οι γυναίκες με τριπλά αρνητικό καρκίνο
του μαστού που έλαβαν πολλαπλές συνταγές αντιβιοτικών μέσα σε τρία χρόνια
μετά τη διάγνωση του καρκίνου είχαν περισσότερες πιθανότητες να εμφανίσουν υ-
ποτροπή της νόσου και να πεθάνουν από
τον καρκίνο σε σύγκριση με εκείνες που έλαβαν λιγότερα φάρμακα, σύμφωνα με τη μελέτη ερευνητών από το πανεπιστήμιο του Stanford.
Η επίδραση στην επιβίωση δεν οφειλόταν σε διαφορές στη σοβαρότητα του καρκίνου. Από την άλλη, ο κίνδυνος αυξήθηκε σημαντικά με τον συνολικό αριθμό και τους τύπους αντιβιοτικών που συνταγογραφήθηκαν για κάθε ασθενή.
«Κάθε επιπλέον αντιβιοτικό αύξανε τον κίνδυνο θανάτου μεταξύ 5% και 18% σε σχέση με ασθενείς στους οποίους δεν είχαν συνταγογραφηθεί αντιβιοτικά» δηλώνει η Julia Ransohoff, συνεργάτης στην Αιματολογία και την Ογκολογία στο Stanford School of Medicine.
«Είναι σημαντικό να ερμηνεύσουμε αυτά
τα ευρήματα με προσοχή, ωστόσο. Δεν μπορούμε να αφήσουμε τις απειλητικές
για τη ζωή λοιμώξεις να περάσουν χωρίς

38 / Μάρτιος-Απρίλιος 2023 ΕΡΕΥΝΑ
αυξάνει τον κίνδυνο υποτροπής του καρκίνου Τι έδειξε μελέτη σε γυναίκες με τριπλά αρνητικό καρκίνο του μαστού Κάθε επιπλέον αντιβιοτικό αυξάνει τον κίνδυνο θανάτου μεταξύ 5% και 18%!
Η χρήση αντιβιοτικών
ΑΙΜΑΤΟΛΟΓΙΑ
θεραπεία. Αλλά αυτή η μελέτη προτείνει να εξετάσουμε τον καλύτερο τρόπο για να τις αντιμετωπίσουμε χωρίς να αυξήσουμε τον κίνδυνο επανεμφάνισης του καρκίνου» προσθέτει.

Η Ransohoff είναι η κύρια συγγραφέας της μελέτης, ενώ ανώτεροι συγγραφείς
είναι η Allison Kurian, καθηγήτρια Ιατρικής και Επιδημιολογίας, και η Ami Bhatt, αναπληρώτρια καθηγήτρια Ιατρικής και Γενετικής.
Η μελέτη
Οι ερευνητές μελέτησαν 772 γυναίκες που διαγνώστηκαν μεταξύ του Ιανουαρίου 2000 και του Μαΐου 2014 και υποβλήθηκαν σε θεραπεία στο Stanford Health Care ή στο νοσοκομείο Palo Alto. Βρήκαν ότι η θεραπεία με αντιμικροβιακά (μια κατηγορία φαρμάκων που περιλαμβάνει αντιβιοτικά για τη θεραπεία βακτηριακών λοιμώξεων και αντιμυκητιασικά για τη θεραπεία μυκητιασικών λοιμώξεων) συσχετίστηκε με μείωση του αριθμού των λεμφοκυττάρων που κυκλοφορούν στο αίμα του ασθενούς.
Ο αριθμός των λεμφοκυττάρων έχει αποδειχθεί ότι συσχετίζεται με την ανταπόκριση στη θεραπεία και τη συνολική επιβίωση σε άτομα με καρκίνο του μαστού (αν και οι ερευνητές μελέτησαν τις συνολικές συνταγές αντιμικροβιακών, το 99% των γυναικών στη μελέτη στις οποίες συνταγογραφήθηκαν αντιμικροβιακά έλαβαν αντιβιοτικά).
Οι ερευνητές πιστεύουν ότι η σχέση μεταξύ των αντιμικροβιακών και του αριθμού των λεμφοκυττάρων βρίσκεται στο έντερο. Είναι καλά τεκμηριωμένο ότι η αντιβιοτική θεραπεία –καθώς και η χημειοθεραπεία– μπορεί να είναι ιδιαίτερα σκληρή για τα βακτήρια που καλύπτουν τα έντερά μας, γνωστά ως «μικροβίωμα του εντέρου». Αυτά τα βακτήρια όχι μόνο μας βοηθούν να αφομοιώσουμε τα τρόφιμα, αλλά επηρεάζουν επίσης πολλές πτυχές της υγείας μας, περιλαμβανομένου και του τρόπου με τον οποίο το ανοσοποιητικό μας σύστημα ανταποκρίνεται σε αναδυόμενες απειλές, όπως λοιμώξεις ή καρκίνους.
«Γνωρίζουμε από καιρό ότι το μικροβίωμα του εντέρου παίζει ρόλο στη διαμόρφωση του ανοσοποιητικού συστήματος και ότι το ανοσοποιητικό σύστημα είναι καθοριστικό στο πώς ανταποκρίνονται οι άνθρωποι στους καρκίνους και τη χημειοθεραπεία» αναφέρει η Ransohoff.
«Βρήκαμε έναν εκπληκτικά ισχυρό και
39 ΑΦΙΕΡΩΜΑ
όσο και με τη συνολική επιβίωση
του καρκίνου.
διαρκή αυξημένο κίνδυνο θανάτου σε ασθενείς που είχαν λάβει πολλαπλά αντιμικροβιακά οποιαδήποτε στιγμή κατά τη διάρκεια των τριών ετών μετά την αρχική τους διάγνωση».
Η μελέτη έχει επιφυλάξεις. Οι γυναίκες διαγνώστηκαν και υποβλήθηκαν σε θεραπεία πριν από το 2021, όταν η χρήση μιας νέας κατηγορίας ανοσοθεραπειών που ονομάζονται «αναστολείς σημείων ελέγχου του ανοσοποιητικού» (checkpoint inhibitors) για τον τριπλό αρνητικό καρκίνο του μαστού πρώιμου σταδίου έγινε ρουτίνα. Οι αναστολείς των σημείων ελέγχου του ανοσοποιητικού συστήματος είναι μονοκλωνικά αντισώματα που αποκλείουν τους αναστολείς της ενεργοποίησης και λειτουργίας των Τ κυττάρων. Χρησιμοποιούνται σε περισσότερα από 14 διαφορετικά είδη καρκίνου και οι επιδράσεις τους μπορεί να διαρκέσουν ακόμα και πάνω από πέντε χρόνια.
Επίσης, ο τριπλά αρνητικός καρκίνος του μαστού είναι μοναδικός μεταξύ των τύπων καρκίνου του μαστού. Είναι πιο σπάνιο και πιο δύσκολο να αντιμετωπιστεί επιτυχώς από άλλους καρκίνους του μαστού.
Αλλά είναι επίσης πιο ευαίσθητος σε επιθέσεις από το ανοσοποιητικό σύστημα, επομένως δεν είναι σαφές αν η συσχέτιση μεταξύ αντιβιοτικών και φτωχότερης επιβίωσης θα ισχύει και σε άλλους τύπους καρκίνου του μαστού.
Χρήση αντιβιοτικών και καρκίνος
Αυτή η μελέτη δεν είναι η πρώτη που δείχνει ότι η χρήση αντιβιοτικών μπορεί να επηρεάσει την επιβίωση του καρκίνου.

Μια προηγούμενη μεγάλη μελέτη από ερευνητές στην Αυστραλία σε περισσότερα
από 7.000 άτομα με καρκίνο βρήκε μια συσχέτιση μεταξύ της χρήσης αντιβιοτικών
τους έξι μήνες πριν από τη διάγνωση των ασθενών και της φτωχότερης επιβίωσης. Και η αντιβιοτική θεραπεία συσχετίζεται
με αυξημένη ανάπτυξη όγκου σε πολλά μοντέλα ποντικών με καρκίνο του μαστού. Άλλες μελέτες έχουν επίσης υποδείξει μια συσχέτιση μεταξύ της υγείας του μικροβιώματος του εντέρου και των ανταποκρίσεων στις θεραπείες για τον καρκίνο.
Αλλά αυτή η νέα μελέτη είναι η πρώτη που συσχετίζει τη χρήση αντιμικροβιακών ουσιών τόσο με τον αριθμό των κυκλοφορούντων λεμφοκυττάρων όσο και με τη συνολική επιβίωση του καρκίνου –και την κάνει σε πολλά χρονικά σημεία μετά τη θεραπεία. «Ενώ άλλες μελέτες έχουν προτείνει ότι το μικροβίωμα του εντέρου είναι διαφορετικό σε ασθενείς με καρκίνο που έχουν κακή απόδοση, έναντι αυτών που τα πηγαίνουν
καλά, λίγοι έχουν αξιολογήσει τις επιλογές που μπορούν να κάνουν οι ασθενείς και οι γιατροί για να επηρεάσουν το μικροβίωμα» επισημαίνει η Bhatt. «Αυτή η μελέτη βοηθά στη σύνδεση ορισμένων από τις κουκκίδες, διαπιστώνοντας ότι η χρήση αντιβιοτικών συνδέεται με χαμηλότερους αριθμούς ενός τύπου κυκλοφορούντων ανοσοκυττάρων που είναι σημαντικά για την καταπολέμηση του καρκίνου. Εξακολουθούμε να μη γνωρίζουμε αν το μικροβίωμα είναι ο κρίσιμος συνδετικός παράγοντας μεταξύ της χρήσης αντιβιοτικών και των αποτελεσμάτων του καρκίνου, αλλά υποψιαζόμαστε ότι μπορεί να είναι βασικός παράγοντας».

40 / Μάρτιος-Απρίλιος 2023 ΕΡΕΥΝΑ
Η νέα μελέτη είναι η πρώτη που συσχετίζει τη χρήση αντιμικροβιακών
ουσιών τόσο με
τον αριθμό των κυκλοφορούντων λεμφοκυττάρων
Η Ransohoff και οι συνεργάτες της χρησιμοποίησαν μια βάση δεδομένων που ονομάζεται Oncoshare, η οποία ενσωματώνει ηλεκτρονικά αρχεία υγείας και δεδομένα
από το Μητρώο Καρκίνου της Καλιφόρνια.
Οι γυναίκες στη μελέτη διαγνώστηκαν με
μη μεταστατικό (στάδια 1 έως 3) τριπλό αρ-
νητικό καρκίνο του μαστού και υποβλήθηκαν σε θεραπεία με χημειοθεραπεία και, αν χρειαζόταν, χειρουργική επέμβαση. Στο 84% των γυναικών συνταγογραφήθη-
καν αντιμικροβιακά κάποια στιγμή μετά
τη διάγνωση του καρκίνου. Το 99% αυτών των συνταγών ήταν για αντιβιοτικά. Ο διάμεσος χρόνος παρακολούθησης για τη μελέτη ήταν 104 μήνες. Οι ερευνητές διαπίστωσαν ότι, κατά τη διάρκεια της πολυετούς περιόδου μελέτης, το 20% των γυναικών στις οποίες δεν συνταγογραφήθηκαν αντιμικροβιακά κατά τη διάρκεια της μελέτης πέθαναν. Αντίθετα, το 23% των γυναικών που είχαν ποτέ λάβει αντιμικροβιακά πέθαναν. Δεν υπήρχε στατιστικά σημαντική διαφορά στον κίνδυνο θανάτου από καρκίνο του μαστού μεταξύ της μέσης γυναίκας που λάμβανε αντιμικροβιακά από τη διάγνωση, γεγονός που υποδηλώνει ότι ο κίνδυνος που σχετίζεται με κάθε συνταγή ήταν μικρός. Ωστόσο, η Ransohoff και οι συνεργάτες της διαπίστωσαν ότι ο κίνδυνος θανάτου από καρκίνο του μαστού αυξήθηκε όχι μόνο με τον συνολικό αριθμό συνταγών που είχε λάβει μια γυναίκα από τη στιγμή της διάγνωσης, αλλά και με τον αριθμό των μοναδικών φαρμάκων στα οποία εκτέθηκε (αμοξικιλλίνη έναντι τετρακυκλίνης, για παράδειγμα).
Η συσχέτιση μεταξύ της χρήσης αντιμικροβιακών και του αυξημένου κινδύνου θανά-
του διήρκεσε περίπου τρία χρόνια μετά τη διάγνωση του καρκίνου των γυναικών. ο κίνδυνος μειώθηκε σταδιακά μετά το τέταρτο και πέμπτο έτος. Περαιτέρω ανάλυση έδειξε ότι η συσχέτιση δεν οφειλόταν στο πόσο άρρωστοι ήταν οι ασθενείς όταν λάμβαναν τα φάρμακα.
Τα δεδομένα από το Oncoshare δεν περιλάμβαναν πληροφορίες σχετικά με τα μικροβιώματα του εντέρου των ασθενών, τα οποία συνήθως λαμβάνονται μέσω δειγμάτων κοπράνων. Αλλά η Ransohoff και οι συνεργάτες της ελπίζουν να σχεδιάσουν μια νέα μελέτη που θα συσχετίζει άμεσα τη σύνθεση του μικροβιώματος του εντέρου με τον αριθμό των λεμφοκυττάρων και τη μακροπρόθεσμη επιβίωση του καρκίνου. «Θα θέλαμε να δούμε απευθείας το μικροβίωμα του εντέρου και να δούμε πώς η έκθεση στα αντιβιοτικά διαμορφώνει το μικροβίωμα του εντέρου» λέει η Ransohoff. «Αλλά αυτή η μελέτη σίγουρα εγείρει το ερώτημα πώς τα ευρήματά μας θα πρέπει να επηρεάσουν την κλινική φροντίδα των ασθενών με καρκίνο. Οι ερευνητές προειδοποιούν να μην εφαρμοστούν τα ευρήματα της μελέτης πολλών εκατοντάδων γυναικών σε οποιοδήποτε άτομο». «Οι ασθενείς δεν πρέπει να πανικοβάλλονται αν υποβληθούν σε θεραπεία με αντιβιοτικά μετά από διάγνωση καρκίνου του μαστού» υπογραμμίζει η Kurian. «Σε κάθε μεμονωμένη περίπτωση, η αύξηση του κινδύνου δεν είναι μεγάλη. Αλλά, συνολικά, αυτά τα ευρήματα υποδηλώνουν μια σχέση μεταξύ της χρήσης αντιβιοτικών, του ανοσοποιητικού συστήματος και της επιβίωσης από τον καρκίνο του μαστού, κάτι που χρήζει περαιτέρω μελέτης».•••


διαπίστωσαν ότι, κατά τη διάρκεια
της πολυετούς
περιόδου
μελέτης, το 20%
των γυναικών
στις οποίες δεν
συνταγογραφήθηκαν αντιμικροβιακά
κατά τη διάρκεια
της μελέτης
πέθαναν.
41 ΑΦΙΕΡΩΜΑ ΑΙΜΑΤΟΛΟΓΙΑ
Οι ερευνητές
Εξελίξεις στο λέμφωμα Hodgkin
Μαγδαληνή Μήγκου, παθολόγο-ογκολόγο, επιμελήτρια Β’ στη Θεραπευτική Κλινική του ΓΝ Αλεξάνδρα, Ιατρική Σχολή ΕΚΠΑ
Ευάγγελο Τέρπο, καθηγητή Θεραπευτικής-Αιματολογίας στη Θεραπευτική Κλινική του ΓΝ Αλεξάνδρα, Ιατρική Σχολή ΕΚΠΑ
Μελέτιο-Αθανάσιο Δημόπουλο, καθηγητή Θεραπευτικής-ΑιματολογίαςΟγκολογίας στη Θεραπευτική Κλινική του ΓΝ Αλεξάνδρα, Ιατρική Σχολή ΕΚΠΑ
Έχουν ήδη δημοσιευτεί τα αποτελέσματα από την πενταετή παρακολούθηση νεοδιαγνωσθέντων ασθενών με σταδίου
ΙΙΙ ή IV κλασικό λέμφωμα Hodgkin, που
ανέδειξαν μακροχρόνια επιβίωση χωρίς
πρόοδο νόσου σε ασθενείς που έλαβαν ως πρώτη γραμμή μπρεντουξιμάβη βεντοτίνη (brentuximab vedotin), ενός συζευγμένου αντισώματος που στοχεύει το CD-30, σε συνδυασμό με δοξορουβικίνη, βινπλαστίνη και δακαρβαζίνη (A+AVD)
[1], σε σύγκριση με το κλασικό σχήμα διξορουβικίνη, μπλεομυκίνη, βινπλαστίνη και δακαρβαζίνη (ABVD).
Σε μια προσχεδιασμένη ενδιάμεση ανάλυση, φάνηκε πιθανό όφελος σε σχέση με την ολική επιβίωση και παρουσιάστηκαν τα αποτελέσματα μετά από μια περίοδο παρακολούθησης 6 ετών. Τυχαιοποιήθηκαν ασθενείς σε 1:1 αναλογία να
λάβουν έως 6 κύκλους είτε A+AVD είτε ABVD. Το πρωτεύον καταληκτικό σημείο ήταν η επιβίωση χωρίς πρόοδο νόσου και έχει ανακοινωθεί σε προηγούμενη δημοσίευση.

Σημαντικό δευτερεύον καταληκτικό σημείο
είναι η ολική επιβίωση στον πληθυσμό με πρόθεση θεραπείας. Επίσης, αναλύθηκε η ασφάλεια. Συνολικά, 664 ασθενείς έ-
42 / Μάρτιος-Απρίλιος 2023
ΑΡΘΡΟ
Από τους:
43 ΑΦΙΕΡΩΜΑ ΑΙΜΑΤΟΛΟΓΙΑ
Τα τελικά αποτελέσματα της
μελέτης NIVAHL
επιβεβαιώνουν την
αποτελεσματικότητα
και το ευνοϊκό
προφίλ τοξικότητας από τη χρήση της νιβολουμάμπης
σε ασθενείς με HL στην πρώτη

γραμμή θεραπείας.
λαβαν A+AVD και 670 έλαβαν ABVD. Μετά από 73 μήνες διάμεση παρακολούθηση, 39 ασθενείς στην ομάδα A+AVD και 64 στην ομάδα ABVD κατέληξαν (hazard ratio, 0.59; 95% confidence interval [CI], 0.40 to 0.88; P=0.009).
Η εξαετής ολική επιβίωση ήταν 93,9% (95% CI, 91.6 to 95.5) στην ομάδα A+AVD και 89,4% (95% CI, 86.6 to 91.7) στην ομάδα ABVD. Η επιβίωση ελεύθερη προόδου νόσου ήταν μεγαλύτερη για την ομάδα A+AVD από ό,τι για την ομάδα ABVD (hazard ratio για πρόοδο νόσου ή θάνατο, 0.68; 95% CI, 0.53 to 0.86). Λιγότεροι
ασθενείς στην ομάδα A+AVD σε σχέση με την ομάδα ABVD έλαβαν επόμενη γραμμή θεραπείας, συμπεριλαμβανομένης της μεταμόσχευσης, και λιγότερες δεύτερες κακοήθειες αναφέρθηκαν με A+AVD (σε 23, έναντι 32 ασθενών). Συστήθηκε η προφυλακτική χορήγηση παράγοντα διέγερσης των αποικιών των κοκκιοκυττάρων μετά την αυξημένη επίπτωση εμπύρετης ουδετεροπενίας που παρατηρήθηκε με το A+AVD. Περισσότεροι ασθενείς στην ομάδα A+AVD εμφάνισαν περιφερική νευροπάθεια από ό,τι στην ομάδα ABVD, αλλά και στις δύο ομάδες αυτή βελτιώθηκε ή εξαφανίστηκε κατά την περίοδο της παρακολούθησης.
Φαίνεται πως οι ασθενείς που λαμβάνουν A+AVD για την αντιμετώπιση σταδίου III ή IV λεμφώματος Hodgkin έχουν πλεονέκτημα επιβίωσης σε σχέση με όσους λαμβάνουν ABVD.
Στην τυχαιοποιημένη, Φάσεως ΙΙ μελέτη
NIVAHL[2] που διενεργήθηκε από τον ερευνητή για ασθενείς με πρώιμο στάδιο με δυσμενή χαρακτηριστικά κλασικού λεμφώματος Hodgkin (HL), δύο διαφορετικά σχήματα με 4 κύκλους από νιβολουμάμπη, δοξορουβικίνη, βινπλαστίνη και δακαρβαζίνη ακολουθούμενη από 30 Gy ακτινοθεραπείας είχαν ως αποτέλεσμα υψηλά ποσοστά ανταπόκρισης και μια σημαντική, 1 έτους επιβίωση ελεύθερης νόσου σε 109 ασθενείς.
Στην τελευταία ανάλυση, που έγινε 3 χρόνια μετά τη συμμετοχή του τελευταίου ασθενούς, συμπεριλαμβάνονται και μακροχρόνια δεδομένα ασφαλείας. Δεν παρατηρήθηκαν δεδομένα επιβίωσης μετά την πρώτη ανάλυση, και μετά από διάμεση παρακολούθηση 41 μηνών, η ολική επιβίωση είναι 100% και στις δύο ομάδες ασθενών.
Η επιβίωση ελεύθερης νόσου ήταν 98% και 100% στο σκέλος με τη διαδοχική και ταυτόχρονη θεραπεία με νιβολουμάμπη, δοξορουβικίνη, βινπλαστίνη και δακαρβαζίνη, αντίστοιχα.
Στην τελευταία επίσκεψη παρακολούθησης, η μέση εξαναγκασμένη εκπνευστική πίεση στο ένα δευτερόλεπτο ήταν 95,5% (SD 12.7%), η μέση ικανότητα διάχυσης μονοξειδίου του άνθρακα προσαρμοσμένη για την αιμοσφαιρίνη ήταν 82,8% (SD 15.4%) και το κλάσμα εξώθησης ήταν φυσιολογικό στο 95% των ασθενών. Υποθυρεοειδισμό που χρειαζόταν μακροχρόνια αγωγή εμφάνισε το 15% των ασθενών και ήταν σχεδόν αποκλειστικά γυναίκες (87%). Δεν υπήρχαν δεύτερες πρωτοπαθείς κακοήθειες και κανένας ασθενής δεν χρειαζόταν αγωγή με κορτικοστεροειδή στην τελευταία επίσκεψη παρακολούθησης. Αυτή η προγραμματισμένη ανάλυση της μεγαλύτερης μελέτης για τη χρήση ενός παράγοντα που στοχεύει την πρωτεΐνη προγραμματισμένου κυτταρικού θανάτου-1 σε ασθενείς με HL στην πρώτη γραμμή θεραπείας επιβεβαιώνει την αποτελεσματικότητα και το ευνοϊκό προφίλ τοξικότητας αυτού του θεραπευτικού πρωτοκόλλου.
Η μελέτη AHL2011[3] έδειξε ότι η αποκλιμάκωση της θεραπείας μετά από τα αποτελέσματα PET μετά από 2 κύκλους ετοποσίδης, κυκλοφωσφαμίδης και δοξορουβικίνης, μπλεομυκίνης, βινκριστίνης, προκαρβαζίνης και πρεδνιζόνης έχει παρόμοια αποτελέσματα σε ό,τι αφορά επιβίωση χωρίς πρόοδο νόσου και ολική επιβίωση και μειώνει την πρώιμη τοξικότητα σε σύγκριση με τη σταθερή θεραπεία. Τον Απρίλιο του 2022, ανακοινώθηκαν τα τελικά αποτελέσματα της μελέτης. Ασθενείς με
44 / Μάρτιος-Απρίλιος 2023
ΑΡΘΡΟ
εκτεταμένο στάδιο νόσου Hodgkin (στάδιο III, IV ή IIB με αναλογία μεσοθωρακίου/ θώρακος > 0,33 ή εξωλεμφική συμμετοχή) ηλικίας 16-60 ετών τυχαιοποιήθηκαν
μεταξύ 6 χ BEACOPP και ενός σκέλους με διενέργεια PET μετά 2 χ BEACOPP, οπότε και χορηγήθηκαν 4 χ ABVD (δοξορουβικίνης, μπλεομυκίνης, βινμπλαστίνης και δακαρβαζίνης) σε PET2– και 4 χ BEACOPP σε PET2+ ασθενείς.
Το PET μετά τους 4 κύκλους χημειοθεραπείας έπρεπε να είναι αρνητικό για να ολοκληρωθεί η προγραμματισμένη θεραπεία. Συνολικά, 823 ασθενείς συμμετείχαν στη μελέτη, 413 στο τυπικό σκέλος και 410 στο σκέλος με το ενδιάμεσο PET. Με 67,2 μήνες διάμεσο χρόνο παρακολούθησης, η πενταετής επιβίωση χωρίς πρόοδο νόσου (87.5% v 86.7%; hazard ratio [HR] = 1.07; 95% CI, 0.74 με 1.57; P = .67) και
ολικής επιβίωσης (97.7% και στα δύο σκέλη; HR = 1.012; 95% CI, 0.50 με 2.10; P = .53) ήταν παρόμοια και στα δύο σκέλη τυχαιοποίησης.
Για το σύνολο των ασθενών, το ενδιάμεσο
PET προέβλεπε την πενταετή PFS (92,3% σε PET2–/PET4–, 75,4% [HR = 3.26; 95% CI, 18.3 to 5.77] σε PET2+/PET4–
και 46,5% [HR = 12.4; 95% CI, 7.31 to 19.51] σε PET4+ ασθενείς, αντίστοιχα; P < .0001) ανεξαρτήτως του διεθνούς προγνωστικού σκορ.
Η πενταετής ολική επιβίωση επηρεάστηκε επίσης από τα αποτελέσματα του ενδιάμεσου PET, και PET2+/PET4– ασθενείς (93.5%; HR = 3.3; 95% CI, 1.07 με 10.1; P = .036) και PET4+ ασθενείς (91.9%; HR = 3.756; 95% CI, 1.07 με 13.18; P = .038) είχαν σημαντικά μικρότερη ολική επιβίωση από τους PET2–/PET4– ασθενείς (98,2%). Εικοσιδύο ασθενείς (2,7%) εμφάνισαν δεύτερη πρωτοπαθή κακοήθεια, 13 (3,2%) και 9 (2,2%) στο τυπικό και στο πειραματικό σκέλος, αντίστοιχα. Η παρατεταμένη παρακολούθηση επιβεβαιώνει την αποτελεσματικότητα και ασφάλεια της μελέτης AHL2011 και της στρατηγικής με αποκλιμάκωση της θεραπείας μετά ενδιάμεσο PET, η οποία δεν είναι κατώτερη της τυπικής θεραπείας με έξι κύκλους BEACOPP. Το PET4 παρέχει επιπρόσθετες προγνωστικές πληροφορίες συγκριτικά με το PET2 και βοηθά στην ανεύρεση ασθενών με ιδιαίτερα φτωχή πρόγνωση. Ασθενείς με ογκώδη κλασική νόσο Hodgkin σταδίου Ι/ΙΙ (cHL) αντιμετωπίζονται με χημειοθεραπεία που ακολουθείται από ακτινοθεραπεία. Απώτερες ανεπιθύμητες ενέργειες που σχετίζονται με την ακτινο-
θεραπεία περιλαμβάνουν τον αυξημένο κίνδυνο δεύτερης κακοήθειας και καρδιαγγειακής νόσου. Οι ερευνητές[4] μελέτησαν μια προσέγγιση στην οποία ασθενείς με ογκώδη κλασική νόσο Hodgkin, σε πρώιμο στάδιο, υποβλήθηκαν σε ενδιάμεσο PET, όπου σε ασθενείς με PETνόσο να παραλείπεται η ακτινοθεραπεία, ενώ σε ασθενείς με PET+ νόσο να γίνεται εντατικοποίηση της θεραπείας. Κατάλληλοι ήταν οι ασθενείς με ογκώδη νόσο (μάζα > 10 εκ ή 1/3 της μέγιστης διαθωρακικής διαμέτρου σε ακτινογραφία θώρακος) οι οποίοι και έλαβαν δύο κύκλους δοξορουβικίνης, μπλεομυκίνης, βινμπλαστίνης και δακαρβαζίνης (ABVD) ακολουθούμενο από ενδιάμεσο PET (PET2). Οι ασθενείς με PET2–, που ορίζεται ως 13 σε κλίμακα 5-βαθμών, έλαβαν ακόμα 4 κύκλους δοξορουβικίνης, μπλεομυκίνης, βινμπλαστίνης και δακαρβαζίνης. Ασθενείς με PET2+ έλαβαν 4 κύκλους αυξανόμενων δόσεων ετοποσίδης, κυκλοφωσφαμίδης και δοξορουβικίνης και σταθερές δόσεις μπλεομυκίνης, βινκριστίνης, προκαρβαζίνης και πρεδνιζόνης, ακολουθούμενη από 30.6 Gy ακτινοθεραπείας.
Από τους 94 αξιολογήσιμους ασθενείς το 53% ήταν γυναίκες με διάμεση ηλικία τα 30 έτη (εύρος 18-58 έτη). Ογδόντα-πέντε (90%) είχαν νόσο σταδίου II, συμπεριλαμβανομένων 48 (51%) με στάδιο IIB/IIBE. Εβδομήντα-οκτώ (78%) ήταν PET2– και 21 (22%) και PET2+. Η κυρίαρχη τοξικότητα ήταν η ουδετροπενία, με 9% των ασθενών να εμφανίζουν εμπύρετη ουδετεροπενία και ένας ασθενής να εμφανίζει σήψη. Το πρωτεύον καταληκτικό σημείο ήταν η τριετής επιβίωση χωρίς πρόοδο νόσου (PFS) και ήταν 93,1% σε PET2– και 89,7% σε PET2+ ασθενείς.
Η τριετής ολική επιβίωση ήταν 98,6% και 94,4%, αντίστοιχα. Η εκτιμώμενη αναλογία κινδύνου συγκρίνοντας το PFS μεταξύ των ασθενών με PET2+ και των ασθενών με PET2- ήταν 1,03, σημαντικά χαμηλότερο από τη μηδενική υπόθεση του 4,1.
Στη μελέτη μας για θεραπεία προσαρμοσμένη στα αποτελέσματα του ενδιάμεσου PET σε ασθενείς με ογκώδη νόσο σταδίου Ι/ΙΙ κλασικού λεμφώματος Hodgkin επετεύχθη το πρωτεύον καταληκτικό σημείο και σχετίστηκε με εξαιρετική τριετή επιβίωση χωρίς υποτροπή της νόσου στο 92,3% για όλους τους ασθενείς, με την πλειοψηφία αυτών να έχουν αποφύγει την ακτινοθεραπεία και την έκθεση σε εντατική χημειοθεραπεία.•••
σταδίου Ι/ΙΙ
Βιβλιογραφία
1. Ansell, S.M., et al., Overall Survival with Brentuximab Vedotin in Stage III or IV Hodgkin’s Lymphoma. New England Journal of Medicine, 2022. 387(4): p. 310-320.
2. Bröckelmann, P.J., et al., Nivolumab and Doxorubicin, Vinblastine, and Dacarbazine in Early-Stage Unfavorable Hodgkin Lymphoma: Final Analysis of the Randomized German Hodgkin Study Group Phase II NIVAHL Trial. Journal of Clinical Oncology. 0(0): p. JCO.22.02355.
3. Casasnovas, R.-O., et al., Positron Emission Tomography–Driven Strategy in Advanced Hodgkin Lymphoma: Prolonged Follow-Up of the AHL2011 Phase III Lymphoma Study Association Study. Journal of Clinical Oncology, 2022. 40(10): p. 1091-1101.
4. LaCasce, A.S., et al., Positron Emission Tomography–Adapted Therapy in Bulky Stage I/II Classic Hodgkin Lymphoma: CALGB 50801 (Alliance). Journal of Clinical Oncology. 0(0): p. JCO.22.00947.
45 ΑΦΙΕΡΩΜΑ ΑΙΜΑΤΟΛΟΓΙΑ
Σε ασθενείς με
ογκώδη κλασική
νόσο Hodgkin
(cHL) μπορεί να
η έκθεση
εντατική χημειοθεραπεία με
ενδιάμεσο PET μετά ABVD.
παραλειφθεί η
ακτινοθεραπεία και
σε
αρνητικό
Από τους:
Ιωάννη Ντάναση-Σταθόπουλο, επιστημονικό συνεργάτη στη
Θεραπευτική Κλινική του ΓΝ Αλεξάνδρα, Ιατρική Σχολή ΕΚΠΑ
Μαρία Γαβριατοπούλου, αναπληρώτρια καθηγήτρια
Θεραπευτικής-Ογκολογίας στη
Θεραπευτική Κλινική του ΓΝ
Αλεξάνδρα, Ιατρική Σχολή ΕΚΠΑ
Μελέτιο-Αθανάσιο Δημόπουλο,
καθηγητή ΘεραπευτικήςΑιματολογίας-Ογκολογίας στη
Θεραπευτική Κλινική του ΓΝ
Αλεξάνδρα, Ιατρική Σχολή ΕΚΠΑ
HΜακροσφαιριναιμία Waldenström (WM) είναι ένα σπάνιο λεμφοπλασματικό λέμφωμα χαμηλής κακοήθειας, που χαρακτηρίζεται από ετερογενές κλινικό και γονιδιωματικό προφίλ. Η παρουσία μεταλλάξεων στο γονίδιο CXCR4 και η θρομβοπενία αποτελούν ανεξάρτητους προγνωστικούς παράγοντες για βραχύτερο διάστημα ελεύθερο προόδου νόσου (PFS) σε ασθενείς που λαμβάνουν θεραπεία με ιμπρουτινίμπη.
Τα θεραπευτικά σχήματα με βάση την μπορτεζομίμπη είναι ιδιαίτερα αποτελεσματικά σε ασθενείς με ανθεκτική νόσο σε αναστολείς της τυροσινικής κινάσης του Bruton, όπως η ιμπρουτινίμπη. Η αποτελεσματικότητα των αναστολέων της τυροσινικής κινάσης του Bruton 1ης και 2ης γενιάς είναι συγκρίσιμη.
Οι αναστολείς 1ης γενιάς εμφανίζουν μεγαλύτερο κίνδυνο για κολπική μαρμαρυγή, ενώ οι αναστολείς 2ης γενιάς εμφανίζουν μεγαλύτερο κίνδυνο για λοιμώξεις και ουδετεροπενία. Οι ασθενείς με WM παρουσιάζουν επηρεασμένη αντισωματική απόκριση μετά τον εμβολιασμό Covid-19, γεγονός το οποίο ενισχύει την ανάγκη για έγκαιρο εμβολιασμό και με τις αναμνηστικές δόσεις με σύγχρονη αυστηρή τήρηση όλων των μέτρων προστασίας.
Η Μακροσφαιριναιμία Waldenström (WM)
είναι ένα σπάνιο λεμφοπλασματικό λέμφωμα χαμηλής κακοήθειας, που χαρακτηρίζεται από ετερογενές κλινικό και γονιδιωματικό προφίλ (Dogliotti et al 2022).
Στη Θεραπευτική Κλινική δείξαμε ότι η χρήση της ιδιαίτερα ευαίσθητης τεχνικής Cast-PCR (competitive allele-specific
polymerase chain reaction) μπορεί να προσφέρει σημαντικά στην καθημερινή κλινική πρακτική για την ανίχνευση της μεταλλαγής L265P του γονιδίου MYD88, που είναι χαρακτηριστικό της WM, τόσο σε DNA του όγκου (tDNA) όσο και σε δείγμα ελεύθερου κυκλοφορούντος DNA στο περιφερικό αίμα (cfDNA) (Bagratuni et al 2022).
Οι νεότερες τεχνικές είναι ιδιαίτερα σημαντικές για την καλύτερη αντιμετώπιση των ασθενών με WM, αλλά είναι εξίσου απαραίτητο να διασφαλιστεί η πρόσβαση των ασθενών σε αυτές τις διαγνωστικές τεχνικές και στις νεότερες θεραπείες (Riva et al 2022).
Η τυροσινική κινάση του Bruton (BTK) είναι σημαντική για τις οδούς σηματοδότησης που απαιτούνται για την επιβίωση των κακοήθων κυττάρων της WM και οι αναστολείς της ΒΤΚ έχουν, επί του παρόντος, κεντρικό ρόλο στη θεραπεία της WM. Η ιμπρουτινίμπη είναι ο βασικότερος αναστολέας της BTK και έχει λάβει έγκριση για τη χορήγηση σε ασθενείς με WM. Η ιμπρουτινίμπη είναι ιδιαίτερα αποτελεσματική και οδηγεί σε μακροχρόνιο έλεγχο της νόσου σε ασθενείς που έχουν λάβει προηγουμένως θεραπεία για την WM, ενώ οι ανεπιθύμητες ενέργειες είναι διαχειρίσιμες.
Η παρουσία μεταλλάξεων στο γονίδιο CXCR4 και η θρομβοπενία αποτελούν ανεξάρτητους προγνωστικούς παράγοντες για βραχύτερο διάστημα ελεύθερο προόδου νόσου (PFS) σε ασθενείς που λαμβάνουν θεραπεία με ιμπρουτινίμπη, σύμφωνα με ανάλυση δεδομένων 319 που
46 / Μάρτιος-Απρίλιος 2023
Εξελίξεις στη
ΑΡΘΡΟ
Μακροσφαιριναιμία Waldenström
έλαβαν μονοθεραπεία με ιμπρουτινίμπη (Castillo et al 2022).
Οι ασθενείς που υποτροπιάζουν υπό θεραπεία με ιμπρουτινίμπη αποτελούν πρόκληση για τον θεράποντα ιατρό. Αναδρομικά δεδομένα δείχνουν ότι τα θεραπευτικά σχήματα με βάση τον αναστολέα πρωτεασώματος μπορτεζομίμπη είναι ιδιαίτερα αποτελεσματικά σε ασθενείς με ανθεκτική νόσο σε αναστολείς της τυροσινικής κινάσης του Bruton, όπως η ιμπρουτινίμπη (Khwala et al 2022).
Το 2022, δημοσιεύτηκαν τα αποτελέσματα μελετών που αξιολόγησαν την αποτελεσματικότητα νεότερων φαρμάκων σε ασθενείς με υποτροπιάζουσα/ανθεκτική WM. Η ζανουμπρουτινίμπη είναι ένας νεότερος αναστολέας της τυροσινικής κινάσης του Bruton και έδειξε ιδιαίτερα ενθαρρυντικά αποτελέσματα όσον αφορά στην αποτελεσματικότητα, την ασφάλεια και την ανοχή σε μια μελέτη Φάσης ΙΙ, στην οποία συμμετείχαν 67 ασθενείς που είχαν δυσανεξία στην ιμπρουνίμπη ή/ και στην ακαλαμπρουτινίμπη (Shadman et al 2022).
Η ορελαμπρουτινίμπη είναι ένας άλλος νεότερος αναστολέας της τυροσινικής κι-
νάσης του Bruton και αξιολογήθηκε σε μια μελέτη Φάσης ΙΙ που πραγματοποιήθηκε στην Κίνα. Πάνω από το 80% από τους 66 ασθενείς με ανθεκτική/υποτροπιάζουσα WM εμφάνισαν μείζονες ανταποκρίσεις με αποδεκτό προφίλ ασφαλείας (Cao et al 2022).
Η τιραμπρουτινίμπη είναι επίσης ένας νεότερος αναστολέας της τυροσινικής κινάσης του Bruton που έδειξε υψηλά ποσοστά άνω του 90% στο διάστημα ελεύθερο προόδου νόσου και στην ολική επιβίωση στα 2 έτη μετά την έναρξη της θεραπείας μεταξύ 27
47 ΑΦΙΕΡΩΜΑ
ΑΙΜΑΤΟΛΟΓΙΑ
Η Μακροσφαιριναιμία Waldenström (WM) είναι ένα σπάνιο λεμφοπλασματικό λέμφωμα χαμηλής κακοήθειας, που χαρακτηρίζεται
από ετερογενές κλινικό και γονιδιωματικό προφίλ.
Βιβλιογραφία
Abushukair H, Syaj S, Ababneh O, et al. First- versus second-generation Bruton tyrosine kinase inhibitors in Waldenström’s Macroglobulinemia: A systematic review and meta-analysis. Am J Hematol. 2022;97(7):942-950.
Bagratuni T, Markou A, Patseas D, et al. Determination of MYD88L265P mutation fraction in IgM monoclonal gammopathies. Blood Adv. 2022;6(1):189-199.
Beaton B, Sasson SC, Rankin K, et al. Patients with treated indolent lymphomas immunized with BNT162b2 have reduced anti-spike neutralizing IgG to SARSCoV-2 variants, but preserved antigenspecific T cell responses. Am J Hematol. 2023;98(1):131-139.
Cao XX, Jin J, Fu CC, et al. Evaluation of orelabrutinib monotherapy in patients with relapsed or refractory Waldenström’s macroglobulinemia in a single-arm, multicenter, open-label, phase 2 study. EClinicalMedicine. 2022;52:101682.
Castillo JJ, Sarosiek SR, Gustine JN, et al. Response and survival predictors in a cohort of 319 patients with Waldenström macroglobulinemia treated with ibrutinib monotherapy. Blood Adv. 2022;6(3):10151024.
ασθενών με WM (Sekigushi et al 2022).
Μια συστηματική ανασκόπηση και μεταανάλυση 11 μελετών έδειξε ότι η αποτελεσματικότητα των αναστολέων της τυροσινικής κινάσης του Bruton 1ης και 2ης γενιάς είναι συγκρίσιμη. Οι αναστολείς
1ης γενιάς εμφανίζουν μεγαλύτερο κίνδυνο για κολπική μαρμαρυγή, ενώ οι αναστολείς 2ης γενιάς εμφανίζουν μεγαλύτερο κίνδυνο για λοιμώξεις και ουδετεροπενία (Abushukair et al 2022).
Οι ασθενείς με αιματολογικές κακοήθειες, συμπεριλαμβανομένης της WM, έχουν μεγαλύτερο κίνδυνο σοβαρής νόσου Covid-19 και εμφανίζουν μειωμένη χυμική ανοσία μετά τον εμβολιασμό τους έναντι του SARS-CoV-2 (Tomowiak et al 2022).
Αυτό οφείλεται και στο ανοσοκατασταλτικό μικροπεριβάλλον, καθώς τα κακοήθη κύτταρα της WM οδηγούν στην επικράτηση υποτύπων λεμφοκυττάρων με ανοσοκατασταλτική δράση, σύμφωνα και με μελέτες ανάλυσης μοναδιαιών κυττάρων (singlecell profiles) (Sun et al 2022).
Αξίζει να σημειωθεί ότι ακόμα και ασθενείς με ασυμπτωματική WM παρουσιάζουν μειωμένη αντισωματική απάντηση
στον εμβολιασμό έναντι του SARS-CoV-2
(Konishi et al 2022). Ωστόσο, οι κυτταρικές ανοσολογικές αποκρίσεις Τ-λεμφοκυττάρων φαίνεται να διατηρούνται (Beaton et al 2022). Πρόσφατα δεδομένα από τη
Θεραπευτική Κλινική δείχνουν ότι ακόμα και ο αναμνηστικός εμβολιασμός με το εμβόλιο BNT162b2 οδηγεί σε χαμηλότερη παραγωγή αντισωμάτων έναντι της πρωτεϊνικής ακίδας και σε υποδεέστερη εξουδετέρωση των υποστελεχών Omicron BA.4/5 του SARS-CoV-2 συγκριτικά με τους υγιείς (Rosati et al 2022).
Η λήψη θεραπείας για το υποκείμενο νόσημα τη στιγμή του εμβολιασμού και ιδιαίτερα η θεραπεία με παράγοντες όπως τα μονοκλωνικά αντισώματα έναντι του CD20 και οι αναστολείς της BTK αποτελούν τους πιο σημαντικούς αρνητικούς προγνωστικούς παράγοντες για μειωμένη αντισωματική απόκριση μετά τον εμβολιασμό σε αυτήν την ομάδα ασθενών (Terpos et al 2022). Συμπερασματικά, οι ασθενείς με WM παρουσιάζουν επηρεασμένη αντισωματική απόκριση, γεγονός που ενισχύει την ανάγκη για έγκαιρο εμβολιασμό και με αναμνηστικές δόσεις με σύγχρονη αυστηρή τήρηση όλων των μέτρων προστασίας.•••
Dogliotti I, Jiménez C, Varettoni M, et al. Diagnostics in Waldenström’s macroglobulinemia: a consensus statement of the European Consortium for Waldenström’s Macroglobulinemia Leukemia. 2022;10.1038/s41375-02201762-3.
Khwaja J, Uppal E, Baker R, et al. Bortezomib-based therapy is effective and well tolerated in frontline and multiply pre-treated Waldenström macroglobulinaemia including BTKi failures: A real-world analysis. EJHaem. 2022;3(4):1330-1334.
Konishi Y, Sklavenitis-Pistofidis R, Yue H, et al. Attenuated response to SARS-CoV-2 vaccine in patients with asymptomatic precursor stages of multiple myeloma and Waldenström macroglobulinemia. Cancer Cell. 2022;40(1):6-8.
Riva E, Duarte PJ, Valca‘rcel B, et al. Treatment and Survival Outcomes of Waldenström Macroglobulinemia in Latin American Patients: A Multinational Retrospective Cohort Study. JCO Glob Oncol. 2022;8:e2100380.
Rosati M, Terpos E, Bear J, et al. Low Spike Antibody Levels and Impaired BA.4/5 Neutralization in Patients with Multiple Myeloma or Waldenström’s Macroglobulinemia after BNT162b2
Booster Vaccination. Cancers (Basel). 2022;14(23):5816.
Sekiguchi N, Rai S, Munakata W, et al. Twoyear outcomes of tirabrutinib monotherapy in Waldenström’s macroglobulinemia. Cancer Sci. 2022;113(6):2085-2096.
Shadman M, Flinn IW, Levy MY, et al. Zanubrutinib in patients with previously treated B-cell malignancies intolerant of previous Bruton tyrosine kinase inhibitors in the USA: a phase 2, open-label, singlearm study. Lancet Haematol. 2022;S23523026(22)00320-9.
Sun H, Fang T, Wang T, et al. Single-cell profiles reveal tumor cell heterogeneity and immunosuppressive microenvironment in Waldenström macroglobulinemia. J Transl Med. 2022;20(1):576.
Terpos E, Fotiou D, Karalis V, et al. SARSCoV-2 humoral responses following booster BNT162b2 vaccination in patients with B-cell malignancies. Am J Hematol. 2022;97(10):1300-1308.
Tomowiak C, Leblond V, Laribi K, et al. Response to vaccination against SARSCoV-2 in 168 patients with Waldenström macroglobulinaemia: A French Innovative Leukaemia Organization study. Br J Haematol. 2022;197(4):424-427.
48 / Μάρτιος-Απρίλιος 2023
ΑΡΘΡΟ
49 ΑΦΙΕΡΩΜΑ
ΑΙΜΑΤΟΛΟΓΙΑ
Από τους:
Π. Μαλανδράκη, ειδικευόμενο Παθολογικής
Ογκολογίας στη Θεραπευτική
Κλινική του ΓΝ Αλεξάνδρα, Ιατρική
Σχολή ΕΚΠΑ
Φ. Θεοδωρακάκου, ειδικευόμενη Αιματολογίας στη
Θεραπευτική Κλινική του ΓΝ
Αλεξάνδρα, Ιατρική Σχολή ΕΚΠΑ
Μ.Α. Δημόπουλο, καθηγητή ΘεραπευτικήςΟγκολογίας-Αιματολογίας στη
Θεραπευτική Κλινική του ΓΝ Αλεξάνδρα, Ιατρική Σχολή ΕΚΠΑ
Ε. Καστρίτη, καθηγητή ΘεραπευτικήςΟγκολογίας στη Θεραπευτική
Κλινική του ΓΝ Αλεξάνδρα, Ιατρική Σχολή ΕΚΠΑ
Στη θεραπεία του πολλαπλού μυελώματος η αναγνώριση των ασθενών υψηλού κινδύνου είναι σημαντική για τη λήψη θεραπευτικών αποφάσεων. Έτσι, η δημιουργία ενός νέου συστήματος σταδιοποίησης (R2-ISS) μπορεί να οδηγήσει στην αποτελεσματικότερη αντιμετώπιση των νεοδιαγνωσθέντων ασθενών. Η προσθήκη νέων παραγόντων (όπως μονοκλωνικών αντισωμάτων) ή νεότερης γενιάς φαρμάκων (αναστολέων πρωτεασώματος δεύτερης γενιάς), βελτιώνει την αποτελεσματικότητα της εισαγωγικής θεραπείας. Η θεραπεία με συνδυασμούς τεσσάρων φαρμάκων (αναστολέα πρωτεασώματος, ανοσοτροποποιητικά, κορτικοειδή και μονοκλωνικά αντισώματα) μπορεί να πετύχει πολύ υψηλά ποσοστά πλήρων ανταποκρίσεων με μη ανιχνεύσιμη ελάχιστη υπολειμματική νόσο. Η αξιολόγηση της ανταπόκρισης στη θεραπεία με νεότερες τεχνικές για την ανίχνευση της ελάχιστης υπολειμματικής νόσου γίνεται όλο και πιο διαδεδομένη.
Στη θεραπεία της υποτροπιάζουσας ή ανθεκτικής νόσου, νέοι συνδυασμοί έδειξαν ότι βελτιώνουν σημαντικά την έκβαση των ασθενών, όπως έδειξαν αποτελέσματα μακράς παρακολούθησης της αποτελεσματικότητας των τριπλών συνδυασμών της πομαλιδομίδης με δεξαμεθαζόνη και ελοτουζουμάβη ή καρφιλζομίμπης με δεξαμεθαζόνη και δαρατουμουμάβη.
Νεότερης γενιάς ανοσοτροποποιητικοί παράγοντες εμφανίζουν υψηλά ποσοστά αποτελεσματικότητας, με αυξημένη ωστόσο τοξικότητα.
Σημαντική εξέλιξη στη θεραπεία του πολ-
λαπλού μυελώματος αποτελεί η έγκριση των κυτταρικών θεραπειών με τροποποιημένα αυτόλογα Τ-λεμφοκύτταρα (CAR Tcells) και των αμφι-ειδικών αντισωμάτων (bi-specifics). Η χορήγησή τους απαιτεί εξειδικευμένα κέντρα για τη διαχείριση των επιπλοκών (σύνδρομο απελευθέρωσης κυτταροκινών και παροδική εγκεφαλοπάθεια).
Θεραπεία πρώτης γραμμής
στο πολλαπλό
μυέλωμα
Οι ασθενείς με νεοδιαγνωσθέν πολλαπλό μυέλωμα μπορεί έχουν ετερογενή αποτελέσματα επιβίωσης και, με βάση τα υπάρχοντα δεδομένα, περίπου το 60% ανήκει σε ενδιάμεση προγνωστική κατηγορία κινδύνου, με βάση το Αναθεωρημένο Διεθνές Σύστημα Σταδιοποίησης (R-ISS). Σε αυτό το σύστημα όμως δεν είχε συμπεριληφθεί η επίδραση της χρωμοσωμικής αύξησης/πολλαπλασιασμού του 1q, που πρόσφατα, με βάση νεότερα δεδομένα, θεωρείται δυσμενής προγνωστικός παράγοντας.
Στο πλαίσιο αυτό, με βάση δεδομένα από 10.843 ασθενείς από 16 κλινικές μελέτες σχεδιάστηκε το 2ο Αναθεωρημένο Διεθνές Σύστημα Σταδιοποίησης (R2ISS), όπου οι ασθενείς με κριτήρια το στάδιο κατά ISS (με βάση τις τιμές της β2-μικροσφαιρίνης και της αλβουμίνης), την παρουσία της απώλειας του 17p (del17p), της αύξησης/ πολλαπλασιασμού του 1q και την αυξημένη τιμή της LDH, κατατάσσονται σε 4 κατηγορίες προγνωστικού κινδύνου, με σημαντική διαφορά τόσο στο PFS όσο και στην ολική επιβίωση, με αποτέλεσμα σημαντικά βελ-
50 / Μάρτιος-Απρίλιος 2023
ΑΡΘΡΟ
Εξελίξεις στο πολλαπλό μυέλωμα και στην
al αμυλοείδωση
τιωμένη διαστρωμάτωση των ασθενών με ενδιάμεσου ρίσκου πολλαπλό μυέλωμα.1 Σε νεοδιαγνωσθέντες ασθενείς με πολλαπλό μυέλωμα φαίνεται ότι η αυτόλογη μεταμόσχευση μετά την εισαγωγική θεραπεία με τον συνδυασμό λεναλιδομίδης
με βορτεζομίδη και δεξαμεθαζόνη (RVD), ακολουθούμενη από θεραπεία συντήρησης με λεναλιδομίδη μέχρι προόδου νόσου, σχετίζεται με μακρύτερο διάστημα ελεύθερο προόδου νόσου (PFS).
Στην τυχαιοποιημένη μελέτη Φάσης ΙΙΙ DETERMINATION, το διάμεσο PFS ήταν
67,5 μήνες για τους ασθενείς που υποβλήθηκαν σε αυτόλογη μεταμόσχευση, έναντι
46,2 για αυτούς που δεν υποβλήθηκαν σε μεταμόσχευση. Ο κίνδυνος προόδου νόσου ή θανάτου ήταν μεγαλύτερος στους ασθενείς που δεν υποβλήθηκαν σε αυτόλογη μεταμόσχευση κατά 53% (HR, 1.53; 95% CI, 1.23 - 1.91, P<0.001). Το συνολικό ποσοστό ανταπόκρισης ήταν 97,5% και 95%, αντίστοιχα (p=0.55), με 46,8% και 42% να πετυχαίνουν πλήρη ύφεση (p=0.99). Όμως, δεν υπήρχε διαφορά στην επιβίωση στα 5 έτη, που ήταν 80,7% και 79,2%, αντίστοιχα (HR:1.10; 95% CI, 0.73 - 1.65)2
Μεταξύ των ασθενών που ωφελήθηκαν περισσότερο από την αυτόλογη μεταμόσχευση και στην ολική επιβίωση ήταν οι ασθενείς υψηλού κινδύνου (δηλαδή αυτοί με δυσμενείς κυτταρογενετικές βλάβες ή/και νόσο προχωρημένου σταδίου κατά ISS). Η προσθήκη των μονοκλωνικών αντισωμάτων στην πρώτη γραμμή θεραπείας και ο συνδυασμός τεσσάρων φαρμάκων γίνονται όλο και πιο ευρέως διαδεδομένα. Σε μελέτη που δημοσιεύθηκε το 2022 στο
Lancet, η προσθήκη της ισατουξιμάμπης, ενός μονοκλωνικόυ αντισώματος έναντι του αντιγόνου CD38, στην εισαγωγική θεραπεία με RVD σε ασθενείς επιλέξιμους για αυτόλογη μεταμόσχευση, οδηγεί σε υψηλότερα ποσοστά μη ανιχνεύσιμης ελάχιστης υπολειπόμενης νόσου (MRD) με τη χρήση της κυτταρομετρίας ροής (50% έναντι 36%; OR, 1.82; 95% CI, 1.33-2.48; P=0.00017). Η ουδετεροπενία και οι λοιμώξεις ήταν πιο συχνές στους ασθενείς που έλαβαν ισατουξιμάμπη (23% έναντι 7% και 12% έναντι 10%)3 Η μελέτη MASTER μελέτησε τον συνδυασμό της δαρατουμουμάβης (μονοκλωνικό αντίσωμα έναντι του CD38) με την καρφιλζομίμπη, τη λεναλιδομίδη και τη δεξαμεθαζόνη (Dara-KRD) σε ασθενείς με νεοδιαγνωσθέν πολλαπλό μυέλωμα. Στη μελέτη αυτή οι ασθενείς έλαβαν εισαγωγική θεραπεία με Dara-KRd, αυτόλογη μεταμόσχευση αρχέγονων αιμοποιητικών κυττάρων, περαιτέρω θεραπεία εδραίωσης με τον ίδιο συνδυασμό Dara-KRd για 4 ή 8 κύκλους, ανάλογα με το βάθος της ανταπόκρισης και με κριτήριο την επίτευξη μη ανιχνεύσιμης ελάχιστης υπολειπόμενης νόσου (MRD αρνητικότητα): Όσοι ασθενείς πέτυχαν δύο διαδοχικές MRD αρνητικές αξιολογήσεις τέθηκαν υπό παρακολούθηση άνευ θεραπείας. Το 80% των ασθενών πέτυχαν με αυτήν τη στρατηγική βαθιά ύφεση (MRD αρνητικότητα), ενώ ειδικά για την υποομάδα των ασθενών που δεν είχαν καμία ή είχαν μόνο μία κυτταρογενετική βλάβη υψηλού ρίσκου, η στρατηγική αυτή θέτει ως εναλλακτική την παρακολούθηση της νόσου μέσω της αξι-

Οι ασθενείς με
νεοδιαγνωσθέν
πολλαπλό μυέλωμα
μπορεί να
έχουν ετερογενή
αποτελέσματα
επιβίωσης και, με
βάση τα υπάρχοντα
δεδομένα, περίπου
το 60% ανήκει
σε ενδιάμεση
προγνωστική
κατηγορία κινδύνου.
51 ΑΦΙΕΡΩΜΑ ΑΙΜΑΤΟΛΟΓΙΑ
Σε ασθενείς που
δεν είναι επιλέξιμοι
για αυτόλογη
μεταμόσχευση
η προσθήκη του
μονοκλωνικού
αντισώματος
έναντι του CD38
δαρατουμουμάβης
πετυχαίνει
βαθύτερες υφέσεις.
ολόγησης της MRD, έναντι της συνεχόμενης θεραπείας συντήρησης.4
Οι ασθενείς που φέρουν κυτταρογενετικές βλάβες υψηλού ρίσκου αποτελούν μια πρόκληση όσον αφορά την επιλογή της ιδανικής θεραπείας. Μια υποανάλυση της μελέτης FORTE, που συνέκρινε τους συνδυασμούς καρφιλζομίμπης, λεναλιδομίδης και δεξαμεθαζόνης (KRd), ακολουθούμενη από αυτόλογη μεταμόσχευση αρχέγονων αιμοποιητικών κυττάρων (ASCT), KRd χωρίς ASCT, και καρφιλζομίμπη, κυκλοφωσφαμίδη και δεξαμεθαζόνη (KCd) ακολουθούμενη από ASCT, καθώς και θεραπεία συντήρησης με καρφιλζομίμπη και λεναλιδομίδη έναντι λεναλιδομίδης μόνο, δημοσίευσε δεδομένα για την κατηγορία των ασθενών αυτών. Ο συνδυασμός KRd ακολουθούμενης από συντήρηση καρφιλζομίμπη-λεναλιδομίδη φάνηκε να υπερτερεί σε ασθενείς με καμία ή μία κυτταρογενετική βλάβη υψηλού ρίσκου, πετυχαίνοντας παρόμοια αποτελέσματα PFS, ενώ οι ασθενείς με τουλάχιστον δύο βλάβες είχαν αυξημένη πιθανότητα προόδου νόσου και μειωμένης επιβίωσης, παρά τα αρχικά υψηλά ποσοστά ανταπόκρισης.5
Σε ασθενείς που δεν είναι επιλέξιμοι για αυτόλογη μεταμόσχευση η προσθήκη του μονοκλωνικού αντισώματος έναντι του CD38 δαρατουμουμάβης πετυχαίνει βαθύτερες υφέσεις, με υψηλότερα
ποσοστά επίτευξης αρνητικής MRD στον μυελό, με τη χρήση νεότερης γενιάς αλληλούχισης (NGS).
Στη μελέτη MAIA, που συνέκρινε τον συνδυασμό λεναλιδομίδης και δεξαμεθαζόνης με ή χωρίς δαρατουμουμάβη, αρνητική MRD στους 6 μήνες πέτυχε το 14,9% των ασθενών που έλαβαν δαρατουμουμάβη έναντι του 4.3% και στους 12 μήνες το 10,9% έναντι του 2,4%. Παρομοίως, στη μελέτη ALCYONE, που συνέκρινε τον συνδυασμό μελφαλάνης με βορτεζομίδη και πρεδνιζόνη με ή χωρίς δαρατουμουμάβη, αρνητική MRD στους 6 μήνες, πέτυχε το 15,7% της ομάδας της δαρατουμουμάβης έναντι του 4,5%, και στους 12 μήνες το 14% έναντι του 2,8%. Η επίτευξη αρνητική MRD στη συνέχεια σχετίστηκε με δραματική βελτίωση του διαστήματος ελεύθερου προόδου νόσου6
πολλαπλού μυελώματος
Η προσθήκη του μονοκλωνικού αντισώματος έναντι του SLAMF7, ελοτουζουμά-
βης, στον συνδυασμό πομαλιδομίδης και δεξαμεθαζόνης πετυχαίνει καλύτερα ποσοστά συνολικής επιβίωσης (OS) σε ασθενείς που έχουν λάβει προηγουμένως τουλάχιστον δύο γραμμές θεραπείας που περιείχαν λεναλιδομίδη και αναστολέα πρωτεασώματος.
Η διάμεσος συνολική επιβίωση (OS) ήταν 29,8 μήνες, έναντι 17,4 μηνών για το σκέλος ελέγχου (HR: 0.59; 95% CI, 0.370.93; P=0.0217)7
Ο συνδυασμός της δαρατουμουμάβης με την καρφιλζομίμπη και τη δεξαμεθαζόνη (KdD) σε ασθενείς με υποτροπιάζον/ ανθεκτικό πολλαπλό μυέλωμα εγκρίθηκε με βάση τα αποτελέσματα της μελέτης Φάσης ΙΙΙ CANDOR. Νεότερα δεδομένα με μεγαλύτερο χρονικό διάστημα παρακολούθησης στη μελέτη δημοσιεύθηκαν πρόσφατα και έδειξαν ότι ο συνδυασμός KdD έναντι του συνδυασμού καρφιλζομίμπης δεξαμεθαζόνης (Kd) υπερτερεί, πετυχαίνοντας διάμεσο διάστημα ελεύθερο προόδου νόσου (PFS) 28,6 μήνες, έναντι 15,2 μηνών (p<0.0001) με αποδεκτό προφίλ τοξικότητας. Αυτό καθιστά τον συνδυασμό αναδυόμενη βέλτιστη ενδεικνυόμενη θεραπεία σε αυτήν την ομάδα ασθενών.8
Η ιμπερδομίδη είναι ένας νεότερος ανοσοτροποποιητικός παράγοντας. Στη μελέτη Φάσης Ι/ΙΙ (CC-220-MM-001), 460 ασθενείς που είχαν λάβει τουλάχιστον δύο προηγούμενες γραμμές θεραπείας με έναν αναστολέα πρωτεασώματος και έναν ανοσοτροποποιητικό παράγοντα έλαβαν ιμπερδομίδη σε διάφορα δοσολογικά επίπεδα (0.3-1.6 mg) σε συνδυασμό με δεξαμεθαζόνη. Το συνολικό ποσοστό ανταπόκρισης στη μέγιστη ανεκτή δόση του 1,6 mg ήταν 26% (28/107).
Η πιο συχνή ανεπιθύμητη ενέργεια βαθμού 3 ή μεγαλύτερου ήταν η ουδετεροπενία (45%), η αναιμία (28%), οι λοιμώξεις (27%) και η θρομβοπενία (22%). Σοβαρές ανεπιθύμητες ενέργειες παρουσίασε ποσοστό 53% των ασθενών, ένας ασθενής κατέληξε λόγω σήψης και πέντε ασθενείς διέκοψαν τη θεραπεία λόγω μη ανεκτής τοξικότητας.9
Το 2022, δημοσιεύθηκαν δεδομένα που αφορούν στην αποτελεσματικότητα τριών αμφιειδικών αντισωμάτων για τη θεραπεία του πολλαπλού μυελώματος σε προθεραπευμένους ασθενείς που έχουν λάβει προηγουμένως αναστολέα πρωτεασώματος, ανοσοτροποιητικό παράγοντα και αντι-CD38 μονοκλωνικό αντίσωμα. Τα αμφιειδικά αντισώματα στοχεύουν το CD3
52 / Μάρτιος-Απρίλιος 2023
Θεραπεία του υποτροπιάζοντος και ανθεκτικού
ΑΡΘΡΟ
επίτοπο στην επιφάνεια των Τ-λεμφοκυττάρων και έναν επίτοπο στην επιφάνεια των πλασματοκυττάρων, φέρνοντας σε επαφή τα δύο κύτταρα.
Το Teclistamab είναι ένα αμφιειδικό αντίσωμα που στοχεύει το αντιγόνο B-cell maturation antigen (BCMA) στην επιφάνεια των πλασματοκυττάρων και έχει λάβει έγκριση από τον FDA και τον ΕΜΑ. Το Teclistamab έλαβε έγκριση με βάση τα αποτελέσματα της μελέτης Φάσης Ι/ΙΙ, MajesTEC-1, στην οποία έλαβαν μέρος 165
ασθενείς με ανθεκτικό και υποτροπιάζον
πολλαπλό μυέλωμα που είχαν προηγουμένως λάβει και anti-CD38 μονοκλωνικό αντίσωμα. Το φάρμακο χορηγήθηκε υποδορίως σε δόση 1,5 mg/kg εβδομαδιαίως. Το συνολικό ποσοστό ανταπόκρισης ήταν 63% και το ποσοστό πλήρους ύφεσης ήταν 39,4%, ενώ 26,7% πέτυχαν ύφεση χωρίς ανιχνεύσιμη ελάχιστη υπολειπόμενη νόσο. Η διάμεση διάρκεια
της ανταπόκρισης ήταν 18,4 μήνες και το
διάμεσο διάστημα ελεύθερο προόδου νόσου ήταν 11,3 μήνες (95% CI, 8,8-17.1). Οι συχνότερες ανεπιθύμητες ενέργειες ήταν το σύνδρομο απελευθέρωσης κυτταροκινών (στο 72,1% των ασθενών και μόνο στο 0,6% ήταν βαθμού 3), η αιματολογική τοξικότητα και οι λοιμώξεις (76,4% και 44,8% ήταν βαθμού 3 ή 4). Νευροτοξικότητα (ICANS) παρουσιάστηκε στο 14,5%
και ήταν βαθμού 1 ή 210 Το αμφιειδικό αντίσωμα Elranatamab στοχεύει επίσης το BCMA στην επιφάνεια των πλασματοκυττάρων και έχει λάβει θετική γνωμοδότηση από τις ρυθμιστικές αρχές, ενώ αναμένεται η τελική έγκριση από τον FDA. Στη μελέτη Φάσης ΙΙ MagnetisMM-3, 123 ασθενείς που είχαν λάβει προηγουμένως πολλαπλές γραμμές θεραπείας και είχαν νόσο ανθεκτική σε αναστολείς πρωτεασώματος ανοσοτροποποιητικά φάρμακα και μονοκλωνικά αντισώματα έναντι του CD38 έλαβαν μέρος. Το φάρμακο χορηγήθηκε υποδορίως σε δόση 76 mg εβδομαδιαίως. Η διάμεση διάρκεια θεραπείας
ήταν 5,3 μήνες (0,03-16,1) και το συνολικό ποσοστό ανταπόκρισης ήταν 61%.

Σύνδρομο απελευθέρωσης κυτταροκινών παρουσίασε το 56,3% και σχετιζόμενη νευροτοξικότητα (ICANS) το 3,4%, όμως
σε όλους τους ασθενείς ήταν βαθμού 1 ή 2. Ανάμεσα στις υπόλοιπες πιο συχνές ανεπιθύμητες ενέργειες ήταν οι λοιμώξεις (61,8%, βαθμού 3 ή 4 στο 31,7%), κυρίως του αναπνευστικού, και η περιφερική νευροπάθεια (17,1%, βαθμού 3 ή 4 στο 0,8%).11
Το Talquetamab είναι ένα αμφιειδικό αντίσωμα που στοχεύει διαφορετικό αντιγόνο στην επιφάνεια των πλασματοκυττάρων, την πρωτεΐνη G protein-coupled receptor, family C, group 5, member D (GPRC5D)
και έχει λάβει θετική γνωμοδότηση από τις ρυθμιστικές αρχές, ενώ αναμένεται η τελική έγκριση από τον FDA.
Στη μελέτη Φάσης Ι ΜonumenTAL-1 εντάχθηκαν 232 ασθενείς με ανθεκτικό/υποτροπάζον μυέλωμα, εκ των οποίων 102 έλαβαν το φάρμακο ενδοφλεβίως και 130 υποδορίως. Οι συνιστώμενες δόσεις για τη Φάση ΙΙ της μελέτης ήταν τα 405 mg/ kg υποδορίως εβδομαδιαίως και τα 800 mg/kg υποδορίως ανά δύο εβδομάδες. Σύνδρομο απελευθέρωσης κυτταροκινών (CRS) παρουσιάστηκε στο 77% και στο 80% (κυρίως βαθμού 1 και 2), αντίστοιχα, δερματική αντίδραση στο 67% και 70%, και δυσγευσία στο 63% και στο 57%. Τα ποσοστά συνολικής ανταπόκρισης ήταν 70% (95% CI, 51-85) και 64% (95% CI, 48-78) ενώ η διάμεση διάρκεια ανταπόκρισης ήταν 10,2 μήνες και 7,8 μήνες, αντίστοιχα12 Τα αποτελέσματα από τη θεραπεία ασθενών με πολύ ανθεκτικό μυέλωμα με γενετικά τροποποιημένα αυτόλογα Τ-λεμφοκύτταρα (CAR-T cell) που στοχεύουν το αντιγόνο BCMA στην επιφάνεια των πλασματοκυττάρων είναι ιδιαίτερα ενθαρρυντικά. Τα προϊόντα αυτά (Ide-cel & ciltacel) έχουν λάβει έγκριση από τον FDA και τον EMA για τη θεραπεία ασθενών με πολλαπλό μυέλωμα μετά από τουλάχιστον 4 γραμμές θεραπείας. Αυξάνοντας τους στόχους των CAR-T θεραπειών δημοσιεύθηκε μία Φάσης Ι μελέτη
Στο Teclistamab το συνολικό ποσοστό
ανταπόκρισης
ήταν 63% και το
ύφεσης ήταν
39,4%, ενώ 26,7%
53 ΑΦΙΕΡΩΜΑ ΑΙΜΑΤΟΛΟΓΙΑ
ποσοστό πλήρους
πέτυχαν ύφεση
χωρίς ανιχνεύσιμη ελάχιστη υπολειπόμενη νόσο.
Βιβλιογραφία
1. D'AGOSTINO, CAIRNS, LAHUERTA, et al. Second Revision of the International Staging System (R2-ISS) for Overall Survival in Multiple Myeloma: A European Myeloma Network (EMN) Report Within the HARMONY Project. J Clin Oncol. Oct 10; 40(29): 34063418.
2. RICHARDSON, JACOBUS, WELLER, et al. Triplet Therapy, Transplantation, and Maintenance until Progression in Myeloma. N Engl J Med. Jul 14; 387(2): 132-147.

3. GOLDSCHMIDT, MAI, BERTSCH, et al. Addition of isatuximab to lenalidomide, bortezomib, and dexamethasone as induction therapy for newly diagnosed, transplantation-eligible patients with multiple myeloma (GMMG-HD7): part 1 of an open-label, multicentre, randomised, active-controlled, phase 3 trial. Lancet Haematol. Nov; 9(11): e810-e821.
4. COSTA, CHHABRA, MEDVEDOVA, et al. Daratumumab, Carfilzomib, Lenalidomide, and Dexamethasone With Minimal Residual Disease Response-Adapted Therapy in Newly Diagnosed Multiple Myeloma. J Clin Oncol. Sep 1; 40(25): 2901-2912.
5. MINA, MUSTO, ROTA-SCALABRINI, et al. Carfilzomib induction, consolidation, and
με CAR T-cell που στοχεύουν το αντιγόνο GPRC5D των πλασματοκυττάρων. Στη μελέτη εντάχθηκαν βαριά προθεραπευμένοι ασθενείς με πολλαπλό μυέλωμα που έλαβαν το φάρμακο σε τέσσερα δοσολογικά σχήματα. Η μέγιστη ανεκτή δόση ήταν τα 150x106 CAR T-cells και δεν παρουσιάστηκε κανένα επεισόδιο ICANS ή βαθμού 3 και 4 CRS. Συνολικά, το 71% ανταποκρίθηκε και το 58% αυτών που έλαβαν τη δόση των 150x106 CAR T-cells13
Αμυλοείδωση
Η θεραπεία της πρωτοπαθούς συστηματικής αμυλοείδωσης από ελαφρές
maintenance with or without autologous stem-cell transplantation in patients with newly diagnosed multiple myeloma: preplanned cytogenetic subgroup analysis of the randomised, phase 2 FORTE trial. Lancet Oncol. Jan; 24(1): 64-76.
6. SAN-MIGUEL, AVET-LOISEAU, PAIVA, et al. Sustained minimal residual disease negativity in newly diagnosed multiple myeloma and the impact of daratumumab in MAIA and ALCYONE. Blood. Jan 27; 139(4): 492-501.
7. DIMOPOULOS, DYTFELD, GROSICKI, et al. Elotuzumab Plus Pomalidomide and Dexamethasone for Relapsed/Refractory Multiple Myeloma: Final Overall Survival Analysis From the Randomized Phase II ELOQUENT-3 Trial. J Clin Oncol. Jan 20; 41(3): 568-578.
8. USMANI, QUACH, MATEOS, et al. Carfilzomib, dexamethasone, and daratumumab versus carfilzomib and dexamethasone for patients with relapsed or refractory multiple myeloma (CANDOR): updated outcomes from a randomised, multicentre, open-label, phase 3 study. Lancet Oncol. Jan; 23(1): 65-76.
9. LONIAL, POPAT, HULIN, et al. Iberdomide plus dexamethasone in heavily pretreated late-line relapsed or refractory
αλυσίδες (AL) βασίζεται σε σχήματα που χρησιμοποιούνται στο πολλαπλό μυέλωμα. Αν και οι κυτταρικές θεραπείες έχουν πάρει έγκριση για το μυέλωμα, δεν έχουν χρησιμοποιηθεί στην αμυλοείδωση, λόγω του φόβου για αυξημένη τοξικότητα σε αυτόν τον ευάλωτο πληθυσμό. Το 2022, δημοσιεύθηκε η πρώτη μελέτη για την ασφάλεια και την αποτελεσματικότητα ενός νέου CAR-T cell (HBI0101) που στοχεύει τον υποδοχέα BCMA στην επιφάνεια των πλασματοκυττάρων. Τέσσερις ασθενείς με ανθεκτική ή υποτροπιάζουσα νόσο έλαβαν τη θεραπεία. Οι τρεις από αυτούς είχαν προσβολή του μυοκαρδίου σταδίου Mayo ΙΙΙΑ. Δύο ασθενείς παρουσίασαν σύνδρομο απελευθέρωσης κυτταροκινών βαθμού 3 και κανένας ασθενής δεν παρουσίασε νευροτοξικότητα.
Τα καρδιακά συμβάματα ήταν διαχειρίσιμα. Όλοι οι ασθενείς πέτυχαν πλήρη αιματολογική ύφεση και βελτίωση στη λειτουργία των οργάνων και σε ένα διάμεσο διάστημα παρακολούθησης 5,2 μηνών και οι τέσσερις ασθενείς διατηρούν τις ανταποκρίσεις.
Συμπερασματικά, φαίνεται, για πρώτη φορά, ότι η θεραπεία με CAR-T cells είναι καλά ανεκτή και αρκετά αποτελεσματική σε ασθενείς με AL αμυλοειδωση14.•••
multiple myeloma (CC-220-MM-001): a multicentre, multicohort, open-label, phase 1/2 trial. Lancet Haematol. Nov; 9(11): e822-e832.
10. MOREAU, GARFALL, VAN DE DONK, et al. Teclistamab in Relapsed or Refractory Multiple Myeloma. N Engl J Med. Aug 11; 387(6): 495-505.
11. BAHLIS, TOMASSON, MOHTY, et al. Efficacy and Safety of Elranatamab in Patients with Relapsed/Refractory Multiple Myeloma Naïve to B-Cell Maturation Antigen (BCMA)-Directed Therapies: Results from Cohort a of the Magnetismm-3 Study. Blood. 140(Supplement 1): 391-393.
12. CHARI, MINNEMA, BERDEJA, et al. Talquetamab, a T-Cell-Redirecting GPRC5D Bispecific Antibody for Multiple Myeloma. N Engl J Med. Dec 15; 387(24): 2232-2244.
13. MAILANKODY, DEVLIN, LANDA, et al. GPRC5D-Targeted CAR T Cells for Myeloma. N Engl J Med. Sep 29; 387(13): 1196-1206.
14. KFIR-ERENFELD, ASHERIE, GRISARIU, et al. Feasibility of a Novel Academic BCMA-CART (HBI0101) for the Treatment of Relapsed and Refractory AL Amyloidosis. Clin Cancer Res. Dec 1; 28(23): 5156-5166.
54 / Μάρτιος-Απρίλιος 2023
ΑΡΘΡΟ

55 ΑΦΙΕΡΩΜΑ ΑΙΜΑΤΟΛΟΓΙΑ Διοργάνωση Σε συνεργασία με την ethosevents.eu 21 ΙΟΥΝΙΟΥ 2023 SAVE THE DATE #porf23 FORUM 2023 RAIL
Από τους:
Δέσποινα Φωτίου, αιματολόγο, επιστημονική
συνεργάτιδα στη Θεραπευτική Κλινική του ΓΝ Αλεξάνδρα, Ιατρική Σχολή
ΕΚΠΑ
Ευάγγελο Τέρπο, καθηγητή Θεραπευτικής-Αιματολογίας στη Θεραπευτική Κλινική του ΓΝ Αλεξάνδρα, Ιατρική Σχολή ΕΚΠΑ
Μελέτιο-Αθανάσιο Δημόπουλο, καθηγητή ΘεραπευτικήςΑιματολογίας-Ογκολογίας στη Θεραπευτική Κλινική του ΓΝ Αλεξάνδρα, Ιατρική Σχολή ΕΚΠΑ
Εξελίξεις στα νεοπλάσματα της μυελικής σειράς
Aξίζει να σημειωθεί ότι, το 2022, εκδόθηκε νέα (5η έκδοση) ταξινόμηση του Παγκόσμιου Οργανισμού Υγείας (WHO 2022) για τις αιματολογικές κακοήθειες από κύτταρα της μυελικής σειράς και των δενδριτικών κυττάρων/ιστιοκυττάρων1. Ορίζονται εκ νέου οι παράγοντες κινδύνου για τη χρόνια μυελογενή λευχαιμία και αφαιρείται η κατηγορία της επιταχυνόμενης φάσης της νόσου και πλέον αναγνωρίζονται μόνο η χρόνια και η βλαστική φάση της νόσου. Εντάσσεται επίσης στην κατηγορία των μυελοϋπερπλαστικών νοσημάτων και η νεανική μυελομονοκυτταρική λευχαιμία ενώ ενημερώνονται τα κριτήρια για τη χρόνια ηωσινοφιλική λευχαιμία και αφαιρείται ο όρος “not otherwise specified”.
Στη νέα αυτή έκδοση ενημερώθηκαν και τα διαγνωστικά κριτήρια της μαστοκυττάρωσης και περιλαμβάνεται, πλέον, η παρουσία CD30 και οποιασδήποτε KIT μετάλλαξης στα ελάσσονα διαγνωστικά κριτήρια ενώ ορίζεται και νέα υποκατηγορία της νόσου, η μαστοκυττάρωση του μυελού των οστών.
Μυελοΐνωση
Το Μάρτιο του 2022, εγκρίθηκε από την Υπηρεσία Τροφίμων και Φαρμάκων των ΗΠΑ (FDA) η πακριτινίμπη (pacritinib, VONJO) για τη θεραπεία ασθενών με συμπτωματική πρωτοπαθή ή δευτεροπαθή μυελοΐνωση ενδιάμεσου ή υψηλού κινδύνου με αριθμό αιμοπεταλίων μικρότερο των 50 x 109/L. Χορηγήθηκε επιταχυνόμενη έγκριση κυκλοφορίας βάσει των αποτελεσμάτων των τυχαιοποιημένων μελετών Φάσης ΙΙΙ PERSIST-1 και PERSIST-2.
Οι αναστολείς JAK1/2 οι οποίοι έχουν έγκριση για την αντιμετώπιση της νόσου (ρουξολιτινίμπη και φεντρατινίμπη) δεν έχουν μελετηθεί σε ασθενείς με επίπεδα αιμοπεταλίων ≤ 50 x 109/L και συχνά περιορίζεται η χρήση τους από τη θρομβοπενία, που σχετίζεται με τη νόσο. Η πακριτινίμπη είναι ένας εκλεκτικός αναστολέας των JAK2, FLT3, IRAK1 και CSF1R. Στη μελέτη PERSIST-12 χορηγήθηκε στην πρώτη γραμμή θεραπείας, στα 400 mg την ημέρα (n=220) έναντι της καλύτερης διαθέσιμης θεραπείας (n=107). Η μελέτη πέτυχε το πρωτεύον καταληκτικό σημείο (μείωση του όγκου του σπληνός κατά 35% ή περισσότερο την εβδομάδα 24 σε 42 ασθενείς (19%), έναντι 5 ασθενών (5%) στην ομάδα που έλαβε την καλύτερη διαθέσιμη θεραπεία (p=0.0003), αλλά τερματίστηκε προσωρινά, λόγω του μεγάλου αριθμού αιμορραγικών και καρδιολογικών ανεπιθύμητων ενεργειών.
Στη μελέτη PERSIST-23 χορηγήθηκε στα 400 mg την ημέρα ή 200 mg δύο φορές την ημέρα σε ασθενείς στην πρώτη υποτροπή με αριθμό αιμοπεταλίων ≤ 100 x109/L έναντι της καλύτερης διαθέσιμης θεραπείας (υδροξυουρία, ρουξολιτινίμπη, παρακολούθηση). Η μελέτη PERSIST-2 τερματίστηκε πρώιμα, αλλά πέτυχε επίσης το καταληκτικό σημείο ανταπόκρισης με βάση τη μείωση του όγκου του σπλήνα. To 18% (n=27) των ασθενών (n=149) πέτυχαν μείωση όγκου σπλήνα κατά 35% στο σκέλος της πακριτινίμπης (p=0.001) και τη βελτίωση του φορτίου συμπτωμάτων στο 25% (n=37) των ασθενών που έλαβαν το ερευνητικό φάρμακο (p=0.01).
56 / Μάρτιος-Απρίλιος 2023
ΑΡΘΡΟ
Και οι δύο μελέτες αξιολογήθηκαν εκ νέου και δεν επιβεβαιώθηκε ο αυξημένος κίνδυνος ανεπιθύμητων ενεργειών. Με βάση και τη μελέτη καθορισμού της προτεινόμενης δόσης PAC2034, καθορίστηκε πως η ασφαλής και αποτελεσματική δόση
της πακριτινίμπης είναι αυτή των 200 mg δύο την ημέρα και δόθηκε τελικά έγκρι-
ση στους ασθενείς εκείνους με μυελοΐνωση και αριθμό αιμοπεταλίων ≤ 50 x 109/L.
Στην Ευρώπη, είχε γίνει αίτημα για τη χορήγηση έγκρισης για το φάρμακο, η οποία όμως αποσύρθηκε, λόγω της καταγραφής
των υψηλών ποσοστών αιμορραγικών συμβαμάτων και καρδιολογικών επιπλοκών. To 2022, παρουσιάστηκαν τα δεδομένα από τη διπλή τυφλή τυχαιοποιημένη πολυκεντρική μελέτη Φάσης ΙΙΙ MOMENTUM5, η οποία αξιολόγησε την ασφάλεια και την αποτελεσματικότητα του momelotinib, ενός αναστολέα του JAK1, JAK2 και του ACVR1 (activin A υποδοχέας τύπου Ι). Η χορήγηση του momelotinib αξιολογήθηκε έναντι της δαναζόλης σε ασθενείς με συμπτωματική μυελοΐνωση και αναιμία οι οποίοι είχαν λάβει προηγουμένως αγωγή με εγκεκριμένο αναστολέα του JAK. Η μελέτη αξιολόγησε την αποτελεσματικότητα του φαρμάκου με βάση την υποχώρηση των συμπτωμάτων, τη μείωση των μεταγγίσεων αίματος και τη μείωση του όγκου του σπλήνα. Οι ασθενείς τυχαιοποιήθηκαν να λάβουν momelotinib (n=130) σε δόση 200 mg έναντι δαναζόλης (n=65) 2:1 και στις 24 εβδομάδες επιτρεπόταν με βάση τη μη ικανοποιητική ανταπόκριση να περάσουν οι ασθενείς από το σκέλος της δαναζόλης στο σκέλος του momelotinib. Στις 24 εβδομά-
δες, η συνολική ανταπόκριση με βάση τη βελτίωση των συμπτωμάτων ήταν 24% στο σκέλος του ερευνητικού φαρμάκου, έναντι 9,2% στους ασθενείς που έλαβαν δαναζόλη (p=.0095). Επίσης το 30,8% των ασθενών στο σκέλος του momelotinib πέτυχαν απεξάρτηση από μεταγγίσεις συμπυκνωμένων ερυθρών, έναντι 20,0% στο σκέλος της δαναζόλης (p=.006) και το 40,6% μείωση του όγκου του σπλήνα κατά 25%, έναντι 6,2% των ασθενών στο σκέλος ελέγχου (P=.006).
Μείωση του όγκου του σπλήνα κατά ≥ 35% πέτυχαν το 23,1% και το 3,1% των ασθενών, αντίστοιχα (p=0.0006). Όλοι οι ασθενείς είχαν λάβει ρουξολιτινίμπη σε προηγούμενη γραμμή και το 5% φεντρατινίμπη. Οι πιο συχνές ανεπιθύμητες ενέργειες βαθμού 3 ήταν η θρομβοπενία στο 22% και η αναιμία στο 8% και λοιμώξεις βαθμού ≥ 3 παρουσιάστηκαν στο 15% των ασθενών στο σκέλος του ερευνητικού φαρμάκου και στο 11% στο σκέλος φαρμάκου ελέγχου. Αυτήν τη στιγμή, έχουν γίνει εγκριτικές αιτήσεις στον FDA και τον EMA και αναμένονται τα αποτελέσματα μέσα στο 2023.
Το 2022, δόθηκε
έγκριση από
τον FDA για την
πακριτινίμπη
(pacritinib, VONJO) για τη
θεραπεία ασθενών
με συμπτωματική
πρωτοπαθή ή
δευτεροπαθή
μυελοΐνωση
ενδιάμεσου ή
υψηλού κινδύνου με
θρομβοπενία.
To 2022, o EMA υιοθέτησε μια νέα ένδειξη για το avapritinib (AYVAKYT) ως μονοθεραπεία για τη θεραπεία ενήλικων ασθενών με επιθετική συστηματική μαστοκυττάρωση (ASM), συστηματική μαστοκυττάρωση με συσχετιζόμενο αιματολογικό νεόπλασμα (SM-AHN) ή λευχαιμία εκ μαστοκυττάρων (MCL), μετά από τουλάχιστον μία συστηματική θεραπεία6

57 ΑΦΙΕΡΩΜΑ ΑΙΜΑΤΟΛΟΓΙΑ
Συστηματική Μαστοκυττάρωση
Εγκρίθηκε το avapritinib από

τον ΕΜΑ για
ενήλικες ασθενείς με προχωρημένη συστηματική
μαστοκυττάρωση (AdvSM), με βάση τις κλινικές μελέτες EXPLORER και PATHFINDER.
To avapritinib είχε λάβει έγκριση από τον FDA το προηγούμενο έτος με βάση τα αποτελέσματα των κλινικών μελετών Φάσης Ι EXPLORER (NCT02561988) 7 και Φάσης ΙΙ PATHFINDER (NCT03580655)8 Το avapritinib είναι αναστολέας κινάσης τύπου 1, ο οποίος έχει καταδείξει βιοχημική in vitro δραστηριότητα στους μεταλλάκτες PDGFRA D842V και KIT D816V και δραστικότητα έναντι των κλινικά συναφών μεταλλάξεων του εξονίου 11 του ΚΙΤ, του εξονίου 11/17 του ΚΙΤ και του εξονίου 17 του ΚΙΤ από ό,τι έναντι του ενζύμου άγριου τύπου του ΚΙΤ. Και στις δύο μελέτες, το συνολικό ποσοστό
ανταπόκρισης (ORR) ήταν 57% (95% CI, 42-70%) (n=53), με 28% πλήρεις υφέσεις
και 28% μερικές υποχωρήσεις. Ο μέσος
χρόνος απόκρισης ήταν 2,1 μήνες και η μέση διάρκεια απόκρισης ήταν 38,3 μήνες (95% CI, 19%-μη εκτιμώμενο). To oίδημα, η διάρροια, η ναυτία και η κόπωση ήταν οι πιο συχνές ανεπιθύμητες ενέργειες
σε ασθενείς που έλαβαν AdvSM (επίπτωση 20%). Η δόση χορήγησης είναι 200 mg από του στόματος μία φορά την ημέρα.
Νεοπλάσματα της Μυελικής και Λεμφικής Σειράς
Στην νέα έκδοση του WHO1 έχουμε νέα κριτήρια για τη χρόνια μυελομονοκυτταρική λευχαιμία (CMML), με χαμηλότερο ποσοστό απόλυτης μονοκυττάρωσης στον ορισμό, και ορίζονται, πλέον, οι υποκατηγορίες της MD-CMLL, που έχει χαρακτη-
ριστικά μυελοδυσπλαστικού συνδρόμου, και της MPCMML, που έχει χαρακτηριστικά μυελοϋπερπλαστικού συνδρόμου, και αφαιρείται η κατηγορία CMML-0. Η άτυπη χρόνια μυελογενής λευχαιμία μετονομάζεται σε μυελοϋπερπλαστικό/μυελοδυσπλαστικό σύνδρομο (MDS/MPN) με ουδετεροφιλία και η MDS/MPN με δακτυλιοειδείς σιδηροβλάστες και θρομβοκυττάρωση ορίζεται εκ νέου με βάση την παρουσία της μετάλλαξης του SF3B1 και ονομάζεται MDS/MPN με θρομβοκυττάρωση και SF3B1 μετάλλαξη.
Νεοπλάσματα της μυελικής/λεμφικής σειράς με διαμετάθεση του FGFR1:
Τον Αύγουστο του 2022, εγκρίθηκε από τον FDA η χορήγηση της πεμιγατινίμπης (pemigatinib, Pemazyre) σε ενήλικες ασθενείς με ανθεκτικά/υποτροπιάζοντα νεοπλάσματα της μυελικής/λεμφικής σειράς με διαμετάθεση του FGFR1.
Η πεμιγατινίμπη είναι ένας αναστολέας κινάσης των FGFR1, 2 και 3, ο οποίος αναστέλλει τη φωσφορυλίωση και τη σηματοδότηση του FGFR και μειώνει την κυτταρική βιωσιμότητα στα κύτταρα που εκφράζουν γενετικές αλλοιώσεις του FGFR. H έγκριση βασίστηκε σε δεδομένα από τη μελέτη FIGHT-203 (NCT03011372)9, μια πολυκεντρική μελέτη ενός σκέλους στην οποία εντάχθηκαν 28 ασθενείς οι οποίοι δεν ήταν επιλέξιμοι ή είχαν υποτροπιάσει μετά από αλλογενή μεταμόσχευση αρχέγονων αιμοποιητικών κυττάρων ή μετά από άλλη θεραπεία. Από τους 18 ασθενείς που βρίσκονταν στη χρόνια φάση της νόσου 14 πέτυχαν πλήρη ύφεση (78%; 95% CI: 5294%), ο μέσος χρόνος ανταπόκρισης ήταν 104 μέρες (εύρος 44-435) και η διάρκεια της ανταπόκρισης δεν καθορίστηκε (1+ με 988+ ημέρες). Συνολικά, 4 ασθενείς βρίσκονταν στη βλαστική φάση της νόσου και 2 πέτυχαν πλήρη ύφεση (διάρκεια 1 έως 94 ημέρες). Στη συνολική ομάδα ασθενών το ποσοστό κυτταρογενετικής ύφεσης ήταν 79% (95% CI: 59-92%).
Οι πιο συχνές ανεπιθύμητες ενέργειες βαθμού (≥20%) ήταν υπερφωσφαταιμία, αλωπεκία, διάρροια, τοξικότητα ονύχων, κόπωση, ναυτία, στοματίτιδα, δυσκοιλιότητα και άλλα. Οι πιο συχνές αιματολογικές τοξικότητες (≥10%) βαθμού 3+ ήταν η υποφωσφαταιμία, λεμφοπενία, θρομβοπενία και ουδετεροπενία.
Το φάρμακο χορηγείται σε δόση 13,5 mg από του στόματος μία φορά την ημέρα μέχρι τοξικότητας ή προόδου νόσου.
58 / Μάρτιος-Απρίλιος 2023
ΑΡΘΡΟ
Μυελοδυσπλαστικά Σύνδρομα
Στη νέα κατάταξη του WHO 20221 αλλάζει η ονομασία των μυελοδυσπλαστικών συνδρόμων σε μυελοδυσπλαστικά νεοπλάσματα (ΜΔΣ). Η υποκατηγορία των ΜΔΣ που χαρακτηρίζονται από γενετικές ανωμαλίες περιλαμβάνει, πλέον, το MDS-5q, MDS-SF3B1 and MDSbiTP53 και αναγνωρίζεται το υποπλαστικό ΜΔΣ ως ξεχωριστή υποκατηγορία. Πλέον, ορίζονται και χρησιμοποιούνται ως όροι το ΜΔΣ με χαμηλό
ποσοστό βλαστών (MDS-LB) και το ΜΔΣ με αυξημένο ποσοστό βλαστών (MDS-IB).
Προτείνεται επίσης και νέο προγνωστικό
σκορ για τους ασθενείς με Μυελοδυσπλαστικά Σύνδρομα (ΜΔΣ), το IPSS-Mοlecular (M), το οποίο είναι ένα επικυρωμένο σκορ που περιλαμβάνει κυτταρογενετικά και μοριακά χαρακτηριστικά των προηγούμενων προγνωστικών σκορ και βασίζεται στην παρουσία μεταλλάξεων. Σε μια ανάλυση 3.000 ασθενών με ΜΔΣ, το IPSS-M είχε βελτιωμένη απόδοση σε σύγκριση με το IPSS-Revised (R). Σχεδόν το 50% των ασθενών εντάχθηκαν σε νέα κατηγορία κινδύνου και βελτιώθηκε η διακριτική ικανότητα του σκορ σε όλα τα κλινικά καταληκτικά σημεία. Το IPSS-M μπορεί να χρησιμοποιηθεί για ασθενείς που έχουν λάβει ή όχι θεραπεία. Αποτελέσματα από την εγκριτική μελέτη Φάσης ΙΙΙ MEDALIST έδειξαν πως το luspatercept (Reblozyl) βελτιώνει την τριετή συνολική επιβίωση σε σύγκριση με το εικονικό φάρμακο σε ασθενείς με μυελοδυσπλαστικό σύνδρομο χαμηλού κινδύνου και δακτυλιοειδείς σιδηροβλάστες10. Το Reblozyl ενδείκνυται από το 2020 για τη θεραπεία ενήλικων ασθενών με εξαρτώμενη από μεταγγίσεις αναιμία λόγω μυελοδυσπλαστικών συνδρόμων (ΜΔΣ) με πολύ χαμηλό, χαμηλό και ενδιάμεσο κίνδυνο που έχουν δακτυλιοειδείς σιδηροβλάστες, οι οποίοι είχαν μη ικανοποιητική ανταπόκριση σε ή είναι ακατάλληλοι για θεραπεία που βασίζεται στην ερυθροποιητίνη. Συνολικά, 229 ασθενείς τυχαιοποιήθηκαν
για να λαμβάνουν υποδορίως luspatercept 1,0 mg/kg (n=153) ή εικονικό φάρμακο (n=76) κάθε 3 εβδομάδες. Συνολικά, 128 (83,7%) και 68 (89,5%) ασθενείς που λάμβαναν luspatercept και εικονικό φάρμακο, αντίστοιχα, ολοκλήρωσαν 24 εβδομάδες θεραπείας.
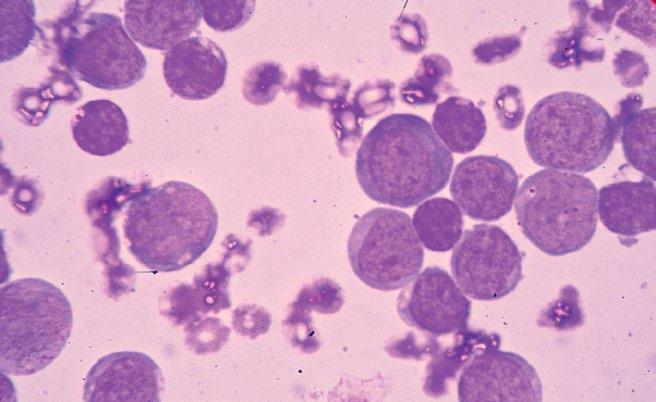
Πιο συγκεκριμένα, από τα δεδομένα της μελέτης MEDALIST, η διάμεση συνολική επιβίωση δεν διέφερε σημαντικά μεταξύ των ασθενών που έλαβαν εικονικό φάρ-
μακο και luspatercept, αλλά οι ασθενείς με ανταπόκριση στο luspatercept είχαν σημαντικά μεγαλύτερη επιβίωση συγκριτικά με τους ασθενείς χωρίς ανταπόκριση την εβδομάδα 25 (HR 0.319, p=0.0003). Επίσης, το ποσοστό των ασθενών με συνολική επιβίωση 36 μήνες ήταν σημαντικά μεγαλύτερο για τους ασθενείς με IPSSR πολύ χαμηλού κινδύνου που έλαβαν luspatercept έναντι του εικονικού φαρμάκου (77,8% έναντι 16,7%, αντίστοιχα; OR 17.5; p=.0088). Η επιβίωση
ελεύθερης
προόδου νόσου ήταν επίσης μεγαλύτερη
στους 36 μήνες στους ασθενείς που έλαβαν luspatercept έναντι εικονικού φαρμάκου για άλλη μία υποομάδα ασθενών, εκείνων με ερυθροποιητίνη ορού από 100-200 U/L στην έναρξη της θεραπείας (97,3% έναντι 78,9%, OR 9.6; p=.0238). Το Reblozyl χορηγείται σε δόση 1,0 mg/kg ανά 3 εβδομάδες και μπορεί να γίνει αύξηση έως και τα 1,75 mg/kg ανά 3 εβδομάδες. Παρουσιάστηκαν επίσης τα καταληκτικά δεδομένα από τη μελέτη Φάσης ΙΙΙ SINTRAREV11 και φαίνεται ότι, συγκριτικά με το εικονικό φάρμακο, η λεναλιδομίδη σε χαμηλή δόση επιμηκύνει το διάστημα για μετάγγιση, μειώνει την πιθανότητα εξάρτησης από μεταγγίσεις και δεν αυξάνει τον κίνδυνο υποτροπής ή εκτροπής της νόσου σε ασθενείς με χαμηλού κινδύνου MDS. Με μια διάμεση παρακολούθηση 5,05 ετών, η χαμηλή δόση λεναλιδομίδης μείωσε τον κίνδυνο εξάρτησης από μεταγγίσεις κατά 69,8% (HR, 0.302; p=.005).
Όσον αφορά την αιματολογική ανταπόκριση, οι ασθενείς που έλαβαν χαμηλή δόση λεναλιδομίδης εμφάνισαν ένα ποσοστό ανταπόκρισης στο 77,8% έναντι 0% εκείνων που έλαβαν εικονικό φάρμακο. Η ομάδα
Παρουσιάστηκαν
τα αποτελέσματα
από την εγκριτική
μελέτη Φάσης ΙΙΙ
MEDALIST, με
βάση τα οποία
το luspatercept
βελτιώνει την τριετή
συνολική επιβίωση
σε σύγκριση με το
εικονικό φάρμακο
σε ασθενείς με
μυελοδυσπλαστικό
σύνδρομο χαμηλού
κινδύνου με
δακτυλιοειδείς
σιδηροβλάστες.
59 ΑΦΙΕΡΩΜΑ ΑΙΜΑΤΟΛΟΓΙΑ
Δόθηκε έγκριση από τον FDA για τη χορήγηση του olutasidenib, ενός επίσης αναστολέα του μεταλλαγμένου
ενζύμου IDH1, σε ασθενείς με υποτροπιάζουσα/
ανθεκτική ΟΜΛ
που φέρουν τη μετάλλαξη IDH1.
που έλαβε λεναλιδομίδη εμφάνισε ποσοστό κυτταρογενετικής ανταπόκρισης στο 94,1% έναντι 0% στην ομάδα του εικονικού φαρμάκου. Επίσης, το διάμεσο διάστημα έως την εξάρτηση από μεταγγίσεις δεν επιτεύχθηκε για την ομάδα της λεναλιδομίδης, έναντι 11,6 μηνών για την ομάδα του εικονικού φαρμάκου. Το 2022, ο FDA έθεσε το eltanexor (KPT-8602) προς έγκριση με επιταχυνόμενες διαδικασίες ως μονοθεραπεία για τη θεραπεία του μυελοδυσπλαστικού συνδρόμου σε για ασθενείς με ανθεκτικό ή/και υποτροπιάζον μυελοδυσπλαστικό σύνδρομο ενδιάμεσου, υψηλού ή πολύ υψηλού κινδύνου και στη συνέχεια το χαρακτήρισε ορφανό φάρμακο στις ΗΠΑ. Το ίδιο έτος, το φάρμακο υπήχθη σε καθεστώς ορφανού φαρμάκου και από τον ΕΜΑ για τη χορήγησή του στην Ευρωπαϊκή Ένωση.
Το eltanexor είναι μια δεύτερης γενιάς αντιστρεπτή ομοιοπολική ένωση εκλεκτικού αναστολέα της πυρηνικής εξαγωγής (SINE) που αποκλείει ειδικά την εξπορτίνη 1 (XPO1). Οι εγκρίσεις αυτές δόθηκαν με βάση τα δεδομένα από τη μελέτη Φάσης
Ι/ΙΙ από τη χορήγηση eltanexor σε ασθενείς με υψηλού κινδύνου μυελοδυσπλαστικό σύνδρομο και βλάστες 5-19%12. Το φάρμακο χορηγήθηκε στα 10 mg και στα 20 mg τις ημέρες 1-5 σε κύκλο 28 ημερών. Στους 20 ασθενείς που εντάχθηκαν με πρωτοπαθές ανθεκτικό ΜΔΣ και διάμεσο αριθμό προηγούμενων θεραπειών 2, το συνολικό ποσοστό ανταπόκρισης στους 15 αξιολογήσιμους ασθενείς ήταν 53,5%, και 7 ασθενείς (46,7%) πέτυχαν πλήρη ύφεση στον μυελό και 1 ακόμα αιματολογική ανταπόκριση. Η διάμεση συνολική επιβίωση στους 15 ασθενείς ήταν 9,86 μήνες. Οι πιο συχνές ανεπιθύμητες ενέργειες ήταν η ναυτία (45%), η διάρροια (35%), η μειωμένη όρεξη (35%) και η ουδετεροπενία (30%). Φαίνεται ότι το eltanexor είναι μια αποτελεσματική και ασφαλής επιλογή για τους ασθενείς με ΜΔΣ υψηλού κινδύνου με πρωτοπαθώς ανθεκτική νόσο.
Οξεία Μυελογενής Λευχαιμία
Το 2022, δημοσιεύθηκε η 5η έκδοση ταξινόμησης του Παγκόσμιου Οργανισμού Υγείας (WHO 2022)1 για τις αιματολογικές κακοήθεις από κύτταρα της μυελικής σειράς και των δενδριτικών κυττάρων/ιστιοκυττάρων και καθορίστηκαν νέα διαγνωστικά κριτήρια για την οξεία μυελογενή λευχαιμία (ΟΜΛ). Η ΟΜΛ, πλέον, κατηγοριοποιείται σε δύο ομάδες: Στην πρώτη, η κατηγοριοποίηση γίνεται με βάση την παρουσία συγκεκριμένων μεταλλάξεων ενώ στη δεύτερη ομάδα η κατηγοριοποίηση γίνεται με βάση τη διαφοροποίηση των κυττάρων.
Στις περισσότερες υποκατηγορίες που εμπίπτουν στην πρώτη ομάδα, η διάγνωση τίθεται με ποσοστό βλαστών <20%. Πλέον, προτείνεται η χρήση του όρου ΟΜΛ σχετιζόμενη με μυελοδυσπλασία (AMLmyelodysplasia related) και περιγράφονται νέα διαγνωστικά κριτήρια. Το 2022, δημοσιεύθηκαν στο NEJM τα δεδομένα της μελέτης Φάσης ΙΙΙ από τους Montesinos et al σε ασθενείς με νέα διάγνωση οξείας μυελογενούς λευχαιμίας με μετάλλαξη IDH1 οι οποίοι δεν ήταν επιλέξιμοι για εντατική εισαγωγική χημειοθεραπεία13. Συνολικά, 146 ασθενείς με αυτά τα χαρακτηριστικά τυχαιοποιήθηκαν να λάβουν ivosidenib από του στόματος (500 mg μία φορά την ημέρα) με υποδόρια ή ενδοφλέβια αζακιτιδίνη (75 mg/m2 για 7 ημέρες σε κύκλο 28 ημέρων) (n=72) ή εικονικό φάρμακο με αζακιτιδίνη (n=74). Με μια διάμεση παρακολούθηση 12,4 μηνών, η επιβίωση ελεύθερη υποτροπής ή άλλου
60 / Μάρτιος-Απρίλιος 2023
ΑΡΘΡΟ
συμβάματος ήταν σημαντικά μεγαλύτερη
για την ομάδα που έλαβε ivosidenib-αζακιτιδίνη έναντι της ομάδας που έλαβε εικονικό φάρμακο-αζακιτιδίνη (HR 0.33
για αποτυχία θεραπείας, υποτροπή με-
τά από ανταπόκριση και θάνατο, 95% CI 0.16-0.69 p=0.002). Η συνολική επιβίω-
ση ήταν επίσης 24 μήνες για την ομάδα που έλαβε τον συνδυασμό ivosidenib-αζακιτιδίνη έναντι 7,9 μηνών για την ομάδα που έλαβε εικονικό φάρμακο-αζακιτιδίνη (HR 0.44; 95% CI 0.27 to 0.73; p=0.001).
Οι συχνότερες ανεπιθύμητες ενέργειες (βαθμού 3+) ήταν το ουδετεροπενικό εμπύρετο, η ουτεροπενία και οι αιμορραγικές επιπλοκές. Η επίπτωση λοιμώξεων οποιουδήποτε βαθμού ήταν 28% στην ομάδα του συνδυασμού έναντι 49% στην ομάδα που έλαβε εικονικό φάρμακο με αζακιτιδίνη. Συνολικά, το ουδετεροπενικό εμπύρετο και οι λοιμώξεις ήταν λιγότερο συχνά στην ομάδα που έλαβε τον συνδυασμό ενώ η ουδετεροπενία και οι αιμορραγικές επιπλοκές πιο συχνά έναντι της ομάδας που έλαβε εικονικό φάρμακο και αζακιτιδίνη. Σύνδρομο διαφοροποίησης περιγρά -
φτηκε στο 14% των ασθενών που έλαβαν ivosidenib-αζακιτιδίνη και στο 8% των ασθενών που έλαβαν αζακιτιδίνη μονοθεραπεία. Συμπερασματικά, ο συνδυασμός του αναστολέα του μεταλλαγμένου ενζύμου IDH1, ivosidenib και της αζακιτιδίνης είναι πιο αποτελεσματικός έναντι της μονοθεραπείας με αζακιτιδίνη σε ασθενείς με νέα διάγνωση ΑΜΛ που φέρουν τη μετάλλαξη IDH1 και δεν είναι επιλέξιμοι για εντατική χημειοθεραπεία με παρόμοιο προφίλ τοξικότητας. Για τον λόγο αυτό, πλέον, προτείνεται πλέον ως θεραπεία εκλογής για τους ασθενείς αυτούς. Το 2022, έλαβε έγκριση από τον FDA το olutasidenib, ένας ακόμα αναστολέας του μεταλλαγμένου ισοενζύμου του IDH1 για τους ασθενείς με ανθεκτική/υποτροπιάζουσα ΟΜΛ που φέρουν μετάλλαξη στον IDH1. Το olutasidenib χορηγείται ως μονοθεραπεία από του στόματος και προσδένει στον μεταλλαγμένο mIDH1, μειώνοντας έτσι τα επίπεδα της 2-hydroxyglutarate και αποκαθιστώντας τη φυσιολογική κυτταρική διαφοροποίηση των μυελοκυττάρων. Η έγκριση δόθηκε με βάση τα δεδομένα από την εγκριτική μελέτη Φάσης ΙΙ, που αξιολόγησε τη χορήγηση olutasidenib σε δόση 150 mg δύο φορές την ημέρα σε 153 ασθενείς με mIDH1 ανθεκτική/υποτροπιάζουσα ΟΜΛ14. Η δόση χορήγησης είναι 150 mg δύο φορές την ημέρα. Το πρωτεύ-
ον καταληκτικό σημείο ήταν συνδυαστικό, το ποσοστό ασθενών με πλήρη ύφεση (CR) μαζί με το ποσοστό ασθενών με πλήρη ύφεση αλλά μερική αιματολογική ανάκαμψη (CRh). Αναλύθηκαν δεδομένα στους 6 μήνες και το ποσοστό CR+CRh σε 147 ασθενείς ήταν 35%. Από τους ασθενείς αυτούς το 92% πέτυχε CR. Η διάμεση διάρκεια ανταπόκρισης ήταν 25,9 μήνες και ο διάμεσος χρόνος ανταπόκρισης 1,9 μήνες. Το φάρμακο είχε καλά ανεκτό προφίλ τοξικότητας, και σύνδρομο διαφοροποίησης παρατηρήθηκε στο 16% των ασθενών, το οποίο ήταν όμως διαχειρισίμο, με διακοπή της θεραπείας και χορήγηση κορτικοστεροειδών. Παρατηρήθηκε επίσης ηπατοτοξικότητα στο 23% των ασθενών.•••
1. KHOYRY JD, SOLARY E, ABLA O, et al. The 5th edition of the World Health Organization Classification of Haematolymphoid Tumours: Myeloid and Histiocytic/Dendritic Neoplasms. Leukemia. 2022;36(7):1703.
2. MESA RA, VANNUCCHI AM, MEAD A, et al. Pacritinib versus best available therapy for the treatment of myelofibrosis irrespective of baseline cytopenias (PERSIST-1): an international, randomised, phase 3 trial. Lancet Haematol. 2017;4(5):e225-e236.
3. MASCARENHAS J, HOFFMAN R, TALPAZ M, et al. Pacritinib vs best available therapy, including ruxolitinib, in patients with myelofibrosis: a randomized clinical trial. JAMA Oncol. 2018;4(5):652-659.
4. GERDS AT, SAVONA MR, SCOTT BL, et al. Determining the recommended dose of pacritinib: results from the PAC203 dosefinding trial in advanced myelofibrosis. Blood Adv. 2020 Nov 24;4(22):5825-5835.
5. MESA RA, GERDS AT, VANNUCCHI A, et al. MOMENTUM: phase 3 randomized study of momelotinib (MMB) versus danazol (DAN) in symptomatic and anemic myelofibrosis (MF) patients previously treated with a JAK inhibitor. J Clin Oncol. 2022;40(suppl 16):7002.
6. Blueprint Medicines’ AYVAKYT (avapritinib) receives European Commission approval for the treatment of adults with advanced systemic mastocytosis. News release. Blueprint Medicines Corporation; March 25, 2022. Accessed March 25, 2022. https://prn. to/3iybxp4
7. DEANGELO DJ, RADIA DH, GEORGE TI, et al. Safety and efficacy of avapritinib in advanced systemic mastocytosis: the phase 1 EXPLORER trial. Nature Medicine. 2021;27: 2183–2191
8. GOTLIB L, REITER A, RADIA H, et al. Efficacy and safety of avapritinib in advanced systemic mastocytosis: interim analysis of the phase 2 PATHFINDER trial. Nature Medicine. 2021;27:2192–2199.
9. GOTLIB L, KILADJIAN JJ, VANNUCCHI A, et al. A Phase 2 Study of Pemigatinib (FIGHT-203; INCB054828) in Patients with Myeloid/Lymphoid Neoplasms (MLNs) with Fibroblast Growth Factor Receptor 1 (FGFR1) Rearrangement (MLN FGFR1). Blood. 2021;138: 385.
10. SANTINI V, FENAUX P, ZEIDAN AM, et al. Overall survival and progression-free survival of patients following luspatercept treatment in the MEDALIST trial. Presented at ASH 2022; December 10-13, 2022. Abstract 1774.
11. CADENAS FL, LUMBRERAS E, GONZALEZ T, et al. Evaluation of lenalidomide (len) vs placebo in nontransfusion dependent low risk del(5q) MDS patients. Final results of Sintra-REV phase III international multicenter clinical trial. Presented at ASH 2022. December 10-13, 2022. Abstract 460
12. LEE S, MOHAN S, KNUPP J, et al. Oral eltanexor treatment of patients with higher-risk myelodysplastic syndrome refractory to hypomethylating agents. J Hematol Oncol. 2022 Aug 3;15(1):103.
13. MONTESINOS P, RECHER C, VIVES S, et al. Ivosidenib and Azacitidine in IDH1Mutated Acute Myeloid Leukemia. N Engl J Med 2022; 386:1519.
14. CORTES JE, FENAUX P, YEE K, et al. Olutasidenib (FT-2102) Induces Durable Complete Remissions in Patients with Relapsed/Refractory mIDH1 Acute Myeloid Leukemia. Results from a Planned Interim Analysis of a Phase 2 Pivotal Clinical Trial. Blood (2022) 140 (Supplement 1): 61936196.
61 ΑΦΙΕΡΩΜΑ ΑΙΜΑΤΟΛΟΓΙΑ
Βιβλιογραφία
Η πρώτη στην
κατηγορία της
θεραπεία για
Tο «πράσινο φως» έλαβε η Bristol Myers Squibb από την Ευρωπαϊκή Επιτροπή για το luspatercept, το οποίο αποτελεί την πρώτη στην κατηγορία της (first-in-class) θεραπευτική επιλογή για την αντιμετώπιση της αναιμίας που σχετίζεται με μη εξαρτώμενη από μεταγγίσεις β-θαλασσαιμία σε ενήλικες ασθενείς. Η χορήγηση της πλήρους άδειας βασίστηκε σε αποτελέσματα που προέρχονται από τη μελέτη Φάσης 2 BEYOND, η οποία αξιολόγησε την αποτελεσματικότητα και την ασφάλεια του luspatercept έναντι εικονικού φαρμάκου.
Το luspatercept αναπτύσσεται και διατίθεται στο πλαίσιο μιας παγκόσμιας συνεργασίας της BMS με τη Merck, μετά την εξαγορά της Acceleron Pharma από τη Merck τον Νοέμβριο του 2021. Κατόπιν της τελευταίας άδειας, πλέον, το luspatercept είναι εγκεκριμένο στην Ευρωπαϊκή Ένωση, τις Ηνωμένες Πολιτείες και τον Καναδά για την αντιμετώπιση της εξαρτώμενης από μεταγγίσεις αναιμίας που σχετίζεται με β-θαλασσαιμία και χαμηλού κινδύνου μυελοδυσπλαστικά σύνδρομα (ΜΔΣ)
Η κεντρική άδεια κυκλοφορίας αφορά
χορήγηση της πλήρους άδειας
που
την έγκριση χρήσης του luspatercept σε όλα τα κράτη μέλη της Ευρωπαϊκής Ένωσης, καθώς και στη Νορβηγία, την Ισλανδία και το Λιχτενστάιν. Η κεντρική άδεια κυκλοφορίας δεν περιλαμβάνει έγκριση για χρήση στη Μεγάλη Βρετανία (Αγγλία, Σκωτία και Ουαλία).
«Η β-θαλασσαιμία είναι μια κληρονομική αιματολογική διαταραχή, που, λόγω της αναιμίας, θέτει τους ασθενείς σε σημαντικό κίνδυνο εκδήλωσης μακροπρόθεσμων επιπλοκών. Ο κίνδυνος αυτός αναδεικνύει την ουσιαστική ανάγκη για την ύπαρξη θεραπευτικών επιλογών, ανεξαρτήτως της εξάρτησης του ασθενούς από μεταγγίσεις αίματος. Η ανακοίνωση αποτελεί μια ευχάριστη είδηση για τους ασθενείς με αναι-
μία που σχετίζεται με μη εξαρτώμενη από μεταγγίσεις β-θαλασσαιμία σε ολόκληρη
την Ευρώπη, οι οποίοι αναζητούν νεότερες θεραπευτικές επιλογές για να αποφύγουν αυτές τις επιπλοκές» δήλωσε ο Noah Berkowitz, MD, PhD, αντιπρόεδρος ανάπτυξης του τομέα Αιματολογίας της Bristol Myers Squibb. «Η πρόσφατη έγκριση αφορά στην τρίτη ένδειξη για το luspatercept στην Ευρώπη και ανυπομονούμε να συνεχίσουμε την αξιολόγηση αυτής της πρώτης στην κατηγορία της (first–in-class) θεραπευτικής επιλογής σε πολλές ακόμη ασθένειες που συνδέονται με την αναιμία, στο πλαίσιο ενός ευρύτατου προγράμματος κλινικής ανάπτυξης».
Η μελέτη BEYOND
Πρόκειται για μια διπλά τυφλή, τυχαιοποιημένη, ελεγχόμενη με εικονικό φάρμακο πολυκεντρική μελέτη Φάσης 2 για την αξιολόγηση της αποτελεσματικότητας και της ασφάλειας του luspatercept έναντι εικονικού φαρμάκου σε ενήλικους ασθενείς με μη εξαρτώμενη από μεταγγίσεις β-θαλασσαιμία. Η μελέτη χωρίζεται στην περίοδο ελέγχου διαλογής, την περίοδο διπλά τυφλής θεραπείας και την περίοδο παρακολούθησης μετά τη θεραπεία. Ο πληθυσμός της μελέτης ήταν 145 ενήλικοι ασθενείς με μη εξαρτώμενη από μεταγγίσεις βθαλασσαιμία. Οι συμμετέχοντες έλαβαν τη βέλτιστη υποστηρικτική αγωγή (BSC), η οποία περιλάμβανε μεταγγίσεις ερυθρών αιμοσφαιρίων και χηλικοποιητικούς παράγοντες σιδήρου, χρήση αντιβιοτικών, αντιιικών και αντιμυκητιασικών θεραπειών ή/και διατροφική υποστήριξη, ανάλογα με τις ανάγκες.
Ως πρωτεύον καταληκτικό σημείο της μελέτης ορίστηκε το ποσοστό των ασθενών
που εμφανίζουν αύξηση της μέσης αιμοσφαιρίνης από την τιμή αναφοράς ≥1,0 g/dL σε συνεχές διάστημα θεραπείας 12
62 / Μάρτιος-Απρίλιος 2023 ΡΕΠΟΡΤΑΖ
Το luspatercept, πλέον, και στην Ευρώπη
για την αντιμετώπιση της αναιμίας
ασθένειες
συνδέονται
αναιμία Η
που
με την
μελέτη
BEYOND. Τρίτη εγκεκριμένη ένδειξη
βασίστηκε σε αποτελέσματα
προέρχονται από τη
Φάσης 2
εβδομάδων από την εβδομάδα 13 έως την εβδομάδα 24, απουσία μεταγγίσεων. Τα κύρια δευτερεύοντα καταληκτικά σημεία περιλαμβάνουν τη μέση μεταβολή της βαθμολογίας όσον αφορά τις αναφερόμενες από τον ασθενή με μη μεταγγισιοεξαρτώμενη β-θαλασσαιμία εκβάσεις (NTDT-PRO) στον τομέα κόπωσης και αδυναμίας, καθώς και στη μέση μεταβολή
από την τιμή αναφοράς της αιμοσφαιρίνης. Τα αποτελέσματα έδειξαν ότι 74 από τους 96 (77,1%) ασθενείς στο σκέλος θεραπείας με luspatercept πέτυχαν το πρωτεύον καταληκτικό σημείο της μελέτης, αύξηση της μέσης αιμοσφαιρίνης από
την τιμή αναφοράς ≥1,0 g/dL, έναντι 0 από τους 49 (0%) ασθενείς στο σκέλος θεραπείας με εικονικό φάρμακο (P<0,0001).
Σε ένα δευτερεύον καταληκτικό σημείο της
μελέτης, 47 από τους 96 ασθενείς (49,0%)
που έλαβαν θεραπεία με luspatercept πέτυχαν μέση αύξηση της αιμοσφαιρίνης
≥1,5 g/dL σε σύγκριση με την τιμή αναφοράς από την εβδομάδα 37 έως την εβδομάδα 48, απουσία μεταγγίσεων, έναντι 0 ασθενών (0%) στο σκέλος θεραπείας με εικονικό φάρμακο (P<0,0001). Στο σκέλος
θεραπείας με luspatercept, το 89,6% των ασθενών δεν χρειάστηκε να υποβληθούν σε μεταγγίσεις κατά τις εβδομάδες 1-24 έναντι του 67,3% των ασθενών στο σκέλος θεραπείας με εικονικό φάρμακο (P=0,0013).
Αξίζει να σημειωθεί ότι διαπιστώθηκε βελτίωση στις αναφερόμενες από τον ασθενή εκβάσεις όσον αφορά στην ποιότητα ζωής (κόπωση και αδυναμία), η οποία συνάδει με την αύξηση των τιμών της αιμοσφαιρίνης.
Σοβαρές ανεπιθύμητες ενέργειες εμφανίστηκαν στο 11,5% των ασθενών (n=11) που έλαβαν θεραπεία με luspatercept. Οι πιο συχνές ανεπιθύμητες ενέργειες που αναφέρθηκαν σε ≥10% των ασθενών ήταν οστικός πόνος (36%), κεφαλαλγία (30%), αρθραλγία (29%), οσφυαλγία (28%), προϋπέρταση (23%), υπέρταση (20%), βήχας (18%), διάρροια (17%), γριπώδης συνδρομή (17%), εξασθένηση (13%), γρίπη (13%), αϋπνία (11%) και ναυτία (10%).
Η β-θαλασσαιμία
Η εν λόγω ασθένεια είναι μια κληρονομική αιματολογική διαταραχή που οφείλεται σε μια γενετική ανωμαλία της αιμοσφαιρίνης. Αποτελεί μία από τις πιο συχνές αυτοσωμικές υπολειπόμενες διαταραχές. Η συνολική ετήσια επίπτωση της συμπτωματικής β-θαλασσαιμίας υπολογίζεται σε 1 περιστατικό ανά 100.000 άτομα σε ολόκληρο τον κόσμο. Η νόσος σχετίζεται με
την αναποτελεσματική ερυθροποίηση, η οποία οδηγεί στην παραγωγή μειωμένων και λιγότερο υγιών ερυθρών αιμοσφαιρίων, καταλήγοντας συνήθως στην εμφάνιση σοβαρής αναιμίας, η οποία ενδέχεται να οδηγήσει σε σοβαρότερες επιπλοκές, καθώς και σε άλλα σοβαρά προβλήματα υγείας. Οι θεραπευτικές επιλογές για την αναιμία που σχετίζεται με τη β-θαλασσαιμία είναι περιορισμένες, καθώς κατά κύριο λόγο περιλαμβάνουν τις τακτικές μεταγγίσεις ερυθρών αιμοσφαιρίων (RBC). Ωστόσο, οι μεταγγίσεις μπορούν να οδηγήσουν στην υπερφόρτωση σιδήρου, η οποία, με τη σειρά της, μπορεί να προκαλέσει σοβαρές επιπλοκές, όπως βλάβη οργάνων. Η μη εξαρτώμενη από μεταγγίσεις β-θαλασσαιμία είναι ένας όρος που χρησιμοποιείται για να περιγράψει τους ασθενείς οι οποίοι δεν χρειάζονται διά βίου τακτικές μεταγγίσεις για να επιβιώσουν, παρόλο που μπορεί να αντιμετωπίσουν διάφορες κλινικές επιπλοκές και να χρειαστεί να υποβληθούν σε μεταγγίσεις περιστασιακά ή ακόμα και σε τακτική βάση, συνήθως για συγκεκριμένη χρονική περίοδο.
Η νέα θεραπεία
Το luspatercept, μια πρώτη στην κατηγορία της (first-in-class) θεραπευτική επιλογή, προάγει την ωρίμανση τελικής φάσης των ερυθρών αιμοσφαιρίων σε ζωικά μοντέλα Το luspatercept αναπτύσσεται και διατίθεται στην αγορά στο πλαίσιο μιας παγκόσμιας συνεργασίας με τη Merck, μετά την εξαγορά της Acceleron Pharma από τη Merck τον Νοέμβριο του 2021. Επί του παρόντος, το luspatercept ενδείκνυται για περιστατικά αναιμίας σε ενήλικους ασθενείς με β-θαλασσαιμία οι οποίοι έχουν ανάγκη από τακτικές μεταγγίσεις ερυθρών αιμοσφαιρίων (RBC) και για περιστατικά αναιμίας που δεν ανταποκρίνεται σε έναν παράγοντα διέγερσης της ερυθροποίησης (ESA) και απαιτεί δύο ή περισσότερες μονάδες ερυθρών αιμοσφαιρίων σε διάστημα οκτώ εβδομάδων, σε ενήλικους ασθενείς με πολύ χαμηλού έως ενδιάμεσου κινδύνου μυελοδυσπλαστικά σύνδρομα (ΜΔΣ) οι οποίοι έχουν δακτυλιοειδείς σιδηροβλάστες ή ασθενείς με μυελοδυσπλαστικό/μυελοϋπερπλαστικό νεόπλασμα με δακτυλιοειδείς σιδηροβλάστες και θρομβοκυττάρωση.
Σημειώνεται ότι το luspatercept δεν ενδείκνυται για χρήση ως υποκατάστατο των μεταγγίσεων ερυθρών αιμοσφαιρίων σε ασθενείς που έχουν ανάγκη από άμεση διόρθωση της αναιμίας.•••
63 ΑΦΙΕΡΩΜΑ ΑΙΜΑΤΟΛΟΓΙΑ
Το luspatercept προάγει την ωρίμανση τελικής
φάσης των ερυθρών αιμοσφαιρίων σε ζωικά μοντέλα.
Παχυσαρκία: «Μεταβολική βόμβα»
Από τους:
Κώστα Αθανασάκη, επίκουρο καθηγητή Οικονομικών της
Υγείας και Οικονομικής Αξιολόγησης των
Τεχνολογιών Υγείας στο Τμήμα Πολιτικών Δημόσιας Υγείας του ΠαΔΑ, πρόεδρο του Ινστιτούτου Οικονομικών της Υγείας
Ευθύμιο Καπάνταη, παθολόγο με εξειδίκευση στον Σακχαρώδη Διαβήτη, γενικό γραμματέα της Ελληνικής Ιατρικής Εταιρείας Παχυσαρκίας
Αναστασία Μπαρμπούνη, καθηγήτρια Δημόσιας Υγείας, Υγιεινής και
Πρόληψης Νόσων στο Τμήμα Δημόσιας & Κοινοτικής Υγείας της Σχολής Δημόσιας
Υγείας του ΠαΔΑ
Νικόλαο Τεντολούρη, καθηγητή Παθολογίας στην Ιατρική Σχολή
του Πανεπιστημίου Αθηνών, πρόεδρο
της Ελληνικής Εταιρείας Εσωτερικής Παθολογίας
Σύμφωνα με τα τελευταία επίσημα στοιχεία, η πορεία της παχυσαρκίας λαμβάνει ανησυχητική τροπή, με την Ελλάδα να κατέχει μία από τις υψηλές θέσεις στην παγκόσμια κατάταξη σε ποσοστά παχυσαρκίας των πολιτών της. Η θέση της ανεβαίνει ακόμα υψηλότερα όσον αφορά το ποσοστό παχυσαρκίας στα παιδιά.
Το 2019, παχύσαρκος ήταν 1 στους 6 πολίτες (17%) και σχεδόν 1 στους 2 (50%) είχε βάρος πάνω από το φυσιολογικό. Αντίστοιχη υψηλή συχνότητα παχυσαρκίας διαπιστώνεται και στα παιδιά ηλικίας 7 έως 9 ετών. Μόνο το 30,3% του γενικού πληθυσμού έχει κανονικό βάρος. Η παχυσαρκία είναι μια παγκόσμια επιδημία. Αναγνωρισμένη ως νόσος από τον Παγκόσμιο Οργανισμό Υγείας και την Ευρωπαϊκή Ένωση, αποτελεί μια πολυπαραγοντική κατάσταση στενά συνδεδεμένη με τις ατομικές συμπεριφορές, τις οικογενειακές συνθήκες και συνήθειες και τα κοινω-

64 / Μάρτιος-Απρίλιος 2023
που
απειλεί την υγεία
ΑΡΘΡΟ
της κοινωνίας μας

65
Σήμερα, το 60% του παγκόσμιου πληθυσμού
στον δυτικό και αναπτυσσόμενο κόσμο είναι υπέρβαροι και το 25% παχύσαρκοι.
νικά πρότυπα. Αυτές οι πολλαπλές «ρίζες» του φαινομένου δείχνουν και τη δυσκολία της αντιμετώπισής του. Με βάση δεδομένα του ΟΟΣΑ, σήμερα το 60% του παγκόσμιου πληθυσμού στον δυτικό και αναπτυσσόμενο κόσμο είναι υπέρβαροι και το 25% παχύσαρκοι (OECD analyses on the WHO Global Health Observatory, 2018). Οι εκτιμήσεις για το μέλλον είναι ότι το ποσοστό της παχυσαρκίας στην επόμενη δεκαετία θα φθάσει στο 50%, με τους μισούς από τους παχύσαρκους να έχουν νοσογόνο παχυσαρκία.
Η παχυσαρκία, ως νόσος αλλά και ως αιτιολογικός παράγοντας, επιβαρύνει σημαντικά το συνολικό φορτίο νοσηρότητας, καθώς συνδέεται με μια σειρά από νοσήματα όπως ο Σακχαρώδης Διαβήτης τύπου 2, η δυσλιπιδαιμία, τα καρδιαγγειακά νοσήματα, ο καρκίνος, η κατάθλιψη, τα προβλήματα του μυοσκελετικού κ.ά. Συνεπώς, δεν αποτελεί έκπληξη το γεγονός ότι η παχυσαρκία επιβαρύνει σημαντικά και τα οικονομικά του συστήματος υγείας, ως αποτέλεσμα των αυξημένων αναγκών σε φροντίδα των πασχόντων από τα σχετιζόμενα με την παχυσαρκία νοσήματα. Με βάση εκτιμήσεις για την Ελλάδα, η συνολική οικονομική επιβάρυνση από την παχυσαρκία στη χώρα μας ανέρχεται σε ποσοστό περίπου 2,4% του ΑΕΠ ή, σε νομισματικά μεγέθη, σε 4,3 δισ. ευρώ ετησίως. Πάνω από το 50% αυτής της δαπάνης αφορά σε απώλειες παραγωγικότητας, δηλαδή επηρεάζει το σύνολο της οικονομίας, ως αποτέλεσμα της απουσίας
από την εργασία λόγω προβλημάτων υγείας που συνδέονται με την παχυσαρκία. Κάθε χρόνο, η νοσοκομειακή δαπάνη του δημόσιου συστήματος υγείας για την αντιμετώπιση της παχυσαρκίας (και των συνδεόμενων με αυτή νοσημάτων) υπερβαίνει τα 650 εκατ. ευρώ, σε ένα σύστημα το οποίο διαχρονικά, αλλά και ιδιαιτέρως στις μέρες μας, λειτουργεί με μεγάλο φόρτο.
Ο σύγχρονος τρόπος ζωής, αλλά και οι αλλαγές στο φυσικό και τεχνητό περιβάλλον, θέτουν σύνθετα ζητούμενα από το σύστημα υγείας, με κυριότερο οι «υγιείς» να καταφέρουν να διατηρήσουν την υγεία τους και στο μέλλον, σε πείσμα των ανερχόμενων απειλών για την υγεία μας.
Τα αίτια της αυξημένης συχνότητας παχυσαρκίας σχετίζονται με αυξημένη κατανάλωση ενέργειας μέσω των τροφών και του καθιστικού τρόπου ζωής και εργασίας. Διαχρονικά, το μέγεθος των σακχαρούχων ποτών, των ειδών ζαχαροπλαστικής
και των σνακ αυξήθηκε σε μέγεθος από 20% έως 100% από το 1960. Οι Ευρωπαίοι περνούν καθιστοί περισσότερες από 5 ώρες τη μέρα. Στον χώρο εργασίας
η ενέργεια που καταναλώνεται σήμερα
είναι κατά 15% λιγότερη σε σύγκριση με το 1960. Το 60% των Ευρωπαίων προτιμούν να χρησιμοποιούν στις καθημερινές μετακινήσεις τους το αυτοκίνητό τους και μόνο το 19% αυτών χρησιμοποιούν τακτικά τα μέσα μαζικής μεταφοράς. Ταυτόχρονα, οι πολίτες της ΕΕ προσλαμβάνουν 500 kcal την ημέρα περισσότερες συγκριτικά με πριν από 40 χρόνια.
Σύμφωνα με μελέτη του ΟΟΣΑ σε 46 χώρες (OECD analyses based on the SPHePNCDs model), η μείωση κατά 20% των εμπεριεχόμενων θερμίδων στις ενεργειακά πυκνές τροφές θα μπορούσε να οδηγήσει, τον χρόνο, σε πρόληψη 1.100.000 περιπτώσεων μη μεταδιδόμενων νόσων, σε 1.400.000 επιπρόσθετες ημέρες εργασίας, εξοικονόμηση 13.000.000.000 δολ. και αύξηση 0,5% στο Ακαθάριστο Εθνικό Προϊόν.
Για το κοινό η παχυσαρκία είναι υποεκτιμημένη ως νόσος. Το 84% των ατόμων δεν γνωρίζουν ότι η παχυσαρκία αυξάνει τον κίνδυνο για την εμφάνιση πολλών καρκίνων, το 50% αγνοεί τη σχέση της παχυσαρκίας με τα καρδιοαγγειακά συμβάματα και το 25% δεν γνωρίζει ότι η παχυσαρκία αυξάνει τον κίνδυνο για διαβήτη τύπου 2, αρτηριακή υπέρταση και δυσλιπιδαιμία. Η πραγματικότητα είναι ότι η παχυσαρκία είναι αιτία σοβαρών, ακόμα και απειλητικών,
66 ΑΡΘΡΟ / Μάρτιος-Απρίλιος 2023
για τη ζωή καταστάσεων. Όσο περισσότερο παχύσαρκος είναι κάποιος τόσο μεγαλύτερος είναι ο κίνδυνος να αποκτήσει μια σχετιζόμενη με την παχυσαρκία χρόνια πάθηση.
Οι κοινωνικοί παράγοντες που επιδρούν
στην υγεία, δηλαδή οι συνθήκες υπό τις οποίες γεννιόμαστε, μεγαλώνουμε, εργαζόμαστε, ζούμε, γερνάμε και πεθαίνουμε, ασκούν τη μεγαλύτερη επίδραση στην υγεία του ατόμου και χαρακτηρίζονται ως οι κοινωνικοί προσδιοριστές της υγείας (ΠΟΥ). Έχει τεκμηριωθεί ότι οι κοινωνικές και οικονομικές συνθήκες, το εισόδημα και η εκπαίδευση, καθώς επίσης και μια σειρά συμπεριφορικών παραγόντων, έχουν σημαντική συμβολή στο πρόβλημα της παχυσαρκίας. Υπάρχει δε ιδιαίτερα ισχυρή αντίστροφη σχέση του μορφωτικού επιπέδου με το σωματικό βάρος στο γυναικείο φύλο, αλλά και αντίστροφη σχέση
του εισοδήματος με την παχυσαρκία και
στα δύο φύλα. Βεβαίως, έχει ενδιαφέρον το ότι η αντιμετώπιση των παραπάνω παραγόντων συμβάλλει θετικά στην άμβλυνση των κοινωνικών ανισοτήτων στην υγεία και την ιατρική περίθαλψη. Τα δεδομένα δείχνουν ότι όσο υψηλότερο είναι το επίπεδο εισοδηματικής ανισότητας
στις ευρωπαϊκές χώρες τόσο αυξάνεται ο αριθμός των υπέρβαρων παιδιών, ενώ η παχυσαρκία στα παιδιά της Ευρώπης σχετίζεται στενά με την κοινωνικοοικονομική κατάσταση των γονέων τους. Υψηλότερα ποσοστά παχυσαρκίας και στην πατρίδα μας ανευρίσκονται στα άτομα με χαμηλό κοινωνικοοικονομικό ή/ και εκπαιδευτικό επίπεδο και με ανεπαρκή
σωματική δραστηριότητα. Η χώρα μας, δυστυχώς, κατέχει πολύ υψηλή θέση στην παιδική παχυσαρκία μεταξύ των ευρωπαϊκών χωρών και ο ρυθμός αύξησης της υπερβαρότητας και παχυσαρκίας στα παιδιά εξακολουθεί να είναι ανοδικός, μια τραγική υποθήκη για το μέλλον της υγείας της κοινωνίας μας. Επίσης, στην Ελλάδα, όσον αφορά παράγοντες που επιδρούν στην εμφάνιση της παχυσαρκίας, σημειώνεται υψηλή πρόσληψη ζάχαρης και χαμηλή πρόσληψη φυτικών ινών, ενώ παρατηρούνται υψηλά ποσοστά κατάθλιψης και αγχωδών διαταραχών. Εντοπίζονται, επίσης, υψηλά ποσοστά παθήσεων που σχετίζονται με την παχυσαρκία, όπως ο σακχαρώδης διαβήτης, ο καρκίνος της μήτρας και του μαστού κ.λπ. Για τη χώρα μας προβλέπεται ότι, το 2030, σχεδόν ένας στους τρεις κατοίκους θα είναι παχύσαρκος, με τον ρυθμό ετήσιας αύξησης του ποσοστού από το 2010 έως το 2030 να είναι 1,5%, ενώ στα παιδιά ο αντίστοιχος ετήσιος ρυθμός αύξησης είναι 2,1%. Η άκρως δυσοίωνη πρόβλεψη είναι ότι, το 2060, το 75% των κατοίκων της Ελλάδας θα είναι υπέρβαροι ή παχύσαρκοι! Η καταπολέμηση της παχυσαρκίας αποτελεί μια σημαντική συνιστώσα στην παγκόσμια προσπάθεια μείωσης της νοσηρότητας και θνησιμότητας από τα χρόνια μη μεταδιδόμενα νοσήματα και βελτίωσης της συνολικής υγείας του πληθυσμού. Η προοπτική είναι αμφίβολη, δεδομένου του ότι το φαινόμενο της παχυσαρκίας διευρύνεται ενώ δεν υπάρχουν ενδείξεις μείωσης σε διεθνή κλίμακα.
67
Το 84% των ατόμων
δεν γνωρίζουν ότι η
παχυσαρκία αυξάνει
τον κίνδυνο για εμφάνιση πολλών καρκίνων.
Για τη χώρα μας προβλέπεται ότι, το 2030, σχεδόν ένας στους τρεις κατοίκους θα είναι παχύσαρκος.
Η κατάσταση αυτή περικλείει κινδύνους για τη δημόσια υγεία, αφενός στο επίπεδο υγείας του πληθυσμού και αφετέρου στην αύξηση της ζήτησης για το σύστημα ιατρικής περίθαλψης, το οποίο με δυσκολία μπορεί να ανταποκριθεί επαρκώς στις αναδυόμενες ανάγκες. Κατά τον Οργανισμό Οικονομικής Συνεργασίας και Ανάπτυξης (ΟΟΣΑ), η παχυσαρκία ενοχοποιείται για τη μείωση του προσδόκιμου ζωής και τη μείωση του ΑΕΠ. Μόνο στην Ευρώπη, οι πρόωροι θάνατοι που οφείλονται στην παχυσαρκία και τις συνέπειές της ξεπερνούν τους 337.000 ετησίως, ενώ το κόστος ξεπερνά τα 70 δισ. ευρώ ετησίως. Είναι όμως προφανές ότι η οικονομική επιβάρυνση των ιατρικών υπηρεσιών για την αντιμετώπιση της παχυσαρκίας είναι συνάρτηση του Δείκτη Μάζας Σώματος (ΔΜΣ).
Η αναγνώριση της παχυσαρκίας ως χρόνιου νοσήματος είναι επιβεβλημένη για την προτεραιοποίησή της στην πολιτική υγείας και την ενσωμάτωσή της στην ιατρική περίθαλψη. Τα προκύπτοντα οφέλη μπορεί να είναι σημαντικά και βεβαίως είναι ανάλογα της απώλειας του σωματικού βάρους. Σύμφωνα με τον ΟΟΣΑ, για κάθε ευρώ που επενδύεται στην πρόληψη της παχυσαρκίας με μέτρα τεκμηριωμένης αποτελεσματικότητας, περίπου έξι ευρώ επιστρέφουν στην κοινωνία σε όρους οικονομικού οφέλους Παραδοσιακές παρεμβάσεις, όπως η υγιεινή διατροφή και η φυσική άσκηση, βοηθούν στην αντιμετώπιση του βάρους, αλλά ακόμη και η εισαγωγή εμποδίων εμπορικού χαρακτήρα με την ίδια σκόπευση έχει ελπιδοφόρα προοπτική. Σε κάθε περίπτωση, η αντιμετώπιση της παχυσαρκίας απαιτεί κυρίως παρεμβάσεις κοινοτικής προσέγγισης με τη συνεργασία των υπηρεσιών πρωτοβάθμιας φροντίδας και δημόσιας υγείας στην οικογένεια, στο σχολείο, στους χώρους εργασίας και στους «θύλακες» ευάλωτων ομάδων του πληθυσμού.
Ο απώτερος σκοπός των παρεμβάσεων αυτών είναι να βελτιωθεί η υγειονομική και διατροφική εγγραμματοσύνη των πολιτών και η προσαρμογή της συμπεριφοράς των νοικοκυριών σε καλές πρακτικές, που συνδυάζουν την υγεία, την ευεξία και την απόλαυση της καθημερινής ζωής.
Στη χώρα μας είναι υπό ανάπτυξη ένα σχέδιο δράσης για την αντιμετώπιση της παιδικής παχυσαρκίας και της παχυσαρκίας των ενηλίκων, με παρεμβάσεις που στοχεύουν σε ευρύτερες αλλαγές σε θεσμικό
επίπεδο, σε επίπεδο δημόσιας πολιτικής, οι οποίες θα δημιουργήσουν ένα ευνοϊκό περιβάλλον, που θα διευκολύνει την αντιμετώπιση του προβλήματος.
Όπως όλοι γνωρίζουν, οι πολιτικές δημόσιας υγείας αποτελούν μια επένδυση πολυετή, που ξεπερνά τους εκάστοτε κυβερνητικούς ορίζοντες, αλλά αποτελούν απόλυτη προτεραιότητα και απαιτούν σύμπνοια και την προσήλωση όλων στην επίτευξη των στόχων τους.
Σύμφωνα με το μοντέλο αυτό, η βελτίωση και η αλλαγή του τρόπου ζωής και των κοινωνικών, οικονομικών και περιβαλλοντικών συνθηκών που επηρεάζουν την υγεία οδηγεί σε βελτίωση της διατροφής, αύξηση της φυσικής δραστηριότητας και διατήρηση ενός υγιούς βάρους, με απώτερο στόχο τη συνεπακόλουθη βελτίωση των δεικτών νοσηρότητας και την πρόληψη των χρονίων νοσημάτων που σχετίζονται με το σωματικό βάρος.

Τέλος, η πανδημία Covid-19 πυροδότησε μια μεγάλη κρίση παγκόσμιας υγείας και επέφερε σημαντική επιδείνωση των μη μεταδιδόμενων νόσων, οι οποίες αποτελούσαν ήδη μια σημαντική πρόκληση πριν το ξέσπασμα της πανδημίας. Έτσι, και σε επίπεδο ΕΕ, τα μαθήματα που λάβαμε κατά την πανδημία επέβαλαν την επαναξιολόγηση της πολιτικής και, πλέον, η Ευρωπαϊκή Επιτροπή έχει θέσει σε προτεραιότητα την καταπολέμηση της υπερβαρότητας και της παχυσαρκίας και τη βελτίωση της διατροφής, που συνιστούν καθοριστικούς παράγοντες εμφάνισης πολλών μη μεταδιδόμενων νόσων, περιλαμβανομένου και του καρκίνου. Η αντιμετώπιση της παχυσαρκίας είναι πολύπλοκη και απαιτεί διεπιστημονικές και διατομεακές παρεμβάσεις σε βάθος χρόνου, με συνέπεια και συνέχεια. Η παχυσαρκία συνιστά πρόβλημα κατά βάση κοινωνικοπολιτικό και δευτερευόντως ιατρικό. Για να προστατεύσουμε το μέλλον της υγείας της κοινωνίας μας απαιτείται η εφαρμογή των κατάλληλων πολιτικών από την Πολιτεία, η ευαισθητοποίηση και εκπαίδευση των γιατρών και των επαγγελματιών υγείας, η ενημέρωση και η ευαισθητοποίηση των πολιτών και η ενθάρρυνση υιοθέτησης συμπεριφορών υγιούς διαβίωσης, καθώς και η συνδρομή της Αυτοδιοίκησης.
Η Παγκόσμια Ημέρα Παχυσαρκίας μάς θυμίζει ότι η απασφάλιση αυτής της «μεταβολικής βόμβας» συνιστά ύψιστη προτεραιότητα στην ιεράρχηση των εθνικών υγειονομικών στόχων.•••
68 ΑΡΘΡΟ / Μάρτιος-Απρίλιος 2023
69
Ο Ευρωπαϊκός
Χώρος Δεδομένων
Υγείας στοχεύει
στη δημιουργία
μιας ευρωπαϊκής
υποδομής και συνεκτικών διαδικασιών.
Συστάσεις
Η κοινή δράση TEHDAS πραγματοποιείται από 25 ευρωπαϊκές
Σε 9 συστάσεις για τις ευρωπαϊκές χώρες κατά τον σχεδιασμό της εθνικής νομοθεσίας για τη δευτερογενή χρήση δεδομένων υγείας καταλήγει η κοινή δράση TEHDAS. Το έργο ξεκίνησε τον Φεβρουάριο του 2021, συμμετέχουν 25 ευρωπαϊκές χώρες και συντονίζεται από το Φινλανδικό Ταμείο Καινοτομίας, Sitra.
Η Ελλάδα –όπως έχουμε παρουσιάσει σε προηγούμενο τεύχος– είναι ουραγός στον συγκεκριμένο τομέα. Συνεπώς, το συγκεκριμένο έργο έχει ξεχωριστή σημασία για χώρες όπως η δική μας, προκειμένου να αξιοποιήσει τις συστάσεις και να ρυθμίσει με επάρκεια και αποτελεσματικότητα τη δευτερογενή χρήση δεδομένων υγείας. Η τελική έκθεση που παρουσιάζουμε εγκρίθηκε τον Ιανουάριο του 2023 και περιλαμβάνει βασικές συστάσεις που αποσκοπούν στη διευκόλυνση του σχεδιασμού (και της εφαρμογής) της εθνικής νομοθεσίας για τη δευτερογενή χρήση δεδομένων υγείας. Αυτές οι συστάσεις βασίζονται σε μια τεκμηριωμένη περίληψη σε πολυεθνικό επίπεδο των εμπειριών και των συμπερασμάτων πρωτοπόρων ευρωπαϊκών χωρών που διαθέτουν ήδη τέτοια εθνική νομοθεσία σε συνδυασμό με τις ανάγκες άλλων ευρωπαϊκών χωρών από την άποψη αυτή. Ο Γενικός Κανονισμός Προστασίας Δε-
δομένων-GDPR έχει ιδιαίτερη σημασία όταν εξετάζεται η ανταλλαγή δεδομένων για δευτερογενείς σκοπούς. Η έκθεση αναλύει και περιγράφει τις υφιστάμενες διαφορές στα κράτη μέλη και το πώς αυτές επηρεάζουν τη δυνατότητα δευτερογενούς χρήσης δεδομένων υγείας.
Στο πλαίσιο του έργου, ελήφθησαν συνεντεύξεις από τους υπεύθυνους 6 «προχωρημένων» χωρών της ΕΕ σχετικά με τις βέλτιστες πρακτικές και τα διδάγματα που αντλήθηκαν στο πλαίσιο της προετοιμασίας και της εφαρμογής της εθνικής νομοθεσίας και ειδικότερα όσον αφορά ορισμένες νομικές διατάξεις στο πλαίσιο της εθνικής δομής και των διαδικασιών σε σχέση με τη δευτερογενή χρήση δεδομένων υγείας. Οι χώρες αυτές είναι: Ισπανία (περιοχή της Αραγονίας), Τσεχία, Φινλανδία, Γαλλία, Γερμανία και Λετονία.
Ευρωπαϊκός Χώρος
Δεδομένων Υγείας
Η Ευρωπαϊκή Στρατηγική για τα δεδομένα που παρουσιάστηκε το 2020 πρακτικά σηματοδοτεί την έναρξη των σχεδίων της Επιτροπής για τους ευρωπαϊκούς χώρους δεδομένων. Ο Ευρωπαϊκός Χώρος Δεδομένων Υγείας (European Health Data Space, EHDS) στοχεύει στη δημιουργία
70 / Μάρτιος-Απρίλιος 2023
9
για τη δευτερογενή χρήση δεδομένων υγείας
χώρες Το έργο συγχρηματοδοτήθηκε από το 3ο Πρόγραμμα Υγείας της Ευρωπαϊκής Ένωσης (2014-2020) ΡΕΠΟΡΤΑΖ
μιας ευρωπαϊκής υποδομής και συνεκτικών διαδικασιών που διευκολύνουν τη διασυνοριακή δευτερογενή κοινή χρήση και χρήση δεδομένων υγείας. Η πρωτοβουλία
είναι αποτέλεσμα των προκλήσεων για την αξιοποίηση της ισχύος των δεδομένων υγείας από τους υπεύθυνους χάραξης πολιτικής, τους ερευνητές και άλλους ενδιαφερόμενους φορείς.
Την ίδια ώρα, τεράστιες ποσότητες δεδομένων υγείας παράγονται και αποθηκεύονται σε διάφορες πηγές καθημερινά για πιθανή χρήση. Έτσι, από την προοπτική
του EHDS και σε συνεργασία με τα κράτη μέλη, φιλοδοξία είναι να δημιουργηθεί μια κοινή υποδομή, ένα δίκτυο για τη σύνδεση πηγών δεδομένων υγείας μεταξύ των κρατών μελών, με εναρμονισμένες διαδικασίες πρόσβασης.
Από νομικής πλευράς, η κοινή χρήση δεδομένων για δευτερογενή χρήση είναι πρόκληση για τις περισσότερες χώρες, από πολλές απόψεις. Διαφορετικά κράτη μέλη έχουν διαφορετικές υποδομές, μοντέλα διακυβέρνησης, κεντρικούς υπολογιστές/ιδιοκτησία δεδομένων και διαχείριση δεδομένων υγείας, που αποτελούν όλα μέρος ενός νομοθετικού και ρυθμιστικού πλαισίου. Ευρωπαϊκοί νόμοι, όπως ο Γενικός Κανονισμός Προστασίας Δεδομένων (GDPR), ο Νόμος για τη Διακυβέρνηση Δεδομένων
(DGA), το πλαίσιο για την ασφάλεια στον κυβερνοχώρο (οδηγία NIS2) και ο Κανονισμός Ιατρικών Συσκευών (MDR), καθώς και προτάσεις που είναι ακόμη υπό διαμόρφωση, όπως ο νόμος για τα δεδομένα (DA) και ο νόμος περί τεχνητής νοημοσύνης (AI Act) επηρεάζουν τους εθνικούς νόμους. Επιπλέον, η νέα πρόταση της Επιτροπής για τον κανονισμό EHDS βρίσκεται υπό διαπραγμάτευση με το Ευρωπαϊκό Κοινοβούλιο και τα κράτη μέλη. Πακέτο Εργασίας 5 (WP5): Η «κοινή χρήση δεδομένων για την υγεία» σχετίζεται με διαφορετικές προοπτικές σχετικά με την κοινή χρήση δεδομένων για δευτερεύουσα χρήση και, επομένως, λαμβάνει υπόψη όλες τις πτυχές που εισήχθησαν παραπάνω.

Μεθοδολογία και ανάλυση
Το έργο υπήρξε εξαιρετικά σύνθετο. Ανάμεσα στα άλλα, οι συντάκτες της έκθεσης είχαν να μελετήσουν και να χαρτογραφήσουν την υφιστάμενη κατάσταση, αναλύοντας τις εμπειρίες ορισμένων χωρών, τα εμπόδια, τις βέλτιστες πρακτικές κ.λπ., ώστε τελικά να διαμορφωθούν οι κατάλληλες συστάσεις.
Στην πορεία, αποδείχθηκαν πολύτιμες οι πληροφορίες και οι γνώσεις από προηγούμενες μελέτες (π.χ. η μελέτη EU Health
71
Support, η λεγόμενη μελέτη Nivel), που συμπληρώθηκαν από έρευνα και σε βάθος συνεντεύξεις με νομικούς εμπειρογνώμονες, για να κατανοηθούν οι νομικές προϋποθέσεις και επιλογές των κρατών μελών. Το γεγονός ότι πολλά κράτη μέλη έχουν εθνικούς νόμους για την προστασία των δεδομένων υγείας αποτελεί πρόκληση για την επίτευξη ομοιομορφίας μεταξύ των χωρών και, ως εκ τούτου, μια σημαντική βάση για έναν διασυνοριακό χώρο δεδομένων υγείας. Έτσι, οι εθνικοί νόμοι πρέπει να εξεταστούν και να αναλυθούν σε βάθος. Επιπλέον, αξιοποιήθηκαν τα αποτελέσματα άλλης έρευνας, που αφορούσε τη χαρτογράφηση του τοπίου των δεδομένων υγείας 12 χωρών και των υποδομών για δευτερογενή χρήση δεδομένων υγείας. Η έρευνα παρείχε σημαντικές εισροές κατά την εξέταση των νομοθετικών πλαισίων ως ακρογωνιαίο λίθο για τη διασυνοριακή ανταλλαγή και δευτερογενή χρήση δεδομένων.
Επιχειρηματικά μοντέλα
Οι συστάσεις που δίνονται σε αυτήν την έκθεση θα πρέπει να περιλαμβάνουν παραδείγματα βιώσιμων επιχειρηματικών μοντέλων. Στο πλαίσιο αυτό, σύμφωνα με τις απαντήσεις στις συνεντεύξεις και τις έρευνες, οι περισσότερες χώρες που είτε έχουν δημιουργήσει είτε βρίσκονται στη διαδικασία δημιουργίας κόμβων που διαχειρίζονται διαδικασίες για δευτερογενή χρήση δεδομένων υγείας σε εθνικό επίπεδο έχουν επίσης το εξής: η εθνική τους νομοθεσία επέτρεπε σε αυτές τις αρχές να χρεώνουν τέλη για τις υπηρεσίες τους ή
τους επέτρεψαν να ιδρύσουν εταιρείες υπό τις αρμοδιότητές τους για την πώληση πρόσθετων υπηρεσιών.
Τα τέλη που μπορούν να χρεώσουν οι αρχές συνδέονται, για παράδειγμα, με υπηρεσίες που συγκεντρώνουν, κατηγοριοποιούν, τελειοποιούν ή προετοιμάζουν δεδομένα πριν από τη διανομή των συνόλων δεδομένων. Σε ορισμένες περιπτώσεις, ενδέχεται να ισχύουν επίσης χρεώσεις όταν τα δεδομένα συλλέγονται από διαφορετικούς κατόχους δεδομένων προκειμένου να ενσωματωθούν.
Ωστόσο, οι περισσότερες αρχές και οργανισμοί δεν έχουν ακόμη αρχίσει να χρησιμοποιούν τις δυνατότητες χρέωσης τελών ή δημιουργίας πρόσθετων υπηρεσιών. Ο στόχος τους ήταν να δημιουργήσουν τον οργανισμό τους και να μπορέσουν να προσφέρουν τις αρχικές βασικές υπηρεσίες. Ο πρωταρχικός σκοπός είναι να ενεργοποιηθεί η δευτερεύουσα χρήση και όταν ενεργοποιηθεί, να εξεταστούν οι δυνατότητες των επιχειρηματικών μοντέλων που θα είναι απαραίτητα για τη διατήρηση της λειτουργίας του συστήματος. Ως εκ τούτου, αυτή η έκθεση δεν περιλαμβάνει ανάλυση για την οικονομική βιωσιμότητα. Έμφαση δίνει στο να ενεργοποιήσει τη δευτερεύουσα χρήση, προκειμένου να εξεταστούν ακόμη και οι δυνατότητες για επιχειρηματικά μοντέλα.
Νομικά εμπόδια
Ούτε ένα ούτε δύο, αλλά 11 νομικά εμπόδια εντοπίστηκαν, και μάλιστα έξι από αυτά προκαλούνται από διαφορετικές ερμηνείες και εφαρμογή του γενικού κανονισμού GDPR. Οι συστάσεις που δίνονται, λοιπόν, σε αυτήν την έκθεση συνδέονται άμεσα με αυτά τα εμπόδια:
1. Δεν υπάρχει κοινή ευρωπαϊκή ερμηνεία του τι συνιστά «επαρκή ανωνυμοποίηση» για τη μετατροπή των προσωπικών δεδομένων σε μη προσωπικά δεδομένα.
2. Δεν υπάρχει κοινή ευρωπαϊκή ερμηνεία του τι συνιστά «ψευδώνυμο».
3. Δεν υπάρχει κοινή ευρωπαϊκή ερμηνεία για το τι είναι και τι δεν είναι «δευτερογενής χρήση» δεδομένων.
4. Οι ευρωπαϊκές χώρες έχουν εθνικούς νόμους/κανόνες για δεδομένα υγείας και έρευνας εκτός από τον GDPR.
5. Οι ευρωπαϊκές χώρες έχουν τη δυνατότητα να ορίζουν τις δικές τους παρεκκλίσεις βάσει του GDPR.
6. Οι ευρωπαϊκές χώρες έχουν διαφορε-

72 ΡΕΠΟΡΤΑΖ / Μάρτιος-Απρίλιος 2023
Η νέα πρόταση της Επιτροπής για τον κανονισμό EHDS βρίσκεται υπό διαπραγμάτευση με το Ευρωπαϊκό Κοινοβούλιο και τα κράτη μέλη.
τικές προτιμήσεις ως προς την επιλογή
της νομικής βάσης για την επεξεργασία
στο πλαίσιο του GDRP.
7. Τα δεδομένα υγείας θεωρούνται ευαίσθητα δεδομένα, π.χ. δεδομένα ειδικής
κατηγορίας βάσει του GDPR και αντιμετωπίζονται διαφορετικά από άλλους
τύπους δεδομένων όσον αφορά τη δεοντολογία, τη διαχείριση και τη χρήση των δεδομένων υγείας.
Συμπεράσματα
Σε γενικό επίπεδο, διαφορετικές ερμηνείες των κανονισμών της ΕΕ είναι αρκετά κοινές σε όλους τους τομείς και δεν αποτελούν φαινόμενο μόνο στην πρακτική
του GDPR. Ένας νόμος, είτε εθνικός είτε ευρωπαϊκός, θα ερμηνεύεται διαφορετικά από διαφορετικούς φορείς, η ερμηνεία μπορεί ακόμη και να διαφέρει σε εθνικό επίπεδο.
Είναι πάντα, τελικά, το Ευρωπαϊκό Δικαστήριο εκείνο που δίνει ερμηνευτική προτεραιότητα στη νομοθεσία της ΕΕ. Υπάρχουν επίσης παραδείγματα βάσει των οποίων
τα κράτη μέλη δεν έχουν ρυθμίσει άλλους δευτερογενείς σκοπούς για τους οποίους μπορούν να χρησιμοποιηθούν δεδομένα.
Από την έρευνα και τις συνεντεύξεις, καθώς και από τα ευρήματα της βιβλιογραφίας, το συμπέρασμα είναι ότι τα κράτη μέλη δεν έχουν ουσιαστικά αποκλίνουσες ερμηνείες για βασικές πτυχές του GDPR, αλλά το πλαίσιο της υποδομής μιας χώρας, της οργάνωσης της υγειονομικής περίθαλψης, της νομοθεσίας που ίσχυε πριν από τον GDPR κ.λπ. προκαλεί τις διαφορές στην εφαρμογή του. Ένα συμπέρασμα είναι ότι τα κράτη μέλη τείνουν να ρυθμίζουν τους δευτερογενείς σκοπούς για τους οποίους μπορούν να χρησιμοποιηθούν τα δεδομένα. Σε αυτό το
πλαίσιο, οι (εθνικοί) νομοθέτες μπορούν
να αφήσουν εκείνους που θέλουν να χρησιμοποιήσουν τα δεδομένα για την άμεση
εφαρμογή των διατάξεων των άρθρων 5 (παράγραφος 1 στοιχείο β) και 6 (παράγραφος 4).
Ωστόσο, οι (εθνικοί) νομοθέτες φαίνεται να προτιμούν να εισαγάγουν νομοθεσία για τη δευτερογενή χρήση και τις απαραίτητες διασφαλίσεις ως μορφή περαιτέρω επεξεργασίας. Στην περίπτωση αυτή, ο νομοθέτης διενεργεί τον έλεγχο συμβατότητας και αξιολογεί τη συμμόρφωση σε σχέση με το άρθρο 23 του GDPR περί περιορισμών.
Ενώ το άρθρο 5 παράγραφος 1 στοιχείο β) και το άρθρο 6 παράγραφος 4 μπο-
ρούν να εφαρμοστούν τόσο απευθείας από τους υπευθύνους επεξεργασίας όσο και μέσω κανονιστικών ρυθμίσεων μέσω της εθνικής νομοθεσίας, τα περισσότερα κράτη μέλη φαίνεται να βλέπουν αποκλειστικά τη δευτερογενή χρήση ως προϊόν νομοθετικής ρύθμισης των δυνατοτήτων περαιτέρω επεξεργασίας. Αυτό μπορεί να θεωρηθεί ότι περιορίζει τις δυνατότητες περαιτέρω επεξεργασίας που παρέχονται σύμφωνα με το άρθρο 5 παράγραφος 1 στοιχείο β) αντί να τις επιτρέπει, που είναι και ο σκοπός που τα κράτη μέλη επιλέγουν να το ρυθμίσουν.
Τι ισχύει σε άλλες χώρες
Έχει αξία να δούμε δύο παραδείγματα χωρών:
Γαλλία: Η δευτερογενής χρήση δεδομένων υγείας στη Γαλλία παρέχεται μέσω ενός νέου νόμου που ψηφίστηκε τον Ιούλιο του 2019. Το γαλλικό κέντρο δεδομένων υγείας (Health Data Hub) είναι αποτέλεσμα αυτού του νόμου. Ο νόμος ήταν, με τη σειρά του, αποτέλεσμα μιας έκθεσης σχετικά με την τεχνολογία τεχνητής νοημοσύνης το 2018 από τον βουλευτή του γαλλικού κοινοβουλίου Cédric Villani, που διερευνούσε τις διαφορετικές πτυχές της τεχνολογίας AI, ιδιαίτερα στον τομέα της υγείας. Οι ιδιωτικές εταιρείες μπορούν να έχουν πρόσβαση στα δεδομένα, αποδεικνύοντας ότι η έρευνά τους εκπληρώνει το δημόσιο συμφέρον. Πρέπει να περιγράψουν στο αίτημά τους πώς το έργο τους, που βασίζεται σε δεδομένα υγείας, έχει δημόσιο συμφέρον. Ο επικεφαλής του έργου πρέπει να υποβάλει αίτημα στο Health Data Hub για πρόσβαση σε δεδομένα για ένα έργο. Το αίτημα εξετάζεται από μια ανεξάρτητη επιτροπή δεοντολογίας και στη συνέχεια η γαλλική αρχή για την προστασία δεδομένων/προστασίας της ιδιωτικής ζωής (CNIL) είναι αυτή που δίνει την τελική έγκριση. Τα δεδομένα ψευδοανωνυμοποιούνται από τον κάτοχο των δεδομένων προτού παρασχεθούν στον επικεφαλής του έργου από το Health Data Hub. Ο γαλλικός νόμος δεν επιτρέπει την πρόσβαση σε ακατέργαστα προσωπικά δεδομένα και, ως εκ τούτου, το Γαλλικό Κέντρο Δεδομένων Υγείας δεν χειρίζεται ακατέργαστα (προσωπικά) δεδομένα.
Φινλανδία: Η Φινλανδία έχει νομοθετήσει σχετικά
73
με τη δευτερογενή χρήση δεδομένων υγείας και κοινωνικών δεδομένων. Η
Οι περισσότερες
οργανισμοί
έχουν ακόμη αρχίσει να χρησιμοποιούν τις δυνατότητες χρέωσης τελών ή δημιουργίας πρόσθετων υπηρεσιών.
αρχές και
δεν
Ούτε ένα ούτε
δύο, αλλά 11
νομικά εμπόδια εντοπίστηκαν, και
μάλιστα έξι από
αυτά προκαλούνται από διαφορετικές
ερμηνείες και
εφαρμογή του
γενικού κανονισμού GDPR.
νομοθεσία τέθηκε σε ισχύ τον Απρίλιο του 2019. Παράλληλα, η Φινλανδία επεξεργάστηκε τον νόμο για το Εθνικό Ινστιτούτο Υγείας και Πρόνοιας. Η χώρα διαθέτει μια ανεξάρτητη αρχή που ονομάζεται FinData, η οποία είναι εκείνη που διαχειρίζεται
τα δεδομένα υγείας και παρέχει άδεια δευτερογενούς χρήσης των δεδομένων αυτών. Τα δεδομένα παρέχονται στους ενδιαφερόμενους ψευδοανωνυμοποιημένα.
Οι συστάσεις
Νομική διαλειτουργικότητα
Κατά την υιοθέτηση της εθνικής νομοθεσίας, τα κράτη μέλη πρέπει να εξετάζουν
πώς το εθνικό τους δίκαιο θα είναι διαλειτουργικό με το δίκαιο άλλων κρατών μελών. Αυτό είναι πρωτίστως ζήτημα του πόσο τα κράτη μέλη είναι πρόθυμα να προσαρμόσουν την εθνική τους νομοθεσία στη νομοθεσία άλλων κρατών μελών.
Η δεύτερη πτυχή είναι αν τα κράτη μέλη είναι πρόθυμα να εξετάσουν τη δυνατότητα αποδοχής των διασφαλίσεων άλλων κρατών μελών ως διασφαλίσεις που γίνονται δεκτές από τη δική τους εθνική νομοθεσία. Σε κάποιο βαθμό, οι εθνικές νομοθεσίες στα κράτη μέλη μπορούν να είναι διαλειτουργικές, όπως φαίνεται για παράδειγμα στον τομέα των φαρμακευτικών προϊόντων.
Η νομική διαλειτουργικότητα μεταξύ των διαφορετικών εθνικών κανονισμών των κρατών μελών είναι δύσκολο να επιτευχθεί χωρίς τουλάχιστον κάποιο ελάχιστο σύνολο κατανόησης
και δομών σχετικά με τον τρόπο με τον οποίο επιτρέπεται η δευτερογενής χρήση δεδομένων υγείας.
Μια προϋπόθεση για τη διαλειτουργικότητα είναι η ανάγκη κατανόησης με ποια νομική βάση συλλέγεται και υποβάλλεται σε επεξεργασία το αρχικό σύνολο δεδομένων. Η κατανόηση της νομικής βάσης παρέχει κατανόηση των δικαιωμάτων του ατόμου και των τυχόν περιορισμών που ενδέχεται να ισχύουν για τη χρήση και την επεξεργασία των δεδομένων. Ωστόσο, δεδομένου του ότι τα κράτη μέλη μπορούν να θεσπίσουν πρόσθετους εθνικούς κανόνες που ισχύουν για τα δεδομένα υγείας, υπάρχει ανάγκη κατανόησης των εθνικών κανόνων κάθε κράτους μέλους και του τρόπου λειτουργίας τους. Μπορεί, για παράδειγμα, να είναι η δυνατότητα
του ατόμου να εξαιρεθεί από ορισμένους δευτερογενείς σκοπούς ή περιορισμούς
για τον υπεύθυνο επεξεργασίας ως προς
τη χρήση των δεδομένων.
Επομένως, υπάρχει ανάγκη, με έναν εύκολο και δημοσίως διαθέσιμο τρόπο, για πρόσβαση και κατανόηση των κανόνων
που ισχύουν για διαφορετικά σύνολα δεδομένων για δευτερογενή χρήση. Η πρόταση EHDS για έναν κατάλογο δεδομένων (άρθρο 37), που προτείνει να συμπεριληφθούν λεπτομέρειες σχετικά με την πηγή και τις προϋποθέσεις για τη διάθεση των δεδομένων, αποτελεί ένα βήμα προς αυτήν την κατεύθυνση. Αν ο στόχος είναι να επιτευχθεί όσο το δυνατόν μεγαλύτερη διαλειτουργικότητα, τα κράτη μέλη θα πρέπει να προσπαθήσουν να χρησιμοποιούν
παρόμοια νομική βάση για την πρωτογενή συλλογή και επεξεργασία δεδομένων
υγείας και όσο το δυνατόν περισσότερο
να απέχουν από την εφαρμογή πρόσθετων όρων για τα δεδομένα.
Παρ’ όλο που τα κράτη μέλη θα προσπαθούν όσο το δυνατόν περισσότερο να χρησιμοποιούν την ίδια νομική βάση ή να μην εισάγουν πρόσθετες απαιτήσεις βάσει των εθνικών κανόνων, θα εξακολουθήσει να υπάρχει ένας βαθμός διαφοράς στην εφαρμογή των διατάξεων του GDPR, ειδικά προσαρμοσμένος στις δομές και τους οργανισμούς κάθε κράτους μέλους. Η χρήση, για παράδειγμα, διασφαλίσεων είναι προσαρμοσμένη στις κουλτούρες, τις δομές και την οργάνωση κάθε κράτους μέλους. Προκειμένου να καταστεί δυνατή η διαλειτουργικότητα, τα κράτη μέλη πρέπει να κατανοούν και να χρησιμοποιούν παρόμοιες διασφαλίσεις, σύμφωνα με το άρθρο 89 παράγραφος 1 του GDPR, για παράδειγμα τις ανάγκες για επιτροπές ή αρχές δεοντολογικού ελέγχου, ψευδωνυμοποιήσεις, και να εργαστούν για την αποδοχή των διασφαλίσεων άλλων κρατών μελών. Υπάρχει περαιτέρω ανάγκη να διασφαλιστεί ότι οι νόμοι περί απορρήτου ή άλλοι τέτοιοι νόμοι (π.χ. Νόμοι για την Προστασία Διαβαθμισμένων Πληροφοριών) τηρούνται για τους σκοπούς της διασυνοριακής ανταλλαγής δεδομένων. Τα νόμιμα συμφέροντα και τα προστατευόμενα δικαιώματα (προστασία του εμπορικού απορρήτου, δικαιώματα πνευματικής ιδιοκτησίας, διπλώματα ευρεσιτεχνίας, εμπορικά σήματα, σχέδια και γειτονικά δικαιώματα, γεωγραφικές ενδείξεις και δικαιώματα φυτικής ποικιλίας κ.λπ.) θα πρέπει επίσης να προστατεύονται πλήρως. Η Πολιτική 0070 του Ευρωπαϊκού οργανισμού Φαρμάκων (EMA) μπορεί να χρησιμεύσει ως πρότυπο για τη διατήρηση εμπορικών μυστικών και διπλώματα ευρεσιτεχνίας από τους κατόχους δεδομένων.
74 ΡΕΠΟΡΤΑΖ /
2023
Μάρτιος-Απρίλιος
Κοινή ερμηνεία της
ανωνυμοποίησης και της ψευδωνυμοποίησης
Η σύστασή μας προς τα κράτη μέλη κατά
τη σύνταξη εθνικής νομοθεσίας για δευτερογενή χρήση θα ήταν να ρυθμίσουν ή
να ορίσουν τι πρέπει να θεωρείται επαρκής ψευδωνυμοποίηση ή ανωνυμοποίηση.
Ο νόμος θα μπορούσε να κάνει αναφορά στην ανάγκη για μια τέτοια διασφάλιση και μάλλον να ορίζει μια αρχή ή άλλο τέτοιο όργανο να αποφασίζει και να εκδώσει τέτοιες κατευθυντήριες γραμμές. Δεδομένου του ότι η τεχνολογία είναι ένα ταχέως εξελισσόμενο θέμα και οι προηγμένες νέες τεχνικές εμφανίζονται πιο συχνά από ό,τι μπορεί να αλλάξει η νομοθεσία, είναι ευκολότερο να οριστούν αυτές οι πιο τεχνικές πτυχές σε κατευθυντήριες γραμμές. Στη συνέχεια, είναι επίσης ευκολότερο να προσπαθήσουμε να επιτύχουμε συναίνεση μεταξύ των κρατών μελών σχετικά με τις κατευθυντήριες γραμμές, οι οποίες μπορούν να χρησιμοποιηθούν σε όλα τα κράτη μέλη.
Ρύθμιση δευτερογενούς χρήσης
Η σύστασή μας προς τα κράτη μέλη θα ήταν να μη βασίζονται μόνο στις διαθέσιμες δυνατότητες, σύμφωνα με το άρθρο 5 παράγραφος 1 στοιχείο β) του GDPR για περαιτέρω επεξεργασία. Τα κράτη μέλη μπορούν και πρέπει, σε μεγαλύτερο βαθμό, να προσπαθήσουν να ρυθμίσουν ότι τα δεδομένα μπορούν να υποβάλλονται σε επεξεργασία για άλλους σκοπούς. Θα μπορούσε να γίνει περισσότερο σαφές αν μπορεί επίσης να γίνει επίκληση του άρθρου 5 παράγραφος 1 στοιχείο β) σε μεγαλύτερο βαθμό και υπό ποιες συνθήκες, αν το θέμα αντιμετωπιστεί από τις επερχόμενες κατευθυντήριες γραμμές
EDPB σχετικά με τη δευτερεύουσα χρήση για ερευνητικούς σκοπούς.

Η πρόταση της Επιτροπής για το EHDS είναι ένα βήμα προς αυτήν την κατεύθυνση, ρυθμίζοντας τη δυνατότητα για δευτερεύουσα χρήση μέσω της νομοθεσίας της ΕΕ. Ωστόσο, για το πλήρες δυναμικό μιας τέτοιας ρύθμισης υπάρχει ανάγκη να αντιμετωπιστούν οι δυνατότητες για διαφορετικούς εθνικούς κανονισμούς. Όπως έδειξε η έρευνα, αυτός είναι ένας από τους κύριους λόγους, εκτός από τους τεχνικούς και σημασιολογικούς, για τους οποίους δεν έχει ακόμη μπορέσει να αξιοποιηθεί
το πλήρες δυναμικό της διασυνοριακής κοινής χρήσης δεδομένων.
Περαιτέρω εναρμόνιση της εθνικής νομοθεσίας Οι συστάσεις μας προς τα κράτη μέλη κατά τον σχεδιασμό εθνικής νομοθεσίας για δευτερογενή χρήση δεδομένων υγείας θα ήταν πρώτα να διαπιστωθεί αν υπάρχουν εθνικές διατάξεις που έχουν εγκριθεί βάσει των δυνατοτήτων για παρεκκλίσεις που προβλέπονται από τον GDPR. Σε περίπτωση
που υπάρχουν τέτοιες παρεκκλίσεις, η σύστασή μας θα ήταν να εξετάσουν τα κράτη μέλη αν οι παρεκκλίσεις μπορούν να καταργηθούν. Δεύτερον, για τις διατάξεις του GDPR για τις οποίες απαιτείται εθνική νομοθεσία για να είναι αυτές εφαρμοστέες, τα κράτη μέλη θα πρέπει να προσπαθήσουν να καταλήξουν σε κοινή κατανόηση σχετικά με το τι συνιστά, για παράδειγμα, διασφαλίσεις σύμφωνα με το άρθρο 89 παράγραφος 1.
Τα κράτη μέλη θα πρέπει, στη συνέχεια, να εξετάσουν το ενδεχόμενο αναθεώρησης της εθνικής νομοθεσίας, ώστε να μπορούν να αναγνωρίζονται ισοδύναμες διασφαλίσεις σύμφωνα με την εθνική νομοθεσία άλλων κρατών μελών ως εγγυήσεις ισοδύναμες με τις εθνικές τους όταν η αίτηση προέρχεται από άλλη χώρα. Υπάρχουν επίσης πτυχές άλλων εθνικών νόμων που πρέπει να ληφθούν υπόψη σχετικά με τη διασυνοριακή ανταλλαγή δεδομένων υγείας. Μπορεί να υπάρχουν νόμοι που θα απαγορεύουν την εξαγωγή των δεδομένων εκτός χώρας, για παράδειγμα νομοθεσία ασφάλειας. Τα κράτη μέλη θα πρέπει επίσης να εξετάσουν το ενδεχόμενο αναθεώρησης αυτών.
διαφορετικά
διαφορετικούς φορείς, η ερμηνεία μπορεί ακόμη και να διαφέρει σε εθνικό επίπεδο.
75
Ένας νόμος, είτε εθνικός είτε ευρωπαϊκός, θα ερμηνεύεται
από
πεξεργασία από τον νόμο (άρθρο 4 παράγραφος 7 και 4 παράγραφος 8), αυτός
ο ορισμός θα πρέπει να είναι σύμφωνος με τις διατάξεις του υπεύθυνου επεξεργασίας και να συμμορφώνεται με τον GDPR.
Αντιμετώπιση της ασφάλειας
από την αρχή
Η σύστασή μας προς τα κράτη μέλη είναι ότι όλες οι πτυχές της ασφάλειας –κυβερνοασφάλεια, ασφάλεια πληροφοριών– θα πρέπει να συμπεριληφθούν σε πρώιμο στάδιο. Αυτό είναι ένα πολύ σημαντικό βήμα για την αποφυγή δυσκολιών υλοποίησης και εφαρμογής. Η ασφάλεια από τον σχεδιασμό θα πρέπει ήδη να λαμβάνεται υπόψη στις προπαρασκευαστικές εργασίες, που οδηγούν στη νομοθεσία για τη δευτερεύουσα χρήση.
Καλή επικοινωνία με το κοινό
Η σύστασή μας προς
τα κράτη μέλη είναι ότι όλες οι πτυχές της ασφάλειας –
κυβερνοασφάλεια, ασφάλεια πληροφοριών–
θα πρέπει να
συμπεριληφθούν σε πρώιμο στάδιο.
Επιλογή
νομικής βάσης Τα κράτη μέλη θα πρέπει να προσπαθήσουν όσο το δυνατόν περισσότερο και να απέχουν από το να βασίζονται στη συλλογή δεδομένων υγείας με βάση τη συναίνεση για πρωτογενή χρήση και σε μεγαλύτερο βαθμό να επιδιώκουν τη συλλογή και χρήση δεδομένων υγείας μέσω νομικής βάσης με τη μορφή δημόσιου συμφέροντος
ή νομικής υποχρέωσης. Αυτό θα επέτρεπε σε υψηλότερο επίπεδο τις δυνατότητες για δευτερογενή χρήση όταν χρειάζεται.
Να κατανοήσουν τις σχέσεις
ελεγκτή και επεξεργαστή
Τα κράτη μέλη πρέπει να διερευνήσουν
και να κατανοήσουν πλήρως τον τρόπο με τον οποίο συγκροτούνται οι αρμοδιότητες των υπευθύνων επεξεργασίας και των εκτελούντων την επεξεργασία εντός της υπάρχουσας υποδομής και του οργανισμού τους και το πού βρίσκονται αυτές οι αρμοδιότητες. Σε αυτόν τον τομέα πρέπει να δοθεί προτεραιότητα.
Τα κράτη μέλη θα πρέπει επίσης να προβούν σε διεξοδική ανάλυση του κατά πόσον η ανάγκη για τυχόν προτεινόμενες νέες δομές πηγάζει από την εθνική νομοθεσία ή από το δίκαιο της ΕΕ. Επίσης, θα πρέπει να γίνει ενεργοποίηση δευτερογενούς χρήσης στην πράξη, με αλλαγή των σχέσεων ελεγκτών και επεξεργαστών. Επιπλέον, θα πρέπει να εξετάσουν αν χρειάζεται να αποσαφηνιστούν οι ρόλοι τους στην εθνική νομοθεσία.
Ενώ ο GDPR επιτρέπει τον διορισμό υπευθύνου επεξεργασίας ή εκτελούντος την ε-

Η σύστασή μας προς τα κράτη μέλη βρίσκεται ήδη στο πλαίσιο των προπαρασκευαστικών εργασιών που οδηγούν στην εθνική νομοθεσία για τη δευτερογενή χρήση, ώστε να αντιμετωπίσουν την ανάγκη κατάρτισης ενός σχεδίου για τον τρόπο επικοινωνίας με το κοινό. Αυτό το σχέδιο θα πρέπει να τεθεί σε εφαρμογή το συντομότερο δυνατό και θα πρέπει να διατεθούν αρκετοί πόροι για την εφαρμογή του.
Εξασφάλιση αρκετών πόρων για την υλοποίηση
Η σύστασή μας προς τα κράτη μέλη είναι να διασφαλίσουν ότι οι προπαρασκευαστικές εργασίες που οδηγούν σε προτάσεις νόμου για τη δευτερεύουσα χρήση θα έχουν μια ενδελεχή ανάλυση των πόρων που απαιτούνται για την εφαρμογή του νόμου. Η ανάλυση δεν θα πρέπει να εξετάζει μόνο τους οικονομικούς πόρους που απαιτούνται για τη δημιουργία νέων λύσεων πληροφορικής.
Είναι σημαντικό να αναλυθούν διεξοδικά το ανθρώπινο δυναμικό που απαιτείται για τη λειτουργία των νέων δομών, φορέων και καθηκόντων. Θα πρέπει επίσης να αναλυθεί η ανάγκη για πρόσθετους πόρους για τους κατόχους δεδομένων, καθώς συχνά θα έχουν νέες απαιτήσεις προς συμμόρφωση.
Ενθαρρύνουμε σθεναρά την εκπόνηση πρακτικών και εύχρηστων κατευθυντήριων γραμμών, που εκπονούνται σε όλα τα κράτη μέλη, οι οποίες θα παρέχουν πιο συγκεκριμένα και ισχυρά στοιχεία, στα οποία θα βασίζεται η αξιολόγηση της ανωνυμοποίησης.•••
76 ΡΕΠΟΡΤΑΖ / Μάρτιος-Απρίλιος 2023
κατάλληλης





77 www.ethosmedia.eu info@ethosmedia.eu Ασφάλιση. Α πό το « A » ... Αποτελεσµατικά εργαλεία δουλειάς για τους επαγγελµατίες της ασφάλισης Πολύπλευρη ενηµέρωση από την αγορά Ανάλυση των εξελίξεων και τάσεων στον ασφαλιστικό κλάδο Εξειδικευµένο, πρωτότυπο και αποκλειστικό περιεχόµενο
Εξαιρετικά ανήσυχοι
Eξαιρετικά ανήσυχοι για την ασφάλεια των προσωπικών τους δεδομένων εμφανίζονται οι Έλληνες. Το 80% των χρηστών στην Ελλάδα δηλώνουν ότι προβληματίζονται ή ότι ανησυχούν αρκετά για την ασφάλεια της ψηφιακής τους ταυτότητας.
Ειδικότερα, οι μισοί χρήστες στην Ελλάδα (το 49%) απαντούν ότι ανησυχούν αρκετά, ενώ προβληματισμένο δηλώνει περίπου το ένα τρίτο (28%). Μόλις το 2% των πολιτών στην Ελλάδα απαντούν ότι δεν τους απασχολεί καθόλου το θέμα της ασφάλειας, ενώ ένα 8% απαντά «όχι και τόσο».
Μάλιστα, η Ελλάδα είναι 13η παγκοσμί-
ως στον βαθμό ανησυχίας για την ασφάλεια των data. Οι πλέον προβληματισμένοι

πολίτες για την ασφάλεια των δεδομένων τους είναι οι κάτοικοι του Χονγκ Κονγκ και οι πολίτες της Ισπανίας (σ.σ. το 84% απαντά ότι ανησυχεί από αρκετά έως πολύ για το θέμα αυτό).
Η Σιγκαπούρη (83%) και η Ινδία (81%) βρίσκονται επίσης ψηλά στην παγκόσμια κατάταξη των χωρών που έχουν τις μεγαλύτερες ανησυχίες για το θέμα των δεδομένων.
Στον αντίποδα, οι Σουηδοί, οι Γερμανοί και οι Δανοί (με 55%, 53% και 43%, αντίστοιχα) είναι οι λαοί που φαίνεται να δίνουν τη μικρότερη σημασία στην ασφάλεια των data.
78 / Μάρτιος-Απρίλιος 2023
οι Έλληνες
προσωπικά
13η η Ελλάδα παγκοσμίως στον βαθμό ανησυχίας για την ασφάλεια των data Οι πολίτες του Χονγκ Κονγκ και της Ισπανίας οι πλέον φοβικοί ΡΕΠΟΡΤΑΖ Ο φόβος
δεδομένων επηρεάζει σαφώς και τη συμπεριφορά των καταναλωτών.
για τα
δεδομένα
για μια πιθανή παραβίαση των
προσωπικών
Φοβούνται λιγότερο
οι νέοι
Οι νέοι στην Ελλάδα, όπως και διεθνώς, ανησυχούν λιγότερο για την προστασία των δεδομένων τους συγκριτικά με τα άτομα μεγαλύτερης ηλικίας. Προφανώς, λόγω της εξοικείωσής τους με το Διαδίκτυο, οι νεότεροι χρήστες δείχνουν πιο ατρόμητοι
όσον αφορά την ασφάλεια της ψηφιακής
τους ταυτότητας και την πιθανότητα παρα-
βίασης των προσωπικών τους δεδομένων.
Έτσι, ενώ το 57% των νέων ηλικίας 18 έως
24 ετών δηλώνουν ότι ανησυχούν πολύ ή
αρκετά για την ασφάλεια των δεδομένων
τους, στις ηλικίες άνω των 55 το ποσοστό
αυτό αυξάνεται στο 73%.
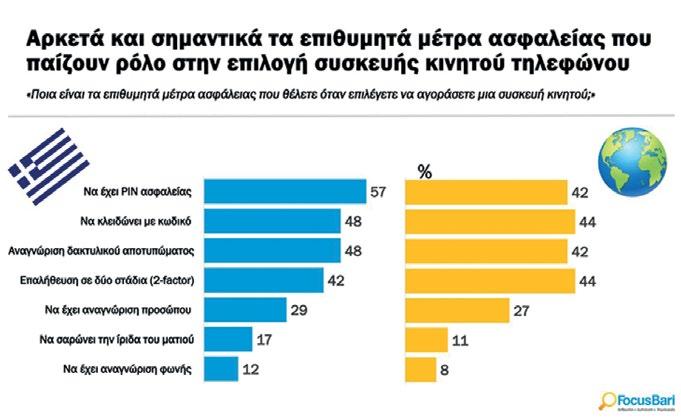

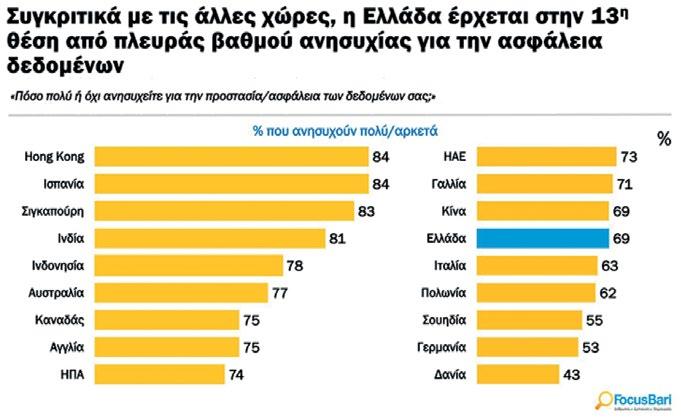
Αναζητούν ασφαλή smartphones
Ο φόβος για μια πιθανή παραβίαση των προσωπικών δεδομένων επηρεάζει σαφώς και τη συμπεριφορά των καταναλωτών όταν αγοράζουν ένα νέο smartphone, με τις απαιτήσεις ασφάλειας που παρέχει μια συσκευή να παίζουν κεντρικό ρόλο στην απόφαση αγοράς της. Στην ερώτηση έρευνας της Focus Bari «ποια είναι τα επιθυμητά μέτρα ασφάλειας που θέλετε όταν επιλέγετε μια συσκευή κινητού;» οι Έλληνες απαντούν: να έχει ΡΙΝ ασφαλείας (57%), να κλειδώνει με κωδικό (48%), να έχει αναγνώριση δακτυλικού αποτυπώματος (48%), να έχει δυνατότητα επαλήθευσης σε δύο στάδια (42%), να διαθέτει αναγνώριση προσώπου (29%), να σαρώνει την ίριδα του ματιού (17%) και να έχει αναγνώριση φωνής (12%).
Εμφανείς είναι οι διαφορές ανάμεσα στα άτομα μεγαλύτερης ηλικίας και στους νέους αναφορικά με τις δικλίδες ασφαλείας που προτιμούν για τη θωράκιση των
ψηφιακών τους δεδομένων. Σύμφωνα με
την ίδια έρευνα, οι νεαρές ηλικίες –και στην Ελλάδα και διεθνώς– προτιμούν περισσότερο την αναγνώριση προσώπου και τη σάρωση της ίριδας του ματιού από ό,τι οι μεγαλύτερες, ενώ οι μεγαλύτερες προτιμούν πιο πολύ τον «κλασικό» προσωπικό κωδικό.•••
Πηγή: ΣΕΠΕ
79




















www.ethosmedia.eu
Future health today









+30 216 2005600 Info@innovispharma.gr www.innovispharma.gr INV-I_AB01-0922 / # 035 / Ιανουάριος-Φεβρουάριος 2016 ISSN: 2241-0961