
15 minute read
Definizione, diagnosi e classificazione della miopia
è il principale indicatore di una futura miopia (3) anche se l’accuratezza di questo indicatore non è tale da giustificare interventi terapeutici Altri modelli predittivi (4) mettono in relazione la rifrazione con la profondità della camera anteriore, lo spessore del cristallino e la profondità della camera vitreale per prevedere la comparsa di miopia. Sarà necessario integrare molti più elementi per giungere a modelli di previsione della comparsa della miopia sufficientemente attendibili da giustificare terapie preventive e tra questi non si potranno ignorare il numero dei genitori miopi, il livello d’istruzione dei genitori, il tempo trascorso all’aperto, il tasso di allungamento del bulbo oculare, la frequenza delle variazioni della rifrazione e anche componenti genomiche
(5, 6, 7, 8) . Esiste un rapporto tra rifrazione in cicloplegia ed età che può indicare una maggiore probabilità di sviluppare miopia: – 6-7 anni / +0.75 – 7-8 anni / +0.50 – 9-10 anni / +0.25 – 11 anni / emmetropia.
Advertisement
La miopia patologica Anche se le modificazioni strutturali a carico del bulbo oculare dovute alla miopia sono più comuni nella miopia elevata, introdurre delle soglie sulla base dell’entità del difetto rifrattivo o della lunghezza assiale per identificare la miopia patologica non è opportuno per varie ragioni: – la maculopatia miopica è riscontrabile anche in soggetti con miopia bassa (9) . – lo stafiloma posteriore è rilevabile anche in occhi con lunghezza assiale inferiore a 26,5 mm (10) – studi longitudinali hanno messo in evidenza che la prevalenza della miopia patologica è più legata all’età che all’entità del difetto rifratti-
vo (11, 12) . Nel sistema classificativo ICD10 si trova il termine “miopia degenera-
ICD11 è stato inserito il termine “miopia elevata degenerativa”. Nell’ICD10-CM include cinque condizioni che sono classificate come suddivisioni della miopia degenerativa: neovascolarizzazione coroideale (CNV), foro maculare, distacco di retina, foveoschisi e altre maculopatie. Vi sono vari altri termini comunemente usati: degenerazione maculare miopica, maculopatia miopica, La patologia oculare miopica • Pasquale Troiano retinopatia miopica, atrofia corioretinica miopica, CNV miopica. Il Gruppo di Studio Internazionale per la Metanalisi della Miopia Patologica ha pubblicato (13) un sistema di classificazione e gradazione della maculopatia miopica basato su riferimenti fotografici. Questo sistema identifica 4 categorie di maculopatia miopica e tre tipi di lesioni aggiuntive (plus) possono essere presenti contemporaneamente alle lesioni previste nelle 4 categorie (fig. 1).
Figura 1. Categorie di maculopatia miopica con tasso di progressione e lesioni aggiuntive
tiva” e nel successivo aggiornamento ICD11 è stato inserito il termine “miopia elevata degenerativa”. L’ICD10-CM include cinque condizioni che sono classificate come suddivisioni della miopia degenerativa: neovascolarizzazione coroideale (CNV), foro maculare, distacco di retina, foveoschisi e altre maculopatie. Vi sono vari altri termini comunemente usati: degenerazione maculare miopica, maculopatia miopica, retinopatia miopica, atrofia corioretinica miopica, CNV miopica. Il Gruppo di Studio Internazionale per la Metanalisi della Miopia Patologica ha pubblicato (13) un sistema di classificazione e gradazione della maculopatia miopica basato su riferimenti fotografici.
Questo sistema identifica 4 categorie di maculopatia miopica e tre tipi di lesioni aggiuntive (plus) che possono essere presenti contemporaneamente alle lesioni previste nelle 4 categorie (fig. 1).
Categoria 1 = Fondo Tessellato
Il fondo tessellato (spesso descritto semplicemente “corioretinopatia miopica”) è dovuto all’assottigliamento dell’EPR e della coriocapillare conseguente all’allungamento assiale del bulbo oculare. La ridotta densità di pigmento rende visibile la vascolarizzazione coroideale. Un modesto grado di fondo tessellato si può riscontrare anche in un fondo normale con l’invecchiamento. Il fondo tessellato miopico è caratterizzato da vasi coroideali ben definiti e chiaramente visibili attorno alla fovea e in prossimità delle arcate vascolari. Nella fig. 2 vediamo delle fotografie standard del fondo tessellato. A sinistra come si presenta in un fondo molto pigmentato. In centro in un fondo poco pigmentato. A destra un fondo tassellato discutibile poiché i vasi coroideali sono ben definiti e chiaramente visibili in prossimità delle arcate ma non in tutta l’area maculare.
Categoria 2 = Atrofia corioretinica diffusa
Il polo posteriore si presenta di colorito bianco-giallastro. L’estensione dell’atrofia varia da un’area ristretta attorno alla papilla ottica e una parte della macula fino all’intero polo posteriore.
Fig. 1: categorie di maculopatia miopica con tasso di progressione e lesioni aggiuntive
Categoria 1 = Fondo Tessellato
Il fondo tessellato (spesso descritto semplicemente “corioretinopatia miopica”) è dovuto all’assottigliamento dell’EPR e della coriocapillare conseguente all’allungamento assiale del bulbo oculare. La ridotta densità di pigmento rende visibile la vascolarizzazione coroideale. Un modesto grado di fondo tessellato si può riscontrare anche in un fondo normale con l’invecchiamento. Il fondo tessellato miopico è caratterizzato da vasi coroideali ben definiti e chiaramente visibili attorno alla fovea e in prossimità delle arcate vascolari. Nella fig. 2 vediamo delle fotografie standard del fondo tessellato. A sinistra come si presenta in un fondo molto pigmentato. In centro in un fondo poco pigmentato. A destra un fondo tassellato discutibile poiché i vasi coroideali sono ben definiti e chiaramente visibili in prossimità delle arcate ma non in tutta l’area maculare.

Figura 2 fig. 2
Categoria 2 = Atrofia corioretinica diffusa
Il polo posteriore si presenta di colorito bianco-giallastro. L’estensione dell’atrofia varia da un’area ristretta attorno alla papilla ottica e una parte della macula fino all’intero polo posteriore. Nella figura 3 vediamo due fotografie standard di atrofia corioretinica diffusa con le frecce che la delimitano.

Figura 3 fig. 3
Nella figura 3 vediamo due fotografie standard di atrofia corioretinica diffusa con le frecce che la delimitano.
Categoria 3 = Atrofia corioretinica localizzata
Si presenta con lesioni giallo-grigiastre, ben definite, di dimensioni variabili, localizzate nell’area maculare o attorno alla papilla ottica. L’atrofia corioretinica localizzata è caratterizzata dalla perdita completa
Categoria 3 = Atrofia corioretinica localizzata
Si presenta con lesioni giallo-grigiastre, ben definite, di dimensioni variabili, localizzate nell’area maculare o attorno alla papilla ottica. L’atrofia corioretinica localizzata è caratterizzata dalla perdita completa della coriocapillare e può causare la perdita degli strati retinici esterni e dell’EPR. Sono identificabili tre tipi di atrofia corioretinica localizzata: uno che deriva dalle lacquer cracks, uno che si forma all’interno di un’area di grave atrofia corioretinica diffusa e uno che si sviluppa lunga il bordo di uno stafiloma. Nella figura 4 possiamo vedere delle fotografie standard di atrofia corioretinica localizzata. In alto a sinistra e a destra aree di atrofia corioretinica localizzata di dimensioni inferiori a 1 all’area del disco ottico (DA). In basso a sinistra atrofia corioretinica localizzata di oltre 9 DA con atrofia maculare. In basso a destra atrofia corioretinica localizzata di oltre 9 DA.

fig. 4 Figura 4
Categoria 4 = Atrofia Maculare
L’atrofia maculare è caratterizzata da lesione atrofica corioretinica, di forma circolare e di colore giallogrigiastro che si forma attorno a una membrana fibrovascolare regredita e che si allarga col tempo. L’atrofia maculare dev’essere distinta dall’atrofia corioretinica localizzata. L’atrofia maculare è centrata sulla fovea ed è rotondeggiante, mentre l’atro una forma irregolare. 96 fia corioretinica localizzata non è centrata sulla fovea ed ha Nella figura 5 possiamo vedere delle fotografie standard di atrofia maculare. 4
della coriocapillare e può causare la perdita degli strati retinici esterni e dell’EPR. Sono identificabili tre tipi di atrofia corioretinica localizzata: uno che deriva dalle lacquer cracks, uno che si forma all’interno di un’area di grave atrofia corioretinica diffusa e uno che si sviluppa lunga il bordo di uno stafiloma. Nella figura 4 possiamo vedere delle fotografie standard di atrofia corioretinica localizzata. In alto a sinistra e a destra aree di atrofia corioretinica localizzata di dimensioni inferiori a 1 area del disco ottico (DA). In basso a sinistra atrofia corioretinica localizzata di oltre 9 DA con atrofia maculare. In basso a destra atrofia corioretinica localizzata di oltre 9 DA.
Categoria 4 = Atrofia Maculare
L’atrofia maculare è caratterizzata da lesione atrofica corioretinica, di forma circolare e di colore giallo-grigiastro che si forma attorno a una membrana fibrovascolare regredita e che si allarga col tempo. L’atrofia maculare dev’essere distinta dall’atrofia corioretinica localizzata. L’atrofia maculare è centrata sulla fovea ed è rotondeggiante, mentre l’atrofia corioretinica localizzata non è centrata sulla fovea ed ha una forma irregolare. Nella figura 5 possiamo vedere delle fotografie standard di atrofia maculare.

Figura 5 fig. 5
Lacquer cracks
Le lacquer cracks sono delle rotture meccaniche della membrana di Bruch e si presentano come delle spesse line di colore giallastro nell’area maculare. In alcuni casi varie linee di frattura si incrociano tra loro al polo posteriore. Solitamente le rotture non corrono parallele ai sottostanti vasi coroideali ma spesso li incrociano. Quando si forma una nuova rottura si verifica un’emorragia nell’area maculare in assenza di una nota CNV.
Lacquer cracks
Le lacquer cracks sono delle rotture meccaniche della membrana di Bruch e si presentano come delle spesse line di colore giallastro nell’area maculare. In alcuni casi varie linee di frattura si incrociano tra loro al polo posteriore. Solitamente le rotture non corrono parallele ai sottostanti vasi coroideali ma spesso li incrociano. Quando si forma una nuova rottura si verifica un’emorragia nell’area maculare in assenza di una nota CNV. Nella figura 6 possiamo vedere delle fotografie standard di atrofia mafig. 5 culare. Le punte di freccia indicano le rotture mentre le frecce (nell’im Lacquer cracks magine di destra) indicano le emorragie che precedono la formazione Le lacquer cracks sono delle rotture meccaniche della membrana di Bruch e si presentano come delle spesse line di colore giallastro nell’area maculare. In alcuni casi varie linee di frattura si incrociano tra loro di una nuova rottura. al polo posteriore. Solitamente le rotture non corrono parallele ai sottostanti vasi coroideali ma spesso li incrociano. Quando si forma una nuova rottura si verifica un’emorragia nell’area maculare in assenza di una nota CNV. Nella figura 6 possiamo vedere delle fotografie standard di atrofia maculare. Le punte di freccia indicano le rotture mentre le frecce (nell’immagine di destra) indicano le emorragie che precedono la formazione di una nuova rottura.


fig. 6 Figura 6
Neovascolarizzazione coroideale miopica
La presenza di una CNV attiva è testimoniata da modificazioni essudative della retina localizzate nello spazio intraretinico, sottoretinico o attraverso l’epitelio pigmentato sottoretinico. Inoltre, può essere presente anche un distacco retinico sieroso. Nella figura 7 possiamo vedere una fotografia standard di CNV miopica attiva. 5
fig. 7 Figura 7

Macchia di Fuchs
La macchia di Fuchs rappresenta la fase cicatriziale di una CMV miopica. La lesione è asciutta e la membrana fibrovascolare si è ridotta e appiattita. Si presenta come una cicatrice grigiastra o pigmentata. Nella figura 8 possiamo vedere una fotografia standard di alcune forme di macchia di Fuchs. 6
Neovascolarizzazione coroideale miopica
La presenza di una CNV attiva è testimoniata da modificazioni essudative della retina localizzate nello spazio intraretinico, sottoretinico o attraverso l’epitelio pigmentato sottoretinico. Inoltre, può essere presente anche un distacco retinico sieroso. Nella figura 7 possiamo vedere una fotografia standard di CNV miopica attiva.
Macchia di Fuchs
La macchia di Fuchs rappresenta la fase cicatriziale di una CNV miopica. La lesione è asciutta e la membrana fibrovascolare si è ridotta e appiattita. Si presenta come una cicatrice grigiastra o pigmentata. Nella figura 8 possiamo vedere una fotografia standard di alcune forme di macchia di Fuchs.

Stafiloma posteriore miopico
Lo stafiloma posteriore è una estroflessione della sclera localizzata al polo posteriore. La classificazione di riferimento dello stafiloma miopico è quella di Curtin (15). Questa classificazione però non è di facile utilizzo ed è stata semplificata in base alla dimensione e alla sede: - coinvolgente la macula: grande, piccolo, inferiore - non coinvolgente la macula: peripapillare, nasale, inferiore - altri.
fig. 7
Macchia di Fuchs
La macchia di Fuchs rappresenta la fase cicatriziale di una CMV miopica. La lesione è asciutta e la membrana fibrovascolare si è ridotta e appiattita. Si presenta come una cicatrice grigiastra o pigmentata. Nella figura 8 possiamo vedere una fotografia standard di alcune forme di macchia di Fuchs.

Figura 8
Stafiloma posteriore miopico
Lo stafiloma posteriore è una estroflessione della sclera localizzata al polo posteriore. 99 La classificazione di riferimento dello stafiloma miopico è quella di Curtin (15). Questa classificazione però non è di facile utilizzo ed è stata semplificata in base alla dimensione e alla sede: - coinvolgente la macula: grande, piccolo, inferiore non coinvolgente la macula: peripapillare, nasale, inferiore

fig. 8 fig. 8 Nella figura 9Figura 9 possiamo vedere fotografie standard di altri sottotipi di stafiloma miopico: da sinistra nasale, inferiore non coinvolgente la macula, inferiore coinvolgente la macula. Nella figura 9 possiamo vedere fotografie standard di altri sottotipi di stafiloma miopico: da sinistra nasale, inferiore non coinvolgente la macula, inferiore coinvolgente la macula.
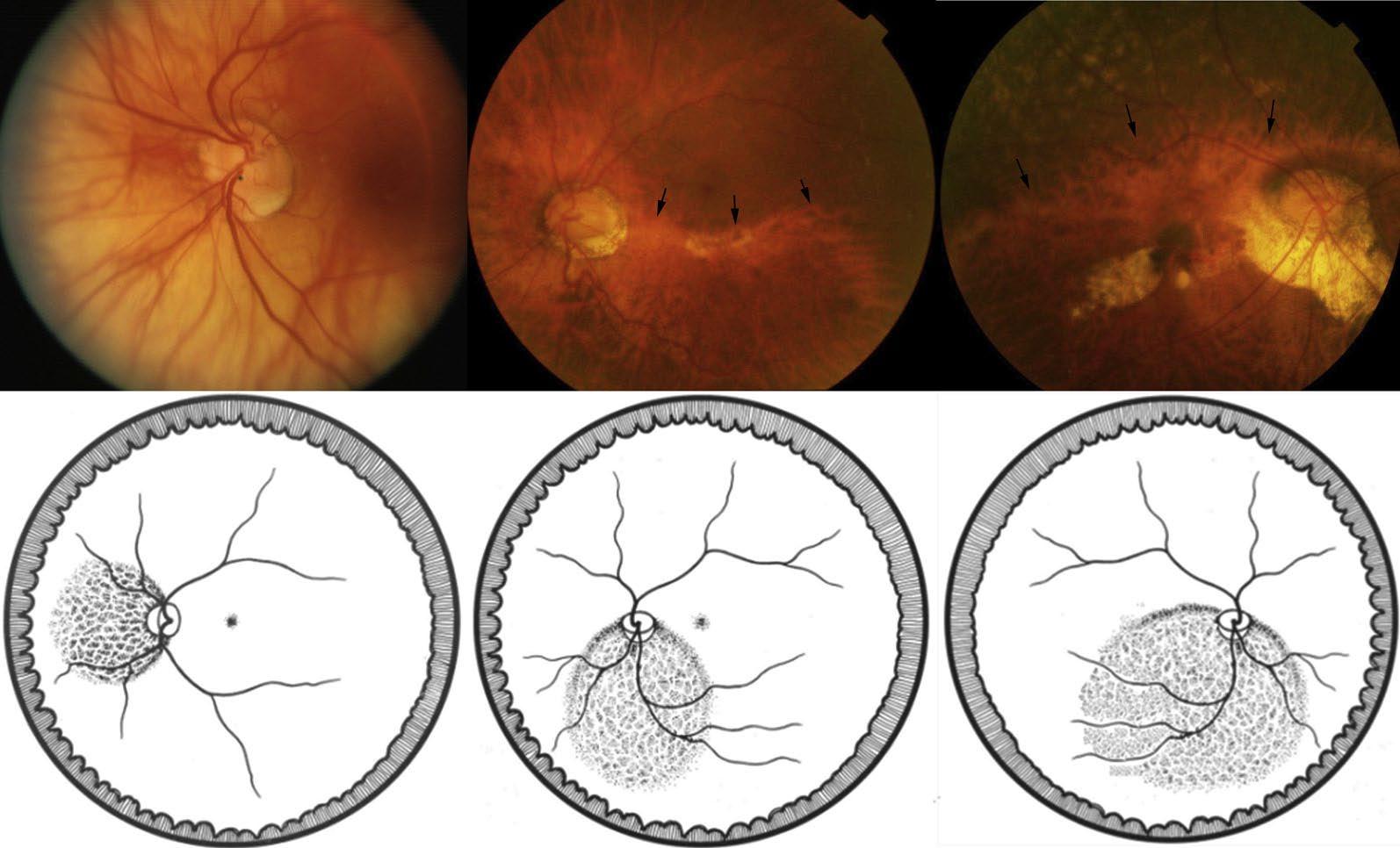
fig. 9 Figura 10 fig. 9
Nella figura 9 possiamo vedere fotografie standard di alcuni sottotipi di stafiloma miopico: da sinistra maculare grande, maculare piccolo, peripapillare. Nella figura 10 possiamo vedere fotografie standard di altri sottotipi di stafiloma miopico: da sinistra nasale, inferiore non coinvolgente la macula, inferiore coinvolgente la macula.
Bibliografia
1) Flitcroft DI, He M, Jonas JB, et al. IMI – Defining and classifying myopia: a proposed set of standards for clinical and epidemiologic studies. Invest Ophthalmol Vis Sci. 2019;60:M20–M30. https://doi.org/ 10.1167/iovs.18-25957 2) Mutti DO, Hayes JR, Mitchell GL, et al. Refractive error, axial length, and relative peripheral refractive error before and after the onset of myopia. Invest Ophthalmol
Vis Sci. 2007;48:2510–2519. 3) Zadnik K, Sinnott LT, Cotter SA, et al. Prediction of juvenile onset myopia. JAMA
Ophthalmol. 2015;133:683–689. 4) Zhang M, Gazzard G, Fu Z, et al. Validating the accuracy of a model to predict the onset of myopia in children. Invest Ophthalmol Vis Sci. 2011;52:5836–5841 5) Jones-Jordan LA, Sinnott LT, Manny RE, et al. Early childhood refractive error and parental history of myopia as predictors of myopia. Invest Ophthalmol Vis Sci. 2010;51:115–121. 6) French AN, Morgan IG, Mitchell P, Rose KA. Risk factors for incident myopia in Australian schoolchildren: the Sydney Adolescent Vascular and Eye Study. Ophthalmology. 2013;120:2100–2108. 7) O’Donoghue L, Kapetanankis W, McClelland JF, et al. Risk factors for childhood myopia: findings from the NICER Study. Invest Ophthalmol Vis Sci. 2015;56:1524–1530. 8) Tedja MS, Wojciechowski R, Hysi PG, et al. Genome-wide association meta-analysis highlights light-induced signaling as a driver for refractive error. Nat Genet. 2018;50:834–848. 9) Vongphanit J, Mitchell P, Wang JJ. Prevalence and progression of myopic retinopathy in an older population. Ophthalmology 2002;109:704–711.
10) Wang NK, Wu YM, Wang JP, et al. Clinical characteristics of posterior staphylomas in myopic eyes with axial length shorter than 26.5 millimeters. Am J Ophthalmol. 2016;162:180–190. 11) Fang Y, Yokoi T, Nagaoka N, et al. Progression of myopic maculopathy during 18year follow-up. Ophthalmology. 2018;125:863–877. 12) Hayash K, Ohno-Matsui K, Shimada N, et al. Long-term pattern of progression of myopic maculopathy: a natural history study. Ophthalmology. 2010;117:1595–1611. 13) Ohno-Matsui K, Kawasaki R, Jonas JB, et al. International photographic classification and grading system for myopic maculopathy. Am J Ophthalmol. 2015;159:877–883. 14) Ruiz-Moreno JM, Arias L, Montero JA, Carneiro A, Silva R. Intravitreal anti-VEGF therapy for choroidal neovascularization secondary to pathological myopia: 4-year outcome. Br J Ophthalmol 2013;97(11):1447–1450. 15) Curtin BJ. The posterior staphyloma of pathologic myopia. Trans Am Ophthalmol
Soc 1977;75:67–86. 16) Ward DM. The heavy eye phenomenon. Trans Ophthalmol Soc U K. 1967; 87():71726.
Forme particolari di miopia
Pasquale Troiano
Alcune condizioni oculari possono determinare uno spostamento miopico della rifrazione senza un aumento della lunghezza assiale del bulbo oculare. Tra queste ricordiamo la miopia da curvatura, la miopia d’indice e la miopia traumatica.
Miopia da curvatura
Può essere dovuta ad alterazioni patologiche della curvatura della cornea o del cristallino. Il cheratocono è la causa classica di miopia da curvatura. La conizzazione della cornea produce un “allungamento” anteriore del bulbo oculare che, insieme all’astigmatismo irregolare, induce miopia. Di maggiore impatto nella realtà clinica sono le variazioni della curvatura corneale da ectasia dopo LASIK che può determinare una miopizzazione oltre 2 diottrie associata ad astigmatismo irregolare. L’aumento della curvatura lenticolare può avere varia eziologia. Una miopia permanente si osserva per l’aumento della curvatura dell’intero cristallino o solo dei sui poli. L’aumento complessivo della curvatura lenticolare si osserva nella microfachia dove il cristallino è molto piccolo e assume un aspetto sferico (sferofachia). Questa condizione caratterizza le sindromi di Marfan e Marchesani - malattie congenite del tessuto connettivo che, nono-
stante producano quadri clinici sistemici profondamente diversi, sono caratterizzate dalle stesse manifestazioni oculari - ed è responsabile di miopia elevata cui si associa l’ectopia lentis con la miopia elevata rilevabile nella porzione fachica del forame pupillare. Il lenticono, anteriore e posteriore, è caratterizzato da un anomalo accrescimento localizzato della capsula e della corticale lenticolare polare. Il lenticono anteriore bilaterale è più spesso una condizione acquisita che entra a far parte di quadri sindromici come la sindrome di Alport. La sindrome di Alport è un disordine primario della membrana basale dovuto alla mutazione dei geni che codificano il collagene di tipo IV. Le membrane basali sono assemblate attraverso l’interazione del collagene IV con le laminine e i proteoglicani solfati, la capsula lenticolare è una membrana basale. La sindrome di Alport è caratterizzata da insufficienza renale progressiva, sordità neurosensoriale, retinopatia, lenticono anteriore e – più raramente - posteriore, distrofia corneale polimorfa posteriore. Il lenticono anteriore progredisce verso l’opacità. Molto raramente ci può essere la presenza contemporanea di lenticono anteriore e posteriore. Il lenticono posteriore è più spesso una pura anomalia oftalmica di natura congenita. Il lenticono posteriore sporadico è solitamente monolaterale e per questo, oltre che per il fatto di essere congenito, è fortemente ambliopizzante. Le rare forme bilaterali riconoscono una trasmissione autosomica dominante. In considerazione anche dell’evoluzione del lenticono posteriore verso l’opacamento il trattamento dovrà prevedere la rimozione del cristallino. La chirurgia del cristallino in presenza di lenticono è una chirurgia ad alto rischio per l’estrema fragilità della capsula. Spesso risulta molto complesso eseguire una capsuloressi curvilinea continua centrale per






