






El átomo consta de un núcleo con carga positiva, rodeado de cierto número de partículas cargadas negativamente, llamadas electrones, de tal modo que, en conjunto, el átomo resulta eléctricamente neutro. Los núcleos atómicos están construidos a base de dos partículas fundamentales, protón y neutrón, que se designan frecuentemente con el nombre genérico de nucleón. El protón transporta una unidad de carga positiva, igual en magnitud a la carga electrónica. Se identifica, en realidad, con el núcleo del átomo de hidrógeno, es decir, un átomo de hidrógeno que ha perdido su único electrón. El neutrón es ligerísimamente más pesado que el protón, y como su nombre indica, se trata de una partícula neutra que no transporta carga eléctrica. Con excepción de los del hidrógeno ordinario, todos los núcleos contienen, además de protones, uno o más neutrones.
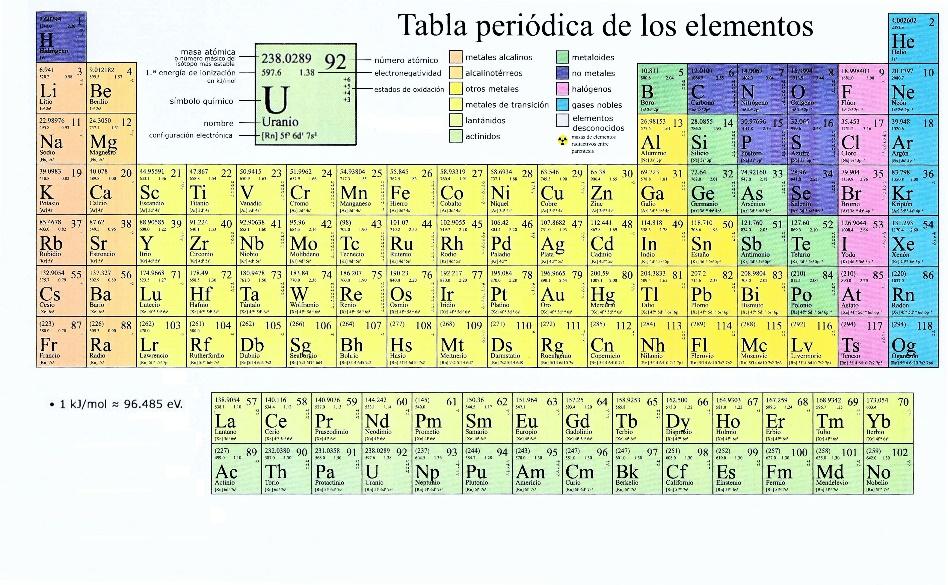
Para un elemento determinado, el número de protones existentes en el núcleo atómico, que es igual al número de cargas positivas que transporta, recibe el nombre de número atómico del elemento, y se representa generalmente por la letra Z. Es idéntico al número de orden del elemento en la tabla periódica de los elementos químicos. Así, pues, el número atómico del hidrógeno es 1, el del helio 2, el del litio 3, y así sucesivamente, hasta llegar al número 92 correspondiente al uranio, que es el elemento de masa atómica más elevada, entre todos los existentes en la naturaleza en cantidad apreciable. Cierto número de elementos más pesados que el uranio han sido preparados artificialmente; de estos, el plutonio (número atómico 94) tiene gran importancia en la producción de energía nuclear.
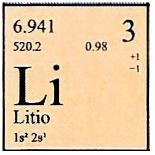



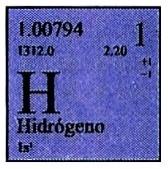
El número total de nucleones (protones y neutrones) existentes en el núcleo atómico recibe el nombre de número másico del elemento y se representa por la letra A. Como Z es el número de protones, el número de neutrones contenidos en el núcleo atómico vendrá representado por A Z. Por otra parte, como las masas del protón y del neutrón poseen ambos valores muy próximos a la unidad en la escala de masas atómicas, resulta evidente que el número másico es el número entero más próximo a la masa atómica de la especie considerada.
Lo que determina la naturaleza química de un elemento es su número atómico, es decir, el número de protones existentes en el núcleo. Esto se debe a que las propiedades químicas dependen de los electrones orbitales en torno del núcleo, y el número de estos es necesariamente igual al número de protones, ya que el átomo es una entidad eléctricamente neutra. En consecuencia, átomos cuyos núcleos contienen el mismo número de protones (igual número atómico), pero que difieren en número másico, son, desde el punto de vista químico, esencialmente idénticos, si bien presentan con frecuencia marcadas diferencias en sus características nucleares. Tales especies, con idéntico número atómico y diferente número másico, reciben el nombre de isótopos. Las especies isotópicas son, en general, químicamente indistinguibles, pero poseen masa atómica diferente. Para identificar cada uno de los isótopos de un elemento determinado, se escribe el número másico a continuación del nombre o símbolo del elemento. Así, por ejemplo, el isótopo más abundante del oxígeno, de número másico 16 (núcleo con 8 neutrones y 8 protones), se representa de una de estas formas: oxígeno-16, 0-16 u O18. Es conveniente a veces, aunque no necesario, indicar también el número atómico; esto se hace incorporándolo al símbolo del elemento como subíndice, por ejemplo, 8O16 El elemento oxígeno, que hasta 1962 se utilizó como patrón de la escala de masas atómicas, se presenta en la naturaleza como mezcla de tres isótopos, O16, 0IT y O18, los dos últimos en proporciones relativamente pequeñas. Esta situación originó que se establecieran dos sistemas diferentes para representar las masas atómicas. En la escala química de masas atómicas, se asignó el valor exacto 16,00000 a la masa media (ponderada) de los átomos de los tres isótopos del oxígeno, en las proporciones existentes en la atmósfera. En cambio, otra escala de masas alrededor del 0,028 por ciento más altas que las correspondientes masas atómicas en la escala química. Desde el 1 de enero de 1962, todas las masas atómicas deberán expresarse en una escala unificada, en la que se asigna el valor exacto 12,00000 al isótopo más abundante del carbono, C12. Esto significa una disminución de 37 partes por millón de las masas atómicas en la escala química y de 318 partes por millón de las masas atómicas en la escala física, ambas anteriormente en uso. Ahora bien, como los nuevos valores tardarán algunos años en introducirse definitivamente en la literatura científica, todas las masas atómicas que se citan en este libro se basan en la antigua escala física (oxígeno-16), atómicas, la llamada escala física, adoptó como base la asignación de una masa exacta de 16,00000 al isótopo oxígeno-16. Las masas atómicas en esta última escala son, por consiguiente,




En física nuclear y disciplinas afines, las masas de los átomos, núcleos y partículas se han expresado invariablemente en la llamada escala física. La unidad de masa atómica (uma) se define, pues, como la dieciseisava parte de la masa del átomo O16 exactamente*. En función de una unidad más práctica, 1 uma puede representarse por 1/Na gramos, siendo Na el número de Avogadro, que es el número de átomos individuales existentes en 16,00000 gramos del isótopo O18 (1 átomo-gramo), a saber, 0,6025 X 1024. De aquí se deduce que 1 uma es equivalente a 1,660 X 10-24 gramos. La masa del protón es 1,007596 una, o sea, 1,6725 X 10-24 gramos, mientras que la del neutrón vale 1,008986 uma, es decir, 1,674 X 10-24 gramos. La masa del electrón es solamente 0,000549 uma, o sea, 9,11 X 10-28 gramos, lo cual indica que casi toda la masa de un átomo se debe a los protones y neutrones existentes en el núcleo. En la actualidad, el uranio es el elemento más importante para la producción de energía nuclear por fisión. Existe en la naturaleza, por lo menos, en tres formas isotópicas, de números másicos 234, 235 y 238. Las proporciones de estos isótopos en el uranio natural, juntamente con sus respectivas masas atómicas, figuran en la Tabla 1.1. Como se ve, el uranio 238 es con mucho el isótopo más abundante, mientras que el uranio 235 está presente en proporción ligeramente superior al 0,7 %. Ambos isótopos tienen un papel importante en la producción de energía nuclear, si bien, como se verá oportunamente, es en realidad el uranio 235 el isótopo directamente utilizable para la liberación de energía de fisión. En cuanto al isótopo más ligero de los tres que figuran en la tabla, uranio 234, se presenta en proporciones tan pequeñas en los minerales uraníferos, que puede ignorarse totalmente a efectos prácticos. Otro elemento importante desde el punto de vista de la energía nuclear es el torio, de número atómico 90. Se presenta en la naturaleza casi exclusivamente con una sola especie nuclear, de número másico 232. Existen indicios de otras formas isotópicas, pero sus proporciones son despreciables.
 OXÍGENO 16 COMPOSICIÓN ISOTÓPICA DEL URANIO NATURAL TORIO 90
OXÍGENO 16 COMPOSICIÓN ISOTÓPICA DEL URANIO NATURAL TORIO 90
La determinación directa de masas nucleares o isotópicas por espectrografía de masas y otros procedimientos, ha demostrado que la masa real de un núcleo es siempre inferior a la suma de masas de los nucleones constituyentes. Esta diferencia, que recibe el nombre de defecto másico, guarda estrecha relación con la energía que mantiene ligadas las partículas en el interior del núcleo, y puede determinarse del modo siguiente. Como el átomo es eléctricamente neutro, debe contener Z electrones exteriores al núcleo, además de los Z protones y A Z neutrones existentes en el interior del mismo. Si representamos por mp, mn y me las masas del protón, del neutrón y del electrón, respectivamente, la suma de masas de los constituyentes de un átomo será Zmp + Zme + (A Z) mn. Siendo M la masa observada (isotópica) del átomo, se obtiene para el defecto másico la siguiente expresión:
Defecto másico = [Z (mp + me) + (A Z) mn] M
= Z mH +(A Z) mn - M (1.1) en la que se ha sustituido mp + me por mH, masa del átomo de hidrógeno. Como mH y mn se conocen con gran precisión, a saber, 1,008145 y 1,008986 uma, respectivamente, resulta que puede calcularse el defecto másico de cualquier especie nuclear o núclido siempre que se conozca su masa isotópica determinada experimentalmente.
Según el concepto de equivalencias entre masa y energía, consecuencia de la teoría de la relatividad especial, el defecto másico es una medida de la energía que se pondría en libertad si los Z protones y los A Z neutrones individuales se combinaran entre sí para formar un núcleo*. Recíprocamente, el defecto másico es numéricamente igual a la energía que sería necesario suministrar al núcleo para romperle en sus nucleones constituyentes. Por esta razón, la energía equivalente al defecto másico recibe el nombre de energía de enlace del núcleo.
Si m es la pérdida de masa en un proceso determinado, la cantidad equivalente de energía puesta en libertad, E, viene dada por la ecuación de Einstein, E = mc2 (1.2)
siendo c la velocidad de la luz. En el sistema absoluto de unidades, c = 2,998 X 1010 cm/s, de modo que la energía vendrá expresada por E (ergios) = m (gramos) x (2,998x1010)2 = m(gramos) x (8,990 x 1020 ) (1.3)
* Los Z electrones contribuyen con una pequeña cantidad a la energía de enlace, pero esta contribución ha sido tenida en cuenta, prácticamente, al sustituir mp, por mH en la ecuación (1.1).
En física nuclear se ha generalizado el uso del electrón-voltio (eV) como unidad de energía; es la energía que adquiere la unidad de carga (electrón) cuando se acelera con el potencial de 1 voltio.
La carga electrónica vale 1,602 X 10-19 culombios, así que 1 eV es equivalente a 1,602 X 10-19 julios, o bien, a 1.602 X 10-12 ergios; 1 millón de electrón-voltios (1 MeV) es equivalente a 1,602 X 10-6 ergios, de suerte que la ecuación (1.3) se transforma en
E (MeV) = m (gramos) X 5,614 X 1026
Finalmente, para expresar la diferencia de masas m en uma, basta multiplicar el segundo miembro de esta última ecuación por 1,660 X 10-24 gramos (1 uma) obteniéndose:
E (MeV) = 931 m (uma) (1.4)
Así pues, de acuerdo con la ecuación (1.4), para obtener el valor numérico de la energía de enlace nuclear, en MeV, basta con multiplicar por 931 el defecto másico, expresado en uma. Más importante que la energía de enlace total (E.E.) es la energía media de enlace por nucleón, que se obtiene dividiendo la primera por el número total de nucleones, es decir, por el número másico A; de las ecuaciones (1.1) y (1.4) se deduce:
EE /A = 931/A [ 1,008145Z + 1,00898(A Z) M].
En consecuencia, puede calcularse la energía media de enlace por nucleón, en cualquier núcleo, siempre que se conozca su masa isotópica (atómica) M.
Determinar la energía de enlace por nucleón en: a) estaño-120, para el cual M= 119,9401 uma, y b) uranio-235.
El número atómico del estaño es 50; por consiguiente, para el núclido de número másico 120, se obtiene: B.E./ A =931/120[(1,00814 X 50) + (1,00898 X 70)- 119.9401] = 8,50 MeV por nucleón.
El número atómico del uranio es 92; la masa isotópica del uranio-235, que figura en la tabla 1.1, es 235,1175; por consiguiente, B.E./ A =931/120[(1,00814 X 50) + (1.00898 X 143) - 235.1175) = 7,59 MeV por nucleón.
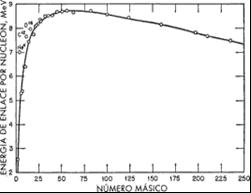
Se han representado en la figura 1.1 valores de la energía de enlace por nucleón en diversos núcleos, calculados en la forma que acabamos de describir, en función del número másico. La mayoría de los puntos se distribuyen sobre una curva única, o están muy próximos a ella. Esta curva muestra que, para núcleos de número másico pequeño, la energía de enlace por nucleón es relativamente baja; aumenta con el número másico, hasta alcanzar un amplio máximo alrededor de los 8 MeV, en la zona de masas comprendida más o menos entre 50 y 75; a partir de aquí, la energía de enlace por nucleón disminuye de modo constante. Se demuestra con facilidad que todo proceso en el cual uno o varios núcleos de energía de enlace por nucleón pequeña, es decir, menos estables, se convierten en otros de energía de enlace por nucleón mayor, esto es, más estables, debe ir acompañado de una cierta liberación de energía. Por consiguiente, resulta claro de la figura 1.1 que debe obtenerse energía por combinación (fusión) de los núcleos más ligeros, o por ruptura (fisión) de los núcleos de número másico más elevado.
Fig. 1.1. Variación de la energía de enlace por nucleón con el número másico
La figura 1.2 es una representación del número de neutrones existentes en cada uno de los 270 núcleos estables conocidos, en función del correspondiente número de protones. Se ha representado también la recta diagonal, sobre la que se sitúan los núcleos con igual número de neutrones y protones. Como se ve, en la mayoría de los núcleos estables de número másico pequeño, hasta 40, los números de neutrones y protones son iguales o muy aproximadamente iguales. Dicho de otro modo, la relación neutrón/protón es exactamente la unidad o ligerísimamente superior. En cambio, para valores crecientes del número másico o atómico un núcleo es estable cuando contiene mayor número de neutrones que de protones. Así, vemos que, en los núcleos estables más pesados, de número atómico superior a 80, la relación neutrón/protón ha subido hasta 1,5.
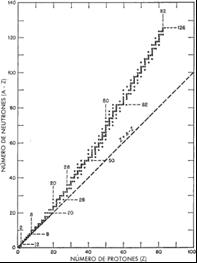
Antes de intentar la interpretación de los resultados anteriores, conviene destacar que ciertos núcleos muestran una estabilidad excepcional. Son aquéllos que contienen los denominados números mágicos de protones (2, 8, 20, 50, 82) o de neutrones (2, 8, 20, 50, 82, 126), indicados en la figura 1.2 por líneas de puntos. Los núcleos que poseen número mágico tanto de protones como de neutrones, se dice que son “doblemente mágicos”; ejemplos de esta clase son 8O16, 20Ca40 y 82Pb208. Un ejemplo muy ilustrativo de la estabilidad asociada a los números mágicos lo constituye el estaño, cuyo núcleo contiene 50 protones, del cual existen hasta 10 formas isotópicas estables. En general, como se deduce de la figura 1.2, los núclidos mágicos son bastante frecuentes en la naturaleza.
La especial estabilidad de los núcleos mágicos se atribuye a la presencia de capas completas o cerradas de neutrones, de protones o de ambos. Análogamente a lo que ocurre con los elementos inertes helio, neón, argón, etc., los cuales poseen capas cerradas de electrones que les confieren gran estabilidad química, así también las especies nucleares con números mágicos de neutrones o protones muestran una estabilidad nuclear excepcional. Además de los números mágicos que representan capas principales completas, hay también números semi mágicos, tales como 6, 14 y 28, que corresponden a una o varias capas cerradas más una subcapa completa. Están comprendidos en esta categoría los isótopos de los elementos carbono y silicio, tan abundantes en la naturaleza. Prescindiendo de detalles relacionados con los números mágicos, puede justificarse el carácter general de la figura 1.2 admitiendo la existencia de dos tipos de fuerzas intranucleares. Están en primer lugar las fuerzas atractivas entre nucleones, todas ellas del mismo orden de magnitud, es decir, protones atraen a otros protones, neutrones atraen a neutrones y protones atraen a neutrones, más o menos en la misma cuantía. Son estas fuerzas característicamente intranucleares, que solamente actúan a distancias muy cortas, del orden de 10-13 cm. Como consecuencia de su corto alcance, la fuerza atractiva total es proporcional en primera aproximación al número de nucleones existentes en el núcleo. Esta es la causa fundamental de que se mantenga constante la energía de enlace por nucleón, en un amplio intervalo de números másicos (fig. 1.1). Además de las fuerzas de corto enlace (atractivas), existen también fuerzas repulsivas, de carácter electrostático (culombianas), que se ejercen entre los protones cargados positivamente, y que son capaces de actuar a distancias relativamente grandes. La fuerza total de repulsión electrostática entre todos los protones existentes en el núcleo es proporcional al cuadrado del número de estos, es decir, a Z2. Se ejercen entre los nucleones otras fuerzas de carácter repulsivo, pero no tienen mayor importancia en el problema que ahora nos ocupa.
ig. 1.2. Número de neutrones y protones existentes en los núcleos estables. (Las líneas de trazos cortos indican los números mágicos de neutrones y protones)
Tratándose de núcleos de número atómico y másico pequeño, la fuerza repulsiva entre protones es también pequeña. De aquí que, al ser más o menos iguales las fuerzas protón-protón, neutrón-neutrón y protón-neutrón, sean de esperar valores próximos a la unidad para la relación neutrón/protón, como condición de estabilidad. Ahora bien, al ir aumentando el número atómico, se va haciendo cada vez mayor la repulsión electrostática entre protones, que es proporcional a Z2. Para mantenerse estables, los núcleos deben, pues, contener una mayor proporción de neutrones, con el fin de que las fuerzas atractivas neutrón-neutrón y neutrón-protón puedan compensar las fuerzas de repulsión entre protones, rápidamente crecientes. Hay un límite, sin embargo, al exceso de neutrones sobre protones que un núcleo puede contener, manteniéndose estable. Como consecuencia de este límite, los elementos de número atómico superior a 84 no poseen isótopos estables; cierto que existen en la naturaleza los elementos comprendidos entre el 84 (polonio) y 92 (uranio), pero se trata de isótopos inestables, que presentan el fenómeno conocido con el nombre de radioactividad.
Los núclidos radioactivos se desintegran espontáneamente con una velocidad determinada, que depende de la naturaleza del núclido. El núcleo inestable emite una partícula (o radiación) característica, transformándose de este modo en un núcleo diferente, que también puede ser o no radioactivo. Los núclidos cuya inestabilidad se debe al elevado valor de su número másico, o bien emiten partículas alfa cargadas positivamente, que son idénticas a los núcleos de helio y constan de dos protones y dos neutrones, o bien emiten partículas beta negativas, idénticas a los electrones ordinarios. El núcleo en sí, no contiene electrones, de suerte que, en la desintegración beta, el electrón procede de la conversión espontánea de un neutrón en un protón, según el esquema siguiente: Neutrón → Protón + Electrón (partícula beta) +
La partícula supletoria, neutra, de masa prácticamente nula, llamada neutrino se lleva parte de la energía liberada en la transformación radioactiva.
Se deduce de las anteriores consideraciones que el núcleo resultante o hijo de una desintegración alfa tiene dos protones y dos neutrones menos que el núcleo progenitor, de suerte que su número másico es inferior en cuatro unidades. En cambio, en la desintegración beta, el núcleo resultante tiene un neutrón menos y un protón más que su progenitor, quedando, pues, inalterado el número másico.
En núcleos de número atómico no muy alto, la radioactividad puede proceder de otra causa. Como se aprecia en la figura 1.2, los puntos que representan núcleos estables están comprendidos entre límites estrechos de la relación neutrón/protón. Todo núclido cuya composición cae fuera de este intervalo. es radioactivo. Si el núcleo está por encima del intervalo de estabilidad, es decir, contiene más neutrones de los que corresponden a su número atómico para ser estable, entonces presenta radioactividad beta, similar a la descrita anteriormente. Un neutrón es reemplazado en el núcleo por un protón, y de este modo la relación neutrón/protón disminuye; el núcleo hijo será siempre más estable que su progenitor, aunque no necesariamente totalmente estable.
En el caso de que un núclido contenga insuficiente número de neutrones para formar un núcleo estable con un determinado número de protones, cabe la posibilidad de que se convierta en un núcleo más estable por emisión de una partícula alfa, puesto que ello implica un incremento de la relación neutrón/ protón. Esta transformación, sin embargo, casi nunca tiene lugar en núclidos inestables de número másico intermedio o bajo; con muy pocas excepciones, la desintegración alfa se observa únicamente en los núclidos más pesados. Otra posibilidad es que el núcleo capture un electrón orbital,' que luego se combina con un protón para formar un neutrón (más un neutrino); el resultado neto es asimismo un aumento de la relación neutrón/protón. Sin embargo, lo más frecuente es que se produzca una desintegración beta positiva, es decir, la emisión de un electrón positivo positrón como resultado de la transformación:
Aunque se conocen numerosas especies radioactivas que muestran actividad beta positiva, ninguna de ellas aparece en el funcionamiento de los reactores nucleares.
En la mayoría de los casos, aunque no siempre, la desintegración radioactiva viene asociada con la emisión de rayos gamma, acompañado de la emisión de una partícula alfa o beta. Los rayos gamma son radiaciones electromagnéticas penetrantes, de gran energía, esencialmente idénticas a los rayos X. En efecto, la única diferencia entre los rayos gamma y los rayos X estriba en que los primeros proceden de un núcleo atómico, mientras que los segundos se originan mediante procesos que tienen lugar fuera del núcleo. Aparece radiación gamma, en una transformación radioactiva, cuando el núcleo resultante queda en lo que se llama un estado excitado, es decir, un estado que posee mayor energía interna que el estado normal o fundamental de dicho núcleo. El exceso de energía se emite entonces, casi instantáneamente, en forma de radiación gamma. Señalemos también que la radiación gamma acompaña a otros procesos nucleares en los que se producen núcleos en estado excitado.
Aunque los neutrones, en general, se encuentran ligados en el interior de los núcleos, es posible obtenerlos en estado libre (§ 2.71). Estos neutrones libres interaccionan de modo diverso con los núcleos atómicos. Por el momento, las interacciones neutrón-núcleo que nos interesan están comprendidas en una de estas tres categorías: dispersión, captura y fisión. La primera etapa de tales interacciones consiste, por regla general, en la absorción de un neutrón por el núcleo, dando lugar a la formación de un núcleo compuesto en estado excitado, de energía interna elevada. En las reacciones de dispersión, el núcleo compuesto expulsa rápidamente un neutrón cuya energía cinética es inferior a la del neutrón capturado, quedándose el núcleo residual con el correspondiente exceso de energía. Si esta energía adicional se manifiesta en forma de energía interna, lo que equivale a decir que el núcleo queda en estado excitado, el fenómeno se conoce con el nombre de dispersión inelástica En cambio, cuando la energía extra adquirida por el núcleo es de naturaleza exclusivamente cinética, se dice que se ha producido una forma de dispersión elástica El empleo del término “dispersión” para describir estas reacciones se justifica por el hecho de que, en general, la dirección del neutrón después de la interacción es diferente a la que tenía antes de la interacción con el núcleo. Inmediatamente de quedar en libertad, los neutrones poseen por lo regular energías cinéticas muy elevadas, del orden de millones de electrón-voltios, razón por la cual se denominan neutrones rápidos. Ahora bien, como consecuencia de las colisiones de dispersión con los diversos núcleos existentes en el medio en que los neutrones se mueven, pierden estos, gran parte de su energía cinética y se convierten en neutrones lentos, de energías no superiores a 1 electrón-voltio. En el último estadio, la energía cinética puede llegar a reducirse en tal grado que, prácticamente, su valor medio coincide con el correspondiente a los átomos o moléculas que integran el medio. Como en este caso el valor de la energía cinética depende de la temperatura, recibe el nombre de energía térmica. Los neutrones cuyas energías han quedado reducidas a este nivel se denominan neutrones térmicos. A temperatura ambiente, la energía más probable de estos neutrones es solamente de 0,025.
En lugar de expulsar un neutrón, el núcleo compuesto excitado formado como consecuencia de la absorción del neutrón incidente puede emitir su exceso de energía en forma de radiación gamma. Este proceso se conoce con el nombre de captura radiactiva o, simplemente, captura. El núcleo residual posee un neutrón extra, siendo por tanto un isótopo del núcleo original, de número másico una unidad mayor. Los procesos de captura radiactiva, que se representan mediante el símbolo (n, y), son muy frecuentes. Casi sin excepción, se producen con mayor facilidad con neutrones lentos que con neutrones rápidos. Únicamente se produce fisión en ciertos núcleos de número atómico cien con el funcionamiento de los reactores nucleares, pero sólo citaremos ahora dos de interés inmediato. La primera es la captura de neutrones por uranio238, el isótopo natural más abundante de este elemento (Tabla 1.1); el proceso (n, Ƴ) puede representarse en este caso del modo siguiente: 92U238 + on1 > 92U239 + Ƴ. El núcleo resultante, uranio-239, es radioactivo) y se desintegra por emisión de una partícula beta negativa, que se representa mediante el símbolo -1β° (carga 1, masa cero); por consiguiente, 92U239 -» -1 β ° + 93Np239 siendo el producto 93Np239, un isótopo del elemento de número atómico 93, llamado neptunio, elemento que no existe normalmente en la naturaleza en cantidades detectables. El neptunio-93 presenta también actividad beta y se desintegra bastante rápidamente según el proceso. 92U239 → -1 β ° + 94Pu239 para formar el isótopo Pu239 del elemento denominado plutonio, cuya presencia en la naturaleza se reduce a indicios solamente.
Una serie de procesos similar a la que acabamos de describir se inicia por reacción (n, y) con el elemento natural torio-232. En efecto, 90Th232 + on1 →90Th233 + → γ
obteniéndose como producto resultante el isótopo torio-233. Este experimenta dos etapas sucesivas de desintegración beta, la primera de las cuales
90Th233 →-1 β 0 + 91Pa233,
conduce a un isótopo del protactinio, mientras que la segunda, 91Pa233→-1 β 0 + 92U233, produce uranio-233, un isótopo del uranio que no se encuentra en la naturaleza en cantidades apreciables.
El tercer tipo importante de interacción entre neutrones y núcleos, se conoce con el nombre de fisión, o - con mayor propiedad- fisión nuclear. Como el proceso de fisión es fundamental en el funcionamiento de los reactores nucleares, trataremos de él a continuación más detalladamente que lo fueron los otros dos tipos de interacción neutrón - núcleo.
Solamente se produce fisión en ciertos núcleos de número atómico y másico elevado, siendo un factor que contribuye de modo importante el alto valor de Z2 y, por consiguiente, el de la fuerza repulsiva existente en el interior del núcleo (§ 1.24). En el proceso de fisión, el núcleo compuesto excitado, que se forma tras la absorción de un neutrón, se escinde en dos núcleos más ligeros, denominados fragmentos de fisión. Cuando la energía cinética del neutrón incidente es pequeña, es decir, se trata de un neutrón lento, los dos fragmentos poseen generalmente masas desiguales. Dicho de otro modo, la fisión simétrica por neutrones lentos es infrecuente; en la mayoría de las fisiones provocadas por neutrones lentos, la relación de masas de los fragmentos de fisión es aproximadamente de 2 a 3. Solamente tres núclidos (uranio-233, uranio-235 y plutonio-239), con estabilidad suficiente para que puedan ser almacenados durante largo tiempo, son fisionables por neutrones de todas las energías, desde valores térmicos o inferiores hasta millones de electrón-voltios. De los tres, únicamente el uranio-235 existe en la naturaleza; los otros dos se producen artificialmente a partir de uranio-238 y torio-232, en la forma antes descrita, esto es, por captura neutrónica seguida de dos desintegraciones beta. Se conocen algunas especies más, capaces de experimentar fisión por neutrones de cualquier energía, pero son fuertemente radiactivas y se desintegran tan rápidamente, que carecen de valor práctico para la obtención de energía nuclear. Además de los núclidos fisionables por neutrones de cualquier energía, hay otros que requieren neutrones rápidos para producir fisión; entre estos, merecen citarse torio-232 y uranio-238. Con neutrones de energía inferior a 1 Mev, la única reacción que tiene lugar es la de captura radiactiva, pero por encima de este valor umbral, también se produce fisión en cierta cuantía. Puesto que la fisión de torio-232 y uranio-238 sólo es posible con neutrones suficientemente rápidos, se les designa con el nombre de núclidos fisionables. Para distinguirlos, al uranio-233, uranio-235 y plutonio-239, que experimentan fisión por neutrones de cualquier energía, se les da el nombre de núclidos fisibles. Finalmente, como el torio-232 y el uranio238 pueden convertirse en especies fisibles (uranio-233 y plutonio-239, respectivamente), se les denomina núclidos fértiles Desde el punto de vista de la utilización de la energía nuclear, la importancia del proceso de fisión radica en dos hechos. El primero es que, en dicho proceso, se libera una gran cantidad de energía por unidad de masa de combustible nuclear, y el segundo es que la reacción de fisión, iniciada por neutrones, origina la liberación de más neutrones. La combinación de estas dos circunstancias es, justamente, lo que hace posible el diseño de un reactor nuclear, en el que se establece una reacción de fisión en cadena, auto sustentada, con producción de energía en forma continua. Una vez iniciada la reacción de fisión en unos cuantos núcleos, mediante una fuente externa de neutrones, los neutrones producidos en la reacción la propagan a otros núcleos. Hay que hacer notar, sin embargo, que una reacción en cadena auto sustentada solamente es posible con núclidos fisibles. Ni el torio-232, ni el uranio238 pueden mantener una reacción en cadena, debido a que la probabilidad de fisión es pequeña, incluso para neutrones de energía superior al umbral de 1 MeV y también a que la dispersión inelástica reduce rápidamente la energía de los neutrones por debajo de este valor umbral. La liberación de neutrones en el proceso de fisión puede explicarse del siguiente modo. En el núcleo compuesto U236, que se forma cuando el núcleo de uranio-235 captura un neutrón, la relación de neutrones a protones es del orden de 1,57; en consecuencia, al escindirse este núcleo en dos fragmentos con uranio-235 captura un neutrón, la relación de neutrones a protones es del orden neutrón/protón debe tener el mismo valor en los productos instantáneos. Ahora bien, en la figura 1.2 se ve claramente que este valor de la relación neutrón/protón es demasiado alto, a efectos de estabilidad, tratándose de núcleos de masa intermedia. Por consiguiente, si estos núcleos producidos por fisión disponen de energía de excitación suficiente, pueden emitir neutrones, tendiendo con ello a adquirir mayor estabilidad.
El número de neutrones emitidos de esta forma es insuficiente, sin embargo, para conferir estabilidad a los fragmentos de fisión resultantes. Estos poseen todavía una relación neutrón/protón demasiado alto; por consiguiente, son radioactivos y muestran actividad beta negativa. Por término medio, los fragmentos de fisión experimentan tres etapas de desintegración radioactiva, antes de convertirse en núcleos estables. Se aplica la denominación general de productos de fisión a la mezcla compleja de núclidos, fuertemente radioactiva, consistente en los fragmentos de fisión y sus diversos productos de desintegración.
Para calcular la cantidad de energía puesta en libertad por fisión de un núcleo atómico, basta con determinar la disminución neta de masa, a partir de las correspondientes masas isotópicas, y aplicar luego la relación masa-energía de Einstein. Otro procedimiento muy simple e instructivo, aunque menos exacto, consiste en lo siguiente. Prescindiendo de los neutrones que intervienen en el proceso, cuya contribución es despreciable a efectos de este cálculo, la reacción de fisión puede representarse en forma aproximada del modo siguiente:
Uranio-235 > Producto de fisión A + Producto de fisión B → Energía
Como hemos visto en el Ejemplo 1.1, la energía media de enlace por nucleón en uranio-235 es de unos 7,6 MeV, de modo que podemos escribir: 92 p + 143 n → Uranio-235 + (235 X 7,6) MeV
representando p y n, protones y neutrones, respectivamente. Los números másicos de ambos productos de fisión están comprendidos, en su mayor parte, en el intervalo 95 140, al que corresponden energías de enlace por nucleón (por ejemplo, estaño-120) del orden de 8,5 MeV. Por tanto, 92 p +143 n > Productos de fisión A y B + 210 MeV
Restando miembro a miembro las dos expresiones de energía de enlace, se obtiene como resultado: Uranio-235 > Productos de fisión A y B + 210 MeV
Así pues, la fisión de un núcleo de uranio-235 u otro similar deja en libertad cantidades de energía superiores a 200 MeV Si se compara esta cifra con la de 4 ev que se producen, aproximadamente, por combustión de un átomo de carbono-12, se llega a la conclusión de que la fisión del uranio posee un rendimiento energético alrededor de 2,5 millones de veces superior al que se obtiene por combustión de igual masa de carbón. Dicho de otro modo, 1 libra de material fisionable posee capacidad para producir la misma cantidad de energía que 1400 toneladas de carbón, con un poder calorífico de 13.000 Btu/lb.
Para convertir en unidades prácticas los valores de la energía de fisión, recordemos que 1 MeV es igual a 1,60 X 10-6 erg, equivalente a 1,60 X 10-13 W-s. Por consiguiente, la energía total* disponible por fisión (200 MeV) es del orden de 3,2 X 10-11 vatios-segundo, de suerte que para producir la energía de 1 vatio-segundo son necesarias 3,1 X 1010 fisiones. En otros términos, con un ritmo de 3,1 X 1010 fisiones por segundo, se obtiene la potencia de 1 W.
Un átomo-gramo de cualquier elemento masa atómica del elemento expresada en gramos contiene 0,602 X 1024 (número de Avogadro) núcleos individuales; si todos ellos experimentaran fisión, la energía puesta en libertad sería (0,602 X 1024) (3,2 X 10-11) = 1,9 X 1013 vatios-segundo, es decir, 5,6 X 106 kWh. Esta es la cantidad total de calor que se produciría por fisión completa de 233 gramos de uranio-233, 235 gramos de uranio-235 o 239 gramos de plutonio-239. Prescindiendo de las ligeras diferencias existentes entre las masas anteriores, podemos considerar que los resultados de la Tabla 1.2 son aplicables a cualquiera de los materiales citados. Un hecho que conviene recordar es que la potencia producida por fisión de 1 gramo de material por día es, aproximadamente, 106 W, es decir, 1 MW. Sin embargo, la masa consumida es realmente superior a 1 gramo, debido a las pérdidas de núcleos fisionables, como consecuencia de reacciones de captura no seguidas de fisión.
TABLA 1.2. CALOR LIBERADO POR 1 LIBRA DE MATERIAL FISIONABLE
0,9 x 10u cal
1,0 x 107 kWh 2,8 x 1013 ft-lb 3,6 x 1010 Btu
Ejemplo 1.2. La exposición cumulativa del combustible nuclear en un reactor (“grado de quemado”) se expresa corrientemente en megavatio-días (MWd) por tonelada de uranio total existente en el combustible. Los metalúrgicos, en cambio, expresan la irradiación en fisiones por cm3 de combustible. Deducir el factor de conversión entre estas dos unidades. Un combustible de dióxido de uranio, de densidad 10,2 g/cm, tiene un grado de quemado de 10 000 MWd/t. Calcular el número de fisiones por cm3.
Como 1 MW = 106 W; 1 día = 8,64 X 104 seg; 1 t = 106 g, resulta: 1 MW-d/t U = 106 X 8,64 X 104/106 = 8,64 X104 W-s/g U.
Por otra parte, 3,1 X 1010 fisiones producen 1 W-s; en consecuencia,
1 MW-d/t U = 8,64 X 104 X 3,1 X 1010 = 2,68 X 1015 fisiones/g- U = (2,68 X 1015) (g U/cm3) fisiones/cm3.
Así pues, para convertir MWd/t en fisiones/cm3, basta multiplicar el grado de quemado por el factor 2,68 X 1015 y por el número de gramos de uranio por cm3 de combustible.
Suponiendo que todo el uranio del dióxido es uranio-238, resulta que 238 + 32 = 270 g UO2 contienen 238 g U.
La densidad del UO2 es 10,2 g/cm3, lo que corresponde a (10,2) (238) /270 = 8,99 g U/cm3. De aquí se deduce, 10 000 MWd/t = (104) (2,68 X 1013) (8,99) = 2,41 X 1020 fisiones/cm3
La mayor parte de la energía de fisión más del 80 por ciento aparece como energía cinética de los fragmentos de fisión, la cual se transforma en calor inmediatamente. Parte del 20 por ciento restante se presenta en forma de radiación gamma instantánea, procedente de los fragmentos de fisión excitados, y como energía cinética de los neutrones de fisión. Corresponde el resto a la energía de las partículas beta y rayos gamma emitidos por los productos de fisión radiactivos, energía que se va liberando gradualmente, según dichos productos se van desintegrando a lo largo del tiempo. Esta energía de desintegración se manifiesta, en último término, en forma de calor, ya que las radiaciones interaccionan con la materia y son absorbidas por ella. En la Tabla 1.3 figura la distribución de la energía de fisión para el caso del uranio-235, que puede considerarse aproximadamente aplicable a las tres especies fisibles más importantes.
TABLA 1.3. DISTRIBUCIÓN
MeV
Energía cinética de los fragmentos de fisión 165
Energía de la radiación gamma instantánea 7
Energía cinética de los neutrones de fisión 5
Partículas beta de los productos de fisión 7
Rayos gamma de los productos de fisión 6
Neutrinos 10
Energía de fisión total 200
Los 10 Mev de los neutrinos asociados a la desintegración beta no son aprovechables para la producción de energía, a causa de que la interacción de estas partículas con la materia es muy débil. Prácticamente, pues, todos los neutrinos escapan de un reactor de fisión, transportando con ellos toda su energía.
Como en cada acto de fisión se liberan dos o tres neutrones y solamente se necesita uno para mantener la fisión en cadena, parece a primera vista que, iniciada la reacción en una masa determinada de material fisionable, esta se mantendrá luego por sí misma. No es este el caso, sin embargo, porque no todos los neutrones de fisión son aprovechables para mantener la reacción en cadena. Algunos neutrones se pierden por reacciones distintas de fisión, principalmente captura radiactiva, con los diversos materiales extraños existentes en el sistema e incluso con la propia especie fisionable, mientras que otros neutrones escapan definitivamente del sistema. La fracción de neutrones que escapan, es decir, que se salen de los límites geométricos del sistema, puede reducirse convenientemente aumentando el tamaño o la masa del material fisionable. Pues bien, la cantidad mínima de dicho material capaz de mantener la fisión en cadena, una vez que se ha iniciado con una fuente externa de neutrones, recibe el nombre de masa crítica
La masa crítica necesaria para el funcionamiento de un reactor depende de un gran número de factores, pero para un sistema reactor determinado tiene siempre un valor definido. Así, por ejemplo, la masa crítica de uranio-235 puede variar desde menos de 1 kg, cuando se trata de sistemas constituidos por disoluciones acuosas de una sal de uranio con el 90 por ciento de isótopo fisible, hasta más de 200 kg que contendrían 30 toneladas de uranio natural incrustadas en una matriz de grafito. El uranio natural sólo, con un contenido aproximado del 0,7 por ciento de uranio-235, no puede alcanzar nunca la criticidad, por grande que sea su masa, debido a que se pierde una fracción excesivamente grande de neutrones por reacciones distintas de fisión.
Fig. 1.3. Representación esquemática de un sistema reactor nuclear
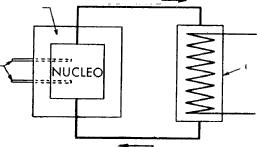
A pesar de las numerosas variedades de sistemas de reactores nucleares, tanto en lo que se refiere a diseño como a componentes, hay, sin embargo, cierto número de características generales que todos estos sistemas poseen en común, en mayor o menor grado. En esquema (fig. 1,3), un reactor consta de un núcleo activo, en el que se mantiene la cadena de fisiones y en donde se libera casi toda la energía de fisión en forma de calor. El núcleo del reactor contiene el combustible nuclear, constituido por un núclido fisible al que se adiciona con frecuencia un material fértil. Si se desea caso más corriente que la mayoría de las fisiones sean producidas por neutrones lentos, se necesita también un moderador. La función del moderador no es otra que frenar los neutrones de gran energía procedentes de la reacción de fisión, principalmente por medio de colisiones de dispersión elástica. Los mejores moderadores son aquellos materiales que están constituidos por elementos de número másico pequeño, con poca tendencia a capturar neutrones; como ejemplos de esta clase, tenemos el agua ordinaria, agua pesada (óxido de deuterio), berilio, óxido de berilio, carbono (en forma de grafito) e hidrocarburos. La naturaleza del combustible y del moderador, así como las proporciones relativas de ambos, determinan las energías de la mayoría de los neutrones que producen fisión.
El núcleo del reactor está rodeado por un reflector de neutrones, constituido por un material cuya naturaleza viene determinada, en gran parte, por la distribución energética de los neutrones existentes en el reactor. La misión del reflector es reducir la pérdida de neutrones por escape, contra dispersando gran parte de los que han logrado escapar. Por consiguiente, el empleo de reflector se traduce en una disminución de la masa crítica del núclido fisible. Si el núcleo del reactor contiene un moderador neutrónico, puede utilizarse como reflector este mismo material u otro moderador. En cambio, cuando se requiere que la mayoría de las fisiones sean producidas por neutrones de alta energía, debe evitarse totalmente la presencia de materiales moderadores; en este caso, el reflector ha de estar constituido por un elemento denso, de número másico elevado.
El calor que se genera en el núcleo de un reactor, como consecuencia de las fisiones que allí tienen lugar, se elimina o extrae por medio de un refrigerante adecuado. Entre los refrigerantes empleados hasta ahora o cuyo empleo se está considerando seriamente, ofrecen el mayor interés los siguientes: agua líquida, sodio líquido (o la aleación líquida sodio-potasio), ciertos compuestos orgánicos, y los gases aire, dióxido de carbono y helio. Cuando se ha de convertir en energía eléctrica la energía producida en el reactor, el calor del refrigerante se transfiere en general a un fluido de
trabajo, con el fin de producir vapor de agua o un gas a temperatura elevada. Uno u otro pueden utilizarse luego en un sistema convencional turbina-generador. En algunos reactores, se hace que el agua hierva dentro del núcleo del propio reactor, de suerte que el calor de fisión se utiliza directamente para producir vapor. Cuanto mayor sea la temperatura del vapor o del fluido de trabajo de que se trate, mayor será el rendimiento de conversión en potencia útil. Por consiguiente, en un reactor de potencia, interesa operar prácticamente a la temperatura más alta posible. Por otra parte, desde el punto de vista económico, interesa que la potencia específica del reactor, es decir, la velocidad de generación de calor por unidad de masa de material fisible, sea muy elevada. En lo que respecta a consideraciones nucleares, no existen límites para la temperatura o nivel de potencia que un reactor puede alcanzar. Quiere decirse que las condiciones de operación vienen determinadas, en la práctica, más por limitaciones tecnológicas que por factores propiamente nucleares. La extracción de calor debe hacerse a un ritmo tal que permita al refrigerante alcanzar temperaturas elevadas, pero sin que se establezcan tensiones térmicas ni temperaturas internas peligrosamente altas, que pudieran provocar daños irreparables en el reactor. La generación de calor en un reactor nuclear es proporcional al número de fisiones, y este viene determinado en cada sistema por la densidad neutrónica, es decir, el número de neutrones por unidad de volumen. Por ello, las operaciones de control puesta en marcha, funcionamiento a cualquier nivel de potencia y parada se realizan variando la densidad neutrónica en el núcleo del reactor. Esto puede hacerse de dos maneras: bien mediante barras móviles de un material que captura neutrones con facilidad, es decir, un veneno neutrónico, o bien desplazando parte del núcleo del reactor o del reflector. La introducción de un veneno, por ejemplo, cadmio o boro, origina una disminución de la densidad neutrónica y, por tanto, de la potencia del reactor; la retirada del veneno va seguida de un incremento de ambas magnitudes, densidad neutrónica y nivel de potencia. Análogamente, el desplazamiento de una porción del reflector o del núcleo ocasiona el escape de neutrones, provocando así una disminución de la densidad neutrónica, mientras que su reintegración producirá el efecto opuesto.
Aunque los reactores nucleares pueden clasificarse de varios modos, la distinción más fundamental es la que se basa en la energía cinética o velocidad de los neutrones responsables de la fisión en un reactor determinado. Casi todos los neutrones liberados por fisión poseen energías elevadas y, por tanto, de no existir un moderador en el núcleo o en el reflector, la mayoría de las fisiones serán producidas por neutrones rápidos. El reactor nuclear que corresponde a este caso recibe el nombre de reactor rápido. El combustible de tales reactores debe contener una proporción considerable alrededor del 10 por ciento o más de material fisible. El resto debe consistir en una sustancia de número másico elevado o medio, ya que los elementos de número másico bajo frenarían los neutrones. Asimismo, deben evitarse en lo posible aquellos elementos que puedan provocar dispersión inelástica y, por tanto, moderación de neutrones de energías moderadamente altas.
Si en el núcleo de un reactor rápido, o en lo que se llama capa fértil en torno del mismo, existe una especie fértil, esta se convertirá en fisible por captura neutrónica. El número de capturas inútiles o parásitas de neutrones rápidos es relativamente pequeño, de modo que, si se mantiene mínima la pérdida de neutrones por escape, cabe la posibilidad de que se disponga de más de un neutrón, por fisión, para la conversión de núcleos fértiles en fisibles. En estas condiciones, es posible que se produzca más material fisible, por captura neutrónica, del que se consume por fisión.
Cuando el núclido fisible producido es idéntico al empleado para producir la fisión en cadena, el reactor se denomina reproductor. Un reactor rápido que utiliza plutonio-239 como combustible y uranio-238 como especie fértil puede actuar como reactor de potencia y reproductor, generando energía y, al mismo tiempo, produciendo más plutonio239 del que consume. También es posible un reactor rápido análogo, reproductor y de potencia, que utiliza uranio233 y torio-232 como núclidos fisible y fértil, respectivamente. Parece, sin embargo, que la reproducción en este sistema puede lograrse en reactores de otro tipo que se describirán más adelante, los cuales poseen ciertas ventajas sobre los reactores rápidos.
Cabe la posibilidad de que un reactor rápido utilice uranio-235 como especie fisible, para mantener la reacción nuclear en cadena, y uranio-238 como material fértil, que se convierte en plutonio-239. Este tipo de reactor, denominado convertidor, no es un reproductor en el sentido estricto, aun cuando la cantidad de plutonio-239 producida sea superior a la de uranio-235 consumida. En este último caso, el reactor se denomina a veces pseudoreproductor.
Las reservas de uranio-235, único material fisible existente en la naturaleza, son pequeñas. Por consiguiente, llegará al fin un día en que todo el uranio-235 aprovechable se habrá agotado prácticamente. El aprovechamiento ulterior del uranio-238 restante y del torio-232 tendrá que depender del empleo del plutonio-239 o uranio-233 para mantener la fisión en cadena. Por esta razón, del plutonio-239 o del uranio-233 para mantener la fisión en cadena. Por esta razón son importantes los auténticos reproductores, que producen y consumen eficientes de dichos materiales que hagan viable su utilización como combustibles nucleares, es muy probable que los reactores pseudoreproductores, basados en el uranio-235, desempeñen un papel de gran importancia.
Cuando el núcleo del reactor contiene una proporción considerable de moderador, la elevada energía de los neutrones de fisión cae rápidamente a la región térmica. La mayor parte de las fisiones en un reactor de este tipo, que se denomina reactor térmico, serán, pues, producidas por neutrones térmicos o lentos. Los reactores térmicos tienen sobre los rápidos la ventaja de una mayor flexibilidad de diseño. Dentro de límites razonables, cabe elegir entre diversos moderadores, refrigerantes y materiales combustibles. Según la naturaleza del combustible y del moderador, un reactor térmico puede ser bastante pequeño o relativamente grande. En cambio, los reactores rápidos son generalmente pequeños, lo cual agudiza los problemas de transmisión de calor. En cuanto al combustible de los reactores térmicos, puede variar según las circunstancias desde uranio natural, con un contenido del 0,7 por ciento de uranio-235, hasta uranio enriquecido al 90 por ciento, o más, en el isótopo fisible.
La mayoría de los reactores térmicos contienen una especie fértil, por lo cual actúan como convertidores. En ciertos casos, sin embargo, en que se necesitan reactores muy compactos, el combustible consiste esencialmente en uranio235 puro. Los reactores de este último tipo reciben el nombre de quemadores, debido a que consumen material fisible sin reemplazarlo. Tales reactores sólo están justificados en casos muy especiales, en los que su empleo es imprescindible, por ejemplo, en un submarino.
Como la probabilidad es grande de que los neutrones lentos sean capturados por uranio-235 o plutonio-239 en reacciones distintas de fisión, resulta que, por término medio, se dispone de menos de un neutrón por fisión para la conversión de núcleos fértiles en fisibles, habida cuenta de las pérdidas inevitables
de neutrones por escape. Por consiguiente, la cantidad de plutonio-239 producida en un reactor térmico convertidor no excede, en general, a la cantidad consumida de este isótopo o de uranio-235 para mantener la fisión en cadena. En consecuencia, no es fácil proyectar un reactor térmico reproductor o seudo- reproductor, que utilice como combustible uranio-235 o, por tanto, los re- bien, esto no ocurre cuando el material fisible es uranio-233 y, por tanto, los reproductores térmicos basados en el empleo de este núclido, con torio-232 como especie fértil, son los que ofrecen mayor interés.
La producción de combustible nuclear, su utilización en el reactor y la recuperación de materiales fisibles y fértiles en el combustible gastado, constituyen el ciclo del combustible. Representa este ciclo un aspecto importante del proyecto de un reactor, debido principalmente a su influencia sobre la economía de la energía nuclear. En primer lugar, el proceso de la materia prima minerales de uranio para convertirla en un material de gran pureza que pueda utilizarse como combustible, exige un esfuerzo considerable; el combustible puede ser uranio metálico, óxido o carburo de uranio, o bien una sal soluble en agua como el sulfato de uranio. Más aún, no pocos reactores han de utilizar uranio enriquecido, al menos parcialmente, en el isótopo fisible uranio-235, es decir, con un contenido superior al que existe en este elemento en estado natural. Por consiguiente, para satisfacer este requisito, debe incluirse en la preparación de materiales combustibles un proceso de separación isotópica.
Diversas causas pueden limitar la vida del combustible en un reactor: alteraciones dimensionales de los elementos combustibles sólidos, acumulación de productos de fisión venenosos, especialmente en los reactores térmicos, y agotamiento del material fisible. En general, es preciso reemplazar el combustible cuando se ha consumido un pequeño porcentaje del total de especies fisibles y fértiles. Los materiales no usados deben, por consiguiente, recuperarse y reciclarse, y esto lleva consigo un procedimiento químico muy complejo. A pesar de la pequeña utilización del material fisible, la radioactividad intensa de los productos de fisión introduce un problema peculiar con respecto al tratamiento de combustibles gastados. Hay que establecer un periodo de “enfriamiento”, que puede llegar a ser de 100 días, para que la actividad decaiga en grado tal que permita el procesado ulterior. Como este retraso se suma al coste de inventario o renta del combustible, es preciso tomar en consideración procedimientos que solamente requieran periodos de enfriamiento cortos.
Los procesos químicos y metalúrgicos mediante los cuales se separan el uranio, plutonio y productos de fisión, pueden ser bastante complicados, según la forma en que se encuentre el combustible del reactor. En particular, los reactores térmicos requieren un alto grado de descontaminación, es decir, de eliminación de productos de fisión, con objeto de reducir al mínimo la cantidad de venenos neutrónicos presentes. Este problema es menos serio cuando se trata de combustibles para reactores rápidos, debido a que, en general, la probabilidad de captura sin fisión de neutrones rápidos es pequeña. En cualquier caso, sin embargo, la eliminación de productos de fisión radioactivos es siempre necesaria. con el fin de que pueda fabricarse el material recuperado hasta darle la forma requerida, sin que ello constituya un riesgo biológico.
Mencionaremos, finalmente, el formidable problema que supone el desembarazarse de grandes cantidades de residuos radioactivos, principalmente productos de fisión de intensa radioactividad, procedentes de las plantas de procesado de combustibles. En la mayoría de los casos se concentran primeramente las disoluciones de estos residuos, que luego se trasladan en recipientes fuertemente blindados a emplazamientos convenientes.
Con el fin de que sirvan de fundamento general algunos de los capítulos que siguen, se bosqueja a continuación un resumen histórico del desarrollo de los reactores nucleares. Inmediatamente de hacerse público el descubrimiento de la fisión, se comprendió claramente que este proceso abría amplias perspectivas a la obtención de energía nuclear en forma utilizable. En efecto, ya en mayo de 1939 se solicitó en Suiza patente de invención para un sistema proyectado con esta finalidad, utilizando agua pesada como moderador. Sin embargo, la primera reacción de fisión en cadena, auto sustentada, tardó algún tiempo en realizarse. Este acontecimiento histórico tuvo lugar en los Estados Unidos el 2 de diciembre de 1942, en la Universidad de Chicago. Consistía el combustible en unas 60 toneladas de uranio, en forma de bloques de metal y óxido, distribuidos en una matriz de 385 toneladas, que servía a la vez de moderador y reflector. La potencia nominal de funcionamiento era de 2 kW, de suerte que bastaba el aire ambiente para obtener la refrigeración necesaria. Se construyó la estructura apilando gradualmente bloques de grafito, una capa tras otra, e introduciendo el uranio en orificios practicados en dichos bloques. Por esta razón se denominó “pila”, nombre que se conservó durante varios años, hasta que se generalizó la denominación más apropiada de ‘'reactor nuclear”.
Cuando se planeó originalmente, el estudio del sistema uranio-grafito tenía por objeto determinar si podía realizarse una reacción en cadena, con el fin de utilizar dicha reacción para producir una explosión atómica. Ahora bien, a lo largo del trabajo, se puso de manifiesto que la cadena de neutrones podría utilizarse también para producir plutonio239 (en la forma ya descrita, y emplear este material fisible en la fabricación de armas atómicas. Sería necesario para ello construir reactores grandes, capaces de funcionar a potencias elevadas, y ya en 1942 se iniciaron los planes para que los reactores de Hanford produjeran plutonio-239 en cantidades apreciables. Entre tanto, y con objeto de disponer de cantidades suficientes de este isótopo que permitieran el estudio de sus propiedades, así como la adquisición de experiencia en el manejo y operación de reactores, se decidió construir en Oak Ridge un reactor experimental con una potencia nominal que se estableció inicialmente en 1000 kW. Este reactor comenzó a funcionar en noviembre de 1943, y, al igual que la Pila de Chicago, empleaba grafito como moderador y reflector; el combustible, en cambio, estaba en forma de cilindros de uranio metálico con vaina de aluminio, y se utilizaba circulación forzada de aire para eliminar el calor generado por fisión. Es interesante mencionar que este reactor, el más antiguo de todos los existentes, funciona todavía en el Laboratorio Nacional de Oak Ridge a una potencia de 4000 kW. Se trata de un instrumento experimental de gran valor, para investigaciones en las que se necesitan fuentes neutrónicas intensas.
Originalmente, los reactores de producción de Hanford se proyectaron con la idea de utilizar como refrigerante helio a presión. Sin embargo, tan graves eran los problemas que planteaba el suministro de cantidades grandes de este gas, relativamente escaso, así como la evitación de fugas, que se abandonó esta idea inicial en favor del empleo de agua como refrigerante. Las dificultades que entrañaba la construcción de un reactor grande, moderado por grafito y refrigerado por agua, eran considerables, pero fueron superadas, y el primer reactor de Hanford alcanzó la criticidad en septiembre de 1944. Inmediatamente después se construyeron en Hanford varios reactores más, todos del mismo tipo general, destinados a la producción de plutonio. En ninguno de ellos se aprovecha el calor de fisión, que es disipado al exterior por el agua de refrigeración. Los reactores de producción más recientes, instalados en Savannah River, emplean agua pesada como moderador, ya que ello significa mayor rendimiento de conversión de uranio-238 en plutonio-239. Lo mismo en Inglaterra que en Francia, los reactores originales de plutonio estaban moderados por grafito y refrigerados por aire, desperdiciando el calor producido, como en el caso de los reactores norteamericanos. Sin embargo, los reactores proyectados últimamente son de doble uso; van refrigerados por dióxido de carbono a presión y producen, a la vez, plutonio-239 y potencia utilizable.
Con excepción de los dedicados a la producción de plutonio, prácticamente todos los reactores construidos hasta 1955 eran de tipo experimental, para ser utilizados como instrumentos de investigación física, o para obtener información aplicable al proyecto de reactores de potencia. Entre los destinados a la investigación, dos nuevos prototipos terminaron de construirse en mayo de 1944. Fue uno de ellos el denominado reactor “water boiler” de Los Alamos, que utilizaba como combustible sulfato de uranio parcialmente enriquecido disuelto en agua, actuando el disolvente como moderador. Corresponde a este reactor una doble primacía: ha sido el primer reactor homogéneo, esto es, en el que están mezclados uniformemente combustible y moderador, y también el primer reactor que empleo como combustible uranio enriquecido en el isótopo fisible uranio-235. El otro reactor de investigación, que comenzó a funcionar más o menos al mismo tiempo, fue el CP-3 (Chicago Pile No. 3) del Laboratory de Argonne. Este ha sido el primer reactor moderado por agua pesada.
El moderador se hacía circular por un cambiador de calor externo, donde era refrigerado por agua ordinaria. Tanto el reactor “water boiler” como el Cp-3 han servido como prototipo para la construcción de reactores de investigación, no solo en los Estados Unidos, sino en todo el mundo.
En Canadá, debido principalmente a sus instalaciones para la producción de agua pesada y a disponer de amplios recursos de uranio natural, se interesaron desde el principio en los reactores que utilizan estos materiales. El reactor experimental EEP (Zero Energy Experimental Pile) se terminó en abril de 1945, siguiéndole pronto el reactor NRX de Chalk River (Ontario). Finalizada su construcción en agosto de 1947, fue durante algún tiempo el reactor de mayor flujo térmico (producto de densidad neutrónica por velocidad) entre todos los conocidos. El reactor NRX constituyó en su día una novedad, en el sentido de que, aunque moderado por agua pesada, empleaba agua ordinaria como refrigerante, circulando por canales anulares en torno de los elementos combustibles, constituidos por barras cilíndricas de uranio metálico.
Con el Reactor de Prueba de Materiales (Material Testing Reactor, MTR) construido en la National Reactor Testing Station de Arco (Idaho), se introdujo otro tipo de diseño que luego se aplicaría a reactores posteriores. Se proyectó este reactor, que comenzó a funcionar en marzo de 1952, para disponer de un flujo neutrónico elevado superior al del reactor NRX con fines experimentales en particular para el estudio de los efectos de las radiaciones nucleares sobre los materiales para reactores. El MTR posee dos características especiales de diseño: la primera es el empleo de agua ordinaria circulando a través de un tanque cilíndrico donde se contiene el núcleo del reactor como moderador refrigerante, y en cierto grado, como reflector; la segunda se refiere a los elementos combustibles, que son placas ligeramente curvadas, tipo “sándwich”, consistentes en una aleación de aluminio y uranio enriquecido con recubrimiento de aluminio por ambos lados. Se disponen paralelamente varias de estas placas en un bastidor de aluminio, resultando así un conjunto en forma de caja alargada, de sección aproximada de 3 X 3 pulgadas. Este tipo de elementos combustibles en forma de placa presenta una gran superficie de transmisión de calor, lo cual hace posible que se pueda operar a potencias bastante elevadas (40 Mw).
Con anterioridad a la entrada en funcionamiento del MTR, se habían realizado pruebas preliminares con un modelo, que demostraron la eficiencia y óptimo comportamiento de los elementos combustibles antes descritos. El empleo de estos elementos, tipo MTR, facilitó la construcción del Bulk Shielding Reactor (BSR) en el Laboratorio Nacional de Oak Ridge, hacia finales de 1950. El núcleo de este reactor estaba integrado por un número variable de 16 a 25 de elementos en forma de caja, constituyendo un paralelepípedo, con espacios entre ellos para las barras de control. Todo el conjunto se mantenía suspendido en agua, a una profundidad de 6 metros aproximadamente; la masa de agua servía como moderador, refrigerante y reflector, y también como blindaje de radiaciones. El reactor podía funcionar hasta potencia de 100 kW con refrigeración por convección natural, no siendo necesaria la circulación forzada del agua. El BSR recibió el sobrenombre de reactor “piscina”, a causa del gran tanque de agua en que este contenido. La gran sencillez y comodidad de manejó del reactor “piscina” justifican su adopción por universidades y laboratorios de investigación industrial.
En todos los reactores citados hasta ahora se emplea un moderador para frenar los neutrones; son, pues esencialmente, reactores térmicos. El primer reactor de neutrones rápidos comenzó a funcionar en Los Alamos en noviembre de 1946; el combustible era plutonio-239, siendo esta la primera vez que dicho material ha sido utilizado en un reactor. Refrigerado por mercurio, la potencia de funcionamiento alcanzó el nivel de 25 kW. Naturalmente, no existía moderador, ya que la finalidad perseguida era demostrar que podía realizarse una reacción en cadena controlada, en la cual la mayoría de las fisiones son provocadas por absorción de neutrones rápidos. El segundo reactor rápido fue el Experimental Breeder Reactor (EBR-I), cuya construcción se completó en 1951, en Arco. Este proyecto del Laboratorio Nacional de Argonne tenía por objeto estudiar la posibilidad de reproducción, mediante neutrones rápidos, con generación simultánea de energía eléctrica, así como la de utilizar un metal líquido (aleación sodio-potasio) como refrigerante a temperaturas elevadas (600 °F). Estrictamente hablando, el EBR-I es un pseudoreproductor, ya que las primeras cargas utilizaban uranio-235 como combustible y uranio-238 como material fértil. De todos modos, este reactor sirvió para demostrar que la reproducción era factible. Como cosa de interés histórico, añadiremos que el EBR-I fue el primer reactor que produjo energía eléctrica de origen nuclear, en diciembre de 1951.
Indudablemente, los reactores de investigación son instrumentos experimentales de grandísimo valor, pero el principal significado de los reactores nucleares radica en la posibilidad de producir energía, tanto para utilización normal como para fines especiales. En los Estados Unidos, se vio enseguida que una central de potencia nuclear, compacta, ofrecería grandes ventajas en el campo de la propulsión submarina, ya que permitiría realizar recorridos muy grandes sin necesidad de salir a la superficie ni de repostar. El reactor que se proyectó con esta finalidad utiliza agua a presión como moderador-refrigerante y uranio metálico altamente enriquecido, envainado en zirconio, como combustible. El empleo de estos materiales ha permitido diseñar un reactor de pequeño tamaño y de gran potencia. El agua a presión circula por un cambiador de calor externo, el cual produce vapor para el funcionamiento de las turbinas. Un prototipo del reactor para submarino comenzó a funcionar, en marzo de 1933, en Arco, produciendo cantidades importantes de energía eléctrica a partir de mayo de 1953. El primer submarino con propulsión nuclear, U.S.S. Nautilus, inició sus pruebas en el mar en enero de 1955. La demostración ha sido tan efectiva que, a partir de entonces, se han construido y se están construyendo numerosos submarinos con plantas de propulsión del mismo tipo general.
Resultado de la experiencia adquirida con los reactores para submarinos, de funcionamiento tan satisfactorio, fue el proyecto de la primera central nuclear de potencia de los Estados Unidos, instalada en Shippingport, con un reactor de agua a presión (PWR). La presión de agua en la vasija del reactor es de 2000 psia, y el vapor producido en el cambiador de calor alcanza temperaturas del orden de 490 °F y presiones próximas a 600 psia. Con objeto de rebajar el coste de la energía producida, solamente un número reducido de elementos contienen combustible altamente enriquecido en uranio-235 (aleado con circonio), siendo los restantes de uranio natural (en forma de dióxido). Esta modificación obliga a construir reactores más grandes, pero tal aumento de tamaño no ofrece inconvenientes en instalaciones terrestres. El reactor PWR de Shippingport comenzó a funcionar el 2 de diciembre de 1957, alcanzando su potencia nominal de 60 Mw eléctrica (230 Mw térmicos) tres semanas después. Otros reactores de agua a presión, que han sido construidos posteriormente, utilizan un tipo único de elemento combustible, a base de óxido de uranio ligeramente enriquecido. Unos son reactores grandes, para centrales de potencia, mientras que otros son reactores compactos, de potencia relativamente baja, para ser utilizados en zonas remotas, por ejemplo, en las regiones Ártica y Antártica, en donde los costos de los combustibles convencionales son muy elevados.
Una modificación del sistema de agua a presión consiste en producir vapor directamente, aprovechando el calor de fisión para hacer hervir el agua en el núcleo del reactor, en lugar de hacerlo en un cambiador de calor externo. Tras una serie de experimentos (BORAX) iniciados en Arco en 1953, se construyó el reactor experimental de agua en ebullición (Experimental Boiling Water Reactor, EBWR) en el Laboratorio Nacional de Argonne. Alcanzó la criticidad el 1 de diciembre de 1956, y comenzó a producir electricidad el 23 del mismo mes; seis días después alcanzaba su potencia nominal de 5 MW eléctricos. En la vasija del reactor se produce vapor a la presión de 600 psia, el cual se utiliza una vez seco para alimentar un sistema turbogenerador. El BWR tiene la ventaja sobre el PWR de que puede producir vapor de igual calidad a presiones más bajas y sin necesidad de un generador externo de vapor. Existen en la actualidad varios reactores de agua en ebullición, que han sido desarrollados para la producción de energía a gran escala.
Se ha mencionado ya la diversidad de materiales para reactores combustibles, moderadores y refrigerantes de que se dispone actualmente. Son posibles, pues, numerosas combinaciones, lo cual conduce a toda una gama de tipos de reactores. Alguno de estos puede presentar incompatibilidades fundamentales, pero entre la mayoría de los que parecen realizables prácticamente no se puede decidir con certeza cuál es el “mejor” diseño para un reactor de potencia. Todos los tipos hasta ahora propuestos tienen sus ventajas y sus inconvenientes. La consecuencia ha sido que, en las primeras etapas del desarrollo de reactores de potencia, la línea de conducta seguida por cada país ha venido determinada por uno de estos factores: experiencia tecnológica previa o disponibilidad de materiales. Así, por ejemplo, las primeras centrales nucleares construidas en los Estados Unidos utilizaron el sistema de agua a presión, a causa de la experiencia satisfactoria que se había adquirido al desarrollar el reactor para submarinos, juntamente con la disponibilidad de uranio enriquecido. En Inglaterra, en cambio, la experiencia alcanzada con los reactores de producción de Windscale refrigerados por aire y moderados por grafito que se consideraron menos peligrosos que los reactores de Hanford refrigerados por agua condujo al desarrollo de reactores de doble uso, del tipo de Calder-Hall. Estos reactores utilizan como combustible uranio natural, como moderador grafito, y como refrigerante dióxido de carbono gaseoso. Aparte de su empleo en propulsión submarina, los reactores de agua a presión no atrajeron el interés de los británicos, siendo una de las razones el costo muy elevado del uranio enriquecido.
Las centrales nucleares construidas en Inglaterra, exclusivamente para producción de energía, han seguido los mismos principios básicos de proyecto que los reactores de Calder-Hall. El primer reactor de potencia de la U.R.S.S(5 Mw eléctricos), que comenzó a funcionar en 1954, fue un sistema de combustible ligeramente enriquecido, refrigerado por agua y moderado por grafito, probablemente como resultado de la experiencia obtenida con reactores de producción, tipo Hanford. Otro reactor de potencia (100 Mw eléctricos) de diseño similar comenzó a funcionar en Siberia en 1958. Finalmente, como antes se ha indicado, los reactores preferidos en Canadá emplean agua pesada como moderador y uranio natural como combustible, debido fundamentalmente a la abundancia de los materiales necesarios.
No obstante, el progreso alcanzado, se acepta generalmente que la tecnología de reactores nucleares está todavía en su infancia. Muchas etapas de investigación y desarrollo habrán de recorrer, antes de que pueda fijarse con rigor la potencialidad a largo plazo de los diferentes tipos de reactores, especialmente en sus perspectivas de producción de energía a buen nivel económico. Dada la gran importancia de la reproducción como forma de utilizar al máximo las fuentes de combustibles nucleares, se está realizando en varios países una amplia investigación sobre reactores reproductores de potencia, que utilizan la fisión por neutrones rápidos. La central “Enrico Fermi”, en las proximidades de Monroe, Michigan, será la primera instalación a gran escala que utilice un reactor rápido reproductor. Se estudian, además, otros tipos de sistemas reactores. Así, por ejemplo, en Inglaterra, están recibiendo prioridad los reactores avanzados refrigerados por gas, de combustible enriquecido, y que se proyectan para funcionar a temperaturas elevadas. En los Estados Unidos, además de los sistemas de agua a presión, de agua hirviendo y refrigerados por gas a temperaturas elevadas, se está investigando cierto número de tipos prometedores. Merecen citarse, entre estos, los reactores de agua hirviendo con sobrecalentamiento nuclear, para mejorar el rendimiento, los reactores que emplean líquidos orgánicos como moderadores y refrigerantes para evitar las presiones elevadas que son necesarias con agua, y sistemas con grafito de moderador y sodio líquido como refrigerante, que permiten operar a temperaturas elevadas y a presiones normales. Centrales de todos estos tipos han sido construidas o se están construyendo en los Estados Unidos, con el fin de mejorar la tecnología de los diferentes sistemas de reactores. A lo largo de este resumen histórico, se ha pasado revista a los principales aspectos del desarrollo de reactores, desde 1942. Aunque se ha indicado lo más notable, no ha sido posible tratar de todos los tipos de reactores que han sido estudiados, investigados o realmente construidos. Tampoco se han mencionado algunas ideas prometedoras, como los experimentos con sistemas homogéneos, en los que se utiliza como combustible disoluciones acuosas o en agua pesada de una sal de uranio, y que han sido abandonadas, al menos temporalmente. Creemos, sin embargo, que lo descrito es suficiente para que se tenga una orientación general acerca del pasado, presente y futuro inmediato del programa de reactores nucleares.
