Ths Nguyễn Thanh Tú eBook Collection

WORD VERSION | 2023 EDITION
ORDER NOW / CHUYỂN GIAO QUA EMAIL
TAILIEUCHUANTHAMKHAO@GMAIL COM

Ths Nguyễn Thanh Tú eBook Collection

WORD VERSION | 2023 EDITION
ORDER NOW / CHUYỂN GIAO QUA EMAIL
TAILIEUCHUANTHAMKHAO@GMAIL COM


CĐ1: Mở đầu về Hóa học hữu cơ
CĐ2: Công thức phân tử hợp chất hữu cơ
CĐ3: Cấu trúc phân tử hợp chất hữu cơ
CĐ4: Độ bất bão hòa
CĐ5: Phản ứng hữu cơ
CĐ6: Tổng ôn đại cương Hóa học hữu cơ
KIẾNTHỨCCẦNNHỚ
1.Kháiniệm: Hợp chất hữu cơ là hợp chất của cacbon trừ: oxit cacbon, muối cacbonat, hợp chất xianua, hợp chất cacbua.
2.Phânloại: Gồm hiđrocacbon (chỉ chứa C, H) và dẫn xuất của hiđrocacbon (gồm C, H và các nguyên tố khác).
3. Đặc điểmchungcủahợpchấthữucơ
- Liên kết chủ yếu trong hợp chất hữu cơ là liên kết cộng hóa trị.
- Các hợp chất hữu cơ thường có nhiệt độ nóng chảy, nhiệt độ sôi thấp, tan ít trong nước, tan nhiều trong các dung môi hữu cơ
- Phản ứng hữu cơ thường xảy ra chậm, không hoàn toàn và theo nhiều hướng khác nhau nên thường tạo ra hỗn hợp sản phẩm.
4.Phântích địnhtính: Nhằm xác định sự có mặt của các nguyên tố trong hợp chất hữu cơ.
Nguyên tắc: Chuyển hợp chất hữu cơ thành hợp chất đơn giản sau đó nhận biết bằng các phản ứng
đặc trưng.
5.Phântích địnhlượng: Nhằm xác định tỉ lệ khối lượng (hàm lượng) các nguyên tố trong hợp chất hữu cơ.
Nguyên tắc: Chuyển hợp chất hữu cơ thành hợp chất đơn giản sau đó dùng các phản ứng đặc trưng
để xác định và tính hàm lượng các nguyên tố theo công thức: nguyªn tè hîpchÊt
BÀITẬPTỰ LUẬN
m %m.100% m =
Câu1: Cho các chất sau: C2H4, CO2, CH4, Al4C3, CH3COOH, C2H7NO2, C6H12O6, CaCO3, C6H6, C2H5Cl, C2H5OH, C2H2, NaCN, NaHCO3. Hãy phân loại các chất trên vào bảng sau: Hợpchấthữucơ Hợpchấtvôcơ
Hiđrocacbon Dẫnxuấtcủahiđ
(b) Đốt cháy hoàn toàn một hiđrocacbon X, thu được hỗn hợp khí và hơi Y. Dẫn Y qua bình đựng H2SO4
đặc, thấy khối lượng bình tăng thêm 2,7 gam và có khí Z thoát ra. Dẫn khí Z vào bình đựng Ca(OH)2 dư, thu được 15 gam kết tủa trắng. (Đ/S: % C, %H lần lượt là 85,71%, 14,29%)
(c) Đốt cháy hoàn toàn 9 gam một hợp chất hữu cơ X, thu được hỗn hợp sản phẩm khí và hơi gồm CO2 và
H2O. Dẫn toàn bộ sản phẩm cháy vào bình đựng nước vôi trong dư, thu được 30 gam kết tủa đồng thời thấy khối lượng bình tăng thêm 18,6 gam. (Đ/S: % C, %H, %O lần lượt là 40%, 6,67%, 53,33%)
Câu3: Đốt cháy hoàn toàn 5,05 gam hợp chất X (chứa C, H, Cl) trong oxi dư, sau đó dẫn hỗn hợp sản phẩm qua dung dịch AgNO3 dư thu được 14,35 gam kết tủa trắng. Khí thoát ra cho hấp thụ vào dung dịch Ba(OH)2 dư thấy có 19,7 gam kết tủa. (Đ/S: % C, %H, %Cl lần lượt là 23,76%, 5,94%, 70,3%)
Câu4.[QG.20-201] Thí nghiệm xác định định tính nguyên tố cacbon và hidro trong phân tử saccarozơ được tiến hành theo các bước sau:
Bước1: Trộn đều khoảng 0,2 gam saccarozơ với 1-2 gam đồng(II) oxit, sau đó cho hỗn hợp ống nghiệm khô (ống số 1) rồi thêm tiếp khoảng 1 gam đồng(II) oxit để phủ kín hỗn hợp. Nhồi một nhúm bông có rắc một ít bột CuSO4 khan rồi cho vào phần trên của ống nghiệm số 1 rồi nút cao su có ống dẫn khí.
Bước2: Lắp ống nghiệm 1 lên giá thí nghiệm rồi nhúng ống dẫn khí vào dung dịch Ca(OH)2
đựng trong ống nghiệm (ống số 2).
Bước3: Dùng đèn cồn đun nóng ống số 1 (lúc đầu đun nhẹ, sau đó đun tập trung vào vị trí có hỗn hợp phản ứng).
Cho các phát biểu sau:
(a) Sau bước 3, màu trắng của CuSO4 chuyến thành màu xanh của CuSO4.5H2O.
(b) Thí nghiệm trên còn được dùng để xác định định tính nguyên tố oxi trong phân tử saccarozơ.
(c) Dung dịch Ca(OH)2 được dùng để nhận biết CO2 sinh ra trong thí nghiệm trên.
(d) Ở bước số 2, lắp ống số 1 sao cho miệng ống hướng lên.
(e) Kết thúc thí nghiệm, tắt đèn cồn, để ống số 1 nguội hẳn rồi mới đưa ống dẫn khí ra khỏi dung dịch trong ống số 2.
Số phát biểu đúng là
A. 2.
B. 3.
Hướngdẫngiải Bao gồm: a, c.
(b) Sai vì thí nghiệm chỉ dùng để định tính C và H.
C. 1.
D. 4.
(d) Sai vì phải lắp ống số 1 sao cho miệng ống hướng xuống dưới tránh trường hợp hóa chất ẩm, nước bay ra ngưng tụ và chảy ngược lại trong ống làm vỡ ống.
(e) Sai vì khi kết thúc thí nghiệm phải tắt đèn cồn sau tránh chênh lệch áp suất hút nước ngược trở lại vào ống nghiệm.
BÀITẬPTRẮCNGHIỆM
1.Mức độ nhậnbiết(rấtdễ vàdễ)
Câu1. Hoá học hữu cơ là ngành hoá học chuyên nghiên cứu
A. các hợp chất của cacbon.
B. các hợp chất của cacbon (trừ CO, CO2).
C. các hợp chất của cacbon (trừ CO, CO2, muối cacbonat, xianua, cacbua,…).
D. các hợp chất chỉ có trong cơ thể sống.
Câu2. Cặp hợp chất nào sau đây là hợp chất hữu cơ?
A. CO2, CaCO3. B. CH3Cl, C6H5Br. C. NaHCO3, NaCN. D. CO, CaC2.
Câu3. Dãy chất nào sau đây là hợp chất hữu cơ?
A. (NH4)2CO3, CO2, CH4, C2H6
C. CO2, K2CO3, NaHCO3, C2H5Cl.
Câu4. Trong thành phần của hợp chất hữu cơ
A. luôn có C và H.
C. luôn có C, H và O.
B. C2H4, CH4, C2H6O, C3H9N.
D. NH4HCO3, CH3OH, CH4, CCl4.
B. luôn có C, thường có H và O.
D. luôn có C và O, thường có H.
Câu5. Liên kết hóa học trong phân tử hợp chất hữu cơ chủ yếu là
A. liên kết ion.
C. liên kết cho - nhận.
Câu6. Các chất hữu cơ thường có đặc điểm chung là
A. phân tử luôn có các nguyên tố C, H và O.
B. có nhiệt độ nóng chảy cao.
B. liên kết cộng hóa trị.
D. liên kết hiđro.
C. khả năng phản ứng chậm và không theo một hướng xác định.
D. khó bị phân hủy dưới tác dụng nhiệt.
Câu7. Dẫn xuất hiđrocacbon là các hợp chất mà thành phần nguyên tố
A. chỉ có C và H.
C. ngoài C còn có các nguyên tố khác.
Câu8. Phản ứng hóa học của các chất hữu cơ thường
A. cần đun nóng và có xúc tác.
C. xảy ra rất nhanh.
B. gồm có C, H và O.
D. ngoài C và H còn các nguyên tố khác.
B. có hiệu suất cao.
D. tự xảy ra được.
Câu9. Phương pháp phân tích nhằm xác định các nguyên tố có mặt trong hợp chất hữu cơ bằng cách phân hủy hợp chất đó thành các chất vô cơ đơn giản rồi nhận biết bằng các phản ứng đặc trưng gọi là
A. phân tích hữu cơ.
C. phân tích định tính.
B. phân tích định lượng.
D. phân tích vô cơ.
Câu10. Để xác định hàm lượng các nguyên tố trong hợp chất hữu cơ, bạn có thể sử dụng phương
pháp phân tích nào sau đây?
A. phân tích định tính.
C. phân tích vi lượng.
2.Mức độ thônghiểu(trungbình)
B. phân tích định lượng.
D. phân tích hữu cơ.
Câu11. Nhóm chất nào dưới đây đều là dẫn xuất của hiđrocacbon?
A. CH2Cl2, CH2Br CH2Br, CHCl3, CH3COOCH3, C6H5CH3.
B. CH2Cl2, CH2=CH CHO, CH3COOH, CH2=CH2.
C. CHBr3, CH2=CH COOCH3, C6H5OH, C2H5OH, (CH3)3N.
D. CH3OH, CH2=CH Cl, C6H5ONa, CH≡C CH3.
Câu12. Nguyên tắc chung của phép phân tích định tính là
A. Chuyển hóa các nguyên tố C, H, N,… thành các chất vô cơ dễ nhận biết.
B. Đốt cháy hợp chất hữu cơ để tìm hiđro do có hơi nước thoát ra.
C. Đốt cháy hợp chất hữu cơ để tìm cacbon dưới dạng muội đen.
D. Đốt cháy hợp chất hữu cơ để tìm nitơ do có mùi khét.
Câu13. Để xác nhận trong phân tử chất hữu cơ có nguyên tố H người ta dùng phương pháp nào sau đây?
A. Đốt cháy rồi cho sản phẩm qua P2O5.
B. Đốt cháy rồi cho sản phẩm qua CuSO4 khan.
C. Đốt cháy thấy có hơi nước thoát ra.
D. Đốt cháy rồi cho sản phẩm cháy qua bình đựng H2SO4 đặc.
Câu14. Oxi hóa hợp chất hữu cơ X thành các sản phẩm vô cơ đơn giản. Qua phép phân tích nào sau đây có thể kết luận được trong X có hiđro?
A. Dẫn sản phẩm vào bình chứa dung dịch Ca(OH)2 dư thấy xuất hiện kết tủa trắng.
B. Dẫn sản phẩm vào bình chứa CuSO4 khan thì thấy một phần chất rắn không màu chuyển sang màu xanh.
C. Dẫn sản phẩm vào bình chứa dung dịch AgNO3 thấy xuất hiện kết tủa trắng.
D. Dẫn sản phẩm vào bình chứa dung dịch NaOH thấy thoát ra khí có mùi khai, có khả năng làm quỳ tím hóa xanh.
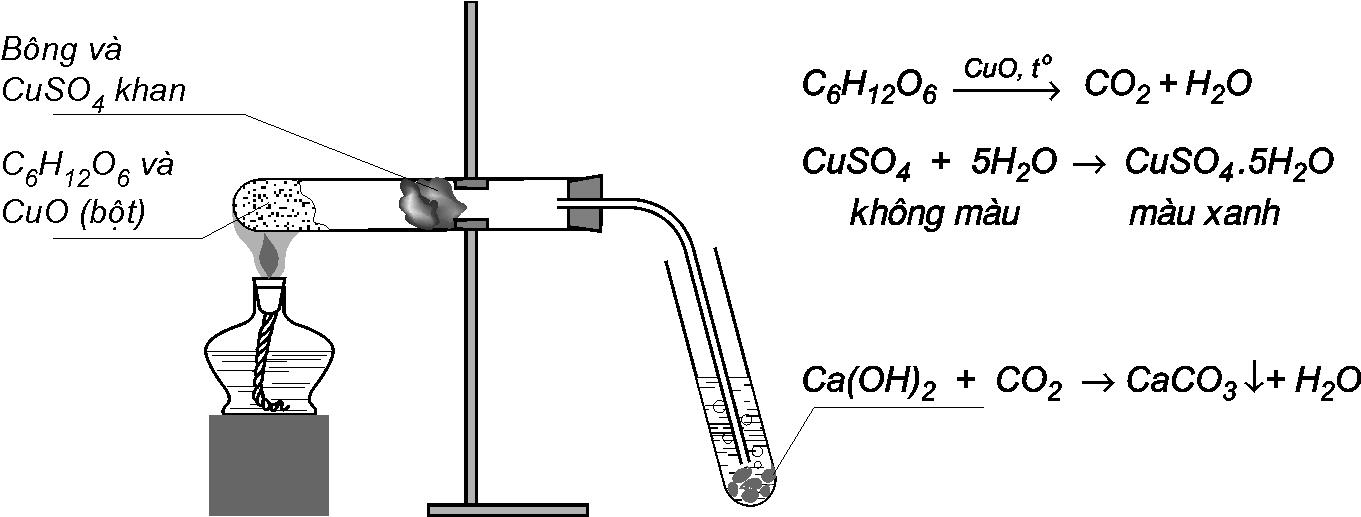
Câu15. Cho hình vẽ thí nghiệm phân tích định tính hợp chất hữu cơ C6H12O6:
Hãy cho biết vai trò của bông và CuSO4 khan trong thí nghiệm trên ?
A. Xác định sự có mặt của O.
C. Xác định sự có mặt của H.
B. Xác định sự có mặt của C và H.
D. Xác định sự có mặt củaC.
Câu16.(QG.15): Để phân tích định tính các nguyên tố trong hợp chất hữu cơ, người ta thực hiện một thí nghiệm được mô tả như hình vẽ:
Hợp chất hữu cơ và CuO Bông trộn CuSO4 khan
Dung dịch Ca(OH)2
Phát biểu nào sau đây đúng?
A. Thí nghiệm trên dùng để xác định clo có trong hợp chất hữu cơ
B. Trong thí nghiệm trên có thể thay dung dịch Ca(OH)2 bằng dung dịch Ba(OH)2.


C. Bông trộn CuSO4 khan có tác dụng chính là ngăn hơi hợp chất hữu cơ thoát ra khỏi ống nghiệm.
D. Thí nghiệm trên dùng để xác định nitơ có trong hợp chất hữu cơ
Câu17. Khi oxi hóa cacbon và hiđro trong hợp chất hữu cơ thành CO2 và H2O rồi dẫn qua bình
đựng dung dịch nước vôi trong dư thì
A. Khối lượng bình tăng lên và có kết tủa trắng xuất hiện.
B. Khối lượng bình giảm xuống và có chất rắn màu xanh xuất hiện.
C. Khối lượng bình tăng lên và có chất rắn màu xanh xuất hiện.
D. Khối lượng bình giảm xuống và có chất rắn màu trắng xuất hiện.
Câu18. Có thể xác định trong thành phần một chất hữu cơ X có clo hay không bằng cách
A. đun chất X với nước.
B. đốt cháy X, dẫn sản phẩm cháy vào dung dịch Ca(OH)2
C. đốt cháy X, dẫn sản phẩm cháy vào dung dịch AgNO3
D. đốt cháy X, dẫn sản phẩm cháy vào dung dịch H2SO4 đặc, nóng. Câu19. Đốt cháy một hợp chất hữu cơ chỉ chứa C, H, O rồi dẫn sản phẩm cháy qua bình chứa dung dịch H2SO4 đậm đặc thì thấy khối lượng bình tăng lên. Nguyên nhân là do H2SO4 đậm đặc đã hấp thụ chất nào trong sản phẩm cháy?
A. CO2. B. H2O. C. HCl. D. NH3. Câu20. Khi phân tích định tính để xác định cacbon trong chất hữu cơ, có thể thay dung dịch nước vôi trong bằng chất nào sau đây?
A. Dung dịch KOH. B. KOH rắn.
C. Dung dịch Ba(OH)2. D. Dung dịch H2SO4 đậm, đặc.
Câu21. Đốt cháy hoàn toàn hợp chất hữu cơ X thu được hỗn hợp CO2 và H2O. Dẫn hỗn hợp này qua bình đựng dung dịch nước vôi trong dư thu được 6 gam kết tủa trắng. Khối lượng cacbon trong X là
A. 0,72 gam. B. 2,64 gam. C. 0,005 gam. D. 0,05 gam.
qua bình đựng dung dịch H2SO4 đặc thì thấy khối lượng bình tăng lên 0,54 gam.
Khối lượng hiđro trong X là
A. 0,015 gam. B. 0,06 gam. C. 0,03 gam. D. 0,3 gam.
Câu23. Đốt cháy hoàn toàn hợp chất hữu cơ X thu được 4,48 lít CO2 (đktc) và 3,6 gam hơi nước. Khối lượng cacbon và hiđro trong X lần lượt là:
A. mC = 2,4 gam; mH = 0,4 gam. B. mC = 0,2 gam; mH = 2,4 gam.
C. mC = 0,4 gam; mH = 2,4 gam. D. mC = 2,4 gam; mH = 0,2 gam.
Câu24. Đốt cháy hoàn toàn hợp chất hữu cơ X thu được 896 ml CO2 (đktc) và 0,9 gam H2O. Số mol hiđro và cacbon trong X lần lượt là:
A. 0,04 và 0,05. B. 0,10 và 0,04. C. 0,05 và 0,04. D. 0,04 và 0,10.
Câu25. Đốt cháy hoàn toàn hợp chất hữu cơ X thu được hỗn hợp CO2 và H2O. Cho hỗn hợp này hấp thụ hoàn toàn vào bình đựng dung dịch Ca(OH)2 dư thì thấy xuất hiện 30 gam kết tủa, khối lượng bình tăng lên 18,6 gam. Khối lượng cacbon và hiđro trong X lần lượt là:
A. 3,6 gam và 0,3 gam.
C. 3,6 gam và 0,6 gam.
B. 0,6 gam và 3,6 gam.
D. 13,2 gam và 0,3 gam.
Câu26. Đốt cháy hoàn toàn 6 gam hợp chất hữu cơ X, thu được 4,48 lít (ở đktc) khí CO2 và 3,6 gam H2O. Khối lượng oxi trong X là
A. 3,2 gam.
B. 3,4 gam.
C. 3,5 gam. D. 4,3 gam.
Câu27. Đốt cháy hoàn toàn hợp chất hữu cơ X thu được hỗn hợp a mol CO2 và b mol H2O. Tổng số mol oxi nguyên tử trong sản phẩm (nO, sp) được tính theo công thức nào dưới đây?
A. O, sp na2b =+
C. O, sp n2ab =+
B. O, sp nab =+
D. O, sp n2a2b =+
Câu28. Đốt cháy hoàn toàn hợp chất hữu cơ X cần a mol O2 thu được b mol CO2 và c mol H2O. Số mol oxi nguyên tử trong hợp chất X (nO, X) được tính theo công thức nào dưới đây?
A. O, X n(bc)a =+−
C. O, X n(2bc)a =+−
B. O, X n(2bc)2a =+−
D. O, X n(b2c)2a =+−
Câu29. Đốt cháy hoàn toàn hợp chất hữu cơ X thu được CO2 và H2O. Dẫn hỗn hợp này qua bình
đựng dung dịch H2SO4 đặc thì thấy khối lượng bình tăng lên 0,54 gam. Khối lượng hiđro trong X là
A. 0,015 gam B. 0,06 gam C. 0,03 gam D. 0,3 gam
Câu30. Đốt cháy hoàn toàn 4,4 gam hợp chất hữu cơ X cần dùng vừa đủ 11,2 lít O2 (đktc), chỉ tạo ra CO2 và H2O. Tổng khối lượng sản phẩm cháy là
A. 20,4 gam B. 12,4 gam C. 11,6 gam D. 3,6 gam
Câu31. Đốt cháy hoàn toàn 8,8 gam hợp chất hữu cơ X cần dùng vừa đủ V lít O2 (đktc), tạo ra
8,96 lít CO2 và 7,2 gam H2O. V có giá trị là
A. 20,4 lít. B. 12,4 lít. C. 11,2 lít D. 3,6 lít.
Câu32. Để đốt cháy hoàn toàn 2,85 gam hợp chất hữu cơ X cần dùng vừa đủ 4,2 lít O2 (đktc). Sản phẩm cháy chỉ có a gam CO2 và b gam H2O
A. 28,07 %. B. 44,44 %.
29,63 %. D. 45,71 %.
Câu33. Đốt cháy hoàn toàn 9 gam hợp chất X thu được 17,6 gam CO2; 12,6 gam H2O và 2,24 lít N2 (đktc). Thành phần phần trăm khối lượng oxi (%mO) trong hợp chất X là
A. O %m15,56 = B. O %m31,11 = C. O %m0,00 = D. O %m23,33 =
Câu34. Đốt cháy hoàn toàn 10,4 gam hợp chất hữu cơ B thu được 13,2 gam CO2; 7,2 gam H2O và 2,24 lít N2 (đktc). Phần trăm khối lượng oxi (%mO) trong hợp chất B là
A. O %m30,77 = B. O %m48,08 =
C. O %m34,62 = D. O %m44,23 =
3.Mức độ vậndụng(khá)
Câu35. Đốt cháy hexan C6H14 rồi dẫn sản phẩm cháy vào bình đựng dung dịch nước vôi trong thấy xuất hiện kết tủa trắng X. Lọc tách kết tủa trắng rồi đun sôi dung dịch Y còn lại thì lại th
Câu37. β-caroten là một chất hữu cơ có trong thành phần củ cà rốt. β-caroten có thể chuyển thành
vitamin A nên còn được gọi là “tiền vitamin A”. Khi oxi hóa hoàn toàn β-caroten thu được một hỗn hợp sản phẩm khí và hơi X gồm CO2 và H2O. Dẫn hỗn hợp X lần lượt qua bình chứa CuSO4 khan (bình 1) và Ca(OH)2 dư (bình 2). Kết quả cho thấy, một phần CuSO4 không màu ở bình 1 chuyển dần sang chất rắn Y màu xanh; ở bình 2 xuất hiện kết tủa trắng Z. Y và Z lần lượt là
A. CuSO4.5H2O và Ca(HCO3)2.
C. CaCO3 và CuSO4.5H2O.
B. CuSO4.5H2O và CaCO3.
D. CuSO4 và CaCO3. Hướngdẫngiải
OCuSOCa(OH) 23 CuSO.5HO
42
CO carotenCOCaCO HO β + −→→→↓ Y:
Câu38. Đốt cháy hoàn toàn hợp chất hữu cơ A thu được hỗn hợp khí và hơi X gồm CO2, H2O và HCl. Dẫn hỗn hợp X qua bình chứa CuSO4 khan thì thấy xuất hiện chất rắn Y màu xanh. Dẫn hỗn hợp X qua bình chứa AgNO3 thì xuất hiện kết tủa Z màu trắng. Dẫn hỗn hợp X vào bình chứa dung dịch Ca(OH)2 dư thì thấy xuất hiện kết tủa T màu trắng. Cho cho biết T, Y và Z lần lượt là
Cho các phát biểu về đặc điểm chung của các phân tử hợp chất hữu cơ:
(1) Thành phần nguyên tố chủ yếu là C và H.
(2) Có thể chứa nguyên tố khác như Cl, N, P, O.
(3) Liên kết hóa học chủ yếu là liên kết cộng hoá trị
(4) Liên kết hoá học chủ yếu là liên kết ion.
(5) Dễ bay hơi, khó cháy.
(6) Phản ứng hoá học xảy ra nhanh.
Các phát biểu đúng là
A. (4), (5), (6). B. (1), (2), (3). C. (1), (3), (5). D. (2), (4), (6). Hướngdẫngiải
Bao gồm: 1, 2, 3.
(4) Sai vì liên kết hóa học chủ yếu trong hợp chất hữu cơ là liên kết cộng hóa trị.
(5) Sai vì các hợp chất hữu cơ dễ cháy.
(6) Sai vì phản ứng hóa học của các hợp chất hữu cơ thường xảy ra chậm, không hoàn toàn.
m19,244.0,57,23,65m13,65gam 35,5.0,1 nn0,1mol%m.100%26%. 13,65
hợp khí và hơi gồm
3 gam hợp chất hữu cơ X bằng CuO dư ở nhiệt độ cao thu được hỗn
ợ
BTNT(N)
NNN 14.0,1 n2n0,1mol%m.100%46,67%.
Bước1: Trộn đều khoảng 0,2 gam saccarozơ với 1 đến 2 gam đồng (II) oxit, sau đó cho hỗn hợp vào ống nghiệm khô (ống số 1) rồi thêm tiếp khoảng 1 gam đồng (II) oxit để phủ kín hỗn hợp. Nhồi một nhúm bông có rắc bột CuSO4 khan vào phần trên ống số 1 rồi nút bằng nút cao su có ống dẫn khí.
Bước2: Lắp ống số 1 lên giá thí nghiệm rồi nhúng ống dẫn khí vào dung dịch Ca(OH)2 đựng trong ống nghiệm (ống số 2).
Bước3: Dùng đèn cồn đun nóng ống số 1 (lúc đầu đun nhẹ, sau đó đun tập trung vào phần có hỗn hợp phản ứng).
Cho các phát biểu sau
(a) CuSO4 khan được dùng để nhận biết H2O sinh ra trong ống nghiệm.
(b) Thí nghiệm trên, trong ống số 2 có xuất hiện kết tủa trắng.
(c) Ở bước 2, lắp ống số 1 sao cho miệng ống hướng lên.
(d) Thí nghiệm trên còn được dùng để xác định định tính nguyên tố oxi trong phân tử saccarozơ
(e) Kết thúc thí nghiệm: tắt đèn cồn, để ống số 1 nguội hẳn rồi mới đưa ống dẫn khí ra khỏi dung dịch trong ống số 2.
A.
3.
Bao gồm: a, b.
(c) Sai vì phải lắp ống số 1 sao cho miệng ống hướng xuống dưới tránh trường hợp hóa chất ẩm, nước bay ra ngưng tụ và chảy ngược lại trong ống làm vỡ ống.
(d) Sai vì thí nghiệm chỉ dùng để định tính C và H.
(e) Sai vì khi kết thúc thí nghiệm phải tắt đèn cồn sau tránh chênh lệch áp suất hút nước ngược trở lại vào ống nghiệm. Câu46.[QG.20-203] Thí nghiệm xác định định tính nguyên tố cacbon và hidro trong phân tử saccarozơ được tiến hành theo các bước sau:
Bước 1: Trộn đều khoảng 0,2 gam saccarozơ với 1-2 gam đồng(II) oxit, sau đó cho hỗn hợp ống nghiệm khô (ống số 1) rồi thêm tiếp khoảng 1 gam đồng(II) oxit để phủ kín hỗn hợp. Nhồi một nhúm bông có rắc một ít bột CuSO4 khan rồi cho vào phần trên của ống nghiệm số 1 rồi nút cao su có ống dẫn khí.
Bước 2: Lắp ống nghiệm 1 lên giá thí nghiệm rồi nhúng ống dẫn khí vào dung dịch Ca(OH)2 đựng trong ống nghiệm (ống số 2).
Bước 3: Dùng đèn cồn đun nóng ống số 1 (lúc đầu đun nhẹ, sau đó đun tập trung vào vị trí có hỗn hợp phản ứng).
Cho các phát biểu sau:
(a) Ở bước 2, lắp ống số 1 sao cho miệng ống hướng lên.
(b) Thí nghiệm trên, CuO có vai trò chuyển nguyên tố C thành CO2, nguyên tố H thành H2O.
(c) Thí nghiệm trên còn được dùng để xác định định tính nguyên tố oxi trong phân tử saccarozơ.
(d) Dung dịch Ca(OH)2 được dùng để nhận biết CO2 sinh ra trong thí nghiệm trên.
(e) Kết thúc thí nghiệm: tắt đèn cồn, để ổng số 1 nguội hẳn rồi mới đưa ống dẫn khi ra khỏi dung dịch trong ống số 2.
Số phát biểu đúng là
A. 2. B. 4. C. 1. D. 3. Hướngdẫngiải Bao gồm: b, d.
(a) Sai vì phải lắp ống số 1 sao cho miệng ống hướng xuống dưới tránh trường hợp hóa chất ẩm, nước bay ra ngưng tụ và chảy ngược lại trong ống làm vỡ ống.
(c) Sai vì thí nghiệm chỉ dùng để định tính C và H.
(e) Sai vì khi kết thúc thí nghiệm phải tắt đèn cồn sau tránh chênh lệch áp suất hút nước ngược trở lại vào ống nghiệm.
Câu47.[QG.20-204] Thí nghiệm xác định định tính nguyên tố cacbon và hidro trong phân tử saccarozơ được tiến hành theo các bước sau:
Bước1: Trộn đều khoảng 0,2 gam saccarozơ với 1 đến 2 gam đồng (II) oxit, sau đó cho hỗn hợp ống nghiệm khô (ống số 1) rồi thêm tiếp khoảng 1 gam đồng (II) oxit để phủ kín hỗn hợp. Nhồi một nhúm bông có rắc bột CuSO4 khan vào phần trên của ống số 1 rồi nút bằng nút cao su có ống dẫn khí.
Bước2: Lắp ống số 1 lên giá thí nghiệm rồi nhúng ống dẫn khí vào dung dịch Ca(OH)2 đựng trong ống nghiệm (ống số 2).
Bước3: Dùng đèn cồn đun nóng ống số 1 (lúc đầu đun nhẹ, sau đó đun tập trung vào phần có hỗn hợp phản ứng).
Cho các phát biểu sau:
(a) Sau bước 3, màu trắng của CuSO4 khan chuyển thành màu xanh của CuSO4.5H2O.
(b) Thí nghiệm trên, trong ống số 2 có xuất hiện kết tủa trắng.
(c) Ở bước 2, lắp ống số 1 sao cho miệng ống hướng lên.
(d) Thí nghiệm trên còn được dùng để xác định định tính nguyên tố oxit trong phân tử saccarozơ
(e) Kết thúc thí nghiệm: tắt đèn cồn, để ống số 1 nguội hẳn rồi mới đưa ống dẫn khí ra khỏi dung dịch trong ống số 2.
Số phát biểu đúng là
A. 4. B. 3. C. 1. D. 2. Hướngdẫngiải Bao gồm: a, b.
(c) Sai vì phải lắp ống số 1 sao cho miệng ống hướng xuống dưới tránh trường hợp hóa chất ẩm, nước bay ra ngưng tụ và chảy ngược lại trong ống làm vỡ ống.
(d) Sai vì thí nghiệm chỉ dùng để định tính C và H.
(e) Sai vì khi kết thúc thí nghiệm phải tắt đèn cồn sau tránh chênh lệch áp suất hút nước ngược trở lại vào ống nghiệm.
KIẾNTHỨCCẦNNHỚ
1.Côngthứctổngquát: Cho biết thành phần nguyên tố trong hợp chất hữu cơ: CxHyOzNtXv.
2.Côngthức đơngiảnnhất: Cho biết tỉ lệ tối giản về số nguyên tử của các nguyên tố trong hợp chất hữu cơ
3.Côngthứcphântử: Cho biết số lượng nguyên tử mỗi nguyên tố trong hợp chất hữu cơ. D
- Giả sử hợp chất hữu cơ có công thức tổng quát: CxHyOzNt. Để xác định công thức đơn giản nhất ta xác định tỉ lệ nguyên tử các nguyên tố thông qua:
+ Hàm lượng các nguyên tố: %C%H%O%N
+ Số mol các nguyên tố: CHON x:y:z:tn:n:n:n =
VÍDỤ MINHHỌA
Câu1: Thiết lập công thức đơn giản nhất của các hợp chất hữu cơ trong các trường hợp sau:
(a) Khi phân tích vitamin A ta thu được 83,9 %C; 10,5%H, còn lại là O. (Đ/S: C20H30O)
(b) Khi phân tích một hợp chất hữu cơ X người ta thu được 32 %C; 6,67 %H; 42,67 %O, còn lại là nitơ. (Đ/S: C2H5O2N)
(c) Khói thuốc lá làm tăng khả năng bị ung thư phổi, hoạt chất có độc trong thuốc lá là nicotin. Phân tích nguyên tố định lượng cho thành phần phần trăm khối lượng như sau:74,031%C, 8,699%H, 17,27%N. (Đ/S: C5H7N)
(d) Đioxin là chất độc Hoá Học mà Quân đội Mĩ dùng nhiều trong chiến tranh với mục đích làm rụng lá cây rừng, trong đó nhiều nhất là ở Việt Nam. Phân tích nguyên tố cho thấy Đioxin có phần trăm khối lượng các nguyên tố C, H và Cl tương ứng là 44,72%; 1,24%; 44,10%, còn lại là oxi.
(Đ/S: C6H2OCl2)
Câu2: Thiết lập công thức đơn giản nhất của các hợp chất hữu cơ trong các trường hợp sau:
(a) Đốt cháy 5,8 gam một hợp chất hữu cơ X bằng oxi dư, sau phản ứng thu được 8,96 lít khí CO2
(đktc) và 9 gam H2O. (Đ/S: C2H5)
(b) Đốt cháy hoàn toàn 1,89 gam melamin thu được 0,81 gam H2O; 1,008 lít CO2 và 1,008 lít khí
(đktc) N2. (Đ/S: CH2N2)
(c) Đốt cháy hoàn toàn 9 gam một hợp chất hữu cơ X, thu được hỗn hợp sản phẩm khí và hơi gồm CO2 và H2O. Dẫn toàn bộ sản phẩm cháy vào bình đựng nước vôi trong dư, thu được 30 gam kết tủa. Khối lượng bình tăng thêm 18,6 gam. (Đ
Câu1. Hợp chất hữu cơ X có 80 % khối lượng là cacbon, còn lại là hiđro. Công thức đơn giản nhất của X là
A. CH3 B. C3H10 C. CH4 D. C4H5.
Câu2. Hợp chất hữu cơ X có 82,76 % khối lượng là cacbon, còn lại là hiđro. Công thức đơn giản nhất của X là
A. CH5. B. C5H.
C. C2H5. D. C5H2.
Câu3. Kết quả phân tích nguyên tố trong hợp chất X cho biết phần trăm khối lượng các nguyên tố là %C = 40,00; %H = 6,67; còn lại là oxi. Công thức đơn giản nhất của hợp chất X là
A. C2H4O. B. CH2O.
C. CHO. D. C2HO2.
Câu4. Trong phân tử hợp chất hữu cơ X, phần trăm khối lượng của cacbon và hiđro lần lượt bằng 52,17 % và 13,04 %, còn lại là oxi. Công thức đơn giản nhất của X là
A. C2H2O. B. CH2O.
C. C2H6O. D. CHO.
Câu5. Khi phân tích thành phần khối lượng các nguyên tố trong vitamin C, thu được kết quả: %C = 40,91; %O = 54,55; còn lại là hiđro. Công thức đơn giản nhất của phân tử vitamin C là
A. C2H5O2. B. C3H4O3. C. C3H5O3.
D. C3H6O3.
Câu6. Trước kia, “phẩm đỏ” dùng để nhuộm áo choàng cho các Hồng y giáo chủ được tách chiết từ một loài ốc biển. Đó là một hợp chất có thành phần nguyên tố như sau: 45,70 %C; 1,90 %H; 7,60 %O; 6,70 %N; 38,10 %Br. Công thức đơn giản của phẩm đỏ là
A. C4H8O2NBr2.
B. C2H4ONBr. C. C8H4ONBr. D. C4H2ONBr. Câu7. Hợp chất X có chứa ba nguyên tố C, H, O với số mol mỗi nguyên tố lần lượt là 0,03; 0,06 và 0,015 mol. Công thức đơn giản nhất của X là
A. C3H6O5. B. CH2O5. C. C2H4O.
D. CH2O.
Câu8. Phân tích định lượng hợp chất hữu cơ X ta thấy tỉ lệ khối lượng các nguyên tố là mC : mH :
mO = 24 : 6 : 16. Công thức đơn giản nhất của hợp chất X là
A. CH3O.
B. C2H6O.
C. C12H3O8.
D. C2H3O.
Câu9. Đốt cháy hoàn toàn 8,8 gam hợp chất hữu cơ X thu được 8,96 lít CO2 (đktc) và 7,2 gam
nước. Công thức đơn giản nhất của X là
A. CH2O. B. C2H4 C. C2H4O. D. CH3O.
Câu10. Đốt cháy hoàn
ẠNG2:THIẾTLẬPCÔNGTHỨCPHÂNTỬ HỢPCHẤTHỮUCƠ
Dạng2.1Thiếtlậpcôngthứcphântử hợpchấthữucơ dựavàohàmlượngcácnguyêntố
LÝTHUYẾTVÀPHƯƠNGPHÁPGIẢI
✧✧ Bàitoán: Cho hợp chất hữu cơ X có hàm lượng các nguyên tố là %mC; %mH; %mO; … Phân
✧
tử khối của X là MX. Xác định công thức phân tử của X.
✧
✧✧ Phương pháp:
-Bước1: Gọi công thức của X là: CxHyOzNt. Từ tỉ lệ nguyên tử các nguyên tố ⇒ CTĐG
CHON %m%m%m%m
-Bước2: Từ CTĐG và phân tử khối ⇒ hệ số n ⇒ CTPT của X.
Chúý: %mC + %mH + %mO + %mN = 100%
VÍDỤ MINHHỌA
Câu1: Tính khối lượng mol phân tử của các chất sau:
(a) Hợp chất hữu cơ X có tỉ khối so với hiđro là 22.
(b) Tỉ khối hơi của X so với heli bằng 18,5.
(c) Hợp chất hữu cơ Y có tỉ khối hơi so với không khí bằng 2,07
(d) Thể tích hơi của 3,3 gam chất X bằng thể tích của 1,76 gam khí oxi (đo ở cùng điều kiện). a b c d
MX = 44 MX = 74 MY = 60 MX = 60
Câu2: Thiết lập công thức phân tử của X trong các trường hợp sau:
(a) Vitamin A có công thức đơn giản nhất là C20H30O. Khối lượng mol của vitamin A gấp 6,5 lần khối lượng mol của CO2. (Đ/S: C20H30O)
(b) Hợp chất hữu cơ X có %C = 85,8%; %H = 14,2%. Phân tử khối của X là 56 đvC. (Đ/S: C4H8)
(c) Người ta xác định được % khối lượng các nguyên tố trong vitamin C: %C = 40,91% ; %H = 4,545% ; %O = 54,545%. Xác định CTPT biết Mvitamin C = 176 đvC. (Đ/S: C6H8O6)
(d) Phenolphtalein là chất chỉ thị màu dùng để nhận biết dung dịch bazơ có % về khối lượng C, H,
O lần lượt là 75,47%; 4,35% và 20,18%. Khối lượng mol phân tử của phenolphtalein = 318 (g/mol). Tìm công thức phân tử của phenolphtalein? (Đ/S: C20H14O4)
(e) Hợp chất hữu cơ X có %C = 51,3%; %H = 9,4%; %N = 12%; %O = 27,3%. Tỉ khối hơi của X
đối với không khí là 4,034. (Đ/S: C5H11O2N)
(g) Hợp chất hữu cơ X có %C = 49,58%; %H = 6,44%. Khi hoá hơi hoàn toàn 5,45 gam X, thu
được 0,56 lít hơi (đktc). (Đ/S: C9H14O6)
Câu3: Khói thuốc lá làm tăng khả năng bị ung thư phổi, hoạt chất có độc trong thuốc lá là nicotin.
Xác định khối lượng phân tử của nicotin có giá trị 162 đvC. Phân tích nguyên tố định lượng cho
thành phần phần trăm khối lượng như sau: 74,07%C, 8,65%H, 17,28%N. Xác định CTPT của nicotin. (Đ/S: C10H14N2)
Câu4: Đioxin là chất độc Hoá Học mà Quân đội Mĩ dùng nhiều trong chiến tranh với mục đích làm rụng lá cây rừng, trong đó nhiều nhất là ở Việt Nam. Phân tích nguyên tố cho thấy Đioxin có phần trăm khối lượng các nguyên tố C, H và Cl tương ứng là 44,72%; 1,24%; 44,10%, còn lại là oxi. Biết tỉ khối của Đioxin so với nitơ là 11,5. Xác định CTPT của đioxin. (Đ/S: C12H4O2Cl4)
BÀITẬPTỰ LUYỆN
Câu1. Phân tích thành phần hợp chất X thu được kết quả về hàm lượng các nguyên tố như sau: %C = 34,62; %H = 3,84; còn lại là oxi. Tỉ khối của X so với heli là 26, công thức phân tử của X là
A. CHO. B. C3H4O4. C. C4H3O3. D. C3H4O2.
Câu2. Phân tích thành phần của hợp chất hữu cơ Y thu được kết quả về hàm lượng các nguyên tố như sau: %O = 40,00; %H = 10,00; còn lại là một nguyên tố#A. Biết rằng 0,5 mol Y có khối lượng bằng 1 mol hơi CH3COOH ở cùng điều kiện nhiệt độ và áp suất. Công thức phân tử của Y là
A. C5H12O3. B. C2H8O3.
Câu3. Khi phân
61,02; %H = 15,52; còn lạ
ợp chất hữu cơ X thu được các kết quả sau: %C = 49,40; %H = 9,80; %N = 19,18; còn lại là oxi. Tỉ khối của A so với heli bằng 18,25. Công thức phân tử của A là
A. C3H6NO.
B. C3H7NO.
C. C3H8NO.
D. C3H9NO.
Câu5. Khi phân tích thành phần hợp chất hữu cơ X thu được các số liệu thực nghiệm như sau: %C = 54,54; %H = 9,09; còn lại là oxi. 0,5 mol X có khối lượng bằng 1 mol CO2 ở cùng điều kiện nhiệt độ và áp suất. Công thức phân tử của X là
A. C4H7O2
Câu6.(M.15): Từ tinh dầu hồi, người ta tách được anetol là một chất thơm được dùng sản xuất kẹo cao su. Anetol có tỉ khối hơi so với N2 là 5,286. Phân tích nguyên tố cho thấy, anetol có phần trăm khối lượng cacbon và hiđro tương ứng là 81,08%; 8,10%, còn lại là oxi. Công thức phân tử của anetol là
Dạng2.2Thiếtlậpcôngthứcphântử hợpchấthữucơ dựavàophản ứngcháy
LÝTHUYẾTVÀPHƯƠNGPHÁPGIẢI
✧ Bàitoán: Đốt cháy hợp chất hữu cơ X thu
MX. Tìm công thức phân tử của X.
PTPƯ cháy: ot xyzt2222 yzyt CHON(x)OxCOHON 4222 ++−→++
a X là
✧
✧✧ Phươngpháp:
–Bước1: Gọi công thức của X là CxHyOzNt. Tính số mol các sản phẩm cháy
Ca(OH)2, NaOH.
⇒ mbình (1) tăng = 2 HO m; mbình (2) tăng = 2 CO m
4. Dẫn CO2, H2O, N2 qua bình đựng dung dịch Ca(OH)2, Ba(OH)2
⇒ mbình tăng = 22 COHOmm + ; mdd tăng = 22 COHO mmm↓ +− ; mdd giảm = 22 COHO m(mm) ↓ −+
5. Trong cùng điều kiện áp suất, to thì tỉ lệ về thể tích bằng tỉ lệ về số mol.
VÍDỤ MINHHỌA
Câu1: Lập công thức phân tử của các hợp chất hữu cơ trong các trường hợp sau:
(a) Từ ơgenol (trong tinh dầu hương nhu) điều chế được metylơgenol là chất dẫn dụ côn trùng. Khi
đốt cháy hoàn toàn 8,9 gam metylơgenol thu được 24,2 gam CO2 ; 6,3 gam H2O. Tỉ khối hơi của X so với heli là 44,5. (Đ/S: C11H14O2)
(b) Paracetamol (X) là thành phần chính của thuốc hạ sốt và giảm đau. Đốt cháy hoàn toàn 5,285 gam X, thu được 2,835 gam H2O; 12,32 gam CO2 và 0,392 lít N2 (đktc). Tỉ khối hơi của X so với hiđro là 75,5. (Đ/S: C8H9O2N)
(c) Đốt cháy hoàn toàn 1,88 gam X (chứa C, H, O) cần 1,904 lít khí O2 (đktc), thu được CO2 và H2O với tỷ lệ mol tương ứng là 4:3. Biết công thức phân tử trùng với công thức đơn giản nh
16
(d) Đốt cháy 14,8 gam một hợp chất hữu cơ X (chỉ chứa C, H, O) trong oxi dư, dẫn sản phẩm cháy qua bình (1) đựng P2O5, sau đó dẫn qua bình (2) đựng dung dịch nước vôi trong dư thấy khối lượng
bình (1) tăng 10,8 gam, bình (2) xuất hiện 60 gam kết tủa. Khi hóa hơi 14,8 gam X thu được thể tích bằng thể tích của 6,4 gam oxi ở cùng điều kiện. (Đ/S: C3H6O2) Hướngdẫngiải
C2H6O)
Câu2. Đốt cháy hoàn toàn 0,18 gam hợp chất X chứa C, H, O cho 0,006 mol CO2 và 0,108 gam
H2O. Tỉ khối hơi của X so với hiđro bằng 30. Công thức phân tử của X là
A. CHO. B. CH2O.
C2H4O2
C2H2O2
Câu3. Đốt cháy hoàn toàn một hợp chất hữu cơ E cần dùng vừa đủ 0,784 lít O2 (đktc), thu được 0,03 mol CO2 và 0,36 gam nước. Biết tỉ khối của E so với heli là 14. Công thức phân t
CO
và 4 lít h
i nước (các thể tích đo ở cùng điều kiện nhiệt độ và áp suất). Công thức phân tử của hợp chất X là
A. C3H8O5.
B. C3H4O2.
C. C3H8. D. C3H4O5.
Câu5. Đốt cháy hoàn toàn 1 lít hợp chất hữu cơ Y cần vừa đủ 2 lít O2, tạo thành 2 lít CO2 và 2 lít hơi nước (các thể tích đo ở cùng điều kiện nhiệt độ và áp suất). Công thức phân tử của hợp chất Y là
A. C2H2O2.
B. CH2O.
C. C2H4O2. D. CHO.
Câu6. Đốt cháy hoàn toàn 2 lít hơi chất hữu cơ Z cần vừa đủ 7 lít O2, tạo thành 6 lít CO2 và 6 lít hơi nước (các thể tích khí đo ở cùng điều kiện nhiệt độ và áp suất). Công thức phân tử của hợp chất Z là
A. C6H7O5.
B. C3H3O2.
C. C6H12O4.
D. C3H6O2.
Câu7. Đốt cháy hoàn toàn 20 ml hơi hợp chất hữu cơ X (chỉ gồm C, H, O) cần vừa đủ 110 ml O2, thu được 160 ml hỗn hợp Y gồm khí và hơi. Dẫn Y qua dung dịch H2SO4 đặc (dư) thì còn lại 80 ml khí Z. Biết các thể tích khí và hơi đo ở cùng điều kiện. Công thức phân tử của X là
A. C4H8O2. B. C4H10O. C. C3H8O. D. C4H8O.
Câu8. Đốt cháy hoàn toàn 7,5 gam hợp chất hữu cơ X thu được một hỗn hợp gồm CO2, H2O, N2
Dẫn hỗn hợp sản phẩm lần lượt qua các bình chứa P2O5 (bình 1) và nước vôi trong dư (bình 2). Sau
khi các phản ứng xảy ra hoàn toàn, chỉ còn lại một khí duy nhất có thể tích 1,12 lít. Khối lượng bình 1 tăng 4,5 gam còn bình 2 xuất hiện 20 gam kết tủa trắng. Công thức phân tử của X là
cphântử hợpchấthữucơ thôngquabiệnluận LÝTHUYẾTVÀPHƯƠNGPHÁPGIẢI
✧✧ Bàitoán: Cho hợp chất hữu cơ X có khối lượng phân tử MX. Tìm công thức phân tử của X.
✧
Hoặc đốt cháy hợp chất hữu cơ X, cho ít (thiếu) dữ kiện. Tìm công thức phân tử của X.
✧
✧✧Phươngpháp:
–Bước1: Gọi công thức của X là CxHyOz (thường X chỉ chứa C, H; C, H, O hoặc C, H, N).
–Bước2: Dựa vào đề bài lập phương trình chứa x, y, z. Giải phương trình nghiệm nguyên tìm x, y, z.
–Bước3: Dựa vào dữ kiện (nếu có), suy ra nghiệm phù hợp.
Chúý:1. Trong các hợp chất hữu cơ chứa C, H, O thì số H luôn là số chẵn và y ≤ 2x+2
2. Bài toán có thể có nhiều nghiệm.
3. Trong công thức đơn giản, số nguyên tử mỗi nguyên tố là nhỏ nhất có thể.
VÍDỤ MINHHỌA
Câu1: Giải các phương trình sau tìm x, y, z biết rằng x, y, z nguyên dương:
(a) 12x + y = 40. (b) 12x + y = 44. (c) 12x + y + 16z = 46. a b c
+ x = 1, y = 28
+ x = 2, y = 16
+ x = 3, y = 4
+ x = 1, y = 32 + x = 2, y = 20 + x = 3, y = 8
Câu2: Xác định công thức phân tử của X trong các trường hợp sau:
+ x = 1, y = 18, z = 1
+ x = 2, y = 6, z = 1
+ x = 1, y = 2, z = 2
(a) Hiđrocacbon X là thành phần chính của khí gas có khối lượng phân tử là 44. (Đ/S: C3H8)
(b) Hiđrocacbon Y là thường dùng làm dung môi để hòa tan các chất hữu cơ có tỉ khối hơi so với hiđro là 39. (Đ/S: C6H6)
(c) Khi bị kiến hoặc ong đốt ta thấy buốt đó là do trong nọc độc của chúng chứa hợp chất axit fomic. Phân tích axit fomic người ta thấy nó chứa C, H, O trong đố số C nhỏ hơn số O và có khối lượng phân tử là 46. (Đ/S: CH2O2)
Câu3: Tìm CTPT của hợp chất hữu cơ A biết MA < 70 g/mol; A chứa C, H, O và 53,33% oxi về khối lượng. (Đ/S: CH2O và C2H4O2)
BÀITẬPTỰ LUYỆN
Câu1. Hợp chất hữu cơ X chỉ chứa C và H có tỉ khối so với hiđro bằng 15. Công thức phân tử của
X là
A. C3H8
B. C4H8
C. C4H10
D. C2H6. Câu2. Hiđrocacbon Y có tỉ khối so với hiđro bằng 29. Số nguyên tử H trong Y là
A. 6. B. 8.
C. 10.
Câu3. Hiđrocacbon X có tỉ khối so với heli bằng 13,5. Số nguyên tử C trong X là
A. 2. B. 3.
C. 4.
D. 12.
D. 5.
Câu4. Ancol etylic (chứa C, H, O) có tỉ khối so với hiđro bằng 23. Số nguyên tử H trong ancol etylic là
A. 2. B. 4.
C. 6.
D. 8.
Câu5. Ancol etylic (chứa C, H, O) có tỉ khối so với hiđro bằng 23. Trong ancol etylic có số nguyên tử oxi khác số nguyên tử hiđro. Số nguyên tử H trong ancol etylic là
A. 2. B. 4. C. 6. D. 8.
Câu6. Giấm gạo là dung dịch axit axetic 5%. Khi hóa hơi 12 gam axit axetic (chứa C, H, O) ta thu
được thể tích hơi bằng thể tích của 0,4 gam khí hiđro ở cùng điều kiện. Axit axetic có số nguyên tử oxi chẵn. Số nguyên tử C trong axit axetic là
A. 1. B. 2. C. 3. D. 4.
KIẾNTHỨCCẦNNHỚ
1.Thuyếtcấutạohóahọc
- Trong phân tử hchc, các nguyên tử liên kết với nhau theo đúng hóa trị và thứ tự nhất định: C(IV), N (III), O (II), H, F, Cl, Br, I (I).
- Trong phân tử hợp chất hữu cơ, cacbon có hóa trị IV. Nguyên tử cacbon không chỉ liên kết với
nguyên tử của các nguyên tố khác mà còn có thể liên kết với nhau thành mạch cacbon (mạch thẳng, mạch nhánh, mạch vòng).
- Tính chất của các chất phụ thuộc thành phần phân tử và cấu tạo hóa học.
2.Liênkết đơn, đôi,ba
- Liên kết đơn: gồm 1 liên kết δ: “–”.
- Liên kết đôi: gồm 1 liên kết δ + 1 liên kết π: “=”
- Liên kết ba: gồm 1 liên kết δ + 2 liên kết π: “≡”
3.Côngthứccấutạo
- Biểu diễn thứ tự và cách thức liên kết giữa các nguyên tử trong phân tử.
4. Đồng đẳng, đồngphân
– Đồng đẳng là hiện tượng các chất có cấu tạo và tính chất tương tự nhau, nhưng CTPT hơn kém nhau một hay nhiều nhóm CH2. Các chất đó hợp thành dãy chất gọi là dãy đồng đẳng.
– Đồngphân là hiện tượng các chất khác nhau (cấu tạo, cấu trúc không gian) nhưng có cùng CTPT. Các chất đó gọi là các đồng phân của nhau.
BÀITẬPTỰ LUẬN
Câu1: Viết các công thức cấu tạo có thể có của các hợp chất hữu cơ có công thức sau:
C4H10
CH3 –CH2 –CH2 –CH3
CH3 –CH(CH3)–CH3
C3H7Cl
CH3 –CH2 –CH2Cl
CH3 –CHCl–CH3
C3H9N
CH3 –CH2 –CH2 –NH2
CH3 –CH(NH2)–CH3
CH3 –NH–CH2 –CH3
(CH3)3N
C3H6
CH2=CH-CH3
C3H8O
CH3 –CH2 –CH2OH
CH3 –CH(OH)–CH3
CH3 –O–CH2 –CH3
C2H4O2 (mạchhở)
CH3COOH
HCOOCH3
HO–CH2 –CHO
Câu2: Viết công thức cấu tạo mạch hở có thể có của các hợp chất hữu cơ sau và cho biết chất nào có đồng phân hình học? Tính số liên kết xich ma (δ) và số liên kết pi (π) trong mỗi trường hợp.
C4H8
(1)CH2 =CH–CH2 –CH3
(2)CH3 –CH=CH–CH3
(3)CH2=C(CH3)2
(1)CH2=CH-CH2-CH2-CH3
C5H10
(2)CH3 –CH=CH-CH2-CH3
(3)CH2=C(CH3)-CH2-CH3
(4)CH3-C(CH3)=CH-CH3
Đồng phân hình học: (2).
Số liên kết δ:11.
Số liên kết π: 1.
Đồng phân hình học: (2).
Số liên kết δ: 14.
Số liên kết π: 1.
(5)CH3-CH(CH3
t(rấtdễ vàdễ)
Câu1. Theo thuyết cấu tạo hóa học, trong phân tử các chất hữu cơ, các nguyên tử liên kết với nhau
A. theo đúng hóa trị.
B. theo một thứ tự nhất định.
C. theo đúng số oxi hóa.
D. theo đúng hóa trị và theo một thứ tự nhất định.
Câu2. Để biết rõ số lượng nguyên tử, thứ tự liên kết và kiểu liên kết của các nguyên tử trong phân tử hợp chất hữu cơ người ta dùng công thức nào sau đây?
A. Công thức phân tử
C. Công thức cấu tạo.
B. Công thức tổng quát.
D. Công thức đơn giản nhất.
Câu3. Công thức thu gọn nào sau đây tương ứng với công thức phân tử C3H4O2?
A. CH3COOCH3
C. HCOOCH2CH3.
B. CH2=CH COOH.
D. CH≡C COOH.
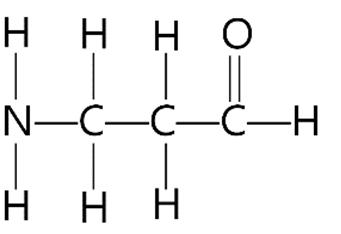
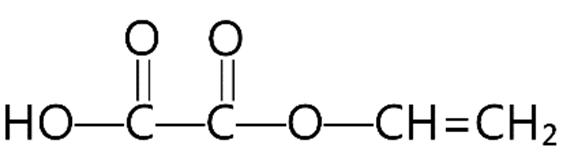
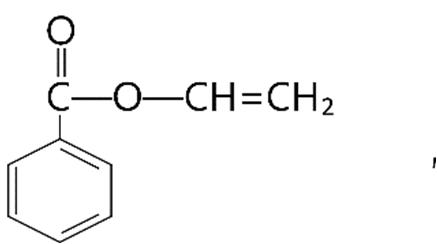
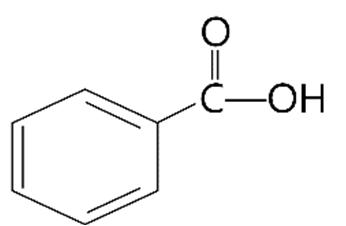
Câu4. Xác định công thức cấu tạo thu gọn của hợp chất sau:
A. CH3CH2CH2COOH.
C. CH3CH2CH2OH.
B. CH3CH2COOH.
D. CH3CH2CHOHCHO.
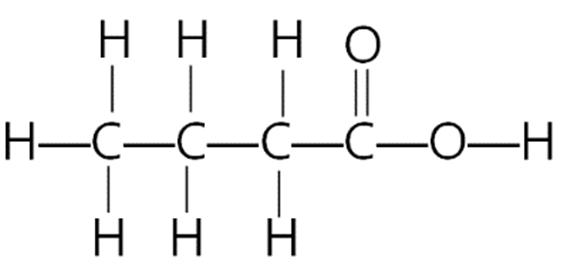
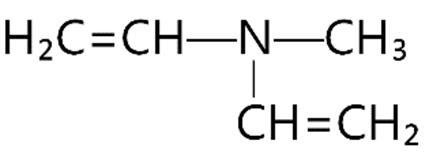
Câu5. Xác định công thức cấu tạo thu gọn của hợp chất sau:
A. NH2CH2CH2CHO.
C. NH2CH2CH2COOH.
Câu6. Đồng phân là
B. NH2CH2CHO.
D. NH2C2H4CHO.
A. những hợp chất có cùng phân tử khối nhưng có cấu tạo hóa học khác nhau.
B. những hợp chất có cùng công thức phân tử nhưng có cấu tạo hóa học khác nhau.
C. những hợp chất có cùng công thức phân tử nhưng có tính chất hóa học khác nhau.
D. những chất khác nhau nhưng có cùng công thức phân tử.
Câu7. Hiện tượng các chất có cấu tạo và tính chất hoá học tương tự nhau, phân tử hơn kém nhau một hay nhiều nhóm metylen (–CH2–) được gọi là hiện tượng
A. đồng phân. B. đồng vị C. đồng đẳng. D. đồng khối. Câu8. Chất nào sau đây là đồng đẳng của CH ≡ CH?
A. CH2=C=CH2. B. CH2=CH‒CH=CH2.
C. CH≡C CH3
D. CH2=CH2
Câu9. Hợp chất nào sau đây là đồng đẳng của axit axetic CH3COOH?
A. HCOOH. B. CH3COOCH3.
C. HOCH2COOH. D. HOOC COOH.
Câu10. Hợp chất nào sau đây là đồng đẳng của axit axetic CH3COOH?
A. HCOOH.
B. CH3COCH3.
C. HOCH2COOH. D. HOOC COOOH.
Câu11.[MH-2021] Cặp chất nào sau đây cùng dãy đồng đẳng?
A. CH4 và C2H4.
C. C2H4 và C2H6.
B. CH4 và C2H6.
D. C2H2 và C4H4.
Câu12. Công thức thu gọn nào sau đây tương ứng với công thức phân tử C3H4O2?
A. CH3COOCH3.
B. CH2=CH COOH.
C. HCOOCH2CH3 D. CH≡C COOH.
Câu13. Trong những dãy chất sau đây, dãy nào có các chất là đồng phân của nhau?
A. C2H5OH, CH3OCH3.
C. CH3CH2CH2OH, C2H5OH.
B. CH3OCH3, CH3CHO.
D. C4H10, C6H6
Câu14. Chất nào sau đây là đồng phân cấu tạo của isopentan (CH3)2CHCH2CH3?
A. CH3CH2CH2CH2CH2CH3.
C. CH3CH2CH2CH2CH3.
B. (CH3)2CH CH(CH3)2.
D. CH3CH2CH2CH3
Câu15. Công thức cấu tạo nào dưới đây là đồng phân của axit propionic CH3CH2COOH?
A. CH2=CH COOCH3.
C. CH3COOCH=CH2.
Câu16. Hai chất CH3COOCH3 và HCOOCH2CH3 là
A. Đồng đẳng.
C. Đồng vị
2.Mức độ thônghiểu(trungbình)
Câu17. Hai chất có công thức:
B. HOCH2CH2CHO.
D. CH3CH2COCH3.
B. Đồng phân cấu tạo.
D. Cùng một chất.
C6H5 - C - O - CH3 vµ CH3 - O - C - C6H5
Nhận xét nào sau đây đúng?
A. Là các công thức của hai chất có cùng công thức phân tử nhưng có cấu tạo khác nhau.
B. Là các công thức của hai chất có cùng công thức phân tử những có cấu tạo tương tự nhau.
C. Là các công thức của hai chất có công thức phân tử và cấu tạo đều khác nhau.
D. Chỉ là công thức của một chất vì công thức phân tử và cấu tạo đều giống nhau.
Câu18. Cho các hợp chất chứa vòng thơm: (X) C6H5OH, (Y) CH3C6H4OH, (Z) C6H5CH2OH, (T)
C2H3C6H4OH. Những hợp chất thuộc cùng một dãy đồng đẳng là:
A. X, Z.
B. X, Y, Z.
Câu19. Chất nào sau đây có đồng phân hình học?
A. CHCl=CH CH3
C. CH3 C≡C CH3.
C. Y, X. D. X, Y, T.
B. CH3 CH2 CH2 CH3
D. CH3 CH=C(CH3)2.
Câu20. Hợp chất hữu cơ nào sau đây không có đồng phân cis-trans?
A. CHCl=CHCl.
C. CH3CH=CHCH3.
Câu21. Chất nào sau đây có đồng phân hình học?
B. CH3CH2CH=C(CH3)CH3
D. CH3CH2CH=CHCH3.
A. 33 CHCCCH. −≡−
C. 22 CHClCHCl.
Câu22. Chất nào sau đây có đồng phân hình học?
A. CH2=CH–CH=CH2.
C. CH3–CH=C(CH3)2.
B. 33 CHCHCHCH. −=−
D. 23 CHCClCH. =−
B. CH3–CH=CH–CH=CH2.
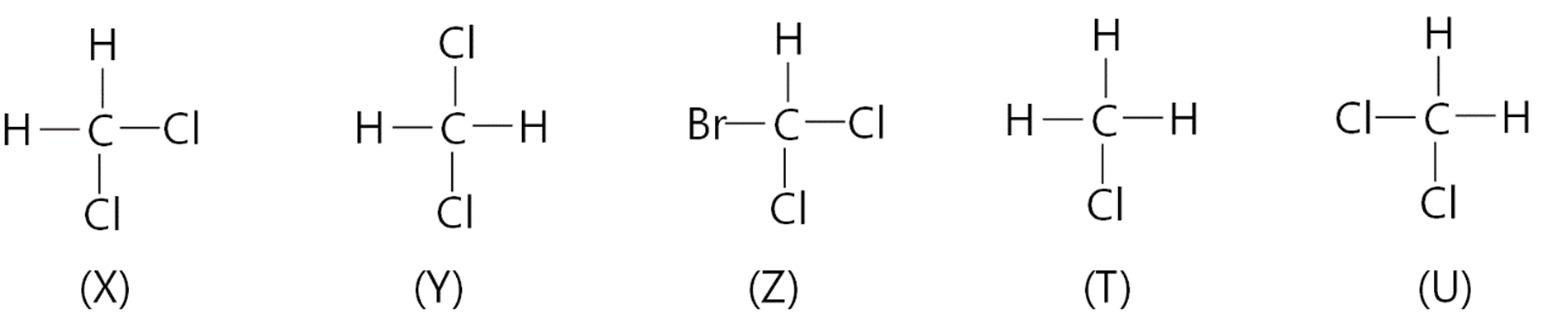
D. CH2=CH–CH2–CH3.
Câu23. Công thức cấu tạo thu gọn nhất của một hợp chất X như sau:
Công thức cấu tạo thu gọn của X là
A. CH2=CH CH2 CH=CH2.
C. CH2=CH CH=CH2.
B. CH2=C=CH2.
D. CH3 CH=CH CH3.
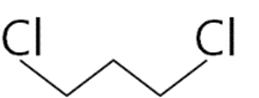
Câu24. Công thức cấu tạo thu gọn nhất của một hợp chất Y như sau:
Công thức cấu tạo thu gọn của Y là
A. Cl CH2CH2 Cl.
C. Cl CH2CH2CH2 Cl.
Câu25. Nhận xét nào sau đây đúng?
B. CH3CH2CH2CHCl2
D. C3H6Cl2
A. Các chất có cùng công thức đơn giản nhất sẽ có cùng công thức phân tử
B. Nhiều hợp chất hữu cơ khác nhau nhưng có công thức đơn giản nhất giống nhau.
C. Các chất đồng phân của nhau thì có công thức phân tử khác nhau nhưng có công thức đơn giản nhất giống nhau.
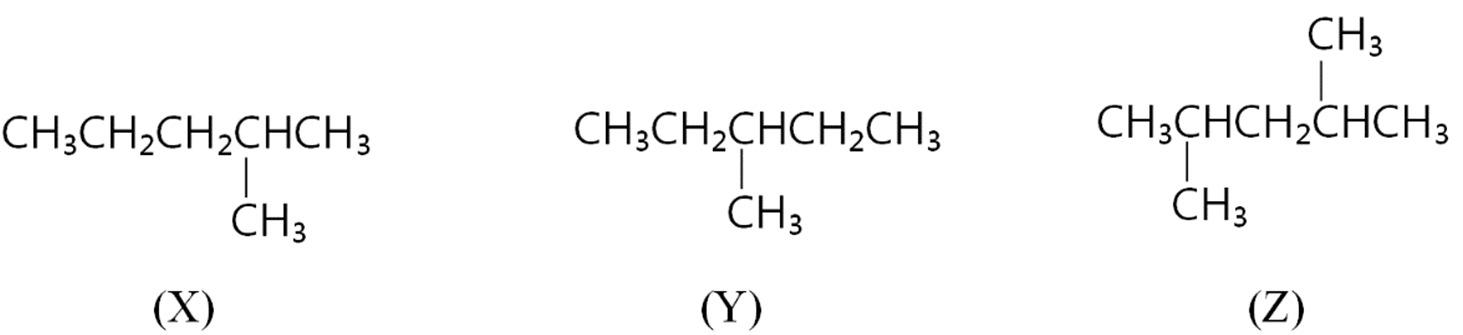
D. Các chất đồng đẳng thì có công thức phân tử giống nhau. Câu26. Cho ba công thức cấu tạo sau:
Kết luận nào sau đây là đúng?
A. X, Y, Z là đồng phân vị trí mạch cacbon.
B. X là đồng đẳng của Y và Z; Y và Z là đồng phân cấu tạo.
C. X, Y, Z thuộc ba dãy đồng đẳng khác nhau.
D. X và Y là đồng phân cấu tạo; Z là đồng đẳng của X và Y. Câu27. Những công thức nào dưới đây biểu diễn cùng một chất:
A. X, Y, Z. B. X, T, U.
3.Mức độ vậndụng(khá)
Câu28. Cho các cặp chất:
(1) CH3CH2OH và CH3OCH3
(3) CH2=CH CH2OH và CH3CH2CHO
C. X, Y, U.
D. Y, T, U.
(2) CH3CH2Br và BrCH2CH3

(4) (CH
)2NH và CH3CH2NH2
Có bao nhiêu cặp là đồng phân cấu tạo?
A. 1. B. 2. C. 3. D. 4.
Hướngdẫngiải
Bao gồm: (1), (3), (4)
(2) là cùng một chất.
Câu29. Cho các cặp chất:
(1) CH3CH2COOH và HCOOCH2CH3
(2) CH3CH2CH2OH và CH3CH2OCH3
Có bao nhiêu cặp là đồng phân cấu tạo?
(3) CH3NHCH3 và NH2CH2NH2
(4) CH2=CH COOH và HCOO CH=CH2
A. 1. B. 2. C. 3. D. 4.
Hướngdẫngiải
Bao gồm: (1), (2), (4).
(3) Khác công thức phân tử.
Câu30. Trong các dãy chất sau đây, có mấy dãy gồm các chất là đồng đẳng của nhau?
(1) C2H6, CH4, C4H10;
(3) CH3OCH3, CH3CHO;
A. 1.
Bao gồm: (1), (2).
B. 4.
Câu31. Cho các chất sau đây:
(I) CH3 CH(OH) CH3
(III) CH3 CH2 CH2 OH
(V) CH3 CH2 CH2 CH2 OH
Các chất đồng đẳng của nhau là
A. (I), (II) và (VI).
C. (II), (III), (V) và (VI).
(2) C2H5OH, CH3CH2CH2OH;
(4) CH3COOH, HCOOH, C2H3COOH
C. 2.
Hướngdẫngiải
(II) CH3 CH2 OH
D. 3.
(IV) CH3 CH2 CH2 O CH3
(VI) CH3 OH
B. (I), III và (IV).
D. (I), (II), (III), (IV).
KIẾNTHỨCCẦNNHỚ
1.Kháiniệm: Độ bất bão hòa (kí hiệu: k; k≥ 0) là khái niệm trong hóa học hữu cơ nhằm xác
định số liên kết pi và số vòng.
2.Cáchtính
(a) Dựa theo công thức cấu tạo: k = số liên kết pi + số vòng.
Qui ước: 1 liên kết đôi: k = 1; 1 liên kết ba: k =2; 1 vòng: k = 1.
(b) Dựa theo công thức phân tử:
+ Với hợp chất CxHy hoặc CxHyOz: +− = 2x2y k
+ Với hợp chất CxHyOzNtXv (X là halogen: F, Cl, Br, I): ++−+ = (2x2t)(yv) k
THĐB: Trong các muối amoni thì (2x2t)(yv)z k 22 ++−+ =+
3. Ứngdụngcủa độ bấtbãohòa
(a) Xây dựng công thức dãy đồng đẳng. Hiđrocacbon: CnH2n+2-2k.
(b) Viết đồng phân của hợp chất hữu cơ
BÀITẬPTỰ LUẬN
Câu1: Tính độ bất bão hòa của các hợp chất sau:
(a) CH3-CH2-CH2-CH3; (b) CH2=CH-CH3; (c)
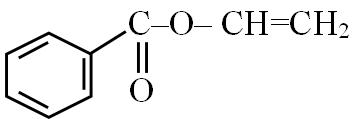
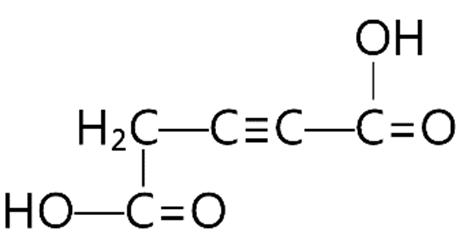
Câu2: Tính độ bất bão hòa của các hợp chất sau:
Câu3. Vitamin A có công thức phân
k=6=5
a
k
t ba. Trong phân tử vitamin A có bao nhiêu liên kết đôi?
C4H8
k=1=1vhoặc1π
CH2 =CH–CH2 –CH3
CH3 –CH=CH–CH3
CH2=C(CH3)2
C4H6
k=2=2π:2C=C,1C≡Choặc2v
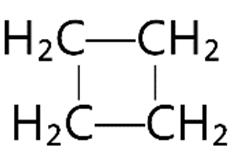
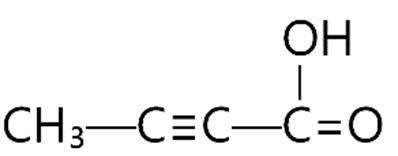
CH2=C=CH-CH3
CH2=CH-CH=CH2
CH≡C-CH2-CH3
CH3-C≡C-CH3
C5H8 (mạchhở)
k=2=2π:2C=Choặc1C≡C
CH2=C=C-CH2-CH3
CH2=CH-CH=CH-CH3
CH2=CH-CH2-CH=CH2
CH2=C(CH3)-CH=CH2
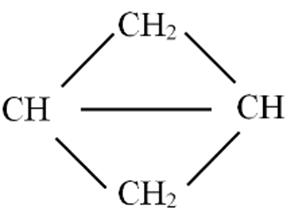
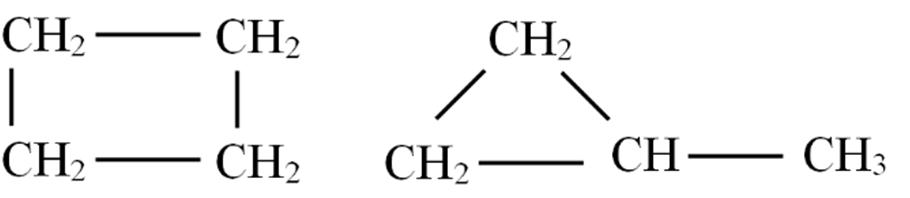
CH≡C-CH2-CH2-CH3
CH3-C≡C-CH2-CH3
CH≡C-CH(CH3)2
BÀITẬPTRẮCNGHIỆM
1.Mức độ nhậnbiết(rấtdễ vàdễ)
C2H4O2 (mạchhở,chứa–CO-)
k=1=1πC=O
CH3COOH
HCOOCH3
HO-CH2-CHO
Câu1. Theo quy ước, một liên kết đôi hoặc một vòng tương ứng với độ bất bão hòa là
A. k = 0. B. k = 1
C. k = 2.
Câu2. Theo quy ước, một liên kết ba tương ứng với độ bất bão hòa là
A. k = 0. B. k = 1.
C. k = 2.
D. k = 3
D. k = 3.
Câu3. Hợp chất hữu cơ X có công thức cấu tạo như sau: CH≡C CH=CH CH=O. Độ bất bão hòa của X là
A. k = 1. B. k = 2.
Câu4. Hợp chất X1 có công thức cấu tạo như sau:
C. k = 3.
D. k = 4.
Độ bất bão hòa của X1 là
A. k = 0. B. k = 1.
Câu5. Hợp chất X2 có công thức cấu tạo như sau:
C. k = 2.
D. k = 3.
Độ bất bão hòa của X2 là
A. k = 0.
B. k = 1.
C. k = 2.
Câu6. Hợp chất X3 có công thức cấu tạo như sau: CH≡C CH=CH CH=O
D. k = 3.
Độ bất bão hòa của X3 là
A. k = 1. B. k = 2.
Câu7. Hợp chất X4 có công thức cấu tạo như sau:
C. k = 3.
D. k = 4.
Độ bất bão hòa của X4 là
A. k = 3. B. k = 4.
Câu8. Hợp chất X5 có công thức cấu tạo như sau:
Độ bất bão hòa của X5 là
A. k = 1. B. k = 2.
Câu9. Hợp chất X6 có công thức cấu tạo như sau:
C. k = 5.
D. k = 6.
Độ bất bão hòa của X6 là
A. k = 2. B. k = 3.
Câu10. Hợp chất X7 có công thức cấu tạo như sau:
C. k = 3.
D. k = 4.
Độ bất bão hòa của X7 là
A. k = 4. B. k = 6.
Câu11. Hợp chất X8 có công thức cấu tạo như sau:
C. k = 4.
D. k = 5.
C. k = 7.
D. k = 5.
Độ bất bão hòa của X8 là
A. k = 2. B. k = 3.
C. k = 4.
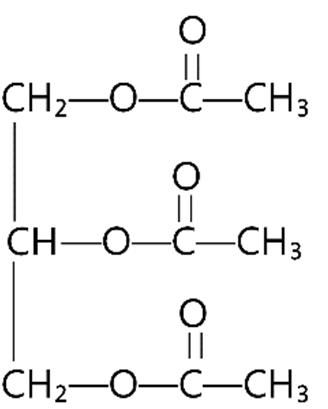
Câu12. Công thức tính độ bất bão hòa của hợp chất CxHyOz là:
A. 2x2y k 2 +− =
C. xyz k 2 ++ =
B. xyz k+1 2 ++ =
D. x2y2 k 2 −+ =
Câu13. Công thức tính độ bất bão hòa của hiđrocacbon CxHy là:
A. xy2 k 2 ++ =
D. k = 5.
B. xy1 k 2 ++ =
C. x2y k 2 +− = D. 2x2y k 2 +− =
Câu14. Độ bất bão hòa của hợp chất có công thức C5H12 là
A. k = 0 B. k = 1
C. k = 2 D. k = 3
Câu15. Độ bất bão hòa của hợp chất có công thức C3H4O2 là
A. k = 1. B. k = 2.
C. k = 3. D. k = 4.
Câu16. Độ bất bão hòa của hợp chất có công thức phân tử C3H8O là
A. k = 0. B. k = 1.
C. k = 2. D. k = 3.
Câu17. Độ bất bão hòa của hợp chất có công thức phân tử C2H5OH là
A. k = 0. B. k = 1.
k = 2.
Câu18. Độ bất bão hòa của hợp chất có công thức phân tử C12H22O11 là
A. k = 0. B. k = 1.
k = 2.
Câu19. Độ bất bão hòa của hợp chất có công thức phân tử C3H4O là
A. k = 0. B. k = 1.
2.Mức độ thônghiểu(thônghiểu)
k = 3.
k = 3.
C. k = 2. D. k = 3.
Câu20. Độ bất bão hòa của hợp chất có công thức CH3CHO là
A. k = 1. B. k = 2.
C. k = 3.
Câu21. Độ bất bão hòa của hợp chất có công thức C17H31COOH là
A. k = 1. B. k = 2.
C. k = 3.
Câu22. Độ bất bão hòa của hợp chất có công thức phân tử C3H5(COOH)3 là
A. k = 0. B. k = 1.
C. k = 2.
Câu23. Độ bất bão hòa của hợp chất có công thức phân tử C17H33COOH là
A. k = 0. B. k = 1.
C. k = 2.
D. k = 4.
D. k = 4.
D. k = 3.
D. k = 3.
Câu24. Độ bất bão hòa của hợp chất có công thức phân tử OH-C3H5(COOCH3)2 là
A. k = 0. B. k = 1.
C. k = 2.
Câu25. Công thức tính độ bất bão hòa của amin đơn chức CxHyN là
A. 2x+2y k 2 = B. 2x+2(1y) k 2 −+ =
C. 2x+21y k 2 +− =
D. k = 3.
D. 2.(x1)y k 2 +− =
Câu26. Công thức tính độ bất bão hòa của hợp chất CxHyOzNtXv (X = halogen) là
A. (2x+2t)(yv) k 2 +−+ = .
C. (2xt)(yv) k. 2 +−+ =
Câu27. Công thức tổng quát của hiđrocacbon là A. CnH2n + 2 - 2k.
Câu28. Công thức dãy đồ
B. (2x+2tz)(yv) k 2 ++−+ = .
D. (2xt)(yvz) k 2 +−++ =
Câu31.(A.13): Số đồng phân cấu tạo, mạch hở ứng với công thức phân tử C4H6 là A. 2. B. 5.
4.
Câu32. Số lượng đồng phân ứng với công thức phân tử C5H12 là
A. 3. B. 5.
4.
Câu33. Số lượng đồng phân ứng với công thức phân tử C4H9Cl là
A. 3. B. 4.
Câu34. Hợp chất C2H6O có tổng số đồng phân là
A. 4. B. 3.
Câu35. Hợp chất C4H10O có tổng số đồng phân là
A. 4. B. 7.
5.
2.
6.
Câu36. Số lượng đồng phân ứng với công thức phân tử C3H9N là
A. 5. B. 7. C. 6.
Câu37. Số lượng đồng phân ứng với công thức phân tử C4H11N là
A. 7. B. 8.
C. 9.
3.
2.
6.
5.
5.
4.
D. 10.
Câu38. Số lượng đồng phân mạch hở, có hai liên kết đôi, ứng với công thức phân tử C4H6 là
A. 3. B. 4. C. 5. D. 2.
Câu39. Số lượng đồng phân mạch hở, có hai liên kết đôi, ứng với công thức phân tử C5H
đây không đúng?
A. Mentol là dẫn xuất của hiđrocacbon.
B. Mentol có cấu tạo mạch hở
C. Mentol có cấu tạo mạch vòng.
D. Mentol có nhiệt độ sôi thấp hơn muối ăn (NaCl).
Hướngdẫngiải
k=2=1πC=C +1v
Câu43.(CĐ-2008): Công thức đơn giản nhất của một hiđrocacbon là CnH2n+1. Hiđrocacbon đó thuộc dãy đồng đẳng của
A. ankan. B. ankin. C. ankađien. D. anken. Hướngdẫngiải CTPT có d
Câu44.(ĐHB-2009): Ba hiđrocacbon X, Y, Z là đồng đẳng kế tiếp, khối lượng phân tử của Z
bằng 2 lần khối lượng phân tử của X. Các chất X, Y, Z thuộc dãy đồng đẳng
A. ankan. B. ankađien. C. anken. D. ankin.
Hướngdẫngiải ZYXXX24 MM14M282MM24:CHAnken =+=+=
1.Phânloạiphản ứngtronghóahọchữucơ
Loạiphản ứng Dạngphươngtrìnhhóahọc
Phản ứngthế là PƯ trong đó một nguyên tử hoặc nhóm nguyên tử trong phân tử hchc bị thay thế bằng một nguyên tử hoặc nhóm nguyên tử khác. A + B oxt,t → C + D
Phản ứngcộng là PƯ trong đó phân tử hchc kết hợp với phân tử khác tạo thành phân tử hợp chất mới.
Phản ứngtách là PƯ trong đó hai hay nhiều nguyên tử bị tách khỏi phân tử hợp chất hữu cơ.
2. Đặc điểmcủaphản ứnghóahọctronghóahọchữucơ
- Các phản ứng hữu cơ thường xảy ra chậm do các liên kết trong phân tử hợp chất hữu cơ ít phân
cực, khó bị phân cắt.
- Phản ứng hữu cơ thường sinh ra hỗn hợp sản phẩm do các liên kết trong phân tử hữu cơ có độ
bền khác nhau không nhiều, có thể bị phân cắt đồng thời.
BÀI TẬP TỰ LUẬN
Câu 1: Cho phương trình hóa học của các phản ứng:
(a) C2H6 + Br2 as → C2H5Br + HBr
(b) C2H4 + Br2 → C2H4Br2
(c) C2H5OH + HBr oxt,t →C2H5Br + H2O
(d) C6H14 oxt,t → C3H6 + C3H8
(e) C6H12 + H2 oxt,t → C6H14
(g) C6H14 oxt,t → C2H6 + C4H8
Trong các phản ứng trên, phản ứng thuộc loại phản ứng thế là (a),(c).
phản ứng thuộc loại phản ứng cộng là (b),(e).
phản ứng thuộc loại phản ứng tách là (d),(g).
Câu 2: Hoàn thành chuỗi phản ứng sau:
(1)(2)(3) 223232 CHCHCHCHCHCHOHCHCHBr ≡→=→−→−
(1)CH≡CH+H2 o 3 Pd/PbCO,t → CH2=CH2
(2)CH2=CH2 +H2O oH,t + → C2H5OH (3)C2H5OH+HBr ot → C2H5Br+H2O
C. một vài nguyên tử hoặc nhóm nguyên tử bị tách ra khỏi phân tử
D. phân tử bị phá hủy hoàn toàn thành các nguyên tử hoặc phân tử nhỏ hơn. Câu2. Loại phản ứng nào được định nghĩa là: “Trong phản ứng, một vài nguyên tử hoặc nhóm nguyên tử bị tách ra khỏi phân tử”?
A. Phản ứng thế
C. Phản ứng tách.
B. Phản ứng cộng.
D. Phản ứng đốt cháy.
Câu3. Loại phản ứng nào được định nghĩa là: “Trong phản ứng, phân tử hợp chất hữu cơ kết hợp với phân tử khác tạo thành phân tử hợp chất mới”?
A. Phản ứng thế
C. Phản ứng tách.
2.Mức độ thônghiểu(trungbình)
B. Phản ứng cộng.
D. Phản ứng đốt cháy.
Câu4. Phản ứng CH3 OH + HBr → CH3 Br + H2O thuộc loại phản ứng nào sau đây?
A. phản ứng cộng.
C. phản ứng thế
B. phản ứng tách.
D. phản ứng phân hủy.
Câu5. Phản ứng CH3COOH + C2H5OH → CH3COOC2H5 + H2O thuộc loại phản ứng nào sau đây?
A. phản ứng cộng.
C. phản ứng tách.
B. phản ứng thế
D. phản ứng phân hủy.
Câu6. Phản ứng CH3COOH + CH ≡ CH → CH3COOCH = CH2 thuộc loại phản ứng nào sau đây?
A. Phản ứng thế
C. Phản ứng tách.
B. Phản ứng cộng.
D. Không thuộc về ba loại phản ứng trên.
Câu7. Phản ứng 2CH3OH → CH3OCH3 + H2O thuộc loại phản ứng nào sau đây?
A. Phản ứng thế.
C. Phản ứng tách.
B. Phản ứng cộng.
D. Không thuộc về ba loại phản ứng trên.
Câu8. Phản ứng CH ≡ CH + 2AgNO3 + 2NH3 → AgC ≡ CAg + 2NH4NO3 thuộc loại phản ứng nào sau đây?
A. Phản ứng thế.
C. Phản ứng tách.
3.Mức độ vậndụng(khá)
Câu9. Cho các phản ứng sau:
(1) CH3CH3 + Br2 as → CH3CH2Br + HBr
(2) CH2=CH2 + Br2 → Br CH2CH2 Br
(3) C3H8 + 5O2 o t → 3CO2 + 4H2O
(4) CH2=CH2 + 3O2 o t → 2CO2 + 2H2O
(5) HCOOH + CH3OH → HCOOCH3 + H2O
Những phản ứng nào thuộc loại phản ứng thế?
Câu10. Cho các phản ứng sau:
(1) CH3CH2CH3 + Cl2 as → CH3CHClCH3 + HCl
(2) CH2=CH2 + Cl2 → CH2Cl CH2Cl
(3) C2H6 + 7 2 O2 o t → 2CO2 + 3H2O
(4) C6H6 + Br2 o Fe t → C6H5Br + HBr
(5) C2H2 + 2HBr → C2H4Br2
B. Phản ứng cộng.
D. Không thuộc về ba loại phản ứng trên.
Phản ứng nào thuộc loại phản ứng cộng?
A. 1 và 2. B. chỉ 2. C. 2 và 5. D. 3 và 4. Câu11. Cho các phản ứng sau:
(1) CH≡CH + Cl2 → CH3CHCl2
(2) CH3COOC2H5 + NaOH → CH3COONa + C2H5OH
(3) C2H5OH → 24 o HSO®Æc 170C CH2=CH2 + H2O
(4) C6H14 o xt, t, p → C3H6 + C3H8
(5) CH3CH3 o xt, t, p → CH2=CH2 + H2
Phản ứng nào thuộc loại phản ứng tách?
A. 1, 2, 4, 5. B. 3, 4, 5. C. 2, 3, 4, 5. D. 2, 3. Câu12. Khi nung nóng khí etan C2H6 xúc tác kim loại, thu được etilen C2H4 và khí hiđro. Phương trình hóa học và loại phản ứng của quá trình trên là
A. C2H4 + H2 o xt t → C2H6 (cộng).
C. C2H6 o xt t → C2H4 + H2 (tách).
B. C2H6 o xt t → C2H4 + H2 (thế).
D. C2H4 + H2 o xt t → C2H6 (tách).
1. Hợp chất hữu cơ là hợp chất của cacbon trừ CO, CO2, H2CO3, CaCO3, NaHCO3, HCN, NaCN, Al4C3, CaC2, …
2. Phân tích định tính nhằm xác định nguyên tố nào có trong hợp chất hữu cơ
Phân tích định lượng nhằm xác định hàm lượng (%m) của nguyên tố trong hợp chất hữu cơ.
3. Công thức tổng quát cho biết thành phần nguyên tố: CxHyOzNtXv
4. Công thức đơn giản nhất cho biết tỉ lệ số nguyên tử mỗi nguyên tố.
5. Công thức phân tử cho biết số lượng nguyên tử mỗi nguyên tố.
6. Trong hợp chất hữu cơ nhất thiết phải chứa C, thường chứa H, O, N, Cl, ...
7. Liên kết chủ yếu trong hóa học hữu cơ là liên kết cộng hóa trị.
Liên kết đơn: “−” chứa 1 liên kết xich ma (δ); liên kết đôi “=” chứa 1δ + 1π; liên kết ba “≡” chứa 1δ + 2π.
8. Phản ứng hóa học của các chất hữu cơ thường xảy ra chậm, không hoàn toàn, không theo hướng xác định.
9. Đồng đẳng là hiện tượng các chất có cấu tạo và tính chất tương tự nhau nhưng thành phần hợn kém nhau 1 hay nhiều nhóm – CH2-
10. Đồng phân là hiện tượng các chất khác nhau nhưng có cùng công thức phân tử.
1. Hợp chất hữu cơ là hợp chất của cacbon trừ: Oxit cacbon (CO, CO2); axit cacbonic (H2CO3); muối cacbonat (CaCO3,NaHCO3, ...); hợp chất xianua (HCN,NaCN,...); hợp chất cacbua (Al4C3,CaC2,...).
2. Hợp chất hữu cơ được chia thành 2 loại:
+ Hiđrocacbon: Chỉ chứa C và H.
+ Dẫnxuấtcủahiđrocacbon: Ngoài C, H còn có nguyên tố khác như O, N, Cl,
OH,C
OH,CHCl
,CH
CO,C
H
- Hợp chất vô cơ gồm: NaHCO3,CaC2,(NH4)2CO3,KCN,CaCO3,Al4C3.
5. Phân tích địnhtính nhằm xác định nguyên tố nào có trong hợp chất hữu cơ.
Phân tích địnhlượng nhằm xác định hàm lượng của các nguyên tố trong hợp chất hữu cơ
6. Công thức đơngiảnnhất cho biết tỉ lệ số nguyên tử mỗi nguyên tố trong hợp chất hữu cơ.
Công thức phântử cho biết số lượng nguyên tử mỗi nguyên tố trong hợp chất hữu cơ.
Công thức cấutạo cho biết thứ tự và cách thức liên kết giữa các nguyên tử trong phân tử
7. Liên kết chủ yếu trong hóa học hữu cơ là liên kết cộnghóatrị.
8. Đồng đẳng là hiện tượng các chất có cấu tạo và tính chất tương tự nhau nhưng thành phần hợn kém nhau 1 hay nhiều nhóm – CH2-.
9. Đồngphân là hiện tượng các chất khác nhau nhưng có cùng công thức phân tử.
10. Một số loại phản ứng hữu cơ thường gặp bao gồm: phản ứngthế,phản ứngcộng,phản ứng tách,phản ứngoxihóa.
5 6 7 8 9 10
12 13 14 15 16 17 18 19 20
Câu1. Hoá học hữu cơ là ngành hoá học chuyên nghiên cứu
A. các hợp chất của cacbon.
B. các hợp chất của cacbon (trừ CO, CO2).
C. các hợp chất của cacbon (trừ CO, CO2, muối cacbonat, xianua, cacbua,…).
D. các hợp chất chỉ có trong cơ thể sống.
Câu2. Liên kết hoá học chủ yếu trong phân tử hợp chất hữu cơ là loại liên kết nào dưới đây?
A. Liên kết ion.
C. Liên kết cho - nhận.
Câu3. Các chất hữu cơ thường có đặc điểm chung là
A. phân tử luôn có các nguyên tố C, H và O.
B. có nhiệt độ nóng chảy cao.
B. Liên kết cộng hoá trị.
D. Liên kết hiđro.
C. khả năng phản ứng chậm và không theo một hướng xác định.
D. khó bị phân hủy dưới tác dụng nhiệt.
Câu4. Để xác định hàm lượng các nguyên tố trong hợp chất hữu cơ, có thể sử dụng phương pháp phân tích nào sau đây?
A. phân tích định tính
C. phân tích vi lượng
B. phân tích định lượng
D. phân tích hữu cơ
Câu5. Độ bất bão hòa của hợp chất có công thức C3H4O2 là
A. k = 1. B. k = 2. C. k = 3. D. k = 4.
Câu6. Số lượng đồng phân mạch hở, có hai liên kết đôi, ứng với công thức phân tử C4H6 là
A. 3. B. 4. C. 5.
D. 2.
Câu7. Phản ứng CH3COOH + CH ≡ CH → CH3COOCH = CH2 thuộc loại phản ứng nào sau đây?
A. Phản ứng thế.
C. Phản ứng tách.
B. Phản ứng cộng.
D. Không thuộc về ba loại phản ứng trên.
Câu8. Nhóm chất nào dưới đây đều là dẫn xuất của hiđrocacbon?
A. CH2Cl2, CH2Br CH2Br, CHCl3, CH3COOCH3, C6H5CH3.
B. CH2Cl2, CH2=CH CHO, CH3COOH, CH2=CH2
C. CHBr3, CH2=CH COOCH3, C6H5OH, C2H5OH, (CH3)3N.
D. CH3OH, CH2=CH Cl, C6H5ONa, CH≡C CH3
Câu9. Đốt cháy hoàn toàn hợp chất hữu cơ X thu được một hỗn hợp khí và hơi. Dẫn hỗn hợp này qua bình đựng dung dịch H2SO4 đặc thì thấy khối lượng bình tăng lên 0,54 gam. Khối lượng hiđro trong X là
A. 0,015 gam B. 0,06 gam C. 0,03 gam D. 0,3 gam
Câu10. Đốt cháy hoàn toàn 4,4 gam hợp chất hữu cơ X cần dùng vừa
2O. Khối lượng sản phẩm cháy bằng
A. 20,4 gam
Hợp ch
t
12,4 gam
Câu12. Phân tích định lượng hợp chất hữu cơ X ta thấy tỉ lệ khối lượng các nguyên tố là mC: mH:
mO = 24: 6: 16. Công thức đơn giản nhất của hợp chất X là
A. CH3O. B. C2H6O. C. C12H3O8 D. C2H3O.
Câu13. Công thức thu gọn nào sau đây tương ứng với công thức phân tử C3H4O2?
A. CH3COOCH3.
C. HCOOCH2CH3
Câu14. Chất nào sau đây là đồng đẳng của CH ≡ CH?
A. CH2=C=CH2.
C. CH≡C CH3.
B. CH2=CH COOH.
D. CH≡C COOH.
B. CH2=CH‒CH=CH2.
D. CH2=CH2
Câu15. Hợp chất nào sau đây là đồng đẳng của axit axetic CH3COOH?
A. HCOOH.
B. CH3COOCH3.
C. HOCH2COOH. D. HOOC COOH.
Câu16. Đồng phân là
A. những hợp chất có cùng phân tử khối nhưng có cấu tạo hóa học khác nhau.
B. những hợp chất có cùng công thức phân tử nhưng có cấu tạo hóa học khác nhau.
C. những hợp chất có cùng công thức phân tử nhưng có tính chất hóa học khác nhau.
D. những chất khác nhau nhưng có cùng công thức phân tử
Câu17. Chất nào sau đây có đồng phân hình học?
A. CHCl=CH CH3. B. CH3 CH2 CH2 CH3.
C. CH3 C≡C CH3 D. CH3 CH=C(CH3)2
Câu18. Cho các cặp chất:
(1) CH3CH2OH và CH3OCH3(2) CH3CH2Br và BrCH2CH3
(3) CH2=CH CH2OH và CH3CH2CHO(4) (CH3)2NH và CH3CH2NH2
Có bao nhiêu cặp là đồng phân cấu tạo?
A. 1. B. 2.
Câu20. Vitamin A có công thức phân tử C20H30O chứa một vòng 6 cạnh, không chứa liên kết ba. Trong phân tử vitamin A có bao nhiêu liên kết đôi?
A. 4. B. 5. C. 6. D. 7.
Câu21. Trong các hợp chất sau: NaHCO3, CaC
H5OH, CaCO3, CHCl3, CH3OH,
H
O, CaC
O4. Có bao nhiêu hợp là chất hữu cơ?
A. 9 B. 12 C. 13 D. 10
Câu22. Một hợp chất hữu cơ A chứa 54,90 %C; 4,58 %H; 9,2 %N còn lại là O. Phân tử khối của A là 153. Công thức phân tử của A là
A. C
Câu23. Đốt cháy hoàn toàn 4,6 gam hợp chất hữu cơ X, thu được hỗn hợp khí và hơi Y. Dẫn Y qua bình chứa
93 ⇒ n = 1 ⇒
C6H7
Câu25. Để đốt cháy hoàn toàn 2,85 gam hợp chất hữu cơ X cần dùng vừa hết 4,2 lít O2 (đktc). Sản phẩm cháy chỉ có CO2 và H2O theo tỉ lệ 44: 15 về khối lượng. Tỉ khối của X so với hiđro bằng 57.
Công thức phân tử của X là
A. C6H10O2. B. C7H14O. C. C5H10O2.
D. C4H10O.
Câu26. Hợp chất hữu cơ X chỉ chứa C và H có tỉ khối so với hiđro bằng 29. Công thức phân tử của X là
A. C3H8 B. C4H8
C. C4H10 D. C5H10.
Câu27. Khi phân tích chất hữu cơ A chứa C, H, O thấy có mC + mH = 3,5mO. Tỉ khối hơi của A so với heli là 18. Công thức phân tử của A là
A. C4H8O.
B. C3H4O2.
C. C5H10O.
D. C3H8O.
Câu28. Trước kia, “phẩm đỏ” dùng để nhuộm áo choàng cho các Hồng y giáo chủ được tách chiết từ một loài ốc biển. Đó là một hợp chất có thành phần nguyên tố như sau: 45,70 %C; 1,90 %H; 7,60 %O; 6,70 %N; 38,10 %Br. Công thức đơn giản của phẩm đỏ là
A. C4H8O2NBr2 B. C2H4ONBr.
C. C8H4ONBr.
D. C4H2ONBr. Câu29. Đốt cháy hoàn toàn 20 ml hơi hợp chất hữu cơ X (chỉ gồm C, H, O) cần vừa đủ 110 ml O2, thu được 160 ml hỗn hợp Y gồm khí và hơi. Dẫn Y qua dung dịch H2SO4 đặc (dư) thì còn lại 80 ml khí Z. Biết các thể tích khí và hơi đo ở cùng điều kiện. Công thức phân tử của X là
A. C4H8O2.
B. C4H10O.
C. C3H8O.
D. C4H8O.
Câu30. Đốt cháy hoàn toàn 3,61 gam hợp chất hữu cơ X thu được hỗn hợp khí và hơi gồm CO2, H2O, HCl. Dẫn hỗn hợp này qua bình đựng AgNO3 lấy dư trong HNO3 ở nhiệt độ thấp thu được 2,87 gam kết tủa và bình chứa tăng thêm 2,17 gam (cho biết chỉ có H2O và HCl bị hấp thụ). Dẫn khí thoát ra cho vào 100 ml dung dịch Ba(OH)2 1 M thu được 15,76 gam kết tủa, đun sôi dung dịch l




CĐ1:Kháiquátvề hiđrocacbon. Đồng đẳng, đồng đồngphân,danhphápankan
CĐ2:Tínhchấtvà điềuchế ankan
CĐ3:Tổngônankan
ĐỒNG ĐẲNG – ĐỒNG PHÂN
KIẾNTHỨCCẦNNHỚ
1.Kháiquátvề hiđrocacbonno
- Hiđrocacbon no là hiđrocacbon trong phân tử chỉ chứa liên kết đơn C – C và C – H.
+ Hiđrocacbon no, mạch hở: ankan: CnH2n+2 (n ≥ 1)
+ Hiđrocacbon no, mạch vòng: xicloankan: CnH2n (n ≥ 3)
2. Đồng đẳng
- Công thức của hiđrocacbon bất kì: CnH2n+2-2k
- Ankan là hiđrocacbon no, mạch hở (k = 0): CnH2n+2 (n ≥ 1).
3. Đồngphân
- Ankan từ C4 trở lên có đồng phân mạch cacbon (mạch thẳng và mạch nhánh).
- Bậc của một nguyên tử cacbon bằng số nguyên tử cacbon liên kết trực tiếp với cacbon đó.
4.Danhpháp
- Tên gọi IUPAC của ankan mạch thẳng (mạch không phân nhánh):
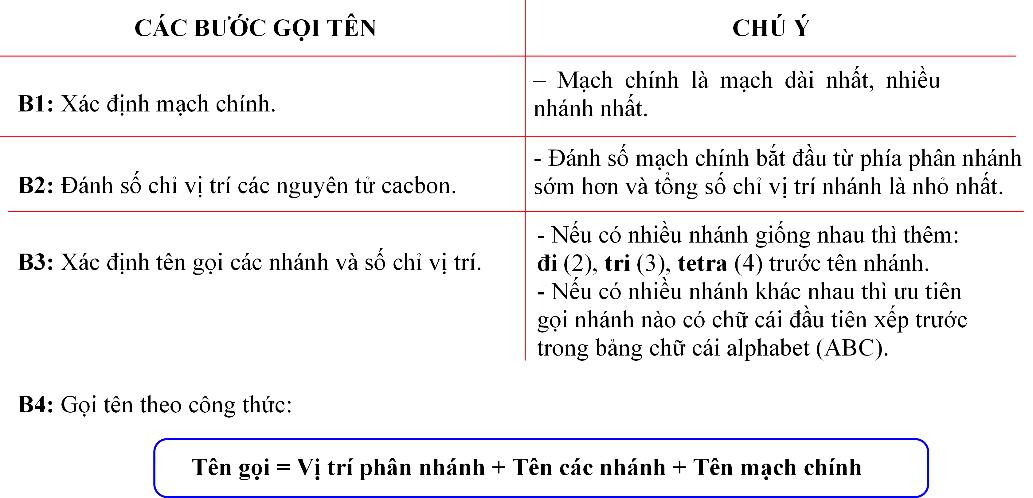
- Tên gọi IUPAC của ankan mạch nhánh:
Chúý: - Chữ với số cách nhau bởi dấu “–”; số với số cách nhau bởi dấu “,”; chữ với chữ viết liền.
- Tên gọi thông thường: Dùng tiền tố iso (có 1 nhánh CH3 ở C2), neo (có 2 nhánh CH3 ở C2).
BÀITẬPTỰ LUẬN
Câu1: Cho các công thức: CH4, C2H4, C3H8, C4H8, C5H10, C6H14. Công thức nào có thể là ankan?
Công thức nào có thể là của xiclo ankan?
Ankan:CH4,C3H8,C6H14.
Xicloankan:C4H8,C5H10.
Câu2: Viết các đồng phân và gọi tên (tên IUPAC và tên thông thường nếu có) của ankan có công thức sau. Xác định bậc của các nguyên tử cacbon trong các đồng phân của C4H10, C5H12.
C4H10
CH3 –CH2 –CH2 –CH3:butan
C5H12
CH3 –CH2 –CH2 –CH2 –CH3:pentan
CH-CH-CH CH :2–metylbutan (isobutan)
33 | 3
323 | 3
CH
CH-C-CH CH
C6H14
CH3 –CH2 –CH2 –CH2 –CH2 –CH3:hexan
3
CH-CH-CH-CH-CH CH :3-metylpantan
| 33 |
CH-CH-CH-CH
:2,2– đimetylbutan(neohexan) 3 ||
CHCH
33
CH-CH-CH-CH CH :2–metylbutan(isopentan) 3 | 33 | 3
:2,2– đimetylpentan(neopentan)
CH-CH-CH-CH-CH
CH3 –CH2 –CH2 –CH2 –CH2 –CH2 –CH3:heptan 32223 | 3 CH-CH-CH-CH-CH-CH CH ; 2 | 3223 3 CH-CH-CH-CH-CH-CH CH | 2 | H 3 323 3 CH CH-C-CCHCH CH | 2 | H 3 323 3 CH CH-C-CCHCH CH ; 3 || 32 33
CH3 –CH2 –CH2 –CH2 –CH3
2,3 – đimetylbutan 2
CH CH-C-CHCH CH
3 | 33 | 3
CH-CH-CH-CH CH
isopentan 323 | 3
CH CH-C-CH CH
neopentan 3 | 33 | 3
CH-CH-CH-CH
323 | 3
CH
3 – etyl – 2 – metylheptan
CH-CH-CH-CH-CH-CH-CH
32223 | 3
CHCH
| 25
CH-CH-CH-CH-CH-CH
Isoheptan 32223 | 3
CH
Neohexan 2
CH CH-C-CHCH CH
3 | 33 | 3
Câu4: Xác định công thức phân tử và số đồng phân cấu tạo của ankan X biết:
(a) Ankan X có phân tử khối là 30
n2n2CH 2633 M14n230n2:CH:CHCH + =+= =−
(b) Ankan X có tỉ khối so với hiđro là 29.
n2n2CH 410 M14n229.2n4:CH:2®p. + =+= =
(c) Ankan X có %mC = 83,72%.
C 614 12n %m.100%83,72%n6:CH: 14n2 == = + 5 đồng phân.
(d) Ankan X có mC : mH = 5.
m 12n 5n5:CH: m2n2 == = + 3 đồng phân.
C 512 H
Câu5: Viết các đồng phân và gọi tên gốc ankyl có công thức C3H7- và C4H9-.
C3H7CH3 –CH2 –CH2 –:propyl
CH-CHCH :isopropyl
3 | 3
C4H9CH3 –CH2 –CH2 –CH2-:butyl
32 |
CH-CH-CHCH :isobutyl
3
32 | 3
CH-CH-CHCH :sec–butyl |
CH CHC CH
:tert–butyl
|
BÀITẬPTRẮCNGHIỆM
1.Mức độ nhậnbiết(rấtdễ vàdễ)
Câu1. Đặc điểm nào sau đây là của hiđrocacbon no?
A. Chỉ có liên kết đôi.
C. Có ít nhất một vòng no.
Câu2. Ankan là các hiđrocacbon
A. no, mạch vòng.
C. không no, mạch hở.
B. Chỉ có liên kết đơn.
D. Có ít nhất một liên kết đôi.
B. no, mạch hở.
D. không no, mạch vòng.
Câu3. Ankan là những hiđrocacbon no, mạch hở, có công thức chung là
A. CnH2n+2 (n ≥1).
C. CnH2n-2 (n ≥2).
B. CnH2n (n ≥2).
D. CnH2n-6 (n ≥6).
Câu4. Các ankan như: CH4, C2H6, C3H8, … hợp thành dãy nào dưới đây?
A. đồng đẳng của axetilen.
C. đồng đẳng của metan.
B. đồng phân của metan.
D. đồng phân của ankan.
Câu5. Nhóm nguyên tử còn lại sau khi lấy bớt một nguyên tử H từ phân tử ankan gọi là ankyl, có công thức chung là
A. CnH2n-1 (n ≥ 1).
C. CnH2n+1 (n ≥ 2).
Câu6. Nhóm nguyên tử CH3- có tên là
A. metyl. B. etyl.
Câu7. Nhóm nguyên tử CH3CH2- có tên là
A. metyl. B. etyl.
Câu8. Nhóm nguyên tử (CH3)2CH- có tên là
B. CnH2n+1 (n ≥ 1).
D. CnH2n-1 (n ≥ 2).
C. propyl. D. butyl.
C. propyl. D. butyl.
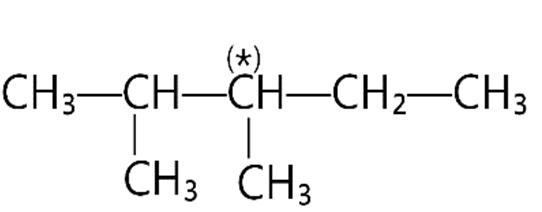
A. metyl. B. etyl. C. propyl. D. isopropyl.
Câu9. Dãy các ankan được sắp xếp theo thứ tự tăng dần phân tử khối là
A. hexan, heptan, propan, metan, etan. B. metan, etan, propan, hexan, heptan.
C. heptan, hexan, propan, etan, metan.
2.Mức độ thônghiểu(trungbình)
D. metan, etan, propan, heptan, hexan.
Câu10. Khi nói về phân tử ankan không phân nhánh thì đặc điểm nào sau đây là đúng?
A. Chỉ có cacbon bậc I và II.
C. Chỉ có cacbon bậc II.
B. Chỉ có cacbon bậc I, II và III.
D. Chỉ có cacbon bậc I.
Câu11. Bậc của nguyên tử cacbon đánh dấu (*) trong hợp chất sau là
A. bậc I.
B. bậc II.
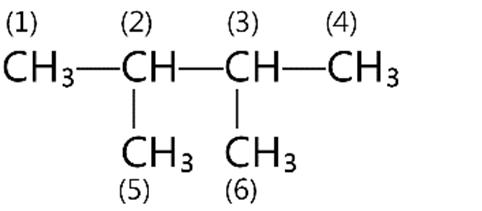
Câu12. Trong phân tử sau đây, các nguyên tử cacbon:
A. 1 và 4 giống nhau; 2 và 3 giống nhau.
C. bậc III.
D. bậc IV.
B. 1 và 4 giống nhau; 5 và 6 giống nhau.
C. 1, 4, 5, 6 giống nhau; 2 và 3 giống nhau.
D. 2 và 3 giống nhau; 5 và 6 giống nhau.
Câu13. Số đồng phân cấu tạo tương ứng với công thức phân tử C5H12 là
A. 1. B. 2.
C. 3.
Câu14. Số đồng phân cấu tạo tương ứng với công thức phân tử C6H14 là
A. 3. B. 4.
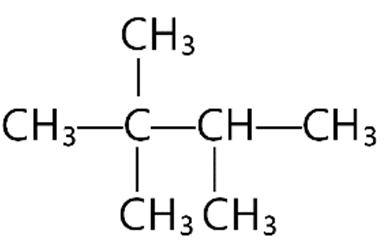
Câu15. Hiđrocacbon X có công thức cấu tạo:
Danh pháp IUPAC của X là
A. 2,3-đimetylpentan.
C. 2,4-đimetylpentan.
Câu16. Hiđrocacbon Y có công thức cấu tạo:
C. 5.
D. 4.
D. 6.
B. 2,4-đimetylbutan.
D. 2,4-metylpentan.
Danh pháp IUPAC của Y là
A. 2,3,3-metylbutan.
C. 2,2,3-trimetylbutan.
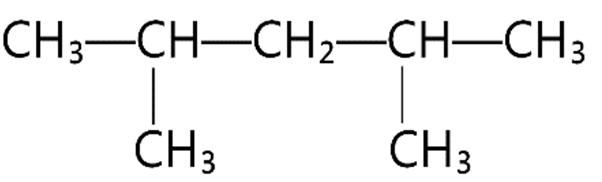
B. 2,2,3-đimetylbutan.
D. 2,3,3-trimetylbutan.
Câu17. Công thức cấu tạo thu gọn của 2,2-đimetylpropan là
A. (CH3)2CHCH2CH3.
C. CH3CH2CH2CH2CH3.
B. (CH3)4C.
D. CH3CH2CH(CH3)2.
Câu18. Công thức cấu tạo thu gọn của 2,3-đimetylbutan là
A. (CH3)2CH CH(CH3)2.
C. (CH3)2C CH(CH3)2
B. (CH3)3C C(CH3)3.
D. CH3CH2C(CH3)3
Câu19. Trong phân tử 2,2,4-trimetylpentan có bao nhiêu nguyên tử hiđro?
A. 8.
B. 12.
Câu20. Phần trăm khối lượng cacbon trong C4H10 là
A. 28,57 %.
B. 82,76 %.
C. 16.
C. 17,24 %.
D. 18.
D. 96,77 %.
Câu21. Theo chiều tăng dần số nguyên tử cacbon trong phân tử, phần trăm khối lượng cacbon
trong phân tử ankan
A. không đổi.
C. giảm dần.
B. tăng dần.
D. biến đổi không theo quy luật.
Câu22. Trong dãy đồng đẳng của metan, ankan nào có hàm lượng hiđro lớn nhất?
A. CH4. B. C3H8.
C. C6H14.
D. C10H22.
Câu23. Phần trăm khối lượng cacbon trong ankan X là 83,33 %. Công thức phân tử của X là
A. CH4. B. C3H8.
C. C5H12.
D. C10H22.
Câu24. Phần trăm khối lượng hiđro trong ankan X là 25,00 %. Công thức phân tử của X là
A. CH4.
B. C2H6.
C. C3H8.
D. C4H10.
Câu25. Hàm lượng nguyên tố hiđro trong ankan X là 82,76 %. Số đồng phân cấu tạo của X là
A. 1. B. 2.
3.Mức độ vậndụng(khá)
C. 3.
D. 4.
Câu26.(A.13): Tên thay thế (theo IUPAC) của (CH3)3
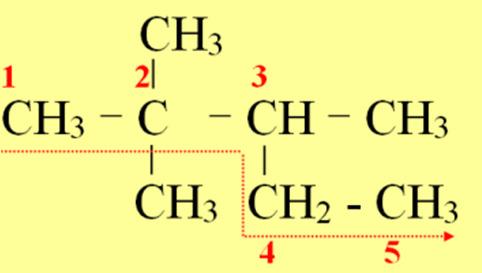
A. 2,2,4,4-tetrametylbutan.
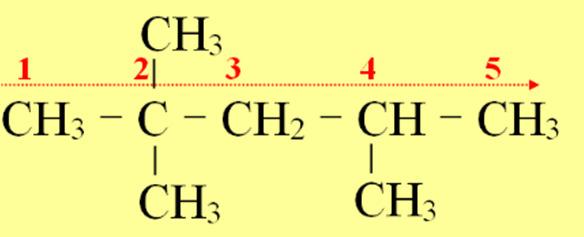
C. 2,2,4-trimetylpentan.
C–CH2–CH(CH3)2 là
B. 2,4,4-trimetylpentan.
D. 2,4,4,4-tetrametylbutan.
Hướngdẫngiải
Câu27. Hiđrocacbon X có công thức cấu tạo:
Số nguyên tử cacbon và số nhánh trong mạch chính của X là:
A. 4 cacbon và 2 nhánh.
C. 5 cacbon và 1 nhánh.
B. 5 cacbon và 2 nhánh.
D. 4 cacbon và 1 nhánh.
Hướngdẫngiải
Câu28. Hiđrocacbon Z có công thức cấu tạo:
Danh pháp IUPAC của Z là
A. 2,2,3-trimetylpentan.
C. 3-etyl-2,2-đimetylbutan.
B. 2,3,3-trimetylpentan.
D. 2-etyl-3,3-đimetylbutan.
Hướngdẫngiải
Câu29. Hiđrocacbon T có công thức cấu tạo:
Danh pháp IUPAC của T là
A. 3-etyl-2,4-đimetylpentan.
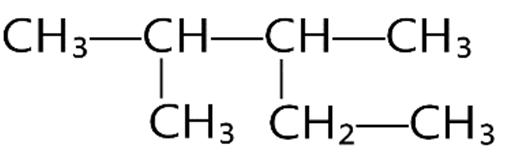
C. 2,4-đimetyl-3-etylpentan.
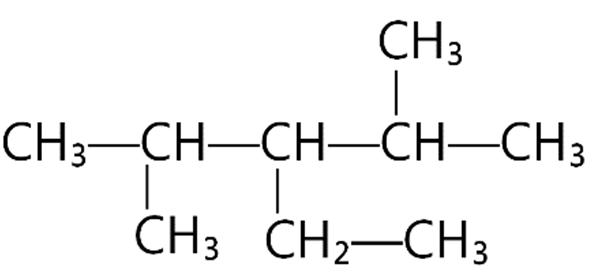
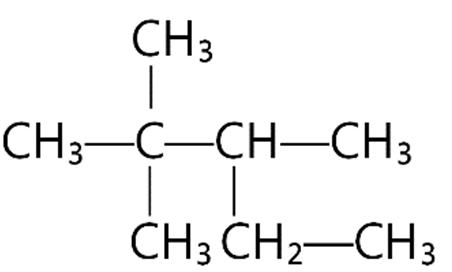
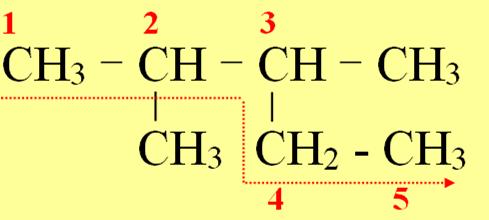
B. 2-metyl-3-propylpentan.
D. 2-propyl-3-metylpentan.
Hướngdẫngiải
Câu30. Ankan X có công thức cấu tạo như sau:
CH3 CH2 CH CH2 CH3
CH CH3
Tên gọi của X là
A. 3- isopropylpentan.
C. 3-etyl-2-metylpentan.
Câu31. Ankan X có công thức cấu tạo như sau: CH
Tên gọi của X là
A. 2-metyl-2,4-đietylhexan.
C. 3,3,5-trimetylheptan.
CH3
B. 2-metyl-3-etylpentan.
D. 3-etyl-4-metylpentan.
B. 2,4-đietyl-2-metylhexan.
D. 3-etyl-5,5-đimetylheptan.
Hướngdẫngiải
KIẾNTHỨCCẦNNHỚ
1.Tínhchấtvậtlí
- Các ankan không màu, nhẹ hơn nước, nhiệt độ nóng chảy, nhiệt độ sôi tăng theo phân tử khối.
- C1 – C4: khí (khí gas); C5 – C17: lỏng (xăng, dầu); C18 trở lên: rắn (nến, sáp).
2.Tínhchấthóahọc
- Ankan chỉ gồm các liên kết đơn C – C, C – H bền vững nên trơ về mặt hóa học. PƯ đặc trưng của
ankan gồm phản ứng thế, phản ứng tách và phản ứng oxi hóa
(a) Phản ứng thế halogen (Cl2, Br2 /askt): CnH2n+2 + aCl2 as 1:a → CnH2n+2-aCla + aHCl
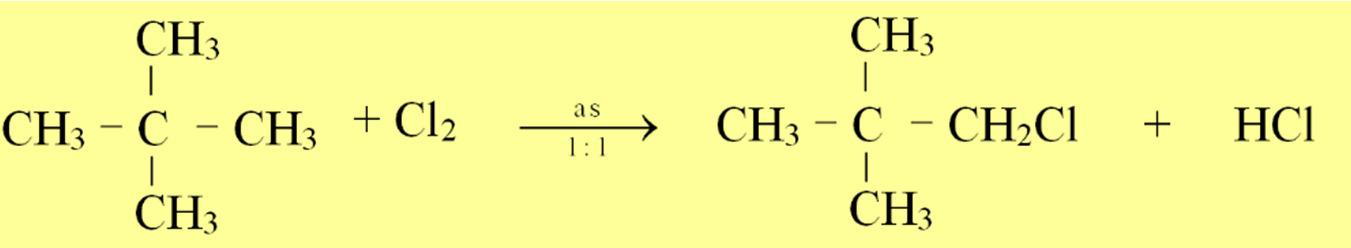
Chú ý: Từ C3H8 trở lên, PƯ tạo ra nhiều sản phẩm thế và tuân theo qui tắc “Ưu tiên thế vào H của
C có bậc cao hơn”.
(b) Phản ứng tách
- PƯ tách hiđro (bẻ gãy liên kết C – H): CnH2n+2 oxt,t → CnH2n+2-2k + kH2
THĐB: 2CH4 o 1500C lµm l¹nh nhanh → C2H2 + 3H2
- PƯ cracking (bẻ gãy liên kết C – C): CnH2n+2 oxt,t → CmH2m+2 + CqH2q (n = m + q)
(c) PƯ oxi hóa: CnH2n+2 + 3n1 2 + O2 ot → nCO2 + (n +1)H2O
Chú ý: Khi đốt cháy ankan ta luôn có: 22 HOCOnn > và ngược lại. 22 ankanHOCO nnn. =−
3. Điềuchế
- Phương pháp vôi tôi xút: CnH2n+1COONa + NaOH oCaO,t → CnH2n+2 + Na2CO3
- Riêng CH4 còn được điều chế bằng cách thủy phân Al4C3: Al4C3 + 12H2O → 4Al(OH)3 + 3CH4
BÀITẬPTỰ LUẬN
Câu1: Trả lời các câu hỏi sau:
(a) Vì sao xăng dầu phải được chứa trong các bình chứa chuyên dụng và phải bảo quản ở những kho riêng?
Vìxăngdầudễ cháynổ.
(b) Vì sao các tàu chở dầu khi bị tai nạn thường gây ra thảm họa cho một vùng biển rất rộng?
Vìdầunhẹ nổilêntrênmặtbiểngâyônhiễmmôitrường ảnhhưởng đếncácsinhvậtsống phíadưới.
(c) Vì sao khi các chi tiết máy hoặc đồ dùng bị bẩn dầu mỡ người ta thường dùng xăng hoặc dầu hoả để lau rửa?
Vìdầumỡ tantrongxănghoặcdầuhỏa.
(d) Vì sao khi bị cháy xăng dầu không nên dùng nước để dập?
Vìxăngkhôngtantrongnước,nhẹ nổilêntrên ⇒ ⇒⇒ ⇒ Nướcchảy đến đâuxănglan đến đólàm đámcháylanrộng.
Câu2: Viết PTHH xảy ra khi cho
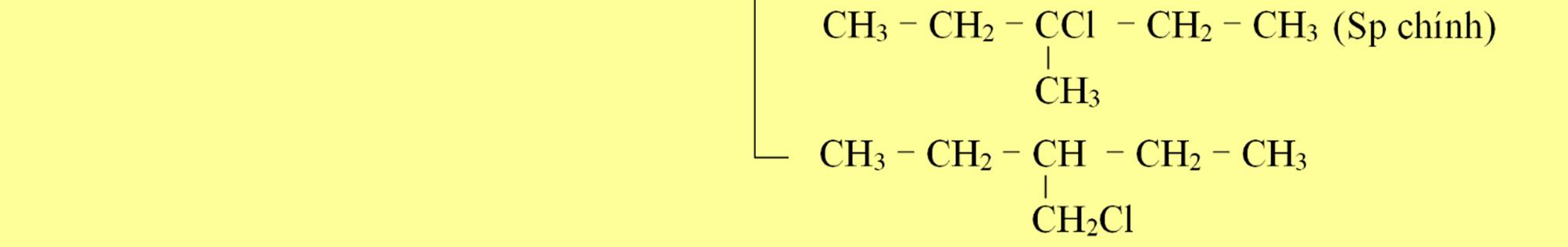
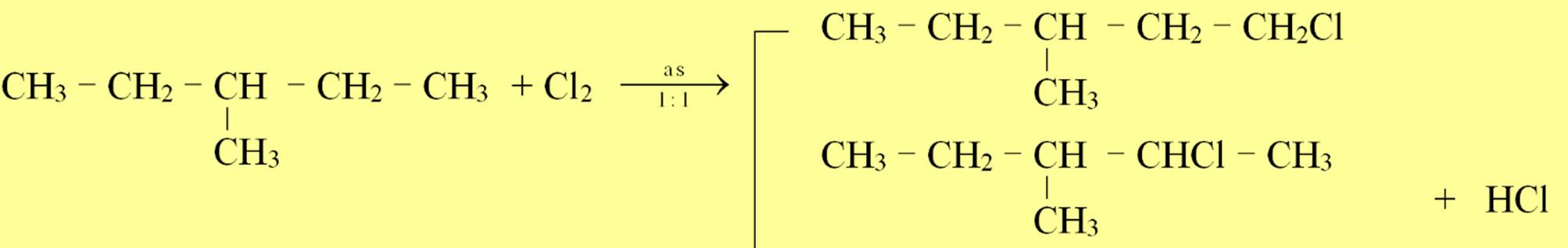
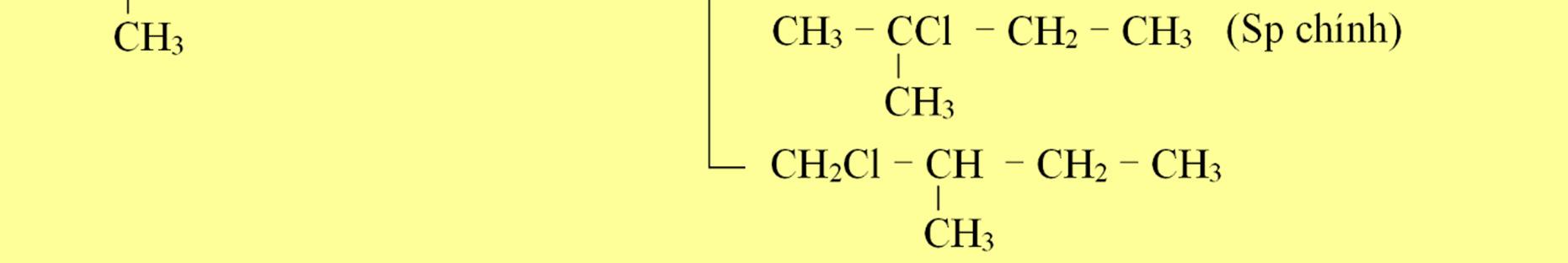
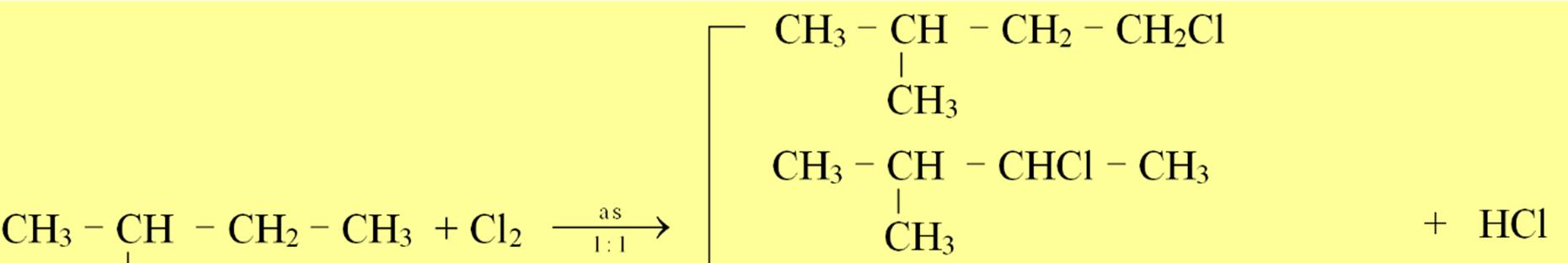
(a) neopentan, isopentan, 3 – metylpentan tác dụng với Cl2 (as, tỉ lệ 1 : 1). Xác định sản phẩm chính.
(b) Etan tác dụng với Br2 (as, t
(c)
1 : 2).
(d)
i liên hệ giữa số mol CO2, H2O và số mol ankan tham gia phản ứng.
CnH2n+2 + 3n1 2 + O2 ot → nCO2 + (n + 1) H2O; 22 ankanHOCO nnn =−
(g) Đốt cháy hiđrocacbon ở dạng tổng quát. Tìm mối liên hệ giữa số mol CO2, H2O và số mol hiđrocacbon tham gia phản ứng.
CnH2n+2-2k + 3n1k 2 +− O2 ot → nCO2 + (n + 1 - k)H2O; 22 COHO HC
Câu3: Hoàn thành chuỗi phản ứng sau:
nn n k1 =
(1) CH3COONa + NaOH oCaO,t → CH4 + Na2CO3
(2) C4H10 Cr¨cking → CH4 + C3H6
(3) Al4C3 + 12H2O → 4Al(OH)3 + 3CH4
(4) 2CH4 o 1500C lµml¹nhnhanh → C2H2 + 3H2
(5) CH4 + Cl2 as 1:1 → CH3Cl + HCl
(6) CH4 + 2O2 ot → CO2 + 2H2O
Câu4: Xác định công thức cấu tạo và gọi tên IUPAC của X trong các trường hợp sau:
(a) Ankan X thể khí điều kiện thường, khi thế clo (as) chỉ cho một sản phẩm thế monoclo.
CH4: metan; CH3 – CH3: etan.
(b) Ankan X có tỉ khối hơi so với hiđro là 36. Khi X thế clo (as) thu được 4 sản phẩm thế monoclo.
MX = 36.2 = 72 = 14n + 2 ⇒ n = 5: C5H12
X thế clo tạo 4 sản phẩm thế monoclo ⇒ X là: (CH3)2 – CH – CH2 – CH3: 2 – metylbutan.
(c) Ankan X có %mC = 83,33%. Khi X thế clo (as) thu được một sản phẩm thế monoclo.
C 512 12n %m.100%83,33%n5:CH 14n2 == = +
X thế được 1 sản phẩm thế monoclo ⇒ (CH3)4C: 2,2 – đimetylpropan (neopentan).
BÀITẬPTRẮCNGHIỆM
1.Mức độ nhậnbiết(rấtdễ vàdễ)
Câu1. Ở điều kiện thường hiđrocacbon nào sau đây ở thể lỏng?
A. C4H10. B. C2H6.
Câu2. Ankan hòa tan tốt trong dung môi nào sau đây?
A. Nước.
C. Dung dịch axit HCl.
C. C3H8.
B. Benzen.
D. Dung dịch NaOH.
Câu3. Trong các chất dưới đây, chất nào có nhiệt độ sôi thấp nhất?
A. Butan. B. Etan.
Câu4. Phản ứng đặc trưng của hiđrocacbon no là
A. Phản ứng tách.
C. Phản ứng cộng.
Câu5. Các ankan không tham gia loại phản ứng nào?
A. Phản ứng thế
C. Phản ứng tách.
Câu6. Thành phần chính của “khí thiên nhiên” là
A. metan. B. etan.
D. C5H12.
C. Metan. D. Propan.
B. Phản ứng thế.
D. Phản ứng oxi hóa.
B. Phản ứng cộng.
D. Phản ứng cháy.
C. propan.
n-butan.
Câu7. Nung nóng isobutan với xúc tác thích hợp thu được isobutilen C4H8, phản ứng đã xảy ra là
Câu9. Khi đốt cháy hoàn toàn một ankan thì:
Câu10. Trong công nghiệp, metan được điều chế từ
A. khí thiên nhiên và dầu mỏ. B. natri axetat.
C. nhôm cacbua. D. canxi cacbua. Câu11. Khi nung natri axetat (CH3COONa) với vôi tôi xút (NaOH/CaO), thu được sản phẩm hữu cơ X. Công thức phân tử của X là
A. CH4. B. C2H6. C. C2H4. D. C2H2. Câu12.[MH1-2020] Nghiền nhỏ 1 gam CH3COONa cùng với 2 gam vôi tôi xút (CaO và NaOH)
rồi cho vào đáy ống nghiệm. Đun nóng đều ống nghiệm, sau đó đun tập trung phần có chứa hỗn hợp phản ứng. Hiđrocacbon sinh ra trong thí nghiệm trên là
A. metan. B. etan. C. etilen. D. axetilen.
Câu13. Khi cho nhôm cacbua vào nước thì thu được một sản phẩm hữu cơ dạng khí X. Tên gọi của X là
A. metan. B. etan. C. propan. D. butan.
Câu14. Trong phòng thí nghiệm có thể điều chế metan bằng cách nào sau đây?
A. Nhiệt phân natri axetat với vôi tôi xút.
B. Crackinh butan.
C. Cho nhôm cacbua tác dụng với nước.
D. Nhiệt phân natri axetat với vôi tôi xút hoặc cho nhôm cacbua tác dụng với nước. Câu15.(QG.15): Khí thiên nhiên được dùng làm nhiên liệu và nguyên liệu cho các nhà máy sản xuất điện, sứ, đạm, ancol metylic,… Thành phần chính của khí thiên nhiên là metan. Công thức phân tử của metan là
A. CH4.
B. C2H4.
C. C2H2.
D. C6H6. Câu16.(QG.19-201). Hiện nay, nhiều nơi ở nông thôn đang sử dụng hầm biogas để xử lí chất thải trong chăn nuôi gia súc, cung cấp nhiên liệu cho việc đun nấu. Chất dễ cháy trong khí biogas là
A. Cl2. B. CH4.
2.Mức độ thônghiểu(trungbình)
C. CO2.
Câu17. Phân tử metan không tan trong nước vì lí do nào sau đây?
A. Phân tử metan không phân cực.
C. Phân tử khối của metan nhỏ.
B. Metan là chất khí.
D. N2.
D. Metan không có liên kết đôi.
Câu18.(A.08): Cho isopentan tác dụng với Cl2 theo tỉ lệ số mol 1: 1, số sản phẩm monoclo tối đa thu được là
A. 5. B. 4.
C. 3.
D. 2.
Câu19. Khi cho 2,2-đimetylpropan phản ứng với clo (tỉ lệ mol 1:1), chiếu sáng thì có thể tạo ra tối đa bao nhiêu sản phẩm thế monoclo?
A. 1.
B. 2.
C. 3.
D. 5.
Câu20. Khi cho 2,3,4-trimetylpentan phản ứng với clo (tỉ lệ mol 1:1), chiếu sáng thì có thể tạo ra tối đa bao nhiêu sản phẩm thế monoclo?
A. 4.
B. 5.
C. 8.
D. 6.
Câu21.(A.13): Khi được chiếu sáng, hiđrocacbon nào sau đây tham gia phản ứng thế với clo theo tỉ lệ mol 1: 1, thu được ba dẫn xuất monoclo là đồng phân cấu tạo của nhau?
A. neopentan.
B. pentan.
C. butan.
D. isopentan.
Câu22. Đồng phân cấu tạo nào của ankan có công thức phân tử C5H12 chỉ tạo ra duy nhất một sản phẩm thế khi phản ứng với clo (tỉ lệ mol 1:1), chiếu sáng?
A. pentan. B. 2-metylbutan.
C. 2,2-đimetylpropan.
D. Không có đồng phân nào.
Câu23. Khi phản ứng với brom (tỉ lệ mol 1:1), chiếu sáng, 2-metylpentan có thể tạo ra sản phẩm chính là dẫn xuất thế ở cacbon nào?
A. C6 . B. C2 .
C. C3 . D. C4 .
Câu24. Nhiệt phân hoàn toàn 2-metylpropan với xúc tác thích hợp chỉ thu được metan và một sản phẩm hữu cơ X. Công thức cấu tạo thu gọn của X là
A. (CH3)2C=CH2.
C. CH2=CH2.
Câu25. Cho phản ứng nhiệt phân sau:
Công thức cấu tạo thu gọn của X là
A. CH3CH2CH3.
C. CH3 CH=CH CH3.
Câu26. Đây là thí nghiệm điều chế và thu khí gì?
Hoãnhôïp CHCOONa,CaO,NaOH
A. O2. B. CH4.
B. CH3 CH=CH2.
D. CH3 CH=CH CH3.
B. CH3 CH=CH2.
D. CH3CH2CH2CH3.
C. C2H2. D. H2.
Câu27. Cho chuỗi phản ứng sau: o 2 NaOH/CaO,Cl(1:1)/askt t 3(1)(2)CHCOONa X Y + + →→
Công thức phân tử của X và Y lần lượt là:
A. CH4 và CHCl3. B. C2H6 và CH3Cl.
C. CH4 và CH3Cl. D. (CH3COO)2Ca và CHCl3.
Câu28.(B.12): Cho phương trính hóa học: 2X + 2NaOH o CaO, t → 2CH4 + K2CO3 + Na2CO3
Chất X là
A. CH2(COOK)2. B. CH2(COONa)2. C. CH3COOK. D. CH3COONa.
Câu29. Khi dẫn ankan qua xúc tác kim loại (Fe, Pt, …), đun nóng thì có thể xảy ra phản ứng tách, khi đó:
A. ankan bị tách hiđro tạo thành xicloankan.
B. ankan bị bẻ gãy các liên kết C C tạo thành cacbon.
C. ankan không những bị tách hiđro tạo thành hiđrocacbon không no mà còn có thể bị bẻ gãy các liên kết C C tạo ra các phân tử nhỏ hơn.
D. ankan bị oxi hóa hoàn toàn bởi oxi trong không khí, tạo thành CO2 và H2O. Câu30. Phát biểu nào sau đây không đúng?
A. Ở điều kiện thường, các ankan từ C1 đến C4 ở trạng thái khí, từ C5 đến khoảng C18 ở trạng thái lỏng, từ khoảng C18 trở đi ở trạng thái rắn.
B. Nhiệt độ nóng chảy, nhiệt độ sôi và khối lượng riêng của ankan nói chung đều giảm theo chiều tăng số nguyên tử cacbon trong phân tử.
C. Ankan không tan trong nước nhưng tan trong dung môi không phân cực như dầu, mỡ
D. Ankan đều là những chất không màu.
Câu31. Phát biểu nào sau đây không đúng?
A. Ankan không tan trong dung dịch NaOH hoặc H2SO4
B. Ankan tan tốt trong nước.
C. Các ankan từ C1 đến C4 là chất khí.
D. Các ankan nhẹ như metan, etan, propan là những khí không màu.
Câu32. Phát biểu nào sau đây không đúng?
A. Khi đốt, các ankan có thể bị cháy tạo ra CO2 và H2O, phản ứng tỏa nhiều nhiệt.
B. Khi có xúc tác và nhiệt độ thích hợp, ankan bị oxi hóa không hoàn toàn tạo thành các hợp chất chứa oxi như HCHO.
C. Trong sản phẩm cháy của ankan, số mol H2O luôn lớn hơn hoặc bằng số mol CO2
D. Ankan không tác dụng được với KMnO4 hoặc H2SO4, dù đó cũng là những chất oxi hóa rất mạnh.
Câu33. Phát biểu nào sau đây không đúng?
A. Trong phân tử ankan chỉ có các liên kết xích-ma σ bền vững.
B. Ankan tương đối trơ về mặt hóa học, ở nhiệt độ thường không phản ứng với axit, bazơ và các chất oxi hóa mạnh như KMnO4.
C. Khi chiếu sáng hoặc đốt nóng hỗn hợp ankan và clo sẽ xảy ra phản ứng thế các nguyên tử cacbon trong ankan bởi clo.
D. Trong phân tử ankan chỉ có các liên kết đơn C H và C C. Câu34. Tính chất nào sau đây không phải của ankan?
A. Khi không chiếu sáng thì không phản ứng được với brom, do vậy không làm mất màu dung dịch brom.
B. Phản ứng với clo khi đun nóng hoặc chiếu sáng, tạo thành hỗn hợp các dẫn xuất clo.
C. Phản ứng mãnh liệt với dung dịch KMnO4 khi đun nóng, tạo thành CO2 và H2O.
D. Tan tốt trong các dung môi không phân cực như dầu mỡ, benzen, … Câu35. Để nhận biết metan và CO2, có thể dùng phương pháp nào sau đây?
A. Dẫn qua nước brom, metan phản ứng làm mất màu nước brom còn CO2 thì không.
B. Dẫn qua dung dịch KMnO4, metan có phản ứng làm mất màu dung dịch còn CO2 thì không.
C. Dẫn qua dung dịch nước vôi trong dư, CO2 phản ứng tạo kết tủa trắng còn metan thì không.
D. Dẫn qua dung dịch HCl, metan có phản ứng thế còn CO2 thì không. Câu36. Để nhận biết metan và SO2, có thể dùng phương pháp nào sau đây?
A. Dẫn qua dung dịch nước brom, metan phản ứng làm mất màu dung dịch còn SO2 thì không.
B. Dẫn qua dung dịch nước brom, metan không phản ứng nhưng SO2 thì có phản ứng làm mất màu dung dịch: SO2 + 2H2O + Br2 → 2HBr + H2SO4
C. Dẫn qua dung dịch HCl dư, metan có phản ứng thế còn SO2 thì không.
D. Dẫn qua dung dịch HCl dư, SO2 có phản ứng còn HCl thì không.
Câu37. Để nhận biết CO2, SO2 và metan có thể dùng hai hóa chất nào trong các chất sau: Ca(OH)2, Br2, HCl, HBr?
A. Br2 và Ca(OH)2 B. Br2 và HCl. C. HBr và Ca(OH)2 D. HCl và Br2
Câu38.(C.07): Khi cho ankan X (trong phân tử có phần trăm khối lượng cacbon bằng 83,72%) tác dụng với clo theo tỉ lệ sốmol 1:1 (trong điều kiện chiếu sáng) chỉ thu được 2 dẫn xuất monoclo
đồng phân của nhau. Tên của X là
A. butan. B. 2,3-đimetylbutan. C. 3-metylpentan. D. 2-metylpropan.
Câu39.(A.08): Khi crackinh hoàn toàn một thể tích ankan X thu được ba thể tích hỗn hợp Y (các thể tích khí đo ở cùng điều kiện nhiệt độ và áp suất); tỉ khối của Y so với H2 bằng 12. Công thức phân tử của X là
A. C5H12. B. C3H8. C. C6H14. D. C4H10.
Câu40.(C.08): Đốt cháy hoàn toàn một hiđrocacbon X thu được 0,11 mol CO2 và 0,132 mol H2O. Khi X tác dụng với khí clo (theo tỉ lệ số mol 1:1) thu được một sản phẩm hữu cơ duy nhấ
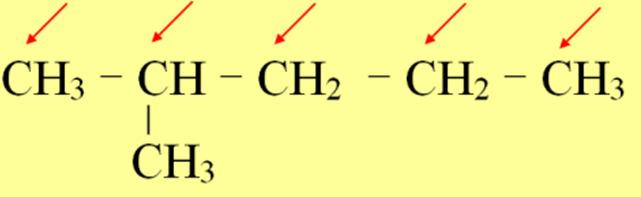
A. 2,2-đimetylbutan.
C. 2-metylpentan.
u sáng?
H
B. 2,3-đimetylbutan.
D. 3-metylpentan.
Câu43. Đồng phân cấu tạo nào của ankan có công thức phân tử C6H14 tạo ra nhiều sản phẩm thế nhất khi phản ứng với clo (tỉ lệ mol 1:1), chiếu sáng?
A. 2-metylpentan.
C. pentan.
B. 3-metylpentan.
D. 2,2-đimetylbutan.
Hướngdẫngiải
Câu44. Cho các chất sau: metan, etan, propan, isobutan, neopentan. Có bao nhiêu chất khi tác dụng với clo (tỉ lệ mol 1:1, chiếu sáng) chỉ thu được duy nhất một dẫn xuất monoclo?
A. 1. B. 2. C. 3. D. 4.
Hướngdẫngiải
Bao gồm: metan, etan, neopentan.
Câu45. Cho các ankan sau: propan (I); 3-metylpentan (II); 2,2-đimetylbutan (III) và 2,3đimetylbutan (IV). Chất nào tác dụng với clo trong điều kiện chiếu sáng thu được ba dẫn xuất monoclo?
A. II và III. B. I, III và IV. C. II, IV. D. Chỉ III.
Hướngdẫngiải
Câu46. Dãy ankan nào sau đây thỏa mãn điều kiện: mỗi công thức phân tử có một đồng phân khi
tác dụng với clo theo tỉ lệ mol 1: 1 tạo ra 1 dẫn xuất monocloankan duy nhất?
A. CH4, C3H8, C4H10, C6H14
C. CH4, C4H10, C5H12, C6H14.
B. CH4, C2H6, C5H12, C8H18
D. CH4, C2H6, C5H12, C4H10.
Hướngdẫngiải
CH4, CH3 – CH3, ,
Câu47. Cho sơ đồ phản ứng sau:
Các hợp chất A, B, C lần lượt là:
A. C5H10, C4H8, C4H9Cl.
C. CH4, C4H8, C4H9Cl.
Hướ
B. CH4, C4H10, C4H9Cl.
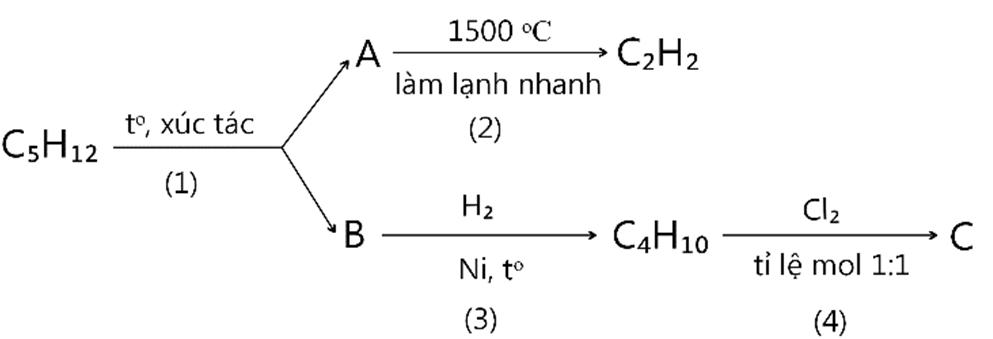
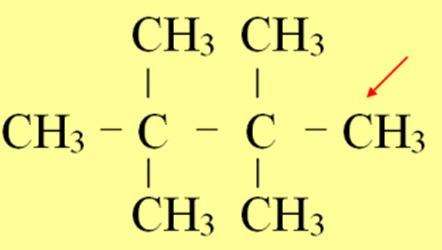
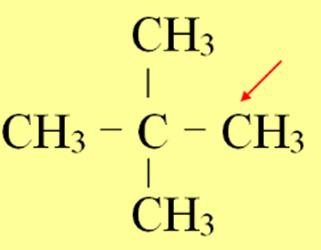
D. H2, C5H10, C4H8
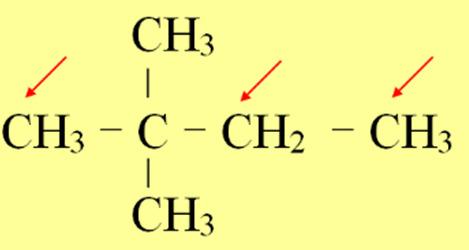
(1) CH3COONa + NaOH
(2) C5H12 Cr¨cking → CH4 + C4H8
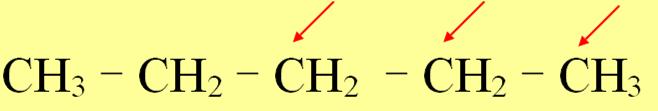
(3)
Câu49. Thực hiện chuỗi phản ứng sau:
(1) C5H12
→ CH4 + C4H8
(2) Al4C3 + 12H2O → 4Al(OH)3 + 3CH4
(3) C4H8 + H2 oNi,t → C4H10
Câu50. Trong các phát biểu sau:
(1) Ankan không tan trong axit H2SO4 loãng
(2) Ankan tan tốt trong dung dịch KMnO4
(3) Ankan tan tốt trong dung dịch NaOH đặc
(4) Ankan tan tốt trong benzen
Những phát biểu không đúng là:
A. 1, 2 và 3.
B. 3 và 4.
C. 1 và 2.
Hướngdẫngiải
D. 2, 3.
Bao gồm: 2, 3 vì ankan chỉ tan trong dung môi hữu cơ không phân cực như xăng, benzen, …
Câu51. Nhỏ lần lượt hexan vào bốn ống nghiệm:
Ống nghiệm 1: chứa dung dịch KOH
Ống nghiệm 2: chứa dung dịch H2SO4 đặc
Ống nghiệm 3: chứa dung dịch KMnO4
Ống nghiệm 4: chứa benzen
Hexan có thể tan trong những ống nghiệm nào?
A. 1, 2 và 3.
B. 1, 2 và 4.
C. chỉ 4.
D. 3 và 4.
Hướngdẫngiải Bao gồm: 4 vì benzen là dung môi không phân cực giống hexan nên hexan có thể tan tốt trong benzen.
Câu52.(C.12): Nung một lượng butan trong bình kín (có xúc tác thích hợp) thu được hỗn hợp khí X gồm ankan và anken. Tỉ khối của X so với khí hiđro là 21,75. Phần trăm thể tích của butan trong
33,33% B. 50,00%
66,67%
25,00%
Câu53.(B.08): Hiđrocacbon mạch hở X trong phân tử chỉ chứa liên kết σ và có hai nguyên tử cacbon bậc ba trong một phân tử. Đốt cháy hoàn toàn 1 thể tích X sinh ra 6 thể tích CO2 (ở cùng điều kiện nhiệt độ, áp suất). Khi cho X tác dụng với Cl2 (theo tỉ lệ số mol 1: 1), số dẫn xuất monoclo tối đa sinh ra là
A. 3. B. 4. C. 2. D. 5. Hướngdẫngiải
Số C = 6, chứa 2 C bậc ba ⇒ X:
||
1. Ankan có công thức: CnH2n+2 (n ≥ 1).
2. Ankan từ C4 trở lên có đồng phân về mạch cacbon: C4H10 (2đp), C5H12 (3đp), C6H14 (5đp).
3. Bậc cacbon = số nguyên tử cacbon liên kết trực tiếp với nguyên tử cacbon đó.
4. Khi gọi tên IUPAC của ankan: Mạch chính là mạch dài nhất, nhiều nhánh nhất; đánh số cacbon mạch chính từ phía gần nhánh nhất sao cho tổng số chỉ vị trí nhánh là nhỏ nhất.
5. Khi gọi tên thông thường: Nếu C số 2 có 1 nhánh –CH3 thì thêm tiền tố “iso”; nếu C số 2 có 2 nhánh –CH3 thì thêm tiền tố “neo”.
6. Ở đk thường, ankan C1 – C4: khí (khí gas); C5 – C17: lỏng (xăng, dầu); C18 trở lên: rắn (nến, sáp).
7. Qui tắc thế vào ankan: Ưu tiên thế vào nguyên tử hiđro của cacbon có bậc cao hơn.
8. Công thức phân tử một số ankan khi thế halogen thu được một dẫn xuất mono duy nhất: CH4,
C2H6, C5H12, C8H18.
9. Khi đốt cháy ankan ta luôn có: 22 HOCOnn > và ngược lại. 22 ankanHOCO nnn. =−
10. Một số phản ứng đặc biệt: (1) 2CH4 o 1500C lµm l¹nh nhanh
→ C2H2 + 3H2
(2) CH3COONa + NaOH → oCaO,t CH4 + Na2CO3
(3) Al4C3 + 12H2O → 4Al(OH)3 + 3CH4
1. Ankan là hiđrocacbon no, mạch hở có công thức là CnH2n+2 (n ≥ 1).
2. Bậc của một nguyên tử cacbon bằng số nguyêntử cacbon liên kết trực tiếp với nguyên tử cacbon đó.
3. Số đồng phân của ankan: C4H10 (2 đp), C5H12 (3 đp), C6H14 (5 đp).
4. Hoàn thành bảng sau:
CH3 – CH2 – CH2 – CH3 Butan
CH3 – CH(CH3) – CH2 – CH3
CH3 – CH(CH3) – CH(CH3) – CH2 – CH3
2–metylbutan
2,3– đimetylhexan
isopentan
2, 3 – đimetylbutan
3 – etyl – 2 – metylpentan
5. Ở đk thường, ankan C1 – C4: khí; C5 – C17: lỏng; C18 trở lên: rắn.
6. Khi thế vào ankan, ưu tiên thế vào nguyên tử hiđro của nguyên tử cacbon cóbậccaohơn.
7. Trong phòng thí nghiệm, metan được điều chế bằng phương pháp vôitôixút hoặc thủy phân nhômcacbua.
8. Hoàn thành các PTHH sau:
(1) CH4 + Cl2 → as 1:1 CH3Cl+HCl
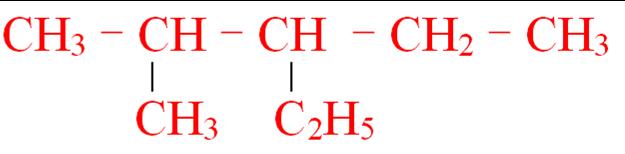
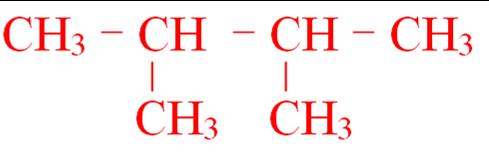
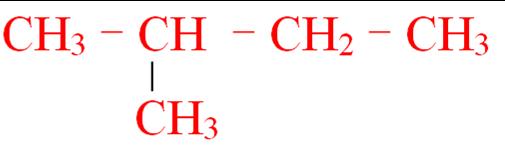
(2) CH4 + 2Cl2 → as 1:2 CH2Cl2 +2HCl
(3) CH3-CH2-CH3 + Cl2 → as 1:1 CH3 –CH2 –CH2Cl+HCl CH3 –CHCl–CH3 +HCl
Câu1. Ở điều kiện thường hiđrocacbon nào sau đây ở thể lỏng?
A. C4H10.
C5H12.
Câu2.(QG.15): Khí thiên nhiên được dùng làm nhiên liệu và nguyên liệu cho các nhà máy sản xuất điện, sứ, đạm, ancol metylic,… Thành phần chính của khí thiên nhiên là metan. Công thức phân tử của metan là
A. CH4.
B. C2H4.
C. C2H2.
D. C6H6.
Câu3.(QG.19-201). Hiện nay, nhiều nơi ở nông thôn đang sử dụng hầm biogas để xử lí chất thải trong chăn nuôi gia súc, cung cấp nhiên liệu cho việc đun nấu. Chất dễ cháy trong khí biogas là
A. Cl2. B. CH4. C. CO2.
Câu4. Các ankan không tham gia loại phản ứng nào?
A. Phản ứng thế.
C. Phản ứng tách.
D. N2.
B. Phản ứng cộng.
D. Phản ứng cháy.
Câu5. Có bao nhiêu đồng phân cấu tạo có công thức phân tử là C6H14 ?
A. 3 đồng phân. B. 4 đồng phân.
C. 5 đồng phân.
Câu6.(A.13): Tên thay thế (theo IUPAC) của (CH3)3C–CH2–CH(CH3)2 là
A. 2,2,4,4-tetrametylbutan.
C. 2,2,4-trimetylpentan.
B. 2,4,4-trimetylpentan.
D. 2,4,4,4-tetrametylbutan.
D. 6 đồng phân.
Câu7.(A.13): Khi được chiếu sáng, hiđrocacbon nào sau đây tham gia phản ứng thế với clo theo tỉ
lệ mol 1: 1, thu được ba dẫn xuất monoclo là đồng phân cấu tạo của nhau?
A. neopentan. B. pentan. C. butan. D. isopentan.
Câu8. Ankan X có công thức cấu tạo như sau:
Tên của X là
A. 1,1,3-trimetylheptan.
C. 2-metyl-4-propylpentan.
Câu9. Ankan X có công th
B. 2,4-đimetylheptan.
D. 4,6-đimetylheptan.
Tên gọi của X là
A. 2-metyl-2,4-đietylhexan.
C. 3,3,5-trimetylheptan.
B. 2,4-đietyl-2-metylhexan.
D. 3-etyl-5,5-đimetylheptan.
i đa thu được là
Câu10.(A.08): Cho isopentan
A. 5. B. 4.
C. 3.
D. 2.
Câu11.(B.12): Cho phương trính hóa học: 2X + 2NaOH o CaO, t → 2CH4 + K2CO3 + Na2CO3
Chất X là
A. CH2(COOK)2. B. CH2(COONa)2. C. CH3COOK. D. CH3COONa.
Câu12. Isohexan tác dụng với clo (có chiếu sáng) có thể tạo tối đa bao nhiêu dẫn xuất monoclo ?
A. 3. B. 4. C. 5. D. 6.
Câu13. Dãy ankan nào sau đây thỏa mãn điều kiện: mỗi công thức phân tử có một đồng phân khi tác dụng với clo theo tỉ lệ mol 1: 1 tạo ra 1 dẫn xuất monocloankan duy nhất?
A. CH4, C3H8, C4H10, C6H14.
. C. CH4, C4H10, C5H12, C6H14.
Câu14.(C.14): Hiđrocacbon X tác dụng với brom, thu được dẫn xuất monobrom duy nhất có tỉ khối hơi so với H2 bằng 75,5. Chất X là
A. 2,2-đimetylpropan B. pentan
C. 2-metylbutan D. but-1-en
Câu15.(C.07): Khi cho ankan X (trong phân tử có phần trăm khối lượng cacbon bằng 83,72%) tác dụng với clo theo tỉ lệ số mol 1:1 (trong điều kiện chiếu sáng) chỉ thu được 2 dẫn xuất monoclo
đồng phân của nhau. Tên của X là
A. butan.
C. 3-metylpentan.
B. 2,3-đimetylbutan.
D. 2-metylpropan.
Câu16.(C.08): Đốt cháy hoàn toàn một hiđrocacbon X thu được 0,11 mol CO2 và 0,132 mol H2O.
Khi X tác dụng với khí clo (theo tỉ lệ số mol 1:1) thu được một sản phẩm hữu cơ duy nhất. Tên gọi của X là
A. 2-metylbutan.
C. 2,2-đimetylpropan.
B. etan.
D. 2-metylpropan.
Câu17. (C.12): Đốt cháy hoàn toàn hỗn hợp X gồm hai hiđrocacbon kế tiếp nhau trong dãy đồng đẳng, thu được 2,24 lít khí CO2 (đktc) và 3,24 gam H2O. Hai hiđrocacbon trong X là A. C
CO2 (ở cùng
điều kiện nhiệt độ, áp suất). Khi cho X tác dụng với Cl2 (theo tỉ lệ số mol 1: 1), số dẫn xuất monoclo tối đa sinh ra là
A. 3. B. 4. C. 2. D. 5. Hướngdẫngiải
Số C = 6, chứa 2 C bậc ba ⇒ X:
Câu20.(C.07): Đốt cháy hoàn toàn một thể tích khí thiên nhiên gồm metan, etan, propan bằng oxi không khí (trong không khí, oxi chiếm 20% thể tích), thu được 7,84 lít khí CO2 (ở đktc) và 9,9 gam nước. Thể tích không khí (ở đktc) nhỏ nhất cần dùng để đốt cháy hoàn toàn lượng khí thiên nhiên
56,0 lít.
78,4 lít.
Dạng1:Bàitoánvề phản ứngthế
Dạng2:Bàitoánvề phản ứngtách(táchH2 vàcracking)
Dạng3:Bàitoánvề phản ứng đốtcháyankan
D
+ NaOH → NaX + H2O
- Nếu phản ứng cùng tỉ lệ mà có nhiều sản phẩm thế thì %mX trong mỗi sản phẩm thế là như nhau và mdẫn xuất = s¶nphÈmthÕm
VÍDỤ MINHHỌA
Câu1. Tính m hoặc V trong các trường hợp sau:
(a) Cho 4,48 lít khí etan (ở đktc) tác dụng với clo (as, tỉ lệ 1: 1) vừa đủ, sau phản ứng thu được m gam dẫn xuất monoclo. Tính m.
(b) Cho V lít khí butan (ở đktc) tác dụng với clo (as, tỉ lệ 1: 2) vừa đủ, sau phản ứng thu được 25,4 gam dẫn xuất điclo. Tính V.
Câu2. Xác định công thức cấu tạo và tên gọi của ankan X trong các trường hợp sau:
(a) (B.07): Khi brom hóa một ankan X chỉ thu được một dẫn xuất monobrom duy nhất có tỉ khối hơi đối với hiđro là 75,5.
(b) Cho ankan X tác dụng với clo theo tỉ lệ mol 1:1, thu được hai dẫn xuất monoclo Y1 và Y2 Trong Y1 và Y2 đều có 45,22 % clo về khối lượng.
(c) Cho 1,08 gam ankan X tác dụng với brom theo tỉ lệ mol 1:1 thu được 2,265 gam dẫn xuất monobrom duy nhất.
(d) Cho 5,8 gam ankan X tác dụng với brom theo tỉ lệ mol 1:1, thu được hai dẫn xuất monobrom có khối lượng lần lượt là 11,1 và 2,6 gam.
Câu3. Clo hóa 0,1 mol ankan A thu được duy nhất một sản phẩm hữu cơ là dẫn xuất clo B có khối lượng 9,9 gam. Công thức phân tử của B là
ướngdẫngiải
PTHH: CnH2n+2 + xCl2 → CnH2n+2-xClx + xHCl 0,1 → 0,1 mol
Mdx = 99 = 14n + 34,5x +2 ⇒ 14n + 34,5x = 97
Câu4. Cho ankan X tác dụng với clo (as), thu được 26,5 gam hỗn hợp các dẫn xuất clo (monoclo và điclo). Khí HCl bay ra được hấp thụ hoàn toàn bằng nước, sau đó trung hòa bằng dung dịch
NaOH, thấy dùng hết 500 ml dung dịch NaOH 1M. Công thức phân tử của X là
m thế monoclo có 70,3 %
clo về khối lượng. Công thức phân tử của B là
A. CH4. B. C3H8. C. C5H12. D. C6H14.
Câu7. Ankan A phản ứng với Cl2 (tỉ lệ mol 1:2) thu được duy nhất một sản phẩm có chứa 83,53 %
clo về khối lượng. Công thức phân tử của A là
A. CH4. B. C2H6. C. C3H8. D. C5H12.
Câu8. Cho 3,2 gam ankan X tác dụng với brom theo tỉ lệ mol 1:1 chỉ tạo ra 19 gam monobrom duy nhất. Công thức phân tử của X là
A. CH4. B. C3H8.
C. C4H10.
D. C5H12.
Câu9. Cho 2,16 gam ankan X tác dụng với clo theo tỉ lệ mol 1:1 tạo ra 3,195 gam dẫn xuất monoclo duy nhất. Công thức phân tử của X là
A. CH4 B. C3H8
C. C4H10
D. C5H12
Câu10.(C.14): Hiđrocacbon X tác dụng với brom, thu được dẫn xuất monobrom duy nhất có tỉ khối hơi so với H2 bằng 75,5. Chất X là
A. 2,2-đimetylpropan. B. pentan.
C. 2-metylbutan. D. but-1-en.
Câu11. Cho 7,2 gam ankan X tác dụng với clo theo tỉ lệ mol 1:1 tạo ra 10,65 gam dẫn xuất monoclo duy nhất. Công thức cấu tạo thu gọn của X là
A. (CH3)2CH CH(CH3)2.
C. (CH3)4C.
B. CH4.
D. CH3CH2CH2CH2CH3.
Câu12.(C.07): Khi cho ankan X (trong phân tử có phần trăm khối lượng cacbon bằng 83,72%) tác dụng với clo theo tỉ lệ sốmol 1:1 (trong điều kiện chiếu sáng) chỉ thu được 2 dẫn xuất monoclo
đồng phân của nhau. Tên của X là
A. butan.
C. 3-metylpentan.
B. 2,3-đimetylbutan.
D. 2-metylpropan.
Câu13. Cho ankan X tác dụng với brom theo tỉ lệ mol 1:1 thu được ba dẫn xuất monobrom. Cả ba dẫn xuất đều có 52,98 % brom về khối lượng. Tên gọi của X là
A. 2,2-đimetylpropan.
C. 2,2-đimetylpentan.
B. 2-metylbutan.
D. pentan.
Câu14. Cho ankan X tác dụng với clo theo tỉ lệ mol 1:1 thu được sáu dẫn xuất monoclo Y1, Y2, Y3, Y4, Y5, Y6 đều có 26,39 % clo về khối lượng. Công thức phân tử của X là
A. C5H12 B. C6H14 C. C7H16 D. C8H18
Câu15. Cho ankan X tác dụng với brom theo tỉ lệ mol 1:1 thu được hỗn hợp hai dẫn xuất monobrom có cùng thành phần phần trăm khối lượng brom là 58,39 %. X là
A. 2-metylpropan.
C. butan hoặc 2-metylpropan.
B. butan.
D. 2-metylbutan.
Câu16. Cho ankan Y tác dụng với clo theo tỉ lệ mol 1:1 thu được hỗn hợp hai dẫn xuất monoclo Z1
và Z2 có cùng thành phần phần trăm khối lượng clo là 29,46 %. Công thức phân tử của Y là
A. 3-metylpentan.
C. 2,3-đimetylbutan.
B. 2-metylpentan.
D. 2,2-đimetylbutan.
Câu17. Cho 5,8 gam ankan X tác dụng với brom theo tỉ lệ mol 1:1 thu được hai dẫn xuất monobrom Y và Z có khối lượng lần lượt là 11,1 gam và 2,6 gam. Tên gọi của X là
A. 2-metylpropan.
C. butan hoặc 2-metylpropan.
B. butan.
D. 2,4-đimetylpentan.
Câu18. Cho 8,6 gam ankan A tác dụng với clo theo tỉ lệ mol 1:1 thu được ba dẫn xuất monoclo có khối lượng lần lượt là 3,4 gam; 4,05 gam và 4,6 gam. Công thức phân tử của A là
A. C6H14. B. C4H10. C. C7H16. D. C2H6.
Câu19. Cho 12,9 gam ankan X tác dụng với brom theo tỉ lệ mol 1:1 thu được năm sản phẩm thế monoclo có tổng khối lượng là 24,75 gam. Tên gọi của X là
A. 2-metylpentan. B. 3-metylpentan.
C. 2,3-đimetylbutan.
D. 2,2-đimetylbutan.
Câu20. Cho 10 gam ankan X tác dụng với clo theo tỉ lệ mol 1:1 thu được sáu dẫn xuất monoclo với tổng khối lượng là 13,45 gam. Công thức phân tử của X là
A. C6H14. B. C7H16. C. C8H18.
D. C5H12.
Câu21. Cho 18 gam X tác dụng với brom theo tỉ lệ mol 1:1 thu được bốn dẫn xuất thế monobrom Y1, Y2, Y3, Y4 có tổng khối lượng là 37,75 gam. Tên gọi của X là
A. 2,2-đimetylpropan.
B. 2,2-đimetylpentan.
C. 2-metylbutan. D. 2-metylpentan.
Câu22. Brom hóa 0,02 mol ankan X thu được 5,06 gam dẫn xuất brom Y. Công thức phân tử của
Y là
A. CH2Br2
B. CHBr3
C. C2H4Br2
D. C3H5Br3
Câu23. Cho 0,25 mol ankan A tác dụng với brom chỉ thu được duy nhất một sản phẩm hữu cơ là dẫn xuất brom B có khối lượng 37,75 gam. Tên gọi của A là
A. 2-metylbutan.
C. pentan.
B. 2,2-đimetylpropan.
D. 2,3-đimetylpropan.
Câu24. Trong phân tử hiđrocacbon X có 6 nguyên tử cacbon và chỉ có liên kết σ. Khi clo hóa X (tỉ lệ mol 1:1, chiếu sáng) thu được hai sản phẩm thế monoclo là đồng phân của nhau. Tên gọi của X là
A. 2-metylpentan.
C. 3-metylpentan.
B. 2,3-đimetylbutan.
D. 2,2-đimetylbutan.
Hướngdẫngiải X chỉ có liên kết σ và dựa vào đáp án ⇒ X là ankan có 6C. X thế clo thu được 2 dẫn xuất monoclo nên X là
CHCHCHCH CHCH : 2, 3 - đimetylbutan.
33 || 33
Câu25. Hai hiđrocacbon A và B đều có công thức phân tử C5H12 cùng tác dụng với clo theo tỉ lệ mol 1:1 (chiếu sáng) thì A tạo ra một dẫn xuất monoclo duy nhất, B tạo ra bốn dẫn xuất. Tên gọi của A và B lần lượt là:
A. 2,2-đimetylpropan và butan.
C. 2-metylbutan và butan.
B. 2,2-đimetylpropan và 2-metylbutan.
D. 2-metylbutan và 2,2-đimetylpropan.
Hướngdẫngiải
CH3 –CH2 –CH2 –CH2 –CH3:pentan(3dẫnxuất)
:2–metylbutan(4d
:2,2– đimetylpentan(1d
CmH2m+2 + CqH2q (n = m + q) - Phương pháp: BTKL: mT = mS ⇔ nT. TM = nS. SM Chú ý: nkhí tăng = 2 Hankanph¶nøngnk.n = == = ; nếu k = 1 (tạo anken) ⇒ nkhí tăng = nankan phản ứng.
- Công thức tính nhanh hiệu suất phản ứng tách: Hỗn hợp ankan X oxt,t → Hỗn hợp Y X
M H%1.100%
VÍDỤ MINHHỌA
( XYM,M là khối lượng mol trung bình của X, Y)
Câu1. Tính m trong các trường hợp sau:
(a) Cracking m gam butan ở điều kiện thích hợp thu được 0,75 mol hỗn hợp X có tỉ khối hơi so với H2 là 11,2.
(b) Nung nóng m gam hỗn hợp X gồm etan, propan và butan (xúc tác thích hợp) thu được 0,84 lít (ở đktc) hỗn hợp Y có tỉ khối so với H2 là 16.
Đápsố:(a)16,8gam;(b)26,88gam.
Câu2. Cracking 2,24 lít hỗn hợp X gồm ba ankan thu được 5,264 lít hỗn hợp Y. Các thể tích khí đo cùng điều kiện. Tỉ khối của hỗn hợp X so với hỗn hợp Y là A. 2,35. B. 0,43. C. 1,18. D. 0,85.
Câu3. Nung nóng 134,4 cm3 hỗn hợp ankan X (xúc tác thích hợp) thu được 168 cm3 hỗn hợp Y có tỉ khối hơi so với hiđro là 20. Thể tích các khí đo ở điều kiện tiêu chuẩn. Khối lượng mol trung bình của hỗn hợp X là
A. 50 g/mol. B. 25 g/mol. C. 250 g/mol. D. 5 g/mol. Câu4. Xác định công thức phân tử của ankan X biết
(a) Dẫn 1 mol ankan X qua xúc tác niken nung nóng, sau một thời gian thu được 2 mol hỗn hợp Y có tỉ khối so với hiđro bằng 14,5.
(b) (A.08): Khi cracking hoàn toàn một thể tích ankan X thu được ba thể tích hỗn hợp Y (các thể tích khí đo ở cùng điều kiện nhiệt độ và áp suất); tỉ khối của Y so với H2 bằng 12.
(c) Nung nóng V lít ankan X (xúc tác thích hợp) thu được 2V lít hỗn hợp Y có tỉ khối hơi so với hiđro bằng 18. Các giá trị thể tích đo ở cùng điều kiện nhiệt độ và áp suất.
Đápsố:(a)C4H10;(b)C5H12;(c)C5H12.
Câu5. Phản ứng cracking propan diễn ra
c h
u suất phản ứng cracking là
Câu6. Tính hiệu suất phản ứng cracking ankan trong các trường hợp sau:
(a) Tiến hành crackinh 10 lít khí butan, sau phản ứng thu được 18 lít hỗn hợp khí X gồm etan, metan, eten, propilen, butan (các khí đo cùng điều kiện).
Hướngdẫngiải butanp−khÝt¨ng
(b) Dẫn một lượng butan qua xúc tác niken nung nóng, giả sử chỉ xảy ra phản ứng cracking: C4H10 ⟶ C3H6 + CH4. Sau một thời gian, thu được hỗn hợp Y có tỉ khối hơi so với hiđro là 18,125. Hướngdẫngiải
(c) (C.12): Nung một lượng butan trong bình kín (có xúc tác thích hợp) thu được h
ố mol của nó).
2 ankanHXankanankan512 n4mol;n1molm4M2.15.58M72:CH
Câu9.[QG.21-201] Nung nóng một lượng butan trong bình kín (với xúc tác thích hợp), thu được
0,82 mol hỗn hợp X gồm H2 và các hiđrocacbon mạch hở (CH4, C2H4, C2H6, C3H6, C4H8, C4H10). Cho toàn bộ X vào bình chứa dung dịch Br2 dư thì có tối đa a mol Br2 phản ứng, khối lượng bình tăng 15,54 gam và thoát ra hỗn hợp khí Y. Đốt cháy hoàn toàn Y cần vừa đủ 0,74 mol O2, thu được CO2 và H2O. Giá trị của a là
t lượng butan trong bình kín (với xúc tác thích hợp), thu
được 0,48 mol hỗn hợp X gồm H2 và các hidrocacbon mạch hở (CH4, C2H
C4H10). Cho toàn b
, C
khối so với H2 là 9. Giá trị của a là
A. 1,35. B. 0,675.
C. 2,70.
D. 6,75.
Câu12. Nhiệt phân a gam ankan (xúc tác thích hợp) thu được 896 ml (ở đktc) hỗn hợp khí có tỉ khối so với heli là 5. Giá trị của a là
A. 0,8. B. 0,04.
C. 0,2.
D. 0,02.
Câu13. Nung nóng hỗn hợp X gồm propan và butan (xúc tác thích hợp) thu được 560 ml (ở đktc) hỗn hợp Y có tỉ khối so với H2 là 16. Khối lượng hỗn hợp X là
A. 0,8 gam. B. 0,4 gam. C. 0,04 gam. D. 0,2 gam.
Câu14. Nung nóng hỗn hợp X gồm butan, pentan và hexan (xúc tác thích hợp) thu được 291,2 cm3 (đktc) hỗn hợp Y có tỉ khối hơi so với heli là 11. Khối lượng hỗn hợp X là
A. 5,72 gam. B. 0,286 gam. C. 2,86 gam. D. 0,572 gam.
Câu15. Cracking 1,792 lít hỗn hợp A gồm C4H10 và C6H14 thu được 4,032 lít hỗn hợp B có tỉ khối so với hiđro là 20,5. Thể tích các khí đo ở điều kiện tiêu chuẩn. Khối lượng mol trung bình của hỗn hợp B là
A. 92,25. B. 46,13. C. 4,61.
D. 9,22.
Câu16. Nung nóng 336 ml hỗn hợp propan và butan (xúc tác thích hợp) thu được 840 ml hỗn hợp
X gồm H2, CH4, C2H4, C3H6, C3H8 (dư) và C4H10 (dư). Các thể tích khí đo ở cùng điều kiện. Tỉ khối của X so với hỗn hợp ankan ban đầu là
A. 0,4. B. 0,8.
C. 0,2.
D. 5.
Câu17.(C.12): Nung một lượng butan trong bình kín (có xúc tác thích hợp) thu được hỗn hợp khí
X gồm ankan và anken. Tỉ khối của X so với khí hiđro là 21,75. Phần trăm thể tích của butan trong X là
A. 33,33% B. 50,00% C. 66,67%
D. 25,00%
Câu18. Cracking hoàn toàn 1 mol ankan A thu được 5 mol hỗn hợp B có tỉ khối so với H2 bằng
8,6. Công thức phân tử của ankan A là
A. CH4. B. C3H8.
0,05. B. 0,025.
C5H12.
C6H14. Câu19. Nung nóng V lít ankan X (xúc tác thích hợp) thu được 2V lít hỗn hợp Y có tỉ khối hơi so với hiđro bằng 14,5. Các giá trị thể tích đo ở cùng điều kiện nhiệt độ và áp suất. Nếu ban đầu có 0,05 mol X phản ứng thì có mấy mol Y tạo thành?
0,1.
0,25.
Câu20. Nung nóng V lít ankan A (xúc tác thích hợp) thu được 3V lít hỗn hợp B có tỉ khối hơi so với hiđro bằng 12. Các giá trị thể tích đo ở cùng điều kiện nhiệt độ và áp suất. Công thức phân tử của ankan A là
A. C3H8 B. C4H10 C. C5H12 D. C6H14
Câu21. Nung nóng V lít ankan X (xúc tác thích hợp) thu được V lít hỗn hợp Y có tỉ khối so với heli bằng 4. Các giá trị thể tích đo ở cùng điều kiện nhiệt độ và áp suất. X tác dụng với brom theo tỉ lệ mol 1:1 chỉ tạo ra một dẫn xuất thế monobrom duy nhất. Tên gọi của X là
A. metan.
C. 2,3-đimetylbutan.
B. 2,2-đimetylpropan.
D. 2,2,3,3-tetrametylbutan.
Câu22. Cracking hoàn toàn một thể tích ankan A thu được ba thể tích hỗn hợp B (các thể tích khí đo ở cùng điều kiện nhiệt độ và áp suất); tỉ khối của B so với H2 bằng 16,67. A có cấu tạo mạch
thẳng. Tên gọi của A là
A. pentan. B. hexan. C. heptan. D. octan.
Câu23. Nung nóng 1 mol butan (xúc tác thích hợp), giả sử chỉ xảy ra phản ứng cracking sau:
C4H10 oxt,t
CH4 + C3H6
Sau phản ứng, thu được 0,4 mol metan. Hiệu suất phản ứng cracking là
A. 60,00 %. B. 40,00 %. C. 66,67 %. D. 33,33 %.
Câu24. Nung nóng 0,01 mol propan (xúc tác thích hợp), giả sử chỉ xảy ra phản ứng cracking sau:
C3H8 o
ng nhiệt phân metan: 2CH4 o 1500 C → C2H2 + 3H2 Nhiệt phân 1 mol metan, sau một thời gian thu được hỗn hợp X gồm C2H2, H2 và CH4 dư có tỉ khối so với H2 bằng 5. Hiệu suất phản ứng nhiệt phân metan là
A. 30 %. B. 40 %.
C. 60 %. D. 70 %.
Câu31. Nhiệt phân 1 mol metan, sau một thời gian thu được hỗn hợp Y gồm ba chất khí. Tỉ khối hơi của hỗn hợp Y so với heli bằng 3,3. Hiệu suất phản ứng nhiệt phân metan là
A. 10,5 %. B. 21,22 %. C. 79,0 %. D. 89,5 %.
Câu32. Nhiệt phân một lượng metan, sau một thời gian thu được hỗn hợp X gồm C2H2, H2 và CH4 dư có tỉ khối so với hiđro là 5,75. Hiệu suất phản ứng nhiệt phân metan là
A. 39,13 %. B. 19,56 %. C. 60,87 %. D. 80,44 %.
Câu33.[QG.21-203] Nung nóng một lượng butan trong bình kín (với xúc tác thích hợp), thu
được 0,4 mol hỗn hợp X gồm H2 và các hiđrocacbon mạch hở (CH4, C2H4, C2H6, C3H6, C4H8, C4H10). Cho toàn bộ X vào bình chứa dung dịch Br2 dư thì có tối đa a mol Br2 phản ứng, khối lượng
bình tăng 8,12 gam và thoát ra hỗn hợp khí Y. Đốt cháy hoàn toàn Y cần vừa đủ 0,30 mol O2, thu
được CO2 và H2O. Giá trị của a là
hoàn toàn m1 gam pentan bằng V lít khí O2 vừa đủ, sau phản ứng thu được 2,24 lít khí CO2 và m2 gam nước. Biết rằng các thể tích đều đo ở đktc, tính V, m1, m2
Đápsố:m1 =1,44gam;m2 =2,16gam;V=3,584lít.
Câu2. Khi đốt cháy hoàn toàn 7,84 lít hỗn hợp khí gồm CH4, C2H6, C3H8 (đktc) thu được 16,8 lít
khí CO2 (đktc) và a gam H2O. Tính a.
Đápsố:a=19,8gam.
Câu3. Xác định công thức phân tử, viết các đồng phân và gọi tên X trong các trường hợp sau:
(a) (C.08): Đốt cháy hoàn toàn một hiđrocacbon X thu được 0,11 mol CO2 và 0,132 mol H2O.
(b) Đốt cháy hoàn toàn hiđrocacbon X cần vừa đủ 0,065 mol O2. Dẫn sản phẩm tạo thành qua
bình đựng nước vôi trong dư thì thấy xuất hiện 4 gam kết tủa trắng.
(c) (C.12): Đốt cháy hoàn toàn hỗn hợp X gồm hai hiđrocacbon kế tiếp nhau trong dãy đồng
đẳng, thu được 2,24 lít khí CO2 (đktc) và 3,24 gam H2O.
(d) Đốt cháy hoàn toàn hỗn hợp gồm hai hiđrocacbon X và Y liên tiếp trong cùng dãy đồng
đẳng, thu được hỗn hợp gồm CO2 và H2O có tỉ lệ thể tích là 22 COHO V:V12:17. = Các thể tích đo ở
cùng điều kiện, MX < MY.
(e) Đốt cháy hỗn hợp gồm hai hiđrocacbon cùng dãy đồng đẳng X và Y (MX < MY) thu được
5,28 gam CO2 và 3,96 gam hơi nước.
Đápsố:(a)C5H12;(b)C4H10;(c)CH4 vàC2H6;(d)C2H6 vàC3H8;(e)
Câu4. Đốt cháy hoàn toàn hỗn hợp X gồm hai hiđrocacbon liên tiếp nhau trong dãy đồng đẳng, thu
được hỗn hợp sản phẩm gồm CO2 và H2O. Dẫn hỗn hợp sản phẩm lần lượt đi qua hai bình hóa chất:
Bình 1: chứa H2SO4 đặc, thấy khối lượng bình phản ứng tăng lên 6,3 gam.
Bình 2: chứa Ca(OH)2 dư, thấy xuất hiện 25 gam kết tủa.
th
c phân tử của các hiđrocacbon trong hỗn hợp X là:
Câu5.(C.07): Đốt cháy hoàn toàn một thể tích khí thiên nhiên gồm metan, etan, propan bằng oxi không khí (trong không khí, oxi chiếm 20% thể tích), thu được 7,84 lít khí CO2 (ở đktc) và 9,9 gam nước. Thể tích không khí (ở đktc) nhỏ nhất cần dùng
ậc ba trong một phân tử Đốt cháy hoàn toàn 1 thể tích X sinh ra 6 thể tích CO2 (ở cùng điều kiện nhiệt độ, áp suất). Khi cho X tác dụng với Cl2 (theo tỉ lệ số mol 1: 1), số dẫn xuất monoclo tối đa sinh ra là
A. 3. B. 4. C. 2. D. 5. Hướngdẫngiải
CHCHCHCH CHCH
Số C = 6, chứa 2 C bậc ba ⇒ X: 33 || 33
Câu7. Đốt cháy hoàn toàn một lượng hiđrocacbon Z thu được 2,688 lít CO2 (đktc)và 2,52 gam nước. Z tác dụng với clo khi có ánh sáng khuếch tán theo tỉ lệ mol 1:1 chỉ tạo ra ba sản phẩm thế (trong đó có hai sản phẩm thế vào nguyên tử cacbon bậc một). Tên gọi của Z là
A. 2,3-đimetylbutan. B. 2,2-đimetylbutan. C. 3-metypentan. D. 2-metylpentan.
Hướngdẫngiải
COHOZ614 0,12 n0,12mol;n0,14molC6:CH 0,140,12
Z thế monoclo tạo 3 sản phẩm thế trong đó có 2 sản phẩm thế vào cacbon bậc một nên Z là
CH CH-C-CHCH CH
BÀITẬPTỰ LUYỆN
Câu8. Đốt cháy hoàn toàn một hiđrocacbon A thu được 1,32 gam CO2 và 0,72 gam H2O. Tên gọi của A là
A. metan. B. etan. C. propan. D. butan.
Câu9. Đốt cháy hoàn toàn hiđrocacbon B thu được 13,44 lít CO2 (đktc) và 13,5 gam hơi nướ
Công thức phân tử của B là
A. C4H8. B. C4H10.
C. C3H8.
D. C3H6.
Câu10. Đốt cháy hoàn toàn hiđrocacbon X thu được 3,36 lít CO2 (đktc) và 3,15 gam hơi nước.
Công thức phân tử của X là
A. C4H10
Câu11. Đốt cháy hoàn toàn hiđrocacbon X
thức phân tử của X là A.
. Dẫn sản phẩm cháy vào bình đựng nước vôi trong dư thì thấy tạo ra 50 gam kết tủa trắng. Công thức phân tử của X là
A. C4H10
B. C5H12
C. C6H14
D. C8H18
Câu14. Đốt cháy hoàn toàn hiđrocacbon X cần vừa đủ 2,8 lít O2 (đktc), sản phẩm tạo thành được dẫn qua bình đựng nước vôi trong dư, tạo ra 8 gam kết tủa. Công thức phân tử của X là
Câu15. Đốt cháy hoàn toàn 1 hiđrocacbon Y thu được số mol H2O gấp 1,5 lần số mol CO2. Công thức phân tử của Y là A.
Câu16. Đốt cháy 1 mol hiđrocacbon X thu được ít hơn 3 mol CO2 và CO2
n n 0,5 = . Công thức phân tử của X là
Câu17. Đốt cháy hoàn toàn 0,56 lít butan (ở đktc) và cho tất cả sản phẩm cháy hấp thụ vào bình
đựng 750 ml dung dịch Ba(OH)2 0,2 M. Khối lượng kết tủa tạo thành là
A. 9,85 gam. B. 12,40 gam. C. 19,70 gam. D. 23,30 gam.
Sử dụng dữ kiện sau để trả lời các câu hỏi 18, 19, 20
Đốt cháy hoàn toàn 0,56 lít butan (ở đktc) và cho tất cả sản phẩm cháy hấp thụ vào bình đựng
400 ml dung dịch Ba(OH)2 0,2 M.
Câu18. Khối lượng kết tủa tạo thành là
A. 9,85 gam. B. 9,98 gam. C. 10,40 gam. D. 11,82 gam.
Câu19. Khối lượng bình dung dịch Ba(OH)2 tăng lên
A. 5,56 gam. B. 6,10 gam. C. 6,65 gam. D. 10,08 gam.
Câu20. Khối lượng dung dịch trong bình thay đổi như thế nào?
Câu21.(C.08): Đốt cháy hoàn toàn một hiđrocacbon X thu được 0,11 mol CO2 và 0,132 mol H2O.
Khi X tác dụng với khí clo (theo tỉ lệ số mol 1:1) thu được một sản phẩm hữu cơ duy nhất. Tên gọi
của X là
A. 2-metylbutan. B. etan.
C. 2,2-đimetylpropan. D. 2-metylpropan.
Câu22.(C.10): Đốt cháy hoàn toàn 6,72 lít (đktc) hỗn hợp gồm hai hiđrocacbon X và Y (MY >
MX), thu được 11,2 lít CO2 (đktc) và 10,8 gam H2O. Công thức của X là
A. C2H6
B. C2H4
C. CH4
D. C2H2
Câu23. Đốt cháy hoàn toàn 19,2 gam hỗn hợp hai ankan liên tiếp nhau trong dãy đồng đẳng, thu
được 57,2 gam CO2. Công thức phân tử của hai ankan là:
A. CH4 và C2H6
C. C3H8 và C4H10.
B. C2H6 và C3H8
D. C2H6 và C4H10.
Câu24. Đốt cháy hoàn toàn 9,64 gam hỗn hợp hai ankan liên tiếp nhau trong dãy đồng đẳng thu
được 29,04 gam CO2. Công thức phân tử của hai ankan là:
A. CH4 và C2H6
C. C3H8 và C4H10.
B. C2H6 và C3H8
D. C4H10 và C5H12.
Câu25. Đốt cháy hoàn toàn 3,39 gam hỗn hợp hai ankan liên tiếp trong dãy đồng đẳng thu được
10,34 gam CO2. Công thức phân tử của hai ankan là:
A. CH4 và C2H6
C. C3H8 và C4H10.
B. C2H6 và C3H8
D. C4H10 và C5H12.
Câu26. Đốt cháy hoàn toàn hỗn hợp gồm hai hiđrocacbon mạch thẳng X và Y liên tiếp nhau trong
cùng dãy đồng đẳng (MX < MY), thu được hỗn hợp CO2 và H2O có tỉ lệ thể tích 22 COHO V:V8:13 = .
Tên gọi của X là
A. metan. B. etan.
C. propan. D. butan.
Câu27. Đốt cháy hỗn hợp hiđrocacbon X thu được a mol CO2 và b mol hơi nước. Trong trường hợp nào dưới đây, có thể kết luận X là hỗn hợp của các ankan?
A. a = 0,25; b = 0,225.
C. a = 0,025; b = 0,03.
B. a = 0,05; b = 0,04.
D. a = 0,22; b = 0,22.
Câu28. Đốt cháy hỗn hợp hiđrocacbon A, thu được a lít CO2 (đktc) và b gam hơi nước. Trong trường hợp nào dưới đây thì có thể kết luận A là hỗn hợp của các ankan?
A. a = 4,48; b = 5,4.
C. a = 1,792; b = 1,44.
B. a = 6,72; b = 4,5.
D. a = 7,84; b = 5,4.
Câu29. Đốt cháy hỗn hợp hiđrocacbon X thu được hỗn hợp CO2 và H2O. Nếu dẫn hỗn hợp sản phẩm cháy qua bình chứa H2SO4 đậm đặc, thấy khối lượng bình tăng lên 2,7 gam. Nếu dẫn bình qua bình chứa dung dịch nước vôi trong dư, thấy khối lượng bình tăng lên m gam. Trong trường hợp nào sau đây, có thể kết luận X là hỗn hợp ankan?
A. m = 7,1. B. m = 9,3. C. m = 11,5. D. m = 15,9. Câu30. Đốt cháy hoàn toàn hỗn hợp ankan X cần vừa đủ 0,672 lít O2 (ở đktc). Sản phẩm tạo thành
được dẫn qua bình đựng dung dịch Ca(OH)2 thì thấy tạo ra m gam kết tủa. Trong trường hợp nào dưới đây thì có thể kết luận X là hỗn hợp hai ankan?
A. m = 1,5. B. m = 2,0. C. m = 2,5. D. m = 2,2. Câu31. Đốt cháy hỗn hợp gồm hai hiđrocacbon cùng dãy đồng đẳng X và Y (MX < MY) thu được 22,44 gam CO2 và 14,58 gam nước. Biết Y có nhiều hơn X hai nguyên tử cacbon. Y là
metan. B. propan. C. butan. D. hexan.
Câu32. Đốt cháy hoàn toàn hỗn hợp A gồm metan, etan và propan thu được 4,928 lít CO2 (ở
2 + ==→==
Câu33. Đốt cháy hoàn toàn hỗn hợp khí thiên nhiên gồm CH4, C2H6, C3H8 và C4H10 thu được
18,144 lít CO2 và 19,98 gam H2O. Thể tích oxi cần dùng để đốt cháy hỗn hợp khí thiên nhiên trên
là (biết các thể tích khí đo ở điều kiện tiêu chuẩn)
A. 30,576 lít. B. 25,760 lít. C. 32,816 lít. D. 34,832 lít.
Hướngdẫngiải
Hướngdẫngiải
22 COHO 410 0,4 n0,4mol;n0,5moln4:CH 0,50,4
Y thế brom tạo 2 sản phẩm thế monoclo trong đó có 1 sản phẩm thế vào cacbon bậc ba nên Y là
CH-CH-CH CH :2–metylbutan
33 | 3
Câu35. Hiđrocacbon mạch hở Y trong phân tử chỉ có liên kết đơn và có một nguyên tử cacbon bậc bốn. Đốt cháy hoàn toàn Y thu được 0,1 mol CO2 và 2,16 gam nước. Brom hóa Y (chiếu sáng) theo tỉ lệ mol 1:1 thì số dẫn xuất monobrom tối đa tạo thành là
Câu36. Hiđrocacbon mạch hở Z trong phân tử chỉ có liên kết σ và một nguyên tử cacbon bậc bốn.
Câu1. Phản ứng đặc trưng của hiđrocacbon no là
A. Phản ứng thế
C. Phản ứng oxi hóa.
B. Phản ứng tách.
D. Phản ứng cộng.
Câu2. Ở điều kiện thường hiđrocacbon nào sau đây ở thể lỏng?
A. C5H12. B. C3H8.
Câu3. Thành phần chính của “khí thiên nhiên” là
A. butan. B. etan.
C. C4H10.
D. C2H6.
C. metan. D. propan.
Câu4. Ankan là những hiđrocacbon no, mạch hở, có công thức chung là
A. CnH2n (n ≥2).
C. CnH2n-6 (n ≥6).
Câu5. Nhóm nguyên tử CH3CH2- có tên là
A. metyl. B. etyl.
B. CnH2n+2 (n ≥1).
D. CnH2n-2 (n ≥2).
C. propyl. D. butyl.
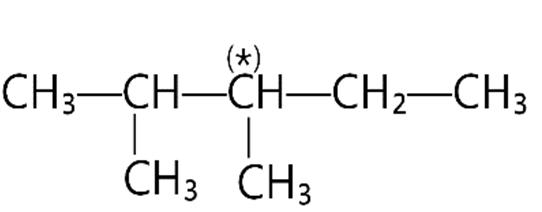
Câu6.(QG.15): Khí thiên nhiên được dùng làm nhiên liệu và nguyên liệu cho các nhà máy sản xuất điện, sứ, đạm, ancol metylic,… Thành phần chính của khí thiên nhiên là metan. Công thức phân tử của metan là A. CH4
Câu7.(QG.19-201). Hiện nay, nhiều nơi ở nông thôn đang sử dụng hầm biogas để xử lí chất thải trong chăn nuôi gia súc, cung cấp nhiên liệu cho việc đun nấu. Chất dễ cháy trong khí biogas là
A. Cl2 B. CH4
Câu8. Bậc của nguyên tử cacbon đánh dấu (*) trong hợp chất sau là
A. bậc I.
B. bậc II.
C. bậc III.
N2
D. bậc IV.
Câu9. Nung nóng isobutan với xúc tác thích hợp thu được isobutilen C4H8, phản ứng đã xảy ra là
A. C4H8 + H2 oxt,t →
.
H6 Câu10. Khi đốt cháy một hiđrocacbon, thu được a mol CO2 và b mol H2O. Trong trường hợp nào sau đây có thể kết luận rằng hiđrocacbon đó là ankan?
A. a > b. B. a < b. C. a = b. D. a ≥ b.
Câu11. Có bao nhiêu đồng phân cấu tạo có công thức phân tử là C5H12?
A. 4 đồng phân. B. 5 đồng phân. C. 3 đồng phân. D. 6 đồng phân.
Câu12. Ankan X có công thức cấu tạo như sau: CH3 CH CH2 CH CH2 CH2 CH3
Tên của X là
A. 1,1,3-trimetylheptan.
C. 4,6-đimetylheptan.
B. 2-metyl-4-propylpentan.
D. 2,4-đimetylheptan.
Câu13.(A.13): Tên thay thế (theo IUPAC) của (CH3)3C–CH2–CH(CH3)2 là
A. 2,2,4,4-tetrametylbutan. B. 2,4,4-trimetylpentan. C. 2,2,4-trimetylpentan. D. 2,4,4,4-tetrametylbutan.
Câu14.(B.12): Cho phương trính hóa học: 2X + 2NaOH o CaO, t → 2CH4 + K2CO3 + Na2CO3 Chất X là
A. CH2(COOK)2. B. CH2(COONa)2. C. CH3COOK. D. CH3COONa.
Câu15.(A.08): Cho isopentan tác dụng với Cl2 theo tỉ lệ số mol 1: 1, số sản phẩm monoclo tối đa thu được là
A. 5. B. 4. C. 3. D. 2.
Câu16.(A.13): Khi được chiếu sáng, hiđrocacbon nào sau đây tham gia phản ứng thế với clo theo tỉ lệ mol 1: 1, thu được ba dẫn xuất monoclo là đồng phân cấu tạo của nhau?
A. neopentan. B. pentan. C. butan. D. isopentan.
Câu17. Khi phản ứng với brom (tỉ lệ mol 1:1), chiếu sáng, 2-metylpentan có thể tạo ra sản phẩm chính là dẫn xuất thế ở cacbon nào?
Câu18. Khi cho 2-metylbutan tác dụng với Cl2 theo tỉ lệ mol 1: 1 thì tạo ra sản phẩm chính là
A. 2-clo-2-metylbutan.
C. 1-clo-3-metylbutan.
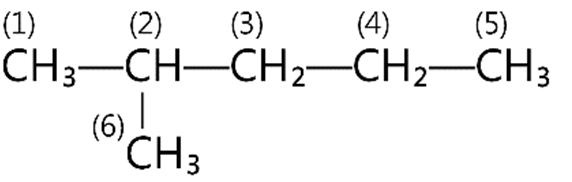
B. 2-clo-3-metylbutan.
D. 1-clo-2-metylbutan.
Câu19. Khi được chiếu sáng, hiđrocacbon nào sau đây tham gia phản ứng thế với clo theo tỉ lệ mol 1:1, thu được nhiều dẫn xuất monoclo là đồng phân cấu tạo của nhau nhất?
A. butan. B. pentan. C. neopentan. D. isopentan.
Câu20. Khi clo hóa hỗn hợp 2 ankan, người ta chỉ thu được 3 sản phẩm thế monoclo. Tên gọi của 2 ankan đó là
A. isobutan và pentan.
B. neopentan và etan.
C. etan và propan. D. propan và isobutan.
Câu21. Hai hiđrocacbon X và Y có cùng công thức phân tử C5H12 tác dụng với Cl2 theo tỉ lệ mol 1: 1, X tạo ra 1 dẫn xuất duy nhất, còn Y cho 4 dẫn xuất. Tên gọi của X và Y lần lượt là
A. 2-metylbutan và pentan.
C. 2,2-đimetylpropan và 2-metylbutan.
B. 2,2-đimetylpropan và pentan.
D. 2-metylbutan và 2,2-đimetylpropan.
Câu22. Trong phòng thí nghiệm có thể điều chế metan bằng cách nào sau đây?
A. Cho nhôm cacbua tác dụng với nước.
B. Nhiệt phân natri axetat với vôi tôi xút hoặc cho nhôm cacbua tác dụng với nước.
C. Nhiệt phân natri axetat với vôi tôi xút.
D. Crackinh butan.
Câu23. Phân tử metan không tan trong nước vì lí do nào sau đây?
A. Phân tử metan không phân cực.
B. Metan là chất khí.
C. Phân tử khối của metan nhỏ.
D. Metan không có liên kết đôi. Câu24. Hợp chất hữu cơ X có tên gọi là: 2-clo-3-metylpentan. Công thức cấu tạo của X là
A. CH3CH2CH(Cl)CH(CH3)2
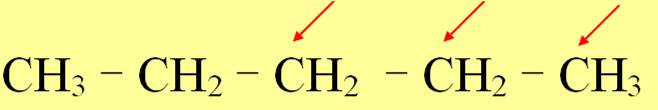
C. CH3CH(Cl)CH3CH(CH3)CH3.
Câu25. Hiđrocacbon T có công thức cấu tạo:
B. CH3CH2CH(CH3)CH2CH2Cl.
D. CH3CH(Cl)CH(CH3)CH2CH3.
Danh pháp IUPAC của T là
A. 3-etyl-2,4-đimetylpentan.
C. 2,4-đimetyl-3-etylpentan.
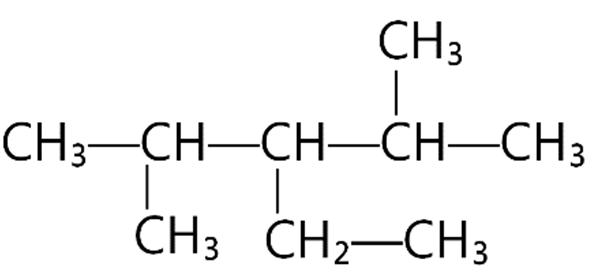
Câu26. Phát biểu nào sau đây không đúng?
B. 2-metyl-3-propylpentan.
D. 2-propyl-3-metylpentan.
A. Ở điều kiện thường, các ankan từ C1 đến C4 ở trạng thái khí, từ C5 đến khoảng C18 ở trạng thái lỏng, từ khoảng C18 trở đi ở trạng thái rắn.
B. Nhiệt độ nóng chảy, nhiệt độ sôi và khối lượng riêng của ankan nói chung đều giảm theo chiều tăng số nguyên tử cacbon trong phân tử
C. Ankan không tan trong nước nhưng tan trong dung môi không phân cực như dầu, mỡ.
D. Ankan đều là những chất không màu.
Câu27. Tính chất nào sau đây không phải của ankan?
A. Khi không chiếu sáng thì không phản ứng được với brom, do vậy không làm mất màu dung dịch brom.
B. Phản ứng với clo khi đun nóng hoặc chiếu sáng, tạo thành hỗn hợp các dẫn xuất clo.
C. Phản ứng mãnh liệt với dung dịch KMnO4 khi đun nóng, tạo thành CO2 và H2O.
D. Tan tốt trong các dung môi không phân cực như dầu mỡ, benzen, …
Câu28. Cho các chất sau: metan, etan, propan, isobutan, neopentan. Có bao nhiêu chất khi tác dụng với clo (tỉ lệ mol 1:1, chiếu sáng) chỉ thu được duy nhất một dẫn xuất monoclo?
Bao gồm: metan, etan, neopentan.
Câu29. Thực hiện chuỗi ph
Câu30. Nhỏ lần lượt hexan vào bốn ống nghiệm:
Ống nghiệm 1: chứa dung dịch KOH
Ống nghiệm 2: chứa dung dịch H2SO4 đặc
Ống nghiệm 3: chứa dung dịch KMnO4
Ống nghiệm 4: chứa benzen
Hexan có thể tan trong những ống nghiệm nào?
A. 1, 2 và 3. B. 1, 2 và 4. C. chỉ 4.
D. 3 và 4. Hướngdẫngiải
Bao gồm: 4 vì benzen là dung môi không phân cực giống hexan nên hexan có thể tan tốt trong benzen.





CĐ1:Kháiquátvề hiđrocacbonkhôngno.Anken
CĐ2:Ankađien
CĐ3:Ankin
CĐ4:Tổngônhiđrocacbonkhôngno
KIẾNTHỨCCẦNNHỚ
1.Hiđrocacbonkhôngno
- Hiđrocacbon không no là hiđrocacbon trong phân tử có chứa liên kết pi (π) gồm các liên kết C=C hoặc C≡C.
+ Anken: Hiđrocacbon không no, 1C=C, mạch hở: CnH2n (n ≥ 2).
+ Ankađien: Hiđrocacbon không no, 2C=C, mạch hở: CnH2n-2 (n ≥ 3).
+ Ankin: Hiđrocacbon không no, 1C≡C, mạch hở: CnH2n-2 (n ≥ 2).
2. Đồng đẳng, đồngphân,danhphápanken
- Công thức chung: CnH2n (n ≥ 2).
- Đồng phân: ĐP về mạch cacbon, ĐP về vị trí nối đôi, ĐP hình học.
- Danh pháp: Tên IUPAC = VT nhánh + tên nhánh + tên mạch chính (đổi an → VT nối đôi + en).
Tên thông thường = tên ankan tương ứng (đổi an → ilen)
3.Tínhchấthóahọccủaanken
(a) Phản ứng cộng
- Cộng X2: CnH2n + H2 o Ni,t → → CnH2n+2
CnH2n + Br2 → CnH2nBr2 (PƯ làm mất màu dung dịch Br2 dùng để nhận biết anken).
- Cộng HX: CnH2n + HX → CnH2n+1X.
QuitắccộngMac–côp–nhi–côp: Khi cộng HX vào liên kết đôi C=C bất đối xứng, H cộng ưu tiên vào C chứa nhiều H hơn, X cộng vào bên còn lại.
(b) Phản ứng trùng hợp: nMonome o xt,t,p → Polime
(c) Phản ứng oxi hóa hoàn toàn (cháy): CnH2n + 3n 2 O
Ngoài ra anken còn tham gia phản ứng oxi hóa không hoàn toàn, làm mất màu dung dịch KMnO4.
4. Điềuchế anken
- Tách nước từ ancol etylic: C2H5OH o 24®Æc HSO,170C
- Tách hiđro từ ankan: CnH2n+2 oxt,t
BÀITẬPTỰ LUẬN
CnH2n + H2
Câu1: Viết đồng phân và gọi tên anken từ C2 → C6.
C2H4
CH2=CH2
C4H8
C2H4 + H2O
CH2=CH-CH2-CH3
but –1 – en
CH3-CH=CH-CH3
but –2 – en
CH2=C(CH3)CH3
metylpropen
C3H6
CH2=CH2-CH3
C5H10
CH2=CH-CH2-CH2-CH3
pent –1 – en CH3-CH=CH-CH2-CH3
pent –2 – en (cis/ trans)
CH2=C(CH3)-CH2-CH3
CH2=CH-CH2-CH2-CH2-CH3
hex – 1 – en
CH3 –CH2-CH=CH-CH2-CH3
hex – 3 – en (cis/ trans)
CH2=CH-CH(CH3)-CH2-CH3
3 – metylpent – 1 – en
CH3-C(CH3)=CH-CH2-CH3
2 – metylpent – 2 – en
CH3-CH=CH-CH(CH3)-CH3
2 – metylbut – 1 – en CH2=CH-CH(CH3)-CH3
3 – metylbut – 1 – en CH3-C(CH3)=CH-CH3
2 – metylbut – 2 – en
C6H12
CH3-CH=CH-CH2-CH2-CH3
hex – 2 – en (cis/ trans)
CH2=C(CH3)-CH2-CH2-CH3
2 – metylpent – 1 – en
CH2=CH-CH2 -CH(CH3)-CH3
4 – metylpent – 1 – en
CH3-CH=C(CH3)-CH2-CH3
3 – metylpent – 2 – en (cis/ trans)
CH2=C(CH3)-CH(CH3)-CH3
2,3 – đimetylbut – 1 – en CH2=CH-C(CH3)2-CH3 CH3-C(CH3)=C(CH3)-CH3
4 – metylpent – 2 – en (cis/ trans)
3,3 – đimetylbut – 1 – en
2, 3 – đimetylbut – 2 – en CH2=C(C2H5)-CH2-CH3
2 – etylbut – 1 – en
Câu2: Viết phương trình hóa học ứng với các trường hợp sau:
(a) Cho etilen tác dụng với H2 (Ni, to)
C2H4 +H2 o Ni,t → C2H6
(b) Cho propilen phản ứng với dung dịch Br2.
C3H6 +Br2 → C3H6Br2
(c) Cho propilen phản ứng với dung dịch HCl. Gọi tên sản phẩm chính.
CH3-CH(Cl)-CH3 (spc)
CH2=CH2-CH3 +HCl 2-clopropen
CH3-CH2-CH2Cl(spp)
(d) Cho but-1-en phản ứng H2O (H+, to). Gọi tên sản phẩm chính. CH3-CH(OH)-CH2-CH3 (spc)
CH2=CH-CH2-CH3 +H2O butan-2-ol
CH2(OH)-CH2-CH2–CH3 (spp)
(e) Trùng hợp etilen.
nC2H4 o xt,t,p → -(CH2-CH2)-n
(g) Đốt cháy anken ở dạng tổng quát. Tìm mối liên hệ giữa số mol CO2, H2O.
CnH2n + 3n 2 O2 ot → nCO2 +nH2O
22 COHOn=n
(h) Cho etilen tác dụng với dung dịch KMnO4.
3CH2=CH2 +4H2O+2KMnO4 → →→ → 3CH2(OH)-CH2(OH)+2MnO2↓ +2KOH
Câu3: Bằng phương pháp hóa học hãy nhận biết các chất khí: metan, etilen, oxi, cacbon đioxit. CH4 C2H4 O2 CO2
Ca(OH)2 X X X ↓ trắng
ddBr2 X Mấtmàu X
O2,to Bùngcháy X
PTHH: (1) CO2 +Ca(OH)2 → →→ CaCO3↓ +H2O
(2) C2H4 +Br2 → C2H4Br2
(3) CH4 +2O2 ot → CO2 +2H2O
Câu4: Xác định công thức phân tử và gọi tên X trong các trường hợp sau:
(a) Anken X có tỉ khối so với hiđro bằng 21.
M=21. 2=4214n=42n=3:CH
Hướngdẫngiải n2nCH 36
(b) Cho anken X tác dụng với dung dịch HCl thu được sản phẩm có %mCl = 55,04%.
Hướngdẫngiải
CnH2n + HCl → CnH2n+1Cl
%mCl = 35,5 100% 14n+36,5 = 55,04% n = 2: C2H4
(c) Cho 8,4 gam anken X tác dụng vừa đủ với 200 ml dung dịch Br2 1M.
Hướngdẫngiải
2Br n=0,2 .1=0,2 (mol)
CnH2n + Br2 → CnH2nBr2 0,2 ←0,2 n2nCH 36 8,4 M== 4214n= 42n= 3:CH 0,2
(d) Cho 2,24 gam một anken X tác dụng với dung dịch Br2 dư, thu được 8,64 gam sản phẩm cộng.
Hướngdẫngiải
2Br 8,64-2,24 n== 0,04 160(mol)
CnH2n + Br2 → CnH2nBr2 0,2 ←0,2
M== 5614n= 56n= 4CH 0,04
n2nCH 48 2,24
(g) Cho 7 gam hỗn hợp X gồm 2 hiđrocacbon kế tiếp trong dãy đồng đẳng của etilen tác dụng vừa
đủ với dung dịch Y chứa 32 gam brom.
2Br 32 n==0,2160(mol)
CnH2n + Br2 → CnH2nBr2 0,2 ←0,2
Hướngdẫngiải
7CH
M==3514n=35n=2,5 0,2CH
24 CH 36
n2n
(e) Đốt cháy hoàn toàn 3,36 lít một anken X (ở đktc) sau phản ứng thu được 13,2 gam CO2.
Hướngdẫngiải
nX = X 3,36 n==0,15(mol) 22,4 ; 2CO 13,2 n==0,344(mol)
CnH2n + 3n 2 O2 ot → nCO2 + nH2O
Số nguyên tử C: 2 n2n
n0,3 n===2:CH n0,15
CO 24 CH
BÀITẬPTRẮCNGHIỆM
1.Mức độ nhậnbiết(rấtdễ vàdễ)
Câu1. Anken là những hiđrocacbon có đặc điểm là
A. không no, mạch hở, có một liên kết ba C≡C.
B. không no, mạch vòng, có một liên kết đôi C=C.
C. không no, mạch hở, có một liên kết đôi C=C.
D. no, mạch vòng.
Câu2. Anken là các hiđrocacbon không no, mạch hở, có công thức chung là
A. CnH2n+2 (n ≥ 1).
C. CnH2n (n ≥ 3).
B. CnH2n (n ≥ 2).
D. CnH2n-2 (n ≥ 2).
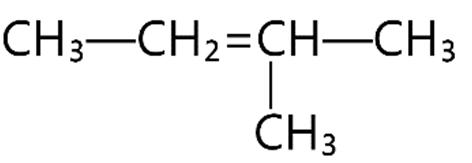
Câu3. Các hiđrocacbon C2H4, C3H6, C4H8, … có công thức chung là CnH2n và hợp thành dãy đồng
đẳng của
A. metan. B. etilen. C. axetilen. D. xiclopropan.
Câu4. Trong anken, mạch chính là
A. mạch dài nhất và có nhiều nhánh nhất.
B. mạch có chứa liên kết đôi và nhiều nhánh nhất.
C. mạch có chứa liên kết đôi, nhiều nhánh nhất và phân nhánh sớm nhất.
D. mạch có chứa liên kết đôi, dài nhất và nhiều nhánh nhất.
Câu5. Anken CH3 CH=CH CH3 có tên là
A. 2-metylprop-2-en. B. but-2-en.
Câu6. Anken sau có tên gọi là
C. but-1-en. D. but-3-en.
A. 2-metylbut-2-en.
C. 2-metybut-3-en.
B. 3-metylbut-2-en.
D. 3-metylbut-3-en.
Câu7.(A.14): Chất X có công thức cấu tạo: CH3-CH(CH3)-CH=CH2. Tên thay thế của X là
A. 3-metylbut-1-in.
C. 2-metylbut-3-en.
B. 3-metylbut-1-en.
D. 2-metylbut-3-in.
Câu8. Anken X có công thức cấu tạo: CH3–CH2–C(CH3)=CH–CH3. Tên gọi của X theo danh pháp
IUPAC là
A. isohexan.
C. 3-metylpent-2-en.
B. 3-metylpent-3-en.
D. 2-etylbut-2-en.
Câu9. Chất X có công thức: 332 CHCH(CH)CHCH −−= . Tên gọi của X theo danh pháp IUPAC là
A. 2-metylbut-3-in.
C. 3-metylbut-1-in.
Câu10. Nhóm CH2=CH– có tên là
A. etyl. B. vinyl.
Câu11. Nhóm CH2=CH-CH2- có tên là
B. 2-metylbut-3-en.
D. 3-metylbut-1-en.
C. anlyl. D. phenyl.
A. etyl. B. vinyl.
Câu12. Danh pháp IUPAC của α-butilen là
A. but-1-en.
C. 2-metylbut-1-en.
C. anlyl. D. phenyl.
B. but-2-en.
D. 2-metylpropen.
Câu13. Khi có mặt chất xúc tác Ni ở nhiệt độ thích hợp, anken cộng hiđro vào liên kết đôi tạo
thành hợp chất nào dưới đây?
A. ankan.
C. ankin.
B. xicloankan.
D. anken lớn hơn.
Câu14. Phản ứng hiđro hóa anken thuộc loại phản ứng nào dưới đây?
A. phản ứng thế.
C. phản ứng cộng.
B. phản ứng tách.
D. phản ứng phân hủy.
Câu15. Anken không phản ứng được với chất nào dưới đây?
A. Br2. B. Cl2.
C. NaCl.
Câu16. Chất nào sau đây không thể cộng hợp vào anken?
A. HCl. B. NaOH.
Câu17. Anken có thể cộng hợp nước khi có xúc tác là
D. H2.
C. H2O.
D. H2SO4.
A. bazơ. B. MnO2. C. axit. D. KMnO4.
Câu18. Phản ứng đặc trưng của anken là
A. Phản ứng tách. B. Phản ứng thế.
C. Phản ứng cộng. D. Phản ứng oxi hóa.
Câu19. Sản phẩm tạo thành khi cho propen tác dụng với H2 (Ni, to) là
A. propyl. B. propan. C. pentan. D. butan.
Câu20. Chất nào sau đây có khả năng làm mất màu dung dịch brom?
A. etan. B. propan. C. butan. D. etilen.
Câu21.(QG.18-202): Ở điều kiện thường, chất nào sau đây làm mất màu dung dịch Br2?
A. benzen. B. etilen. C. metan. D. butan.
Câu22.[QG.20-201] Ở điều kiện thường, chất nào sau đây làm mất màu dung dịch Br2?
A. Butan. B. Metan. C. Etilen. D. Propan.
Câu23.[QG.20-202] Ở điều kiện thường, chất nào sau đây làm mất màu dung dịch Br2?
A. Metan. B. Butan. C. Propen. D. Etan.
Câu24.[QG.20-203] Ở điều kiện thường, chất nào sau đây làm mất màu dung dịch Br2?
A. Etilen. B. Propan. C. Metan. D. Etan.
Câu25.[QG.20-204] Ở điều kiện thường, chất nào sau đây làm mất màu dung dịch Br2?
A. Propen. B. Etan. C. Metan. D. Propan.
Câu26. Trùng hợp etilen, sản phẩm thu được có cấu tạo là
A. ( 22n CHCH) = . B. ( 22n CHCH) .
C. ( nCHCH) = D. ( 33n CHCH)
Câu27. Đốt cháy hiđrocacbon Y thu được sản phẩm có 22 COHOnn = thì Y là
A. ankan. B. xicloankan.
C. anken. D. xicloankan hoặc anken.
Câu28. Đốt cháy hiđrocacbon mạch hở Z thu được sản phẩm có 22 COHOnn = thì Z là
A. ankan. B. xicloankan.
C. anken. D. xicloankan hoặc anken.
Câu29. Oxi hoá etilen bằng dung dịch KMnO4 thu được sản phẩm là:
A. MnO2, C2H4(OH)2, KOH.
B. C2H5OH, MnO2, KOH.
Câu30. Phương pháp điều chế etilen trong phòng thí nghiệm là
A. Đun C2H5OH với H2SO4 đặc ở 170oC.
B. Crackinh ankan.
C. Tách H2 từ etan.
D. Cho C2H2 tác dụng với H2 (xt: Pd/PbCO3).
Câu31.[MH2-2020] Cho 2 ml ancol etylic vào ống nghiệm đã có sẵn vài viên đá bọt. Thêm từ từ 4 ml dung dịch H2SO4 đặc vào ống nghiệm, đồng thời lắc đều rồi đun nóng hỗn hợp. Hiđrocacbon sinh ra trong ống nghiệm trên là
A. etilen. B. axetilen. C. propilen. D. metan.
Câu32. Trong công nghiệp, các anken đơn giản như etilen, propilen, butilen được điều chế bằng phương pháp nào dưới đây?
A. đun ancol với axit sunfuric đậm đặc.
B. tách từ khí thiên nhiên.
C. tách hiđro hoặc cracking ankan.
D. oxi hóa các ankan tương ứng bằng oxi dư.
Câu33.(QG.16): Trước những năm 50 của thế kỷ XX, công nghiệp tổng hợp hữu cơ dựa trên nguyên liệu chính là axetilen. Ngày nay, nhờ sự phát triển vượt bậc của công nghệ khai thác và chế biến dầu mỏ, etilen trở thành nguyên liệu rẻ tiền, tiện lợi hơn nhiều so với axetilen. Công thức phân tử của etilen là A.
2.Mức độ thônghiểu(trungbình)
Câu34. Số lượng đồng phân cấu tạo mạch hở ứng với công thức phân tử C4H8 là
A. 2. B. 3. C. 4. D. 5.
Câu35. Số lượng đồng phân cấu tạo mạch hở ứng với công thức phân tử C5H10 là
A. 2. B. 3. C. 4. D. 5.
Câu36.(B.14): Trong phân tử propen có số liên kết xich ma (σ) là
A. 7. B. 9. C. 8. D. 6.
Câu37. Chất nào sau đây có đồng phân hình học?
A. 33 CHCCCH. −≡− B. 33 CHCHCHCH. −=−
C. 22 CHClCHCl.
D. 23 CHCClCH. =−
Câu38. Hợp chất hữu cơ nào sau đây không có đồng phân cis-trans?
A. CHCl=CHCl.
C. CH3CH=CHCH3
B. CH3CH2CH=C(CH3)CH3.
D. CH3CH2CH=CHCH3
Câu39.(C.11): Chất nào sau đây có đồng phân hình học?
A. CH2=CH-CH=CH2
C. CH3-CH=CH-CH=CH2
B. CH3-CH=C(CH3)2
D. CH2=CH-CH2-CH3
Câu40. (C.10): Chất nào sau đây có đồng phân hình học?
A. 2-clopropen. B. But-2-en.
C. 1,2-đicloetan. D. But-1-en.
Câu41. Số lượng đồng phân mạch hở ứng với công thức phân tử C4H8 là
A. 2. B. 3. C. 4. D. 5.
Câu42. Trong số các anken có đồng phân cấu tạo C5H10, có bao nhiêu chất có đồng phân hình học?
A. 1. B. 2. C. 3. D. 4.
Câu43.(B.08): Ba hiđrocacbon X, Y, Z là đồng đẳng kế tiếp, khối lượng phân tử của Z bằng 2 lần khối lượng phân tử của X. Các chất X, Y, Z thuộc dãy đồng đẳng nào dưới đây?
A. ankan. B. ankađien. C. anken. D. ankin.
Tên gọi của anken trên là
A. cis-but-2-en.
B. trans-but-2-en. C. but-2-en. D. cis-pent-2-en.
Câu44. Cho anken có công thức:
Tên gọi của anken trên là
A. trans-pent-2-en.
C. cis-pent-2-en.
Câu45. Phát biểu nào sau đây là đúng?
A. Anken là chất kị nước.
C. Liên kết đôi kém bền hơn liên kết đơn.
B. cis-pent-3-en.
D. trans-pent-3-en.
B. Anken là chất dễ tan trong dầu mỡ
D. Liên kết π kém bền hơn liên kết σ
Câu46. Sản phẩm tạo thành từ phản ứng: 2-metylpropen + H2 o Ni,t → là
A. isobutan.
B. butan.
C. xiclobutan. D. 2-metylbutan.
Câu47. Sản phẩm tạo thành từ phản ứng: 2-metylbut-2-en + H2 o Ni,t → là
A. trans-2-metylbut-2-en. B. 2-metylbutan.
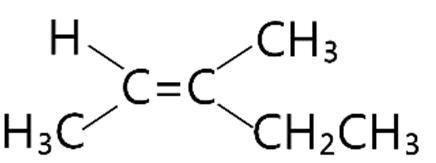
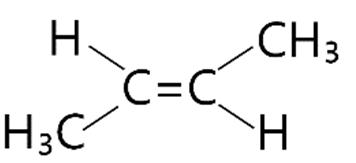
C. 2,2-đimetylpropan. D. butan.
Câu48.(B.13): Hiđrocacbon nào sau đây khi phản ứng với dung dịch brom thu được 1,2đibrombutan?
A. But-1-en. B. Butan. C. Buta-1,3-đien. D. But-1-in.
Câu49. Khi dẫn etilen vào dung dịch nước brom thì dung dịch bị nhạt màu, nguyên nhân là do
A. Etilen có phản ứng cộng brom tạo ra 1,2-đibrometan.
B. Etilen có phản ứng thế brom tạo ra 1,2-đibrometan.
C. Etilen đẩy brom ra khỏi dung dịch.
D. Etilen có phản ứng tách với brom tạo ra 1,2-đibrometan.
Câu50. Cho hai bình hóa chất mất nhãn chứa etilen và etan. Có thể nhận biết các hóa chất trong
mỗi bình bằng chất nào?
A. dung dịch NaCl.
C. dung dịch nước brom.
B. quỳ tím.
D. dung dịch Na2SO4.
Câu51. Sản phẩm tạo thành từ phản ứng giữa 2-metylpropen và Br2 là
A. CH2Br CHBr(CH3)2.
C. CH3 CH(CH
CHBr
B. CH2Br CH(CH3) CH2Br.
D. CH
CH
CH
Câu52. Dẫn xuất halogen X dưới đây:
Có thể tạo thành từ phản ứng giữa brom với chất nào dưới đây?
A. but-2-en. B. xiclopropan.
C. but-1-en. D. 2-metylpropen.
Câu53. Anken nào sau đây có tính đối xứng qua liên kết đôi?
A. CH3 CH=CH2
C. CH2=CH2
B. CH3 CH=C(CH3)2
D. CH2=C(CH3)2
Câu54. Anken nào sau đây không có tính đối xứng qua liên kết đôi?
A. (CH3)2C=C(CH3)2.
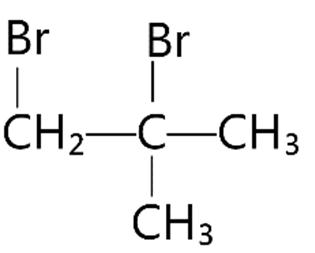
B. CH3 CH=CH CH3.
C. (CH3)2C=CH2.
Câu55. Etilen cộng hợp HBr có thể tạo ra tối đa bao nhiêu sản phẩm hữu cơ?
A. 0. B. 1.
C. 2.
Câu56. Propen cộng hợp HBr có thể tạo ra tối đa bao nhiêu sản phẩm hữu cơ?
A. 0. B. 1.
C. 2.
D. CH2=CH2.
D. 3.
D. 3.
Câu57. Anken A có công thức phân tử C4H8. Khi cộng nước vào A (có xúc tác axit) chỉ tạo ra một sản phẩm duy nhất. Tên gọi của A là
A. xiclopropan.
C. but-2-en.
B. but-1-en.
D. 2-metylpropen.
Câu58. Theo quy tắc Mac-côp-nhi-côp, trong phản ứng cộng nước hoặc axit (kí hiệu chung là HA) vào liên kết C=C của anken thì H sẽ ưu tiên cộng vào nguyên tử cacbon có đặc điểm nào?
A. nguyên tử cacbon liên kết với nhóm metyl.
B. nguyên tử cacbon liên kết với nhiều nguyên tử hiđro hơn.
C. nguyên tử cacbon liên kết với ít nguyên tử hiđro hơn.
D. nguyên tử cacbon liên kết với nhiều nguyên tử cacbon khác hơn.
Câu59. Sản phẩm chính của phản ứng cộng hợp nước vào 2-metylpropen là
A. CH3 CH(OH) CH3.
C. HO CH2CH2CH3.
B. CH3CH2CH2 OH.
D. CH3 O CH2CH3.
Câu60. Anken X có công thức phân tử C5H10. X có đồng phân hình học, khi tác dụng với H2 tạo ra ankan mạch thẳng. Sản phẩm chính tạo ra từ phản ứng cộng HBr vào X là
A. CH3 CHBr CH2CH2CH3
C. CH3CH2 CHBr CH2CH3.
B. CH2Br CH2CH2CH2CH3
D. CH2Br CH2CH(CH3)2.
Câu61. Anken X có công thức phân tử C6H12. X không có đồng phân hình học, khi tác dụng với H2 tạo ra ankan mạch thẳng. Sản phẩm chính tạo ra từ phản ứng giữa X với H2O (xúc tác H+) là
A. CH2OH CH2CH2CH2CH2CH3.
C. CH3 CHOH CH(CH3)3
B. CH3 CHOH CH2CH(CH3)2.
D. CH3 CHOH CH2CH2CH2CH3
Câu62.(A.07): Hiđrat hóa 2 anken chỉ tạo thành 2 ancol. Hai anken đó là
A. eten và but-2-en.
C. propen và but-2-en.
Câu63. Cho phản ứng: 224 (lo·ng) CHCH +KMnO =→
B. 2-metylpropen và but-1-en.
D. eten và but-1-en.
Sản phẩm hữu cơ của phản ứng trên là
A. CH3CHO. B. (CH2OH)2 C. CH≡CH. D. C2H6
Câu64. Cho 2 ống nghiệm đều chứng dung dịch KMnO4 loãng. Nhỏ vào ống thứ nhất vài giọt hexan, nhỏ vào ống thứ hai vài giọt hexen thì quan sát thấy hiện tượng:
A. Dung dịch KMnO4 trong hai ống đều nhạt màu.
B. Dung dịch KMnO4 trong ống thứ nhất nhạt màu, ống thứ hai không đổi màu.
C. Dung dịch KMnO4 trong ống thứ hai nhạt màu, ống thứ nhất không đổi màu.
D. Dung dịch KMnO4 trong hai ống đều không đổi màu.
Câu65. Hóa chất nào sau đây có thể dùng để phân biệt propan và propen: brom (1); KMnO4 (2); nước (3); dầu mỡ (4)?
A. Chỉ 1. B. Chỉ 2. C. 3 và 4. D. 1 và 2.
Câu66. Trong phòng thí nghiệm, khi điều chế C2H4 từ C2H5OH và dung dịch H2SO4 đặc ở 170oC, khí sinh ra có lẫn SO2 và CO2. Dùng dung dịch nào sau đây có để loại bỏ tạp chất, thu C2H4 tinh khiết?
A. dd KMnO4. B. dd NaOH. C. dd Na2CO3. D. dd Br2.
Câu67.(B.09): Cho hiđrocacbon X phản ứng với brom (trong dung dịch) theo tỉ lệ mol 1: 1, thu
được chất hữu cơ Y (chứa 74,08% Br về khối lượng). Khi X phản ứng với HBr thì thu được hai sản phẩm hữu cơ khác nhau. Tên gọi của X là
A. but-1-en. B. xiclopropan. C. but-2-en. D. propilen.
Câu68.(A.07): Một hiđrocacbon X cộng hợp với axit HCl theo tỉ lệ mol 1:1 tạo sản phẩm có thành phần khối lượng clo là 45,223%. Công thức phân tử của X là
A. C3H6. B. C3H4. C. C2H4. D. C4H8.
Câu69.(B.14): Đốt cháy hoàn toàn 0,2 mol hỗn hợp X gồm một ankan và một anken, thu được 0,35 mol CO2 và 0,4 mol H2O. Phần trăm số mol của anken trong X là
A. 40%. B. 75%.
C. 25%.
D. 50%.
Câu70.(C.09): Để khử hoàn toàn 200 ml dung dịch KMnO4 0,2M tạo thành chất rắn màu nâu đen cần V lít khí C2H4 (ở đktc). Giá trị tối thiểu của V là A. 2,240.
3.Mức độ vậndụng(khá)
Câu71. Cho các anken: CH2=CH CH3 (X); CH3 CH=CH CH3 (Y); (CH3)2C=CH2 (Z). Anken nào có đồng phân hình học?
A. X và Y.
B. X và Z.
C. Chỉ Y.
D. Chỉ Z.
Câu72. Cho các anken: CH3 CH=CH C2H5 (X); CH3 CH=CH CH3 (Y); CH2=CH C2H5 (Z); CH3 CH=C(CH3)2 (T). Anken nào có đồng phân hình học?
A. X, Y và Z. B. X và Y. C. Y, Z và T. D. T và Z.
Câu73. Cho các anken sau: CH3 CH=CH CH3 (X); CH3 CH=CH2 (Y); CH2=CH2 (Z); CH2=C(CH3)2 (T); (CH3)2C=C(CH3)2 (U). Những anken nào khi cộng hợp với HBr chỉ tạo ra một sản phẩm hữu cơ?
A. X, Z, T. B. Y, T, U. C. X, Z, U. D. Y, Z, T.
Câu74. Cho các anken sau: CH3 CH=CH2 (X); CH2=CH CH2CH3 (Y); CH2=CH2 (Z); (CH3)2C=CH2 (T); (CH3)2C=C(CH3)2 (U). Những anken nào khi cộng hợp với HBr tạo ra hai sản phẩm hữu cơ?
A. X, Y, T.
Câu75. Cho các anken sau: but-2-en (X); 2-metylpropen (Y); 2-metylbut-1-en (Z); 2-metylbut-2en (T); 2,3-đimetylbut-2-en (U). Những anken nào khi cộng hợp với HBr tạo ra hai sản phẩm hữu cơ?
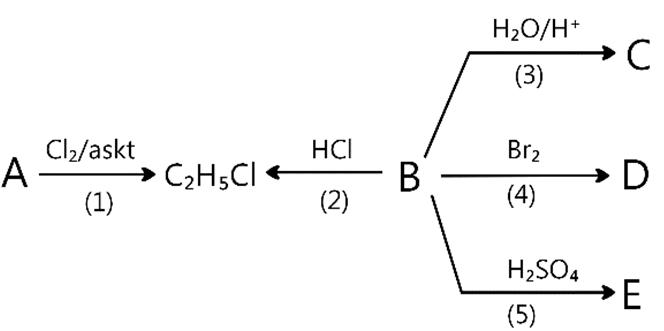
A. X, Y, U. B. Y, Z, T. C. X, Z, T. D. Y, Z, U. Câu76. Cho các anken: cis-3-metylbut-2-en (X); 2-metylbut-2-en (Y); pent-1-en (Z); 2-metylbut1-en (T). Những anken nào khi tác dụng với H2, xúc tác Ni/to đều tạo thành 2-metylbutan?
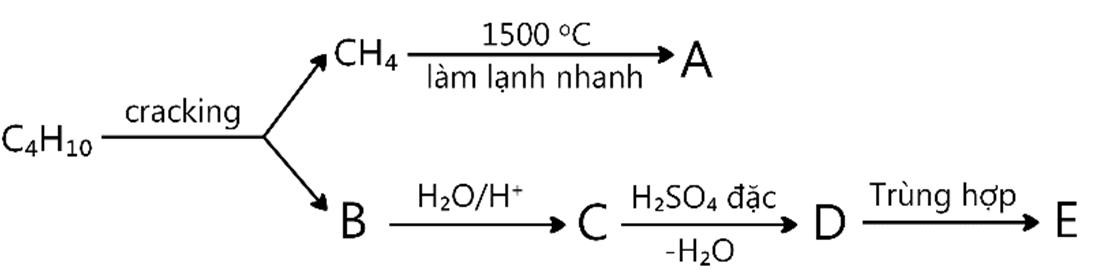
A. X, Y, Z. B. Z, T. C. X, Y, T. D. Chỉ T. Câu77. Có bốn đồng phân anken A
đồng phân hình học). Trong đó A1, A
và A
(tính cả
tác dụng với hiđro tạo ra sản phẩm giống nhau. A1 và
A2 tác dụng với brom cho sản phẩm giống nhau. A3 và A4 lần lượt là:
A. cis-but-2-en và trans-but-2-en.
C. 2-metylpropen và but-1-en.
Sử dụng dữ kiện sau để trả lời các câu hỏi 78, 79
Cho chuỗi phản ứng sau:
Câu78. Các chất A, C, B lần lượt là:
A.
OH.
C. C2H4, C2H6, C2H5OH.
Câu79. Chất E là
B. trans-but-2-en và cis-but-2-en.
D. but-1-en và 2-metylpropen.
A. CH2=CH2 B. CH3CH2 OSO3H.
C. CH3CH2Cl.
D. CH3CH2 SO3H.
Câu80. Các chất A và E trong chuỗi phản ứng sau lần lượt là:
A. C2H2 và polietilen.
C. HCHO và polietilen.
B. HCHO và polipropilen.
D. C2H2 và polipropilen.
Câu81.(A.12): Hỗn hợp X gồm H2 và C2H4 có tỉ khối so với H2 là 7,5. Dẫn X qua Ni nung nóng, thu được hỗn hợp Y có tỉ khối so với H2 là 12,5. Hiệu suất của phản ứng hiđro hoá là
C. 60%.
KIẾNTHỨCCẦNNHỚ
1. Đồng đẳng, đồngphân,danhpháp
- Công thức chung: CnH2n-2 (n ≥ 3).
- Đồng phân: ĐP về mạch cacbon, ĐP về vị trí nối đôi, ĐP hình học.
- Danh pháp: Tên IUPAC = VT nhánh + tên nhánh + tên mạch chính (đổi n trong an → VT 2 nối đôi + đien).
- Phân loại: + Ankađien liên hợp: 2 liên kết đôi cách nhau 1 liên kết đơn. + Ankađien không liên hợp: 2 liên kết đôi xa nhau. + Ankađien có liên kết đôi cạnh nhau.
2.Tínhchấthóahọc
(a) Phản ứng cộng
- Cộng X2: CnH2n-2 + 2H2 o Ni,t → CnH2n+2. CnH2n-2 + 2Br2dư → CnH2n-2Br4 (PƯ làm mất màu dung dịch Br2 ⇒ nhận biết ankađien).
- Cộng HX: CnH2n-2 + 2HX → CnH2nX2
Quitắccộngvàoankađien: Khi cộng HX hoặc X2 vào ankađien (tỉ lệ 1 : 1) thì ở nhiệt độ thấp ưu tiên cộng 1, 2; ở nhiệt độ cao thì ưu tiên cộng 1, 4.
(b) Phản ứng trùng hợp: CH2=CH-CH=CH2 o xt,t,P → –(–CH2-CH=CH-CH2–)n–butađien polibutađien hay cao su buna
(c) Phản ứng đốt cháy: CnH2n-2 + 3n1 2 O2 ot → nCO2 + (n-1)H2O
Ngoài ra ankađien còn tham gia phản ứng oxi hóa không hoàn toàn, làm mất màu dd KMnO4.
3. Điềuchế
- Tách nước từ ancol etylic: 2C2H5OH → 23 o AlO,ZnO 450C C4H6 + H2 + 2H2O
- Tách hiđro từ ankan: CnH2n+2 oxt,t → CnH2n-2 + 2H2
BÀITẬPTỰ LUẬN
Câu1: Viết các đồng phân cấu tạo và gọi tên các ankađien có công thức C3H4, C4H6, C5H8. Trường hợp nào có đồng phân hình học?
C3H4
CH2=C=CH2
Propađien
CH2=C=CH-CH2-CH3
penta – 1, 2 – đien
CH3-CH=C=CH-CH3
penta – 2,3 – đien
CH2=C=CH(CH3)-CH3
C4H6
CH2=C=CH-CH3 :buta-1,2-đien
CH2=CH–CH=CH2 :buta-1,3-đien
C5H8
CH2=CH-CH=CH-CH3
penta – 1, 3 – đien (cis/trans)
CH2=CH-CH2-CH=CH2
penta – 1,4 – đien
CH2=C(CH3)–CH=CH2
3 – metylbuta – 1,2 – đien 2 – metylbuta – 1,3 – đien
Câu2: Viết phương trình hóa học xảy ra khi
(a) butađien và isopren tác dụng với H2 dư (Ni, to).
CH2=C=CH-CH3 +2H2 o t,Ni → CH3-CH2-CH2-CH3
CH2=C(CH3)–CH=CH2 +2H2 o t,Ni → CH3-CH(CH3)-CH2-CH3
(b) isopren tác dụng với brom (tỉ lệ 1 : 1). Viết tất cả các sản phẩm thu được.
CH2=C(CH3)–CH=CH2 +Br2
(c) trùng hợp butađien; isopren.
CH3-CH(CH3)–CH=CH2
CH2=C(CH3)–CH2-CH3
CH2=CH-CH=CH2 o xt,t,P →–(–CH2-CH=CH-CH2–)n–
CH2=C(CH3)–CH=CH2 o xt,t,P →–(–CH2-C(CH3)=CH-CH2–)n–
(d) tách H2 từ butan và isobutan để thu được ankađien liên hợp tương ứng.
CH3-CH2-CH2-CH3 oxt,t → CH2=CH–CH=CH2 +2H2
CH3-CH(CH3)-CH2-CH3 oxt,t → CH2=C(CH3)–CH=CH2 +2H2
Câu3: Xác định công thức phân tử và gọi tên X trong các trường hợp sau:
(a) Ankađien X có tỉ khối so với hiđro bằng 27.
M= 27 . 2 = 5414n - 2 = 54n = 4:CH
Hướngdẫngiải n2n-2CH 46
(b) Ankađien X có %mC = 88,24%.
Hướngdẫngiải
CTPT: CnH2n-2: C 58 12n %m=.100%=88,24%n=5:CH 14n-2
(d) Cho 8 gam ankađien X tác dụng với lượng dư dung dịch brom thì thấy có 0,4 mol Br2 phản ứng.
Hướngdẫngiải
CnH2n-2 + 2Br2dư → CnH2n-2Br4
0,2 ←0,4
8
M== 40=14n-2n=3:CH 0,2
n2n-2CH 34
BÀITẬPTRẮCNGHIỆM
1.Mức độ nhậnbiết(rấtdễ vàdễ)
Câu1. Hiđrocacbon mà trong phân tử có hai liên kết đôi C=C được gọi là
A. ankan. B. anken.
Câu2. Ankađien liên hợp là các đien có đặc điểm là
A. hai liên kết đôi liền nhau.
B. hai liên kết đôi cách nhau một liên kết đơn.
C. hai liên kết đơn cách nhau một liên kết đôi.
C. ankađien.
D. xicloankan.
D. hai liên kết đôi cách nhau nhiều hơn một liên kết đơn.
Câu3. Hiđrocacbon nào sau đây thuộc loại ankađien liên hợp?
A. CH2=C=CH2.
C. CH2=CH CH=CH2.
Câu4. Công thức cấu tạo thu gọn của buta-1,3-đien là
A. CH2=C=CH CH3.
C. CH2=CH CH2 CH=CH2.
Câu5. Công thức cấu tạo thu gọn của isopren là
A. CH3 CH=C=CH CH3
C. CH2=CH CH2 CH=CH2.
B. CH3 CH=CH CH3.
D. CH2=CH CH2 CH=CH2.
B. CH2=CH CH=CH2.
D. CH3 CH=CH CH3.
B. CH2=C(CH3) CH=CH2
D. CH2=CH CH=CH CH3.
Câu6. Ankađien có thể cộng hợp với hiđro theo tỉ lệ mol 1:1 tạo ra chất nào dưới đây?
A. ankan. B. anken.
C. xicloankan. D. ankin.
Câu7. Ankađien có thể cộng hợp với hiđro theo tỉ lệ mol 1:2 tạo ra chất nào dưới đây?
A. ankan. B. anken. C. xicloankan. D. ankin.
Câu8. Hiđro hóa hoàn toàn isopren thu được chất nào dưới đây?
A. 2-metylbut-1-en. B. 3-metylbut-1-en. C. 2-metylbutan. D. pentan.
Câu9. Trùng hợp CH2=CH CH=CH2, thu được chất nào dưới đây?
A. poliisopren. B. poli(vinyl clorua).
C. polibutađien. D. polietilen.
Câu10.(B.14): Trùng hợp hiđrocacbon nào sau đây tạo ra polime dung để sản xuất cao su buna?
A. 2-metylbuta-1,3-đien.
C. But-2-en.
B. Penta-1,3-đien.
D. Buta-1,3-đien.
Câu11. Buta-1,3-đien không phản ứng với chất nào sau đây?
A. Br2. B. H2/Ni, to .
C. HBr. D. NaOH.
Câu12. Trong công nghiệp, buta-1,3-đien và isopren được điều chế bằng phương pháp nào dưới đây?
A. đốt cháy ankan.
C. phân hủy polibutađien và poliisopren.
2.Mức độ thônghiểu(trungbình)
Câu13. C4H6 có bao nhiêu đồng phân ankađien?
A. 2. B. 3.
B. tách hiđro từ ankan tương ứng.
C. cộng hiđro vào anken tương ứng.
C. 4.
Câu14. Số đồng phân cấu tạo là ankađien ứng với công thức C5H8 là
A. 6. B. 3.
C. 4.
Câu15. Số đồng phân cấu tạo là ankađien liên hợp ứng với công thức C5H8 là
A. 2. B. 3.
C. 4.
Câu16.(C.11): Chất nào sau đây có đồng phân hình học?
A. CH2=CH-CH=CH2 B. CH3-CH=CH-CH=CH2
C. CH3-CH=C(CH3)2 D. CH2=CH-CH2-CH3
D. 5.
D. 5.
D. 5.
Câu17.(A.08): Cho các chất sau: CH2=CH-CH2-CH2-CH=CH2, CH2=CH-CH=CH-CH2-CH3, CH3-C(CH3)=CH-CH3, CH2=CH-CH2-CH=CH2. Số chất có đồng phân hình học là
A. 4. B. 1. C. 2. D. 3.
Câu18. (C.09): Cho các chất: CH2=CH–CH=CH2; CH3–CH2–CH=C(CH3)2; CH3–CH=CH–CH=CH2; CH3 – CH =CH2; CH3–CH=CH–COOH. Số chất có đồng phân hình học là
A. 1.
B. 3.
C. 4
D. 2.
Câu19. Công thức phân tử của buta-1,3-đien (đivinyl) và isopren (2-metylbuta-1,3-đien) lần lượt là:
A. C4H6 và C5H10.
C. C4H6 và C5H8.
B. C4H4 và C5H8.
D. C4H8 và C5H10.
Câu20.(B.07): Dãy gồm các chất được dùng để tổng hợp cao su Buna-S là:
A. CH2=C(CH3)-CH=CH2, C6H5CH=CH2.
C. CH2=CH-CH=CH2, CH3-CH=CH2
B. CH2=CH-CH=CH2, C6H5CH=CH2.
D. CH2=CH-CH=CH2, lưu huỳnh.
Câu21. Sản phẩm chính tạo thành từ phản ứng cộng brom vào buta-1,3-đien (tỉ lệ mol 1:1) ở nhiệt
độ thấp (khoảng 80 oC) là
A. CH2Br CH=CH CH2Br.
C. CHBr2 CH2 CH=CH2.
B. CH2Br CHBr CH=CH2.
D. CH3 CBr2 CH=CH2.
Câu22. Sản phẩm chính tạo thành khi cộng brom vào ankađien liên hợp (tỉ lệ mol 1:1) ở nhiệt độ thấp là
A. sản phẩm cộng 1,4.
B. sản phẩm cộng 2,3.
C. sản phẩm cộng 3,4.
D. sản phẩm cộng 1,2.
Câu23. Sản phẩm chính tạo thành phản ứng cộng brom vào buta-1,3-đien (tỉ lệ mol 1:1) ở nhiệt độ cao (khoảng 40 oC) là
A. CH2Br CH=CH CH2Br.
C. CHBr2 CH2 CH=CH2
B. CH2Br CHBr CH=CH2.
D. CH3 CBr2 CH=CH2
Câu24. Sản phẩm chính tạo thành khi cộng brom vào ankađien liên hợp (tỉ lệ mol 1:1) ở nhiệt độ cao là
A. sản phẩm cộng 1,4.
C. sản phẩm cộng 3,4.
B. sản phẩm cộng 2,3.
D. sản phẩm cộng 1,2.
Câu25.(A.11): Cho buta-1,3-đien phản ứng cộng với Br2 theo tỉ lệ mol 1:1. Số dẫn xuất đibrom (đồng phân cấu tạo và đồng phân hình học) thu được là
KIẾNTHỨCCẦNNHỚ
1. Đồng đẳng, đồngphân,danhpháp
- Công thức chung: CnH2n-2 (n ≥ 2).
- Đồng phân: ĐP về mạch cacbon, ĐP về vị trí nối ba.
- Danh pháp: Tên IUPAC = VT nhánh + tên nhánh + tên mạch chính (đổi an → VT nối ba + in).
Tên thông thường = tên R + tên R’ + axetilen (R-C≡C-R’).
2.Tínhchấthóahọc
(a) Phản ứng cộng
- Cộng X2: CnH2n-2 + 2H2 dư oNi,t
CnH2n+2.
CnH2n-2 + H2 dư o 3 Pd/PbCO,t → CnH2n
CnH2n-2 + 2Br2 → CnH2n-2Br4 (PƯ làm mất màu dung dịch Br2 dùng để nhận biết ankin).
- Cộng HX: CnH2n-2 + 2HX → CnH2nX2.
THĐB: CH≡CH + H2O 2oHg,H,t ++ → [CH2=CH-OH] → CH3CHO
(b) Phản ứng đime hóa, trime hóa
- PƯ đime hóa (nhị hợp): 2C2H2 oxt,t → C4H4 (CH≡C-CH=CH2)
- PƯ trime hóa (tam hợp): 3C2H2 o C,600C → C6H6 (benzen)
(c) Phản ứng thế với AgNO3/NH3 của ank – 1 – in.
RC≡CH + AgNO3 + NH3 ot → RC≡CAg↓ + NH4NO3
THĐB: CH≡CH + 2AgNO3 + 2NH3 ot → CAg≡CAg↓+ 2NH4NO3
PƯ tạo kết tủa vàng dùng để nhận biết ank – 1 – in.
(d) Phản ứng oxi hóa hoàn toàn (cháy): CnH2n-2 + 3n1 2 O2 ot → nCO2 + (n-1)H2O
Ngoài ra ankin còn tham gia phản ứng oxi hóa không hoàn toàn, làm mất màu dung dịch KMnO4
3. Điềuchế
- Thủy phân canxi cacbua: CaC2 + 2H2O → C2H2 + Ca(OH)2.
- Nhiệt phân metan: 2CH4 o 1500C lln → C2H2 + 3H2
BÀITẬPTỰ LUẬN
Câu1: Viết đồng phân và gọi tên ankin từ C2 → C5.
CH≡CH:etin
C2H2
C4H6
CH≡C-CH2-CH3:but-1-in
CH3-C≡C-CH3:but-2-in
CH≡C-CH3:propin
C3H4
C5H8
CH≡C-CH2-CH2-CH3:pent-1-in
CH3-C≡C-CH2-CH3 :pent-2-in
CH≡C-CH(CH3)-CH3:3-metylbut-1-in
Câu2: Viết phương trình hóa học ứng với các trường hợp sau:
(a) Cho axetilen tác dụng với H2 dư (Ni, to)
C2H2 +2H2 dư oNi,t → C2H6
(b) Cho axetilen tác dụng với H2 (Pd/PbCO3, to)
C2H2 +H2 o 3 Pd/PbCO,t → C2H4
(c) Cho metyl axetilen phản ứng với dung dịch Br2 dư.
CH3-C≡CH + 2Br2 → →→ → C3H4Br4
(d) Đốt cháy ankin ở dạng tổng quát. Tìm mối liên hệ giữa số mol CO2, H2O.
CnH2n-2 + 3n1 2 O2 ot → nCO2 +(n-1)H2O
22 ankinCOHO n=n-n
(e) Cho propin phản ứng với AgNO3/NH3.
CH3-C≡CH+AgNO3 +NH3 ot → CH3-C≡CAg↓ +NH4NO3
(g) Nhị hợp và tam hợp axetilen.
2C2H2 oxt,t → C4H4 (CH≡C-CH=CH2)
3C2H2 o C,600C → C6H6
(h) Cho axetilen phản ứng với nước (xt, to)
CH≡CH+H2O 2oHg,H,t ++ → [CH2=CH-OH] → CH3CHO
Câu3: Bằng phương pháp hóa học hãy
3
(17) CH3-CH2-CH=CH2 +H2O o H,t + → CH3-CH2-CH(OH)-CH3
(18) CH3-CH2-CH=CH2 +H2 oNi,t → CH3-CH2-CH2-CH3
(19) C4H10 oxt,t → CH4 +C3H6
(20) C4H10 + Cl2 a/s → C4H9Cl+HCl
Câu5: Xác định công thức phân tử và gọi tên X trong các trường hợp sau:
(a) Ankin X có tỉ khối so với hiđro bằng 20.
Hướngdẫngiải
M= 20 . 2 = 4014n - 2 = 40n = 3:CH.
n2n-2CH 34
(b) Ankin X có %mC = 88,24%.
Hướngdẫngiải
CTPT: CnH2n-2: C 58 12n %m=100%=88,24%n=5:CH 14n-2
(c) Cho 10,8 gam ankin X tác dụng với lượng dư dung dịch Br2 thấy có 64 gam Br2 phản ứng.
Hướngdẫngiải
2Br 64 n0,4160(mol)==
CnH2n-2 + 2Br2dư → CnH2n-2Br4 0,2 ←0,4
n2n-2CH 46 10,8 M== 54n=4:CH 0,2
(d) Cho 8 gam propin tác dụng với lượng dư dung dịch AgNO3/NH3 thu được m gam kết tủa. Tính m.
34CH 8 n0,240(mol)==
Hướngdẫngiải
CH3-C≡CH + AgNO3 + NH3 ot → CH3-C≡CAg↓ + NH4NO3 0,2→ 0,2
m = 0,2.147 = 29,4 (gam)
(g) Đốt cháy hoàn toàn một ankin X bằng oxi dư sau phản ứng thu được 13,2 gam CO2 và 3,6 gam
H2O. Hướngdẫngiải
(mol) =−=−=
Số nguyên tử C: n = 2CO 22
BÀITẬPTRẮCNGHIỆM
1.Mức độ nhậnbiết(rấtdễ vàdễ)
Câu1. Ankin là
A. những hiđrocacbon mạch hở có một liên kết đôi trong phân tử.
B. những hiđrocacbon mạch hở có một liên kết ba trong phân tử.
C. những hiđrocacbon mạch hở có một liên kết bội trong phân tử.
D. những hiđrocacbon mạch hở có một vòng no trong phân tử.
Câu2.(MH.15). Ankin là những hiđrocacbon không no, mạch hở, có công thức chung là
A. CnH2n+2 (n ≥ 1).
C. CnH2n-2 (n ≥ 2).
Câu3. Ankin CH3 C≡C CH3 có tên gọi là
A. but-1-in.
B. but-2-in.
Câu4. Ankin dưới đây có tên gọi là
A. 3-metylpent-2-in.
C. 4-metylhex-2-in.
CH3 C C CH CH3
Câu5. Ankin dưới đây có tên gọi là
A. 4-etylpent-2-in.
C. 4-metylhex-2-in.
Câu6. Ankin dưới đây có tên gọi là
A. 3,3-đimetylpent-2-in.
C. 4,4-đimetylhex-2-in.
B. CnH2n (n ≥ 2).
D. CnH2n-6 (n ≥ 6).
C. metylpropin.
CH2 CH3
B. 2-metylhex-4-in.
D. 3-metylhex-4-in.
CH3 C C CH CH2
CH3 CH3
B. 2-etylpent-3-in.
D. 3-metylhex-4-in.
D. meylbut-1-in.
B. 4,4-đimetylpent-3-in.
D. 3,3-đimetylpent-4-in.
Câu7. Ankin nào sau đây có đồng phân hình học?
A. CH3 C≡C CH3.
B. CH3CH2 C≡C CH2CH3.
C. CH≡CH.
D. Không ankin nào có đồng phân hình học.
Câu8.[MH2-2020] Chất nào sau đây có một liên kết ba trong phân tử?
A. Metan. B. Etilen. C. Axetilen. D. Benzen.
Câu9. Phương trình phản ứng cháy của ankin là
A. ot n2n2222 3n1 CH + O nCO+(n1)HO 2 →−
B. ot n2n2222 3n1 CH O nCO+(n1)HO 2 + +→−
C. ot n2n222 3n CH O nCO+nHO 2 +→
D. ot n2n2222 3n1 CH O nCO+(n1)HO 2 +→+
Câu10. Hiđro hóa hoàn toàn ankin tạo thành ankan tương ứng. Sản phẩm trung gian của phản ứng này là
A. anken. B. ankin. C. ankađien. D. xicloankan.
Câu11. Nếu muốn phản ứng: CH≡CH + H2 o t → dừng lại ở giai đoạn tạo thành etilen thì cần sử dụng xúc tác nào dưới đây?
A. H2SO4 đặc. B. Pd/PbCO3
n ứng trên là
A. CH2=CH OH.
Cho phản ứng: 2HC≡CH
Sản phẩm của phản ứng trên là
A. buta-1,3-đien. B. vinylaxetilen. C. but-2-en.
Câu16. Cho phản ứng: 3HC≡CH o than ho¹t tÝnh 600 C →
Sản phẩm của phản ứng trên là
A. C4H6. B. C4H4. C. C6H12.
Câu17. Ankin nào sau đây không có nguyên tử hiđro linh động?
D. butan.
D. C6H6.
A. CH3 C≡CH. B. CH3CH2 C≡CH. C. CH3 C≡C CH3 D. HC≡CH.
Câu18. Ankin nào sau đây không có nguyên tử hiđro linh động?
A. axetilen. B. but-2-in. C. pent-1-in. D. propin.
Câu19. Ankin nào sau đây có nhiều nguyên tử hiđro linh động nhất?
A. but-1-in. B. hex-1-in. C. propin. D. axetilen.
Câu20.(QG.18-201): Chất nào sau đây tác dụng được với dung dịch AgNO3 trong NH3?
A. Etilen B. Metan C. Benzen D. Propin
Câu21.(QG.18-204): Sục khí axetilen vào dung dịch AgNO3 trong NH3 thu được kết tủa màu gì?
A. vàng nhạt. B. trắng. C. đen. D. xanh.
Câu22. Khi cho axetilen phản ứng với lượng dư AgNO3/NH3 tới khi phản ứng xảy ra hoàn toàn, thu được sản phẩm hữu cơ là
A. HC≡CH. B. HC≡CAg. C. AgC≡CAg. D. CH2=CH2
Câu23. Chất nào sau đây không phản ứng được với AgNO3/NH3?
A. but-2-in. B. propin. C. axetilen. D. but-1-in.
2.Mức độ thônghiểu(trungbình)
Câu24. Có bao nhiêu ankin tương ứng với công thức phân tử C5H8?
A. 2. B. 3. C. 4. D. 5.
Câu25. Có bao nhiêu đồng phân ankin C5H8 tác dụng được với dung dịch AgNO3/NH3 tạo kết tủa?
A. 3. B. 2.
C. 4.
Câu26. Có bao nhiêu ankin tương ứng với công thức phân tử C6H10?
D. 1.
A. 5. B. 6. C. 7. D. 8.
Câu27. Có bao nhiêu đồng phân ankin có công thức phân tử C6H10 tác dụng được với dung dịch
AgNO3/NH3 tạo ra kết tủa màu vàng nhạt?
A. 4. B. 5.
C. 3.
Câu28.(C.13): Số đồng phân cấu tạo, mạch hở ứng với công thức phân tử C4H6 là
A. 2. B. 5.
C. 4.
Câu29. Số lượng đồng phân cấu tạo mạch hở ứng với công thức phân tử C5H8 là
A. 9. B. 10.
Câu30. Ankin dưới đây có tên gọi là
A. 1,4-đimetylpent-2-in.
C. 1,4-đimetylhex-2-in.
Câu31. Công thức cấu tạo của 3-metylbut-1-in là
A. (CH3)2CH C≡CH.
C. CH3 C≡C CH2CH3.
Câu32. Công thức cấu tạo của 4-metylpent-2-in là
A. CH3 C≡C CH2CH2CH3
C. CH3CH2 C≡CH CH2CH3.
C. 6.
D. 2.
D. 3.
D. 3.
B. 5-metylhept-3-in.
D. 4-metylhex-3-in.
B. CH3CH2CH2 C≡CH.
D. CH3CH2 C≡C CH3.
B. (CH3)2CH C≡CH CH3
D. (CH3)3C C≡CH.
Câu33. Số liên kết δ và liên kết π trong phân tử vinylaxetilen: CH ≡C–CH=CH2 lần lượt là?
A. 7 và 2. B. 7 và 3.
C. 3 và 3.
D. 3 và 2.
Câu34. Khi cho but-2-in phản ứng với brom dư, tới khi phản ứng xảy ra hoàn toàn thu được sản phẩm hữu cơ là
A. CH3CBr2 CBr2CH3
C. CH3CH2CHBr CBr3.
Câu35. Cho phản ứng: CH3 C≡CH + H2O 4 o 24
Sản phẩm chính của phản ứng trên là
B. CH3CHBr CHBrCH3
D. CHBr2 CBr2CH2CH3.
HgSO HSO, 80C →
A. CH3CH2 CH=O.
C. CH2=C(CH3) OH.
Câu36. Cho phản ứng: 2CH≡C CH3 4 o NHCl, CuCl t →
Sản phẩm của phản ứng trên là
B. CH3 CO CH3.
D. HO CH=CH CH3.
A. C6H6. B. C6H8. C. C6H10. D. C4H6.
Câu37. X là một ankin, có thể tham gia phản ứng trime hóa sau:
Công thức cấu tạo của X là
A. CH3 CH=CH2.
C. HC≡CH.
B. CH3 C≡CH.
D. CH3 C≡C CH3
Câu38. Cho ankin A tác dụng với H2 dư trên xúc tác Ni/to. Sau khi phản ứng xảy ra hoàn toàn thu
được một sản phẩm hữu cơ duy nhất là pentan. Khi A tác dụng với H2, Pd/PbCO3 thì thu được anken C có đồng phân hình học. Tên gọi của A là
A. pent-2-in. B. pent-1-in.
C. 3-metylbut-1-in. D. pent-1-en.
Câu39. Cho ankin X tác dụng với H2 dư (xúc tác Ni/to). Sau khi phản ứng xảy ra hoàn toàn, thu
được một sản phẩm hữu cơ duy nhất là 2-metylbutan. Tên gọi của X là
A. 2-metylbut-1-in.
C. 3-metylbut-2-in.
B. 2-metylbut-2-in.
D. 3-metylbut-1-in.
Câu40. Cho ankin X tác dụng với H2 dư (xúc tác Pd/PbCO3) thu được duy nhất một sản phẩm hữu
cơ Y có đồng phân hình học. Khi hiđro hóa Y thì tạo thành 2-metylpentan. Tên gọi của X là
A. 2-metylpent-1-in.
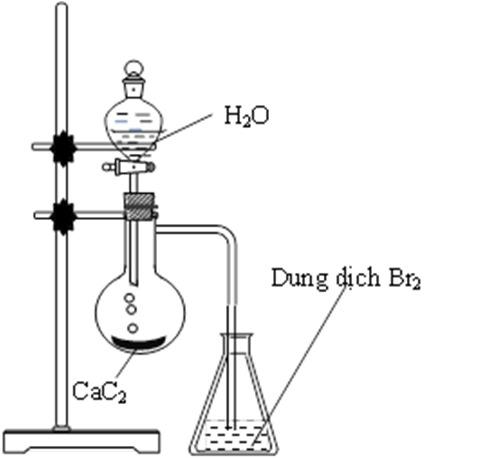
C. 4-metylpent-2-in.
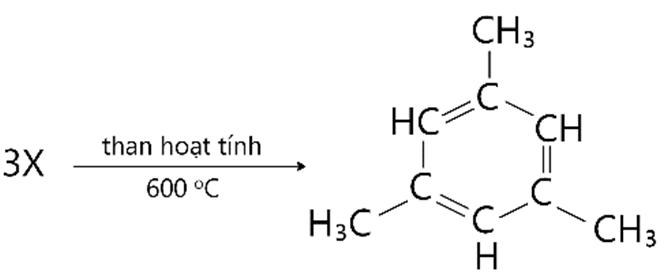
B. 2-metylpent-2-in.
D. 4-metylpent-1-in.
Câu41. Cho 3-metylbut-1-in tác dụng với H2 (xúc tác Pd/PbCO3) tới khi phản ứng hoàn toàn thu được hỗn hợp Y chỉ có hai hiđrocacbon. Công thức cấu tạo của hai hidrcacbon lần lượt là:
A. CH≡C CH(CH3)2 và CH3CH2CH(CH3)2
B. CH2=CH CH2CH2CH3 và CH3CH2CH(CH3)2.
C. CH≡C CH(CH3)2 và CH2=CH CH(CH3)2.
D. CH2=CH CH(CH3)2 và CH3CH2CH(CH3)2
Câu42. Công thức cấu tạo của ankin có thể tạo thành từ phản ứng tách hiđro của pent-2-en là
A. CH2=C=CH CH2CH3.
C. CH3 C≡C CH3.
B. CH3 C≡C CH2CH3.
D. CH3 CH=C=CH CH3.
Câu43.(QG.18-201): Thực hiện thí nghiệm như hình vẽ dưới đây:
Hiện tượng xảy ra trong bình chứa dung dịch Br2 là
A. có kết tủa đen.
C. có kết tủa trắng.
B. dung dịch Br2 bị nhạt màu.
D. có kết tủa vàng.
Câu44.(QG.18-202): Thực hiện thí nghiệm như hình vẽ bên. Kết thúc thí nghiệm, trong bình
đựng dung dịch AgNO3 trong NH3 xuất hiện kết tủa màu vàng nhạt.
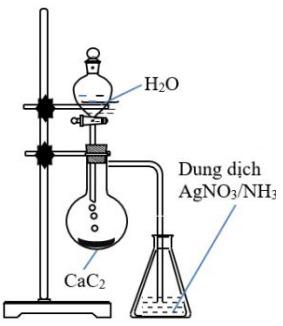
A. CaO. B. Al4C3
C. CaC2
Câu45.(QG.18-203): Thí nghiệm được tiến hình như hình vẽ bên.
D. Ca.
Hiện tượng xảy ra trong bình đựng dung dịch AgNO3 trong NH3 là
A. có kết tủa màu nâu đỏ.
C. dung dịch chuyển sang màu da cam.
B. có kết tủa màu vàng nhạt.
D. dung dịch chuyển sang màu xanh lam.
Câu46.(QG.18-204): Thực hiện thí nghiệm như hình vẽ bên. Kết thúc thí nghiệm, dung dịch Br2 bị mất màu.
Chất X là
A. CaC2 B. Na.
Câu47. Phát biểu nào sau đây không đúng?
C. Al4C3
D. CaO.
A. Các ankin HC≡CH, CH3 C≡CH, … có công thức chung là CnH2n-2 (n ≥ 2) tạo thành dãy đồng đẳng của axetilen.
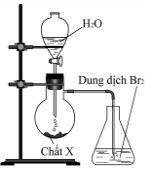
B. Liên kết ba của ankin được tạo nên từ ba liên kết π.
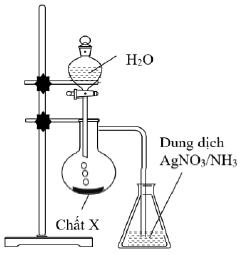
C. Các ankin 2C và 3C chỉ có duy nhất một đồng phân cấu tạo.
D. Ankin không có đồng phân hình học như anken.
Câu48. Phát biểu nào sau đây không đúng?
A. Ankin cũng có thể làm mất màu dung dịch KMnO4 như anken.
B. Trong phản ứng cháy của ankin, số nguyên tử cacbon trong ankin bằng 2
C. Trong phản ứng cháy của ankin, 22 ankinCOHO nnn =− .
Câu49. Phát biểu nào sau đây không đúng?
n n .
ankin CO
D. Phương trình phản ứng cháy của ankin là: ot n2n2222 3n1 CH O nCO+(n1)HO 2 +→− .
A. Nguyên tử hiđro đính vào cacbon của liên kết ba linh động hơn nhiều so với nguyên tử hiđro đính vào cacbon của liên kết đôi và liên kết đơn.
B. Thuốc thử Tollens có thể viết là AgNO3/NH3.
C. Axetilen là ankin duy nhất có hiđro linh động.
D. Nguyên tử hiđro linh động trong ankin có thể bị thay thế bởi ion kim loại. Câu50. Phát biểu nào sau đây không đúng?
A. Axetilen có thể tham gia phản ứng thế với tối đa hai ion bạc.
B. Kết tủa Ag2C2 có màu vàng nhạt.
C. But-2-in chỉ có thể tham gia phản ứng thế với một ion bạc.
D. Propin phản ứng với AgNO3/NH3 tạo ra kết tủa CH3 C≡CAg
Câu51.Không thể phân biệt metan và axetilen bằng chất nào sau đây?
A. NaOH. B. Br2
C. KMnO4
Câu52. Có thể phân biệt axetilen, etilen và metan bằng hóa chất nào sau đây?
A. KMnO4 và NaOH.
C. AgNO3/NH3
D. AgNO3/NH3
B. KMnO4 và quỳ tím.
D. Br2 và AgNO3/NH3
Câu53. Có thể phân biệt các đồng phân của hợp chất butin bằng hóa chất nào sau đây?
A. KMnO4. B. Br2.
C. AgNO3/NH3.
Câu54. Có thể phân biệt but-1-in, but-2-in, metan bằng hóa chất nào sau đây?
A. AgNO3/NH3.
C. KMnO4 và AgNO3/NH3.
B. Br2 và quỳ tím.
D. HBr và Br2.
D. Quỳ tím.
Câu55.(B.13): Cho 3,36 lít khí hiđrocacbon X (đktc) phản ứng hoàn toàn với lượng dư dung dịch AgNO3 trong NH3, thu được 36 gam kết tủa. Công thức phân tử của X là
A. C4H4. B. C3H4. C. C4H6. D. C2H2.
Câu56.(A.14): Hỗn hợp khí X gồm etilen và propin. Cho a mol X tác dụng với lượng dư dung dịch AgNO3 trong NH3, thu được 17,64 gam kết tủa. Mặt khác a mol X phản ứng tối đa với 0,34 mol H2. Giá trị của a là
A. 0,32. B. 0,34. C. 0,46. D. 0,22.
3.Mức độ vậndụng(khá)
Sử dụng dữ kiện sau để trả lời các câu hỏi 57, 58, 59 Cho chuỗi phản ứng sau:
Câu57. Công thức phân tử của A là
A. CH4. B. C2H4. C. C4H4. C. C2H6.
Câu58. Công thức phân tử của B, C lần lượt là:
A. C2H4 và C4H10. B. C2H2 và C4H8.
C. C4H4 và C3H6. D. C2H4 và C4H8.
Câu59. Tên gọi của D và E lần lượt là:
A. axetilen và etan. B. etilen và butan. C. butan và etan. D. etan và etan.
Sử dụng dữ kiện sau để trả lời các câu hỏi 60, 61, 62, 63
Cho chuỗi phương trình phản ứng sau:
Câu60. Công thức phân tử của A là
A. C2H4.
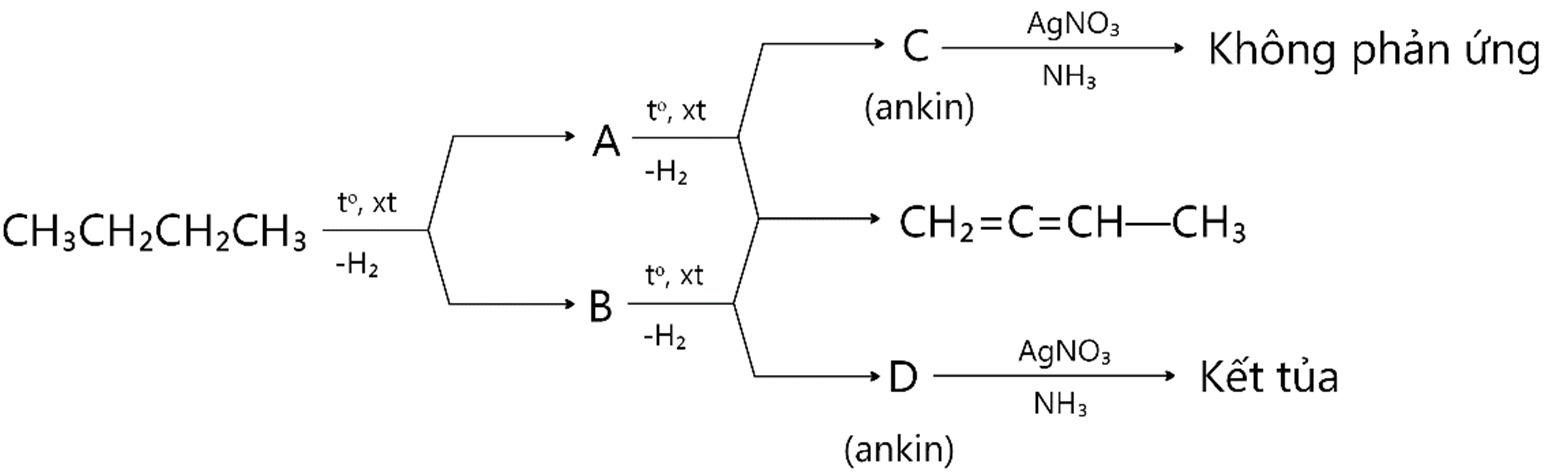
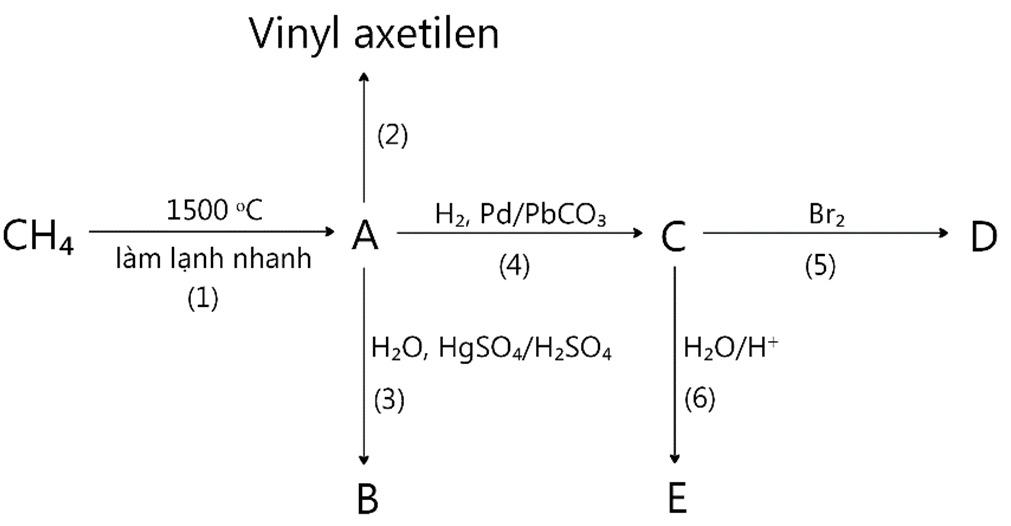
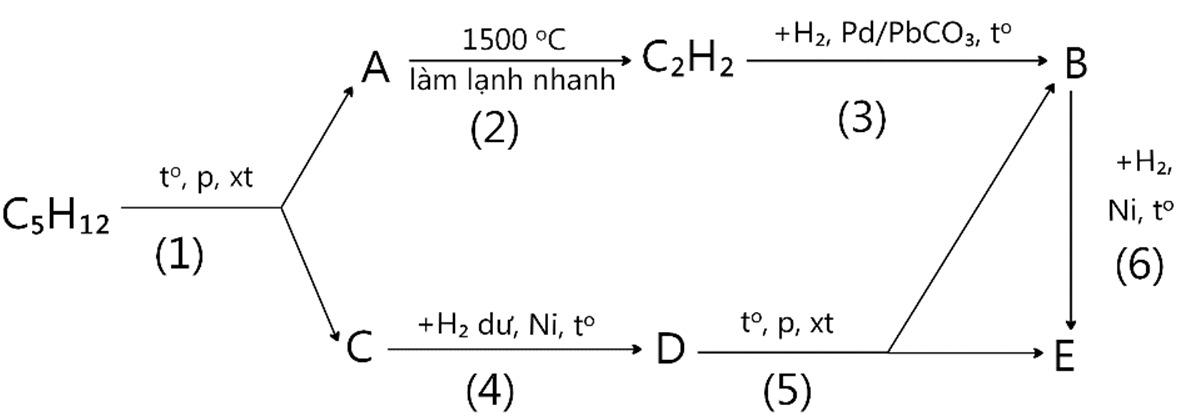
B. C4H6.
C. C6H6.
Câu61. Phản ứng (2) thuộc loại phản ứng nào dưới đây?
A. đime hóa. B. trime hóa.
C. thủy phân.
Câu62. Công thức cấu tạo thu gọn của B và E lần lượt là:
A. CH2=CH OH và CH3CH2 OH.
C. CH3 CH=O và CH3CH2 OH.
Câu63. Công thức cấu tạo thu gọn của D là
A. CH2Br CH2Br. B. CH3 CHBr2.
Sử dụng dữ kiện sau để trả lời các câu hỏi 64, 65
Cho chuỗi phản ứng sau:
Câu64. Tên gọi của A và B lần lượt là:
D. C2H2.
D. hiđro hóa.
B. CH3 CH=O và CH2=CH OH.
D. CH3CH2 OH và CH2=CH OH.
C. CHBr2 CHBr2.
D. CH3 CH2Br.
A. but-2-en và but-1-en.
C. but-1-en và xiclobutan.
Câu65. Công thức cấu tạo của C và D lần lượt là:
A. xiclobutan và but-1-in.
C. but-1-in và but-2-in.
B. but-2-in và but-1-in.
D. but-1-en và but-2-en.
B. but-1-in và but-2-en.
D. but-2-in và but-1-in.
Sử dụng dữ kiện sau để trả lời các câu hỏi 66, 67, 68, 69
Cho chuỗi phản ứng sau:
Câu66. Để thực hiện phản ứng (1), axetilen cần phản ứng với chất nào dưới đây?
A. KMnO4. B. Ag2O. C. AgCl. D. AgNO3/NH3.
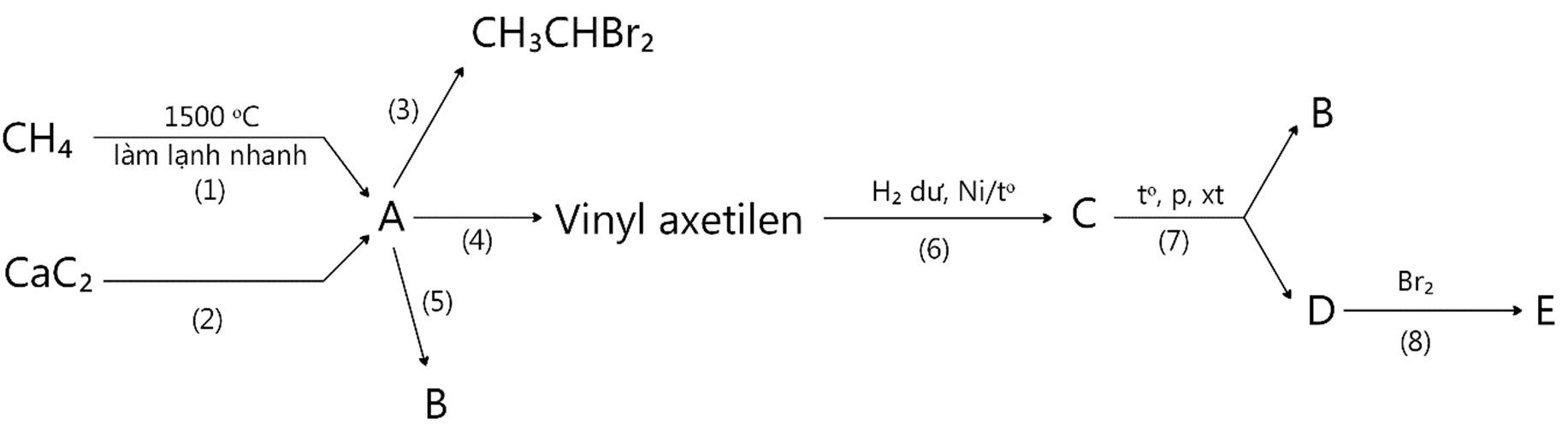
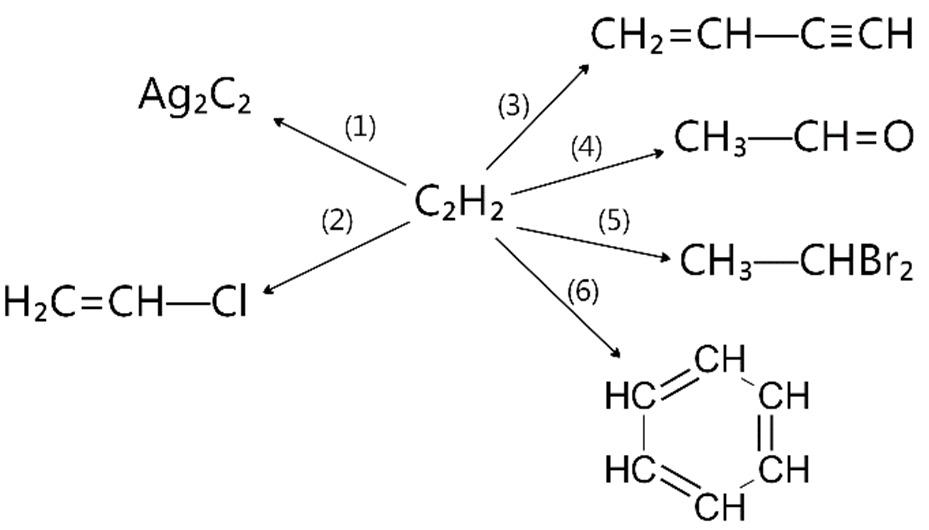
Câu67. Để thực hiện phản ứng (2), axetilen cần phản ứng với chất nào dưới đây?
A. HCl. B. Cl2
Câu68. Các phản ứng nào thuộc dạng oligome hóa?
A. (1) và (3). B. (3) và (6).
C. CH3CH2Cl.
C. (4) và (6).
D. HClO.
D. (2) và (5).
Câu69. Thực hiện phản ứng nào thì C2H2 phải cộng H2O, xúc tác HgSO4, H2SO4, to?
A. (3). B. (4). C. (5).
Sử dụng dữ kiện sau để trả lời các câu hỏi 70, 71, 72, 73, 74
D. (6).
Câu70. Công thức phân tử của A là
A. C2H4. B. CH4.
Câu71. Phản ứng (4) thuộc loại phản ứng nào?
A. Hiđro hóa. B. Trime hóa.
Câu72. Công thức phân tử của E là
A. C2H5Br. B. C2H4Br2
Câu73. Tên gọi của B là
A. Etilen. B. Etan.
Câu74. Phản ứng (7) thuộc loại phản ứng nào?
A. tách.
C. cộng.
C. C2H2.
C. Đime hóa.
C. C2H2Br4
C. Axetilen.
B. thế
D. oxi hóa hoàn toàn.
D. CO2.
D. Tách hiđro.
D. C3H6Br2
D. Metan.
Sử dụng dữ kiện sau để trả lời các câu hỏi 75, 76, 77
Câu75. Công thức phân tử của A là
A. C4H10. B. CH4.
Câu76. Tên gọi của D là
A. but-1,3-đien. B. axetilen.
Câu77. Công thức cấu tạo thu gọn của E là
C4H8.
but-2-en.
C2H4.
A. CH2=CH OH.
CH3 CH=O. C. HO CH2CH2 OH.
CH3 CO CH3.
Câu78.(C.13): Cho 27,2 gam ankin X tác dụng v
Câu79.(A.10): Đun nóng hỗn hợp khí X gồm 0,02 mol C2H2 và 0,03 mol H2 trong một bình kín (xúc tác Ni), thu được hỗn hợp khí Y. Cho Y lội từ từ vào bình nước brom (dư), sau khi kết thúc các phản ứng, khối lượng bình tăng m gam và có 280 ml hỗn hợp khí Z (đktc) thoát ra. Tỉ khối của Z so với H2 là 10,08. Giá trị của m là
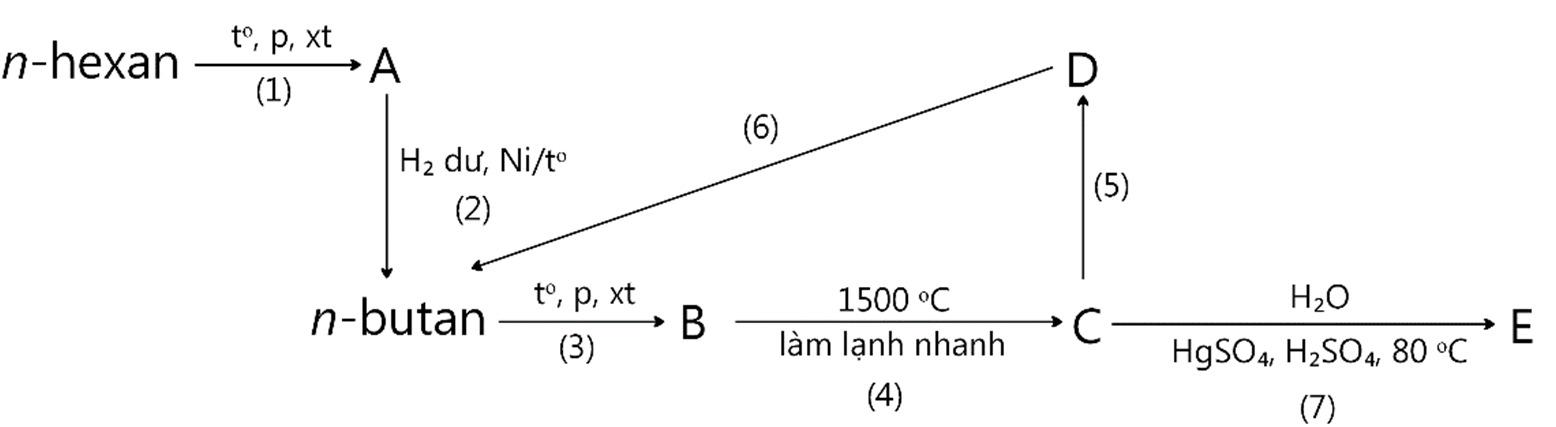
1. Anken: CnH2n (n ≥ 2); ankađien: CnH2n-2 (n ≥ 3); ankin (n ≥ 2).
2. Điều kiện có đồng phân hình học: (1) chứa liên kết đôi C=C, (2) mỗi nhóm gắn với C nối đôi phải khác nhau ⇒ anken và ankađien có khả năng có đồng phân hình học.
3. CH2=CH2: etilen; CH2=CH-CH3: propilen; CH2=C=CH2: anlen; CH2=CH-CH=CH2: butađien; CH2=C(CH3) – CH=CH2: isopren; CH≡CH: axetilen; CH≡C – CH=CH2: vinyl axetilen.
4. Qui tắc cộng mac-côp-nhi-côp: Khi cộng HX vào hợp chất bất đối xứng, H cộng ưu tiên vào C của nối đôi chứa nhiều H hơn, X cộng vào bên còn lại.
5. Để chuyển ankin thành anken ta dùng phản ứng cộng H2 với xúc tác Pd/PbCO3, to .
6. Các hiđrocacbon không no (anken, ankađien, ankin) đều có khả năng làm mất màu dung dịch brom và dung dịch thuốc tím KMnO4 ⇒ Thuốc thử nhận biết.
7. Trong các hiđrocacbon, chỉ có hợp chất có liên kết ba đầu mạch (CH≡C-) mới có khả năng tác dụng với AgNO3/NH3 dư tạo kết tủa vàng ⇒ Thuốc thử nhận biết.
8. Anken và ankađien chứa liên kết đôi C=C nên có khả năng tham gia PƯ trùng hợp tạo polime.
9. Ankin không có phản ứng trùng hợp nhưng có phản ứng nhị hợp và tam hợp.
10. Một số phản ứng đặc biệt: (1) 2C2H2
4 o CuCl,NHCl t C4H4 (CH≡C-CH=CH2: vinyl axetilen)
C6H6 (benzen)
(3)
1. Công thức của anken: CnH2n (n ≥ 2); ankađien: CnH2n-2 (n ≥ 3); ankin: CnH2n-2 (n ≥ 2).
2. Qui tắc cộng mac-côp-nhi-côp: Khi cộng HX vào liên kết đôi C=C bất đối xứng, H cộng ưu tiên
vào C chứa nhiều H hơn, X cộng vào bên còn lại.
3. Hoàn thành bảng sau: Têngọi Côngthức Têngọi Côngthức
2-CH3 (7) 3-metylbut-1-in CH≡C-CH(CH3)-CH3
(4) butađien CH2=CH-CH=CH2 (8) vinyl axetilen CH≡C-CH=CH2
4. Đánh dấu “X” vào các trường hợp có phản ứng xảy ra trong bảng sau: Metan Etilen Butađien Axetilen Vinyl axetilen Cl2 (as) X
H2 (Ni, to)
Dung dịch Br2
AgNO3/NH3 dư, to X X
Trùng hợp
4
5. Bằng phương pháp hóa học hãy nhận biết các chất khí sau:
(a) metan, etilen, axetilen.
CH4 CH2=CH2 CH≡CH
+AgNO3/NH3 X X ↓ vàng
PTHH:
(b)
(2)
etilen,
phương trình hóa học điều chế PE, PVC, cao su buna. Hướngdẫngiải
* PE
2CH4 o 1500C → lµm l¹nh nhanh C2H2 + 3H2
C2H2 + H2 o 3t,Pd/PbCO → C2H4
CH2=CH2 o t,p,xt → ( 22n CH-CH)
* PVC
CH≡CH + HCl o t,xt → CH2=CH-Cl
CH2=CH-Cl t,p,xt → ( 2n CH-CH(Cl)) .
* Cao su buna
2C2H2 oxt,t → C4H4
CH≡C-CH=CH2 + H2 o 3 Pd/PbCO,t → CH2=CH-CH=CH2
CH2=CH-CH=CH2 o xt,t,P →–(–CH2-CH=CH-CH2–)n–
7. Từ than đá, đá vôi và các điều kiện cần thiết hãy viết các phương trình hóa học điều chế butan, metyl clorua, poli(vinyl clorua).
* Butan
CaCO3 + C ot → CaC2 + C2H2
2C2H2 oxt,t → C4H4
Hướngdẫngiải
CH≡C-CH=CH2 + 3H2 → oNi,t CH3-CH2-CH2-CH3
* Metyl clorua
CH3-CH2-CH2-CH3 oxt,t → CH4 + C3H6
CH4 + Cl2 a/s → CH3Cl + HCl
* Poli(vinyl clorua)
CH≡CH + HCl o t,xt → CH2=CH-Cl
CH2=CH-Cl t,p,xt → ( 2n CH-CH(Cl))
ĐỀ LUYỆNHIĐROCACBONKHÔNGNO
20câu–30phút 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20
Câu1.(MH.15). Ankin là những hiđrocacbon không no, mạch hở, có công thức chung là
A. CnH2n+2 (n ≥ 1).
C. CnH2n-2 (n ≥ 2).
B. CnH2n (n ≥ 2).
D. CnH2n-6 (n ≥ 6).
Câu2.(QG.18-204): Sục khí axetilen vào dung dịch AgNO3 trong NH3 thu được kết tủa màu
A. vàng nhạt. B. trẳng. C. đen. D. xanh.
Câu3.(QG.18-203): Chất nào sau đây không làm mất màu dung dịch Br2?
A. Axetilen. B. Propilen. C. Etilen. D. Metan.
Câu4.(QG.18-202): Ở điều kiện thường, chất nào sau đây làm mất màu dung dịch Br2?
A. benzen. B. etilen. C. metan. D. butan.
Câu5.(QG.16): Trước những năm 50 của thế kỷ XX, công nghiệp tổng hợp hữu cơ dựa trên nguyên liệu chính là axetilen. Ngày nay, nhờ sự phát triển vượt bậc của công nghệ khai thác và chế biến dầu mỏ, etilen trở thành nguyên liệu rẻ tiền, tiện lợi hơn nhiều so với axetilen. Công thức phân tử của etilen là
A. C2H4.
B. C2H6. C. CH4. D. C2H2.
Câu6.(C.11): Chất nào sau đây có đồng phân hình học?
A. CH2=CH-CH=CH2
C. CH3-CH=C(CH3)2
B. CH3-CH=CH-CH=CH2
D. CH2=CH-CH2-CH3
Câu7.(B.14): Trùng hợp hiđrocacbon nào sau đây tạo ra polime dung để sản xuất cao su buna?
A. 2-metylbuta-1,3-đien. B. Penta-1,3-đien.
C. But-2-en.
D. Buta-1,3-đien.
Câu8.(A.14): Chất X có công thức: CH3-CH(CH3)-CH=CH2. Tên thay thế của X là
A. 3-metylbut-1-in.
B. 3-metylbut-1-en.
C. 2-metylbut-3-en. D. 2-metylbut-3-in.
Câu9.(C.13): Số đồng phân cấu tạo, mạch hở ứng với công thức phân tử C4H6 là
A. 2. B. 5. C. 4. D. 3.
Câu10.(A.07): Hiđrat hóa 2 anken chỉ tạo thành 2 ancol. Hai anken đó là
A. eten và but-2-en. B. 2-metylpropen và but-1-en.
C. propen và but-2-en. D. eten và but-1-en.
Câu11.(B.14): Đốt cháy hoàn toàn 0,2 mol hỗn hợp X gồm một ankan và một anken, thu được 0,35 mol CO2 và 0,4 mol H2O. Phần trăm số mol của anken trong X là
A. 40%. B. 50%. C. 25%. D. 75%.
Câu12.(A.08): Cho các chất sau: CH2=CH-CH2-CH2-CH=CH2, CH2=CH-CH=CH-CH2-CH3, CH3-C(CH3)=CH-CH3, CH2=CH-CH2-CH=CH2. Số chất có đồng phân hình học là
A. 4. B. 1. C. 2. D. 3.
Câu13.(B.13): Cho 3,36 lít khí hiđrocacbon X (đktc) phản ứng hoàn toàn với lượng dư dung dịch
AgNO3 trong NH3, thu được 36 gam kết tủa. Công thức phân tử của X là
A. C4H4 B. C3H4 C. C4H6 D. C2H2
Câu14.(C.08): Đốt cháy hoàn toàn hỗn hợp M gồm một ankan X và một ankin Y, thu được số mol
CO2 bằng số mol H2O. Thành phần phần trăm về số mol của X và Y trong hỗn hợp M lần lượt là:
A. 75% và 25%. B. 20% và 80%. C. 35% và 65%. D. 50% và 50%.
Câu15.(QG.18-204): Thực hiện thí nghiệm như hình vẽ bên. Kết thúc thí nghiệm, dung dịch Br2 bị mất màu.
Chất X là
A. CaC2 B. Na. C. Al4C3
D. CaO.
Câu16.(A.07): Ba hiđrocacbon X, Y, Z kế tiếp nhau trong dãy đồng đẳng, trong đó khối lượng phân tử Z gấp đôi khối lượng phân tử X. Đốt cháy 0,1 mol chất Y, sản phẩm khí hấp thụ hoàn toàn vào dung dịch Ca(OH)2 (dư), thu được số gam kết tủa là
A. 30. B. 10. C. 40. D. 20.
Câu17.(A.08): Hỗn hợp X có tỉ khối so với H2 là 21,2 gồm propan, propen và propin. Khi đốt cháy hoàn toàn 0,1 mol X, tổng khối lượng của CO2 và H2O thu được là
+ 3,2H2O 2 2 22 COHO COHO n3.0,10,3mol;n3,2.0,10,32molmm18,96gam. ==== += Câu18.(A.08): Đun nóng hỗn hợp khí gồm 0,06 mol C2H2 và 0,04 mol H2 với xúc tác Ni, sau một thời gian thu đượ

Dạng1:Bàitoánvề phản ứngcộngH2,Br2
Dạng2:Bàitoánvề phản ứngthế củaank-1-in
Dạng3:Bàitoánvề phản ứng đốtcháy
DẠNG1:BÀITOÁNVỀ PHẢN ỨNGCỘNGH2,Br2 LÝTHUYẾTVÀPHƯƠNGPHÁPGIẢI
- PƯ tổng quát: CnH2n+2-2k + kH
- Bảo toàn liên kết π: mol liên kết π = 22 lkBrH nk(nn) π =+
- Với phản ứng cộng H2; BTKL: mT = mS ⇔ TTSS n.Mn.M = nkhí giảm = 2 Hph¶nøng n
VÍDỤ MINHHỌA
Câu1. Hiđro hóa hoàn toàn 5,6 gam anken A tạo ra 5,8 gam ankan. Công thức phân tử của A là
A. C4H10. B. C5H12. C. C4H8. D. C5H10.
Câu2. Anken X tác dụng với dung dịch brom thu được duy nhất một hợp chất hữu cơ Y chứa
74,08 % brom về khối lượng. Công thức phân tử của X là
A. C3H6 B. C4H8 C. C5H10 D. C2H4
Câu3. Hỗn hợp Z gồm H2 và C3H6 có tỉ khối hơi so với H2 là 11. Dẫn 4,48 lít khí Z (đktc) qua bột
Ni/to thu được hỗn hợp khí T có tỉ khối so với H2 là 13. Số mol hỗn hợp khí T là
A. 0,17. B. 0,24. C. 0,34. D. 0,085.
Câu4. Hỗn hợp A gồm C3H6 và H2. Dẫn 1 mol hỗn hợp A qua bột Ni/to, sau một thời gian hỗn hợp
B. Tỉ khối của B so với A là 1,25. Khối lượng ankan tạo thành là
A. 8,8 gam. B. 4,2 gam. C. 8,4 gam. D. 70,4 gam.
Câu5.(A.12): Hỗn hợp X gồm H2 và C2H4 có tỉ khối so với H2 là 7,5. Dẫn X qua Ni nung nóng, thu được hỗn hợp Y có tỉ khối so với H2 là 12,5. Hiệu suất của phản ứng hiđro hoá là
Câu7.(C.10): Cho 3,12 gam ankin X phản ứng với 0,1 mol H2 (xúc tác Pd/PbCO3, t0), thu đượ
hỗn hợp Y chỉ có hai hiđrocacbon. Công thức phân tử của X là
CnH2n-2 + H2 o 3 Pd/PbCO,t → CnH2n
Vì sau phản ứng thu được 2 hiđrocacbon ⇒ Ankin X dư ⇒ nX > nankin pư = nH2 = 0,1 mol
⇒ X22 3,12 M31,2XlµCH(M26) 0,1 <= =
Câu8.(C.13): Cho 27,2 gam ankin X tác dụng với 15,68 lít khí H2 (đktc) có xúc tác thích hợp, thu
được hỗn hợp Y (không chứa H2).
c phân tử của X là
Câu9.(QG.18-201): Cho 11,2 lít (đktc) h
Hỗn hợp X gồm C2H2 và H2 có cùng số mol. Lấy một lượng hỗn hợp X cho qua chất xúc tác nung nóng, thu được hỗn hợp Y gồm C2H4, C2H6, C2H2 và H2. Sục Y vào dung dịch brom (dư) thì khối lượng bình brom tăng 10,8 gam và thoát ra 4,48 lít hỗn hợp khí (đktc) có tỉ khối so với H2 là 8. Thể tích O2 (đktc) cần để đốt cháy hoàn toàn hỗn hợp Y là
ở đktc) gồm 2 hiđrocacbon mạch hở lội từ từ qua bình chứa 1,4 lít dung dịch Br2 0,5M. Sau khi phản ứng hoàn toàn, số mol Br2 giảm đi một nửa và khối lượng bình tăng thêm 6,7 gam. Công thức phân tử của 2 hiđrocacbon là:
A. C2H2 và C4H6. B. C2H2 và C4H8.
C. C3H4 và C4H8. D. C2H2 và C3H8. Hướngdẫngiải
nX = 0,2 mol, 2 2 Br Brp− n1,4.0,50,7moln0,35mol == =
TH1: X chỉ có 1 hiđrocacbon phản ứng với dd Br2 §¸p¸n → D. C2H2 và C3H8
n n0,175molm4,556,7(lo¹i) 2 == =≠
Brp− CH CH
2 22 22
TH2: X gồm cả 2 hiđrocacbon đều phản ứng với dd Br2
mX = 6,7 gam ⇒ X 6,7 M33,5Lo¹iC. 0,2 == 0,35 k1,75Lo¹iA 0,2 == ⇒ Chọn B.
Câu16.[MH-2022] Nung nóng a mol hỗn hợp X gồm propen, axetilen và hiđro với xúc tác Ni trong bình kín (chỉ xảy ra phản ứng cộng H2), sau một thời gian thu được hỗn hợp khí Y có tỉ khối so với X là 1,25. Đốt cháy hết Y, thu được 0,87 mol CO2 và 1,05 mol H2O. Mặt khác, Y phản ứng tối đa với 0,42 mol brom trong dung dịch. Giá trị của a là
khối so với He là 5. Hiệu suất của phản ứng hiđro hoá là A. 25% B. 20% C. 50% D. 40% H
c hỗn hợp khí X gồm C3H4, C3H6, C3H8, H2. Dẫn hỗn hợp X qua bình đựng dung dịch brom dư thì còn lại
1,68 lít (ở đktc) hỗn hợp khí Z. Tổng số mol H2 và C3H8 trong hỗn hợp khí Z là A. 0,075. B. 0,15. C. 0,75. D. 0,05. Hướngdẫngiải Hỗn hợp khí Z thoát ra chính là H2 và C3H8 ⇒ 238 H,CHZ nn0,075mol. ==
Câu27.(A.10): Đun nóng hỗn hợp khí X gồm 0,02 mol C2H2 và 0,03 mol H2 trong một bình kín (xúc tác Ni), thu được hỗn hợp khí Y. Cho Y lội từ từ vào bình nước brom (dư), sau khi kết thúc các phản ứng, khối lượng bình tăng m gam và có 280 ml hỗn hợp khí Z (đktc) thoát ra. Tỉ khối của Z so với H2 là 10,08. Giá trị của m là
A. 0,585. B. 0,620. C. 0,205. D. 0,328. Hướngdẫngiải
BTKL
0,02.260,03.2m0,0125.2.10,08m0,328gam.
Câu28. Đun nóng hỗn hợp khí gồm 0,1 mol C2H2 và 0,2 mol H2 với xúc tác Ni, sau một thời gian thu được hỗn hợp khí Y. Dẫn toàn bộ hỗn hợp Y lội từ từ qua bình đựng dung dịch brom (dư) thì còn lại 3,136 lít hỗn hợp khí Z (ở đktc) có tỉ khối so với H2 là 3. Khối lượng bình brom tăng lên bao nhiêu gam?
3,00 gam.
2,60 gam.
2,16 gam.
0,84 gam. Hướngdẫngiải
BTKL t¨ngt¨ng mm
→+=+ =
0,1.260,2.2m0,14.2.3m2,16gam.
Z
Câu29. Đun nóng 0,1 mol hỗn hợp khí gồm C2H2 và H2 (tỉ lệ mol 1:1) với xúc tác Ni, sau một thời gian thu được hỗn hợp khí Y. Dẫn toàn bộ hỗn hợp Y lội từ từ qua bình đựng dung dịch brom (dư)
thì còn lại 0,672 lít hỗn hợp khí Z (ở đktc) có tỉ khối so với He là 4. Khối lượng bình brom tăng lên bao nhiêu gam?
Hướngdẫngiải 2
BTKL YYHp−XY 0,1.260,2.280,3.2n.2.11n0,4molnnn0,2mol→++= = =−=
222224
BTpi Hp−Brp−CHCH nn2nn0,2a2.0,10,2a0,2mol→+=+⇔+=+ = Câu31. Hỗn hợp X gồm C2H2 và H2 có cùng số mol. Lấy m gam hỗn hợp X cho qua xúc tác Ni nung nóng, thu được hỗn hợp khí Y. Dẫn hỗn hợp khí Y vào dung dịch brom dư thì khối lượng bình brom tăng thêm 10,8 gam và thoát ra 4,48 lít hỗn hợp khí (đktc) có tỉ khối so với heli bằng 4. Khối lượng C2H2 và H2 trong hỗn hợp ban đầu lần lượt là:
A. 13 gam và 1 gam.
B. 0,88 gam và 11,5 gam.
C. 11,5 gam và 0,88 gam. D. 1 gam và 13 gam. Hướngdẫngiải
22442 22 H(X)H(CH,CH)H(H)HH nnn0,50,32nn0,1mola0,10,10,2mol =+⇔=+
Câu35.[QG.22-202] Hỗn hợp E gồm các hiđrocacbon mạch hở có cùng số nguyên tử hiđro. Tỉ khối của E đối với H2 là 12,5. Đốt cháy hoàn toàn a mol E cần vừa đủ 0,11 mol O2 thu được CO2 và
H2O. Mặt khác, a mol E tác dụng tối đa với x mol Br2 trong dung dịch. Giá trị của x là
Hỗn hợp E gồm các hiđrocacbon mạch hở có cùng s
4NO3
C2Ag2 + 2HCl → C2H2 + 2AgCl↓
VÍDỤ MINHHỌA
Câu1. Dẫn axetilen qua bình chứa lượng dư dung dịch AgNO3 trong NH3 thấy khối lượng bình
tăng thêm 2,6 gam. Lượng kết tủa tạo thành sau phản ứng là
A. 13,3 gam. B. 21,6 gam. C. 24,0 gam. D. 21,4 gam.
Câu2. Dẫn một lượng but-1-in qua bình chứa lượng dư dung dịch AgNO3/NH3 thì thu được 5,635 gam kết tủa màu vàng. Khối lượng ankin ban đầu là
A. 1,96 gam. B. 1,89 gam.
C. 37,80 gam. D. 3,78 gam.
Câu3.(A.14): Hỗn hợp khí X gồm etilen và propin. Cho a mol X tác dụng với lượng dư dung dịch
AgNO3 trong NH3, thu được 17,64 gam kết tủa. Mặt khác a mol X phản ứng tối đa với 0,34 mol H2.
Giá trị của a là
A. 0,32. B. 0,34.
C. 0,46.
D. 0,22.
Câu4.(B.13): Cho 3,36 lít khí hiđrocacbon X (đktc) phản ứng hoàn toàn với lượng dư dung dịch
AgNO3 trong NH3, thu được 36 gam kết tủa. Công thức phân tử của X là
A. C4H4.
B. C3H4.
C. C4H6.
D. C2H2.
Câu5.(A.11): Cho 13,8 gam chất hữu cơ X có công thức phân tử C7H8 tác dụng với một lượng dư dung dịch AgNO3 trong NH3, thu được 45,9 gam kết tủa. X có bao nhiêu đồng phân cấu tạo thỏa mãn tính chất trên?
A. 2. B. 5.
C7H8: k = 4; nX = nkết tủa = 0,15 mol ⇒ Mkế
CH≡C – CH2 – CH2 – CH2 – C≡CH
CH≡C – CH(CH3) – CH2 – C≡CH
CH≡C – C(CH3)2 – C≡CH
CH≡C – CH(C2H5) – C≡CH
C. 4.
D. 6. Hướngdẫngiải
tủa = 306 (chẵn) ⇒ X chứa 2 liên kết ba đầu mạch.
Chú ý: Trong pư thế Ag của ank – 1 – in nếu số Ag thế lẻ thì Mkt lẻ, số Ag thế chẵn thì Mkt chẵ
Câu6.(B.14): Một bình kín chỉ chứa các chất sau: axetilen (0,5 mol), vinylaxetilen (0,4 mol), hiđro (0,65 mol) và một ít bột niken. Nung nóng bình một thời gian, thu được hỗn hợp khí X có t
kh
i so với H2 bằng 19,5. Khí X phản ứng vừa đủ với 0,7 mol AgNO3 trong dung dịch NH3, thu
Câu7.(B.09): Cho hỗn hợp X gồm CH
Lấy 8,6 gam X tác dụng hết với dung dịch brom (dư) thì khối lượng brom phản ứng là 48 gam. Mặt khác, nếu cho 13,44 lít (ở đktc) hỗn hợp khí X tác dụng với lượng dư dung dịch AgNO3 trong NH3, thu được 36 gam kết tủa. Phần trăm thể tích của CH4 có trong X là
20%.
50%. C. 25%.
3, C4H4: CH2=CH-C≡CH.
BÀITẬPTỰ LUYỆN
Câu9. Dẫn một lượng propin qua bình đựng lượng dư AgNO3 trong NH3 thì thấy khối lượng bình tăng thêm 4,0 gam. Lượng kết tủa tạo thành sau phản ứng là
A. 21,6 gam. B. 14,7 gam. C. 25,4 gam. D. 10,8 gam.
Câu10. Dẫn V lít axetilen (ở đktc) qua bình chứa lượng dư AgNO3/NH3. Sau phản ứng thu được
12 gam kết tủa màu vàng nhạt. Giá trị của V là
A. 0,224. B. 0,112.
C. 1,12.
D. 2,24.
Câu11. Dẫn V lít axetilen (ở đktc) qua bình chứa lượng dư AgNO3/NH3. Sau phản ứng, thu được
12 gam kết tủa màu vàng nhạt. Nếu dẫn V lít propin (ở đktc) qua bình chứa lượng dư AgNO3/NH3 thì lượng kết tủa tạo thành là
A. 21,6 gam.
B. 14,7 gam.
C. 7,35 gam.
D. 29,4 gam.
Câu12. Dẫn một ankin mạch hở vào bình chứa dung dịch AgNO3/NH3 dư thu được 8,4 gam kết tủa. Đồng thời, khối lượng bình chứa tăng lên 0,91 gam. Công thức phân tử của ankin ban đầu là
A. C2H2
B. C3H4
C. C4H6
D. C5H8
Câu13. Dẫn một ankin mạch hở vào bình chứa dung dịch AgNO3/NH3 (dư), thu được 2,205 gam kết tủa. Đồng thời, khối lượng bình chứa tăng lên 0,6 gam. Tên của ankin ban đầu là
A. axetilen. B. propin. C. but-1-in.
D. but-2-in.
Câu14. Dẫn một ankin mạch hở vào bình chứa dung dịch AgNO3/NH3 dư, thu được 1,932 gam kết tủa. Đồng thời, khối lượng bình chứa tăng lên 0,648 gam. Tên gọi của ankin ban đầu là
A. axetilen. B. propin. C. but-1-in.
D. but-2-in.
Câu15. Cho m gam ankin mạch hở X tác dụng với lượng dư dung dịch AgNO3/NH3 thu được 3,5 gam kết tủa vàng. Cũng m gam ankin này sục qua bình đựng dung dịch brom dư thì thấy dung dịch brom nhạt màu, khối lượng bình tăng 1,36 gam. Khi hiđro hóa hoàn toàn X với xúc tác Ni thu được một ankan phân nhánh. Ankin X là
A. 3-metylbut-1-in. B. pent-1-in.
C. propin. D. 4-metylhex-1-in. Hướngdẫngiải Khối lượng bình brom tăng là khối lượng của ankin.
3,51,361,36
Ankin X phân nhánh ⇒
CHCCH(CH):3metylbut1in. ≡−−−−
Dẫn V lít (ở đktc) hỗn hợp X gồm axetilen và hiđro đi qua ống sứ đự
bộ
niken nung nóng, thu được khí Y. Dẫn Y vào lượng dư AgNO3 trong dung dịch NH3 thu được 12 gam kết tủa. Khí đi ra khỏi dung dịch phản ứng vừa đủ với 16 gam brom và còn lại khí Z. Đốt cháy hoàn toàn khí Z thu được 2,24
ỌA
Câu1. Đốt cháy hoàn toàn hiđrocacbon mạch hở A thu được 6,16 lít CO2 (đktc) và 4,95 gam H2O. A có tỉ khối so với H2 là 28. Công thức phân tử của A là
A. C2H4. B. C3H6.
C. C4H8.
D. C5H10.
Câu2. Đốt cháy hoàn toàn hiđrocacbon B thu được 1,1 gam CO2 và 0,45 gam H2O. Tỉ khối hơi của B so với heli là 17,5. B có cấu trúc không phân nhánh, không có đồng phân hình học. Công thức cấu tạo của B là
A. CH3 CH=CH CH2CH3.
C. CH2=CH CH(CH3)2.
B. CH2=CH CH2CH2CH3.
D. CH2=C(CH3) CH2CH3.
Câu3. Đốt cháy hoàn toàn ankin X, sau đó dẫn hỗn hợp sản phẩm qua bình chứa dung dịch H2SO4
đặc thấy khối lượng bình tăng lên 0,216 gam và thoát ra một khí Y. Dẫn khí Y vào bình chứa dung dịch Ca(OH)2 dư thấy xuất hiện 2,4 gam kết tủa. Công thức phân tử của ankin X là
A. C2H2
H4 Câu4. Đốt cháy hoàn toàn ankin X cần vừa đủ 13,44 lít O2 (ở đktc). Sau phản ứng dẫn hỗn hợp sản phẩm vào bình đựng dung dịch nước vôi trong thì thu được 15 gam kết tủa trắng Y. Lọc tách kết tủa
Y, đun nóng dung dịch thì thu được tiếp 15 gam kết tủa trắng Y. Công thức phân tử của ankin X là
A. C2H2. B. C3H4. C. C4H6. D. C5H8.
Câu5.(A.07): Ba hiđrocacbon X, Y, Z kế tiếp nhau trong dãy đồng đẳng, trong đó khối lượng phân tử Z gấp đôi khối lượng phân tử X. Đốt cháy 0,1 mol chất Y, sản phẩm khí hấp thụ hoàn toàn vào dung dịch Ca(OH)2 (dư), thu được số gam kết tủa là
A. 30.
B. 10.
C. 40.
D. 20.
Câu6.(B.14): Đốt cháy hoàn toàn 0,2 mol hỗn hợp X gồm một ankan và một anken, thu được 0,35 mol CO2 và 0,4 mol H2O. Phần trăm số mol của anken trong X là
A. 40%. B. 50%.
C. 25%. D. 75%.
Câu7.(C.08): Đốt cháy hoàn toàn hỗn hợp M gồm một ankan X và một ankin Y, thu được số mol CO2 bằng số mol H2O. Thành phần phần trăm về số mol của X và Y trong hỗn hợp M lần lượt là:
A. 75% và 25%. B. 20% và 80%.
C. 35% và 65%.
D. 50% và 50%.
Câu8.(A.09): Hỗn hợp khí X gồm anken M và ankin N có cùng số nguyên tử cacbon trong phân
tử. Hỗn hợp X có khối lượng 12,4 gam và thể tích 6,72 lít (ở đktc). Số mol, công thức phân tử của M và N lần lượt là:
A. 0,1 mol C2H4 và 0,2 mol C2H2.
B. 0,2 mol C2H4 và 0,1 mol C2H2.
C. 0,1 mol C3H6 và 0,2 mol C3H4 D. 0,2 mol C3H6 và 0,1 mol C3H4
Câu9.(A.08): Hỗn hợp X có tỉ khối so với H2 là 21,2 gồm propan, propen và propin. Khi đốt cháy
hoàn toàn 0,1 mol X, tổng khối lượng của CO2 và H2O thu được là
A. 16,80 gam. B. 20,40 gam. C. 18,96 gam. D. 18,60 gam. Hướngdẫngiải
Gọi công thức chung của hỗn hợp X là C3Hx ⇒ MX = 12.3 + x = 21,2.2 ⇒ x = 6,4:
n3.0,10,3mol;n3,2.0,10,32molmm18,96gam.
+= Câu10.(C.13): Hỗn hợp khí X gồ
y ra hoàn toàn, thu được m gam kết tủa. Giá trị của m là
9,85. B. 5,91. C. 13,79. D. 7,88. Hướngdẫngiải
ọi công thức chung của X là
: Đố
PTỰ LUYỆN
Câu16. Đốt cháy hoàn toàn ankin X, sau đó dẫn hỗn hợp sản phẩm qua bình chứa dung dịch H2SO4 đặc thấy khối lượng bình tăng lên 0,378 gam và thoát ra một khí Y. Dẫn khí Y vào bình chứa dung dịch Ca(OH)2 dư thấy xuất hiện 4,2 gam kết tủa. Tên gọi của X là
A. axetilen. B. propin. C. but-1-in. D. pent-1-in.
Câu17. Đốt cháy hoàn toàn ankin B, sau đó dẫn hỗn hợp sản phẩm qua bình chứa dung dịch H2SO4 đặc thấy khối lượng bình tăng lên 1,62 gam và thoát ra một khí X. Dẫn khí X vào bình chứa dung dịch Ca(OH)2 dư thấy xuất hiện 12 gam kết tủa. Tên gọi của B là
A. axetilen. B. propin. C. but-1-in. D. pent-1-in.
Câu18. Đốt cháy hoàn toàn ankin X cần vừa đủ 2,464 lít O2 (ở đktc). Sau phản ứng dẫn hỗn hợp sản phẩm vào bình đựng dung dịch nước vôi trong thì thu được 6 gam kết tủa trắng Y. Lọc tách kết tủa Y, đun nóng dung dịch thì thu được tiếp 1 gam kết tủa trắng Y. Công thức phân tử của ankin X là
A. C2H2 B. C3H4
C. C4H6
D. C5H8
Câu19. Đốt cháy 0,035 mol hiđrocacbon mạch hở X thu được hỗn hợp CO2 và H2O. Dẫn hỗn hợp sản phẩm vào dung dịch nước vôi trong thấy xuất hiện 14 gam kết tủa và khối lượng bình tăng thêm
8,68 gam. X có đồng phân hình học. Công thức cấu tạo của X là
A. CH3 CH=CH CH3. B. CH2=CH CH2CH3.
C. CH3CH2 CH=CH CH2CH3
D. CH3 CH=CH CH2CH3
Câu20.(B.12): Đốt cháy hoàn toàn hỗn hợp X gồm hai hiđrocacbon (tỉ lệ số mol 1: 1) có công thức đơn giản nhất khác nhau, thu được 2,2 gam CO2 và 0,9 gam H2O. Các chất trong X là
A. một ankan và một ankin.
C. hai anken.
B. hai ankađien.
D. một anken và một ankin.
Câu21.(B.08): Đốt cháy hoàn toàn 1 lít hỗn hợp khí gồm C2H2 và hiđrocacbon X sinh ra 2 lít khí CO2 và 2 lít hơi H2O (các thể tích khí và hơi đo ở cùng điều kiện nhiệt độ, áp suất). Công thức phân tử của X là
Dẫn 1,68 lít hỗn hợp khí X gồm hai hiđrocacbon vào bình đựng dung dịch brom (dư). Sau khi phản ứng xảy ra hoàn toàn, có 4 gam brom đ
t cháy hoàn
2 2BrHCcßnl¹in2nCO 36n0,025molnanken:CH:0,025moln0,050,025n0,125n3:CH
Câu24.(C.08): Đốt cháy hoàn toàn 20,0 ml hỗn hợp X gồm C3H6, CH4, CO (thể tích CO gấp hai lần thể tích CH4), thu được 24,0 ml CO2 (các thể tích khí đo ở cùng điều kiện nhiệt độ và
n0,05molm0,125.440,1.187,3gam. n2n0,1mol
Câu26. Hỗn hợp khí A gồm axetilen, propin và but-2-in có tỉ khối hơi so với H2 là 21,4. Đốt cháy
hoàn toàn 3,36 lít hỗn hợp A (ở đktc) rồi dẫn toàn bộ sản phẩm cháy vào bình đựng dung dịch
Ca(OH)2 dư thì khối lượng kết tủa tạo thành là
A. 21,12 gam. B. 45 gam. C. 48 gam. D. 15 gam.
⇒ 32
CaCOCO CaCO nn3,2.0,150,48molm48gam. ===
Cho
(ở đktc). Giá trị của m
18 19 20 21 22 23 24 25 26 27 28 29 30
Câu1.(QG.18-202): Ở điều kiện thường, chất nào sau đây làm mất màu dung dịch Br2?
A. benzen. B. etilen. C. metan. D. butan.
Câu2.(QG.16): Trước những năm 50 của thế kỷ XX, công nghiệp tổng hợp hữu cơ dựa trên nguyên liệu chính là axetilen. Ngày nay, nhờ sự phát triển vượt bậc của công nghệ khai thác và chế biến dầu mỏ, etilen trở thành nguyên liệu rẻ tiền, tiện lợi hơn nhiều so với axetilen. Công thức phân tử của etilen là
A. C2H4. B. C2H6. C. CH4. D. C2H2.
Câu3.(MH.15). Ankin là những hiđrocacbon không no, mạch hở, có công thức chung là
A. CnH2n+2 (n ≥ 1).
C. CnH2n-2 (n ≥ 2).
B. CnH2n (n ≥ 2).
D. CnH2n-6 (n ≥ 6).
Câu4.(C.13): Số đồng phân cấu tạo, mạch hở ứng với công thức phân tử C4H6 là
A. 2. B. 5.
C. 4. D. 3.
Câu5.(QG.18-201): Chất nào sau đây tác dụng được với dung dịch AgNO3 trong NH3?
A. Etilen B. Metan C. Benzen D. Propin
Câu6.(QG.18-204): Sục khí axetilen vào dung dịch AgNO3 trong NH3 thu được kết tủa màu gì?
A. vàng nhạt. B. trẳng. C. đen. D. xanh.
Câu7.(B.14): Trong phân tử propen có số liên kết xich ma (σ) là
A. 7. B. 6. C. 8. D. 9.
Câu8.(C.10): Số liên tiếp σ (xích ma) có trong mỗi phân tử: etilen; axetilen; buta-1,3-đien lần lượt là
A. 3; 5; 9 B. 5; 3; 9 C. 4; 2; 6 D. 4; 3; 6
Câu9.(C.08): Công thức đơn giản nhất của một hiđrocacbon là CnH2n+1. Hiđrocacbon đó thuộc dãy đồng đẳng của
A. ankan. B. ankin. C. ankađien. D. anken.
Câu10. (C.10): Chất nào sau đây có đồng phân hình học?
A. But-2-in B. But-2-en C. 1,2-đicloetan D. 2-clopropen
Câu11.(QG.18-203): Chất nào sau đây không làm mất màu dung dịch Br2?
A. Axetilen. B. Propilen.
C. Etilen.
D. Metan.
Câu12.(A.14): Chất X có công thức: CH3-CH(CH3)-CH=CH2. Tên thay thế của X là
A. 3-metylbut-1-in.
C. 2-metylbut-3-en.
B. 3-metylbut-1-en.
D. 2-metylbut-3-in.
Câu13.(C.11): Chất nào sau đây có đồng phân hình học?
A. CH2=CH-CH=CH2
C. CH3-CH=C(CH3)2
B. CH3-CH=CH-CH=CH2
D. CH2=CH-CH2-CH3
Câu14.(B.13): Hiđrocacbon nào sau đây khi phản ứng với dung dịch brom thu được 1,2đibrombutan?
A. But-1-en. B. Butan.
C. Buta-1,3-đien. D. But-1-in.
Câu15.(A.07): Hiđrat hóa 2 anken chỉ tạo thành 2 ancol. Hai anken đó là:
A. eten và but-2-en.
C. propen và but-2-en.
B. 2-metylpropen và but-1-en.
D. eten và but-1-en.
Câu16.(B.13): Tên gọi của anken (sản phẩm chính) thu được khi đun nóng ancol có công thức (CH3)2CHCH(OH)CH3 với dung dịch H2SO4 đặc là
A. 3-metylbut-2-en.
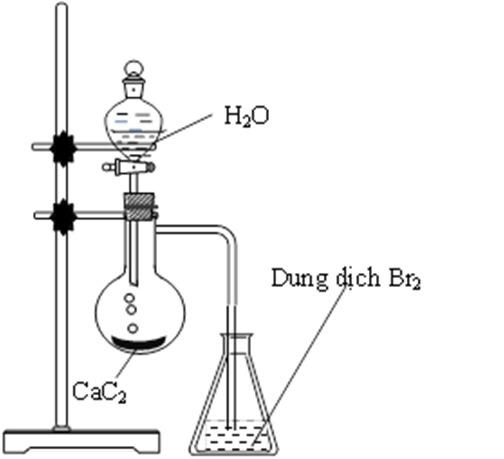
C. 2-metylbut-2-en.
B. 2-metylbut-1-en.
D. 3-metylbut-1-en.
Câu17.(B.14): Trùng hợp hiđrocacbon nào sau đây tạo ra polime dung để sản xuất cao su buna?
A. 2-metylbuta-1,3-đien. B. Penta-1,3-đien. C. But-2-en. D. Buta-1,3-đien.
Câu18.(B.07): Dãy gồm các chất được dùng để tổng hợp cao su Buna-S là:
A. CH2=C(CH3)-CH=CH2, C6H5CH=CH2.
C. CH2=CH-CH=CH2, CH3-CH=CH2.
B. CH2=CH-CH=CH2, C6H5CH=CH2.
D. CH2=CH-CH=CH2, lưu huỳnh.
Câu19.(B.08): Ba hiđrocacbon X, Y, Z là đồng đẳng kế tiếp, khối lượng phân tử của Z bằng 2 lần
khối lượng phân tử của X. Các chất X, Y, Z thuộc dãy đồng đẳng của
A. ankan.
B. ankađien.
C. anken. D. ankin.
Câu20.(A.11): Cho buta-1,3-đien phản ứng cộng với Br2 theo tỉ lệ mol 1:1. Số dẫn xuất đibrom (đồng phân cấu tạo và đồng phân hình học) thu được là
A. 2. B. 4. C. 3. D. 1.
Câu21. Dãy gồm các chất đều tác dụng với AgNO3 trong dung dịch NH3 là:
A. propin, axetilen, etilen. B. axetilen, vinylaxetilen, propin.
C. metan, but-1-in, etilen. D. etilen, axetilen, but-2-in.
Câu22. (C.13): Chất nào dưới đây khi phản ứng với HCl thu được sản phẩm chính là 2-clobutan?
A. But-1-en. B. Buta-1,3-đien. C. But-2-in. D. But-1-in. Câu23.(QG.15): Hỗn hợp X gồm 2 hiđrocacbon mạch hở, có thể là ankan, anken, ankin, ankadien. Đốt cháy hoàn toàn một lượng X, thu được CO2 và H2O có số mol bằng nhau, X không thể gồm
A. ankan và ankin B. ankan và ankađien C. hai anken D. ankan và anken
Câu24.(QG.18-201): Thực hiện thí nghiệm như hình vẽ dưới đây:
Hiện tượng xảy ra trong bình chứa dung dịch Br2 là
A. có kết tủa đen. B. dung dịch Br2 bị nhạt màu.
C. có kết tủa trắng.
D. có kết tủa vàng.
Câu25.(QG.18-202): Thực hiện thí nghiệm như hình vẽ bên. Kết thúc thí nghiệm, trong bình đựng dung dịch AgNO3 trong NH3 xuất hiện kết tủa màu vàng nhạt.
Chất X là
A. CaO. B. Al4C3.
C. CaC2.
D. Ca.
Câu26. (C.09): Cho các chất: CH2=CH–CH=CH2; CH3–CH2–CH=C(CH3)2; CH3–CH=CH–CH=CH2; CH3 – CH =CH2; CH3–CH=CH–COOH. Số chất có đồng phân hình học là
A. 1. B. 3.
C. 4
D. 2.
Câu27. Cho các chất: metan, propen, axetilen, vinylaxetilen và isopren. Trong các chất trên, số chất phản ứng đuợc với dung dịch brom là
A. 4. B. 3.
C. 5.
D. 2.
Câu28. (C.13): Cho các chất: but-1-en, but-1-in, buta-1,3-đien, vinylaxetilen, isobutilen, anlen. Có bao nhiêu chất trong số các chất trên khi phản ứng hoàn toàn với khí H2 dư (xúc tác Ni, đun nóng) tạo ra butan?
A. 6. B. 5.
C. 4.
D. 3.
Câu29.(A.12): Hiđro hóa hoàn toàn hiđrocacbon mạch hở X thu được isopentan. Số công thức cấu tạo có thể có của X là
A. 6. B. 7.
C. 4.
Hướngdẫngiải X phải là hiđrocacbon không no và có mạch giống isopentan
(1) CH2=C(CH3) – CH2 – CH2

(2) (CH3)2 – C=CH-CH3
(3) (CH3)2 – CH – CH=CH2
(4) CH2=C(CH3) – CH=CH2
(5) (CH3)2 – C = C = CH2
(6) CH2=C(CH3) – C≡CH
(7) (CH3)2 – CH – C≡CH
D. 5.
Câu30.(QG.16): Cho 3 hiđrocacbon mạch hở X, Y, Z (MX < MY < MZ < 62) có cùng số nguyên
tử cacbon trong phân tử, đều phản ứng với dung dịch AgNO3 trong NH3 dư.
Trong các phát biểu sau:
(a) 1 mol X phản ứng tối đa 4 mol H2 (Ni, t0)
(b) Chất Z có đồng phân hình học.
(c) Chất Y có tên gọi là but-1-in.
(d) Ba chất X, Y, Z đều có mạch cacbon không phân nhánh.
Số phát biểu đúng là
gồm: a, d.
X: C4H2: CH≡C – C≡CH
Y: C4H4: CH≡C – CH=CH2
Z: C4H6: CH≡C – CH2 – CH3
(b) Sai vì Z không có đồng phân hình học.
(c) Sai vì Z mới là but – 1 – in.


CĐ1: Benzen và đồng đẳng. Một số hiđrocacbon thơm khác
CĐ2: Tổng ôn hiđrocacbon thơm
CĐ3: Hệ thống hóa về hiđrocacbon
MỘT SỐ HIĐROCACBON THƠM KHÁC
KIẾNTHỨCCẦNNHỚ
Hiđrocacbon thơm (Aren) là những HC trong phân tử có chứa một hay nhiều vòng benzen.
A.Benzenvàankylbenzen
1.Cấutạo, đồng đẳng, đồngphân,danhpháp
- Cấu tạo: Trong phân tử benzen cả 6 nguyên tử C và H đều nằm trên 1 mặt phẳng. 6 nguyên tử C liên kết với nhau bằng 3 liên kết đôi xen kẽ 3 liên kết đơn tạo thành hình lục giác đều.
- Công thức chung: CnH2n-6 (n ≥ 6).
- Đồng phân: ĐP về vị trí tương đối các nhóm ankyl và ĐP mạch cacbon của mạch nhánh.
- Danh pháp: Tên IUPAC = VT nhánh + tên nhánh + benzen
2.Tínhchấtvậtlí
- Các HC thơm là những chất lỏng hoặc rắn ở điều kiện thường, không màu, có mùi đặc trưng, không tan trong nước, tan trong các dung môi hữu cơ không phân cực.
- Nhiệt độ nóng chảy tăng theo chiều tăng của phân tử khối.
3.Tínhchấthóahọc
(a) Phản ứng thế Cl2, Br2 (Fe, to)
(b) Phản ứng với HNO3/H2SO4 đặc (thế -NO2)
Quitắcthế: Khi vòng benzen có sẵn nhóm thế đẩy e: CnH2n+1-, -OH, -NH2 hoặc -Cl, -Br,… thì ưu tiên thế vào vị trí o, p. Ngược lại, nếu vòng benzen có nhóm thế hút e: -NO2, -COOH, … thì ưu tiên thế vào vị trí m.
(c) Phản ứng cộng H2 (Ni, to); cộng Cl2.
(d) Phản ứng oxi hóa
- Đồng đẳng của benzen có khả năng làm mất màu dung dịch KMnO4 khi đun nóng (benzen không có tính chất này).
- PƯ cháy: CnH2n-6 + 3n3 2 O2 ot → nCO2 + (n - 3)H2O
4. Điềuchế
- Tách H2 từ ankan tương ứng: CnH2n+2
- Riêng etylbenzen: C6H6 + CH2=CH2
1.Stiren(C8H8:C6H5CH=CH2)
xt,t
C6H5CH2CH3
- Là chất lỏng, không màu, nhẹ hơn nước và không tan trong nước.
- Có tính không no và tính thơm: Tham gia PƯ cộng H2, cộng Br2, trùng hợp, bị oxi hóa bởi KMnO4.
2.Naphtalen(C10H8)
- Là chất rắn, màu trắng, dễ thăng hoa, còn gọi là băng phiến.
- Có tính thơm: Tham gia phản ứng thế với Br2, HNO3/H2SO4 đặc; phản ứng cộng H2 (Ni, to)
BÀITẬPTỰ LUẬN
Câu1: Viết đồng phân và gọi tên ankyl benzen: C8H10, C9H12.
C8H10
(1)etylbenzen
(2)o- đimetylbenzen
(3)m- đimetylbenzen
(4)p- đimetylbenzen
(1)propylbenzen
(2)isopropylbenzen
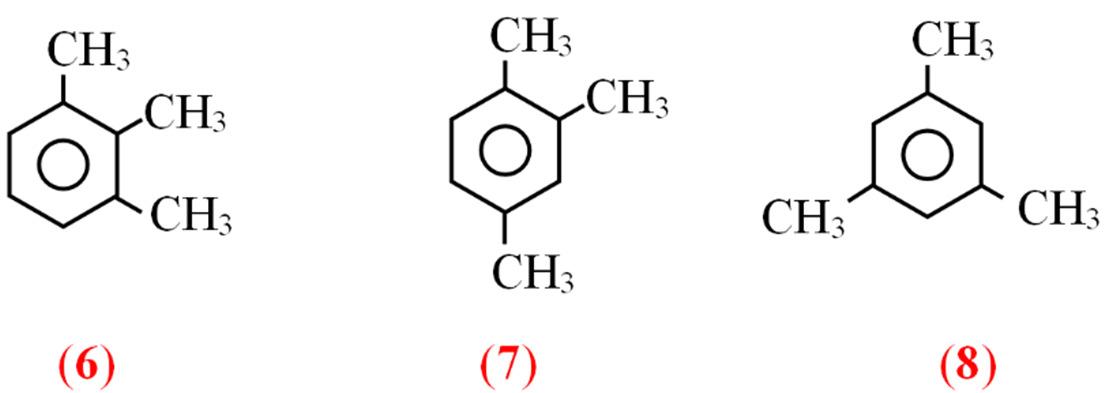
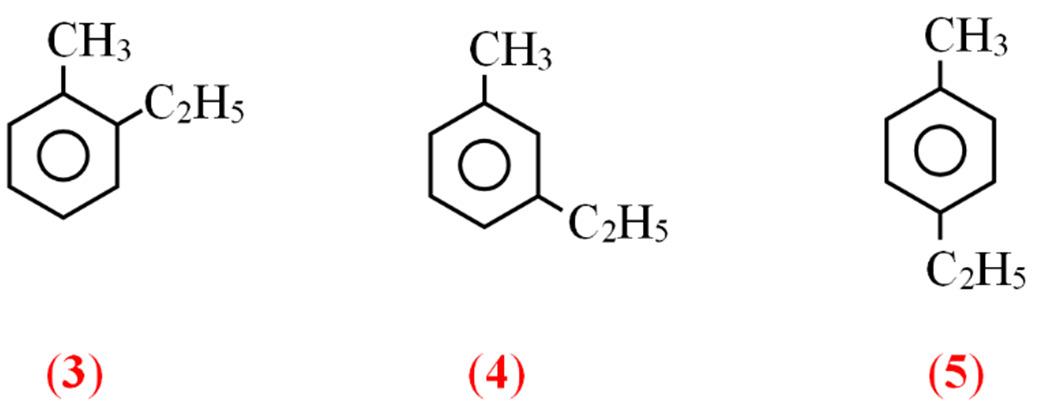
C9H12
(3)o–etylmetylbenzen
(4)m–etylmetylbenzen
(5)p-etylmetylbenzen
(6)1,2,3–trimeylbenzen
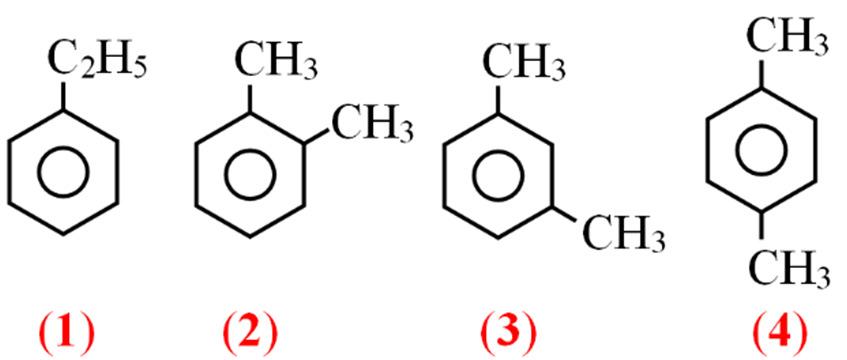
(7)1,2,4–trimeylbenzen
(8)1,3,5–trimeylbenzen
Câu2: Viết phương trình hóa học ứng với các trường hợp sau:
(a) Cho benzen tác dụng với Br2 (Fe, to)
C6H6 +Br2 oFe,t → C6H5Br+HBr
(b) Cho toluen tác dụng với Br2 (askt)
C6H5CH3 +Br2 as → C6H5CH2Br+HBr
(c) Cho toluen tác dụng với HNO3/H2SO4 (tỉ lệ mol 1 : 1). Xác định sản phẩm chính.
(d) Cho benzen, stiren, naphtalen tác dụng với H2 (Ni, to)
C6H6 +3H2 o Ni,t → C6H12
C6H5-CH=CH2 +4H2 o Ni,t → C6H11-CH2-CH3
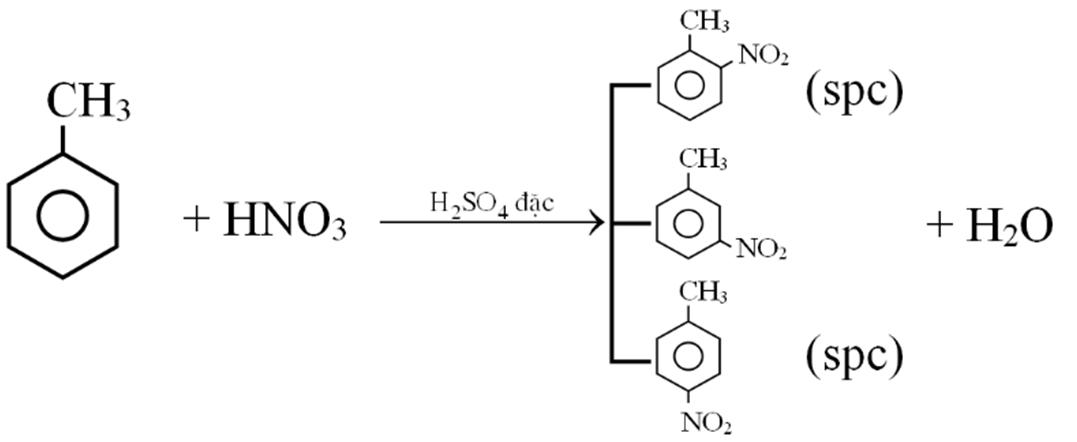

C10H8 +5H2 o Ni,t → C10H18
(e) Trùng hợp stiren.
(g) Cho toluen tác dụng với dung dịch KMnO4, đun nóng.
Ề HIĐROCACBONTHƠM
I -
ng đẳng: CnH2n-6 + 3n3 2 O2 ot → nCO2 + (n - 3)H2O
- Phản ứng cộng brom của stiren: C6H5CH=CH2 + Br2 → C6H5CHBr-CH2Br
VÍDỤ MINHHỌA
Câu4. Xác định công thức phân tử, viết các đồng phân (nếu có) và gọi tên X trong các trường hợp sau:
(a) Ankylbenzen X có tỉ khối hơi so với hiđro bằng 46.
(b) Ankylbenzen X có phần trăm khối lượng cacbon bằng 90,57%.
(c) Brom hóa hiđrocacbon X thuộc dãy đồng đẳng của benzen thu được dẫn xuất monobrom trong đó brom chiếm 50,96% về khối lượng.
(d) Đốt cháy một hiđrocacbon X thuộc dãy đồng đẳng của benzen bằng oxi dư, sau phản ứng thu được 15,68 lít khí CO2 (ở đktc) và 7,2 gam H2O. (a) (b)
C7H8
C8H10
C6H6
C7H8
Câu5. Đốt cháy hết 9,18 gam 2 hiđrocacbon kế tiếp thuộc dãy đồng đẳng của benzen A, B thu được H2O và 30,36 gam CO2. Xác định công thức phân tử của A và B.
Đápsố:C8H10 vàC9H12
Câu6. Đốt cháy hoàn toàn hỗn hợp gồm một ankan và một ankylbenzen thấy số mol CO2 thu được bằng số mol nước. Phần trăm thể tích ankan trong hỗn hợp là
A. 75% B. 25% C. 33,33% D. 66,67%
Câu7. Cho m gam stiren tác dụng vừa đủ với 32 gam Br2 thu được x gam dẫn xuất đibrom. Giá trị của m và x lần lượt là:
A. 20,8 và 52,8.
B. 10,4 và 42,4.
C. 41,6 và 73,6.
D. 15,6 và 47,6.
Câu8. Cho 13 gam hỗn hợp gồm benzen và stiren làm mất màu vừa đủ dung dịch chứa 8 gam brom. Tỉ lệ mol benzen và stiren trong hỗn hợp ban đầu là
A. 1: 1. B. 1: 2.
C. 2: 1.
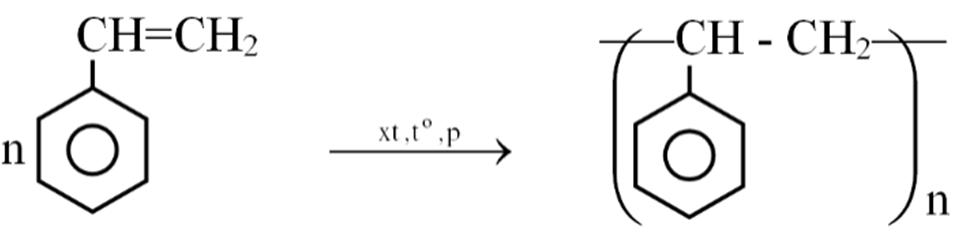
D. 2: 3.
Câu9. Hiđro hoá hoàn toàn 12,64 gam hỗn hợp etylbenzen và stiren cần 8,96 lít H2 (đktc). Thành phần
Câu10. Người ta điều chế
của x là
A. 1,5. B. 1. C. 1,3. D. 1,2.
Câu13. Đốt cháy hoàn toàn m gam một ankylbenzen (X) thu được 0,35 mol CO2 và 0,2 mol H2O. Giá trị m và công thức phân tử của X lần lượt là:
A. 4,6 và C7H8. B. 4,6 và C8H8. C. 4,4 và C8H8.
D. 4,4 và C7H8.
Câu14. Đốt cháy hoàn toàn 0,02 mol một hiđrocacbon (X) là đồng đẳng của benzen thu được 7,04 gam CO2. X có công thức phân tử là
A. C6H6. B. C7H8. C. C8H10. D. C8H8.
Câu15. Đốt cháy hoàn toàn m gam hỗn hợp benzen và toluen được 0,65 mol CO2 và 0,35 mol H2O. Thành phần phần trăm về số mol của benzen là
A. 40%. B. 25%. C. 50%. D. 35%.
6H6 và C2H2. D. C2H2 và C4H4. Hướngdẫngiải 22 2 CCOHOHHOCHn nn0,01mol;n0,005moln2n0,01moln:n1:1A,B:(CH) ===
M2613nn2CH M3.267813nn6:CH
===
COHOCHxxy 449 n:n:2:1n:n1:1A:CHO 4418 == = ot xxy222 CHO(1,25x0,5y)OxCO0,5xHO +−→+
bài ⇒ §¸p¸n 88 x2y0(lo¹i) 1,25x0,5y10 x8,y0CH = < −=→
=
monobrom duy nhất. Tên của X là
A. Toluen. B. 1,3,5-trimetyl benzen.
Hướ
ngd
ngi
V
ất
Câu1. Số nguyên tử cacbon và hiđro trong benzen l
A. 12 và 6.
B. 6 và 6.
t là:
C. 6 và 12.
C. 6 và 14.
Câu2. Khi thay các nguyên tử hiđro trong phân tử benzen bằng nhóm ankyl thì thu được
A. toluen. B. ankylbenzen.
C. phenol.
D. axit benzoic.
Câu3. Các ankylbenzen hợp thành dãy đồng đẳng của benzen có công thức chung là
A. CnH2n-6 (n ≥ 2).
C. CnH2n-2 (n ≥ 2).
Câu4. Số liên kết đôi trong phân tử ankylbenzen là
A. 1. B. 2.
Câu5. Hợp chất nào sau đây không tồn tại?
B. CnH2n+2 (n ≥ 6).
D. CnH2n-6 (n ≥ 6).
C. 3.
D. 4.
A. B. C.
Câu6. Cho hai hiđrocacbon thơm có cùng công thức phân tử C9H12:
Hai hợp chất trên là
A. Đồng phân không gian.
B. Đồng phân vị trí nhóm thế trong vòng benzen.
C. Đồng phân mạch cacbon.
D. Đồng phân vị trí liên kết đôi.
Câu7. Cho ba đồng phân của hiđrocacbon thơm có hai nhóm thế A, B như sau: A
D.
Phát biểu nào sau đây không đúng?
A. (2) là đồng phân meta.
C. (3) là đồng phân para.
B. (1) là đồng phân ortho.
D. (1), (2), (3) là đồng phân không gian.
Câu8. Gốc C6H5-CH2- và gốc C6H5- có tên gọi lần lượt là:
A. phenyl và benzyl.
C. anlyl và Vinyl.
B. vinyl và anlyl.
D. benzyl và phenyl.
Câu9. Công thức của toluen (hay metylbenzen) là
A. B.
Câu10. Công thức của etylbenzen là
A. B.
Câu11. Công thức của cumen (isopropylbenzen) là
A. B.
Câu12. Hiđrocacbon X có công thức cấu tạo như sau:
C.
D.
C.
D.
C.
D.
Tên gọi của X là
A. đimetylbenzen.
C. m-đimetylbenzen.
Câu13. Hiđrocacbon Y có công thức cấu tạo như sau:
Tên gọi của Y là
A. etylbenzen.
C. o-đietylbenzen.
Câu14. Công thức cấu tạo thu gọn của toluen là
A. C6H5 CH3.
C. C6H5 CH=CH2.
Câu15. Công thức cấu tạo thu gọn của cumen là
A. C6H4(C2H5)2
C. C6H4(CH3)2
Câu16. Xilen là tên thường gọi của chất nào dưới đây?
B. o-đietylbenzen.
D. m-đietylbenzen.
B. m-đietylbenzen.
D. p-đietylbenzen.
B. C6H5 CH2CH3.
D. C6H5 CH(CH3)2.
B. C6H5 CH2CH2CH3
D. C6H5 CH(CH3)2
A. metylbenzen. B. isopropylbenzen. C. đimetylbenzen. D. etylbenzen.
Câu17. Hợp chất nào sau đây là m-xilen?
A. B.
Câu18. Công thức cấu tạo thu gọn của p-xilen là
A. p-CH3 C6H4 CH3
C. p-CH3 C6H4 C2H5
C. D.
B. m-CH3 C6H4 CH3
D. p- C2H5 C6H4 C2H5
Câu19. Benzen không làm mấy màu dung dịch nước brom nhưng có thể phản ứng với brom khan khi có mặt xúc tác bột sắt. Phản ứng này thuộc loại phản ứng nào?
A. Phản ứng thế.
C. Phản ứng tách.
B. Phản ứng cộng.
D. Phản ứng đốt cháy.
Câu20. Khi được chiếu sáng, benzen có thể phản ứng với clo tạo thành sản phẩm nào?
A. C6H5Cl.
B. C6H11Cl.
C. C6H6Cl6.
D. C6H12Cl6.
Câu21. Khi đun nóng với xúc tác Ni hoặc Pt, benzen và ankylbenzen có khả năng cộng hiđro tạo thành hợp chất nào dưới đây?
A. anken. B. xicloankan. C. ankan. D. xiclohexan. Câu22(C.14): Chất nào sau đây làm mất màu dung dịch KMnO4 ở điều kiện thường?
A. Benzen. B. Metan. C. Toluen. D. Axetilen.
Câu23. Tính chất nào không phải của benzen?
A. Tác dụng với Br2 (to, Fe).
C. Tác dụng với dung dịch KMnO4.
2.Mức độ thônghiểu(thônghiểu)
B. Tác dụng với HNO3 (đ) /H2SO4(đ).
D. Tác dụng với Cl2 (as).
Câu24. Ứng với công thức phân tử C7H8 có số đồng phân thơm là
A. 1. B. 2.
C. 3.
D. 4.
Câu25.(A.08): Số đồng phân hiđrocacbon thơm ứng với công thức phân tử C8H10 là
A. 2. B. 4.
C. 3.
Câu26. Số hiđrocacbon thơm có cùng công thức phân tử C9H12 là
A. 7 B. 9 C. 5
Câu27. Hợp chất X có công thức cấu tạo như sau:
Tên gọi của X là
D. 5.
D. 8
A. m-clotoluen. B. clobenzen. C. p-clotoluen. D. o-clotoluen.
Câu28. Hợp chất Y có công thức cấu tạo như sau:
Tên gọi của Y là
A. nitrobenzen. B. m-nitrobenzen. C. p-nitronbenzen. D. m-nitrotoluen.
Câu29. Hợp chất Z có công thức cấu tạo như sau:
Tên gọi của Z là
A. 1,3,5-nitrobenzen. B. 1,3,5-trinitrotoluen.
C. 2,4,6-trinitrotoluen. D. 1,3,5-trinitrobenzen.
Câu30. (C.11): Chất X tác dụng với benzen (xt, t°) tạo thành etylbenzen. Chất X là
A. C2H4. B. C2H2.
C. CH4. D. C2H6.
Câu31. Xét các chất: (a) toluen; (b) o-xilen; (c) etylbenzen; (d) m-đimetylbenzen; (e) stiren. Đồng đẳng của benzen là:
A. (a), (d).
C. (a), (b), (c), (d).
B. (a), (e).
D. (a), (b), (c), (e).
Câu32. Hiđrocacbon nào sau đây không phải ankylbenzen?
A. B.
C.
D.
C8H8. Trong phân tử stiren có bốn liên kết đôi. Stiren là chất nào sau đây?
Câu33. Stiren là một hiđrocacbon thơm có công thức phân tử
A.
B.
C. D.
Câu34. Khi vòng benzen chứa sẵn nhóm thế nào sau đây thì sản phẩm thế ưu tiên vào vị trí –o, –p?
A. –NO2 B. –COOH.
C. –CH3 D. –SO3H.
Câu35. Dãy các nhóm thế khi gắn vào vòng benzen thì sản phẩm thế ưu tiên vào vị trí –o, –p là
A. –CH3, –COOH, –COOCH3.
C. –CH3, –OH, –NH2.
B. –NO2, –Cl, –NH2.
D. –Cl, –SO3H, –COOH.
Câu36. Dãy các nhóm thế khi gắn vào vòng benzen thì sản phẩm thế ưu tiên vào vị trí –m là
A. –CH3, –C2H5, –OH.
C. –SO3H, –CHO, –COOH.
B. –NO2, –CH3, –COOH.
D. –OH, –NH2, –Cl.
Câu37. Phản ứng sau có thể tạo thành tối đa bao nhiêu sản phẩm thế?
A. 1. B. 2.
C6H5 CH3 + Br2 tØlÖ mol 1:1 Fe →
C. 3. D. 4.
Câu38. Đun nóng toluen với brom khan, xúc tác Fe, sản phẩm chính được tạo thành là
A. o- và m-bromtoluen.
C. o- và p-bromtoluen.
B. o-bromtoluen.
D. m-toluen.
Câu39.(C.11): Sản phẩm chủ yếu trong hỗn hợp thu được khi cho toluen phản ứng với brom theo tỉ lệ số mol 1:1 (có mặt bột sắt) là
A. p-bromtoluen và m-bromtoluen.
C. o-bromtoluen và p-bromtoluen.
B. benzyl bromua.
D. o-bromtoluen và m-bromtoluen.
Câu40. So với benzen, khả năng phản ứng của toluen với dung dịch HNO3(đ)/H2SO4 (đ) như thế nào?
A. Dễ hơn, tạo ra o – nitro toluen và p – nitro toluen.
B. Khó hơn, tạo ra o – nitro toluen và p – nitro toluen.
C. Dễ hơn, tạo ra o – nitro toluen và m – nitro toluen.
D. Dễ hơn, tạo ra m – nitro toluen và p – nitro toluen.
Câu41. Tiến hành thí nghiệm cho nitro benzen tác dụng với HNO3 (đ)/H2SO4 (đ), nóng ta thấy:
A. Không có phản ứng xảy ra.
B. Phản ứng dễ hơn benzen, ưu tiên vị trí meta.
C. Phản ứng khó hơn benzen, ưu tiên vị trí meta.
D. Phản ứng khó hơn benzen, ưu tiên vị trí ortho.
Câu42. Cho phản ứng hóa học sau: C6H5 COOH + Br2 tØlÖ mol 1:1 Fe →
Sản phẩm chính tạo thành là
A. m-Br C6H4 COOH.
C. p-Br C6H4 COOH.
B. o-Br C6H4 COOH.
D. m-Br C6H4 Br.
Câu43. Nếu đun nóng ankylbenzen với Br2 không có xúc tác Fe mà chiếu sáng thì xảy ra phản ứng nào?
A. thế ở vòng benzen. B. cộng ở nhánh. C. tách ở nhánh. D. thế ở nhánh.
Câu44. Cho phản ứng hóa học sau: C6H5 CH3 + Br2 tØlÖmol 1:1 chiÕu s¸ng
Sản phẩm chính tạo thành là
A. m-bromtoluen. B. o-bromtoluen. C. benzyl bromua. D. p-bromtoluen.
Câu45. Phát biểu nào sau đây không đúng?
A. Benzen và ankylbenzen là chất lỏng không màu, hầu như không tan trong nước.
B. Benzen có khả năng hòa tan nhiều đơn chất và hợp chất như brom, iot, cao su.
C. Các hiđrocacbon thơm còn được gọi là aren.
D. Công thức chung của benzen và ankylbenzen là CnH2n-6 (n ≥ 2)
Câu46. Phát biểu nào sau đây không đúng?
A. Các aren đều là những chất có mùi.
B. Các aren đều là những chất gây hại cho sức khỏe.
C. Do có nhiều liên kết đôi trong phân tử nên benzen cũng thuộc nhóm anken.
D. Benzen và toluen thường dùng làm dung môi hữu cơ. Câu47. Phát biểu nào sau đây không đúng?
A. Khi cho benzen hoặc ankylbenzen tác dụng với hỗn hợp HNO3 và H2SO4 đậm đặc thì xảy ra phản ứng thế nitro vào vòng benzen.
B. Phản ứng thế nitro không tuân theo các quy tắc thế ở vòng benzen.
C. Đun nóng m-nitrotoluen với hỗn hợp HNO3 và H2SO4 đậm đặc (tỉ lệ mol 1:1) thì tạo ra sản phẩm thế m-đinitrobenzen.
D. Toluen tham gia phản ứng thế nitro dễ dàng hơn benzen. Câu48. Phát biểu nào sau đây không đúng?
A. Benzen không làm mất màu dung dịch KMnO4
B. Khi đun nóng, các ankylbenzen phản ứng với KMnO4 theo sơ đồ sau:
C. Các aren có thể bị đốt cháy hoàn toàn tạo thành CO2 và H2O, phản ứng tỏa nhiều nhiệt.
D. Benzen dễ tham gia phản ứng cộng, khó tham gia phản ứng thế Câu49. Cho sơ đồ phản ứng sau: C6H5 CH2CH3 42 o KMnO,HO HCl t X Y →→
X và Y đều là các sản phẩm hữu cơ. Công thức cấu tạo thu gọn của X, Y lần lượt là:
A. C6H5 COOH, C6H5 COOK.
C. C6H5 COOK, C6H5 COOH.
B. C6H5 CH2COOK, C6H5 CH2COOH.
D. C6H5 CH2COOH, C6H5 CH2COOK.
Câu50. Cho sơ đồ phản ứng sau: C6H5 CH(CH3)2 42 o
KMnO,HO HCl t X Y →→
X và Y đều là các sản phẩm hữu cơ. Công thức cấu tạo thu gọn của X là
A. C6H5 CH(COOH)2.
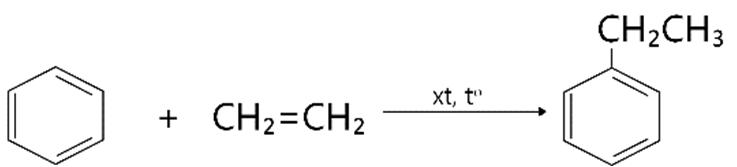
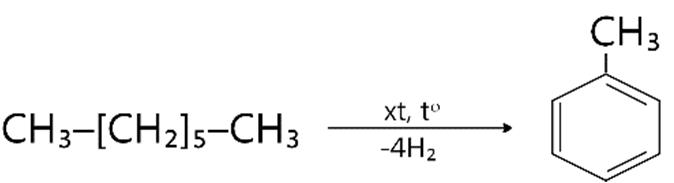

C. C6H5 COOK.
B. C6H5 COOH.
D. C6H5 CH(COOK)2.
Câu51. Thuốc nổ TNT (trinitrotoluen) được điều chế từ phản ứng giữa toluen vớ
mol 1:3. Công thức cấu tạo của TNT là
Câu52. Phát biểu nào sau đây không đúng?
A. Các aren như benzen, toluen, xilen thường tách được bằng cách chưng cất dầu mỏ và nhựa than đá.
B. Từ ankan hoặc xicloankan có thể điều chế được aren, ví dụ như phản ứng sau:
C. Etylbenzen có thể được điều chế từ phản ứng giữa benzen với etilen:
D. Benzen và toluen có mùi thơm dễ chịu, rất tốt cho sức khỏe con người. Câu53. Có thể dùng chất nào sau đây để phân biệt etylbenzen và stiren?
A. H2/Ni, t0 . B. KMnO4/t0 . C. Dung dịch Br2. D. Cl2/Fe,t0 .
Câu54. Dung dịch brom có thể phân biệt cặp chất nào sau đây?
A. eten và propen.
C. metan và propan.
B. etilen và stiren.
D. toluen và stiren.
Câu55. Nếu phân biệt các hiđrocacbon thơm: benzen, toluen và stiren chỉ bằng một thuốc thử thì nên chọn thuốc thử nào dưới đây?
A. dung dịch KMnO4.
C. dung dịch HCl.
B. dung dịch Br2.
D. dung dịch NaOH.
Câu56. Dãy nào sau đây không phân biệt được từng chất khi chỉ có dung dịch KMnO4?
A. benzen, toluen và stiren.
C. benzen, toluen và hexen.
3.Mức độ vậndụng(khá)
B. benzen, etylbenzen và phenylaxetilen.
D. benzen, toluen và hexan.
Câu57. Chất nào sau đây không thể chứa vòng benzen?
C6H8: 2.628 k3 2 +− == : vòng benzen có k = 4
Chú ý: Điều kiện một chất có vòng benzen là k ≥ 4.
Câu58. Chất nào sau đây có thể chứa vòng benzen?
không thể chứa còng benzen.
A. C10H16 B. C9H14BrCl. C. C8H6Cl2
Hướngdẫngiải
C8H6Cl2: 2.8262 k5 2 +−− == ⇒ có thể chứa vòng bezen.
C7H12
Câu59. A là đồng đẳng của benzen có công thức nguyên là: (C3H4)n. Công thức phân tử của A là
A. C3H4 B. C6H8 C. C9H12 D. C12H16
Hướngdẫngiải
A: (C3H4)n = C3nH4n ⇒ 4n = 2.3n – 6 ⇒ n = 3: C9H12.
Câu60. Cho các hợp chất sau: C6H5 COOH (X); C6H5 CH3 (Y); C6H5 CH(CH3)2 (Z); C6H5 NO2 (T); C6H5 NH2 (U). Những hợp chất nào khi phản ứng với HNO3/H2SO4 (đặc, nóng) thì tạo ra sản phẩm thế ở
vị trí meta?
A. X, T, U. B. Y, Z, U. C. X, T. D. Y, Z.
Hướngdẫngiải Các hợp chất có nhóm thế hút e sẽ thế ưu tiên vào vị trí meta ⇒ X, T. Câu61. Ở điều kiện thích hợp (nhiệt độ, áp suất, chất xúc tác), benzen tác dụng được với tất cả các chất trong dãy nào dưới đây?
A. HCl, HNO3, Cl2, H2
C. HNO3, Cl2, KMnO4, Br2
A loại HCl; B loại H2O; C loại KMnO4
B. HNO3, H2, Cl2, H2O.
D. HNO3, H2, Cl2, O2
Hướngdẫngiải
Câu62. Xét phản ứng: C6H5CH3+ KMnO4 0t → C6H5COOK+ MnO2↓+KOH+H2O.
Tổng hệ số (nguyên, tối giản) các chất trong phương trình trên là
A. 10. B. 9.
C. 12. D. 8.
Hướngdẫngiải
C6H5CH3 + 2KMnO4 0t → C6H5COOK+ 2MnO2↓ + KOH + H2O
⇒ Tổng hệ số = 1 + 2 + 1 + 2 + 1 + 1 = 8.
Câu63.(B.11): Cho phản ứng:
Tổng hệ số (nguyên, tối giản)
A. cumen.
C. 1,3,5-trimetylbenzen
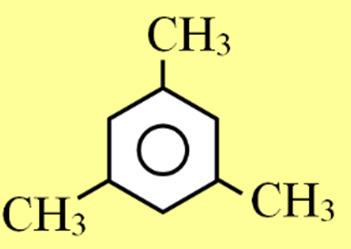
B. propylbenzen.
D. 1-etyl-3-metylbenzen H
: 1, 3, 5 - trimetylbenzen
1. Công thức chung của benzen và đồng đẳng:
2. Trong phân tử benzen cả 6 nguyên tử C và
bằng 3 liên kết đôi xen
3. Khi vòng benzen có sẵn nhóm thế ở vị trí số 1 ⇒ vị trí ortho (2, 6); vị trí para (4); vị trí meta (3, 5)
4. Toluen: C6H5-CH3; xilen: CH3-C6H4-CH3; cumen: (CH3)2CHC6H4; stiren: C6H5CH=CH2; trinitro toluen (TNT): CH3C6H2(NO2)3; naphtalen (băng phiến): C10H8.
5. Tính thơm: Dễ thế, khó cộng và bền với các chất oxi hóa.
6. Khi thế Cl2, Br2 điều kiện Fe, to ⇒ thế vào vòng benzen; điều kiện as ⇒ thế vào nhánh ankyl.
7. Qui tắc thế: Khi vòng benzen có sẵn nhóm thế đẩy e: CnH2n+1-, -OH, -NH2 hoặc -Cl, -Br, … thì
ưu tiên thế vào vị trí o, p. Ngược lại, nếu vòng benzen có nhóm thế hút e: -NO2, -COOH, … thì ưu tiên thế vào vị trí m.
8. Ankyl benzen có khả năng làm mất màu dung dịch KMnO4 khi đun nóng, benzen không có phản ứng này ⇒ Thuốc thử nhận biết.
9. Stiren vừa có vòng benzen, vừa có liên kết đôi C=C ⇒ Stiren có tính thơm và tính không no.
10. Một số phản ứng đặc biệt: 3C2H2 o C,600C → C6H6 (benzen)
C6H6 + 3Cl2 as → C6H6Cl6 (thuốc trừ sâu 6, 6, 6)
C6H5CH3 + 2KMnO4 ot → C6H5COOK + 2MnO2 + KOH+ H2O
1. Công thức chung của benzen và đồng đẳng là CnH2n-6 (n ≥ 6).
2. Trong phân tử benzen cả 6C và 6H đềunằmtrên một mặt phẳng, 6 nguyên tử C liên kết với nhau bằng 3liênkết đôi xen kẽ 3liênkết đơn tạo thành hình lục giác đều.
3. Khi vòng benzen có sẵn nhóm thế đẩy e: CnH2n+1-, -OH, -NH2 hoặc -Cl, -Br, … thì ưu tiên thế vào vị trí o,p. Ngược lại, nếu vòng benzen có nhóm thế hút e: -NO2, -COOH,… thì ưu tiên thế vào vị trí m.
4. Hoàn thành bảng sau:
(1) Benzen
(2) Toluen (metyl benzen)
(3) Etyl benzen
(4) p – Xilen
(1,4 – đimetyl benzen)
(5) Cumen (isopropyl benzen)
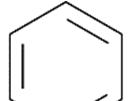
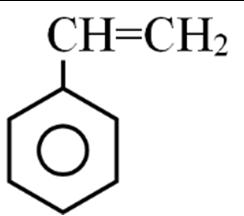
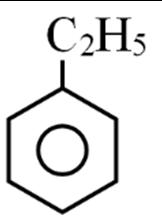
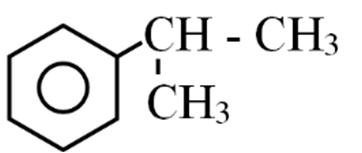
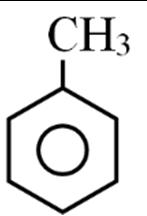
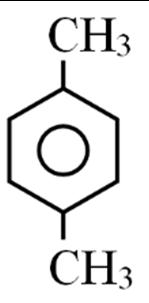
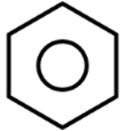
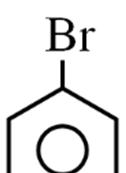
(6) Stiren (vinyl benzen)
- Những chất tác dụng với H2 (Ni, to): (1),(2),(3),(4),(5),(6)
- Những chất làm mất màu dung dịch Br2: (6)
- Những chất làm mất màu dung dịch KMnO4 (ở nhiệt độ thường): (6)
- Những chất làm mất màu dung dịch KMnO4 (to): (2),(3),(4),(5)
- Những chất tham gia phản ứng trùng hợp tạo polime: (6)
Câu1. Gốc C6H5-CH2- và gốc C6H5- có tên gọi lần lượt là:
A. phenyl và benzyl. B. vinyl và anlyl. C. anlyl và Vinyl. D. benzyl và phenyl. Câu2. (CH3)2CHC6H5 có tên gọi là
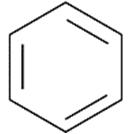
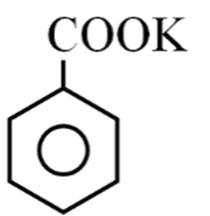
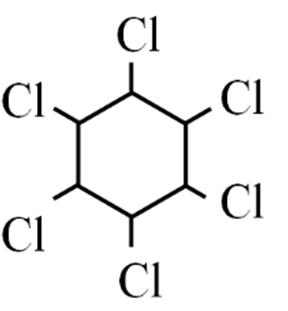
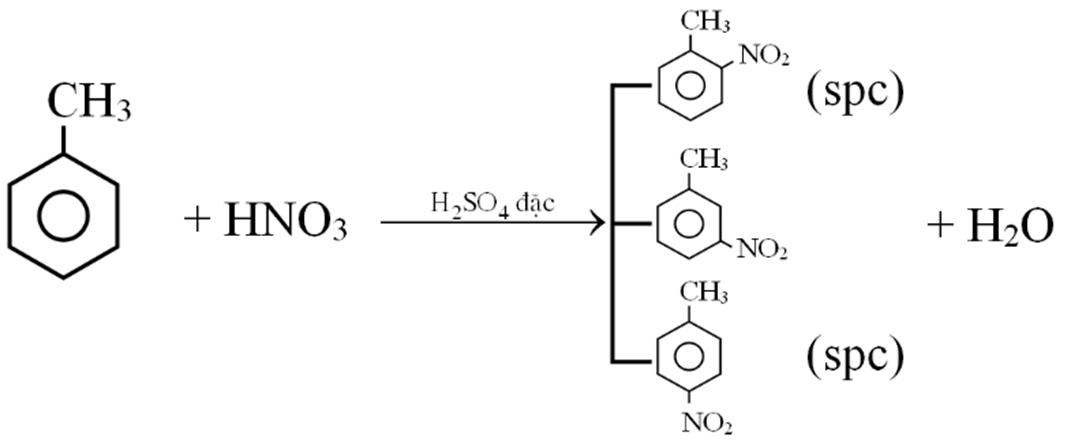
A. propylbenzen. B. n-propylbenzen. C. iso-propylbenzen. D. đimetylbenzen.
Câu3. (C.11): Chất X tác dụng với benzen (xt, t0) tạo thành etylbenzen. Chất X là
A. CH4 B. C2H2 C. C2H4.
D. C2H6
Câu4.(C.14): Số hiđrocacbon là đồng phân cấu tạo của nhau, chứa vòng benzen, có cùng công thức phân tử C8H10 là
A. 4. B. 2. C. 5.
Câu5. Chất nào sau đây không thể chứa vòng benzen?
A. C8H10. B. C6H8.
C. C8H8.
Câu6. Cho sơ đồ phản ứng: 1 mol Toluen + 1 mol Cl2 as
A. C6H5CH2Cl.
Câu7. Thuốc nổ TNT được điều chế trực tiếp từ chất nào?
D. 3.
C9H12.
A. benzen. B. metylbenzen. C. vinylbenzen. D. p-xilen.
Câu8. Toluen không phản ứng với chất nào sau đây?
A. Dung dịch Br2. B. KMnO4/t0 .
Sản phẩm chủ yếu trong hỗ
1:1 (có mặt bột sắt) là
A. o-bromtoluen và p-bromtoluen
C. p-bromtoluen và m-bromtoluen
benzyl bromua
Câu10. Khi trên vòng benzen có sẵn nhóm thế -X, thì nhóm thứ hai sẽ ưu tiên thế vào vị trí o- và p-. Vậy -X là những nhóm thế nào?
A.-CnH2n+1, -OH, -NH2.
C. -CH3, -NH2, -COOH
B. -OCH3, -NH2, -NO2.
D. -NO2, -COOH, -SO3H.
Câu11. Lượng clobenzen thu được khi cho 15,6 gam C6H6 tác dụng hết với Cl2 (xúc tác bột Fe) với hiệu suất phản ứng đạt 80% là
A. 14 gam. B. 16 gam.
C. 18 gam. D. 20 gam.
Câu12. Nếu phân biệt các hiđrocacbon thơm: benzen, toluen và stiren chỉ bằng một thuốc thử thì nên chọn thuốc thử nào dưới đây?
A. dung dịch KMnO4.
B. dung dịch Br2.
D. dung dịch NaOH. Câu13. Đốt cháy hoàn toàn m gam một ankylbenzen (X) thu được 0,35 mol CO2 và 0,2 mol H2O. Giá trị m và công thức phân tử của X lần lượt là:
C. dung dịch HCl.
A. 4,6 và C7H8.
Câu14. Cho dãy các chất: cumen, stiren, isopren, axetilen, benzen. Số chất trong dãy làm mất màu dung dịch brom là
A. 5. B. 4.
Tổng hệ số các chất trong phương trình trên
A. 10. B. 9.
8. Câu16. Cho các chất sau: metan (1); etilen (2); axetilen (3); benzen (4); stiren (5); toluen (6). Các chất có khả năng làm mất màu dung dịch KMnO4 ở điều kiện thích hợp là:
A. 2, 3, 5, 6. B. 3, 4, 5, 6. C. 2, 3, 4, 5. D. 1, 3, 4, 5, 6. Câu17.(B.11): Cho các phát biểu sau:
(a) Khi đốt cháy hoàn toàn một hiđrocacbon X bất kì, nếu thu được số mol CO2 bằng số mol H2O thì X là anken.
(b) Trong thành phần hợp chất hữu cơ nhất thiết phải có cacbon.
(c) Liên kết hóa học chủ yếu trong hợp chất hữu cơ là liên kết cộng hóa trị
(d) Những hợp chất hữu cơ khác nhau có cùng phân tử khối là đồng phân của nhau.
(e) Phản ứng hữu cơ thường xảy ra nhanh và không theo một hướng nhất định
(g) Hợp chất C9H14BrCl có vòng benzen trong phân tử
Số phát biểu đúng là
A. 4
B. 3
C. 2
Hướngdẫngiải Bao gồm: b, c.
(a) Sai vì X có thể chứa 1 vòng (xicloankan).
D. 5
(d) Sai vì các chất hữu cơ khác nhau có cùng công thức phân tử mới là đồng phân của nhau.
(e) Sai vì phản ứng hữu cơ thường xảy ra chậm.
(g) Sai vì C9H14BrCl có k = 2 không thể chứa vòng benzen. Câu18. Cho 13 gam hỗn hợp gồm benzen và stiren làm mất màu vừa đủ dung dịch chứa 8 gam brom. Tỉ lệ mol benzen và stiren trong hỗn hợp ban đầu là
A. 1: 1. B. 1: 2.
C. 2: 1.
D. 2: 3.
Câu19. Đốt cháy hết 9,18 gam 2 đồng đẳng kế tiếp thuộc dãy của benzen A, B thu được H2O và 30,36 gam CO2. Công thức phân tử của A và B lần lượt là:
A. C6H6 ; C7H8. B. C8H10 ; C9H12. C. C7H8 ; C9H12. D. C9H12 ; C10H14.
Câu20. Đốt cháy hỗn hợp X gồm ba chất thuộc dãy đồng đẳng benzen cần dùng V lít không khí (chứa 20% O2 và 80% N2 ở đktc). Cho hấp thụ sản phẩm cháy vào bình đự
2H4
CH2=CH2 +Br2 → CH2Br–CH2Br
CH≡CH+2Br2 → CHBr2 –CHBr2
CH2=CH-CH=CH2 +2Br2 → CH2Br–CHBr–CHBr–
CH2Br
CH2=CH2 +HCl → CH3-CH2Cl CH2=CH
CH3CH2OH QuitắccộngMaccopnhicop:KhicộngHXvàoanken bất đốixứngthìHcộng ưutiênvàoCcónhiềuHhơn, XcộngvàobênCcònlại.
2.Phản ứngtrùnghợp CH2=CH2 o xt,t,p → -(CH2-CH2-)nEtilen polietilen(PE)
3.Phản ứngvớiAgNO3 củaank–1–in (nhận biết)
RC≡CH+AgNO3 +NH3 ot → RC≡CAg↓ +NH4NO3
THĐB:CH≡CH+2AgNO3 +2NH3 ot →
CAg≡CAg↓+2NH4NO3
PƯ đặc trưng: PƯ thế
1.Phản ứngthế halogen
C6H6 +Cl2 oFe,t 1:1 → C6H5Cl + HCl Qui tắc thế vào vòng benzen: + Khi vòng benzen chứa sẵn nhóm thế loại 1: CnH2n+1-, -OH, -NH2, … làm tăng khả năng thế vào vòng benzen và thế ưu tiên vào vị trí o, p. + Khi vòng benzen chứa sẵn nhóm thế loại 2: C6H5-, -NO2, - COOH, … làm giảm khả năng thế vào vòng benzen và thế ưu tiên vào vị trí m.
2.Phản ứngoxihóakhônghoàn toànbởiKMnO4 (nhận biết)
-Ankylbenzenbị oxihóakhông hoàntoànlàmmấtmàudung dịchKMnO4 khi đunnóng, benzenkhôngcóphản ứngnày.