4 minute read
Actividad antimicrobiana de las NP de ZnO y su mecanismo de acción
materiales de envasado antimicrobianos se utilizan para inhibir y controlar el crecimiento microbiano, retener la humedad, garantizar la seguridad, resistir la penetración de líquidos o gases y controlar la vida útil. Dichos agentes
antimicrobianos se clasifican ya sea como compuestos orgánicos, como sales de amonio cuaternario, compuestos halogenados, fenoles, quitosano y quitina, o materiales inorgánicos, incluidos metales y óxidos
metálicos. Los metales y los óxidos metálicos siempre han sido importantes debido a su excelente actividad antimicrobiana y alta estabilidad en esta atmósfera. En particular, no es necesario que las partículas de óxido de metal entren necesariamente en las células para inducir toxicidad; las partículas reaccionan incluso cuando entran en contacto con las paredes celulares bacterianas o el abdomen de un crustáceo. En consecuencia, se han
informado varias modificaciones en la superficie de contacto organismo-partícula para mejorar la solubilidad de las partículas metálicas o desarrollar ROS (especies reactivas de oxígeno)
extracelulares que dañan las membranas celulares. Recientemente, con el advenimiento de la nanotecnología, los materiales inorgánicos como óxido de titanio (TiO2), ZnO, óxido de magnesio (MgO) y óxido de calcio (CaO) han llamado mucho la atención en la investigación debido a su estabilidad y resistencia en condiciones de procesamiento y eficaz comportamiento biocida contra patógenos transmitidos por los alimentos.
Investigaciones anteriores han demostrado que las actividades antibacterianas de las NP de ZnO están muy influenciadas por el tamaño de las partículas, la concentración del polvo y sus propiedades fotocatalíticas, ya que estas complementan su eficacia antimicrobiana.
Actividad antimicrobiana de las NP de ZnO y su mecanismo de acción
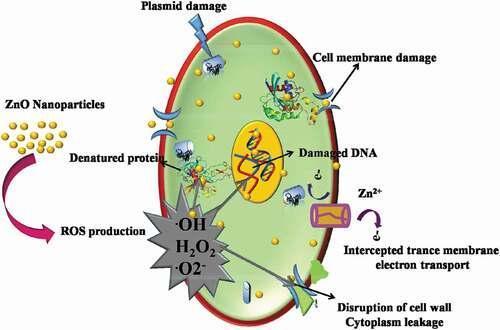
En general, cuando el tamaño de partícula disminuye su actividad antibacteriana aumenta. La actividad antibacteriana de ZnO es una consecuencia de su contacto directo con la pared celular microbiana, lo que da como resultado la destrucción de la integridad de la célula bacteriana, ya que ocurre la liberación de iones Zn2+ antimicrobianos y la generación
de ROS (especies de oxígeno reactivo, radicales libres). Además, se evaluaron las NP de ZnO (de 70 nm de diámetro) suspendidos en soluciones a varias concentraciones contra Escherichia coli (0157:H7), y se observó una mayor inhibición del crecimiento de la bacteria con concentraciones crecientes. Investigadores observaron que el ZnO tenía una actividad antibacteriana superior para Staphylococcus aureus en comparación con el MgO y el CaO. También demostraron que las NP de ZnO mostraron una actividad antibacteriana superior contra Listeria monocytogenes y Salmonella enteritidis en medios de cultivo líquidos cuando se evaluaron diferentes formas de ZnO, como polvo y película. Se evaluó la tasa de crecimiento bacteriano en Pseudomonas spp. utilizando el método de conteo de colonias y se observó que las nanopartículas de ZnO redujeron la tasa de crecimiento y aumentaron el daño a la membrana celular bacteriana. Otro estudio demostró que las NP de ZnO poseen una mejor actividad antimicrobiana contra los patógenos transmitidos por los alimentos, como Bacillus cereus, E. coli, Staphylococcus aureus y S. enteritidis, en comparación con el polvo de ZnO a granel.
Diagrama esquemático que muestra el mecanismo por el cual las NP de ZnO son tóxicas para las bacterias
Recientemente, se verificó que el compuesto de poli(butileno succinato) (PBS)/ZnO tiene una actividad antibacteriana considerable contra E. coli y S. aureus. También se ha demostrado que los aceites esenciales son agentes antimicrobianos potenciales en las películas de PBS, pero sus fuertes olores limitan su uso con productos alimenticios. La acción inhibitoria del aceite de carvacrol contra S. aureus y E. coli fue analizada y se notó que su aceptación era limitada debido a su mal olor. Sin embargo, se introdujo ZnO en esta
película de PBS para minimizar el mal olor, y se observó que el producto final mostraba una mejor actividad antibacteriana sin que se detectaran
olores de volátiles.
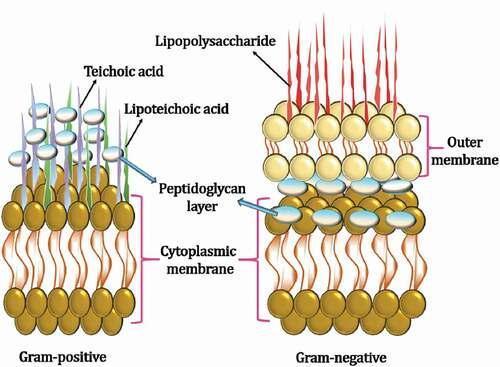
Características de la membrana bacteriana Gram-positiva y Gram-negativa
El estrés oxidativo generado por las NP de ZnO tiene un gran efecto sobre su actividad antibacteriana. La formación de iones Zn2+ a partir de ZnO inhibe las actividades de las enzimas respiratorias al interactuar con ellas, por lo tanto, se produce un daño irreversible en la membrana celular bacteriana. Las NP de ZnO inducen la despolarización de las membranas celulares, la
deformación de la arquitectura celular y el aumento de la fluidez y la fuga de proteínas; modifican el ADN y las mitocondrias en hongos y otros eucariotas al absorber los iones Zn2+ , llevando finalmente a la muerte
celular. Cuando las bacterias poseen potenciales de superficie negativos e interactúan con la superficie de ZnO cargada positivamente, la producción de oxígeno reactivo se ve reforzada, lo que da como resultado la despolarización de la membrana. En comparación con las bacterias Gram-positivas, las bacterias Gram-negativas exhiben un mayor potencial negativo debido a la existencia de una membrana externa adicional de lipopolisacáridos con un potencial negativo. La membrana celular de S. aureus que está menos cargada negativamente que la membrana celular de E. coli es una de las razones de la mayor actividad de las NP de ZnO en E. coli. Para ilustrar las diferencias en la actividad antibacteriana del ZnO frente a bacterias Gram-positivas y Gram-negativas, se han propuesto diferentes mecanismos. Sin embargo, se requieren más estudios para explicar la razón exacta de la sensibilidad de estas células bacterianas a las NP de ZnO.
Acinetobacter baumannii, un patógeno oportunista que causa neumonía y meningitis en humanos, se utilizó para analizar la eficacia de ZnO en combinación con antibióticos convencionales, como ciprofloxacina y ceftazidima. La adición de NP de ZnO en una concentración subinhibitoria exhibió una actividad antibacteriana mejorada. Esto se atribuyó al aumento de la absorción de antibióticos y al cambio en la morfología de las células bacterianas debido a la presencia de NP de ZnO.
También se comprobó la actividad antibacteriana de las NP de ZnO contra Vibrio cholera (un agente causante de la diarrea acuosa grave).


