ATTUALITÀ
ATTUALITÀ
ATTUALITÀ
La chimica europea in cerca di ducia
La chimica europea in cerca di ducia
La chimica europea in cerca di ducia
STRUMENTAZIONE I misuratori di portata a ultrasuoni
STRUMENTAZIONE I misuratori di portata a ultrasuoni
STRUMENTAZIONE I misuratori di portata a ultrasuoni
APPROFONDIMENTI I farmaci orfani per malattie rare
APPROFONDIMENTI I farmaci orfani per malattie rare
APPROFONDIMENTI I farmaci orfani per malattie rare
RIVISTA DELL’
RIVISTA DELL’
RIVISTA DELL’
INDUSTRIA CHIMICA E FARMACEUTICA






INDUSTRIA CHIMICA E FARMACEUTICA
icf ANNOXV NUMERO1 FEBBRAIO/MARZO2024 www.interprogettied.com POSTE ITALIANE SPA - SPED. IN ABB. POSTALE 70% - LO/MI - COSTO COPIA €10,00
INDUSTRIA CHIMICA E FARMACEUTICA
icf ANNOXV NUMERO1 FEBBRAIO/MARZO2024 www.interprogettied.com POSTE ITALIANE SPA - SPED. IN ABB. POSTALE 70% - LO/MI - COSTO COPIA €10,00
C M Y CM MY CY CMY K C M Y CM MY CY CMY K
icf ANNOXV NUMERO1 FEBBRAIO/MARZO2024 www.interprogettied.com POSTE ITALIANE SPA - SPED. IN ABB. POSTALE 70% - LO/MI - COSTO COPIA €10,00




www.interprogettied.com
www.interprogettied.com




























2 icf RIVISTA DELL’INDUSTRIA CHIMICA E FARMACEUTICA Sommario INDUSTRIA CHIMICA E FARMACEUTICA icf ANNOXV NUMERO1 FEBBRAIO/MARZO2024 www.interprogettied.com ATTUALITÀ cerca fiducia portata ultrasuoni per malattie rare INDUSTRIA CHIMICA E FARMACEUTICA RIVISTA DELL’ icf 4 Editoriale Transizione digitale: se la spinta viene dal pharma 6 Storia di copertina Tecnica per la misura di pressione e livello nei processi biotecnologici 10 Attualità La chimica europea in cerca di fiducia 14 Attualità 20 Appuntamenti A Parma l’automazione intelligente e green 24 Appuntamenti 28 Industria farmaceutica 30 Ricerca 32 Ambiente 34 Convalida Dieci anni di affidabilità al servizio del pharma 38 Macchine Comprimitrici dal design semplice e facile da pulire Sommario
42 Macchine
43 Sicurezza
46 Componenti
Un partner completo per la farmaceutica e non solo

49 Componenti
52 Materiali
FEB/MAR 2024 NUMERO 1
54 Software
Dalla flessibilità alla conformità: così il pharma accelera sul digitale

58
Strumentazione
TOC: un parametro cruciale per la qualità dell’acqua

61
Strumentazione
62
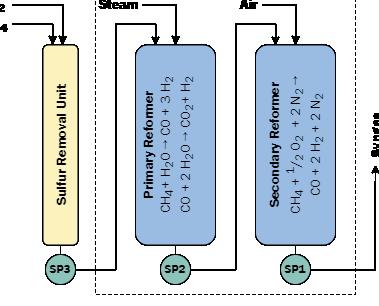
Strumentazione Ammoniaca e idrogeno: sulla strada della transizione
66
Strumentazione Lo sviluppo continuo dei misuratori di portata ad ultrasuoni

70
Automazione
L’automazione che supera le barriere

74
Approfondimenti
Farmaci orfani per malattie rare: un settore in forte sviluppo

“L’industria dei medicinali equivalenti e dei biosimilari è strategica per il ruolo centrale che ha assunto nel garantire accesso al farmaco ed equilibrio economico alla spesa pubblica: in 20 anni è arrivata a garantire oltre il 30% del fabbisogno farmaceutico nazionale”. Stefano Collatina, presidente di Egualia, pagina 20
Sommario RIVISTA DELL’INDUSTRIA CHIMICA E FARMACEUTICA icf 3
Febbraio/Marzo 2024

Transizione digitale: se la spinta viene dal pharma
di Alessandro Bignami
Spesso, talvolta a ragione, l’industria chimico-farmaceutica viene definita conservativa e poco incline a modificare i propri processi produttivi e a introdurre sistemi radicalmente innovativi. Ciò si spiega in gran parte con l’oneroso impegno di dover sottoporre a convalida e qualifica di volta in volta il nuovo sistema o le nuove apparecchiature implementate. Chi è certo di produrre a regola d’arte e nel rispetto delle normative vigenti ci pensa molto prima di toccare le linee produttive. Ma la normativa, in ambito farmaceutico, è così centrale che può determinare in modo profondo sia la resistenza al cambiamento sia, al contrario, la necessità di affrontarlo per essere conformi e competitivi. Nel caso della transizione digitale pare che i vincoli della regolamentazione farmaceutica, che tra l’altro hanno visto recentemente numerosi aggiornamenti, abbiano funzionato più da stimolo che da inibizione. Le aziende chimico-farmaceuti-
che stanno infatti puntando sull’adozione di sistemi digitali avanzati proprio per ottenere e dimostrare più facilmente la piena conformità, senza per questo perdere in flessibilità o alterare significativamente i propri processi. I vantaggi sono evidenti sotto il profilo della sicurezza, della tracciabilità e dell’integrità del dato. La spinta della digitalizzazione verso la trasparenza e l’efficienza dei processi aiuta dunque a rispondere più efficacemente alle esigenze di una regolamentazione così severa. Tutto questo ha reso l’industria farmaceutica, come ci ha spiegato un esperto di informatica e software come Pier Alberto Guidotti, fondatore di Analysis, un settore trainante per la transizione digitale. Tanto da diventare un modello di riferimento per le aziende di altri settori manifatturieri che, pur non essendo sottoposte a un quadro regolatorio altrettanto rigido, intendono accelerare sulla via della digitalizzazione.
Editoriale 4 icf RIVISTA DELL’INDUSTRIA CHIMICA E FARMACEUTICA
Febbraio/Marzo 2024

Tecnica per la misura di pressione e livello nei processi biotecnologici
Le biotecnologie si stanno sempre più affermando ed è in atto la trasformazione di molti processi chimici e farmaceutici in processi biotech. In questo contesto, l’azienda spagnola TECNIC Bioprocess Equipment Manufacturing supporta i propri clienti in tutte le fasi di un bioprocesso, affidandosi alla strumentazione di VEGA per la misura di livello e pressione.
a cura di
Marzia Savino

Dalla sua fondazione risalente a dieci anni fa, TECNIC Bioprocess Equipment Manufacturing si è affermata molto rapidamente. Con una superficie di produzione di 5.000 m², oggi l’azienda si annovera tra gli specialisti per la fornitura di equipaggia-
mento per applicazioni biotecnologiche e farmaceutiche per laboratori, impianti pilota e impianti di produzione. L’azienda si occupa dell’intero processo di produzione, dalla costruzione 3D alla programmazione e strumentazione delle apparecchiature, fino alla messa in servizio. TECNIC dispone di labora-
tori BSL2 per colture cellulari e microbiche che impiega a sostegno dei propri clienti. “Assistiamo i nostri clienti nella pianificazione di equipaggiamenti per settori a monte o a valle o nella fase di scale-up. Fungiamo da anello di congiunzione tra i dipartimenti di ricerca e sviluppo e la produzione e offriamo soluzioni scalabili per accelerare il processo di industrializzazione”, spiega Manel Estany, direttore operativo di TECNIC.
Mentre nei primi anni l’azienda si è concentrata esclusivamente sulle applicazioni farmaceutiche, nel 2018 si è aggiunta una nuova divisione di biotecnologia. Nel frattempo TECNIC copre tutti i processi tipici del settore biotecnologico: upstream (bioreattori e reattori) e downstream (equipaggiamento per la filtrazione a flusso tangenziale).
L’azienda dispone di un’ampia gamma di apparecchiature per applicazioni di laboratorio (eLAB), pilota (ePILOT) e di produzione (ePROD).
I bioreattori sono apparecchiature che riproducono in maniera ottimale le condizioni per la crescita di colture cellulari o microbiche, regolando temperatura, valore di pH, pressione parziale dell’ossigeno (pO2) e concentrazione di gas disciolti e, opzionalmente, la densità ottica (TCD), la densità cellulare (VCD) o la CO2 disciolta. L’ossigeno disciolto nel mezzo per la coltura viene controllato tramite una regolazione a cascata che gestisce variabili come miscelazione, aerazione o aerazione in atmosfera arricchita di ossigeno. Per garantire la sterilità nel reattore biologico sono stati sviluppati valvole di addizione sterili e un sistema di prelievo campioni interamente asettico collegati al sistema SIP (Sterilization in Place).
Viscosità e turbolenze I valori di misura affidabili sono essenziali per i processi sofisticati. Da
6 icf RIVISTA DELL’INDUSTRIA CHIMICA E FARMACEUTICA Storia di copertina

quando ha intrapreso l’attività nel settore biotecnologico, per la misura di pressione e livello l’azienda si affida quasi esclusivamente ai sensori di livello e pressione di VEGA. “Nella maggior parte delle applicazioni, le tempera ture sono comprese tra -10°C e +140°C necessari per i processi di sterilizzazione”, spiega Ma nel Estany, descrivendo le con dizioni di lavoro che caratte rizzano i bioreattori prodotti da TECNIC. “Spesso abbiamo a che fare con sostanze viscose e turbolente, ma anche il vapore e gli spruzzatori CIP rappresentano una sfida per i sensori”.
Ampia gamma di sensori
Negli impianti sono installati sensori VEGA dei tipi più diversi. Gli strumenti trasmettono i propri segnali analogici e digitali 4 … 20 mA al software aziendale eSCADA. Questo software di TECNIC si basa sulla piattaforma AVEVA e gestisce i parametri di controllo e l’esecuzione delle ricette conformemente a GAMP5 e CFR21. “Mettiamo in servizio i sensori autonomamente, ma possiamo sempre contare sul supporto tecnico di VEGA”, spiega Estany.
Il VEGABAR 28 è per così dire il sensore standard per la misura di pressione. Con il suo aiuto si regolano i processi di sterilizzazione nei bioreattori. Il sensore è essenziale per garantire una pressione di 1,3 bar. Il VEGABAR 28 è un sensore di pressione con cella di misura in ceramica impiegabile universalmente per la misura su gas, vapori e liquidi fino a 130°C. L’elemento sensore è la collaudata cella di misura in ceramica CERTEC® che, oltre ad avere un’eccellente stabilità nel lungo termine, ha anche un’elevata resistenza al sovraccarico. Si tratta
inoltre di una cella a secco che lavora senza olio. Il VEGABAR 29 è invece il sensore standard negli impianti di filtrazione a flusso tangenziale (TFF), quindi nelle applicazioni a valle dei processi biotecnologici. Qui il sensore effettua il monitoraggio della TMP (Trans Membrane Pressure), un parametro critico per la filtrazione. Questo parametro di processo è la pressione media dell’afflusso sul lato del permeato della membrana. Il sistema di filtrazione tangenziale (TFF) di TECNIC è interamente automatizzato, in modo che la TMP possa essere predefinita e il processo controllato agendo sulla valvola del retentato.
Nell’azienda, la sonda di misura capacitiva a barra VEGACAL 62 viene invece impiegata in un numero limitato di applicazioni, ma negli impianti CIP (Cleaning in Place) è molto apprezzata per la sua elevata resistenza agli agenti chimici. La sua funzione è la misura continua di livello. Il VEGAFLEX 81 invece trova applicazione nei punti più diversi dei processi, ad esempio per la misura di livello nei serbatoi della filtrazione a flusso tangenziale, dove il valore di misura è necessa rio per ottenere una misu ra affidabile.
Gli interruttori di livel lo VEGAPOINT 11 e VE GAPOINT 23 effettuano il monitoraggio del livel lo nei punti in cui è richie sto il rispetto degli standard ASME-BPE, EHEDG o GMP, ad esempio nel settore delle pompe. Anche questi senso ri sono idonei ai processi di sterilizzazione. Grazie agli attacchi universali per adat
Storia di copertina
tatori igienici, l’impegno per l’installazione è ridotto. Inoltre, i sensori possono essere impiegati nell’applicazione senza necessità di taratura. Il sensore radar compatto VEGAPULS 21, anch’esso in grado di resistere a processi CIP fino a 80°C, viene impiegato per monitoraggi del volume non critici che non richiedono il contatto con il prodotto. Le misure di livello di massima precisione senza contatto con il prodotto sono invece affidate al VEGAPULS 6X, che sorveglia alcuni volumi critici nei processi. Il sensore radar a 80 GHz per la misura continua di livello su liquidi è idoneo anche ai processi SIP. Infinire, è frequente anche l’installazione di interruttori di livello a vibrazione VEGASWING 51 e VEGASWING 61, soprattutto in applicazioni in cui non valgono le normative ASME-BPE, EHEDG o GMP.
Assistenza e supporto molto apprezzati

“Apprezziamo soprattutto l’affidabilità dei sensori VEGA. Per noi però sono molto importanti anche l’assistenza e soprattutto il supporto tecnico fornito in tutto il mondo da VEGA, poiché commercializziamo i nostri impianti a livello internazionale”, chiarisce Manel Estany. Per quanto riguarda l’installazione ormai i tecnici sono convinti della connettività Bluetooth dei sensori. “Il collegamento wireless con gli strumenti di calibrazione è decisamente molto utile per la messa in servizio e la verifica. Ma anche nella pratica quotidiana è possibile individuare molto più velocemente eventuali anomalie”, conclude Manel Estany. l
Sensore radar
VEGAPULS 6X per la misura di livello continua su liquidi e solidi in pezzatura

Sensore di pressione
VEGABAR 28 con cella di misura in ceramica
Sensore radar compatto
VEGAPULS 21 per la misura di livello continua
RIVISTA DELL’INDUSTRIA CHIMICA E FARMACEUTICA icf 7 Febbraio/Marzo 2024
La Ceo & founder Gilda
D’Incerti
PQE Group supera i 100 milioni di euro di fatturato

PQE Group, società di riferimento nella consulenza in ambito LifeScience, archivia l’anno 2023 con una crescita del 10% e un fatturato in rialzo che eccede i 100 milioni di euro. “In un periodo dove molte aziende stanno lottando per navigare nelle complessità del panorama geopolitico, della crisi climatica e dei tassi d’inflazione, PQE Group ha dimostrato non solo di saper resistere, ma di avere la capacità di adattarsi a tempi incerti potenziato tutti gli indicatori finanziari”, ha af-
fermato Gilda D’Incerti, Ceo & founder del Gruppo toscano nato 25 anni fa.
“Questo successo è frutto di una pianificazione attenta, investimenti oculati in nuove tecnologie e di una cultura aziendale che premia l’agilità e l’innovazione”.
L’anno appena concluso per PQE Group ha una indentità ben precisa: ottimizzazione dei processi e investimenti in digitalizzazione. L’azienda, dopo aver concluso il bilancio 2022 con un 68% in più di fatturato rispetto all’esercizio precedente, ha concretizzato nel 2023 un approccio riorganizzativo solido che sta posizionato PQE Group al massimo della sua efficienza. Da qui la recente istituzione di ReSQ-Up, Contract Research Organization (CRO) interna al Gruppo, che supporta le aziende in collaborazione con ospedali, start up e istituti di ricerca nei loro studi clinici di fase I e II. Un nuovo paradigma
Fidia Farmaceutici rafforza la presenza in oftalmologia
Fidia Farmaceutici ha iniziato il 2024 con il completamento di due operazioni che le consentono di consolidare la leadership nel mercato italiano dei prodotti per la salute degli occhi.
La prima operazione riguarda l’acquisizione del 100% del business oftalmico di Sanifarma, primaria azienda italiana nel settore del benessere oculare in farmacia, attiva anche nei canali GDO e online, e che nel 2023 ha registrato una quota di mercato sul territorio nazionale pari a circa il 70% relativamente alla vendita di lenti a contatto monouso (8 milioni di unità vendute) e del 35% per le soluzioni per lenti (dati Iqvia).
L’investimento comprende marchi leader di mercato come Contacta® e Correct® che oggi vantano un’ampia gamma di prodot-
ti, tra cui linee di lenti a contatto giornaliere per miopia e soluzioni per la manutenzione, una linea di gocce oculari naturali e una vasta scelta di occhiali (da presbiopia, da sole e protettivi da schermi luminosi). A questi prodotti si aggiungono una linea di integratori per il benessere psico-fisico e la linea di repellenti alla citronella e anti-meduse, Respingo.
Ad assistere Fidia Farmaceutici per la parte legale è stato lo studio Curtis Mallet Prevost, per gli aspetti fiscali e finanziari è stata assistita dallo Studio Spada & Partners, e l’advisor finanziario è stata Ethica Group con il team di M&A Advisory.
Sanifarma è stata assistita da Clearwater International (M&A Advisor) e per gli aspetti finanziari e fiscali e dallo Studio legale FDG&A Professionisti Riuniti.
nella ricerca clinica che pone uno specifico accento sulla salute femminile e l’utilizzo della cannabis terapeutica. Parallelamente, PQE Group ha ampliato la sua presenza globale con l’apertura di nuovi uffici in Canada, Arabia Saudita, Irlanda e Singapore, arivando a 45 sedi in tutto il mondo e 26 entità giuridiche. Questa espansione strategica mira a collegare il Gruppo PQE con mercati in crescita, in particolare nel Sud-est asiatico.
“Abbiamo condotto investimenti mirati in soluzioni digitali e scelte eco-sostenibili, consentendo la riduzione di 900 trasferte di lavoro in un anno. Un risparmio che in km equivale a compiere quasi tre volte il giro del mondo. Questo non solo aumenta la nostra efficienza, ma contribuisce anche alla tutela dell’ambiente”, ha evidenziato Stefano Carganico, chief innovation officer di PQE Group.
La seconda operazione ha per oggetto un nuovo accordo commerciale con la multinazionale Novartis, leader nello sviluppo di farmaci innovativi, per la distribuzione già a partire dal mese di marzo 2024, di 6 specialità medicinali oftalmologiche per il trattamento del glaucoma.
“Questo ulteriore rafforzamento del nostro listino oftalmico ci permette di ambire ad una crescita del fatturato 2024 superiore alle previsioni”, dichiara Carlo Pizzocaro, presidente e Ceo di Fidia Farmaceutici.
“Con l’ingresso di un marchio come Contacta entreremo con una posizione da leader nel mercato delle lenti a contatto monouso e liquidi, rafforzando parallelamente la nostra presenza nel canale farmacia già presidiato con numerose referenze in altre aree terapeutiche”.

Febbraio/Marzo 2024 Attualità 8 icf RIVISTA DELL’INDUSTRIA CHIMICA E FARMACEUTICA




La chimica europea in cerca di fiducia
Nell’UE l’industria chimica sta vivendo un momento difficile causato soprattutto dagli elevati costi dell’energia e delle materie prime. Reggono però i sottosettori, che nel 2023 hanno mostrato segnali di ripresa.
a cura di Eva De Vecchis
La fine del 2023 ha confermato alcune tendenze che erano già in atto nel corso dell’anno: indebolimento dei livelli di fiducia nell’economia dell’UE27, contrazione delle vendite e produzione
in calo. I fattori di stress, come l’aumento dei costi energetici e la mancanza di domanda, stanno d’altronde incidendo pesantemente sulla competitività dell’industria chimica in Europa. Le importazioni cinesi stanno colpendo i produttori dell’UE e si teme che sia solo l’inizio, poiché l’offerta ci-
nese in eccesso è destinata ad essere esportata e l’Europa è una destinazione chiave.
Ci sono però alcuni accenni di ripresa per i sottosettori chimici. I dati del novembre 2023 mostrano, infatti, che la produzione chimica dell’UE è stata di circa l’1% superiore al livello del 2022. È ancora troppo presto per confermare se questa ripresa sarà stabile, intanto, nel 2024 si prevede una crescita più rapida, ma il miglioramento sarà graduale.
Il sentiment dell’industria UE rimane invariato Nel complesso, a dicembre 2023, l’Economic Sentiment Indicator (ESI) è aumentato nell’UE. Tra le maggiori economie del continente l’ESI è migliorato in Italia, Spagna e Germania, ma è diminuito nei Paesi Bassi e in misura minore in Francia, mentre è rimasto sostanzialmente stabile in Po-
10 icf RIVISTA DELL’INDUSTRIA CHIMICA E FARMACEUTICA
Attualità
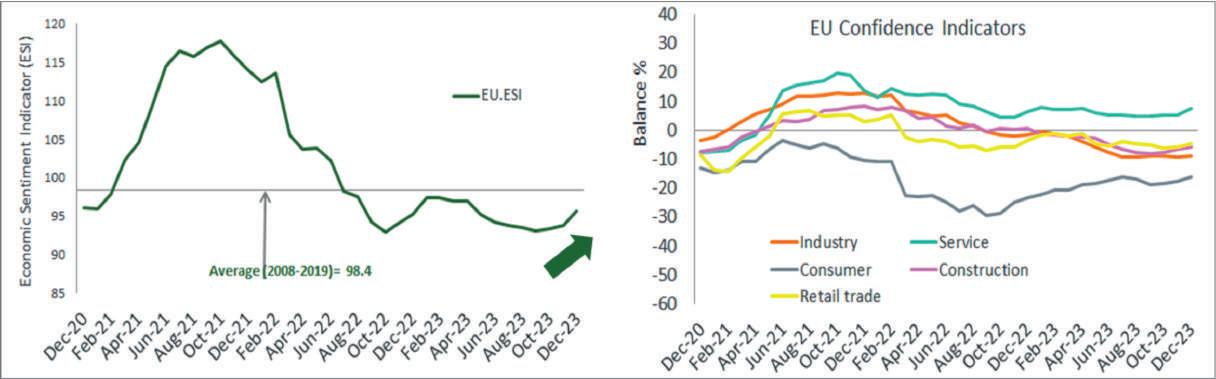
lonia. Il miglioramento dell’ESI è stato determinato dall’aumento della fiducia da parte dei consumatori e dei dirigenti verso il commercio al dettaglio, i servizi e le costruzioni, mentre la fiducia nell’industria è rimasta stabile per cinque mesi consecutivi. Mentre le valutazioni dei dirigenti sull’attuale livello degli ordini complessivi hanno continuato a diminuire rispetto a maggio 2023, un numero minore di dirigenti ha considerato le scorte di prodotti finiti superiori alla norma, mentre le loro aspettative sulla produzione sono rimaste invariate. I dati mostrano che le valutazioni dei portafogli ordini per le esportazioni sono peggiorate (come testimonia un’indagine presso le imprese e i consumatori dell’UE, realizzata a dicembre 2023).
La fiducia nel settore chimico è in lieve calo
L’ultima indagine economica mostra un leggero calo della fiducia verso l’industria chimica dell’UE27. Nel dicembre 2023, le aspettative sulla produzione chimica sono scese per la prima volta dopo quattro mesi di miglioramenti costanti. Tuttavia, le cifre continuano a rimanere positive, mentre le valutazioni sulle scorte di prodotti finiti sono leggermente diminuite. L’opinione dei dirigenti sull’attuale livello del portafoglio ordini complessivo non mostra alcun miglioramento. L’indicatore di fiducia nel settore chimico è ancora a un livello basso e non si osserva alcun segnale di forte ripresa.
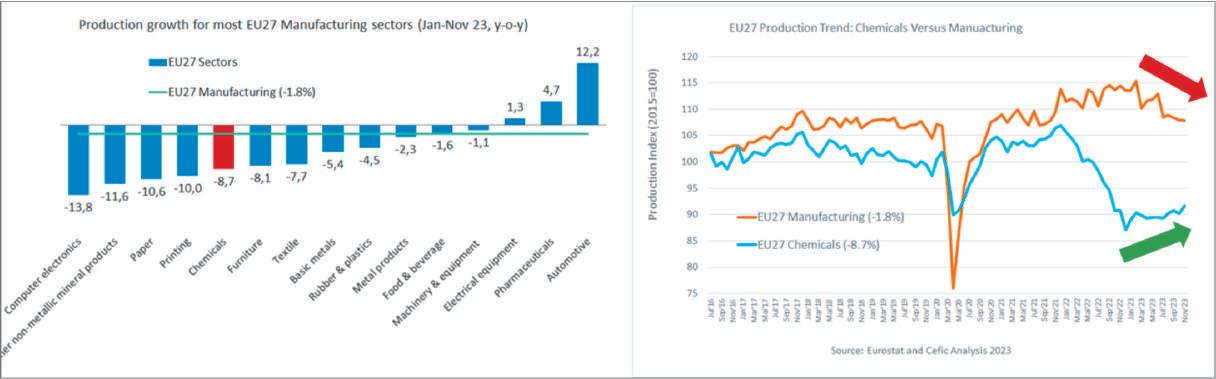
Il rischio di perdere competitività a livello globale
La produzione manifatturiera dell’UE nel 2023 è stata significativamente inferiore rispetto allo stesso periodo dell’anno precedente (-1,8%). Settori come quello delle apparecchiature elettriche, farmaceutico e automobilistico hanno contribuito a limitare gli effetti della crisi energetica sul settore manifatturiero dell’UE nel suo complesso. Con un calo dell’8,7%, l’industria chimica dell’UE ha registrato nel 2023 (gennaio-novembre) il quinto maggior calo di produzione. L’utilizzo della capacità produttiva nell’industria chimica dell’UE è ancora inferiore rispetto al livello dell’anno precedente. L’industria chimica europea continua a per-
Fonte: Indagine della Commissione UE27 su imprese e consumatori e analisi Cefic (2024)
Fonte: Eurostat e analisi Cefic (2024)
RIVISTA DELL’INDUSTRIA CHIMICA E FARMACEUTICA icf 11 Febbraio/Marzo 2024 Attualità
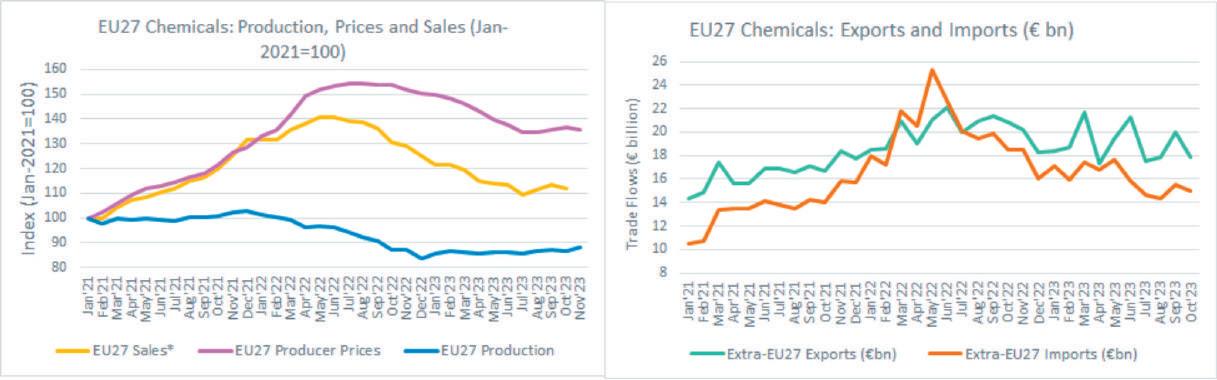
dere competitività sui mercati chimici globali a causa degli elevati costi regionali dell’energia e delle materie prime. Nonostante questo, la produzione chimica dell’UE ha registrato un leggero aumento dell’1,6% nel novembre 2023 rispetto a ottobre dello stesso anno. I dati di novembre 2023 mostrano che la produzione chimica dell’UE ha superato per la prima volta di circa l’1% il livello del 2022.
La frenata della chimica di base
Focalizzando l’attenzione sui settori chimici più ampi, i settori della chimica di base hanno continuato a registrare un calo a due cifre. La produ-
zione 2023 di prodotti petrolchimici è stata inferiore dell’11,7% rispetto allo stesso periodo dell’anno precedente. Una marcata flessione è stata registrata per i polimeri (-11,4%). Il calo della produzione di prodotti inorganici di base e di specialità chimiche è stato moderato (meno del 7%).
Con una crescita del 3,5%, i prodotti chimici di consumo (saponi, detergenti e cosmetici) continuano a registrare risultati positivi rispetto agli altri sottosettori chimici. Nel complesso, la produzione di prodotti chimici è diminuita dell’8,7% nei primi undici mesi del 2023 rispetto allo stesso periodo del 2022.

La Cina batte ogni record La Cina continua a registrare il più alto livello di produzione chimica di sempre. La produzione di prodotti chimici nel gigante asiatico sembra migliorare di mese in mese da giugno 2023. La produzione cinese di prodotti chimici ha superato del 9,5% il livello dell’anno precedente (gennaio-novembre). Nell’UE-27, l’industria chimica sta perdendo competitività sui mercati chimici globali a causa degli elevati costi regionali dell’energia e delle materie prime. La produzione e l’attività commerciale stanno diminuendo significativamente e sono al di sotto dei livelli del 2022. La produzione chimica globale crescerà di circa il 2% nel 2023. Per il 2024 si prevede una crescita inferiore a quella strutturale del 3,5%.
Vendite in calo
Con 553 miliardi di euro, le vendite dell’industria chimica dell’UE nei primi dieci mesi del 2023 sono inferiori ai livelli registrati nello stesso periodo dell’anno precedente (-15,5%). I dati mensili mostrano un calo di vendite di prodotti chimici dell’UE nell’ottobre 2023 dell’1% rispetto a settembre 2023. Infine, il livello delle vendite nell’ottobre 2023 è stato del 14,3% inferiore al livello dell’anno precedente.
12 icf RIVISTA
E FARMACEUTICA Attualità
DELL’INDUSTRIA CHIMICA
Fonte: Eurostat e analisi Cefic (2024)

S S4 Qualità
Difficile descriverla in modo oggettivo facile rilevarne la mancanza
Dalla fase progettuale a quella produttiva, dall’installazione alla convalida: il controllo della contaminazione dell’aria nella sua interezza.
• Progettazione • Pianificazione
• Ingegneria di base
• Ingegneria di dettaglio
• Construction & Commissioning
• Equipment & Validation • Turnkey
Supporto • Manutenzione
• Utilities
• Analisi dei flussi d’aria per un controllo della contaminazione sempre più efficace
www.s4ssrl.it


•
CLEAN ROOM . CAPPE . FLUSSI LAMINARI . PASS BOX . DOCCE D’ARIA . PASSA MATERIALI . LAF . GLOVEBOX

Endress+Hauser ha festeggiato i
Endress+Hauser ha registrato un forte sviluppo nell’anno del suo 70esimo anniversario. La società ha aumentato il suo fatturato consolidato dell’11%, superando i 3,7 miliardi di euro nel 2023, e ha creato 715 nuovi posti di lavoro in tutto il mondo. Alla fine dell’anno, il Gruppo contava 16.532 dipendenti. Endress+Hauser prevede di continuare a crescere anche nell’anno in corso.
“Endress+Hauser ha registrato una forte crescita organica nel 2023, favorita da ordini record all’inizio
70 anni rafforzandosi
dell’anno”, ha dichiarato il direttore finanziario Luc Schultheiss. I singoli mercati e i vari settori industriali si sono sviluppati in modo molto diverso. Lo slancio economico è rallentato notevolmente nella seconda metà dell’anno. “Ciononostante, siamo riusciti a mantenere i nostri ordini a un buon livello e vogliamo sfruttare le opportunità di crescita anche nel 2024”, ha sottolineato Peter Selders, nuovo CEO del Gruppo dall’inizio dell’anno.
Nel 2023 Endress+Hauser ha festeggiato il suo 70esimo compleanno. Il
Una nuova sede per Novo Nordisk Italia
È all’insegna dell’innovazione e della sostenibilità la scelta della nuova sede di Novo Nordisk Italia. Un cambiamento che testimonia quanto l’Italia rivesta un ruolo strategico per l’azienda danese a livello mondiale, in termini di ricerca, sviluppo e investimenti.
Dopo quasi 30 anni nella storica sede di via Elio Vittorini a Roma, è il moderno EuroHive ad ospitare la sede italiana di Novo Nordisk, un edificio innovativo che rappresenta l’evoluzione del workplace e che si inserisce nel più ampio progetto di evoluzione urbana – eUrban – dove si incontrano business, arte e natura. “La scelta fatta riflette il nostro impegno verso la creazione di valore per le persone e per il paese nel quale operiamo”, commenta Drago Vuina, general manager & corporate vice president di Novo Nordisk Italia. “Partiamo con questa novità che sarà solo la prima di una serie di importanti scelte strategiche e innovazioni che porteremo avanti in Italia nel corso del 2024”.
I numeri dell’affiliata italiana confermano questo impegno. Più di 370 dipenden-
ti, 440 milioni di euro di fatturato, 100% di utilizzo di energia rinnovabile e prima al mondo per città coinvolte nel progetto Cities Changing Diabetes. La volontà era anche quella di trovare una nuova sede di lavoro che rispondesse al raggiungimento degli obiettivi di sostenibilità ambientale dell’azienda, in linea con Circular For Zero, la strategia di impatto ambientale zero entro il 2045. Questo trasferimento rappresenta un passo importante in questo senso; la nuova sede è dotata di certificazione WELL livello Gold, il primo sistema al mondo a definire i parametri con cui gli edifici possono migliorare la nostra vita ed è avvolta dal “Bosco transitorio”, uno spazio di 400 alberi e oltre 50 arbusti che porterà benefici come oltre 250 tonnellate di CO2 assorbite, il recupero delle polveri sottili e degli agenti inquinanti. Inoltre, a disposizione dei dipendenti, sono state installate trenta colonnine per la ricarica di veicoli elettrici e un servizio navetta dalla metropolitana per incentivare l’utilizzo di trasporti non inquinanti. Alla base di questo cambiamento ci sono
momento culminante è stata la settimana dell’anniversario in Svizzera: 5.500 dipendenti hanno partecipato a una grande festa a Basilea e hanno ricordato sette decenni di storia. Al primo Endress+Hauser Global Forum, oltre 800 clienti hanno discusso su come gestire con successo la trasformazione sostenibile dell’industria di processo. Centinaia di dipendenti hanno partecipato a conferenze interne; al Young Generation Networking Day, 600 giovani talenti hanno scambiato preziose idee per il futuro.

infine i valori della NovoNordiskWay che contraddistinguono l’azienda danese fin dalla sua fondazione: innovazione, sostenibilità e flessibilità. “Come dipendenti di Novo Nordisk crediamo che l’ambiente fisico nel quale operiamo debba riflettere i nostri valori fondamentali ed essere percepito come parte di un insieme visivo e comprensibile in tutto il mondo”, conclude Vuina. “Un luogo di lavoro non è solamente uno spazio. È una risorsa che dovrebbe creare una differenza positiva per tutti coloro che lo utilizzano”. Gli uffici si trovano in via Giorgio Ribotta nel quartiere Eur di Roma.
Febbraio/Marzo 2024 Attualità 14 icf RIVISTA DELL’INDUSTRIA CHIMICA E FARMACEUTICA
Il Ceo Peter Selders
Automazione: Coesia acquisisce AMC
Coesia, attraverso FlexLink, ha concluso l’acquisizione del 100% del capitale sociale dell’azienda americana Automation & Modular Components. Automation & Modular Components, LLC. (AMC), con sede a Davisburg (Michigan, Usa), produce sistemi di automazione con controlli integrati per la movimentazione dei materiali, nastri trasportatori da integrare in sistemi di assemblaggio e in linee di produzione. Grazie alle sue applicazioni per carichi pesanti, AMC serve diversi settori industriali, tra cui apparecchi medicali, farmaceutica, food packaging, automotive, lavorazione dei metalli, elettronica, vetro, energie alternative.
AMC rafforzerà la presenza di Coesia e FlexLink sul mercato statunitense, in particolare nel settore delle batterie e laddove sono richieste applicazioni di movimentazione di materiali pesanti e
leggeri in processi di assemblaggio o di produzione combinati.
“Siamo lieti di accogliere AMC nel nostro Gruppo: consideriamo quest’azienda un asset strategico soprattutto per lo sviluppo di FlexLink, la cui esperienza nella robotica e nella movimentazione dei materiali sarà ulteriormente potenziata e ampliata dai nastri trasportatori per carichi pesanti di AMC”, spiega Alessandro Parimbelli, chief executive officer di Coesia. “L’introduzione di AMC nel portfolio di Coesia negli Stati Uniti rafforzerà le capacità dell’organizzazione e consentirà al Gruppo di continuare a essere tra i leader nella fornitura di soluzioni di automazione”. “Coesia e FlexLink sono due realtà perfette per AMC, che le consentiranno di proseguire il suo percorso di crescita e di espandere ulteriormente la sua presenza globale. AMC continuerà a sup-

portare aziende, in oltre 25 settori in sei continenti, per produrre più velocemente e con maggiore efficienza”, afferma Dick Shore, ex proprietario di AMC. Coesia intende continuare ad investire in tecnologie legate all’automazione industriale, un settore in costante crescita, puntando su una crescita organica e inorganica sia negli Stati Uniti sia a livello globale.
Nuova Guseo da oltre 100 anni, grazie a innovazione tecnologica e a una struttura organizzativa orientata alla piena soddisfazione del cliente, è un punto di riferimento nella progettazione e realizzazione di impianti di macinazione, micronizzazione e contenimento per il settore chimico farmaceutico.
Pronti a ogni nuova sfida, affrontiamo il futuro su basi solide, mettendo a disposizione KNOW HOW, AFFIDABILITÀ ed EFFICIENZA, maturate nel corso della nostra lunga storia aziendale.




Attualità
icf 15 Febbraio/Marzo 2024
RIVISTA DELL’INDUSTRIA CHIMICA E
FARMACEUTICA
“LE NOSTRE REALIZZAZIONI SONO LA NOSTRA MIGLIORE PUBBLICITÀ” CALIBRATORI CONICI IMPIANTI DI MICRONIZZAZIONE Nuova Guseo Srl - Via Dante 8 Cap 29010 Villanova sull’ Arda (PC) Italia - Tel : 0523 837149 Per informazioni contattaci via Mail : ufficio.commerciale@nuovaguseo.eu www.nuovaguseo.eu www.nuovaguseo.eu
SISTEMI DI CONTENIMENTO IMPIANTI DI MACINAZIONE
Wenglor potenzia la propria machine vision con l’intelligenza artificiale
Wenglor sensoric group – azienda tedesca che sviluppa, produce e commercializza sensori intelligenti, dispositivi di sicurezza e sistemi avanzati di elaborazione di immagini – ha recentemente acquisito deevio, start-up berlinese fondata nel 2018, specializzata nello sviluppo di soluzioni hardware e software per applicazioni automatizzate di elaborazione delle immagini basate sull’intelligenza artificiale e sul data science. Con questa acquisizione, è nata la nuova società wenglorDeevio gmbh che permetterà a wenglor di rafforzare la propria expertise e le proprie capacità in tema di visione artificiale.
“Siamo davvero felici che il team di deevio sia entrato a far parte della innovative family di wenglor, siamo certi che questa collaborazione si rifletterà positivamente sulle nostre attività di ricerca e sviluppo”, ha dichiarato Elio Bolsi, general manager di wenglor sensoric italiana.
Oggi le tecnologie di visione artificiale permettono ai computer di comprendere ciò che viene visualizzato, simulando in modo intelligente le capacità umane di percezione visiva. L’integrazione con l’intelligenza artificiale permetterà ai sistemi di visione di analizzare e interpretare le immagini in modo più rapido ed efficiente rispetto ai metodi tradizionali. Gra-

Da sinistra: Christian Vollrath - Managing Director di wenglorDeevio, Rafael Baur - socio di wenglor sensoric group, Tassilo Glander e Damian Heimelsoci fondatori di deevio
zie all’apprendimento automatico e all’elaborazione dei dati, i sistemi basati sull’IA sono in grado di rilevare pattern, oggetti, movimenti e anomalie con una precisione e una velocità senza precedenti e ciò aprirà nuovi scenari applicativi in molti settori tra cui il farmaceutico, il food & beverage, la sicurezza e la robotica. Nell’ambito industriale e in particolare nel controllo qualità, l’impiego della machine vi-
ADL Farmaceutici e USP Group lanciano ADL
ADL Farmaceutici, supportata dall’Advisor SHC, sviluppa una nuova strategia commerciale internazionale che prevede una partnership con USP Group, gruppo mondiale dedicato alla salute del consumatore operante in 12 paesi europei, dando vita alla costituzione della nuova azienda ADL Unilab. L’obiettivo dell’operazione è quello di migliorare la presenza sul mercato e le performance di vendita di alcune linee di prodotti selezionati per i mercati italiano ed internazionale.
USP Group è una società con sede negli
sion con integrazione dell’IA permette di automatizzare i processi di validazione che devono essere eseguiti manualmente in quanto impossibili da gestire tramite un’eleborazione di immagini basata su regole prestabilite.
L’acquisizione di deevio da parte di wenglor è avvenuta poche settimane dopo il lancio della rivoluzionaria Smart Camera B60 che ha portato la machine vision ad un livello superiore. Tramite l’efficace integrazione tra hardware rinnovato e software altamente performante (uniVision), è possibile realizzare soluzioni complete e scalabili per applicazioni di elaborazione immagini di qualsiasi genere, anche le più complesse. “Nei prossimi mesi, con il valore aggiunto di deevio, saremo in grado di innovare ulteriormente questa soluzione di elaborazione delle immagini tramite l’integrazione dell’intelligenza artificiale”, conclude Elio Bolsi.
I team di sviluppo di wenglor e deevio stanno già lavorando attivamente per integrare la tecnologia deevio nell’ambiente software uniVision di wenglor.
Unilab
Stati Uniti che investe attivamente nel settore sanitario dal 1990. Il focus geografico è principalmente in Europa centrale e orientale, ed in particolare la Polonia rappresenta un mercato strategico chiave per il Gruppo. Il portafoglio prodotti di USP Group include marchi ben noti e apprezzati. USP Group e ADL Farmaceutici condividono valori e missioni simili: hanno sempre posto le persone e le loro esigenze al centro della loro attenzione.
SHC Advisor, nella persona di Filippo Ponsone, ha assistito ADL Farmaceutici, faci-
litando il processo di selezione di un partner commerciale e affinando il quadro della transazione aziendale, mentre USP Group è stato assistito durante le negoziazioni da Enlife Consulting tramite Gianluca Basso. Per la parte legale, ADL è stata seguita da LCA Studio Legale.
Antonio de Laurentiis assume la posizione di Ceo della nuova azienda ADL Unilab, la quale si occuperà di gestire il marketing della gamma di prodotti Olinorm per la linea ginecologica e alcuni prodotti dedicati alla linea urologica in Italia e in Europa.

Attualità 16 icf RIVISTA DELL’INDUSTRIA CHIMICA E FARMACEUTICA Febbraio/Marzo 2024
Guarnizioni per industria chimica e petrolchimica


GUARNIZIONI TRANCIATE E FUSTELLATE
Nella realizzazione delle guarnizioni in giunto è necessario tener conto di alcuni criteri fondamentali. In particolare: adattabilità alle superfici delle flange e alla loro eventuale irregolarità; impermeabilità agli agenti a contatto; resistenza alla pressione specifica. Nella scelta del tipo di giuntura da utilizzare occorre conoscere la natura degli agenti a contatto, la temperatura di esercizio e la pressione interna.

5500 TEXLON® PIATTINE SOFFICI AUTOADESIVE
Sono fogli di guarnizioni di qualità composti da puro PTFE espanso multidirezionale senza riempitivi, coloranti o inchiostri. Le guarnizioni prodotte da lastre Texlon® si adattano perfettamente alle superfici irregolari. Conforme alle norme FDA 21 CFR 177.1550 e testato in accordo con la normativa EC 19352004.

6630I TEXUNIVERSAL
Giuntura compressa esente amianto composta da fibre aramidiche e riempitivi termo-resistenti legati con NBR ad alto contenuto di acrilonitrile. Il materiale soddisfa i requisiti igienici degli impianti di trattamento delle acque.

5211 JOINTEX® RED
Giuntura in lastra di alta qualità, costituita da PTFE caricato con quarzo e pigmentato. Materiale innovativo sostitutivo delle tenute in amianto e dei convenzionali prodotti in PTFE.
RIVISTA DELL’INDUSTRIA CHIMICA E FARMACEUTICA icf 17 Febbraio/Marzo 2024
Texpack® srl - unipersonale - Via Galileo Galilei, 24 - 25030 Adro (BS) Italia Tel. +39 030 7480168 - Fax +39 030 7480201 - info@texpack.it - www.texpack.it
PAD. 2 - STAND S69
ESPONIAMO AL
Stefano Collatina eletto presidente di Egualia
Il successore di Häusermann: “Tra le priorità del settore dei farmaci equivalenti e biosimilari in Italia ci sono la compatibilità fra salute pubblica e sostenibilità industriale e la competitività dei farmaci maturi e fuori brevetto”.

Il neopresidente di Egualia Stefano Collatina
L’assemblea di Egualia – l’associazione dei produttori di farmaci equivalenti, biosimilari e Value Added Medicines – si è riunita a inizio marzo per rinnovare i propri organi istituzionali per il biennio 2024-2025.
Il Consiglio direttivo scelto dall’assemblea di Egualia ha eletto alla guida dell’associazione Stefano Collatina, presidente e amministratore delegato di Baxter Spa, affiliata italiana di Baxter Healthcare: il neo-eletto è anche responsabile della Business Unit Pharmaceutical Central&South Europe per i principali mercati europei, presidente del Cda di Baxter Srl che gestisce l’impianto di Compounding di Sesto Fiorentino. In oltre 20 anni ha ricoperto ruoli di crescente responsabilità a livello nazionale e internazionale. Prima di diventare presidente in Egualia ha ricoperto il ruolo di vice presidente e coordinatore del Gruppo italiano biosimilari.
Collatina subentra ad Enrique Häusermann – ininterrottamente alla guida dell’associazione, prima denominata Assogenerici, dal 2013 – che resta past president.
“Un’industria strategica per garantire l’accesso al farmaco”
”Mi sento particolarmente grato ad Enrique Häusermann per l’incredibile impegno di questi 11 anni che hanno trasformato l’industria dei farmaci equivalenti e biosimilari in Italia”, ha dichiarato il neopresidente Stefano Collatina. “Un’industria strategica per il ruolo centrale che ha assunto nel

garantire accesso al farmaco ed equilibrio economico alla spesa pubblica e che in 20 anni è arrivata a garantire oltre il 30% del fabbisogno farmaceutico nazionale. Il nostro comparto si prepara ad affrontare delle sfide importanti a partire da tre principali priorità: rendere compatibili gli interessi di salute pubblica con la sostenibilità industriale, rafforzare la competitività del settore dei farmaci maturi e fuori brevetto quale perno nell’accesso alle terapie croniche e guidare al meglio l‘implementazione di dossier europei cruciali sul fronte regolatorio e ambientale. Sono fiducioso che il dialogo avviato con questo Governo possa portare a programmare le migliori soluzioni per queste sfide”. In apertura dei lavori l’intervento del sottosegretario alla Salute, Marcello Gemmato, che ha auspicato il mantenimento del clima di dialogo e confronto instaurato dal Governo con i vertici di Egualia. “Dall’inizio del mandato abbiamo cercato di affrontare passo passo alcuni dei nodi principali del settore, a partire dall’insediamento del tavolo delle carenze: un fenomeno che abbiamo visto essere sovrastimato ed abbiamo fatto uno sforzo comune per interpretare questo momento. È stata affrontata con una norma già all’esame del Parlamento la richiesta delle aziende di riduzione del preavviso per la segna-
lazione delle carenze e siamo impegnati ad affrontare il tema della sostenibilità dei farmaci con un prezzo inferiore ai 5 euro”. Gemmato ha ricordato infine il tema cruciale della governance, da declinare attraverso lo spostamento di categorie dalla distribuzione diretta alla convenzionata, possibile secondo quanto previsto dalla norma della Legge di Bilancio 2024. “È un tema su cui il ministero sta lavorando anche su sollecitazione delle associazioni dei pazienti e che riteniamo particolarmente importante, perché rendere il farmaco accessibile serve ai pazienti ma serve anche a migliorare le performance del SSN”. Ad affiancare Collatina nel Consiglio di presidenza, nel ruolo di vicepresidenti, sono Umberto Comberiati (Teva Italia), Cinzia Falasco Volpin (Zentiva Italia) Davide Businelli (Lab. Farmacologico Milanese), Paolo Angeletti (S.A.L.F.), Massimiliano Rocchi (Accord Healthcare Italia), Salvatore Butti (EG - Stada), Fabio Torriglia (Viatris Italia), Marco Forestiere (Sandoz) e Riccardo Zagaria (DOC Generici). In qualità tesoriere dell’associazione, è stato confermato Giovanni Sala (Medac Pharma) Fanno parte del Consiglio direttivo anche Marco Pianta (Fresenius Kabi Italia), Fabio Scaccia (Farmitalia), Giorgio Oberrauch (Doppel Farmaceutici), Andrea Rottura (Towa Pharmaceutical).
Attualità 18 icf RIVISTA DELL’INDUSTRIA CHIMICA E FARMACEUTICA Febbraio/Marzo 2024
Nuovo medical director in Amgen Italia
Amgen Italia, filiale dell’azienda americana leader globale nelle biotecnologie mediche, ha una nuova responsabile della direzione medica. È Alessandra Brescianini, che subentra in questo ruolo a Maria Luce Vegna, che conclude il suo percorso professionale in azienda. Alessandra Brescianini, laurea in Medicina, Università degli studi di Brescia, ha praticato la professione medica in Francia in ematologia clinica, presso le strutture ospedaliere e universitarie di Marsiglia.
Approda in Amgen nel 2014, prima come medical advisor ematologia, con incarichi di responsabilità crescente in Francia, in seguito con ruoli internazionali in Svizzera.
In questo periodo, Brescianini è coinvolta direttamente nel processo di sviluppo del primo anticorpo bispe-
cifico con l’innovativa tecnologia BiTE, e oggi approvato in tutto il mondo per il trattamento della leucemia linfoblastica acuta, fino a entrare a far parte del team globale di Amgen impegnato su questo farmaco. “In Amgen ho sempre potuto coltivare il mio interesse verso la ricerca clinica, che ho considerato complementare alla mia formazione medica”, dichiara Alessandra Brescianini. “Oggi l’azienda mi offre la grande opportunità di ampliare e approfondire l’area del mio impegno, focalizzato sullo sviluppo dell’innovazione al servizio dei pazienti. So di poter contare sulle competenze di un team molto motivato, sul valore della ricerca clinica promossa da Amgen Italia e su una eccellente collaborazione con il mondo accademico italiano”.
Tra gli obiettivi della nuova Medical Director c’è, ai primi posti, quello di valorizzare ulteriormente il ruolo dell’Italia nello sviluppo clinico delle terapie più innovative di Amgen, che dispone oggi di una pipeline di R&D tra le più promettenti. L’attenzione si concentrerà in particolare in area cardiometabolica, dove si esploreranno ulteriormente le potenzialità terapeutiche di uno dei primi farmaci silenziatori dell’Rna, oltre che uno dei più ampi programmi di studi di Amgen in area obesità; in onco-ematologia, con le prime applicazioni della tecnologia dei bispecifici, fin qui utilizzata con successo in ematologia, nel campo dei tumori solidi, come quelli al polmone e alla prostata; nelle malattie rare, la più recente area di intervento di Amgen, con un focus sull’oculopatia tiroidea.






Le misure in ambiente farmaceutico secondo Swan






















AMI LineTOC Compact
Immediata rilevazione del trend senza costose analisi di laboratorio, semplice e ridotta manutenzione. Versione compatta, ideale per installazioni in spazi comuni di montaggio su skid di puri cazione o di distribuzione dell'acqua.
AMI Codes-II O 3
Metodo di misura colorimetrico standard secondo DIN 38408-3, dati af dabili anche in assenza prolungata di ozono.
Swan Analitica Srl ∙ IT-16167 Genova www.swananalitica.it swan@swananalitica.it
Attualità
E FARMACEUTICA icf 21 Febbraio/Marzo 2024
RIVISTA
DELL’INDUSTRIA CHIMICA
Acqua Farmaceutica
AMI Codes-II O
3
AMILineTOC Compact
Alessandra Brescianini

A Parma l’automazione intelligente e green
AI, sostenibilità e formazione saranno al centro della dodicesima edizione di SPS Italia, che continua a interpretare le tendenze più innovative che attraversano le industrie manifatturiere.
a cura di Alessandro Bignami
SPS Italia si appresta a vivere la sua dodicesima volta, consapevole di essere ormai il punto di incontro e confronto fra le aziende e le tendenze più innovative che stanno attraversando il settore dell’automazione industriale. Ecco perché non potranno che essere intelligenza artificiale, green manufacturing e nuove competenze i temi chiave dell’edizione 2024. Nell’avveniristica sala del MEET Digital Culture Center di Milano, a gennaio è stato dato il via al rush finale del percorso che nei prossimi mesi – fra tavole rotonde e ultime adesioni all’esposizione – por-
terà all’apertura dei padiglioni di Parma, dove si svolgerà, dal 28 al 30 maggio, la fiera dell’automazione e del digitale per l’industria intelligente e sostenibile.
Avviando la conferenza di presentazione, l’amministratore delegato di Messe Frankfurt Italia Donald Wich, pur consapevole dei complessi scenari globali, non ha mostrato dubbi: “Crediamo che quella del 2024 sarà una bellissima edizione, anche perché il settore viene da un anno positivo nonostante i conflitti internazionali e la recessione della Germania. La formazione sarà uno dei temi dei più interessanti che SPS intende affrontare, proponendosi come un punto d’incontro fra aziende e giovani. E ovviamente l’intelligenza artificiale sarà
una grande protagonista della manifestazione. Siamo felici del progetto – ha aggiunto Wich – che trova slancio innanzitutto nell’offerta tecnologica degli espositori e nelle collaborazioni con i partner, per una dodicesima edizione che, in continuità con le precedenti, sarà punto di riferimento e confronto sui risvolti della trasformazione ecologica e digitale delle imprese”. Tutti gli esponenti delle aziende coinvolte nella tavola rotonda di Milano hanno condiviso una certa preoccupazione per la prima parte del 2024 e la necessità di adeguarsi a cambiamenti sempre più veloci. Un’altra questione emersa durante il dibattito è stata quella femminile che, al di là di slogan e buone intenzioni, non è così facile da affrontare, soprattutto in un settore a prevalenza maschile come quello dell’automazione industriale. C’è anche un gap generazionale da colmare, per la difficoltà di trovare e inserire giovani preparati, ma anche per la convivenza non priva di incomprensioni fra le diverse generazioni.
20 icf RIVISTA DELL’INDUSTRIA CHIMICA E FARMACEUTICA
Appuntamenti
Anie Automazione: “Continua la crescita post-pandemica, anche se più lentamente”
Andrea Bianchi, presidente di Anie Automazione, ha ricordato come nel 2023 export e inflazione abbiano sostenuto i ricavi delle industrie italiane, pur nella consapevolezza di essere di fronte a un lungo periodo di incertezze: “Abbiamo confermato il nostro spazio istituzionale nel District 4.0; stiamo ora lavorando per definire i contenuti della collaborazione con OPC UA Foundation che sarà estesa quest’anno anche all’Associazione VDMA Automation, e alle novità editoriali che presenteremo in fiera tra cui una Guida sull’evoluzione delle tecnologie per interconnessione e controllo e la nuova edizione dell’Osservatorio 2023 con i dati del comparto. Secondo le ultime stime, prosegue il trend di crescita post pandemia del comparto, seppure con un aumento più contenuto del fatturato legato ad un andamento più frenato dell’ordinato nella seconda metà dell’anno. In generale, nonostante il permanere delle tensioni geopolitiche, i soci si esprimono con toni positivi per il 2024 grazie anche ad auspicati incrementi della domanda conseguente al nuovo piano di incentivi 5.0”.
In tour nei distretti italiani È già partita intanto SPS Italia On Tour, la rassegna di incontri sul territorio di avvicinamento alla fiera, per parlare di trasformazione digitale, attraverso i distretti produttivi: la prima tappa è stata Ancona, a cui seguiranno quella di Padova (27 marzo, Competence Center Smact) e Torino (17 aprile, Competence Center CIM4.0).
Tecnologie, percorsi ed eventi in sei padiglioni
A fine maggio nel quartiere espositivo di Fiere di Parma sei padiglioni presenteranno le soluzioni all’avanguardia per il comparto manifatturiero. A guidare il visitatore nel panorama delle nuove tecnologie ci sarà District 4.0, il percorso con demo funzionanti di robotica e meccatronica, Industrial IT & AI, Additive Manufacturing. Sustainable Innovation, all’ingresso del padiglione 4, aprirà l’itinerario con un’area dedicata alle soluzioni per la transizione green e l’energy efficiency. Sarà adiacente alla stampa 3D industriale, due ambiti con ampie potenzialità nella riduzione degli sprechi e la salvaguardia del pianeta. Al centro degli eventi, nelle arene Industry, Tech e Next, i principali trend del sistema industriale: intelligenza artifi-
ciale, Industry 5.0, sostenibilità, per citarne alcuni. Focus sul settore dell’additive manufacturing nel seminario Discover 3D Printing, secondo il format ideato da ACAM - Aachen Center for Additive Manufacturing e Formnext.
Il secondo volume del position paper Tra le novità di SPS Italia 2024 c’è la pubblicazione della seconda edizione del Position Paper. Un progetto a cui lavora il Comitato Scientifico della manifestazione, composto da oltre 150 realtà produttive italiane, per offrire linee guida utili alla comprensione dell’evoluzione tecnologica e digitale. In risposta al grande interesse espresso dal settore, il secondo volume completa con nuovi approfondimenti il precedente documento. Verrà presentato in fiera, insieme ai risultati di una survey condotta sul tema dell’AI.

“La seconda edizione si prefigge, dando seguito a quanto dichiarato nella prima, di integrare, modificare ed espandere i contenuti della sua prima uscita, ma anche e soprattutto di aggiungere nuove parti relative a tecnologie e loro modelli applicativi che, per motivi di spazio, la prima edizione del Position Paper non aveva affrontato o perché nel frattempo queste si sono mol- Un momento della tavola rotonda nel corso della presentazione di SPS Italia 2024 lo scorso gennaio a Milano. Hanno partecipato: Giorgio Ferrandino, managing director di SEW-Eurodrive; Stefano Gandolfi, regional marketing manager di Omron; Costantino Ghigliotti, amministratore delegato di Sick; Marcello Perini, ammnistratore delegato di Gefran
RIVISTA DELL’INDUSTRIA CHIMICA E FARMACEUTICA icf 21 Febbraio/Marzo 2024 Appuntamenti



La nuova area
“Education” punta l’attenzione sulla sfida della formazione e si rivolge alle generazioni che nei prossimi anni entreranno nella fabbrica digitalizzata
to sviluppate e/o consolidate e quindi hanno assunto un’importanza molto maggiore rispetto ad un anno fa”, ha commentato Oronzo Lucia, Scientific Coordinator Comitato Scientifico SPS Italia. “Nella seconda edizione del Position Paper verranno anche riportati i risultati della Survey sulla AI. Anche questa volta è stata mantenuta la regola per cui la bussola che guida il documento deve indicare tutti gli aspetti che circondano gli argomenti trattati, cercando di analizzare sia gli aspet-
ti potenzialmente positivi che quelli che vanno ad aggiungere complessità e/o criticità. Nella frenesia del business è facile dare priorità alla velocità, ma non sempre questo è ciò che veramente può portare benefici all’organizzazione, la chiave del successo starebbe invece nell’avere una chiara direzione. Andare molto veloci, ma nella direzione sbagliata non può aiutare. Essere guidati da una visione strategica porta molti più frutti perché presuppone un percorso studiato e condiviso. Lo sviluppo della tecnologia e il business reale viaggiano in modo indipendente e solo con una visione chiara si possono trovare le connessioni per far convergere necessità e benefici ottenibili. Non possiamo immaginare completamente il futuro, ma il Position Paper può dare una guida per identificare le tecnologie e la loro maturità valutandone gli impatti e prevedendo la loro capacità di generare valore”.
Education: scuola e industria si incontrano al padiglione 8 Nell’ambito di District 4.0, con accesso dedicato nel padiglione 8, la nuova area “Education” si rivolge alle generazioni che nei prossimi anni entreranno nella fabbrica digitalizzata. Uno spazio in continuità con l’impegno di SPS Italia nell’accorciare le distanze tra scuola e industria. L’Arena Next sarà palcoscenico di incontri e laboratori organizzati da espositori e partner rivolti ai ragazzi di università e istituti tecnici. Prosegue l’iniziativa “Lezioni in fiera” come risposta concreta al mismatch delle competenze. Sempre attivo il Live Streaming per le scuole in occasione degli incontri di SPS Italia On Tour.
Dalle start-up tante idee per il manifatturiero
Al mondo delle Start-Up e delle PMI innovative, presenti con un’area espositiva nel padiglione 7, è dedicata SPS Italia Up Challenge, una nuova competi-
zione che premia con uno stand in fiera le cinque realtà con i progetti più interessanti in ambito manifatturiero. In questo contesto si inserisce anche Access2Tech South. L’Arena Next ospiterà l’iniziativa sviluppata da EIT Manufacturing con il supporto di SPS Italia per mettere in contatto le principali aziende presenti in fiera con le startup manifatturiere europee più performanti e innovative.
She SPS Italia
Con She SPS Italia, la fiera affronta la questione del gender gap, che nel mondo industriale risulta ancora ampio da colmare. Un progetto per diffondere storie di mentorship al femminile ed evidenziare le opportunità legate alle figure professionali emergenti. SPS Italia ha istituito un premio e creato sinergie con associazioni, docenti universitarie e community di riferimento, con la comune volontà di promuovere il cambiamento. Il primo appuntamento di networking di She SPS Italia ha preceduto la conferenza stampa della manifestazione il 16 gennaio a Milano.
Contro la plastica in mare SPS Italia si impegna a favore della sostenibilità in collaborazione con One Ocean Foundation, fondazione senza scopo di lucro nata con l’obiettivo di accelerare soluzioni per le problematiche dell’oceano e di promuovere una blue economy sostenibile. La fiera supporta attivamente il progetto “NoPlasticIntheOcean” per contrastare l’inquinamento marino derivante da plastica e microplastica in paesi in via di sviluppo. L’impegno è di raccogliere cinque tonnellate di plastica nel 2024. Sempre in collaborazione con One Ocean Foundation, SPS Italia condurrà una survey volta a raccogliere dati e sensibilizzare la comunità dell’automazione e del digitale per l’industria riguardo alle questioni legate all’economia circolare e alla tutela dell’ambiente marino.
22 icf RIVISTA DELL’INDUSTRIA CHIMICA E FARMACEUTICA Appuntamenti
BEHIND GREAT

RAW MATERIALS SATISFACTION ARE ALWAYS GREAT
AGENTI FILMANTI - DISGREGANTI - LUBRIFICANTI - GLIDANTI - LEGANTI - DILUENTI - OPACIZZANTI - AMIDI E DERIVATIPOLIALCOLI - ZUCCHERI - DOLCIFICANTI - VISCOSIZZANTICONSERVANTI - CORRETTORI DI PH - ANTIAGGLOMERANTI - PRINCIPI ATTIVI - PLASTICIZZANTI
Gli eccipienti e le materie prime distribuite da Faravelli ti aiutano a raggiungere la formulazione farmaceutica perfetta, proprio quella che stai cercando: funzionale, sicura, efficace, performante. La formula che rende ogni cliente soddisfatto e felice.
“Accompagniamo con competenza globale e sensibilità locale i nostri partner verso scelte innovative, per formulare il futuro con ingredienti e soluzioni affidabili e sostenibili”.
VIA MEDARDO ROSSO, 8 - 20159 MILANO - WWW.FARAVELLI.IT - PHARMA@FARAVELLI.IT
#FaravelliPharmaDivision APIs? NOW WE CAN!
Al Simposio AFI le sfide dell’industria farmaceutica
Si terrà al Palacongressi di Rimini il 63esimo Simposio AFI, intitolato “Le Sfide dell’Industria Farmaceutica: Ricerca, Innovazione, Sostenibilità”.
Nella magnifica cornice di Palazzo Clerici a Milano, in una sala gremita di partecipanti, si è tenuta lo scorso febbraio la serata di presentazione, che ha introdotto i contenuti scientifici e gli aspetti organizzativi dell’evento.
Riconfermati i corner istituzionali, situati al centro dell’area espositiva e dedicati alle associazioni di categoria, che quest’anno saranno ancora più numerosi: un’ulteriore dimostrazione dell’importanza del Simposio, evento dell’Associazione Farmaceutici Industria che da 60 anni coinvolge tutti gli stakeholder del mondo pharma a livello nazionale ed è un’essenziale occasione di confronto sulle novità e sulle prospettive dell’industria del farmaco.
Il fil rouge che unirà tutte le sessioni scientifiche sarà costituito dalle parole ricerca, innovazione e sostenibilità. Tematiche di estrema attualità che rappresentano le sfide imprescindibili che il mondo della salute deve affrontare.
Il programma, illustrato dal presidente dell’AFI Giorgio Bruno, prevede 19 Sessioni Scientifiche che, come di consueto. saranno il risultato delle attività dei vari gruppi di studio AFI e toccheranno quindi molte aree tematiche: energia e sostenibilità, supply chain, materiali di confezionamento, salute digitale, ricerca clinica, qualità, HTA, deblistering, environmental risk assessment, dispositivi medici, biotech, farmacovigilanza, pubblicità e IMS, scienze farmaceutiche, parenterali, innovazione, API, produzioni speciali.
Il programma prevede due Lectio Magistralis di altissimo profilo, tenute da Marcello Cat-

tani, presidente di Farmindustria e Sanofi Italia, e da Elena Cattaneo, farmacologa e biologa di fama internazionale e senatrice a vita della Repubblica, che interverrà sul tema della ricerca. Il Programma del Simposio include workshop digitali e fisici, che daranno spazio alle aziende e a tutte le novità del settore:
La Piazza delle Start Up - Una sessione in cui le nuove realtà che operano nell’ambito del farmaco, dei Medical Device, della tecnologia e della terapia digitale possono presentare la propria attività e i propri progetti. La Piazza delle Donne - Continua anche quest’anno il viaggio nel mondo delle donne del pharma-biotech con testimonianze di passione, intraprendenza, intelligenza e sapiente capacità di
A Bergamo una giornata per l’automazione
Il 17 aprile alla Fiera di Bergamo torna l’appuntamento dedicato all’innovazione industriale con Save, la mostra convegno verticale dedicata all’automazione industriale e di processo, alla strumentazione e sensoristica e alle tecnologie 4.0. Save Bergamo è un’occasione per scoprire le ultime Innovazioni nell’ambito dell’automazione industriale, con approfondimenti dedicati al tema dell’intelligenza artificiale applicata alla produzione, con sessioni che si concentreranno su solu-
collaborazione.
La Sessione Poster - la Sessione Poster prevederà come di consueto la presentazione di lavori originali, su argomenti che interessano l’intera filiera dei farmaci.
Riconfermata e ulteriormente ampliata l’Area Espositiva (con ben 141 stand a disposizione degli espositori), in cui la disposizione degli spazi è stata espressamente concepita per garantire una modalità di visita più interattiva, dinamica e personalizzata, per agevolare le opportunità di networking e di creazione di business.
L’accesso sarà a pagamento per le Sessioni Scientifiche e sarà invece gratuito per l’area espositiva, la Piazza delle Startup, la Piazza delle Donne del Pharma, la Sessione Poster.
industriale
zioni per migliorare l’efficienza delle operazioni industriali. L’intelligenza artificiale sta rivoluzionando il mondo industriale, introducendo nuove frontiere di efficienza, produttività e innovazione. Nel cuore di questa trasformazione, troviamo soluzioni avanzate che rendono possibile un futuro più competitivo: automazione intelligente, manutenzione predittiva e ottimizzazione dei processi sono solo alcune delle applicazioni che stanno ridefinendo le regole del gioco nell’industria.
Save Bergamo ospiterà il convegno su Intelligenza Artificiale e 4.0 per l’industria, coordinato da Armando Martin, giornalista e scrittore scientifico, dedicato alle sfide e alle opportunità dell’AI e alle nuove soluzioni del 4.0 per l’industria. Nel corso della sessione saranno presentati modelli applicativi e organizzativi dell’IA in ambito industriale, una panoramica su Industria 4.0 coniugando nuovi modelli organizzativi e produttivi con le tecnologie più innovative.
Appuntamenti 24 icf RIVISTA DELL’INDUSTRIA CHIMICA E FARMACEUTICA


La prima pompa a girante flessibile con sistema di drenaggio per la sanificazione.
Design igienico, in conformità alle buone norme di fabbricazione per macchine destinate ai settori alimentare e farmaceutico.
igh quality materials
Materiali di alta qualità, idonei all’uso a contatto di alimenti. ygienicdesign
yper versatility
La stessa pompa può trattare prodotti liquidi e anche molto densi, dall’acqua alle creme e gel.
WWW.WOLHFARTH.IT
Achema 2024: spazio al dialogo tra scienza e industria con oltre 750 conferenze
“Il dialogo fra scienza e industria è sempre stato il credo di Dechema e in Achema trova una pratica viva grazie al programma di conferenze e congressi”, afferma Andreas Förster, direttore esecutivo di Dechema, che organizza la principale fiera al mondo delle tecnologie per l’industria di processo. “Il successo ci dà ragione: gli oltre 20.000 partecipanti ai congressi nel 2022 ha nettamente superato quelli dell’edizione 2018, che aveva fino a quel momento avuto il maggior numero di registrazioni”.
Il programma congressuale di quest’anno si concentra sui temi dell’idrogeno, della sostenibilità, dell’economia circola-
L’AGENDA
Making Pharmaceuticals
26-27 marzo 2024
Milano www.makingpharma.it
Analytica
9-12 aprile 2024
Monaco, Germania www.analytica.de
Helsinki Chemical Forum
10-11 aprile 2024
Helsinki, Finlandia helsinkichemicalsforum.messukeskus.com
SAVE Bergamo
17 aprile 2024
Bergamo www.exposave.com
Cosmofarma
17-19 aprile 2024
Milano www.cosmofarma.com
re e della digitalizzazione. Nei sei Innovation Stages della fiera e nelle cinque sessioni clou del congresso, Achema 2024 affronterà questi e altri temi dell’industria di processo.
Il GEA Process Innovation Stage nel padiglione 9.0 si concentrerà su temi quali l’elettrificazione, la flessibilità e l’evoluzione biotecnologica dei processi chimici, nonché sui contributi delle tecnologie digitali intelligenti nella costruzione e nel funzionamento degli impianti. Nella sessione “La natura come modello - massima efficienza delle risorse nell’industria chimica”, gli esperti discuteranno della visione di un’industria chimica piena-
CPhI Japan
17-19 aprile 2024
Tokyo, Giappone www.cphi.com/japan/en/home.html
Interphex
18-24 aprile 2024
New York City, Usa www.interphex.com
Pharmap
22-23 aprile 2024
Amsterdam, Paesi Bassi www.pharmap-congress.com
CPhI North America
7-9 maggio 2024
Philadelphia, Usa www.cphi.com/northamerica/en/home.html
IVS
15-16 maggio 2024
Bergamo www.industrialvalvesummit.com
mente efficiente in termini di risorse.
Lo ZETA Pharma Innovation Stage nel padiglione 4.1 riguarderà la produzione biofarmaceutica oltre a molti altri argomenti relativi alla produzione e al confezionamento farmaceutici, che saranno anche al centro della Pharma Highlight Session di lunedì 10 giugno. Con il titolo “Produzione farmaceutica di prossima generazione: attuali progressi nella terapia cellulare e genica”, la Pharma Highlight Session esaminerà da vicino la produzione centralizzata e decentralizzata di terapie cellulari e le attuali sfide della ricerca traslazionale e della commercializzazione
Packaging Première
21-23 maggio 2024
Milano
www.packagingpremiere.it
SPS Italia
28-30 maggio 2024
Parma www.spsitalia.it
Solids
5-6 giugno 2024
Parma www.solids-parma.de
Achema
10-14 giugno 2024
Francoforte, Germania www.achema.de
MedPharmPlast Europe
12-13 giugno 2024
Malmo, Svezia www.medpharmplasteurope.org
Chemspec Europe
19-20 giugno 2024
Düsseldorf, Germania www.chemspeceurope.com
delle terapie.
Oggi più che mai, il successo in laboratorio è determinato dal le tecnologie utilizzate e nelle interfacce tra ingegneria e pro duzione. Questo è il focus del le presentazioni al Lab Innova tion Stage nel padiglione 12.0. Oltre al Lab Innovation Stage, Achema 2024 presenterà anche un’area operativa dedicata al laboratorio digitalizzato, miniaturizzato e automatizzato del futuro. Oltre alle innovative applicazioni bioanalitiche e (bio)farmaceutiche, verranno messi in risalto anche la sostenibilità, nonché la pianificazione, la costruzione, le attrezzature e il funzionamento dei laboratori.

CPhI South East Asia
10-12 luglio 2024
Bangkok, Thailandia www.cphi.com/sea/en/home.html
Farmaforum
25-26 settembre 2024
Madrid, Spagna www.farmaforum.es
CPhI Milano 8-10 ottobre 2024
Milano europe.cphi.com
Analytica China
18-20 novembre 2024
Shanghai, Cina www.analyticachina.com.cn/en-us
Pharmintech
27-30 maggio 2025
Milano www.pharmintech.it
Appuntamenti 26 icf RIVISTA DELL’INDUSTRIA CHIMICA E FARMACEUTICA
Process Service

37 anni di esperienza al servizio della chimica fine e dell’industria farmaceutica.
Impianti di chimica fine
Purificazioni per alte purezze
Reparti di produzione APIs in Bulk Linee di produzione sterili (Bulk, filling & lyophilization)
Impianti biofarmaceutici (Fermentazioni, DSP, mAbs)
Reparti di produzione API Altamente Attivi (HP API)
Progettazione Sistemi Utilities e Clean Utilities
REPARTI DI PRODUZIONE ALTAMENTE ATTIVI (HP APIs)
Laboratori R&D e QC Kilolabs




Small Scale



Impianti ad altissimo contenimento validato fino a 10 nanogrammi/m3 YOUR PHARMA ENGINEERING PARTNER Via A. De Gasperi 111, 20017 Rho (MI) | Tel. +39 02 93909272 | Email info@process-service.it | www.process-service.it
Radiofarmaco per il rilevamento di placche amiloidi cerebrali
GE HealthCare, azienda esperta nell’innovazione della tecnologia medica, della diagnostica farmaceutica e delle soluzioni digitali, ha stretto un accordo con il Centro La Maddalena – centro d’eccellenza attivo da più di 15 anni sul territorio siciliano
come Officina Farmaceutica – per la produzione di un radiofarmaco marcato con F18 (Fluoro 18) per il rilevamento di placche amiloidi cerebrali. Questo accordo rappresenta un grande passo avanti per la fruibilità degli esami PET in tutta l’isola: si tratta infatti del primo centro che produrrà in Sicilia il biomarcatore e renderà accessibili ai centri di medicina nucleare siciliani ed ai pazienti esami che prima non era possibile eseguire in loco.
La Tomografia a emissione di positroni (PET Positron Emission Tomography) è un esame che comporta la somministrazione per via endovenosa di una sostanza normalmente presente nel nostro organismo come, ad esempio, il glucosio o altre molecole target specifiche, che vengono
marcate con una sostanza radioatti va detta radiofarmaco. Questo esame funzionale è molto importante per ché è in grado di rilevare i processi biologici legati ad una specifica ma lattia. Il radiofarmaco è l’elemento principale per la riuscita dell’esame, ma è al contempo quello di maggior deperibilità, poichél’efficienza si de teriora in breve tempo (circa 8 ore dalla produzione).
Il progetto di collaborazione tra GE HealthCare e il centro palermitano è iniziato nel 2020, ma per poter ini ziare la produzione del radiofarmaco, La Maddalena ha dovuto richiedere un adeguamento all’AIFA che ha au torizzato la produzione di farmaci in asepsi e successivamente l’ulteriore green light dalla marketing authori zation a livello europeo (EMA).
Chiesi aggiorna i risultati sullo studio della malattia di Fabry
Chiesi Global Rare Disease, business unit del Gruppo Chiesi nata per offrire terapie e soluzioni innovative alle persone con malattie rare, annuncia la pubblicazione dei dati di Fase 3 dello studio Balance che valuta l’efficacia, sicurezza e tollerabilità del pegunigalsidasi alfa verso agalsidasi beta in pazienti adulti con Malattia di Fabry trattati in precedenza con agalsidasi beta e con deterioramento della funzionalità renale. I risultati sono stati pubblicati nella peer-reviewed del Journal of Medical Genetics (“Head-to-head trial of pegunigalsidase alfa versus agalsidase beta in patients with Fabry di-
sease and deteriorating renal function: results from the 2-year randomised phase III Balance study” Wallace EL, et al. J Med Genet 2023; doi: 10.1136/jmg2023-109445).
Pegunigalsidasi alfa, una terapia enzimatica sostitutiva (enzyme replacement therapy-ERT) PEGilata, è una forma ricombinante dell’enzima alfa-galattosidasi A umano, espresso in colture di cellule vegetali, approvata negli Stati Uniti, Unione Europea e Gran Bretagna per il trattamento di pazienti adulti affetti dalla malattia di Fabry.
“Questo studio rappresenta una fonte importante di nuove evidenze cliniche poi-
ché è il più recente studio randomizzato, controllato, in doppio cieco testa a testa fra terapie enzimatiche sostitutive nella malattia di Fabry”, afferma Antonio Pisani, professore di Nefrologia dell’Università degli Studi di Napoli Federico II. “I risultati hanno prodotto nuove evidenze di valore relative all’efficacia e sicurezza di pegunigalsidasi alfa confrontata con agalsidasi beta valutate per un periodo di trattamento di due anni”. “C’è ancora una generale mancanza di conoscenza e una scarsa consapevolezza delle numerose e peculiari sfide che le persone con malattia di Fabry devono affrontare”, dichiara Giacomo
Chiesi, responsabile della Chiesi Global rare Disease. “Questo studio, che è il più recente clinical trial di ER Ts head to head, randomiz zato, in doppio cieco, non si sarebbe potuto realizza re senza il supporto dei ri cercatori, dei pazienti e del le loro famiglie che hanno dedicato due anni della lo ro vita a questa importan te ricerca per la cura della malattia di Fabry. Siamo or gogliosi di poter fornire al le persone che soffrono di questa patologia una op zione terapeutica ulterio re e continueremo il nostro impegno nei confronti dei milioni di persone che nel mondo soffrono di patolo gie rare”.

28 icf RIVISTA DELL’INDUSTRIA CHIMICA E FARMACEUTICA
Industria farmaceutica











Ricerca
Spark Pisa compie 5 anni
Dal 2019 finanzia progetti innovativi sviluppati da gruppi di ricerca dell’Università di Pisa attivi nel settore medico-farmaceutico. È Spark Pisa, il primo nodo italiano della rete internazionale “Spark Global”, fondata dalla Stanford University, che ha da poco compiuto cinque anni di attività e i cui membri si sono riuniti a Pisa per un primo bilancio e per definire gli obiettivi del futuro. Incontro a cui hanno preso parte anche Daria Mochly Rosen dell’Università di Stanford, presidente della rete globale “Spark” e ideatrice dell’iniziativa, Corrado Pria-

mi, prorettore dell’Ateneo pisano per la valorizzazione della conoscenza e suo impatto, e Maria Letizia Trincavelli, direttrice del Dipartimento di Farmacia dell’Università di Pisa e vicedirettrice di Spark Pisa.
“Per l’Università di Pisa è un onore essere entrati, per primi in Italia, a far parte della rete Spark che riunisce alcuni dei più prestigiosi centri di ricerca traslazionale al mondo”, ha commentato Corrado Priami. “Ogni anno, attraverso Spark Pisa, il nostro Ateneo sostiene, attraverso un apposito bando, un Proof of Concept (PoC) al fine di favorire il passaggio dall’idea al prototipo funzionante e arrivare, così, al trasferimento verso le imprese o il mercato, favorendo in questo mondo il trasferimento tecnologico”. Sei i PoC finanziati dal 2019 al 2023, tra innovativi metodi di diagnosi basati sull’AI a nuovi sistemi di prevenzione e cura di malattie come il diabete o
la Retinite Pigmentosa. Il primo, in ordine di tempo, è stato il progetto “NeurATy” (Neuroprotection and Anti-inflammatory activity of TSPO ligands), che propone l’utilizzo di una particolare molecola in grado di legare la proteina TSPO per il trattamento dello stato infiammatorio in soggetti affetti da Retinite Pigmentosa, con l’obiettivo di proteggere i neuroni e mantenere la vista. È stata poi la volta del progetto “DROP” (Digital Research in Oncologic Pathology), che mira a sviluppare e convalidare un innovativo strumento, basato sull’AI, in grado di analizzare le immagini digitali tratte dai vetrini di pazienti affetti da cancro. Si propone, invece, di sviluppare un sensore come strumento specifico per valutare la presenza e la quantità di proteine virali in fluidi biologici il progetto “FACT” (Fret sensor for the Assessment of Coronavirus Titre”).
Offre una nuova metodologia di prevenzione della disfunzione endoteliale indotta dal dia-
bete “Melodie” (Metformin-isothiocyanate: a noveL apprOach to prevent Diabetes-Induced Endothelial dysfunction) che ha vinto il bando nel 2021. Nel 2022 è stata poi la volta di “PROMET” (progetto che si ponte come obiettivo quello di valutare l’utilità clinica del DNA tumorale derivato (ctDNA) circolante come marcatore del parametro della malattia minima residua (MRD), o malattia residua misurabile, che definisce quante cellule neoplastiche rimangono dopo la resezione chirurgica delle metastasi epatiche del cancro del colon-retto (CRLM).
Infine, “Gene Destiny” (GENomic approach integratED with artificial intelligencE for the management of Small cell lung cancer patients Treated with ImmuNotherapY) mira a convalidare una firma genetica come biomarcatore predittivo indipendente per la risposta alle terapie chemio-immunologiche nei pazienti con carcinoma polmonare a piccole cellule (SCLC).
UniTo inaugura la biobanca di neuroscienze “Davide Shiffer”
Il Dipartimento di Neuroscienze “Rita Levi Montalcini” dell’Università di Torino – due volte Dipartimento di Eccellenza (2018-2022, 2023-2027) – ha inaugurato la Biobanca intitolata a Davide Schiffer (19282020), neurologo torinese di fama internazionale.
La biobanca di neuroscienze “Davide Schiffer” raccoglierà campioni biologici (sangue, DNA, liquor, cellule, tessuti) per metterli a disposizione dei ricercatori, al fine di favorire nuove conoscenze e individua-
re nuove terapie, operando in un ambito particolarmente delicato, quello sanitario, dove è necessario implementare precise procedure e criteri di qualità a livello di strutture, processi e personale, volti a garantire i diritti delle persone coinvolte e della collettività.
La biobanca è una unità di servizio finalizzata alla raccolta organizzata, processazione, conservazione e distribuzione di campioni biologici e di dati correlati, per finalità di ricerca e di diagnosi.

Lo scoprimento della targa con Alessandro Mauro, direttore del Dipartimento di Neuroscienze “Rita Levi Montalcini”, e Isabella Schiffer

30 icf RIVISTA DELL’INDUSTRIA CHIMICA E FARMACEUTICA
C M Y CM MY CY CMY K
NUOVO
CONTROLLO MULTIPLO DELLA MESSA A TERRA
SG/E-MGS01-V1 (EX)
Scarica elettrostatica sicura delle postazioni collegate
Possibilità di collegare a terra fino a 10 postazioni
Processo di carica o scarica a contatto libero dal potenziale
Conforme a IEC/TS60079-32-1 e NFPA77
Certificato ATEX e IECEx
Livello di sicurezza SIL2

◆ ◆ ◆ ◆ ◆ ◆
RadiciGroup presenta il suo piano di sostenibilità

Un progetto ambizioso, ideato per valorizzare la trasparenza e l’impegno di RadiciGroup nello sviluppo di un business responsabile lungo tutta la catena del valore sotto il profilo economico, sociale ed ambientale e per essere focalizzati sulle richieste normative in materia di sostenibilità sempre più capillari e stringenti. Sono queste le caratteristiche e le finalità del piano di sostenibilità presentato dal Gruppo e denominato “From Earth to Earth”, proprio per sottolineare l’intento di mettere al centro l’attenzione verso la Terra e le future generazioni. Il documento si colloca all’interno di una strategia di più ampio respiro. RadiciGroup è, infatti, da molto tempo impegnata su numerosi temi di carattere ambientale e sociale e sta strutturando sempre più la propria gover-
nance secondo i principi ESG, come dimostrato anche dai risultati messi in luce nell’annuale Bilancio di Sostenibilità, che quest’anno giungerà alla ventesima edizione.
Il progetto è il risultato di un impegno pluriennale svolto in collaborazione con Deloitte, che ha consentito di avere un punto di vista esterno e oggettivo sulla definizione di target e temi materiali. Non è stato però costruito a tavolino, ma è frutto di una capillare attività di ascolto degli interlocutori interni ed esterni esperti di sostenibilità, che hanno definito una rosa di temi strategici sia per il Gruppo che per i suoi principali stakeholder. Questi sono stati poi analizzati nel dettaglio da tavoli di lavoro tematici per individuare gli obiettivi nei tre ambiti Environmental, Social e Governance e le relative azioni concrete per raggiungerli, in linea con le politiche europee di decarbonizzazione e transizione energetica e con i target di sviluppo sostenibile delle Nazioni Unite, fonte di orientamento a livello mondiale. In particolare, tra gli obiettivi ambientali si evidenziano l’incremento del 20% e la differenziazione del consumo di energia elettrica proveniente da fonti rinnovabili, l’abbattimento
dell’80% entro il 2030 delle emissioni dirette totali di gas serra rispetto al 2011, l’attenzione al consumo delle risorse idriche per limitare l’impatto sulle comunità locali e la biodiversità, l’estensione al 70% dei prodotti, in termini di peso, realizzati a livello di Gruppo della misurazione attraverso la metodologia Life Cycle Assessment (LCA), la collaborazione tra i vari attori delle filiere in logica di eco-design e la ricerca di soluzioni di packaging sempre più sostenibili e circolari. Gli obiettivi per gli aspetti sociali si concentrano invece sul miglioramento del benessere, della salute e della sicurezza dei dipendenti attraverso la formazione e il coinvolgimento dei collaboratori, sulla sicurezza in ambito informatico implementando soluzioni digitali all’avanguardia, sullo sviluppo delle relazioni con le comunità locali e sulla valorizzazione del rapporto con gli istituti scolastici per favorire l’inserimento dei giovani nel mondo del lavoro e la crescita dei talenti. Infine, dal punto di vista della governance, il Gruppo punta sulla creazione di valore lungo tutta la value chain per favorire la continuità del business, sulla massima condivisione dei valori del Gruppo e sulla gestione responsabile della catena di fornitura.
Il programma europeo per la decarbonizzazione delle imprese
Supportare progetti di decarbonizzazione dei sistemi produttivi e iniziative legate alla produzione dell’idrogeno rinnovabile. Questo l’obiettivo dell’infoday nazionale sul programma di finanziamento dell’Unione europea “Innovation Fund”, che si è tenuto a Roma presso la sede di Confindustria. L’evento è stato organizzato dal Mini-
stero dell’Ambiente e della Sicurezza Energetica (MASE), in collaborazione con ENEA e Confindustria, con il fine di presentare lo strumento di finanziamento e di promuovere la partecipazione delle imprese italiane, rendendo l’Italia sempre più protagonista di questo strumento.
“I nuovi bandi del Fondo mettono a
disposizione un budget di 4,8 miliardi di euro derivanti dai proventi del sistema EU-ETS. Attualmente l’Innovation Fund supporta 12 progetti in Italia, per un budget complessivo di circa 170 milioni di euro”, ha spiegato Giulia Monteleone, direttrice del Dipartimento ENEA di Tecnologie energetiche e fonti rinnovabili.
Ambiente 32 icf RIVISTA DELL’INDUSTRIA CHIMICA E FARMACEUTICA
Covestro punta a ridurre le emissioni scope 3
Covestro ha pubblicato i suoi obiettivi per la neutralità climatica relativi alle emissioni scope 3, completando la propria strategia di riduzione delle emissioni di gas serra. Come obiettivo di breve termine, l’azienda prevede di ridurre le emissioni di gas serra di 10 milioni di tonnellate entro il 2035. Questo corrisponde a una diminuzione del 30% in confronto al 2021, anno di riferimento, includendo già anche le emissioni legate alla crescita. Nel lungo termine, Covestro prevede di raggiungere la neutralità climatica a livello di emissioni scope 3 entro il 2050.
Nel 2022 Covestro aveva già pubblicato i propri ambiziosi obiettivi legati alle emissioni scope 1 e scope 2, fra i quali raggiungere la neutralità climatica operativa entro il 2035. Le emissioni scope 1 derivano dai processi produttivi aziendali, mentre le emissioni scope 2 sono legate alle fonti
Listello passacavo per l‘industria alimentare
Listello passacavo per cavi con connettore per l‘industria alimentare con grado di protezione IP65, compatibile con le aperture dei connettori industriali.
IP65
dell’energia che viene acquistata. Le emissioni scope 3 includono tutti gli altri gas serra prodotti nella filiera sia a monte che a valle. Questi compongono circa l’80% delle emissioni totali di gas serra dell’azienda. Le materie prime acquistate da Covestro sono responsabili della maggior parte delle emissioni scope 3.
Ridurre le emissioni scope 3 comporterà la trasformazione di tutta la filiera. Una grande varietà di fattori si influenzano reciprocamente – fra questi la disponibilità di materie prime alternative, di energie rinnovabili, di innovazioni tecnologiche e nuovi processi, così come le trasformazioni del mercato – e giocano un ruolo in questo processo. Per raggiungere le zero emissioni, Covestro prevede di fare investimenti mirati di diverse centinaia di milioni di euro nei prossimi 10 anni. Nella sua strategia per il clima, nel breve e medio termine Covestro si sta concentrando

in particolare su quattro categorie legate alle emissioni scope 3. Lavorando su queste quattro categorie, che insieme fanno 21,3 milioni di tonnellate di gas serra per anno (riferite all’anno base 2021), Covestro sarà in grado di ridurre le emissioni scope 3 di 10 milioni di tonnellate entro il 2035. Per fare questo, Covestro ha identificato quattro leve chiave. I progetti collegati sono già in corso, con in arrivo l’implementazione di ulteriori misure concrete.

Ti interessa?
Richiedi ora il tuo campione gratuito

Ambiente
www.icotek.com in progress
Dieci anni di affidabilità al servizio del pharma
a cura di Marzia Savino

L’ampliamento dei servizi e delle risorse ha permesso a PVS Group di proporsi come un partner di riferimento nelle attività di qualifica e convalida lungo l’intera filiera farmaceutica.
In attesa del Compliance Day 2024, i responsabili dell’area Sales & Business Development raccontano come la società ha saputo consolidare il rapporto di fiducia con il mercato.
Partito dai servizi di consulenza e qualifica per produzioni API e HPAPI, il Gruppo PVS (Process Validation Service) ha esteso in pochi anni l’attività lungo l’intera filiera farmaceutica, crescendo a livello di esperienze e risorse e affrontando sfide sempre più complesse. L’apertura di tre sedi, la partecipazione e l’organizzazione di eventi di divulgazione tecni-
co-scientifica, l’ampliamento dei servizi con la fondazione della società SolTech rendono PVS una realtà molto attiva sul territorio e in grado di costruire relazioni positive. Per conoscere meglio l’approccio del Gruppo al mercato, abbiamo rivolto alcune domande a figure chiave dell’area Sales & Business Development: Stefano Moltani, Chiara Mariani e Manfredi Musmarra.
Stefano Moltani, può descriverci il valore aggiunto e le competenze che hanno costruito finora l’identità del Gruppo PVS?
Moltani: “In questi dieci intensi anni di attività, l’azienda è stata in grado di interpretare le richieste dei vari clienti, spendendosi sempre per ricercare soluzioni e supportando le esigenze volte a finalizzare le aspettative dei ‘goal’ di progetto in termini di tempistiche e qualità. Sulla base delle pregresse esperienze dei soci fondatori – Rodolfo Russo, Antonino Manoli, Antonio Santisi – l’azienda ha mosso i primi passi nell’erogazione di servizi consulenziali e di qualifica per impianti di produzione API e HPAPI e la correlata automazione (DCS, SCADA, PLC/HMI, sistemi di registrazione…), sia per progetti di tipo green field o legati a revamping, o per attività di mantenimento routinarie. I buoni risultati ottenuti hanno permesso a PVS di introdurre molte risor-
34 icf RIVISTA DELL’INDUSTRIA CHIMICA E FARMACEUTICA
Convalida

se: questo ci ha proiettati progressivamente a operare all’interno di tutta la filiera farmaceutica, acquisendo sempre più esperienza e opportunità di confronto con nuove sfide. Direi che i plus aziendali rimangono la flessibilità, la dinamicità e l’affidabilità. Ovviamente la qualità resta un elemento imprescindibile della nostra attività”.
Quali sono stati i principali risultati raggiunti in questi primi dieci anni e quali le prossime tappe?
Moltani: “Nel primo anno di operatività, le risorse e la strumentazione erano più ‘misurate’, mentre oggi l’organico di PVS sta per raggiungere le 50 unità e il nostro parco strumenti è diventato importante in termini di ti-
spingono a impegnarci ancora di più. Ripensando al nostro percorso, i risultati sono stati moltissimi, anche a livello di struttura aziendale. Negli anni abbiamo aperto ben tre sedi: a Paderno Dugnano (MI), Vicenza e Latina. Dal primo piccolo ufficio in affitto, oggi la sede centrale di Paderno Dugnano è di nostra proprietà e occupa una superficie di oltre 600 m2. Un importante risultato, anche sotto il profilo patrimoniale, che racconta l’impegno e la volontà di creare un ambiente sereno e di confronto. Negli anni qui sono cresciuti professionisti esperti e persone di valore, che sono ancora oggi parte integrante dell’azienda e forza trainante per i nuovi colleghi in termini di responsabilità, competenze e maturità”.

pologie e quantità. Con l’attuale forza tecnica e strumentale, siamo stati in grado di gestire progetti di qualifica complessi, raggiungendo una quota significativa dei servizi erogati sul territorio nazionale e aumentando notevolmente il portafoglio clienti. Questo per noi è motivo di soddisfazione e i riscontri che abbiamo ottenuto ci
Stefano Moltani: “Oggi l’organico di PVS sta per raggiungere le 50 unità e il nostro parco strumenti è diventato importante per tipologie e quantità: risorse che ci consentono di gestire progetti di qualifica complessi”
Chiara Mariani, qual è l’approccio al cliente e al mercato che il team di PVS predilige?
Mariani: “Lo spirito aziendale di PVS è costituito da valori in cui crediamo fortemente, che ci piace portare avanti e ribadire nelle relazioni che costruiamo con i nostri clienti: la condivisione, l’impegno e l’affidabilità. Questo perché siamo dell’idea che un confronto onesto e costruttivo sia la base di ogni relazione professionale serena. In azienda siamo abituati a parlare in maniera diretta, a mettere sul tavolo
I responsabili dell’area Sales & Business Development di PVS Group: da sinistra, Manfredi Musmarra, Chiara Mariani e Stefano Moltani
RIVISTA DELL’INDUSTRIA CHIMICA E FARMACEUTICA icf 35 Febbraio/Marzo 2024 Convalida
Convalida

PVS è da molti anni presente presso le aziende chimiche e farmaceutiche nell’ambito dei servizi GMP.
Da operazioni puramente tecniche, i suoi interventi si sono spesso trasformati in occasioni di supporto consulenziale
esperienze e problematiche, e quello che viviamo ogni giorno nel nostro ambiente, cerchiamo di ricrearlo anche dai clienti, che lo percepiscono e lo apprezzano. I nostri clienti si fidano di noi, e questo è il successo più grande che si possa desiderare. A livello operativo, su ogni attività e per ogni cliente assegniamo un referente tecnico dedicato, e in caso di progetti particolarmente complessi, procediamo anche internamente a riunioni periodiche di analisi sullo stato di avanzamento delle attività. Valutiamo insieme ogni singolo cliente per le sue caratteristiche, e cerchiamo di seguire quanto più possibile le sue esigenze, facendo sì che si senta compreso e ci veda partecipi nel raggiungimento dei suoi obiettivi”.
Come vi ponete nei confronti degli eventi di settore?
Mariani: “Dal punto di vista commerciale, gli eventi di settore sono un’importante azione strategica a livello di posizionamento e comunicazione. Dal punto di vista delle relazioni, per noi sono un’occasione di incontro e di confronto con i nostri clienti. PVS ci tiene ad avere una presenza forte nel contesto di tutti i più importanti eventi che vedono protagonista il suo campo operativo (i convegni delle associazioni, i congressi fieristici, i seminari scientifici ecc.), anche attraverso azioni di sponsorizzazione o con
un proprio stand, che diventa punto di richiamo per appuntamenti di lavoro o, come spesso accade, occasione per scambiare saluti e approfondimenti in un ambiente più informale. Non è tutto, però. Perché per noi è fondamentale condurre il gioco in prima persona. È per questo che PVS promuove da anni il proprio Compliance Day, un seminario gratuito rivolto ai nostri clienti, che si tiene con cadenza annuale. Le tematiche trattate vanno
Chiara Mariani: “I nostri clienti si fidano di noi, questo è il successo più grande che si possa desiderare”
dagli approcci risk based nella qualifica e nel commissioning ai servizi a valore aggiunto per l’industria delle life sciences, e molto altro, con programmi che vengono aggiornati a seconda degli argomenti di maggior interesse del momento. I docenti vengono scelti tra i nostri project manager – persone di alta competenza tecnica, che affrontano ogni giorno le sfide sul campo, e che quindi hanno molto da raccontare – e alcune figure chiave tra le nostre società partner, tra le quali Endress+Hauser e QualiWare. Quest’anno il Compliance Day si terrà ad Aprilia (LT) il prossimo 3 ottobre: naturalmente, siete tutti invitati!”.
Manfredi Musmarra, da quali premesse e con quali obiettivi è nata SolTech?
Musmarra: “Si è trattato di un’evoluzione naturale di ciò che è avvenuto nel tempo attraverso la collaborazione con i nostri clienti e partner. PVS è da molti anni presente presso le aziende chimiche e farmaceutiche nell’ambito dei servizi GMP, e l’apprezzamento ricevuto da parte del nostro gruppo di tecnici ha spesso trasformato i nostri interventi da servizi di carattere puramente tecnico in occasioni di supporto a livello consulenziale. Tutto questo si è tradotto in una nuova consapevolezza delle nostre potenzialità. I clienti ci hanno riconosciuto una grande affidabilità e, sempre più spesso, ci hanno coinvolto nella scelta di soluzioni tecnologicamente adatte al loro contesto, nella ricerca di soluzioni alternative e anche nella gestione di progetti. Negli anni, quindi, ci siamo ricavati una posizione nel nostro segmento di riferimento, non solo come PVS, ma come un gruppo di aziende in grado esprimere un valore aggiunto nel campo dei servizi di ingegneria, progettazione e di consulenza altamente specializzata in ambito GMP. Forti di questa fiducia da parte dei clienti e della consapevolezza del livello tecnico raggiunto, l’ulteriore obiettivo del nostro Gruppo si è tradotto nella creazione di un nuovo soggetto che potesse perfezionare il complesso dei servizi che volevamo, e potevamo, offrire al mercato. SolTech è nata da questa spinta iniziale, per integrare la nostra proposta, dando ai clienti l’opportunità di rivolgersi a un’azienda specializzata nella ricerca di soluzioni e prodotti tecnologici, innovativi e adeguati alla variegata realtà produttiva del panorama industriale italiano e non solo”.
36 icf RIVISTA DELL’INDUSTRIA CHIMICA E FARMACEUTICA
Quali soluzioni mette in campo SolTech e per quali applicazioni farmaceutiche?
Musmarra: “Siamo molto ben introdotti nel mercato dei prodotti e dei sistemi specializzati per il mondo farmaceutico. Questo non significa che offriamo solo soluzioni innovative, ma anche che possiamo selezionare prodotti o servizi già presenti, o comunque i più adeguati alle reali esigenze dei clienti. Spesso, infatti, la scelta delle migliori tecnologie da integrare nei progetti necessita di una conoscenza dei vari prodotti disponibili sul mercato e di un’imprescindibile verifica della sua concreta applicabilità alle realtà e ai processi produttivi. In tal senso, SolTech propone prodotti monouso, apparecchiature di processo e per i laboratori, sistemi di automazione (basati sia su architetture già presenti sul mercato, che realizzabili con prodotti alternativi e adeguati a ogni budget). L’ultima idea, per esempio, è stata studiata e realizzata per il calcolo dell’MKT, con il fine di integrare questa funzionalità su sistemi in cui non è presente, ma conciliando la solidità del sistema, con l’economicità che tale introduzione richiede. La ricerca di prodotti di qualità, con una ormai necessaria vocazione green, ci ha portato inoltre a selezionare un’ampia gamma di prodotti monouso – tute integrali, in particolare – che dispone anche di una certificazione ISCC+, fondamentale per attestare la reale partecipazione alla catena del riciclo dei prodotti più moderni. Le attività chiavi in mano, ultimamente, stanno rivestendo particolare importanza nel nostro business. Gli interventi sulla registrazione dei parametri ambientali nei labo-
PVS Group organizza da diversi anni, in collaborazione con aziende partner, una giornata di approfondimento sulle sfide tecnologiche del settore life science.
Prossimo appuntamento: il Compliance Day ad Aprilia (LT), il 3 ottobre 2024
ratori e magazzini sono diventati molto rilevanti, consentendoci di fornire la gamma completa dei servizi, grazie alla totale presa in carico del progetto: dalla fase di studio e compliance normativa, fino alla fornitura e realizzazione di prodotti su misura, installazione in campo e, ovviamente, qualifica impianto e convalida dei sistemi a esso collegati”.
C’è l’idea di ampliare la gamma dei marchi partner?
Musmarra: “Certo. Rappresentare per i nostri clienti un partner affidabile e competente, significa impegnarsi a essere sempre informati su ciò che viene ideato e messo a disposizione dal mercato. Nel corso di quest’anno, contiamo di espandere le nostre rappresentanze e collaborazioni con altre realtà produttive. Il mercato dell’automazione, in generale, rappresenta da sempre il nostro riferimento principale: molti di noi vengono da questo mondo e, con gli ultimi ingressi nel gruppo di personale specializzato, prevediamo ulteriori sviluppi anche per la realizzazione di progetti più complessi e fortemente customizzati”.
Come avviene la sinergia con il gruppo PVS?
Musmarra: “La sinergia è il nostro punto di forza. Contiamo da sempre
Manfredi Musmarra: “SolTech integra la proposta di PVS Group, proponendo prodotti monouso, apparecchiature di processo e per i laboratori, oltre a sistemi di automazione”
sulla collaborazione tra gli ingegneri di Process Service, azienda specializzata nella progettazione di impianti chimico-farmaceutici, e i tecnici e consulenti di PVS in Italia e all’estero. Possiamo quindi completare la nostra proposta disponendo di esperti di processo, tecnici specializzati, consulenti GMP, e di impianti anche molto particolari (penso alla nostra sezione interna che si occupa di TOC), oltre che esperti di automazione con i quali poter sviluppare progetti di notevole importanza. Teniamo molto a questa sinergia tra le varie competenze ed esperienze dei nostri colleghi. Questo ci permette di essere dei consulenti con un ampio spettro di conoscenze, che possono affrontare anche problemi complessi grazie alla presenza nel gruppo di personale con esperienza su argomenti tecnici molto specifici. Questo approccio ci rende un partner significativo: un consulente con una ‘visione’ che non rimane focalizzata solo su singole questioni, ma che è in grado di non prescindere dal contesto generale”. l

E
icf 37 Febbraio/Marzo 2024 Convalida
RIVISTA DELL’INDUSTRIA CHIMICA
FARMACEUTICA

Comprimitrici dal design semplice e facile da pulire
Con le tecnologie di Romaco Kilian, il produttore serbo di farmaci generici Hemofarm ottimizza i processi di pulizia, grazie alle parti a cambio rapido e a un secondo piatto portamatrici intercambiabile.
di Jan Clement
Direttore vendite, Romaco Kilian
Un’ampia gamma di prodotti e i conseguenti frequenti cambi formato, unitamente alle diverse esigenze di produzione, rendono la pulizia rapida e semplice delle comprimitrici una necessità vitale per Hemofarm, casa farmaceutica serba. Per questo mo-
tivo, l’azienda produttrice di farmaci generici si affida alle tecnologie di Romaco Kilian, caratterizzate dal design semplice e facile da pulire. Nella sua sede di Vršac, Hemofarm ha ridotto al massimo i tempi di inattività legati alla pulizia delle due comprimitrici ad alta velocità KTP 420X e KTP 590X, gra-
zie all’impiego di parti a cambio rapido e di ulteriori piatti portamatrici intercambiabili.
Hemofarm è leader di mercato nel settore farmaceutico serbo e la più grande esportatrice di farmaci del Paese. Dal 2006, l’azienda – che produce oltre 6,6 miliardi di compresse e capsule all’anno – fa parte del gruppo tedesco STADA, una delle maggiori aziende produttrici di farmaci generici al mondo.
Con sede a Vršac, in Serbia, Hemofarm realizza sia farmaci originali che prodotti per il Gruppo STADA, molti dei quali con le due comprimitrici KTP
38 icf RIVISTA DELL’INDUSTRIA CHIMICA E FARMACEUTICA
Tutte le foto © Romaco
420X e 590X di Romaco Kilian. La KTP 420X raggiunge una produzione massima di 360.000 compresse monostrato all’ora. La KTP 590X, con una produzione massima di 511.200 compresse all’ora, è stata sviluppata per un rapido passaggio dalla produzione monostrato a quella bistrato e per la produzione ad alta velocità di compresse effervescenti.
Le richieste nei confronti delle comprimitrici non potrebbero essere più ampie: complessivamente, vengono realizzati più di 200 prodotti farmaceutici con formulazioni che differiscono notevolmente, in lotti da 100 a 2.200 kg. La forza di compressione può variare da 5 a 80 kN, e gli ingredienti possono essere lavorati sotto forma di granuli umidi o secchi o compressi direttamente. Sulla KTP 590X vengono attuati uno o due cambi prodotto alla settimana, mentre sulla KTP 420X si arriva fino a tre o quattro, per cui è indispensabile una pulizia intensiva delle aree di lavorazione delle compresse e delle parti della pressa a contatto con il prodotto. Inoltre, tra i lotti dello stesso prodotto viene eseguita una pulizia parziale.


Basso numero di componenti Nell’area di compattazione le moderne comprimitrici di Romaco Kilian presentano un numero di componenti notevolmente inferiore rispetto ai modelli convenzionali, il che è determinante per la pulizia e rappresenta un vantaggio importante nella produzione quotidiana. “Il ridotto numero di parti a contatto con il prodotto, il concetto di igiene ottimizzata e diverse caratteristiche speciali quali il sistema a soffietto brevettato per punzoni rendono la pulizia delle presse serie KTP un gioco da ragazzi”, spiega Ivan Djokic, direttore di produzione presso lo stabilimento di Hemofarm di Vršac. “Tutte le parti intercambiabili sono leggere, possono essere smontate senza l’aiuto di attrezzi e sono facili da riassemblare. Ecco perché i nostri operatori affermano che è un piacere lavorare con le presse Kilian”. Anche la scarpetta di riempimento può essere rimossa da una sola persona senza alcun problema, perché la scatola degli ingranaggi si trova al di fuori dell’area di lavoro. Fatta eccezione per il piatto portamatrici, tutte le parti intercambiabili della pressa Kilian hanno un peso inferiore a 15 kg.
Area di compattazione separata e sigillata
Le presse Kilian KTP 420X e 590X sono inoltre caratterizzate da aree di lavoro e di servizio rigorosamente separate, in modo da impedire alla polvere delle compresse di penetrare nel vano macchine. L’area di compattazione è molto piccola e ricorda una gabbia in acciaio inossidabile sigillata ermeticamente. La superficie da pulire è stata ridotta di circa un terzo, portando a una notevole diminuzione dei tempi di pulizia. Tutte le presse della serie KTP di Kilian hanno un ingombro molto ridotto, grazie al loro design compatto e alle piccole aree delle finestre: ad esempio, 1.080 x 1.115 mm per la KTP 420X o non più di 1.230 x 1.325 mm nel caso della KTP 590X. Se le finestre sono aperte, le misure della KTP 420X sono solo di 2.303 x 2.268 mm, mentre quelle della KTP 590X sono di 2.567 x 2.472 mm. Grazie a questo uso economico dello spazio, il consumo di energia nella camera bianca è proporzionalmente inferiore, con una conseguente riduzione dei costi di gestione.
Hemofarm
riduce i tempi di pulizia utilizzando piatti portamatrici intercambiabili, che vengono semplicemente sostituiti alla fine di un lotto
Un solo operatore necessita di al massimo 15 minuti per installare le parti intercambiabili e il piatto portamatrici
Macchine RIVISTA DELL’INDUSTRIA CHIMICA E FARMACEUTICA icf 39
Febbraio/Marzo 2024
Hemofarm dispone di otto comprimitrici Romaco Kilian
Pulizia delle parti intercambiabili durante la lavorazione del lotto
Le due serie di parti intercambiabili utilizzate da Hemofarm per entrambe le comprimitrici includono la scarpetta di riempimento, il raschietto per compresse, la copertura del punzone superiore, gli ugelli di aspirazione e la copertura tra i blocchi dei rulli pressori. Queste parti sono conservate, sempre pronte, in un carrello di trasferimento chiuso e vengono installate nell’area di lavorazione della comprimitrice in caso di cambio prodotto. Le parti rimosse al termine del lotto precedente vengono pulite durante la produzione del lotto successivo.
La pressa ad
alta velocità
KTP 590X è in uso presso
Hemofarm
24/7 e viene completamente riorganizzata e pulita una o due volte alla settimana
L’ulteriore piatto portamatrici aumenta la flessibilità
Al fine di ridurre ulteriormente i tempi di inattività durante il cambio prodotto, oltre alle parti a cambio rapido Hemofarm si serve di un secondo piatto portamatrici intercambiabile per ciascuna delle due comprimitrici.
“Quando si tratta di ottimizzare l’OEE e il TCO, spesso si sottovaluta l’impatto di un piatto portamatrici intercam-


biabile”, commenta Gerd Heinen, Area Sales Manager di Romaco Kilian, che ha seguito il progetto Hemofarm fin dall’inizio. “Investendo in piatti portamatrici intercambiabili, Hemofarm dimostra di adottare un approccio intelligente e proiettato al futuro”.
I piatti portamatrici vengono puliti rimuovendo la camma superiore insieme ai punzoni, mentre la camma inferiore rimane nell’area di compattazione. Per evitare che la polvere penetri nell’area “grigia” della macchina durante la pulizia, dopo aver rimosso il piatto portamatrici viene montata una copertura cieca. I punzoni, le matrici e altre parti intercambiabili vengono puliti in una lavatrice industriale. Il piatto portamatrici stesso viene pulito manualmente presso Hemofarm. È sufficiente un solo addetto Hemofarm per occuparsi del ciclo completo di cambio prodotto, compresa la pulizia delle parti intercambiabili e del piatto portamatrici, per cui sono necessarie circa sei ore. Per l’installazione delle parti sostituite insieme al piatto portamatrici, sono necessari solo dai 10 ai 15 minuti. Tra due lotti dello stesso prodotto, le comprimitri-
ci vengono parzialmente pulite utilizzando un aspirapolvere come da procedura di pulizia validata: il piatto portamatrici, le matrici e i punzoni, oltre a tutte le altre parti a contatto con il prodotto, rimangono nell’area di compattazione, mentre vengono smontate solo la scarpetta di riempimento e la relativa tramoggia. Questo processo di pulizia parziale può essere completato in circa un’ora.
Otto comprimitrici Kilian in cinque siti produttivi
Hemofarm utilizza le tecnologie Romaco Kilian sin dal 2002 e attualmente si avvale di un totale di otto comprimitrici Kilian in funzione nei suoi cinque siti produttivi. A Vršac, le rotative monostrato della serie KTP operano su tre turni, cinque (KTP 420X) o sette (KTP 590X) giorni alla settimana. “Nel nostro lavoro quotidiano, le presse Kilian si sono dimostrate molto versatili, robuste e affidabili”, afferma Djokic. “E se insorgono problemi di servizio, ci avvaliamo anche dei tempi di risposta brevi e della competenza in materia di assistenza del team Kilian”.
Macchine 40 icf RIVISTA DELL’INDUSTRIA CHIMICA E FARMACEUTICA
ROBOTICS
Profonda esperienza per ogni grado di produzione farmaceutica

Lo stato dell’arte della robotica per una produzione sicura
Nei contesti in cui è necessario un grado estremo di igiene, come gli ambienti sterili o di classe B, i robot Stäubli garantiscono le massime performance rispetto alle normative, alla pulizia e alla sanificazione. Sia che si tratti di operazioni complesse o di routine, contribuiscono ad aumentare l’efficienza operativa del manufacturing farmaceutico.
Stäubli – Experts in Man and Machine
www.staubli.com
Stäubli Italia S.p.A. (Carate Brianza MB – IT), Tel. +39 0362 944241, robot.it@staubli.com
Granulatori di precisione per applicazioni medicali

CMG presenta una serie di granulatori di dimensioni ridotte destinata all’applicazione nell’industria medicale. Le caratteristiche della nuova serie G17-MED sono molteplici e contribuiscono
tutte ad ottenere il massimo grado di precisione e pulizia, qualità di rimacinato (omogeneità dimensionale delle particelle di rimacinato e assenza di polvere), efficienza di funzionamento. I nuovi granulatori G17-MED sono applicabili ai processi di stampaggio ad iniezione e soffiaggio. Nella configurazione ET1 o ET2, sono adatti per applicazioni di estrusione.
La serie di granulatori G17MED è progettata per ottenere rimacinato con forma e dimensioni omogenee, con nessuna presenza di polvere. Un ulteriore beneficio esclu-
sivo di questa nuova linea è la capacità di produrre rimacinato di dimensioni molto piccole. Il granulo di piccole dimensioni non ha impatti negativi sulla qualità del prodotto medicale finito. I sistemi per piccole produzioni, macchine per stampaggio o estrusori, sono dotati di viti di plastificazione di piccolo diametro che non sono in grado di processare granuli con dimensioni maggiori a quelle del granulo vergine. I granulatori G17-MED producono un rimacinato con dimensioni comparabili a quelle del granulo vergine.
Riempitrice con piattaforma servo-assistita flessibile
Steriline, produttore europeo di riempitrici robotizzate altamente specializzate e di linee complete di riempimento sterile, parteciperà a Interphex, che si svolgerà dal 16 al 18 aprile 2024 presso il Javits Center a New York. Si tratta di un evento nordamericano nel settore farmaceutico e biotecnologico. L’azienda accoglierà i visitatori nello stand n. 2537 per presentare la macchina riempitrice di flaconi robotizzata con sistema di movimentazione planare, una tecnologia di trasporto a levitazione magnetica. Questa soluzione consiste in una piattaforma esclusiva (con tecnologia simile al treno proiettile Maglev) per la levitazione dei mover al di sopra di una superficie inossidabile che fornisce 6 gradi di movimento preciso e zero attrito. Ciò consente il trasporto dei contenitori (siano questi flaconi, siringhe, carpule, ecc.) da una stazione all’altra del processo di riempimento
e tappatura senza alcun componente meccanico. La combinazione di questa tecnologia, con l’uso della robotica per il carico e lo scarico, si traduce in una piattaforma altamente flessibile e pulita.
“Steriline continua ad essere in prima linea nel settore delle implementazioni robotiche in ambienti asettici con oltre 150 sistemi robotizzati installati negli ultimi dieci anni, a dimostrazione del fatto che siamo stati tra i primi ad adottare tecnologie innovative fino alla loro commercializzazione”, spiega James Rorke, vicepresidente Steriline North America. “Lo sviluppo delle tecnologie del sistema di movimentazione planare in ambienti asettici alza ora ulteriormente l’asticella verso una maggiore flessibilità e un maggiore controllo della contaminazione”.
“La revisione dell’Annex 1 delle GMP dell’UE sta incentivando l’adozione, nell’industria farmaceutica, di tecnologie
Una caratteristica aggiuntiva del G17-MED è rappresentata dall’alta qualità dei gradi di acciaio inossidabile, leghe speciali e trattamenti anticorrosione utilizzati per la fabbricazione di tutte le parti a contatto con i polimeri. La pulizia del G17-MED avviene in pochi minuti. Tutte le parti sono accessibili senza l’utilizzo di attrezzi e possono essere pulite con aspirazione. I nuovi carter insonorizzanti della serie G17MED sono realizzati per trasmettere le onde sonore ai pannelli fonoassorbenti al fine di ottenere livelli sonori ben al di sotto di quelli accettabili dall’industria (EN12012-1).
in grado di migliorare la qualità dei prodotti e la sicurezza degli operatori”, afferma Federico Fumagalli, direttore commerciale di Steriline. “Lo sguardo del reparto Ricerca e Sviluppo di Steriline è sempre rivolto al futuro con l’obiettivo di identificare opportunità tecnologiche, come appunto questa soluzione con sistema di movimentazione planare, da implementare nelle nostre future macchine e linee. È un approccio che riteniamo lungimirante per favorire l’innovazione e permettere così a Steriline di essere vista sempre più come un fornitore forte e di riferimento per l’industria farmaceutica”.

Macchine 42 icf RIVISTA DELL’INDUSTRIA CHIMICA E FARMACEUTICA
Custodia morbida per cappucci di emergenza
I cappucci di emergenza sono dispositivi che consentono l’evacuazione da zone pericolose in sicurezza e, in quanto tali, devono rispondere a tre requisiti fondamentali: poterli estrarre velocemente dalla custodia, essere facili da indossare e offrire la massima protezione. Durante gli interventi il cappuccio di emergenza è normalmente fissato alla cintura dell’operatore o, in alternativa, si può indossare a tracolla. Per questo motivo, una particolare attenzione è riservata anche all’ergonomia e al comfort dell’imballaggio che può essere rigido (garantendo protezio-
ne contro polvere e spruzzi d’acqua a norma IP54) oppure morbido (protezione dalla polvere a norma IP5). Da sempre attenta alle esigenze dell’utilizzatore finale, Dräger ha riprogettato la custodia morbida “Soft Pack” per renderla ancora più performante e confortevole. Realizzato con un materiale ancora più robusto e facile da pulire con un panno umido, l’imballaggio è dotato di una fascia riflettente per una visibilità ottimale. Sulla linguetta di protezione è presente, sulla parte frontale, un pittogramma che illustra il campo di applicazione e il tipo di filtro. Sol-
levandola è inoltre possibile vedere la finestra trasparente per il controllo della data di scadenza, mentre sul retro sono riportate informazioni sull’omologazione e un QR Code che rimanda al sito web Drager. Il sigillo di sicurezza rimane protetto sotto la linguetta nella parte superiore della custodia e si rompe automaticamente in fase di apertura consentendo un utilizzo immediato del dispositivo di fuga. La serie di cappucci di emergenza Dräger Parat è disponibile in tre versioni: Parat 4700 (per aree industriali), Parat 5500 (per fuga in caso d’incendio) e Parat 7500
> estrusori > dosatori > componenti > trasporto pneumatico > sistemi completi
NUOVA GENERAZIONE DI DOSATORI FARMACEUTICI. UNA CLASSE SUPERIORE.
+ Dosatori ad alta precisione per un dosaggio ottimale degli ingredienti
+ Cambio rapido tra configurazione a vite singola e a vite doppia
+ Un unico riduttore di velocità offre una gamma completa di portate per tutti i modelli
+ Ingombri ridotti ideale per sistemi multi componente
+ Inclinazione dosatore di 2 gradi per un migliore
drenaggio nel WIP
+ Facile da smontare e pulire
Montenegro S.r.l.
Via Volturno, 37 20861 Brugherio (MB)
Tel: +39 039 883107
Fax: +39 039 880023
info@montenegrosrl.it

(per aree industriali e fuga in caso d‘incendio). In tutte le versioni la sostituzione del filtro dopo otto anni, ad opera di tecnici qualificati, prolunga la durata utile del cappuccio fino a 16 anni.


I nuovi dosatori farmaceutici Coperion K-Tron sono ideali sia per applicazioni a batch che continue. Il concetto generale è impostato specificamente per una rapida pulizia e smontaggio, richiede solo pochi secondi disconnettere la tramoggia semisferica, l’agitatore, le viti di estrazione e la tramoggia di stoccaggio dal riduttore. www.coperion.com/it/dosatori-farmaceutici

Sicurezza
ICF_CK-IT_Pharma-Feeders_194x121mm_it_2023.indd 1 12.01.2023 10:16:16
Armadi e contenitori di derivazione in acciaio inox
A volte anche gli armadi e i contenitori di derivazione devono essere eleganti oltre a dover proteggere apparecchiature e unità di controllo sensibili, anche in condizioni avverse. Questo vale già per le versioni standard della gamma AX e KX di Rittal, con le loro durevoli verniciature a polvere. Rittal propone ora nuove versioni in acciaio inox. Gli armadi compatti sono dotati di un sistema brevettato di bugnature interne lungo tutto il perimetro dell’armadio. Questo significa che, insieme alle guide per l’installazione interna, riproducono lo schema del passo meccanico da 25 mm del sistema di armadi di grandi dimensioni VX25. Grazie a questo sistema unico e brevettato, gli armadi compatti AX sono pronti per tutti i tipi di configurazioni e installazioni interne.
I componenti e gli accessori
del sistema, dagli interruttori di posizione della porta e dai montanti, alle guaine per cavi, fino alle lampade a LED, possono essere installati sugli chassis di montaggio in modo semplice, rapido e sicuro, senza la necessità di lavorazioni meccaniche. Grazie allo spazio predefinito tra gli chassis, è possibile utilizzare anche gli accessori del sistema di accessori come i profilati forati.
Il nuovo design semplifica inoltre la messa a terra, grazie alla compensazione automatica di potenziale anche per i modelli AX e KX in acciaio inox. Sui contenitori KX, ad esempio, le staffe a “L” posizionate sui laterali sono state ottimizzate per il collegamento PE. Per sfruttare ancora meglio la profondità del contenitore KX, la guida di montaggio può essere montata direttamente sul fondo del contenitore grazie ad
un accessorio dedicato venduto separatamente. Un’altra novità della gamma KX è l’introduzione di una nuova tipologia di contenitore, E-Box, il quale viene fornito con un sistema di chiusura e coperchio incernierato con una cerniera a 180°, per agevolare le operazioni di manutenzione e service. Sia nella serie AX che nella serie KX, il retro è completamente chiuso, ma nei quattro angoli c’è una predisposizione per favorire il montaggio dei sistemi di fissaggio a parete. I nuovi armadi e contenitori in acciaio in inox sono già predisposti per il tracciamento digitale dei processi produttivi di realizzazione di quadri elettrici, processi molto richiesti in tempi di sistemi sempre più complessi e di carenza di manodopera qualifica-

ta. Tutti i dati sono disponibili per Eplan. Il gemello digitale del quadro elettrico creato dal progetto Eplan contiene anche tutti i dati necessari per l’elaborazione automatica da parte dei quadristi, ad esempio, con le forature e le lavorazioni con i centri lavoro Perforex. Il codice QR presente su tutti i modelli della nuova gamma in inox permette di attivare l’innovativo sistema ePOCKET, la tasca porta schemi digitale che permette l’archiviazione di tutti gli schemi elettrici, manuali d’uso e manutenzione, e molto altro.
Soluzioni per il trasporto sicuro dell’ammoniaca
Oltre a favorire la crescita dell’elettrificazione, l’idrogeno svolgerà un ruolo cruciale come elemento chiave della transizione energetica. La Germania non dispone dello spazio necessario per coprire l’intera do-

manda futura attraverso la produzione nazionale. Oggi si presume che le sue importazioni si aggireranno tra il 60 e il 70%. L’idrogeno sarà trasportato via nave, il che può rappresentare un problema. Il trasporto dell’ammoniaca, invece, è un processo ben consolidato, con circa 20 milioni di tonnellate trasportate ogni giorno.
Per questo motivo, importanti fornitori hanno deciso di produrre ammoniaca unendo l’idrogeno verde con l’azoto, e di trasportare l’ammoniaca con i metodi consolidati. Tuttavia, trattandosi di una sostanza tossica ed esplosiva, è necessa-
rio adottare misure di sicurezza adeguate. Dallo sbarco e dall’ulteriore trasporto via terra, alle ulteriori fasi di lavorazione, i prodotti Pepperl+Fuchs sono presenti nei vari sistemi utilizzati, come gli amplificatori di commutazione della serie KSystem che separano in modo sicuro i dispositivi di campo dai controllori. Inoltre, un’ampia gamma di barriere può essere adattata ai rispettivi sistemi. Gli switch Ethernet-APL sono sempre più utilizzati per la moderna trasmissione di dati, consentendo di supportare elevate velocità di trasferimento dati in un ambiente sicuro.
Sicurezza 44 icf RIVISTA DELL’INDUSTRIA CHIMICA E FARMACEUTICA

VISITA SOLIDS PARMA!
INDUSTRIA DI PROCESSO: SOLIDS TORNA A PARMA
La fiera per le tecnologie dei granuli, delle polveri e dei solidi sfusi
La due giorni dedicata alle macchine e alle soluzioni più innovative del settore Bulk Handling nei settori gomma e plastica, alimentare, agricoltura e mangimi, chimico e farmaceutico, cosmetico, lavorazione dei metalli, minerario, carta e vetro, recycling.
• Apparecchiature di dosaggio, pesatura e misura
• Tecnologia di miscelazione e omogeneizzazione
• Essiccatori e attrezzatura per l‘essiccazione
• Macinazione e frantumazione
• Trasporto e movimentazione
SOLIDS PARMA
5-6 Giugno 2024, Fiere di Parma www.solids-parma.it


• Stoccaggio e distribuzione
• Imballaggi e servizi di imballaggio
• Sicurezza e ambiente
• Tecnologie di riciclaggio e recupero
• Componenti



Un partner completo per la farmaceutica e non solo
Aseptconn si propone come un interlocutore unico per i settori farmaceutico, nutraceutico, cosmetico, alimentare e chimico, in grado di integrare la vendita di componenti alla progettazione di soluzioni ad hoc e all’offerta di servizi altamente qualificati come ingegneria computazionale e digitalizzazione.



Aseptconn AG è un’azienda svizzera con sede amministrativa a Dietikon ed un sito produttivo, in continua espansione, a Bulle, nel Canton Friburgo.
Con un focus specifico sui liquidi sterili, Aseptconn è fornitore leader di componenti, sistemi, software e servizi applicabili nei settori



farmaceutico, biofarmaceutico e in altri settori critici, quali l’industria alimentare e la cosmesi.
L’azienda, nata nel 2016 ed in progressiva crescita, ha scelto di presentarsi al mercato come un interlocutore unico, in grado di integrare alla vendita di componenti, la progettazione e la produzione di soluzioni interne, oltre a servi -
zi specifici e qualificati, quali l’ingegneria computazionale e la digitalizzazione.
Potenziato il sito produttivo di Bulle
Attraverso investimenti mirati, Aseptconn è impegnata ogni giorno a sviluppare e proporre soluzioni innovative che contribuiscano
Componenti
46 icf RIVISTA DELL’INDUSTRIA CHIMICA E FARMACEUTICA
a migliorare in modo sostenibile i processi dei propri clienti. Con questo obiettivo, lo scorso anno ha visto il convogliarsi di molte energie, sia operative che finanziarie, sullo sviluppo del sito produttivo di Bulle. Lo stabilimento si sviluppa su 1.200 m 2 e prevede l’operatività full time di 10 persone, oltre al supporto di team specializzati. Al suo interno vengono sviluppati servizi di produzione, lavorazioni meccaniche ed elettroerosione per tutte le tipologie di parti metalliche. Sono disponibili torni, macchine per elettroerosione, fresatu -

ra, saldatura e lucidatura. Nel 2023
è stata inoltre integrata la produzione di aghi di riempimento e lavaggio.
Single use, aghi e altre lavorazioni Accanto alle produzioni Aseptconn più tradizionali, quali tubi flessibili e raccordi, i team specializzati sono dedicati alla progettazione e produzione di soluzioni customizzate single use, aghi di lavaggio e riempimento e sistemi in acciaio inossidabile e lega Hastelloy. Il dipartimento di ingegneria è in grado di creare parti specializzate ad alta
precisione, completamente allineate alle specificità dell’applicazione, fra cui: adattatori, tanks, carrelli, coperchi sterili, assemblaggi, contenitori in acciaio inox ecc. Con i sistemi single use, le aziende possono aumentare la propria capacità produttiva, anche con un budget di avvio limitato. I processi di sterilizzazione e pulizia vengono eliminati con una riduzione dei costi di installazione assistenza. Le soluzioni single use, infatti, spesso richieste per sistemi di riempimento e campionamento, si completano con la possibilità di









Componenti RIVISTA DELL’INDUSTRIA CHIMICA E FARMACEUTICA icf 47
Febbraio/Marzo 2024

richiedere packaging personalizzati e processi di sterilizzazione che vengono certificati secondo le normative vigenti.
Ponendo invece l’accento sugli aghi progettati e realizzati da Aseptconn, si tratta di soluzioni che si adattano perfettamente alle macchine di riempimento e che garantiscono la conformità agli standard qualitativi. Gli aghi vengono utilizzati in tutte le macchine dosatrici per riempire con precisione la dose corretta di liquido da 0,005 a 250 ml con sistemi volumetrici o peristaltici. La produzione degli aghi di riempimento, pur essendo customizzata, avviene in tempi molto competitivi ed il servizio post-vendita risulta rapido e flessibile.


La digitalizzazione dei P&IDs
Un altro elemento che caratterizza il portafoglio delle soluzioni Aseptconn è il sistema informatico AseptSoft.
Lo scopo principale di tale sistema informativo è la digitalizzazione dei P&IDs e delle relative modifiche, accompagnata dalla possibilità di visualizzare il flusso del fluido coinvolto e di generare dati esportabili necessari ai documenti di qualifica. L’utilizzo di P&IDs digitalizzati consente di essere molto flessibili e veloci in caso di modifiche e, di conseguenza, di essere più efficienti nelle procedure di validazione. Il P&IDs digitalizzato diventa, così, un documento “intelligente” che può essere sviluppato ed interrogato nel tempo per lo sviluppo continuo dei progetti. Con AseptSoft è possibile in-
fatti: generare automaticamente le specifiche funzionali per i documenti IQ/OQ; generare automaticamente il flusso del fluido, in funzione dello stato dei componenti; modificare i P&IDs in ogni momento; sviluppare i design del processo da qualsiasi luogo ci si trovi.
Dosaggio per liquidi altamente viscosi
Tra le novità dell’ultimo anno, va menzionata l’acquisizione da parte di Aseptconn della rappresentanza in Italia e Svizzera dell’innovativo sistema di dosaggio Viscotec, adatto anche a liquidi altamente viscosi. Questa sua peculiarità lo rende idoneo ad una gamma di mercato che non abbraccia solo il mondo pharma, ma anche l’industria cosmetica ed alimentare. l
Componenti 48 icf RIVISTA DELL’INDUSTRIA
E FARMACEUTICA
CHIMICA
Lo stabilimento di Aseptconn a Bulle, in Svizzera
Profili a spazzola per la gestione dei cavi
I profili a spazzola icotek BES sono una soluzione pratica per organizzare i cavi di rete negli armadi rack da 10 pollici (BES 10) e 19 pollici (BES 19) di vari produttori. Si caratterizzano per il montaggio e lo smontaggio senza l’ausilio di attrezzi grazie all’innesto a molla. Per in-
stallare o rimuovere i profili a spazzola è sufficiente rilasciare i blocchi a molla su entrambi i lati.
Il profilo a spazzola consente di far passare facilmente i cavi di rete, mascherando la vista dei cavi all’interno dell’armadio e garantendo un aspetto organizzato.

Inoltre, i profili a spazzola proteggono dall’ingresso di polvere e sporcizia e allo stesso tempo garantiscono la circolazione dell’aria necessaria per i dispositivi. Queste caratteristiche aumentano l’affidabilità e la durata dei dispositivi di rete. I profili a spazzole BES sono

adatti a temperature comprese tra -30°C e 80°C e sono realizzati in acciaio verniciato a polvere con spazzole in poliammide. I BES di icotek sono robusti e durevoli, il che garantisce un funzionamento affidabile per un periodo di tempo prolungato
Avvitatori in classe A per sistemi robotizzati pick & place
La giapponese Coretec, partner esclusivo di Burster Italia per la zona EMEA, ha recentemente presentato l’aggiornamento degli avvitatori venduti in tutto il mondo da oltre 30 anni. Tra le novità risulta la serie compatta “CUBE” anche per piccole coppie di 0,25 Nm fondo scala. Le note distintive di questi tools sono la compattezza a parità di coppia e la dichiarata grande affidabilità.
Pressione a 4 bar per ridurre i consumi
La prassi più diffusa nella progettazione dei macchinari si fonda sullo sfruttare una pressione operativa compresa circa tra i 6 e gli 8 bar. Tuttavia, riducendo questo valore ad esempio da 7 a 4 bar, gli utenti finali potrebbero abbattere i costi energetici fino al 29%. Pur non essendo diffusa, la frontiera del 4 bar è già realtà in alcune aziende e richiesta da alcuni utilizzatori finali. Puntare a questo obiettivo, o quantomeno a una sensibile riduzione della pressione operativa, sarà la sfida del prossimo futuro per la pneumatica, che ha ancora molto da dire come tecnologia di automazione per semplicità ed efficacia di utilizzo. L’aumento dei costi energetici, il rilascio di nuove normative, le aspettative per un’industria sem-
pre più efficiente e a basso impatto di emissioni favoriranno questa transizione.
La riduzione della pressione a 4 bar in talune applicazioni può richiedere l’uso di un attuatore con diametro maggiore per garantire la forza richiesta. In questo caso l’utilizzo di moltiplicatori a basso consumo SMC (VBA-X3145 e VBA-X3239) possono superare l’ostacolo, evitando di utilizzare un cilindro con diametro maggiorato dove gli spazi non lo consentono, raggiungendo anche il 40% in meno dei consumi.

In casi dove lo spazio è basilare, cilindri più compatti e leggeri come le serie J di SMC e con diametri intermedi rispetto alle proposte standard, rappresentano una soluzione che permette una progettazione moderna, innovativa e sostenibile. Una ulteriore opzione è utilizzare cilindri compatti con doppia spinta (CDQ2B-X3166). La funzionalità di un impianto a 4 bar si ottiene anche con la gestione ottimale dei soffi tramite soluzioni come ugelli di potenza ad alta efficienza (KNH)
che migliorano del 10% la resa; con amplificatori di portata (ZHV) che aumentano di 4 volte la portata; e con sistemi per il vuoto a elevato risparmio energetico (ZK2) che rispetto a un classico eiettore a singolo stadio senza controllo possono arrivare al 93% di risparmio d’aria. Senza dimenticare che superati sensibilmente i 4 bar gli eiettori non migliorano le performance di aspirazione, aumentando invece i consumi in quanto si entra in una zona non ottimale della curva di rendimento. Man mano che le nuove macchine a pressione ridotta popoleranno le fabbriche, gli utilizzatori finali potranno ridurre la pressione di linea, con ulteriori risparmi sul consumo elettrico totale delle sale compressori e sull’incidenza delle perdite negli stabilimenti.
Componenti RIVISTA DELL’INDUSTRIA CHIMICA E FARMACEUTICA icf 49 Febbraio/Marzo 2024
PLC di sicurezza per applicazioni fino alla categoria SIL3
Il nuovo controllore di sicurezza AXC F XT SPLC 3000 di Phoenix Contact viene utilizzato come modulo di espansione sul lato sinistro dei PLCnext Control AXC F 2152 o AXC F 3152 e completa la gamma PLCnext con un potente PLC di sicurezza per i dispositivi Profisafe nelle reti Profinet. Il controllore di sicurezza può essere utilizzato in applicazioni fino alla categoria di sicurezza SIL3 in conformità con le norme IEC 61508/61511
e PL e secondo EN ISO 13849-1. Come F-Host, SPLC 3000 può comunicare con un massimo di 300 F-Device e contemporaneamente agire come F-Device. Il controllore di sicurezza è completamente integrato nell’ecosistema aperto PLCnext Technology e offre un elevato grado di modularità in combinazione con le estensioni Profisafe I/O dell’Axiobus, che possono essere aggiunte sul lato destro. Le potenti e ridondanti CPU
Pompa per il dosaggio chimico di precisione
Watson-Marlow Fluid Technology Solutions (WMFTS) ha lanciato la pompa dosatrice e per il dosaggio chimico di precisione Qdos™ H-FLO, progettata specificamente per erogare portate più elevate, fino a 600 l/h.
La pompa Qdos H-FLO offre le stesse straordinarie caratteristiche di precisione e affidabilità delle altre pompe Qdos, ma per portate più elevate, con una varietà di teste e materiali per i tubi che garantiscono la compatibilità chimica con il fluido di processo.
La pompa ad alta precisione Qdos H-FLO garantisce la flessibilità necessaria per scalare con i processi dei clienti, sia che si tratti di trattamento idrico e delle acque reflue, di estrazione mineraria e di lavorazione dei minerali, di applicazioni chimiche nel settore alimentare o della cellulosa e della carta.
Il lancio di Qdos H-FLO amplia la gamma
di pompe Qdos con portate fino a 600 l/h e capacità di pressione fino a 7 bar (102 psi). Come il resto della gamma di pompe peristaltiche Qdos, Qdos H-FLO riduce i costi grazie a un dosaggio chimico ancora più preciso, con un’accuratezza di ±1% e una ripetibilità di dosaggio di ±0,5%.
Qdos H-FLO offre vantaggi per applicazioni quali il dosaggio di: disinfettanti, coagulanti, flocculanti, alcali/sostanze alcaline, reagenti minerari, tensioattivi.

di sicurezza basate su ARM sono diversitarie e hanno una frequenza di 800 MHz per il canale 1 e di 600 MHz per il canale 2.
ni con portate più elevate. Qdos H-FLO mira a rendere il dosaggio chimico più semplice ed efficiente per i team operativi, di manutenzione ed EHS. Inoltre, offre diverse opzioni di comunicazione di bordo per l’integrazione con SCADA e PLC per ottimizzare i processi”.
I vantaggi offerti dalla nuova pompa Qdos H-FLO includono:
• Portate da 2,0 ml/min a 600 l/h
• Capacità di pressioni fino a 7 bar
• Il rilevamento RFID della testa garantisce l’installazione della testa corretta

“Noi di Watson-Marlow Fluid Technology Solutions crediamo nell’innovazione tecnica per risolvere i problemi complessi dei clienti, offrendo soluzioni semplici da utilizzare”, ha spiegato Adeel Hassan, Product Manager di WMFTS. “L’elevata precisione e ripetibilità delle nostre pompe contribuiscono a ridurre i costi di utilizzo delle sostanze chimiche e aiuta i clienti a raggiungere gli obiettivi net zero. Se, da un lato, la pompa ha ereditato le caratteristiche uniche dell’attuale gamma Qdos, dall’altro presenta diverse novità per rendere il dosaggio chimico più semplice, sicuro ed economico. Il feedback dei clienti è stato fondamentale per lo sviluppo della serie Qdos per applicazio-
• Contagiri per la manutenzione della testa
• Il rilevamento delle perdite e il contenimento dei fluidi, che prevengono le fuoriuscite e l’esposizione a sostanze chimiche alla scadenza della testa.
Le opzioni di collegamento in rete, controllo e comunicazione includono Ethernet/IP, Profinet e Profibus per una facile integrazione con SCADA/PLC
Un’unità di pompaggio comune con diverse opzioni di teste per un’ampia gamma di condizioni di processo e di prodotti chimici Qdos H-FLO è accompagnata da un kit opzionale di rilevamento della pressione che consente di monitorare la pressione in tempo reale, garantendo la sicurezza del processo e migliorando la protezione degli operatori.
Il kit opzionale di rilevamento della pressione è dotato di allarmi configurabili per il monitoraggio del processo.
50 icf RIVISTA DELL’INDUSTRIA CHIMICA E FARMACEUTICA Componenti
C M Y CM MY CY CMY K


Flacone di resina riciclata

Bormioli Pharma, esperta internazionale nel confezionamento farmaceutico e nei dispositivi medici, e Loop Industries, Inc., una società di tecnologia green la cui missione è accelerare un’economia circolare della plastica attraverso la produzione di PET riciclato al 100% e di fi-
bra di poliestere, hanno annunciato una collaborazione per un innovativo flacone ad uso farmaceutico prodotto con resina PET Loop™ 100% riciclata di qualità vergine. Il prodotto è stato presentato a Pharmapack Europe 2024 presso lo stand di Bormioli Pharma.
L’industria farmaceutica sta riconoscendo sempre più l’importanza di implementare pratiche e materiali sostenibili per ridurre il suo impatto ambientale. Il PET di qualità vergine riciclato al 100% di Loop può aiutare le aziende farmaceutiche ad adottare un’alternativa di packaging sostenibile e rispondere alla crescente domanda di
azioni responsabili dal punto di vista ambientale.
La tecnologia Infinite Loop ricicla i rifiuti di PET e fibra di poliestere di minore pregio e li trasforma in resina PET Loop di elevata qualità. Un recente test, eseguito da un leader mondiale nelle analisi di laboratorio, conferma che la resina PET Loop ha soddisfatto con successo i rigorosi standard e requisiti delineati dalla Farmacopea europea (Ph.Eur. 3.1.15, Polietilene Tereftalato per Contenitori per Preparazioni non destinate a usi parenterali) e dalla Farmacopea statunitense (USP <661.1>, materiali plastici di costruzione) ed è confor-
Soluzioni per lo sviluppo di farmaci in piccoli lotti
Stevanato Group Spa, fornitore globale di soluzioni per il contenimento e la somministrazione di farmaci e per la diagnostica destinate all’industria farmaceutica, biotecnologica e life science, ha presentato due nuove offerte per efficientare la produzione farmaceutica in piccoli lotti: EZ-fill® Kit e il servizio non GMP di Fill and Finish da laboratorio presso i suoi Technology Excellence Center (TEC). Il nuovo EZ-fill Kit di Stevanato Group offre un rapido accesso a una soluzione personalizzabile e versatile per le aziende farmaceutiche e biotecnologiche che necessitano di riempire piccoli lotti con formulazioni iniettabili di alta qualità durante gli studi clinici o le fasi commerciali.
L’impennata registrata dall’industria biofarmaceutica per il trattamento di una
varietà di malattie in diverse aree terapeutiche può segnalare un potenziale di crescita significativo per le aziende farmaceutiche. Gli iniettabili, che rappresentano più del 60% degli oltre 21.000 farmaci at tualmente in fase di sviluppo, di cui il 44% biofarmaci, richiedono tecnologie di confezionamento primario e di somministrazione ad alte prestazioni per una corretta conservazione e somministrazione.
me ad essere utilizzata per il confezionamento farmaceutico. La resina PET Loop contribuisce all’economia circolare, riducendo le emissioni di gas serra e permettendo di risparmiare fino a 360.000 tonnellate di CO2 all’anno rispetto al PET vergine prodotto da combustibili fossili.
Bormioli Pharma ha testato la resina PET Loop nella sua offerta di packaging primario, commissionando a terze parti indipendenti ulteriori analisi per verificare i livelli di extractables con diversi solventi, prendendo in considerazione anche le condizioni sperimentali più sfidanti.
EZ-fill Kit si basa sulla sua piattaforma esistente ready-to-use di soluzioni di contenimento pre-sterilizzate (flaconi, cartucce e siringhe) consentendo ai clienti di analizzare efficacemente diver-
si imballaggi primari in combinazione con prodotti farmaceutici. Il kit sarà disponibile come scatola modulare composta da contenitori in vetro pronti all’uso per farmaci, e da componenti aggiuntivi su richiesta, spediti tramite corriere. In questo modo, la piattaforma può offrire ai pazienti alti livelli di qualità e sicurezza durante l’intero ciclo di vita dei farmaci e migliorare la velocità con cui i nuovi farmaci entrano nel mercato. EZfill Kit è stato presentato a Pharmapack e la sua commercializzazione si prevede sarà disponibile a partire dal secondo trimestre del 2024.

Materiali 52 icf RIVISTA DELL’INDUSTRIA CHIMICA E FARMACEUTICA



Dalla flessibilità alla conformità: così il pharma accelera sul digitale
L’industria chimico-farmaceutica, sollecitata dalle normative e dalle esigenze di sicurezza e tracciabilità, sta giocando un ruolo trainante nella transizione digitale della manifattura italiana. Ne abbiamo parlato con Pier Alberto Guidotti, fondatore e Ceo di Analysis, oltre che ideatore del software per la compliance QualiWare.
di Alessandro Bignami
L’industria chimico-farmaceutica rappresenta uno dei comparti più coinvolti dalla transizione digitale, tanto da diventare un modello di riferimento per altre filiere. Il rigoroso apparato regolatorio non ha in questo caso frenato gli slanci innovativi, ma ha anzi spinto all’adozione di sistemi digitali in grado di aumentare sicurezza, tracciabilità e integrità del dato. In questo scenario, sta crescendo il contributo di QualiWare, il software modulare per la gestione della compliance alle normative sviluppato dalla società Analysis, fondata dall’ingegner Pier Alberto Guidotti nel 1995. Proprio con Guidotti, dalla quarantennale esperienza in informatica e autore di due libri sul tema “Digitalizzare l’impresa”, abbiamo avuto l’opportunità di riflettere su come l’industria italiana,
e quella chimico-farmaceutica in particolare, stia affrontando le sfide della transizione digitale.
Ingegner Guidotti, qual è oggi il livello di digitalizzazione dell’industria italiana?
“Il tessuto industriale del nostro paese, con la sua prevalenza di piccole e medie imprese, non è un terreno particolarmente fertile per l’evoluzione digitale. Lo confermano le statistiche elaborate sui risultati dei Check UP ICT effettuati da Confindustria Emilia, ai quali io stesso collaboro in qualità di esperto. Fra le aziende coinvolte, emerge chiaramente che il livello di digitalizzazione si abbassa in modo proporzionale alla dimensione. Salvo ovviamente eccezioni, perché non mancano i piccoli imprenditori illuminati che credono nel digitale. Ma la tendenza è chiara, oltre che significativa: nelle piccole strutture si tende a non investire su ciò che ‘non fa

54 icf RIVISTA DELL’INDUSTRIA CHIMICA E FARMACEUTICA Software


truciolo’, ovvero su una soluzione immateriale che non ha una relazione immediata con la crescita della produzione e del fatturato. Sebbene resti ancora molto da fare, l’Italia in questi anni ha fatto comunque passi avanti, anche per merito degli incentivi e in particolare del piano Industria 4.0”.
Questo discorso vale anche per la chimico-farmaceutica?
“La questione delle dimensioni vale pressoché per tutti i settori. La chimico-farmaceutica ha però la specificità della forte pressione regolatoria, che in molti casi include la digitalizzazione, finalizzata all’efficienza e alla trasparenza dei processi. Le rigide linee guida hanno spinto l’adozione di sistemi digitali, tanto che il settore life science si è affermato come un modello da seguire per altri comparti industriali. Nel pharma sono tanti gli aspetti sensibili dove le infrastrutture digitali sono essenziali: dalla cybersecurity alla protezione del dato, dalla tracciabilità al change management, dal controllo delle abilitazioni agli audit trail. Noi stessi abbiamo deciso di estendere le soluzioni che avevamo già implementato in aziende farmaceutiche a tutti i settori dove è stato possibile”.
Quali sono gli obiettivi di compliance che le soluzioni di QualiWare consentono di raggiungere?
“Mi soffermo su due aspetti della conformità: il primo riguarda la necessità di dare evidenza alla conformità del
Pier Alberto Guidotti, fondatore e Ceo di Analysis, è autore di due volumi dedicati al tema “Digitalizzare un’impresa”: “Manuale di sopravvivenza ICT per imprenditori e informatici” e “Riflessioni sul futuro digitale fra impresa e società”, entrambi pubblicati da Giraldi Editore
processo di produzione, attraverso la raccolta e l’archiviazione di tutti i dati necessari a questo scopo. Il secondo si concentra invece sulla possibilità di definire le proprie registrazioni come effettivamente elettroniche: perché è solo in questo caso che l’azienda può rinunciare alla documentazione cartacea e quindi dematerializzare”.
Come approcciate questi aspetti?
“In un modo un po’ diverso rispetto alla rigidità di molti strumenti digitali presenti sul mercato, che spesso imbrigliano le attività e la stessa evoluzione delle aziende. Sappiamo che oggi le attività produttive e le normative sono in costante cambiamento. Questo scenario impone la difficile sfida di tenere unite conformità e flessibilità, una sfida che QualiWare ha deciso di far propria fin dall’inizio. Crediamo infatti in un percorso che conduca dalla flessibilità alla conformità e non viceversa. Lo abbiamo vissuto in prima persona, essendo nati come spin-off di una piccola realtà, ormai 30 anni fa. Ci siamo poi concentrati sulla conformità, ma senza mai perdere l’approccio flessibile degli albori”.
Supportate le aziende nell’interpretazione dei tanti dati a disposizione e nella scelta di quelli più strategici per le loro decisioni?
“Le rigide linee guida hanno spinto l’adozione di sistemi digitali nel pharma, che si è così affermato come un modello da seguire per altri comparti industriali”
RIVISTA DELL’INDUSTRIA CHIMICA E FARMACEUTICA icf 55 Software
“Premetto che siamo degli operatori informatici e che non possiamo entrare nel vivo delle valutazioni strategiche di un’azienda. Tuttavia, la massima che ho sentito da un ingegnere di Formula 1 ci ricorda che ‘i dati non contano nulla se non sono interpretati nel modo corretto’. Dopo la corsa all’oro e al petrolio, oggi tutti inseguono il dato. Il problema che notiamo, però, è che spesso si accumula una massa di informazioni che poi nessuno guarda. Guardare i dati significa capire quali sono quelli davvero importanti per orientare la propria attività. Quello che noi possiamo fare è aiutare a fare sintesi, un po’ come nel display che si trova sul volante di una macchina di Formula 1 – per tornare a uno sport a me caro – il pilota vede solo i parametri essenziali alla guida. Nei corsi di formazione che conduco e nei due libri che ho scritto cerco di spiegare come si definiscono gli indicatori fondamentali e, soprattutto, a chi devono essere resi accessibili. Le informazioni che servono a una figura operativa sono in gran parte diverse
“L’intelligenza artificiale non crea, non intuisce, non immagina come fa l’essere umano, ma lo aiuta a mettere in fila le conoscenze necessarie a trovare una soluzione”
da quelli utili a un manager. Non basta produrre dati, occorre farne sintesi e indirizzarli in modo accurato. Altrimenti non servono o, se visti da chi non dovrebbe, fanno persino danni”.
Quali sono le difficoltà e i rischi che un’industria di processo può incontrare nella transizione digitale?
“Il rischio che vedo sta nella grande velocità con cui si sta muovendo il settore informatico. Per le imprese utenti è molto difficile stare al passo e spesso si trovano in affanno e confuse. Alcuni imprenditori arrivano a dichiarare che è inutile rinnovarsi se poi il giorno dopo le cose sono già cambiate. Io invece credo siano importanti anche i piccoli avanzamenti, che si concentrino su progressi concreti e non sulle mode. Penso all’intelligenza artificiale, di cui si raccontano potenzialità strabilianti ma che è già molto utile se applicata solo alle operazioni basiche, come il data entry. Ci vogliono gradualità e al contempo la visione di una prospettiva futura”.
Teme un atteggiamento rinunciatario delle imprese italiane di fronte all’incalzare della rivoluzione digitale?
“In Italia bisogna lavorare molto su una questione anzitutto culturale. Molte aziende abituate a sistemi che hanno sempre funzionato sono restie a cambiare. In tal modo però si evita di
guardare avanti, per poi accorgersi che, quando il cambiamento diventa inevitabile, si è rimasti troppo indietro”.
Come si può innescare un cambiamento culturale?
“Sarebbe d’aiuto che chi si occupa di innovazione digitale in azienda possa sedersi al tavolo dove si prendono le decisioni. Il problema è che non è facile trovare un dirigente interessato alla digitalizzazione e al contempo immerso nei processi aziendali. Spesso questa figura è scissa in due: da una parte il tecnico informatico che sa poco del processo, dall’altra il manager o il responsabile di reparto abilissimo nel suo lavoro ma lontano dal mondo ICT. Con l’affacciarsi delle nuove generazioni, credo tuttavia che presto sarà più facile interagire con figure dalle competenze trasversali”.
Qual è il ruolo della persona in questa transizione?
“L’uomo resterà fondamentale, perché la tecnologia, da sola, non può fare nulla. È la persona che traduce la tecnologia in efficienza e la rende davvero determinante per il progresso di un’azienda. Uno strumento ottimo in mano a operatori poco formati o motivati serve a poco. Viceversa uno strumento non eccellente in mano a chi lo sa usare bene può dare grandi risultati. L’Industria 5.0 parla proprio di questo”.
56 icf RIVISTA DELL’INDUSTRIA CHIMICA E FARMACEUTICA
Software
Dashboard scadenzario attività
Come si superano le resistenze al cambiamento tecnologico?
“Basterebbe una sola parola per rispondere: coinvolgimento. È importante che le persone si sentano parte attiva di questo processo, attraverso iniziative di condivisione e formazione”.
Come prevede inciderà l’intelligenza artificiale nello sviluppo e nella produzione di farmaci?
“Nella ricerca di nuovi farmaci, ossia al livello più alto della progettazione, l’AI viene applicata già da tanto tempo. La sfida più attuale e complicata è quella di portare i sistemi di intelligenza anche a supporto della produzione vera e propria. Alcune aziende farmaceutiche l’hanno implementata, per esempio, nell’ambito della qualità e dell’ottimizzazione. Ma non è una strada semplice ed economica, perché occorre inizialmente un lungo lavoro di équipe fra tecnici informatici e specialisti di processo. L’intelligenza generativa GPT sta però creando altre opportunità, grazie a nuovi modi di estrarre conoscenza dalle informazioni. Ciò consente di automatizzare le operazioni di data entry, ma anche, in prospettiva, di sintetizzare la mole di informazioni non strutturate e provenienti da diverse fonti al fine di usarle per scopi precisi. Per esempio, se ho un problema sul processo, posso chiedere all’AI di suggerirmi delle soluzioni sulla base di come un proble-

ma simile è stato risolto in passato. L’intelligenza artificiale funziona tramite modelli probabilistici, facendoci risparmiare molto tempo in ricerche di documentazione o in tentativi già falliti in precedenza. Ma alla fine è ancora la persona a valutare e scegliere la soluzione più corretta. L’AI non crea, non intuisce, non immagina come fa l’uomo, ma aiuta a mettere in fila le conoscenze necessarie a trovare una soluzione”.
Che effetto ha avuto la pandemia sulla transizione digitale delle imprese?
“L’effetto più diretto è stato quello di sdoganare l’uso di modalità digitali di lavoro, a partire dello smart working, che ha portato alcuni vantaggi, come la riduzione degli spostamenti con le relative emissioni e la maggiore compatibilità fra vita professionale e familiare. Ma oltre a questo cambiamento, più visibile e diffuso, c’è stata anche un’accelerazione degli investimenti sulla digitalizzazione in generale. Un circolo virtuoso che include il potenziamento di infrastrutture e reti, grazie anche ai fondi del PNRR, e dei sistemi

di gestione. Il Covid insomma ha messo l’accento su digitalizzazione e sostenibilità, proprio i temi che sono al centro della nostra attività”.
C’è un’effettiva tendenza al ritorno dal cloud all’on premise?
“Non posso dire che al momento ci sia questa tendenza, però sono convinto che in futuro emergerà. Il susseguirsi di emergenze ed eventi traumatici sta mettendo in allerta le aziende, che sempre più vorranno avere i propri asset disponibili off line e sul posto. Credo che l’ideale sia adottare delle soluzioni ibride, che prevedano entrambe le possibilità, in modo che se succede qualcosa in rete, o viceversa nel proprio stabilimento, i sistemi siano comunque sempre disponibili all’uso, con interruzioni di servizio minime. La business continuity è d’altronde una delle principali sfide della transizione digitale. Le aziende chimico-farmaceutiche, per la rilevanza e i rischi della loro filiera, lo hanno capito molto bene”.
Quali obiettivi si è posto per il 2024?
“Vogliamo consolidare la posizione di QualiWare sul mercato e farla crescere ulteriormente nel settore chimico-farmaceutico. Intendiamo spiegare i plus del nostro sistema e raccontare le possibili applicazioni dell’intelligenza generativa. Ci interessa fare chiarezza non solo sulla tecnologia, ma anche sul contesto in cui essa può essere applicata e sui vantaggi concreti che consente di ottenere”. l
L’home page di QualiWare, il software modulare per la gestione della compliance alle normative sviluppato da Analysis
RIVISTA DELL’INDUSTRIA CHIMICA E FARMACEUTICA icf 57 Febbraio/Marzo 2024
Software
AMI-II LineTOC

TOC: un parametro cruciale per la qualità dell’acqua
L’acqua usata nell’industria farmaceutica deve rispettare specifici requisiti, tra cui quello del TOC, carbonio organico totale: per il suo monitoraggio in continuo, SWAN ha sviluppato una nuova versione del suo analizzatore, ancora più compatta e semplice da gestire.
L’acqua è ampiamente utilizzata nell’industria farmaceutica come materia prima, ingrediente e solvente nella lavorazione, formulazione e fabbricazione di prodotti, principi attivi e intermedi.
Per raggiungere la qualità dell’acqua richiesta dagli standard della farmacopea USP <1231>, la produzione nel settore farmaceutico deve soddisfare alcuni requisiti specifici: tra questi, il TOC è uno dei parametri cruciali e richiede spesso un monitoraggio
in continuo. Il TOC, acronimo dell’inglese Total Organic Carbon, è un parametro aspecifico che riporta il peso in parti per miliardo (ppb) di carbonio derivante dalle sostanze organiche presenti nell’acqua. Nell’ottica di un costante miglioramento tecnico, Swan Analytical Instruments ha sviluppato l’analizzatore in continuo AMI-II LineTOC Compact, una nuova versione che si affianca al collaudato modello precedente riducendone le dimensioni, in modo da semplificare installazione e manutenzione anche su impianti con ingombri ridotti.
La nuova piattaforma AMI-II si arricchisce di ulteriori caratteristiche in grado di rispondere in modo semplice
58 icf RIVISTA DELL’INDUSTRIA CHIMICA E FARMACEUTICA Strumentazione
Compact senza cover
ai crescenti requisiti del settore farmaceutico, come la conformità a FDA 21 CFR Part 11 e Data Integrity.
Le tecniche analitche
Swan utilizza da sempre il metodo dell’ossidazione diretta mediante reattore UV, una metodica collaudata e diffusa nel settore farmaceutico.
In questo articolo viene approfondita tale tecnica analitica, arricchita dalle migliorie apportate allo strumento di misura AMI-II LineTOC per potenziarne la performance del reattore UV e, di conseguenza, anche la precisione della misura stessa.
I più diffusi processi per la determinazione del TOC si basano sull’ossidazione del carbonio organico presente nell’acqua e la conseguente misura del biossido di carbonio (CO2) prodotto: decomposizione termica catalitica e misura della CO2 con detector NDIR (IR Non Dispersivo), decomposizione con UV-persolfato e misura di CO2 con detector NDIR o misura di conducibilità, oppure ossidazione UV diretta e misura di conducibilità.
Ogni metodo ha vantaggi e svantaggi, a seconda di quanto ossidazione e misura siano tecnicamente efficaci; perciò, ogni applicazione deve essere esaminata per decidere quale metodo sia più adeguato.
Ossidazione UV diretta
La possibile contaminazione organica nell’acqua ultrapura dell’industria farmaceutica si trova generalmente in concentrazioni molto piccole, il che rende l’ossidazione UV diretta un metodo efficace: in ogni caso, i prerequisiti per una completa ossidazione del carbonio organico sono un reattore UV ottimizzato e adeguate condizioni di misura.
Procedura di misurazione
Come schematizzato in figura 1, dopo la prima misura di conducibilità (To-
tal Inorganic Carbon, TIC), il campione entra nel reattore UV, dove avviene l’ossidazione del carbonio organico, ed è poi inviato alla seconda misura di conducibilità (Total Carbon, TC); dalla differenza di conducibilità tra i due sensori, si calcola il contenuto di TOC, secondo la seguente formula:
TOC = TC – TIC
Come ogni altro metodo, l’ossidazione UV diretta ha le sue peculiarità:
• intervallo di misura limitato < 2 μS/ cm a 20°C / < 1 ppm TOC;
• misura influenzata da effetti termici;
• riproducibilità dell’ossidazione UV insufficiente.
Per evitare o limitare questi aspetti, gli sforzi per sviluppare ulteriormente lo strumento si sono concentrati sui seguenti obiettivi:
• stabilizzazione delle condizioni termiche del dispositivo;
• aumento della densità di radiazione durante l’ossidazione;
• ottimizzazione del flusso campione nel sistema.
Stabilizzazione delle condizioni termiche
La temperatura ha un’influenza significativa sulla misura di conducibilità e, durante l’ossidazione UV diretta, l’energia prodotta dalla lampada UV può aumentare la temperatura dell’acqua di oltre 10°C, a seconda del design del reattore: tale differenza deve essere compensata, ma ogni compensazione è solo un’approssimazione e comporta un errore, l’entità del quale dipende da temperatura e conducibilità. Il problema è stato tecnicamente aggirato collegando uno scambiatore di calore a monte del reattore, in modo tale che l’acqua in uscita dal reattore stesso riscaldi quella in ingresso, in controcorrente.
Con questo accorgimento, la differen-
za di temperatura tra le due letture rimane al di sotto di 0,2°C: soprattutto i campioni con bassi valori di TOC beneficiano di questo metodo, con letture considerevolmente più stabili e meno soggette a fluttuazioni.
Aumento della densità di radiazione durante l’ossidazione
Le lampade UV usate al giorno d’oggi (lampade al quarzo a bassa pressione di Hg) producono piena potenza in uno stretto range di temperatura, solitamente tra 40 e 50°C; una variazione di temperatura di lavoro di 10°C può risultare in una perdita di potenza di quasi 20% ed è quindi molto importante mantenere la temperatura della lampada nel range migliore: un elemento riscaldante (C in figu-

ra 2) o refrigerante aggiuntivo (a seconda dell’applicazione) permette di stabilizzare con precisione una temperatura target di 42°C e di raggiungere la massima efficienza di radiazione, risultante in un’ottimale ed uniforme ossidazione.
Ottimizzazione del flusso campione
Le innovazioni tecniche menzionate mostrano già un sostanziale miglioramento del sistema, ma solo ottimizzando il flusso campione si può raggiungere il pieno potenziale. Nel design classico di un reattore UV,
RIVISTA DELL’INDUSTRIA CHIMICA E FARMACEUTICA icf 59 Febbraio/Marzo 2024 Strumentazione
AMI-II LineTOC Compact con cover in acciaio inox
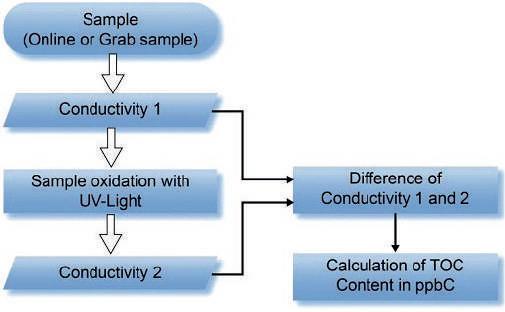
AMI-II LineTOC (A: blocco d’ingresso; B: scambiatore di calore; C: elemento riscaldante; D, E: sensori di conducibilità; F: reattore UV)
il campione fluisce attorno alla lampada, con inevitabili perdite per diffusione, riflessione ed accumulo di depositi sulla superficie direttamente irradiata, che, sul lungo periodo, comporta una riduzione della densità di radiazione. Questi effetti collaterali possono essere evitati solo mediante il diretto contatto tra lampada UV e campione: nel reattore UV recentemente sviluppato (figura 3), il campione fluisce direttamente lungo la sorgente UV, con una distanza massima dal centro della lampada di 8 mm ed uno strato campione spesso appena 0,5 mm.
La struttura ermetica evita la produzione di ozono e perdite per diffusione, con un netto aumento della densità di radiazione, risultante poi in una completa ossidazione dei composti organici presenti nel campione. La lampada UV è parte integrante del reattore che, in caso di guasto, può essere interamente sostituito e riciclato, per una manutenzione più facile e veloce.
Campionamento automatico
Nell’AMI-II LineTOC la misura è resa indipendente dal flusso campione gra-

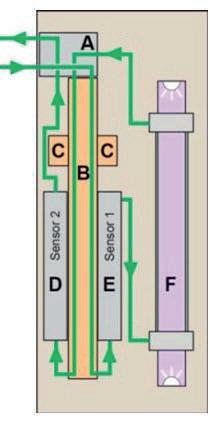
zie ad una pompa peristaltica, posta a valle del sistema, che aspira solo una limitata quantità di acqua (300 ml/h); inoltre, una valvola a spillo permette di regolare la velocità di campionamento e garantire una misura sempre rappresentativa anche con analizzatore distante dal punto di spillamento. Un flussimetro digitale permette di monitorare costantemente il flusso dell’acqua che passa all’interno dell’analizzatore ed interrompere l’analisi nel caso di assenza campione, generando un apposito allarme. L’analizzatore riprende automaticamente il suo funzionamento una volta che il flusso campione è ristabilito.
Applicazione farmaceutica
Gli strumenti impiegati in applicazioni farmaceutiche devono superare un test di verifica, il System Suitability Test (SST), obbligatorio e strettamente normato dalla farmacopea ufficiale (USP 643 / EP 2.2.24). L’AMI-II Line TOC ha in dotazione di serie tutto il
necessario per eseguire la verifica anche in modo autonomo da parte del cliente. La procedura automatica limita qualsiasi rischio di errore umano. Con la nuova piattaforma AMI-II è stata aggiornata la gestione dei dati rispondendo a quanto previsto dalla FDA 21 CFR Part 11, migliorando le seguenti funzionalità:
• cronologia non modificabile delle attività eseguite (Audit Trail);
• password univoche per ciascun utente;
• firma elettronica;
• download di data logger criptato non modificabile.
Analisi di campioni manuali
Un ulteriore vantaggio dell’AMI-II LineTOC è la possibilità di esaminare un “grab sample”: un campione, prelevato manualmente in apposita bottiglia, viene facilmente collegato allo strumento e misurato semplicemente premendo un tasto. Le uscite del segnale rimangono in “hold” per tutto il tempo della misura e del successivo risciacquo.
Conclusioni
L’attenzione nello sviluppo dell’analizzatore di TOC si è focalizzata su tre aree:
• stabilizzazione delle condizioni termiche;
• aumento della densità di radiazione;
• ottimizzazione del flusso campione nel sistema.
Le soluzioni tecniche presentate hanno portato evidenti miglioramenti in precisione ed accuratezza dell’ossidazione diretta UV. Inoltre, nella fase di sviluppo dello strumento sono stati presi in considerazione i severi requisiti dell’industria farmaceutica riguardanti le procedure di calibrazione e verifica. Tutte queste innovazioni tecniche sono presenti nello strumento AMI-II LineTOC di Swan Analytical Instruments. l
60 icf RIVISTA DELL’INDUSTRIA CHIMICA E FARMACEUTICA Strumentazione
Figura 1: Diagramma schematico dell’ossidazione UV diretta
Figura 2: Reattore
Figura 3: Sezione di un reattore UV
Figura 2
Valvola a saracinesca scorrevole per l’industria di processo
Vulcanizzare, sterilizzare, cuocere ed essiccare: molti processi industriali richiedono un controllo molto preciso dei mezzi liquidi, gassosi e vaporosi. Lo specialista in valvole Schubert & Salzer Control Valves, distribuito in Italia da Precision Fluid Controls, con la sua nuova valvola a saracinesca scorrevole tipo 8028 ha sviluppato una soluzione particolarmente compatta, leggera ed efficiente energeticamente per tutte le aree dell’industria di processo.
Inoltre, con un attuatore pneumatico a membrana da 80 millimetri e un posizionatore digitale, la valvola di controllo è molto veloce, quasi priva di usura e di manutenzione, e a bassa rumorosità. Grazie alle sue piccole dimensioni e al design salvaspazio della flangia intermedia, il tipo 8028 è eccellente in spazi limitati. Con una dimensione nominale di DN100, per esempio, la dimensione totale della
versione GS1 è solamente di 487 millimetri. Il design compatto, inoltre, abbassa il consumo energetico durante le operazioni e conserva le risorse nei settori manifatturiero e logistico. La tecnologia a saracinesca scorrevole usata nel tipo 8028 controlla il flusso in millisecondi, pertanto due dischi scanalati disposti verticalmente alla direzione del flusso scorrono uno sull’altro in un movimento lineare. L’attuatore deve quindi superare la frizione di scorrimento tra i due dischi. La forza attuatrice richiesta è del 90 percento inferiore rispetto alle valvole a sfera con la medesima misura nominale e stessa pressione differenziale.
Le brevi escursioni dell’attuatore di soli 6-9 millimetri riducono l’usura nell’imballaggio e nell’azionamento della valvola di controllo. Anche quando i materiali difficili rimangono attaccati allo stelo del pistone la
tenuta delle valvole di precisione rimane sempre intatta in quanto lo stelo del pistone si muove appena nell’imballaggio.
Schubert & Salzer Control Systems offre il tipo 8028 di valvola a porta scorrevole in misure nominali da 15 a 150 millimetri. Questa controlla il prodotto con temperature che vanno da -60 a 35°C e può essere usata a temperatura ambiente da -30 a 100°C. La massima pressione di esercizio arriva a 40 bar a seconda della grandezza nominale. L’elasticità di funzionamento è di 40:1 lineare e 80:1 per uguale percentuale di flusso.
Barriere reflex con rilevamento tramite luce rossa a LED
Wenglor sensoric group, azienda tedesca che sviluppa e produce sensori intelligenti, dispositivi di sicurezza e sistemi avanzati di elaborazione di immagini, amplia ulteriormente il suo portafoglio di dispositivi optoelettronici PNG//smart con le nuove barriere reflex P1PM. Con un innovativo metodo di rilevamento tramite luce rossa a LED, le barriere reflex P1PM sono in grado di riconoscere oggetti di qualsiasi forma, colore e materiale, individuando l’intensità della luce retrodiffusa e la distanza. Le barriere reflex P1PM, disponibili in quattro varianti, convincono soprattutto per la loro versatilità che le rende adatte ad applicazioni più disparate: controllo di presenza, riconoscimento di contrasto, verifica del livello di riempimento e controllo dell’espulsione. Grazie al principio di rilevamento combinato, le barriere reflex rile-
vano, oltre all’intensità della luce retrodiffusa, anche la distanza del punto luminoso da uno sfondo di riferimento precedentemente impostato tramite funzionalità Teach-in. Le distanze e le caratteristiche degli oggetti vengono rilevate in modo affidabile fino a un metro, indipendentemente dal colore, dalla forma e dal materiale delle superfici.
Il rilevamento di oggetti lucidi, irregolari e persino semitrasparenti avviene in modo affidabile, senza che ciò richieda un catarinfrangente.
Le caratteristiche in breve:
• Riconoscimento dell’oggetto senza contatto tramite luce rossa a LED, indipendentemente da colore, forma e materiale delle superfici dell’oggetto, senza necessità di un catarifrangente aggiuntivo.

• Rilevamento affidabile di oggetti lucidi, irregolari e semitrasparenti.
• Innovativo metodo di rilevazione, che rileva la distanza e l’intensità.
• Quattro varianti con due modalità operative separate: teach-in su sfondo di riferimento statico e mobile.
• Regolazione dinamica per un rilevamento ancora più affidabile.
• IO-Link 1.1 per un facile settaggio e una facile integrazione.
• Nessuna zona cieca.

Strumentazione
Febbraio/Marzo 2024
icf 61
RIVISTA DELL’INDUSTRIA CHIMICA E
FARMACEUTICA
Ammoniaca e idrogeno: sulla strada della transizione energetica
SICK offre un’ampia serie di soluzioni di misura per il ciclo produttivo dell’ammoniaca, un settore in crescita e destinato ad avere un ruolo importante nell’economia verde, sia in relazione alla produzione di idrogeno sia come carburante a basso impatto ambientale.
di Alessandro Bignami
L’ammoniaca è una delle sostanze chimiche più prodotte al mondo. La sua produzione avviene in più di 600 impianti, con un tasso di crescita annuo del 3-5%. È un materiale di partenza per una grande varietà di prodotti, tra cui fertilizzanti (circa 85%), poliammidi (circa 5%), acido nitrico (circa 5%) e i suoi derivati. Ma soprattutto è una delle sostanze destinate ad avere un ruolo strategico nell’ambito della transizione ecologica ed energetica. Fondamentale in questo senso è anche la strumentazione di misura, che viene applicata nel suo ciclo produttivo e che vede SICK fra i maggiori produttori internazionali. Da questi spunti ha preso il via la nostra conversazione con l’ingegner Alberto Pronzati, Sales Manager di SICK S.p.A.
Ingegner Pronzati, ci può accennare all’offerta tecnologica di SICK dedicata al processo di produzione dell’ammoniaca...
“La nostra divisione dedicata alla strumentazione per il monitoraggio delle emissioni e al controllo di processo offre importanti applicazioni nella produzione di ammoniaca, un mercato che sta crescendo molto, sia in relazione alla filiera dei fertilizzanti sia a quella dei combustibili alternativi. I nostri strumenti consentono ai grandi produttori internazionali di ottimizzare il processo e ridurre gli sprechi e le emissioni. Possiamo fornire soluzioni per i più tradizionali sistemi di produzione dell’ammoniaca, come il processo Haber-Bosch, che prevede la sintesi di idrogeno e azoto, con il recupero e la rimessa in produzione dell’idrogeno che non si è legato all’azoto. In tale processo è necessario un controllo accurato sull’eventuale uscita di ammoniaca dal ciclo di produzione. Con la tecnologia dei nostri analizzatori è possibile misurare concentrazioni molto basse di ammoniaca, fino a 20 ppm, con un sistema di analisi estrattivo, quindi

62 icf RIVISTA DELL’INDUSTRIA CHIMICA E FARMACEUTICA Strumentazione
più conveniente rispetto ai gascromatografi. Inoltre, durante la sintesi di ammoniaca, CO e CO2 agirebbero come avvelenamento del catalizzatore, provocando la formazione di sali. Pertanto, è necessario eliminarli quasi del tutto prima della fase di sintesi. Per contenere al massimo i problemi causati da CO e CO2 è necessario rilevarli già nel range di ppm molto basso”.

La produzione di ammoniaca e di fertilizzanti è ancora fortemente legata al reforming del metano... “A questo proposito forniamo un pacchetto di strumenti completo, nell’ambito della produzione di idrogeno tramite steam reforming. In tale contesto, gli strumenti di SICK consentono il monitoraggio dei gas e dei vari componenti della miscela, che viene generata lungo i vari cicli di filtrazione e separazione. Gli analizzatori delle famiglie S700 e GMS800 costituiscono la base per l’analisi personalizzata di gas di processo, al fine del monitoraggio dei processi e delle emissioni durante la produzione di idrogeno e ammoniaca. Con S700 e con GMS800 è possibile misurare tutti i composti di gas rilevanti per questo processo, di volta in volta, con due, tre o persino sei diversi tipi di moduli di analisi. A seconda del compito di misura, del luogo d’impiego e delle condizioni ambientali, sono disponibili diversi tipi di custodie. Tra queste vi sono anche custodie a parete conformi alla direttiva ATEX per zone con pericolo di esplosione, che possono essere utilizzate in ambienti industriali difficili. Equipaggiato con un modernissimo software, il GMS800 dispone anche delle interfacce necessarie per un controllo a distanza, tra-
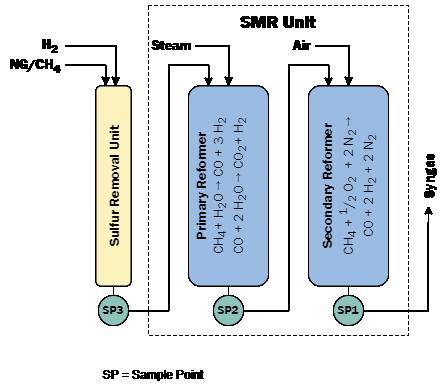
Il monitoraggio del processo di produzione dell’ammoniaca presenta delle sfide specifiche?
“Una delle principali forme in cui l’ammoniaca viene distribuita è quella in granuli. Ciò comporta un attento controllo della qualità dell’aria all’interno dell’unità di granulazione, attraverso, per esempio, la misurazione della presenza di sali e polveri di ammoniaca, che può avvenire con i nostri misuratori di polvere. Penso al polverimetro FWE200DH concepito per la misura continua delle concentrazioni di polvere nei gas

L’ammoniaca giocherà un ruolo strategico nella transizione energetica?
“Sì, e non solo in relazione alla produzione di idrogeno, ma anche in sé come combustibile alternativo a basso impatto ambientale. Proprio la produzione di combustibili di sintesi, come l’ammoniaca, spingerà anche l’Europa a investire in impianti di produzione di idrogeno, per lo più in contesti locali, al fine di evitare i maggiori costi e le problematiche delle infrastrutture
Alberto Pronzati, Sales Manager
SICK S.p.A.
CHIMICA E FARMACEUTICA icf 63 Strumentazione
di
produzione di idrogeno
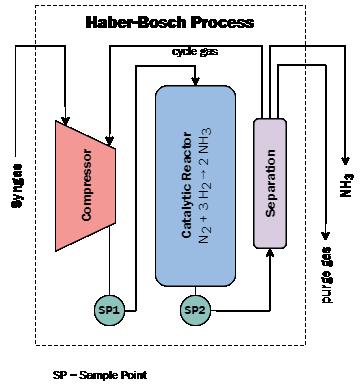
Harber-Bosch
Process per la produzione di ammoniaca
Stiamo quindi parlando di un carburante sostenibile…
“Sì, ad oggi anche più dell’idrogeno, poiché l’ammoniaca è più facile da gestire e trasportare. L’utilizzo è da prevedere soprattutto per le grandi navi commerciali e da crociera, che usano notoriamente combustibili con un alto impatto ambientale, ma senza escludere i mezzi pesanti su gomma. Dato che la produzione di ammoniaca dal reforming del metano comporta delle emissioni di CO2, la quale andrebbe stoccata, l’ideale sarebbe la produzione a partire da idrogeno ottenuto in modo sostenibile. Questo è il punto più delicato di questo disegno, poiché la produzione di idrogeno con energie

rinnovabili è ancora troppo bassa per rispondere a questa domanda a costi accessibili. Il metodo più conveniente per produrre idrogeno resterà ancora per diversi anni lo steam reforming del metano, ma ciò non esclude le grandi prospettive a lungo termine per l’ammoniaca verde. Si tratta di un percorso articolato, che ha bisogno di investimenti importanti nelle infrastrutture e nelle attrezzature per l’elettrolisi dell’acqua. I nostri strumenti sono intanto già ampiamente utilizzati nella produzione più tradizionale dell’ammoniaca, dove contribuiscono a rendere il processo più efficiente e sostenibile, anche grazie all’aumento dei punti di misura e controllo lungo il ciclo produttivo”.
I vostri strumenti vengono applicati anche per le misurazioni nei blending di gas?
“Sì. Oggi, tra l’altro, l’utilizzo più concreto e immediato dell’idrogeno, in qualità di vettore energetico, è proprio quello nei blending immessi all’interno della rete del gas, nelle basse percentuali previste dalle normative. SICK, a tal proposito, mette a disposizione la famiglia di dispositivi FLOWSIC500 e 600XT, già predisposti per misurazioni in percentuale di idrogeno, fino al 30%, ben oltre i limiti al momento autorizzati e quindi già pronti per chi sta investendo con uno sguardo al futuro. Sono strumenti smart e con una lunga aspettativa di vita, circa 15 anni, con la flessibilità per adattarsi a diverse percentuali di idrogeno non solo per composizioni che possono cambiare nel tempo, ma anche perché lo stesso blending può presentare diverse concentrazioni di idrogeno a seconda del punto di controllo. La tecnologia ultrasonica, inoltre, offre, senza bisogno di aggiungere ulteriori sistemi, sia la misura della portata sia della qualità dell’idrogeno conte-
nuto, consentendo così di quantificare il valore energetico del blending, che è ciò che conta di più. SICK produce misuratori di portata gas a ultrasuoni da molti anni, pertanto, la capacità di misura di questi prodotti è nota e collaudata”.
La transizione energetica offrirà insomma tante opportunità per l’applicazione delle vostre tecnologie… “SICK sta investendo molto nella transizione, sviluppando e fornendo soluzioni per i suoi diversi aspetti, dalla produzione di idrogeno ed ammoniaca al monitoraggio delle emissioni, fino alla cattura e stoccaggio di CO2. Tutto questo senza in realtà inventarsi nulla, ma proponendo e adattando tecnologie che fanno già parte della nostra gamma. Accettare la sfida della transizione ecologica, e dell’idrogeno green in particolare,

64 icf RIVISTA DELL’INDUSTRIA CHIMICA E FARMACEUTICA Strumentazione
Analizzatore di gas estrattivo GMS800
Sistema modulare S700

Misuratore a ultrasuoni del flusso di gas FLOWSIC600-XT
ha significato per l’azienda, infatti, far evolvere le famiglie di misuratori precedenti, come FLOWSIC600, rendendole ancora più performanti ed affidabili. Oggi, FLOWSIC600-XT garantisce un agevole e preciso bilanciamento della rete, grazie alla capacità di misurare precisamente il flusso di gas anche alle portate minime e a nuove funzioni innovative e rivoluzionarie”.
Il mercato italiano a che punto è su questi temi?
“La maggior parte degli investimenti fa capo ai pochi grandi distributori di gas, interessati a rendere efficiente la rete per ridurre gli sprechi e ottimizzare la filiera. Sulle energie rinnovabili, tuttavia, si fa ancora troppo poco. L’iniziativa è lasciata alla buona volontà delle singole aziende. Sul fronte dell’idrogeno prevalgono i piccoli impianti, sotto i 5 MW, per produzioni locali. Manca una regia complessiva, una politica energetica che scelga i vettori su cui puntare e che crei le condizioni per sviluppare il know-how necessario, anche alla luce degli asset specifici della nostra industria. In ogni caso SICK, con la sua strumentazione avanzata, si propone come uno dei protagonisti tecnologici di questa sfidante transizione, accanto ai grandi player industriali ed energetici con cui da tempo lavora, in Italia e nel mondo”.
S700
Con il sistema modulare S700 è possibile configurare diverse applicazioni di analisi fatte su misura. Per la realizzazione di soluzioni di sistema compatte e a basso costo si può dotare un involucro S700, in modo standard, con al massimo 3 moduli di analisi. Sono a disposizione fino a 5 diversi moduli per l’analisi di più di 60 componenti di gas. In base alla matrice di gas, al luogo d’impiego e alle condizioni ambientali ci sono le seguenti tipologie d’involucro: S710 in versione rack 19’’ per sistemi di analisi e applicazioni standard, S715 con custodia a parete in condizioni di impiego difficili e zona Ex 2 (ATEX), S720 resistente alla pressione, pressurizzato per zona Ex 1 (ATEX).
GMS800
La famiglia di prodotti GMS800 è costituita da innovativi analizzatori di gas estrattivi, in grado di misurare oltre 60 diversi componenti del gas. L’analizzatore di gas GMS800 si caratterizza per il sobrio design modulare, costituito da: 6 moduli di analisi, un modulo gas, moduli I/O e unità di controllo. Per l’integrazione economica nel sistema, può essere utilizzata una custodia a innesto standard da 19”. Nei difficili ambienti industriali sono utilizzate custodie a pareti con omologazione ATEX per zone Ex. Dotato di moderno software facile da utilizzare, il GMS800 dispone di tutte le interfacce necessarie per il controllo remoto tramite rete e per il collegamento a un sistema di controllo di processo.
FLOWSIC600-XT
FLOWSIC600-XT, lo strumento di misura del flusso di gas con tecnologia a ultrasuoni, definisce nuovi standard nel proprio segmento di mercato. È disponibile come variante con 4, 4+1, 4+4 e 8 percorsi di misura per soddisfare diverse esigenze applicative, come solu-

zione singola o di sistema. Oltre ai requisiti di OIML R 137 Class 1.0, FLOWSIC600-XT soddisfa appieno anche i requisiti Class 0.5 e AGA9. Lo strumento di misura comprende i-diagnostics™, una funzione per applicazioni di diagnosi intelligenti, e PowerIn Technology™, che consente la prosecuzione ininterrotta della misurazione fino a tre settimane, anche in caso di interruzione della corrente. Queste funzioni facilitano le applicazioni e supportano la sicurezza di funzionamento, garantendo un’ottimale precisione di misura e stabilità a lungo termine.
FWE200DH
Il polverimetro FWE200DH è stato concepito per la misura continua delle concentrazioni di polvere nei gas umidi. Il gas viene prelevato tramite una sonda di campionamento del gas e riscaldato in un ciclone termico ad una temperatura sopra il punto di rugiada dei gas. Le gocce contenute nel gas vengono vaporizzate e perciò non possono più alterare il risultato della misurazione. Il principio molto sensibile di misurazione luce diffusa consente misurazioni accurate anche delle minime concentrazioni di polvere. L’FWE200DH soddisfa i requisiti delle normative EN 14181 e EN 15267. l


Febbraio/Marzo 2024 RIVISTA DELL’INDUSTRIA CHIMICA E FARMACEUTICA icf 65 Strumentazione
FLOWSIC600
FLOWSIC500
Lo sviluppo continuo dei misuratori di portata ad ultrasuoni
La famiglia di dispositivi Prosonic Flow di Endress+Hauser è in costante evoluzione. Grazie ai sensori clamp-on, gli strumenti non interferiscono con il processo all’interno della tubazione e non vengono danneggiati da eventuali liquidi aggressivi.
Imisuratori di portata a ultrasuoni hanno fatto grandi progressi da quando hanno cominciato a essere utilizzati nella tecnologia di misurazione industriale. La tecnologia è ormai completamente sviluppata, ma c’è ancora spazio per miglioramenti. Endress+Hauser sta portando avanti lo sviluppo dei suoi misuratori di portata clamp-on con misurazione a ultrasuoni del tempo di volo in tre modi: migliorando le prestazioni, semplificando la gestione durante l'intero ciclo di vita ed espandendo le aree di applicazione per includere anche gli utilizzi off-label.
guarnizioni. I sensori non entrano mai in contatto con il mezzo liquido, quindi liquidi aggressivi, corrosivi o abrasivi non rappresentano un problema per la strumentazione.

per verificare il funzionamento della strumentazione in linea esistente.
Proline Prosonic Flow W 400 e P 500
Prosonic Flow W 400 e Prosonic Flow P 500 sono i due misuratori di portata a ultrasuoni clamp-on di Endress+Hauser. Essi possono fare ciò che ci si aspetterebbe dalla tecnologia utilizzata: misurare, totalizzare e bilanciare la quantità e il volume dei flussi di liquidi nelle tubazioni e quindi monitorare i processi o rilevare perdite. In linea di principio, i sensori clamp-on possono essere installati senza aprire il tubo: questo significa che, a differenza della strumentazione in linea, non sono necessarie
Clamp-on significa anche che possono essere adattati a sistemi esistenti senza interferire con le tubazioni mentre il processo è in corso. Attualmente, ciò è necessario ad esempio nei circuiti ausiliari o nei circuiti rilevanti dal punto di vista energetico, che originariamente non richiedevano alcuna strumentazione o richiedevano solo una strumentazione molto semplice a livello di controllo di processo, ma che ora devono essere registrati in modo più preciso, ad esempio per il bilanciamento e l'ottimizzazione dell'energia. È anche possibile impostare temporaneamente un punto di misura clamp-on, ad esempio
Applicazioni Ex e non Ex "Prosonic Flow W 400 è stato originariamente progettato pensando alla tecnologia dell'acqua e delle acque reflue, mentre Prosonic Flow P 500 per la tecnologia di processo, ovvero per un'ampia varietà di liquidi come idrocarburi o sostanze chimiche", afferma Thomas Jahn, responsabile della gestione dei prodotti a ultrasuoni presso Endress +Hauser. Tuttavia questa origine non ha influito sugli effettivi campi di applicazione. “I reali requisiti del punto di misura sono sempre decisivi nella scelta del sistema. Ex, SIL, temperatura e requisiti per ingressi e uscite sono le parole chiave più importanti in questo caso”, aggiunge Thomas Jahn.

66 icf RIVISTA DELL’INDUSTRIA CHIMICA E FARMACEUTICA Strumentazione
Misuratori di portata clamp-on a ultrasuoni


Prosonic Flow P 500 garantisce la sicurezza funzionale in conformità con la norma IEC 61508 (SIL) e può essere utilizzato in applicazioni legate alla sicurezza; dispone delle consuete autorizzazioni internazionali per atmosfere potenzialmente esplosive e può quindi essere utilizzato in aree pericolose, mentre Prosonic Flow W 400 è più adatto alle applicazioni di base.
I due dispositivi condividono dati tecnici di base; le prestazioni e la precisione di misurazione saranno le stesse per le generazioni di hardware a partire da
maggio 2024. Entrambi coprono diametri nominali dei tubi da 15 a 4000 mm, sufficienti anche per tubi ad alta pressione negli impianti di stoccaggio di energia elettrica. I sensori a ultrasuoni stessi sono robuste strutture in acciaio inossidabile e sono disponibili trasduttori per tutti i materiali comuni dei tubi, inclusi plastica e vetroresina, con e senza rivestimento. A seconda del diametro nominale, la temperatura del mezzo consentita va da -40°C a +130°C (W 400) o da -40°C a +550°C (P 500) e il campo di misura è 0–15 m/ S.
La turbolenza non è più un fattore di disturbo Pressione, densità e conduttività del medium non influenzano la misurazione del flusso con gli ultrasuoni per la maggior parte dei liquidi, ma per altri devono essere presi in considerazione. Per il petrolio greggio e i prodotti petroliferi raffinati in particolare, o più in generale per gli idrocarburi, la portata volumetrica effettiva viene determinata attraverso la compensazione della pressione e della temperatura. Endress+Hauser fornisce uno speciale pacchetto applicativo petrolifero che calcola i valori di correzione necessari sulla base delle tabelle di calcolo API MPMS e ASTM.
La compensazione basata su software aggiusta anche i risultati della misurazione in altri punti e consente di posizionare i dispositivi Prosonic Flow in quasi qualsiasi punto del sistema di tubazioni. Restrizioni e piegature causano turbolenze nel medium, che tipicamente distorcono i dati se il punto di misurazione è posizionato troppo vicino a questi disturbi. Endress+Hauser ha dotato entrambi i misuratori di portata della funzione interna FlowDC, dove DC sta per compensazione dei disturbi. FlowDC è una funzione supportata dal software che richiede solo pochi dati, in particolare la lunghezza del tratto di ingresso e il tipo di fattore di disturbo, per esempio una curvatura del tubo. Con l'aiuto di FlowDC il punto di misura può essere spostato fino al doppio del diametro del tubo fino al punto di interferenza, dove altrimenti sarebbe necessario un tratto rettilineo circa sette volte più lungo, cosa che spesso non è disponibile in sistemi angusti. Per la sezione di uscita è sufficiente anche il doppio del diametro nominale. I misuratori di portata FlowDC possono quindi essere installati anche dove non c’è una sezione di tubo rettilineo disponibile per altri dispositivi.
Sensori clamp-on di Endress+Hauser per misure di portata non invasive senza lavori sulle tubazioni o interruzioni del processo
RIVISTA DELL’INDUSTRIA CHIMICA E FARMACEUTICA icf 67 Febbraio/Marzo 2024 Strumentazione

Quando lo spazio è limitato: misuratore di portata clampon a ultrasuoni con funzione
FlowDC per prestazioni costantemente elevate anche con tratti di ingresso solo 2 x DN
FlowDC Strumentazione
Misurazione della portata a ultrasuoni in un impianto energetico: sensori clampon esenti da manutenzione su un tubo
DN 2000, con funzione
Web server nel dispositivo per un accesso diretto a tutte le funzioni Il supporto utente tramite software è una caratteristica fondamentale di entrambi i dispositivi Prosonic Flow. Tutti i dati diagnostici, di configurazione e del dispositivo sono accessibili direttamente e con una chiara guida per l'utente tramite il server web integrato. Anche durante l'installazione, la qualità del segnale può essere verificata tramite il pannello di controllo del trasmettitore o tramite il browser web di un dispositivo mobile. Ciò rende molto semplice determinare la posizione ottimale dei sensori. Il server web nel dispositivo elimina la necessità di strumenti e dati esterni, velocizzando tutto, dalla configurazione alla manutenzione del dispositivo.
La tecnologia Heartbeat integra funzioni di test
Come l'intera gamma di prodotti Proline, i dispositivi Prosonic Flow sono dotati della tecnologia Heartbeat. Questi dispositivi dispongono di funzioni di autodiagnostica, automonitoraggio e verifica, possono segnalare regolarmente il proprio stato al cloud e, ad esempio, consentire di pianificare i prossimi lavori di manutenzione utilizzando l'analisi delle tendenze. Le funzioni diagnostiche possono essere attivate anche manualmente in qualsiasi momento tramite il cloud. I messaggi diagnostici sono standardizzati secondo NAMUR NE 107.
Pensare fuori dagli schemi: le applicazioni off-label
La trasmissione degli ultrasuoni al medium nel tubo dipende dal perfetto accoppiamento acustico. I gel e le paste che garantiscono un collegamento senza spazi tra il sensore e il tubo presentano però un grande svantaggio: invecchiano e possono essere lavate via o seccarsi a seconda delle condizioni ambientali, modificando così le loro proprietà acustiche nel processo. Il risultato è una tendenza permanente difficile da prevedere perché fortemente influenzata da fattori variabili come le condizioni ambientali.
Endress+Hauser utilizza invece cuscinetti stabili a lungo termine o lamine metalliche resistenti al calore, che rendono superflua la sostituzione regolare di pasta o gel. Se si esclude il deterioramento dovuto all'invecchiamento, la deviazione sistematica dei valori misurati rispetto ad altri punti di misura può quindi essere attribuita ad altre cause, come ad esempio la formazione di depositi nel tubo. La modifica del contenuto di gas o particelle nel medium può avere un effetto simile sui valori misurati. "Possiamo anche determinare indirettamente qualcosa di più della semplice portata", afferma Thomas Jahn. “Come tali applicazioni off-label possono essere utilizzate in modo innovativo è qualcosa che dob-

biamo individuare insieme al cliente per casi specifici. Tuttavia, stiamo già valutando l’uso sperimentale in applicazioni reali”, aggiunge Jahn.
Semplicità significa efficienza in termini di costi
Dal punto di vista ingegneristico, le prestazioni tecniche sono senza dubbio un argomento chiave a favore o contro un particolare strumento. I criteri di selezione possono essere chiaramente definiti e applicati. Lo sforzo richiesto per il montaggio e l'installazione, la parametrizzazione e la messa in servizio, la manutenzione e l'assistenza nel corso della vita utile non è specificato in nessuna scheda tecnica con valori rigidi. Il punto è che si tratta di costi che spesso non vengono registrati a livello di dispositivo.
L'OPEX, ovvero le spese operative, e i costi del ciclo di vita (TCO) non sono la responsabilità principale dei dipartimenti di ingegneria e tecnologia. Tuttavia, a questo livello si notano costi operativi e di manutenzione elevati, anche se in una valuta diversa: le ore di lavoro. I misuratori di portata clamp-on di Endress+Hauser risolvono questo problema a tutti i livelli con la massima semplicità possibile. Installazione semplice durante il processo in corso, facile configurazione e parametrizzazione, facile accesso agli apparecchi tramite browser web da qualsiasi parte del mondo, esente da manutenzione permanente, accoppiamento acustico: tutto questo si traduce in un chiaro vantaggio in termini di profitti. Le prestazioni tecniche già elevate nelle principali aree di applicazione e le prime entusiasmanti applicazioni off-label, come il rilevamento di depositi nei tubi o di gas e particelle nel flusso volumetrico, fanno sì che possiamo aspettarci molto di più dal Prosonic Flow clamp-on: una famiglia di dispositivi in continuo sviluppo.
68 icf RIVISTA DELL’INDUSTRIA CHIMICA E FARMACEUTICA
INSPIRING SUSTAINABLE CONNECTIONS

10 - 14 June 2024
Frankfurt am Main, Germany
#ACHEMA24
World Forum and Leading Show for the Process Industries
ACHEMA is the global hotspot for industry experts, decision-makers and solution providers. Experience unseen technology, collaborate cross-industry and connect yourself worldwide to make an impact.
Are you ready? Join now!
L’automazione che supera le barriere
Emerson considera la Boundless Automation come una svolta per il superamento delle barriere imposte ai dati e per la modernizzazione delle operazioni. Al Global Exchange organizzato dall’azienda a Düsseldorf, molti player internazionali hanno potuto conoscere meglio questa tecnologia.
Sotto: l’area espositiva all’Emerson Exchange Emea 2024, che si è svolto a febbraio a Düsseldorf
Emerson, protagonista internazionale nel settore tecnologie e software, si prepara a trasformare la produzione industriale con un’architettura di automazione di nuova generazione, progettata per abbattere i silos e liberare i dati e tutta la potenza del software con la Boundless Automation™.
Ora che molte aziende fanno fatica
a estrarre tutto il valore disponibile dai loro sforzi di trasformazione digitale, diventano evidenti i limiti delle architetture di automazione odierne. Gli stack di tecnologie costruiti intorno a ciascun reparto funzionale (produzione, affidabilità, sicurezza e, più di recente, sostenibilità) hanno prodotto isole di dati frammentati, che si stanno rivelando difficili da integrare


o utilizzare. I vantaggi delle nuove informazioni approfondite promessi dalla trasformazione digitale restano di conseguenza solo sulla carta. Per risolvere questo problema e aiutare i clienti a raggiungere i loro obiettivi di ottimizzazione operativa, Emerson presenta una visione e una strategia pratica in grado di avvicinare una maggiore potenza di calcolo ai punti dove questa è necessaria e di definire il progetto di un moderno ambiente di elaborazione industriale. Questo ambiente comprende flessibilità di implementazione del software in tutto il campo intelligente, edge moderno definito dal software e cloud. I tre domini sono connessi mediante un’infrastruttura dati unificata, contribuendo a mantenere il contesto dei dati, migliorarne l’usabilità e potenziare la sicurezza.
“Dopo decenni di implementazione di strategie di automazione in continua evoluzione, i produttori hanno individuato l’esigenza di estrarre maggior valore dai dati bloccati in architetture di automazione rigide e obsolete”, ha dichiarato Lal Karsanbhai, presidente e Ceo di Emerson. “La proliferazione dei dati e lo sviluppo di software avanzati stanno aprendo a un’era di pro-
Automazione
Lal Karsanbhai, presidente e Ceo di Emerson
duttività che non ha precedenti. I dati copiosi e approfonditi e i software avanzati stanno convergendo e creando il prossimo importante punto di svolta nel settore”.
Karsanbhai si è rivolto ai leader del settore a Düsseldorf durante l’Emerson Exchange Emea 2024, la tradizionale conferenza internazionale organizzata per i clienti dei settori chimico, biotecnologico, dei metalli e dell’estrazione mineraria, dell’energia, dell’idrogeno, dei biocombustibili e della cattura del carbonio.
Un’architettura più “democratica” La moderna architettura di automazione definita dal software di Emerson è destinata a scompaginare le reti gerarchiche, democratizzando e contestualizzando in modo sicuro i dati per le persone e i motori di intelligenza artificiale (IA) che dipendono da un flusso di informazioni continuo. Emerson continua a innovare il suo vasto portafoglio di tecnologie in fase di sviluppo, affinché questo diventi la base per il futuro della Boundless Automation.
“Grazie a uno stack di tecnologie leader nel settore e a decenni di com-
provata esperienza, Emerson è posizionata in modo unico per progettare e implementare un’automazione in grado di ottimizzare l’estrazione di valore dagli investimenti tecnologici dei clienti e offrire miglioramenti misurabili delle prestazioni”, ha affermato Karsanbhai.
L’architettura della Boundless Automation di Emerson abbatterà le barriere e i silos di dati su campo intelligente, edge e cloud. L’integrazione di questi sistemi eterogenei con un’infrastruttura dati unificata offre nuove informazioni e aiuta le aziende a ottimizzare le operazioni in termini di produzione, affidabilità, sicurezza, sostenibilità e forza lavoro.

Emerson introduce con la Boundless Automation una moderna e sicura architettura di automazione, che libera i dati per utilizzare al meglio la potenza del software
Campo intelligente edge e cloud
Campo intelligente: un campo intelligente semplifica l’accesso a più dati da più fonti e crea opportunità per una maggiore varietà delle applicazioni. Con dispositivi più intelligenti e nuove tecnologie di connessione, come 5G e APL, i clienti possono semplificare sia la connettività da qualsiasi luogo del mondo, sia l’integrazione con la nuova architettura.
Edge: il nuovo edge OT crea un ambiente di calcolo moderno, sicuro e a bassa latenza, avvicinando i nuovi stru-
La Boundless Automation di Emerson trasforma architetture di automazione obsolete in un moderno framework di calcolo intelligente per campo, edge e cloud, connessi mediante un’infrastruttura dati unificata

menti software e i dati utili agli utenti. L’ambiente edge migliorato crea una piattaforma per i colleghi IT e OT per innovare e collaborare più di quanto sia mai accaduto prima. Cloud: il cloud offre funzionalità complesse per le funzioni operative e di progettazione on-premise e in tutta l’azienda, con infinite capacità di elaborazione analitica, collaborazione a livello aziendale, costi del ciclo di vita convenienti e supporto e assistenza a richiesta. l
La conferenza plenaria all’Emerson Exchange Emea 2024
RIVISTA DELL’INDUSTRIA CHIMICA E FARMACEUTICA icf 71 Febbraio/Marzo 2024 Automazione

May 15 TH 16 TH May 2024
ORGANIZERS


Leading the global market flow ⁕ Forum for the industrial valves industry ⁕ Innovations’ platform and technology summit ⁕ Trend-setting meeting point ⁕ Take-off for investment decisions ⁕ International network of experts and specialists INTERNATIONAL EXHIBITION AND CONFERENCE ON VALVE AND FLOW CONTROL TECHNOLOGIES 5 TH Attending IVS - Industrial Valve Summit gives you the opportunity to share knowledge, experience and ideas with other leading industry professionals anda organisations. IVS - INDUSTRIAL VALVE SUMMIT IS THE: industrialvalvesummit.com Organising Secretariat Ph. +39 035 3230911 e-mail info@industrialvalvesummit.com Bergamo, Italy
Farmaci orfani per malattie rare: un settore in forte sviluppo
Solo un decimo circa dei medicinali che hanno ricevuto la designazione a farmaco orfano nel periodo 2000-2022 hanno raggiunto l’ottenimento dell’autorizzazione all’immissione in commercio. Ciò nonostante, il settore delle malattie rare e dei farmaci orfani rimane uno dei più interessanti per le aziende, e dovrebbe venire rinnovato dalla revisione della legislazione farmaceutica europea ancora in corso.

elevati in fase di contrattazione tra le aziende produttrici e le autorità competenti a livello nazionale, oltre che dal poter godere di numerosi incentivi per il loro sviluppo.
di Filippo Neri
Ibisogni medici insoddisfatti hanno rappresentato uno degli ambiti di ricerca e sviluppo di nuovi medicinali più attrattivi per le aziende farmaceutiche nel corso dell’ultimo trentennio. In questo contesto, un posto di tutto rilievo è quello dei farmaci destinati al trattamento delle cosiddette “malattie rare”, ovvero quelle malattie che colpiscono – secondo la definizione che ne dà l’Unione Europea –meno di cinque persone ogni 10 mila. L’esiguità delle popolazioni di pazienti ha storicamente reso poco interessante sul piano economico lo sviluppo di medicinali dedicati alle malattie rare, una vasta famiglia di prodot-
ti che viene nel suo complesso indicata col termine “farmaci orfani”. Ma è proprio così?
Se è vero che a ogni malattia rara corrisponde una assai piccola popolazione di pazienti, lo scenario potrebbe cambiare se si va a osservare il quadro complessivo: secondo i dati dell’Agenzia europea dei medicinali (EMA), infatti, alle oltre 6 mila malattie rare conosciute corrisponderebbe nell’Unione Europea un volume complessivo di potenziali pazienti pari a circa 26 milioni di persone (un paziente ogni 17 abitanti). Un dato che deve venire considerato anche alla luce del fatto che questo tipo di prodotti riesce spesso a spuntare prezzi molto
In questo articolo approfondiamo i criteri di designazione a farmaco orfano, i percorsi dedicati di sviluppo e approvazione regolatoria e gli incentivi di cui possono usufruire le aziende farmaceutiche che s’impegnano in questo tipo di attività.
Designazione è diverso da autorizzazione
Secondo gli ultimi dati EMA, il numero di medicinali che hanno ricevuto la designazione a farmaco orfano nel periodo 2000-2022 è di oltre 2.730 prodotti. Sono però solo poco più di 230 i medicinali orfani autorizzati per l’immissione in commercio sul mercato dell’Unione europea nello stesso periodo.
Non è detto, quindi, che un medicinale che sia stato designato come farmaco orfano da parte del Committee for Orphan Medicinal Products (COMP) di
74 icf RIVISTA DELL’INDUSTRIA CHIMICA E FARMACEUTICA Approfondimenti

Tabella 1: Politica EMA di riduzione delle tariffe per farmaci orfani, 2022 (fonte: EMA, “Annual report on the use of the special contribution for orphan medicinal products. Year 2022”)
% di riduzione sulla tariffa Tipo di domanda totale applicabile Richiedente Richiedente non PMI PMI
Assistenza per protocollo (non pediatrico), diversi dall’università
Assistenza per protocollo, università
Assistenza per protocollo (pediatrico)
Servizi scientifici
Ispezioni (pre-autorizzazione)
Domanda autorizzazione immissione in commercio
Attività post-autorizzazione, incluse le tariffe annuali, nel primo anno dopo l’autorizzazione - 100%
Ispezioni (post-autorizzazione)
EMA raggiunga anche lo stadio di deposito della domanda di autorizzazione AIC e passi la conseguente valutazione da parte del Comitato EMA per i medicinali a uso umano (CHMP). A fronte dei 182 prodotti che hanno ricevuto la designazione a farmaco orfano nel corso del 2022, ad esempio, solo 24 medicinali sono stati raccomandati dal CHMP per l’autorizzazione
90%
all’immissione in commercio da parte della Commissione europea (figure 1 e 2).
Tutti i medicinali che hanno ricevuto una designazione a farmaco orfano sono elencati, inclusa l’indicazione, nell’apposita sezione del Registro dell’Unione dei prodotti medicinali (Community Register of orphan medicinal products, accessibile online al
link https://ec.europa.eu/health/documents/community-register/html/ reg_od_act.htm?sort=n).
Oltre che il criterio numerico sulla popolazione di pazienti sopra menzionato, la designazione a farmaco orfano da parte del comitato COMP prende anche in considerazione la gravità della malattia, la mancanza di ritorni economici per le aziende sviluppatrici e l’assenza di metodi soddisfacenti per la diagnosi, prevenzione o trattamento della patologia (o, ove esistenti, l’apporto di un beneficio addizionale significativo, vedi box a pag. 78). Non rientrano, invece, nella definizione di farmaci orfani i prodotti di medicina personalizzata basati sull’utilizzo di biomarcatori per l’identificazione delle sottopopolazioni di pazienti su cui un certo medicinale è atteso essere efficace. La presentazione delle domande di designazione a farmaco orfano rimane un processo tipico delle grandi aziende farmaceutiche: i dati EMA (“Orphan Medicinal Product Designation. Overview 2000-2022”) indicano per il 2022 un contributo al fenomeno da parte delle piccole e medie aziende pari al 26% del totale. La grande maggioranza dei prodotti in sviluppo designati come farmaci orfani, inoltre, sono prodotti di stampo più tradizionale (88%). Solo una piccola quota (12%) appartiene alla categoria delle terapie avanzate. I due terzi circa dei prodotti, infine, negli ultimi anni hanno basato la designazione a farmaco orfano sul criterio del beneficio significativo (66% nel 2022). Nello stesso anno, le nuove condizioni hanno rappresentato il 16% del totale delle designazioni. Sempre con riferimento al 2022, le categorie terapeutiche più rappresentate sono state riferite ai prodotti per il trattamento di malattie congenite, familiari o genetiche (62), malattie del sistema nervoso (29) e malattie del sangue e del sistema linfa-
RIVISTA DELL’INDUSTRIA CHIMICA E FARMACEUTICA icf 75 Febbraio/Marzo 2024 Approfondimenti
75% 100%
100% 100%
100% 100%
- 100%
100% 100%
10% 100%
-
Tabella 2: Tipologie di riduzioni tariffarie processate da EMA nel 2022 (fonte: EMA, “Annual report on the use of the special contribution for orphan medicinal products. Year 2022”)
Procedura/Tipo di domanda Numero di
tariffe 2022
tico (22). Le domande di autorizzazione attive riferite a medicinali orfani seguono un andamento simile per le prime due posizioni (47 per malattie congenite e familiari, 23 per malattie del sangue e linfatiche), mentre al terzo posto si collocano i medicinali contro neoplasie benigne e maligne (22), seguiti da quelli per le infezioni (11).
La maggior parte dei prodotti designati come orfani sono destinati a malattie che colpiscono sia gli adulti che le popolazioni pediatriche; solo il 4% dei prodotti sono destinati in modo mirato unicamente a queste ultime.
Il processo di sviluppo
La designazione a farmaco orfano è un evento che si colloca all’inizio del percorso di sviluppo di un nuovo medicinale. Ciò implica che questi prodotti non possono normalmente essere impiegati sui pazienti (serve l’autorizzazione AIC), in quanto seppur promettenti potrebbero ancora mancare di sufficienti evidenze di efficacia. Le Question and Answers pubblicate da EMA nel 2018 (EMA/551338/2017) specificano che è possibile in casi eccezionali un utilizzo dei farmaci designati orfani in base a programmi per uso compassionevole, ove non esistano altre possibilità per il paziente, ov-
vero potrebbero venire avviate sperimentazioni cliniche a cui potrebbe essere possibile partecipare.
La designazione a farmaco orfano, inoltre, non ha effetti sul tempo necessario a completare lo sviluppo. Una volta ricevuta l’autorizzazione all’immissione in commercio, inoltre, il comitato COMP di EMA è chiamato a confermare o annullare la designazione a farmaco orfano sulla base delle nuove evidenze emerse nel corso dello sviluppo stesso.
Le designazioni ad opera di autorità regolatorie di altre aree geografiche, come l’americana FDA, non sono valide nell’Unione europea, in quanto basate su criteri di valutazione (tra cui la soglia di prevalenza della malattia) diversi da quelli adottati in Europa. Gli accordi di confidenzialità in essere tra EMA e FDA permettono, invece, di condividere informazioni sui medicinali orfani. Le autorità regolatorie sulle due sponde dell’Atlantico, inoltre, hanno sviluppato procedure comuni per presentare le domande di designazione e i report annuali sullo stato dello sviluppo dei farmaci designati orfani.
Un elemento significativo dello sviluppo di un farmaco orfano è rappresentato dalla dimostrazione del “beneficio significativo”, che si differenzia dalla dimostrazione del rapporto
beneficio-rischio richiesta in generale per tutti i medicinali. I farmaci orfani devono apportare benefici aggiuntivi rispetto ai trattamenti già disponibili, ad esempio portare a esiti migliori o consentire modalità di somministrazione più facili o agevoli. Il rapporto beneficio-rischio, invece, si basa sulla dimostrazione che gli esiti di salute ottenibili con la somministrazione del medicinale superano gli effetti avversi ad esso correlati. Una volta ottenuta l’autorizzazione all’immissione in commercio con procedura centralizzata gestita da EMA, l’effettiva disponibilità del medicinale orfano nei diversi paesi membri dell’UE dipende dai passaggi di negoziazione di prezzo e rimborso che sono in carico alle singole autorità competenti a livello nazionale. Le differenze dei criteri di health technology assessment, utilizzati nei diversi paesi per definire i requisiti e le priorità dei rispettivi sistemi sanitari, sottolineano le Q&A di EMA, spiegano il fatto che a volte un certo farmaco orfano sia disponibile solo in alcuni paesi e non in altri. A questo livello, possono entrare in gioco anche comparazioni con altre tecnologie sanitarie o valutazioni value-for-money rispetto all’impatto atteso per il sistema sanitario del paese.
Gli attuali incentivi
Secondo la legislazione europea sui farmaci orfani attualmente in vigore (Regolamento europeo (EC) 141/2000), una volta ottenuta l’autorizzazione all’immissione in commercio e confermata la designazione, questi prodotti possono godere di un periodo di esclusività di mercato pari a dieci anni, al fine di favorire i ritorni sugli investimenti delle aziende che hanno affrontato lo sviluppo. Altri due anni di estensione dell’esclusività di mercato conferita dai certificati di protezione complementare (SPC) sono concessi ai medicinali pediatrici
76 icf RIVISTA DELL’INDUSTRIA CHIMICA E FARMACEUTICA Approfondimenti
Riduzioni
transazioni 2022 Euro % del totale Domanda completa 40 -2.592.140 € 19,95% Ispezioni pre-autorizzazione 38 -842.300 € 6,53% Assistenza protocollo follow up 45 -1.328.950 € 10,31% Assistenza protocollo follow up 96 -6.541.150 € 50,73% Trasferimento 1 -7.800 € 6,00% Variazioni tipo I 18 -101.400 € 79,00% Variazioni tipo II 12 -846.000 € 6,56% Tariffa annuale 6 -655.500 € 5,08% TOTALE 256 12.895.240 € 100,00%
Figura 1: Numero di medicinali che hanno ricevuto una designazione a orfani, 2001-2022
(fonte: EMA, Factsheet “Orphan medicines in the EU”)
Figura 2: Numero di medicinali orfani raccomandati da EMA per l’autorizzazione AIC, 2001-2022
(fonte: EMA, Factsheet “Orphan medicines in the EU”)
autorizzati sulla base degli studi definiti all’interno di un Piano di indagine pediatrica (PIP).
Questo è solo l’ultimo di una serie di incentivi pensati per sostenere le aziende lungo l’intero percorso di svi-
luppo. La designazione a farmaco orfano è un passaggio essenziale che permette di accedere, tra gli altri, ad attività di scientific advice e assistenza alla messa a punto dei protocolli sperimentali da parte di EMA pensa-
te in modo mirato per questa tipologia di prodotti, oltre che a facilitazioni sulle tariffe regolatorie (in particolare per le micro, piccole e medie imprese e per gli sponsor universitari). Più in particolare, ogni anno l’Unione europea destina un certo budget (il “contributo speciale”) a favore di EMA per coprire le riduzioni delle tariffe per i medicinali orfani (tabella 1). Gli ultimi dati relativi al 2022 indicano uno stanziamento totale di poco meno di 12,9 milioni di euro; il 61% delle tariffe hanno coperto attività di supporto allo sviluppo da parte dell’Agenzia, il 26% attività finalizzate all’approvazione regolatoria, incluse le ispezioni pre-autorizzazione (dati EMA, tabella 2).
Il percorso di sviluppo di ogni farmaco che ha ricevuto la designazione a orfano, infine, è monitorato dal comitato COMP di EMA per mezzo di un rapporto annuale che gli sponsor devono presentare all’Agenzia.
Gli incentivi previsti dalla revisione della legislazione farmaceutica La proposta di regolamento pubblicata dalla Commissione il 26 aprile 2023 (COM(2023) 193 final), che è parte della più ampia manovra di revisione della legislazione farmaceutica europea, ridefinisce ad ampio raggio lo schema per la concessione degli incentivi per lo sviluppo di nuovi medicinali, compresi quelli destinati a malattie rare e farmaci orfani. In seguito alla conclusione del processo legislativo in corso, l’entrata in vigore del nuovo regolamento dovrebbe portare a una semplificazione normativa, con abrogazione dell’attuale regolamento sui farmaci orfani e di quello generale sui medicinali a uso umano ((EC) 726/2004), oltre che all’incorporazione di parti significative del regolamento sui farmaci pediatrici ((EC) No 1901/2006).
La bozza di regolamento si focalizza,
RIVISTA DELL’INDUSTRIA CHIMICA E FARMACEUTICA icf 77 Febbraio/Marzo 2024 Approfondimenti
64 49 55 73 88 80 98 73 106 128 107 148 136 187 190 209 147 169 112 149 170 182 0 55 110 165 220 2001 2003 2005 2007 2009 2011 2013 2015 2017 2019 2021 29 35 19 28 20 42 45 60 108 47 82 47 74 67 79 67 78 62 61 76 75 65 3 4 5 6 4 9 13 6 9 4 5 10 7 15 14 14 14 22 5 21 17 24 0 30 60 90 120 150 2001 2003 2005 2007 2009 2011 2013 2015 2017 2019 2021 Altri medicinali Medicinali orfani
in modo particolare sulle aree di cosiddetto “elevato bisogno medico insoddisfatto” (HUMN), caratterizzate da rischi e incertezze maggiori a livello delle attività di R&D. I criteri proposti per l’identificazione dei prodotti mirati a esercitare i loro effetti terapeutici all’interno di tali aree prevedono l’assenza di medicinali già autorizzati per una certa patologia o l’apporto di eccezionali progressi terapeutici. Il nuovo farmaco dovrebbe, inoltre, apportare una significativa riduzione della morbilità o mortalità associate alla malattia.
Per quanto riguarda i farmaci orfani, i nuovi criteri di modulazione degli incentivi prevedono che essi possano godere di un periodo di esclusività di dieci anni nel caso si rivolgano a “elevati bisogni medici insoddisfatti”. Tale periodo si riduce a cinque anni nel caso di medicinali orfani di uso già ben consolidato, ed è in generale di nove anni per tutti gli altri farmaci orfani.
A ciò si potrebbe aggiungere un ulteriore anno di esclusiva qualora il medicinale venga commercializzato in tutti i paesi UE. Anche le prime due nuove indicazioni di medicinali orfani già autorizzati dovrebbero poter godere di un ulteriore anno di esclusività (che si estenderebbe all’intero prodotto, purché l’approvazione sia concessa almeno due anni prima dalla scadenza del periodo di esclusiva). In totale, quindi, i farmaci orfani dovrebbero poter godere, alla luce della nuova normativa, di un massimo di dodici anni di protezione del mercato.
Significativa, da questo punto di vista, risulterebbe anche l’introduzione di un approccio complessivo alle autorizzazioni AIC per una stessa sostanza attiva: qualora, infatti, il titolare AIC possieda più di una autorizzazione per la stessa sostanza, la bozza di regolamento prevede che venga conteggiato un unico periodo di esclusi-
I criteri per la designazione a farmaco orfano
• Il medicinale deve trattare, prevenire o diagnosticare una malattia che metta il paziente a pericolo di vita o sia cronicamente debilitante, ovvero sia improbabile che il medicinale generi ritorni sufficienti a giustificare l’investimento necessario per il suo sviluppo;
• la malattia non deve affliggere più di 5 persone ogni 10 mila nell’Unione europea;
• non esistono metodi soddisfacenti di diagnosi, prevenzione o trattamento, ovvero dove tali metodi esistano, il medicinale deve apportare un beneficio addizionale significativo alle persone affette dalla patologia.
(fonte: EMA, Factsheet “Orphan medicines in the EU”)
vità a partire dalla data di concessione della prima autorizzazione all’immissione in commercio come farmaco orfano. È anche prevista la possibilità per i generici e biosimilari di ottenere un’autorizzazione AIC a partire da due anni di esclusività residua, così da favorire il tempestivo accesso al mercato al momento della scadenza finale. Altre misure allo studio per i farmaci orfani, in particolare quelli per il trattamento di bisogni HUMN, prevedono l’ulteriore rafforzamento del supporto regolatorio e scientifico da parte di EMA e procedure di valutazione accelerata sul modello di quanto avvenuto con lo schema Prime e nel periodo Covid.
La prevista riorganizzazione dei comitati di EMA dovrebbe portare con sé anche il passaggio dalla Commissione europea alla stessa Agenzia europea dei medicinali per quanto riguarda la decisione finale circa la designazione a farmaco orfano. I medicinali orfani per la diagnosi, prevenzione o trattamento di malattie gravemente debilitanti o a pericolo di vita o da utilizzarsi in caso di situazioni di emergenza sanitaria dovrebbero rientrare tra le categorie per le quali sarà possibile concedere autorizzazioni AIC condizionate sulla base di dati ancora incompleti. EMA potrà anche raccomandare alla Commissione l’adozione di criteri di designazione a farmaco orfano particolari per specifiche malattie, qualora quelli generali non risultino per esse appropriati. Anche la definizione di beneficio significativo dovrebbe diventare più stringente. Dovrebbe venire invece, abolito il criterio basato sui ritorni sugli investimenti, scarsamente utilizzato. La designazione a farmaco orfano dovrebbe avere una durata di sette anni, con la possibilità di estensione a specifiche condizioni in base a richieste giustificate, e potrà essere ritirata su richiesta dello sponsor.
78 icf RIVISTA DELL’INDUSTRIA CHIMICA E FARMACEUTICA Approfondimenti

DIRETTORE RESPONSABILE: Simone Ghioldi
REDAZIONE: Alessandro Bignami (a.bignami@interprogettied.com), Eva De Vecchis (e.devecchis@interprogettied.com)
GRAFICA: Studio Grafico Page Vincenzo De Rosa, Rossella Rossi - www.studiograficopage.it
HANNO COLLABORATO A QUESTO NUMERO: Jan Clement, Filippo Neri, Marzia Savino
INTERPROGETTI EDITORI S.R.L.
via Roggia Borromea, 16 - 22060 Carugo (CO)
Redazione, vendite e abbonamenti
Tel./fax +39 031 3665163
www.interprogettied.com
DIRETTORE COMMERCIALE: Marika Poltresi
VENDITE: Simone Ghioldi (vendite@interprogettied.com) Michela Ghioldi (estero, michela@interprogettied.com)
AMMINISTRAZIONE: amministrazione@interprogettied.com
SEGRETERIA COMMERCIALE: Raffaella Sepe (raffaella@interprogettied.com)
©Copyright Interprogetti Editori Srl
Le rubriche e le notizie sono a cura della redazione. È vietata la riproduzione, anche parziale, di testi, fotografie e disegni senza autorizzazione scritta.
TARIFFE ABBONAMENTI:
Italia: spedizione ordinaria € 45,00, contrassegno € 48,00
Estero: spedizione ordinaria € 60,00, spedizione prioritaria Europa € 70,00
Spedizione prioritaria Africa, America, Asia € 85,00
Spedizione prioritaria Oceania € 100,00
Una copia: € 10,00
L’Iva sugli abbonamenti nonché sulla vendita dei fascicoli separati è assolta dall’editore ai sensi dell’art. 74 primo comma lettera C del 26/10/72 n. 633 e successive modificazioni e integrazioni. Pertanto non può essere rilasciata fattura.
Registrazione Tribunale di Milano n. 259 in data 07/05/2010 - Iscrizione al ROC nr. 19882
Direttore Responsabile: Simone Ghioldi Finito di stampare il 18/3/2024 presso Aziende Grafiche Printing S.r.l.
Via Milano, 5 - 20068 Peschiera Borromeo (MI)
Informativa ai sensi dell’art. 13 d. leg. 196/2003. I dati sono trattati, con modalità anche informatiche, per l’invio della rivista e per svolgere le attività a ciò connesse. Titolare del trattamento è Interprogetti Editori S.r.l. - via Maggiolino 34F - 23849 Rogeno (LC). Le categorie di soggetti incaricati al trattamento dei dati per le finalità suddette sono gli addetti alla registrazione, modifica, elaborazione dati e loro stampa, al confezionamento e spedizione delle riviste, al call center, alla gestione amministrativa e contabile. Ai sensi dell’art. 7 d. leg. 196/2003 è possibile esercitare i relativi diritti tra cui consultare, modificare, aggiornare e controllare i dati, nonché richiedere elenco completo ed aggiornato, rivolgendosi al titolare al suddetto indirizzo.
Informativa dell’editore al pubblico ai sensi del decreto legislativo 30 giugno 2003, n° 196 e dell’art. 2 comma 2 del Codice deontologico relativo al trattamento dei dati personali nell’esercizio dell’attività giornalistica. Interprogetti Editori - titolare del trattamento - rende noto che presso i propri locali siti in Rogeno (LC) vengono conservati gli archivi personali e di immagini fotografiche cui i giornalisti, praticanti e pubblicisti e altri soggetti (che occasionalmente redigono articoli o saggi) che collaborano con il predetto titolare attingono nello svolgimento della propria attività giornalistica per le finalità di informazione connesse allo svolgimento della stessa.
I soggetti che possono conoscere i predetti dati sono esclusivamente i predetti professionisti, nonché gli addetti preposti alla stampa ed alla realizzazione editoriale della testata. Ai sensi dell’art. 7 d. lgs. 196/2003 si possono esercitare i relativi diritti, tra cui consultare, modificare, cancellare i dati od opporsi al loro utilizzo, rivolgendosi al predetto titolare. Si ricorda che, ai sensi dell’art. 138 d. lgs. 196/2003, non è esercitabile il diritto di conoscere l’origine dei dati personali ai sensi dell’art. 7, comma 2, lettera a), d. lgs. 196/2003, in virtù delle norme sul segreto professionale, limitatamente alla fonte della notizia.
80 icf RIVISTA DELL’INDUSTRIA CHIMICA E FARMACEUTICA INDUSTRIA CHIMICA E FARMACEUTICA RIVISTA DELL’ icfANNOXV NUMERO1 FEB/MAR2024
questo numero abbiamo
In nero sono indicate le inserzioni pubblicitarie: ACHEMA 26, 69 ADL FARMACEUTICI 16 ADL UNILAB .......................................................................... 16 AMC...................................................................................... 15 AMGEN ITALIA ....................................................................... 19 ANALISYS 54 ANIE AUTOMAZIONE 20 ASEPTCONN 1, 46 BEA TECHNOLOGIES 9 BORMIOLI PHARMA ................................................................ 52 BRUNO WOLHFARTH.............................................................. 25 BURSTER ITALIA 49 CEFIC 10 CHIESI 28 CMG 42 COESIA ................................................................................. 15 COPERION............................................................................. 43 CORETEC................................................................................ 49 COVESTRO 33 CSV LIFE SCIENCE BATTENTE 1A COP. DRÄGER 43 EFFEBI 5 EGUALIA ............................................................................... 18 EIOM FIERE ........................................................................... 24 ELLAB 2A COP. EMA 74 EMERSON 70 ENDRESS+HAUSER 14, 66 ENEA .................................................................................... 32 FARAVELLI............................................................................ 23 FIDIA FARMACEUTICI 8 GE HEALTHCARE 28 HEMOFARM 38 ICOTEK 33, 49 IVS - INDUSTRIAL VALVE SUMMIT .....................................72-73 LOOP INDUSTRIES .................................................................. 52 MERCURI ANGELO FRINDES ................................................... 51 MONTENEGRO 43 NOVO NORDISK 14 NUOVA GUSEO 15 PEPPERL+FUCHS 44 PHOENIX CONTACT .................................................................. 50 PQE GROUP.............................................................................. 8 PRECISION FLUID CONTROLS 29, 61 PROCESS SERVICE 27 PVS 4A COP. QUALIWARE 54 RADICIGROUP ........................................................................ 32 RITTAL .................................................................................. 44 ROMACO ................................................................................ 38 S4S 13 SCHUBERT & SALZER CONTROL VALVES 61 SICK 62 SIMPOSIO AFI 24 SMC ...................................................................................... 49 SOLIDS ................................................................................. 45 SOLTECH 3A COP. SPS ITALIA 20, 53 STÄUBLI 41 STERILINE 42 STEVANATO GROUP.................................................................. 52 STUVEX ................................................................................ 31 SWAN ANALITICA 19, 58 TEXPACK 17 UNIVERSITÀ DI PISA 30 UNIVERSITÀ DI TORINO 30 USP GROUP ........................................................................... 16 VEGA .........................................................................1A COP., 6 WATSON-MARLOW FLUID TECHNOLOGY SOLUTIONS...................... 50 WENGLOR SENSORIC GROUP 16
In
parlato di…













































































































































































































































