4 minute read
Rhéomètre de couple mélangeur comme outil d'application de la qualité par conception QbD) dans le développement de granulés pharmaceutiques
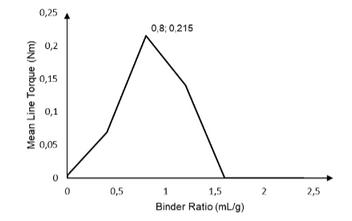
Cet équipement fonctionne avec de petites quantités de matière première (15 à 20 grammes), qui sont réparties dans un compartiment de mélange. Deux lames rotatives, couplées à un transducteur de signal, homogénéiseront l'échantillon. Pour qu 'il soit possible d' obtenir une valeur de couple, mesurée et calculée par le logiciel CalevaMTR®, à travers l' une des trois méthodes analytiques différentes: Cohérence (utilisée pour vérifier les propriétés des poudres produites dans les systèmes de granulation à grande échelle et peut être utilisée comme outil de contrôle qualité), Variable Mixed Time (fournit une indication de la réponse du couple par rapport au rapport de liant et au temps de mélange) et Multiple Addition (utilisé pour étudier la meilleure condition de granulation et déterminer son point final). F e b . d e 2De plus, la 0 2 0 | V ométhode l . 8d' addition multiple, associée à la planification statistique de la formulation des granulés pharmaceutiques, permet l' optimisation du développement des formulations multiparticulaires, permettant de choisir les meilleures proportions de principe actif pharmaceutique (API) et d' excipients pour la composition de la formulation. Ainsi, le formulateur acquiert une parfaite connaissance de la formulation et de ses paramètres de traitement, garantissant la qualité du produit dès les premières étapes de développement, comme le prévoit Quality by Design (QbD) (MISHRA; ROHERA, 2016). A titre d' exemple pratique, il y a la caféine, un API qui a un faible débit, un faible indice de compressibilité et peut être utilisé à fortes doses comme complément énergétique. Dans ce contexte, la production de comprimés contenant de la caféine est conditionnée à sa granulation. Afin de choisir la meilleure formulation contenant de la caféine et de déterminer son point final, un plan factoriel fractionnaire 33-1, aboutissant à 9 formulations, a été planifié et évalué sur le MTR dans les conditions suivantes: temps de mélange de 60 secondes, rotation de la lame à 50 tr / min et une durée d' enregistrement de 20 secondes. Après avoir évalué les résultats des 9 formulations, celle avec la valeur de couple maximum la plus élevée a été choisie, constituée de 30% de caféine, 1% de carraghénane et d'Avicel® 101 en quantité suffisante pour compléter 15 grammes d'échantillon. Ensuite, grâce au profil rhéologique de cette formulation (figure 3), il a été possible de déterminer le point final de granulation de. Il est important de souligner que, comme présenté par Belem et Ferraz (2020), l'étape finale idéale reste un sujet contradictoire entre plusieurs auteurs. Certains défendent le choix d' un point entre les étages pendulaire et funiculaire, d' autres défendent un point entre le funiculaire et le capillaire et, enfin, il y a ceux qui suivent la ligne que l'étage capillaire peut être considéré comme une bonne approximation du point final de granulation. Dans la présente étude, nous avons choisi de suivre cette dernière ligne de recherche, de sorte que l'étage capillaire (couple maximal) a été adopté comme point final de granulation. Selon la figure 3, le rapport liquide / solide requis pour atteindre la valeur de couple la plus élevée est de 0,8 ml / g. Ainsi, pour produire 200 grammes de ce granulé, il est nécessaire d' ajouter 160 mL du liant liquide au mélange solide, définissant ainsi le point final de granulation.
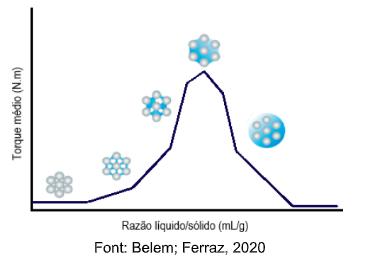
Figure 2. Courbe d'intensité du couple moyen en fonction du rapport liquide / solide.
Advertisement
Figure 3. Courbe d'intensité du couple moyen en fonction de la quantité de liant ajoutée à un mélange de 15 grammes contenant de la caféine (30%), du carraghénane (1%) et de l'Avicel® 101 (q.s.p)
F e b . d e 2 0 2 0 | V o l . 8
Le travail en question a été réalisé au Laboratoire de développement et d'innovation pharmaceutique de la Faculté des sciences pharmaceutiques de l'Université de São Paulo (Deinfar FCF / USP), sous la coordination du Prof. Dr. Humberto Gomes Ferraz. Deinfar a été le premier laboratoire au Brésil à investir dans un rhéomètre à poudre humide et, depuis son acquisition, plusieurs projets de développement de formulations de dosage pharmaceutique solide ont été menés en utilisant plusieurs principes actifs. En outre, le laboratoire a présenté la technique et ses avantages dans différents cours et travaux académiques, remplissant son rôle dans la diffusion des connaissances et de l'innovation dans l'industrie pharmaceutique brésilienne.
Références
BELEM, B. R.; FERRAZ, H. G.. Rheological profile in mixer torque rheometer of samples containing furazolidone and different binders. Chemical Engineering Research And Design, [S.L.], v. 160, p. 533539, ago. 2020. Elsevier BV. http://dx.doi.org/10.1016/j.cherd.2020.06.022. ENNIS, B. . Theory of granulation: a engineering perspective. In: PARIKH, D. M. (Ed.). Handbook of pharmaceutical granulation technology. 3. ed. CRC Press, 2016. p.676. HANCOCK, B. C.; YORK, P.; ROWE, R. C. An assessment of substrate-binder interactions in model wet masses. 1: Mixer torque rheometry. International Journal of Pharmaceutics, v. 102, n. 1–3, p. 167–176, 1994. MISHRA, Saurabh M.; ROHERA, Bhagwan D.. An integrated, quality by design (QbD) approach for design, development and optimization of orally disintegrating tablet formulation of carbamazepine. Pharmaceutical Development And Technology, [S.L.], v. 22, n. 7, p. 889-903, 27 jun. 2016. Informa UK Limited. http://dx.doi.org/10.1080/10837450.2016.1199566. SAKR, W. F.; IBRAHIM, M. A.; ALANAZI, F. K.; SAKR, A. A. Upgrading wet granulation monitoring from hand squeeze test to mixing torque rheometry. Saudi Pharmaceutical Journal, v. 20, n. 1, p. 9–19, 2012. SURESH, P.; SREEDHAR, I.; VAIDHISWARAN, R.; VENUGOPAL, A. A comprehensive review on process and engineering aspects of pharmaceutical wet granulation. Chemical Engineering Journal, v. 328, p. 785–815, 2017. ZHANG, S.; LAMBERTO, D. J. Development of new laboratory tools for assessment of granulation behavior during bulk active pharmaceutical ingredient drying. Journal of Pharmaceutical Sciences, v. 103, n. 1, p. 152–160, 2014.










