THIẾT KẾ VÀ XÂY DỰNG BÀI TẬP HÓA HỮU
CƠ PHẦN “HYDROCARBON” THEO YÊU CẦU
CỦA CHƯƠNG TRÌNH GDPT NĂM 2018

HYDROCARBON NO –
KHÔNG NO –
HYDROCARBON
HYDROCARBON THƠM
PDF VERSION | 2023 EDITION
ORDER NOW / CHUYỂN GIAO QUA EMAIL
TAILIEUCHUANTHAMKHAO@GMAIL COM
Hỗ trợ trực tuyến Fb www.facebook.com/DayKemQuyNhon
0905779594
liệu chuẩn
ảo Phát triển kênh bởi Ths Nguyễn Thanh Tú Đơn vị tài trợ / phát hành / chia sẻ học thuật : Nguyen Thanh Tu Group BÀI TẬP HÓA HỮU CƠ HYDROCARBON
Mobi/Zalo
Tài
tham kh
Ths Nguyễn Thanh Tú
eBook Collection
com/28062440
vectorstock
DẠYKÈMQUYNHƠNOFFICIAL


1 TRƯỜNG ĐẠI HỌC SƯ PHẠM – ĐẠI HỌC ĐÀ NẴNG KHOA HÓA HỌC PHỤ LỤC KHÓA LUẬN TỐT NGHIỆP Đề tài: Thiết kế và xây dựng bài tập Hóa hữu cơ phần “Hydrocarbon” theo yêu cầu của Chương trình GDPT năm 2018. Giảng viên hướng dẫn: TS. Trần Đức Mạnh Sinh viên thực hiện: Nguyễn Thị Mỹ Thuận _ Lớp 18SHH Đà Nẵng, ngày 19 tháng 05 năm 2022
Hệ thống bài tập: Gồm 4 dạng cơ bản Dạng 1: Bài tập về đồng phân và danh pháp
Dạng 2: Bài tập về tính chất hóa học

Dạng 3: Bài tập tính toán
Dạng 4: Bài tập giải thích vấn đề

DẠYKÈMQUYNHƠNOFFICIAL








2
HYDROCARBON NO – ALKANE
Dạng 1.1: Đồng phân
Ví dụ: Hãy viết đồng phân cấu tạo
của C5H12
Bước 1: Số carbon cần viết: 5 nguyên tử C.

Bước2: Viết mạch C dưới dạngthẳng nnguyêntửC.Đượcđồngphânthứnhất
Bước 3: Vì đây là C5 > C4 nên ta tiến hành bẻ nhánh cắt 1 C đi dạng (4+1)

(còn 1 nguyên tử C nên đặt nó ở các vị trí tránh ở đầu mạch và xét ở vị trí đối xứng như trên)
Phương pháp giải
Cách viết đồng phân:
Bước 1: Xác định số carbon cần vi
Bước 2: Ưu tiên viết mạch carbon theo mạch thẳng
Bước 3: Từ C4 trở đi bắt đầu bẻ nhánh (chú ý đặt nhánh không gắn ở đầu mạch và để ý tính đối xứng của ch tránh trùng lặp). a các
Sau đó ta tiến hành bẻ nhánh cắt 2 C dạng (3+1+1) như sau:
CTTQ của Alkane: CnH2n+2 (n ≥ 1).
Alkane chỉ có đồng phân mạch carbon và từ C4 trở đi mới xuất hiện đồng phân: 3<n<7
Công thức tính nhanh: 2n-4 +1
Bước 4: Điền H để đảm bảo hóa trị các nguyên tố.
Vậy C5H12 có 3 đồng phân cấu tạo.
Bài tập vận dụng
Bài tập tự luận:
Câu 1: Hãy viết các đồng phân cấu tạo mạch hở của các hydrocarbon no có công thức phân tử sau:
a. C4H10
b. C6H14
c. C8H18
Câu 2: Hãy viết công thức phân tử của các alkane dưới đâyvà cho biết số đồng phân cấu tạo.
a. Alkane E có chứa 4 nguyên tử C.
b. Alkane F có chứa 12 nguyên tử H.
c. Alkane G có tổng số nguyên C và H là
20.
DẠYKÈMQUYNHƠNOFFICIAL
Câu 3: Hãy cho biết trong bốn công thức cấu tạo, công thức nào là đồng phân của chất (A), công thức nào là chính chất (A).
3
nguyên
CHƯƠNG 2 DẠNG 1: BÀI TẬP VỀ ĐỒNG PHÂN VÀ DANH PHÁP 1
1.1
1.2 1.2.1
Bài tập trắc nghiệm
Câu 1: Alkane A có công thức đơn giản nhất là C4H10. Số đồng phân cấu tạo của A là
A. 1. C. 2.
B. 3 D. 4
Câu 2: Trong các công thức cấu tạo sau, công thức nào là đồng phân cấu tạo của C4H10?
A. B.
C.
D.
Câu 4: Alkane B có công thức đơn giản nhất là C6H14. Số đồng phân cấu tạo của B là
A. 2. C.3.
B. 4. D.5.

Câu 5: Trong bốn công thức cấu tạo sau, hãy cho biết đâu là đồng phân cấu tạo của C5H12 ở dạng mạch có nhánh?
B.
DẠYKÈMQUYNHƠNOFFICIAL
4
A.
C.
CHƯƠNG 2 DẠNG 1: BÀI TẬP VỀ ĐỒNG PHÂN VÀ DANH PHÁP
D. (A) (B) (C) (D) 1.2.1
Câu 3: Công thức phân tử của alkane có
chứa 14 nguyên tử H là
A. C3H14. C. C4H14.
B. C5H14 D. C6H14
Câu 6: Cho các công thức phân tử
sau: C2H6; C3H8; C4H10; C5H12. Hãy cho
biết công thức phân tử nào có 3 đồng
phân cấu tạo?
A. C2H6 C. C4H10
B. C3H8 D. C5H12
Dạng 1.2: Danh pháp
Phương pháp giải Dạng 1.2.1: Tên thay thế
Theo IUPAC, tên của một số alkane và nhóm ankyl không phân nhánh được g

Cách gọi tên Alkane:
- Alkane không phân nhánh: Tên alkane = tên mạch chính + ane.
Lưu ý: + Cần nhớ tên mạch chính của 10 alkane + Tên gốc ankyl đổi đuôi an thanh đuôi yl.
- Alkane phân nhánh:
Bước 1: Chọn mạch C là mạch dài nhất làm mạch chính.
DẠYKÈMQUYNHƠNOFFICIAL
5
ả
nhánh và tên tốc alkyl tương ứng CTCT CTPT Tên Gốc alkyl Tên gốc CH4 CH4 Methane CH3 Methyl CH3CH3 C2H6 Ethane CH3 CH2 Ethyl CH3CH2CH3 C3H8 Propane CH3 CH2 CH2 Propyl CH3[CH2]2CH3 C4H10 Butane CH3 [CH2]2 CH2 Butyl CH3[CH2]3CH3 C5H12 Pentane CH3 [CH2]3 CH2 Pentyl CH3[CH2]4CH3 C6H14 Hexane CH3 [CH2]4 CH2 Hexyl CH3[CH2]5CH3 C7H16 Heptane CH3 [CH2]5 CH2 Heptyl CH3[CH2]6CH3 C8H18 Octane CH3 [CH2]6 CH2 Octyl CH3[CH2]7CH3 C9H20 Nonane CH3 [CH2]7 CH2 Nonyl CH3[CH2]8CH3 C10H22 Decane CH3 [CH2]8 CH2 Decyl
ọi theo b
ng sau: Bảng 1.1. Danh pháp của một số alkane không
2 2.1 CHƯƠNG 2 DẠNG 1: BÀI TẬP VỀ ĐỒNG PHÂN VÀ DANH PHÁP
Bước 2: Đánh số thứ tự C gần mạch nhánh nhất sao cho tổng vị trí nhánh là nhỏ nhất và số
nhánh là lớn nhất.
Bước 3: Tên alkane = số thứ tự của nhánh + tên nhánh + tên mạch chính.

Lưu ý: + Nếu có nhiều nhánh giống nhau thì gọi thêm số đếm: 2- di, 3- tri, 4- tetra,
+ Nếu có nhiều nhánh khác nhau thì gọi tên theo thứ tự chữ cái trong bảng chữ cái tiếng việt.
Dạng 1.2.2: Tên thông thường
- Trong trường hợp không có nhóm thế, IUPAC vẫn cho dùng các tên không hệ thống sau đây:
- Tên gọi của nhóm ankyl phân nhánh được quy định như sau:
+ Sec: gốc ở vị trí C bậc hai.
+ Ter: gốc ở vị trí C bậc ba.
+ Neo: 3 nhóm methyl ở đầu mạch
+ Iso: 2 nhóm methyl ở đầu mạch.
Tên
DẠYKÈMQUYNHƠNOFFICIAL
6
Sec-butyl Bậc của Alkane Bậc của một nguyên tử C ở phần tử alkane bằng số nguyên tử C liên kết trực tiếp với nó.
ỉ chứa C
ậc I và II là alkane
ử
ứ
C bậc III hoặc bậc IV là alkane phân nhánh.
p vậ
ng CHƯƠNG 2 DẠNG 1: BÀI TẬP VỀ ĐỒNG PHÂN VÀ DANH PHÁP 2.2
gọi của một số nhánh hay gặp Isopropyl Ter-butyl Ter-pentyl
Alkane ch
b
không phân nhánh (mạch thẳng), còn phân t
có ch
a
Bài tậ
n dụ
a. Methane, propane, hexane.
b. 2-methylbutane; 2,2-dimethylpropane.
c. 3-ethyl-2-methylheptane; 3,3-diethylpentane.
Câu 1: Tên gọi (theo danh pháp IUPAC)
của alkane sau là
A. 2,2-dimethylpentane.

B. 2,3-dimethylhexane
Câu 6: Tên gọi (theo danh pháp IUPAC)
của alkane sau:
A. 2-methyl-3-butylpentane
DẠYKÈMQUYNHƠNOFFICIAL
B. 3-ethyl-2-methylheptane.
7 Bài tập tự luận
Câu 1: Hãy gọi tên các công thức cấu tạo dưới đây theo tên IUPAC và chỉ rõ bậc của từng nguyên tử C. a. (1) (2) (3) b. (4) (5) c. (6) Câu 2: Viết các công thức cấu tạo của các dãy chất sau:
ập
ắc
ệ
Bài t
tr
nghi
m
2.2.1
CHƯƠNG 2 DẠNG 1: BÀI TẬP VỀ ĐỒNG PHÂN VÀ DANH PHÁP
2.2.2
C. 2,2-methylhexane.
D. 2,2-dimethylhexane
Câu 2: Một đồng phân của C6H14 có công
thức cấu tạo như sau: CH3
3
Bậc của nguyên tử carbon số 2 trong mạch
chính là
A. bậc I. C. bậc II.
B. bậc III. D. bậc IV.
Câu 3: Tên gọi của alkane sau:
C. 3-isopropylheptane.
D. 2-methyl-3-ethyl-heptane
Câu 7: Một đồng phân của C5H12 có công
thức cấu tạo như sau:
C H3 2 C 3 C H2 4 C H3
CH3
Nguyên tử carbon trong mạch chính có bậc cao nhất được đánh số thứ tự là
A. số 1. C. số 3.
B. số 2. D. số 4.
Câu 8: Tên gọi của alkane sau:
theo danh pháp IUPAC là
A. 2,2-dimethylpropane
B. 2-dimethylpropane.
C. 2,2-methylpropane.
D. 3-methylpropane
Câu 4: Cho dãy gồm các alkane: butane, isobutane, isopentane, neopentane Alkane
nào trong dãy có chứa C bậc IV?
A. Butane. C. Isobutane.
IUPAC là
A. pentane.
theo danh pháp
B. 2-dimethylbutane.
C. 3-methylbutane
D. 2-methylbutane.
Câu 9: Trong phân tử hydrocarbon X có
tỉ lệ khối lượng ����:���� = 5 : 1. Đồng phân
cấu tạo của X có mạch carbon không phân
nhánh có tên gọi là
DẠYKÈMQUYNHƠNOFFICIAL
A. butane
C. hexane
8
1 C H
2 C 3 C
2 4 C
3
H
H3 CH
1
B. Isopentane. D. Neopentane. B. pentane. D. heptane.
Câu 5: 2,2,3,3-tetramethylbutane có bao
nhiêu nguyên tử C và H trong phân tử?
A. 8C; 16H
C. 8C; 12H
B. 8C; 14H
D. 8C, 18H
Câu 10: Cho alkane có công thức cấu tạ
như sau: (CH3)2CHCH2C(CH3)3
Tên gọi của alkane là
A. 2,2,4-trimethylpentane.
B. 2,4-trimethylpethane

C. 2,4,4-trimethylpentane.
D. 2-dimethyl-4-methylpentane
DẠYKÈMQUYNHƠNOFFICIAL
9
o
CHƯƠNG 2 DẠNG 1: BÀI TẬP VỀ ĐỒNG PHÂN VÀ DANH PHÁP
Phương pháp giải
1.1
Sơ đồ tư tuy về tính chất hóa học của alkane
TÍNH CHẤT
HÓA HỌC
CỦA ANKAN
Tác nhân thế halogen: Cl2, Br2, ...
CnH2n+2+aX2 ���� →
CnH2n+2-aXa+ aHX
Nguyên tử H liên
kết với nguyên tử C
bậc cao dễ bị thế hơn
H liên kết với C bậc
thấp.
Cracking xúc tác: 450 -5500 , xt alumosilicat hoặc nhôm chlororua (cơ chế dị li).
CnH2n+2 ���� →
CxHx+2+ CyH2y
(n= x+y, x≥1, y≥2)

Cracking nhiệt: 550- 650OC (cơ chế gốc).
Phản ứng oxi hóa hoàn toàn:
CnH2n+2 + ����+�� �� O2 ���� → nCO2 + (n+1)
H2O
•Số mol H2O> Số mol CO2
•Số mol alkane = n H2O - n CO2
Phản ứng oxi hóa không hoàn toàn:
Cácankanbịoxi hóa không hoàn toàn
tạo ra những sản phẩm khác nhau (HCHO, C, ...).
Phản ứng này nhằm thay đổi cấu cấu trúc của hydrocarbon theo hướng đồng phân hóa (tăng chỉ số octan) mà không gây ra những đổi đáng kể về khối lượng phân tử
Điều kiện: p: 35-65 atm, to:450-500oC, xt Pd, Pt, nhôm oxit hoặc nhôm slicat.
Phản ứng này bắt đầu từ sự dehydro hóa ankan thành anken có thể tạo ra theo hai hướng đồng phân hóa tạo alkene mạch nhánh hoặc vòng hóa rồi thơm hóa.

DẠYKÈMQUYNHƠNOFFICIAL
10
CHƯƠNG 2 DẠNG 2: BÀI TẬP VỀ TÍNH CHẤT HÓA HỌC 1
PHẢN ỨNG THẾ PHẢN ỨNG CRACKING PHẢN ỨNG OXI HÓA PHẢN ỨNG REFORMING
Cách xác định xác định sản phẩm chính phụ ở phản ứng thế
Cách xác định sản phẩm chính và sản phẩm phụ
Nguyên tắc: Khi phản ứng xảy ra theo tỉ lệ 1:1 (a = 1) thì trong phân tử alkane có bao nhiêu vị trí carbon khác nhau còn hydro sẽ cho ta bấy nhiêu dẫn xuất monohalogen. Khi đó sản phẩm chính tạo ra ưu tiên thế vào nguyên tử C có bậc cao nhất, bởi vì gốc tự do có bậc càng cao càng
bền.
Nguyên tử hydro liên kết với nguyên tử carbon bậc cao sẽ là sản phẩm chính.
Nguyên tử hydro liên kết với nguyên tử carbon bậc thấp hơn sẽ là sản phẩm phụ.
Bài tập vận dụng
Bài tập tự luận
Câu 1: Viết phương trình hóa học của các phản ứng sau:

a. Propane tác dụng với chloro (theo tỉ lệ mol 1:1) khi chiếu sang.
b. Tách một phân tử hydro từ phân tử propane.
c. Đốt cháy hexane.
d. Oxi hóa không hoàn thoàn methane trong không khí có xúc.
Câu 2: Hoàn thành chuỗi phản ứng sau bằng phương trình hóa học:
DẠYKÈMQUYNHƠNOFFICIAL
11
1.2 1.3 1.3.1 CHƯƠNG 2 DẠNG 2: BÀI TẬP VỀ TÍNH CHẤT HÓA HỌC
Câu 3: Alkane X không có nhánh có công thức đơn giản nhất là C4H10
a. Tìm CTPT. Viết CTCT và gọi tên.
b. Viết phương trình phản ứng X Cl2 có ánh sáng. Xác định sản phẩm chính.
1.3.2
Bài tập trắc nghiệm
Câu 1: Hợp chất Z sau đâycó thể tạo được
bao nhiêu dẫn xuất monohalogen?
CH3 - CH - CH2 - CH3
CH3
Câu 2: Sản phẩm của phản ứng thế Chloro
(1:1, ánh sáng) vào 2,2-dimethyl propane là
(1) CH3C(CH3)2CH2Cl
(2) CH3C(CH2Cl)2CH3
(3) CH3ClC(CH3)3
A. (1), (2).
C. (2).
B. (2), (3).
D. (1).
Câu 3: Alkane nào sau đây chỉ cho 1 sản phẩm thế duy nhất khi tác dụng với Cl2 (as)
theo tỉ lệ mol (1:1)
(1) CH3CH2CH3
(2) CH4.
(3) CH3C(CH3)2CH3
(4) CH3CH3
(5) CH3CH(CH3)CH3.
Câu 6: Cho isopentane tác dụng Cl2 theo
tỉ lệ 1:1 về số mol, có ánh sáng. Sản phẩm
monochloro nào dễ hình thành nhất là
A. 3-methylpentane.
B. 2,3-dimethylbutane
C. 2- methylpropane.
D. butane.
Câu 7: Khi Chloro hoá hỗn hợp 2 alkane
người ta chỉ thu được 3 sản phẩm thế
monochloro. Tên gọi của 2 alkane đó là
A. ethane và propanee.
B. propane và iso butane
C. iso butane và pentane
D. neo pentane và ethane
Câu 8: Cho 4 chất: CH4, C2H6, C3H8,
C4H10. Số lượng chất tạo được một sản phẩm
thế monocle duy nhất là
A. 1 B. 2
DẠYKÈMQUYNHƠNOFFICIAL
12
A.1 C. 2 B.3 D. 4
C. 3. D.4. CHƯƠNG 2 DẠNG 2: BÀI TẬP VỀ TÍNH CHẤT HÓA HỌC
A. (a), (e), (d). B. (b), (c), (d).
C. (c), (d), (e). D. (a), (b), (c), (e), (d)
Câu 4: Cho dãy gồm các alkane: butane, isobutane, isopentanee, neopentane. Alkane
nào trong dãy có chứa C bậc IV?
A. Butane C. Isobutane
B. Isopentane D. Neopentane
Câu 9: Trong phân tử hydrocarbon X có tỉ
lệ khối lượng mC : mH = 5 : 1. Đồng phân cấu
tạo của X có mạch carbon không phân nhánh
có tên gọi là
A. butane C. hexane
B. pentane. D. heptane.
Câu 5: Khi cho 2-methylbutane tác dụng
với Cl2 theo tỉ lệ 1:1 thì tạo ra sản phẩm chính
là
A. 1-chloro-2-methylbutane.
B. 2-chloro-2-methylbutane.
C. 2-chloro-3-methylbutane
D. 1-chloro-3-methylbutane.

Câu 10: Có bao nhiêu alkane là chất khí ở
điều kiện thường khi phản ứng với chloro (có
ánh sáng, tỉ lệ mol 1:1) tạo ra 2 dẫn xuất monochloro?

A. 4.
C. 5.
B. 2.
D. 3.
DẠYKÈMQUYNHƠNOFFICIAL
CHƯƠNG 2 DẠNG 2: BÀI TẬP VỀ TÍNH CHẤT HÓA HỌC
Dạng 1: Bài tập tính toán về phản ứng thế của Alkane
Phương pháp giải:
PHƯƠNG PHÁP GIẢI CÁC BÀI TẬP PHẢN ỨNG THẾ CỦA ALKANE

* Nhận xét chung:
- Do trong phân tử chỉ có các liên kết đơn là các liên kết bền nên ở điều kiện thường các alkane
tương đối trơ về mặt hóa học. Alkane không bị oxi hóa bởi các dung dịch H2SO4 đặc, HNO3,
KMnO4
- Khi có as, to, xt thì alkane tham gia các phản ứng thế, tách và oxi hóa.
Phương pháp giải bài tập thế halogen
Bước 1: Viết phương trình phản ứng của alkane với Cl2 hoặc Br2. Nếu đề bài không cho biết sản phẩm thế là monohalogen, đihalogen, … thì ta phải viết phản ứng ở dạng tổng quát: CnH2n+2 + xBr2 ���� → CnH2n+2-xBrx + xHBr
hoặc CnH2n+2 + xCl2 ���� → CnH2n+2-xClx + xHCl
Bước 2: Tính khối lượng mol của sản phẩm thế hoặc khối lượng mol trung bình của hỗn hợp sản phẩm để tìm số nguyên tử carbon trong alkane hoặc mối liên hệ giữa số carbon và số

nguyên tử chloro, bromo trong sản phẩm thế, từ đó xác định được số nguyên tử carbon và số
nguyên tử chloro, bromo trong sản phẩm thế. Suy ra công thức cấu tạo của alkane ban đầu và
công thức cấu tạo của các sản phẩm thế
Bài tập vận dụng
Câu 1: Một trong những thành phần không thể thiếu cho các
động cơ để có thể hoạt động và làm việc là alkane có thành phần phần trăm C là 83,33%. Tìm CTPT và xác định CTCT đúng của alkane đó biết rằng khi cho alkane đó tác dụng với Cl2 theo tỉ lệ mol
1: 1 ta chỉ thu được 1 sản phẩm thế monochloro.
DẠYKÈMQUYNHƠNOFFICIAL
14
CHƯƠNG 2 DẠNG 3: BÀI TẬP TÍNH TOÁN 1 1.1 1.2
Câu 2: Khi thực hiện chloro hóa alkane X theo tỉ lệ mol 1: 1 tạo sản phẩm dẫn xuất monochloro là khí chính trong công nghiệp hàn cắt có thành phần khối lượng chloro là 45,223%. Tìm công thức phân tử của X.
Câu 4: Khi bromo hóa một alkane chỉ thu
được một dẫn xuất monobromo duy nhất có tỉ
khối hơi đối với hydro là 75,5. Xác định tên
của alkane đó. (Sau khi làm ra kết quả hãy thử quét mã QR dưới đây)

Câu 3: Đã bao gi n nghe qua: LPG (một khídầu mỏ hóa lỏng haykhí gas). Là một trong những thành phần không thể thiếu ở các khí trên và có mặt ở hầu hết trong các nhiên liệu, khi phản ứng vừa đủ với V lit Cl2(đktc) thu
được hh sản phẩm chỉ gồm 2 dẫn xuất monochloro và 1 chất vô cơ X. Mỗi dẫn xuất monochloro đều chứa 38,38% khối lượng là

chloro. Biết tổng khối lượng 2 dẫn xuất chloro

lớn hơn khối lượng của X là 8,4 gam. Hãy tìm
CTCT và giá trị của V từ những dữ liệu trên.
Câu 5: Là một dung môi trong công
nghiệp, làm môi trường phản ứng polyme hoá.
Khi refoming, có thể chuyển thành benzene, là một thành phần không mong muốn của xăng vì

có chỉ số octan thấp. Khi cho dung môi trên (trong phân tử có phần trăm khối lượng carbon
bằng 83,72%) tác dụng với Chloro theo tỉ lệ số mol 1:1(trong điều kiện chiếu sáng) chỉ thu
được2 dẫn xuất monochloro đồng phân của nhau. Tìm tên dung môi.

DẠYKÈMQUYNHƠNOFFICIAL
15
CHƯƠNG 2 DẠNG 3: BÀI TẬP TÍNH TOÁN
Dạng 2: Bài tập về phản ứng cracking của alkane
Phương pháp giải:
DẠNG BÀI TẬP CƠ BẢN
Dạng 2.1: Xác định công thức phân tử của alkane trong phản ứng cracking.
Phương pháp: Áp dụng định luật toàn khối: “Khối lượng của các chất trước phản hồi bằng
tổng kết của các chất sau phản hồi” kết hợp với chất lượng của phương pháp tự chọn.
Đề mẫu: Khi cracking hoàn toàn một thể tích alkane X thu được b thể tích hỗn hợp Y (các thể tích đo được ở cùng điều kiện nhiệt độ và áp suất). Tỷ khối hơi của Y so với H2, bằngM
Công thức của X là:
Bước 1: Do các thể tích được đo ở cùng điều kiện nhiệt độ và áp suất nên tỉ lệ thể tichsd
cũng chính là tỉ lệ về số mol.
Bước 2: Gọi CTPT của alkane X là CnH2n+2 (với nX = a mol, nY = b mol)

Bước 3: dy/M từ đây suy ra My và mY.
Bước 4: Áp dụng định luật bảo toàn khối lượng.
Ta có được mx và Mx từ đó xác định được công thức của X.
Dạng 2.2: Tính số mol hoặc thể tích các chất trong phản ứng cracking.
Phương pháp: Đối với bài toán dạng này, không cần quan tâm tới sản phẩm chỉ cần biết sản phẩm chắc chắn có alkane (có thể là hydro).
CnH2n+2 > CmH2m+2 + CpH2p (n = m + p) x mol > x mol x mol
Tổng số mol trước phản ứng: ntrước = x +y (mol)
- Tổng số mol sau phản ứng: nsau = 2x + y (mol) - nphản ứng = nsau - ntrước
DẠYKÈMQUYNHƠNOFFICIAL
16
2
CHƯƠNG 2 DẠNG 3: BÀI TẬP TÍNH TOÁN
2.1
- Vphản ứng = Vsau - Vtrước
Đề mẫu: Craking V lít Alkane thu được V khí X khác nhau, các khí đều đo ở (đktc). Thể tích alkane X chưa bị craking.
Bước 1: Tìm thể tích phản đã ứng bằng công thức sau:
Vphản ứng = Vsau - Vtrước

Bước 2: Sau khi đãtìm được thể tích phản ứng từ đó dễ dàng tìm được thể tích chưa cracking bằng công thức sau:
Vchưa craking = Vban đầu - Vphản ứng
Dạng 2.3: Bài tập liên quan đến đốt cháy sản phẩm thu được sau khi thực hiện phản ứng
craking alkane
Phương pháp: Ví dụ đề có dữ kiện sau: Craking ankamn A, sau 1 thời gian thu được hỗn hợp các hydrocarbon gôm n chất. Đốt cháy hoàn toàn hỗn hợp đó thu được bao nhiêu lít CO2
bao nhiêu gam nước, sục vào các bình thấy khối lượng bình tăng bao nhiêu gam? Thì ta coi
như đốt cháy alkane A.
Đề mẫu: Craking m gam alkane. Sau phản ứng thu được hỗn hợp gồm n hydrocarbon. Đốt
cháy hoàn toàn hỗn hợp A thu được m gam H2O. Tìm giá trị của m.
Bước 1: Lập luận vì đây là loại phản ứng cracking mà liên quan đến đốt cháy nên ta coi như
không có craking nên quy về bài toán đốt cháy.
Bước 2: Tìm số mol của alkane.
Bước 3: Trình bày phương trình đốt cháy của alkane, từ phương trình đó ta dễ dàng có được
số mol H2O.
Có số mol H2O sau đó suy ra được khối lượng của H2O.
Dạng 2.4: Bài tập liên quan đén phản ứng tách H2 từ alkane
Phương pháp: Áp dụng như dạng 1.
DẠYKÈMQUYNHƠNOFFICIAL
17
CHƯƠNG 2 DẠNG 3: BÀI TẬP TÍNH TOÁN
Dạng 2.5: Tính hiệu suất trong phản ứng craking alkane
Phương pháp:
- Giả sử ta có phản ứng:
CnH2n+2 > CmH2m+2 + CpH2p ( n = m + p)
nphản ứng: x mol > x mol > x mol
nalkane dư: y mol
Vậy: H= �� ��+�� 100%
Đề mẫu: Cracking alkane X thu được hỗn hợp A gồm n hydrocarbon có khối lượng phân tử trung bình bằngM. Hiệu suất của quá trình craking là:
Bước 1: Trình bày phản ứng cracking.
CnH2n+2 > CmH2m+2 + CpH2p (n = m + p)
sau đó giả sử mol của alkane là x mol
nphản ứng: x mol > x mol > x mol
nalkane dư: y mol
Bước 2: Theo giả thuyết đề bài cho và kết hợp với bước 1 thì ta tìm ra x mol.
Bước 3: Áp dụng công thức tính hiệu suất:
lấy mol phản ứng /( mol phản ứng + mol alkane dư ) .100%
2.2

Bài tập vận dụng
Câu 1: Xăng thì rất giàu hydrocarbon đặc biệt là alkane có chứa

(C, H). Khi cracking hoàn toàn một thể tích alkane X thu được ba thể
tích hỗn hợp Y (các thể tích đo được ở cùng điều kiện nhiệt độ và áp
suất). Tỷ khối hơi của Y so với H2, bằng 12. Công thức của X là.
DẠYKÈMQUYNHƠNOFFICIAL
18
CHƯƠNG 2 DẠNG 3: BÀI TẬP TÍNH TOÁN
Câu 2: Sự hòa tan C4H10 có thể gây hưng phấn, buồn ngủ, bất tỉnh, ngạt thở, rối loạn nhịp tim, huyết áp dao động và mất trí nhớ tạm thời, khi lạm dụng trực tiếp từ bình chứa có áp suất cao và có thể dẫn đến
tử vong do ngạt thở và rung thất. Khi Craking 560 lít C4H10 thu được


1010 lít khí X khác nhau, các khí đều đo ở (đktc). Thể tích C4H10 chưa
bị craking.
Câu 3: Thành phần chính của alkane chứa (C, H). Khi thực hiện phản ứng tách H2 từ 1 alkane
với hiệu suất 75% thu được hỗn hợp X có tỉ khối so với hydro là 16,571. Thêm 0,1 mol C2H4 vào m gam hỗn hợp Y. Đốt hỗn hợp Y cần 32,928 lít O2 (đktc). Tính giá trị của m.
Câu4:C4H10 cũngđượcsửdụnglàmnhiên liệunhẹhơncho mộtchiếc
bật lửa thông thường. Khi Cracking C4H10 thu được hỗn hợp A gồm 5
hydrocarbon có khối lượng phân tử trung bình bằng 36,25. Tính hiệu suất của quá trình craking.

Câu 5: C4H10 thông thường có thể được sử dụng để pha trộn xăng, làm nhiên liệu khí đốt chủ yếu đồng thời được sử dụng bởi các nhà máy lọc dầu để nâng cao (tăng) trị số của xăng động cơ. Khi Craking 29 gam
C4H10. Sau phản ứng thu được hỗn hợp gồm 5 hydrocarbon. Đốt cháy
hoàn toàn hỗn hợp A thu được m gam H2O. Tính giá trị của m.
Dạng 3: Bài tập về phản ứng oxi hóa hoàn toàn alkane
Phương pháp giải:
DẠYKÈMQUYNHƠNOFFICIAL
19
CÁC LƯU Ý KHI GIẢI CÁC BÀI TẬP ĐỐT CHÁY ALKANE Phản ứng đốt cháy có dạng: CnH2n+2 + 3��+1 2 O2 ���� → nCO2 + (n+1) H2O { nCO2 < nH2O nAnkan= nH2O - nCO2 BTNT O: 2nO2 pứ=2nCO2 + nH2O Số C= nCO2 nAnkan 2 2.1
DẠNG BÀI TẬP CƠ BẢN
Dạng 3.1: Xác định công thức phân tử của alkane từ giả thuyết CO2 và H2O
Đề mẫu: Đốt cháy một hydrocarbon A thu được x(g) CO2 và y(g) H2O.
Bước 1: Cần chứng minh được hydrocarbon cần tìm là alkane. Nếu ������2 < ����2�� A là alkane.
Bước 2: Để tìm ra n có thể sử dụng một trong hai cách sau:
Cách 1: Hệ số cân bằng của H2O Số mol H2O = Hệ số cân bằng của CO2 Số mol CO2 (Với hệ cân bằng của H2O = n+1; hệ số cân bằng của CO2 bằng n)
Tìm được n Tìm được CTPT của alkane A.
Cách 2: Áp dụng một số công thức (*) để tìm được n(số C) Tìm ra CTPT của alkane cần tìm.
Dạng 3.2: Xác định công thức phân tử của alkane khi biết khối lượng của alkane và số mol của CO2 (hoặc H2O).
Dạng 3.2: Xác định công thức phân tử của alkane khi biết khối lượng của alkane và số mol của CO2 (hoặc H2O).
Đề mẫu: Đốt cháy hoàn toàn x(g) alkane X thu được V (l) CO2 (đktc). Tìm CTPT của alkane X?

Bước 1: Tính số mol alkane theo n.
Bước 2: Tính khối lượng mol của alkane theo n
Bước 3: Áp dụng công thức m = n.M
Bước 4: Giải tìm n Tìm ra công thức phân tử của alkane.
Dạng 3.3: Xác định công thức phân tử của alkane khi biết số mol O2 cháy và số mol CO2 (hoặc H2O).
DẠYKÈMQUYNHƠNOFFICIAL
20
CHƯƠNG 2 DẠNG 3: BÀI TẬP TÍNH TOÁN
Số C= nCO2 nAnkan Tìm được CTPT của A.
Dạng 3.4: Xác định công thức phân tử của hỗn hợp alkane từ CO2 và H2O
Đề mẫu: Đốt cháy x(g) một hỗn hợp alkane (gồm alkane A và alkane B) ở thể khí thấy sinh
ra V(l) CO2 (đktc)

Bước 1: Gọi CTPT của alkane A là CnH2n+2 (x mol).
Gọi CTPT của alkane B là CmH2m+2 (y mol).
Gọi công thức trung bình của hai alkane là ������2��+2 (a mol)
Với �� là số carbon trung bình và a = x + y) n <�� <��
Bước 2: Áp dụng các công thức để tìm ra ��.
Có thể tính số mol hỗn hợp (x, y) dựa vào �� và theo phương pháp đường chéo. n m - �� x
DẠYKÈMQUYNHƠNOFFICIAL
Tìm được m và n Tìm được CTPT của alkane A và alkane B.
21
ần dùng
được V1 (l)
đị
CTPT
ủa A?
Cách 1: Bước 1: Lập tỉ lệ: Hệ số cân bằng của O2 Số mol O2 = Hệ số cân bằng của CO2 Số mol CO2 Bước 2: Với hệ cân bằng của O2 = 3��+1 2 ; hệ số cân bằng của CO2 bằng n Tìm được n Tìm được CTPT củ
Đề mẫu: Đốt cháy hoàn toàn alkane A c
V(l) O2 (đktc) thu
CO2 (đktc). Xác
nh
c
a alkane A.
O2 pứ=2nCO2+nH2O
Cách 2: Bước 1: Áp dụng ĐLBT O: 2n
Tìm được ����2��
số nAnkan= nH2O-nCO2và
Bước 2: Áp dụng công thức
��
�� – n y
m
CHƯƠNG 2 DẠNG 3: BÀI TẬP TÍNH TOÁN
Dạng 3.5: Tính toán khối lượng, số mol, thể tích các chất trong phản ứng đốt cháy alkane

(Áp dụng công thức * để giải bài toán.)
2.2
Bài tập vận dụng
Câu 1: Trong một thế giới ngày càng phát triển và lượng năng
lượng sử dụng ngày càng tăng, cùng với áp lực phải cắt giảm khí thảinhàkínhngàycàng cao,khíthiênnhiênsẽtrởthành mộttrong
những nguồn năng lượng quan trọng nhất để đáp ứng nhu c trong tương lai. Khí thiên nhiên chủ yếu chứa methane và ethane
với một chút propane và butane Nếu dùng nhiệt đốt cháy hoàn
toàn m (g) khí thiên nhiên gồm các alkane: CH4 (methane), C2H6 (ethane) và C4H10 (butane) thì sẽ thu được 3,3g CO2 và 4,5 g H2O. Hãy tính giá trị của m là?
Câu 2: Đốt cháy hoàn toàn một hydrocarbon X thu được 6,72 lít CO2 (đktc) và 7,2 g H2O.

a. Tính thể tích oxi (đktc) dùng để đốt cháy hoàn toàn hydrocarbon X?
b. Tìm CTPT hydrocarbon. (Sau khi làm ra kết quả hãy thử quét mã QR dưới đây)

Câu 3: Đốt cháy hoàn toàn một alkane có trong bật lửa gas, thu 22 gam CO2 và 13,44 lit hơi nước (đktc).
a. Tìm CTPT hydrocarbon.

DẠYKÈMQUYNHƠNOFFICIAL
22
b. Viết đồng phân và gọi tên biết khi tác dụng Cl2 (1:1) cho một sản phẩm monochloro duy nhất. CHƯƠNG 2 DẠNG 3: BÀI TẬP TÍNH TOÁN
Câu 4: Khí thiên nhiên và khí thiên nhiên hóa lỏng có vai trò quan trọng trong việc sản xuất
nhiệt năng, điện năng năng, cơ năng trong hoạt động sản xuất ngày nay. Khí methane (CH4) là thành phần chính của khí thiên nhiên. Nếu người ta đem đốt cháy hoàn toàn 6,8g hỗn hợp khí X
gồm: alkane A và methane (CH4), biết alkane A là thành phần chính của khí thiên nhiên lỏng. Sản

phẩm cháy dẫn vào bình 1 đựng P2O5 vvà bình 2 đựng 1200ml Ba(OH)2 20,25M. Sau thí nghiệm khối lượng bình 1 tăng 12,6g
a. Tìm công thức phân tử của A, biết VA: VCH4 = 2:3.
b. Tính khối lượng các chất trong X.
Câu 5: Đốt cháy hoàn toàn một chất hữu cơ X, biết X là nguyên liệu thô quan trọng cho công nghiệp hóa dầu và là nguồn nhiên liệu quan trọng nhất của kinh tế thế giới, khi đốt cháy cần 7,84 l khí O2 (đktc). Sản phẩm cháy gồm chất hấp thụ hết vào bình đựng dung dịch Ba(OH)2, thấy 19,7g kết tủa xuất hiện và khối lượng dung dịch giảm 5,5 g. Lọc bỏ kết tủa, đun nóng nước lọc
lại thu được 9,85 g kết tủa nữa. Tìm CTPT của X?
Câu 6: Một vấn đề lớn mang tính chất toàn cầu đối với môi trường hiện
nay là hiệu ứng nhà kính, để giảm thải được CO2 thải ra ngoài môi trường

cần sử dụng các nguồn năng lượng sạch, khí thiên nhiên thường được mô tả
là loại nhiên liệu hóa thạch sạch nhất, tuy nhiên về mặt tuyệt đối, lượng khí
CO2dokhí tựnhiêngâyra vẫnở mộtconsố khổnglồ.Trong mộtthí nghiệm
nhỏ, người ta đốt cháy 8,8 g một hỗn hợp 2 alkane (trong đó 1 alkane là
thành phần của khí thiên nhiên, alkane còn lại thành phần của khí hóa lỏng) ở
thể khí thấy sinh ra 13,44 lit CO2 ở (đktc)

a. Tính tổng số mol 2 alkane
b. Tính thể tích khí oxi (đktc) cần để đốt cháy ½ hỗn hợp trên.
c. TìmCTPT của 2 alkane biết rằng thể tích 2 alkane trong hỗn hợp bằng nhau.
Câu 7: Khí Gas là loại nhiên liệu sạch nhất hiện nay, không gây ô nhiễm cho môi trường
và được sử dụng rộng rãi trong dân dụng, thương mại, vận tải và các ứng dụng công nghiệp, Khí
DẠYKÈMQUYNHƠNOFFICIAL
Gas là là hỗn hợp khí hydrocarbon, nhẹ, ở thể khí, khí Gas là " Khí dầu mỏ hóa lỏng " hay được
23
CHƯƠNG 2 DẠNG 3: BÀI TẬP TÍNH TOÁN
gọi tên đơn giản là " Khí hóa lỏng ". Dùng nhiệt đốt cháy hỗn

hợp khí X gồm 2 hydrocarbon no (hai hydrocarbon no là thành
phần chủ yếu của khí Gas), mạch hở A và B là đồng đẳng kế tiếp.

Đốt cháy X với 64g O2 (dư) rồi dẫn sản phẩm thu được qua dung
dịch Ca(OH) 2 thu được 100g kết tủa. Khí bay ra khỏi bình có
thể tích 11,2 l ở 0oC và 4 atm. Tìm CTPT của A và B?
DẠYKÈMQUYNHƠNOFFICIAL

24
CHƯƠNG 2 DẠNG 3: BÀI TẬP TÍNH TOÁN
Giải thích các vấn đề thực tiễn
Câu hỏi Hình ảnh
Câu 1: Hãy giải thích:
a. Tại sao không được để các bình chứa xăng dầu (gồm các alkane) gần lửa, trong khi đó người ta có thể nấu chảy nhựa đường (trong thành phần cũng có các alkane) để làm đường giao thông.

b. Không dùng nước để dập các đám cháy xăng, mà phải dùng cát hoặc bình chứa khí carbonic.

Câu 2: a. Vì sao có khí methane thoát ra từ ruộng lúa hoặc các ao (hồ)?
b. Khi methane gây nguy hiểm như thế nào khí làm trong hầm mỏ?
Câu 3: a. Vì sao đốt xăng, cồn thì cháy hết sạch, còn khi đốt gỗ, than đá lại còn tro?
b. Trong các hầm mỏ, than đá nếu không cẩn thận sẽ xảyra các vụ nổ, nguyên nhân gâyra các
vụ nổ này là gì? Người ta thường ngăn ngừa các
hiện tượng nổ bằng những biện pháp nào?
Câu 4: Biết rằng thành phần chủ yếu của
xăng dầu là hydrocarbon. Hãy giải thích:


DẠYKÈMQUYNHƠNOFFICIAL
25
2 CHƯƠNG 2 DẠNG 4: GIẢI THÍCH CÁC VẤN ĐỀ THỰC TIỄN
a/ Vì sao xăng dầu phải được chứa trong các
thùng chứa chuyên dụng và phải bảo quản ở

những kho riêng?
b/ Vì sao các tàu chở dầu khi bị tai nạn thường
gây ra thảm họa cho một vùng biển rất rộng?
c/ Vì sao khi các chi tiết máy hoặc đồ dùng bị
bẩn dầu mỡ người ta thường dùng xăng hoặc
dầu hỏa để lau rửa?
d/Vìsaokhibịcháyxăngdầukhôngnêndùng
nước để dập đám cháy?
e/ Khi tới các trạm xăng thì nhìn lên các cây
xăng thường xuất hiện các chỉ số E92, E95,...và
người ta thường hay đổ các loại xăng E95.Vậy cácchỉsốE92,E95cóýnghĩagìvàvìsaongười ta thường chọn xăng E95 thay E92?

Câu 5: Bình gas sử dụng trong đun nấu hàng
ngày chứa hỗn hợp hóa lỏng của propane và butane. Tuy hai hydrocarbon này thuộc dãy


đồngđẳngalkane, không màu không mùinhưng
thực tế khí ga lại có mùi trứng thối rất đặc trưng.
Mùi này xuất phát từ phân tử ethanthiol (gần giống H2S) được nhà sản xuất cố tình nạp thêm
một lượng nhỏ vào trong ga hóa lỏng nhằm phát
hiện ra khí ga rò rỉ khi sử dụng. Việc rò rỉ ga có
nhiều nguyên nhân, trong đó có thể kể đến sử
dụng bình ga kém chất lượng, dây dẫn ga bị
chuột cắn hoặc rạn nứt, lơ là để bếp bị tắt khi
đang đun, ... Trong trường hợp ngửi thấy mùi
DẠYKÈMQUYNHƠNOFFICIAL
khí ga rò rỉ, chúng ta cần phải làm gì?
26
CHƯƠNG 2 DẠNG 4: GIẢI THÍCH CÁC VẤN ĐỀ THỰC TIỄN
Số câu trả lời đúng: .../...
Hướng dẫn làm bài:
1. Phần trắc nghiệm: Đọc kỹ câu hỏi và đáp án cho sẵn ở đề thi, chọn đáp án đúng nhất và đánh dấu bằng cách tô đen () vào một trong những đáp án A, B, C, D ở phần trả lời.

2. Phần tự luận: Đọc kỹ câu hỏi và trả lời câu hỏi vào giấy thi.
D.
a alkane sau:

A. 2-methyl-3-butylpentane.

B. 3-ethyl-2-methylheptane.
C.3-isopropylheptane.
D. 2-methyl-3-ethyl-heptane.
Câu 5: Phần trăm khối lượng carbon trong phân tử alkane Y bằng 83,33%. Công thức phân
DẠYKÈMQUYNHƠNOFFICIAL
27 ĐỀ ÔN TẬP CHƯƠNG 2 – ALKANE ĐỀ 1
ĐIỂ
tử có
Liên
ết
dạng mạch hở hoặc C H.
Liên kết đơn
dạng mạch hở hoặc dạng mạch vòng.
Liên kết đôi
M: I-Trắc nghiệm: (7 điểm) Câu 1: Alkane là hydrocarbon trong phân
A.
k
đơn C C
B.
C C
C.
C=C.
Liên
ế
C Câu 2: Alkane B có công thức đơn giản nhất là C6H14. Số đồng phân cấu tạo của B là A. 2. B.3. C.4. D.5. Câu 3: Công thức phân tử của alkane có chứa 14 nguyên tử H là A. C3H14 C. C4H14 C. C5H14 D. C6H14 Câu 4: Tên gọ
IUPAC) củ
k
t ba C ≡
i (theo danh pháp
A. C2H6 B.C3H8 C. C4H10 D. C5H12. ĐỀ
Ể
tử của Y là
KI
M TRA ÔN TẬP CHƯƠNG 2
A. ethane và propane.
B. propane và iso butane.
C. iso butane và pentane
D. neo pentane và ethane.
Câu 8: Khi cho 2-methylbutane
A. 1-chloro-2-methylbutane.
B. 2-chloro-2-methylbutane.
C. 2-chloro-3-methylbutane.
D. 1-chloro-3-methylbutane. Câu 9: Khi bromo hóa mộ
A. 3,3-dimethylhecxan.
B. 2,2-dimethylpropane.
C. isopentane.
D. 2,2,3-trimethylpentane
Câu 10: Xăng thì rất giàu hydrocarbon đặc biệt là alkane có chứa (C, H). Khi cracking hoàn toàn một thể tích alkane X thu được ba thể tích hỗn hợp Y (các thể tích đo được ở cùng điều kiện nhiệt độ và áp suất). Tỷ khối hơi của Y so với H2, bằng 12. Công thức của X là.
DẠYKÈMQUYNHƠNOFFICIAL
28
ột đồng phân của C5H12 có công thức cấu tạo như sau: 1 C H3 2 C 3 C H2 4 C H3 CH3
tử carbon trong mạch chính có bậc cao nhất được đánh số thứ tự là
số 1 C. số 3 C. số 2 D. số 4
Câu 6: M
Nguyên
A.
hợp 2 alkane người ta chỉ thu được 3 sản phẩm thế monochloro.
Câu 7: Khi chloro hoá hỗn
Tên gọi của 2 alkane đó là
tác dụng với Cl2 theo tỉ lệ 1:1 thì tạo ra sản phẩm chính là:
chỉ thu được một dẫn xuất monobromo duy nhất có tỉ khối hơi đố
ớ
75,5. Xác định tên của alkane đó là
t alkane
i v
i hydro là
A. C7H16. B. C4H10. C. C6H14. D. C5H12. Phần trả
lời
II- Tự luận
Câu 1: Hãy viết các đồng phân cấu tạo mạch hở của các hydrocarbon no có công thức phân tử là C6H14 và gọi tên các đồng phân theo tên thay thế.
Câu 2: a. Hoàn thành chuỗi phản ứng hóa học sau:
b. Giải thích vấn đề thực tiễn sau:
(b.1) Tại sao không được để các bình chứa xăng dầu (gồm các alkane) gần lửa, trong khi đó người ta có thể nấu chảy nhựa đường (trong thành phần cũng có các alkane) để làm đường giao thông.
(b.2) Không dùng nước để dập các đám cháy xăng, mà phải dùng cát hoặc bình chứa khí carbonic.
Câu 3: Khí Gas là loại nhiên liệu sạch nhất hiện nay, không gây ô nhiễm cho môi trường và
được sử dụng rộng rãi trong dân dụng, thương mại, vận tải và các ứng dụng công nghiệp, Khí Gas là là hỗn hợp khí hydrocarbon, nhẹ, ở thể khí, khí Gas là " Khí dầu mỏ hóa lỏng " hay
được gọi tên đơn giản là " Khí hóa lỏng ". Dùng nhiệt đốt cháy hỗn hợp khí X gồm 2 hydrocarbon no (2) hydrocarbon no là thành phần chủ yếu của khí Gas), mạch hở A và B là
đồng đẳng kế tiếp. Đốt cháy X với 64g O2 (dư) rồi dẫn sản phẩm thu được qua dung dịch
Ca(OH)2 thu được 100g kết tủa. Khí bay ra khỏi bình có thể tích 11,2 l ở 0oC và 4 atm. Tìm
CTPT của A và B?
DẠYKÈMQUYNHƠNOFFICIAL
29 Câu A B C D Câu A B C D 1 6 2 7 3 8 4 9 5 10
ĐỀ ÔN TẬP CHƯƠNG 2 – ALKANE ĐỀ 2
Số câu trả lời đúng: .../...
ĐIỂM:
I-Trắc nghiệm: (7 điểm)
Hướng dẫn làm bài:
1. Phần trắc nghiệm: Đọc kỹ câu hỏi và đáp án cho sẵn ở đề thi, chọn đáp án đúng nhất và đánh dấu bằng cách tô đen () vào một trong những đáp án A, B, C, D ở phần trả lời.
2. Phần tự luận: Đọc kỹ câu hỏi và trả lời câu hỏi vào giấy thi.
Câu 1: Alkane là những hydrocarbon no, mạch hở, có công thức chung là:
A. CnH2n+2 (n ≥1) C. CnH2n-2 (n ≥2)
B. CnH2n (n ≥2) D. CnH2n-6 (n ≥6)
Câu 2: Trong các mệnh đề sau, mệnh đề nào là mệnh đề sai?
A. Tất cả các alkane đều có CTPT là CnH2n+2
B. Tất cả các chất có cùng CTPT CnH2n+2 đều là alkane
C. Tất cả các alkane đều chỉ có lien kết đơn trong phân tử
D. Tất cả các chất chỉ có liên kết đơn trong phân tử đều là alkane
Câu 4: Hợp chất có tên gọi 2,2,3,3-tetramethylbutane có bao nhiêu nguyên tử C và H trong phân tử?
A. 8C, 16H
C. 6C, 12H
B. 8C, 14H D. 8C, 18H
Câu 5: Cho công thức cấu tạo dưới đây có tên là?
DẠYKÈMQUYNHƠNOFFICIAL
30
A. 3-ethyl-4-methylpentane
B. 3,3-dimethylpentane
C. 2-methyl-3ethylpentane
D. 3-ethyl-2-methylpentane
Câu 6: Methane được điều chế từ phản ứng nào sau đây?
A. Nung CH3COONa trong vôi tôi xút ở nhiệt độ cao
B. Nung vôi tôi xút ở nhiệt độ cao
C. Nung HCOONa trong vôi tôi xút ở nhiệt độ cao
D. Khi nung CH3COONa ở nhiệt độ cao
Câu 7: Phản ứng đặc trưng của hydrocarbon no là?
A. Phản ứng tách
B. Phản ứng cộng
C. Phản ứng thế
D. Phản ứng tách
Câu 8: Khi đốt cháy methane trong khí chloro sinh ra muội đen và một chất khí làm giấy quỳ
tím ẩm hoá đỏ. Sản phẩm của phản ứng là?
A. CH2Cl2 và HCl
B. C và HCl
C. CH3Cl và HCl
D. CCl4 và HCl
Câu 9: Sản phẩm của phản ứng thế chloro (1:1, ánh sáng) vào 2,2- dimethyl propane là:
(1) CH3C(CH3)2CH2Cl; (2) CH3C(CH2Cl)2CH3 ; (3) CH3ClC(CH3)
A. (1); (2).
B. (2); (3).
C. (2)
D. (1)
Câu 10: Đốt cháy hoàn toàn một hydrocarbon thu được số mol H2Ogấp đôi số mol CO2. Công thức phân tử của hydrocarbon là?
A. C2H2
B. C2H6
Phần trả lời:
C. C3H8
D. CH4
DẠYKÈMQUYNHƠNOFFICIAL
31
A B C D Câu A B C D 1 6
Câu
8
II- Tự luận
Câu 1:( 1,5 điểm) Hoàn thành chuỗi phản ứng sau: (ghi rõ điều kiện cụ thể)
Câu 2:(2 điểm) Một alkane không thể thiếu trong cuộc sống hằng ngày của chúng ta, alkane này được sử dụng chủ yếu làm nhiên liệu và dung môi, xăng dầu cho động cơ, dầu thắp sáng và đun nấu, có sản phẩm thế monochloro trong đó chloro chiếm 33,33 % về khối lượng.
a. Xác định CTPT và CTCT của alkane.
b. Viết CTCT các đồng phân monochloro và gọi tên chúng. C5H12
Câu 3:(1,5 điểm) C5H12 là alkane tương đối rẻ tiền trên thị trường và là alkane lỏng dễ bay hơi nhất ở nhiệt độ phòng, vì vậy chúng thường được sử dụng trong phòng thí nghiệm làm dung môi có thể bay hơi nhanh và thuận tiện. Khi cracking 3,6 gam C5H12 thu được hỗn hợp X
và H2. Đốt cháy hoàn toàn X thu được sản ph
O. Dẫn toàn bộ sản phẩm chính qua bình đựng Ca(OH)2 dư thu được m(g) kết tủa và khối lượng bình tăng lên a (gam).
Tính giá trị của m và a tương ứng là?
Câu 4:(1điểm) Methan là một nhiên liệu quan trọng. Ở nhiều nơi, methan được dẫn tới từng nhà nhằm mục đích sưởi ấm và nấu ăn. Đồng thời khí methane gây nguy hiểm trong hầm mỏ
Giải thích khí methane gây nguy hiểm như thế nào?
DẠYKÈMQUYNHƠNOFFICIAL
32 2
3
4
7
9
5
10
gồm:
4
C2H6
C3H8
C5H10
C4H8
C3H6
5H10
2
CH
,
,
,
,
,
, C
ẩm chính gồm CO2 và H
ĐỀ ÔN TẬP CHƯƠNG 2 – ALKANE ĐỀ 3
Số câu trả lời đúng: .../...
ĐIỂM:
I-Trắc nghiệm: (7 điểm)
Hướng dẫn làm bài:
1. Phần trắc nghiệm: Đọc kỹ câu hỏi và đáp án cho sẵn ở đề thi, chọn đáp án đúng nhất và đánh dấu bằng cách tô đen () vào một trong những đáp án A, B, C, D ở phần trả lời.
2. Phần tự luận: Đọc kỹ câu hỏi và trả lời câu hỏi vào giấy thi.
Câu 1: Trong các nhận xét dưới đây, nhận xét nào sai ?
A.Tất cả các alkane đều có công thức phân tử CnH2n+2.
B. Tất cả các chất có công thức phân tử CnH2n+2 đều là alkane
C. Tất cả các alkane đều chỉ có liên kết đơn trong phân tử.
D. Tất cả các chất chỉ có liên kết đơn trong phân tử đều là alkane.
Câu 2: Alkane hòa tan tốt trong dung môi nào sau đây ?
A. Nước. B. Benzene. C. Dung dịch axit HCl. D. Dung dịch NaOH.
Câu 3: Phản ứng đặc trưng của hydrocarbon no là ?
A.Phản ứng tách. B. Phản ứng thế C. Phản ứng cộng.
D. Phản ứng oxi hóa.
Câu 4: Các alkane không tham gia loại phản ứng nào ?
A.Phản ứng thế. B. Phản ứng cộng. C. Phản ứng tách.
D. Phản ứng cháy.
Câu 5: Phân tử methane không tan trong nước vì lí do nào sau đây ?
A.Methane là chất khí.
B.Methane không có liên kết đôi.
Câu 6: Cho các chất sau:
C2H6 (I); C3H8 (II); n-C4H10 (III); i-C4H10 (IV).
Nhiệt độ sôi tăng dần theo dãy là:
A.(III) < (IV) < (II) < (I).
B. Phân tử methane không phân cực.
D. Phân tử khối của methane nhỏ.
DẠYKÈMQUYNHƠNOFFICIAL
B. (III) < (IV) < (II) < (I).
33
C.(I) < (II) < (IV) < (III). D. (I) < (II) < (III) < (IV).
Câu 7: Có bao nhiêu đồng phân cấu tạo có công thức phân tử là C6H14 ?
A. 3 đồng phân. B. 4 đồng phân. C. 5 đồng phân. D. 6 đồng phân.
Câu 8: Có bao nhiêu đồng phân cấu tạo có công thức phân tử là C4H9Cl?
A. 3 đồng phân. B. 4 đồng phân. C. 5 đồng phân. D. 6 đồng phân.
Câu 9: Khi được chiếu sáng, hydrocarbon nào sau đây tham gia phản ứng thế với chloro theo tỉ lệ mol 1:1, thu được ba dẫn xuất monochloro là đồng phân cấu tạo của nhau?
A.isopentane B. neopentane C. pentane D. butane
Câu 10: Dãy alkane nào sau đây thỏa mãn điều kiện: mỗi công thức phân tử có một đồng phân khi tác dụng với chloro theo tỉ lệ mol 1 : 1 tạo ra 1 dẫn xuất monochloroalkane duy nh
H10, C6H14
II- Tự luận
Câu 2(1đ): Khi đốt cháy một thể tích alkane ở thể tích với lượng chloro vừa đủ người ta thu
được sản phẩm khí duy nhất có thể tích gấp 10 lần thể tích alkane ban đầu.
a/ Xác định công thức phân tử alkane
b/ Nếu tiến hành phản ứng thế giữa alkane nói trên với chloro chỉ thu được 2 dẫ
đichloro. Xác định công tức cấu tạo của alkane.
Câu 3(1đ): Nhiệt phân 8,8 gam C3H8 giả sử xảy ra hai phản ứng:
DẠYKÈMQUYNHƠNOFFICIAL
34
ấ
A.CH
C4
B. CH4, C2H6, C5H12
C8H
B.CH4
4
C5
6
D. CH4, C2H6, C5H12, C4H10. Phần trả lời Câu A B C D Câu A B C D 1 6 2 7 3 8 4 9 5 10
t?
4, C3H8,
,
18
, C
H10,
H12, C
H14.
khí
gồm C2H4, C2H2 và C2H6. Đốt cháy hoàn
2O. Tính
trị của
Câu 1(1đ): Một hỗn hợp
X
toàn m gam X thu được 3,52 gam CO2 và 1,44 gam H
giá
m?
ấ
n xu
t
C3H8 ���� → CH4
C2H4 và C3H8 ���� → C3H6 + H2
+
Thu được hỗn hợp khí X. Biết có 90% C3H8 bị nhiệt phân.
a/ Tính khối lượng mol trung bình của hỗn hợp X.
b/Tính thể tích oxi dùng để đốt cháy hỗn hợp X và khối lượng CO2 , H2O thu được trong phản ứng này.
c/ Nếu cho hỗn hợp X qua nước bromo dư còn lại khí Y có dY/H2 =7,3. Xác định thành phần
của hỗn hợp Y.
DẠYKÈMQUYNHƠNOFFICIAL
35
HYDROCARBON KHÔNG NO
Chương 3.1: ALKENE









Hệ thống bài tập: Gồm 3 dạng cơ bản
Dạng 1: Bài tập về đồng phân và danh pháp

Dạng 2: Bài tập về tính chất hóa học
Dạng 3: Bài tập tính toán
DẠYKÈMQUYNHƠNOFFICIAL
36
Dạng 1.1: Đồng phân
Phương pháp giải
Ví dụ: Hãy viết đồng phân cấu tạo
của C4H8 1.1.1


Bước 1: Số carbon cần viết: 4 nguyên tử C
Bước2: Viết mạch C dưới dạngthẳng nnguyêntửC.Đượcđồngphânthứnhất
Bước 3: Đồng phân thứ hai được viết sẽ di chuyển vị trí nối đôi, ta được
Vì đây có 4C nên bắt đầu bẻ nhánh theo
dạng 3+1 và mạch chính lúc này có 3C
nên vị trí nối đôi sẽ đặt ở đầu ( đã xét tính đối xứng)
Đồng phân cấu tạo
Cách viết đồng phân:
Bước 1: Xác định số carbon cần viết.
Bước 2: Ưu tiên viết mạch carbon theo mạch thẳng.
Bước3:TừC4trởđibắtđầubẻnhánhchúý đặtnhánh
không gắn ở đầu mạch và để ý tính đối xứng cũng như
là vị trí liên kết đôi của mạch tránh trùng lặp).
Bước 4: Điề ể a các nguyên tố.
Bước 4: Điền H để đảm bảo hóa trị
các nguyên tố
Vậy C4H8 có 3 đồng phân cấu tạo.
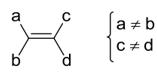
Đồng phân hình học
Những alkene mà mỗi nguyên tử carbon ở vị trí liên kết đôi liên kết với hai nhóm nguyên tử
khác nhau sẽ có sự phân bố không gian khác nhau của mạch chính xung quanh liên kết đôi. Sự
phân bố khác nhau đó tạo ra đồng phân về vị trí không gian của nhóm nguyên tử gọi là đồng phân
hình học.
Nguyên nhân xuất hiện đồng phân hình
học:
Do bộ phận cứng nhắc của phân tử làm cản
trở sự quay tự do của các nhóm thế xung quanh
trục liên kết.
Bộ phận cứng nhắc là liên kết đôi:
Điều kiện cần và đủ để xuất hiện đồng
phân hình học:
Phân tử phải có bộ phận cứng nhắc cản trở sự quay tự do của hai nguyên tử ở bộ phận đó.
Ở mỗi nguyên tử carbon của liên kết đôi và ở
ít nhất hai nguyên tử carbon của vòng no phải có hai nguyên tử hoặc nhóm nguyên tử khác nhau.
DẠYKÈMQUYNHƠNOFFICIAL
37
CHƯƠNG 3.1 DẠNG 1: BÀI TẬP VỀ ĐỒNG PHÂN VÀ DANH PHÁP
1
1.1 1.1.1
Phân loại: Đồng phân hình học gồm đồng phân cis và đồng phân trans:
Đồng phân cis: mạch C chính cùng một phía của mặt phẳng chứa liên kết pi.
Đồng phân trans: mạch C chính ở khác phía của mặt phẳng chứa liên kết pi.
Danh pháp:
cis/trans – tên của hợp chất hữu cơ

*Ví dụ: Hãy viết và gọi tên đồng phân hình học ứng với công thức cấu tạo CH3 ‒CH=CH‒CH3
cis-but-2-en
Bài tập vận dụng
Bài tập tự luận
Câu 1: Hãyviết các đồng phân cấu tạo mạch hở của các hydrocarbon no có công thức phân tử sau:
a. C4H8
b. C5H10
c. C6H12
Bài tập trắc nghiệm
Câu 1: Alkene X có đặc điểm: Trong phân tử có 8 liên kết xích ma (σ). CTPT của X là
A. C2H4 B. C4H8.
C.C3H6 D. C5H10.
Câu 2: Những hợp chất nào sau đây có
đồng phân hình học (cis-trans)?
trans-but-2-en
Câu 2: Hãy viết công thức phân tử của các alkene dưới đây và cho biết số đồng phân cấu tạo.
a. Alkene E có chứa 2 nguyên tử C
b. Alkene F có chứa 6 nguyên tử H
c. Alkene G có tổng số nguyên C và H là 21.
Câu 5: Hợp chất C5H10 có bao nhiêu
đồng phân cấu tạo?
A. 4. B. 5.
C. 6 D. 10.
Câu 6: Trong những alkene sau:
propene, but‒1‒ene, but‒2‒ene, pent‒1‒ene.
Những hydrocarbon có đồng phân cis-trans là
DẠYKÈMQUYNHƠNOFFICIAL
A. propene, but-1-ene
38
1.2 1.2.1 1.2.2 CHƯƠNG 3.1 DẠNG 1: BÀI TẬP VỀ ĐỒNG PHÂN VÀ DANH PHÁP
CH3CH=CH2 (I); CH3CH=CHCl (II);
CH3CH=C(CH3)2 (III); C2H5C(CH3)=C(CH3)–
C2H5 (IV); C2H5–C(CH3)=CCl–CH3(V).
A. (I), (IV). B. (IV), (V)
C. (III), (IV). D. (III), (IV), (V)
Câu 3: Hợp chất C5H10 có bao nhiêu đồng phân alkene?
A. 4.
C. 6.
7.
Câu 4: Cho các chất sau:
CH3C(CH3)=CHCH3
CH3CH2CH=CHCH2CH3;
CH3C(CH3)=CHCH2CH3;
CH3CH2C(CH3)=C(C2H5)CH(CH3)2
CH3CH=CHCH3.
Số chất có đồng phân hình học là
A. 4. B. 1.
C. 2. D. 3.
Dạng 1.2: Danh pháp
Phương pháp giải
Tên thay thế
B. propene, but-2-ene
C. pent-1-ene, but-1-ene.
D. but-2-ene.
Câu 7: Những chất nào sau đây không có
đồng phân hình học:
A.CH3CH=CHCH3 B.CH3CH=C(CH3)2
C.CH3CH=CHCH D. Cả A, B.
Câu 8: Alkene có đồng phân hình học?
A. pent-1-ene.
B. pent-2-ene.
C. 2-methylbut-2-ene
D. 3-methylbut-1-ene
Theo IUPAC, tên của một số alkene được gọi theo bảng sau:
ng 1.2. Tên thay thế của một số alkene
DẠYKÈMQUYNHƠNOFFICIAL
39
B. 5.
D.
B
Công thức cấu
ạo Công thức phân tử Tên thay thế CH2=CH2 C2H4 Etene CH2=CH‒CH3 C3H6 Propene CH2=CH‒CH2‒CH3 C4H8 but-1-ene CH2=C(CH3)2 C4H8 Methylpropene CH2=CH‒[CH2]2‒CH3 C5H10 pent-1-ene 2 2.1 CHƯƠNG 3.1 DẠNG 1: BÀI TẬP VỀ ĐỒNG PHÂN VÀ DANH PHÁP
ả
t
CH2=CH‒[CH2]3‒CH3
CH2=CH‒[CH2]4‒CH3
CH2=CH‒[CH2]5‒CH3
Cách gọi tên Alkene:
C6H12
C7H14
C8H16
hex-1-ene
hept-1-ene
oct-1-ene
Alkene không phân nhánh: Tên alkene = tên mạch chính + ene
Alkene phân nhánh:
Quy tắc:
Số chỉ vị trí ‒ Tên nhánh Tên mạch chính ‒ số chỉ vị trí ‒ đuôi ene
Mạch chính là mạch chứa liên kết đôi, dài nhất và có nhiều nhánh nhất.
Đánh số C mạch chính bắt đầu từ phía gần liên kết đôi hơn.
Sốchỉvịtríliênkếtđôighingaytrướcđuôi ene(khimạchchínhchỉ có 2hoặc 3 nguyêntử C thì không cần ghi).
Tên thông thường
- Xuất phát từ tên alkane có cùng số nguyên tử C bằng cách đổi đuôi –ane thành –ylene.
Bài tập vận dụng
Bài tập tự luận
Câu 1: Cho các chất : 2-methylbut-1-ene (1); 3,3-dimethylbut-1-ene (2); 3-methylpent-1-ene (3); 3-methylpent-2-ene (4); 3-methylbut-2-ene (5). Viết CTCT của các chất. Những chất nào là
đồng phân của nhau?
Câu 2: Viết các đồng phân cấu tạo và gọi tên alkene C5H10.
Câu 3: Hãy viết công thức cấu tạo và thu gọn nhất của các chất sau:
a) 2-methylbut-1-ene
Bài tập trắc nghiệm
b) isobutylene
c) 3-methylhex-2-ene

DẠYKÈMQUYNHƠNOFFICIAL
40
2.2 2.2.1 2.2.1 CHƯƠNG 3.1 DẠNG 1: BÀI TẬP VỀ ĐỒNG PHÂN VÀ DANH PHÁP
Câu 1: Alkene X có công thức cấu tạo: CH2C(CH3)=CHCH3. Tên của X là
A. isohexane.
B. 3-methylpent-3-ene
C.3-methylpent-2-ene.
D. 2-ethylbut-2-ene.
Câu 2: Tên theo danh pháp quốc tế của chất (CH3)2CHCH=CHCH3 là
A. 1-methyl-2-isopropyletene.
B.1,1-đimethylbut-2-ene.
C. 1-Isopropylpropene.

D.4-methylpent-2-ene.
Câu 3: Chất X có công thức CH3 –

CH(CH3) – CH = CH2. Tên thay thế của X là
A.2-methylbut-3-ene. B. 3-methylbut-1-ane.
C.3-methylbut-1-ene. D. 2-methylbut-3-ane
Câu 4: Hai alkene có CTPT là C3H6 và
C3H8 khi phản ứng với HBr thu được 3 sản phẩm, vậy 2 alkene là
A. propylene và but-1-ene.
B. propene và but-1-ene.
C. prooene và but-2-ene.
D. propene và but-2-ene.
Câu 5: Alkene X hợp nước tạo thành 3ethylpentane-3-ol. Tên của X là
A. 3-ethylpent-2-ene.
B. 3-ethylpent-3-ene.
C. 3-ethylpent-2-ene.
D. 2-ethylpent-2-ene.
Câu 6: Hydrocarbon nào sau đây khi phản
ứng với dung dịch bromo thu được 1,2dibromobutane?
A. But -1-ene. B. Butane.
C. But -2-ene. D. 2-methylpropene.
DẠYKÈMQUYNHƠNOFFICIAL
CHƯƠNG 3.1 DẠNG 1: BÀI TẬP VỀ ĐỒNG PHÂN VÀ DANH PHÁP
Sơ đồ tư duy về tính chất hóa học của alkene

Phản ứng trùng hợp
Là quá trình kết hợp liên tiếp nhiều phân tử
nhỏ giống nhau hoặc tương tự nhau tạo thành
những phân tử rất lớn (gọi là polyme).
Ví dụ:
nCH2=CH ��0 , ���� CH2-CH
CH3 CH3 n
Phản ứng oxi hóa
Phản ứng cháy
CnH2n + 3�� 2 O2 ��0 → nCO2 + nH2O
Phản ứng oxi hóa không hoàn toàn
3CnH2n + 2KMnO4 + 4H2O → 3CnH2n(OH)2 + 2MnO2+ 2KOH
Cộng hydro tạo ankan
Khi đun nóng có kim loại nickel (platin) làm xúc tác, anken kết hợp với hydro tạo thành ankan tương ứng.
CnH2n + H2 ��0 , ���� CnH2n+2
Ví dụ:
CH2=CH2 + H2 ����, ��0 CH3-
CH3
Cộng halogen X2 (Cl2, Br2)
CnH2n + X2 → CnH2nX2
Ví dụ:
CH2=CH2 + Br2(dd) → CH2BrCH2Br
Do anken làm mất màu dung dịch bromo nên người ta dung dung dịch bromo làm thuốc thử để nhận biết alkene và alkane.
Cộng HX
CnH2n + HX → CnH2n+1X
Nếu anken có cấu tạo không
đối xứng khi cộng HX có thể cho hỗn hợp hai sản phẩm.
Ví dụ:
CH3-CH=CH2 + HBr
CH3-CH2-CH2Br (spp)
CH3-CHBr-CH3 (spc)



DẠYKÈMQUYNHƠNOFFICIAL
42
1
C
ỦA ANKEN
TÍNH CHẤT HÓA HỌ
C
Phản ứng cộng CHƯƠNG 3.1 DẠNG 2: BÀI TẬP VỀ TÍNH CHẤT HÓA HỌC
Quy tắc Mac-côp-nhi-côp trong phản ứng cộng: Trong phản ứng cộng HX vào liên kết đôi, nguyên tử H (phần mang điện dương) chủ yếu cộng vào nguyên tử C bậc thấp hơn (có nhiều H hơn), còn nguyên hay nhóm nguyên tử X (phần mang điện âm) cộng vào nguyên tử C bậc cao hơn (ít H hơn).
Bài tập vận dụng
Bài tập tự luận
Câu 1: Viết phương trình hóa học của phản ứng xảy ra khi:
a. Propylene tác dụng với hydro, đun nóng (xúc tác Ni)

b. But-2-ene tác dụng với hyrdo chlororua.
c. Methylpropene tác dụng với nước có xúc tác acid
d. Trùng hợp but-1-ene.
Câu 2: Hoàn chuỗi phản ứng hóa học sau:
Câu 3: Trình bày phương pháp hóa học để:
a. Phân biệt methane và ethylene.

b. Tách lấy khí methane từ hỗn hợp ethylene
c. Phân biệt hai bình không dán nhãn đựng hexane và hex-1-ene.
Viết phương trình hóa học của phản ứng đã dùng.
Bài tập trắc nghiệm
DẠYKÈMQUYNHƠNOFFICIAL
43
2.1 2
CHƯƠNG 3.1 DẠNG 2: BÀI TẬP VỀ TÍNH CHẤT HÓA HỌC
2.2
Câu 1: Công thức tổng quát của Alkene
là:
A. CnH2n+2 (n≥0)
B. CnH2n (n≥2).
C. CnH2n (n≥3).
D. CnH2n-6 (n≥6).

Câu 2: Có thể nhận biết Alkene bằng cách:
A. Cho lội qua nước.
B. Đốt cháy.
C. Cho lội qua dung dịch axit.
D. Cho lội qua dung dịch nước bromo hoặc dung dịch KMnO4.
Câu 3: Một hydrocarbon mạch hở A tác dụng với HCl tạo ra sản phẩm có tên gọi là 2chloro-3-methyl butane Hydrocarbon đó có
tên gọi là:
A. 3-methyl but-1-en. B. 2-methyl but-1-en.
C. 2-methyl but-2-en. D. 3-methyl but-2-en.
Câu 4: Khi cho but-1-en tác dụng với dung dịch HBr, theo quy tắc Maccopnhicop sản phẩm nào sau đây là sản phẩm chính?
A. CH3–CH2–CHBr–CH2Br.
B. CH2Br–CH2–CH2–CH2Br.
C. CH3–CH2–CHBr–CH3.
D. CH3–CH2–CH2–CH2Br.
Câu 5: Mệnh đề nào sau đây là mệnh đề đúng?
A. Những hydrocarbon có 1 liên kết đôi trong phân tử là alkene.
B. Những hydrocarbon mạch hở, có 1 liên kết đôi trong phân tử là alkene.
C. Alkene là những hydrocarbon có liên kết ba trong phân tử.
D. Alkene là những hydrocarbon mạch hở có liên kết ba trong phân tử.
Câu 6: Oxi hóa ethylene bằng dung dịch
KMnO4 thu được sản phẩm là:
A. MnO2, C2H4(OH)2, KOH.
B. C2H5OH, MnO2, KOH.
C. K2CO3, H2O, MnO2.
D. C2H4(OH)2, K2CO3, MnO2
Câu 7: Đốt cháyhoàn toàn a gamhỗn hợp eten, propene, but-2-en cần dung vừa đủ b lít oxi đktc thu được 56,76 lít CO2 và 43,2g
nước. Giá trị b là?
A. 92,4 B. 94,2
C. 80,64 D. 24,9
Câu 8: Áp dụng quy tắc Maccopnhicop vào trường hợp nào sau đây?
A. Phản ứng cộng Br2 với alkene đối xứng.
B. Phản ứng trùng hợp của alkene.
C. Phản ứng cộng của HX vào alkene đối xứng
D. Phản ứng cộng HX vào alkene bất đối xứng.
DẠYKÈMQUYNHƠNOFFICIAL
44
CHƯƠNG 3.1 DẠNG 2: BÀI TẬP VỀ TÍNH CHẤT HÓA HỌC
Dạng 3.1: Phản ứng cộng X2, HX, H2O, H2
Phương pháp giải
PHƯƠNG PHÁP
Đối với cộng HX, X2 ta cần xác định tỉ lệ mol giữa HX, X2 với CxHy để từ đó => CTTQ
của hợp chất hữu cơ.
Giả sử với CnH2n: nX2 nCxHy =1
CnH2n+2: nX2 nCxHy >1
CnH2n-2: nX2 nCxHy <1

Đối với phản ứng cộng H2:
Số mol khí giảm sau phản ứng bằng số mol của C2H2 đã phản ứng.
Sau khi cộng H2 mà khối lượng mol trung bình của sản phẩm tạo thành nhỏ hơn 28 thì chắc
chắn có H2 dư.
Đề mẫu: Cho hydrocarbon X phản ứng với Bromo (trong dung dịch) theo tỉ lệ mol 1:1, thu
được chất hữu cơ Y (chứa a% Br về khối lượng). Khi X pư với HB thì thu được 2 sản phẩm hữu cơ khác nhau. Tìm tên gọi của X.
Bước 1: X phản ứng với Br2 theo tỉ lệ 1:1 hay ����2 ���������� =1 nên CTTQ của X là CnH2n CnH2n + Br2 CnH2nBr2
Bước 2: Sử dụng giả thuyết của đề để tìm n Theo đề: Trong sản phẩm Y có chứa a% Br về khối lượng thành phần của
n dụng
Câu 1: Cho hydrocarbon X có ứng dụng trong điều chế axit hữu cơ, keo dán, chất dẻo, tham gia phản ứng trùng hợp thu được polyme để chế tạo màng mỏng, bình chứa, ống dẫn nước. Khi cho hydrocarbon X phản ứng với bromo (trong dung dịch) theo tỉ lệ mol 1:1 thu được chất hữu
cơ Y (chứa 74,08% Br về khối lượng). Khi X phản ứng với HBr thì thu được 2 sản phẩm hữu cơ
khác nhau. Tìm tên gọi của X.
DẠYKÈMQUYNHƠNOFFICIAL
45
CnH2n là 100%a% Ta có: MBr.2 MCnH2n = %Br/hỗn hợp %CnH2n/hỗn hợp ↔ 80.2 14n = a% 100%-a% Tìm được n Tìm được X Gọi tên X. Bài tập vậ
1 1.1 .1 1.1
CHƯƠNG 3.1 DẠNG 3: BÀI TẬP TÍNH TOÁN
.1
Câu 2: Dẫn từ từ 3,36 lít hỗn hợp gồm ethylene và propylene (đktc) vào dung dịch bromo thấy dungdịchbịnhạt màuvàkhôngcókhíthoátra. Khốilượngdungdịchsauphảnứngtăng4,90gam.
a. Viết các phương trình hóa học và giải thích các hiện tượng ở thí nghiệm trên.
b. Tính thành phần phần trăm về thể tích của mỗi khí trong hỗn hợp ban đầu.
(Sau khi làm ra kết quả hãy quét thử mã QR dưới đây để xem có điều gì thú vị xuất hiện)

Câu 3: Methane và ethylene là hai hydrocaconbon điển hình lần lượt thuộc dãy đồng đẳng alkane và alkene, cả hai khí methane và ethylene đều có vai trò nhất định trong đời sống, methane là một thành phần chính của khí tự nhiên, khí dầu mỏ, khí bùn ao hay đầm lầy nên nó còn được gọi là khí đầm lầy và khí bùn, còn ethylene được biết đến là một chất sinh trưởng tự nhiên, không chỉ ethylene làm chín trái cây, thúc đẩy sự chín sớm của nhiều loại trái cây mà nó còn kích thích cho khoai tây sớm nảy mầm, làm cho dứa nhanh chóng ra hoa trái vụ, gây rụng lá ở một số loại cây, ... Trong một thí nghiệm, người ta cho 4,48 lít khí gồm methane và ethylene đi qua dung dịch bromo dư, thấy dung dịch nhạt màu và còn 1,12 lít khí thoát ra. Các thể tích khí đo ở điều kiện tiêu chuẩn. Thành phần phần trăm thể tích của khí methane trong hỗn hợp.
Câu 4: Cho H2 và 1 olefin (được ứng dụng trong phản ứng trùng hợp butilen thu được polyme để chế tạo màng mỏng, bình chứa, ống dẫn nước, ...) có thể tích bằng nhau qua Nickel nung nóng

ta thu được hỗn hợp A. Biết tỉ khối hơi của A với H2 là 23,2. Hiệu suất phản ứng hydro hóa là 75%.
Tìm CTPT của olefin.
Câu 5: Hỗn hợp khí X gồm H2 và một alkene có khả năng cộng HBr cho sản phẩm hữu cơ
DẠYKÈMQUYNHƠNOFFICIAL
nhấ
Tỉ khối của X so với H2 bằng 9,1. Đun nóng X có xúc tác Ni, sau khi phản ứng xảy ra

46
CHƯƠNG 3.1 DẠNG 3: BÀI TẬP TÍNH TOÁN
duy
t.
hoàn toàn, thu được hỗn hợp khí Y không
13. Tìm công thức cấu tạo của alkene.
Dạng 3.2: Phản ứng oxi hóa Ph
Phản ứng oxi hóa không hoàn toàn
Các alkene làm mất màu dung d
Bài tập vận dụng
Câu 1: Alkene A phản ứng hoàn toàn với dung dịch KMnO4 được chất hữu cơ B có MB = 1,81MA.
(Sau khi làm ra kết quả hãy quét thử mã QR dưới đây để xem có điều gì thú vị xuất hiện)


Câu 2: Để khử hoàn toàn 200 ml dung dịch KMnO4 0,2M tạo thành chất rắn màu nâu đen
cần V lít khí C2H4 (đktc). Giá trị tối thiểu của V.
Câu 3: Đốt cháy hoàn toàn 2,24 lít (đktc) 1 hydrocarbon X mạch hở, sau đó dẫn sản phẩm

cháy lần lượt qua dung dịch H2SO4 và dung dịch Ca(OH)2 dư. Sau thí nghiệm thấy khối lượng
bình đựng dung dịch axit tăng 5,4g, bình đựng dung dịch Ca(OH)2 có 30g kết tủa. Tìm CTPT của
DẠYKÈMQUYNHƠNOFFICIAL
47
mất màu nướ
ủ
với H2 bằng
làm
c bromo; tỉ khối c
a Y so
ng gặp trong dạng này
ồ
ản ứng thườ
g
m:
ị
KMnO4. Phản ưng này dùng để phân biệt alkene và alkane 3CnH2n + 2KMnO4 + 4H2O → 3CnH2n(OH)2 + 2MnO2 + 2KOH
ch
ả
ứng đốt cháy)
C
H2n + 3�� 2 O2 ���� → nCO2 + nH2 (������2 = ����2��)
Phản ứng oxi hóa hoàn toàn (ph
n
n
2
CHƯƠNG 3.1 DẠNG 3: BÀI TẬP TÍNH TOÁN
X.
2.1
Khối lượng bình đựng dung dịch axit H2SO4 là
khối lượng H2O (Dung dịch H2SO4 có tính háo
nước) Tính được số mol của H2O
Từ giả thuyết dẫn sản phẩm cháy qua bình đựng dung dịch Ca(OH)2 dư và thấy 30 (g) kết tủa xuất
hiện Tìm được số mol CO2 (vì CO2 phản ứng với Ca(OH)2 dư).
Từsố mol H2O và số mol CO2 TìmđượcCTPT của X.
Câu 4: Alkene X được biết đến với đặc tính kích thích sự sinh trưởng của các tế bào thực vật, vì vậy alkene X được ứng dụng vào mục đích làm tăng trưởng kích thước cây trồng, đồng thời khích thích ra hoa ở các loại cây ăn trái. Người ta làm một thí nghiệm với alkene X bằng cách dùng nhiệt đốt cháy hoàn toàn 0,1 mol alkene X thu được CO2 và hơi nước. Hấp thụ hoàn sản phẩm bằng 100g dung dịch NaOH 21,62%, thu được dung dịch mới trong đó nồng độ NaOH chỉ

còn 5%. Tìm CTPT đúng của X.


Gọi công thức phân tử của alkene cần tìm: CnH2n (n≥2)
Sử dụng dữ kiện nồng độ NaOH chỉ còn 5% (nghĩa khối lượng NaOH còn dư trong khối lượng dịch sau phản ứng là 5%) để tìm được n Tìm
được CTPT của X
mNaOH dư = mNaOH ban đầu – mNaOH phản ứng
mdd sau phản ứng = ������2 + ����2�� + mdd NaOH
Câu 5: Alkene và dẫn xuất của alkene là nguyên liệu cho nhiều quá trình sản sản xuất hóa học ví dụ như ethylene, propylene, butilen được dùng làm chất đầu tổng hợp các polyme có nhiều ứng dụng. Trong một thí nghiệm người ta đốt cháy hoàn toàn 8,96 lít (đktc) hỗn hợp 2 alkene là đồng



















đẳng liên tiếp thu được m gam nước và (m+39) gam CO2. Tìm CTPT của alkene đó.
Gọi CTPT trung bình của 2 alkene ������2��
Từ dữ kiện tiếp thu được m gam nước và (m+39) gam CO2 để tìm ��.
������2 - ����2�� = m+39 – m (Từ dữ kiện đề bài kết hợp viết phương trình phản ứng đốt cháy để đưa
������2 và ����2�� theo ẩn ��)
Vì 2 anken là đồng đẳng liên tiếp nên từ �� tìm ra
được CTPT của anken cần tìm.
DẠYKÈMQUYNHƠNOFFICIAL
48
CHƯƠNG 3.1 DẠNG 3: BÀI TẬP TÍNH TOÁN
HYDROCARBON KHÔNG NO
Chương 3.2: ALKYNE








Hệ thống bài tập: Gồm 3 dạng cơ bản
Dạng 1: Bài tập về đồng phân và danh pháp

Dạng 2: Bài tập về tính chất hóa học
Dạng 3: Bài tập tính toán

DẠYKÈMQUYNHƠNOFFICIAL
49









































































