11 minute read
Bioaktív rezin újszerű alkalmazási lehetőségei perforációk, gyökér-reszorpciók és endo-parodontális léziók ellátása során
Dr. Marta Maciak (Lengyelország) BIOAKTÍV REZIN ÚJSZERŰ ALKALMAZÁSI LEHETŐSÉGEI PERFORÁCIÓK, GYÖKÉR-RESZORPCIÓK ÉS ENDOPARODONTÁLIS LÉZIÓK ELLÁTÁSA SORÁN
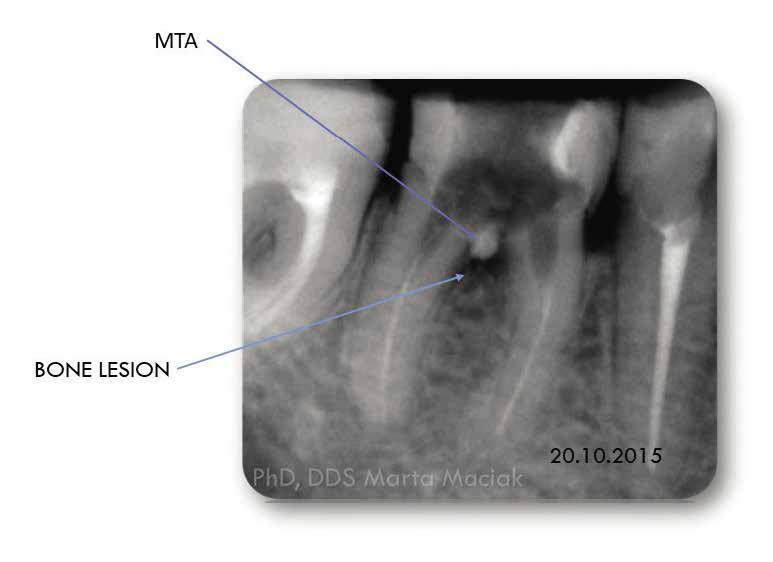
1. ábra
Advertisement
Bevezetés
Az elmúlt évtizedben nagyon sok figyelmet fordítottak az úgynevezett bioaktív anyagok fejlesztésére. Annak érdekében, hogy jobban megértsük ezen anyagok működési elvét, valamint elkerülhessük, hogy a hatásmechanizmusuk téves ismerete miatt hibás következtetéseket vonjunk le, szükség van a rendelkezésre álló szakirodalmi adatok rövid áttekintésére és a kapcsolódó fogalmak tisztázására. Jelenleg már több, olyan fogászati anyag érhető el a kereskedelmi forgalomban, amelyet bioaktív anyagként tartunk számon. Többek között az összes fluorid leadásra képes anyag, a kalcium-szilikát és a kalcium-aluminát alapú cementek, továbbá a kalciumalapú vagy kalciumtartalmú anyagok. Az implantológia területén bioanyagokkal dolgozó kutatók a bioaktív jelzőt olyan anyagokra használják, amelyek biomineralizált felszínen keresztül kapcsolódnak egymáshoz. Úgy tűnik, hogy jelenleg nincs egyetértés a fogorvoslás területén dolgozó szakemberek (kutatók, fogorvosok, iparági képviselők) között, hogy melyik anyagokat lehet megalapozottan bioaktívnak vagy biomineralizáló hatásúnak nevezni, valamint abban sem értenek egyet, hogy milyen fokú biomineralizációt lehet elérni fogászatban használt anyagokkal. 1 A bioaktivitást többféleképpen lehet értelmezni, és ennek megfelelően több eltérő definíció is született a leírására. Az alábbiakban egy általános, széles körű értelmezést lehetővé tevő definíció olvasható: Egy olyan anyag, amelynek lehet biológiai hatása, vagy egy olyan anyag, amely biológiailag aktív, és kapcsolatot hoz létre az élő szövetekkel.2 Az irányított szövettervezés (tissue engineering) területén azokat az anyagokat nevezik bioaktívnak, ame-

4. ábra 5. ábra
lyek képesek olyan biológiailag aktív molekulák és ionok felszabadítására, amelyek sejtszintű változásokat tudnak indukálni. Ilyen anyagokra példa az irányított lágy- és keményszövet tervezés során is alkalmazott különböző bioaktív üvegek. 3,4 Ezen felül a bioaktív üvegek bioaktív tulajdonságait főemlősökön végzett pulpasapkázások hatásait vizsgáló kísérletek során is igazolták.5
Az orvostudomány területén bioaktívként tekintünk minden anyagra, ami hatással van az élő sejtekre vagy szövetekre. Ezáltal a gyógyszerek hatóanyagai is ebbe a csoportba tartoznak. A bioanyagokkal foglalkozó tudományterületen – a biokerámiákra és a bioaktív üvegekre vonatkoztatva –, egy anyag bioaktivitása általában azt jelenti, hogy az anyag képes a felszínén in vitro és in vivo körülmények között is hydroxiapatit kristályok formázására. 6 Ezen a ponton fel kell tennünk a következő elméleti kérdést: Bioaktívnak tekinthetjük-e azt az anyagot, amely ionokat ad le a biomineralizáció megindításához, vagy az a felszín számít igazából bioaktívnak, ahol a biomineralizáció lejátszódik? A fogászati anyagokkal kapcsolatban a bioaktivitás arra utal, hogy ezek az anyagok képesek olyan reakciók elindítására, amelyek során a dentin felszínéhez specifikus reakciók révén mineralizált kapcsolatot alakítanak ki. 7 Lööf és mtsai. másként definiálták a bioaktivitás fogalmát: „Egy kerámiaalapú anyag esetében a bioaktivitás a kerámia felszínének egy olyan tulajdonságát jelenti, ami lehetővé teszi, hogy közvetlen, kötőszöveti réteg nélküli kapcsolat alakuljon ki az anyag és az élő szövetek között”.8 Egy másik definícióban az alábbiak szerint határozták meg a bioaktivitás fogalmát: „Bioaktív az az anyag, amely szervetlen foszfátionok jelenlétében a felületén egy apatitszerű felszíni réteget alakít ki.”9 Az utóbbi definíció szerint az ACTIVA BioACTIVE-RESTORATIVE és az ACTIVA BioACTIVE-BASE/LINER (Pulpdent) tulajdonságai alapján bioaktív hatással rendelkezik. Az ACTIVA BioACTIVE termékei az első olyan fogászatban alkalmazott rezinek, amelyek bioaktív ionos rezin mátrixszal rendelkeznek. A mátrix tartalmaz egy rugalmas erőelnyelő rezinkomponenst, és a saját foganyag fizikai és kémiai tulajdonságait utánzó üvegionomer töltőanyagszemcséket is. Ezek a bioaktív anyagok aktív részesei azoknak az ioncsere folyamatoknak, amelyek szabályozzák a fogak felszínén és a nyálban lezajló kémiai folyamatokat, és hozzájárulnak a fogak keményszöveteinek szerkezeti integritásához és a szájüreg egészségének a megőrzéséhez. Az ACTIVA egyszerre rendelkezik a rezintartalmú kompozitok ellenálló képességével, esztétikai és fizikai tulajdonságaival, és

8. ábra 9. ábra
ezen felül kifejezettebb bioaktív tulajdonságokkal bír, mint az üvegionomer cementek.10 Az ACTIVA hatékonyan biztosítja a fogak mikroszivárgással szembeni védelmét11,12, és képes nagy mennyiségű kalcium-, foszfát- és fluoridion hosszan tartó folyamatos leadására és felvételére, ami hosszú távú előnyöket biztosít a páciensek számára. Az Amerikai Egyesült Államokban az ACTIVA-t – az első bioaktív rezinalapú anyagként – már elismerték bioaktív hatású készítményként. A cikk szerzője az ásványi trioxid aggregátum (mineral trioxide aggregate, MTA) and Biodentine (Septodont) helyett az ACTIVA BioACTIVE-RESTORATIVE-ot és ACTIVA BioACTIVE-BASE/LINER-t használt bizonyos endodonciai, valamint más jellegű beavatkozások során. Erre a fent említett anyagok stresszelnyelő és a töréssel szembeni ellenálló képességet növelő és szabadalmaztatott rugalmas rezinkomponens által biztosított erősség és terhelhetőségnek köszönhetően volt lehetőség. A cikkben bemutatott esetek ellátása során az ACTIVA BioACTIVE-BASE/LINER-t a gyártó által meghatározott indikációs területein kívül eső beavatkozások elvégzésére használtuk. Az ellátásra kerülő fogak hosszú távú megtarthatóságának az esélye alacsony volt, sőt a klinikai helyzet alapján a fogak eltávolítása (majd később egy implantátummal történő pótlása) megfelelően alátámasztott terápiás lehetőségnek mutatkozott. Tehát az ACTIVA BioACTIVE-BASE/LINER cikkünkben bemutatott felhasználási területe nem tartozik a gyártó által meghatározott beavatkozások körébe, továbbá a cikk szerzője ezeket csak azután végezte el, hogy a páciensekkel részletesen ismertette a kezelés lehetséges előnyeit és hátrányait.
Esetbemutatás
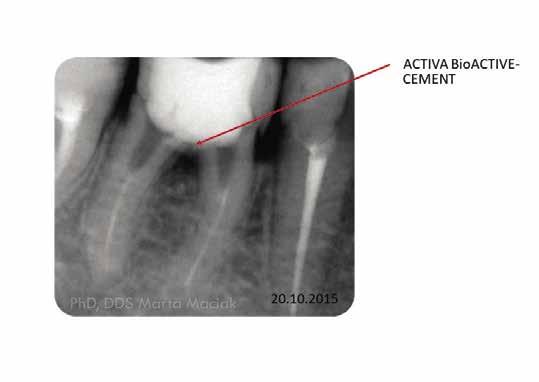
1. eset Egy 28 éves hölgypácienst a jobb alsó első nagyőrlőfogából (4.6) kiinduló fájdalom miatt utalták be a rendelőnkbe. A beutalón feltüntették, hogy a pácienst endodoncia kezelés céljából irányítják hozzánk, valamint, hogy korábban perforáció történt, amit MTA-val zártak. A páciens jelentős fájdalomról számolt be, ami rágás és a fogsorok zárása közben jelentkezett. Az anamnézisében nem szerepelt semmilyen kontraindikáció, ami ellenjavalttá tette volna a fogászati kezelés megkezdését. A klinikai vizsgálat során megállapítottuk, hogy a 4.6-os fogában egy ideiglenes tömés található. A 2015. október 20-án a fent jelölt fogról készült periapikális felvételen jól látható, hogy a furkációnak megfelelően MTA extrudálódott a periodontális térbe, valamint egy csontdefektus jelenléte is nyilvánvalóvá vált (1. ábra). A röntgenfelvétel kiértékelése során a pulpakamra aljának perforációját sikerült megállapítani. Az ideiglenes tömés eltávolítását követően nagy mennyiségű purulens exudátum jelent meg a pulpakamrában. A purulens váladék és az MTA eltávolítását követően a furkációt átöblítettük metronidazollal (folyadék, Polpharma) és 2%os klórhexidin-nel (Cerkamed). A perforáció határain frissen vágott dentint hoztunk létre egy karbidfúró segítségével, majd a pulpakamra teljes belső felszínét 10 másodpercig 37,5%-os orthofoszforsavval fedtük, melyet a behatási idő elteltét követően alaposan leöblítettünk. A perforációs nyíláson keresztül egy kollagén mátrix darabot helyeztünk a csontfelszínre (ANTEMA, Molteni Dental), hogy ezzel védjük a csontot, valamint, hogy megfelelően alátámasszuk az applikálni kívánt ACTIVA Bio-ACTIVE-BASE/LINER réteget. A kollagén mátrix darab nem ad röntgenárnyékot, ezért nem látható a röntgenfelvételen. A gyökércsatorna-bemeneti nyílásokat vattagombócokkal zártuk, majd a pulpakamra teljes belső felszínét bonddal fedtük (DenTASTIC UNO, Pulpdent). A bond megvilágítását követően a pulpakamra alját teljesen befedtük ACTIVA BioACTIVE-BASE/LINER-rel (2. ábra). A fogat hosszú távú ideiglenes ellátásként GIZ üvegionomer (Ihde Dental) töméssel láttuk el. A páciens két nap múlva a panaszok megszűnéséről számolt be. A beavatkozás után 14 nappal készült kontroll röntgenfelvételen (2015. november 3.) megfigyelhettük a csontos regeneráció jeleit, a furkáció területének megfelelően (3. ábra).
2. eset Egy 16 éves férfi pácienst a bal felső nagymetszőjén (2.1) kialakult reszorpció kezelése céljából utalták a rendelőnk-

10. ábra 11. ábra
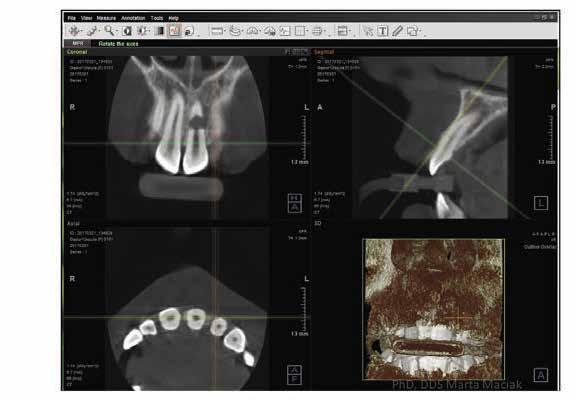
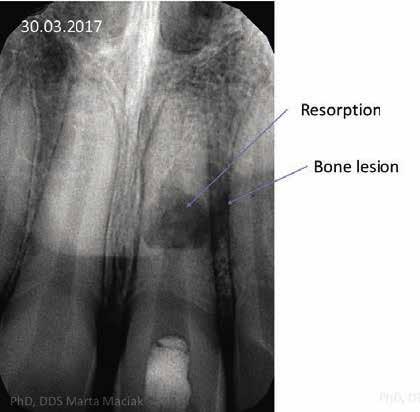
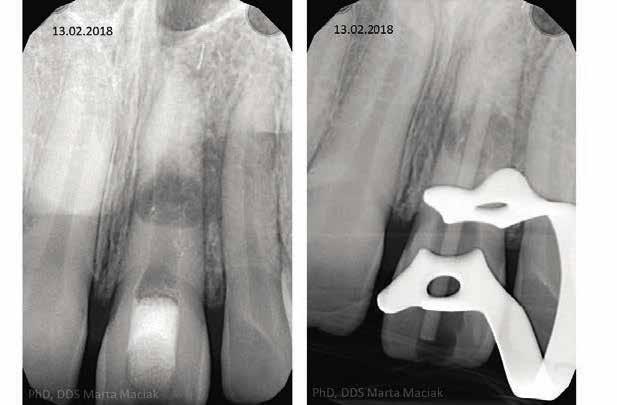
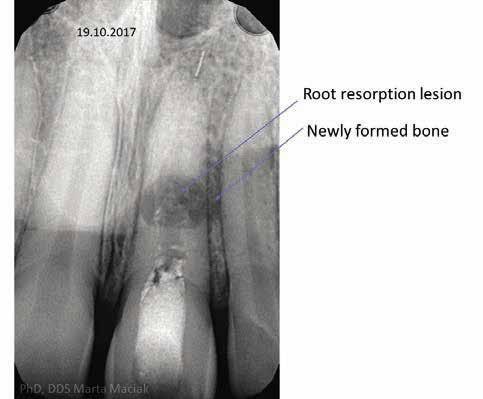
be. A 2017. március 30-án készül röntgen- és CBCT felvételeken egyértelműen igazolható volt a reszorpció jelenléte, valamint lokalizálható volt az elhelyezkedése és a kiterjedése. A pulpakamra ideiglenes tömőanyaggal volt feltöltve és lezárva. A páciens anamnézisében nem találtunk semmi kiemelendőt. A vizsgálatot követően a fent jelölt fognál belső- és külső reszorpció diagnózist állítottunk fel. Az ideiglenes tömés eltávolítását követően láthatóvá vált, hogy a gyökércsatornát granulációs szövet tölti ki. Annak ellenére sikerült a gyökércsatornát a teljes munkahossznak megfelelően szondázni, hogy a gyökércsatorna apikális harmada kalcifikálódott. A gyökércsatorna feltágítását a Self-Adjusting File (SAF) System-mel (ReDent NOVA) és az XP-endo Finisher-rel (FKG Dentaire) végeztük el. Átöblítésre 5,25%-os nátrium-hypokloritot (NaClO), 17% EDTA-t (Cerkamed) és metronidazol-t (Polpharma) használtunk. A gyökércsatornában lévő gyulladásos szövet miatt az első ülést követően a Dexadent-tel (Chema-Elektromet) töltöttük fel a csatornát, és egy hétre ideiglenesen zártuk. A végső ülést megelőző kezelések során a gyökércsatornát 40%-os citromsavval (Cerkamed) és 2%-os klórhexidinnel (Cerkamed) öblítettük át, a mechanikai megmunkálást pedig a SAF System-mel és az XP-endo Finisher-rel végeztük. A köztes ülések végén a gyökércsatornát 2%-os klórhexidinnel kevert Multi-Cal-lal (Pulpdent) töltöttük fel, majd ideiglenesen zártuk. A kezdetben ezt a gyógyszeres zárást kéthetente cseréltük annak érdekében, hogy elősegítsük a granulációs szövet eltávolítását, továbbá stimuláljuk a csont regenerációját. A kezelés megkezdését követő 7. hónapban készült röntgen- (6. ábra) és CBCT-felvételeken, valamint a nagy nagyítás mellett végzett obszerváció során a csontban lévő lézió méretének csökkenését tudtuk megfigyelni. Az utolsó ülésre a kezelés megkezdését követő 11 hónap után került sor (7. ábra). A kezelés során a gyökércsatornát XP-endo Finisher-rel munkáltuk meg, és EDTA-val, valamint 2%-os klórhexidinnel öblítettük át. A reszorpciós területnek megfelelően egy kollagén mátrix darabot (Antema) helyeztünk a gyökércsatornába, hogy megfelelően alá tudjuk támasztani az ACTIVA BioACTIVE CEMENT-et, hogy elkerülhessük ennek az anyagnak a gyökér külső felszínére kerülését, illetve a csontállománnyal történő érintkezését. Ezt követően a gyökércsatorna belső felszínét bonddal kezeltük (All-Bond Universal, Bisco), és megvilágítás nélkül egy puszter segítségével kis erősségű levegőbefújással elvékonyítottuk, majd a gyökércsúcstól kezdve egészen a pulpakamráig feltöltöttük ACTIVA BioACTIVE-BASE/LINER-rel. Az ACTIVA-val történő feltöltést követően közvetlenül egy üvegszálas csapot (Cytec blanco, Hahnenkratt) helyeztünk a gyökércsatornába. Ezt követően 20 másodpercet vártunk, majd három irányból 20-20 másodpercen keresztül megvilágítottuk. A végeredményt a 2018. február 13-án készült kontroll röntgenfelvételen lehet megfigyelni (8. ábra.). A rezorbeálódott területnek megfelelően a csontállomány teljes regenerációját sikerült elérni. A behelyezett üvegszálas csap jól látható a röntgenfelvételen, de a kollagén mátrix, valamint az ACTIVA BioACTIVE CEMENT nem rendelkezik elegendő radioopacitással, hogy megfigyelhető legyen.
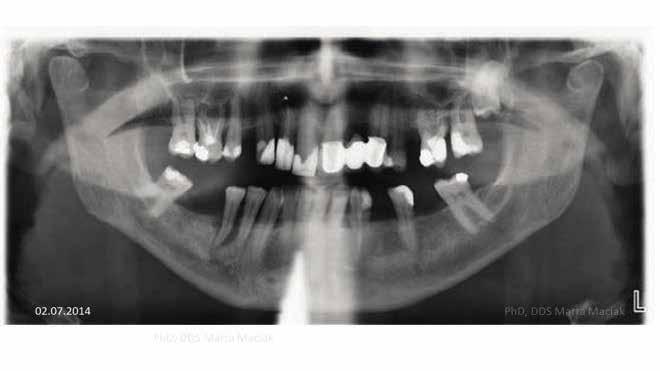
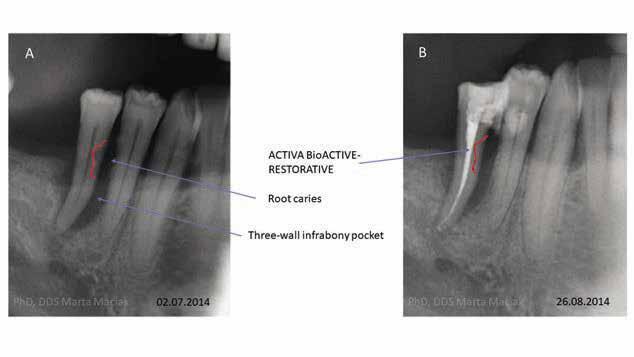
3. eset Egy 63 éves hölgypáciens fogászati kezelés céljából kereste fel a rendelőnket. A vizsgálat során panoráma röntgenfelvétel készült. A páciens hiányos, részben helyreállított fogazattal rendelkezett. A szájüregében láthatóak voltak szólókoronák és egy háromtagú híd is, valamint megállapítottuk, hogy mindkét fogívében több foghiány van. A páciens a jobb alsó premoláris régióból eredő fájdalomra panaszkodott. Az anamnézis felvétel során nem derült fény bármilyen olyan kontraindikációra, amely a fogászati kezelésének megkezdését nem javasolná. A páciensnek a jobb alsó második kisőrlőfogának (4.5) eltávolítását javasoltuk. A hölgy jelezte, hogy a fog eltávolítását el szeretné kerülni, és érdeklődött, hogy elérhető-e olyan terápia, amivel, akár ideiglenesen is, de meg lehet kísérelni a fog megtartását. A páciens beleegyezett a felajánlott kezelési tervbe, és megértette, hogy a kívánt eredmény elérése nem garantálható. A klinikai vizsgálat során a fent jelölt fog melletti tasakból genny ürült, valamint a fog III. fokú mobilitást mutatott. A röntgenfelvételen egy gyökércsúcsig érő háromfalú csonttasakot figyeltünk meg (10/a. ábra). A vizsgálatot követően periodontitis periapicalis chronica purulenta és
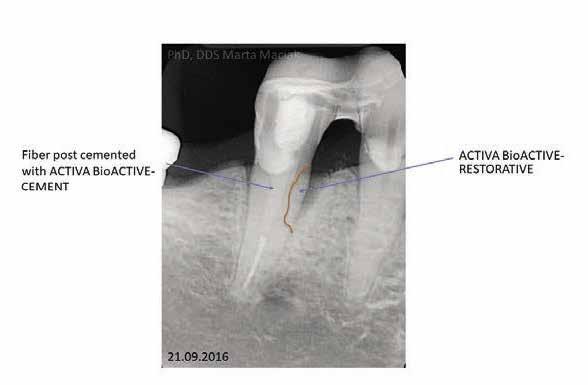
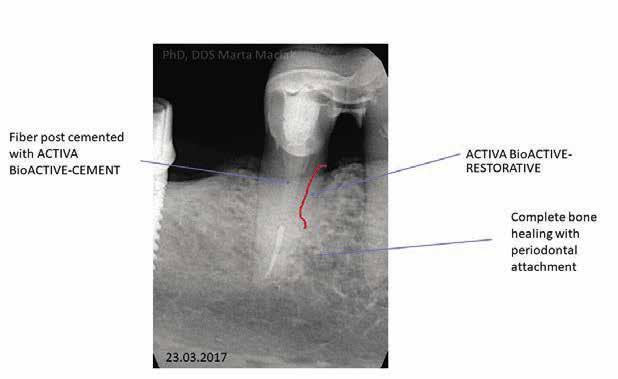
12. ábra 13. ábra
mesialis gyökércaries diagnózisokat állítottunk fel. A panoráma röntgenfelvétel elkészítését és a polimeráz-láncreakció (realtime polymerase chain reaction; PET test, PET Plus, MIP Pharma) elvégzését követően megkezdtük a kombinált endodonciai és parodontológiai terápiát. Az endodonciai beavatkozások megkezdésére 2014. július 2-án került sor. A gyökércsatornát 25.04-es méretű HyFlex eszközzel (COLTENE) és a SAF System segítségével tágítottuk fel. A feltágítást követően levezettük a gyökércsatornában megjelenő gennyes exudátumot, majd ezt követően 5,25%-os nátrium-hipoklorittal (NaOCl) és metronidazole oldattal átöblítettük. Az átöblítés után a gyökércsatornát Dexadent pasztával feltöltöttük, és 1 hétig ideiglenesen zártuk. A kezelés költségeinek csökkentése érdekében nem végeztünk csontpótlást, csak egy alapos kürettálás történt.
Okkluzális irányból történő üregalakítást követően, az elkészült kavitást feltöltöttük ACTIVA BioACTIVE-RESTORATIVE-vel, majd az approximálisan elhelyezkedő kisőrlőhöz síneztük üvegszálas szalag és ACTIVA segítségével (10. b ábra). A sín felhelyezésével az volt a célunk, hogy stabilizáljuk a III. fokú mobilitással rendelkező fogat, valamint, hogy így optimálisabb körülményeket biztosítsunk a csontos regeneráció számára. Néhány nap múlva a páciens a fájdalmak megszűnését jelezte, valamint a továbbiakban a gyökércsatornában nem volt genny detektálható. 2014. július 10-én a gyógyszeres gyökértömést eltávolítottuk, majd a gyökércsatornát 2%-os klórhexidinnel kevert Multi-Cal-lal (Pulpdent) töltöttük fel, majd 2 hétre ideiglenesen lezártuk. Két hét elteltével a SAF System, valamint 40%-os citromsav és desztillált víz segítségével a Multi-Cal-t eltávolítottuk. Ezt követően a gyökércsatornát átöblítettük 2%-os klórhexidinnel (CHX), majd kiszárítottuk. Egy kloroformmal lágyított mesterpoént helyeztünk a csatornába, sealerként pedig GuttaFlow-t (COLTENE) használtunk. A gyökércsatorna apikális harmadát vertikális meleg kondenzációs technikával zártuk. A gyökércsatorna többi részét pedig a continuous wave technikát alkalmazva töltöttük fel guttaperchával. A kezelés sikerességének megállapítását a következő kezeléstől tettük függővé. Az obszervációs időszak alatt további regenerációt figyelhettünk meg a csontdefektusnak megfelelően (11. ábra). Három hónap múlva a gyökércsatornában lévő guttapercha részleges eltávolításra került. A gyökércsatorna belső felszínét megsavaztuk, majd lemosást és szárítást követően bonddal fedtük (All-Bond Universal). A csatornát ACTIVA CEMENT-tel feltöltöttük, majd ezt követően egy üvegszálas csapot helyeztünk a gyökércsatornába. Megközelítőleg 20 másodperc várakozást követően megkezdtük a csap megvilágítását (12. ábra). A kezelés befejezését követően 3 évvel készült kontroll röntgenfelvételen jól megfigyelhető a csontállomány teljes regenerációja, valamint a gyökérhártya-rés is fiziológiás állapotban látható.
Összegzés
A jelenleg elérhető szakirodalmi adatokra, az ACTIVA BioACTIVE anyagok hatékonyságát megalapozó kezdeti sikereket bemutató cikkekre, az anyagok pH-jára, a kalcium- és foszfátionok leadási képességére, valamint a nyálas közegben történő apatitképző hatására alapozva úgy döntöttünk, hogy megpróbáljuk tapasztalati úton kibővíteni az anyag indikációs körét. Annak ellenére, hogy az egyik bemutatott eset ellátása során sem tudtuk a pozitív végeredményt garantálni, legalább három, de egyes eseteknél több mint 3 év távlatából is úgy tűnik, hogy sikeres volt a kezelésünk. Ezek igazolják, hogy az ACTIVA BioACTIVE anyagok bioaktív hatással rendelkeznek, és az osteoblast stimuláló, valamint apatitképző hatásuk miatt – megfelelő körülmények között – hatékonyan alkalmazhatóak a kezelési céljaink elérésére. Ezt a cikkünkben bemutatott CBCT- és röntgenfelvételeken megfigyelhető csontos regenerációval tudjuk egyértelműen alátámasztani. Annak ellenére, hogy nem rendelkezünk szövettani eredményekkel, a periodoncium klinikai és radiológiai vizsgálata a tapadás létrejöttét igazolja az itt bemutatott eseteknél.
(A cikk megírása során felhasznált szakirodalmi hivatkozások listája a szerkesztőségünkben elérhető.) Forrás: Roots 2018/4








