2 minute read
Cuestionario
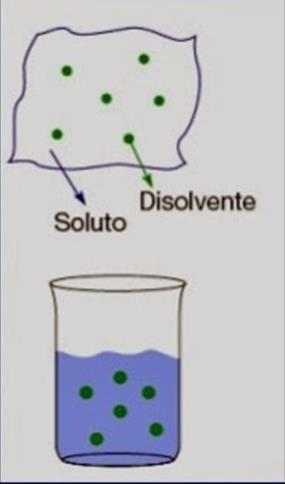
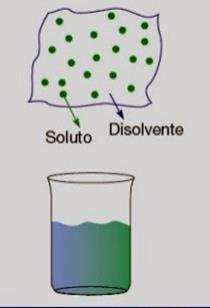
a) ¿Cuáles son los componentes de una disolución?
Fase dispersa (soluto) se disuelve y se encuentra en menor proporción. Fase dispersante (disolvente) es el que se disuelve y se encuentra en mayor porción.
Advertisement
b) ¿Cuáles son las propiedades de una disolución?
Varían según el tamaño de las partículas que la forman, se clasifican en verdaderas, coloides y finas.
c) ¿Qué factores determinan el estado físico de una disolución?
Tamaño de partículas, temperatura, presión y agitación.
b) ¿Por qué se le considera al agua disolvente universal?
Porque el agua disuelve gran cantidad de componentes orgánicos de carácter polar e iónico debido a su estructura química molecular de carácter polar.
e) ¿Cómo se define la solubilidad?
A la capacidad que tiene una sustancia determinadas condiciones. para disolverse en un disolvente bajo
f) ¿Cómo se clasifican las disoluciones de acuerdo a la solubilidad del soluto en el disolvente?
El término de concentración de una disolución expresa la cantidad de soluto disuelto, determinada la cantidad de disolvente. Se clasifican en 2: Empírica y diluida.
g) ¿Por qué el hexano disuelve al benceno pero no al cloruro de sodio?
Porque el hexano y el benceno son componentes polares, mientras que el cloruro de sodio es un compuesto polar.
h) Menciona y describe brevemente los factores que afectan a la solubilidad.
Tamaño de partícula de soluto: La solubilidad se ve favorecida cuando las partículas del soluto están finamente divididas. Temperatura: Un aumento de temperatura del sistema incrementa la energía, con lo que se favorece en su movimiento. Presión: Afecta a la solubilidad de un gas en el agua, a mayor presión, mayor solubilidad. Agitación: Permite acelerar la difusión de las partículas del soluto entre las moléculas de agua.
DESCRIPCIÓN
I N S A T U R A D A
Es un compuesto químico que contiene enlaces carbono-carbono dobles o triples, como los que se encuentran en los alquenos o alquinos, respectivamente. Precisamente, el número de enlaces dobles y triples de un compuesto nos indica su grado de insaturación
S O B R E S A T U R A D A
El término sobresaturación se refiere a una solución que ha pasado el límite de soluto que el solvente puede admitir, por lo que este exceso de soluto aparece como un precipitado. También se puede referir a un vapor de un compuesto que tiene mayor presión parcial que la presión de vapor de ese compuesto.
S A T U R A D A
Puede referirse a un compuesto saturado, formado por moléculas orgánicas que no contienen dobles enlaces ni triples enlaces carbono-carbono. Una disolución saturada, es aquella que contiene la mayor concentración de soluto posible en un volumen de disolvente dado y para cierta temperatura.