
Outros títulos de interesse
Dietoterapia nas Doenças do Adulto, 2a Ed. Aline Marcadenti de Oliveira Flávia Moraes Silva
Fisiopatologia da Nutrição e Dietoterapia Carla de Oliveira Barbosa Rosa Helen Hermana Miranda Hermsdorff

Imunologia Aplicada à Nutrição Mariana Grancieri Hércia Stampini Duarte Martino
Interpretação de Exames Laboratoriais Aplicados à Nutrição Clínica Larissa Calixto-Lima Nelzir Trindade Reis
Nutrição Clínica – Bases para Prescrição Nelzir Trindade Reis Larissa Calixto-Lima
Nutrição Clínica no Dia a Dia, 2a Ed. Larissa Calixto-Lima Maria Cristina Gonzalez
Nutrição em Cardioendocrinologia Aline Marcadenti de Oliveira Gabriela Corrêa Souza
Terapia Nutricional em UTI, 2a Ed. Diogo Toledo Melina Castro Saiba mais sobre estes e outros títulos em nosso site: www.rubio.com.br
Organizadoras
Aline Pereira Pedrosa
Nutricionista.
Doutorado em andamento em Ciências Nutricionais pela Universidade Federal do Rio de Janeiro (UFRJ). Mestre em Nutrição Clínica pela UFRJ.
Especialista em Nutrição Oncológica pelo Instituto Nacional de Câncer/Ministério da Saúde (Inca/MS) – Programa de Residência Multiprofissional em Oncologia.
Taiara Scopel Poltronieri
Nutricionista.
Doutorado em andamento em Endocrinologia pela Universidade Federal do Rio Grande do Sul (UFRGS). Especialista em Nutrição Oncológica pelo Instituto Nacional de Câncer/Ministério da Saúde (Inca/MS) – Programa de Residência Multiprofissional em Oncologia.
Especialista em Nutrição Clínica pela Universidade Municipal de São Caetano do Sul (USCS), SP.
Emanuelly Varea Maria Wiegert
Nutricionista.
Doutora em Ciências Nutricionais pela Universidade Federal do Rio de Janeiro (UFRJ). Mestre em Nutrição Humana pela UFRJ.
Especialista em Nutrição Hospitalar pela Universidade Federal de Mato Grosso (UFMT). Membro da Academia Nacional de Cuidados Paliativos (ANCP).
Nutricionista do Instituto Nacional de Câncer/Ministério da Saúde (Inca/MS).
Larissa Calixto‑Lima
Nutricionista.
Doutora em Alimentação, Nutrição e Saúde pela Universidade do Estado do Rio de Janeiro (UERJ). Mestre em Alimentação, Nutrição e Saúde pela UERJ.
Especialista em Nutrição Clínica – Cirurgia Geral e Transplante Hepático pelo Programa de Residência do Hospital Universitário Oswaldo Cruz (HUOC).
Especialista em Nutrição Parenteral e Enteral pela Sociedade Brasileira de Nutrição Parenteral e Enteral (Braspen).
Nutricionista do Instituto Nacional de Câncer/Ministério da Saúde (Inca/MS).
Nutrição Oncológica no Dia a Dia
Copyright © 2023 Editora Rubio Ltda. ISBN 978‑65‑88340‑44‑8
Todos os direitos reservados. É expressamente proibida a reprodução desta obra, no todo ou em parte, sem autorização por escrito da Editora.
Produção Equipe Rubio Capa Bruno Sales Imagens de capa iStock.com/bit245/FatCamera
Diagramação Estúdio Castellani
CIP‑BRASIL. CATALOGAÇÃO NA PUBLICAÇÃO SINDICATO NACIONAL DOS EDITORES DE LIVROS, RJ
R175o
Nutrição Oncológica no Dia a Dia/organizadoras Aline Pereira Pedrosa, Taiara Scopel Poltronieri, Emanuelly Varea Maria Wiegert; Larissa Calixto Lima. – 1. ed. – Rio de Janeiro: Rubio, 2023. 236p.; 21cm. Inclui bibliografia ISBN 978 65 88340 44 8
1. Nutrição. 2. Câncer – Paciente – Cuidado e tratamento. 3.Oncologia – Cirurgia. I. Pedrosa, Aline Pereira. II. Poltronieri, Taiara Scopel. III. Wiegert, Emanuelly Varea Maria. IV. Calixto Lima, Larissa.
18 53126
Editora Rubio Ltda. Av. Franklin Roosevelt, 194 s/l 204 – Centro 20021‑120 – Rio de Janeiro – RJ Telefone: +55(21) 2262‑3779 E‑mail: rubio@rubio.com.br www.rubio.com.br
Impresso no Brasil Printed in Brazil
CDD: 616.994 CDU: 616 006 052
Colaboradoras
Amine Farias Costa Nutricionista.
Doutora em Saúde Coletiva pela Universidade Federal do Rio de Janeiro (UFRJ). Mestre em Saúde Coletiva pela Universidade Federal Fluminense (UFF), Niterói – RJ. Nutricionista do Instituto Nacional de Câncer/Ministério da Saúde (Inca/MS).
Cristiane D’Almeida Nutricionista.
Doutora em Ciências Nutricionais pela Universidade Federal do Rio de Janeiro (UFRJ).
Mestre em Nutrição Humana pela UFRJ.
Coordenadora na empresa Nutri Oncoessencial.
Nutricionista do Instituto Nacional de Câncer/Ministério da Saúde (Inca/MS).
Membro do Comitê de Assistência Domiciliar e do Grupo de Oncologia da Sociedade Brasileira de Nutrição Parenteral e Enteral (Braspen).
Diana Borges Dock‑Nascimento Nutricionista.
Doutora em Ciências pela Universidade de São Paulo (USP).
Mestre em Saúde e Ambiente pela Universidade Federal do Mato Grosso (UFMT).
Especialista em Nutrição Parenteral e Enteral pela Sociedade Brasileira de Nutrição Parenteral e Enteral (Braspen).
Professora Associada do Curso de Nutrição da UFMT.
Nutricionista do Projeto ACERTO (Aceleração da Recuperação Total Pós‑operatória).
Gabriella da Costa Cunha Nutricionista.
Mestrado em andamento em Oncologia pelo Programa de Pós‑graduação em Oncologia (PPGO) do Instituto Nacional de Câncer/Ministério da Saúde (Inca/MS).
Especialista em Nutrição Oncológica pelo Inca/MS – Programa de Residência Multiprofissional em Oncologia.
Ignez Magalhães de Alencastro Nutricionista.
Doutora em Alimentação, Nutrição e Saúde pela Universidade do Estado do Rio de Janeiro (UERJ).
Mestre em Bioética, Ética Aplicada e Saúde Coletiva pela Escola Nacional de Saúde Pública, Fundação Oswaldo Cruz (Fiocruz), RJ.
Nutricionista do Instituto Nacional de Câncer/Ministério da Saúde (Inca/MS).
Karla Santos da Costa Rosa Nutricionista.
Mestre em Oncologia pelo Programa de Pós‑graduação em Oncologia (PPGO) do Instituto Nacional de Câncer/Ministério da Saúde (Inca/MS). Nutricionista do Inca/MS.
Livia Costa de Oliveira Nutricionista.
Doutora em Ciências Nutricionais pela Universidade Federal do Rio de Janeiro (UFRJ). Mestre em Nutrição Humana pela UFRJ. Nutricionista do Instituto Nacional de Câncer/Ministério da Saúde (Inca/MS).
Luciana Grucci Maya Moreira Nutricionista.
Mestre em Saúde Pública pela Escola Nacional de Saúde Pública, Fundação Oswaldo Cruz (Fiocruz), RJ.
Especialista em Nutrição Clínica pela Universidade Gama Filho (UGF). Nutricionista do Instituto Nacional de Câncer/Ministério da Saúde (Inca/MS).
Renata de Souza Silva Nutricionista.
Mestrado em andamento em Oncologia pelo Programa de Pós‑graduação em Oncologia (PPGO) do Instituto Nacional de Câncer/Ministério da Saúde (Inca/MS).
Especialista em Nutrição Oncológica pelo Inca/MS – Programa de Residência Multiprofissional em Oncologia.
Simone Garruth dos Santos Machado Sampaio Médica.
Doutora em Medicina pela Universidade do Estado do Rio de Janeiro (UERJ).
Mestre em Medicina pela UERJ. Médica do Instituto Nacional de Câncer/Ministério da Saúde (Inca/MS). Diretora Científica da Academia Nacional de Cuidados Paliativos – Seccional Rio de Janeiro (ANCP/RJ).
Viviane Dias Rodrigues Nutricionista.
Mestre em Ciências pela Universidade do Estado do Rio de Janeiro (UERJ). Especialista em Nutrição Oncológica pelo Instituto Nacional de Câncer/Ministério da Saúde (Inca/MS).
Nutricionista do Inca/MS.
Dedicatória
Aos pacientes portadores de câncer, em quem encontramos valores que os livros não nos ensinam.
As Organizadoras
Agradecimentos
Aos colaboradores, que cederam em letras o seu conhecimento acumulado em anos de estudo e vivência na ciência do nutrir e do cuidar.
À equipe de produção da Editora Rubio, que, além de acreditar neste sonho, dedicou‑se para transformá‑lo em realidade.
As Organizadoras
Apresentação
A Oncologia evoluiu excepcionalmente ao longo dos últimos anos, e com ela a compreen são da Nutrição como pilar fundamental para prevenção e tratamento do câncer. Diante das diferentes faces da Nutrição Oncológica, as autoras desta obra buscam apresentar os prin cipais temas relacionados à abordagem nutricional de pacientes portadores de câncer de maneira dinâmica e sistematizada, com base em informações de alta qualidade científica e em evidências. Os 14 capítulos contemplam as mais relevantes vertentes dos cuidados nu tricionais, como a avaliação do estado nutricional, incluindo aspectos atuais como avaliação da massa muscular, funcionalidade e prognóstico e a intervenção nutricional como terapia nutricional e manejo dos sintomas de impacto nutricional. Também preconizam as reco mendações nutricionais mais recentes para cada fase do tratamento antineoplásico, como quimioterapia, radioterapia, cirurgia, terapia intensiva, transplante de células‑tronco hema topoiéticas e cuidados paliativos. Por fim, abordam o uso de nutrientes adjuvantes e dietas restritivas, temas importantes na atualidade, assim como a nutrição como medida de pre venção e sobrevivência ao câncer.
Nutrição Oncológica no Dia a Dia nasce da experiência acadêmico‑assistencial das or ganizadoras do livro, que conferem identidade e praticidade ao material. A obra é escrita em texto objetivo e de compreensão clara, destinado a estudantes, nutricionistas, pesqui sadores e demais profissionais de saúde, para uso em universidades, hospitais, ambulató rios e consultórios, atendimento domiciliar, entre outros. Esperamos que esta obra possa contribuir para atualização contínua e para o cuidado integral do paciente com câncer, por meio da ciência da nutrição.
As Organizadoras
A Editoria Rubio produz mais um livro sobre a importância da nutrição no dia a dia. Esta obra tem uma relevância científica ímpar dentro da Oncologia, sobretudo por estar emba sada cientificamente nas maiores referências mundiais da Nutrição Clínica. Sendo assim, o livro Nutrição Oncológica no Dia a Dia é um excelente material para estudos, dúvidas clínicas e acompanhamento prático do dia a dia para profissionais que atuam no cenário do doente oncológico, mas também para todos os profissionais de saúde que têm inte resse sobre essa temática. Ressalto que o material é de fácil leitura, extremamente didáti co e composto por ilustrações e quadros que sintetizam as melhores evidências científicas atuais da Nutrição Oncológica.
Atualmente, o câncer é a segunda causa de morte por doença no Brasil. Dados da Or ganização Mundial da Saúde (OMS) demonstram que determinados fatores dietéticos são responsáveis pelo desenvolvimento em cerca de 30% dos cânceres nos países desenvol vidos e 20% nos países em desenvolvimento. Além disso, quando a doença oncológica já está diagnosticada, 50% dos pacientes apresentam perda de peso durante o tratamento do câncer, principalmente em tumores de trato gastrintestinal e pulmão. Outro ponto de contato de extrema relevância durante a jornada oncológica é o paciente sobrevivente do câncer, este que diversas vezes abandona o tratamento após a “cura”, deve ter acompanha mento, monitoramento e reabilitação do estado nutricional de forma integral e coordenada.
Neste cenário, o impacto da Nutrição Oncológica vai desde a prevenção primária, por meio da orientação de alimentação saudável e equilibrada para prevenção de alguns tipos de câncer, até a importância do cuidado nutricional após a doença instalada e durante todo tratamento clínica e/ou cirúrgico da doença oncológica. Vale ressaltar, que diante da maior sobrevida dos pacientes oncológicos, deve haver um rigoroso monitoramento dos cuidados nutricionais dos cancer survivors
Este livro tem suma importância ao abordar os cuidados nutricionais do paciente onco lógico, citando, de forma prática, todas as necessidades nutricionais calóricas e proteicas, nos mais variados cenários: quimioterapia, radioterapia, imunoterapia e transplante de cé lulas tronco hematopoiéticas. Outrossim, o livro permeia a área da oncologia hospitalar em pacientes clínicos de complicações inerentes à própria doença oncológica e/ou à toxicida de relacionadas ao tratamento. A jornada do paciente cirúrgico oncológico no perioperató rio também foi detalhadamente descrita, pontuando a necessidade de preparo nutricional no pré operatório e a manutenção de um conjunto de ações integradas para recuperação acelerada no pós operatório.
Os capítulos relacionados à análise de composição corporal e diagnóstico de sarcopenia demonstraram claramente a necessidade de triagem e avaliação de força muscular, determi nação de quantidade e qualidade do músculo esquelético e provas de capacidade funcional. Também, reforça que pacientes oncológicos com disfunção muscular têm piores desfechos
Prefácio
clínicos (toxicidade dose limitante, sobrevida global) e maiores complicações cirúrgicas (deiscência de anastomoses, complicações infecciosas e não infecciosas pós operatórias).
O capítulo sobre cuidados paliativos tem relevância excepcional, descrevendo aborda gem integral, humanizada e direcionada de acordo com as etapas da progressão do cuida do paliativo referente às limitações e a mudança do foco da terapia nutricional. Esta obra ressalta a necessidade e a valorização das atividades interprofissionais e multidisciplinares que envolvem não só os aspectos biológicos do paciente oncológico, mas também aspec tos sociais, econômicos, éticos e ambientais.
Enfim, é um livro para leitura obrigatória para toda equipe de saúde integral que suporta os cuidados no paciente oncológico. Sinto me muito honrado em compartilhar estes sin ceros escritos com os leitores.
Tenham uma excelente leitura!
Thiago José Martins Gonçalves
Presidente da Sociedade Brasileira de Nutrição Parenteral e Enteral (Braspen). Doutor em Ciências Médicas pela Universidade Nove de Julho (Uninove). Pesquisador em Composição Corporal e Sarcopenia.
CAPÍTULO
Emanuelly Varea Maria Wiegert
Livia Costa de Oliveira
Larissa Calixto-Lima
Emanuelly Varea Maria Wiegert
Taiara
Emanuelly Varea Maria Wiegert
Larissa Calixto-Lima
Sumário
1 Triagem e Avaliação do Estado Nutricional 1
Avaliação do estado nutricional 4 Caquexia do câncer 14 Obesidade e câncer 14 Rotina de avaliação nutricional nas diferentes fases do tratamento 17 Massa muscular 25 Força muscular 39 Funcionalidade/capacidade funcional 39 CAPÍTULO 2 Massa Muscular, Força Muscular e Funcionalidade 23 Renata de Souza-Silva Larissa Calixto-Lima Aline Pereira Pedrosa
Recomendações nutricionais 49 Recomendações nutricionais em situações específicas no paciente com câncer 50 CAPÍTULO 3 Recomendações Nutricionais nas Diferentes Fases do Tratamento 47
Scopel Poltronieri
Aline Pereira Pedrosa Nutrientes adjuvantes para o paciente com câncer . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 65 Dietas restritivas 67 CAPÍTULO 4 Nutrientes Adjuvantes e Dietas Restritivas 63 Taiara Scopel Poltronieri Amine Farias Costa Terapia nutricional oral 73 Terapia nutricional enteral 74 Terapia nutricional parenteral 78 Escolha da via de administração 82 Monitoramento da terapia nutricional 82 Terapia nutricional em condições específicas 82 CAPÍTULO 5 Terapia Nutricional 71 Taiara Scopel Poltronieri Emanuelly Varea Maria Wiegert Larissa Calixto-Lima Aline Pereira Pedrosa
Tipos
Classificação
Avaliação
CAPÍTULO
Paciente
Avaliação
CAPÍTULO
Aline Pereira Pedrosa
Taiara Scopel Poltronieri
Cristiane D’Almeida
CAPÍTULO
Aline Pereira Pedrosa
Taiara Scopel Poltronieri
Cristiane D’Almeida
CAPÍTULO
Taiara Scopel Poltronieri
Larissa Calixto-Lima
Diana Borges Dock-Nascimento
Aline Pereira Pedrosa
Diana Borges Dock-Nascimento
de quimioterapia 89 Protocolos em quimioterapia 89 Avaliação nutricional 89 Recomendações nutricionais para o paciente em quimioterapia 104
6 Quimioterapia 87
da radioterapia 109 Avaliação nutricional 109 Recomendações nutricionais para o paciente em radioterapia 111
7 Radioterapia 107
nutricional 117 Recomendações nutricionais para o paciente com câncer cirúrgico 120 Terapia nutricional para o paciente cirúrgico com câncer 122 Planejamento de alta 128
8 Cirurgia 115
9
Crítico 131
do estado nutricional 133 Recomendações nutricionais para o paciente crítico 133 Terapia nutricional no paciente crítico 139 Tipos de regime de condicionamento . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 147 Tipos de transplante de células-tronco hematopoiéticas 148 Complicações após o transplante de células-tronco hematopoiéticas 148 Avaliação nutricional 150 Recomendações nutricionais 151 Terapia nutricional 152 Nutrientes específicos 154 Condutas nutricionais em situações específicas 155 CAPÍTULO 10 Transplante de Células tronco Hematopoiéticas 145 Gabriella da Costa Cunha Renata de Souza-Silva Viviane Dias Rodrigues Avaliação do paciente em cuidados paliativos 165 Conduta nutricional para o paciente em cuidados paliativos 167 Recomendações nutricionais específicas 170 CAPÍTULO 11 Cuidados Paliativos 163 Emanuelly Varea Maria Wiegert Larissa Calixto-Lima Ignez Magalhães de Alencastro Livia Costa de Oliveira
Avaliação Prognóstica
Sintomas de Impacto Nutricional
Ferramentas diagnósticas
Saciedade
Diarreia
Disgeusia
Xerostomia
Disfagia
Mucosite
Hábitos
Fatores prognósticos
Livia Costa de Oliveira
Karla Santos da Costa Rosa
Simone Garruth dos Santos Machado Sampaio
CAPÍTULO
Karla Santos da Costa Rosa
Larissa Calixto-Lima
Emanuelly Varea Maria Wiegert
Aline Pereira Pedrosa
CAPÍTULO
para Prevenção e Sobreviventes do Câncer
Taiara Scopel Poltronieri
Luciana Grucci Maya Moreira
176 Predição clínica de sobrevida 179 Modelos prognósticos 179 CAPÍTULO 12
173
189 Abordagem nutricional para o controle dos sintomas 192 Anorexia 192
precoce 194 Náuseas e vômitos 195 Constipação intestinal 196
197
. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 200
200
201
201
13
187
de vida e alimentação na prevenção do câncer 209 Recomendações para prevenção do câncer 209 Sobreviventes de câncer 218
14 Nutrição
207
Triagem e Avaliação do Estado Nutricional
Emanuelly Varea Maria Wiegert Livia Costa de Oliveira
Larissa Calixto-Lima
Avaliação Nutricional
CAPÍTULO 1
Introdução
As mudanças do estado nutricional nos pacientes com câncer diferem das encontradas em doenças de etiologia não oncológica e apresentam caráter multifatorial. São decorrentes das alterações fisiopatológicas ocasionadas pela interação tumor‑hospedeiro, tais como:1,2
Aumento da atividade pró‑inflamatória.
Mudanças da sinalização neuroendócrina.
Catabolismo proteico.
Alterações quimiossensoriais.
Diminuição da ingestão alimentar.
Maior ocorrência de sintomas de impacto nutricional (Figura 1.1).
A maioria dos pacientes com câncer apresenta comprometimento do estado nutricio nal ainda nos estágios iniciais da doença, com aumento da prevalência à medida que ela progride.3‑5 Esse comprometimento está associado à localização e ao estágio do tumor, ao tipo de tratamento antineoplásico empregado e ao método de avaliação utilizado para o diagnóstico nutricional.1,6
Independentemente do diagnóstico nutricional – desnutrição associada à doença, ca quexia do câncer ou sarcopenia –, as alterações nutricionais em pacientes com câncer es tão associadas a resultados desfavoráveis, incluindo aumento do risco de toxicidade à qui mioterapia, complicações cirúrgicas, maior tempo de hospitalização, aumento dos custos, redução da qualidade de vida, alterações psicológicas e pior prognóstico.1,7 Notadamente, a definição do diagnóstico nutricional é importante; porém, a necessidade de ser absoluto
Fatores derivados do tumor
Fator mobilizador de
Fator indutor de
Citocinas pró-inflamatórias (IL-1, IL-6, TNF-γ, ITF-α)
Fatores secudários (disfagia, náuseas, obstruções, constipação, diarreia, dor, depressão etc.)
Alterações
Neoglicogênese, glicólise, ciclos fúteis, resistência à insulina, lipólise
Sistema nervoso central Aumento da taxa metabólica basal
Eixo-hipotalâmico (fatores anorexígenos/ orexígenos)
Anorexia, saciedade precoce
com
gama; TNF
fator de necrose tumoral alfa
Triagem e Avaliação do Estado Nutricional
Microambiente tumoral HospedeiroTumor
3 C AP í TULO 1
lipídios
proteólise Lipólise
metabólicas
Proteólise
Figura 1.1 Fisiopatologia das alterações do estado nutricional em pacientes
câncer IL 1: interleucina 1; IL 6: interleucina 6; ITF γ: interferon
α:
Fonte: adaptada de Tan et al., 2014.8
Dia com relação a eles é superada pela de reconhecer o impacto negativo do câncer e de seu tratamento na nutrição do hospedeiro. Sendo assim, a triagem nutricional e a avaliação do estado nutricional (AEN) devem ser rotineiramente incluídas no acompanhamento dos pa cientes acometidos pela doença.1,9
Nutrição Oncológica no Dia a
O diagnóstico nutricional é o primeiro passo para que sejam tomadas medidas de in tervenção na tentativa de prevenir a deterioração do estado nutricional, ou promover sua recuperação e auxiliar na evolução do tratamento, no alívio dos sintomas e na redução da morbimortalidade.1,10 Nesse sentido, os serviços de nutrição e oncologia devem implantar protocolos de atendimento nutricional com o objetivo de assegurar o cuidado adequado aos pacientes e a intervenção precoce, sempre que possível. Desse modo, o registro da AEN, do planejamento nutricional e de quaisquer outras informações relevantes em pron tuário é essencial para o compartilhamento dos dados com toda a equipe assistencial.10,11
Avaliação do estado nutricional
A AEN é um processo sistemático, constituído por obtenção, análise e interpretação de in dicadores com a finalidade de identificar alterações do estado nutricional, elaborar o diag nóstico nutricional e subsidiar o plano de cuidados, de forma a auxiliar na recuperação e/ou manutenção do estado de saúde do indivíduo.11,12 É uma etapa essencial da assistên cia nutricional, preconizada para os cuidados de pacientes com câncer, independentemente da fase da doença.1,13 Trata‑se de um processo dinâmico, feito por meio de comparações entre os dados obtidos e os padrões de referência, envolvendo monitoramento e reavalia ção periódicos da evolução do estado nutricional.1
A importância da triagem nutricional e da AEN no paciente com câncer é incontestável, re conhecida pelas principais sociedades mundiais de nutrição e de oncologia.1,13‑15 Sua imple mentação é recomendada pelo Ministério da Saúde, que tornou obrigatória a implantação de protocolos de triagem nutricional e AEN para pacientes internados pelo Sistema Único de Saú de (SUS), como condicionante para remuneração de terapia nutricional enteral e parenteral.16
Triagem nutricional
Tem como objetivo identificar pacientes com risco nutricional, ou seja, detectar precocemente aqueles mais suscetíveis a desenvolver complicações relacionadas ao seu estado nutricio nal. Por meio da triagem, é possível verificar se uma AEN mais completa é necessária com a finalidade de melhorar ou manter o estado nutricional e, consequentemente, otimizar a alocação dos recursos disponíveis. Nesse sentido, deve ser um procedimento simples, de fácil execução, rápido, reprodutível e realizável, se possível, por qualquer membro da equi pe multiprofissional previamente treinado.13,17
A maioria das ferramentas disponíveis para triagem nutricional avalia indicadores co muns, como alteração do peso corporal, índice de massa corporal (IMC) e diminuição da ingestão alimentar. 18 Entre os métodos preconizados para a população com câncer, destacam‑se:
Triagem de risco nutricional 2002 (NRS; do inglês, Nutrition Risk Screening [Tabela 1.1]).
Instrumento universal de triagem de desnutrição (MUST; do inglês, Malnutrition Universal Screening Tool).
Instrumento de triagem de desnutrição (MST; do inglês, Malnutrition Screening Tool).
Escore de risco nutricional em pacientes críticos (NUTRIC Score; do inglês, Nutrition Risk in Critically Ill).
Avaliação subjetiva global produzida pelo próprio paciente (ASG‑PPP [Tabela 1.2]).
Miniavaliação nutricional (MNA®; do inglês, Mini Nutritional Assessment [Tabela 1.3]).10,19,20
4
Massa Muscular, Força Muscular e Funcionalidade
Renata de Souza-Silva Larissa Calixto-Lima Aline Pereira Pedrosa Emanuelly Varea Maria Wiegert
Massa Muscular e Função Física
CAPÍTULO 2
Massa muscular
A existência de células malignas repercute em alterações metabólicas que expõem o in divíduo a risco nutricional. Sobretudo no paciente com câncer, as mudanças ocasionadas pela interação tumor‑hospedeiro acarretam a depleção acentuada dos depósitos proteicos, de modo que a característica fenotípica clinicamente mais relevante da desnutrição asso ciada ao câncer é a perda de massa muscular esquelética (MME; do inglês, skeletal mus cle mass), definida, nesse contexto, como sarcopenia.1‑3 Entre os fatores etiológicos en volvidos na acentuada depleção da MME em pacientes com câncer, destaca‑se o estado pró‑inflamatório crônico, caracterizado por aumento das citocinas, como a interleucina‑6, e do fator de necrose tumoral alfa.4,5 Os desfechos clínicos mais associados à baixa MME estão descritos na Figura 2.1.
Compartimento muscular
Vários termos têm sido utilizados para descrever o compartimento muscular, tais como MME, massa magra e massa livre de gordura (MLG; do inglês, fat free mass). Contudo, eles não são sinônimos, e estão relacionados ao método utilizado para avaliação da massa muscular – cada um tem características próprias e avalia compartimentos distintos (Figura 2.2), conforme a seguir:6‑9
MME: componente primário do tecido magro. É o compartimento corporal de real inte resse no estudo do componente muscular. O padrão‑ouro de avaliação é a ressonância magnética (RM); porém, na prática, é mais comumente estimada pela área transversal muscular, avaliada por tomografia computadorizada (TC).
Maior frequência de complicações pós-operatórias Câncer colorretal, ginecológico,11 13 14 15 16renal, pulmonar, gástrico
Maior mortalidade pós-operatória Câncer colorretal11, 12
Pior qualidade de vida Câncer gástrico, colorretal17, 18 19
Menor função física Câncer de pulmão, TGI, TGI e geniturinário 20, 21 22 23
Menor sobrevida global Câncer de pulmão, pâncreas, TGI alto, CP, avançado (vários locais)
6 88 9 10
Baixa massa muscular esquelética (MME)
Maior toxicidade à quimioterapia Câncer de pâncreas, esôfago, cólon 7 24 25
Figura 2.1 Associação entre baixa massa muscular esquelética e desfechos clínicos em pacientes com câncer
25 C AP í TULO 2 CP: cabeça e pescoço; TGI: trato gastrintestinal. Fonte: adaptada de Lee et al., 2021;10 Kim et al., 2021;11 Tang et al., 2021;12 Yamahara et al., 2021;13 van Seventer et al., 2021;14 Trejo Avila et al., 2021;15 Argillander et al., 2021;16 Sehouli et al., 2021;17 Watanabe et al., 2021;18 Tanaka et al., 2021;19 Olmez et al., 2021;20 Zou et al., 2021;21 Huang et al., 2017;22 Besson et al., 2021;23 Kong et al., 2020;24 Naito et al., 2017;25 Moreau et al., 2019;26 Anderson et al., 2020;27 Anandavadivelan et al., 2016;28 Feliciano et al., 2017.29
Massa Muscular, Força Muscular e Funcionalidade
a
Dia MLG : é um tecido destituído de gordura extraível, que inclui músculo esquelético e outros componentes, como água, ossos, pele, tendões e tecido conjuntivo. É o compartimento corporal avaliado pelos métodos bicompartimentais (modelo de dois compartimentos), cujo peso é estimado dividindo‑o em massa gorda (MG) e MLG. A água, que constitui de 60% a 75% do peso corporal, é o componente mais variável da MLG; logo, o estado de hidratação pode induzir flutuações em intensidades variáveis nesse compartimento.
Nutrição Oncológica
Massa magra ou massa corporal magra: diferentemente da MLG, a massa magra considera uma pequena quantidade de gordura essencial nos órgãos internos, na medula óssea e nos tecidos nervosos. Na prática clínica, nenhum método é capaz de avaliar a massa magra, termo erroneamente usado como sinônimo de MLG.
Tecido mole magro (TMM): é um componente isento de gordura e tecido mineral ósseo, ou seja, MLG sem osso.
Tecido mole magro apendicular (TMMA; do inglês, appendicular lean soft tissue): refere‑se à soma do TMM (MLG sem osso) de ambos os braços e pernas (apendicular), avaliado por absorciometria por dupla emissão de raios X (DEXA). Muitas vezes, esse compartimento é descrito erroneamente na literatura como MME apendicular; no entanto, a medida de TMMA é um somatório de músculo esquelético (75% a 85%), pele e tecido conjuntivo (Figura 2.3). Em idosos, a possível não associação entre a massa muscular avaliada por DEXA e a função muscular se deve ao aumento da porção não muscular do TMMA que ocorre com o envelhecimento. Desse modo, a avaliação da sarcopenia em idosos com ou sem câncer deve incluir medidas de função.
Métodos de avaliação da massa muscular
Há uma série de métodos para a avaliação da massa muscular, que variam segundo bases físicas, custo, acurácia e facilidade de utilização. Na prática clínica, as técnicas mais acuradas, como DEXA e TC, tornam‑se inviáveis devido à necessidade de profissional treinado, além de exames como o de TC serem considerados de conveniência para avaliação da massa muscular (pela exposição à radiação).30‑32 Desse modo, o uso de técnicas menos acuradas,
2.2
de massa muscular
MLG: massa livre de gordura; MME: massa muscular esquelética; TMM: tecido mole magro. Fonte: adaptada de Buckinx et al.,
26
no Dia
Massa corporal total Gordura 81% MLG Osso 91% TMM Outros órgãos 53% MME Massa corporal total (=peso corporal) Figura
Compartimentos
2018.7
Recomendações Nutricionais nas Diferentes Fases do Tratamento
Taiara Scopel Poltronieri
Emanuelly Varea Maria Wiegert
Larissa Calixto-Lima
Aline Pereira Pedrosa
CAPÍTULO
Nutricionais
3 Recomendações
Recomendações nutricionais
O paciente com câncer apresenta diferentes demandas nutricionais conforme o seu estado nutricional, o tipo, o estadiamento e a localização tumoral, e o tratamento oncológico em pregado. Uma oferta nutricional adequada é fundamental para evitar depleções das reser vas corporais e prevenir deficiências de nutrientes, contribuindo para melhor resposta ao tratamento antitumoral e impactar nos desfechos clínicos.1,2

Necessidades nutricionais no paciente com câncer
A presença do tumor provoca alterações fisiopatológicas e metabólicas, dentre as quais res salta‑se o aumento da proteólise e lipólise e o uso não efetivo da glicose consumida. Além disso, o tratamento antineoplásico pode gerar demandas nutricionais aumentadas para suprir situações como trauma, cicatrizações, supressão do sistema imune, além de outros efeitos colaterais que prejudicam a ingestão alimentar e a absorção de nutrientes.2‑6 As principais alterações provocadas pelo tumor que impactam o gasto energético (GE) do paciente com câncer incluem (Figura 3.1):7
Sexo.
Idade.
Estado nutricional.
Composição corporal.

Atividade física, entre outros.
Existem vários métodos para estimar o GE, sendo a calorimetria indireta o método de referência. É um exame pouco invasivo, que estima a quantidade de calorias diárias que o organismo gasta em repouso (GE basal) determinado pelo consumo de oxigênio e produção
Câncer
Sintomas de impacto nutricional Tratamento Cirurgia
Redução da ingestão alimentar e da atividade física
Recomendações Nutricionais nas Diferentes Fases do Tratamento
Alterações no peso corporal
pacientes com câncer com impacto nas
paratireoide; SNC: sistema nervoso central; TNF-α: fator de
49 C AP í TULO 3
Metabolismo energético alterado Inflamação Alterações na composição corporal SNC Sistema imune Fatores derivados do câncer PTH Miostatina Ativina IL-1 IL-6 TNF-α Figura 3.1 Principais alterações metabólicas em
necessidades nutricionais IL 1: interleucina 1; IL 6: interleucina 6; PTH: hormônio da
necrose tumoral alfa. Fonte: adaptada de Pagano et al., 2022.7
Dia de gás carbônico obtidos pela análise do ar inspirado e expirado pelos pulmões.2,8 Devido ao alto custo e baixa disponibilidade do equipamento na prática clínica, equações prediti vas são frequentemente utilizadas para estimar o GE de pacientes com câncer.2 Contudo, estas possuem baixa precisão e podem subestimar ou superestimar o GE, independente mente do tipo de tumor e do tipo de terapia anticâncer recebida, ademais, as principais equações disponíveis (p. ex., Harris‑Benedict, Mifflin‑St Jeor) são derivadas de populações jovens e saudáveis.7,8
Nutrição Oncológica no Dia a
Atualmente, não existem equações de predição validadas especificamente para estimar o GE de pacientes com câncer, sendo o cálculo realizado na prática por meio das “fórmulas de bolso”.9,10 Cabe ressaltar que estas não consideram fatores como composição corporal, sexo e atividade física. Os valores recomendados de energia e proteínas são expressos em quantidade de calorias e gramas de proteína por kg de peso corporal/dia de acordo com as recomendações preconizadas nos consensos nacionais e internacionais atualizados.3‑6,9,10
As recomendações nutricionais de acordo com o momento do tratamento e condição clínica específica de cada indivíduo estão descritas na Tabela 3.1.11 16
Recomendações nutricionais em situações específicas no paciente com câncer
Caquexia
A caquexia é definida como uma síndrome multifatorial caracterizada pela perda contínua de massa muscular (com ou sem redução de massa gorda) que não pode ser totalmente revertida com o uso de suporte nutricional e leva ao comprometimento funcional progres sivo (ver Capítulo 1, Triagem e Avaliação do Estado Nutricional).15,16 A caquexia do câncer apresenta três estágios de relevância clínica (Figura 3.2).
O prognóstico dos pacientes com caquexia do câncer pode ser alterado conforme a evo lução da condição caquética, e o manejo nutricional deve ser precoce e acompanhar esse processo, com adequações sempre que necessário, conforme apresentado na Tabela 3.2.
As recomendações nutricionais para caquexia do câncer incluem dieta hipercalórica e hiperproteica (Tabela 3.3).1,3,17
Pré-caquexia
Inflamação sistêmica
Caquexia
Caquexia refratária
Normal
Perda de peso <5%
Inflamação sistêmica Perda de peso >5% (2% se sarcopenia ou índice de massa corporal <20kg/estatura² [m])
Câncer avançado refratário ao tratamento antineoplásico Expectativa de vida <3 meses
Fase de cuidados de fim de vida
Perda de massa celular (perda de peso, massa magra corporal)
Alterações metabólicas, normalmente associadas a sintomas, como anorexia
Figura 3.2
da caquexia do câncer
Fonte: adaptada de Fearon et al., 2011;15 Arends et al., 2021.17
Óbito
50
Estágios
Nutrientes Adjuvantes e Dietas Restritivas
Taiara Scopel Poltronieri Amine Farias Costa
CAPÍTULO
e Dietas
4 Nutrientes Adjuvantes
Restritivas
Nutrientes adjuvantes para o paciente com câncer
A oferta nutricional adequada em macro e micronutrientes é uma das bases da prescrição da dieta para o paciente com câncer.1 No entanto, a nutrição moderna tem possibilitado o reco nhecimento e o desenvolvimento de nutrientes adjuvantes que podem beneficiá‑lo, tais como:
Ácidos graxos ômega‑3.
Probióticos.
Glutamina.
Beta hidroxi beta metilbutirato.
Fitoterápicos.
Antioxidantes.
Atualmente, existem diferentes dados disponíveis na literatura científica sobre a eficácia e a segurança do uso desses compostos na população oncológica, as quais precisam ser asseguradas para o uso.2‑5 Por isso, é dever do nutricionista basear‑se em evidências cien tíficas robustas para indicar, ou não, a utilização destes.
Ácidos graxos ômega-3
Os ácidos graxos ômega‑3 são um grupo de ácidos graxos poli‑insaturados composto pelo ácido eicosapentaenoico (EPA) e pelo ácido docosa‑hexaenoico (DHA).3,6,7 Os estudos têm mostrado a eficácia deles em: modular o sistema imune, regular a inflamação, aumentar o apetite e, consequentemente, a ingestão alimentar, atenuar a degradação proteica, es tabilizar o peso corporal e melhorar a morbidade pós cirúrgica e a qualidade de vida em pacientes com câncer e perda de peso, bem como naqueles em tratamento de quimiote rapia e/ou radioterapia.2,3,8,9
A suplementação de ácidos graxos ômega 3 apresenta boa tolerância, mas sintomas gas trintestinais leves podem ocorrer, tais como desconforto abdominal, flatulência, náuseas, vômitos ou esteatorreia, e sabor residual de peixe. Não foram relatados efeitos colaterais graves ou sangramentos pelos estudos atuais.2,3,8,10
Doses de 4 a 6g por dia de óleo de peixe e 1 a 2g por dia de ácidos graxos ômega 3 geralmente são bem toleradas por pacientes com tipos de câncer distintos e em estágios avançados da doença.11 O uso combinado de EPA e DHA, em doses de até 5g/dia, e a in gestão de suplementos contendo somente EPA até 1,8g/dia mostraram‑se medidas seguras em adultos.11,12 Porém, as evidências quanto ao tempo de uso ainda não são conclusivas.3,13
Não há comprovação de que os ácidos graxos ômega 3 atenuem a eficácia de quimio terápicos,11,14 e não existem dados suficientes que comprovem seu efeito no paciente com câncer em estado crítico.3
O que dizem as diretrizes
Braspen, 2019; Espen, 2021: há recomendação para a suplementação de ácidos graxos ômega-3 em pacientes com câncer avançado em tratamento antineoplásico, com risco de desnutrição e/ou desnutridos, com objetivo de estabilizar ou melhorar o apetite, a ingestão alimentar, a massa magra e o peso corporal.2,3
Braspen, 2019: é preciso ter cautela com a suplementação de ácidos graxos ômega 3 em pacientes com plaquetopenia, pois alguns estudos menos recentes relataram prejuízos à agregação plaquetária durante seu uso. No entanto, na literatura atual, não houve relatos de sangramento pelo uso desse composto.3
Espen, 2021: não é indicada a associação de óleo de peixe com ibrutinibe (fármaco usado no tratamento de linfoma linfocítico crônico) devido à possível apresentação de epistaxe.2
65 C AP í TULO 4 Nutrientes Adjuvantes e Dietas Restritivas
Nutrição Oncológica no Dia a Dia Probióticos
Os probióticos são microrganismos vivos que, quando utilizados corretamente, atuam na modulação da microbiota, da barreira intestinal e do sistema imune, além de apresentarem atividade anti‑inflamatória.3,15‑17
Os achados disponíveis na literatura são divergentes quanto à utilização de probióticos em pacientes com câncer. Estudos demonstram falta de evidências na prevenção da diar reia associada a quimioterápicos,18 e outros mostram benefícios na diminuição de efeitos colaterais dos tratamentos oncológicos, como a própria diarreia, mucosite e infecções.3,19‑23
O que dizem as diretrizes
Braspen, 2019: é baixo o nível de evidência para o uso de probióticos na prevenção e no tratamento da diarreia em pacientes com câncer.3
Braspen, 2019; Espen, 2021: embora existam dados indicando resultados promissores do uso de probióticos em pacientes com câncer, eles ainda são heterogêneos quanto à posologia e ao tempo de utilização;3 por isso, nenhuma recomendação nesse sentido pode ser feita atualmente.2
Devido à suscetibilidade de pacientes imunocomprometidos desenvolverem infecções e apresentarem maior resistência a antibióticos, cuidados extras são necessários para o uso de probióticos nesta população. Portanto, mais estudos comprovando sua segurança são essenciais, não sendo indicada a utilização nessa situação.2,3,19‑21,24
Glutamina
A glutamina é um aminoácido não essencial que atua como substrato energético para ente rócitos, linfócitos, macrófagos e gliconeogênese, além de influenciar na biossíntese da enzi ma antioxidante glutationa peroxidase. Na presença de infecções, inflamações ou traumas, a glutamina tem função de nutriente na síntese de proteína muscular, tornando‑a menos disponível para o intestino e para as células imunológicas e, por conseguinte, condicional mente essencial.8,25,26 Ademais, esse aminoácido serve como combustível para a rápida absorção e metabolização pelas células tumorais.3,27,28
Atualmente, as evidências científicas são heterogêneas quanto aos benefícios da glutami na em situações como mucosite, esofagite, enterite ou diarreia no paciente em tratamento oncológico.2,3,28‑33 Pondera‑se também que ela atue na prevenção da perda muscular e na melhora da composição corporal, embora mais estudos sejam necessários.2,3,8
O que dizem as diretrizes
Braspen, 2019; Espen, 2021: devido à falta de estudos consistentes e de qualidade quanto aos benefícios e aos efeitos metabólicos tumorais da glutamina, sua aplicação no paciente com câncer não é recomendada.2,3
Beta‑hidroxi‑beta‑metilbutirato
O beta‑hidroxi beta metilbutirato (HMB) é um metabólito da leucina, um aminoácido de cadeia ramificada. É reconhecido por sua ação anticatabólica, principalmente por minimizar a degradação proteica.2,8,34‑37
A literatura científica ressalta a ação anticatabólica da suplementação de HMB (dose usual de 3g/dia).2,34 Os resultados disponíveis em pacientes com câncer parecem favoráveis, mas ainda são inconsistentes. Diante disso, é preciso avaliar melhor a eficácia da suplementação de HMB não associado a outros aminoácidos, as doses e o tempo de uso necessários, as características clínicas da população em que se mostra mais efetivo, entre outras questões ainda não elucidadas.8,37
66
Terapia Nutricional
Taiara Scopel Poltronieri
Larissa Calixto-Lima
Emanuelly Varea Maria Wiegert
Aline Pereira Pedrosa
CAPÍTULO
Nutricional
5 Terapia
Introdução
A terapia nutricional (TN) está indicada para pacientes com câncer que estejam em risco nutricional ou desnutridos, com dificuldade de ingestão e/ou absorção de alimentos.1 A via de administração adequada depende do diagnóstico oncológico, do tratamento antineoplá sico, das condições clínicas, do prognóstico do paciente e da duração do suporte nutricional, que pode ser por meio de terapia nutricional oral (TNO), terapia nutricional enteral (TNE) e terapia nutricional parenteral (TNP) (Figura 5.1).2
Figura 5.1 Vias de acesso para terapia nutricional
TNE: terapia nutricional enteral; TNO: terapia nutricional oral; TNP: terapia nutricional parenteral.
Terapia nutricional oral
Pacientes com câncer são frequentemente suscetíveis a alterações do estado nutricional, pro vocadas tanto pela doença per se quanto pelo seu tratamento. Por isso, a intervenção espe cializada é fundamental para minimizar ou evitar mudanças significativas e pode ser feita por meio do aconselhamento nutricional e/ou da oferta de nutrientes, por TNO, TNE e/ou TNP.3
O aconselhamento nutricional é a primeira intervenção utilizada e abrange adequações dietoterápicas quantitativas e qualitativas, tais como alterações de consistência da dieta (Figura 5.2), características (p. ex., relacionadas à presença de comorbidades e de sinto mas de impacto nutricional – ver Capítulo 13, Sintomas de Impacto Nutricional), volume e fracionamento, sempre considerando a condição clínica do paciente, seus hábitos alimen tares e seu estilo de vida.4
coco, caldos, mingau etc.
gelatina etc. usual
bem-cozidos
Figura 5.2
coados etc.
Evolução das consistências da dieta via oral
Terapia Nutricional
73 C AP í TULO 5
Dia A TNO por meio de suplementos alimentares está indicada a pacientes que não con seguem atingir as necessidades nutricionais estimadas com a ingestão de alimentos e líquidos enriquecidos, e em pacientes desnutridos ou com risco de desnutrição (Tabela 5.1).1,4 Em casos em que o trato gastrintestinal (TGI) está funcionante e não se encontra obstruído, a TNO é a primeira opção, visto ser a mais fisiológica e menos invasiva. 1,4,5 Para sua prescrição, é importante avaliar as características dos produtos disponíveis, tais como volume, densidade calórica, teor proteico, presença de fibras, sacarose e nutrien tes específicos (Tabela 5.2).
Nutrição Oncológica no Dia a
Tabela 5.1 Indicações da terapia nutricional oral no paciente com câncer
Referência Indicação da terapia nutricional
MS/Inca, 20155 Se a ingestão por via oral for menor que 70% das necessidades nutricionais nos últimos 3 dias Idosos: quando a ingestão alimentar for menor que 75% das recomendações em até 5 dias, sem expectativa de melhora da ingestão
Braspen, 20191 Se não houver a ingestão via oral de nenhum alimento por mais de 1 semana, ou se a ingestão for menor que 60% da necessidade por mais de 2 semanas
Espen, 20174 Se a ingestão alimentar for menor que 60% das necessidades por mais de 1 ou 2 semanas
Virizuela et al., 20182
Se a ingestão alimentar for menor que 60% das necessidades por mais de 10 dias
Fonte: adaptada de Horie et al., 2019;1 Virizuela et al., 2018;2 Arends et al., 2017;4 Brasil, 2015.5
O que dizem as diretrizes
Espen, 2017: durante a radioterapia, principalmente em região de cabeça e pescoço, tórax e TGI, o aporte nutricional adequado deve ser garantido por meio de aconselhamento nutricional e/ou TNO ou TNE.4
O desmame da TNO deve ser gradual e progressivo, iniciado quando a ingestão por via oral da alimentação convencional for maior que 70% das necessidades nutricionais por 3 dias consecutivos.5 Para idosos, o desmame deverá acontecer quando a ingestão alimentar for maior que 75% do gasto energético total por 5 dias consecutivos.5,6 Recomenda se a suspensão da TNO na presença de instabilidade hemodinâmica, disfagia e odinofagia gra ves, obstrução do TGI, vômitos incoercíveis, risco de broncoaspiração, recusa do paciente e intolerância ao suplemento.5
Terapia nutricional enteral
A nutrição enteral é o procedimento pelo qual se administram soluções de nutrientes para dentro do TGI através de um tubo. A Resolução da Diretoria Colegiada (RDC) no 21 da Agên cia Nacional de Vigilância Sanitária do Ministério da Saúde (Anvisa/MS), de 13 de maio de 2015,7 propõe uma definição mais completa:
“Alimento para fins especiais industrializado apto para uso por tubo e, opcional mente, por via oral, consumido somente sob orientação médica ou de nutricionis ta, especialmente processado ou elaborado para ser utilizado de forma exclusiva ou complementar na alimentação de pacientes com capacidade limitada de ingerir, digerir, absorver ou metabolizar alimentos convencionais ou de pacientes que pos suem necessidades nutricionais específicas determinadas por sua condição clínica.”
74
Quimioterapia
Aline Pereira Pedrosa
Taiara Scopel Poltronieri
Cristiane D’Almeida
CAPÍTULO 6 Quimioterapia
Introdução
A quimioterapia (QT) é definida como “a forma de tratamento sistêmico do câncer que usa medicamentos denominados quimioterápicos (ou antineoplásicos) administrados em in tervalos regulares, que variam de acordo com o esquema terapêutico”.1
Os quimioterápicos podem causar sintomas de impacto nutricional (SIN), proporcionan do redução da ingestão alimentar e, consequentemente, depleção do estado nutricional, o que eleva os índices de morbimortalidade.2 Dessa forma, a assistência nutricional precoce auxilia na redução das alterações do estado nutricional.
Tipos de quimioterapia
Os medicamentos quimioterápicos podem ser classificados de acordo com a indicação (Tabela 6.1).
Protocolos em quimioterapia
Na maioria dos cânceres, a QT com associação de fármacos tem melhores resultados do que o tratamento com um único medicamento. As vantagens são:
Promoção do máximo de morte celular dentro da faixa de toxicidade tolerada.
Eficácia contra uma faixa maior de linhagens celulares nas populações tumorais hete rogêneas.
Possibilidade de retardar ou evitar o desenvolvimento de linhagens celulares resistentes.
Vários protocolos de tratamento de câncer foram desenvolvidos, e cada um é aplicável a uma condição particular da doença.3 Alguns exemplos de protocolos de tratamento do câncer estão apresentados na Tabela 6.2.
Avaliação nutricional
Os métodos de avaliação nutricional utilizados em pacientes em QT não diferem daquele para indivíduos com câncer em geral (ver Capítulo 1, Triagem e Avaliação do Estado Nutri cional). No entanto, é importante atentar‑se para a existência de edema, frequente nesses
Quimioterapia
Tabela 6.1 Classificação da quimioterapia de acordo com a indicação
Tipo de quimioterapia Indicação
Curativa
Prévia, neoadjuvante ou citorredutora
Adjuvante ou profilática
Paliativa
Fonte: adaptada de Brasil, 2021.1
Empregada com o objetivo de conseguir o controle completo do tumor
Indicada para a redução de tumores locais ou regionalmente avançados, seja para torná los ressecáveis, seja para melhorar o prognóstico do paciente
Indicada após o tratamento cirúrgico curativo, quando o paciente não apresenta qualquer evidência de neoplasia maligna detectável por exame físico e exames complementares
Indicada para paliação de sintomas que comprometem a capacidade funcional do paciente, mas não repercute, obrigatoriamente, na sua sobrevida
89 C AP í TULO 6
Nutrição Oncológica no Dia a Dia
pacientes. Se estiver presente, deve‑se descontar do peso atual de acordo com o grau do edema (Tabela 6.3). Ademais, como parte da avaliação nutricional de pacientes em QT, é imprescindível o levantamento das interações fármaco‑nutrientes e a avaliação de SIN.
Os indicadores de risco nutricional para pacientes em QT seguem descritos na Tabela 6.4.
Tabela 6.2
Protocolos com a combinação dos quimioterápicos mais utilizados na prática clínica de acordo com o diagnóstico oncológico
Diagnóstico Protocolo de QT Quimioterápicos associados
Câncer colorretal
FOLFOX
5 fluorouracil, leucovorina, oxaliplatina
FOLFIRI 5 fluorouracil, leucovorina, irinotecano
XELOX Capecitabina e oxaliplatina
FLOX Oxaliplatina, folinato de cálcio e 5 fluorouracil
XELIRI Irinotecano e capecitabina
Câncer de mama AC Doxorrubicina e ciclofosfamida
FAC Doxorrubicina, ciclofosfamida e 5 fluorouracil
CMF 5 fluorouracil, metotrexato e ciclofosfamida
Câncer gástrico ECF Epirrubicina, cisplatina e 5 fluorouracil
ECX Epirrubicina, cisplatina e capecitabina
EOF Epirrubicina, oxaliplatina e 5 fluorouracil
DCF Docetaxel, cisplatina e 5 fluorouracil
Hepatocarcinoma GEMOX Gencitabina, oxaliplatina
Linfoma de Hodgkin
ABVD
Doxorrubicina, bleomicina e vimblastina
BEACOPP Bleomicina, etoposídeo, doxorrubicina, ciclofosfamida, vincristina, procarbazina, prednisona e filgastim
DHAP Dexametasona, cisplatina, citarabina e filgastim
ICE Ifosfamida, etoposídeo e carboplatina
IGEV Ifosfamida, gencitabina, vinorelbina e prednisolona
Linfoma não Hodgkin
R CVP
Ciclofosfamida, vincristina, prednisona e rituximabe
R CHOP Rituximabe, ciclofosfamida, doxorrubicina, vincristina, prednisona
R FND Rituximabe, fludarabina, mitoxantrona e dexametasona
5 FRC Fludarabina e ciclofosfamida
90
QT: quimioterapia. Fonte: adaptada de Chabner, 2015;4 Neto, 2013.5 Tabela 6.3 Excesso de peso atribuído à presença de edema e ascite Edema Tornozelo (+/4+) 1kg Joelho (++/4+) 3 a 4kg Base da coxa (+++/4+) 5 a 6kg Anasarca (++++/4+) 10 a 12kg Edema periférico Leve 1kg Moderado 5kg Grave 10kg Ascite Leve 2,2kg Moderada 6kg Grave 14kg Fonte: adaptada de Materese, 1997;6 James, 1989.7
Radioterapia
Aline Pereira Pedrosa
Taiara Scopel Poltronieri
Cristiane D’Almeida
CAPÍTULO 7 Radioterapia
Introdução
A radioterapia é definida como “o método de tratamento local ou locorregional do câncer, que utiliza técnicas e equipamentos variados para irradiar áreas do organismo humano, pré via e cuidadosamente demarcadas”. Tem como objetivo diminuir a taxa de multiplicação das células neoplásicas por meio de diferentes técnicas, que podem ser indicadas de acor do com a região tumoral, sua extensão e o estado geral de saúde do paciente. Os diversos tipos de radioterapia incluem:1
Braquiterapia: fontes de radiação ionizante são inseridas no paciente e posicionadas em contato direto com o tumor. Essa técnica, frequentemente empregada em tumores ginecológicos, recebe o nome de intracavitária (dentro da cavidade abdominal).
Iodoterapia: tipo de radioterapia com fonte não selada, com iodo radioativo, que é indicado para tratamento de carcinoma diferenciado de tireoide.
Teleterapia ou radioterapia externa: aplicação de uma dose de radiação durante um período predeterminado a partir de uma fonte de radiação localizada longe do organismo.
A adequada abordagem nutricional durante a radioterapia pode diminuir o impacto dos efeitos colaterais do tratamento, minimizar a perda de peso, melhorar a qualidade de vida e ajudar os pacientes na recuperação mais rápida após o término do tratamento.2
Classificação da radioterapia
A radioterapia antineoplásica pode ser classificada de acordo com a indicação (Tabela 7.1).
Avaliação nutricional
Os métodos de avaliação nutricional utilizados em pacientes em radioterapia não diferem daqueles aplicados aos com câncer em geral, sendo imprescindível a avaliação de sinto mas de impacto nutricional em virtude dos possíveis efeitos colaterais da radioterapia que podem atrapalhar a ingestão alimentar.
Os métodos de avaliação nutricional no paciente com câncer podem ser encontrados no Capítulo 1, Triagem e Avaliação do Estado Nutricional. Os indicadores de risco nutricional para pacientes em radioterapia seguem descritos na Tabela 7.2.
Curativa
Tem como objetivo a cura do paciente, e a dose utilizada é geralmente a máxima que pode ser aplicada na área. Em alguns casos, a radioterapia curativa pode ser realizada de forma concomitante a algum tipo de tratamento sistêmico, com a finalidade de potencializar seu efeito
Pré operatória (prévia, neoadjuvante ou citorredutora)
Pós operatória ou pós quimioterápica (profilática ou adjuvante)
Paliativa
Antecede a cirurgia, com o objetivo de reduzir o tamanho do tumor e facilitar o procedimento operatório
Indicada após tratamento cirúrgico ou quimioterapia, quando o paciente não apresenta qualquer evidência de neoplasia maligna detectável por exame físico e complementares. Essa modalidade de tratamento diminui o risco de recidiva no local operado ou nos linfonodos regionais
Objetiva o tratamento local do tumor primário ou de metástase(s), sem necessariamente influenciar a taxa da sobrevida global do doente. As principais indicações para radioterapia paliativa são antiálgica, anti hemorrágica e para síndrome de compressão medular e para o sistema nervoso central
Fonte: adaptada de Brasil, 2021.1
Tabela 7.1 Classificação da radioterapia de acordo com a indicação Tipo de radioterapia Indicação
109 C AP í TULO 7 Radioterapia
Tabela 7.2
Nutrição Oncológica
Indicadores de risco nutricional ou desnutrição para pacientes em radioterapia
NRS-2002 ≥3
ASG-PPP = B ou C e ASG-PPP VR ≥9
Ingestão alimentar reduzida nas últimas 2 semanas
Sintomas de impacto nutricional, como disfagia, odinofagia, xerostomia, trismo, diarreia e mucosite
Localização tumoral: cabeça e pescoço, TGI ou pulmão
Perda de peso não intencional nas últimas 2 semanas
Redução da atividade física/funcional que impeça ou limite realizar atividades rotineiras
Idade ≥60 anos
No caso de pacientes idosos em radioterapia, além dos indicadores de risco nutricional ou desnutrição citados anteriormente, considerar também:
y Albumina: <3,5g/mL
y Colesterol sérico: <160mg/dL
y PC‑R: >10mg/dL
ASG PPP: Avaliação Subjetiva Global Produzida pelo Paciente; ASG PPP VR: avaliação subjetiva global produzida pelo paciente – versão reduzida; NRS: nutrition risk screening; TGI: trato gastrintestinal; PC-R: proteína C-reativa. Fonte: adaptada de SBNO, 2021.2
Sintomas de impacto nutricional associados à radioterapia
Os efeitos colaterais da radioterapia dependem do tumor, do local irradiado, da duração, da dose e do fracionamento do tratamento.3 A irradiação da região de cabeça e pescoço e da região do esôfago pode promover mucosite, diminuição da ingestão alimentar e perda de peso em mais de 80% dos pacientes.4‑6 De forma similar, a radioterapia na região pél vica está associada a sintomas gastrintestinais em 80% dos pacientes.7 Devido a esses fa tores, todos os indivíduos submetidos à radiação do trato gastrintestinal (TGI) ou da região de cabeça e pescoço devem receber aconselhamento e terapia nutricional adequada de acordo com os sintomas e o estado nutricional.8
Os efeitos colaterais agudos e tardios relacionados à radioterapia das regiões da cabeça e pescoço, tórax, sistema nervoso central, abdome e pelve estão descritos na Tabela 7.3. A gravidade pode ser avaliada pela escala de gravidade adotada pelo Radiation Therapy Oncology Group (Tabela 7.4).9
O aconselhamento nutricional para os diferentes sintomas associados à radioterapia an tineoplásica está descrita no Capítulo 13, Sintomas de Impacto Nutricional.
O que dizem as diretrizes
Braspen, 2019: todos os pacientes submetidos à radiação da região de cabeça e pescoço devem receber avaliação nutricional completa, orientação nutricional adequada e, se necessário, terapia nutricional de acordo com os sintomas e o estado nutricional5
Espen, 2021: durante a radioterapia, principalmente nas regiões de cabeça e pescoço, tórax e TGI, adequada ingestão alimentar deve ser assegurada por meio de aconselhamento nutricional individualizado e/ou uso de suplementos nutricionais, a fim de evitar deterioração nutricional e interrupções da radioterapia6
Espen, 2021; Asco, 2020: a utilização de terapia nutricional enteral (TNE) é recomendada quando os sintomas associados à radioterapia limitam ou impossibilitam a alimentação por via oral. Se a alimentação oral ou enteral não for possível, como nos casos de enterite grave por radiação ou má absorção grave, a terapia nutricional parenteral (TNP) será recomendada6,11
110
no Dia a Dia
Cirurgia
Taiara Scopel Poltronieri Larissa Calixto-Lima
Diana Borges Dock-Nascimento
CAPÍTULO 8 Cirurgia
Introdução
A cirurgia é um procedimento importante e comum no tratamento do paciente com cân cer,1,2 e o estado nutricional está intimamente relacionado a desfechos pós‑operatórios.3 Pacientes desnutridos apresentam maior risco de complicações (infecciosas e não infeccio sas), além de aumento do tempo de internação, da mortalidade e dos custos hospitalares. 3‑8 Assim, a terapia nutricional (TN) perioperatória é fundamental para melhorar os desfechos de pacientes com câncer cirúrgicos e, consequentemente, para o sucesso do tratamento.
Avaliação nutricional
O acompanhamento por nutricionista durante todo o período perioperatório, iniciando por triagem e avaliação nutricional, é fundamental para uma intervenção nutricional adequada para o paciente cirúrgico com câncer.3,8 Entre os fatores que podem levar ao aumento do gasto energético desses indivíduos estão a demanda energética do próprio tumor, a presença de inflamação e infecções graves, a composição corporal do paciente, o uso de analgesia e sedação, a elevação da temperatura corporal e a ocorrência de alterações hemodinâmicas, disfunções orgânicas e lesões abdominais extensas.8‑11
Os métodos de avaliação nutricional utilizados em pacientes cirúrgicos não diferem da queles para os pacientes com câncer em geral (ver Capítulo 1, Triagem e Avaliação do Estado Nutricional); no entanto, é imprescindível a avaliação de sintomas de impacto nutri cional no pós‑operatório, em virtude dos possíveis efeitos que podem atrapalhar a ingestão alimentar (Tabela 8.1) e a digestão e absorção de nutrientes, a depender da área resseca da (Figura 8.1 e Tabela 8.2).
Os indicadores de risco nutricional grave para pacientes cirúrgicos seguem descritos na Tabela 8.3.
Tabela 8.1 Alterações nutricionais no pós operatório de cirurgias de cabeça e pescoço conforme o local de ressecção
Procedimento cirúrgico Efeitos sobre a ingestão alimentar
Queilectomia parcial
Glossectomia parcial
Queilectomia e glossectomia (50%)
Maxilectomia
Pelvectomia
Dificuldade no vedamento labial
Dificuldade no disparo da reação da deglutição
Descontrole na condução do bolo alimentar (risco de broncoaspiração)
Refluxo para cavidade nasal
Alteração da deglutição e da mastigação
Estase de alimento
Alteração da mobilidade da língua
Descontrole na condução do bolo alimentar (risco de broncoaspiração)
Mandibulectomia
Laringectomia parcial
Dificuldade na mastigação
Trismo
Dificuldade no selamento labial (incontinência salivar e alimentar)
Disfagia temporária
Risco de broncoaspiração
Laringectomia total Risco de estreitamento do esfíncter faringoesofágico
Risco de fístula faringocutânea
Fonte: adaptada de Reis et al., 2018.5
117 C AP í TULO 8 Cirurgia
Fígado
Sais biliares
Emulsificante
Triglicerídios
Lipases ProteasesAmilases
Duodeno Aminoácidos absorbidos
Monoglicerídios absorvidos
Pâncreas
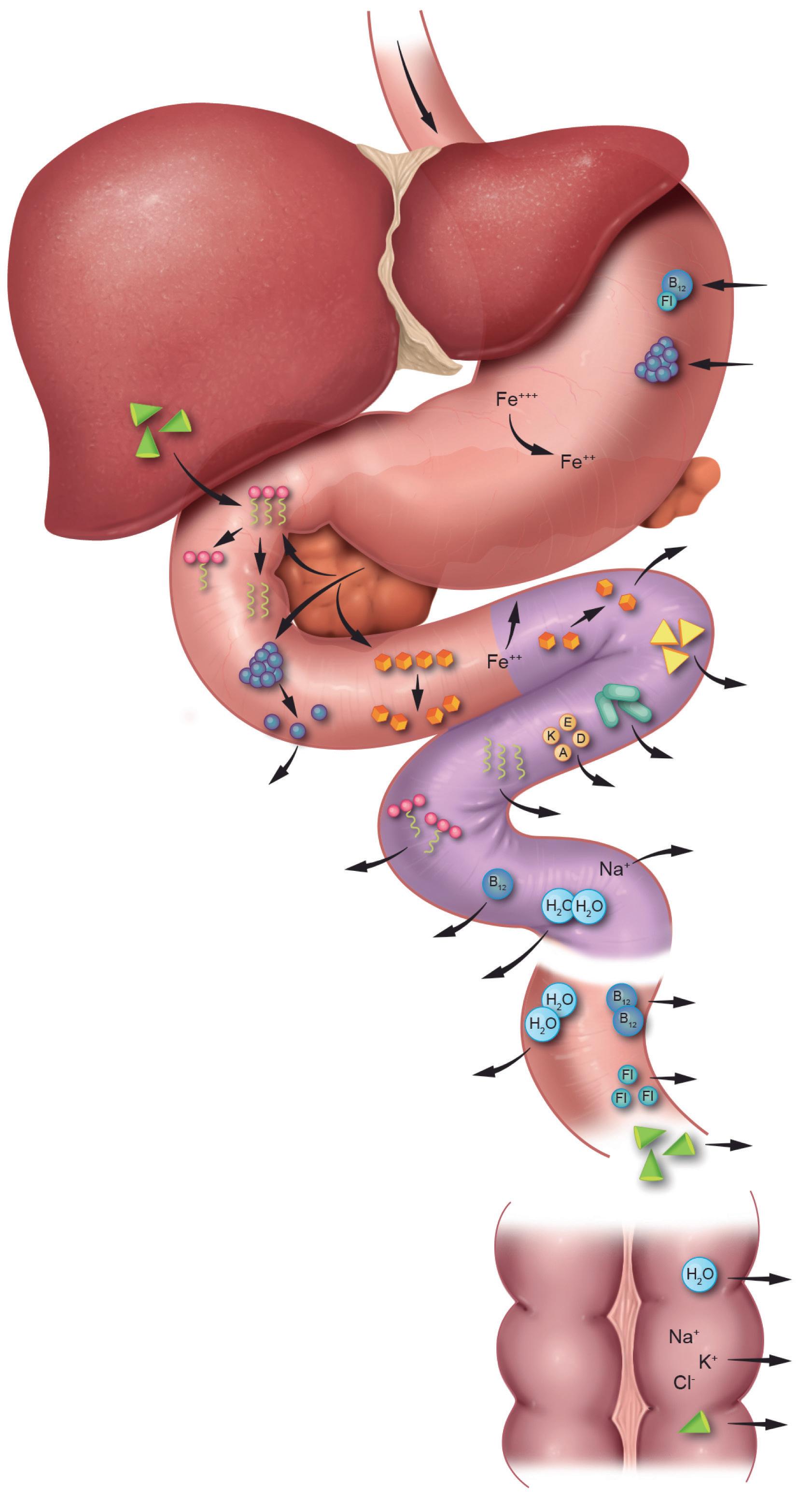
Ferro absorvido
CHO Dissacarídios
B12 absorvida (pequenas quantidades)
Água absorvida (quantidade moderada)
Sódio absorvido (pequena quantidade)
Fator intrínseco ligado à vitamina B12 Pepsina inicia a digestão da proteína
Cólon
118 Nutrição Oncológica no Dia a Dia Ácidos graxos
Dissacarídios da borda em escova Jejuno
Monossacarídios absorvidos Cálcio absorvido
Folato absorvido Vitaminas lipossolúveis absorvidas Ácidos graxos livres absorvidos
Água e sódio absorvidos (quantidade moderada)
B12 absorvida
Íleo
Fator intrínseco absorvido Ácidos biliares reabsorvidos para reciclagem no fígado
Água absorvida (pequena quantidade)
Eletrólitos absorvidos (pequena quantidade)
Ácidos biliares reabsorvidos (pequena quantidade)
Nutrientes combinados com amilases salivares
Proteína
Monoglicerídio+Ácidos graxos
Figura 8.1 Sítios de digestão e absorção dos nutrientes no trato gastrintestinal
CAPÍTULO
Paciente Crítico
Aline Pereira Pedrosa Diana Borges Dock-Nascimento
Paciente Crítico
9
Introdução
Pacientes com câncer podem necessitar de cuidados intensivos ao longo do tratamento. A doença crítica leva à desnutrição aguda grave com perda significativa da massa muscu lar, o que está associado ao aumento de complicações e ao óbito.1 Assim, o paciente com câncer internado em unidade de terapia intensiva (UTI) precisa de terapia nutricional (TN) com oferta adequada de nutrientes.
O objetivo da TN é modular a resposta imunoinflamatória e, com isso, contribuir para a melhora clínica, redução do tempo de internação e das complicações e a diminuição da ocorrência de óbito.2,3 Sistematicamente, os pacientes em cuidados intensivos devem pas sar pela rotina de triagem e avaliação nutricional, seguida de estimativa das necessidades nutricionais, escolha da via de alimentação, monitoramento à beira do leito e, por último, planejamento de alta da UTI. Nesta última fase, a equipe deve compreender que muitos pacientes críticos necessitarão de acompanhamento nutricional prolongado, com interven ção variando de 2 a 6 meses.2,4‑7
Avaliação do estado nutricional
Inicialmente, o paciente crítico deve ser avaliado quanto à gravidade do risco nutricional. O que permanece internado por mais de 48h na UTI é classificado como em risco de des nutrição e, por isso, necessita de TN especializada.2 Dessa maneira, o diagnóstico da con dição nutricional é o primeiro passo para o início de uma intervenção segura e adequada.8
As ferramentas de avaliação do risco nutricional indicadas para o paciente crítico são o Nutritional Risk Screening 2002 (NRS‑2002; Tabela 9.1) e o Nutrition Risk in the Critically ill (NUTRIC score; Tabela 9.2).2,9,10 Para preenchimento do NUTRIC score, é necessário o cálculo do escore Sequential related Organ Failure Assessment I (SOFA) (Tabela 9.3), do Acute Physiology and Chronic Health Evaluation II (APACHE) (Tabela 9.4) e da Escala de Coma de Glasgow (ECG) (Tabela 9.5).
Vale ressaltar que, até o momento, a ferramenta mais específica para avaliação do risco nutricional do paciente crítico é o NUTRIC score ou sua versão modificada (sem a inter leucina‑6 [IL‑6]), que considera parâmetros relacionados com a resposta inflamatória e as falências orgânicas.11,12 Porém, independentemente da ferramenta utilizada para a triagem nutricional, a equipe deve entender que, devido à resposta aguda imunoinflamatória, os pacientes críticos são considerados em risco de desnutrição.
Sarcopenia adquirida na unidade de terapia intensiva
Dados da literatura mostram que a prevalência de baixa massa muscular em pacientes críti cos varia de 30,2% a 60%.13 15 Quanto maior a perda de massa e função musculares, pio res os desfechos clínicos.16 Os métodos de avaliação da massa muscular em pacientes com câncer seguem descritos no Capítulo 2, Massa Muscular, Força Muscular e Funcionalidade
Recomendações nutricionais para o paciente crítico
A calorimetria indireta é considerada o padrão‑ouro para determinar a necessidade ener gética do paciente crítico. Na ausência desse método, as fórmulas preditivas e a caloria por quilograma de peso corporal (kcal/kg de peso) estão indicadas para estimar as necessida des nutricionais.2
A resposta aguda ao trauma constitui uma reação primária de defesa do organismo a agressões. Nessa fase, a oferta calórica deve ser baixa, pois tem por objetivo evitar a sobrecarga metabólica (Tabela 9.6). A oferta elevada de calorias nos primeiros 3 a
133 C AP í TULO 9 Paciente Crítico
Tabela 9.1
Nutrição Oncológica
Rastreamento de Risco Nutricional – Nutritional Risk Screening‑2002 (NRS 2002)
Paciente: ___________________________________________________________________________ Data: ___ /___
Triagem inicial Perguntas Sim Não
1. IMC <20,5kg/estatura2(m)?
2. Perda de peso nos últimos 3 meses?
3. Redução da ingestão na última semana?
4. O paciente está com alguma doença grave?
Em caso de resposta afirmativa a qualquer um dos itens, continuar para triagem final
Triagem final
Pontuação Estado nutricional
0 = ausente Estado nutricional normal
1 = leve Perda de peso >5% em 3 meses ou ingestão alimentar entre 50% e 75% dos requerimentos normais na semana anterior
2 = moderada Perda de peso >5% em 2 meses ou IMC entre 18,5 e 20,5 ou ingestão alimentar entre 25% e 60% na semana anterior
3 = grave Perda de peso >5% em 1 mês ou IMC <18,5 ou consumo alimentar entre 0% e 25% na semana anterior
Pontuação Gravidade da doença
0 = ausente Requerimentos nutricionais normais
1 = leve Fraturas, pacientes crônicos com complicações agudas (cirrose, diabetes, câncer, hemodiálise)
2 = moderada Cirurgia abdominal, pneumonia grave, AVE
3 = grave Transplante, UTI, TCE
Acrescentar 1 ponto para pacientes com idade superior a 70 anos Diagnóstico
( ) Escore ≥3: paciente em situação de risco nutricional. Iniciar um plano de cuidados nutricionais ( ) Escore <3: realizar rastreamento semanal do paciente
IMC: índice de massa corporal; AVE: acidente vascular encefálico; TCE: traumatismo cranioencefálico. UTI: unidade de terapia intensiva. Fonte: adaptada de Kondrup et al., 2003.17
134
no Dia a Dia
/___
Tabela 9.2 Ferramenta para avaliação do risco nutricional em pacientes críticos (NUTRIC score) Variáveis do NUTRIC score Intervalo Pontos Idade <50 50 a 74 ≥75 0 1 2 APACHE II <15 15 a 19 20 a 27 ≥28 0 1 2 3 SOFA <6 6 a 9 ≥10 0 1 2 Número de comorbidades 0 ou 1 ≥2 0 1 Dias de internação hospitalar até a entrada na UTI 0 ≥1 0 1 IL 6 0 a 300 ≥400 0 1 (continua)
Transplante de Células‑tronco Hematopoiéticas
Gabriella da Costa Cunha
Renata de Souza-Silva
Viviane Dias Rodrigues
CAPÍTULO
de Células
tronco
10 Transplante
‑
Introdução
O transplante de células tronco hematopoiéticas (TCTH) é um tipo de tratamento amplamente utilizado em enfermidades hematológicas benignas e malignas, poten cialmente curativo e promotor de aumento da sobrevida. 1 Sua aplicação depende de diagnóstico, estadiamento, idade do paciente e status da doença, ou seja, se está ativa ou em remissão.
Em pacientes com doenças malignas, o TCTH é precedido pela administração de regi mes preparatórios (condicionamento), visando reduzir a carga tumoral e fornecer imunos supressão do receptor para evitar a rejeição do enxerto.2
Entre as doenças malignas mais comuns para a realização do TCTH estão:
Mieloma de células plasmáticas.
Linfoma não Hodgkin.
Linfoma de Hodgkin.
Leucemia mieloide aguda e crônica.
Leucemia linfoblástica aguda.
A depender do tipo de enfermidade, há variação no condicionamento empregado e no tipo de TCTH a ser realizado.3
As células tronco hematopoiéticas (CTH) utilizadas para o enxerto podem ter como fon te a medula óssea, o sangue periférico ou o sangue de cordão umbilical.4 Podem também ser provenientes do próprio paciente, de familiares compatíveis ou de doadores não apa rentados compatíveis.
A seleção dos doadores é feita por meio da avaliação de compatibilidade do HLA (antí geno leucocitário humano; do inglês, human leukocyte antigen), com o intuito de reduzir a rejeição das novas células não apenas na direção do hospedeiro contra o enxerto, mas também como doença do enxerto contra o hospedeiro (DECH). Na ausência de um doador com HLA totalmente compatível, a seleção de um doador parcialmente compatível (haploi dêntico, normalmente um dos pais ou outro parente) é uma opção.3
Para delimitar as fases do TCTH, a contagem de dias no pré e no pós transplante é reali zada de forma diferenciada. Todos os dias anteriores ao dia da infusão das células são conta dos regressivamente em números negativos (...D 3, D 2, D 1); o dia da infusão das células, ou seja, do transplante, é considerado o dia zero (D0); e após o transplante, a contagem é realizada de forma crescente com números positivos (D+1, D+2, D+3…).
Tipos de regime de condicionamento
Os regimes de condicionamento utilizados podem ser de três tipos:3,5
1. Não mieloablativo: é realizado por meio da administração de quimioterapia não mie loablativa, com o objetivo exclusivo de erradicação ou remissão da doença, ou seja, sem o comprometimento da medula.
2. Mieloblativo: é composto por altas doses de quimioterapia e pode estar associado à radioterapia de corpo inteiro (TBI; do inglês, total body irradiation), com o intuito de erradicar as células malignas, fornecer imunossupressão e criar um ambiente propício para o enxerto das CTH do doador.
3. Mieloablativo de intensidade reduzida: é utilizado em pacientes idosos e com co morbidades, os quais podem não tolerar o condicionamento em sua forma plena, devi do à elevada toxicidade. É considerado um intermediário entre o mieloablativo e o não mieloablativo.
Transplante de Células-tronco Hematopoiéticas
147 C AP í TULO 10
Nutrição Oncológica no Dia a Dia
Tipos de transplante de células‑tronco hematopoiéticas
Existem três modalidades de transplante, que diferem de acordo com o doador de CTH (Tabela 10.1):5
Autólogo: quando as CTH são provenientes do próprio paciente.
Alogênico: quando as CTH são provenientes de outro doador, que pode ser aparentado (irmão ou outro parente) ou não aparentado (do Registro Brasileiro de Doadores Voluntários de Medula Óssea [REDOME] ou do banco de sangue de cordão umbilical e placentário).
Singênico: quando as CTH são doadas por irmão gêmeo univitelino (idêntico).
Tabela 10.1
Características das diferentes modalidades de transplante de células-tronco hematopoiéticas
Tipos de transplante Fonte de CTH Doador
Autólogo
Medula óssea
Sangue periférico
Sangue de cordão umbilical e placentário
Alogênico
Medula óssea
Sangue periférico
Sangue de cordão umbilical e placentário
Singênico
Medula óssea
Sangue periférico
CTH: células-tronco hematopoiéticas.
Fonte: adaptada de Barban et al., 2020.5
O próprio paciente
Aparentado (irmão ou outro parente)
Não aparentado: qualquer pessoa sem laços familiares com o paciente
Irmão gêmeo univitelino (idêntico)
Complicações após o transplante de células‑tronco hematopoiéticas
Em decorrência das doses de quimioterapia e radioterapia utilizadas em regimes de condicionamento mieloablativo e em alguns de intensidade reduzida, células saudá veis são afetadas, principalmente as de alta replicação, como os linfócitos e as células do trato gastrintestinal (TGI) – enterócitos e colonócitos. Com isso, após a infusão de CTH, podem haver complicações precoces e tardias relacionadas a toxicidade e imuno deficiência (Figura 10.1). 4 6
Doença do enxerto contra o hospedeiro
A DECH é um tipo de reação autoimune mediada pela ativação dos linfócitos T do doador, que reconhecem os antígenos do hospedeiro como não próprios e atacam seus tecidos, afetando órgãos como pele, pulmões, fígado, TGI, timo e sistema hematopoiético.7 Os fa tores de risco para DECH incluem idade do paciente, estágio da doença e incompatibilida de de sexo, no caso de doadora feminina e paciente masculino, devido ao reconhecimen to de antígenos associados ao cromossomo Y.3 Para profilaxia e tratamento dessa doença, são administrados diversos medicamentos, em especial imunossupressores na prevenção e corticosteroides e imunossupressores no tratamento.3,7
A DECH aguda ocorre nos primeiros meses (geralmente até 100 dias) pós transplante e se caracteriza por danos à pele, ao fígado e ao TGI, causando exantema da pele, enterite e hepatite colestática. A DECH crônica pode desenvolver se em vários meses a anos pós trans plante, com danos progressivos do tipo ulcerativo em mucosas e lesões em vários órgãos
148
Cuidados Paliativos
Emanuelly Varea Maria Wiegert
Ignez Magalhães de Alencastro
Larissa Calixto-Lima
Livia Costa de Oliveira
Cuidados Paliativos
CAPÍTULO 11
Introdução
A Organização Mundial da Saúde (OMS) define cuidado paliativo como uma abordagem que promove a melhora da qualidade de vida de pacientes e familiares que enfrentam doenças que ameaçam a continuidade da vida e que previne e alivia o sofrimento por meio de iden tificação precoce, avaliação e tratamento de sintomas de natureza física, psicossocial e espi ritual.1 Trata‑se, portanto, de um tratamento que envolve o indivíduo em sua integralidade.2
Pensando, portanto, em uma abordagem integral para o paciente em condição de saúde crônica, progressiva e debilitante, com alto impacto físico, psicológico e social, a assistência nutricional é de suma importância. Os objetivos da atenção nutricional nos cuidados paliati vos variam de acordo com a fase da doença e abrangem controle de sintomas, recuperação, manutenção ou retardo do comprometimento do estado nutricional, além de melhora da capacidade funcional, promoção da qualidade de vida e ressignificação da alimentação.3‑5
Na prática clínica, os objetivos da assistência nutricional podem ser divididos em três fa ses (Figura 11.1):3‑6
1. Inicial: quando a nutrição é considerada obrigatória e consiste em ofertar nutrientes em quantidades suficientes para atender as demandas fisiológicas e recuperar ou manter o estado nutricional.
2. Avançada: fase em que o objetivo principal é reduzir o impacto dos sintomas, mini mizar os déficits nutricionais evitáveis e melhorar a capacidade funcional com foco na qualidade de vida.
3. Final de vida: o objetivo é prioritariamente proporcionar conforto e qualidade de morte.
Avaliação do paciente em cuidados paliativos
O plano de cuidados nutricionais para o paciente com câncer em cuidados paliativos deve rá ser individualizado e adaptado a cada momento da evolução da doença. Deve pautar‑se, principalmente, na avaliação clínica, prognóstica, nutricional e bioética.6
FOCO DO CUIDADO NUTRICIONAL
Expectativa de vida de anos ou meses
Ofertar nutrientes (ou TN) para recuperar ou manter estado nutricional (impacto sobre desfechos clínicos)
Expectativa de vida de meses ou semanas
Controlar sintomas, melhorar funcionalidade e QV, ressignificar a alimentação
Expectativa de vida de dias ou horas
Proporcionar conforto e qualidade de morte, ressignificar a alimentação
Figura 11.1 Fases do cuidado nutricional no paciente em cuidados paliativos oncológicos
QV: qualidade de vida; TN: terapia nutricional.
Fonte: adaptada de Lima et al., 2015;3 Magalhães et al., 2018;4 Bottoni et al., 2019;5 Brasil, 2015.6
165 C AP í TULO 11 Cuidados Paliativos
ÓBITO
Nutrição Oncológica no
O que dizem as diretrizes
Espen, 2021: as intervenções nutricionais em pacientes com câncer avançado devem ter como base no prognóstico da doença maligna e o benefício esperado na qualidade de vida e na sobrevida do paciente.7
Braspen, 2019: a estratégia nutricional para pacientes em cuidados paliativos deve considerar o prognóstico, o estado nutricional, a ingestão alimentar e a expectativa de vida do paciente. A tomada de decisão deve ser sempre em conjunto com o paciente, a família e a equipe multiprofissional.8
Avaliação clínica e prognóstica
A avaliação clínica deverá contemplar informações como:6
Localização e estadiamento tumoral.
Progressão da doença.
História do tratamento oncológico prévio.
Presença de comorbidades.
Medicações utilizadas.
Condições socioeconômicas, entre outras (ver Capítulo 12, Avaliação Prognóstica).
A avaliação da capacidade funcional e da presença de sintomas (ver capítulo 13, Sinto mas de Impacto Nutricional), sobretudo na fase mais avançada da doença, oferece infor mações importantes para subsidiar a gestão dos cuidados.
Avaliação nutricional
Alterações do estado nutricional são frequentes em pacientes em cuidados paliativos oncoló gicos.9‑12 No entanto, devido ao tempo de sobrevida geralmente reduzido desses pacientes, os métodos utilizados para avaliar o estado nutricional devem considerar a avaliação clínica e o prognóstico, com objetivo de identificar aqueles em condições passíveis de melhora e com melhor prognóstico, além de situações em que intervenções nutricionais específicas poderiam ser consideradas desproporcionais ao avanço da doença.
Diferentes métodos de diagnóstico nutricional podem ser utilizados (ver Capítulo 1, Tria gem e Avaliação do Estado Nutricional). A versão resumida da Avaliação Subjetiva Global Produzida pelo Paciente (ASG‑PPP) destaca‑se por contemplar os principais domínios das definições conceituais da desnutrição e por ser um método pouco invasivo13‑15 e reconhe cidamente associado a desfechos desfavoráveis nessa população.9,12,16 Contudo, a ASG‑PPP não abrange a avaliação de parâmetros relacionados com a resposta inflamatória sistêmica, que notadamente desempenha papel fundamental na etiologia das principais alterações fisiopatológicas do estado nutricional em indivíduos com câncer. Nesse sentido, a classifi cação do Escore Prognóstico de Glasgow modificado (EPG‑m)17 destaca‑se como método objetivo e válido que está associado ao prognóstico e à gravidade do estado nutricional em pacientes com câncer em cuidados paliativos podendo ser utilizado de forma complemen tar à ASG PPP (ver Capítulo 12, Avaliação Prognóstica).9,10
Aspectos bioéticos
O processo de tomada de decisão na prática clínica diante de um conflito é um aspecto es sencial e requer que os profissionais de saúde considerem não somente a biotecnociência, mas também outras dimensões que fazem parte do ser humano, como questões culturais, psicológicas e morais para que decisões mais acertadas sejam tomadas.18 A pertinência dessa percepção global é fundamental em cuidados paliativos, sobretudo quando, no de correr do tratamento e do acompanhamento do paciente, surgem conflitos e dilemas rela cionados à implementação ou à suspensão da alimentação.
166
Dia a Dia
Prognóstica
Livia Costa de Oliveira Karla Santos da Costa Rosa Simone Garruth dos Santos Machado Sampaio
CAPÍTULO
Avaliação Prognóstica
Avaliação
12
Introdução
A avaliação prognóstica pode auxiliar os profissionais de saúde, pacientes e familiares a to marem decisões esclarecidas a respeito de cuidados de saúde, baseando‑se em informa ções disponíveis atualmente para predição de desfechos. Vale ressaltar que, em oncologia, o prognóstico não está apenas associado à predição de sobrevida, mas também à recidiva da doença, entre outros fatores.1‑3 Trata‑se de um processo dinâmico que pode se modificar de acordo com a resposta ao tratamento e o desenvolvimento de complicações agudas ou outras comorbidades. Dessa forma, eventos sentinelas, como a constatação da progressão da doença e a ocorrência de hospitalizações, devem desencadear novas discussões prog nósticas por toda a equipe multiprofissional.1,2
O processo de avaliação prognóstica deve ser composto de duas fases: formulação e comunicação. Para a primeira, devem ser utilizadas ferramentas apropriadas ao estágio da doença oncológica. Nos estágios iniciais do câncer, o prognóstico pode ser impulsionado por fatores relacionados à doença e ao próprio paciente. Na fase avançada, consiste necessaria mente em elementos relacionados ao paciente (Tabela 12.1).1,2 Quanto à comunicação, os
mais utilizados em oncologia
Fatores/modelos
Estágios do câncer Inicial Avançado
Clínicos Estágio da doença (0 a 4)
Região acometida pela doença Tamanho do tumor
Patológicos Grau histológico: 0 a 3
Moleculares Genéticos Microarray
Região acometida pela doença
Laboratoriais Hipoalbuminemia, hipogonadismo, hipercalcemia, hiponatremia, aumento da LDH Inflamatórios Elevação de PC R, RPA, RNL, RPL, EPGm
Sintomas Presença e intensidade de sintomas e refratariedade
Nutricionais
Desnutrição: presença ou ausência
Sarcopenia: presença ou ausência
Caquexia: não caquético, pré caquético, caquético ou caquético refratário
Funcionalidade
ECOG‑PS: 0 a
PPS:
Pergunta clássica: “Quanto tempo o paciente viverá?
Questão surpresa: “Eu me surpreenderia se o paciente morresse em (tempo)?”
Pergunta probabilística: “Qual a probabilidade de sobrevivência do paciente em (tempo)?”
Escore Prognóstico de Glasgow modificado;
proteína C reativa; PPI: Palliative Prognostic
neutrófilo/linfócito; RPA: razão PCR albumina; RPL: razão plaqueta/linfócito.
175 C AP í TULO 12 Avaliação Prognóstica Tabela 12.1 Fatores e modelos prognósticos
ECOG‑PS: 0 a 5
5 KPS: 100% a 0 PPS: 100% a 0 Medidas fisiológi cas objetivas ângulo de fase Força de preensão manual Predição clínica de sobrevida
”
Modelos prognósticos IPI: 0 1; 2; 3; 4 5 EPGm: 0, 1 ou 2 PAP‑Score: A, B ou C PPI: A, B ou C EPGm: 0, 1 ou 2 ECOG PS: Eastern Cooperative Oncology Group Performance Status; EPGm:
ESAS: Edmonton Symptom Assessment System; IPI: International Prognostic Index; KPS: Karnofsky Performance Status; LDH: desidrogenase láctica; PAP Score: Palliative Prognostic Score; PC R:
Index;
Palliative Performance Scale; RNL: razão
Nutrição Oncológica
PROGNÓSTICO
Melhor Pior
Não desnutrido Não sarcopênico Não caquético
Intermediário
Desnutrido Sarcopênico Caquético
Desnutrido grave Sarcopênico grave Caquético refratário
Óbito
Os instrumentos que podem ser utilizados para avaliação da capacidade funcional de pa cientes com câncer estão descritos no Capítulo 2, Massa Muscular, Força Muscular e Funcio nalidade. Eles podem ser usados para caracterizar o impacto da doença em todos os seus estágios, considerando que a menor funcionalidade está associada a pior prognóstico.45 48
Medidas objetivas
O ângulo de fase (AF)49 e a força de pressão manual (FPM)50 são medidas objetivas, reprodu tíveis, não invasivas e fáceis de usar. O AF, expresso por meio da impendância bioelétrica, é um indicador de saúde e integridade da membrana celular, hidratação e estado nutricional e pode ter aplicação adicional como marcador prognóstico em pacientes com câncer (Tabela 12.5).49
Similarmente, a medida da FPM é um poderoso preditor de desfechos adversos nesse grupo.51 Além disso, Wiegert et al. (2021)50 descreveram valores de referência para FPM de adultos com câncer incurável em um estudo de coorte desenvolvido no Brasil (ver Capítulo 2, Massa Muscular, Força Muscular e Funcionalidade) e verificaram seu poder prognóstico. Quando comparados com pacientes com FPM a partir do percentil 50 dos valores de refe rência, os pacientes com FPM menor ou igual ao percentil 10 tiveram sobrevida significativa mente menor, assim como os classificados abaixo dos pontos de corte da FPM (Tabela 12.6). Cabe destacar que a comparação de medidas repetidas desses parâmetros, ou seja, a avalia ção evolutiva deles em cada paciente pode oferecer importantes considerações prognósticas.
Shachar et al.,
Fukuta et al., 201952
Aahlin et al., 201753
Wiegert et al., 202039
Menor sobrevida
Menor sobrevida livre de
Menor sobrevida
Menor sobrevida
Menor sobrevida global
Menor sobrevida global
Menor sobrevida livre de recidiva
Menor sobrevida específica do câncer
Toxicidade de QT
Complicações cirúrgicas
Menor sobrevida global
ASG PPP VR: Avaliação Subjetiva Global Produzida pelo Paciente – versão reduzida; PP: perda de peso; QT: quimioterapia;
qualidade
178 Fonte: adaptada de Cunha et al., 2021;16 Cong et al., 2020;36
no Dia a Dia Rademacher et al., 2020;37 Wiegert et al., 2020;39 Daly et al., 2020;42 Shachar et al., 2016;43 Fukuta et al., 2019;52 Aahlin et al., 2017.53
Figura 12.1 Relação prognóstica do estado nutricional em pacientes com câncer Funcionalidade
Tabela 12.4 Avaliação prognóstica por meio de alguns métodos de avaliação do estado nutricional no câncer Autor Estado nutricional Desfecho Cong et al., 202036 Desnutrição
global
recidiva Cunha et al., 202116 ASG PPP VR ≥15 pontos
global Daly et al., 202042 Grade de classificação de PP 3 e 4
global Le Rademacher et al., 202037 PP >2%
201643 Sarcopenia
Caquexia do câncer
QV:
de vida.
Le
Sintomas de Impacto Nutricional
Karla Santos da Costa Rosa
Larissa Calixto-Lima
Emanuelly Varea Maria Wiegert
Aline Pereira Pedrosa
Sintomas de Impacto Nutricional
CAPÍTULO 13
Introdução
Os sintomas de impacto nutricional (SIN) são aqueles suscetíveis a apresentar consequên cia desfavorável para a saúde do indivíduo, aumentando o risco de déficits nutricionais, sen do os principais anorexia, saciedade precoce, náuseas, vômitos, constipação intestinal (CI), diarreia, disgeusia, xerostomia, disfagia e mucosite.1,2 Esses sintomas estão frequentemente relacionados com a presença do tumor (implicação mecânica ou na absorção dos nutrien tes) e os diferentes tratamentos antineoplásicos (cirurgia, quimioterapia, radioterapia). 2,3
A existência de SIN está associada a redução da ingestão alimentar, comprometimento do estado nutricional e, por conseguinte, diminuição da qualidade de vida e da sobrevida.4‑7
Cabe ressaltar que alguns pacientes com câncer podem apresentar, além dos SIN, outros sintomas concomitantes que podem interferir na aceitação do alimento, como ansiedade, depressão, fadiga, dispneia, sonolência e dor. O caráter múltiplo dos sintomas requer ava liação inicial sistemática e o monitoramento da sua evolução, incluindo frequência e inten sidade, variação ao longo do tempo, fatores desencadeantes de agravamento e de alívio, outros sintomas associados, impacto nas atividades da vida cotidiana, impacto emocional e respostas às intervenções realizadas.8
Ferramentas diagnósticas
Há diversos instrumentos para avaliar os SIN apresentados pelos pacientes com câncer; no entanto, poucos são validados para a população brasileira.9 O instrumento NIS (do inglês, nutrition impact symptoms) (Tabela 13.1) é uma ferramenta para verificar sintomas que afetam o estado nutricional de pacientes com câncer em fase de tratamento da doença.9 O questionário inclui oito sintomas que potencialmente afetam a função ou a integridade do trato gastrintestinal (TGI) e outros quatro generalizados que podem estar associados à diminuição da ingestão nutricional.1,9,10 Outra ferramenta é o questionário de apetite e sin tomas para pacientes com câncer (CASQ; do inglês, appetite and symptoms questionnai re for patients with cancer) (Tabela 13.2), composto de 12 perguntas cujas respostas são definidas em uma escala Likert de cinco pontos.11,12
Tabela 13.1 Escala nutrition impact symptoms (NIS)
Eu tenho apetite reduzido e/ou ingestão oral reduzida por causa de:
Estomatite (aftas e/ou inflamação na mucosa da boca)
Alterações de sabor e cheiro
Disfagia (dificuldade para engolir)
Dor no estômago
Dor abdominal
Constipação intestinal (melhora do apetite após evacuações)
Diarreia
Defecação após as refeições
Dor
Dispneia (dificuldade para respirar)
Fadiga
Outros motivos (náuseas, vômito etc.)
Fonte: adaptada de Omlin et al., 2013;1 Tsunada et al., 2019.9
Sintomas de Impacto Nutricional
Nenhum (1)
Pouco (2)
Moderado (3) Muito (4)
189 C AP í TULO 13
Tabela 13.2 Questionário de apetite e sintomas para pacientes com câncer (CASQ)
Meu apetite é…
( ) ( ) ( ) ( ) ( )
Muito pouco Pouco
Médio Bom Muito bom
Quando como, eu me sinto cheio…
( ) ( ) ( ) ( ) ( )
Sem ter comido nada
Depois de comer apenas um pouco
Depois de comer cerca de um terço de uma refeição
Depois de comer mais da metade de uma refeição
Depois de comer uma refeição completa
Antes de comer, eu sinto fome…
( ) ( ) ( ) ( ) ( )
Raramente
Ocasionalmente
Boa parte do tempo
A maior parte do tempo
O tempo todo
Eu gosto da comida que como…
( ) ( ) ( ) ( ) ( )
Na maioria das vezes
Frequentemente
Algumas vezes
Raramente
Nunca
Atualmente, eu como…
( ) ( ) ( ) ( ) ( )
Menos de uma refeição por dia Uma refeição por dia Duas refeições por dia Três refeições por dia
Mais de três refeições por dia Atualmente, eu como (em adição ou em substituição às refeições)…
( ) ( ) ( ) ( ) ( )
Nenhum lanche
Um lanche por dia Dois lanches por dia Três lanches por dia
Quatro ou mais lanches por dia Comparativamente a antes de estar doente, o sabor da comida é…
( )
( )
( ) ( )
( )
190 Nutrição Oncológica no Dia a Dia Pior
Muito pior
Tão bom quanto antes Melhor
Muito melhor
(continua)
Nutrição para Prevenção e Sobreviventes do Câncer
Luciana Grucci Maya Moreira
Taiara Scopel Poltronieri
CAPÍTULO 14 Prevenção e Sobreviventes
Hábitos de vida e alimentação na prevenção do câncer
Durante muitos anos, acreditou‑se que a maior contribuição para o desenvolvimento do câncer era a genética familiar. Porém, atualmente, sabe‑se que fatores relacionados ao hos pedeiro, ao ambiente, à dieta e ao comportamento têm influência na carcinogênese, e as evidências científicas apontam para os aspectos ambientais e de estilo de vida como os principais fatores de risco para a maioria dos tipos da doença. Nesse contexto, já existem fortes evidências de que a má alimentação, o excesso de gordura corporal e a inatividade física são causas de diferentes tipos de câncer (Figura 14.1).1‑5
A Organização Mundial da Saúde (OMS) estima que entre 30% e 50% dos casos de câncer possam ser prevenidos. Para isso, é necessário fortalecer políticas e ações nacionais, a fim de aumentar a conscientização, promover estilos de vida saudáveis e reduzir a expo sição aos fatores de risco da doença.5
Recomendações para prevenção do câncer
O Instituto Nacional de Câncer José Alencar Gomes da Silva (Inca/MS), com base no Terceiro Relatório de Especialistas do Fundo Mundial de Pesquisa do Câncer, elaborou 11 recomenda ções para prevenção de câncer por meio de alimentação, nutrição e atividade física voltadas para a população brasileira, considerando o cenário epidemiológico nacional (Figura 14.2).6,7
Nutrição para Prevenção e Sobreviventes do Câncer
Epitélio normal Pré-neoplasia
Câncer invasivo CARCINOGÊNESE
Genética, epigenética, microbioma, idade, sexo, estado metabólico, estado inflamatório, função imune e outros fatores do hospedeiro
Fatores do hospedeiro
Fatores ambientais
Contaminantes em alimentos, vírus, radiação UV, carcinógenos ambientais e outros fatores ambientais
Fatores dietéticos e comportamentais
Nutrientes, consumo de energia, fitoquímicos, outros componentes dos alimentos, atividade física, álcool, tabagismo e outros fatores comportamentais
Figura 14.1 Influência da dieta, da nutrição, da atividade física, da exposição a aspectos ambientais e dos fatores do hospedeiro no processo de carcinogênese
UV: ultravioleta
Fonte: adaptada de Inca, 2020.6
209 C AP í TULO 14
Nutrição Oncológica no Dia a Dia
Evitar o consumo de alimentos ultraprocessados, bebidas açucaradas e fast-food
Limitar o consumo de carne vermelha a 500g por semana
Evitar o consumo de carne processada
Evitar o consumo de bebidas alcoólicas
Fazer dos alimentos de origem vegetal a base da alimentação
Ser fisicamente ativo como parte da rotina diária
Manter o peso corporal saudável
RECOMENDAÇÕES PARA PREVENÇÃO DE CÂNCER
Evitar o consumo de chimarrão em temperatura superior a 60°C
Não usar suplementos alimentares para a prevenção do câncer
Se possível, amamentar seu bebê
Se puder, procurar seguir essas recomendações após o diagnóstico de câncer
Figura 14.2 Recomendações para prevenção do câncer no Brasil
Fonte: adaptada de Inca, 2020.6
Manter o peso corporal saudável
Os desarranjos metabólicos causados pela obesidade são chaves para o desenvolvimento e o crescimento de células malignas. O excesso de gordura corporal ocasiona um estado inflamatório crônico de baixo grau por meio de diferentes mecanismos, o que eleva o nível circulante de adipocinas, citocinas pró‑inflamatórias e fatores de crescimento celular, impor tantes no estímulo do desenvolvimento tumoral.8‑12
O intervalo de índice de massa corporal (IMC) considerado saudável durante a infância e a adolescência varia com a idade.13 Para adultos, é 18 a 24,9 kg/estatura2(m).14
Estima‑se que, em 2012, 4,9% (21.182) dos casos e 6,9% (13.011) dos óbitos por câncer no Brasil sejam atribuídos ao excesso de gordura corporal,15 que está fortemente associado a diversos tipos de câncer (Tabela 14.1).
Ser fisicamente ativo como parte da rotina diária
A atividade física parece atuar na modulação sistêmica de fatores importantes para a re gulação de mecanismos celulares e, consequentemente, para o desenvolvimento e o crescimento tumoral, como o metabolismo de glicose e insulina, a função imunológica, o perfil inflamatório (estresse oxidativo e citocinas) e os hormônios sexuais. Ela também pode reduzir indiretamente o risco de câncer, uma vez que ajuda no controle da obesi dade.2,3,10‑12,16‑19
Crianças, adultos e indivíduos mais velhos são aconselhados a se manterem fisicamen te ativos de forma habitual e a reduzir o tempo gasto com comportamentos sedentários. É provável que o benefício da atividade física na prevenção do câncer seja proporcional à quantidade em que é praticada6,20 (Tabela 14.2).

210
Tabela 14.1 Evidências sobre a relação entre gordura e peso corporal e o risco de desenvolvimento de câncer
Variáveis
Excesso de gordura corporal na fase adulta
Localização do tumorNível de evidência
Boca, laringe e faringe Estômago (porção cárdia)
Vesícula biliar Próstata avançado Ovário
Excesso de gordura corporal na fase adulta Esôfago (adenocarcinoma) Pâncreas Fígado Cólon e reto Mama pós menopausa Endométrio Rim
Evidência provável de aumento do risco
Evidência convincente de aumento do risco
Ganho de peso na idade adultaMama pós menopausaEvidência convincente de aumento do risco
Alto peso ao nascer
Excesso de gordura corporal na idade adulta
Excesso de gordura corporal na idade adulta jovem (18 a 30 anos)
Mama pré menopausaEvidência provável de aumento do risco
Mama pré menopausaEvidência convincente de aumento do risco
Mama pré e pós menopausaEvidência convincente de aumento do risco
Fonte: adaptada de Inca, 2020;6 WCRF/AICR, 2018.21
Tabela 14.2 Evidências disponíveis para a relação entre os níveis de atividade física e o risco de desenvolvimento de câncer
Variáveis
Atividade física (moderada e vigorosa)
Localização do tumor/ relação com câncer
Cólon e reto
Nível de evidência
Evidência convincente de diminuição do risco
Mama pós menopausaEvidência provável de diminuição do risco
Endométrio
Atividade física aeróbica (moderada e vigorosa)
Atividade física (vigorosa)
Caminhada
Tempo de tela (comportamento sedentário) em crianças
Tempo de tela (comportamento sedentário) em adultos
Risco de ganho de peso, sobrepeso e obesidade
Mama pré e pós menopausa
Risco de ganho de peso, sobrepeso e obesidade
Risco de ganho de peso, sobrepeso e obesidade
Risco de ganho de peso, sobrepeso e obesidade
Fonte: adaptada de Inca, 2020;6 WCRF/AICR, 2018.20
Nutrição para Prevenção e Sobreviventes do Câncer
Evidência provável de diminuição do risco
Evidência provável de diminuição do risco
Evidência provável de diminuição do risco
Evidência convincente de diminuição do risco
Evidência convincente de aumento do risco
Evidência provável de aumento do risco
211 C AP í TUL O 14
A Oncologia evoluiu excepcionalmente ao longo dos últimos anos e com ela a compreensão da nutrição como pilar fundamental para a prevenção e o tratamento do câncer. Diante das diferentes faces da nutrição oncológica, as autoras desta obra organizaram um guia prático e didático, com informações de alta qualidade científica relativas ao atendimento nutricional de pacientes com câncer na prática cotidiana.
O livro é composto por 14 capítulos que abordam de forma objetiva as principais vertentes dos cuidados nutricionais em oncologia, a saber: avaliação do estado nutricional, incluindo aspectos relacionados a avaliação da massa muscular, funcionalidade e prognóstico; planejamento dietoterápico nas diferentes fases do tratamento antineoplásico, como quimioterapia, radioterapia, cirurgia, terapia intensiva, transplante de células-tronco hematopoiéticas e cuidados paliativos; manejo dos sintomas de impacto nutricional; uso de nutrientes adjuvantes e dietas restritivas; assim como a nutrição para prevenção e sobreviventes do câncer. Para tanto, foram preconizadas as recomendações nutricionais mais recentes publicadas pelas principais sociedades nacionais (Diten) e internacionais (Aspen e Espen).

Nutrição Oncológica no Dia a Dia oferece informações de forma dinâmica e sistematizada, fundamentadas em tabelas e apoiadas por textos concisos, com o uso de cores diversas que facilitam o entendimento do leitor. Certamente, é uma ferramenta que ajudará a melhorar o atendimento nutricional a pacientes com câncer, seja em consultório, hospitais ou domicílio.








Áreas de interesse Nutrição Oncologia 9 786588 34044 8
