
Escanéame para la reconciliación



Escanéame para la reconciliación

Liofilizado y disolvente en suspensión inyectable para bovino. Cada dosis de 2 ml contiene: Liofilizado: Herpes Virus Bovino tipo 1 vivo con deleción genética doble gE- tk- (BoHV-1), cepa CEDDEL: 106,3 – 107,3 DICC50 Disolución tampón de fosfato. Especies de destino: Bovino (terneros y vacas). Para la inmunización activa de bovino a partir de los 3 meses frente al Herpes Virus Bovino, tipo 1 (BoHV-1) para reducir los signos clínicos de la Rinotraqueítis bovina infecciosa (IBR) y la excreción del virus de campo.
21 días después del programa de vacunación básico. 6 meses después del programa de vacunación básico. Solo se deben vacunar animales sanos. En raras ocasiones se han notificado reacciones de hipersensibilidad, incluida la anafilaxia (a veces fatal). Laboratorios Hipra, S.A., Amer (Girona), ESPANA.
5 dosis: EU/2/10/114/001. 30 dosis: EU/2/10/114/003.


Vacuna trivalente frente al virus de la Diarrea Vírica Bovina, el virus de la Parainfluenza tipo 3, y el virus Respiratorio Sincitial Bovino. Liofilizado y suspensión para preparación de suspensión inyectable para bovino. Fracción liofilizada: Virus Respiratorio Sincitial Bovino, vivo atenuado, cepa Lym-56 ≥ 104 CCID50.* I *CCID50: Dosis infectiva 50% en cultivo celular. Fracción líquida: Virus de la Parainfluenza-3 inactivado, cepa SF4: IHA* ≥ 16. Virus de la Diarrea Vírica Bovina inactivado, cepa NADL:SN** ≥ 20. * IHA: Titulo medio de inhibición de la hemaglutinación inducido en conejos (≥ 480 UHA antes de la inactivación). ** SN: Titulo medio de inhibición de la ser neutralización inducido en conejos (≥ 106 DICT50 antes de la inactivación). Bovinos adultos (vacas y novillas): Prevención de la Diarrea vírica bovina (incluida la enfermedad de las mucosas) (BVD). Terneros: Prevención de la Parainfluenza-3 (PI3), Enfermedad de las mucosas o Diarrea vírica bovina (BVD) y Neumonía por Virus Respiratorio Sincitial Bovino (BRS). Puede utilizarse en cualquier momento durante la gestación y durante la lactancia. Conservar y transportar entre +2 y +8oC. No congelar. Mantener fuera del alcance de los niños.

Superando a duras penas a las intensas sequías, olas de calor y fuertes lluvias torrenciales que llevan azotando a nuestro territorio en lo que llevamos de año, el sector bovino se enfrenta a una nueva amenaza sanitaria, el avance de la Enfermedad Hemorrágica Epizoótica (EHE).
Las condiciones meteorológicas extremas de las que ya nos avisaban los científicos hace décadas son una certeza innegable con previsiones de episodios de temperaturas extremas, sequías y tempestades cada vez más frecuentes e intensas.
Han corrido ríos de tinta sobre la contribución del sector ganadero al Cambio Climático. Sin embargo, un aspecto que requiere una atención y preparación pormenorizada es el impacto que tendrá en la producción ganadera.
Lo primero que se nos viene a la cabeza es el aumento de las temperaturas, con olas de calor cada vez más prolongadas que pondrán a prueba nuestra capacidad para mitigar el estrés térmico en los animales, un fenómeno que tiene serias consecuencias para su salud y productividad, pudiendo observarse un aumento de la mortalidad, mayor propensión a desarrollar infecciones por un debilitamiento del sistema inmunitario y pérdidas de rendimiento reproductivo.
Por ello, la adaptación de las instalaciones y la optimización de los sistemas de climatización para lograr unas condiciones ambientales adecuadas con un consumo energético mínimo son objetivos que deben estar contemplados dentro de la estrategia de toda granja para hacer frente al Cambio Climático.
Las condiciones climáticas extremas condicionan los rendimientos y la calidad de los cultivos de materias primas para alimentación animal, lo que, unido al incremento de los costes y al agotamiento de los recursos hídricos, requerirá de la aplicación de medidas destinadas a maximizar el aprovechamiento y minimizar el desperdicio de estos recursos tan valiosos.
En este sentido, las estrategias basadas en la economía circular, el aprovechamiento de subproductos agroindustriales y la selección de animales con mayor capacidad de aprovechamiento de los recursos son estrategias que merecen ser exploradas.
En el ámbito sanitario, la tropicalización del clima conlleva un mayor riesgo de emergencia de enfermedades transmitidas por artrópodos vectores en áreas nuevas debido a cambios que favorecen su proliferación y, con ello, la propagación de patógenos.
Ejemplo de ello es la actual expansión de la Enfermedad Hemorrágica Epizoótica (EHE) cuya prevención, a falta de una vacuna eficaz, solo puede prevenirse con medidas enfocadas en evitar las picaduras de los mosquitos Culicoides spp. Esperemos que el otoño e invierno traigan consigo unas condiciones más inhóspitas para estos vectores que contribuyan a frenar su avance, al menos, por ahora…

Estos son solo algunos ejemplos de cómo el Cambio Climático impactará al sector ganadero, siendo fundamental comprender en profundidad los puntos vulnerables de forma que se puedan implementar políticas y adoptar medidas que tengan en cuenta el contexto socioeconómico de las granjas y que permitan una sostenibilidad efectiva a largo plazo.
EDITOR
GRUPO DE COMUNICACIÓN AGRINEWS S.L.
PUBLICIDAD
Laura Muñoz +34 629 42 25 52 laura@mediatarsis.com
Luis Carrasco +34 605 09 05 13 lc@agrinews.es
DIRECCIÓN TÉCNICA
Christian de la Fe Rodríguez
Luis Miguel Jiménez Galán
REDACCIÓN
Daniela Morales
Osmayra Cabrera
COLABORADORES
Carlos Ramón Romero Sala
Fernando Bacha
Foix Queraltó
Gema Chacón
María Fernández
ADMINISTRACIÓN
Mercè Soler
Tel: +34 93 115 44 15
info@grupoagrinews.com www.rumiantes.com
Precio de suscripción anual: España 30 € Internacional 90 €
DIRIGIDA A VETERINARIOS DE RUMIANTES
Depósito legal rumiNews B-8798-2019
ISSN (Revista impresa): 2696-8185
ISSN (Revista digital): 2696-8193
Revista trimestral
Pero más allá de las variaciones térmicas, las amenazas vienen en la forma de escasez de recursos naturales y retos sanitarios.
La dirección de la revista no se hace responsable de las opiniones de los autores. Todos los derechos reservados. Imágenes: Noun Project / Freepik/Dreamstime/BioRender
4
Bioseguridad global en riesgo, ¿estamos preparados?
Dr. Hugo Estavillo, DMV Consultor y Capacitador para Latinoamérica en Buenas Prácticas Ganaderas, Trazabilidad y Bienestar Animal
La globalización, el aumento de la población mundial y la variación acelerada de las características de los patógenos hacen que sea urgente mejorar las medidas de control de las enfermedades, con especial énfasis en las zoonosis.
Enfermedades clostridiales en ganado bovino 11
Cristina Baselga y Oihane Alzuguren
Exopol S.L.
Las clostridiosis son enfermedades infecciosas no contagiosas que, en la mayoría de las ocasiones, son de carácter agudo y terminan con la muerte del animal.
20
Boehringer Ingelheim pone el foco en el pasado, presente y futuro de la BVD
Servicio Técnico de Boehringer Ingelheim
Animal Health España
Navegando la burocracia ganadera: Nueva ordenación de explotaciones bovinas
Foix Queraltó Salguero
Veterinaria Oficial
El Real Decreto 1053/2022 establece las normas fundamentales para la ordenación zootécnica y sanitaria de las explotaciones de ganado bovino.
Uso de grasas en nutrición bovina 40
Aníbal Fernández Mayer
Nutricionista EEA INTA Bordenave (CERBAS) MSc y Doctor en Cs Veterinarias


El suministro de grasas protegidas es apropiado para vacas de alta producción, pero debe calcularse correctamente su proporción.
Colina, aliada frente al hígado graso y la cetosis 46
Luis Felipe Hernández Calderón
Asesor Técnico en Rumiantes
La suplementación con colina en vacas en periodo de transición tiene un efecto positivo más allá de prevenir la acumulación de grasa.
Mortalidad de terneros por deficiencia de selenio en un rebaño de raza Wagyu
Ángel Revilla Ruiz1 , Javier Brieva Saenz 2 y Juan Vicente González Martín3
1Residente del Colegio Europeo de Medicina Bovina (ECBHM). Facultad de Veterinaria, UCM
2Bricalvet Servicios Veterinarios
3Profesor Titular Dpto. de Medicina y Cirugía Animal, Facultad de Veterinaria, UCM. TRIALVET Asesoría e Investigación Veterinaria SL
En este artículo se presenta el caso de un rebaño de terneros de raza Wagyu con una alta tasa de mortalidad.

Micotoxicosis en vacasPatogénesis, signos y lesiones
Sabry El-khodary
Profesor de Medicina Interna y Vicedecano de Estudios de Postgrado e Investigación, Facultad de Medicina Veterinaria de la Universidad de Mansoura, Egipto
Tradicionalmente, los rumiantes se han considerado menos vulnerables a las micotoxinas, pero aquellas que son capaces de resistir la degradación en el rumen pueden causar signos clínicos de intoxicación.
La paratuberculosis, “algo más” que una infección crónica en los pequeños rumiantes
Christian de la Fe, Antonio Sánchez, Joaquín Amores, Xóchitl Hernández y Juan Carlos Corrales
Grupo de Investigación Sanidad de Rumiantes, Departamento de Sanidad Animal, Facultad de Veterinaria, Universidad de Murcia. Campus Regional de Excelencia Internacional Mare Nostrum
La Paratuberculosis es una infección compleja cuyos efectos, enmascarados en muchos momentos, han motivado que no se le haya prestado atención a la hora de plantear estrategias de control efectivas.
Abordaje sostenible al control parasitario en pequeños rumiantes
Leyla Ríos de Álvarez
Profesora Asistente Extensión/Investigación, Department of Animal and Dairy Sciences, Mississippi State University



El abordaje sostenible al control parasitario se basa en usar alternativas que eviten resistencias y la aparición de enfermedades.
Agradecemos a nuestros anunciantes por hacer posible la publicación de esta revista: Arvet Veterinaria, Bioplagen, Boehringer Ingelheim Animal Health, Elanco, Hipra, Lidervet, Qualivet, Syva y Vetia Animal Health.
La báscula CIMA Control Cattle permite el pesaje de vacas y terneros en movimiento, sin tener que encerrarlos o detenerlos.

Peso a la entrada de los terneros. Curvas de crecimiento.
Peso a la carga para matadero.
Peso de la primera cubrición de las novillas.
Peso al parto.
Variaciones de peso de las vacas.
Asociacion a identificación electronica, Crotales FDX i HDX by Rango de peso entre 25 kg1.200 kg.

 Dr. Hugo Estavillo, DMV Consultor y Capacitador para Latinoamérica en Buenas Prácticas Ganaderas, Trazabilidad y Bienestar Animal he@trazur.com.uy
Dr. Hugo Estavillo, DMV Consultor y Capacitador para Latinoamérica en Buenas Prácticas Ganaderas, Trazabilidad y Bienestar Animal he@trazur.com.uy
La reciente pandemia encontró al mundo algo distraído, aunque desde hace ya varios años algunos profesionales venimos alertando de los riesgos sanitarios que vive, al que voy a denominar, el “sistema semicerrado - mundo”
El 60% de los patógenos que causan enfermedades en los seres humanos provienen de los animales domésticos y salvajes.
El 75% de los patógenos humanos emergentes son de origen animal.
El 80% de los patógenos utilizados en bioterrorismo son de origen animal.
Este análisis de la OIE debería haber sido suficiente para tomar las precauciones correspondientes hace bastante tiempo:
Se necesitarán el 70% de proteínas de origen animal adicionales para alimentar al mundo en 2050.
Más del 20% de la producción animal mundial se pierde por enfermedades de los animales.
Varios son los factores que pueden haber incidido en esta situación, pero cabe resaltar uno que, tal vez, es de los más relevantes desde que el ser humano comenzó a producir sus propios alimentos.
Hace 10.000 años, el ser humano y sus animales de producción formaban menos del 0,1% de la biomasa de vertebrados terrestres, mientras que en 2007 componían el 98% de la biomasa

Es crucial entender la conexión entre biodiversidad, ecosistema y las enfermedades infecciosas.
Las enfermedades de los animales ponen en riesgo la rentabilidad de las comunidades rurales que dependen de la producción ganadera.
Es más que evidente el desequilibrio en el ecosistema que provoca esta variable, pero el asunto no termina aquí, sino que el aumento de la población humana mundial sigue en ascenso (Figura 1)
Se estima que para el año 2050 seremos sobre 10.000.000.000 de habitantes en el planeta.
Figura 1. Incremento de la población humana a nivel mundial (1750-2050) (Fuente: United Nations, 1999).Actualmente, según la OIE, la humanidad se enfrenta a varios retos críticos:
El desafío más relevante es proveer de alimentos a una población creciente, según la proyección estimada, por lo menos hasta el 2050.
No vamos a profundizar en los beneficios de la proteína animal en la alimentación humana ya que existen multitud de trabajos sobre este tema.
Sin embargo, debemos recordar que hacia el 2050 debemos superar en un 70% el aporte de proteínas de origen animal y, al mismo tiempo, según las estimaciones, los ganaderos pierden un 20% por enfermedades de los animales La presión de algunos intereses comerciales y filosóficos por sustituir las proteínas de origen animal en la alimentación humana es cada vez mayor, y es responsabilidad de todos los agentes del sector ganadero contrarrestar estas tendencias ya que, definitivamente, somos la fuente más eficaz y eficiente para satisfacer las necesidades primordiales de alimentación en combinación con otras, sin duda.
Por otro lado, debemos tener en cuenta la situación medioambiental ya que la desertificación conlleva la pérdida de áreas aptas para la ganadería y agricultura.
En resumen, el desafío de los ganaderos es producir más, con menor superficie apta para la ganadería, y tratar de disminuir las pérdidas por enfermedades.

SALUD MUNDIAL
A estas alturas ya es más que evidente que el concepto “ONE HEALTH - UNA SOLA SALUD” es la visión que debemos tener los profesionales relacionados con la salud animal, humana y el medioambiente.

IDENTIFICACIÓN Y TRAZABILIDAD 1
Agente y su origen Poblaciones susceptibles
Vías de ingreso
En este sentido, toman relevancia la identificación y trazabilidad animal, la vigilancia epidemiológica y la gestión de puntos críticos de control.
La globalización, el aumento de la población mundial y la variación acelerada de las características de los patógenos hacen que sea urgente mejorar las medidas de control de las enfermedades, con especial énfasis en las zoonosis.
Fronteras
Vectores
Vehículos
PLAN DE DIAGNÓSTICO PRECOZ 2
ANÁLISIS DE INCIDENCIA 3
RECOMENDACIONES 4
VIGILANCIA EPIDEMILÓGICA“Hay mucho por hacer a través de la visión de ONE HEALTHUNA SOLA SALUD”.
La triada médicos humanos - médicos veterinarios - ambientalistas debe preocuparse por mejorar y alcanzar una BIOSEGURIDAD MUNDIAL:
Salud humana y animal
Inocuidad alimentaria
Seguridad alimentaria
Sostenibilidad medioambiental
Es la aplicación de una secuencia de medidas que interactúan entre sí, que son repetibles, fáciles de aplicar y que mejoran la eficacia y eficiencia de la producción:
Identificación y Trazabilidad Animal
Identificación y Georreferenciación de la finca
Plan Sanitario
Vigilancia epidemiológica de la finca

Bienestar animal
Bienestar de los trabajadores
Siguiendo las recomendaciones de la Norma ISO-9000, es aconsejable organizarse en un sistema basado en procesos
Se entiende por proceso como el “conjunto de actividades mutuamente relacionadas que interactúan, transformando entradas en salidas con algún valor agregado”. En todo sistema, un proceso puede ser el punto de entrada a otro y también la salida de otro.
Existen varias herramientas para trabajar, pero se debe utilizar de forma ordenada y sincronizada, siendo la aplicación de las Buenas Prácticas la única forma de ser eficaz y eficiente en los resultados
En muchos ámbitos ya es muy común la aplicación de este sistema, pero todavía falta mucho por hacer a nivel de la producción de alimentos, principalmente en ganadería.
Cuidado del medioambiente
Las Buenas Prácticas Ganaderas pueden aplicarse a efectos de mejorar la eficacia y eficiencia de las granjas, pero además se pueden certificar mediante protocolos internacionales, nacionales o de un grupo de productores, logrando de esta forma brindar al consumidor la confianza de calidad, inocuidad y origen del alimento consumido.
La producción primaria es uno de los principales eslabones en la cadena de producción alimentaria y, por tanto, la trazabilidad y la aplicación de buenas prácticas debe ser un hilo conductor a lo largo de toda ella, desde el campo al plato.

1 4 3 2



En la producción primaria, el futuro está en la implementación de las Buenas Prácticas Ganaderas como concepto holístico en todas las actividades que se desarrollan para producir alimentos de origen animal de calidad e inocuos, contribuyendo así a la sostenibilidad de un medio ambiente armónico con la vida sobre el planeta Tierra.

Bioseguridad global en riesgo, ¿estamos preparados?


DESCÁRGALO EN PDF
ACCEDER A BIBLIOGRAFÍA
Las clostridiosis son enfermedades infecciosas no contagiosas de gran relevancia en la ganadería, ya que en la mayoría de las ocasiones son de carácter agudo (con curso de 24-48 horas) y terminan con la muerte del animal.

Estas enfermedades están causadas por bacterias del género Clostridium que se caracterizan por crecer en condiciones de anaerobiosis y sobrevivir en el medio ambiente durante largos períodos de tiempo en condiciones desfavorables gracias a su forma vegetativa (esporas).
 Cristina Baselga y Oihane Alzuguren Exopol S.L.
Cristina Baselga y Oihane Alzuguren Exopol S.L.
Muchas de las especies de clostridios son comensales del tracto intestinal de los animales y el ganado convive con estas bacterias sin manifestar ninguna enfermedad.
Sin embargo, cuando las condiciones son favorables para la multiplicación de las bacterias, invaden los tejidos del organismo, normalmente con un desenlace fatal.

Las enfermedades clostridiales suelen aparecer de manera repentina y, en muchas ocasiones, no se observan signos clínicos previos a la muerte.
Este curso agudo, la naturaleza explosiva de los brotes y las lesiones observadas al realizar la necropsia son útiles para diagnosticar las clostridiosis.

El movimiento de animales infectados o portadores, así como de productos animales contaminados (huesos, pieles y carne), puede ayudar a la propagación de estas bacterias a áreas previamente no contaminadas.
A excepción de alguna especie de Clostridium, la mayoría se encuentran de forma natural en las explotaciones por lo que debe mantenerse un buen programa de vacunación frente a ellos, evitando de esta forma futuros problemas.
No obstante, es importante tener en cuenta los síntomas y lesiones observadas en los animales y los resultados del diagnóstico laboratorial, para establecer un plan de prevención efectivo en la granja.
En la Tabla 1 se muestran las especies de clostridios más habituales que afectan al ganado bovino y las características de las enfermedades que provocan.
Nombre enfermedad Especie bacteriana Naturaleza de las toxinas Factores predisponentes Signos clínicos
EDEMA MALIGNO C. septicum (también C. sordellii, C. chauvoei y C. novyi) Histotóxicas Entrada a través de heridas
PIERNA NEGRA (CARBUNCO SINTOMÁTICO) C. chauvoei Histotóxicas
EDEMA HEMORRÁGICO CERVICAL AGUDO (GANGRENA GASEOSA) C. sordellii Histotóxicas
Entrada a través de heridas o por ingestión Época cálida Estrés
Entrada a través de heridas (rara vez) Cambios de dieta Mayor predisposición en otoño/invierno
HEMOGLOBINURIA BACILAR C. haemolyticum Histotóxicas
Infección vía oral Lesiones hepáticas causadas por trematodos
ENFERMEDAD NEGRA HEPATITIS NECRÓTICA INFECCIOSA C. novyi Histotóxicas
Infección a través de heridas o ingestión Lesiones hepáticas causadas por trematodos
Mayor predisposición en otoño/invierno
ENTEROTOXEMIA C. perfringens Enterotóxicas
Estrés Cambios de dieta Encalostramiento deficiente Enfermedad entérica previa
TÉTANOS C. tetani Neurotóxicas
Entrada de la bacteria o las toxinas a través de heridas
Lesiones
Enfisema y edema en la zona de la herida Fiebre Depresión Enfisema y edema en la zona de la herida
Cojera Fiebre Depresión Enfisema y edema bajo la piel Muerte en 12-48 h
Fiebre
Depresión
Enfisema y edema subcutáneo Muerte en 24-48 h
Palidez de mucosas
Inapetencia
Dolor abdominal
Hemoglobinuria Ictericia
Bajada drástica de la producción láctea
Muerte en 12 h - 4 días
Estreñimiento
Letargo
Disminución del apetito Disminución frecuencia cardiaca y pulmonar
Disminución del apetito
Diarrea sanguinolenta
Dolor abdominal
Ataxia
Depresión
Opistótonos
Parálisis tetánica
Temblor
Rigidez muscular
Dificultad para tragar y masticar
Convulsiones
Hipersensibilidad a luz, sonido y movimiento
Muerte en 3-10 días
Parálisis flácida
Espuma por los orificios Necrosis, edema y enfisema en los músculos afectados Subcutáneo con exudado sanguinolento y gas Hígado con lesiones gaseosas
Enfisema y edema subcutáneo Hígado con lesiones gaseosas
Necrosis hepática Ictericia
Edema y necrosis hepática
Enteritis necrótica/ hemorrágica
Abomasitis
Riñón pulposo
Apenas se observan lesiones, únicamente en la zona de penetración de la toxina/bacteria
BOTULISMO C. botulinum Neurotóxicas
Ingestión de toxinas procedentes del agua o alimentos contaminados
Debilidad
Falta de coordinación
Depresión
Parálisis
No hay lesiones evidentes
En la mayoría de las clostridiosis, salvo en tétanos y botulismo, se observa rigidez cadavérica y la autolisis de los órganos es rápida.

Debido a la baja prevalencia de casos de tétanos y botulismo, los siguientes apartados sobre el diagnóstico laboratorial y las medidas de control se centrarán en las clostridiosis causadas por C. septicum, C. chauvoei, C. sordellii, C. haemolyticum, C. novyi y C. perfringens.
A la hora de realizar una primera aproximación al diagnóstico clínico y seleccionar las muestras a enviar al laboratorio el tiempo transcurrido entre la muerte del animal y la realización de la necropsia es determinante
El cuadro clínico de la enfermedad clostridial es muy característico y, en la mayoría de las ocasiones, el diagnóstico del proceso se basa únicamente en el diagnóstico clínico. Sin embargo, es aconsejable realizar el diagnóstico etiológico en el laboratorio para conocer qué especie de clostridio está causando las lesiones y poder tomar las medidas oportunas.
Se recomienda que la toma de muestras para confirmar la etiología del proceso se realice en animales que hayan causado baja en un máximo de 6 horas previas a la necropsia, especialmente en la época estival, cuando las temperaturas son más elevadas y el proceso de autolisis avanza más rápido.
Los clostridios se encuentran tanto en el ambiente como en el interior del organismo. Por ello, con la muerte de un animal, y a medida que avanza el tiempo, estas bacterias proliferan y pueden provocar lesiones postmortem que lleven a un diagnóstico erróneo. 6h
Los órganos con las lesiones típicas (congestión generalizada del órgano y necrosis) son los adecuados para realizar se recogen
El diagnóstico laboratorial se puede realizar mediante diversas técnicas (Tabla 2).
Técnica laboratorial Ventajas Limitaciones
Muy sensible y rápida
qPCR (PCR a tiempo real)
Permite detectar, cuantificar y realizar el toxinotipado de ciertas especies de Clostridium para valorar su implicación en el proceso
Cultivo microbiológico
Permite aislar la cepa para realizar estudios en mayor profundidad, como caracterización y determinación de la sensibilidad antibiótica
Identificación de las toxinas mediante pruebas ELISA
Permite asociar la lesión con la presencia de toxinas
Tabla 2. Ventajas y limitaciones de las principales técnicas laboratoriales empleadas en el diagnóstico de clostridiosis.
Cuando se presencian bajas súbitas en la granja, se debe realizar un diagnóstico diferencial con otras enfermedades además de las clostridiosis como:

Ántrax (Carbunco bacteridianoBacillus anthracis)
Leptospirosis
Intoxicación por plantas o sustancias químicas
Hipomagnesemia
Enfermedades hemoparasitarias
Detecta el material genético, por lo que no se pueden hacer estudios posteriores sobre aislamientos
Requiere que las bacterias sean viables
Al ser bacterias ubicuas, el aislamiento de la cepa no es un diagnóstico definitivo
En general, las toxinas tienen una vida media corta y se degradan rápidamente
Estas enfermedades tienen orígenes y lesiones muy diferentes. Por ello, ante casos de muertes repentinas, es muy importante realizar una anamnesis detallada para poder enfocar el diagnóstico laboratorial a un número reducido de enfermedades compatibles.
A continuación, se muestra la prevalencia observada en casos analizados en el laboratorio Exopol durante el periodo 2018-2023.
El análisis de los clostridios que proliferan en los órganos parenquimatosos y liberan allí las toxinas se realiza en Exopol con el panel diagnóstico de clostridiosis sistémicas que detecta mediante qPCR la presencia de:
C. chauvoei
C. novyi
C. sordellii
C. septicum
C. haemolyticum
El diagnóstico de C. perfringens se realiza mediante qPCR sobre muestras digestivas, ya que prolifera en este órgano y son sus toxinas las que viajan hasta los órganos parenquimatosos.
El panel de clostridiosis sistémica se realizó sobre 66 muestras clínicas y la detección de C. perfringens sobre 150 casos clínicos.
Los resultados mostrados en la Gráfica 1 corresponden a muestras en las que se han detectado concentraciones altas y moderadas de las distintas especies de clostridios (Cq inferior a 33).
La mera detección de clostridios en las muestras clínicas no confirma su implicación en las lesiones observadas, por tanto, se considera que un resultado positivo en concentración baja (Cq por encima de 33) no confirma un caso de clostridiosis.

Gráfica 1. Porcentaje de muestras positivas (Cq<33) a las especies de Clostridium más prevalentes en casos compatibles con clostridiosis recibidos en Exopol en el periodo 2018-2023.

En el panel de clostridiosis sistémica, C. haemolyticum fue la especie más prevalente con un 32% de las muestras clínicas positivas, seguido de C. sordellii y C. septicum, detectándose en el 20% y 18% de los casos analizados, respectivamente.
C. chauvoei y C. novyi se encontraron en un porcentaje muy bajo de los casos analizados (3% y 2%, respectivamente).
Cabe destacar que en el 47% de las muestras positivas se detectó más de una especie de clostridio.
Un 42% de los casos analizados con clínica compatible con clostridiosis resultaron negativos al panel realizado, descartando por un lado la implicación de estas bacterias en el proceso y haciendo sospechar de otros agentes infecciosos o no infecciosos como causa de las bajas súbitas observadas en la granja.
Los resultados obtenidos revelan que en el 60% de los casos compatibles con enterotoxemia se detectó C. perfringens en concentraciones medias y altas, lo que pone de manifiesto la importancia de la enterotoxemia en los casos de bajas súbitas, siendo normalmente una patología de etiología múltiple.
En los casos compatibles con enterotoxemia, el 21% resultaron negativos.
Dado que la enterotoxemia o la patología digestiva es de etiología múltiple, lo recomendado en este caso sería la realización de un diagnóstico diferencial con otros agentes causantes de patología digestiva.
Aunque las clostridiosis son enfermedades presentes en todas las granjas, podemos observar que el volumen de casos clínicos analizados es reducido. Esto puede atribuirse a la baja prevalencia de las clostridiosis gracias a la amplia vacunación que se realiza frente a estos patógenos.
Las herramientas terapéuticas para las clostridiosis son limitadas debido a la rápida evolución de estas patologías, siendo el tratamiento con antitoxinas, antibióticos y antiinflamatorios costoso y pocas veces resulta eficaz.
Por ello, implementar estrategias de prevención basadas en el diagnóstico laboratorial de la patología de la granja siempre es la mejor opción, siendo importante:
Adoptar buenas prácticas de manejo e higiene de las herramientas utilizadas durante la aplicación de medicamentos
Reducir el riesgo de lesiones o heridas
Evitar los cambios bruscos de dieta Prevenir mediante la vacunación
La vacunación es uno de los pilares más importantes en la prevención de las clostridiosis. De hecho, la vacuna de clostridios es la más generalizada en el sector, pues su eficacia en la reducción de la morbilidad y mortalidad en los rebaños está más que demostrada.
El protocolo vacunal a utilizar dependerá de:
El plan sanitario elaborado por el veterinario de explotación
La vacuna comercial y su ficha técnica.
Además, es importante tener en cuenta los factores individuales de cada ganadería, como la ubicación geográfica, el sistema de producción y los riesgos específicos.
Enfermedades clostridiales en el ganado bovino DESCÁRGALO EN PDF
Porque importa
A las clostridiosis, mejor plantarles cara










Protección frente a 9 tipos de clostridios


2 Autorizada en gestantes y lactantes
A partir de la 2ª semana de vida*

3
* Si proceden de madres no vacunadas.
Proteger frente a 9 tipos de clostridios, es la tranquilidad de saber que lo estás haciendo bien
SYVA·BAX


































Vacuna inactivada polivalente en suspensión inyectable Uso veterinario. Medicamento sujeto a prescripción veterinaria. En caso de duda consulte a su veterinario.

La I Jornada de los Premios BVDzero reunió a medio centenar de veterinarios y fue el punto de partida de los Premios BVDzero 2023


El pasado mes de junio, la sede de Boehringer Ingelheim España, ubicada en Sant Cugat del Vallés, acogió la I Jornada de los Premios BVDzero.
Con la Diarrea Vírica Bovina (BVD) como protagonista, el evento reunió a medio centenar de veterinarios en torno a un completo programa de ponencias inaugurado por Nacho de Blas.
Servicio Técnico de Boehringer Ingelheim Animal HealthEl profesor titular de la Facultad de Veterinaria de la Universidad de Zaragoza, expuso de forma muy didáctica la importancia de los datos y la estadística en los estudios de campo.

Posteriormente, llegó el turno de una amplia revisión y análisis de la BVD.
Con el objetivo de analizarla al detalle, la jornada contó con la participación de Juanma Loste, Javier Diéguez y Susana Astiz para abordar el pasado, presente y futuro de la BVD desde tres puntos de vista:
Clínico
Diagnóstico y control
Epidemiológico
Hablar de la BVD es hablar de la enfermedad vírica más frecuente en el ganado bovino. En palabras de Juanma Loste (veterinario clínico de Albaikide), se trata de la “enfermedad vírica de ganado bovino que más pérdidas produce en todo el mundo”.

Es, por tanto, un tema que preocupa y capta el interés de la comunidad veterinaria y ganadera.
Desde el punto de vista veterinario, la visión de la enfermedad en los últimos 25 años ha cambiado mucho, paralelamente con el papel de los veterinarios en las granjas, tal como explica Juanma Loste:
“Al principio, para nosotros era una enfermedad clínica y solo actuábamos cuando aparecía un animal enfermo o una sospecha de animal persistentemente infectado (PI), con enfermedad de las mucosas… Esto ha ido cambiando y hemos ido buscando la enfermedad, monitorizando las granjas y adelantándonos a la presencia del virus”.
Esta es una opinión que respalda ampliamente Javier Diéguez (Universidad de Santiago de Compostela), quien añade su valoración desde el ámbito del diagnóstico donde, según reconoce, ha habido bastantes cambios.



“Uno de los primeros cambios es que, tradicionalmente, nos basábamos en un diagnóstico individual y en la actualidad lo que se hace es no esperar a que aparezcan los problemas sino tratar de prevenirlos. Esto ha llevado a que se haya pasado de técnicas de diagnóstico basadas en el individuo a técnicas más basadas en el conjunto”, explica.
También ha ido cambiando la forma de luchar contra la enfermedad, tal y como señala Juanma Loste:
Primero con vacunas polivalentes de eficacia reducida.
Luego, poco a poco introdujimos vacunas monovalentes con cierta protección fetal.
Hace unos años apareció Bovela®, que supuso un cambio en la manera de afrontar la enfermedad.
A nivel epidemiológico, los aspectos más relevantes para la BVD son “la altísima prevalencia con la que empezamos en prácticamente todas las regiones, la variabilidad genética y una epidemiología de la enfermedad muy peculiar” explica Susana Astiz (INIA-CSIC).


“Prácticamente en todos los sitios damos por hecho que la prevalencia es altísima, quitando excepciones de países o regiones muy concretas. Lo cierto es que, donde no imponemos sistemas de control obligatorios y bien impuestos, la BVD campa a sus anchas”, afirma Susana Astiz.
En este sentido, Susana tiene claro que:
“La vacunación es fundamental, sobre todo en países en los que comenzamos con una alta incidencia, un programa de control y la existencia de factores de riesgo que nos distorsionan mucho, como la gran densidad de animales y/o una gran circulación de animales. En España importamos mucho y tenemos mucha densidad, con lo que comenzar un programa de control sin vacunación sería muy arriesgado y asumiría un coste económico enorme”.
Llegados a este punto, da un paso más allá y compara las vacunas vivas de última generación contra la BVD frente a las vacunas inactivadas.
En este sentido, apunta que “la principal ventaja de las vacunas vivas de última generación es su gran eficacia en la protección fetal que, cercana al 100%, es una herramienta muy potente para controlar la BVD, ya que el PI es el principal foco mantenedor de la infección”.
Hablando de programas de control, lo cierto es que en la actualidad solo en Galicia existe un Plan de Control de la BVD. Ante esta realidad, Javier Diéguez explica que “la situación en España es, en general, desconocida, porque los programas de control son voluntarios. Por eso, a día de hoy sigue siendo difícil hasta que se pueda establecer un programa global”.
En cuanto al plan que se aplica en Galicia:
“Se lleva a cabo a través de las Agrupaciones de Defensa Sanitaria. En 2004 se empezaron a establecer programas de control que se basan en monitorizar el rebaño utilizando muestras de tanque de leche. Esto se combina con análisis de novillas que nacieron en la granja, lo que nos permite conocer, en caso de que haya infección, si fue más o menos reciente, y en caso de que se note algo anómalo se entiende que puede estar circulando el virus y se procede a la búsqueda y eliminación de los PI”.
En el año 2015, la aparición de Bovela® marcó un punto de inflexión en el sector, siendo la primera vacuna MLV frente a la BVD que garantizaba al 100% la protección fetal, incluyendo cepas no citopáticas de los dos genotipos de virus:
BVD-1
BVD-2
Además, Bovela® se presentaba como una vacuna que podía aplicarse en animales muy jóvenes, independientemente del estado reproductivo.
El lanzamiento de Bovela® supuso una revolución en el control de la BVD con fortalezas como una única aplicación, incluso en primo-vacunación y protección durante un año (período tras el cual se debe revacunar al animal).
Estos valores respaldan su continuo crecimiento que le ha llevado a superar, recientemente, las 25 millones de dosis, tanto en vacuno lechero como de carne.
Para Manuel Cerviño, asesor técnico de rumiantes de Boehringer Ingelheim Animal Health España, este hecho “supone un éxito. Bovela® ha supuesto un paso adelante en el control y el manejo de la enfermedad. Ha sido un éxito para Boehringer Ingelheim, pero también para el mercado español y europeo, porque con Bovela® se ha facilitado la mejora de los resultados de BVD en nuestro país, hasta el punto que hemos erradicado la enfermedad en explotaciones concretas y en grandes áreas”.

Este hito alcanzado representa la colaboración activa de la vacuna en la eliminación de los animales PI y refleja la gran fortaleza de Bovela® que no es otra que la de haber “conseguido mantener todas las ventajas de una vacuna viva, pero con la seguridad de una vacuna inactivada”.
Convocatoria de los Premios BVDzero abierta hasta el 30 de septiembre Boehringer Ingelheim Animal Health España tiene abierta la convocatoria de la 4ª edición de los premios BVDZERO España.
Dirigida a los profesionales del sector bovino con ejercicio profesional en España, todos los interesados pueden presentar sus casos hasta el 30 de septiembre.

La convocatoria, que otorgará seis premios valorados en un total de 8.000€, tiene como objetivo promover el interés por la BVD en todos sus aspectos y su investigación con ánimo divulgativo.
La intención es ligarse al día a día de la profesión, poniendo el foco en las situaciones cotidianas donde se manifiesta la enfermedad.
Más información sobre Bovela® en Bovela (europa.eu)
En caso de duda consulte a su veterinario
Más información sobre los premios en www.bvdzero.es
Foix Queraltó Salguero Veterinaria Oficial

El Real Decreto 1053/2022 establece las normas fundamentales para la ordenación zootécnica y sanitaria de las explotaciones de ganado bovino.
LEER Real Decreto de 27 de diciembre, por el que se establecen normas básicas de ordenación de las granjas bovinas.

El presente RD se ha realizado debido a que, al contrario que otros sectores ganaderos, como es el caso del porcino, el avícola, el cunícola o el equino, el sector bovino, tanto el cárnico como el lácteo, no contaba con una norma nacional específica que estableciera los requisitos básicos para su gestión sectorial. La evolución del sector en los últimos años, su importante componente social, la elevada profesionalización e internacionalización, unida a los nuevos retos en materia medioambiental y climática, de seguridad alimentaria, bioseguridad y de bienestar animal, han hecho que sea necesario el desarrollo de una normativa básica estatal que reúna todos estos aspectos.
Por otra parte, se justifica la necesidad de acometer los nuevos retos que se plantean en el marco de la nueva Política Agraria Común 2023-2027, bajo los objetivos específicos medioambientales y sociales relacionados con las demandas de los consumidores, así como afrontar los nuevos retos del Green Deal y las estrategias derivadas del mismo, como la Farm to Fork Strategy y la nueva Estrategia de Biodiversidad.


La ausencia de una normativa específica sobre la gestión de las explotaciones ganaderas bovinas no implica que no existan numerosas normas aplicables a este sector, que incluyen diversos aspectos que, en sí mismos, forman parte de un proceso de gestión, tanto de carácter zootécnico, como de trazabilidad e identificación animal, bienestar animal, bioseguridad y medioambiente.
También hay que añadir que ciertas comunidades autónomas ya han desarrollado su normativa referente a la ordenación del sector bovino y de aplicación en sus ámbitos territoriales.
Todos estos motivos han propiciado la elaboración del RD 1053/2022 que a continuación desgranaremos para facilitar su comprensión.
En el RD 1053/2022 se establecen las normas básicas para la ordenación zootécnica y sanitaria del sector bovino referente a:
La capacidad productiva máxima.
Las condiciones mínimas de infraestructura, equipamiento y manejo.
La ubicación.
La bioseguridad.
El bienestar animal.
Las condiciones higiénico-sanitarias y requisitos medioambientales.
Las responsabilidades y obligaciones que permitan un desarrollo eficaz y adecuado de la actividad.
Las disposiciones que se recogen en este RD están dirigidas a las explotaciones en las que se críen, o mantengan con fines productivos o reproductivos, animales de las especies de ungulados que pertenezcan a los géneros Bisonte, Bos y Bubalus, y la descendencia de los cruces entre estas especies a los que, sin perjuicio de la normativa que les sea de aplicación,

El RD 1053/2022 distingue 4 tipos distintos de clasificación según:
Según el Tipo de Explotación, nos distingue 8 subtipos diferentes:
Explotaciones de Producción y Reproducción
Pastos
Explotaciones de tratantes u operantes comerciales de ganado bovino que, a su vez, se distinguen en 2 tipos distintos según la actividad comercial que realicen:
A. Tratantes para Vida: aquellas explotaciones cuya actividad sea la venta de animales con destino a Explotaciones de Producción y Reproducción a excepción de los Cebaderos, a los que se podrán llevar animales únicamente de forma excepcional.
B. Tratantes para Cebo o Sacrificio: aquellas cuya actividad sea la venta de animales con destino a Cebaderos o directamente al Matadero.
Centros de Concentración de Ganado Bovino: cualquier emplazamiento, incluidas Explotaciones, Centros de Recogida y Mercados, en los que se reúna a animales de la especie bovina procedentes de distintas explotaciones para formar lotes destinados al Comercio. El periodo entre la salida del animal desde el establecimiento de origen y su salida del centro de agrupamiento no será superior a 14 días. En este tipo de centros están incluidos:
A. Certámenes ganaderos: lugares autorizados en los que se reúne el ganado bovino en instalaciones adecuadas:
Con destino a su transacción comercial, sea para reproducción, cebo o sacrificio.
Con destino a su exposición o muestra, o su valoración y posterior premio, en su caso.
Pueden participar todos los ganaderos o personas interesadas que reúnan, en cada caso, los requisitos exigibles por la norma de sanidad vigente.
Este podrá tener la consideración de:
Permanente: Ferias y Mercados.
No Permanente: Exposiciones.
B. Centro de tipificación de ganado bovino: centro de concentración que tiene como finalidad la obtención de lotes de animales homogéneos para su comercialización inmediata, procedentes únicamente de explotaciones de reproducción que tengan la misma base social justificada, como son las Cooperativas y las Agrupaciones de Defensa Sanitaria Ganadera. Es importante destacar que en estas instalaciones no se podrá llevar a cabo el cebo de los animales.
C. Puestos de Control
Centros de testaje y/o Selección y Reproducción de ganado bovino: aquellas explotaciones reconocidas específicamente para este fin y que valoran o seleccionan y crían reproductores.
Centros de Concentración de Lidia: explotación compuesta por machos de lidia, cabestros y, en su caso, hembras que proceden de distintas ganaderías de reses de lidia y destinadas a lidia o sacrificio en matadero. No se considerarán centros de concentración de lidia las plazas de toros ni las instalaciones anejas.
Explotación de Cabestros: explotación constituida exclusivamente por cabestros, destinados a prestar servicios para el manejo de reses de lidia en plazas de toros e instalaciones anejas a las mismas u otros lugares autorizados para realizar festejos o espectáculos taurinos.
Explotaciones o Centros de Cuarentena: explotaciones en las que se mantienen los animales en observación y control sanitario antes de su traslado definitivo a la
4. explotación ganadera. 5. 6. 7. 8. POR TIPO DE EXPLOTACIÓN 1. Explotaciones de Producción y Reproducción 2. Pastos 3. Explotaciones de tratantes u operantes comerciales 4. Centros de Concentración de Ganado Bovino 5. Centros de testaje y/o Selección y Reproducción de ganado bovino 6. Centros de Concentración de Lidia 7. Explotación de CabestrosEl nuevo RD clasifica las explotaciones de bovino según su clasificación zootécnica en dos grupos claramente diferenciados. Por un lado, están las Explotaciones de Producción y Reproducción y, por otro, los Pastos.
En cuanto a las Explotaciones de Producción y Reproducción se distinguen 5 subgrupos:
Explotación para la producción de leche: aquella que tiene por objeto la producción y, en su caso, comercialización de leche o productos lácteos, y en la que se somete a las hembras bovinas reproductoras a ordeño.
Explotación para la producción de carne: aquella que tiene por objeto la obtención de bovinos de producción propia destinados a su cría o engorde para la producción de carne, de manera que las hembras reproductoras no son sometidas al ordeño de forma regular.
Explotación para la producción mixta: aquella que reúna las orientaciones productivas anteriores.
Explotación de recría de novillas: aquella dedicada a la cría de hembras bovinas para su destino posterior a la reproducción exclusivamente, ya sea para explotaciones de producción de leche, carne o mixtas.
Cebaderos: aquellas dedicadas al engorde de bovinos con destino final al matadero, directo o a través de otros cebaderos, tratantes o certámenes ganaderos permanentes, o a exportación. Estos pueden ser a su vez:
A. Cebaderos de Ciclo Cerrado: aquellos cuyos animales no pasan por otros cebaderos antes de llegar al matadero.
B. Cebaderos de Ciclo Abierto: aquellos cuyos animales sí pasan por otros cebaderos antes de llegar al matadero.
Las Explotaciones Tipo Pasto se pueden clasificar, con carácter voluntario, según su orientación productiva de acuerdo con los subapartados 1, 2 y 3 del apartado anterior pero no como explotaciones de recría de novillas ni cebaderos.
1. 2. 3. 4. 5.En función del Sistema de Producción las explotaciones se pueden clasificar en:
Explotaciones de producción y reproducción que, a su vez, pueden ser:
A. Explotaciones Extensivas: aquellas en las que los animales no están alojados dentro de una instalación de forma permanente y, para su alimentación, utilizan la mayor parte del tiempo una base territorial con aprovechamiento de pasto o recursos agroforestales, complementando el pastoreo con aportes de materias primas vegetales o piensos, en función de las condiciones climáticas y la disponibilidad de pastos.

B. Explotaciones Semiextensivas: aquellas que no pudiendo considerarse extensivas, disponen de una base territorial a su disposición cuyo aprovechamiento se realiza con base en pastoreo y donde los animales realizan esta actividad un número significativo de horas a determinar por la Autoridad Competente (AC) de la Comunidad Autónoma (CA) conforme a la práctica habitual en los distintos territorios que la integran.
Explotaciones no extensivas: el resto.
Explotaciones tipo pasto que se clasifican a efectos del Registro General de Explotaciones Ganaderas (REGA) como explotaciones Extensivas.
Explotaciones de producción Ecológica, aquellas que cumplan con lo dispuesto en el Reglamento (UE) 2018/848 sobre producción ecológica y etiquetado de los productos ecológicos, que se podrán clasificar a efectos del REGA con carácter voluntario.
Por su capacidad productiva se distinguirán dos grupos:
Las explotaciones bovinas de producción y reproducción para la producción de carne, leche, mixtas y recría de novillas, que no tengan la condición de explotación extensiva conforme a lo previsto en el apartado anterior, ni sean cebaderos, se clasifican en función de su capacidad productiva (UGM) de la siguiente forma:

Grupo I: hasta 20 UGM inclusive.
Grupo II: superior a 20 y hasta 180 UGM inclusive.
Grupo III: superior a 180 y hasta 850 UGM inclusive.
Grupo IV: superior a 850 UGM que a la fecha de entrada en vigor del presente RD ya se encontraran en funcionamiento, ya hubieran obtenido la autorización correspondiente o se encontraran pendientes de obtener dicha autorización conforme a lo establecido en la disposición transitoria primera.
Las explotaciones bovinas de producción y reproducción definidas como Cebaderos se clasifican en función de su capacidad productiva (UGM) de la siguiente forma:

Grupo I: hasta 20 UGM inclusive.
Grupo II: superior a 20 y hasta 360 UGM inclusive.
Grupo III: superior a 360 y hasta 850 UGM inclusive.
Grupo IV: superior a 850 UGM que, a la fecha de entrada en vigor del presente RD, ya se encontraran en funcionamiento, ya hubieran obtenido la autorización correspondiente o se encontraran pendientes de obtener dicha autorización conforme a lo establecido en la disposición transitoria primera.
Las autoridades competentes podrán incrementar la capacidad productiva establecida para las explotaciones del Grupo III hasta un máximo de un 10%. El umbral inferior para las explotaciones contempladas en el Grupo IV quedará redefinido consecuentemente con dicho incremento.
Todas las explotaciones de los Grupos II, III o IV, incluidas las que ya existían antes de la entrada en vigor de este RD, contarán con un Sistema Integral de Gestión de las Explotaciones Bovinas (SIGE) cuyo contenido deberá actualizarse, al menos, cada 5 años y, en cualquier caso, siempre que la explotación modifique sustancialmente sus instalaciones o prácticas de manejo.
Cebaderos

El RD 1053/2022 establece que el Responsable de la aplicación de las medidas y requisitos en materia de formación, higiene, bioseguridad, bienestar y sanidad animal es el titular de la explotación o el titular de los animales, no el veterinario. También señala que se tienen que cumplir las obligaciones de vigilancia del operador y el Plan Sanitario Integral de las Explotaciones Ganaderas Bovinas (SIGE) que está regulado en el artículo 9 del presente RD y detalla el contenido mínimo en el ANEXO III.
El titular de la explotación o, en el caso de las explotaciones tipo pasto, el titular de los animales, se tiene que asegurar de que todas las personas que trabajan con ganado bovino en la explotación tengan una formación adecuada y suficiente:
El personal debe tener acreditada su formación con una duración mínima
 Grupo I (≤20 UGM)
Grupo II (>20 UGM y ≤360 UGM)
Grupo III (>360 UGM y ≤850 UGM)
Grupo IV (>850UGM)
Grupo I (≤20 UGM)
Grupo II (>20 UGM a ≤180 UGM)
Grupo III (>180 UGM a ≤850 UGM)
Grupo IV (>850 UGM)
Explotaciones bovinas de producción y reproducción
Grupo I (≤20 UGM)
Grupo II (>20 UGM y ≤360 UGM)
Grupo III (>360 UGM y ≤850 UGM)
Grupo IV (>850UGM)
Grupo I (≤20 UGM)
Grupo II (>20 UGM a ≤180 UGM)
Grupo III (>180 UGM a ≤850 UGM)
Grupo IV (>850 UGM)
Explotaciones bovinas de producción y reproducción
Sin embargo, las autoridades competentes pueden eximir a los empleados de este requisito si pueden demostrar que tienen al menos 3 años de experiencia laboral en un campo relacionado con la cría de ganado, lo que garantiza que tienen al menos un conocimiento básico de los temas mencionados en el ANEXO II.
Este requisito no se aplicará a quien esté en posesión de alguna de las siguientes acreditaciones o titulaciones superiores a las mismas:
Título de técnico en producción agropecuaria.
Título de técnico superior en ganadería y asistencia en sanidad animal.
De manera adicional, el titular de la explotación se asegurará de que todos los trabajadores en contacto con ganado bovino realicen, de manera periódica y en todo caso al menos una vez cada 5 años, cursos de adecuación de los conocimientos a los avances técnicos de la actividad basados en las materias incluidas en el ANEXO II, con una duración mínima de 10 horas. El titular de la explotación, o de los animales, tiene que vigilar su salud y comportamiento y comunicar al veterinario de la explotación cualquier cambio en los parámetros normales de producción que puedan hacer sospechar de una enfermedad listada o emergente, así como los casos de mortalidad anormal y otros indicios de enfermedad grave.
Todas las explotaciones bovinas, incluidas las existentes antes de la entrada en vigor del presente RD, deberán cumplir las condiciones mínimas de infraestructuras, equipamiento y manejo. Nos recuerda que el diseño y construcción tiene que presentar unas condiciones adecuadas para el confort ambiental y así minimizar el estrés térmico. Los materiales tienen que ser seguros para los animales y los trabajadores
Las instalaciones permanentes deben estar delimitadas y cubiertas para poder proteger al ganado de otros animales silvestres, plagas, fenómenos meteorológicos, etc.
La colocación de los utensilios deberá hacerse de forma que facilite las tareas de limpieza, higiene, desinsectación y desratización.
Los empleados deben tener a su disposición los sistemas necesarios para un manejo adecuado y seguro de los animales, debiendo estar diseñados y construidos de tal forma que permitan la realización de las actuaciones sanitarias o cualquier otra actividad que requiera el manejo o la inspección de los animales con las debidas garantías de seguridad, tanto para ellos como para el personal que las ejecute.
Las instalaciones permanentes tendrán capacidad para alojar a todos los animales bovinos en caso de tener que confinarlos de acuerdo con la capacidad máxima registrada para la explotación y no con la capacidad censal.
Todas las explotaciones bovinas, incluidas las existentes antes de la entrada en vigor del RD, deberán disponer de utillajes de limpieza y manejo, así como ropa y calzado de uso exclusivo de la explotación.
Deberán contar con equipos y medios de higiene suficientes, al menos agua y jabón para el lavado de manos.
Los biocidas, fitosanitarios y otros productos para la salud o limpieza animal deberán almacenarse en un lugar seguro, bien vigilado y claramente señalizado.
Si el agua no procede de la red de suministro municipal, el titular de la explotación debe efectuar controles de calidad, al menos una al año.
Se deberá realizar, al menos una vez al día, una revisión del estado sanitario de los animales que abarcará a todos los grupos de animales de la explotación.
Para la observación y aislamiento de animales que deban mantenerse apartados de los demás por razones de salud o bienestar animal, la explotación deberá tener la capacidad de crear un espacio adecuado (permanente o temporal).
Cuando se realice reposición externa, la granja deberá disponer de una superficie suficiente (ya sea permanente o temporal) para poner en cuarentena a los animales.
Existe una serie de medidas para la gestión y ahorro de agua y energía, así como otros aspectos medioambientales que deben cumplir las explotaciones. Para ello, deberán disponer de un plan de gestión de residuos integrado en el Sistema Integral de Gestión de Explotaciones Bovinas (SIGE).
Con el fin de garantizar un uso eficiente del agua, las explotaciones deben cumplir con las siguientes condiciones:
La acometida y el suministro de agua para los animales y para la limpieza de la explotación deben disponer de una configuración que optimice su consumo, evitando en la medida de lo posible las pérdidas.
Deben utilizarse sistemas de alta presión para la limpieza de los alojamientos de los animales y equipos, siempre y cuando sea posible, en función del sistema productivo.
Se utilizarán equipos de bebida adecuados para cada categoría específica de animales presentes en la explotación, que garanticen la disponibilidad y el ahorro de agua.
Las explotaciones de producción y reproducción clasificadas como explotaciones para la producción de leche y mixta, además, deberán cumplir los siguientes requisitos:
Las zonas de ordeño y almacenamiento de leche deberán estar diseñadas para minimizar el riesgo sanitario originado por el tránsito tanto de personas como de vehículos.
Cumplir los criterios de higiene recogidos en el Reglamento (CE) 853/2004.
LEER ARTÍCULO H igiene en el ordeño
Todas las explotaciones ganaderas deben cumplir los requisitos mínimos de bienestar animal. Para garantizar el máximo bienestar y reducir el riesgo de accidentes y enfermedades, las instalaciones permanentes deben contar con un lugar para acostarse con un suelo uniforme y una cama cómoda, limpia y seca. La zona de descanso debe estar libre de rejas y lo más alejada posible de ellas.
Todas las explotaciones bovinas se encuentran sometidas a las siguientes limitaciones respecto a las siguientes prácticas y procedimientos:
No justificados por motivos terapéuticos o de diagnóstico, o destinados a la identificación de los animales de conformidad con la normativa pertinente.
Que provoquen lesiones o la pérdida de una parte sensible del cuerpo o la alteración de la estructura ósea.
La amputación del rabo y la modificación o la mutilación de la lengua.
Veterinario con anestesia y analgesia
Existen algunas EXCEPCIONES a lo establecido anteriormente, siempre que estas prácticas sean realizadas por:
Persona formada en
Descornamiento por ablación quirúrgica.
Desbotonamiento por ablación quirúrgica y el desbotonamiento por cauterización de animales de más de 4 semanas de edad.

Castración de machos y hembras y vasectomía.
Desbotonamiento por cauterización de animales de hasta cuatro semanas de edad mediante cauterización química o cauterización por quemadura.
Colocación de anillas nasales.
Las excepciones contempladas únicamente podrán realizarse en beneficio de los animales o, si fuera necesario, para la protección de las personas que estén en contacto directo con ellos.
Se prohíbe el uso de aparatos que emitan descargas eléctricas que no sean los destinados al cercado o las picas eléctricas en los términos establecidos en la normativa. No obstante, la autoridad competente podrá autorizar su uso durante el periodo necesario para el amaestramiento, siempre que se examine convenientemente y, si fuera necesario, reajustando a cada animal. En cualquier caso, no deberán utilizarse durante la gestación y el periodo inmediatamente perinatal.
Con el fin de reducir el riesgo de difusión de enfermedades infectocontagiosas en el ganado bovino, las autoridades competentes podrán establecer en su territorio distancias entre las explotaciones de bovino de nueva instalación con respecto a las explotaciones ya existentes, y con respecto a cualquier otro establecimiento o instalación que pueda representar un riesgo higiénico-sanitario.
De manera general, las explotaciones de ganado bovino estarán ubicadas de tal forma que se minimicen ruidos y olores en las poblaciones cercanas. Su orientación permitirá las mejores condiciones de ventilación natural, de gestión energética y de iluminación.
Los terneros de edad superior a 8 semanas de edad no se mantendrán en recintos individuales, salvo recomendación veterinaria.
La autoridad competente podrá limitar la instalación y ampliación de explotaciones de ganado bovino y la capacidad máxima de las mismas por razones medioambientales o sanitarias, en zonas declaradas por la comunidad autónoma como de alta densidad ganadera o como vulnerables.
Se prohíbe atar el rabo de las vacas de forma permanente.
Con el objeto de evitar impactos negativos sobre el medioambiente, los proyectos de construcción de nuevas explotaciones de ganado bovino se someterán al proceso de evaluación ambiental simplificada.

Se deben gestionar los estiércoles reduciendo la diseminación de agentes patógenos y los riesgos de filtración y escorrentías.
En caso de que el titular de la explotación realice la valoración agronómica de los estiércoles en el suelo, deberá disponer de superficie agrícola suficiente, propia o concertada.

El titular de la explotación bovina es el responsable de asegurar la trazabilidad de los estiércoles.
Se podrá manipular el estiércol en la propia explotación:
Siempre que no implique la mezcla con estiércoles de otras explotaciones.
Siempre que el destino final del mismo sea alguno de los destinos descritos en el apartado anterior.
Si se almacena estiércol sólido en la propia granja, hay que tener un área designada para ello con un suelo impermeabilizado que esté diseñado para detener la fuga de cualquier posible lixiviado.
Las explotaciones de nueva instalación de los Grupos II y III, y todas las explotaciones existentes de los Grupos III y IV, deberán cubrir el estiércol durante el tiempo que lo almacenen en su explotación.
En el caso de generar purines, la explotación deberá disponer de un sistema de almacenamiento delimitado perimetralmente y en cumplimiento con los requisitos de ubicación establecidos por la autoridad competente en la autorización concedida.
Estos sistemas de almacenamiento:
Deberán contar con materiales adecuados para estar impermeabilizados, natural o artificialmente, para evitar el riesgo de filtración y contaminación de las aguas superficiales y subterráneas, así como las pérdidas por rebosamiento o por inestabilidad geotécnica.
Deberán contar con el tamaño adecuado para poder almacenar el purín producido durante los periodos en los que no es posible proceder a su aplicación al campo y, al menos, durante 3 meses.
Deberán estar diseñados de tal modo que se evite el contacto de los animales con las emisiones generadas.
Para el cálculo del volumen del sistema de almacenamiento se podrán utilizar los valores que figuran en el ANEXO IV.
Hembras 14
Sementales 9
Vacuno de leche
Cría 0,4
Reposición 5,5
Engorde 3,6
Reproductores 9
Cría 0,5
Vacuno de carne
Reposición 5,5
Engorde 3,6
Especie CategorÍa Purín (m 3/plaza y año)Los titulares de las explotaciones deberán llevar, de manera actualizada, un libro de registro de formato aprobado por la autoridad competente.
Dicho libro se llevará de forma manual o informatizada, y será accesible para la autoridad competente, manteniendo los datos correspondientes al período que ésta determine y que, en cualquier caso, no podrá ser inferior a los últimos 3 años de actividad de la explotación.
No tendrán consideración de nueva instalación aquellas explotaciones que, al aumentar y sobrepasar el límite de su grupo, no superen en 50 UGMs el límite inferior del nuevo grupo.
El titular de la explotación deberá facilitar a la autoridad competente:
La información necesaria para el registro de su explotación antes del comienzo de su actividad (Obtener código REGA).
La información relativa a los cambios que se produzcan en los datos de su explotación, incluidos aquellos que supongan un cambio de clasificación.
Asimismo, deberá comunicar a las autoridades competentes las técnicas aplicadas en la explotación con la finalidad de mitigar las emisiones de gases contaminantes y de gases de efecto invernadero a la atmósfera.

Posteriormente, deberán presentar anualmente (antes del 1 de marzo de cada año), una declaración de dichas técnicas aplicadas en su explotación durante el año anterior, siempre que se hayan modificado las existentes o siempre que se hayan incorporado nuevas, en el formato que determine la autoridad competente de la comunidad autónoma.
Navegando la burocracia
ganadera: Nueva ordenación de explotaciones bovinas
DESCÁRGALO EN PDF
Aníbal Fernández Mayer
Nutricionista EEA INTA Bordenave (CERBAS) MSc y Doctor en Cs Veterinarias
El uso de las grasas en la dieta de los rumiantes no siempre se realiza adecuadamente, siendo frecuente que no se alcancen los resultados productivos esperados debido a un consumo elevado o a un uso inapropiado de la fuente rica en ácidos grasos (AG).

Cuando la ración contiene un exceso de grasa, especialmente de ácidos grasos insaturados, repercute negativamente sobre el crecimiento de las bacterias del rumen, viéndose más afectadas las bacterias celulolíticas que las amilolíticas.
De todos los ácidos grasos insaturados evaluados, el ácido oleico (C18:1) tiene el mayor efecto inhibidor.
Cuando un alimento entra en el rumen y se “empapa” en aceite o grasas se producen los siguientes efectos:
Menor degradabilidad de la fibra del alimento
Menor consumo voluntario de alimento
Posibles trastornos digestivos (diarrea)
No se recomienda que la concentración total de grasas (extracto etéreo) supere el 5-6% en la dieta total de un rumiante, independientemente de su aptitud.
Los AG insaturados tienen un mayor efecto negativo sobre los microorganismos que los saturados, aunque a nivel intestinal tienen una mayor digestibilidad.
Por lo tanto, a medida que se incrementa el grado de saturación de una grasa (mediante biohidrogenación en el rumen u otra vía de hidrogenación externa) disminuyen los efectos negativos sobre la fermentación ruminal, pero también se reduce la digestibilidad intestinal de dichos ácidos grasos.


En cuanto a las grasas protegidas, una de sus principales características es que permanecen inertes en el rumen, sin afectar a los microorganismos, mientras que a nivel intestinal son totalmente digeridas.
Las grasas protegidas son un medio para incrementar el consumo diario de grasa en el ganado rumiante sin que se vea afectado su metabolismo.
Actualmente, existen dos tipos de grasas protegidas:
Sales cálcicas de ácidos grasos o jabones cálcicos: ampliamente utilizadas como fuente de grasa protegida en el rumen debido a su muy baja disociación a pH < 6,0, y su satisfactoria estabilidad a pH 5,5.


Sin embargo, en el abomaso el pH disminuye unos 2-2,5 puntos, por lo que se produce la disociación, dando lugar a calcio y a los AG libres correspondientes que son digeridos en el intestino delgado (Mateos et al., 1996).
La mayoría de los jabones cálcicos disponibles se fabrican a partir de los AG destilados de la palma, cuyo perfil es apropiado para los rumiantes (punto de fusión entre 38-39 °C, próximo a la temperatura corporal del animal y, además, de alta digestibilidad).
Grasas saturadas o hidrogenadas: inertes en el rumen (baja solubilidad) debido a que sus propiedades físicoquímicas limitan su utilización por los microorganismos ruminales, permitiéndoles llegar al intestino delgado para su utilización como fuente de energía y AG (Davis, 1993).
El proceso de obtención de este tipo de grasas consiste en hidrogenar parcialmente los dobles enlaces de diversos AG con el fin de elevar su punto de fusión, reduciendo de esta forma su actividad en el rumen al aumentar su insolubilidad. Las principales fuentes utilizadas en la confección de estas grasas son sebos y subproductos del refinado del aceite de palma y de pescado.
o algodón. Sin embargo, las semillas “enteras” reducen el aprovechamiento proteico y se incrementan las pérdidas en heces.
Al procesarse (molienda o aplastado) liberan aceites y generan un ambiente ruminal inadecuado (lipólisis y enranciamiento), e incluso se pueden producir toxinas que afectan a la salud del animal.
También se pueden encapsular las grasas con un recubrimiento proteico que, a su vez, se protege con formaldehído contra la deshidratación en el rumen. Durante este procedimiento, complejo y costoso, se pueden romper dichas cápsulas liberando las grasas en el rumen.
Por otro lado, el extrusado permite reducir los efectos negativos del enranciamiento, aunque cuando se emplean temperaturas
>150 °C la composición química de grasas y proteínas puede verse afectada. En algunos casos incrementa el poder “bypass” de ambos, pero en otros se reduce la digestibilidad a nivel ruminal e intestinal , perdiéndose así gran parte de la proteína y grasa en las heces.
Como ya hemos comentado, se trata de grasas saturadas por hidrogenación (con alta proporción de ácido palmítico y esteárico) con un elevado punto de fusión y baja inhibición microbiana. Los resultados en producción láctea y porcentaje de grasa de la leche son muy variables (aleatorios) debido a su baja digestibilidad.

La protección de los ácidos grasos se realiza a través de una saponificación con calcio. El resultado, como también hemos visto anteriormente, es una grasa inerte a nivel de rumen que no afecta a la fermentación bacteriana y se digiere muy bien a nivel intestinal, previa hidrólisis en abomaso. Además, posee una alta palatabilidad y se aglomera muy bien con granos y forraje (ensilados o henos) de tamaño fino.

El suministro de grasas protegidas es apropiado para vacas de alta producción o al inicio de la lactación, cuando la ración tradicional no proporciona suficiente energía para sostener la producción, la condición corporal del animal y su eficiencia reproductiva. Sin embargo, para un uso eficaz del suplemento graso debe calcularse el coste por unidad de energía de dicho suplemento.

En los últimos años se ha desarrollado la tecnología necesaria para incluir ácidos grasos poliinsaturados tipo omega en la manufactura de los jabones cálcicos. Esta estrategia es la única que permite suplementar de manera eficaz dichos compuestos en la alimentación de rumiantes (Thatcher, 2008).
Uso de grasas en nutrición bovina DESCÁRGALO EN PDF




La capacidad de las vacas lecheras para adaptarse al balance energético negativo (BEN) durante los primeros días de lactancia es un factor fundamental en la producción de leche, ya que las demandas no podrán ser cubiertas por la ingesta de alimento (Herdt et al., 2000).

Las vacas que son incapaces de realizar una transición adecuada (±21 días del parto) tienen un mayor riesgo de presentar trastornos metabólicos y de ver disminuida su producción láctea (Cameron et al., 1998; Drackley, 1999; Herdt et al., 2000).
Uno de estos trastornos es la hipercetonemia o cetosis, que se desarrolla como consecuencia de una mala respuesta adaptativa al balance energético negativo, y tiene lugar cuando el hígado esta saturado por la acumulación de ácidos grasos no esterificados (NEFAs, del ingles Non-Esterified Fatty Acids).
Asesor Técnico en RumiantesDebido al bajo consumo energético del animal durante la etapa de transición, el organismo comienza a movilizar reservas de grasa corporal, aumentando la concentración de NEFAs y betahidroxibutirato (BHBA) en sangre (Li et al., 2016).

Este trastorno metabólico puede clasificarse según la concentración de BHBA en sangre:
Cetosis clínica: BHBA > 1,2 mmol/l
Cetosis subclínica: BHBA = 0,8-1,2 mmol/l
La prevalencia en animales de alta producción puede llegar hasta un 15% y un 60% para cetosis clínica y subclínica, respectivamente.
Una de las principales consecuencias de la cetosis en el ganado es la disminución en la producción de leche, llegando hasta un 7% de pérdidas durante toda la lactancia.
El impacto de la cetosis dependerá de la concentración de BHBA:
Cada 0,1 mmol/l por encima de 1,2 mmol/l se asocia a 498,95 g menos de leche durante los primeros 30 DEL (días en leche).
En el caso de la cetosis clínica la disminución es de 5.987,41 g diarios de leche, lo que refleja la repercusión económica que puede tener este trastorno.
Otra de las principales consecuencias de la cetosis es el descarte de animales, habiéndose reportado que los animales que presentan cetosis ven aumentado 3 veces el riesgo de ser desechados
Por cada 0,1 mmol/l por encima de 1,2 mmol/l de aumento de BHBA, el riesgo de desechar un animal aumenta
1,4 veces (J. A. A. McArt et al., 2012).
En términos reproductivos se ha demostrado que concentraciones de BHBA en sangre superiores a 1,2 mmol/l durante la primera semana después del parto:
Aumentan hasta 7 veces el riesgo de desplazamiento de abomaso
Aumentan 3,4 veces el riesgo de metritis
Disminuyen la fertilidad en el primer servicio
(Otzel & McGuirk, 2010)
La colina es un nutriente esencial para los rumiantes ya que participa en diferentes procesos fisiológicos como el metabolismo y el transporte de lípidos.
Es necesaria para la formación del principal fosfolípido en los rumiantes, la fosfatidilcolina, que participa en la absorción y transporte de lípidos (Zeisel y Da Costa, 2009).
En general, los costes derivados de la cetosis son por:
Problemas clínicos como metritis o desplazamientos de abomaso (35%)
Problemas reproductivos (28%)
Pérdidas en producción de leche (22%)
Desecho (13%)
El impacto económico de la cetosis asciende hasta 256,71€ por animal (Deniz et al., 2020).
Por tal motivo, es importante estimular la función hepática para prevenir estos trastornos, y es aquí donde la colina juega un papel fundamental
La fosfatidilcolina es una pieza fundamental en la formación de lipoproteínas de baja densidad (VLDL), responsables de la expulsión de grasas en el hígado, función fundamental sobre todo durante el periodo de transición, en el que la vaca sufrirá una pérdida de condición corporal (CC) (Yao & Vance, 1988).
Todas las vacas pierden CC durante los primeros 30 DEL y el valor para considerarlo como pérdida de CC es de 0,5% - 0,75%, lo que equivale a 40,55 kg de grasa y proteína (un punto equivale en promedio a 70 kg, dependiendo del tamaño de la vaca).
Más del 50% de las vacas en lactación temprana desarrollan hígado graso moderado o severo (Bobe et al., 2004; Lima et al., 2012).

El hígado pesa 9 kg y puede acumular más de 450 g de grasa el día después del parto (Drackley, 2001). ¡Un punto de pérdida de CC se traducirá en 4,5 - 5,5 kg de grasa en el hígado!
Al disminuir la función hepática la vaca entrará en cetosis.
Procede señalar que, mientras el animal se encuentra en BEN, los niveles de colina en sangre se encuentran en las más bajas concentraciones durante las primeras semanas de producción (Arshad et al., 2020).
Por lo tanto, es importante suplementar al animal con una fuente de colina protegida con el objetivo de que la población microbiana no la degrade y esta pueda ser absorbida en el intestino.
La colina protegida:
Mejora la movilización de reservas de energía y disminuye el riesgo de cetosis
Aumenta la concentración de glicógeno en el hígado
Ayuda a tener una mejor oxidación de los ácidos grasos
Disminuye la prevalencia de problemas de salud y mejora la reproducción y la producción (Jayapraksh et al., 2016)
* p <0,05 comparado con d -14
Se ha demostrado que, mediante la suplementación de colina protegida durante el periodo de transición, el consumo de materia seca aumenta hasta 0,5 kg/día. Además, se ha observado una ganancia de peso de 30 kg en los animales suplementados con colina protegida durante los primeros DEL.
Los resultados del mismo estudio han evidenciado que, con la suplementación de colina protegida, la producción de leche puede aumentar hasta 1,6 kg/día (incluso 2 kg/día), en combinación con metionina protegida.
La suplementación de este nutriente antes y después del parto ayuda a aumentar los niveles de glucosa en sangre. Asimismo, ayuda a que los niveles de ácidos grasos en sangre después del parto disminuyan (Arshad et al., 2020).
Los beneficios de suplementar con colina durante el periodo de transición van más allá de los primeros 21 días postparto, ya que las vacas mantienen un nivel de producción mayor durante la etapa de lactación postsuplementación.
Investigaciones recientes han demostrado que la suplementación con colina en el preparto tiene un efecto positivo en la siguiente generación, ya que estas vacas producen más calostro y con una concentración de IgG mayor (Zenobi et al,. 2018).
Calidad (brix) y cantidad de calostro en vacas suplementadas con colina y sin colina (Zenobi et al., 2018 - JDS 101_1088).
Concluyendo, los estudios demuestran que la suplementación con colina en vacas que se encuentran en periodo de transición tiene un efecto positivo más allá de prevenir la acumulación de grasa en el hígado:

Aumenta la producción durante toda la etapa de lactación
Aumenta las concentraciones plasmáticas de calcio
Tiene efectos positivos en la siguiente generación
Grafica 2. Curva de lactación de vacas suplementadas con y sin colina protegida (Zenobi et al., 2018 - JDS 101:1088).
Ángel Revilla Ruiz1, Javier Brieva Saenz2 y Juan Vicente González Martín3
1Residente del Colegio Europeo de Medicina Bovina (ECBHM). Facultad de Veterinaria, UCM
2Bricalvet Servicios Veterinarios
3Profesor Titular Dpto. de Medicina y Cirugía Animal, Facultad de Veterinaria, UCM. TRIALVET Asesoría e Investigación Veterinaria SL
Originaria de Japón, la raza Wagyu se caracteriza por producir una carne muy apreciada por su característico marmoleado, un elevado contenido de ácidos grasos omega 3 y 6, y una intensa jugosidad y sabor.

En este artículo se presenta el caso de un rebaño de terneros de raza Wagyu con una alta tasa de mortalidad.

El caso se presentó en una granja de nodrizas con 80 vacas de raza Wagyu en sistema de estabulación libre con cama de paja y acceso a una zona de tierra (5 ha) donde los animales pasan el resto del día.

Su alimentación se basa en una ración unifeed compuesta de paja picada y concentrado todos los días, encontrándose bebederos y comederos con paja a libre disposición distribuidos por todo el establo y en la zona de tierra.

ENCALOSTRAMIENTO
Dada la extensión de la finca, no existe una zona específica para partos y los terneros maman de su madre desde el nacimiento sin intervención, a no ser que sea necesaria.
Si el ternero al nacimiento no toma por sí solo el calostro, se le administra 1,5 L de calostro (con unos 25 kg de peso corporal) por sondaje esofágico y después continúan mamando de la madre.
Siempre que sea posible, el calostro sondado procede de la madre, pero si esta opción no es posible, se utiliza calostro congelado.
No se mide rutinariamente la calidad del calostro ni se evalúa la transferencia de inmunidad pasiva en los terneros.
Los terneros son castrados con 15 días de edad y luego se engordan hasta los 30 meses, cuando son sacrificados, que es la edad de sacrificio típica de esta raza.
Los trabajadores de la granja realizan un seguimiento rutinario de las enfermedades, pero no se almacenan datos.
La granja tiene una baja incidencia de enfermedades con una mortalidad en los terneros igual o menor al 5%, normalmente por diarrea, porcentaje adecuado según la bibliografía (USDA, 2010).
El motivo de la visita a la explotación fue un aumento repentino de la mortalidad en los terneros, habiendo fallecido tres terneros en la última semana. Estos aparecieron tumbados y, pese a los distintos tratamientos administrados, no se volvieron a levantar hasta sucumbir a la muerte.
En el momento de la visita, había tres terneros afectados, dos en decúbito esternal y uno en decúbito lateral.
Comenzando con la exploración del ternero de dos meses de vida que se encontraba en decúbito lateral, por presentar la sintomatología más severa, se observaron los siguientes signos clínicos:
Dado el estado clínico del primer animal, y a petición del veterinario, se decidió eutanasiar a los terneros para hacer un estudio en profundidad del caso y tomar muestras para su análisis.
Se tomó una muestra de sangre previa a la necropsia y, durante la misma, no se apreciaron alteraciones significativas en los órganos, apareciendo normales al examen macroscópico, salvo algunas zonas de palidez de los músculos esqueléticos de las patas traseras (Imágenes 1 y 2) y amplias zonas blancas en el miocardio (Imagen 3).

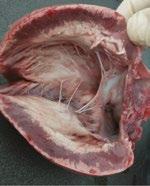
Un estado de depresión severa. Hipotermia.
Bradicardia (50 latidos/minuto) y taquipnea (65 respiraciones/minuto, muy superficiales).
Sin signos de deshidratación o de toxemia.
Sin heces en el momento de la exploración.
El ternero, que no respondía a los estímulos, había recibido un tratamiento de soporte previo con Ringer lactato, fluidos glucosados y vitamina B parenteral, sin apenas mejoría.
Los otros dos animales, de un mes de vida, se encontraban en decúbito esternal y eran capaces de tomar leche. Si bien, presentaban una temperatura corporal normal y ausencia de signos de deshidratación o toxemia, mostraron una leve taquicardia y taquipnea.
Asimismo, al realizar la histología se observaron lesiones degenerativas en el músculo, que pueden estar asociadas a la enfermedad de músculo blanco.
 Imágenes 1 y 2. Palidez de los músculos esqueléticos de las extremidades traseras.
Imagen 3. Zonas blancas en el miocardio.
Imágenes 1 y 2. Palidez de los músculos esqueléticos de las extremidades traseras.
Imagen 3. Zonas blancas en el miocardio.
Resumiendo, los casos atendidos eran terneros que se presentaban en decúbito con lesiones en musculatura estriada y cardiaca con una tasa de mortalidad muy elevada, presentando algunos de ellos indicios de diarrea.
Atendiendo a los signos de distrofia muscular y posición en decúbito esternal, entraron en el diagnóstico diferencial las siguientes posibles causas (Constable et al., 2017):
Deficiencia de selenio y vitamina E (Enfermedad del músculo blanco) Neumonía
Miopatías traumáticas o infecciosas
El principal diagnóstico presuntivo, deficiencia de selenio y vitamina E, se basó en:
Los signos clínicos de los animales: Debilidad.


Fiebre y taquipnea (68 rpm).
Rigidez bilateral de la marcha.
Reticencia al movimiento y decúbito. (Constable et al., 2017; Żarczyńska et al., 2019; Maplesden et al., 1960)
Los hallazgos de la necropsia en los dos terneros (uno el día de la visita y el segundo unos días después):
Palidez de los músculos esqueléticos de las patas traseras (el músculo bíceps femoral es particularmente susceptible en los terneros; Constable et al., 2017) (Imágenes 1 y 2).
Zonas blancas en el miocardio (Buergelt et al., 2018) (Imagen 3).
Los análisis laboratoriales: niveles séricos de creatina quinasa (CPK) y aspartato aminotransferasa (AST) (Tabla 1) (Abutarbush et al., 2003).
Tabla 1. Valores séricos y referencias (Constable et al., 2017)
Todos los demás diferenciales se descartaron en base a los hallazgos en la necropsia (Buergelt et al., 2018):
Septicemia por Histophilus somni: no se observaron signos de septicemia (miocarditis, artritis; Harris y Janzen, 1989) en la necropsia.
Neumonía: los lóbulos pulmonares no estaban afectados por la inflamación (no se observaron patrones de neumonía y el pulmón no se palpaba firme).
Poliartritis: no se encontró líquido sinovial turbio ni fibrina en ninguna articulación principal tras la inspección de diferentes articulaciones en la necropsia.
Miopatías traumáticas o infecciosas: no se observó miositis gangrenosa ni pericarditis fibrinosa.
Fracturas de huesos largos: las fracturas se descartaron tras la exploración inicial.
Intoxicaciones cardiacas por gosipol o monensina: fueron descartadas por la edad y porque estos animales solo se alimentaban de leche.


ANÁLISIS LABORATORIAL
Los elevados niveles de creatinina quinasa permitieron confirmar el diagnóstico, siendo la enzima más utilizada para el diagnóstico laboratorial de la deficiencia de selenio (Se) y vitamina E.
Es muy específica del miocardio y de musculatura esquelética y aumenta sus valores cuando existe miodegeneración.
La aspartato aminotransferasa también presentó unos niveles elevados y es una enzima que indica daño muscular, pero es menos fiable que la CPK, ya que también puede estar relacionada con daño hepático.
De forma complementaria, y para confirmar el diagnóstico, se analizaron también las muestras de sangre de varios terneros y de animales adultos, obteniéndose un perfil mineral que reveló varias muestras con niveles de selenio por debajo del valor fisiológico.
MIOPATÍA PRIMARIA AGUDA
La enfermedad del músculo blanco afecta sobre todo a animales jóvenes, con síntomas que aparecen hasta los 6 meses de edad en terneros.
A medida que la enfermedad progresa, los animales se tumban y son incapaces de levantarse. Incluso cuando se les ayuda, los terneros mantienen una posición erguida y pueden mostrar temblores musculares, particularmente en las extremidades posteriores (Zarczynska et al., 2019).
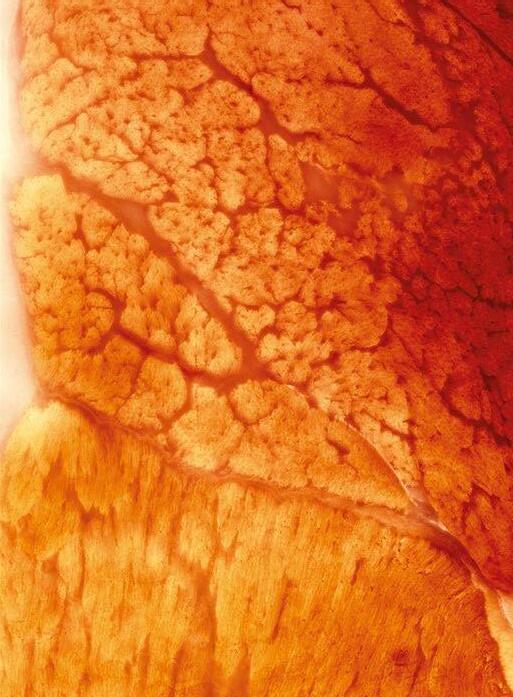
En términos generales, en la miopatía primaria aguda se produce una aparición repentina de debilidad y parálisis de los músculos afectados, lo que provoca paresia y decúbito y, en muchos casos, insuficiencia respiratoria y circulatoria.
Los animales afectados suelen permanecer alerta, pero pueden tener signos de dolor.
La temperatura suele ser normal, pero puede estar ligeramente elevada en casos graves de miopatía.
Pueden presentar taquicardia y arritmias.
Los animales con casos agudos de miopatía primaria suelen morir en las 24 horas siguientes a la aparición de los signos.
El cambio característico en la mayoría de los casos varía desde la degeneración hialina a la necrosis coagulativa, afectando particularmente a los músculos pesados de los muslos y a los músculos del diafragma.
Las lesiones miocárdicas también suelen asociarse a la degeneración del músculo esquelético y, cuando son graves, provocan la muerte rápida en unas horas o días.
Los efectos visibles de las lesiones son diversos grados de debilidad muscular, dolor muscular, decúbito, marcha rígida, incapacidad para mover las extremidades y desarrollo de insuficiencia respiratoria y circulatoria (Constable et al. 2017).
En la miopatía secundaria resultante de isquemia puede haber múltiples áreas focales de necrosis, lo que causa debilidad muscular y da lugar a un aumento de las enzimas musculares en el suero.
El grado de regeneración de las fibras musculares depende de la gravedad de la lesión.
El apetito y la actitud mental suelen ser normales.
No se suelen palpar anomalías musculares.
Con un tratamiento de apoyo y una buena cama, la mayoría de los animales se recuperan en pocos días (Constable et al. 2017).
La vitamina E y el selenio son esenciales para los animales y las personas, relacionándose su deficiencia con dietas pobres en estos dos nutrientes.

El selenio es un oligoelemento que desempeña un papel importante en la salud y la producción animal. Actúa sinérgicamente con la vitamina E en el mantenimiento del estado antioxidante del organismo.
Requerimientos nutricionales diarios estimados de selenio para terneros y ganado vacuno adulto: 100 µ g/kg MS/ día (Jobling, 2012; Mehdi y Dusfranse, 2016).
La vitamina E es esencial para la integridad y el buen funcionamiento de los sistemas reproductivo, muscular, circulatorio, nervioso e inmunitario, y participa en el metabolismo de las prostaglandinas (Sapkota, 2020).
Requerimientos diarios de vitamina E para terneros: 40-60 UI (Jobling, 2012).
Las dietas deficitarias en selenio y/o vitamina E no proporcionan suficiente protección frente a la lipoperoxidación “fisiológica” que se produce normalmente a nivel celular, lo que conduce a una lipoperoxidación tisular generalizada que lleva a la degeneración hialina y la calcificación de las fibras musculares.
El tratamiento elegido en este caso fue la administración parenteral de selenio, no solo a los terneros recién nacidos sino también a las vacas adultas un mes antes del parto.
Por otro lado, se corrigió la deficiencia mineral en la ración de los animales adultos.
Los brotes de la enfermedad se producen en terneros en los que hasta el 15% de los animales susceptibles pueden desarrollar la forma aguda y la letalidad se aproxima al 100% (Constable et al. 2017).
Una vez aplicado el tratamiento parenteral de selenio a las vacas y terneros, y gracias a la corrección del aporte de minerales en la ración, ningún animal recién nacido volvió a presentar distrofia muscular aguda ni decúbito.
Como se ha comentado anteriormente, la Enfermedad del músculo blanco está asociada al consumo de dietas deficientes en selenio y/o vitamina E, pudiendo estar además condicionada por:
Una excesiva cantidad de ácidos grasos poliinsaturados en la dieta.
La cantidad de selenio que hay en el suelo donde se cultivan los productos utilizados en la ración, siendo concentraciones inadecuadas las que se encuentran por debajo de 0,5 mg/kg de selenio.
El almacenamiento de las materias primas durante largos periodos de tiempo, produciéndose una pérdida de vitamina E.
El diagnóstico de este caso clínico de un rebaño con una mayor incidencia de animales recién nacidos con distrofia muscular y posición de decúbito se resolvió en base a la sintomatología clínica, los hallazgos de la necropsia y los niveles de CPK y AST, atribuyéndose a una deficiencia de selenio de etiología dietética, con prevención inmediata de nuevos casos tras cambios nutricionales.
Mortalidad de terneros por deficiencia de selenio en un rebaño de raza Wagyu
DESCÁRGALO EN PDF

Sabry El-khodary
Profesor de Medicina Interna y Vicedecano de Estudios de Postgrado e Investigación, Facultad de Medicina Veterinaria de la Universidad de Mansoura, Egipto
Tradicionalmente, los rumiantes se han considerado menos vulnerables a los efectos adversos de las micotoxinas en comparación con los animales monogástricos. Esta afirmación se relaciona con la capacidad de la microbiota residente en el rumen de degradar e inactivar las micotoxinas, protegiendo así al animal (FinkGremmels, 2008a).


Sin embargo, las micotoxinas que son capaces de resistir la degradación en el rumen pueden, sin duda, causar signos clínicos de intoxicación.

Las vacas lecheras pueden estar expuestas a un número variable de micotoxinas procedentes de diferentes materias primas, como forrajes y concentrados (Smith, 2014).

Las micotoxinas más conocidas por su importancia agrícola son:
Las Aflatoxinas (AF) producidas por especies de Aspergillus.
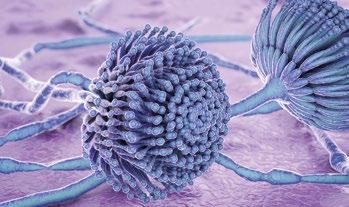
Las Fumonisinas (FUM), la Zearalenona (ZEN), la toxina T-2 (T-2) y el Deoxinivalenol (DON) producidos por especies de Fusarium.
La Ocratoxina A (OTA) producida por especies de Aspergillus y Penicillium.

(Changwa et al., 2018; Njobeh et al., 2012)
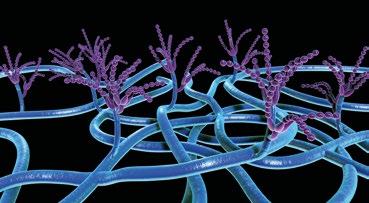
Debido a un balance energético negativo preexistente, las vacas en periodo de transición son especialmente sensibles a la exposición a piensos contaminados con mohos, esporas fúngicas y micotoxinas (Donkor et al., 2016).
Las micotoxinas afectan a los animales a través de diferentes mecanismos y varios factores influyen en el impacto que pueden tener, entre ellos:
Tipo de micotoxina
Especie animal
Edad del animal
Nivel y duración de la exposición a las micotoxinas
(Pier et al., 1980)
La contaminación de los piensos para ganado lechero con micotoxinas ha sido señalada con frecuencia, lo que supone una grave limitación para la salud y la productividad de los animales.
Además, algunas micotoxinas y sus metabolitos se excretan en la leche, especialmente la Aflatoxina M1 (AFM1), lo que significa que los seres humanos también pueden verse afectados (Kemboi et al., 2020).

AFM1
Algunas micotoxinas afectan a órganos específicos como el hígado o los riñones (Elgioushy et al., 2020)
Sin embargo, las condiciones ambientales, el estado de salud de los animales y otros factores estresantes también influyen en los efectos negativos de las micotoxinas (Tola y Kebede, 2016).
Aspergillus fumigatus es uno de los principales hongos micotoxigénicos que infectan forrajes en condiciones cálidas (Alonso et al., 2015; Frisvad et al., 2009; Storm et al., 2008).


Produce más de 226 metabolitos secundarios potencialmente bioactivos (Frisvad et al., 2009).
Por ejemplo:
El DON y otros Tricotecenos, como las toxinas T-2 y HT-2, el Diacetoxiscirpenol (DAS) y el Nivalenol (NIV), son micotoxinas producidas por Fusarium, y se sospecha que están implicadas en brotes de enfermedades de animales de granja en muchas zonas del mundo (Antonissen et al., 2014).
Penicillium roqueforti y P. paneum producen varios metabolitos secundarios con efectos inmunosupresores, antibacterianos y otros efectos toxicológicos en animales (Gallo et al., 2015; O’Brien et al., 2006).
El punto de partida para que las micotoxinas afecten a la salud y la productividad de los animales es la inducción de estrés oxidativo, hipoxia, disminución de la fagocitosis e inmunosupresión (Oswald et al., 2005).
Por ejemplo, se ha detectado gliotoxina, un inmunosupresor, en animales infectados por A. fumigatus con el consiguiente aumento de su virulencia (Sutton et al., 1996), y se ha descubierto que las aflatoxinas suprimen las citoquinas inflamatorias en el ganado (Kurtz y Czuprynski, 1992).
Las micotoxinas pueden afectar negativamente a la integridad intestinal que actúa como barrera física que impide el paso de patógenos y toxinas al sistema circulatorio. También aumentan la permeabilidad intestinal y reducen la viabilidad de las células intestinales (Awad et al., 2017; Gao et al., 2020).
Por otro lado, afectan a la microbiota intestinal, provocando un desequilibrio en la población bacteriana con una disminución de las poblaciones beneficiosas y un aumento de las patógenas. En consecuencia, predisponen al hospedador a desarrollar diversos grados de enfermedad clínica (Guerre, 2020).

Por ejemplo, la Zearalenona y sus metabolitos pueden causar cambios en el ecosistema ruminal poco después de la ingestión, incluidos los eucariotas ruminales (Hartinger et al., 2023).
Determinadas micotoxinas ocasionan daños en el tejido hepático y, en consecuencia, influyen en su capacidad de detoxificación (Średnicka et al., 2021).
Las fumonisinas actúan alterando la biosíntesis de los esfingolípidos, provocando la acumulación de esfinganina y toxicidad (Mathur et al., 2001).


También inducen la formación de trampas extracelulares de neutrófilos (NETs), aumentan los niveles de especies reactivas de oxígeno (EROs) y disminuyen la actividad de SOD y CAT. Al mismo tiempo, la exposición a las fumonisinas provoca una fosforilación dependiente de la concentración de ERK-1/2 y p38 en los neutrófilos (Wang et al., 2020).

Las micotoxinas producidas por Fusarium spp. y Aspergillus spp. en las dietas de vacas lecheras pueden influir negativamente en:
El recuento de células somáticas
Los parámetros sanguíneos
La inmunidad (Jovaišienė et al., 2016)
Además, la respuesta de anticuerpos primarios a la inmunización con ovoalbúmina y las concentraciones séricas de sodio y osmolaridad son mayores en las vacas alimentadas con una dieta contaminada con micotoxinas de Fusarium, pero la acción fagocítica de los neutrófilos está deprimida (Korosteleva et al., 2009).
La Citrinina es una micotoxina nefrotóxica producida por varias especies de los géneros
Aspergillus y Penicillium (Chain, 2012), pero también puede aparecer como contaminante indeseable en productos de fermentación de Monascus ruber y en concurrencia con OTA en alimentos o materias primas para piensos (Bouslimi et al., 2008).
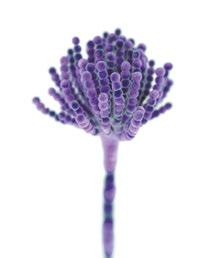
Los experimentos de campo han sugerido que las vacas alimentadas con dietas contaminadas con Citrinina muestran signos de prurito, pirexia y síndrome hemorrágico, así como fiebre, diarrea y uremia (Lloyd, 1980).
Finalmente, las micotoxinas también tienen el potencial de afectar a la función reproductora del ganado (Caloni et al., 2009). Por ejemplo:

Un estudio controlado con vacas no lactantes alimentadas con 500 mg de Zearalenona (concentraciones dietéticas calculadas de aproximadamente 25 ppm de Zearalenona) mostró que los cuerpos lúteos eran más pequeños en las vacas tratadas.

La ingesta de Zearalenona a través de la dieta, incluso cuando está por debajo del nivel umbral de contaminación permitido en Japón, puede afectar las poblaciones de folículos antrales ováricos, pero no la fertilidad, de las vacas postparto (Fushimi et al., 2015).
Se ha encontrado que la contaminación por Zearalenona también es perjudicial para la calidad de los ovocitos en novillas (Silva et al., 2021).
Las micotoxinas, alcaloides, ciertas lactonas y cumarinas, así como los ésteres carboxílicos eicosanoicos, no son degradados (al menos, no completamente) por la microbiota ruminal y pueden producir signos clínicos (Fink-Gremmels, 2008b)
Toxinas específicas afectan a órganos o tejidos concretos como el hígado, el riñón, la mucosa oral y gástrica, el cerebro o el tracto reproductor (FinkGremmels, 2008b)

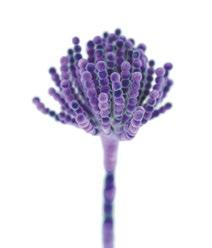
Las micotoxinas pueden provocar episodios agudos cuando los animales consumen cantidades críticas.

En la micotoxicosis aguda, los signos de la enfermedad suelen ser marcados y directamente referibles a los órganos diana afectados.
A concentraciones más bajas (exposición crónica), los efectos de las micotoxinas son más variables.
Reducen la tasa de crecimiento de los animales jóvenes y algunos interfieren con los mecanismos de resistencia a las enfermedades y alteran la capacidad de respuesta inmunitaria, haciendo que los animales sean más susceptibles a las infecciones (Pier et al., 1980).
Bajo estas circunstancias es frecuente observar problemas crónicos como:
Una mayor incidencia de enfermedades
Un rendimiento reproductivo deficiente
Una producción de leche subóptima
(Whitlow y Hagler Jr, 2010)
Basándonos en la experiencia de campo, los principales hallazgos clínicos de la aflatoxicosis en rumiantes son:
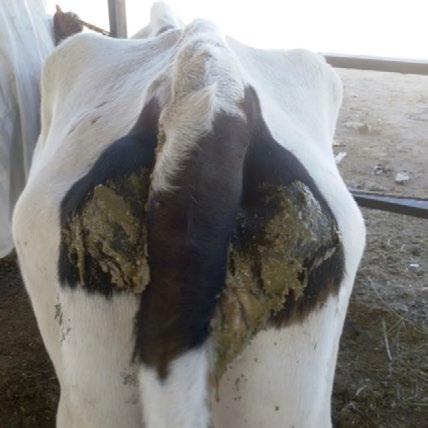

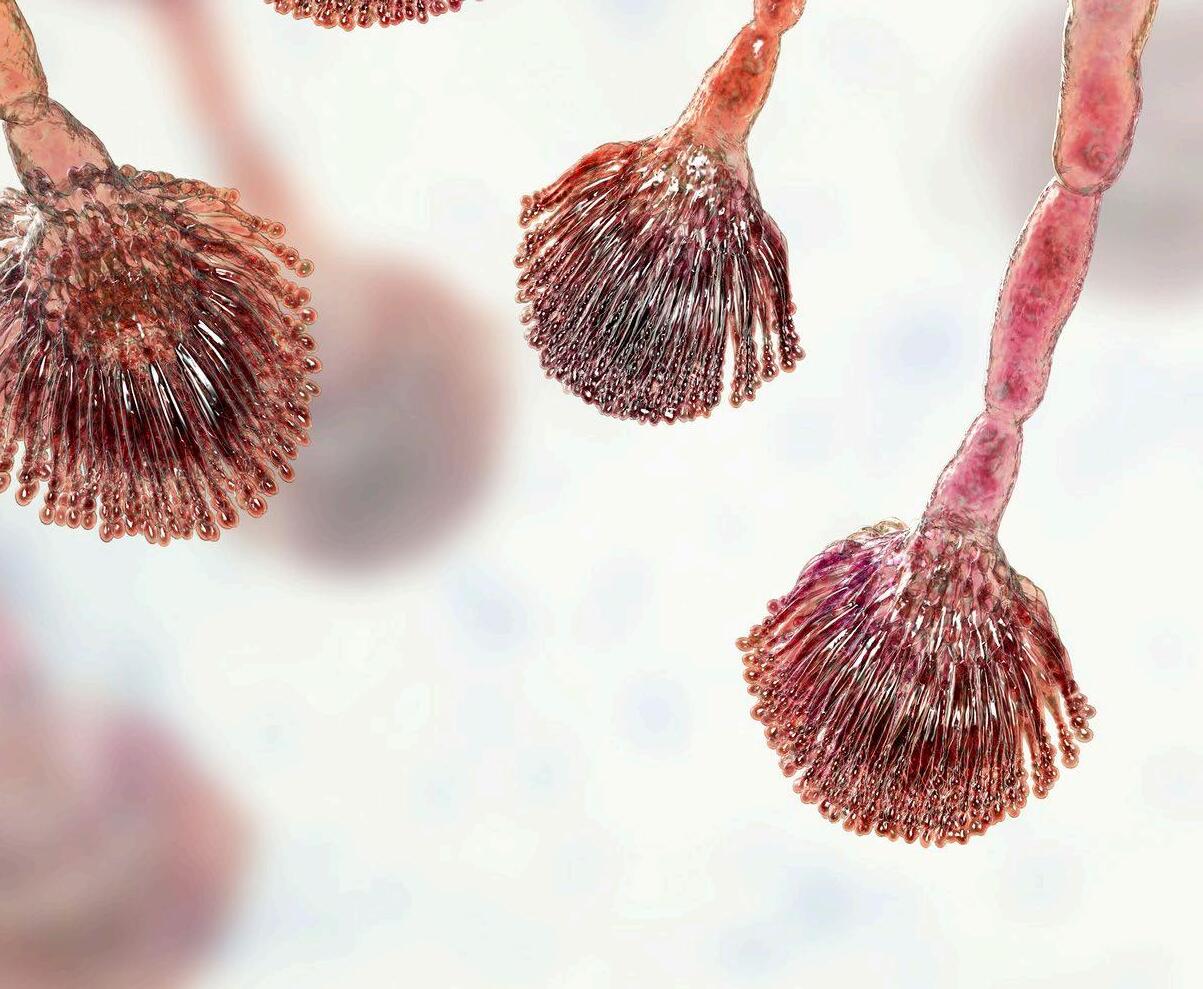
Muerte súbita (Imagen 1)
Diarrea (Imagen 2)
Anorexia
Pelaje áspero
Imagen 1. Muerte súbita de una vaca por aflatoxicosis. Imagen 2. Vaca con signos de diarrea asociada a aflatoxicosisA continuación, se muestran algunos estudios que ponen de relieve los signos clínicos asociados a las aflatoxicosis.
Un brote de aflatoxicosis en ganado vacuno evidenció que la depresión y la inapetencia eran los hallazgos clínicos predominantes (Elgioushy et al., 2020).
Van Halderen et al. (1989) describieron un brote de mortalidad en el campo de 7/25 terneros alimentados con raciones que contenían maíz con 11,79 μg de Aflatoxinas/kg.
Los signos clínicos incluían pérdida de masa corporal, pelaje áspero, diarrea y prolapso rectal.
En Australia, se reportó una aflatoxicosis aguda que causó la muerte de 12/90 terneros afectados por la sequía alimentados con heno de maní que contenía 2.230 μg AF/kg (McKenzie et al., 1981).
En Pakistán se registraron 45 casos de aflatoxicosis en una granja local de Okara (Sohooa et al., 2015).
Las vacas fueron alimentadas con forraje rico en maíz con 33,5 μg de AF/kg y los signos clínicos observados fueron anorexia, depresión, fotosensibilización y diarrea, lo que provocó la muerte de 15 animales.

La aflatoxicosis experimental también se ha asociado a signos clínicos de reducción de la ingesta y la conversión alimentarias, reducción de la producción de leche, reducción de la capacidad reproductiva, cojera, inmunosupresión, hepatotoxicidad y nefrotoxicidad (Gonçalves et al., 2015).
Se observó una disminución significativa de la producción de leche en el ganado alimentado con 13 mg de AFB1/día durante 7 días (Applebaum et al., 1982).
También se describió una disminución numérica de la producción de leche en vacas alimentadas con 75 μg/kg de ingesta de materia seca (IMS) (1.725 μg/cabeza/día) durante 5 días (Ogunade et al., 2016) y (Jiang et al., 2018).
En otro estudio (Sulzberger et al., 2017), se registró una depresión en la producción de leche y la conversión alimentaria a 100 μg AFB1/kg de IMS.
En cambio, algunos estudios sobre niveles bajos de aflatoxinas han mostrado una disminución poco significativa en la producción de leche (Kutz et al., 2009; Masoero et al., 2007; Sumantri et al., 2012).
La exposición a las aflatoxinas también afecta a la fermentación ruminal, reduciendo la utilización de nutrientes y afectando finalmente a la productividad animal (Kemboi et al., 2020).
Por ejemplo, se ha descrito una reducción de la producción de gas, de la digestibilidad de la materia seca y de las concentraciones de amoníaco-N causadas por la AFB1 in vitro (Mojtahedi et al., 2013).
En otro estudio, la AFB1 redujo las concentraciones de amoníaco-N y ácidos grasos volátiles (AGV) sin reducir la digestibilidad de la materia seca ni afectar a los patrones de AGV (Jiang et al., 2012).

Se ha observado que el DON afecta a la fermentación ruminal y puede reducir la producción de leche (Whitlow y Hagler, 2010).
En un estudio sobre el efecto de una dieta contaminada con DON en vacas lecheras Holstein no lactantes alimentadas con una dosis de 1,5 mg DON/kg y 6,4 mg DON/kg de alimento durante 6 semanas, se produjo un ligero descenso en el consumo de alimento tras el cambio de la dosis baja (1,5 mg DON/kg) a la dosis alta (6,4 mg DON/kg) (Trenholm et al., 1985).

En terneros, se encontró una insuficiencia hepática severa en terneros de 2-3 meses de edad sin rumen funcional inducida por 1,13 mg DON/kg de alimento (Valgaeren et al., 2019).
Los rumiantes son más resistentes a la toxicidad de las fumonisinas que los animales monogástricos (Mathur et al., 2001), sin embargo:
En pruebas de alimentación con 75 mg FB1/kg, 94 mg FB1/kg y 105 mg FB1/kg durante 14 días, 253 días, y 31 días, respectivamente, se encontró una reducción de la producción de leche, un menor consumo de alimento, hepatotoxicidad, nefrotoxicidad y problemas de reproducción (Richard et al., 1996).
La administración intravenosa experimental de 1 mg FB1/kg a terneros durante 7 días causó letargo, pérdida de apetito, hepatotoxicidad y nefrotoxicidad (Mathur et al., 2001).
En un estudio con terneros machos Holstein alimentados con leche de 7 a 14 días tratados diariamente con 1 mg FB1/kg (iv) hasta la eutanasia el día 7, estaban letárgicos y tenían menos apetito a partir del día 4 (Mathur et al., 2001).
La ocratoxicosis es raramente reportada en bovinos, lo que se atribuye a la capacidad de la microbiota ruminal para degradar fácilmente la OTA a formas no tóxicas (Richard et al., 1996).
Sin embargo, se ha registrado experimentalmente anorexia, diarrea, dificultad para levantarse y cese de la producción de leche con recuperación al 4º día en ganado alimentado con una dosis única alta de OTA (13,3 mg DON/kg), mientras que en el campo, dosis bajas (0,2 mg DON/kg, 0,75 mg DON/kg, y 1,66 mg DON/kg) durante 5 días, no produjeron enfermedad clínica (Ribelin et al., 1978).
En el ganado lechero, la Toxina T-2 se ha asociado con gastroenteritis hemorrágica (Whitlow y Hagler Jr, 2010), rechazo del alimento y lesiones gastrointestinales (Weaver et al., 1980).
Weaver et al. (1980) reportaron depresión severa, ataxia de los cuartos traseros, knuckling de las patas traseras, apatía y anorexia en un ternero alimentado con 0,6 mg de Toxina T-2/kg durante siete días consecutivos.
La reducción de la producción de leche y la ausencia de celo también se han asociado a la Toxina T-2 (Whitlow y Hagler, 2010).
Se han registrado abortos precoces en ganado alimentado con heno que contenía 10 mg de ZEN/kg (Kallela y Ettala, 1984).
Se han reportado ciclos estrales anormales, vaginitis, celo conductual en animales gestantes, desarrollo mamario en vaquillas prepuberales y esterilidad en ganado alimentado con 1,5 mg de ZEN/kg de alimento (Gupta, 2012).
Estudios experimentales utilizando 500 mg y 250 mg de Zearalenona purificada al 99% en una cápsula de gelatina administrada por vía oral al ganado lechero lactante y novillas vírgenes, respectivamente, no mostraron efectos, excepto la depresión en la tasa de concepción en las novillas primerizas (Weaver et al., 1986a, b).
Según la experiencia de campo, la vesícula biliar, el hígado y los riñones son los órganos más comúnmente afectados en casos de aflatoxicosis (Imágenes 3, 4 y 5).


 Imagen 3. Vesícula biliar agrandada en una vaca muerta afectada por aflatoxicosis.
Imagen 4. Congestión renal en ganado bovino afectado por aflatoxicosis.
Imagen 3. Vesícula biliar agrandada en una vaca muerta afectada por aflatoxicosis.
Imagen 4. Congestión renal en ganado bovino afectado por aflatoxicosis.
Se ha observado que la toxicidad aguda por aflatoxinas provoca importantes signos de lesiones hepáticas que dan lugar a congestión y hemorragias (Pier, 1992; Pier y Richard, 1992).
La aflatoxicosis también provoca la acumulación de ácidos grasos en el hígado, los riñones y el corazón, y puede ser responsable de encefalopatías y edemas (Pfohl-Leszkowicz, 2000).

Sin embargo, la aflatoxicosis crónica es más frecuente y, en este caso, el hígado es el principal objetivo.
Las aflatoxinas actúan como agentes intercalantes del ADN, uniéndose a las bases de guanina y provocando la muerte celular o la formación de tumores (Pfohl-Leszkowicz, 2000).
La administración oral de una dieta que contenía FB1 (2,36 mg FB1/kg/día incrementado a 3,54 mg FB1/kg/día) a terneros durante 239 a 253 días mostró proporciones elevadas de esfinganina/ esfingosina con cambios morfológicos hepatocelulares leves acompañados de cambios epiteliales leves del conducto biliar (Baker y Rottinghaus, 1999).
Las concentraciones de esfinganina y esfingosina en hígado, riñón, pulmón, corazón y músculo esquelético aumentaron en terneros Holstein machos alimentados con leche de 7 a 14 días de edad tratados con 1 mg/kg (iv) diariamente hasta su eutanasia el día 7.
Las lesiones hepáticas se caracterizaban por cordones hepáticos desorganizados, apoptosis de hepatocitos de gravedad variable, proliferación de hepatocitos y proliferación de células de los conductos biliares.
Las lesiones renales consistían en cambios vacuolares, apoptosis, cariomegalia y proliferación de células tubulares renales proximales, así como dilatación de los túbulos renales proximales (Mathur et al., 2001).
Además, en dos terneros alimentados con el nivel máximo de Fumonisinas se describieron aumentos significativos de la actividad de las enzimas hepáticas en suero, con lesiones hepáticas microscópicas leves y una alteración final de la blastogénesis linfocitaria (Osweiler et al., 1993).
Artículo adaptado de “Micotoxinas en rumiantes - Síntomas, lesiones y patogénesis desde el punto de vista clínico” publicado en mycotoxinsite.com
 ACCEDER A BIBLIOGRAFÍA
Micotoxicosis en vacasPatogénesis, signos y lesiones DESCÁRGALO EN PDF
ACCEDER A BIBLIOGRAFÍA
Micotoxicosis en vacasPatogénesis, signos y lesiones DESCÁRGALO EN PDF
La paratuberculosis (PTB) es una infección ocasionada por una bacteria del género Mycobacterium (concretamente, M. avium subsp. paratuberculosis) que puede afectar a multitud de especies animales domésticas y silvestres entre las que podemos incluir a los rumiantes domésticos y salvajes.



 Christian de la Fe, Antonio Sánchez, Joaquín Amores, Xóchitl Hernández y Juan Carlos Corrales Grupo de Investigación Sanidad de Rumiantes, Departamento de Sanidad Animal, Facultad de Veterinaria, Universidad de Murcia. Campus Regional de Excelencia Internacional Mare Nostrum
Christian de la Fe, Antonio Sánchez, Joaquín Amores, Xóchitl Hernández y Juan Carlos Corrales Grupo de Investigación Sanidad de Rumiantes, Departamento de Sanidad Animal, Facultad de Veterinaria, Universidad de Murcia. Campus Regional de Excelencia Internacional Mare Nostrum
En el ámbito de los pequeños rumiantes, al ser una infección que raramente se manifiesta afectando a muchos animales a la vez, se ha cometido el error durante muchos años de no tenerla en consideración en referencia al control.
El resultado es bien conocido por todos… Su carácter endémico y la elevada distribución del agente, tanto en las explotaciones caprinas como en las ovinas.
¿La solución? Compleja pero posible, al menos para disminuir su prevalencia y el efecto perjudicial sobre el conjunto del rebaño.
La paratuberculosis ocasiona una enteritis granulomatosa de curso crónico que, progresivamente, ocasiona un síndrome de malabsorción en los animales infectados.
Los animales, que habitualmente se infectan tras el nacimiento -aunque hay otras posibilidades-, normalmente manifiestan un cuadro clásico de adelgazamiento progresivo y episodios de diarrea en la fase final de la infección que precede a una muerte segura.
En esta fase clínica, que no es más que la fase final de la infección, el animal excreta una gran cantidad de microrganismos a través de las heces, contaminando el ambiente y favoreciendo la supervivencia de la bacteria en la explotación.



Desafortunadamente, la importancia económica de la infección se ve enmascarada por el carácter inespecífico de los síntomas y el escaso número de animales que los desarrollan a la vez en los rebaños afectados, a lo que se une el limitado número de casos en el que se realiza el diagnóstico específico de la infección.

Si bien las pérdidas directas asociadas a la mortalidad (~10%) pueden ser las más evidentes y, en ocasiones, las únicas perceptibles por parte del ganadero, lo cierto es que el efecto de la paratuberculosis va mucho más allá.
Para empezar, hay que contabilizar el efecto que ocasiona el desvieje prematuro de una serie de animales que, alrededor de los 2-3 años de edad, se encuentran en su mejor momento productivo.
Hay explotaciones que, si tienen una elevada tasa de desvieje, puede ser que ni siquiera lleguen a observar la clínica propia de la infección, aunque lo cierto es que cada vez se observa la paratuberculosis clínica en individuos más jóvenes.
Por otro lado, hay que considerar las pérdidas indirectas asociadas a la infección que, en conjunto, pueden llegar a ser más importantes que las directas. En función de la prevalencia, puede registrarse:

Una disminución importante de las producciones (láctea y cárnica).
Una mayor predisposición a padecer otro tipo de procesos, entre los que destacan las mamitis, por su efecto sobre la economía de las explotaciones lecheras
La Paratuberculosis puede afectar a múltiples especies entre las que se incluyen los caballos, los perros, los cerdos o los conejos, donde M. avium subsp. paratuberculosis puede generar cuadros clínico-lesionales muy importantes.
Todo ello complica muchísimo determinar cuál es el reservorio principal de la infección.
Si bien todos los factores que generan estrés en los animales predisponen a la aparición de la sintomatología clínica, lo cierto es que la susceptibilidad a la infección disminuye con la edad.
Los animales jóvenes son los más sensibles a la infección, lo cual no quiere decir que los animales adultos no puedan infectarse.
Sin embargo, en este último caso, es bastante improbable que lleguen a desarrollar un proceso clínico, pero pueden ser portadores y eliminar el microorganismo sin manifestar síntomas.
Hay que tener claro que el microorganismo se elimina a través de las heces de los animales infectados (Imagen 1), facilitando enormemente su supervivencia en las explotaciones, lo que supone un serio hándicap para el control efectivo de la explotación.
Los animales infectados excretan la bacteria a través de las heces durante varios años, de forma intermitente antes de desarrollar el cuadro clínico. Además, también se ha demostrado su presencia en otras posibles fuentes de infección, como la leche o el semen.
Clínicamente, la presentación esporádica de los casos ha conducido, desafortunadamente, a menospreciar su importancia.
Como ya hemos comentado, se trata de la fase final de la infección, una fase en la que la bacteria ha vencido todos los recursos disponibles por parte del sistema inmunitario del hospedador, incapaz de controlar la diseminación de la bacteria.
El adelgazamiento progresivo (Imagen 2) se produce inevitablemente, aunque el animal sigue comiendo, lo que ha conllevado la aplicación errónea de medidas y tratamientos diversos para tratar de recuperar animales clínicamente afectados.
Imagen 1. La excreción fecal de M. avium subsp. paratuberculosis contamina todo y complica enormemente el control de la infección.
Se trata de un microorganismo que sobrevive mucho tiempo en el exterior, especialmente en zonas húmedas y sombrías, permaneciendo infectante durante meses.

El contagio es fundamentalmente fecal-oral pues, en el caso de desarrollarse la lactancia natural, los animales se infectan al mamar de las ubres sucias de sus madres.
La transmisión venérea y el contagio a través de pastos o agua contaminada también son posibles vías de infección.
En las cabras y ovejas la diarrea no siempre está presente, o al menos es menos frecuente que en el ganado bovino, sin embargo, se presenta.
En ocasiones, y aunque el adelgazamiento es lo más característico, la hipoproteinemia da lugar a la presentación de edemas subcutáneos que aparecen en algunas zonas anatómicas del animal afectado (papada, ubre, labios, etc.).
La producción de leche en los animales disminuye progresivamente ya que, aunque coman normalmente, la absorción de nutrientes está muy limitada a nivel intestinal.

Imagen 2. El adelgazamiento progresivo en las fases finales de la infección constituye una de las imágenes clásicas de la Paratuberculosis en los pequeños rumiantes.

Lo primero que se debe tener claro es que no es una lucha sencilla y no hay un tratamiento eficaz para la infección. infección. Por eso, lo más importante es eliminar a los individuos afectados lo antes posible, pues todo el tiempo que permanezcan en la explotación estarán excretando la bacteria, favoreciendo así su mantenimiento en el rebaño.
A partir de ahí, la forma de proceder dependerá de muchos factores entre los que deberían considerarse la prevalencia de la infección y, posiblemente lo más importante, las “posibilidades de trabajo” de la explotación.
Si el objetivo es disminuir la prevalencia e incluso llegar a la erradicación, se debe tener en cuenta que el diagnóstico no es sencillo y se complica especialmente en los estadios iniciales de la infección.
Tal y como se ha señalado anteriormente, la gran capacidad de supervivencia del bacilo en el exterior implica la existencia de un verdadero reservorio telúrico frente al que es muy complicado luchar.
Para el control de la Paratuberculosis se deben considerar las siguientes medidas, teniendo en cuenta que lo primordial es tratar de evitar o limitar la infección de los individuos jóvenes de la explotación:
Higiene y limpieza exhaustiva, tratando de limitar el contacto con las heces de los individuos jóvenes.
Limpieza y desinfección de las instalaciones, considerando el vacío sanitario de los lotes.
Uso de calostro tratado y lactancia artificial (Imagen 3) para la reposición para evitar que los jóvenes contacten con las heces de los adultos y puedan infectarse.

Separación de los jóvenes de los adultos en la explotación, con todas las consideraciones que ello conlleva para el manejo general.
Imagen
Cuando estas medidas sean inviables (o al menos no aplicables en su totalidad), existen vacunas que reducen la excreción de la bacteria en las heces y limitan muchísimo la presentación de síntomas clínicos.
Es importante recordar que la vacuna no previene la infección, pero limita sus consecuencias. En algunas comunidades autónomas su uso está o ha estado restringido, por lo que hay que consultar las condiciones de su uso en cada zona.
La Paratuberculosis es una infección compleja cuyos efectos, enmascarados en muchos momentos, han motivado que no se le haya prestado atención a la hora de plantear estrategias de control efectivas.
No todas las explotaciones tienen los recursos necesarios para plantear un programa de control y erradicación y, en estos casos, la vacunación se presenta como una estrategia útil y rentable para mitigar el efecto clínico de la infección en los rebaños ovinos y caprinos.
3. La lucha frente a la infección debe basarse en una serie de pilares básicos, entre los que la lactancia artificial es, sin duda, uno de los más importantes. La paratuberculosis, “algo más” que una infección crónica en los pequeños rumiantes DESCÁRGALO EN PDF
Leyla Ríos de Álvarez Profesora Asistente Extensión/Investigación, Department of Animal and Dairy Sciences, Mississippi State University leyla.rios@msstate.edu
Uno de los problemas que mayores pérdidas económicas ocasiona en los sistemas de producción de pequeños rumiantes son los nematodos gastrointestinales (NGI) La mayoría de estos NGI tienen un ciclo vital directo, es decir, no tienen hospedador intermediario.
De este modo, el hospedador (ovino o caprino) presenta los nematodos adultos que se reproducen, permitiendo que las hembras excreten huevos.
En la Figura 1 se puede observar cómo los huevos de nematodos salen al medioambiente a través de las heces y, al entrar en contacto con el suelo, el calor y la humedad favorecen su eclosión.

Los nematodos adultos del tracto digestivo de las ovejas ponen huevos
Los huevos pasan a los pastos a través del estiércol
Las larvas infecciosas son ingeridas por las ovejas que pastan
Figura 1. Esquema general del ciclo vital de los nematodos que afectan al ganado ovino y caprino.
Las larvas brotan de los huevos y se desarrollan hasta el 3er estadio infeccioso en suelo y estiércol
El desplazamiento de las larvas L3 dependerá de:
Estructura del pastizal (Silva et al., 2008)
Precipitaciones (Santos et al., 2012)
Humedad del suelo (Khadijah et al., 2013)
Radiación solar (van Dijk et al., 2009)
Al eclosionar los huevos se producen las larvas L1, que se desarrollan y mudan la cutícula, pasando a L2 dentro de las heces gracias a las condiciones medioambientales y a la presencia de bacterias que les sirven de alimento. Una segunda muda les permite desarrollarse hasta larvas L3
Las larvas L3, aun con la cutícula y fuera de las heces, mueven hacia los pastos y, cuando los animales pastan, consumen las larvas y se parasitan, comenzando nuevamente el ciclo (Rios-de Alvarez, 2009).

Esto explica por qué las larvas L3 están presentes en mayor proporción en los estratos bajos del pastizal y que su supervivencia y diseminación se vean favorecidas por las precipitaciones y la baja intensidad de luz solar.
Las condiciones ambientales también afectan a la duración del ciclo vital (7-21 días), dependiendo de si son más o menos favorables.
Además de los recuentos de huevos en heces (HPG, huevos/g de heces), existen indicadores de salud del animal (ausencia o nivel mínimo de parasitismo) que se resumen en el Five Point Check© (Bath and van Wyk, 2009) (Figura 2).
Estos indicadores son importantes para decidir si un animal debe o no desparasitarse
1
Descarga nasal: si bien no está directamente relacionada con los NGI, la presencia de secreción nasal clara o purulenta puede deberse a la presencia de larvas de la mosca Oestrus ovis.
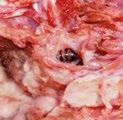
Esta es una infección que, además de afectar al bienestar de los animales, puede conducir a problemas secundarios de inmunodepresión e infecciones bacterianas.
Nariz (descarga)

Ojo (anemia)
Lomo (condición corporal)
Mandíbula (hinchazón)
2 3
Cola (suciedad)
Mucosa ocular: el uso de la tarjeta
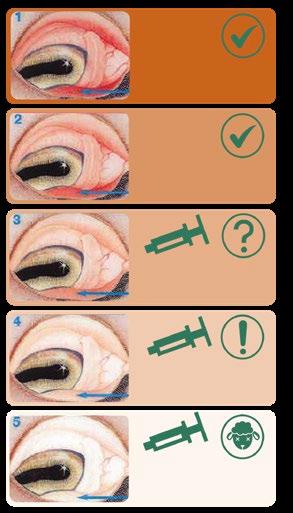
(Figura 3) permite estimar el grado de anemia producido por el NGI hematófago Haemonchus contortus.
*Esta figura constituye una aproximación y no debe usarse como reemplazo de la tarjeta original.
Edema submaxilar: su aparición es un indicador típico de parasitismo y de hipoproteinemia producida por los NGI.
Figura 2. Indicadores del Five Point Check© (Bath and van Wyk, 2009). Figura 3. Tarjeta FAMACHA© - Guía de anemia que indica el momento adecuado para desparasitar el animal según la coloración de la mucosa ocular. Imagen 1. Presencia de larva de Oestrus ovis en cavidad nasal (Cortesía de Avega Gestión, Albacete). FAMACHA©4
Condición corporal: medición subjetiva de la CC, ya sea de manera visual (en el caso de ovinos y caprinos de pelo corto) o por palpación del lomo y costados (en animales de lana). Se utiliza una escala del 1 al 5 (Figura 4).
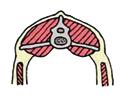
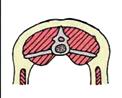
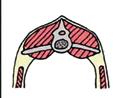
5
Dag Score: utilizada para medir, de manera subjetiva, el nivel de suciedad por heces blandas o diarrea que se acumula en la parte trasera de los animales.


Tanto en la medición de la CC como en el Dag Score es recomendable que el evaluador sea siempre el mismo para minimizar el error humano.
En la Figura 5 se muestran todas las escalas utilizadas en el Five Point Check©.
Figura 4. Escala de condición corporal usada para pequeños rumiantes (Thompson y Meyer, 1994). Figura 5. Cartilla que incluye todas las escalas e indicaciones para realizar el Five Point Check© en ovinos y caprinos (Bath and van Wyk, 2009). CC 1: Emaciada CC 2: Delgada CC 4: Gorda CC 5: Obesa

Cuando se habla de control sostenible del parasitismo, se refiere al uso de alternativas que eviten la aparición de resistencias y minimicen la aparición de enfermedades y pérdidas productivas (Besier, 2012)
Por otra parte, el control integrado de parásitos es la combinación del control tradicional junto con el control alternativo, para así no depender exclusivamente de los antihelmínticos comerciales, sino utilizar indicadores y otras medidas de control que permitan espaciar el uso de los mismos (Kahn and Woodgate, 2012).
El objetivo al final es mantener parte de la población parasitaria “en refugio”, es decir, desparasitar solo aquellos animales que lo requieran, evitando así que todos los NGI estén expuestos a los compuestos comerciales y que desarrollen resistencias (Figura 6).
Entre las alternativas incluidas en el control sostenible de NGI se encuentran aquellas que ayudan a reducir la ingestión de larvas infectivas (L3) y aquellas dirigidas al animal (hospedador).
A. ESTRATEGIAS BASADAS EN EL ADECUADO MANEJO DEL PASTIZAL PARA MINIMIZAR LA INGESTIÓN DE LARVAS (L3)
Adecuados períodos de rotación/descanso del pastizal entre un grupo de animales y el siguiente, tratando de evitar que las larvas del primer grupo de animales contaminen al siguiente.
Pastoreo de animales jóvenes/con baja inmunidad en praderas “limpias”, es decir, que no hayan sido previamente pastoreadas por animales adultos contaminados.
Evitar el sobrepastoreo ya que, a medida que los animales consumen demasiado la biomasa de la pradera, se acercan a los estratos inferiores donde la posibilidad de contaminación con larvas L3 o estadios infectivos de los NGI es mayor.
LA IMPORTANCIA DE PRESERVAR EL “REFUGIO”
Población de parásitos en el rebaño:
Al tratar todo el rebaño, no se conserva ningún refugio
Al tratar solo el 50% del rebaño, se converva algún refugio
Todos los parásitos susceptibles mueren, quedando solo los parásitos resistentes que se reproducen y transmiten genes de resistencia a su descendencia
Algunos parásitos susceptibles permanecen para diluir los parásitos resistentes, retrasando el desarrollo de una población totalmente resistente
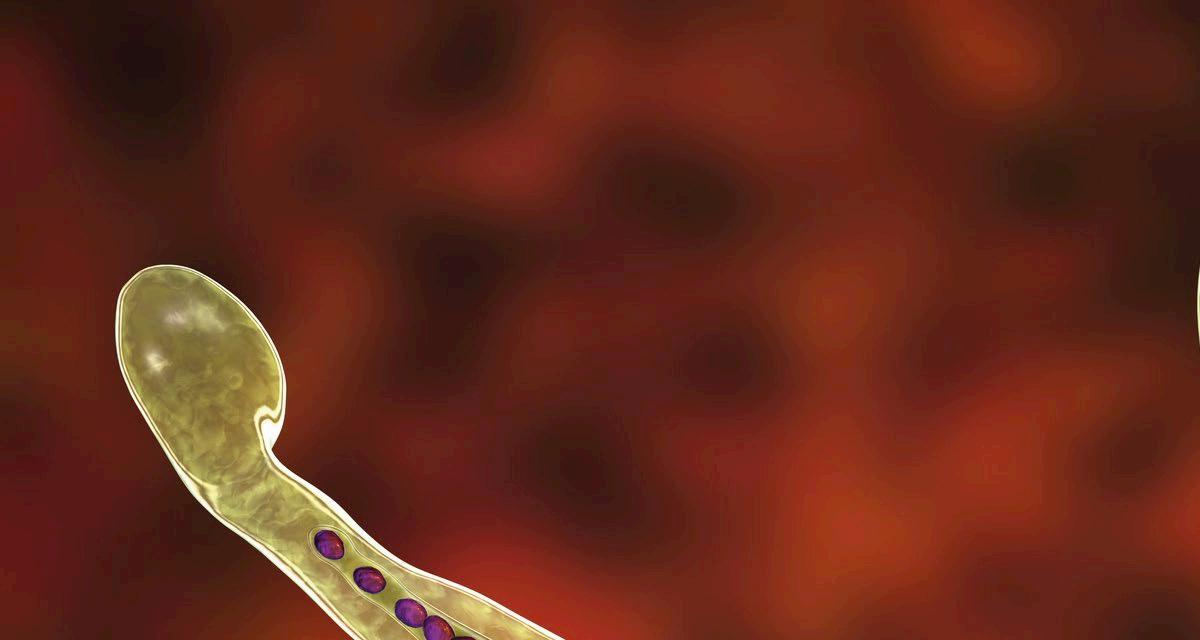 Figura 6. Esquema explicativo sobre la importancia de preservar la población parasitaria “en refugio” en los animales (Mallet, 2021).
Figura 6. Esquema explicativo sobre la importancia de preservar la población parasitaria “en refugio” en los animales (Mallet, 2021).
Uso de forrajes bioactivos o plantas que contengan metabolitos secundarios: los taninos, saponinas y lectinas, entre otros, pueden tener efecto antihelmíntico, contribuyendo a la disminución de las cargas parasitarias.
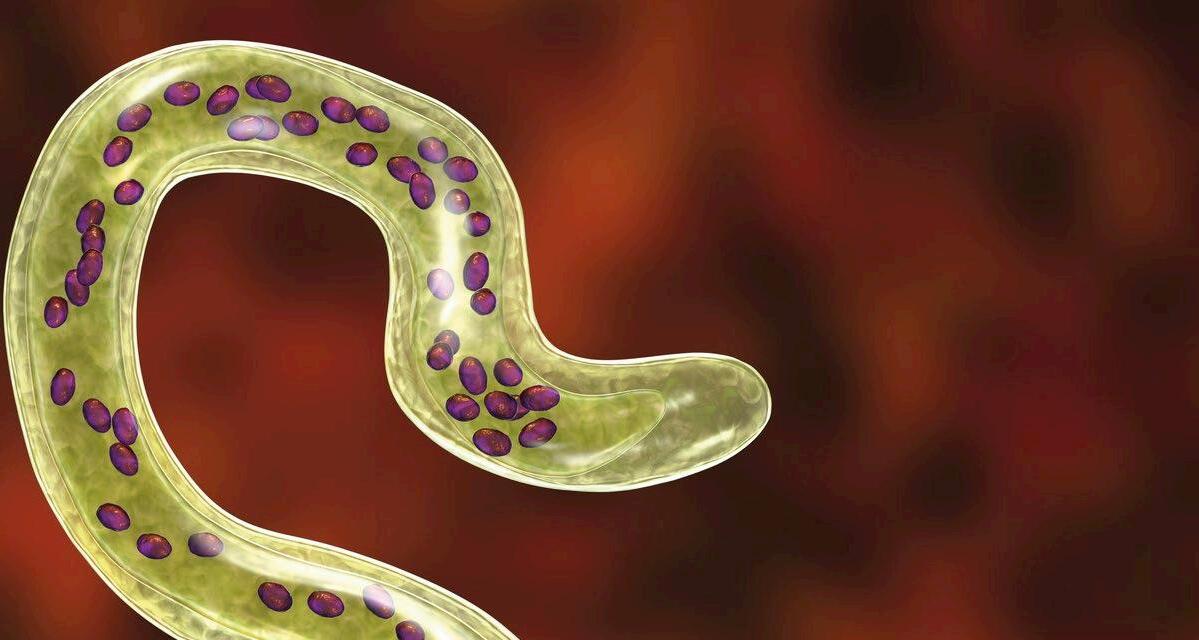
Uso de praderas multiespecie, de forma que los animales tengan acceso a una dieta adecuada y diversa que les permita cubrir mejor sus requerimientos nutricionales, mejorando así su capacidad de respuesta inmunitaria frente a los parásitos.
Además, tienen más posibilidades de acceder a plantas con metabolitos secundarios.
Uso de estratos vegetales de diferentes alturas: esto permite que los animales (principalmente cabras) puedan alternar el pastoreo con el ramoneo y así reducir el consumo en los estratos más contaminados.

Pastoreo mixto: la combinación de ovinos y caprinos con otras especies como bovinos o equinos se refleja en una disminución de la carga de larvas infectivas en los potreros de manera que, tras el pastoreo de los pequeños rumiantes, dejaremos pastar a bovinos o equinos, que actuarán como “aspiradoras de larvas L3”.
Tratamientos alternativos, como el uso de hongos nematófagos (p.ej. Duddingtonia flagrans), que se suministran a los animales a través del alimento, desarrollándose estos en las heces, atrapando las larvas y evitando que contaminen los pastos y recontaminen a los animales.
Selección/descarte de animales: conservar en el rebaño los animales más productivos y resistentes al parasitismo, y descartar aquellos que requieran constantes desparasitaciones o que permanentemente presenten cargas parasitarias elevadas.

También podemos descartar animales en edad avanzada ya que pueden presentar problemas de dentadura, lo cual afecta a su alimentación, comprometiendo su inmunidad y haciéndolos más susceptibles a enfermedades.
Uso de razas más resistentes: algunas razas tienden a ser mas tolerantes al parasitismo y, a pesar de la carga parasitaria, crecen y se reproducen de manera adecuada.
En el caso de los ovinos de pelo son conocidas las razas St. Croix y Katahdin por su mayor resistencia al parasitismo (Burke and Miller, 2004).
Desparasitación selectiva, a través del uso de los indicadores antes mencionados, como FAMACHA© o la medición de la CC.
Es importante tener mucho cuidado con aquellos animales con la inmunidad comprometida (próximos al destete o periparto), así como con los animales nuevos en el rebaño.
Suplementación estratégica: la relación entre una adecuada nutrición y una buena inmunidad es de sobra conocida, por lo que es muy importante
DESCARGAR BIBLIOGRAFÍA
Abordaje sostenible al control parasitario en pequeños rumiantes
DESCÁRGALO EN PDF
¿Quieres calcular el retorno de tu inversión?

Escanea el QR y utiliza la calculadora Mastivac
MASTIVAC suspensión inyectable para bovino. Vacuna inactivada polivalente frente a la mamitis.
Composición por dosis (5 ml): Antígenos inactivados de S. agalactiae cepa LO1 ≥1 PR; S. dysgalactiae cepa ATCC 43078 ≥1 PR; S. uberis cepa LO1 ≥1 PR; S. pyogenes cepa LO1 ≥1 PR; S. aureus cepa LO1 ≥1 PR; A. pyogenes cepa ATCC 9730 ≥1 P.R; E. coli cepa Bov-10 ≥1 PR; E. coli cepa Bov-14 ≥1 PR; E. coli cepa Bov-15 ≥1 P.R; E. coli cepa Suis-21 ≥1 PR; E. coli cepa J5 ATCC 43745 ≥1 PR. Indicaciones y especies de destino: Bovino (novillas y vacas). Para la inmunización activa frente a las mamitis clínicas y/o subclínicas producidas por S. agalactiae, S. dysgalactiae, S. uberis, S. pyogenes, S. aureus, A. pyogenes y E. coli. Reducción de los signos clínicos de las mamitis clínicas producidas por S. dysgalactiae, S pyogenes, A. pyogenes y E. coli. Reducción del recuento de células somáticas en las mamitis subclínicas producidas por S. agalactiae, S. uberis y S. aureus Vía de administración: Subcutánea. Posología: 5 ml. Pauta de vacunación: Primovacunación: Administrar 2 dosis separadas 15 días. Novillas: Administrar 2 meses antes del primer parto. Vacas: Administrar en cualquier momento independientemente del estado fisiológico del animal. Revacunación: cada 6 meses. Contraindicaciones: Ninguna. Tiempo de espera: Cero días. Presentación: 20 ml y 100 ml. Con prescripción veterinaria. Titular: CZ Veterinaria S.A. Reg. Nº: 2990 ESP
En caso de duda consulte a su veterinario

