INOCUA

Revista Científica

Volumen1|Número1|EneroaJunio|Año2023
e-ISSN: xxxxxxxxxxxxxxx
Revista semestral
Autor: Universidad Nacional Agraria La Molina Web:
Copyright © Universidad Nacional Agraria La Molina
E-mail:
Correspondencia: Universidad Nacional Agraria La Molina, Av. La Molina s/n distrito La Molina.
Telf.:
Volumen 1 Número 1 Año 2023
Validación de método para contenido estomacal en osteíctios en el Perú
Juan C. Saldaña Guerrero; Victoria N. Cabanillas Rojas
Metodología para validación de determinación de sólidos totales suspendidos en agua potable
Lucy Torres; Diana campos; Carmen Quispe; Juliana Legua; César Córdova
Procedimiento para la calificación de personal en laboratorios de ensayo
Lizet Arango; Vanessa Farfán; Evelyn Alcalá; Edson Sanchez; Victor Ponce; Francis Mejia
Estimación de la incertidumbre de resultados de ensayos
DalidAlarcón Cabrera; GiuseppeA. Guardamino Chávez;Aurora Huanca Ochoa; Karin Oros Fuerte; Cristina Rivera Romero
Autorización de personal para la realización de ensayos
Liliana Balbín; José Quinte; MagalyAcosta; Manuel Gamboa
Presentación
La Universidad Nacional Agraria La Molina es una institución líder en investigación en el campo de la agricultura y la alimentación en Perú. Es por ello que realizar investigación científica en temas como la inocuidad alimentaria, el sistema de calidad, los sistemas de seguridad, el medio ambiente y los residuos sólidos es de vital importancia en esta universidad.
La investigación científica es esencial para el desarrollo del conocimiento en cualquier campo. En la agricultura y la alimentación, la investigación puede conducir a la generación de nuevos conocimientos y la actualización de los ya existentes. Por ejemplo, los estudios sobre la inocuidad alimentaria pueden llevar a mejoras en la calidad y la seguridad de los productos alimentarios, lo que beneficia tanto a los consumidores como a los productores.
Además, la investigación científica permite resolver problemas prácticos en el campo de la agricultura y la alimentación. Por ejemplo, se puede investigar cómo mejorar la eficiencia en la producción de alimentos y reducir el impacto ambiental de la producción. También se pueden desarrollar tecnologías y prácticas para garantizar la seguridad de los alimentos y reducir la cantidad de residuos generados por la producción y el consumo de alimentos.
Otro beneficio de la investigación científica es que puede ayudar a establecer estándares y regulaciones para garantizar la calidad y la seguridad de los productos alimentarios. Los resultados de la investigación pueden servir como base para desarrollar políticas públicas y para establecer sistemas de certificación y etiquetado de alimentos.
Finalmente, los profesionales que realizan investigación científica en la Universidad Nacional Agraria La Molina pueden mejorar su capacitación y adquirir habilidades valiosas en la investigación y la innovación. La investigación científica les brinda la oportunidad de trabajar en proyectos que tienen un impacto real y duradero en la sociedad, y les permite estar a la vanguardia de las últimas tendencias y desarrollos en el campo de la agricultura y la alimentación.
Dr. Marcial Silva Jaimes EditorIntroducción
Un artículo científico es un documento escrito que presenta los resultados de una investigación científica. Este tipo de documento se utiliza para comunicar los hallazgos de la investigación a la comunidad académica y científica.
Un artículo científico típicamente consta de varias secciones clave. La sección de introducción es donde se proporciona una revisión de la literatura existente en el campo de investigación y sepresentalajustificaciónylosobjetivosdelestudio.Enlaseccióndemetodología,se describe cómo se realizó la investigación y los métodos utilizados para recolectar y analizar los datos.
La sección de resultados presenta los hallazgos del estudio en detalle y se apoya en gráficos, tablas y otros recursos visuales. En la sección de discusión, se interpretan los resultados y se hace una evaluación crítica del estudio. Finalmente, la sección de conclusiones resume los principales hallazgos y su importancia en el contexto del campo de investigación.
En general, los artículos científicos deben seguir una estructura clara y concisa para permitir queotros investigadores puedan entendery evaluarel estudio. Además,los artículos científicos deben estar escritos en un lenguaje técnico y preciso para garantizar que los hallazgos sean comunicados de manera clara y rigurosa.
Ing. Víctor Meneses Taboada Coordinador AcadémicoISSN (Versión electrónica)


Website:
ARTÍCULO ORIGINAL –RESEARCHARTICLE
Validación de método para contenido estomacal en osteíctios en el Perú
Method validation in stomach contents osteichthyes in the Peru
Juan C. Saldaña Guerrero1; Victoria N. Cabanillas Rojas2
1 Universidad Nacional San Luis Gonzaga de Ica, Ica, Perú.
2 Universidad Nacional Mayor de San Marcos, Lima, Perú.
*Autor de correspondencia: Email: ORCID:
Recibido: 31/01/2016; Aceptado: 30/06/2017; Publicado: 30/06/2023
Resumen
Con el objetivo de validar un método no normalizado para los laboratorios hidrobiológicos, se realizó el análisis del contenido estomacal de los peces en tres laboratorios; los índices que se usaron para la comparación se obtuvieron del análisis de la fase cuantitativa que se utiliza para hallar la amplitud de la dieta. Mientras que, la determinación de la precisión se realizó mediante las condiciones de repetibilidad (ISO 5725-1, 3.14) y reproducibilidad (ISO 57251, 3.18). En conclusión, la validación de un método analítico es un paso fundamental para asegurar que los resultados entregados sean confiables.
Palabras clave: osteíctios; validación; morfométricos; meriticos; veracidad; precisión; repetibilidad; reproducibilidad; incertidumbre.
Abstract
In order to validate a non-standardized method for hydrobiological laboratories, the analysis of the stomach contents of the fish was carried out in three laboratories; the indices that were used for comparison were obtained from the analysis of the quantitative phase that is used to find the breadth of the diet. Whereas, the determination of the precision was made by means of the conditions of repeatability (ISO 5725-1, 3.14) and reproducibility (ISO 5725-1, 3.18). In conclusion, the validation of an analytical method is a fundamental step to ensure that the results delivered are reliable.
Keywords: osteíctios; validation; morphometric; meritic; veracity; precision; repeatability; reproducibility; uncertainty.


Forma de citar el artículo: Saldaña, J., & Cabanillas, V. (2023). Validación de método para contenido estomacal en osteíctios en el Perú. xxxx 1(1): 1-11 (2023). DOI:
DOI:
© Los autores. Este artículo es publicado por la revista xxxxxxx de la Universidad Nacional Agraria La Molina. Este es un artículo de acceso abierto, distribuido bajo los términos de la Licencia Creative Commons Atribución 4.0 Internacional.(https://creativecommons.org/licenses/by/4.0/) que permite Compartir (copiar y redistribuir el material en cualquier medio o formato), Adaptar (remezclar, transformar y construir a partir del material) para cualquier propósito, incluso comercialmentte.
Validación de método para contenido estomacal en osteíctios en el Perú
1. Introducción
Los peces, viven en un medio difícil de estudiar por diversos aspectos. Uno de ellos es su dieta. Por ello, una forma deestablecer el régimen alimenticio de los peces es mediante el análisis de su contenido estomacal. Dicho análisis es unaherramienta que permite inferir cómo en una cadena trófica, los peces interactúan con otras especies (animales y vegetales) y con su medio (Krebs, 1989). Siendo la descripción y cuantificación de la dieta de los organismos acuáticos la base para comprender los ciclos energéticos (Trujillo et al., 2016).
Para realizar el análisis, se utilizan líneas metodológicas definidas, las cuales se eligen en función de las particularidades de la dieta delasespecies enestudio (Ramírez-Herrejón et al., 2013). Ello se debe porque los peces son un grupo diverso y ocupan una gran amplitud de funciones en los sistemas que habitan, desde los consumidores primarios hasta carnívoros tope (Torres-Rojas,2011); por lo tanto, según lo reportado por CantoMaza y Vega-Cendejas, (2008) losestudios del contenido estomacal se tienen que adaptar a las características propias del estudio y al tipo de sistema acuático.Sin embargo, esto plantea una dificultad para homogenizarlasmetodologías eimposibilita la utilización de un mismo procedimiento para todos los grupos de peces (TorresRojas, 2011). Debido a la variedad de técnicas y a la diversidad en losmétodos existentes el objetivo del estudio fue validar un método no normalizado que serealiza en los laboratorios hidrobiológicos, el cual consiste en el análisis de contenido estomacal en peces.
2. Materiales y métodos Conservación de muestras en campo
Las muestras de peces fueron colectadas de las playas de Chincha, Perú, de las faenas de pesca en campo; para el traslado a los laboratorios, las muestras, fueron colocadas en bolsas de polietileno, debidamente etiquetadas, indicando la estación, el arte de pesca, el número de cala y la fecha. Luego se almacenaron en contenedores con hielo para reducir la descomposición. Al llegar al laboratorio, en observaciones de las fichas de datos morfométricos, se indicó si las
muestras llegaron o no al laboratorio con hielo. Si la respuesta es negativa, se registra y coloca el hielo en los contenedores.
Datos morfométricos y merísticos
Antes de iniciar el muestreo biológico, el investigador de turno debía de contar con mandil, guantes y lentes antiimpacto. Los pescados, fueron identificados, separados por especie y colocados en bandejas de plástico dispuestos ordenadamente. Los ejemplares fueron medidos y pesados para obtener su longitud total, longitud estándar, peso, peso eviscerado, sexo, estadio sexual. Los datos fueron colocados en las fichas de muestreo biológico.
Determinación del contenido estomacal de peces
El presente protocolo propone un análisis numérico, gravimétrico y volumétrico del contenido estomacal de peces adaptado de la propuesta de Hyslop (1980).
Procesamiento inicial
El investigador, debe contar con un equipo de protección personal (mandil, guantes, mascarilla y lentes google) antes de iniciar la verificación de los datos del estómago a analizar en la ficha de muestreo biológico correspondiente. Una vez identificado, se pesó el estómago con una balanza analítica (0,0001g) e inmediatamente se realizó una incisión desde el esófago y a lo largo de todo el estómago empleando una tijera de disección. Todo el contenido estomacal fue extraído con ayuda de pinzas y piceta. El procedimiento se realizó sobre una placade vidrio petri de 15cm. Luego, se procedió a la separación, verificación taxonómica y fotografiado de cada ítem alimenticio mediante el empleo de un microscopio estereoscópico y microscopio compuesto. Para la verificación taxonómica se emplearon claves taxonómicas especializadas. En el caso de la Materia Orgánica No Digerida (MOND), esta fue tamiza a través de una malla de 50µm y se le realizó el análisis gravimétrico y volumétrico.
Análisis numérico
Una vez identificado los ítems alimenticios,
se contaron cada uno de sus individuos. Enophiuroideos frágiles secontaronsolo los discos (no los brazos), en poliquetos se contaron solo las regiones cefálicas (prostómio) y en los crustáceos se contaron individuos con cefalotórax. Sin embargo, esta técnica presenta dificultades para aplicarse en especies omnívoras que ingieran detritus (Hyslop, 1980; Canto-Maza y VegaCendejas, 2008) y no es aplicable a especies quepresentensistemas dentariosque trituran el alimento. Es particularmente adecuada para carnívoros y zooplantofagos (Hyslop, 1980).
Análisis gravimétrico
Cada ítem alimenticio (o partes del mismo) fue pesado en una balanza analítica (0,0001g). En caso que no sea percibido por la balanza se asignó un peso de 0,0001g.
Análisis volumétrico
Para determinar el volumen de cada ítem alimenticio se emplearon probetas de 10ml, 25ml y 50ml y jeringas de 1ml, 3ml y 20ml.
Conservación de los ítems alimenticios
Los ítems alimenticios identificados fueron colocados en frascos viales de vidrio de 10ml con alcohol al 70%. En papel vegetal se anotó la especie de pescado, N° de estómago, el ítem alimenticio y la campaña de evaluación. Estos datos deben coincidir con la ficha técnica de análisis del contenido estomacal.
Almacenamiento final de muestras
Los frascos viales, los tubos de microcentrífuga y otros frascos pequeñosse colocaron en contenedores con tapa para evitar la emanación de vapores.
Descarte de residuos
Los restos orgánicos fueron colocados en bolsas de polietileno y colocados en un recipiente de basura al finalizar el trabajo.
Análisis estadístico
Los datos fueron sometidos al análisis estadístico, el cual contempla los siguientes análisis: 1) Análisis aplicando el test de Normalidad y 2) Aplicación de Test de Students y Test F.
3. Resultados y discusión Veracidad
Estudios de comparación interlaboratorio con base en los resultados de los programas de ensayos de aptitud. Si un programa de ensayosdeaptitudexisteparaunanalitodado, losresultadossedebeninterpretarusando los criterios de aceptación del organizador. Dado que muchos procedimientos analíticos han sido implantados con meses o años de antelación estos se consideran procedimientos históricos dentro del laboratorio y por lo tanto es preferible una verificación interlaboratorio de la veracidad, que una comparación de métodos (Nava & López, 2008). El criterio de aceptabilidad para los procedimientos de examen que los laboratorios van a acreditar deben demostrar consistencia en al menos los últimos doce meses en la participación y en los resultados de programas de ensayos de aptitud (Nava & López, 2008).
En la Tabla 1 se muestran los resultados de tres índices determinados en tres laboratorios: Biodiversidad de Margalef (DMg), Shannon y Wiener (H’) y Equidad de Pielou (J’).
*Mín: valor mínimo del índice de los tres valores obtenido por Laboratorio.
#Med: valor medio del índice de los tres valores obtenido por Laboratorio.
°Max: valor máximo del índice de los tres valores obtenido por Laboratorio.
Validación de método para contenido estomacal en osteíctios en el Perú
Índice de Margalef reportado por los tres laboratorios
Para los datos del Índice de Margalef,en la Figura 1 se presenta la Prueba de Normalidad, para los datos de los tres laboratorios. Los valores reportados por los laboratorios muestran un P-valor mayor a 0,05 lo cual indica una distribución normal y la prueba de T-Student para los resultados Laboratorio 2 - Laboratorio 1 (Tabla 2) y Laboratorio 3 - Laboratorio 1 (Tabla 3), generan valores p-valor mayor a 0,05;
por tanto, a un 95% de nivel de confianza no hay diferencia significativa entre los Laboratorios Laboratorio 2 - Laboratorio 1 y Laboratorio 3 - Laboratorio 1. Mientras que, parademostrarlaigualdad devarianzaseusó la prueba F obteniendo un P-valor mayor al 0,05 por tanto a un 95% de nivel de confianza las varianzas son iguales (Tabla 4 y 5) y en la Figura 2 se muestra la comparación de las Desviación Estándar entre el Laboratorio 2 y Laboratorio 1 y, para el Laboratorio 1 y Laboratorio 3.
T de dos muestras para Laboratorio 1 y Laboratorio 2
Error estándar
N Media Desv.Est. de la media
Laborat. 2 3 3,110 0,606 0,35
Laborat. 3 3 3,120 0,421 0,24
Diferencia = mu (Laboratorio 2) - mu (Laboratorio 1)
Estimado de la diferencia: -0,010
IC de 95% para la diferencia: (-1,367; 1,347)
Prueba T de diferencia = 0 (vs. no =): Valor T = -0,02 Valor P= 0,983 GL= 3
Enero - Junio 2023

Tabla 3: Prueba T e IC de dos muestras: Laboratorio 3, Laboratorio 1
T de dos muestras para Laboratorio 3 vs. Laboratorio 1 Error estándar N
de la media
Diferencia = mu(Laboratorio1) - mu(Laboratorio3)
Estimado de la diferencia: -0,870 IC de 95% para la diferencia: (-2,288; 0,548)
Prueba T de diferencia = 0 (vs. no =): Valor T = -1,95 Valor P= 0,146 GL = 3
Tabla 4: Prueba e IC para dos varianzas: Laboratorio 2, Laboratorio 1
Intervalos de confianza de 95% IC para IC para Distribución relación de relación de de los datos Desv.Est. varianza
(0,230; 8,983) (0,053; 80,701)
Continuo ( *, *) ( *, *)
Pruebas Estadística

GL1 GL2 de prueba Valor P
Tabla 5: Prueba e IC para dos varianzas: Laboratorio 3, Laboratorio 1
Intervalos de confianza de 95% IC para IC para Distribución relación de relación de de los datos Desv.Est. varianza
(0,246; 9,580) (0,060; 91,769)
Continuo ( *, *) ( *, *) Pruebas
y,
Validación de método para contenido estomacal en osteíctios en el Perú
Índice de Shannon reportado por los tres laboratorios
Para los datos del Índice de Shannon,en la Figura 3 se presenta la Prueba de Normalidad, para los datos de los tres laboratorios. Los valores reportados por los laboratorios muestran un P-valor mayor a 0,05 lo cual indica una distribución normal y la prueba de T-Student para los resultados Laboratorio 2 - Laboratorio 1(Tabla 6) y Laboratorio 3 - Laboratorio 1 (Tabla 7), generan valores p-valor mayor a 0,05; por
tanto, a un 95% de nivel de confianza no hay diferencia significativa entre los tres laboratorios. Mientras que, para demostrar la igualdad de varianza se usó la prueba F obteniendo un P-valor mayor al 0,05 por tanto a un 95% de nivel de confianza las varianzas son iguales (Tabla 8 y 9) y en la Figura 4 se muestra la comparación de las Desviación Estándar entre el Laboratorio 2 y Laboratorio 1 y, para el Laboratorio 1 y Laboratorio 3.
T de dos muestras para Laboratorio 2 vs. Laboratorio 1
1
Diferencia = mu (Laboratorio 2) - mu (Laboratorio 1)

Estimado de la diferencia: 0,223
IC de 95% para la diferencia: (-0,243; 0,689)
Prueba T de diferencia = 0 (vs. no =): Valor T = 1,52 Valor P= 0,225 GL = 3
Tabla 7: Prueba T e IC de dos muestras: Laboratorio3, Laboratorio1
T de dos muestras para Laboratorio 3 vs. Laboratorio 1
Diferencia = mu (Laboaratorio 3) - mu (Laboratorio 1)

Estimado de la diferencia: -0.460
IC de 95% para la diferencia: (-1,765; 0,845)
Prueba T de diferencia = 0 (vs. no =): Valor T = -1,52 Valor P= 0,269 GL =2
Tabla 8: Prueba e IC para dos varianzas: Laboratorio 2, Laboratorio 3
Intervalos de confianza de 95% IC para IC para Distribución relación de relación de de los datos Desv.Est. varianza
Normal (0,106; 4,152) (0,011; 17,243)
Continuo ( *, *) ( *, *)
Pruebas Estadística
Método GL1 GL2 de prueba Valor P
Tabla 9: Prueba e IC para dos varianzas: Laboratorio 3, Laboratorio 1
Intervalos de confianza de 95% IC para IC para Distribución relación de relación de de los datos Desv.Est. varianza
Normal (0,364; 14,214) (0,133; 202,049)
Continuo ( *, *) ( *, *)
Pruebas Estadística
Método GL1 GL2 de prueba Valor P
Validación de método para contenido estomacal en osteíctios en el Perú
Para los datos del Índice de Equidad de Pielou reportado por los tres laboratorios
Para los datos del Índice de Equidad, en la Figura5sepresentalaPruebadeNormalidad, para los datos de los tres laboratorios. Los valores reportados por los laboratorios muestran un P-valor mayor a 0,05 lo cual indicaunadistribuciónnormalylaprueba de T-Student para los resultados Laboratorio2Laboratorio 1(Tabla 10) y Laboratorio 3 - Laboratorio 1 (Tabla 11), generan valores
p-valor mayor a 0,05; por tanto, a un 95% de nivel de confianza no hay diferencia significativa entre los tres laboratorios. Mientras que, para demostrar la igualdad de varianza se usó la prueba F obteniendo un Pvalor mayor al 0,05 por tanto a un 95% de nivel de confianza las varianzas son iguales (Tabla 12 y 13) y en la Figura 6 se muestra la comparación de las Desviación Estándar entreel Laboratorio 2 yLaboratorio 1 y,para el Laboratorio 1 y Laboratorio 3.
Figura 5: Prueba de Normalidad para Laboratorio 1 (A), 2 (B) y 3 (C)

Tabla 10: Prueba T e IC de dos muestras: Laboratorio 2, Laboratorio 1
T de dos muestras para Laboratorio 2 vs. Laboratorio 1
Diferencia = mu (Laboratorio 2) - mu (Laboratorio 1)
Estimado de la diferencia: 0,127
IC de 95% para la diferencia: (-0,204; 0,457)
Prueba T de diferencia = 0 (vs. no =): Valor T = 1,22 Valor P= 0,310 GL = 3
Tabla 11: Prueba T e IC de dos muestras: Laboratorio 3, Laboratorio 1
T de dos muestras para Laboratorio 3 vs. Laboratorio 1
la
media
Diferencia = mu (Laboratorio 3) - mu (Laboratorio 1)
Estimado de la diferencia: 0,013
IC de 95% para la diferencia: (-0,328; 0,355)
Prueba T de diferencia = 0 (vs. no =): Valor T = 0,12 Valor P = 0,909 GL= 3
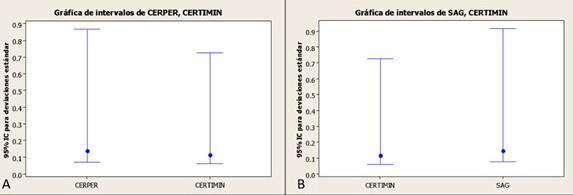
Tabla 12: Prueba e IC para dos varianzas: Laboratorio 2, Laboratorio 1
Intervalos de confianza de 95% IC para IC para Distribución relación de relación de de los datos Desv.Est. varianza
Normal (0,192; 7,471) (0,037; 55,812)
Continuo ( *, *) ( *, *)
Pruebas Estadística
Método GL1 GL2 de prueba Valor P
Tabla 13: Prueba e IC para dos: Laboratorio 3, Laboratorio 1
Intervalos de confianza de 95%
Intervalos de confianza de 95% IC para IC para Distribución relación de relación de de los datos Desv.Est. varianza
(0,202; 7,891) (0,041; 62,263)
Continuo ( *, *) ( *, *)
Pruebas Estadística Método GL1 GL2 de prueba Valor P
Validación de método para contenido estomacal en osteíctios en el Perú
Precisión
La precisión se estableció en términos de repetibilidad y reproducibilidad. El gradode precisión se expresa habitualmente en términos de imprecisión y se calcula como desviación estándar de los resultados.
Repetibilidad
Es la precisión bajo las condiciones de repetibilidad, es decir, condiciones dondelos resultados de análisis independientes se obtienen con el mismo método en ítems de análisis idénticos en el mismo laboratorio por el mismo operador utilizando el mismo equipamiento dentro de intervalos cortos de tiempo.
Reproducibilidad
Es la precisión bajo las condiciones de reproducibilidad,esdecir,condicionesdonde los resultados de los análisis se obtienencon el mismo método en ítem idénticos de análisis en condiciones diferentes ya sea de laboratorio, diferentes operadores, usando
o verificado por el laboratorio, se realice la determinación de las diferentes fuentes o componentes de la incertidumbre de la medición presentes: muestreo, efectos de la muestra (tipo de matriz, almacenamiento, etc.); sesgos instrumentales, las debidas a las características de los equipos utilizados para realizar las medidas (deriva, resolución, magnitudes de influencia); pureza de reactivos (materiales de referencia, preparación de estándares); analista, las debidas ala seriede mediciones (variaciones en observaciones repetidas bajo condiciones aparentemente iguales); condicionesde medición, las debidas al certificadode calibración, en él se establecen las correcciones y las incertidumbres asociadas a ellas, para un valor de k determinado, en las condiciones de calibración. Ejemplo: material volumétrico, etc. y condiciones de medición (temperatura, humedad, etc.).
La Incertidumbre expandida es representada por la siguiente fórmula : U = k.
u (Incertidumbre Combinada). Según la SNA-acr-09D (Directriz para la Estimación y Expresión de la Incertidumbre de la Medición) queda fuera de su alcance los métodos semi – cuantitativos (INDECOPISNA, 2014).
4. Conclusiones
Dónde U (Incertidumbre Expandida); K (Factor de Cobertura α = 0,05, k=2 y distintos equipos, entre otros. Para determinar la reproducibilidad interlaboratorios para fines de validación de un método, deben participar diferentes laboratorios, se debe tener en consideración que estos utilicen el mismo método y misma muestra, en un intervalo de tiempo preferentemente establecido, se determinade este modo la desviación estándar de los resultados obtenidos por los diferentes laboratorios.
Incertidumbre
La incertidumbre es factible a partir de los ensayos de aptitud y del programa de control interno de cada laboratorio. En los ensayos de aptitud es común que al laboratorio le reporten un valor de índice de desviación, o una puntuación del índice de varianza en ambos casos le proporcionan un valor del sesgo respecto al valor de consenso o alvalor considerado como verdadero.
La incertidumbre de una medición es el parámetro asociado al resultado,es decir, caracteriza la dispersión de los valores que razonablemente pueden ser atribuidos al mesurando. En este sentido,es importante que, para un método validado
Enbasealosresultadosobtenidosseconcluye que, determinar la veracidad se realiza mediante el análisis de interlaboratorio; mientras que, los índices de biodiversidad (Riqueza específica (d), Biodiversidad de Margalef (DMg), Shannon y Wiener (H’)y Equidad de Pielou (J’) se obtienen del análisis de la fase cuantitativa que se utiliza parahallarlaamplituddedieta;y, determinar la precisión se determina mediante las condiciones de repetibilidad (ISO 5725-1, 3.14) y condiciones de reproducibilidad (ISO 5725-1, 3.18).
5. Literatura citada
Krebs, CJ. 1989. Ecological Methodology. Harper and Row. New York, USA. 550 p.
Canto-Maza, WG.; Vega-Cendejas, ME.
2008. Hábitos alimenticios del pez Lagodon rhomboides (Perciformes: Sparidae) en la laguna costera de Chelem, Yucatán, México. Revista de Biología Tropical 56 (4): 1837-1846.
Hyslop, EJ. 1980. Stomach contents analysis a review of methods and their application. Journal of sh biology 17(4): 411-429
INDECOPI - SNA-acr-09D. 2014. Directriz para la Estimación y Expresión de la Incertidumbre de la Medición, Versión 02. Lima, Perú.
Nava, H. & López, M. 2008.Guía para la validación y la verificación de los procedimientos de examen cuantitativos empleados por el laboratorio clínico. Disponible en: http://consultaema. mx:75/pqtinformativo/GENERAL/ Cli nicos/ Carpeta _2_Crit erios_ evaluacion/CLINICOS_ValidacionVerificacion.pdf
Ramírez-Herrejón, JP.; Castañeda-Sam, LS.; Moncayo-Estrada, R.; Caraveo-Patiño, J.; Balart, EF. 2013. Trophic ecology of the exotic Lerma livebearer Poeciliopsis infans (Cyprinodontiformes: Poeciliidae) in the Lago de Pátzcuaro, Central Mexico. Revista de Biología Tropical 61(3): 1289-1300.
Torres-Rojas, YE. 2011. Nicho trófico de pelágicos mayores capturados en la boca del Golfo de California. Tesis doctoral, Centro Interdisciplinario de Ciencias Marinas-Instituto Politécnico Nacional, La Paz Baja California Sur, México, 185 p.
Trujillo, W.; Rodríguez, C.; Reyes, O. 2016. Análisis del contenido estomacaly la ecologíatrófica dela Triportheus auritus (Jolombo). Revista electrónica de Veterinaria 17(11): 1-9.
ISSN (Versión electrónica)


Website:
ORIGINAL –RESEARCHARTICLE
Metodología para validación de determinación de sólidos totales suspendidos en agua potable
Methodology for validation of determination of total solids suspended in drinking water

Lucy Torres1; Diana Campos1; Carmen Quispe1; Juliana Legua1; César Córdova1
1 Investigadores independientes, Lima, Perú. Email:
*Autor de correspondencia: Email: ORCID:
Recibido: 31/01/2016; Aceptado: 30/06/2017; Publicado: 30/06/2023
Resumen
Con objetivo de mantener la competitividad, las empresas buscan satisfacer las necesidades de los clientes mediante el cumplimiento de los requerimientos del mercado. Para ello, se realizó la validación basándonos en el método normalizado Estándar Method 2540D. También, se realizaron pruebas estadísticas para validar el método mencionado y proponer una metodología adecuada para la determinación de sólidos suspendidos totales en agua potable reduciendo el tiempo y costos. En conclusión, los resultados de este estudio son precisos y la validación de la determinación de sólidos totales suspendidos en agua potable, cumple con la evaluación de parámetros de validación.
Palabras clave: sólidos totales; agua; 2540D; agua potable.
Abstract
In order to maintain competitiveness, companies seek to satisfy the needs of customers by meeting market requirements. For this, validation was performed based on the standard method Standard Method 2540D. Also, statistical tests were carried out to validate the aforementioned method and to propose an adequate methodology for the determination of total suspended solids in drinking water, reducing time and costs. In conclusion, the results of this study are accurate and the validation of the determination of total solids suspended in drinking water complies with the evaluation of validation parameters.
Keywords: total solids; Water; 2540D; drinking water.

Forma de citar el artículo: Torres, L., Campos, D., Quispe, C., Legua, J., & Córdova, C. (2023). Metodología para validación de determinación de sólidos totales suspendidos en agua potable. XXXX 1(1): 12 - 15 (2023).
DOI:
DOI:
© Los autores. Este artículo es publicado por la revista xxxxxxx de la Universidad Nacional Agraria La Molina. Este es un artículo de acceso abierto, distribuido bajo los términos de la Licencia Creative Commons Atribución 4.0 Internacional.(https://creativecommons.org/licenses/by/4.0/) que permite Compartir (copiar y redistribuir el material en cualquier medio o formato), Adaptar (remezclar, transformar y construir a partir del material) para cualquier propósito, incluso comercialmentte.
1. Introducción
Elaguaesconsideradaunsolventeuniversal; segúnTeijónyGarrido(2006),estapropiedad está relacionada con su estructura molecular, que le permite disolver con facilidad compuestos iónicos y compuestos polares y solubilizar otros de carácter lipídico. Esta característica distintiva le permite tener diversas aplicaciones; Además de ser un elemento esencial para el mantenimiento de la vida en el planeta. El agua potable, es aquella que se puede ingerir por los seres humanos y satisfacer sus necesidades. Por su composición química no presenta contaminantes objetables.
Los avances de la tecnología y el mal manejo de los residuos sólidos por parte del ser humano han generado la contaminación del recursohídrico, causando que gran parte de este se encuentre contaminado. Vargas et al. (2009) mencionan que el ambiente se ha afectado en las últimas décadas a causa del inadecuado manejo y disposición de desechos generados por las ciudades y centros industriales. Por ello, se han creado reglamentos y legislaciones que estipulan parámetros químicos, físicos o microbiológicos que permiten catalogarel grado de contaminación en distintas matrices, del suelo, aire y agua.
La densidad, se trata de una propiedad que indica la cantidad de masa que contiene un determinado volumen y en el caso de las aguas potables es un parámetro importante, ya que la cantidad de sólidos disueltos y no disueltos la hacen variar (Rodríguezet al., 2009). También debe considerarseque, según Heyward (2006), la densidad depende de la temperatura y la presión; con una temperatura de 20 °C la densidad es de 0,99820 g/mL, mientras que a 27 °C es de 0,99650 g/mL, por lo que la temperatura de trabajo también tiene incidencia en la densidad y debe considerarse. Es importante determinar la densidad en las aguas ya que, según Seoánez (2001), es un indicador de la cantidad de materiales que llegan a un cuerpo receptor (contaminación mecánica).
Los sólidos, se refieren a la materia en suspensión o disuelto en agua o aguas residuales. Los sólidos pueden afectar agua o la calidad del efluente de manera adversa en un número de maneras. Aguas con alto contenido de sólidos disueltos
generalmente pueden inducir una reacción fisiológica desfavorable en el consumidor. Por esas razones, un límite de sólidos disueltos es 500 mg/L para aguas potables. Las aguas altamente mineralizadas también son adecuadas para muchas aplicaciones industriales. Mientras que, el agua con alto contenidodesólidosensuspensiónpuedeser estéticamente insatisfactorio para fines tales como bañarse.
Lacompetitividadesun factorprimordial que prevalece en el mercado actual de cualquier tipo de producto o servicio, donde sesolicitaresultadosinmediatosydecalidad. Por este motivo el objetivo del presente estudio fue mantener la competitividad de las empresas mediante el cumplimiento de los requerimientos del mercado a través de validar un método normalizado como el Estándar Method 2540 D.
2. Materiales y métodos
La determinación de los sólidos totales, se determinó, a través de una muestra, bien mezclada, que se pasa a través de un filtro de fibrade vidrio estándar.Para ello, primero se pesa el filtro y el residuo en el filtro; el aumento de peso del filtro representa los sólidos totales en suspensión; luego se lleva auntiempodesecado en estufapor unahora, lacual valida el método paraun tiempode45 min en estufa. Para obtener unaestimación del total de sólidos en suspensiónes calcular la diferencia entre el totaldesólidosdisueltos y sólidos totales.
El estudio de validación, se realizó bajo loscriteriosdescritosenlaguíadevalidación de Nº 0008-2003/INDECOPI-CRT. Para ello, se consideraron tres niveles de rango de trabajo, para la determinación de sólidos totales en suspensión en agua potable (30 ppm, 100 ppm, 500 ppm).
Los datos experimentales son evaluados en veracidad y precisión (RSD de Horwitz), mediante el material de referencia, que consistió en soluciones de tierra diatomea.
3. Resultados y discusión
En la Tabla 1 se detallan los resultados de evaluación obtenidos en soluciónde tierra diatomea de 100 ppm con un tiempo de secado de 1 hora y 45 min (Tiempo de validación). Los resultados
Metodología para validación de determinación de sólidos totales suspendidos en agua potable
de las repeticiones son veraces al 95 % de confianza, con un p-Value 0,489 ≥ 0,05.Por otro lado, IDEAM (2017) indica que la determinación de sólidos disueltos totales debe ser secados a 180°C en agua, por el
mg/L respectivamente. Siendo el límite de cuantificación de método 15 mg/L.
Tabla 2: Precisión al utilizar el RSD de Horwitz método gravimétrico SM 2540 C. Mientras que, método normalizado Estándar Method 2540 es entre 103°C – 105 °C.
En la Tabla 2, se muestra que los resultados son precisos. Mientras que, los parámetros de límite de detección y cuantificación se determinaron mediante un blanco fortificado, analizando siete réplicas por tres analistas. El LD y LC máximo obtenido
4,7 mg/L
En la Tabla 3 se evalúa los resultados de las soluciones de tierra diatomea para el parámetro de especificidad. La *Prueba Normalidad: p-Value 0,907 ≥ 0,05; *Prueba t: p-Value 0,367 ≥ 0,05. El método es específico al 95% de confianza. Para el parámetro de robustez, resultados deTSS (mg/L) en un tiempo de secado de 60 min. Vs secado de 45 min. Evaluación: p-Value 0,476 ≥ 0,05. Prueba de varianzas: Evaluación p-Value: 0,644 ≥0,05.
4. Conclusión
Basándonos en los resultados obtenidos se concluye que los resultados son precisos y que, la validación en determinación de sólidos totales suspendidos en agua potable,
Tabla 1:Validación de la concentración de sólidos totales Tabla 3: soluciones de tierra diatomeaTorres, L., Campos, D., Quispe, C., Legua, J., & Córdova, C.
XXXXX 1(1): 12 - 15 (2023)
cumple con la evaluación de parámetros de validación.
5. Literatura citada Heyward,V.2001.Evaluaciónyprescripción del ejercicio. 2 ed. Barcelona: Paidotribo
IDEAM. 2017. Instructivo de ensayo. Determinación sólidos totales secados a 103° - 105°C. SM 2540 B. Disponible en: http://sgi.ideam.gov. co/ts/412030/35488871/M-S-LC-I0 17++INSTRUCTIVO+DE+ENSAY O+DETERMINACI%C3%93N+S% C3%93LIDOS+TOTALES+SECA DOS.pdf/cf17614e-b3af-48f3-a5a41c76060?version=1.0
Resolución Comisión de Reglamentos Técnicos y Comerciales Nº 00082003/INDECOPI-CRT. (Lima 16 de enero de 2003).
Rodríguez, J.; Vargas, E.; Gómez, M. 2009. Procesos Industriales: Manual de Laboratorio para el análisis químico y control de calidad. Heredia, C.R.: Universidad Nacional.
Seoánez, M. 2001. Tratado de gestión del medio ambiente. Madrid: MundiPrensa.
Teijón, J.; Garrido,A. 2006. Fundamentos de bioquímica estructural. 2 ed. Madrid: Editorial Tébar.
Vargas, E.; Gómez, M.; Rodríguez, J. 2009. Procesos industriales: manual de laboratorio para el análisis químico y control de calidad. Heredia. EUNA.
154 p.
ISSN (Versión electrónica)
Website: ARTÍCULO ORIGINAL –RESEARCHARTICLE
Procedimiento para la calificación de personal en laboratorios de ensayo
Procedure for the qualification of personnel in test laboratories
LizetArango1; Vanessa Farfán1; EvelynAlcalá2; Edson Sanchez3; Victor Ponce3; Francis Mejia3

1 Titulado en Farmacia y Bioquímica, Lima, Perú.
2 Titulado Ingeniería Agroindustrial, Lima, Perú.
3Titulado en Farmacia y Bioquímica, Lima, Perú.
*Autor de correspondencia: Email: . ORCID:
Recibido: 31/01/2016; Aceptado: 30/06/2017; Publicado: 30/06/2023
Resumen
El presente trabajo de investigación tuvo como objetivo evaluar los resultados obtenidos de dosanalistas(AnalistapatrónconAnalista1),atravésdeldosajedeparacetamolentabletasde 500mg. Debido a que, una de las actividades principales dentro de un laboratorio de ensayo, es la calificación de los analistas, lo cual permite garantizar que los resultados obtenidos en distintos tipos de análisis sean válidos, con esta implementación se busca obtener resultados lo más cercanos posibles entre analistas y asegurar la confiabilidad de los análisis. Esto es un requisito imprescindible para establecer un adecuado sistema de gestión de calidad de laboratorios siguiendo los lineamientos de la NTP ISO/IEC 17025:2006. Se concluye que, los métodos estadísticos utilizados para la evaluación de los analistas, emiten resultados confiables dentro de un sistema de gestión de calidad y, con la aplicación del Procedimientos Operativos Estandarizados de Saneamiento (POES), se logra cumplir con el sustento para la autorización de los analistas en determinadas pruebas analíticas.
Palabras clave: acreditación; NTP-ISO/IEC 17025:2006; productos; calidad.
Abstract
The objective of this research work was to evaluate the results obtained from two analysts (Standard Analyst with Analyst 1), by dosing paracetamol in 500mg tablets. Because one of the main activities within a testing laboratory is the qualification of analysts, which allows us to guarantee that the results obtained in different types of analysis are valid, with this implementation we seek to obtain results that are as close as possible between analysts and ensure the reliability of the analyzes. This is an essential requirement to establish an adequate laboratoryquality management system following the guidelines of the NTPISO / IEC 17025: 2006. It is concluded that the statistical methods used for the evaluation of the analysts, emit reliable results within a quality management system and, with the application of the Standardized Sanitation Operating Procedures (POES), it is possible to comply with the support for the authorization of analysts in certain analytical tests.


Keyword: accreditation; NTP-ISO / IEC 17025: 2006; products; quality.

Forma de citar el artículo: Arango, L., Farfan, V., Alcalá, E., Sanchez, E., Ponce, V., & Mejia, F. (2023). Procedimiento para la calificación de personal en laboratorios de ensayo. XXX 1(1): 16 - 20 (2023). DOI:
DOI:
© Los autores. Este artículo es publicado por la revista xxxxxxx de la Universidad Nacional Agraria La Molina. Este es un artículo de acceso abierto, distribuido bajo los términos de la Licencia Creative Commons Atribución 4.0 Internacional.(https://creativecommons.org/licenses/by/4.0/) que permite Compartir (copiar y redistribuir el material en cualquier medio o formato), Adaptar (remezclar, transformar y construir a partir del material) para cualquier propósito, incluso comercialmentte.
1. Introducción
El mundo está globalizado, con ello surge la necesidad de ser competitivos con los productos y servicios que se comercializan para cumplir con la calidad. Además, la demanda de los mercados europeos o asiáticos y las alarmas alimenticias ocurridas en las últimas décadas, cada vez más exigentes, han sido elementos determinantes para que las empresas asimilen la necesidad de asumir el reto de asegurar la calidad, mejorar continuamente, aumentar la productividad, reducir costos y, en suma, incrementar la satisfacción del cliente (Burga y Moreno, 2017).
La calidad, es cuando un producto o servicio satisface los requerimientos o expectativas de un cliente. Para determinar la calidad, se requiere que se definan los requerimientos del cliente y que estos requerimientos se vayan revisando, actualizando o definiendo en el tiempo, conforme van variando (Aronés y Concepción, 2008). La calidad se puede asegurar y mejorar continuamente (Burga y Moreno, 2017), a través de actividades que implican inspección y control en los ensayos de laboratorio. La calidad en laboratorios, es fundamental en el trabajo de análisis químicos, físicos, microbiológicos, sensoriales, entre otros. La NTP ISO/IEC 17025: 2005, indica que muchos factores determinan si los ensayos y calibraciones realizadas por un laboratorio son correctos y confiables (INDECOPI, 2006). Los resultados de cualquier determinación analítica deben ser realizados bajo la “supervisión” de un sistema de gestión. Actualmente, las normas de aplicación de la calidad en laboratorios se agrupan en la ISO/ IEC 17025:2005, norma que el Perú adoptó en el año 2006, evaluados por el servicio nacional de acreditación del INDECOPI, con la finalidad de asegurar la competencia técnica de dicha entidad de evaluación de laconformidadparaelrubrodeservicios que opera. Según Burga y Moreno (2017) actualmente existen 69 laboratorios de ensayo acreditados por la dirección de acreditación del INACAL bajo la NTP ISO/ IEC 17025:2006.
En el Perú, las perspectivas son que los laboratorios de ensayo sean organismos de evaluación de la conformidad y que cuenten con la competencia técnica adecuada para
generar resultados altamente confiables.Por ello, El objetivo del presente estudio fue evaluar el desempeño de un analista en entrenamiento, en relación a un analista de referencia,mediante el análisis estadístico de los datos generados en la determinación de dosajeenmuestrasdeparacetamolentabletas de 500mg, aplicando el procedimiento para la autorización de analistas comprendido dentro del Sistema de Gestión de la Calidad en un laboratorio de ensayo.
2. Materiales y métodos
Las muestras se sometieron por cromatografía líquida de alta performance (HPLC). La primera fase, es la Fase móvil: Metanol y agua (1:3). La solución estándar estaba conformada por 0,01 mg/mL de ER Acetaminofén (paracetamol), en Fase móvil. La solución madre de la muestra es nominalmente 0,5mg/mL de acetaminofén (paracetamol), cuya preparación se detalla a continuación:
Primero, se debe pesar y moler hasta reducir a polvo fino, no menor de 20 tabletas. Luego transferir el equivalente a 100 mg de acetaminofén (paracetamol), a partir de una porción de tabletas reducidas a polvo, a un matraz volumétrico de 200 mL, agregar 100 mL de Fase móvil, agitar mecánicamente durante 10 minutos, someter a ultrasonido durante 5 minutos y diluir con Fase móvil a volumen.
La solución muestra: Nominalmente 0,01 mg/mL de acetaminofén (paracetamol) en Fase móvil, se preparó a partir de Solución madre de la muestra. Se pasó una porción de esta solución a través de un filtro transparente con un tamaño de poro de 0,5 μm o menor, desechando los primeros 10 mL del filtrado.
Sistema cromatográfico presentó una columna de 3,9 mm x 30 cm; relleno L1. La velocidad de flujo fue 1,5 ml/min. y el volumen de inyección fue de 10 Μl. La aptitud del sistema fue: muestra (Solución estándar), requisitos de aptitud, factor de asimetría (no más de 2) y desviaciónestándar relativa (no más de 2,0%).
3. Resultados y discusión
En la Tabla 1, se muestra los resultados obtenidos al aplicar el procedimiento.
Procedimiento para la calificación de personal en laboratorios de ensayo
La Prueba de normalidad ANDERSON
–DARLING, se obtiene con la Fórmula 1, donde: (Varianza muestral), (Media muestral) y (Valores individuales de la muestra) . El Planteamiento de hipótesis: H0 (Los datos de la muestra poseen distribución normal) e H1 (Los datos de la muestra poseen distribución normal). Si: p- value > 0,05 (se acepta Hipótesis Nula) y si p- value < 0,05 (se rechaza la HipótesisAlterna).


Fórmula 1

Tabla 1: Resultados del Analista patrón y prueba
En la Figura 1 se muestra la Prueba de normalidad de los datos de calificación de analistas y en la Tabla 2 se presenta la Prueba de Z-SCORE, se aplicó la Fórmula 2, siendo los criterios estadísticos señaladosen la Figura 2. Los resultados de la prueba de datos atípicos, indican que ningún conjunto de datos posee datos atípicos. En la prueba
= (S2 / S2 ). Donde y se
1 2 disponen en la ecuación de manera que F > 1. El número de grados de libertad del numerador y el denominador será n1-1 yn21; respectivamente. Si la hipótesis es verdadera entonces la relación de varianzas debería ser próxima a 1.
Arango, L., Farfan, V.,Alcalá, E., Sanchez, E., Ponce, V., & Mejia, F. XXXX 1(1): 16 - 20 (2023)
Prueba e IC para dos varianzas: Analista patrón,Analista 1
Método
Hipótesis nula
Sigma (Analista Patron)/Sigma (Analista 1) = 1
Hipótesis alterna
Sigma (Analista Patron)/Sigma (Analista 1) not = 1
Nivel de significancia Alfa = 0,05
Estadísticas
Variable N Desv.Est. Varianza Analista patrón 10 0,909 0,826 Analista 1 10 1,260 1,589

Relación de deviaciones estándar = 0,721
Relación de varianzas = 0,520
Intervalos de confianza de 95%
IC para IC para Distribución relación de relación de de los datos Desv.Est. varianza
Normal (0,359; 1,447) (0,129; 2,094)
Continuo (0,333; 1,864) (0,111; 3,475)
Pruebas
Método GL1 GL2 de prueba Valor P
Prueba F 9 9 0,52 0,344
En la Figura 3 se muestra la gráfica de caja del Analista Patrón y Analista 1. El P-value = 0,344 <0,05; motivo por el cual se acepta la hipótesis nula y se afirma que no existe diferencia significativa entre las varianzas de los analistas.
Figura 3: Gráfica de caja del Analista Patrón yAnalista 1
La Prueba T-STUDENT de dos muestras se realizó mediante la Fórmula 3, donde S es igual a la Fórmula 4. Donde t tiene n1+n2 -1 grados de libertad. Para que la hipótesis nula sea rechazada se debe cumplir que: ttabla < t experimental.
Fórmula 3
Fórmula 4
Prueba T e IC de dos muestras: Analista Patrón,Analista 1
T de dos muestras para ANALISTA PATRON
Diferencia = mu (Analista Patron) - mu (Analista 1)
Estimado de la diferencia: -0,611
IC de 95% para la diferencia: (-1,644; 0,421)
Prueba T de diferencia = 0 (vs, no =): Valor
T = -1,24 Valor P = 0,229 GL= 18
Ambosutilizan Desv.Est. agrupada =1,0989
Procedimiento para la calificación de personal en laboratorios de ensayo
Interpretación: El P-Value= 0,229 > 0,05; es decir no existe diferencia significativa entre las medias de los grupos.
4. Conclusiones
Delos resultadosobtenidos se concluyeque, los métodos estadísticos utilizados para la evaluación de los analistas, emiten resultadosconfiablesdentrodeunsistema de gestión de calidad y con la aplicacióndel POES, se logra cumplir con el sustento para la autorización de los analistas en determinadas pruebas analíticas.
5. Literatura citada
Aronés, C. y Concepción, J. 2008. Diseño y desarrollo de un Sistema de Gestión de Calidad en base a la norma NTPISO/IEC 17025:2006 para el laboratorio Certipez EIRL. Tesis Ing. Lima, Perú, UNALM. 199 p. Burga, M.; Moreno, d. 2017. Diseño de un Sistema de Gestión en base a la NTPISO/IEC 17025:2006 para el Laboratorio de Industrias Lácteas Peruanas S.A. Trabajo académico para optar el título de Ingeniero en Industrias Alimentarias, Universidad Nacional Agraria La Molina, Lima, Perú. 291 p.
INDECOPI (Instituto Nacional de Defensa de la Competencia y la Protección de la Propiedad Intelectual, Perú). 2006. Requisitos generales para la competencia de los laboratorios de ensayo y calibración. NTP-ISO/IEC 17025:2006. 2 ed. 49 p.
ISSN (Versión electrónica) Website: ARTÍCULO ORIGINAL –RESEARCHARTICLE

Estimación de la incertidumbre de resultados de ensayos
Estimation of uncertainty of test results of benthic macroinvertebrates

1Titulado en Física, Universidad Nacional FedericoVillarreal, Lima, Perú.
2 Universidad Nacional Mayor de San Marcos, Lima, Perú.
3 Universidad Nacional de Piura Lima, Perú.
4 Universidad Nacional del Callao, Perú.
*Autor de correspondencia: Email: ORCID:
Recibido: 31/01/2016; Aceptado: 30/06/2017; Publicado: 30/06/2023
Resumen
El objetivo del presente estudio fue enfocarse en el desarrollo de un procedimiento, para la determinación de la incertidumbre para laboratorios de ensayo que utilicen la técnica de la DeterminacióndeMacroinvertebradosbentónicos, siguiendo loscriterios yrecomendaciones de las normas ISO/IEC 17025:2005. Se describen los factores que influyen en éste análisis, dentrodeloscuales,setienenlosequiposeinstrumentosdemediciónutilizados;ademásdela destreza del ejecutante del ensayo, bajo conceptos estadísticos como son la repetibilidad (σr) y reproducibilidad (σR) del método.Además se presenta una recopilación bibliográfica de las especificaciones de calidad que debe cumplir mediante el análisis de las Normas 17025. En conclusión, los componentes que influyen en el análisis de macroinvertebrados bentónicos son la incertidumbre estándar relativa de la distribución natural de los microorganismos. Palabras clave: Estimación; incertidumbre; factores; procedimiento; ensayo.
Abstract
The objective of the present study was to focus on the development of a procedure for determining uncertainty for testing laboratories using the Benthic Macroinvertebrate Determination technique, following the criteria and recommendations of the ISO / IEC 17025: 2005 standards. The factors that influence this analysis are described, among which are the equipment and measuring instruments used; in addition to the skill of the test performer, under statistical concepts such as the repeatability (σr) and reproducibility (σR) of the method. In addition, a bibliographic compilation of the quality specifications that must be met through the analysis of the 17025 Standards is presented. In conclusion, the components that influence the analysis of benthic macroinvertebrates are the relative standard uncertainty of the natural distribution of the microorganisms


Keywords: estimation; uncertainty; factors; procedure; test.
Forma de citar el artículo:Alarcón, D., Guardamino, G., Huanca,A., Oros, K., & Rivera, C. (2023). Estimación de la incertidumbre de resultados de ensayos. XXXX 1(1): 21 - 28 (2023). DOI:
DOI:
© Los autores. Este artículo es publicado por la revista xxxxxxx de la Universidad Nacional Agraria La Molina. Este es un artículo de acceso abierto, distribuido bajo los términos de la Licencia Creative Commons Atribución 4.0 Internacional.(https://creativecommons.org/licenses/by/4.0/) que permite Compartir (copiar y redistribuir el material en cualquier medio o formato), Adaptar (remezclar, transformar y construir a partir del material) para cualquier propósito, incluso comercialmentte.
Estimación de la incertidumbre de resultados de ensayos.
1. Introducción
En la actualidad el empleo de comunidades de macroinvertebrados bentónicos como indicadores de calidad de agua de cursos loticos viene incrementándose en los últimos años, en lo que respecta a la protección de los ambientes acuáticos. Los invertebrados pueden distribuirse en distintos nivelesde condiciones ambientales, así como ser muy susceptibles a la contaminación,motivo por lo que son recomendados en el establecimiento de sistemas de vigilancia y control de los ecosistemas hídricos (Leslie et al. 1999; Ogbeibu & Oribhabor, 2002).
La aplicación de la incertidumbre de las mediciones en los métodos de ensayos, es una forma de incrementar la información sobre un resultado analítico, de formacomún se expresa como un valor absoluto; sin embargo, los analistas de los laboratoriosde ensayo, conocen que todo resultado tieneun componente de variabilidad, por lo que es más conveniente expresar un resultado como un intervalo de valores probables (JCGM 200, 2008; ISO/IEC, 2009).
Estaformadeexpresión, se justificabajo un enfoqueestadístico, no seutilizade forma regular para expresar los resultados de un ensayo, debido entre otras razones,a la cómoda forma tradicional de expresar un resultado con un valor único, sin tener que realizar interpretación de un intervalode resultados, aunque este aporte mayor información al usuario (Betancourt, 2013).
En la actualidad, existen varias normas internacionales que buscan armonizar los resultados y abordan la estimaciónde la incertidumbre de los ensayos por diferentes procedimientos con resultados
laboratorios que operan bajo la norma ISO/ IEC 17025:2005.
2. Materiales y métodos
El presente estudio consta de seis etapas. Etapa 1 (definición del mensurando), en ella realiza la descripción de lo que se medirá, incluyendo la relación entre el mensurando y los factores de los cuales depende.Además de plantear la ecuación matemática según corresponda. Etapa 2 (identificación delas fuentes de incertidumbre), consiste en documentar las fuentes de incertidumbre del proceso analítico, como: definición del mensurando, efectos atribuibles a los instrumentos de medición incluyendo la calibración, número de cifras significativas; efectos atribuibles a los patrones de medición, efectos atribuibles al métodode ensayo y precisión de las mediciones.Etapa 3 (cuantificación de las fuentes de incertidumbres), se utilizan dos formas básicas para estimar los componentes individualesdelas fuentesdeincertidumbre: Métodos de evaluación de tipo A: Esta medición se realiza experimentalmente en un método bien caracterizado y bajo condiciones controladas (Fórmula 1).
Fórmula 1 u(xi ) = s(q)
Donde n es el número de mediciones repetidas y s(q) representa la desviación estándar experimental de la media (Fórmula 2):
comparables, siendo las estimaciones realizadas en laboratorio de forma individual o colaborativos entre varios laboratorios
Fórmula 2
Endonde, q
s(qk ) = es el resultado dela k-ésima (Eurolab, 2006). La incertidumbre del ensayosepuedeevaluarpordesglosedecada etapa o de manera global y el procedimiento a seguir estará en correspondencia con la necesidad que se tenga del conocimientodel ensayo y la complejidad del mismo (EURACHEM/CITA, 2000).
El objetivo del presente estudio fue estimar la incertidumbre de la composición faunística, riqueza de familias y calidad del agua con base en el índice biótico; a través de los requisitos básicos para los
medición y q es la media aritmética de los n resultados considerados, y n-1 es el número de grados de libertad para una evaluación de tipo A. También, se puede estimar incertidumbre en base a resultados o datos previos de la validación de un método de ensayo.
Métodos de evaluación de tipo B: Son aquellas fuentes que se obtienen de información externa al proceso de medición u obtenida por experiencia. Estas fuentes
pueden obtenerse del Certificado de calibración, manuales del instrumento de medición, especificaciones del instrumento, normas o literatura, valores de mediciones
anteriores, conocimiento sobre las características o el comportamiento del sistema de medición. Para el cálculo de evaluaciones de tipo B se utilizaron las siguientes distribuciones estadísticas: Distribución Normal: Se utiliza cuando se declare en los documentos o información externa,quelosdatossiguenunadistribución normal o se indique un nivel de confianza (Fórmula 3).
Fórmula 3
U = Es el valor de la Incertidumbre
expandida declarada en el Certificado.
k = Factor de cobertura
Distribución Rectangular: Se utiliza cuando no existe conocimiento específico acercadelosposiblesvaloresdeXi dentrodel intervalo, entonces es conservador suponer una distribución rectangular (Fórmula 4).
Donde u(a), u(b) y u(c), son respectivamente las incertidumbres estándar de los resultados parciales a, b y c.
Regla 2: El resultado “y” se obtiene por productos y/o cocientes de a, b y c En este caso hay que utilizar las incertidumbres estándar relativas Fórmula 7
Fórmula7 uc ( y) = y
Etapa 5 (Estimación de la incertidumbre expandida ¨u¨) Fórmula 8
Fórmula 8 U = k uc( y)
Se utiliza esta fórmula cuando las distribuciones resultantes siguen una distribución normal, bajo cualquiera de los siguientes criterios: La suma de variables aleatorias con distribuciones independientes es aproximadamente normal. El número
Fórmula 4 u(xi) = a de observaciones es > 30. Si se demuestra estadísticamente que los datos siguen una distribución normal. Si la mayoría de las distribuciones delas incertidumbres estándar siguen una distribución normal. Entonces
Donde a/2 es el semiancho del intervalo de a= ± a Fórmula 5. semultiplica laincertidumbrecombinadapor un nivel de confianza, llamado factor de cobertura (k).
a
Fórmula 5 u(xi ) = Etapa 6 (Reporte para la estimación de laincertidumbredeensayos).Losreportes se realizaran progresivamente en un formato que puede ser denominado Reporte de Donde a/2, es el semiancho del intervalo de a = ± a.
combinada se obtiene mediante Fórmula 6.
Etapa4(Estimacióndelaincertidumbre).
Estimación de la incertidumbre de resultados de ensayos.
Estimación de la Incertidumbre. Se debe adjuntar un informe detallado del procesode estimación de incertidumbre el cual debeconsignar en todas sus hojas el número de reporte registrado en el respectivo formato, los mismos que deben ser remitidos al equipo de gestión de la calidad y ala jefaturadelaboratorios de control de calidado sus equivalentes según el organigrama de la empresa. No se redondeará en las estimaciones parciales hasta el valor final de la estimación de la incertidumbre, que se expresaráconalomásdoscifras significativas.
Podrá excluirse de la estimación de la incertidumbre a aquella fuente identificada en el presupuesto de incertidumbre que no contribuya significativamente en el valor de incertidumbre, la misma que debe ser demostrada.Laincertidumbreen los reportes o informes de resultados se expresará de la siguiente manera: Incertidumbre estándar expandida Fórmula 9.
Fórmula 9 [Y ± U ] (unidades)
Donde U, es la incertidumbre expandida con un nivel de confianza del 95 por ciento.
Una vez concluida la estimación de la incertidumbre de un determinado mensurando, el grupo de trabajo para la estimación de la incertidumbre podrá evaluar la posibilidad de recalcular el valor de dicha incertidumbre si se ve afectada una de las fuentes de incertidumbre consideradas dentro del proceso de estimación. Como por ejemplo en los siguientes casos: Cuando el equipo y/o material utilizado sea prestado de otra institución y/o cuando se ha calibrado nuevamente el equipo o instrumento. Los casos especiales según consideración del grupo de trabajo para la estimación de Incertidumbre.
Dispersión de Poisson: Es el elemento dominante de la incertidumbre cada vez que el conteo observada es menor a aproximadamente 25. Cuando la diluciónes innecesario y la incertidumbre de la interpretación es pequeño. Distribución de Poisson incluso podría ser suficiente hasta aproximadamente 100 colonias por placa. En estas los casos los valores del intervalo de confianza inferior y superior se pueden obtener a partir de la distribución de probabilidad acumulativa generada a partir
se pueden leer para obtener el intervalo de confianza del 95%. Los límites de confianza son aproximados debido a que el verdadero valor de la media no es conocida yel número observado (z) de las colonias se utiliza como su estimación. Los límites obtenidos son ligeramente demasiado estrecho, debido a la incertidumbre de la media no está incluido (5) .
Elmétodoutilizadoparaladeterminación del macroinvertebrados bentónicos corresponde a un método normalizado del Standard Methods for the Examination of Water and Wastewater.
3. Resultados y discusión
En la Tabla 1 se presentan los resultados obtenidos de la estimación de la incertidumbre estandar relativa de la distribución natural de los microorganismos (Wz2); según la fórmula de varianza de la distribución de Poisson (Fórmula 11). Mientras que, en la Tabla 2 se muestra la estimacion estandar relativa del conteo de microorganismo (Wt2); según Fórmula 12.
Fórmula 11 Wz2 = 1/z
Donde: Z, es el número de la especie de 1 microorganismo en un ensayo.
Fórmula 12 Wt2= media ∑ (W 2)
Donde: W 2 , es la varianza de la lectura de los analistas entre la media de sus datos.
En la Tabla 3 se muestran la estimación de la incertidumbre estandar relativo debido de la Fórmula 10.
alos duplicados de los análisis (W la Fórmula 13: 2);según
Fórmula 10
En la fórmula, P es laprobabilidad acumulativa, μ es la media y x es el número de colonias
Fórmula 13 W 2= 2 x (D1-D2/D1+D2)2
Donde: (partículas). Inserción sucesivamente todos W 2 , es la varianza de los duplicados de los los valores de x desde 0 en adelante, y el trazado de los valores de la suma, da la
distribución de probabilidad acumulativa de la que el 2,5% y el 97,5% valores de x
Estimación de la incertidumbre de resultados de ensayos.
análisis.
D1, es el resultado del primer análisis. D2, es el resultado del segundo análisis.
Alarcón, D., Guardamino, G., Huanca,A., Oros, K., & Rivera, C.
En la Tabla 4 se presenta la estimación de la incertidumbre estandar reltiva
raíz cuadrada de la suma de los cuadrados de los componentes de incertidumbre, según
debido al efecto matriz (W 2); Se calcula el análisis que corresponda, de acuerdo a la restando a la incertidumbre relativa siguiente fórmula:
debido a los duplicados (W 2) el resto de la incertidumbres consideradas en cada Fórmula 15 W =
W 2 + W 2 + W 2 + análisis, según la Fórmula 14.
Fórmula 14 W 2 = W
– (W
+W
En la Tabla 5 se presenta la estimación de la incertidumbre estandar relativa
combinada (Wy2), se calcula sacando la
Estimación de la incertidumbre de resultados de ensayos.
W y, es la incertidumbre estándar combinada.
Alarcón, D., Guardamino, G., Huanca,A., Oros, K., & Rivera, C. XXXXX 1(1): 21 - 28 (2023)
Tabla 3: Estimación de la incertidumbre estandar relativo a los duplicados de los análisis
Estimación de la incertidumbre de resultados de ensayos.
Tabla 5: Incertidumbre estandar relativa combinada

En la Tabla 6 se presenta el intervalo de confianza al 95%; para la incertidumbre del resultado a través de un intervalo de confianza al 95%, se calculla a través de la Fórmula 16 y 17.
Fórmula 16 LS = Z/V x(1 + 2 Wy)
Fórmula17 LI=Z/Vx(1–2Wy2/1 +2Wy)
Donde: LS, es el límite superior LI, es el límite inferior Z, es el número de microorganismo V, es la porción del volumen de prueba Wy,eslaincertidumbreestándarcombinada.
Tabla 6: Intervalo de confianza al 95%
4. Conclusiones
En conclusión, los componentes queinfluyen en el análisis de macroinvertebrados bentónicos son la incertidumbre estándar relativa de la distribución natural de los microorganismos. La incertidumbre estándar relativa del conteo de microorganismos. La incertidumbre estándar relativa debido a los duplicados de los análisis y la incertidumbre estándar relativa debido al efecto matriz. La incertidumbe combinada es la que se utiliza paraladeterminacióndemacroinvertebrados bentónicos y se calcula para cada especie que se determina en un análisis.
5. Literatura citada
Betancourt, A. 2013. La incertidumbre asociada al resultado analítico en los laboratorios de ensayo de la rama agropecuaria. Revista Salud Animal 35(2) 73-78.
EURACHEM/CITAC. 2000. Guide, Quantifying Uncertainty inAnalytical Measurement, Second Edition, QUAM:2000.P1, 2000.
Eurolab. 2006. Guide to the Evaluation of Measurement Uncertainty for Quantitative Test Results, Technical Report No. 1/2006.
ISO/IEC. 2009. Guide 98-1. Uncertainty of measurement Part 1: Introduction to the expression of uncertainty in measurement, 2009.
ISO/IEC 17025:2005. Requisitos generales para la competencia de los laboratorios de ensayo y de calibración. Disponible en https:// www.iso.org/obp/ui/#iso:std:isoiec:17025:ed-2:v1:es
JCGM 200. 2008. Vocabulario Internacional de Metrología. Conceptos fundamentalesy generales,y términos asociados (VIM), 2008.
Leslie HA, Pavluk TI, bij de Vaate A, Kraak MH. 1999. Triad assessment of the impact of chromium contaminación on benthic macroinvertebrates in che Chusovaya river (Urals, Russia). Arch. environm. contam. Toxicol. 37: 182-189.
OgbeibuAE,OribhaborBJ.2002.Ecological impact of river impoundment using
benthic macro-invertebrates as indicators.WaterRes. 36: 2427-2436.
Estimación de la incertidumbre de resultados de ensayos.
XXXXX 1(1): 29 - 37 (2017)
ISSN (Versión electrónica)


Website:
ARTÍCULO ORIGINAL –RESEARCHARTICLE
Autorización de personal para la realización de ensayos
Personal authorization for testing
Liliana Balbín1; José Quinte1; MagalyAcosta1; Manuel Gamboa1

1Investigador independiente, Lima, Perú.
*Autor de correspondencia: Email: ORCID:
Recibido: 31/01/2016; Aceptado: 30/06/2017; Publicado: 30/06/2023
Resumen
El objetivo del presente estudio fue evaluar la competencia del Personal Técnico del Laboratorio,encargadoderealizarlosensayos.Paraello,seaplicaronherramientasestadísticas parala aprobación del personal, los cuales dan laseguridad de quelos resultados sean veraces y precisos. Además, para desarrollar el procedimiento de aprobación se utilizó una muestra analizada en el Laboratorio de calidad, la cual fue tomada como una muestra de referencia. El analista en entrenamiento analiza la muestra de referencia; los resultados obtenidos son evaluados, obteniendo un promedio, del cual se concluye si elAnalista se encuentra apto o no para realizar el ensayo. Este tipo de Evaluación permite destacar la Competencia Técnica del Personal, para que se tenga así una herramienta a fin de demostrar la competencia técnica de acuerdo con ISO/IEC 17025:2005. De los resultados obtenidos se concluye que, el analista 2 y 4 califican en precisión y veracidad, siendo los autorizados para la ejecución del ensayo de determinación de contenido por HPLC del producto Lorexona tabletas recubiertas.
Palabras clave: Material de Referencia; Herramientas estadísticas; Competencia Técnica.
Abstract
The objective of this study was to evaluate the competence of the Laboratory Technical Personnel, in charge of carrying out the tests. For this, statistical tools were applied for the approval of the staff, which give the assurance that the results are truthful and accurate. In addition, a sample analyzed in the Quality Laboratory was used to develop the approval procedure, which was taken as a reference sample. The analyst-in-training analyzes the reference sample; the results obtained are evaluated, obtaining an average, from which it is concluded whether the Analyst is fit or not to carry out the test. This type of Evaluation highlights the Technical Competence of the Personnel, so that there is a tool to demonstrate technical competence in accordance with ISO / IEC 17025: 2005. From the results obtained, it is concluded that analyst 2 and 4 qualify in precision and veracity, being authorized to carry out the content determination test by HPLC of the Lorexona product coated tablets.
Keywords: Reference Material;Tools statistics; Technical Competence.

Forma de citar el artículo: Balbín, L., Quinte, J., Acosta, M., & Gamboa, M. (2023). Autorización de personal para la realización de ensayos. Inocua 1(1): 29 - 37 (2023). DOI:
DOI:
© Los autores. Este artículo es publicado por la revista xxxxxxx de la Universidad Nacional Agraria La Molina. Este es un artículo de acceso abierto, distribuido bajo los términos de la Licencia Creative Commons Atribución 4.0 Internacional.(https://creativecommons.org/licenses/by/4.0/) que permite Compartir (copiar y redistribuir el material en cualquier medio o formato), Adaptar (remezclar, transformar y construir a partir del material) para cualquier propósito, incluso comercialmentte.
Estimación de la incertidumbre de resultados de ensayos
1. Introducción
La NORMA ISO/IEC 17025, fue preparada por ISO (Organización Internacional de Normalización) /CASCO (Comité de ISO paralaevaluacióndelaconformidad),Comité de evaluación de la conformidad (NORMA ISO/IEC 17025, 2005) y, se desarrolló con el fin de establecer los requisitos para acreditar el Sistema de Gestión de Calidad y la Competencia Técnica de los Laboratorios de ensayo y/o calibración, en la realización de ensayos o de calibraciones, incluido el muestreo (Intedya, 2016).
En el numeral 5.2.5 de la Norma ISO/ IEC 17025 (2005) acota: “La dirección debe autorizar a miembros específicos del personal para realizar tipos particulares de muestreos, ensayos o calibraciones, para emitir informes de ensayos y certificadosde calibración, para emitir opinionese interpretaciones y para operar tipos particulares de equipos. El laboratorio debe mantener registros de las autorizaciones pertinentes, de la competencia, del nivel de estudios y de las calificaciones profesionales, de la formación, de las habilidades y de la experiencia de todo el personal técnico, incluido el personal contratado. Esta información debe estar fácilmente disponible y debe incluir la fecha en la que se confirma la autorización o la competencia”
Conelobjetivodeevaluarlacompetencia del Personal Técnico del Laboratorio para autorizar a los analistas realizar ensayos.Se evalúa la calidad de las actividades realizadas al asegurar que, los resultados sean veraces y precisos. Al autorizar al personal, se demuestra la competencia que tieneel Laboratorio para realizar los análisis, la responsabilidad del personal para ejecutar funciones específicas dentro del alcance total del trabajo; lo que permite demostrar a la organización su responsabilidad en los resultados obtenidos.
2. Materiales y métodos
La metodología para la Autorización del Personal para la realización de ensayos, se realiza al ejecutar la realización del análisis de contenido de principio activo de Loratadina y Dexametasona en el medicamento LOREXONA. Para ello, se analiza la muestra, con seis repeticiones.
Los resultados obtenidos son analizados a través del Minitab, Programa de Computadora utilizado en la ejecución de funciones estadísticasy avanzadas.Seutilizó la Prueba de Anderson Darling, para evaluar la Normalidad de los resultados obtenidos por elAnalista en capacitación (Fórmula 1).
Fórmula 1
Donde, n: Es el número de datos; zi: Es el valor del resultado estandarizado de la posición i-ésima ordenado de menor a mayor; F: Función de Probabilidad Normal Acumulada y, AD: Estadístico de Anderson Darling.
El Estadístico de Contraste se determina mediante la Fórmula 2. Donde, Si AD > CV los datos no se distribuyen normalmente al 95% de confianza, caso contrario estos se distribuyen normalmente; sí P-Value, es menor que el Nivel de Significancia (0,05) los datos no se distribuyen normalmente.

Para evaluar la Veracidad de los datos obtenidos. Al evaluar la Normalidad y obtenerlos datos quetienen unaDistribución Normal, se aplicó la Prueba T- Student de una muestra. La Prueba T-Student se utilizó para contrastar la hipótesis nula de una muestra que procede de una población en la que la media de x es igual a una constante. También,seutilizólaPrueba T-Student para evaluar la Veracidad de los datos obtenidos. Para una muestra, se calcula el estadístico experimental t (Fórmula 3).
Donde,x:Media,µ0:ValordeReferencia a probar y, s: Desviación típica.
El estadístico de tabla se determina mediante la Fórmula 4. La decisión es, si el valor absoluto de (t experimental) > ttabla el promedio de los datos no coincide
con el valor de referencia, caso contrario coincide. Se debe realizar mediante el análisis de determinación de Loratadina y dexametasona tabletas método por HPLC. Otra forma de evaluar es con el P-value, si 1(α), indica que el promedio de los datos es diferente al valor de referencia.
Fórmula 4 t [1-(α/2), n-1]


Evaluación de la precisión del Analista, se evalúa aplicando el RSD (Desviación Estándar Relativa) (Fórmula 5), que es un parámetro estadístico independiente de las unidades de medida empleadas. Donde, si el RSD Horwitz ≥ RSD Experimental; existe precisión.
RSD: s/x
RSD Experimental = s x /x *100
3. Resultados y discusión
En la Tabla 1 se muestran los resultados obtenidosporlosAnalistasenEntrenamiento realizado. Especialización de Loratadina (9 mg-11 mg) y Especialización de Dexametasona (1,80 mg-2,2 mg); mientras que, en las Figuras 1, 2, 3 y 4 se presentan la gráfica de probabilidad de la Loratadina y en la Figuras 5, 6, 7 y 8 se presentan la gráfica de probabilidad de la Dexametasona
Estimación de la incertidumbre de resultados de ensayos
Prueba T e IC de dos muestras: Analista 1,Analista 3
T de dos muestras para Analista 1 vs. Analista 3
Error estándar de la N Media Desv.Est. media Analista 1 6 9,9921 0,0547 0,022 Analista 3 6 10,073 0,255 0,10
Diferencia = mu (Analista 1) - mu (Analista 3)
Estimado de la diferencia: -0,081
IC de 99% para la diferencia: (-0,510; 0,349)
Prueba T de diferencia = 0 (vs. no =): Valor T =
-0,76 Valor P = 0,482 GL= 5
Prueba T e IC de dos muestras: Analista 1,Analista 2
T de dos muestras para Analista 1 vs. Analista 2
Error estándar de la
Diferencia = mu (Analista 1) - mu (Analista 2)
Estimado de la diferencia: 0,0066
IC de 99% para la diferencia: (-0,1082; 0,1214)
Prueba T de diferencia = 0 (vs. no =): Valor T =
0,19 Valor P = 0,855 GL = 9
Prueba T e IC de dos muestras: Analista 1,Analista 4
T de dos muestras para Analista 1 vs. Analista 4
Error estándar

Diferencia = mu (Analista 1) - mu (Analista 4)
Estimado de la diferencia: -0.0058
IC de 99% para la diferencia: (-0,1512; 0,1396)
Prueba T de diferencia = 0 (vs. no =): Valor T = -0,13 Valor P = 0,897 GL= 8
Prueba e IC para dos varianzas: Analista 1,Analista 2
Método
Hipótesis nula:
Sigma(Analista 1)/Sigma(Analista 2) = 1
Hipótesis alterna
Sigma(Analista 1)/Sigma(Analista 2) not = 1
Nivel de significancia Alfa = 0,01
Estadísticas
Relación de deviaciones estándar = 0,816
Relación de varianzas = 0,666
Intervalos de confianza de 99%
IC para IC para Distribución relación de relación de de los datos Desv.Est. varianza Normal (0,211; 3,154) (0,045; 9,946)
Continuo (0,047; *) (0,002; *)
Pruebas
Estadística
Prueba e IC para dos varianzas: Analista 1,Analista 3
Método
Hipótesis nula
Sigma(Analista 1) / Sigma(Analista 3) = 1
Hipótesis alterna
Sigma(Analista 1)/Sigma(Analista 3) not = 1
Nivel de significancia Alfa = 0,01
Estadísticas
Relación de deviaciones estándar = 0,214
Relación de varianzas = 0,046
Intervalos de confianza de 99%
IC para IC para Distribución relación de relación de de los datos Desv.Est. varianza
Normal (0,055; 0,829) (0,003; 0,687)
Continuo (0,013; *) (0,000; *)
Pruebas
Estadística
Estimación de la incertidumbre de resultados de ensayos
Prueba e IC para dos varianzas: Analista 1,Analista 4
Método
Hipótesis nula
Sigma(Analista 1)/Sigma(Analista 4) = 1






Hipótesis alterna
Sigma(Analista 1)/Sigma(Analista 4) not = 1
Nivel de significancia Alfa = 0,01
Estadísticas
Variable N Desv.Est. Varianza
de Relación de deviaciones estándar = 0,601
Relación de varianzas = 0,362
Intervalos de confianza de 99%
Figura 6: Dexametasona,
Distribución de los datos
IC para relación de Desv.Est.
IC para relación de varianza
Normal (0,156; 2,324) (0,024; 5,401)
Continuo (0,037; *) (0,001; *)
Pruebas Estadística
Método GL1GL2de pruebaValor P
Prueba F (normal) 5 5 0,36 0,288
Prueba de Levene 1 10 0,54 0,479 (cualquiera continua)
Balbín, L., Quinte, J.,Acosta, M., & Gamboa, M.
XXXXX 1(1): 29 - 37 (2023)
Estimación de la incertidumbre de resultados de ensayos
Prueba T e IC de dos muestras: Analista
1,Analista 2
T de dos muestras para Analista 1 vs. Analista 2
Prueba T e IC de dos muestras: Analista
1,Analista 4
T de dos muestras para Analista 1 vs. Analista 4
Diferencia = mu (Analista 1) - mu (Analista 2)
Estimado de la diferencia: -0,0129
IC de 99% para la diferencia: (-0,0558; 0,0300)
Prueba T de diferencia = 0 (vs. no =): Valor T =
-1,05 Valor P = 0,328 GL= 7
Prueba T e IC de dos muestras: Analista
1,Analista 3
T de dos muestras para Analista 1 vs. Analista 3
Diferencia = mu (Analista 1) - mu (Analista 4)
Estimado de la diferencia: -0,0198
IC de 99% para la diferencia: (-0,0583; 0,0187)
Prueba T de diferencia = 0 (vs. no =): Valor T =
-1,72 Valor P = 0,123 GL= 8
Prueba e IC para dos varianzas: Analista
1,Analista 2
Método
Hipótesis nula
Sigma(Analista 1) / Sigma(Analista 2) = 1
Hipótesis alterna
Sigma(Analista 1) / Sigma(Analista 2) not = 1
Nivel de significancia Alfa = 0,01
Estadísticas
Diferencia = mu (Analista 1) - mu (Analista 3)
Estimado de la diferencia: -0,0744
IC de 99% para la diferencia: (-0,2269; 0,0781)
Prueba T de diferencia = 0 (vs. no =): Valor T =
-1,97 Valor P = 0,106 GL= 5
Relación de deviaciones estándar = 0,565
Relación de varianzas = 0,319
Balbín, L., Quinte, J.,Acosta, M., & Gamboa, M. XXXXX 1(1): 29 - 37 (2023)
Intervalos de confianza de 99% IC para ICpara Pruebas Estadística
Distribución relación de relación de de los datos Desv.Est. varianza
Método GL1 GL2 depruebaValor P Prueba F (normal) 5 5 0,03 0,001 Prueba de Levene 1 10 3,81
(cualquiera continua)
Pruebas Estadística
Método GL1GL2 depruebaValorP
(cualquiera continua)
Prueba e IC para dos varianzas: Analista 1,Analista 3
Método Hipótesis nula
Sigma(Analista 1) / Sigma(Analista 3) = 1
Hipótesis alterna Sigma(Analista 1) / Sigma(Analista 3) not = 1
Nivel de significancia Alfa = 0,01
Estadísticas
Relación de deviaciones estándar = 0,162
Relación de varianzas = 0,026
Prueba e IC para dos varianzas: Analista 1,Analista 4
Método
Hipótesis nula
Sigma(Analista 1) / Sigma(Analista 4) = 1
Hipótesis alterna
Sigma(Analista 1) / Sigma(Analista 4) not = 1
Nivel de significancia Alfa = 0,01
Estadísticas
Variable N Desv.Est. Varianza
Analista 1 6 0,015 0,000
Analista 4 6 0,024 0,001
Relación de deviaciones estándar = 0,619
Relación de varianzas = 0,383
Intervalos de confianza de 99% IC para IC para Distribución relación de relación de los datos Desv.Est. devarianza
Normal (0,160; 2,391) (0,026; 5,719)
Continuo(0,241;413,371) (0,058;170875,524)
Intervalos de confianza de 99% Pruebas
IC para IC para Distribución relación de relación de de los datos Desv.Est. varianza
Normal (0,042; 0,625) (0,002; 0,390)
Continuo (0,063; *) (0,004; *)
Estadística
Método GL1 GL2 de prueba Valor P
Prueba F (normal) 5 5 0,38 0,315
Prueba de Levene 1 10 0,93 0,358 (cualquiera continua)
Estimación de la incertidumbre de resultados de ensayos
4. Conclusiones
En base a los resultados obtenidos se autorizó al Analista 1 por ser que obtuvo el menor resultado en comparación a la desviación estándar relativa RSD (%) de Horwitz.Además, los datos de contenido de Loratadina y Dexametasona obtenidospor los analistas 1, 2, 3 y 4 presentan una distribución normal. Por lo tanto, el analista 2 y 4 califican en precisión y veracidad, son los autorizados para la ejecución del ensayo de determinación de contenido por HPLC del producto LorexonaTabletas Recubiertas.
5. Literatura citada
Intedya. 2016. Nueva versión de la norma
ISO/IEC 17025: Sistema de Gestión para los Laboratorios de Ensayo y/o Calibración. Fechas y principales cambios. Disponible en https://www. intedya.com/internacional/intedyanoticias.php?id=1309#submenuhome
NORMA ISO/IEC 17025. 2005. Requisitos generales para la competencia de los laboratorios de ensayo y de calibración. Disponible en https:// www.medicinalaboraldevenezuela. com.ve/archivo/otras-normas/ iso_17025_es.pdf
SISTEMAS DE GESTIÓN DE LA SEGURIDAD, SALUD OCUPACIONAL Y MEDIO AMBIENTE (SSOMA)
INGENIERIA DE LA CALIDAD Y PROCESOS
GESTION AMBIENTAL PARA EL DESARROLLO SOSTENIBLE

SISTEMA DE GESTION DE CALIDAD E INOCUIDAD EN LA INDUSTRIA ALIMENTARIA (SGCIA)
SISTEMA DE GESTION DE LA CALIDAD EN LABORATORIO
ISO/IEC 17025
SISTEMAS INTEGRADOS DE GESTIÓN (SIG)
GERENCIA, MANEJO Y GESTION INTEGRAL DE RESIDUOS SOLIDOS
www.lamolinavirtual.org
www.facebook.com/inocuaperu2
www.youtube.com/@InocuaPeru2

