
© David Parkins - www.davidparkins.com



© David Parkins - www.davidparkins.com

Henvis høyrisiko nmCRPC-pasienter* med raskt stigende PSA til onkolog.

Behandling med NUBEQA® forlenger tiden til utvikling av metastaser1-3 og forbedrer totaloverlevelsen hos pasienter med PSA doblingstid ≤ 10 måneder.1-3
Sikkerhetsinformasjon1
• Overvåk nøye for bivirkninger hos pasienter med alvorlig nedsatt nyre eller leverfunksjon.
• Seponer Nubeqa permanent ved unormale leverfunksjonsprøver som tyder på idiosynkratisk legemiddelindusert leverskade.
• Sikkerhet ved kardiovaskulær sykdom siste 6 mnd. er ikke fastslått; behandle klinisk signifikante tilfeller iht. retningslinjer, og vurder nytte-/risikoforhold ved QT-forlengelse før oppstart med Nubeqa.
• Vanlige bivirkninger (≥ 10 %): nmCRPC: fatigue/astenitilstander, redusert antall nøytrofile, økt bilirubin, økt ASAT. mHSPC med docetaksel: hypertensjon, utslett, redusert antall nøytrofile, økt bilirubin, ALAT, ASAT.
• Andre viktige bivirkninger (≥ 1/100, < 1/10): nmCRPC: iskemisk hjertesykdom, hjertesvikt, utslett, smerter (ekstremitet, muskler, skjelett), frakturer. mHSPC: frakturer, gynekomasti.
Se felleskatalogtekst for mer informasjon, merk spesielt kontraindikasjoner, forsiktighetsregler, interaksjoner og bivirkninger. Basert på SPC: 05/2024.
*Ingen metastaser oppdaget ved bruk av konvensjonell bildediagnostikk. nmCRPC=ikke-metastatisk kastrasjonsresistent prostatakreft; PSA=Prostataspesifikt antigen; Referanser: 1. NUBEQA SPC 05/2024. 2. Fizazi K, Shore N, Tammela TL et al. Darolutamide in Nonmetastatic, Castration-Resistant Prostate Cancer. N Engl J Med. 2019;380:1235–1246. 3. Fizazi K, Shore N, Tammela TL et al. Nonmetastatic, castration-resistant prostate cancer and survival with darolutamide. N Engl J Med. 2020;383:1040–1049.
Det primære effektmålet i ARAMIS var metastasefri overlevelse (darolutamid 40,4 måneder vs placebo 18,4 måneder; HR:0,41; 95% CI: 0,34-0,50; P<0,001) og total overlevelse var et sekundært effektmål (HR: 0,69; 95 % Cl: 0,53-0,88; P=0,003). Sluttanalysen av overlevelsesdataene ble utført etter 254 dødsfall (148 (15 %) i darolutamid + ADT-gruppen og 106 (19 %) i ADT-gruppen (placebogruppen).
▼NUBEQA® (darolutamid) 300 mg filmdrasjerte tabletter. ATC-nr: L02B B06. Indikasjoner: Nubeqa er en androgenreseptorhemmer indisert til behandling av voksne menn med: 1. ikke-metastatisk, kastrasjonsresistent prostatakreft (nmCRPC), som har høy risiko for å utvikle metastatisk sykdom; 2. metastatisk hormonsensitiv prostatakreft (mHSPC) i kombinasjon med docetaksel og androgen deprivasjonsbehandling. Dosering: Anbefalt dose er 600 mg (2 tabletter à 300 mg) 2 ganger daglig, tilsv. total daglig dose 1200 mg. Medisinsk kastrasjon med GnRH-analog skal fortsette under behandling hos pasienter som ikke er kirurgisk kastrert. Kontraindikasjoner: Overfølsomhet for virkestoffet eller noen av hjelpestoffene (laktose). Kvinner som er eller kan bli gravide. Forsiktighetsregler: Pasienter med alvorlig nedsatt nyrefunksjon eller moderat/alvorlig nedsatt leverfunksjon skal overvåkes nøye mht. bivirkninger pga. forhøyet eksponering. Tilgjengelige data for pasienter med alvorlig nedsatt nyrefunsjon samt pasienter med moderat svekket leverfunksjon er begrenset. Darolutamid er ikke undersøkt hos pasienter med alvorlig svekket leverfunksjon. Hjerte/ kar: Sikkerhet er ikke fastslått ved kardiovaskulær sykdom de siste 6 månedene. Ved forskrivning skal
Nubeqa® er innført av Beslutningsforum til behandling av voksne menn med ikke-metastatisk kastrasjonsresistent prostatakreft (nmCRPC) som har høy risiko for å utvikle metastatisk sykdom. Nubeqa er rangert som førstevalg i LIS anbud 2407 Onkologi for nmCRPC. Nubeqa i kombinasjon med docetaksel og androgen deprivasjonsbehandling er innført til menn med metastatisk hormonsensitiv prostatakreft (mHSPC) når abirateron ikke er egnet. Vilkår: - Behandlingen er kun aktuell for pasienter med komorbiditet som gjør abirateron uegnet. – Dette gjelder pasienter med dårlig regulert eller ukontrollert diabetes, vanskelig regulerbar hypertensjon, eller levertoksisitet under abirateronbehandling. Nubeqa forskrives på H-resept.
Les mer om NUBEQA®

pasienter med klinisk signifikant kardiovaskulær sykdom behandles for disse tilstandene iht. fastsatte retningslinjer. Ved risikofaktorer for QT-forlengelse i anamnesen og ved samtidig bruk av legemidler som kan forlenge QT-intervallet, skal nytte-/risikoforholdet vurderes, inkl. potensialet for torsades de pointes, før oppstart med darolutamid. Behandlingen med darolutamid skal seponeres permanent ved unormale resultater av leverfunksjonsprøver som tyder på idiosynkratisk legemiddelindusert leverskade. Bruk av sterke CYP3A4- og P-gp-induktorer ved behandling med darolutamid kan redusere plasmakonsentrasjonen av darolutamid og anbefales ikke med mindre det ikke finnes andre behandlingsalternativer. Bruk av et annet legemiddel med mindre potensial for induksjon av CYP3A4 eller P-gp, skal vurderes ved samtidig administrering. Pasienter skal overvåkes med hensyn til bivirkninger av BCRP-, OATP1B1- og OATP1B3-substrater, fordi samtidig administrering av darolutamid kan øke plasmakonsentrasjonen av disse substratene. Samtidig administrering av rosuvastatin bør unngås, med mindre det ikke finnes andre behandlingsalternativer. Bivirkninger: 1. Hos pasienter med nmCRPC: Svært vanlige (≥ 1/10): Fatigue/astenitilstander, redusert antall nøytrofile, økt bilirubin og ASAT. Vanlige (≥ 1/100, < 1/10): Iskemisk hjertesykdom og hjertesvikt, utslett, smerter i ekstremiteter, smerter i muskler og skjelett samt frakturer. 2. I kombinasjon med docetaksel hos pasienter med mHSPC: Svært vanlige (≥ 1/10): Hypertensjon, utslett, redusert antall nøytrofile, økt bilirubin, ALAT og ASAT. Vanlige (≥ 1/100, < 1/10): Frakturer, gynekomasti. Basert på SPC godkjent av DMP/EMA: 05/2024 . Konsulter preparatomtalen (SPC) for mer informasjon. Pakninger og priser: 112 stk. (blister) AUP 46.636,30 NOK Varenr: 063426. R.gr. C, H-resept. For oppdaterte priser se: www.felleskatalogen.no. Kontaktinformasjon: Bayer AS, Drammensveien 288, NO-0283 OSLO, Postboks 193, 1325 Lysaker, tlf: +47 23 13 05 00, www.bayer.no MA-NUB-NO-0005-3, 09-2024
▼Dette legemiddelet er under spesiell overvåkning for å oppdage ny sikkerhetsinformasjon så raskt som mulig. Du kan bidra ved å melde enhver mistenkt bivirkning via relis.no.

KOMMENDE TEMAER I 2025:
Nr. 1. Plastikkirurgi
Nr. 2. Bryst- og endokrinkirurgi
Nr. 3. IBD
Nr. 4. Nevrokirurgi
INNLEVERINGSFRISTER:
Kirurgen nr 1-25: 24. januar
Kirurgen nr 2-25: 24. april
Kirurgen nr 3-25: 24. august
Kirurgen nr 4-25: 24. oktober
Kirurgen ønsker å være en nasjonal plattform for kirurgi ved å inspirere til faglig kompetanseheving, bedre utdanning og opplæring av unge kirurger, samt øke interessen for kirurgisk forskning.
– VISJON, KIRURGEN
UTGIVER
Norsk Kirurgisk Forening
Pb 17 Kjelsås, 0411 Oslo
ISSN 1504-88 88
REDAKSJON Tobias Hauge (redaktør) OUS Ullevål tobias@kirurgen.no
Marte Bliksøen (redaksjonsmedlem) OUS Rikshospitalet marte@kirurgen.no
Saira Mauland Mansoor (redaksjonsmedlem) Vestre Viken Bærum sykehus saira@kirurgen.no
Ingvar Rognum (redaksjonsmedlem) Vestre Viken Bærum sykehus ingvar@kirurgen.no
David Hui (redaksjonsmedlem) OUS Rikshospitalet david@kirurgen.no
LAYOUT, PRODUKSJON OG ANNONSESALG WebPress
Tlf.: 22 76 00 00 john@webpress.no www.webpress.no





Hvorfor skal kirurger engasjere seg i forskning?
A brief introduction to surgical research
Når er en kirurgisk metode etablert behandling?
Moralske valg er en del av god forskning
Hvorfor er forskning viktig for kirurger?
Kvalitetsforbedring – The missing link for kirurger?
utenfor universitetssykehusene
lese en vitenskapelig artikkel?
Narrekirurgi – nytte og etikk 222
3rd Nordic meeting on Barretts esophageal and early esophageal cancer
Nytt Handlingsprogram for kreft i spiserør og magesekk
MINISERIE: FORSKNING OG
VITENSKAPELIG SKRIVING
Del 1: Hvordan komme i gang?
Del 2: Fra idé til ferdig artikkel
226
229
Del 3: Formidling av forskningen i moderne tid – bedre tilgang, nye medier og fagfellerollen 238
Årets artikkel i Kirurgen 2023/2024
FUNKs ærespris til Kirurger 2023/2024
Den akademiske kirurgen – et leserinnlegg fra Kirurgisk Høstmøte 2024 244
Screening for abdominalt aortaaneurisme (AAA) blant 65 år gamle menn i Oslo 246
– Quality Improvement in the Treatment of Hip Fractures 248

The intelligent performance of Signia™ with Tri-Staple™ technology provides better staple formation across sizes and delivers distinct advantages compared to the da Vinci SureForm™* robotic stapler.1,†
The intelligent performance of Signia™ with Tri-Staple™ technology provides better staple formation across sizes and delivers distinct advantages compared to the da Vinci SureForm™* robotic stapler.1,†
staple
Test tissue thickness
Test tissue thickness SureForm™* stapler (indicated tissue thickness)
Extra thick
Extra thick
2.80–3.2 2mm
2.80–3.2 2mm
Thick 2.50–2.80 mm
Medium/Thick 1.90 mm
SureForm™* stapler (indicated tissue thickness)
Signia™ linear stapler with Tri-Staple™ technology (indicated tissue thickness)
Signia™ linear stapler with Tri-Staple™ technology (indicated tissue thickness)

Staple formation reference
Staple formation reference
Black (2.30–4.00 mm)
(2.30–4.00 mm)

Green (2.00–3.30 mm)
mm)
Blue (1.50–2.40 mm)

114% greater staple line security across staple sizes1,†
114% greater staple line security across staple sizes1,†
Black (2.29–3.00 mm)
mm)


Optimally formed staple
Optimally formed staple

Undercrimped staple
Undercrimped staple
mm)
Purple (1.50–2.29 mm)


Functional closure
Functional closure
Signia™ with Tri-Staple™ black staple lines can withstand 20% greater leak pressure1,† than SureForm™* black staple lines
Signia™ with Tri-Staple™ black staple lines can withstand 20% greater leak pressure1,† than SureForm™* black staple lines
Signia™ with Tri-Staple™ tan staple lines are 37% less likely to bleed1,†,‡ than SureForm™* white staple lines
Signia™ with Tri-Staple™ tan staple lines are 37% less likely to bleed1,†,‡ than SureForm™* white staple lines
Meet clinical challenges with confidence. Visit https://www.medtronic.com/covidien/en-gb/surgical-stapling-innovation.html
Contact your Medtronic representative today to experience the Signia™ stapler with Tri-Staple™ technology.
Contact your Medtronic representative today to experience the Signia™ stapler with Tri-Staple™ technology.
Meet clinical challenges with confidence. Visit https://www.medtronic.com/covidien/en-gb/surgical-stapling-innovation.html
†When fired in indicated porcine tissue thickness. Preclinical testing may not be indicative of clinical performance. ‡P-value of 0.061, statistical significance seen at 10-minute time point.
†When fired in indicated porcine tissue thickness. Preclinical testing may not be indicative of clinical performance.
‡P-value of 0.061, statistical significance seen at 10-minute time point.
1. Based on internal report #RE00498029, Competitive evidence final report — Signia™ with Tri-Staple™ technology vs. Intuitive’s da Vinci robotic stapling system with SureForm™* SmartFire technology.
1. Based on internal report #RE00498029, Competitive evidence final report — Signia™ with Tri-Staple™ technology vs. Intuitive’s da Vinci robotic stapling system with SureForm™* SmartFire technology.
©2024 Medtronic. Medtronic, Medtronic logo, and Engineering the extraordinary are trademarks of Medtronic.
©2024 Medtronic. Medtronic, Medtronic logo, and Engineering the extraordinary are trademarks of Medtronic.
™* Third-party brands are trademarks of their respective owners. All other brands are trademarks of a Medtronic company. emea-st-2400048-signia-and-tri-staple-vs-sureform-ad--emea-14451623
™* Third-party brands are trademarks of their respective owners. All other brands are trademarks of a Medtronic company. emea-st-2400048-signia-and-tri-staple-vs-sureform-ad--emea-14451623

TOBIAS HAUGE , REDAKTØR
TOBIAS @ KIRURGEN.NO
Overskriften er et sitat som tilhører min forgjenger, Marte Bliksøen. Temaet for denne utgaven av Kirurgen er forskning. Dette er en utgave jeg, som redaktør av Kirurgen, er utrolig stolt over at vi har fått til. Dere vil på de følgende sidene finne artikler skrevet av toneangivende norske og internasjonale forskere og klinikere. Artikler som jeg håper klarer å overbevise dere om at kirurgi er mer enn et håndverk.
Det 99. Kirurgiske Høstmøtet er akkurat ferdig. Tradisjonelt sett har Høstmøtet vært den uken i året hvor norske kirurger, uavhengig av arbeidssted og spesialitet har hatt mulighet til å møtes. Det har vært stedet hvor både yngre og eldre kollegaer, fra små og store sykehus, har kunnet presentere sine arbeider. Mange av disse arbeidene har vært kvalitetsforbedringsarbeider med presentasjon av egne pasientmaterialer. Hensikten har vært flerdelt: viktigst, den enkelte avdeling får oversikt over sine egne resultater. Hvordan går det egentlig med de pasientene vi opererer? Som kirurger må vi vite hvordan det går med pasientene våre! For mange har innsending av abstrakt til Høstmøtet også vært det lille ekstra som har «pushet» en til å fullføre dette viktige, men ofte tidkrevende, kvalitetsarbeidet. Høstmøtet har også vært stedet hvor yngre kollegaer får øve seg på å presentasjonsteknikk og for mange kanskje også det første møtet med å presentere et arbeide for kolleger. Sist, men ikke minst, et akseptert foredrag, var ofte billetten til å reise på Høstmøtet.
Det er derfor med stor frykt at jeg i år ser at det er en drastisk nedgang i antall innsendte frie foredrag innenfor gastroenterologisk kirurgi, spesielt innenfor kolorektalkirurgi hvor kun ett foredrag ble presentert. Jeg håper dette endrer seg markant til neste år!
Misforstå meg ikke, Høstmøtet er fortsatt et veldig bra møte som vi må verne om! Urologene hadde i år et rekordår når det gjelder antall innsendte abstrakter og flere måtte refunderes grunnet plassmangel. Den økte andelen av symposier har virkelig hevet den faglige kvaliteten på møtet. Jeg ønsker spesielt å trekke fra symposiet: «Den akademiske kirurgen». Et meget godt symposium, med gode foredragsholdere som jeg tror inspirerte de fleste i salen til å ha en noe mer akademisk tilnærming i hverdagen. Vi kan ikke lengre skjule oss bak en misoppfattelse om at kirurgi kun er et håndverk. Vi er nødt til å ha en akademisk tilnærming. Det betyr ikke alle kirurger må ha en doktorgrad, men vi må holde oss faglig oppdaterte. Vi må vite hvor vi finner oppdatert faglig korrekt informasjon og ikke minst må vi vite hvordan det går med våre pasienter. Holdningen om at «slik gjør vi det bare» er ikke god nok.
Med dette ønsker jeg dere alle riktig god lesning og etter hvert en god og velfortjent jule og nyttårsfeiring!




Foto: Arkady Rutkovskiy

November er en måned folk flest kunne klart seg uten. Mørkt, vått, kaldt, surt og glatt. Ikke heller «Movember» får november til å fremstå i bedre lys. Ingen nyanlagt bart eller skjegg er morsomt nok for å radere november melankolien.
Tror Piet Hein skrev dette i november, om november: Lyset er grått og været er vått, Og føret er kun for vadere, Og jeg er så sur, - og det gjør meg så glad, For nå kan jeg kun bli gladere!
Men heihei, noen av oss har bursdag i november og har vært «tvunget» til å se denne måneden som en av de beste i hele året. Det innebærer gaver, blomster og mange hyggelige meldinger som hjelper en å steppe opp på et høyere nivå (les: å bli eldre). Og har man ikke bursdag, så kan det være andre lysglimt uansett det mørke og dystre: gode kolleger, venner som bryr seg og støtte fra familien. Både de i medvind og uten, gi november en sjans, folkens.
Hva angår tidligere NKF ledere vites ikke, men nåværende er nok passe naiv: trodde at etter Høstmøtet (takk, det ble en superfin en J) ville det bli litt roligere dager, at man kanskje kunne rekke hjem til barneTV og lage middag til familien. Bare rosa briller! Influensa, covid, alminnelig snørr og magesjau gjør også kirurger sjuke, og de friske må løpe fortere, tenke smartere, visitere visere, operere flere etc. Men det er håp. Snart er det over. November er straks slutt! Og da kommer selveste magiske
julemåneden, ren kos med pepperkaker, nisser, peis, festsveis og håp om at de sjuke blir friske og at en holder seg selv frisk. Så la oss, hvor hen enn vi er: på uro og plast, endokrin, gastro og thorax, orto, neuro, kar og barn, gå inn mot 2025 duftende av inntatt hvitløk og påsmurt tigerbalsam, med imodium i lomma, for det finnes håp for 2025!
De på Traume derimot, de som redder dem som reddes kan, år inn og år ut, mandag, tirsdag, onsdag, torsdag, fredag, lørdag, søndag, julaften, 1. og 2. juledag, påsken og pinsen etc. – hva med dem? Er det håp for normalt arbeidshverdag for overlegene på traume på OUS? Varslinger, SOSrop via media, drøftingsmøter og stor bekymring helt siden sommeren og lenge før det, hva mer kan voksne folk gjøre for å verne mot undergang av et veloppbygd system som vi alle i Norge har behov for? Det er et retorisk spørsmål, med hint av resignasjon og hjelpeløshet. Traumekirurger er ikke bare lokale helter for Helse SørØst sin befolkning men jobber for hele landet som base for Nasjonalt Senter for Traumatologi med 24/7 engasjement for både behandling, og trening og opplæring i traumekirurgi for hele landet. La oss håpe at ledelsen i OUS tar sin nasjonale oppgave på alvor, og at traumeavdelingen består. Eller bør vi allikevel be til alle de 3427 (eller flere?) guder som finnes. For sikkerhets skyld.
Med
håp, Mari-Liis Kaljusto Leder NKF
• Egner seg for klinikere og forskere innen medisin og helsefag med noe eller liten publiseringserfaring.
• Dekker alle faser i en publiseringsprosess, fra planlegging, skriving, tittel og abstrakt, til utarbeidelse av tabeller og figurer.
• Kurslærerne er erfarne forskere og redaktører, blant annet fra tre av verdens mest prestisjetunge medisinske tidsskrifter.
• Forelesninger og gruppeundervisning med skrivetrening og tilbakemelding på egne abstrakt, tabeller og figurer.
Kurssted
Legenes hus Christiania torv 5, Oslo
Kursavgift
7 300 kroner, som også dekker lunsj, kaffe og kursdiplom.
Språk Kurset blir holdt på engelsk.
Forarbeid
Utkast til abstrakt, tabeller og figurer må sendes inn for vurdering i forkant av kursstart. Mer info vil bli gitt etter påmelding.
Kurslærere
Darren Taichman Deputy Editor, New England Journal of Medicine
Christine Laine
Editor-in-chief, Annals of Internal Medicine
David Weinberg
Editor-in-chief, Gastroenterology
Erfarne forskere og redaktører fra Universitetet i Oslo og Tidsskrift for Den norske legeforening.
Kurskoordinator
Line Anne Hovdenakk Universitetet i Oslo
Påmelding
Snarest mulig, og senest 15. april 2025. Det er et begrenset antall plasser. Påmelding ved å følge QR-koden:
Abraham Verghese skriver i boken “Cutting for Stone”: “Life, too, is like that. You live it forward, but understand it backward. It is only when you stop and look to the rear that you see the corpse caught under your wheel.”
LISE MØRKVED HELSINGEN FØRSTEAMANUENSIS OG UNDERVISNINGSLEDER I KLOK ( KUNNSKAPSHÅNDTERING, LEDELSE OG KVALITETSFORBEDRING )
INSTITUTT FOR HELSE OG SAMFUNN, DET MEDISINSKE FAKULTET, UNIVERSITETET I OSLO
KORRESPONDANSE: LISEMHE @ MEDISIN.UIO.NO

Vi er ofte så fokusert på fremtiden at vi glemmer å reflektere over konsekvensene av handlingene våre.
En viktig lærdom fra Vergheses sitat er verdien av retrospektiv forståelse. Dette gir oss muligheten til å lære av våre feil, noe som er kritisk i kirurgi hvor små feil kan ha store konsekvenser. Ved å reflektere over erfaringer kan vi oppdage ”liket under hjulene” – de feilene vi overså. Gjennom forskning og forbedringsarbeid kan vi forstå og rette opp disse feilene. I flere av artiklene i dette nummeret av Kirurgen får vi eksempler på hvordan fravær av forskning kan føre til overvurdering av kirurgiens nytte og undervurdering av risikoene.
Selvfølgelig skal ikke alle kirurger vie livet sitt til forskning, det er verken nødvendig eller riktig bruk av kompetanse. Skal man lytte til HansOlov Adamis råd (som ofte er gode, men radikale), bør man unngå en aka
demisk karriere med mindre andre alternativer er komplett uattraktive!
Men, like fullt, bør leger ha en grunnleggende akademisk nysgjerrighet og kompetanse. Dette er nødvendig for å kunne vurdere faglitteratur kritisk, ta veloverveide beslutninger og drive kontinuerlig forbedring. – Med andre ord er det nødvendig for å kunne drive en kunnskapsbasert praksis og ivareta pasientsikkerheten. Det er dette som er kjernen i KLoKfaget (Kunnskapshåndtering, ledelse og kvalitetsforbedring) ved medisinstudiet i Oslo, som jeg for tiden vier mye av mitt liv til.
Dette standpunktet om en grunnleggende akademisk nysgjerrighet og kompetanse hos alle leger er ikke bare altruistisk fundert. Akademisk kompetanse rettferdiggjør vår profesjon. Tar vi ikke dette seriøst, risikerer vi å bli redusert til produksjonsarbeidere som bare følger protokoller uten å forstå dem. Hvis ikke vi ønsker at andre tar over må vi selv eie vårt fags kunnskapsproduksjon og forståelse.
Jeg håper årets siste nummer av Kirurgen inspirerer til refleksjon og engasjement for forskning, forskningsforståelse og kvalitetsarbeid. La oss fremme en kultur hvor forskning, forbedringsarbeid og klinisk praksis går hånd i hånd, til beste for både pasientene og samfunnet og vår egen profesjon.
Med ønske om en god jul og god lesning!
The Nordic countries have unique prerequisites to undertake cutting-edge surgical research, but this opportunity is underutilized. A limited set of strategic initiatives might improve the situation. Leaders in surgical research need a deep understanding of epidemiologic theory and should master a broad repertoire of study designs. Resources – human, financial and others – should focus on large, original studies with a high likelihood to improve clinical practice.
HANS - OLOV ADAMI
EMERITUS PROFESSOR AND FORMER CHAIR ( PREFEKT ) AT HARVARD UNIVERSITY AND KAROLINSKA INSTITUTET MEMBER OF THE SWEDISH ROYAL ACADEMY OF SCIENCES
KORRESPONDANSE: HANS - OLOV.ADAMI @ KI.SE
Clinicians often think of epidemiology as distinct from clinical research. As a consequence epidemiologic methods have been taught chiefly in epidemiology departments and at schools of public health. Many of these institutions, however, have become too isolated from the practice of medicine and the conduct of clinical research. And both camps – epidemiologic and clinical research –have suffered from this mutual isolation. Epidemiology would be fertilized by close interaction with clinical medicine, while offering clinical researchers a powerful toolbox derived from advanced methodologic developments. Epidemiologic principles and methods are not only integral to public health, but also highly relevant to clinical research. Still today, this fundamental fact is not adequately appreciated by many clinical researchers.
Could epidemiologic methods and clinical epidemiology indeed revolutionize clinical research? Would methodologic rigor, adequate sample size, and skilled statistical analyses allow more rapid progress and quicker implementation of important discoveries? This bold and perhaps naïve idea came to my mind some 40 years ago and
my initial hunch that it is true has grown ever since. Still a practicing surgeon at the time, my own research forced and encouraged some familiarity with the fundamental principles of epidemiology. And this familiarity truly changed my perspective on my professional performance in the operating room, clinical ward, outpatient departments, emergency units, and in the classroom where I lectured to medical students.
Foremost, my slowly growing familiarity with epidemiologic methodology helped me understand the fundamental prerequisites for causal inference – after all, a successful treatment is little more than a cause of good outcome. This insight made me increasingly uncertain about the real benefit of our therapeutic interventions and the performance of our diagnostic technologies. This was a time when hip replacement, coronary bypass surgery, breastconserving surgery, laparoscopic cholecystectomy, kidney transplantation, vascular reconstruction, radical prostatectomy and ESWL treatment for kidney stones (just to mention a few examples) transformed our work in the operating room – often without any support from randomized trials that these new technologies
added substantial benefits. At the same time, endoscopic examinations, computerized tomography, ultrasound, PET scans, and subsequently, magnetic resonance revolutionized our ability to visualize organs and assess bodily functions. Today, the flow of novel therapeutic and diagnostic techniques is even more intense.
As a surgeon I navigated through these years with two competing feelings. One was a growing frustration with how haphazardly clinical methods were used and combined; that novel surgical procedures – unlike the strictly regulated approval of new drugs – could be introduced overnight, often with no strategy to quantify risks and benefits. As a corollary, decisions influencing the life and health of our patients were based on little, if any, scientific evidence. But another feeling grew too – a fascination with epidemiologic theory and methodology as directly relevant to advancing the evidence base for clinical practice. After 17 years I left the operating room peacefully, permanently, and with no subsequent regret to become a fulltime epidemiologist.
Persuading clinicians that methods of extraordinary relevance for their research are readily available in the epidemiologic toolbox can be challenging. Trickier still 40 years ago was to find text that helps a surgical researcher see the light and opportunities. Today, however, an abundance of books has been published that predominantly deal with the theory of epidemiologic research whilst fewer accessible texts are available specifically about methods in clinical research. As a start, I would strongly recommend anyone who plans to undertake surgical research to familiarize themselves with at least one of the following books: “Epidemiology – An Introduction” by Kenneth J. Rothman and coauthors (1), or “Clinical Epidemiology: Principles, Methods, and Applications for Clinical Research” by Diederick E. Grobbee and Arno W. Hoes (2).
I wish that such texts had been available to me 40 years ago. I congratulate all those younger colleagues who now receive a firm and stable helping hand in their necessary endeavor to study a wide variety of clinical phenomena. And I hope that these books will also be read by the growing number of clinicians who also need to understand the sophisticated methods used in clinical research.
Although beyond the scope of this short appetizer, I can only encourage those contemplating to undertake cuttingedge research to dive into the literature to broaden their methodologic repertoire and deepen their understanding of the underlying theory. The reward will become lifelong in terms of improved research quality, greater flexibility in choosing the study design best aligned with your research hypotheses, and a deeper understanding of the best published research. For the purposes of this short introduction, I will focus on two fundamental areas of surgical research.
Unlike the predominant surgical research assessing outcome with and without therapeutic intervention, diagnostic research is crosssectional with no timedimension and confounding being of no relevance. As we all know, diagnosis of a disease is rarely based on a single test. Instead, the predominant sequence is history taking, clinical examination followed by laboratory and imaging tests. We also know that novel, technically sophisticated and often expensive diagnostic technologies are constantly added to our armament. Hence, the scientific challenge is rarely to assess the properties of one diagnostic test but instead the added value of one particular examination. To allow costeffective use of resources, the optimal order in which diagnostic technologies are used should also be investigated. This increasingly important area of research, hitherto largely neglected, should offer interesting opportunities in all surgical disciplines.
The outcome of diagnostic research is surprisingly simple because sensitivity and specificity captures all essential information about test performance. Positive and negative predictive value may add utility with one caveat: These measures depend entirely on disease prevalence among the patients under investigation which limits their generalizability. When diagnostic test results are continuous rather than dichotomous (a common situation) receiver operating characteristics (ROC) curves can be constructed. Such curves allow more nuanced interpretation based on different combinations of sensitivity and specificity. But they also complicate our task to unequivocally answer if a diagnostic test provides meaningful added value beyond what has already been achieved.
The main stray of research we are concerned with is whether surgical interventions improve patient outcomes, and if benefits outweigh harms. The relevant outcomes range from postoperative complications and reoperations to recurrence, quality of life, and death. But they all have one fundamental feature in common; persontime. To illustrate we could ask how many diseaserelated deaths would be expected if we followed a million operated patients for zero seconds. Conversely, how many deaths would be expected if we follow zero patients for one million years? The answer in both instances is, of course, zero. Neither people nor time alone provides adequate information about the outcome among patients, and must both be taken into account. Persontime is the sum of all the time contributed to a study by subjects at risk of outcome. As a corollary, the fundamental challenge in outcome research is to harvest causal information from a defined set of person-time.
The randomized control trial (RCT) remains the gold standard to maximize prerequisites for causal inference in outcome research. In such a study of adequate size, the randomized groups are balanced with regard to all extraneous factors that affect the outcome; the only difference is the intervention under study. Occasionally, clinically useful information can be generated through observational studies of patient cohorts (3). But even seemingly straightforward issues such as interpretation of trends in cancer patients’ survival may be surprisingly complex and uncertain (4). Nevertheless, many – if not the majority of – burning, unanswered clinical questions and related research hypothesis cannot be tested in RCTs because logistic, ethical and financial obstacles are unsurmountable. A surgical researcher would therefore be severely constrained if mastering only the theory of RCTs.
So far, my message has been that access to a broad methodologic repertoire is a sine qua non to harvest causal information from a defined set of persontime. To illustrate my point, let us work through an example. In inflammatory bowel disease (IBD), sulfasalazine has remained first line therapy for more than half a century. Because chronic inflammation might be a driver of malignant transformation and sulfasalazine has anti
inflammatory properties, it might reduce the excess risk of colorectal cancer in patients with IBD. The burning question is then how this plausible, clinically relevant but never tested, hypothesis can be investigated.
Consider first an RCT. Many thousand patients, preferably with newly diagnosed IBD would need to be randomized to receive or denied sulfasalazine, compliance with randomized assignment should be monitored and the incidence of colorectal cancer ascertained during several decades of followup. Such a trial would be both unethical, prohibitively expensive and nonfeasible. Would a cohort study be an alternative? Because the exposure of interest (treatment with sulfasalazine) is beyond the investigator’s control, information on treatment and numerous potential confounders must be prospectively recorded or abstracted from medical records. But only a small minority – definitely less than 5% of the patients with IBD will develop colorectal cancer, and to achieve adequate statistical power the cohort must encompass many thousand patients. The cohort study design is therefore highly inefficient and, in the end, not feasible.
One alternative remains, namely a casecontrol study nested in a large cohort of patients with IBD. This design preserves the validity of the underlying cohort study, provides largely similar statistical power but reduces the workload by almost two orders of magnitude. Cases are all patients with IBD diagnosed with colorectal cancer. Information about their use of sulfasalazine and relevant confounders is abstracted from medical records and compared with the same information in a properly selected sample of patients with IBD and no colorectal cancer. Based on this information, we can readily quantify any reduction in cancer risk attributable to treatment with sulfasalazine (5).
A cookbook prescription of the research process is beyond the scope of this short essay, but key elements are summarized in Box 1. In my experience, the first four components are often treated too haphazardly. Defining an original, clinically relevant and crystalclear hypothesis, is often a protracted process – and should be allowed to remain so. Likewise, discussion about study design deserves unlimited time and effort (6). Do not become surprised, let alone frustrated, if this initial pro
cess last for one or a few years. Decisions reflected and justified in the protocol might influence your scholarly work for many years, and you will never regret such an investment.
Regardless of how valid the design is, the study likely becomes uninformative if statistical power is inadequate. Far too many clinical studies are hopelessly underpowered. Further, enrollment into RCTs typically takes at least twice as long as predicted. Therefore, perseverance and close interaction with collaborators is profoundly important throughout the process of patient enrollment.
Finally, access to solid biostatistical support remains an Achille’s heal in many Nordic academic settings. Such expertise is nevertheless a must. In cuttingedge clinical research, advanced, sophisticated biostatistical analyses are indeed becoming common practice. As a first step, develop and adhere to a solid statistical analysis plan. And refrain from endless exploratory analyses that unavoidably generate significant findings due to play of chance. The majority of published research results never becomes confirmed by other independent investigators and an estimated 85% of research resources are wasted (7, 8). Hence, it should be our overarching responsibility as surgical researchers to not burden the scientific community with even more noise.
A FEW HUMBLE RECOMMENDATIONS
Prioritize
As a researcher, you work in a context that is brutally competitive, everexpanding, and global. Unless you get published, read, understood, believed, remembered, and cited you have likely worked in vain. Sadly, only a small minority of all published work achieve these fundamental goals. To merely expand your list of publications is after all a trivial and transient reward. Indeed, eons of time and Herculean efforts would be saved if we eliminated research that does not expand the realm of human knowledge, is never cited, and has zero impact on clinical practice. By all means protect yourself from becoming a big producer of small things.
Instead, remember that virtually everything remains to be discovered in clinical medicine with surgery as no exception. The future will be surprised how little we knew. All research findings are preliminary and research
1. Define precisely a testable hypothesis.
2. Develop in great detail a study design optimally aligned with the study hypothesis.
3. Define sample size based on realistic statistical power calculations.
4. Write and rewrite a detailed study protocol ultimately approved by all collaborators.
5. Apply for approval from all relevant ethical instances.
6. Obtain adequate funding to pursue the study without compromising validity or statistical power/sample size.
7. Design an optimal machinery for complete and timely enrollment of eligible patients.
8. Whenever appropriate, appoint an external advisory committee.
9. Devote continuous effort to foster perseverance, patience, and collaborative spirit.
10. Develop and pursue a statistical analysis plan.
11. Embrace unexpected findings.
12. Sort out authorship issues transparently and early, appoint first and senior author(s).
13. Design an inclusive and efficient mechanism for manuscript writing. And devote unlimited efforts to achieve linguistic quality and clarity.
14. Format your manuscript pedantically to accommodate all journal instructions. Submit your manuscript and keep your fingers crossed.
has no end. If you embrace these prerequisites, there can be no urgency in defining your research hypothesis. Read, ponder, and discuss with critical colleagues. In the end, choose a hypothesis that profoundly stimulates your curiosity, is feasible to investigate and has a realistic chance to influence clinical practice. And embrace the fact that you probably start a journey taking one decade and often longer.
Far too often, the research process and the joy of creative human interaction is poisoned by controversies on authorship. Admittedly, publications are the driving force for recognition, fame and academic promotion, perhaps even salary increase. Hence, it is not at all surprising that human greed comes into play. Nevertheless, authorship should be earned not bestowed. It often struck me that among those who argued loudly about their own presence or position in the author list, few, if any, became a partic
ularly successful scholar. These colleagues may win one battle or two but lose countless future opportunities because they become unattractive as collaborators.
Having said this, dealing with issues of authorship with fairness and justice is likely to become increasingly complex. Cuttingedge research will require more and more of large teams with investigators representing a variety of complementary expertise. How then can we navigate in this archipelago that becomes more and more complex? I can see no alternative to an open respectful discourse beginning early rather than late during the research process.
The pleasure of finding things out
Do not devote your short life to scholarly work unless other alternatives are deterrently unattractive. And choose your environment, supervisors, mentors, and collaborators carefully and critically; referees, publication records and funding situation often provides useful guidance. Remember that creativity requires freedom and tolerance. And do not dismiss unexpected findings; they may be more important than the expected ones and sometimes define the beginning of a journey towards a Nobel Prize! The purpose of science is not to confirm prej
udices. And foster all aspects of generosity: With ideas, support, resources, appreciation, and encouragement. If all these aspects are successfully considered, chances are good that from time to time you and your colleagues may enjoy the pleasure of finding things out (9).
Unlike experimental laboratory research – in which hypotheses may be tested and results unfold in a short timeperiod clinical research is predominantly a drawnout process. Fundamental discoveries that entail shifts in paradigm and clinical practice often require a series of studies or even lifelong efforts. Clinical investigators therefore need to adopt the ethos from the most successful basic researchers; do not give up after your first attack but refine, revise, or change your study hypothesis, perhaps also your study design. And keep digging until your treasure is found.
REFERANSER :
Se bakerst i nettutgaven på kirurgen.no
Kirurgen deler ut fire billetter til vitenskapelig skrivekurs hvor du kan lære fra redaktørene i de høyest rangerte internasjonale tidsskriftene! Kurset foregår 1617. juni 2025 i Oslo (se annonse side 194 i denne utgaven av Kirurgen). Redaksjonen i Kirurgen vil plukke ut de fire beste pasientkasuistikkene sendt oss innen 01.04.25 og vinnerartiklene vil bli publisert i Kirurgen 2/2025.
Følgende krav til pasientkasuistikken stilles:
• MAKSIMALT 1250 ord.
• Inntil 5 illustrasjoner (flytskjema, bilder, figurer og tabeller)
• Det må i artikkelen presiseres at pasienten har samtykket til publikasjon.
Artikkelen sendes tobias@kirurgen.no innen 01.04.2025
Legemidler er strengt regulert med hensyn til kvantifisering av positive behandlingseffekter, bivirkninger og komplikasjoner før godkjenning til klinisk bruk. For kirurgiske metoder er regelverket mindre gjennomarbeidet og systematisert. Det kan derfor være uklart når en kirurgisk metode; et nytt kirurgisk utstyr eller en ny måte å gjøre kirurgiske inngrep på, er «etablert» i forstand av at den kan og bør brukes i klinikken. Det finnes i dag ingen generelt akseptert konsensus for hva etablert behandling betyr innen kirurgi og beslektede fagområder. I denne artikkelen beskrives prinsippene som ligger til grunn for diskusjonene om når en behandling kan kalles etablert.
MICHAEL BRETTHAUER
PROFESSOR, INSTITUTT FOR KLINISK MEDISIN, UNIVERSITETET I OSLO
OVERLEGE OG SEKSJONSLEDER, AVDELING FOR TRANSPLANTASJONSMEDISIN, OSLO UNIVERSITETSSYKEHUS
ASSOCIATE EDITOR, ANNALS OF INTERNAL MEDICINE, PHILADELPHIA, USA
KORRESPONDANSE: MICHAEL.BRETTHAUER @ MEDISIN.UIO.NO
Medisinsk praksis fornyes kontinuerlig. Hva vi i dag anser som beste behandling eller beste diagnostiske metode kan være utdatert allerede neste uke. Det gjør medisin spennende og hverdagen interessant. Men det betyr også at vi som klinikere kontinuerlig må evaluere kunnskapen om behandlingene vi tilbyr og vurdere om nye behandlinger skal innføres eller ikke. Noen ganger lønner det seg å vente fordi sikker kunnskap om fordeler og ulemper er mangelfull, andre ganger kan vi bli beskyldt for å være altfor sent ute med behandlinger som for lengst er innført med påstått god effekt i «utlandet» (1).
UTPRØVENDE VERSUS EKSPERIMENTELL BEHANDLING
Internasjonalt skilles medisinske behandlinger og intervensjoner i «eksperimentelle» og «etablerte». I Norge har man innført en særregel som er ukjent i andre land. I for
bindelse med innføring av benmargstransplantasjoner ved Rikshospitalet på 1980tallet ble kategorien «eksperimentell» delt i to, nemlig «eksperimentell» og «utprøvende» (2). Denne underlige delingen fikk dessverre innpass i den såkalte prioriteringsforskriften da den kom i 2001 (3). Forskriften sier at «eksperimentell behandling er udokumentert behandling som ikke er ledd i kontrollerte undersøkelser, og hvor virkning, risiko og bivirkninger er ukjent eller ufullstendig klarlagt», mens «utprøvende behandling er behandling som utprøves som ledd i en vitenskapelig studie, men der kravene til fullverdig dokumentasjon i forhold til etablert behandling ennå ikke er tilfredsstillende» (3).
Nasjonalt råd for prioritering i helse og omsorgstjenesten (som ble avviklet i 2017) påpekte allerede i 2009 at det særnorske skillet mellom «eksperimentell» og «utprøvende»
“En kirurgisk behandling eller intervensjon regnes altså ikke som etablert bare fordi ett eller flere fagmiljøer starter å bruke den.”
er klinisk uhensiktsmessig og etisk ulogisk. Rådet skrev at forskriftsteksten er «til hinder for å synliggjøre overgangen mellom forskning og behandling» og vanskeliggjør at «ressursene i helsetjenesten brukes til godt dokumentert (med andre ord «etablert») behandling» (4). Rådet ba Helsedirektoratet om endring i forskriften, men teksten er uforandret i dag (3).
Mange er i dag enig med Prioriteringsrådet om at forskriften bør endres. Det er medisinsk, etisk og vitenskapelig logisk og riktig at uttrykket «eksperimentelt» på norsk oversettes med «utprøvende», fordi et eksperiment er en utprøving. Det finnes ingen logisk distinksjon mellom «eksperimentelt» og «utprøvende» og delingen er forvirrende og kontraproduktiv. I denne artikkelen brukes utrykket utprøvende.
EQUIPOISE
Begrepet «equipoise» er sentralt for å avgjøre om en kirurgisk behandling eller metode er etablert eller ikke. Equipoise betyr at det er usikkerhet om en ny behandling eller metode er bedre eller dårligere enn etablerte behandlinger (5). Equipoisebegrepet kan også brukes når to eller flere nye (utprøvende) behandlinger eller metoder sammenlignes. En vurdering av equipoise er avgjørende for å vurdere om det er etisk forsvarlig å kategorisere en behandling som etablert, og at den derved kan brukes i regulær klinisk praksis, eller om metoden er utprøvende og derved ikke bør tilbys pasienter utenfor kliniske studier (2). Equipoise er et internasjonalt begrep med franske og engelske røtter.
ETABLERT ELLER UTPRØVENDE - HVEM BESTEMMER?
I den offentlige helsetjenesten i Norge har pasienter rett til behandling eller helsehjelp når behandlingen har «forventet nytte» og ressursbruken står i rimelig forhold til nytten (3). Det betyr at pasienter kun har rett til de behandlinger eller intervensjoner som er blitt kategorisert som etablert. Behandlinger eller intervensjoner som ikke er kategorisert som etablerte bør kun tilbys innenfor kliniske studier som er godkjent av regional etisk komite (2).
«Nye metoder» er et nasjonalt system som overtok etter det tidligere Nasjonale rådet for prioritering i helse og omsorgstjenesten. Nye metoder eies av de regionale helseforetakene og har siden 2020 hatt ansvar for vurdering av innføring og utfasing av metoder i spesialisthelsetjenesten (6). En kirurgisk behandling eller intervensjon regnes altså ikke som etablert bare fordi ett eller flere fagmiljøer starter å bruke den. Det forekommer at det oppstår uenighet mellom fagmiljøer eller mellom et fagmiljø og etisk komite eller myndighetsorgan som Nye metoder eller lokale metodeutvalg. Et eksempel fra norsk kirurgi og hjertemedisin som skapte debatt i 2011 vises i boks 1.
Det som er klart, er at det ikke er det enkelte fagmiljøet ved et sykehus eller en avdeling som bør avgjøre om en behandling er etablert eller utprøvende. Denne avgjørelsen krever et systematisk litteratursøk og vurdering av kunnskapsgrunnlaget etter forhåndsdefinerte kriterier som oppfyller internasjonale krav til kunnskapsbasert medisin. Videre kreves det en transparent og tallfestet vurdering av fordeler og ulemper av behandlingen sammenlignet med alternativene som er etterprøvbar av andre. Det finnes gode norske læringsressurser for hvordan man gjør slike vurderinger (7). Medisinstudentene i Oslo og Tromsø har nå egne fag på studiet der de trener på systematisk vurdering av behandlinger og intervensjoner for å kunne anvende de når de blir klinikere.
TERSKELEN FOR ETABLERT BEHANDLING
Det vanskeligste med prosessen for å avgjøre om en kirurgisk behandling er etablert eller utprøvende er å finne terskelen mellom de to kategoriene. Med andre ord; når er kunnskapen god nok til å si at behandlingen er etablert og kan tilbys til alle?
Det finnes i dag ingen allment gyldig terskel for når en kirurgisk intervensjon eller behandling krysser grensen fra utprøvende til etablert. Det bør være vår ambisjon at de aller fleste kirurgiske metoder testes i godt designede randomiserte studier med pasientrelevante endepunkter. Dessverre gjelder dette få kirurgiske metoder som benyttes i dag.
BOKS 1: KATETERBASERT INNSETTING AV PULMONALKLAFF FOR BARN PÅ RIKSHOSPITALET I 2011.
ETABLERT ELLER UTPRØVENDE BEHANDLING?
I 2011 publiserte barnekardiologisk fagmiljø på Rikshospitalet resultater med kateterbasert innsetting av kunstig pulmonalklaff hos 10 barn med medfødt hjertefeil i Tidsskriftet (1). Fagmiljøet hadde ikke søkt etisk komite og pasientene hadde ikke samtykket som i en klinisk studie. Fagmiljøet innrømmet at behandlingen var ny og derved ikke etablert ved Rikshospitalet eller i Norge, men at den var blitt brukt i utlandet hos mer enn 1.000 pasienter og derved kunne anses som etablert (1).
Daværende leder for regional etisk komite og overlege ved Rikshospitalet Stein Evensen kritiserte fagmiljøet og mente at prosjektet brøt med viktige etiske prinsipper. Evensen påpekte at det fantes ingen randomiserte studier noe sted i verden som kartla fordeler og ulemper med innsetting av kunstig pulmonalklaff hos barn med medfødt hjertefeil og at kunnskapsgrunnlaget derfor var for svakt til at behandlingen kunne kalles etablert (2).
Tidsskriftets redaktører var enig med Evensen i at fagmiljøet på Rikshospitalet burde ha forespurt etisk komite før de startet å tilby behandlingen (3). Det
er de etiske komiteene som etter loven skal vurdere om en behandling er utprøvende og derved kommer innunder reglene i Helseforskningsloven, eller er etablert og derved kan tilbys utenfor en klinisk studie. Men redaktørene mente også at det finnes noen få nye behandlinger der man med bakgrunn i kunnskap generert utenom kliniske studier med stor sannsynlighet kan si at den nye behandlingen er bedre enn det man hadde før, og at man i disse tilfeller kan argumentere for at kliniske studier med kontrollgruppe er uetiske (4). Perkutan kateterbasert innsetting av kunstig pulmonalklaff hos barn med medfødt hjertefeil kunne etter redaksjonens vurdering være en slik metode.
1. Wyller VB, Aaberge L, Thaulow E et al. Perkutan kateterbasert innsetting av kunstig pulmonalklaff ved medfødt hjertefeil. Tidsskr Nor Legeforen 2011; 131: 128993.
2. Evensen S. Etikkvurdering ved innføring av ny behandling. Tidsskr Nor Legeforen 2011;131:1276
3. Bretthauer M, Haug C. Hva er etablert behandling? Tidsskr Nor Legeforen 2011;131:1275
“Når er kunnskapen god nok til å si at behandlingen er etablert og kan tilbys til alle?”
At slike studier er vanskelig og dyre å gjennomføres er ikke gode argumenter for å la være. Det er tross alt våre pasienter som må betale prisen når vi innfører noe som ikke er godt nok dokumentert og fører til mer pasientskade enn gagn. Det finnes flere eksempler innen kirurgi der det har vært tilfelle, for eksempel med brystimplantater som lakk eller hofteproteser som brakk (8,9). Ingen av dem var blitt testet i gode kliniske studier før de ble tatt i bruk som etablert behandling.
KONKLUSJON
En behandling er ikke etablert fordi et fagmiljø tar den i bruk. En god hovedregel er at metoder, instrumenter og teknikker som ikke er utprøvd grundig i kliniske studier, anses som utprøvende. Vi bør diskutere åpent og transparent når vi har nok kunnskap til å definere en kirurgisk behandling eller metode som etablert og klar til å tilbys alle.
REFERANSER : Se bakerst i nettutgaven på kirurgen.no
Helseforetakene skal fremme forskning, men dette nedprioriteres ofte til fordel for kortsiktig produktivitet. Produksjons- og markedskrav gjelder også i forskningen, noe som kan gi insentiver for juks som skader forskningens kvalitet og tillit og svekker helsevesenets grunnlag ytterligere. Både forskeren og institusjonene har ansvar for å motvirke dette. Institusjonene må gi opplæring i forskningsetikk og sørge for at forskningen kan gjennomføres i robuste miljøer med tilstrekkelig tid og ressurser, og forskningslederrollen må styrkes. Slik kan forskningen oppfylle normer for kvalitet og etikk og komme pasientene og samfunnet til gode.
OLE M. SEJERSTED OG MATHIS KORSEBERG STOKKE
INSTITUTT FOR EKSPERIMENTELL MEDISINSK FORSKNING, UNIVERSITETET I OSLO OG OSLO UNIVERSITETSSYKEHUS.
KORRESPONDANSE: OLE M. SEJERSTED - O.M.SEJERSTED @ MEDISIN.UIO.NO
HVA ER FORUTSETNINGENE FOR GOD FORSKNING?
Helseforetakene er lovpålagt å drive forskning, og god forskning er avgjørende for kvalitet i diagnostikk og behandling. Likevel er forskning ofte taperen i budsjettkampen og i den daglige driften fordi kravene til kortsiktig effektivitet og produksjon går foran tid til forskning.
Og forskning er en krevende aktivitet, fordi mye må være på plass for at gode forskningsprosjekter kan gjennomføres: Idé, spørsmålsstilling og hypotese må alle være gode, og forankret i eksisterende kunnskap. Ressurser, infrastruktur og godkjenninger må være på plass. Og ikke minst må man ha nok tid. Tradisjonelt har denne tiden blitt tatt fra klinikeres fritid, og selv om det har ført til mye bra er det ikke forenlig med dagens krav til kvalitet. Forskning kan ikke lenger være en enpersons virksomhet basert på offervilje. Forskeren må være del av en forskningsgruppe, med god kontakt til andre medarbeidere som kan veilede og støtte.
Slike robuste rammer for forskningen er også nødvendig for å sikre etterlevelse av forskningsetiske normer, nødvendig av hensyn til pasienter og samfunnet for øvrig. Brudd på forskningsetiske normer har store konsekvenser. Det ødelegger kvaliteten av forskningen, villeder andre forskere og fører til ødsling med samfunnets midler. Det svekker tilliten til forskere og forskningsresultater, og basisen for forbedringer i diagnostikk og behandling, samt grunnlaget for rasjonelle politiske valg. Det er altså all grunn til å sikre tid og ressurser slik at klinisk forskning kan utføres med integritet og i tråd med god etisk praksis.
Men hva er de anerkjente forskningsetiske normene og hvorfor kan man fristes til å bryte dem? I Norge har vi en forskningsetikklov som sier noe om hva som er normbrudd (§8) (1). De klassiske og velkjente normbruddene er fabrikkering, forfalskning og plagiering (FFP). Loven sier også at alvorlige brudd på andre anerkjente
forskningsetiske normer kan være uredelig. I proposisjonen til loven listes forhold som anses som alvorlige brudd på forskningsetiske normer (2) (s.35). Det omfatter blant annet urettmessig forfatterskap, inadekvat datalagring, destruering av datamateriale, selvplagiering, villedende bruk av statistikk, misvisende fremstilling av metode eller resultater med mer.
Det er imidlertid ikke slik at det bare er de alvorlige bruddene på forskningsetiske normer som forringer forskningen. En rekke mer eller mindre alvorlige brudd på normene kan også svekke kvaliteten. Det er en glidende skala fra slurv («er’e så nøye a?») til juks og de alvorlige bruddene. Har man jukset én gang er det lettere å jukse igjen. Hjernen tilpasser seg uærlighet, er det noen som påstår (3). Derfor er det viktig å være nøye med detaljene og ikke gå på akkord med kvalitet eller normer i noen faser av et forskningsprosjekt eller i en forskerkarriere.
All European Academies (ALLEA) har gitt ut en pamflett som nettopp er kommet i ny utgave (4). Det er en kortfattet og grei innføring i forskningsetikk som gjengir de grunnleggende forskningsetiske normene som det er lett å si seg enig i (Tabell 1). I Norge har De nasjonale forskningsetiske komiteene (FEK) lagt ned et betydelig arbeid med å utarbeide forskningsetiske retningslinjer som er lett tilgjengelige på nettet (5). Normene er utformet som overordnede prinsipper og etterlevelsen krever derfor at man bryter dem ned på et praktisk detaljnivå.
Det er for eksempel ikke nok å vite at man skal være ærlig (sannhetsnormen), det må integreres i den daglige arbeidsrutinen. I mer filosofisk språkdrakt omtales dette gjerne som dydsetikk som omhandler holdninger og karakter. For noen år siden ble det publisert en kommentar i Nature som illustrerer hvor viktig etikken er i den daglige forskningsvirksomheten (6). Vi har tillatt oss å gjengi forfatternes tabell over mulige fallgruver (Tabell 2) (6). Det er lett å kjenne seg igjen i flere av disse.
Forskningsetiske normer er ikke noe som er tredd ned over hodene på forskerne. Det er i stor grad normer som forskersamfunnet selv har utviklet gjennom flere hundre år. Det var imidlertid først på 1930tallet at sosiologen Robert F. Merton satte navn på disse normene. Han åpnet et stort forskningsfelt og har satt sitt sterke preg på dette (7). Forskernes selvjustis har altså vært helt sentral i utviklingen av forskningsetikken. Gjennom kollegial kritikk og fagfellevurderinger (som Merton kalte organisert skepsis) og etterstrebing av blant annet åpenhet (som Merton kalte kommunisme (sic!)) mener flere at det er demmet opp for mer utbredt juks. Det er imidlertid
Reliability in ensuring the quality of research, reflected in the design, methodology, analysis, and use of resources.
Honesty in developing, undertaking, reviewing, reporting, and communicating research in a transparent, fair, full, and unbiased way. Respect for colleagues, research participants, research subjects, society, ecosystems, cultural heritage, and the environment.
Accountability for the research from idea to publication, for its management and organisation, for training, supervision, and mentoring, and for its wider societal impacts.
Tabell 2 Fristelsene i forskningshverdagen.
Gjengitt med forfatterens tillatelse (6)
A TABLE OF TRAGEDIES
Nine common pitfalls
The factors that lead to bad decisions can be represented by the mnemonic TRAGEDIES. Here are some examples of each pitfall. Recognizing these and responding appropriately can save a career and strengthen science.
Temptation “Getting my name on this article would look really good on my CV.”
Rationalization “It’s only a few data points, and those runs were flawed anyway.”
Ambition “The better the story we can tell, the better a journal we can go for.”
Group and authority pressure
“The PI’s instructions don’t exactly match the protocol approved by the ethics review board, but she is the senior researcher.”
Entitlement “I’ve worked so hard on this, and I know this works, and I need to get this publication.”
Deception “I’m sure it would have turned out this way (if I had done it).”
Incrementalism “It’s only a single data point I’m excluding, and just this once.”
Embarrassment “I don’t want to look foolish for not knowing how to do this.”
Stupid systems “It counts more if we divide this manuscript into three submissions instead of just one.”
et spørsmål om forskersamfunnet i dag forvalter disse normene godt nok. Eller kanskje det er rettere å spørre om forskersamfunnet i dag har mulighet til å forvalte disse normene på en god nok måte. Dette kommenteres nedenfor.
Ifølge forskningsetikkloven er det ikke tilstrekkelig at det med klar sannsynlighetsovervekt foreligger et alvorlig brudd på forskningsetiske normer for at man kan kalle det uredelighet. Man må også vurdere det som kalles skyldkravet, altså om bruddet er begått med forsett eller ved grov uaktsomhet. Her har loven også lagt terskelen høyt. Skyldkravet kan være vanskelig å avgjøre og en som er anklaget for forskningsjuks vil ofte påberope seg at hen ikke har handlet uaktsomt, men bare slurvet. Det er imidlertid ingen unnskyldning – det er uaktsomt å slurve. For å sitere Store norske leksikon: «Uaktsomhet
er et rettslig begrep for uforsiktighet eller skjødesløshet» Blir det mye slurv kan det fort bli grovt uaktsomt. Det er viktig i forskningshverdagen å legge seg dette på sinnet. Slurv lønner seg ikke.
HVOR HYPPIG ER JUKS?
Ser man på utviklingen internasjonalt, står det dårlig til med hensyn til forskningsjuks. I den ekstreme enden av skalaen finner vi såkalte «paper mills» som produserer oppkonstruerte artikler på bestilling (8) og på nettet kan man kjøpe seg medforfatterskap (9). Rekordmange artikler trekkes tilbake, ofte fra de beste tidsskriftene (10). Det har dukket opp en flora av røvertidsskrifter hvor fagfellevurderingen i beste fall er kursorisk. Det kan være problematisk å orientere seg i denne jungelen, men i Norge gir Kanalregisteret oversikt over godkjente publiseringskanaler og en rangering av disse i nivåene 2, 1, 0 og x. Nivå 0 er ikke godkjent, og x er for tidsskrifter det er tvil om (11).
For norske forhold vil vi trekke fram en spørreundersøkelse blant 285 PhDstudenter i Oslo, Odense og Stockholm (12). I alt 10 % av studentene mente at forfalskning, fabrikkering og plagiat (FFP) var vanlig innen deres felt – altså de alvorligste bruddene på forskningsetiske normer. Nesten 30 % hadde satt inn en eller flere uberettiget(e) medforfattere og flere hadde opplevd påtrykk for å fremstille data på en misvisende måte. Svært få saker meldes imidlertid inn og behandles i Norge. Det kan tyde på en betydelig underrapportering.
HVORFOR ER DET NOEN SOM JUKSER?
Macchiarinisaken ved Karolinska Institutet (KI) illustrerer hvorfor enkelte forskere tyr til juks, og den ikke særlig høye barrieren for å kunne gjøre det. Macchiarini laget en trakea basert på et plastrammeverk og autologe stamceller som han kunne transplantere. Etter at flere pasienter døde ble det påvist betydelige feil i de eksperimentelle artiklene, og han ble dømt til 300 dager i fengsel av Svea Hovrätt (13). Berggren og Karabag bruker saken som eksempel og peker på normkonflikt som en sentral årsak til at forskere tyr til juks (14). Denne oppstår fordi kliniske forskere for det første må forholde seg til den klassiske medisinske etikken som springer ut av den hippokratiske ed, for det andre til et akademisk normsett og for det tredje til et markedsorientert normsett. For vår egen del vil vi dessuten legge til det forskningsetiske normsettet fra ALLEA. Dessuten vil vi hevde at det akademiske normsettet har to komponenter: ett knyttet til kvalitetskrav og ett knyttet til kollegiale forventninger i tråd med Mertons arbeid. Vi har altså å gjøre med medisinsketiske normer, markedsorienterte normer, forskingsetiske normer, kva
litetsnormer og kollegiale normer. Over det hele troner den lovfestede akademiske friheten og idealet om kunnskap for kunnskapens skyld. Vi er enige med Berggren og Karabag i at det må bli et motstridende normgrunnlag for forskningsarbeid av dette!
Om vi skal fremheve en faktor som bidrar spesielt i dagens forskningsvirkelighet er det den markedsorienterte logikken som preger akademisk virksomhet. Det gjelder å publisere mest mulig fortest mulig. Doktorgradsarbeid skal gjennomføres på tre år, mens forskerne som overlever i akademia deretter må skaffe mest mulig eksterne midler og ta ut flest mulig patenter. Denne effektivitetslogikken er ikke urimelig i seg selv og fremmes ofte av politikere og instanser utenfor forskningsinstitusjonene med den begrunnelse at man vil ha noe igjen for skattebetalernes penger. Kravene strider imidlertid ofte med kollegiale normer som åpenhet, allmenngyldighet, ingen personlige interesser og kritisk diskusjon, og kvalitetsnormer som originalitet, faglig forankring, adekvat metode, etterprøvbarhet, samarbeid og veiledning. Å følge slike normer krever imidlertid tid og ressurser. Og med de etiske normene på toppen er det vanskelig å se hvordan alt skal oppfylles. Macchiarinisaken viser likevel at å kompromisse på et av forskningens grunnleggende normsett kan bære galt av sted. Den enkelte forskeren kan åpenbart ikke stå alene om å håndtere dette.
HVEM HAR ANSVARET FOR Å SIKRE FORSKNINGSKVALITETEN?
Universitets og høyskoleloven sier i § 35 at utdanningen skal kvalitetssikres (15), men ikke noe om forskningen. I forbindelse med Macchiarinisaken peker Berggren og Karabag på fragmentert kontroll som en medvirkende årsak (14). Den tradisjonelle kontrollinstansen er intern diskurs og fagfellevurderinger. Denne ser imidlertid ut til å ofres på produktivitetens alter. Den akademiske friheten gir også institusjonene liten eller ingen kontrollmulighet, og mye av ansvaret for kvalitetssikring ligger i praksis hos prosjektleder. Prosjektledere er som regel seniorforskere som har mange roller og ofte ansvar som fagfelle eller redaktør i tidsskrifter. Dermed tillegges disse også et betydelig kvalitetssikringsansvar som ligger utenfor institusjonene. Finansieringsinstitusjonene spiller en tilsvarende rolle gjennom forvaltning av forskningsmidler. Vi kunne nevnt flere instanser, men poenget er her at ansvaret for kvalitetssikring er fragmentert, hvilket gjør det enkelt å navigere utenom «kontrollpunktene» for den som ønsker å jukse.
KAN VI FORBYGGE JUKS I FORSKNING?
Hovedansvaret for juks vil alltid ligge hos den enkelte
forsker, men det er institusjonens ansvar å sørge for at det skal være vanskelig å jukse og at trangen til eller ønsket om å jukse ikke dukker opp. Forskningsetikkloven gjør det klart at forskningsinstitusjonene har et systemansvar for å undervise i forskningsetikk og sikre at forskerne har den nødvendige kompetanse (§5) (1). Dette betyr at lovgiver anser manglende kunnskap og kompetanse som en mulig årsak til juks. På tross av kunnskapen vil det imidlertid alltid være noen som fristes til juks, og ansvaret til institusjonene går derfor langt ut over opplæring. Innen klinisk forskning sørger bestemmelsene i Helseforskningsloven for at forskningsprosessen må følge etiske normer og personvern slik at juks er betydelig vanskeliggjort (16).
Den viktigste forebyggingen skjer imidlertid når etiske normer læres i praksis og integreres. Den sentrale personen er igjen prosjektlederen. Vedkommende fungerer også som mentor og veileder og det er nettopp i mestersvenn relasjonen at normoverføring skjer. Prosjektleder er en viktig rollefigur og skal være et eksempel for sine medarbeidere (17).
En annen rolle mange prosjektledere har er å være leder for en forskningsgruppe. Ved Oslo universitetssykehus kreves det at alle som driver forskning skal tilhøre en forskningsgruppe (18). Gruppen skal ha ansvar for intern diskurs og kvalitetssikring, og forskningsleder skal «sørge for at forskningsgruppens medlemmer er kjent med nasjonale og internasjonale regelverk (eks. Vancouver‐reglene, helseforskningsloven, forskingsetikkloven etc.) og interne retningslinjer, prosedyrer, e-læringskurs og meldesystemer for hendelser i forskning. Dette endrer ikke prosjektleders eller prosjektmedarbeideres/forskeres selvstendige ansvar iht. helseforskningsloven og forskningsetikkloven eller linjens forskningsansvar definert i internt kvalitetssystem.»
Det er et systemansvar å sørge for at en forskningsleder kan fylle rollen på en god måte. I universitets og høgskolesystemet er dessuten retten til akademisk frihet koblet til ansvar og etter forskningsetikkloven (§4) til en aktsomhetsplikt. Å styrke rollen som prosjektleder – ikke gjennom å fjerne ansvar, men å tydeliggjøre det – er derfor den beste kvalitetssikring av forskningen og det beste vern mot juks.
HVA GJØR MAN
HVIS
MAN HAR
MISTANKE
OM AT NOEN JUKSER ELLER HAR JUKSET?
Saker hvor man mistenker juks skal fremmes direkte til den aktuelle institusjonens redelighetsutvalg. Hvem som helst kan gjøre det, også anonymt. Mange utvalg
har opprettet egne hjemmesider med lenke til skjema for melding av saker. Alle institusjoner har plikt til å ha et redelighetsutvalg ifølge Forskningsetikkloven (1), men flere kan gå sammen om å etablere et felles utvalg. I saker hvor det foreligger mistanke om alvorlig brudd på forskningsetiske normer skal utvalgene vurdere 1. om det foreligger uredelighet, 2. om det foreligger systemfeil og 3. om angjeldende arbeid skal trekkes tilbake eller ikke. Utvalgene er faglig uavhengige og rapporterer ikke i linjen, deres uttalelser kan ikke overprøves og skal ikke godkjennes av institusjonen. Det er viktig å si at uredelighetssaker i utgangspunktet ikke er personalsaker, ei heller varslingssaker etter arbeidsmiljøloven, og institusjonen kan ikke bestemme hvilke saker som skal til utvalgene. Utvalgene skal på sin side ikke uttale seg noe om mulige sanksjoner eller personalmessige konsekvenser av uttalelsene de kommer med. Det er opp til institusjonen hvordan de følger opp utvalgenes uttalelser. Utvalgene kan avvise saker hvis det er åpenbart at det f.eks. dreier seg om en personalsak eller at det mangler saklig grunnlag. Krangel om for eksempel medforfatterskap er i utgangspunktet ikke et alvorlig brudd på forskningsetiske normer og bør løses i linjen. Faglig uenighet er heller ikke brudd på forskningsetiske normer, snarere tvert imot (jamfør Mertons krav om diskurs). Flere institusjoner har etablert en ordning med forskningsombud som ofte vil være rett adresse for slike spørsmål. Ofte vil ledere i linjen likevel være involvert når spørsmål om mulig uredelighet dukker opp, og det kan være riktig at ledelsen bidrar til at saken belyses på best mulig måte før den sendes til redelighetsutvalget. Det er imidlertid viktig at det bare er et redelighetsutvalg som kan konkludere med at det foreligger uredelighet.
Etikk er en sentral del av god forskningspraksis, spesielt i medisin. Brudd på etiske normer kan undergrave forskningens kvalitet og samfunnets tillit. God forskning krever tid, ressurser og en solid etisk forankring for å sikre pålitelighet og unngå fristelser til juks. Forskningsinstitusjoner må sørge for nødvendige ressurser og opplæring for å forhindre juks. Samtidig må man hindre at forskere tar dårlige moralske valg i en situasjon hvor publiseringspress og andre forventninger er høye. Ansvaret for å opprettholde forskningsintegritet ligger både hos individuelle forskere og institusjonene de arbeider for.
REFERANSER : Se bakerst i nettutgaven på kirurgen.no
«Åh, så du har fått litt mer plager etter at vi opererte! Da setter vi litt av det vi skar bort tilbake.»
«Ikke blitt helt frisk, sier du? Da tar vi bort litt mer»
Mange medisiner kan titreres opp eller ned ut ifra virkning og bivirkning, men satt på spissen er kirurgien binær. Enten skjærer vi eller så skjærer vi ikke. Vi titrerer ikke operasjoner.
RUNE BRUHN JAKOBSEN
ORTOPEDISK KLINIKK, AKERSHUS UNIVERSITETSSYKEHUS OG UNIVERSITETET I OSLO
KORRESPONDANSE: R.B.JAKOBSEN @ MEDISIN.UIO.NO
Når vi som kirurger har bestemt oss for å operere, er vi nødt til å legge tvilen til side for faktisk å gjøre jobben. I mine øyne er det både det fine og, noen ganger, det fryktelige ved yrket vi har valgt.
Nettopp fordi kirurgien til slutt må være enteneller, eller svarthvitt om du vil, kan det være lett å bli svarthvitt i tilnærmingen til valgene vi gjør. Kan hende dette er en mestringsstrategi som gjør at vi kan gå hjem etter dagen, trygge(re) på at vi har gjort det riktige. Men det er også en fare fordi vi kan gå fra enkeltpasient til enkeltpasient uten å se det større bildet.
Her ligger kjernen i hvorfor det å delta i forskning er viktig for kirurger. Selv om den erfaringsbaserte kunnskapen vi opparbeider oss over tid er en sentral del av kunnskapsbasert praksis, er historien full av eksempler på at vi kan bli lurt. Uten forskning lar vi oss forlede til å
overvurdere behovet for og nytten av kirurgi for en lang rekke problemstillinger, og ikke helt uvesentlig også undervurdere risikoen (13).
Innen ortopedien har det blitt veldig tydelig der narrekirurgi er brukt i randomiserte kliniske studier av blant annet artroskopisk meniskkirurgi. I disse studiene er det ingen tvil om at pasientene faktisk blir bedre etter å ha blitt operert, men dessverre ikke vesentlig bedre enn de som har fått utført narrekirurgi (3). Hadde ingen tatt seg bryet med å gjennomføre slike studier, hadde vi ortopeder trolig fortsatt med å fjerne degenerative menisker i «trygg» forvissning om at det var til det beste og helt nødvendig: Pasienten blir jo bedre. Andre gode eksempler fra de senere årene er randomiserte studier på akillesseneskader og hamstringskader (4, 5). Vi har lenge visst at det går an å behandle slike skader både med og uten operasjon, men vi har manglet randomiserte studier som
“Du går glipp av mye om du aldri er involvert i forskning”
kvantifiserer fordeler og ulemper. Når slike studier først gjennomføres, endrer de nesten over natten retningslinjer for behandling. Ikke nødvendigvis på en slik måte at ingen lenger skal opereres, men «synsingen» om fordeler og ulemper ved behandlingsalternativene kan erstattes av fakta. Det er slike randomiserte kliniske studier som bidrar til den forskningsbaserte kunnskapen vi kirurger trenger for å balansere, eller nyansere, vår erfaringsbaserte kunnskap.
Å delta i forskning kan være så mangt, men i alle tilfeller må det ligge en nysgjerrighet til grunn og en villighet til å se kritisk på alt vi gjør: Er det faktisk slik at denne måten å gjøre det på er bedre enn denne? Går det som vi tror med våre pasienter? Går det like bra for dem vi behandler som for dem andre behandler for samme sykdom?
Noen ganger betyr dette å delta i store sammenlignende multisenterstudier. Andre ganger betyr dette innovasjonsstudier med utvikling av helt nye behandlingsmetoder. For de fleste av oss innebærer forskning å inkludere pasienter i nasjonale eller lokale kvalitetsregistre.
All forskning handler i bunn og grunn om å forsøke på en transparent, etterprøvbar og systematisk måte å svare på spørsmålene som våre pasienter har: Hvilke behandlingsalternativer har jeg? Hva er fordelene og ulempene for meg? Hvor sannsynlig er det at jeg får fordelene og ikke ulempene, og motsatt? Det er ikke tilfeldig at dette er nettopp kjernespørsmålene i samvalg innen kunnskapsbasert praksis: Pasientene må kunne forvente å få svar på disse spørsmålene og bli tatt med på beslutningen (6).
Men å delta i forskning tar tid, tid som kirurger bør bruke til å bli dyktigere til å operere, vil du kanskje innvende. Og det har du rett i. Forskning tar tid. Det er diskusjo
ner, planlegging, protokollskriving, skriving av søknader om penger og søknader om etisk godkjenning, personvernombudsvurderinger, innhenting av samtykker og nitid registrering av utfallsmål. Til tider kan dette være frustrerende, men likevel helt nødvendig.
Som kirurg skal du jobbe et langt liv og min påstand er at du går glipp av mye om du aldri er involvert i forskning i det hele tatt. Du går glipp av diskusjonene med andre forskere om hvordan vi på best mulig måte kan få svar på det vi lurer på: Gjør vi det riktige? Er det nye bedre enn det gamle? Vet vi hva pasientene vil foretrekke? Du går glipp av møter med en perlerekke av flinke folk som kan ha helt andre innfallsvinkler til det du lurer på. Det være seg kollegaer i eget fagfelt i innland og utland, men også statistikere, helseøkonomer og forskningskoordinatorer. I et langt klinisk liv er også forskning et «frirom» med autonomi og tid til refleksjon som gir inspirasjon og ny giv til det kliniske arbeide hvor det alltid er en «neste oppgave» som helst allerede skulle vært gjort.
Å ha vært involvert i forskning gir deg nesten automatisk en mer kritisk tilnærming når ny kunnskap presenteres, fordi du vet hva som må til for å innhente data, analysere og tolke dem, og du vet at all forskning har styrker og svakheter. Og med på kjøpet får du en dypere innsikt i hvor mye av det vi gjør som kirurger som vi ikke helt sikkert vet er det riktige. Det gjør deg til en litt mindre svarthvitt kirurg – og det er en god ting.
REFERANSER
: Se bakerst i nettutgaven på kirurgen.no
Kvalitetsforbedring vekker fort assosiasjoner til prosjekter som kommer ovenfra, som man ikke forstår, og som i en travel klinisk hverdag føles som en ekstra belastning. Medisinstudenter ved Universitetet i Oslo som har faget KLoK (Kunnskapshåndtering, ledelse og kvalitetsforbedring) melder om at de ikke helt får tak på hva kvalitetsforbedring er. Har kvalitetsforbedring et forklaringsproblem for sin egen eksistens?
SIRI ENGEBRETSEN
SEKSJON FOR BRYST- OG ENDOKRINKIRURGI, OUS
SCOTTISH QUALITY AND SAFETY ( SQS ) FELLOW
KORRESPONDANSE: ENGSIR @ OUS - HF.NO
Selv kjenner jeg meg igjen i skepsisen til kvalitetsforbedring. Nå, etter å ha fullført en utdannelse i kvalitetsforbedring i det prestisjefylte programmet SQSF i Skottland (Scottish Quality and Safety Fellowship), har jeg fått ny innsikt. Om lag 40 leger i Norge har gjennomført denne utdannelsen. Flere har sagt at de så verden med nye øyne etter å ha tatt utdannelsen i Skottland, og jeg er enig. Der jeg før hørte kollegaers «klaging» på smått og stort, hører jeg nå mulighet for forbedring. Og det beste er; man vet
hvordan man kan gå frem! Kunnskap om kvalitetsforbedring og kvalitetsforbedringsmetodikk gir håp om at det er mulig å få til endring og forbedring i vårt komplekse system og i vår travle kliniske hverdag.
Alle er for kvalitetsforbedring. Det motsatte ville vært rart. Og poenget med det hele ligger i navnet: øke kvaliteten. Når vi snakker om kvalitetsforbedring i helsetjenesten, mener vi likevel ikke bare at noe har fått høyere


FIGUR 2: PDSA-syklusen. Modell for planlegging og gjennomføring av et kvalitetsforbedringsprosjekt (1) (trykket med tillatelse fra Helsedirektoratet)
kvalitet. Det sentrale er prosessen for å komme dit. Ved bruk av etablerte verktøy og målinger kan vi vise at en forbedring har funnet sted. Som med alt annet som er nytt, trengs det både kunnskap og trening for å få det til, og gjerne støtte fra noen med erfaring. Heldigvis er metodikken enkel og lett tilgjengelig. Likevel tar det litt tid å få taket på hva det hele handler om og hvordan det kan brukes.
Den enkleste måten å si hva kvalitetsforbedring kan brukes til, er alt. Alt i helsetjenesten vår kan forbedres og det overordnede målet er økt kvalitet i alle ledd. Ikke bare for pasientene, men også for oss ansatte. Et godt utgangspunkt for et kvalitetsforbedringsprosjekt er noe en selv er engasjert i eller frustrert over. Et viktig aspekt er muligheten til å påvirke egen arbeidshverdag. Ofte er det de små prosjektene som blir vellykkede og der man får til endringer som utgjør en forskjell.
Eksemplene på vellykkede kvalitetsforbedringsprosjekter er mange og varierte. Enhver kirurg kjenner til WHO´s Surgical Safety Checklist. Dette er et godt eksempel på et forholdsvis enkelt prosjekt med stor gjennomslagskraft og utbredelse. Selv liker jeg å trekke frem to veldig ulike prosjekter fra kollegaer jeg har møtt i Skottland. Det ene ble initiert av en dansk kardiolog som var frustrert over den lange ventetiden for elektrokonvertering ved
atrieflimmer. Ved å identifisere, analysere og adressere årsakene til den lange ventetiden, ble den redusert fra tre uker til null dager. Det andre eksempelet er fra en skotsk gastrokirurg som gjeninnførte vaskbare operasjonsfrakker. Ikke bare er de bra for miljøet, men flere av kirurgene synes de gir bedre beskyttelse (mens noen synes de er varme). Begge prosjektene er eksempler på endring til forbedring der legenes eget engasjement har vært utgangspunktet.
Det finnes mange kvalitetsforbedringsverktøy til ulik bruk. Jeg foreslår her en liten startpakke som er mer enn nok ved et mindre prosjekt.
Utgangspunktet i et kvalitetsforbedringsprosjekt er et problem man ønsker å gjøre noe med. Kanskje må man bruke litt tid på å finne ut hva det egentlige problemet er. Det er lurt å snakke med kollegaer. Det kan være overraskende hvor ulikt vi ser på ulike problemstillinger. Målet i prosjektet beskrives som hva man ønsker å oppnå innen hvilken tid. Det er også greit å ha et lite team av kollegaer rundt seg som støtter opp om prosjektet, samt god forankring hos leder. Trinnene som er naturlig å følge, er illustrert i figur 1.
Når problemet er godt definert, kan man gå videre ved å bruke PDSAsirkelen (Plan Do Study Act) (figur 2).
Dette er et kraftfullt verktøy i all sin enkelhet. Vi kjenner alle til løsningsforslag som blir besluttet rundt et bord, men som viser seg ikke å fungere i praksis. Det er nemlig vanskelig å finne en god løsning på et problem bare ved å snakke sammen. PDSA løser dette. Hovedpoenget er å prøve ut idéen i liten skala, for eksempel på noen få pasienter eller i en kort tidsperiode. Dette er enkelt og innenfor de rammene man allerede har. Etter første testsyklus evalueres det i kollegiet og man gjør justeringer før man prøver ut på ny. Når man har gjennomgått flere testsykluser og systemet fungerer, kan det implementeres. Dersom idéen viser seg å ikke fungere, implementeres den ikkeuten at altfor mye ressurser og tid er brukt. Gjennom en slik prosess får man med seg alle kollegaer til å bidra med tilbakemeldinger, selv de som er skeptiske.
I kvalitetsforbedring må man kunne vise til en positiv endring. I større prosjekter viser man gjerne til store datamaterialer og endring i disse etter testing av forbedringsidéen, for eksempel data knyttet til ventetid for pasientene. I de mindre prosjektene kan «tommel opp» fra kollegiet eller et enkelt spørreskjema duge. Dette er resultatindikatorer. Man bør også være obs på balanserende indikatorer, altså negative konsekvenser av prosjektet. For å vise resultatene, er det vanlig å benytte statistisk prosesskontroll.
Inneholder kvalitetsforbedringsprosjektet flere ulike forslag, er det nyttig å sette opp et driverdiagram. Dette holder oversikten over prosjektet og er et nyttig verktøy for å kommunisere til omgivelsene hva man ønsker å oppnå. Det gjør det også lettere å selge inn prosjektet til ledelsen og kollegaer.
Har du et problem du ønsker å gjøre noe med, er det veldig nyttig å kalle det et kvalitetsforbedringsprosjekt og ta
i bruk kvalitetsforbedringsmetodikken. Bare ved å brukebegrepet kan dører åpnes. Det er lettere for en leder å støtte opp om et kvalitetsforbedringsprosjekt som er godt definert, enn å følge opp løse idéer. Kvalitetsforbedring i helsetjenesten har til og med sin egen forskrift: Forskrift om ledelse og kvalitetsforbedring i helse og omsorgstjenesten.
Det er per i dag utvilsomt et behov for økt kunnskap om kvalitetsforbedring. Mange tiltak gjøres for å få til dette. Medisinstudenter lærer om kvalitetsforbedring under studiet. Studenter ved UiO har i oppgave å planlegge et kvalitetsforbedringsprosjekt ut fra reelle problemstillinger de møter i klinikken. I nåværende LISutdanning skal LIS gjennomføre sitt eget prosjekt. Med andre ord vil vi se en økning i kvalitetsforbedringsprosjekter i årene som kommer. Jeg tror at gjennom økt kunnskap om hva kvalitetsforbedring er og hvordan den brukes, vil flere få taket på metodikken slik at det blir en naturlig del av måten vi jobber på.
Så til slutt, er kvalitetsforbedring The missing link for kirurger? Jeg tror det! Kirurger er kreative og vant til å finne løsninger på operasjonssalen. Med litt drahjelp fra etablert kunnskap om kvalitetsforbedring kan kreativiteten og problemløsningen få en større plass også i resten av arbeidshverdagen vår. For mens forskning kan endre selve faget vårt, kan kvalitetsforbedring endre måten vi jobber på!
REFERANSER :
1. Forbedringsguiden. Teorier, tips og verktøy for forbedringsarbeid i helse- og omsorgstjenesten. Itryggehender 24-7. Tilgjengelig fra: www.itryggehender24-7.no/ kvalitetsforbedring/forbedringsarbeid/her-kan-du-laste-ned-forbedringsguiden
Finn ressurspersoner innenfor kvalitetsforbedring i ditt helseforetak og ta en prat om problemet du ønsker løst!
Sjekk ut hva som finnes av ressurser i helseforetaket ditt, flere steder er det egne elæringskurs i kvalitetsforbedring
Sjekk ut: itryggehender24-7.no

Hør på podcasten
“Design ditt eget liv” i “Burde vært pensum” på NRK radio


POWERSEAL Sealer and Divider
POWERSEAL was designed to become the best-in-class advanced bipolar technology that delivers consistently strong vessel sealing performance throughout the procedure.
Experience True Benefits During Surgery:
Superior haemostasis
Best-in-class dissection
Enhanced usability
For more information please visit our website or follow us
www.olympus.eu/POWERSEAL



Stor forskning kan også gjøres på små sykehus, men kommer ikke av seg selv. Sørlandet sykehus har jobbet målrettet med forskningskultur i mer enn 20 år. Forskning er en av fire lovpålagte oppgaver for helseforetakene i tillegg til behandling, utdanning og pasient- og pårørendeopplæring. Regjeringen Solberg utarbeidet en nasjonal handlingsplan for kliniske studier for perioden 20212025. Målet er hårete og gjelder alle foretak, også utenfor universitetsbyene: Klinisk forskning skal være en integrert del av all pasientbehandling og innen 2025 skal antall kliniske studier dobles (1). Figur 1 viser at vi er langt fra målet.
ØYVIND HOLME
FORSKNINGSSJEF, SØRLANDET SYKEHUS HF KORRESPONDANSE: OYVIND.HOLME @ SSHF.NO
PASIENTER NYTER GODT AV FORSKNING
PÅ SMÅ SYKEHUS
Forskning er åpenbart viktig for pasienten. Deltakelse i kliniske studier gir pasienten mulighet for å få ny og utprøvende behandling, før den er kommersielt tilgjengelig. Noen ganger kan dette være livreddende. Det er viktig med en desentralisering av slike studier. Når vi kan tilby lokal deltakelse, kan pasientene slippe ulempen ved å reise til andre sykehus, og vi kan oppnå målet om redusert ulikhet i helsetilbud mellom sykehus og regioner. Oppfølgingen i kliniske studier kan også være hyppigere og bedre enn det som er standard behandling, og pasientene kan føle seg ekstra godt ivaretatt. For pasientene kan studiedeltakelse også ha en altruistisk dimensjon; man gjør noe for senere pasienter i samme situasjon.
FORSKNING GIR FORDELER FOR SYKEHUSET
Også den kliniske avdelingen nyter godt av å delta i kliniske studier. Man er med i forskningsfronten, forskningskompetansen hos personellet som er involvert i studiene øker og interessen for videre forskning blir for
håpentligvis større. Avdelinger med forskningsaktivitet vil være en attraktiv arbeidsplass for de med akademiske ambisjoner. Ikke minst i den vanskelige rekrutteringssituasjonen vi har i dag, er dette et viktig signal til jobbsøkere til de mindre sykehusene. Forskning kan føre til at vi finner mer effektive måter å bruke ressurser på, som igjen kan få direkte innvirkning på avdelingens drift. På mindre sykehus kan det være kortere veg mellom forskningsresultater og implementering. I tillegg kan helseforetakene spare store summer på høykostmedisiner. I en masteroppgave som undersøkte kliniske studier med høykostmedisiner ved Ahus, kom det frem at sykehuset sparte 1,8 millioner kroner i gjennomsnitt for hver studie de deltok i (2).
FORSKNING PÅ SØRLANDET SYKEHUS
For å øke forskningsaktiviteten har sykehusene rigget seg forskjellig, og hvor stor del av driftsbudsjettet som brukes til forskning varierer. De fleste helseforetak har etter hvert fått egne forskningsenheter som gir administrativ og praktisk støtte, og de har også en kontrollfunksjon
med forskning i egen institusjon. Utvikling i antall publikasjoner har vært jevnt stigende de siste årene og reflekterer økt fokus på forskning og villighet til å bruke interne midler.
Sørlandet sykehus har et opptaksområde på omlag 310 000 personer og har en dekningsgrad på pasientbehandling på over 90%. Dette innebærer at vi behandler og følger opp de aller fleste pasientene selv og har en stor nok populasjon til å forske på behandling og oppfølging av alle vanlige sykdommer. Pasient og praksisnær forskning er hovedregelen. Ved å forske på vanlige sykdommer vi ser i klinisk praksis, kan vi designe studier som er tilpasset lokalbefolkningens behov og sykdomspanorama og helseforetakets utfordringer. Veien fra forskning til implementering kan også tenkes å være kortere når resultater er generert lokalt.
Siden 2004 har Sørlandet sykehus hatt egen forskningsenhet. Vi har åtte heltidsansatte som gir administrativ og praktisk støtte i alle deler av forskningsprosessen. Sykehusledelsen støtter godt opp om visjonen om å drive forskning som kan endre klinisk praksis, og årlig lyses det ut interne midler til inntil fem ph.dprosjekter. Hvert år disputerer mellom fem og ti av våre ansatte (figur 3). Sykehuset har nå besluttet å bevilge interne midler også til forskere etter oppnådd doktorgrad. Målet er å få en solid stamme av erfarne forskere som både kan drive yngre forskere fram og som finner at Sørlandet sykehus er en attraktiv arbeidsplass som verdsetter forskningskompetansen de har opparbeidet seg.
Forskningspoliklinikker blir opprettet på stadig flere sykehus. Disse har svært varierende utforming på sykehusene, men det viktigste innholdet er studiesykepleierne. På Sørlandet sykehus har vi hatt god erfaring i mange år med dedikerte studiesykepleiere ved Senter for kreftbehandling. Etter hvert som aktiviteten har tatt seg opp, har vi nå fire heltidsansatte sykepleiere. Terskelen for å delta i kliniske studier blir lavere for legene, og ikke minst får studiesykepleierne et fagmiljø for økt kompetanse, erfaringsutveksling og muliggjør opplæring av kollegaer på andre avdelinger.
TRUSLER MOT ØKT FORSKNINGSAKTIVITET
Vi opplever flere trusler mot økt forskningsaktivitet, og sannsynligvis er ikke dette unikt for Sørlandet sykehus. Den viktigste er mangel på tid. Som aktiv forsker på et lokalsykehus de siste femten årene har undertegnede
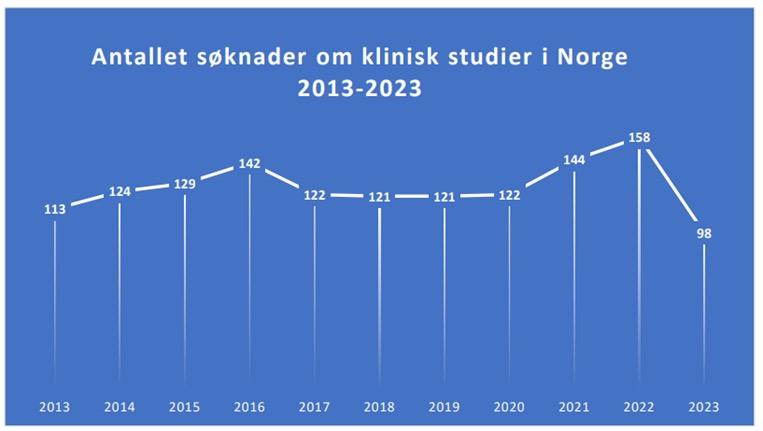
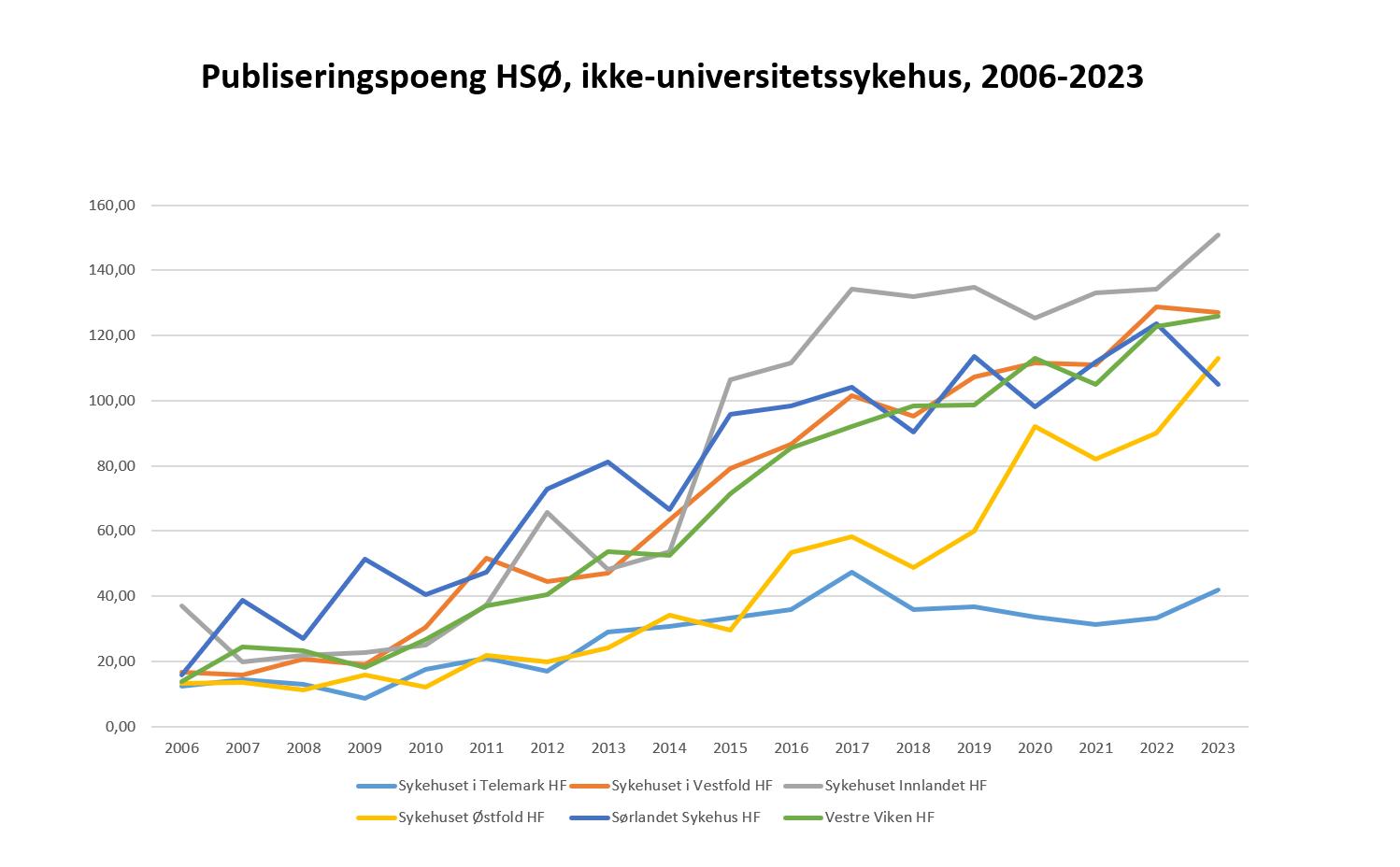
2: Publikasjonspoeng ved ikke-universitetssykehus i Helse SørØst i perioden 2006-2023.
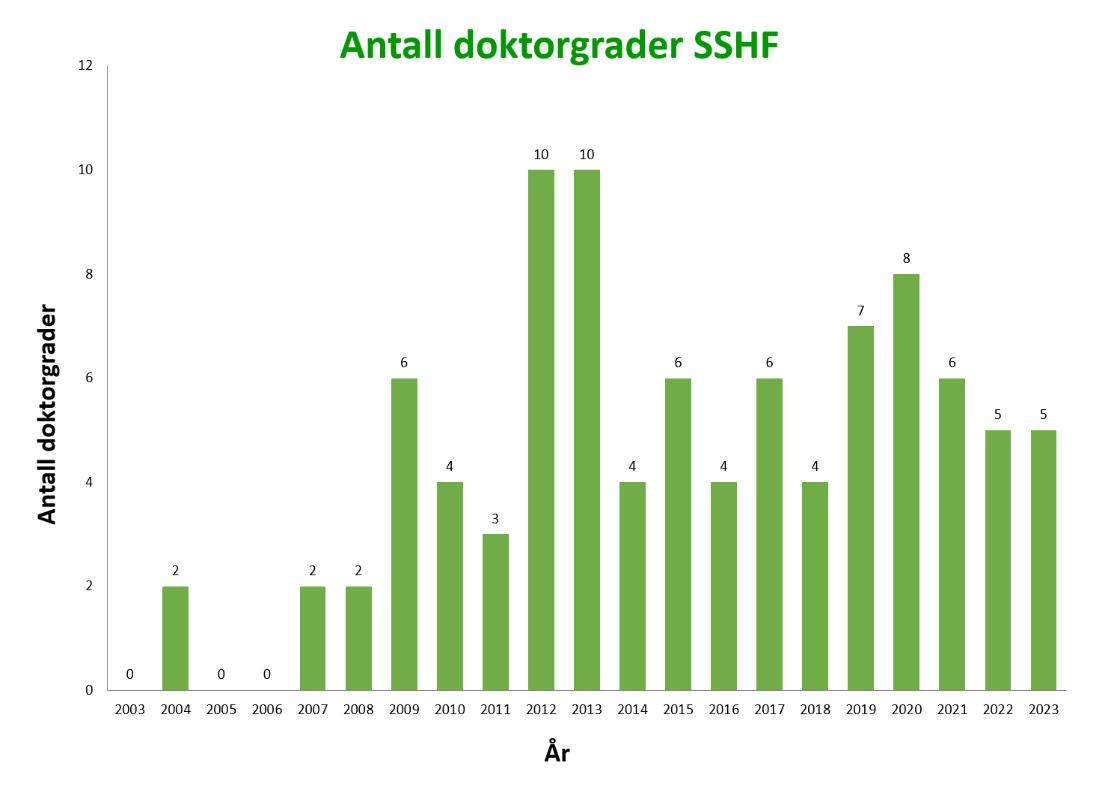
3: Antall ansatte ved Sørlandet sykehus som har disputert i perioden 2010-2023.
“På mindre sykehus kan det være kortere veg mellom forskningsresultater og implementering”
merket det økende trykket på drift og produksjon. Mens vi for femten år siden kunne drive klinisk forskning uten frikjøpt tid er ikke dette mulig i dag. Vi er helt avhengig av dedikert tid til forskning innenfor vanlig arbeidstid, både for oss selv og for studiesykepleiere som blir stadig viktigere når vi driver kliniske studier.
For å drive forskning er vi avhengig av lederstøtte. Øverste leder har et ansvar for at det drives forskning på foretaket og kan gi viktige signaler nedover, blant annet ved å prioritere forskning i sykehusets budsjett. Like viktig er støtten fra forskerens nærmeste leder. Erfaringen fra vårt sykehus viser at avdelinger som har prioritert forskning over tid, har utviklet aktive forskningsmiljøer. Dette krever imidlertid tålmodighet fra lederens side samt gode evner til å prioritere i budsjettet og finne fleksible løsninger. Vi merker etter hvert god støtte for legegruppen fra nærmeste leder, mens sykepleierne møter større utfordringer i sin linje. Årsakene til denne forskjellen er ikke helt klare, men kan ha sammenheng med tradisjoner. En annen forklaring kan være at mange sykepleiere ikke driver egen forskning, men fungerer som studiesykepleiere i kliniske studier. Kanskje blir denne innsatsen vurdert annerledes, til tross for at den er avgjørende for studienes gjennomføring. Avdelingsledere kan oppleve studiesykepleiere som en utgift på avdelingens budsjett, men med økende forskningsaktivitet vil også inntektene øke. Forskning må gjøres i et langtidsperspektiv, og man må tåle økte kostnader i starten. På Akershus universitetssykehus har omfattende satsing på studiesykepleiere gitt gode resultater (3).
Antall kliniske studier i Norge er dalende (figur 1). Årsaken er ikke klar, men det ser ikke ut til at regjerningens målsetning om en dobling av antall kliniske studier innen 2025 vil bli nådd. Vi opplever stor konkurranse mellom land, men også mellom sykehusene i Norge. En stor pasientpopulasjon (les: universitetssykehusene) er
åpenbart mer attraktiv når den farmasøytiske industrien skal finne samarbeidspartnere for sine studier.
Universitetssykehusene og lokalsykehusene konkurrerer om de samme forskningsmidlene. Sterke forskningsmiljøer i universitetsbyene har større mulighet for å få tilslag på sine søknader og kan være en trussel for forskningsaktiviteten på mindre sykehus. Dessverre er potten som prioriteres til ikkeuniversitetssykehusene i de regionale utlysningene så liten at den er uten betydning (4). Derfor er vi avhengig av at de mindre sykehusene prioriterer egne midler til forskning.
Videre opplever også vi den generelle personellutfordringen i helsevesenet. Selv med ekstern finansiering og dedikerte forskere, kan det være vanskelig for underbemannede avdelingsledere å finne en erstatning for kliniker som skal frikjøpes. Det kan være utfordrende for gjenværende helsepersonell å godta at man må arbeide mer for at en kollega skal følge forskerdrømmen. At forskere bidrar til å dekke vakter i høytid og ferier kan bøte på noe av dette og er en nødvendig og innarbeidet praksis på vårt sykehus.
KONKLUSJON
Det drives mye god pasientnær forskning utenfor universitetssykehusene. Forskning er lovpålagt og tidkrevende, og krever at ledere forstår at de må så før de kan høste. Tid er forskningens viktigste mangelvare og må skjermes fra drift. Forskningssykepleiere er gull verdt og bør prioriteres.
REFERANSER :
Se bakerst i nettutgaven på kirurgen.no

For behandling av voksne pasienter med fremskreden hormonsensitiv prostatakreft2
ADT= Androgen Deprivation Therapy



Referanser: 1. Shore ND, et al. N Engl J Med. 2020;382(4):2187–2196. 2. Preparatomtale Orgovyx (relugoliks), seksjon 4.1 og 5.1. www.felleskatalogen.no.
Dette legemidlet er underlagt særlig overvåking. Orgovyx (relugoliks) 120 mg filmdrasjerte tabletter, ATC-nr.: L02BX04, Reseptgruppe: C. Reseptbelagt. Indikasjon: Indikasjon: Behandling av voksne pasienter med fremskreden hormonsensitiv prostatakreft. Dosering og administrasjonsmåte: Behandling med Orgovyx skal startes og overvåkes av spesialleger med erfaring innen medisinsk behandling av prostatakreft. Behandling med Orgovyx skal innledes med en startdose på 360 mg (tre tabletter) på den første dagen, etterfulgt av en dose på 120 mg (én tablett) som tas én gang daglig på omtrent samme tid hver dag. Orgovyx kan tas med eller uten mat. Tablettene bør tas med litt væske etter behov, og skal svelges hele. Kontraindikasjoner: Overfølsomhet for innholdsstoffene. Advarsler og forsiktighetsregler: Androgen deprivasjonsterapi kan forlenge QT-intervallet. Hos pasienter med en historie med eller risikofaktorer for QT-forlengelse samt hos pasienter som samtidig får legemidler som kan forlenge QT-intervallet, må man nøye evaluere samtidig bruk av Orgovyx med legemidler kjent for å forlenge QT-intervallet, eller legemidler som kan indusere torsades de pointes, slik som klasse IA (f.eks. kinidin, disopyramid) eller klasse III (f.eks. amiodaron, sotalol, dofetilid, ibutilid) antiarytmika, metadon, moksifloksacin, antipsykotika osv. Hjerte- og karsykdom slik som myokardinfarkt og slag har blitt rapportert for pasienter som fikk androgen deprivasjonsterapi. Derfor bør alle risikofaktorer for hjerte- og karsykdom tas med i beregningen. Redusert beintetthet kan forekomme. Redusert bentetthet, hos pasienter med ytterligere risikofaktorer, kan føre til osteoporose og økt risiko for benfraktur. Overvåkning av leverfunksjon hos pasienter med kjent eller mistenkt leversykdom er tilrådelig under behandling, da det er observert lette forbigående økninger i ALAT og ASAT. Forsiktighet ved alvorlig nedsatt nyrefunksjon. Eksponeringen for relugoliks hos pasienter med alvorlig nedsatt nyrefunksjon kan være økt med opptil 2 ganger Det må utvises forsiktighet hos pasienter med alvorlig nedsatt nyrefunksjon ved administrasjon av en 120 mg dose med relugoliks én gang daglig. Effekten av Orgovyx skal overvåkes via kliniske parametere og nivåer av prostataspesifikt antigen (PSA) i serum. Interaksjoner: P-gp-hemmere: Samtidig administrasjon av Orgovyx og orale P-gp-hemmere anbefales ikke. Legemidler som er orale P-gp-hemmere inkluderer visse legemidler mot infeksjon (f.eks. azitromycin, erytromycin, klaritromycin, gentamicin, tetracyklin), antimykotika (ketokonazol, itrakonazol), antihypertensiva (f.eks. karvedilol, verapamil), antiarytmika (f.eks. amiodaron, dronedaron, propafenon, kinidin), antianginale legemidler (f.eks. ranolazin), cyklosporin, humant immunsviktvirus (hiv)- eller hepatitt C-virus (HCV)-proteasehemmere (f.eks. ritonavir, telaprevir). Hvis samtidig administrasjon med orale P-gp-hemmere én eller to ganger daglig er nødvendig, skal Orgovyx tas først og den orale P-gp-hemmeren tas 6 timer senere, og pasientene skal overvåkes hyppigere for bivirkninger. Alternativt kan behandling med Orgovyx avbrytes i opptil 2 uker for en kort behandlingsperiode med en P-gp-hemmer. Hvis behandling med Orgovyx avbrytes i mer enn 7 dager, skal administrasjon av Orgovyx gjenopptas med en startdose på 360 mg på den første dagen etterfulgt av 120 mg én gang daglig. Kombinert P-gp- og sterk CYP3A-induktor: Samtidig administrasjon av Orgovyx med kombinert P-gp- og sterk CYP3A-induktor anbefales ikke. Legemidler som er kombinerte P-gp- og sterke CYP3A4-induktorer inkluderer den androgene reseptorinduktoren apalutamid, visse antikonvulsiva (f.eks. karbamazepin, fenytoin, fenobarbital), legemidler mot infeksjon (f.eks. rifampicin, rifabutin), johannesurt (Hypericum perforatum), hiv- eller HCV-proteaseinduktorer (f.eks. ritonavir) og ikke-nukleoside reverstranskriptaseinduktorer (f.eks. efavirenz). Hvis samtidig administrasjon er nødvendig, skal Orgovyx-dosen økes. Etter seponering av den kombinerte P-gp- og sterke CYP3A-induktoren skal den anbefalte dosen Orgovyx gjenopptas én gang daglig. Fertilitet, graviditet og amming: Legemidlet er ikke indisert for kvinner i fertil alder. Det skal ikke brukes hos kvinner som er eller kan være gravide eller som ammer. Bivirkninger: Noen mindre vanlige bivirkninger kan være alvorlige, og lege kontaktes umiddelbart dersom symptomer på urtikaria eller angioødem utvikles (kan forekomme hos opptil 1 av 100 personer). De vanligste bivirkningene under behandling med relugoliks er fysiologiske effekter av testosteronsuppresjon, inkludert hetetokter (54 %), muskel- og skjelettsmerter (30 %) og fatigue (26 %). Andre svært vanlige bivirkninger inkluderer diaré og forstoppelse (12 % hver). Svært vanlige: Karsykdommer: hetetokter. Gastrointestinale sykdommer: diaréa, forstoppelse. Sykdommer i muskler, bindevev og skjelett: muskel- og skjelettsmerter. Generelle lidelser og reaksjoner på administrasjonsstedet: fatigue. Vanlige: Sykdommer i blod og lymfatiske organer: anemi. Endokrine sykdommer: gynekomasti. Psykiatriske lidelser: insomni, depresjon. Nevrologiske sykdommer: svimmelhet, hodepine. Gastrointestinale sykdommer: kvalme. Hud- og underhudssykdommer: hyperhidrose, utslett. Lidelser i kjønnsorganer og brystsykdommer: redusert libido. Undersøkelser: vektøkning, økt glukosed, økt triglyseridd, økt blodkolesterol. Mindre vanlige: Hudog underhudssykdommer: urtikaria, angioødem. Sykdommer i muskler, bindevev og skjelett: osteoporose/osteopeni. Undersøkelser: økt aspartataminotransferase økt alaninaminotransferase. Sjeldne: Hjertesykdommer: myokardinfarkt. Ikke kjent frekvens: Hjertesykdommer: forlenget QT-tid. Pakningsstørrelser og pris: Orgovyx Filmdrasjert tablett, 120 mg: 30 stk. flaske: 1674,6 kr. Blå resept: Blå resept: Ja. Refusjonsberettiget bruk: Behandling av avansert hormonavhengig prostatakreft. Refusjonskoder: ICPC Y77: Ondartet svulst i prostata. ICD C61 Ondartet svulst i blærehalskjertel. Vilkår 9: Behandlingen skal være instituert i sykehus, sykehuspolklinikk eller av spesialist i vedkommande disiplin. Basert på SPC godkjent av DMP/EMA: 07/2024. Innehaver av markedsføringstillatelse: Accord Healthcare S.L.U., World Trade Center, Moll de Barcelona, s/n, Edifici Est 6ª planta, 08039 Barcelona, Spania. Tel: +34 93 301 00 64. Les preparatomtale (SPC) for ytterligere informasjon, se www. felleskatalogen.no NO-Onc-Org-01414
Vitenskapelige artikler er hjørnestenen i forskning. Men vitenskapelige artikler er ikke sannhet. De er i beste fall et tid- og stedbundet øyeblikksbilde, og i verste fall et vrengebilde. Derfor må vi som leger være i stand til å lese dem kritisk. Det krever som alt annet kunnskap og trening. Her får du noen tips til hvordan du kan trene.
ARE BREAN
TIDSSKRIFT FOR DEN NORSKE LEGEFORENING
KORRESPONDANSE: ARE.BREAN @ TIDSSKRIFTET.NO
Å lese forskning er noe annet enn å lese OM forskning, slik som når vi leser en lærebok eller en nyhetsartikkel. Der leser vi oftest teksten kronologisk, fra begynnelse til slutt. En vitenskapelig artikkel bør du derimot helst ikke lese kronologisk, og du bør legge merke til andre ting enn i andre typer tekster. Denne teksten skal ta deg gjennom denne måten å lese på, og forhåpentlig sette deg bedre i stand til å forstå, evaluere og huske vitenskapelige artikler. Men før vi kommer så langt, må vi innom noen spørsmål du bør stille deg selv før du går løs på artikkelen du velger.
HVORFOR?
Det første du bør spørre deg selv, er hvorfor du har lyst til å lese en vitenskapelig artikkel om ditt valgte tema: Er det fordi du er nysgjerrig på det aller siste innen et tema du kjenner godt, er det for å sette deg inn i et ukjent tema, er det for å forberede en internundervisning eller et foredrag, eller er det for å planlegge din egen forskning? Hva du skal bruke artikkelen til har mye å si for hva slags artikkel du bør velge, og hvordan du bør tilnærme deg den.
HVA SLAGS TIDSSKRIFT?
Veldig forenklet kan man dele vitenskapelige tidsskrifter inn i to typer: Den ene, og vanligste, er spesialtidsskriftene. Disse dekker oftest et ganske smalt faglig område. I slike tidsskrifter dominerer de vitenskapelige artiklene,
som regel originalartikler, men også oversiktsartikler og noen ganger kasuistikker. Den andre typen er de generelle medisinske tidsskriftene. Vårt eget tidsskrift, Tidsskrift for Den norske legeforening, er et slikt tidsskrift. Andre eksempler er British Medical Journal (BMJ) og The Lancet. Det finnes også generelle tidsskrifter som dekker mange vitenskapsgrener. Eksempler på det er Science og Nature.
De vitenskapelige artiklene er bærebjelken også i slike tidsskrifter. Men i tillegg finner du debattartikler, lederartikler, nyhetsartikler og mer featurepreget stoff. I en slags mellomposisjon står de noe bredere spesialtidsskriftene. Det er tidsskrifter som ofte dekker en hel spesialitet eller et helt organ. Slike tidsskrifter kan også ha debattstoff, lederartikler og av og til også mer nyhetspregede artikler.
Som leser er det viktig å vite om disse forskjellene mellom tidsskrifter. Det er fordi de ulike artikkeltypene har ulik funksjon, er strukturert ulikt og er ment for ulike formål. Leser du i for eksempel BMJ at ”halvparten av alle briter har forhøyet blodtrykk”, utgjør det en stor forskjell for tyngden av utsagnet om du leste det i en polemisk debattartikkel, eller i en originalartikkel som undersøkte nettopp blodtrykksnivået hos et stort og representativt utvalg briter.
HVILKET TIDSSKRIFT?
Man regner med at det finnes 40 00050 000 vitenskapelige tidsskrifter i verden (1). Økningen har vært enorm de siste tiårene. Samtidig har nye publiseringsmodeller kommet med noen bivirkninger som du som leser må være klar over.
Den viktigste bivirkningen er røvertidsskriftene: Heldigitale tidsskrifter som ser imponerende ut, men som i realiteten ikke foretar særlig (om noen) kvalitetssikring av innholdet (2). Det antas at så mange som 15 000, eller enda flere, vitenskapelige tidsskrifter er røvertidsskrifter (3). Mye av det som publiseres i disse tidsskriftene er jukseforskning. En studie fant at opptil 24% av alle artikler som publiseres innen medisin, enten er kopiert direkte fra andre eller bare er juks og oppspinn (4). Hvordan kan du da som leser vite hvilke tidsskrifter som er ordentlige?
Det viktigste er å være bevisst på hvor du søker etter artikler. Store søkedatabaser, hvorav den viktigste innen medisin er PubMed, har en grundig kvalitetssjekk av tidsskriftene de indekserer. Artikler du finner ved søk i PubMed skal (i alle fall i teorien) derfor være publisert i seriøse tidsskrifter. Andre kilder for å finne tidsskrifter av (i teorien) god kvalitet er Directory of Open Access Journals (DOAJ) (5) og det norske Kanalregisteret (6). Og husk at du kan bruke dette også omvendt: Om du snubler over en artikkel du lurer på om er publisert i et ordentlig tidsskrift, kan du sjekke om tidsskriftet befinner seg i en (eller helst flere) av disse tre kildene.
Tradisjonelt har man også brukt et tidsskrifts impaktfaktor for å vurdere dets kvalitet. Impaktfaktoren er et tall som uttrykker hvor ofte en gjennomsnittlig artikkel i tidsskriftet blir referert til av andre. Det er mye, og berettiget, kritikk av å bruke impaktfaktor for å rangere tidsskrifter. Dels er dette målet lett å manipulere. Dels er det jo egentlig ikke tidsskriftets kvalitet vi er mest interessert i, men den enkelte artikkelens kvalitet. Det sier ikke impaktfaktor noe om. Likevel: Stort sett kan du stole på at et tidsskrift med høy impaktfaktor publiserer artikler som er grundig redaksjonelt kvalitetssjekket og fagfellevurdert.
HVILKEN ARTIKKEL?
Slik jeg nevnte over, er det viktig å være klar over at ulike artikkeltyper (sjangere) er ulike og fyller ulike formål. En original forskningsartikkel presenterer nye data og forfatternes tolkning av disse. En oversiktsartikkel oppsummerer forskningen som allerede finnes innen et felt
eller en problemstilling. En kasuistikk eller en kasusserie presenterer en eller flere enkelthistorier. Og en metodeartikkel kan presentere en ny teknikk eller et nytt verktøy. Dette er bare noen få eksempler på de mange ulike artikkeltypene som finnes. Hver av dem har sine styrker, svakheter og spesifikke bruksområder for deg som leser. En metodeartikkel vil som regel peke fremover (”Se, her er noe nytt!”). En oversiktsartikkel peker i sin natur bakover (”Dette er det som allerede har blitt publisert om temaet”). Og en originalartikkel finner sammenhenger som er forsøksvis sanne for en gitt populasjon på et gitt sted til en gitt tid – og så må nye studier og senere oversiktsartikler si noe om hvorvidt disse sammenhengene er gyldige også for andre populasjoner, steder og tider.
Tenk deg en omfattende og utfyllende oversiktsartikkel om koronavirus fra for eksempel 2018, så forstår du sikkert hvor viktig det er å huske på at en vitenskapelig artikkel aldri presenterer en evig ”sannhet”, men alltid bare et øyeblikksbilde.
”Hva slags artikkel er det jeg har foran meg nå, og når er den skrevet?”, er derfor det første spørsmålet du må besvare før du går i gang med selve lesningen. Ulike artikkeltyper krever deretter ulike tilnærminger. I det følgende skal vi i hovedsak konsentrere oss om den tradisjonelle, kvantitative kliniske originalartikkelen.
HVORDAN BEGYNNE?
Det aller første du bør begynne med er tittelen. Noen tidsskrifter liker deskriptive titler (”Kirurgi ved rotatorcuffruptur – en randomisert kontrollert studie”). Andre tidsskrifter foretrekker spørrende titler (”Er kirurgi nyttig ved rotatorcuffruptur?”). Men vær på vakt for de konklusive titlene (”Kirurgi er nyttig ved rotatorcuffruptur”). Slike titler gir løfte om en ekstern validitet (at resultatene er gyldige også for andre enn de som deltok i studien) det som regel ikke er grunnlag for. Er tittelen konklusiv bør du være litt ekstra på vakt allerede før du har begynt å lese.
Legg så merke til forfatterlisten. En originalartikkel har nesten alltid flere forfattere. Det gjenspeiler at original forskning er en arbeids og tidskrevende affære som krever flere typer ekspertise. Ved å se på affiliasjonene (institusjonstilhørighetene) til forfatterne får du vite om artikkelen springer ut fra ett eller flere forskningsmiljøer, og om studien sannsynligvis er nasjonal eller multinasjonal. I den medisinske tradisjonen er den som står først på for

fatterlisten som oftest den som har gjort mesteparten av arbeidet, mens sisteforfatteren er gruppens senior – den med høyest rang innad i forskergruppen.
FORSTÅ STRUKTUREN
Vitenskapelige originalartikler er rigid strukturerte. Dette er dels for å sikre at all informasjon leseren trenger er kommet med, og dels er det for at denne informasjonen skal være rask og enkel å finne.
I en standard klinisk originalartikkel benyttes den såkalte IMRADstrukturen: Introduction, Methods, Results And Discussion (figur 1). I noen tidsskrifter kalles introduksjonsdelen for Bakgrunn (Background), og diskusjonsdelen kan etterfølges av en konklusjon (Conclusion). Du vil i tillegg finne at enkelte tidsskrifter har en hel haug med underavsnitt – Annals of Internal Medicine har eksempelvis 1011 ulike avsnittsoverskrifter bare i artikkelsammendraget! Når du ser nærmere etter vil du likevel som regel finne at den enkle IMRADstrukturen gjemmer seg bak selv de mest kompliserte artikkelstrukturer.
I de fleste tidsskrifter er artikkelsammendraget (abstrakt) strukturert på samme måte som selve artikkelteksten (det vi kaller ”brødteksten”). Det gjør det lett for deg som leser å hoppe frem og tilbake mellom avsnittene.
HVA BØR DU LESE FØRST?
Noen liker å lese introduksjonsavsnittet først, både for å få den bredere sammenhengen bak studien (jamfør forrige avsnitt) og for å se studiens formål eller forskningsspørsmål. Det gir deg bakgrunn for å vurdere om metoden som er valgt er hensiktsmessig for å besvare spørsmålet. Andre, som undertegnede, liker å lese sammendraget (abstrakt) først. Der får man en rask innføring i de viktigste aspektene av studien, før man går løs på detaljene. Dette er smak og behag, og etter å ha pløyd gjennom en del artikler, finner du raskt din egen foretrukne startmåte.
FIGURER OG TABELLER
FIGUR 1: IMRAD-strukturen:
En mal for hvordan en vitenskapelig artikkel kan bygges opp.
Uansett bør du ganske tidlig se gjennom alle figurer og tabeller. En gyllen regel er at disse skal inneholde nok informasjon til å kunne leses og forstås uavhengig av artikkelen. Ved å lese dem, danner du deg raskt et inntrykk av studiens viktigste resultater, som du deretter kan få utdypet ved å lese mer i brødteksten.
Figurer og tabeller fyller litt ulike funksjoner. En god figur har som regel bare ett budskap (for eksempel at to fenomener samvarierer, eller at et fenomen går opp eller ned over tid). Svært gode figurer kan av og til ha to, en helt sjelden gang tre, slike budskap. Men uansett skal du kunne forstå budskapet i figuren bare ved å kaste et blikk på den.
Tabeller kommer i hovedsak i to varianter. En demonstrasjonstabell har, i likhet med en figur, et budskap. Det foreligger et mønster, en utvikling eller en regelmessighet som du lett kan skjønne ved å studere tallene i tabellen. En referansetabell, derimot, viser frem data som gir bakgrunn for noen av studiens resultater, men som ikke nødvendigvis kan forstås uten ytterligere databearbeiding. Referansetabeller kan av og til være svært store. Noen ganger foreligger de kun som appendix (av og til kalt Supplementary files) til artikkelen.
METODEAVSNITTET
Forskningsspørsmålet du leste i innledningsavsnittet får du bruk for nå. For her i metodeavsnittet skal metoden forskerne har valgt beskrives. Da bør du spørre deg selv: Er denne metoden egnet til å besvare forskningsspørsmålet? Her er fallgruvene mange. En av de vanligste er å ønske å undersøke en kausalitet (fører X til Y?), men så velge en metode som bare kan gi et assosiativt svar (X og Y forekommer sammen eller følger etter hverandre i tid).
Metodeavsnittet skal inneholde nok informasjon til at du skjønner helt nøyaktig hvordan forskerne har gått frem.
“Det antas at så mange som 15 000, eller enda flere, vitenskapelige tidsskrifter er røvertidsskrifter”
Ideelt sett skal du her få nok informasjon til at du selv kan gjenta studien. Et godt tips er å tegne gangen i studieforløpet på et ark mens du leser. Da identifiserer du fort om det er huller i fremstillingen.
I metodeavsnittet skal du også få informasjon om hvilke statistiske beregninger som er gjort, og med hvilke verktøy. Informasjon om nødvendige etiske og personvernmessige tillatelser skal stå her. Det samme skal informasjon om studieregistrering, noe som er obligatorisk for alle kliniske studier. Mangler noe av dette, bør du være på vakt.
RESULTATENE
Før du kommer så langt, vet du nå allerede mye om resultatene, siden du har sett gjennom figurer og tabeller. Når du leser resultatavsnittet bør du derfor konsentrere deg om informasjon som gir en pekepinn om resultatenes gyldighet: Er utvalgsstørrelsen tilstrekkelig stor? Er utvalget representativt for populasjonen som undersøkes? Er det gjort signifikanstesting, og i så fall; gis det konfidensintervaller eller andre spredningsmål? Der det er gjort avanserte statistiske beregninger er det vanskelig å vurdere disse uten å selv ha mye statistisk kompetanse. Er du i tvil, og det er viktig nok: Spør en kollega som kan mer! Husk også at statistisk signifikans langt fra er det samme som klinisk signifikans. Spør deg selv om forskjellen mellom gruppene er stor nok til å gi klinisk mening. I kliniske studier er det ofte viktigere enn statistisk signifikans. Og til slutt: Svarer resultatene på forskningsspørsmålene? Dette fikk du en pekepinn om allerede i metodeavsnittet, men resultatene er selve vannprøven på om forskningsdesignet var riktig for å få svaret på spørsmålet som ble stilt.
DISKUSJONEN
Ofte starter diskusjonsdelen med en kort oppsummering av resultatene, før forfatterne gir sin vurdering av hva resultatene betyr. Er du enig med dem, eller kan du se
andre måter å tolke resultatene på? En god diskusjonsdel skal peke tydelig på studiens svakheter og styrker. Her kan du få se hvor selvkritiske forskerne er. Høy grad av selvkritikk betyr at de har hatt evnen til å tre litt tilbake og betrakte sin egen studie på avstand. Det inngir tillitt. En diskusjonsdel uten slik ”selvpisking” er et dårlig omen for kvaliteten av hele studien.
Etter dette kommer ofte en form for konklusjon. Vær på vakt mot forfattere som overtolker sin egen studie ved å presentere konklusjoner som resultatene ikke gir grunnlag for. Dette er en svært vanlig fallgruve, selv i høyt rangerte tidsskrifter. En enkeltstudie gir eksempelvis aldri grunnlag for generelle konklusjoner (”De gode operasjonsresultatene ved vårt sykehus i fjor betyr at kirurgi alltid er den beste behandlingen ved rotatorcuffruptur”).
Les gjerne sammendraget en gang til. Nå kjenner du hele artikkelen. Det gir et godt grunnlag for å sjekke om sammendraget ga en edruelig oppsummering av hva som ble gjort, hvorfor og med hvilke resultater. Nå helt til sist bør du også sjekke om artikkelen har fått kommentarer fra andre forskere. Det er i så fall ofte nyttig lesning. Husk også å sjekke om artikkelen har en ledsagende kommentar eller lederartikkel. Disse setter ofte artikkelen inn i en bredere sammenheng og belyser styrker og svakheter ved studien. I beste fall inneholder en slik ledsagende artikkel mange av de samme tanker som du har gjort deg. Da kan du si deg fornøyd med å ha gjort et godt og grundig stykke arbeid med kritisk artikkellesning!
Og om du ønsker flere tips for kritisk artikkellesning, finnes det gode og gratis hjelperessurser også på nett (79).
REFERANSER : Se bakerst i nettutgaven på kirurgen.no
Narrekirurgi er oversatt fra det engelske sham surgery som direkte oversatt betyr humbug-kirurgi. Metoden brukes for å undersøke om det er kausal sammenheng mellom en kirurgisk prosedyre og behandlingseffekt, og gjør det mulig å blinde pasienten i randomiserte studier. En kirurg har etiske betenkeligheter med å operere dersom formålet ikke er å utføre en behandlingsprosedyre.
Allikevel - bruk av narrekirurgi i kliniske studier kan gi ny kunnskap av stor betydning for fremtidige pasienter og kan derfor være etisk akseptabelt.
JENS IVAR BROX 1 OG CECILIE PIENE SCHRØDER 2
1 AVDELING FOR FYSIKALSK MEDISIN OG REHABILITERING, OSLO UNIVERSITETSSYKEHUS
OG MEDISINSK FAKULTET, UNIVERSITETET I OSLO
2 KIRURGISK AVDELING, LOVISENBERG DIAKONALE SYKEHUS
KORRESPONDANSE: JENS IVAR BROX - J.I.BROX @ MEDISIN.UIO.NO
Til tross for et utbredt ønske om at vi skal forholde oss til evidensbasert medisin, har det innen kirurgiske fag manglet studier av høy kvalitet, i hovedsak på grunn av mangel på kontrollgrupper. Mange operasjoner utføres regelmessig uten at det finnes god vitenskapelig dokumentasjon for effekten. Av naturlige årsaker er placebostudier uaktuelt ved mange operative inngrep. Ved mindre operasjoner og hvor subjektive utfallsmål, slik som smerter og funksjonsnedsettelse er viktigst, er bruk av narrekirurgi bedre egnet.
EGNE ERFARINGER
Innen ortopedi er artroskopisk kirurgi et fagfelt som ligger til rette for å kunne gjennomføre placebokontrollerte studier. Artroskopisk reparasjon av øvre labrumdefekter i skulderen økte betydelig fra år 2000, både i Norge og internasjonalt. Etter hvert kom publikasjoner om dårlige resultater og komplikasjoner. På bakgrunn av en egen prospektiv studie som viste gode resultater, stilte vi likevel spørsmål ved om dette skyldtes kirurgien så lenge vi ikke hadde noen kontrollgruppe (1). Kirurgen hadde etiske betenkeligheter med å bruke narrekirurgi som kontroll behandling og studien hadde neppe latt seg gjennomføre uten medvirkning av en nestor innen norsk ortopedisk kirurgi, Olav Reikerås.
Vi designet derfor en dobbeltblind, randomisert og placebokontrollert studie. I søknaden til etisk komité og i informasjonsbrevet til aktuelle pasienter påpekte vi at det ikke eksisterte god dokumentasjon om hvilken behandling som hadde best effekt ved denne tilstanden. En gjennomgang av 3000 tidligere artroskopiske skulderoperasjoner ved kirurgisk avdeling på Lovisenberg diakonale sykehus (bilde 1) viste ingen anestesikomplikasjoner og en infeksjonsfrekvens på 0.1%. Placebogruppen i studien ville kun få utført en diagnostisk artroskopi med forventet lavere risiko.
Etter godkjenning fra regional etisk komite inkluderte vi pasienter som fikk muntlig og skriftlig informasjon om at de ville bli artroskopert og at inklusjonen og randomiseringen først ville skje på operasjonsstua dersom en isolert øvre labrumdefekt ble påvist. Pasientene ble først inkludert etter at skriftlig samtykke var gitt. Alle pasientene hadde samme arr, samme fatle og samme postoperativt regime på sykehuset. Alle pasientene hadde dessuten postoperativ fysioterapi, i hovedsak veiledede øvelser. Ingen andre enn operatøren visste hvilken gruppe pasientene havnet i. Til sammen 118 pasienten ble inkludert, 40 pasienter i narrekirurgi gruppen, 39 i bicepstenodese gruppen og 39 i gruppen med labrumreparasjon. Pasien

BILDE 1. Forsiden av A-magasinet 28.07.2017 viser operasjonsstua ved Lovisenberg Diakonale
Sykehus der vi gjennomførte en narrekirurgisk randomisert studie. Er det prosedyren eller forventningene og ritualene som er viktigst for resultatet? (Publisert med tillatelse fra Aftenposten).
tene ble før og etter behandling undersøkt av en observatør (manuellterapeut Øystein Skare) som var blindet for behandlingen.
Vi fant ingen forskjell i smerte og funksjon mellom gruppene etter seks måneder som var det primære endepunkt for studien (2). Ved avsluttende kontroll etter to år fant vi at alle tre gruppene hadde en signifikant bedring både med hensyn på smerte og funksjon. Det var ingen signifikant forskjell mellom gruppene enten de hadde fått kirurgisk behandling eller narrekirurgi.
Resultatene fra denne studien har nytteverdi fordi det har ført til endring i behandling av smerter og funksjonssvikt som skyldes øvre labrumskader. Pasienter vil kunne bli bra uten operativ behandling og denne kunnskapen har ført til en klar reduksjon i disse operasjonene. Resultatene fra studien er presentert både nasjonalt og internasjonalt. Imidlertid er det en lang prosess å endre kirurgers innstilling til indikasjonsstilling og kirurgisk behandling. Det er beskrevet at bare en av fem studier som gir ny medisinsk kunnskap fører til endring av klinisk praksis og at det tar 17 år før evidensbasert kunnskap benyttes i klinikken, men kunnskapen om hvor ofte ny kunnskap fører til endring av og hvor lang ti det tar, er mangelfull (3).
PLACEBOEFFEKT OG PLACEBORESPONS
Hvordan kan pasienter bli bedre uten at den kirurgiske prosedyren blir gjennomført? Skyldes det placebo, naturlig forløp eller postoperativ behandling? Hvordan kan placebo lindre smerte? Den biologiske aktiveringen av placebo ble første gang beskrevet for snart 50 år siden (4). I en klinisk studie fikk pasienter placebo som smertelindring etter å ha fått trukket en tann (4). Forskerne oppdaget at den smertelindrende effekten av placebo opphørte dersom de ga nalokson, og kunne dermed konkludere med at placeboeffekten er biologisk. Studien ble kritisert for metodiske svakheter, men i 1996 fant en annen forskergruppe samme resultat (5). Eksperimentene tyder på at placebo kan redusere smerte ved å aktivere kroppens egne opioider, endorfiner.
Hva er placeboeffekt og hva er placeborespons? I 2018 ble en stor gruppe placeboforskere enige om en definisjon av begrepet placeborespons (6): « The placebo and nocebo response includes all health changes that result after administration of an inactive treatment (i.e., differences in symptoms before and after treatment), thus including natural history and regression to the mean.» Det er altså ikke bare placeboeffekten, men den samlede responsen man observerer når en pasient får placebo.
Placeboeffekten beskriver den effekten som kun skyldes placebo. Det kan for eksempel skyldes forventningen til tabletten eller operasjonen, men det er vanskelig å skille placeboeffekten fra placeboresponsen i kliniske studier. I studier som vår, som sammenlikner effekten av kirurgi og narrekirurgi, er det behandlingsresponsen og placeboresponsen vi studerer. Først når vi i slike studier inkluderer pasienter som ikke får noen behandling, kan vi skille behandlingseffekten og placeboeffekten fra det naturlige forløp. I praksis er studier som inkluderer en gruppe som ikke får noen behandling, vanskelig å gjennomføre.
HVOR STOR ER PLACEBOEFFEKTEN?
Det er en myte at placeboeffekten utgjør 30%, at 1/3 av pasientene responderer på placebo og at effekten er kortvarig. Vi vet i dag at det er umulig å angi en generell placeboeffekt i prosent. Den kan variere fra 0 til 100% og er bl.a. avhengig av pasienten og behandlingssituasjonen. Det er diskutert om kjønn, personlighet og gener kan spille en rolle for hvor stor effekten er, men vi kan i dag ikke konkludere med at noen av disse faktorene har avgjørende betydning. I en oversiktsartikkel om placebo ved langvarige smerter beskrives at jo mer høyteknologisk behandlingen er, jo større er placeboeffekten (7). Den positive forventningen til kirurgi og injeksjoner er stor, og ritualene pasienten går gjennom forsterker mest sannsynlig placeboeffekten. I en oppsummering av resultatene i 22 randomiserte studier der placebo ble sammenliknet med ulike typer invasiv behandling, forklarte placeboresponsen 80% av bedringen av den spesifikke behandlingen (8). Behandlingseffekten varierte i studiene som ble inkludert. Dersom bedringen var stor, var placeboresponsen stor, og dersom bedringen var liten, var placeboresponsen liten. I denne studien var det ikke mulig å skille mellom effekten av placebo, naturlig forløp, regresjon mot gjennomsnittet og andre uspesifikke årsaker til placeboresponsen. Likevel var det altså en sterk tendens til at bedringen i placebogruppen samsvarte med bedringen i den gruppen som fikk spesifikk behandling.
Placeboeffekten kan variere avhengig av hvem som gir behandlingen. De fleste tenker at de ikke vil ha smertelindrende effekt av en sukkerpille eller av narrekirurgi. Dette er naturlig fordi placebotabletten inneholder ingen kjemiske stoffer som kan påvirke smerten, og narrekirurgien medfører ingen strukturelle endringer utover et snitt i huden. Det er situasjonen behandlingen blir gitt i som kan gjøre en forskjell. Ut fra resultatene i en ny åpen placebostudie hadde 40% av pasientene god smertelindrende effekt av en sukkerpille selv om de visste at de fikk en sukkerpille (9). Kanskje du likevel kan ha effekt av en sukkerpille eller av narrekirurgi dersom du har tiltro
til personen som gir deg det? Det er mye placebo i god kommunikasjon.
HVILKE MEKANISMER KAN FORKLARE PLACEBOEFFEKTEN?
Fire ulike mekanismer kan teoretisk forklare placeboeffekten: Positiv forventning, ritualer, læring og hypnose (7, 1012). De kan virke samtidig eller hver for seg. Ikke uventet varierer forventningene pasientene har til en gitt behandling. Vi kan huske tidligere positive opplevelser knyttet til behandling eller negative opplevelser i form av bivirkninger (13).
Dette understreker at variasjon i placeborespons kan være stor. En god og balansert formidling av positiv forventning og nøktern medisinsk informasjon kan kalles legekunst. På den annen side kan bruk av medikamenter, injeksjoner og kirurgi med tvilsom effekt kalles sjarlataneri. Vi ønsker oss ikke tilbake til en tid da sjamanen eller barbereren stod for den kirurgiske behandlingen, selv om effekten av ritualene pasienten gjennomgår ved en operasjon, fra å bli kledd i sykehusklær, til anestetiske prosedyrer og postoperativ oppfølging, ikke skal undervurderes.
Effekten av læring eller klassisk betinging er undersøkt på friske forsøkspersoner ved fysisk aktivitet på høyder fra 3500m til 5500m over havet (10). Ved å erstatte oksygen med placebo etter gjentatte forsøk med oksygen, ble ikke bare trettheten og prestasjonen bedret, men også ventilasjonen og hjertefrekvensen ble redusert. Effekten av klassisk betinging skjer i hjernen. Selv om det umiddelbart er vanskelig å se hvilken betydning det kan ha for effekten av narrekirurgi, reiser det interessante spørsmål om placebo, kanskje også om effekten av høydetrening.
Effekten av åpen placebo, det vil si at pasienten vet at placebo blir gitt, reiser spørsmål om effekten skyldes en form for hypnose mediert gjennom terapeutpasient relasjonen. I en crossoverstudie med pasienter med langvarige ryggsmerter var effekten av åpen placebo like stor som den vi kan forvente ved vanlige behandlingsformer (11).
Forskning på friske forsøkspersoner har gitt oss kunnskap om hvordan placebo og positive forventninger påvirker smerte og hvordan det påvirker hjernen. Smertesignaler tolkes i hjernen og placebo virker i hjernen. Vi har begrenset kunnskap om hvordan dette skjer og om hvordan de ulike nettverkene eller nervebanene kommuniserer. En ny studie publisert i Science i mai 2024 gir oss et perspektiv hvor kompleks hjernen er (14). Forskerne undersøkte 1mm3 av hjernen og i denne lille biten fant de
57000 celler og 150 millioner synapser eller forbindelser mellom nevroner.
NARREKIRURGISKE STUDIER
I dobbeltblinde randomiserte studier har narrekirurgi gitt like gode resultater som den vanlige kirurgiske prosedyren ved ulike vanlige smertetilstander som subakromiale skuldersmerter (impingement syndrom), knesmerter relatert til degenerasjon eller skade av menisken hos middelaldrende, bekken eller iliosacralleddssmerter, osteoporotiske kompresjonsbrudd og angina pectoris, foruten studien vi gjennomførte (1521). De etablerte kirurgiske prosedyrene har ved alle de nevnte smertetilstandene eller diagnosene vært patofysiologisk og logisk forklart. I narrekirurgiske studier har prosedyrene hatt en effekt som er lik placeboresponsen. Dette gir ikke bare grunn til endring av praksis, men også til undring og nysgjerrighet. Hvordan kan en narrestent bedre gangdistansen like mye som en stent ved angina pectoris? Hvordan kan pasientens helserelaterte livskvalitet bedres like mye ved narreoperasjon som ved partiell meniskektomi? Hvordan skal vi forklare disse resultatene til pasienten? Det er mange ubesvarte spørsmål.
Felles for disse vanlige kirurgiske prosedyrene er at det har vært stor tiltro til effekten. Operasjonene utføres fortsatt daglig over hele verden, og til sammen har millioner av mennesker gjennomgått slike operasjoner. Alle de narrekirurgiske studiene har til dels vært heftig kritisert for mer eller mindre viktige metodiske svakheter. For de nevnte smertetilstandene har vi imidlertid ikke bedre studier som har undersøkt den kausale sammenhengen mellom den kirurgiske prosedyren og behandlingseffekten. Når behandlingsresponsen etter en operasjon ikke er forskjellig fra placeboresponsen, er det grunn til å spørre seg om det er etisk akseptabelt å fortsatt informere pasienten om at operasjonen er effektiv.
FORDELEN VED Å DELTA I EN NARREKIRURGISK STUDIE
Mange vil mene at det ikke er etisk forsvarlig å benytte narrekirurgi, narreinjeksjoner eller placebopiller i vanlig klinisk praksis. Bruk av placebo er nyttig i studier som undersøker om behandlingsmetoder har en effekt. Placebo gjør det mulig å benytte best mulig studiedesign i klinisk forskning, en dobbeltblind randomisert studie, til å finne ut om den kliniske prosedyren i seg selv er mer effektiv enn placebo. Forskning som inkluderer placebo har gitt oss innsikt i hvordan vi kan bruke forventninger, ritualer og læring i pasientterapeutrelasjonen, både i tillegg til annen effektiv behandling og når det ikke finnes biomedisinsk effektiv behandling.
I en nylig publisert artikkel konkluderer den amerikanske kirurgen Ali Abassi med at det kan være en fordel for pasientene å delta i en narrekirurgisk studie (22). Hvis den kirurgiske prosedyren viser seg å være effektiv, vil ulempen ved å bli randomisert til narrekirurgi være lengre ventetid på behandling for pasienten, men i studiene han inkluderte var sannsynligheten for dette liten. Kun i en av seks studier var den kirurgiske prosedyren mer effektiv enn narrekirurgi. I artikkelen presenterer han en matematisk modell for beregning av fordeler og ulemper ved å delta i slike studier. Risiko for komplikasjoner ved narrekirurgi er alltid mindre enn ved den kirurgiske prosedyren. I tidligere artikler om etikk er det i stor grad fokusert på mulig risiko ved narrekirurgi uten at den økte risikoen som den kirurgiske prosedyren innebærer er vektlagt og uten å ta hensyn til konsekvenser for fremtidige pasienter (23, 24).
En pågående engelsk og en norsk randomisert studie sammenligner effekten av avstivningsoperasjon med ikkeoperativ behandling ved langvarige uspesifikke ryggsmerter, hvorav en norsk studie (25, 26). Ingen av studiene sammenligner effekten med narrekirurgi. Man kan snu den etiske problemstillingen og spørre seg om det er etisk å gjennomføre en slik studie uten narrekirurgi. Det burde vært gjort, både fordi tidligere studier tyder på at det er tvilsomt om slike operasjoner har effekt og fordi avstivning ikke har noen tilleggseffekt til dekompresjon ved en rygglidelse med potensiell instabilitet, spinal stenose med degenerativ spondylolistese (27).
Langsomt tvinger forskningen fram endring i behandlingsrutiner. Vi fortsetter imidlertid å bruke behandlingsmetoder som er grundig undersøkt og ikke har effekt. I en kunnskapsoversikt som inkluderte behandlingsstudier publisert i det prestisjetunge New England Journal of Medicine gjennom en 10års periode, hadde bare halvparten av en rekke vanlig brukte behandlingsformer i medisin effekt utover placebo (28).
Artikkelen bygger på forfatternes egne erfaringer i gjennomføring av en randomisert studie med narrekirurgi som kontrollgruppe og på et bokmanus skrevet av Jens Ivar Brox: «Placebo- narremedisin og narrekirurgi» under vurdering i et forlag.
REFERANSER : Se bakerst i nettutgaven på kirurgen.no
TOBIAS HAUGE
STYREMEDLEM NORDIC EARLY ESOPHAGEAL NEOPLASIA ASSOCIATION ( NEENA ) OG GASTROKIRURGISK AVDELING, OUS ULLEVÅL
KORRESPONDANSE: TOBIHA @ OUS - HF.NO
Tradisjonen tro var det igjen duket for årets høydepunkt for mange Barretts-interesserte – det 3. nordiske møtet om Barretts øsofagus og spiserørskreft i tidlig stadium. De to første møtene, avholdt i henholdsvis i Stockholm og Oslo, hadde vært en stor suksess, så det var store sko den islandske organisasjonskomiteen skulle fylle. Det skulle derimot vise seg at de besto prøven med glans. De hadde satt sammen et forrykende program bestående av en utsøkt blanding av toneangivende europeiske og japanske forskere og klinikere, blandet med våre lokale nordiske helter.
Totalt 101 deltakere, fra ni land, hadde pakket vinterklærne og tatt turen til Reykjavik 18. og 19. september. Her ventet åtte friske plussgrader og et møte lokalisert til hotell Reykjavik Natura, ca. to km utenfor sentrumskjernen, men nabo til både Universitetssykehuset, Landspitali og innenriksflyplassen, Reykjavíkurflugvöllur. Norge var representert med ni deltakere: fra Oslo, Bergen og Trondheim. Den islandske organisasjonskomiteen, ledet av kirurgen Magnus Konradsson hadde virkelig lagt seg i selene for at de over 100 deltakerne skulle få et høyt faglig, men ikke minst sosialt utbytte av turen til Island.
ETABLERING AV NORDIC EARLY ESOPHAGEAL
NEOPLASIA ASSOCIATION ( NEENA )
De nordiske Barrettsmøtene har hatt til hensikt å drive opplæring av lokale endoskopører, men også å være et sted hvor de nordiske ekspertene kan møtes. Over tid har man sett at ett møte årlig ikke er tilstrekkelig. Det er nødvendig med et kontinuerlig arbeid for å bedre håndteringen av pasienter med Barretts øsofagus og spiserørskreft i tidlig stadium. Det er behov for en felles nordisk assosiasjon som året gjennom, i samarbeid med de nasjonale foreningene, kan øke kunnskapen og bedre håndteringen av pasientgruppen.
Nordic Early Esophageal Neoplasia Association (NEENA) er en slik assosiasjon. Den ble etablert 19.09.2024 i forbindelse med møtet på Island med Peter Elbe, fra Karolinska Instituttet i Stockholm som første lederen. Med seg i sty
ret har han representanter fra hvert av de Nordiske landene, alle aktive klinikere, men hvor også flertallet har vært involvert i organiseringen av de tidligere nordiske Barrettsmøtene. Organisasjonen vil om kort tid åpne for ordinære medlemmer.
DETEKSJON, EVALUERING OG RISIKOSTRATIFISERING Hvert år forsøker en å ha et bestemt fokusområde for møtet. I år var temaet deteksjon, evaluering og risikostratifisering. Som tidligere år, starter det derfor med en stateofthe art lecture fra en av de virkelig store i Barrettverden Roos Pouw fra Amsterdam UMC.
I og med at de aller fleste pasienter med ikkedysplastisk Barretts øsofagus aldri vil utvikle høygradig dysplasi (HGD) eller kreft (insidens på 0,6 0,9 % per år) vil det for de fleste endoskopører gå lang tid mellom hver gang de ser Barrettspasienter utvikle dysplasi eller kreft (1). Skulle først pasienten utvikle neoplasi, er forandringene initialt (når pasienten enda kan behandles endoskopisk) oftest meget subtile, som vanskeliggjør diagnostikken. Pouw poengterte således viktigheten av en systematisk tilnærming, bestående av seks trinn, hos alle pasienter man undersøker med Barretts øsofagus: 1) bruk det beste endoskopet du har, 2) vask spiserøret godt før du begynner og bruk god tid, 3) se spesielt godt etter på predileksjonssted for neoplasi (i distale øsofagus i høyre del av sirkumferensen) og husk retrofleksjon, 4) lær deg å kjenne igjen subtile forandringer på neoplasi, 5) dokumenter

Barrettsutbredelsen etter Prahaklassifikasjonen og alle synlige lesjoner etter Parisklassifikasjonen og 6) bruk biopsiprotokoller (Seattleprotokoll), samt hold deg til European Society of Gastrointestinal Endoscopy (ESGE) guidelines med tanke på oppfølgingstider (2). For å lære seg å gjenkjenne de subtile forandringene (punkt 4) er det utviklet en interaktiv og validert plattform, BORN module – www.best-academia.eu (3). Videre poengterte Pouw viktigheten av at man har en sikker diagnosen før behandling startes. Regranskning av biopsier fra lokalsykehus viser at opp mot 70 % av pasienter som lokalt har fått diagnosen lavgradig dysplasi (LGD) i virkeligheten ikke har det og dermed <1 % årlig risiko for utvikling av HGD eller kreft (1). Skulle dermed diagnosen LGD bli verifisert av en dedikert GIpatolog, har pasienten en reell sannsynlighet for progresjon (9 %/årlig) og behandling er indisert (1).
Opp mot ¼ av pasientene som får påvist adenokarsinom i spiserøret har gjennomgått en tilsynelatende normal gastroskopi, med funn av Barretts øsofagus, det siste året før de får sin kreftdiagnose (4). Med andre ord, vi er ikke gode nok til å diagnostisere HGD/kreft i tidlig stadium. Kanskje bør vi endre dagens strategi? For å utdype dette temaet hadde de invitert professor Rebecca Fitzgerald, fra Universitet i Cambridge (bilde 1). Hun er en av de virkelig ledende i verden når det gjelder ikkeendoskopiske metoder for deteksjon av Barretts øsofagus og bruk av biomarkører. Hun står bak BEST3studien, som i en po
pulasjon på over 13.000 briter, har validert effekten av CytospongeTM (5). Metoden består av en svamp, festet i en snor, som pasienten svelger og når den dras opp gjennom spiserøret samles det prøver for molekylærbiologiske undersøkelser. I BEST3studien viste de at ved rutinemessig å undersøke risikoindivider (menn > 50 år som bruker PPI) med CytospongeTM kan Barretts øsofagus påvises ti ganger hyppigere enn ved ordinær praksis (gastroskopi på indikasjon). På bakgrunn av dette er det i de aktuelle ESGEretningslinjene åpnet for bruk av utvalgte ikkeendoskopiske metoder for deteksjon av Barretts øsofagus hos høyrisikopasienter (case finding) (2). Hvor vidt den økte deteksjonen av Barretts øsofagus virkelig resulterer i lavere mortalitet, undersøkes i den pågående BEST4studien, en RCT med 120.000 briter.
I og med at de fleste pasienter med Barretts øsofagus aldri vil utvikle dysplasi, må en ha en metode for å skille ut de få som gjør det. I dag brukes endoskopi med biopsier. Professor Fitzgerald anser det som en ineffektiv metode den er invasiv og tidkrevende, og metaplasi og dysplasi er ofte «flekkvis» utbredt (6). En er derfor avhengig av biopsi fra nøyaktig riktig område for at korrekt diagnose kan stilles. Et kanskje bedre alternativ, for å finne de som trenger gastroskopi, er hos risikoindivider å bruke ikkeendoskopiske hjelpemidler koblet med biomarkører. Mest lovende er overekspresjon av p53 og/eller forekomst av atypi (høyrisikofaktorer) (7). Undersøker man pasienter som ikke har høyrisikofaktorer ei heller

BILDE 2: Truls Hauge, gastromedisinsk avdeling, OUS Ullevål foreleser om status i Norge når det gjelder diagnostikk og behandling av dysplasi og spiserørskreft i tidlig stadium.
kliniske risikofaktorer (alder > 60 år, mann, lang Barrett) finner man HGD/T1a kreft hos 2 % mot 31 % i høyrisikogruppen (p53 og/eller atypi). Testen har en sensitivitet på 89 % (konfidensintervall 0.770.97), slik at ekstremt få pasienter glipper ved bruk av denne ikkeendoskopiske metoden (7).
For å bedre overlevelsen på spiserørskreft generelt (5års overlevelse alle stadier ca 30 %) er en avhengig av å diagnostiere sykdommen på et tidlig stadium. En utfordring er at halvparten av pasientene med adenokarsinom i spiserøret ikke har histologiske funn som tilsier at de tidligere har hatt Barretts øsofagus (8). Det som også er utfordrende å forklare er hvorfor kun de færreste pasienter med Barretts øsofagus utvikler kreft. Med andre ord, hos mange klarer vi ikke å detektere spiserørskreft tidlig nok og mange av de med Barretts øsofagus vi detekterer, får aldri kreft. En mulig forklaring er at kreften ikke alltid utvikler seg trinnvis med gradvis akkumulering av mutasjoner (8). Det kan være at enkelte individer har celler hvor det allerede i normalt plateepitel foreligger mutasjoner som gjør at de sikkert vil utvikle seg til kreftceller («born bad»). Andre er kanskje ikke «forhåndsprogrammerte», men hvor det forekommer en katastrofal hendelse i cellens liv, som gjør at kreft utvikles («catastrophic event») (8).
ERFARINGER FRA DE NORDISKE LANDENE
De beste godbitene var spart til slutt. Som ved tidligere møter ble også dette møtet avsluttet med en sesjon hvor en representant, fra hvert av de nordiske landene, ga en oversikt over hvordan diagnostikk og behandling av Barrettspasienter var organisert i sitt land. Truls Hauge fra gastromedisinsk avdeling på Ullevål sykehus (bilde 2)

3: Ingrid Vikan Sjurgard, PhD-student ved avdeling for molekylæronkologi, Radiumhospitalet forelser om forskningsprosjekter gruppen har på biomarkører for spiserørskreft.
redegjorde for status i Norge og hvordan behandlingen er organisert hos oss. Nytt av året var at alle land var forespurt om å presentere ett eller flere aktive prosjekter som det arbeides med. Fra Norge ble to prosjekter presentert: 1) Opprettelsen av et nasjonalt prospektivt register over pasienter med dysplasi og spiserørskreft i tidlig stadium og 2) utvikling av biomarkører for deteksjon av spiserørskreft. Inntil nå, har vi på nasjonalt nivå ikke hatt oversikt over endoskopisk behandling og oppfølging av pasienter med dysplasi eller spiserørskreft i tidlig stadium. Nå, som første land i Skandinavia, har vi opprettet et nasjonalt register hvor alle de fire universitetssykehusene som behandler denne tilstanden er med. Et slikt register vil også styrke samarbeidet mellom de få sentrene som behandler tilstanden og ikke minst muliggjøre forskning av høy kvalitet. På sikt er det også tenkt innsamling av biologiske vevsprøver for forskning på biomarkører. Sistnevnte gjøres allerede i dag, på nasjonalt nivå, for pasienter som opereres for spiserørskreft. Ingrid Vikan Sjurgard, PhDstudent ved avdeling for molekylæronkologi (bilde 3), Radiumhospitalet, redegjorde for hvordan de allerede nå arbeider med biomarkører på pasientgruppen og hvordan de ser for seg at biomarkører i framtiden kan diagnostisere spiserørskreft på et tidligere stadium. Begge presentasjonene ble møtt med stor interesse!
Alt i alt var dette et meget vellykket møte, både faglig og sosialt! Neste møte bytter navn til NEENA meeting og foregår 2.3. oktober 2025 i Gøteborg. Hjertelig velkommen!
LITTERATUR: Se bakerst i nettutgaven på kirurgen.no
EIRIK KJUS AAHLIN
LEDER AV FORFATTERGRUPPEN OG NGICG - ØV
I Norge har forekomsten av adenokarsinom i magesekken vært fallende i flere tiår. Samtidig har det vært en kraftig økning i forekomst av adenokarsinom i nedre del av spiserøret og overgangen mot magesekken. Denne økningen har sammenheng med økende forekomst av fedme i befolkningen. Dermed vil de fleste tilfellene av kreft i spiserør og magesekk forekomme i overgangen mellom disse organene. Det er derfor fordelaktig å samle kreft i spiserør og magesekk i ett handlingsprogram.
Det nye handlingsprogrammet for kreft i spiserør og magesekk er betydelig forkortet i forhold til de gamle handlingsprogrammene. Forhåpentligvis vil dette føre til økt brukervennlighet. Det presiseres at handlingsprogrammet ikke er en systematisk gjennomgang av temaene. Handlingsprogrammet baseres på en usystematisk gjennomgang av litteratur samt internasjonale retningslinjer, tilpasset norske forhold.
Behandlingen av kreft i spiserør og magesekk er i dag multimodal og tverrfaglig. I dag vil majoriteten av de som behandles med kurativ hensikt for kreft i spiserør og magesekk, bli varig friske. Dette var ikke tilfelle før multimodal behandling ble innført. I Norge har det over flere år vært en gledelig utvikling hva gjelder prognose ved disse kreftformene.
Det nye handlingsprogrammet omtaler organbevarende behandling som endoskopisk reseksjon og strålebehandling med kurativ intensjon utførlig. Her er balansegangen mellom organbevaring og onkologisk sikkerhet svært krevende.
Det nye handlingsprogrammet vil bli løpende oppdatert, blant annet i tråd med beslutninger i Nye Metoder.
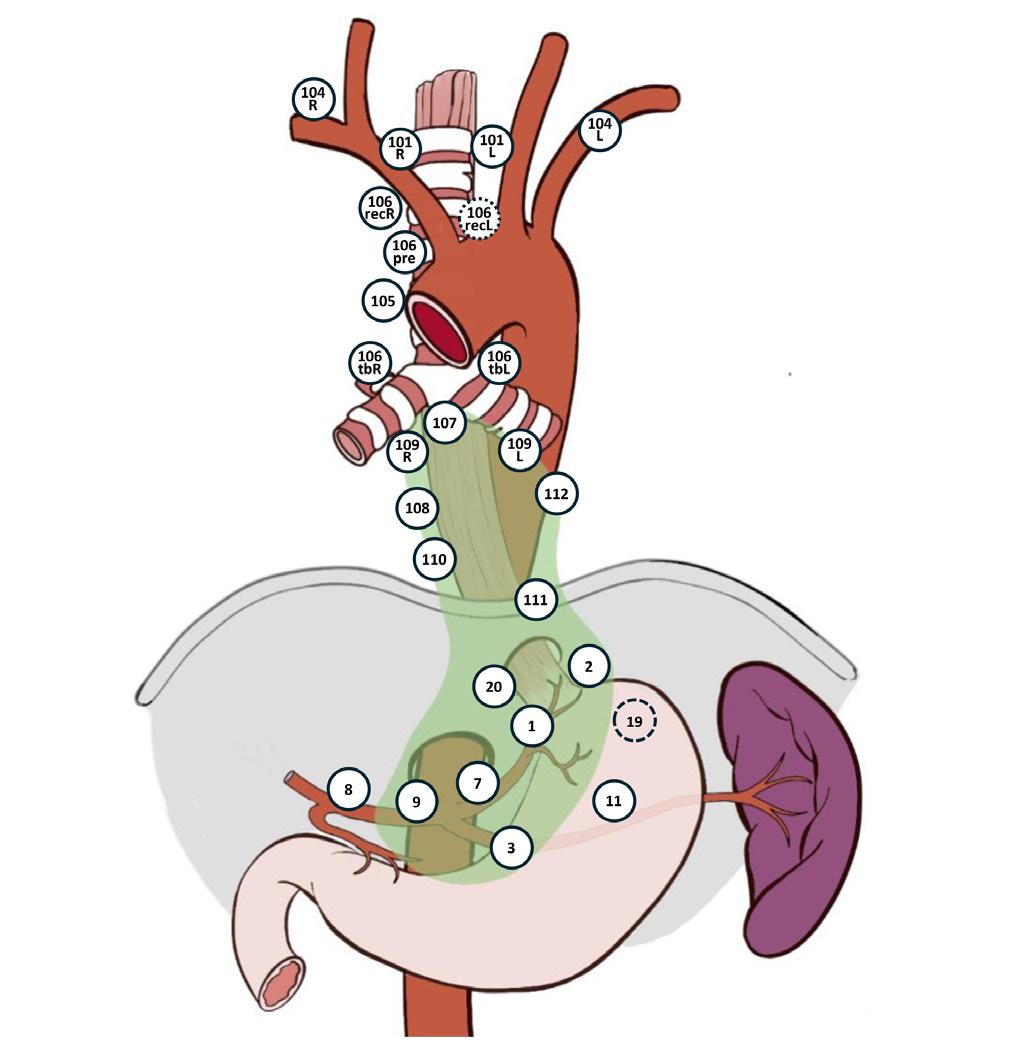
Handlingsprogrammet hadde ikke vært mulig uten stor innsats fra alle forfatterne. Spesielt stor takk rettes til onkolog og gruppemedlem Ghazwan alHaidari som har illustrert det nye handlingsprogrammet.
God lesning!
Du finner alltid det nyeste handlingsprogrammet for kreft i spiserør og magesekk her: www.helsedirektoratet.no/retningslinjer/kreft-i-spiseror-og-magesekk--handlingsprogram
Denne artikkelserien, som består av tre kronikker, belyser faktorer som kan motivere til medisinsk forskning. Ulike typer av medisinske publikasjoner framstilles. I tillegg beskrives forutsetninger som kan bidra til vellykket publisering. Det gis en oversikt over trender i forskningspublisering, samt forklaring av betegnelsene oppdagelse og innovasjon. Her drøftes også forskningen og den vitenskapelige skrivningens rolle og betydning for framgangen innen medisin og helsevesen, og videre belyses sammenhengen mellom medisinsk praksis og forskning. Ikke minst poengteres behov om støtte fra veileder og ledelse i forsknings- og publiseringsprosessen. Kronikk 1 omhandler tema «Hvordan komme i gang?»
AIRAZAT M. KAZARYAN 1-4, TOM MALA 1,2, MARTIN HAGVE 5,6, KNUT MAGNE AUGESTAD 2,7,8 , TOM NORDBY 3, BJØRN EDWIN 2,4,9, WALEED GHANIMA 2,10
1 AVDELING FOR GASTRO - OG BARNEKIRURGI, GASTROKIRURGISK SEKSJON, OSLO UNIVERSITETSSYKEHUS - ULLEVÅL,
2 INSTITUTT FOR KLINISK MEDISIN, UNIVERSITETET OSLO
3 KIRURGISK AVDELING, SYKEHUSET ØSTFOLD
4 INTERVENSJONSSENTERET, OSLO UNIVERSITETSSYKEHUS – RIKSHOSPITALET
5 GASTROKIRURGISK AVDELING, UNIVERSITETSSYKEHUSET I NORD - NORGE
6 GASTROKIRURGISK FORSKNINGSGRUPPE, UNIVERSITETET I TROMSØ – NORGES ARKTISKE UNIVERSITET
7 GASTROKIRURGISK AVDELING, AKERSHUS UNIVERSITETSSYKEHUS
8 KIRURGISK AVDELING, HELGELANDSSYKEHUSET – SANDESSJØEN
9 AVDELING FOR GASTRO - OG BARNEKIRURGI, SEKSJON FOR HPB KIRURGI, OSLO UNIVERSITETSSYKEHUS – RIKSHOSPITALET
10 HEMATOLOGISK SEKSJON OG FORSKNINGS AVDELING, SYKEHUSET ØSTFOLD
KORRESPONDANSE: AIRAZAT M. KAZARYAN - KAZARYAN @ GMAIL.COM
INTRODUKSJON
Kunnskap er helt nødvendig for å praktisere medisin. Stadig ervervelse av ny kunnskap er avgjørende for å utvikle og gjøre framskritt i behandlingen av pasienter. Ny kunnskap innen medisin genereres stort sett gjennom forskning. Dette er et ansvar og en forpliktelse, men også en mulighet vår profesjon og helseforetakene har til å forbedre pasientbehandlingen og kunnskapsgrunnlaget for best mulig behandling. I denne artikkelserien poengteres viktigheten av forskningsarbeid i helsevesenet. Artikkelserien forsøker også å bidra til å motivere flere til forskning.
Essensielt for god forskning er også evnen til å formidle forskningen. Derfor er det en nær sammenheng mellom god forskning og gode forfatter og formidlingsegenskaper.
LOVPÅLAGT OPPGAVE OG KRAV TIL FORSKNINGSFORSTÅELSE INNEN SPESIALISTUTDANNING Forskning er en av fire lovpålagt oppgaver i spesialisthelsetjenesten (jfr. Spesialisthelsetjenestelovens § 38 og helseforetakslovens §§ 1 og 2), sammen med pasientbehandling, utdanning av helsepersonell og opplæring (1).
Kravet til forskningsforståelse, som innebærer innsyn til forskningsmetodikk, evne til analytisk lesing av medisinsk forskningslitteratur, og kjennskap til relevant lovverk og forskningsetikk, er spesifisert i regelverket for spesialistutdanning (2). Beklageligvis er det ikke utarbeidet mekanismer for å kontrollere om spesialistkandidatene oppfyller dette kravet på tilfredsstillende måte i Norge. Slike mekanismer ville trolig medført større forskningsengasjement i norsk helsevesen.
HVORFOR FORSKE OG PUBLISERE?
Årsakene til hvorfor den enkelte forsker ønsker å publisere artikler, er som regel både egoistisk og altruistisk begrunnet (3).
Egoistiske motiver
1. Karriere: Vitenskapelig publisering kan styrke mulighetene for å skape karriere og muligheten til å jobbe med et fagfelt som en ønsker seg. Det gir en mulighet til posisjonering i et fagmiljø. Hvis du vil oppnå en doktorgrad i Norge (og i de fleste land i verden), er publikasjoner grunnleggende for å forsvare avhandlingen. Å inneha en doktorgrad er en fordel i søknadsprosesser for jobb og kanskje spesielt ved et universitetssykehus. Publisering styrker også mulighetene til videre forskning, tilgang til forskningsmidler og stillinger, og det kan gjøre nettverksbygging lettere.
2. Ønske om å bli anerkjent. Mange føler en tilfredshet når de ser navnet sitt i et tidsskrift, og gleder seg over å bli sitert av andre og dermed være en del av den medisinske utviklingen. Mange ønsker å bidra med noe vesentlig og å bli husket for det. For å oppnå dette kan legen publisere hva han eller hun har gjort i sin praksis og/eller gjennom forskning for at det skal være tilgjengelig for andre. Ville noen huske Rudolf Nissen, som foreslo fundoplikasjon for behandling av refluksøsofagitt hvis han ikke hadde publisert metoden sin? (4)
3. Utvide egen kunnskap. Når du begynner å skrive en artikkel trenger du å utdype din kunnskap og forståelse både for aktuelle tema og forskningsmetode. Dette gjelder ikke bare innen ditt eget forskningsfelt, men også for å studere det som er blitt skrevet om dette og relaterte problemer av andre forskere. Dermed forbedrer du
din egen kunnskap til fordel for pasientene og deg selv. Det styrker også muligheten til å tolke og forstå andres forskning. På denne måten kan du bidra til at behandlingen du gir, har best mulig evidens og du kan lettere bidra med kunnskap inn i fagdiskusjoner.
4. Faglig samarbeid. Jo mer du skriver og bidrar inn i et forskningsfeltet, desto mer interessant kan du bli som samarbeidspartner i andre forskningsprosjekter. Samarbeid på eksempelvis internasjonalt nivå, utvider mulighetene til å forske på det aktuelle temaet, samt mulighetene til å publisere. Det gir også grunnlag for ytterligere utveksling av erfaringer og forbedring av kvaliteten på ditt kliniske og vitenskapelige arbeid. For utvikling, implementering og kvalitetssikring av nye metoder er slikt samarbeid av stor verdi.
5. Økonomiske årsaker. De fleste medisinske tidsskrifter publiserer vitenskapelige artikler uten honorar til forfatterne. Enkelte ganger må forfatterne dekke noen av utgiftene (for eksempel for publikasjon av fargeillustrasjoner eller åpentilgang tidsskrifter). Forskningsaktiviteten er i seg selv ikke direkte økonomisk fordelaktig, men betydningsfulle publikasjoner kan styrke mulighetene til å motta forskningsstipend og finansiering, og deltakelse i vitenskapelige konferanser. Det kan også medføre økt fleksibilitet i arbeidssituasjonen. For farmasøytisk forskning og produsenter av medisinsk utstyr er ofte det økonomiske insentivet veldig til stede.
Altruistiske motiver
Francis Scott Fitzgerald uttrykte: “You don’t write because you want to say something, you write because you have something to say.” Ønsket om å dele tanker, erfaring og oppdagelser med andre er utvilsomt også en viktig årsak til at man skriver vitenskapelige artikler. Hovedformålet med profesjonell publisering er å spre kunnskap blant annet for å forbedre pasientbehandlingen og diagnostikken (5). En lege har en forpliktelse til å publisere viktige kliniske observasjoner, uansett om de beskriver legens prestasjoner eller hans uheldige erfaringer. Kunnskapsformidling er også en viktig del av det å bygge opp forskningsinteresse og et miljø som nettopp prioriterer dette.
Andre motiver
Det finnes også et slags nøytralt motiv for å skulle forske som del av legeyrket: Ønsket om å stadig oppdage og finne noe nytt uten en direkte forbindelse med de angitte motivene (”nysgjerrighet”).
HVORDAN KAN LEGER FORSKE?
Leger er ikke bare utøvere av medisin, de er også lærere, forskere og formidlere. Spørsmålet er hvordan man kan ivareta disse tre funksjonene med stadig større krav til kvalitet, spisset klinisk kompetanse, snevre forskningsfelt og et økende press knyttet til arbeidsoppgaver. Å publisere vitenskapelige artikler er krevende og særlig hvis temaet er komplekst og kun av begrenset allmenn interesse. Det finnes likevel mange eksempler på utmerkede vitenskapelige framstillinger hvor verdifull og kompleks informasjon kommer til uttrykk så enkelt og oversiktlig at den lett blir forstått av lesere som selv ikke er spesialister på feltet.
”Hva kan jeg skrive om?” er et vanlig spørsmål. Medisinske vitenskapelige artikler kan deles inn i tre hovedtyper: kasuistikk, originalartikkel og oversiktsartikkel. En interessant kasuistikk kan være det første insentivet til å fordype seg i medisinsk litteratur om den aktuelle problemstillingen, holde en presentasjon for kolleger eller skrive en kasuistikkartikkel for et medisinsk tidsskrift. Mange begynner sin vitenskapelige karriere nettopp med interessante særegne kasuistikker. Imidlertid har mange tidsskrifter enten sluttet å publisere kasuistikker, eller begrenset dem til kun meget unike kasuistikker. Samtidig er det etablert flere tidsskrifter som spesialiserer seg nettopp på kasuistikker.
Originalartikler er den viktigste drivkraften innen medisinen og den primære typen vitenskapelig publikasjon. Oppsummering av sin egen eller institusjonens erfaring med behandling eller diagnostikk i en retrospektiv analyse kan være et alternativ. Dette er gjerne kvalitetssikringsstudier som kan falle utenom etisk komites mandat til forskjell fra forskningsstudier. Grensen mellom hva som er forskning og kvalitetssikring kan være vanskelig å trekke. Prospektive og særlig randomiserte studier gir høyere nivå av forskningsevidens, men innebærer betraktelig mer ressursbruk og forskningsmetodologisk kompetanse. Originalartikler kan også være basert på eksperimentelt materiale. Eksperimentelle studier gir forskeren muligheten til mer målrettet bestemmelse av
visse egenskaper, samt gode muligheter til å teste hypotesene som er fremsatt på grunnlag av foreløpig analyse.
En oversiktsartikkel gjenspeiler typisk de siste trendene og innovasjonene, «state of the art», knyttet til den aktuelle problemstillingen. Andelen av klassiske (nylig kalt beskrivende) oversiktsartikler har avtatt senere år. Nå skrives disse stort sett av kjente eksperter innen den spesifikke problemstillingen, ofte i form av inviterte artikler. Metaanalyser og systematiske oversikter er på vei til å bli den dominerende typen oversiktsartikkel og krever grundige litteratursøk. En metaanalyse av randomiserte studier gir en oppsummering av eksisterende evidens, og karakteriseres som det høyeste nivå av evidens.
Det finnes andre typer artikler som kommentarartikler, kronikkartikkel, debattartikler, forskningsbrev og varianter av disse. De presenterer kortfattede innlegg og kan uttrykke personlig mening uten nødvendigvis sterk forskningsbakgrunn. Dessuten kan de bli publisert uten fagfellevurdering, men kun etter redaktørens beslutning. Slike artikler åpner opp for refleksjoner som kan stimulere til videre forskning.
REKRUTTERING OG MULIGHETER TIL
FORSKNING FOR LEGER
Måter å rekruttere og stimulere leger til å forske på varierer verden rundt, og kan være utfordrende. Forskningsarbeid er ofte dårligere betalt enn klinisk arbeid og forskningsarbeid blir ofte nedprioritert i den kliniske hverdagen. Rekruttering er et problem både i institusjoner som er tilknyttet og ikke tilknyttet et universitet (6). For klinikere kan det være viktigere å posisjonere seg klinisk enn forskningsmessig. En slik nedprioritering kan trolig påvirke mulighetene til å følge evidensbasert medisin i daglig praksis (79).
Ved universitetssykehusene kan forskning utføres innen rammene av akademiske stillinger som professor, førsteamanuensis, lektor og klinisk stipendiat. Disse stillingene innebærer også undervisning. Stillingene professor og førsteamanuensis i klinisk medisin er som regel ordninger kombinert med overlegestillinger ved tilhørende sykehus.
Stipendiatstillinger må knyttes til et universitet med minst en veileder med universitetstilknytning. Fordelen med stillingen er at stipendiaten ofte kan disponere
hele sin tid til forskning. Ulempen er fravær fra klinisk aktivitet og reduksjon i lønn sammenlignet med stillingen lege i spesialisering. Dette gjør at mange velger bort denne type stillinger. Dessuten er disse stillingene basert på tildeling av stipend for et konkret forskningsprosjekt. Konkurransen er stor, så flere potensielt gode forskningsprosjekt får ikke finansiering via stipendiatordningen og blir ikke realisert.
De finnes kombinerte stillinger (tidligere kalt Dstillinger) som ofte innebærer 50 % klinisk stilling og 50 % forskningsstilling. Legen beholder sin lønn som lege i spesialisering, og vedlikeholder og utvikler fortsatt sin kliniske kompetanse. Det finnes store variasjoner i hvordan de kombinerte stillingene praktiseres og reguleres. Enkelte steder innebærer 50 % klinisk stilling at legen beholder vaktene fullstendig, mens «elektiv tid» brukes til forskning. Denne modellen er økonomisk gunstig for avdelingene siden legen kan dekke sine vakter, dvs. den ordinære stillingen lege i spesialisering overføres til kombinert stilling. Andre modeller innebærer at legene går ned til 50 % stilling både i vaktordning og elektiv virksomhet. Dette kan være krevende for avdelingens budsjett.
Frikjøp av leger til forskning er en annen ordning. Ordningen innebærer at man frikjøper en del av legens stilling slik den kan brukes til forskning. Til grunn legges både en vurdering av hvor viktig forskningen er og av hvilke eksisterende kapasiteter som er tilgjengelige for å erstatte de kliniske funksjonene til vedkommende lege. Det finnes store variasjoner ved norske sykehus vedrørende hvor lett en forskningsinteressert lege har anledning til å få innvilget en slik ordning.
Fordypningsdager og overlegepermisjon bør selvsagt også kunne brukes til forskningsmål. Imidlertid er denne tiden ofte for knapp til å kunne sette i gang stor forskningsaktivitet. Det er et velkjent faktum at mange leger bruker sin private ubetalte tid til å forske.
VITENSKAP OG KLINISK PRAKSIS
Mange leger er gode klinikere og trenger ikke nødvendigvis publisere vitenskapelige artikler for å oppnå høy kompetanse, anerkjennelse, status eller privilegier. Men enkelte ønsker å bidra vitenskapelig og bør få muligheter til det innen rammene av forsvarlig drift. En leges engasjement i forskning vil fremme både vedkommendes egen kunnskap og fagutviklingen. En utfordring for noen
er at klinisk arbeid ofte er lettere synlig og belønnes lettere i hverdagen enn forskningsarbeid som ofte er mer usynlig i klinikken.
Alle leger skal og bør ha et visst forhold til forskning selv om man nødvendigvis ikke trenger å bedrive det aktivt gjennom hele karrieren. Dette fordrer at forskning bør være et fokus både på legestudiet og på arbeidsplassen på alle sykehus. Det er viktig at leger som går inn i et forskningsprosjekt og som påtar seg ansvar i den sammenheng, for eksempel knyttet til en klinisk studie, må få rammevilkår tilrettelagt for å kunne gjøre dette.
Forskningserfaring bistår til en mer “kreativ” og mer evidensbasert tankegang. Det kan bidra til bedre kliniske avgjørelser og at man lettere tilegner seg kunnskap (10).
UNG LEGE – FORSK!
Leger som har lyst å komme i gang med forskning, bør få støtte fra seniorkolleger og etablerte forskere for å utvikle vitenskapelig kritisk tenkemåte. Seniorkolleger og etablerte forskere må bidra til at det skapes betingelser for den potensielle forskerens faglige vekst. Slik kan vedkommende lære å generere egne originale ideer, uavhengig formulere forskningsproblemer og løse dem. Det er svært viktig, i tillegg til veiledning, å gi forskeren muligheten til å uttrykke sine egne ideer og meninger, og aktivt argumentere for disse. Rollen til administrative ledere er også viktig. Unge leger med akademiske ambisjoner må få støtte fra ledelsen både i form av oppmuntring til forskning og man må tilstrebe å tilpasse en arbeidsplan slik at leger som er interessert, får anledning til å forske.
Forfatterne vil takke for bidraget fra prof. Lars Aabakken dr. Jan Lambrecht til denne kronikken.
LITTERATUR:
Se bakerst i nettutgaven på kirurgen.no
Denne artikkelserien, som består av tre kronikker, belyser faktorer som kan motivere til medisinsk forskning. Ulike typer av medisinske publikasjoner framstilles. I tillegg beskrives forutsetninger som kan bidra til vellykket publisering. Det gis en oversikt over trender i forskningspublisering samt forklaring av betegnelsene oppdagelse og innovasjon. Her drøftes også forskningen og den vitenskapelige skrivningens rolle og betydning for framgangen innen medisin og helsevesen, og videre belyses sammenhengen mellom medisinsk praksis og forskning. Ikke minst poengteres behov om støtte fra veileder og ledelse i forsknings- og publiseringsprosessen. Kronikk 2 inkluderer tema «Fra idé til ferdig artikkel»
AIRAZAT M. KAZARYAN 1-4, TOM MALA 1,2, MARTIN HAGVE 5,6, KNUT MAGNE AUGESTAD 2,7,8 , TOM NORDBY 3, WALEED GHANIMA 2,9, BJØRN EDWIN 2,4,10
1 AVDELING FOR GASTRO - OG BARNEKIRURGI, GASTROKIRURGISK SEKSJON, OSLO UNIVERSITETSSYKEHUS - ULLEVÅL,
2 INSTITUTT FOR KLINISK MEDISIN, UNIVERSITETET OSLO
3 KIRURGISK AVDELING, SYKEHUSET ØSTFOLD
4 INTERVENSJONSSENTERET, OSLO UNIVERSITETSSYKEHUS – RIKSHOSPITALET
5 GASTROKIRURGISK AVDELING, UNIVERSITETSSYKEHUSET I NORD - NORGE
6 GASTROKIRURGISK FORSKNINGSGRUPPE, UNIVERSITETET I TROMSØ – NORGES ARKTISKE UNIVERSITET
7 GASTROKIRURGISK AVDELING, AKERSHUS UNIVERSITETSSYKEHUS
8 KIRURGISK AVDELING, HELGELANDSSYKEHUSET – SANDESSJØEN
9 HEMATOLOGISK SEKSJON OG FORSKNINGS AVDELING, SYKEHUSET ØSTFOLD
10 AVDELING FOR GASTRO - OG BARNEKIRURGI, SEKSJON FOR HPB KIRURGI, OSLO UNIVERSITETSSYKEHUS – RIKSHOSPITALET
KORRESPONDANSE: AIRAZAT M. KAZARYAN - KAZARYAN @ GMAIL.COM
OPPDAGELSER, INNOVASJON OG FORSKNING
Oppdagelse og innovasjon er begge nyskapninger, men ikke det samme (1). Da Flemming observerte effekten på bakterier i en soppflekk i en gjenglemt petriskål, var det en tilfeldig oppdagelse. Senere ble det gjort en rekke studier for å teste og videreutvikle denne oppdagelsen da man selvsagt bør ha solid kunnskap og analytiske evner for å videreutvikle oppfinnelser til praktisk bruk og nytte. Gjennomføring av et doktorgradsprosjekt bidrar til systematisk ombygning av legens forskningskompetanse og akselerering av videre produktivitet i forskningsarbeid.
Innovasjon kan være basert på noe som allerede eksisterer, men viser nye måter å bruke allerede eksisterende substrat eller metodikk på. For eksempel vurderes kikkhullsoperasjon for fjerning av galleblære å være en betydningsfull innovasjon som videre førte til utvikling av laparoskopisk teknikk innen gastroenterologisk kirurgi. Det er samtidig verdt å merke seg at metodene åpen kolecystektomi og laparoskopi ble praktisert flere tiår i forkant. Kombinasjonen av disse to metodene, sammen med innføring av bildeprojeksjon på skjerm, førte til innovasjon i form av laparoskopisk kolecystektomi.
Det forelå imidlertid ikke solid forskningsevidens som viste at denne metoden var trygg og effektiv før flere år etter at innovasjonen ble tatt i bruk. Likevel ble det publisert en rekke mindre pilotstudier før man gikk videre med studier med høy evidens. Dette viser hvordan implementering av nye oppdagelser til bruk i rutinepraksis kan være tidkrevende og utfordrende. Flere av de tidlige pionerene innen laparoskopisk kirurgi opplevde en lang periode med mistro og motstand fra kolleger. Pionerene risikerte til og med å bli suspendert fra retten til å behandle pasienter (2). Det kan bli virkelig krevende å få aksept for pionerarbeid og å få det publisert i et tidsskrift. Pionerarbeid i klinisk virksomhet innebærer også en risiko for uventet utfall, noe som det må tas høyde for både i planlegging, gjennomføring og pasienthåndtering.
Tilfeldighet kan spille en viktig rolle for innovasjon og medisinske framskritt. Oppdagelse av ciclosporin, som har dramatisk forandret transplantasjonskirurgien, skjedde som overraskende tilfeldig funn ved undersøkelse av jordprøver fra Norge med hensikt å finne antifungale substanser (3). I sin artikkel ‘’On Chance and Necessity’’ sa nobelprisvinner Jacques Monod ‘‘… an event, totally fortuitous, coming with a pure chance may enter into the field of necessity with an implacable certitude’’ (4).
Dette viser hvordan innovasjon og nyskapning sammen med en god porsjon med tilfeldigheter innen forskning fundamentalt kan endre vår kliniske hverdag. Det bør likevel ikke tilsidesette viktigheten bak mer rutinemessig forskning som kvalitetssikrer og videreutvikler de nye metodene innen diagnostikk og behandling, samt populariserer ny kunnskap og sprer den verden rundt (5, 6). Metodene kan også videreutvikles av så vel klinisk erfaring som nyvinninger på andre områder, for eksempel bedre videoprosessorer og bildebrikker i laparoskopi og endoskopi, basert på teknologiutvikling for andre formål. Dette fører til betydelige forbedringer hva gjelder trygghet, effektivitet og resultater enn de man så bare for noen år siden (7, 8).
Spesifikke retningslinjer har blitt utarbeidet for å bistå i utvikling av innovasjoner fra ide / innovasjon til pilot og videre til randomiserte kontrollerte studier. Eksempelvis fikk IDEAL (Idea, Development, Exploration, Assessment, Longterm study) retningslinjene bred aksept innen kirurgi og intervensjonsbehandling (9).
Det finnes prinsipielt to måter å veilede forskeren på. Den ene er sammen med en veileder, vanligvis en kollega med forskererfaring. I tillegg blir forskeren veiledet gjennom fagfellevurderingsprosessen ved å lese kritikk fra fagfellevurderer og redaktører (10). Det publiseres mange flere kongressabstrakter enn originale artikler. Dette indikerer dels hvor vanskelig det er å publisere og dels hvor vanskelig det kan være å nå gjennom seleksjonsprosessen i vitenskapelige medisinske tidsskrifter. Avvisning og videresending til et nytt tidsskrift er vanlig.
I skriveprosessen er det nyttig å tenke på at det er essensen som betyr noe. Uten en god og konkret problemstilling og materiale vil en godt planlagt studie, ikke ha noen vitenskapelig verdi. En protokoll eller plan med gjennomtenkt problemstilling og metode vil lette arbeidet. Originalitet, det vil si nye bidrag til eksisterende litteratur og kunnskap, er en styrke i publiseringsprosessen, men artikler som underbygger tidligere funn er også viktige bidrag.
TILLATELSER OG RAPPORTERING
I tillegg til selve forskningsarbeidet fordrer som regel forskning en rekke tillatelser fra for eksempel forskningsetiske komiteer, Direktoratet for medisinske produkter og personvernombud for å gjennomføre forskningsprosjektet. Ved klinisk forskning kreves pasientens samtykke ofte som forutsetning for oppstart av forskningsdatasamling. Det er krav til gjennomføring av kurs for dyreforsøk med hensyn til dyrevelferd ved eksperimentelle studier på dyr.
De siste årene har mange tidsskrifter krevd presentasjon av artikler etter utarbeidede standardiserte retningslinjer for hver enkel type av artikler. Eksempel er CONSORT (Consolidated Standards of Reporting Trials) for randomiserte studier, PRISMA (Preferred Reporting Items for Systematic Reviews and MetaAnalyses) for systematiske oversikter eller metaanalyser, og STROBE (Strengthening the Reporting of Observational Studies in Epidemiology) for observasjonelle studier (11, 12).
I dag er det vanlig å offentliggjøre protokollene fra randomiserte studier i internasjonale registre over kliniske studier i forkant av oppstart eller tidlig etter oppstart. Et eksempel på dette er clinicaltrial.gov. Publisering i ClinicalTrials.gov (ved U.S. National Library of Medicine) eller
Clinical Trials Information System (ved European Medical Agency) før oppstart av en randomisert kontrollert studie, er også en betingelse for å kunne publisere i fleste anerkjente tidsskrift. De stilles i dag også strengere krav til offentliggjøring av eventuelle interessekonflikter (13) og til spesifisering av hva hver enkelt medforfatter har bidratt med jamfør Vancouverreglene for publisering (14, 15).
Alt dette krever tid å gjennomføre og oppfattes av noen som unødvendig bruk av ressurser. Samtidig bidrar denne ekstra dokumentasjonen til å sikre bedre kvalitet i forskningen, samt at dette gjenspeiler en tendens til krav og forventninger i samfunnet om åpenhet og hensyn til eventuelle interessekonflikter.
Det finnes flere nettbaserte verktøy som tillater forskningsprofiler med flere funksjoner, inkludert forskningssøkemotorer, sporing av egne forskningsartikler og tilgang til internasjonalt nettverk av forskere som jobber innen samme eller lignende forskningsfelt (ORCID; Google Scholar; Scopus Author ID; Researchgate; Web of Science ResearcherID; Publons). Disse gir mulighet til å måle forskningsindekser, blant annet Hindex (Hirsch index). Disse nye registreringsverktøyene forenkler forskerens virksomhet. ORCID (Open Researcher and Contributor ID) skiller seg ut i rekken ved at den gir et unikt IDnummer til forskere som aksepteres av alle de fleste seriøse vitenskapelige tidsskrifter. Dette er en universell ID som forenkler kommunikasjonen mellom forskere og tidsskrifter, både når forskeren er i rollen som forfatter og fagfellevurderer (16). Flere land har også nasjonale forskningsverktøy som blant annet lager forskningsprofiler til individuelle forskere. I Norge finnes CRIStin (Current Research Information SysTem In Norway) – et nasjonalt system for forskningsdokumentasjon som administreres av Universitetet i Oslo.
HVOR SKAL MAN PUBLISERE?
Du har skrevet en artikkel og må finne riktig tidsskrift for publisering (9). Viktige momenter da er: 1) oppnå et bredt spekter av lesere; 2) oppnå en riktig leserkrets; 3) publisere i et godt tidsskrift; 4) minimere muligheten for et avslag; 5) kort behandlingstid.
Dessverre kan ikke disse målene alltid oppnås samtidig (17). En edruelig og objektiv holdning til arbeidets verdi er viktig. Man kan lage en slags algoritme for å finne et
passende tidsskrift. Først og fremst er det viktig at forfatterne undersøker retningslinjene for publisering hos aktuelle tidsskrift og hvilke typer artikler som foretrekkes. De fleste medisinske tidsskrifter fortrekker tradisjonelt originale kliniske eller eksperimentelle studier, og bare noen få fokuserer på oversiktsartikler og kasuistikker. Det viser seg i dag at de fleste store tidsskrifter faktisk øker sin andel av oversiktsartikler siden disse generer flere siteringer. Dette kan kanskje dels forklares av at mange forskere finner det lettere å vise til en oversiktsartikkel enn å lete etter alle originalartiklene for å understøtte en påstand. Innsending av et manuskript til et tidsskrift som ikke matcher, vil resultere i automatisk avvisning. Derfor bør man avgrense omfanget av aktuelle tidsskrifter. Det er hensiktsmessig å sjekke publiserte artikler i de siste utgavene av det aktuelle tidsskriftet og kontrollere om innhold og mønster og stil i egen artikkel er i samsvar med artiklene som er publisert. Hvis du finner ut at et manuskript om samme emne nylig ble publisert i dette tidsskriftet, er det verdt å vurdere å sende artikkelen til et annet tidsskrift. Og hvis artikkelen din kan løse problemet som er omtalt i en tidligere artikkel i et tidsskrift, er det lurt å sende artikkelen dit. Å velge riktig tidsskrift er et viktig steg i hele prosessen. Det kan være nyttig å be om råd fra seniorkolleger som har lang erfaring med aksept og avslag knyttet til publisering av manuskripter.
Det er en tendens til økende krav om evidens i vitenskapelige artikler. Selv om medisin er omtalt som en «hard vitenskap» («hard/exact science»), er den «mykere» enn de klassiske «harde» vitenskapelige disipliner som matematikk, fysikk og kjemi. Som del av dette tilstreber redaktørene av medisinske tidsskrifter krav til strikt statistisk analyse som for eksempel gjennom bruk av avansert statistikk, kunstig intelligens og maskinlæring, og randomiserte multisenterstudier (18).
VURDERING AV FORSKNINGSKVALITET
Skåring av forskningskvalitet er viktig for å kunne kontrollere og prioritere forskningsinnsats på internasjonalt, nasjonalt og institusjonelt nivå. Det er naturlig å tenke at det som nevnes ofte (dvs. siteres eller refereres når det gjelder skriftlig form) er viktig og fortjener omtale. Til tross for svakhetene i denne praksisen, er det bred aksept for at rangering basert på antall refereringer, det vil si impactfactor for tidsskrifter og Hirsch indeks (hindeks) for individuelle forskere, spiller en viktig rolle (19, 20). Noe av problemene med dette er blant annet at publikasjoner
fra lang tid tilbake får lavere siteringsrater selv om de ofte kan ha hatt stor innovativ betydning. Dette gjelder spesielt etter digitaliseringen av forskningsartikler som har gjort at antallet både publikasjoner og siteringer har økt kraftig. Derfor er en rettferdig skåring av forskning utført i forskjellig tidsepoker etter siteringsprinsippet svært krevende og nesten umulig.
Siteringstradisjonen er også forskjellig innen ulike fagfelt. For eksempel siteres artikler innenfor fysikk betydelig mindre enn innenfor medisin. Vekting av forskningskvalitet vil også gi unaturlig høyt antall siteringer til oversiktsartikler da disse ofte er lettere å sitere til enn originalarbeidet. Dessuten fører systemet til at både forskere og tidsskrifter velger å sitere egne arbeider for å øke sin egen siteringshyppighet. Siteringsraten er mangelfull i forhold til studier utført innen hemmelige forskningsprosjekter, som regel tilknyttet nasjonal sikkerhet. Disse studiene kunne hatt stor betydning for menneskeheten. For eksempel gjelder dette studier innen nukleær fysikk. Men disse er enten aldri blitt åpent publisert eller publisert flere tiår etter gjennomføring. Dermed blir ikke disse
«hemmelige forskerne» kreditert for sitt fremragende arbeid (21).
I løpet av de siste årene har flere andre bibliometriske skåringsverktøy økt i bruk, blant dem SCImago journal Rank som er siteringsbasert, samt flere alternative ikkesiteringsbaserte såkalte altmetriske verktøy. Disse verktøyene beregner forskningsinnvirkning basert på mangfoldige online eksponeringer, for eksempel i sosiale medier, nettbaserte nyhetsmedier, online programmer for bibliografistyring og så videre (22, 23). PlumX metrics er det mest kjente almetriske verktøyet i verden, inkludert i Norge.
Forfatterne vil takke for bidraget fra prof. Lars Aabakken til denne kronikken.
LITTERATUR:
Se bakerst i nettutgaven på kirurgen.no
God jul og riktig godt nytt år!
FORSKNING OG VITENSKAPELIG SKRIVING 3:
Denne artikkelserien som består av tre kronikker belyser faktorer som kan motivere til medisinsk forskning. Ulike typer av medisinske publikasjoner framstilles. I tillegg beskrives forutsetninger som kan bidra til vellykket publisering. Det gis en oversikt over trender i forskningspublisering, samt forklaring av betegnelsene oppdagelse og innovasjon. Her drøftes også forskningen og den vitenskapelige skrivningens rolle og betydning for framgangen innen medisin og helsevesen, og videre belyses sammenhengen mellom medisinsk praksis og forskning. Ikke minst poengteres behov om støtte fra veileder og ledelse i forsknings- og publiseringsprosessen. Kronikk 3 omhandler tema «Formidling av forskningen»
AIRAZAT M. KAZARYAN 1-4, MARTIN HAGVE 5,6, TOM MALA 1,2, KNUT MAGNE AUGESTAD 2,7,8 , TOM NORDBY 3, BJØRN EDWIN 2,4,9 , WALEED GHANIMA 2,10
1 AVDELING FOR GASTRO - OG BARNEKIRURGI, GASTROKIRURGISK SEKSJON, OSLO UNIVERSITETSSYKEHUS - ULLEVÅL,
2 INSTITUTT FOR KLINISK MEDISIN, UNIVERSITETET OSLO
3 KIRURGISK AVDELING, SYKEHUSET ØSTFOLD
4 INTERVENSJONSSENTERET, OSLO UNIVERSITETSSYKEHUS – RIKSHOSPITALET
5 GASTROKIRURGISK AVDELING, UNIVERSITETSSYKEHUSET I NORD - NORGE
6 GASTROKIRURGISK FORSKNINGSGRUPPE, UNIVERSITETET I TROMSØ – NORGES ARKTISKE UNIVERSITET
7 GASTROKIRURGISK AVDELING, AKERSHUS UNIVERSITETSSYKEHUS
8 KIRURGISK AVDELING, HELGELANDSSYKEHUSET – SANDESSJØEN
9 AVDELING FOR GASTRO - OG BARNEKIRURGI, SEKSJON FOR HPB KIRURGI, OSLO UNIVERSITETSSYKEHUS – RIKSHOSPITALET
10 HEMATOLOGISK SEKSJON OG FORSKNINGS AVDELING, SYKEHUSET ØSTFOLD
KORRESPONDANSE: AIRAZAT M. KAZARYAN - KAZARYAN @ GMAIL.COM
ÅPEN TILGANG OG ”PREPRINT REPOSITORIES”
Siden 1990tallet har enkelte tidsskrift tilbudt såkalt åpen tilgang til artikler, dog ble dette vanlig først på begynnelsen av 2000tallet (1, 2). BioMed Central var et av disse første forlagene som tilbød et slikt alternativ. Disse tidsskriftene la altså til grunn en annen modell for publikasjoner
– gratis tilgang via internett for lesere av artikler, men forfatteren eller forfatterens institusjon må betale for publiseringen i tidsskriftet. Tross en del skepsis har nå de aller fleste tidsskrifter etter hvert introdusert muligheten for åpen tilgang (Open Access) til sine artikler. Flere tidsskrift har etablert en ekstra versjon av tidsskriftet med
alternativ åpen tilgang som publiseringsplattform som BMJ Open, BJS Open og Ann Surg Open. Flere institusjoner i Norge blant annet Universitetet i Oslo, Universitetet i Bergen, Norges teknisknaturvitenskapelige universitet og Universitetet i Tromsø har utarbeidet klare føringer om publisering som fordrer open accesspublisering (3). Dette ble gjort i samsvar med nye krav fra Forskningsrådet og EU (4, 5).
Det er etablert mange nye åpen tilgang tidsskrifter de siste to tiårene, flere med lave krav til kvaliteten av aksepterte artikler. Åpen tilgang har åpnet for økonomisk profitt på en helt annen måte. Det har derfor vært rettet kritikk mot disse tidsskriftene, da dette potensielt vil promotere kvantitet foran kvalitet, da førstnevnte gir bedre økonomisk profitt. Likevel gir «lavkrav» tidsskriftene muligheter til å publisere kontroversiell forskning med kanskje metodologiske svakheter eller uklarheter som derfor refuseres av velrenommerte tidsskrift, men som prinsipielt kan være nyskapninger innen medisinsk vitenskap.
Det er velkjent at flere store oppdagelser og innovasjoner initialt ikke var forståelig i datidens forskningsmiljø og ble mottatt med skepsis. Det var derfor også utfordrende å publisere dem og spre kunnskapen (68).
Den økende populariteten med åpen tilgang har også ført til etablering av såkalte «røvertidsskrifter» (predatory journals), som publiserer artikler kun for økonomisk profitt, med dårlig eller ingen fagfellevurdering (911). Det kan være utfordrende å definere hva som er et røvertidsskrift (12). Flere åpen tilgangtidsskrifter kan være liberale når det gjelder å akseptere svakere studier for publikasjon, uten at dette nødvendigvis kvalifiserer dem til et røvertidsskrift. Det kan være fordelaktig for en forsker å undersøke om tidsskriftet er godkjent av Norsk Senter for Forskningsdata, samt om det indekseres av PubMed / MedLine og har rimelig impaktfaktor.
I begynnelsen av 1990tallet etablerte det seg også aksept for såkalte ”preprint repositories”, der forfatterne kunne poste sine forskningsartikler før de var blitt fagfellevurdert og publisert. Dette ga mulighet til å dele bred og gratis forskning før man hadde gått via fagfellevurderingsprosessen og fått publisert artikkelen i et tidsskrift. Dette har ikke uventet blitt møtt av en viss skepsis i forskermil
jøene. Det er kun i de siste tre årene at et økende antall seriøse medisinske tidsskrifter har begynt å tilby posting av innsendte manuskripter i preprint repositories før fagfellevurdering og eventuell publisering, som en del av en mer åpen kultur rundt publisering. Noen tidsskrift har faktisk også nå dette som et obligatorisk krav, inkludert høyt rangerte tidsskrifter (13). Research Square er dominerende blant preprint repositories for medisinsk forskning, men det finnes flere andre. Det er også mulig å poste artikler i preprint repositories direkte uten innsendelse av dem til tidsskrifter for fagfellevurdering. Preprint repositories advarer tydelig om at innholdet i preprintene bør brukes med forsiktighet fordi forskningen ikke ble fagfellevurdert og kan representere feilaktige konklusjoner og påstander.
PUBLISERING PÅ NASJONALSPRÅK VERSUS ENGELSK Engelsk er et dominerende fagspråk internasjonalt. Siden 2012 har Tidsskriftet for den Norske Legeforening vært tospråklig, med duplisering av artiklene på engelsk i elektronisk utgave hvis forfatterne skulle ønske dette mot betaling (14). Utfordringen med tidsskrifter på nasjonalspråk er at forskningen kan få begrenset internasjonal gjennomslagskraft (15). Samtidig er en epidemiologisk og samfunnsmedisinsk forskning fokusert på problemstillinger som er unike for et land, ofte mest hensiktsmessig å publisere i nasjonale tidsskrifter og på nasjonalt språk (16, 17). Dette er et av momentene som støtter kritikken mot overdreven bruk av vitenskapelige indekser som impaktfaktorer for å måle kvalitet og viktighet av forskningen (18). Anglifisering av forskning har svekket utvikling og bruk av lokal medisinsk terminologi, også i Norge. Mange nye symptomer og tilstander har ikke fått bredt anerkjente norske navn, og norske leger bruker i stedet engelske ord for å betegne dem.
Publikasjon av identisk eller overlappende forskning både på engelsk og lokalt språk i forskjellige tidsskrifter, kan være kontroversielt siden dette kan tolkes som dobbelpublisering. Likevel er det fortsatt en stor andel av leger og annet fagpersonell i mange land som har begrenset tilgang til internasjonale tidsskrifter, og mange mangler språklige ferdigheter i engelsk. Derfor bør ikke nødvendigvis publisering av identisk eller overlappende forskning på forskjellige språk ansees som dobbelpublisering siden målet er å nå forskjellige grupper av lesere og bidra til mer effektiv spredning av kunnskap (19).
ENGASJEMENT I FAGFELLEVURDERING
OG REDAKSJONELT ARBEID
Fagfellevurdering og redaksjonelt arbeid er viktige verktøy for å utvikle forskeres kyndighet og for kvalitetssikring i publiseringsprosessen. I motsetning til redaktørarbeid som har vært en synlig funksjon og som belønnes som prestisjefullt arbeid, er fagfellevurderingsarbeidet likeså viktig, men tidligere ansett som et utakknemlig arbeid fordi ingen kunne offentlig kvantifisere sin fagfellevurderingsinnsats.
Lanseringen av Publons i 2012 har gitt noen insentiver til fagfellevurdering og redaksjonelt arbeid (20). Publons er et internettbasert verktøy som tilbyr sporing, verifisering og fremvisning av fagfellevurdering og redaksjonelle bidrag i akademiske tidsskrifter. Mot slutten av 2010 tilbød de fleste akademiske tidsskrifter kreditering av fagfellevurderingene i Publons. Dette kan ha økt motivasjonen for å påta seg fagfellevurderingsarbeid. Helt nylig ble Publons en del av Web of Science, verdens største kommersielle plattform som gir tilgang til flere databaser med referanse og siteringsdata fra akademiske publikasjoner. Tradisjonelt var fagfellevurderingene anonyme. Siden slutten av 1990tallet tilbyr enkelte tidsskrifter navn på fagfellevurderere og / eller navn på konkret redaktør ansvarlig for håndtering av publiserte artikler. Dessuten gir enkelte tidskiftet leseren tilgang til kommunikasjon, foretatt før publikasjon, mellom forfatterne, fagfellevurderere og redaktørene. Dette tilsvarer til generelt trend med åpenhet i akademia. Det finnes både fordeler og ulemper med dette. Noen av disse tidsskriftene gir mulighet til fagfellevurderere og redaktørene å velge selv om det vil bli navngitt eller ei, samt om de tillater offentliggjøring av artikkelens prepublikasjons kommunikasjon eller ei.
Fagfellearbeid og redaksjonelt arbeid baserer seg stort sett på frivillighet. Med en publikasjonshverdag med stadig flere tidsskrift, som blir ytterliggere akselerert av økende antall åpen tilgangtidsskrift, blir imidlertid spørsmålet om reell økonomisk kompensasjon for redaksjonelt arbeid aktuelt.
NYE TRENDER OG FORMIDLINGSMETODER
Skrivning og lesing er den klassiske metoden for å lagre og overføre kunnskap. Imidlertid er det velkjent at et bilde sier mer enn tusen ord. En økende grad av
digitalisering har åpnet for større bruk av både video og interaktivitet som enklere, bedre og raskere kan formidle både eksperimentell metodologi og teknologisk nyskapning (21). Å tilknytte forklarende videoer til artikler har blitt vanlig de siste to tiårene. Noen tidsskrifter har spesialisert seg på dette, der videopublikasjon er det primære akademiske produktet. The Video Journal of Clinical Research og the Journal of Visualized Experiments (JoVE) representerer slike videotidsskrifter. Sistnevnte er indeksert av PubMed/Medline. Innenfor kirurgi finnes det flere visuelle akademiske ressurser. En velkjent videoressurs, WebSurg, presenterer ikke seg som samling av forskningsvideoer, men en plattform med fagfellevurderte utdanningsvideoer i kirurgisk teknikk (22). Det er en økende aksept innenfor akademia for å sitere videopublikasjoner (23).
Et visuelt eller grafisk abstrakt med et visuelt sammendrag av nøkkelfunnene i en artikkel har også blitt vanlig da dette raskt vil kunne fange opp og formidle essensen av en studie. Dette kan være nyttig, i lyset av et stadig økende antall publikasjoner, som det kan være utfordrende å navigere blant (24). De siste årene er det krav fra flere og flere tidsskrifter om å legge ved et visuelt abstrakt ved innsending av manuskripter. Visuelle abstrakt har også gjort det lettere å fremvise forskningen i sosiale medier.
Sosiale media har fundamentalt forandret kommunikasjonen mellom mennesker i verden. Dette gjelder alt fra tradisjonelle sosiale medier som Facebook og Twitter, til rene forskerrettede medier og forumer som eksempelvis Researchgate (2528). Egenpromotering via disse kanalene er nå mer og mer vanlig for å øke oppmerksomheten rundt publikasjoner og ny forskning. Det kommer stadig høyere samfunnskrav om formidling av forskningsresultater til den allmenne befolkningen.
Forfatterne vil takke for bidraget fra prof. Lars Aabakken til denne kronikken.
LITTERATUR:
Se bakerst i nettutgaven på kirurgen.no

Vi ser fram til å jobbe med Pentax i Norge og få bidra med veiledning, service og salg til nye og eksisterende kunder.

ERCP-skop
Minimer krysskontaminering ved bruk av steril, distal engangshette.

EUS Den optimale EUS-plattform
Discovery AI Endoskopisystem med artificiell Intelligens.

4K LED
Videoprosessor for fleksibel endoskopi
Kontakt oss gjerne eller besøk vår hjemmeside for mer informasjon om produktene.
JOHN - PEDER ESCOBAR KVITTING OG ØYVIND ULVIK
BEDØMMELSESKOMITTE
Forfatterne Kristoffer Watten Brudvik, Jon-Helge Angelsen og Bård Røsok har i nummer 3 av Kirurgen 2023 skrevet en meget bra oversikt over kirurgisk behandling av kolorektale levermetastaser.
Oversiktsartikkelen setter den kirurgiske behandlingen av kolorektale levermetastaser i et historisk perspektiv og gir en oppdatering av pågående studier innom fagområdet.
Artikkelen gir en god introduksjon til onkologiske, intervensjonelle og kirurgiske landevinninger de seneste årene innen behandlingen av kolorektale levermetastaser. Fagområdet har sett en meget spennende utvikling med flere viktige bidrag fra norske fagmiljøer. Selv om det har vært en positiv utvikling de seneste årene innen fagområdet, gjenstår utfordringer i behandlingen av denne pasientgruppen som forfatterne konsist går gjennom i sin diskusjon. Artikkelen er velskrevet, godt illustrert og gir en fin oversikt til yngre kolleger og kirurger som ikke daglig har avansert leverkirurgi som sin hovedoppgave. Videre ses det som en styrke at den er skrevet av kirurger fra ulike fagmiljøer i Norge. Artikkelen fungerte også utmerket som introduksjon til temanummeret maligne sykdommer i lever og galleveier.
Årets bedømmelseskomitee besto av John-Peder Escobar Kvitting, Thoraxkirurgisk avdeling, OUS Rikshospitalet og Øyvind Ulvik, Urologisk avdeling, Haukeland Universitetssykehus. Redaksjonen ønsker å utdele en stor takk til bedømmelseskomiteen for dens arbeide.

ÅRETS ARTIKKEL I KIRURGEN 2023/2024 gikk til Kristoffer Watten Brudvik og medforfattere. Til venstre John-Peder Ecobar Kvitting fra bedømmelseskomiteen, i midten prisvinner Kristoffer Watten Brudvik og til høyre Tobias Hauge, redaktør av Kirurgen
RAGNHILD L TVEIT
LEDER I FORENING FOR UNGE NORSKE KIRURGER ( FUNK )

Hvert år deler vi ut FUNKs ærespris til en kollega som har utmerket seg med sin innsats for kirurgisk utdanning. Årets ærespris gikk til Branislav Azanjac, ved Ringerike sykehus, som i en årrekke har engasjert seg i utdanning av kirurgiske LIS.
Azanjac var tidlig ute med laparoskopisk kirurgi og som overlege ble han raskt opptatt av opplæring innen laparoskopi. Det å standardisere teknikker har vært viktig for ham – både for å sikre god kvalitet på pasientbehandlingen, men også for å legge til rette for gode utdanningssituasjoner.
Han tilser at utdanningsløpene til LIS tilpasses den enkelte. LIS sine ferdigheter skal bygges fra grunnen av og utfordringene de får tilpasses deres nivå for å fremme mestring. Operasjonene på avdelingen fordeles på LIS ut fra deres nivå, slik at de får best mulig læringsutbytte av operasjonene. Overleger skal som hovedregel ikke operere, men stå ansvarlig for kvaliteten og progresjonen hos LIS.
Med utviklingen av teknologi har robotkirurgien gjort sitt inntog. For Azanjac har det vært naturlig at også LIS skal lære seg å operere på robot. Han har derfor utviklet et systematisk opplæringsprogram innen robotkirurgi for LIS. Her stilles det krav til simulatortrening og prosedyrer som førsteassistent, samt at LIS bidrar i alle ledd både før og etter operasjonene. Samarbeid med hele teamet, fra renhold til kirurg, står i fokus.
Som person beskrives han som empatisk og imøtekommende ovenfor alle sin ansatte. Dette legger til rette for en åpenhetskultur i avdelingen. Han gjør det trygt å snakke om komplikasjoner, uten kritikk eller stigmatisering, slik at en selv og de andre i avdelingen kan lære av situasjonen. I tillegg er han en pådriver for at LIS får dra

på kurs og kongresser utenlands, slik at de får utviklet seg faglig og bygget nettverk også utenfor Norge.
Azanjac beskrives som en eksepsjonelt dyktig kirurg og mentor som har betydd mye for mange unge kirurger –både for dagens LISgruppe på Ringerike, men også ferdigutdannede kirurger som i dag har overlegestillinger på sykehus over hele landet. Det var en ydmyk vinner som mottok prisen under årets Kirurgmiddag.
Det henger gule og røde løv på trærne. Kulden sniker innpå oss. Høsten er kommet til Oslo og det betyr at det nittiniende Kirurgisk Høstmøtet står for tur. Kirurger fra hele landet tar seg en liten pause fra den hektiske og uforutsigbare sykehushverdagen, for å samles til én uke med faglig og sosialt påfyll. Men hva ligger bak de mange inspirerende, lærerike og engasjerende presentasjonen som holdes denne uken?
SAIRA MAULAND MANSOOR
KORRESPONDANSE: SAIRA @ KIRURGEN.NO
Kirurger som disputerte i 2023/2024:
Helle Kristine Skjerven - Improved breast cancer surgery in DCIS, is less more than enough?
Joel K. Touma - The potential role of HCMV infection in breast cancer initiation and progression
Charles Patrick W. Jones - Ureteroscopy in special populations
Saira Mauland Mansoor - Screening for abdominal aortic aneurysm in 65-year-old-men in Oslo - outcomes and benefits
Natkai Safi - Early detection of Micro-and Macro-circulation in the ischemic GI-tract and the diagnosis and treatment of patients with median arcuate ligament syndrome
Benedikte Smenes Nystøyl - Effects of exercise training and cardiorespiratory fitness upon cardiac surgery incidence and outcome
Bjarte Tidemann Andersen - The anatomy of the middle colic artery and inferior mesenteric artery with their branches in colorectal cancer surgery, clarified and illustrated with 3D CT reconstructions and 3D-printed physical models
Gurpreet Singh Banipal - Assessing right colon cancer patients with metastatic (D3) lymph nodes. Identifying the group benefiting from extended mesenterectomy and evaluation of radiological and pathological prognostic factors
Kristin Bentung Lygre - Improving surgery and prognostication in right-sided colon cancer
Umair Majid - Macrophage Dynamics in the Human Colon: Implications in Health and Cancer
Usman Saeed - Body mass index and Cancer
Epidemiology: Unveiling the links in Colon, Rectum, Pancreas, Liver, Bile Ducts and Gallbladder Malignancies
Alina Desiree Sandø - Evaluation of neoadjuvant chemotherapy in patients with resectable gastric adenocarcinoma in central Norway 2007-2016
I år presenterer Norsk Kirurgisk Forening et nytt og spennende symposium med tittelen «Den Akademiske Kirurgen» (bilde 1). Målet er å belyse viktigheten av forskning i det kirurgiske miljøet, samt å gjøre litt stas på kirurger som har disputert det forutgående året. Mens andre spesialitetsspesifikke symposier splitter fagmiljøet, samler dette symposiet hele det norske kirurgiske miljøet rundt et helt essensielt tema: Forskning og klinikk – muligheter og utfordringer. Symposiet byr på meget dyktige foredragsholder som på hver sin måte belyser temaet, med ulike innfallsvinkler basert på personlige erfaringer.
Hvorfor skal en kirurg drive med forskning? Redaskjonsmedlem i Kirurgen og transplantasjonskirurg på Rikshospitalet, Marte Bliksøen (bilde 2), kommer med flere viktige refleksjoner, men jeg har lyst å sitere henne på ett punkt: “Man blir en bedre kirurg gjennom å være en tenkende kirurg, og en tenkende kirurg blir man gjennom å forske”.
Noen kirurger vil kanskje ha en oppfatning om at en akademisk kirurg ikke er forenelig med å være en opererende kirurg, men thoraxkirurg JohnPeder Escobar Kvitting, fra Rikshospitalet presenterer tre pilarer i akademisk kirurgi, nemlig klinikk, forskning og utdanning.
For mange kirurger er det kanskje ikke mangel på motivasjon, men mangel på tid og ressurser, som gjør at forskningen ikke får plass i arbeidshverdagen. Christian Beisland, avdelingsleder på urologisk avdeling på Haukeland universitetssykehus illustrerer hvordan det er mulig å få med en hel avdeling, både overlegere og LIS, på å bygge opp et


3. Christian Beisland illustrerer med dette “enkle” flytskjemaet et “typisk” doktorgrads forløp.

“Man blir en bedre kirurg gjennom å være en tenkende kirurg, og en tenkende kirurg blir man gjennom å forske”
akademisk miljø på en kirurgisk avdeling (bilde 3). Et viktig element på veien til suksess er lagarbeid!
En viktig del av den akademiske kirurgien er også formidling. Nettopp slik vi gjør på Kirurgisk Høstmøte. En annen arena for formidling av forskning er selvsagt å publisere artikler i internasjonale og nasjonale tidsskrift. Dette kan for ferske forskere kanskje være en barriere, men det finnes en “oppskrift”: Redaktøren av Scandinavian Journal of Surgery, Paulina Salminen, gir oss en pragmatisk og strukturert metode for hvordan man bør utforme et manuskript for publikasjon.
Men selv om ikke alle kirurger skal drive med forskning, bør vi alle tilstrebe å utøve evidensbasert kirurgi. Vi er derfor prisgitt at noen av oss engasjerer seg i forskning. Det forutgående året for dette Høstmøte er det hele 12 dyktige kirurger som har disputert innen ulike kirurgiske spesialiteter, hvorav fire av dem tar oss med på deres forskningsreise gjennom «speeddisputasforedrag” (bilde 4).
Med fullsatt sal på årets nye symposium håper vi at suksessen gjentas til neste år – og at nye kirurger kan stå på podiet og bli gjort litt stas på for å ha fullførte doktorgradsarebid.

Hovedmålet med Ph.d. arbeidet mitt har vært å evaluere AAA screening som tilbys 65 år gamle menn i Oslo, som del av et forskningsprosjekt på karkirurgisk avdeling
ved Oslo Universitetssykehus.
SAIRA MAULAND MANSOOR
VESTRE VIKEN, BÆRUM SYKEHUS
KORRESPONDANSE: UXMSAI @ VESTREVIKEN.NO
Et abdominalt aortaaneurisme (AAA) er en utposning og svekkelse av abdominalaorta. Tilstanden er vanligvis asymptomatisk, men ved ruptur er tilstanden tilnærmet 100 % dødelig uten behandling. Mortaliteten ved rumpert AAA er rapportert å være opptil 80 % – mange pasienter dør før de ankommer sykehus, flere pasienter avslås for kirurgi og 30dagers mortalitet etter øhjelps kirurgi er også høy (1). Til sammenlikning er mortaliteten ved elektiv behandling (åpen kirurgi eller endovaskulær behandling) under 5 % (2). Dette illustrerer viktigheten av å avdekke tilstanden tidlig, slik at man kan overvåke og tilby preventiv behandling til pasienter med høy risiko for ruptur.
Lege Fernando Santiago skrev i 1987 i The Journal of the American Medical Association: “AAAs are silent and deep and lethal, like the Uboats of old, and like them they can be found by reflected sound waves and taken out before they torpedo the patient” (3). Fire store randomiserte kontrollerte studier fra Danmark, England og Australia, fra 80 og 90tallet, har vist at AAA screening med ultralyd blant menn > 65 år signifikant reduserer insidensen av rupturer og AAArelatert mortalitet (Figur 1) (46). Det finnes nasjonal screening i Sverige og i England, men også andre land i Europa er i gang med å etablere AAA screening.
I 2011 ble AAA screening for 65 år gamle menn startet som et forskningsprosjekt ved karkirurgisk avdeling på Oslo Universitetssykehus. Målet med mitt doktorgradsarbeid var å evaluere dette screeningprosjektet.
Først kartla vi epidemiologiske faktorer. Vi fant en AAAprevalens på 2,6 % blant 12810 menn som har møtt til screening i perioden 2011 til 2019 (7). Det var en synkende trend i den årlige AAAprevalensen (Figur 2). Røyking, hypertensjon, KMI > 30 og diabetes ble identifi
sert som risikofaktorer for AAA, hvor diabetes var negativt assosiert med AAA (7).
Ved oppfølging av screeningdeltakere som hadde fått påvist AAA, fant vi en absolutt rupturrate på 0,9 % etter en median oppfølgingstid på 7 år (8). Videre hadde 20 % blitt behandlet elektivt for sitt aneurisme (8). Uten screening hadde flere av disse aneurismene ikke blitt fanget opp, og dette indikerer at AAAscreening og overvåkning kan forebygge flere potensielle rupturer.
Det var tre menn med rumpert AAA blant menn som var invitert, men ikke hadde møtt til screening i perioden 2011 til 2019 (9). Årlig oppmøte var 6378 % (Figur 2). Nytten av screening forutsetter en høy oppslutning blant de inviterte, og de som ikke møter har muligens en økt risiko for AAA og ruptur. Ved forsøk på å kartlegge årsaker til at noen ikke møter, fant vi at den vanligste årsaken til å ikke møte på screening var at den inviterte hadde glemt innkallelsen (10). Å sende ut påminnelser kan i fremtiden bidra til økt oppslutning om screeningtilbudet. Videre synes sosioøkonomiske faktorer å påvirke screeningdeltakelse, blant annet faktorer som bosituasjon, hjemmesykepleie og utdannelse. Disse funnene støttes av at det var høyest forekomst av ikkedeltakere i bydelene Grorud og Grünerløkka, som i Oslo er blant de bydelene med lavest sosioøkonomisk status (Figur 3) (10).
Oppsummert synes AAA screeningprosjektet i Oslo å være relevant og effektivt, og kan være en motivator for å innføre nasjonal screening. Helsedirektoratet er nå i en prosess hvor det utredes og vurderes om det er relevant og kostnadseffektivt å innføre nasjonal AAAscreening.
LITTERATUR: Se bakerst i nettutgaven på kirurgen.no
FIGUR 1. Ultralydscreening av abdominalaorta. Bilde brukt med tillatelse fra: Peakstock/stock. adobe.com
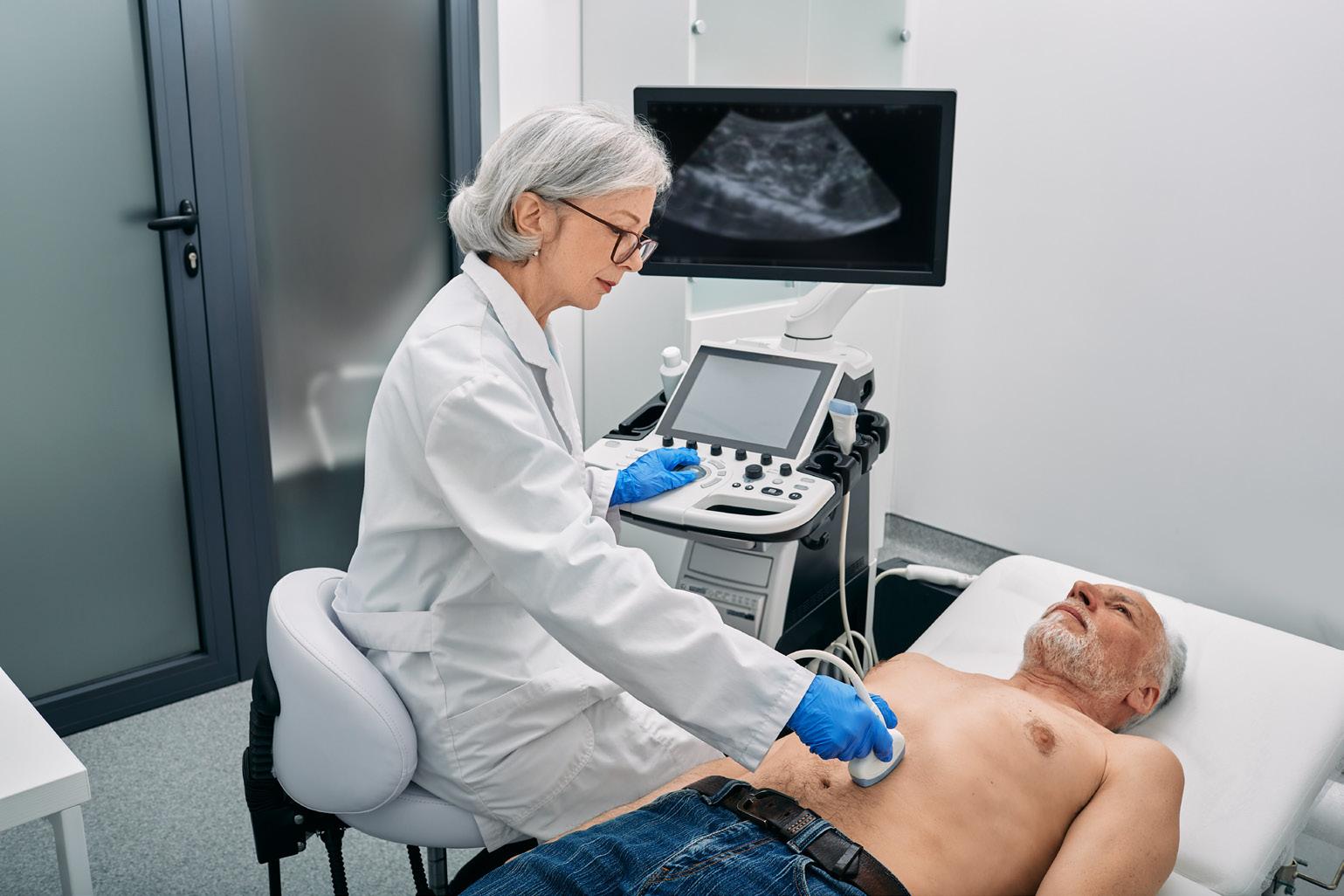
FIGUR 2. Årlig oppmøte til AAA screening og AAAprevalens. Figur reprodusert fra Rabben et al (7)
FIGUR 3. Menn invitert til screening i 2022 fordelt etter oppmøtestatus per bydel i Oslo. Ikke møtt = invitert, men ikke møtt til time uten varsel. Avbestilt = ringt og avbestilt timen uten å ønske nytt tidspunkt for screening. Invitasjon i retur = invitasjonsbrev komme i retur til sender. Figur reprodusert fra Mansoor et al (10).
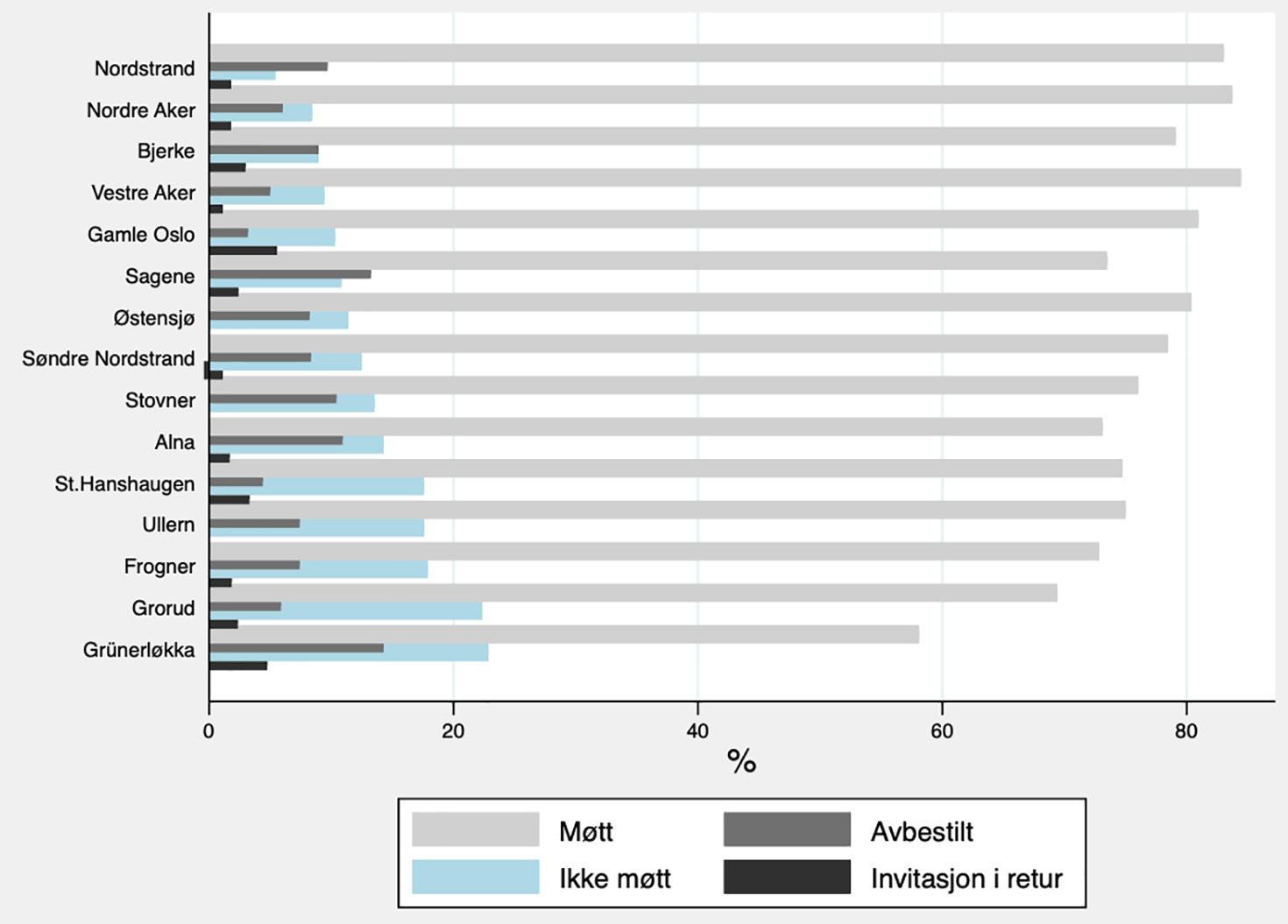
Hoveddelen av PhD-arbeidet mitt besto av et kvalitetsforbedringsarbeid rundt hoftebruddbehandling som er gjennomført, og fulgt opp, ved Ortopedisk avdeling, Bærum sykehus, Vestre Viken HF.
TOM LIAN ORTOPEDISK AVDELING, BÆRUM SYKEHUS KORRESPONDANSE: TOMLIA @ VESTREVIKEN.NO
Forskning på kvalitetsforbedring skiller seg fra tradisjonell forskning på en rekke punkter. Målet er å forbedre de underliggende prosessene til en behandling, som ifølge kjent forskning på enkeltfaktorene, er beste praksis. Det vil si at man går igjennom alle prosesser som fører en pasient igjennom et pasientforløp, for så å endre de prosessene som man tror vil føre til et bedre utfall for pasienten. Det er ikke et mål å undersøke enkeltfaktorer som førte til bedring i behandlingen, målet er derimot at summen av enkeltfaktorene vil være større enn enkeltfaktorene hver for seg.
I vårt prosjekt endret vi seks prosesser i behandlingen av hoftebrudd til beste praksis og fulgte etterlevelsen av disse endringene i åtte år. Vi sammenlignet så perioden før med perioden etter innføring av endringene og fant en reduksjon i komplikasjoner og reoperasjoner på ca. 60 %. For denne skjøre pasientgruppen er dette en betydelig forbedring.
I artikkel to samarbeidet jeg med Nasjonalt hoftebruddregister og så på bruken av forebyggende antibiotika ved operasjon for hoftebrudd. I 2013 kom det nasjonale retningslinjer for antibiotikaprofylakse. Vi så på i hvilken grad disse ble fulgt i Norge og med hvilken hastighet de
ble en del av behandlingsrutinene. Vi fant at tre år etter innføring av disse retningslinjene fikk 99,2 % riktig antibiotika, men i kun tre av fem tilfeller ble profylaksen gitt på riktig måte.
I den siste artikkelen samarbeidet jeg med Stian Svenøy ved Oslo Universitetssykehus for å beskrive en pasientgruppe som foreløpig ikke er beskrevet i noen særlig grad i litteraturen. Gruppen er pasienter med et nytt brudd rundt en halvprotese, som de tidligere fikk i forbindelse med et lårhalsbrudd. Vi fant at disse pasienten klarte seg omtrent likt som pasienter etter primære lårhalsbrudd, men at de hadde en klar økning i pleiebehov etterpå.
HVORFOR BEGYNTE JEG MED FORSKNING?
Jeg ble interessert i forskning for ca. 15 år siden. En av overlegene på den første avdelingen jeg jobbet ved var svært opptatt av forskning og av at alle assistentleger måtte lese og holde seg oppdaterte. Hans glød og entusiasme for forskning smittet over på flere av oss og jeg hadde derfor et ønske om å bidra med noe til forskningen selv. Etter at jeg byttet jobb møtte jeg min veileder Wender Figved. Jeg fortalte han at jeg var interessert i å startet med forskning og han tok meg med i et av hans prosjekter som da senere ble mitt hovedprosjekt i PhDen.
HVA HAR JEG LÆRT AV FORSKNING?
Jeg har lært utrolig mye. PhD slik det er lagt opp i dag er først og fremst en skole for folk som er interessert i forskning. Jeg husker at jeg lærte om hypotetisk deduktive og hermeneutisk metode en gang på Exphil i 1995. Den gangen skjønte jeg ingen ting av hvorfor jeg hadde behov for denne kunnskapen. Men nå har jeg i løpet av årene som jeg har jobbet med PhDen fått en klar forståelse av både disse begrepene samt forskningsmetoder og hvorfor jeg må kunne noe om det for å drive med forskning. Jeg har også hatt en rekke statistikkurs som er uvurderlige når man både skal drive med egen forskning og forstå andres forskning. Når det gjelder mer konkret lærdom så tror jeg at jeg forstå mye bedre nå hvordan ting henger sammen. Hvordan en prosess inne i et sykehus påvirker andre prosesser og hva det kan føre til dersom man endrer på disse, både i positiv og negativ forstand.
KAN JEG DRA NYTTE AV LÆRDOM FRA
DOKTORGRADEN I MITT KLINISKE VIRKE?
Ja. Endring er en del av livet på et sykehus. Nye metoder dukker opp, måter å jobbe på endres og vi må stadig tilpasse oss nye arbeidssituasjoner. Hvordan dette påvirker
kvaliteten på behandlingen vi tilbyr våre pasienter er dessverre ikke alltid en del av regnestykket. Vi må derfor ta en aktiv del i endringen slik at vi i størst mulig grad unngår endringer som har negativ påvirkning. Vi må forstå hvordan endringene påvirker både pasientene, men også de som jobber i systemet. Gjennom mitt arbeid har jeg fått en mye større forståelse av systemene som ligger til grunn for alt vi gjør. Husk for eksempel at vaskepersonalet, sterilsentralen og operasjonssykepleieren er like viktig som kirurgen for at operasjonsstuene skal driftes.
TIPS TIL KIRURGER SOM ØNSKER
Å BEGYNNE MED FORSKNING
Begynn med å sett deg inn i litteraturen. Finn noe du interesserer deg for og begynn med å stille spørsmål. Så må du finne deg en engasjert veileder. Det gjør det hele så mye lettere. Og til slutt sørg for at du får tid til å drive med forskningen. Alt for mange kirurger driver forskning, meg selv inkludert dessverre, på siden av vanlig arbeidstid. Jeg skjønner at man som kirurg er opptatt av knivtid, og det er viktig, men, skal du drive med forskning, uten å slite deg fullstendig ut, må du ha tid.



INFLAMMATORISKE TARMSYKDOMMER
Multimodal prehabilitering
Tverrfaglige tilnærminger
Komplekse pasienter
Oppfølging
KOLOREKTALE POLYPPER OG TIDLIGE CANCERE
Klassifisering og risikovurdering
Endoskopisk behandling
Multidisiplinære polyppmøter
PANELDISKUSJONER OG KASUISTIKKER

PRIS: 7600,INKLUDERER - KONFERANSEAVGIFT - OVERNATTING 2 DØGN - MÅLTIDER
PÅMELDING OG PROGRAM

19.
15:00 20:00 Innsjekking og registrering 20:00 Middag
21:30 "Get together"
TORSDAG 20. STORE KOLOREKTALE POLYPPER OG TIDLIG CANCER
06:30 08:00 Frokost
07:30 07:45 Registrering
08:00 08:05 Velkommen styret i NFKK
KOLON
08:05 08:10 Kort kasuistikk (video)
08:10 08:35 Utredning og malignitetsvurdering av C. Rushfeldt /kolonpolypper J.A. Nilsen
08:35 08:55 Tidlig cancer: klassifisering og risiko for lymfatisk metastasering S. Steigen
08:55 09:05 Tverrfaglig polyppmøte (MDT): organisering og foreløpige erfaringer J.A. Nilsen
09:05 09:25 Endoskopisk submukosal disseksjon (ESD) og endoskopisk mukosal reseksjon (EMR) J.A. Nilsen
09:25 09:45 Kaffepause / besøke stands
09:45 10:05 Endoskopisk fullveggsreseksjon (EFTR) C. Rushfeldt
10:05 10:25 Oppfølging etter ESD, EMR og EFTR J. A. Nilsen /for T1 cancer C. Rushfeldt
10:25 11:00 Kasuistikker / paneldiskusjon alle forelesere
11:00 11:10 Industripresentasjon ved Medtronic
11:10 Lunsj
14:30 15:00 Kaffe / besøke stands
REKTUM
15:00 15:20 Utredning og vurdering av rektale polypper og tidlig cancer: CT/MR/endoskopisk ultralyd A. Nesbakken
15:20 15:40 Endoskopisk behandling av tidlig cancer C. Rushfeldt
15:40 15:55 Transanal minimaltinvasiv kirurgi (TAMIS) T. Stornes
15:55 16:10 Transanal endoskopisk mikrokirurgi (TEM) A. Nesbakken
16:10 16:30 TAMIS/TEM vs. endoskopisk reseksjon/ paneldiskusjon alle forelesere
16:30 16:50 Kaffe / besøke stands
16:50 17:20 Supplerende kirurgi etter lokal reseksjon av T1 cancer T. Stornes
17:20 17:40 Behandling av kolorektal T1 cancer i Sverige P. Buchwald
17:40 18:20 Indikasjoner for lokal reseksjon og ansvar for videre oppfølging / paneldiskusjon alle forelesere
20:00 Middag
FREDAG 21. INFLAMMATORISK TARMSYKDOM
08:00 08:30 Medisinsk behandling hva må kirurgen vite? M. Høivik
08:30 09:00 Multimodal prehabilitering før kirurgi M. Soop
09:00 09:30 Ileocøkal reseksjon og anastomoseteknikk ved Crohns sykdom A. Tøttrup
09:30 10:05 Inflammatorisk tarmsykdom hos barn hva må kirurgen vite? G. Perminow
10:05 10:25 Kaffe / besøke stands
10:25 11:05 Vurdering og kirurgisk strategi ved behandling av kompleks Crohns sykdom M. Soop
11:05 11:45 Kasuistikker / paneldiskusjon alle forelesere
11:45 12:30 Lunsj
12:30 13:00 Kolektomi med ileorektal anastomose hos pasienter med ulcerøs kolitt P. Buchwald
13:00 13:30 Pouchkirurgi hos pasienter med ulcerøs kolitt A. Tøttrup
13:30 14:00 Oppfølging av pasienter med ulcerøs kolitt M. Høivik
14:00 14:30 Kasuistikker / paneldiskusjon alle forelesere
14:30 14:45 Avsluttende ord styret i NFKK
Jan 30-31, 2025
Venue: This is a hybrid meeting onsite at the main auditorium at Akershus University Hospital, Lørenskog or via Zoom participation
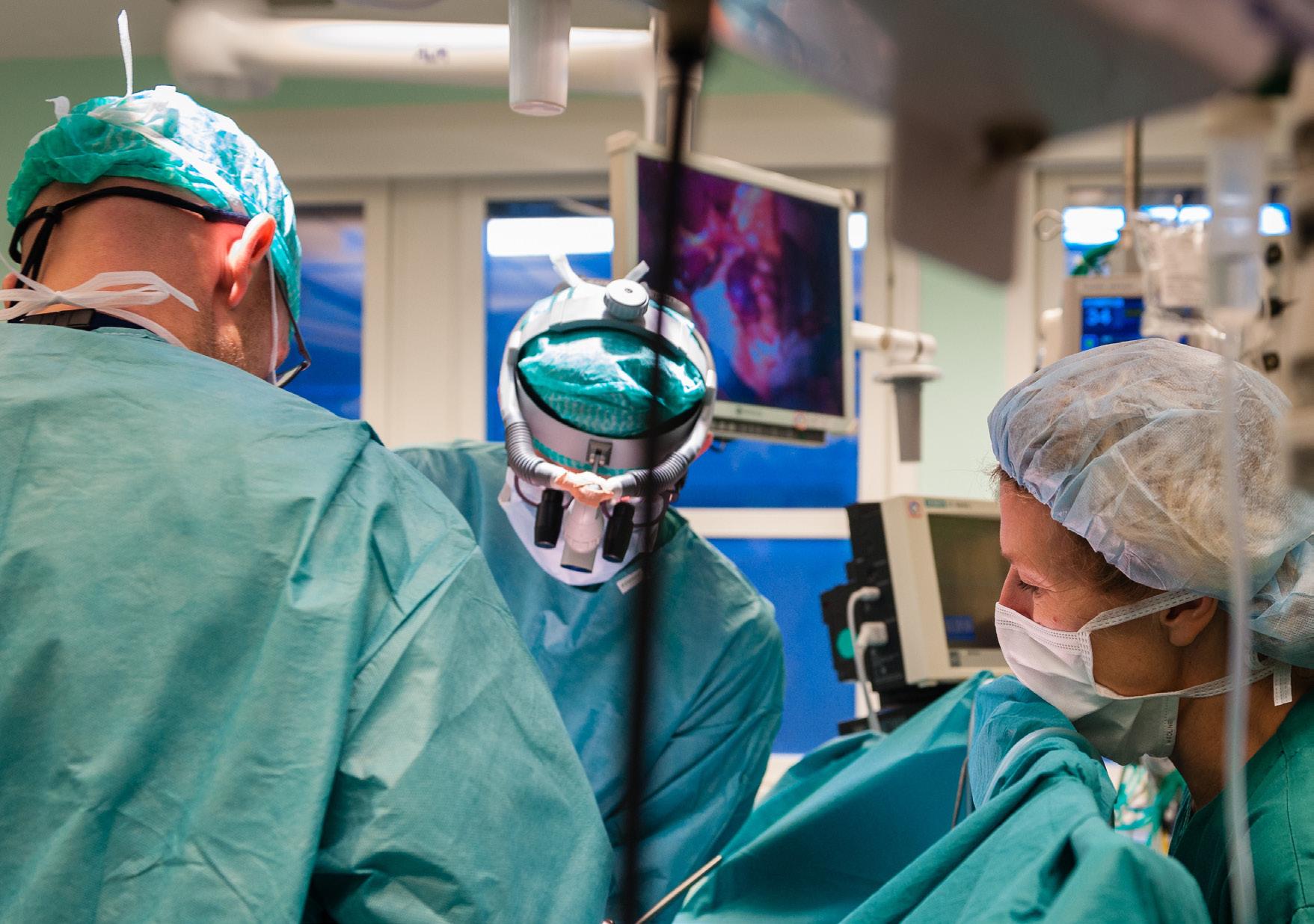
Thursday January 30th 9.00 – 16.30 Colon cancer
Register 08.30
Welcome 09.00
Oral antibiotic bowel Preparation in colorectal cancer, the Mobile trials 09.10
Stoma construction and (early) closure - how to prevent complications 09.30
Early onset CRC 09.50 Coffee 10.10
Endoscopic removal of early colon cancer and polyp scars 10.30
Hybrid wedge resection of early colon cancer 10.50
Immunotherapy of colon cancer 11.10
Surgery after immunotherapy, if, when and how
Panel debate: Do surgeons become superfluous in colon cancer treatment 11.40 Lunch 12.30
Robot assisted versus laparoscopic approach to colon cancer 13.30
Augestad/Schultz
Laura Koskenvuo, FI
Eva Angenete, SE
Anna Martling, SE
Nastazja Pilonis, PL
Erik van Westreenen, NL
Åse Dahle-Smith, Ahus
Erik Kjæstad, Ahus
Pedja Cuk, DK
Ritch Geitenbeek, NL Robotic colorectal surgery – just a cost driver or fundamental improvement?
Indocyanine Green Fluorescence (ICG) – just a hype or a useful adjunct?
Acetylsalicylic acid after colorectal cancer resection – ALASCCA results 14.30
Coffee 14.50
Roel Hompes, NL
Anna Martling, SE
Laurids Poulsen, DK (Neo-) adjuvant treatment of colon cancer – line between over- and undertreatment
MDT meeting colon cancer (3 cases)
Adjourn 16.30
Friday January 31st 09.00 – 14.00 Rectal cancer
Role of MRI staging and restaging of rectal cancers 09.00
Total neoadjuvant therapy in rectal cancer – controversies and future directions 09.20
Intentional watch and wait in early rectal cancer (WW1 & 2 trial Denmark) 09.40
Opportunistic watch and wait strategies (WOW study Sweden) 10.00
Coffee 10.20
Pitfalls of watch and wait strategies – organ preservation at any price? 10.40
Surgical approach to early rectal cancer 11.00
Endoscopic approach to early rectal cancer 11.20
Lunch 11.40
Panel debate: International differences in (neo-)adjuvant treatment strategies 12.30
MDT rectal cancer (2 cases) 13.15
Adjourn 14.00
Anne Negård, Ahus
Anne Hansen Ree, Ahus
Laurids Poulsen, DK
Eva Angenete, SE
Johannes K Schultz, Ahus
Roel Hompes, DK
Nastazja Pilonis, PL
1. Kenneth J. Rothman, Krista F. Huybrechts, Elenor J. Murray. Epidemiology – An Introduction, 3rd edition, Oxford University Press, USA, October 2024.
2. Diederick E. Grobbee, Arno W. Hoes. Clinical Epidemiology: Principles, Methods, and Applications for Clinical Research, 2nd edition, Jones and Bartletts Publishers, Inc., USA, 2014.
3. Xu H, Bretthauer M, Fang F et al. Dramatic improvements in outcome following pancreatoduodenectomy for pancreatic and periampullary cancers. Br J Cancer 2024;131:74754.
4. Dickman P, Adami HO. Interpreting trends in cancer patient survival. J Int Med 2006;260:103-17.
5. Pinczowski D, Ekbom A, Baron J et al. Risk factors for colorectal cancer in patients with ulcerative colitis: a case-control study. Gastroenterology 1994;107:117-20.
6. Kalager M, Adami HO, Lagergren P et al. Cancer outcomes research - a European challenge Measures of the cancer burden. Mol Oncol 2021:3225-41.
7. Ioannidis JP. Why most published research findings are false. PLoS Med 2005;2:e124.
8. Ioannidis JP. How to make more published research true. PLoS Med 2014;11:e1001747.
9. Feynman, R. P. 1., Robbins, J. The pleasure of finding things out: the best short works of Richard P. Feynman. Cambridge, Mass., Perseus Books 1999.
1. Shabana Rehman, Kreft | Samlet inn én million kroner til kreftbehandling: Nå drar hun til Tyskland (sett 20.10.24).
2. Evensen S. Etikkvurdering ved innføring av ny behandling. Tidsskr Nor Legeforen 2011;131:1276
3. Forskrift om prioritering av helsetjenester, rett til nødvendig helsehjelp fra spesialisthelsetjenesten og rett til behandling i utlandet (prioriteringsforskriften) - Lovdata (lest 20.10.24)
4. Saker behandlet av Prioriteringsrådet 2007-2017 - Helsedirektoratet (sett 20.10.24)
5. Freedman, B. Equipoise and the ethics of clinical research. N Engl J Med 1987;317:141145
6. Forside - Nye metoder (sett 20.10.24)
7. Kunnskapsbasertpraksis.no - Helsebiblioteket (sett 20.10.24)
8. Ardaugh BM, Graves SE, Redberg RF. The 510(k) ancestry of ametal-on-metal hip implant. N Engl J Med. 2013;368:97-100.
9. O’Dowd A. French women to have PIP breast implants removed for free. BMJ. 2011;343:d8329.
ER EN DEL AV GOD FORSKNING
1. Lov om organisering av forskningsetisk arbeid (forskningsetikkloven) Lovdata2017 [Available from: https://lovdata.no/dokument/NL/lov/2017-04-28-23.
2. Prop. 158 L (2015 – 2016). Lov om organisering av forskningsetisk arbeid (forskningsetikkloven), (2015-2016).
3. Garrett N, Lazzaro SC, Ariely D, Sharot T. The brain adapts to dishonesty. Nat Neurosci. 2016;19(12):1727-32.
4. ALLEA. The European Code of Conduct for Research Integrity. Revised 2023 ed. Berlin 2023.
5. Generelle forskningsetiske retningslinjer [Available from: https://www.forskningsetikk.no/retningslinjer/generelle/.
6. Gunsalus CK, Robinsom, A. D. Nine pitfalls of research misconduct. Nature. 2018;557:297-9.
7. Kalleberg R. Robert K. Merton:A Modern Sociological Classic. Journal of Classical Sociology. 2007;7(2):131-6.
8. Paper Mills - Research Report from COPE & STM 2022 [updated June 2022. 1:[1-15]. Available from: https://doi.org/10.24318/jtbG8IHL.
9. Else H. Multimillion-dollar trade in paper authorships alarms publishers. Nature. 2023;613:617-8.
10. Van Noorden R. More than 10,000 research papers were retracted in 2023 - a new record. Nature. 2023.
11. Register over vitenskapelige publiseringskanaler [Available from: https://kanalregister.hkdir.no/publiseringskanaler/Forside/.
12. Hofmann B, Bredahl Jensen L, Eriksen MB, Helgesson G, Juth N, Holm S. Research Integrity Among PhD Students at the Faculty of Medicine: A Comparison of Three Scandinavian Universities. J Empir Res Hum Res Ethics. 2020;15(4):320-9.
13. Paterlini M. Paolo Macchiarini: Disgraced surgeon is sentenced to 30 months in prison. BMJ. 2023;381:p1442.
14. Berggren C, Karabag SF. Scientific misconduct at an elite medical institute: The role of competing institutional logics and fragmented control. Research Policy. 2018;48(2):428-43.
15. Lov om universiteter og høyskoler (universitets- og høyskoleloven) Lovdata2024 [Available from: https://lovdata.no/dokument/NL/lov/2024-03-08-9.
16. Lov om medisinsk og helsefaglig forskning (helseforskningsloven): Lovdata; 2008 [Available from: https://lovdata.no/dokument/NL/lov/2008-06-20-44.
17. Leading by example. Nature. 2007;445(7125):229-.
18. Forskningsgrupper – etablering av forskningsgrupper og funksjonsbeskrivelse for forskningsgruppeledere (e-håndbok) [Available from: https://ehandboken.ous-hf. no/document/4018.
1. Wartolowska K, Judge A, Hopewell S, Collins GS, Dean BJ, Rombach I, et al. Use of placebo controls in the evaluation of surgery: systematic review. BMJ (Clinical research ed. 2014;348:g3253.
2. Firanescu CE, de Vries J, Lodder P, Venmans A, Schoemaker MC, Smeets AJ, et al. Vertebroplasty versus sham procedure for painful acute osteoporotic vertebral compression fractures (VERTOS IV): randomised sham controlled clinical trial. BMJ (Clinical research ed. 2018;361:k1551.
3. Sihvonen R, Paavola M, Malmivaara A, Itala A, Joukainen A, Nurmi H, et al. Arthroscopic Partial Meniscectomy versus Sham Surgery for a Degenerative Meniscal Tear. N Engl J Med. 2013;369(26):2515-24.
4. Pihl E, Laszlo S, Rosenlund AM, Kristoffersen MH, Schilcher J, Hedbeck CJ, et al. Operative versus Nonoperative Treatment of Proximal Hamstring Avulsions. NEJM Evid. 2024;3(8):EVIDoa2400056.
5. Myhrvold SB, Brouwer EF, Andresen TKM, Rydevik K, Amundsen M, Grun W, et al. Nonoperative or Surgical Treatment of Acute Achilles’ Tendon Rupture. N Engl J Med. 2022;386(15):1409-20.
6. Stiggelbout AM, Van der Weijden T, De Wit MP, Frosch D, Legare F, Montori VM, et al. Shared decision making: really putting patients at the centre of healthcare. BMJ (Clinical research ed. 2012;344:e256.
S210: KVALITETSFORBEDRING – THE MISSING LINK FOR KIRURGER?
1. Forbedringsguiden. Teorier, tips og verktøy for forbedringsarbeid i helse- og omsorgstjenesten. Itryggehender 24-7. Tilgjengelig fra: www.itryggehender24-7.no/kvalitetsforbedring/forbedringsarbeid/her-kan-du-laste-ned-forbedringsguiden
S214: FORSKNING UTENFOR UNIVERSITETSSYKEHUSENE
1. Nasjonal handlingsplan for kliniske studier 2021-2025 - regjeringen.no
2. Petersen, A. Finansielle besparelser som følger av innføring av kliniske studier. https://www.duo.uio.no/bitstream/handle/10852/96009/Kandidatnummer-113-HADM4502-v-ren-2022.pdf?sequence=1
3. Dagens Medisin: Antallet kliniske studier i Norge har falt. På denne avdelingen peker pilene oppover. https://www.dagensmedisin.no/akershus-universitetssykehus-ahus-klinisk-forskning-kliniske-studier/antallet-kliniske-studier-i-norge-har-falt-pa-denne-avdelingen-peker-pilene-oppover/626609Strategiske forskningsmidler til ikke-universitetssykehus 2025 - Helse Sør-Øst RHF. https:// www.helse-sorost.no/helsefaglig/forskning/forskningsmidler/strategiske-forskningsmidler-til-ikke-universitetssykehus/
1. Curcic D. Number of Academic Papers Published Per Year. Wordsrated 1.6.2023. https:// wordsrated.com/number-of-academic-papers-published-per-year/ Lest 10.10.2024.
2. Brean A. Røverne kommer! Tidsskr Nor Legeforen 2024;144.doi: 10.4045/tidsskr.24.0332.
3. Linacre S. Mountain to climb. Cabells The Source 1.10.2021. https://blog.cabells. com/2021/09/01/mountain-to-climb/ Lest 10.10.2024.
4. Brainard J. Fake scientific papers are alarmingly common. Science 9.5.2023. https:// www.science.org/content/article/fake-scientific-papers-are-alarmingly-common Lest 10.10.2024.
5. Directory of Open Access Journals. https://www.doaj.org/
6. Register over vitenskapelige publiseringskanaler. https://kanalregister.hkdir.no/publiseringskanaler/Forside/
7. JBI Critical Appraisals Tools. https://jbi.global/critical-appraisal-tools (lest 25.10.2024).
8. CASP Critical Appraisal Checklists . https://casp-uk.net/casp-tools-checklists/ (lest 25.10.2024).
9. CBM Critical Appraisal tools. https://www.cebm.ox.ac.uk/resources/ebm-tools/critical-appraisal-tools (lest 25.10.2024).
1. Schrøder CP, Skare Ø, Gjengedal E et al. Long-term results after SLAP repair: a 5-year follow-up study of 107 patients with comparison of patients aged over and under 40 years. Arthroscopy. 2012;28(11):1601-7.
2. Schroder CP, Skare Ø, Reikeraå O et al.Sham surgery versus labral repair or biceps tenodesis foø type II SLAP lesions of the shoulder: a three-armed randomised clinical trial. Br J Sports Med. 2017;51(24):1759-66.
3. Kilbourne AM, Glasgow RE, Chambers DA. What Can Implementation Science Do for You? Key Success Stories from the Field. J Gen Intern Med. 2020;35(Suppl 2):783-7.
4. Levine JD, Gordon NC, Fields HL. The mechanism of placebo analgesia. Lancet. 1978;2(8091):654-7.
5. Benedetti F. The opposite effects of the opiate antagonist naloxone and the cholecystokinin antagonist proglumide on placebo analgesia. Pain. 1996;64(3):535-43.
6. Evers AWM, Colloca L, Blease C et al. Implications of Placebo and Nocebo Effects for Clinical Practice: Expert Consensus. Psychother Psychosom. 2018;87(4):204-10.
7. Kaptchuk TJ, Hemond CC, Miller FG. Placebos in chronic pain: evidence, theory, ethics, and use in clinical practice. BMJ. 2020;370:m1668.
8. Holtedahl R, Brox JI, Tjomsland O. Placebo effects in trials evaluating 12 selected minimally invasive interventions: a systematic review and meta-analysis. BMJ Open. 2015;5(1):e007331.
9. Benedetti F, Shaibani A, Arduino C et al. Open-label nondeceptive placebo analgesia is blocked by the opioid antagonist naloxone. Pain. 2023;164(5):984-90.
10. Benedetti F, Barbiani D, Camerone E. Critical Life Functions: Can Placebo Replace Oxygen? Int Rev Neurobiol. 2018;138:201-18.
11. Carvalho C, Caetano JM, Cunha L et al.Open-label placebo treatment in chronic low back pain: a randomized controlled trial. Pain. 2016;157(12):2766-72.
12. Buergler S, Sezer D, Bagge N etal. et al. Imaginary pills and open-label placebos can reduce test anxiety by means of placebo mechanisms. Sci Rep. 2023;13(1):2624.
13. Colloca L, Sigaudo M, Benedetti F. The role of learning in nocebo and placebo effects. Pain. 2008;136(1-2):211-8.
14. Shapson-Coe A, Januszewski M, Berger DR et al. A petavoxel fragment of human cerebral cortex reconstructed at nanoscale resolution. Science. 2024;384(6696):eadk4858.
15. Paavola M, Malmivaara A, Taimela S et al. Subacromial decompression versus diagnostic arthroscopy for shoulder impingement: randomised, placebo surgery controlled clinical trial. BMJ. 2018;362:k2860.
16. Beard DJ, Rees JL, Cook JA et al. Arthroscopic subacromial decompression for subacromial shoulder pain (CSAW): a multicentre, pragmatic, parallel group, placebo-controlled, three-group, randomised surgical trial. Lancet. 2017.
17. Sihvonen R, Paavola M, Malmivaara A et al. Arthroscopic partial meniscectomy versus sham surgery for a degenerative meniscal tear. NEnglJMed. 2013;369(26):251524.
18. Randers EM, Gerdhem P, Stuge B et al. The effect of minimally invasive sacroiliac joint fusion compared to sham operation: a double-blind randomized placebo-controlled trial. EClinicalMedicine. 2024;68:102438.
19. Buchbinder R, Osborne RH et al. A randomized trial of vertebroplasty for painful osteoporotic vertebral fractures. NEnglJ Med. 2009;361(6):557-68.
20. Kallmes DF, Comstock BA, Heagerty P et al. A Randomized Trial of Vertebroplasty for Osteoporotic Spinal Fractures. New England Journal of Medicine. 2009;361(6):56979.
21. Al-Lamee R, Thompson D, Dehbi HM et al. Percutaneous coronary intervention in stable angina (ORBITA): a double-blind, randomised controlled trial. Lancet. 2018;391(10115):31-40.
22. Abbasi AB, Cifu AS. Why some Patients Benefit from Participating in a Sham Surgery Trial. Ann Surg. 2024;279(4):577-82.
23. London AJ, Kadane JB. Placebos that harm: sham surgery controls in clinical trials. Stat Methods Med Res. 2002;11(5):413-27.
24. Macklin R. The ethical problems with sham surgery in clinical research. N Engl J Med. 1999;341(13):992-6.
25. The Lumbar Interbody Fusion vs. Multidisciplinary Rehabilitation (LIFEHAB) Trial (LIFEHAB) ClinicalTrials.gov ID NCT06169488.
26. The clinical and cost-effectiveness of lumbar fusion surgery for patients with persistent , severe low back pain. NIHR 134859.
27. Kgomotso EL, Hellum C, Fagerland MW et al. Decompression alone or with fusion for degenerative lumbar spondylolisthesis (Nordsten-DS): five year follow-up of a randomised, multicentre, non-inferiority trial. BMJ. 2024;386:e079771.
28. Prasad V, Vandross A, Toomey C et al. A decade of reversal: an analysis of 146 contradicted medical practices. Mayo ClinProc. 2013;88(8):790-8.
1. Duits LC, Phoa KN, Curvers WL, Ten Kate FJ, Meijer GA, Seldenrijk CA, et al. Barrett’s oesophagus patients with low-grade dysplasia can be accurately risk-stratified after histological review by an expert pathology panel. Gut. 2015;64(5):700-6.
2. Weusten BLAM, Bisschops R, Dinis-Ribeiro M, di Pietro M, Pech O, Spaander MCW, et al. Diagnosis and management of Barrett esophagus: European Society of Gastrointestinal Endoscopy (ESGE) Guideline. Endoscopy. 2023(EFirst).
3. Bergman J, de Groof AJ, Pech O, Ragunath K, Armstrong D, Mostafavi N, et al. An Interactive Web-Based Educational Tool Improves Detection and Delineation of Barrett’s Esophagus-Related Neoplasia. Gastroenterology. 2019;156(5):1299-308.e3.
4. Wani S, Holmberg D, Santoni G, Kauppila JH, Farkkila M, von Euler-Chelpin M, et al. Magnitude and Time-Trends of Post-Endoscopy Esophageal Adenocarcinoma and Post-Endoscopy Esophageal Neoplasia in a Population-Based Cohort Study: The Nordic Barrett’s Esophagus Study. Gastroenterology. 2023;165(4):909-19.e13.
5. Fitzgerald RC, di Pietro M, O’Donovan M, Maroni R, Muldrew B, Debiram-Beecham I, et al. Cytosponge-trefoil factor 3 versus usual care to identify Barrett’s oesophagus in a primary care setting: a multicentre, pragmatic, randomised controlled trial. Lancet. 2020;396(10247):333-44.
6. Shaheen NJ, Odze RD, Singer ME, Salyers WJ, Srinivasan S, Kaul V, et al. Adjunctive Use of Wide-Area Transepithelial Sampling-3D in Patients With Symptomatic Gastroesophageal Reflux Increases Detection of Barrett’s Esophagus and Dysplasia. Official journal of the American College of Gastroenterology | ACG. 2024;119(10).
7. Pilonis ND, Killcoyne S, Tan WK, O’Donovan M, Malhotra S, Tripathi M, et al. Use of a Cytosponge biomarker panel to prioritise endoscopic Barrett’s oesophagus surveillance: a cross-sectional study followed by a real-world prospective pilot. Lancet Oncol. 2022;23(2):270-8.
8. Killcoyne S, Fitzgerald RC. Evolution and progression of Barrett’s oesophagus to oesophageal cancer. Nat Rev Cancer. 2021;21(11):731-41.
S230: HVORDAN KOMME I GANG?
1. https://lovdata.no/dokument/NL/lov/1999-07-02-61#KAPITTEL_3
2. https://www.helsedirektoratet.no/tema/autorisasjon-og-spesialistutdanning/spesialistutdanning-for-leger/generell-kirurgi/felles-kompetansemal?query=forskningsforstaelse#utdypende_1436f234-185e-4cb7-b3dd-3ea85c37091d1.
3. Schein M, Farndon JR, Fingerhut A. Why should a surgeon publish? Br J Surg. 2000 Jan;87(1):3-5
4. Schein M, Schein H, Wise L. Rudolf Nissen: the man behind the fundoplication. Surgery. 1999 Mar;125(3):347-53.
5. Popper KR. 1983. Realism and the aim of science. Hutchin & son & Co., London.
6. Jiwa M. Doctors and medical science. Australas Med J. 2012;5(8):462-7
7. Harding KE, Porter J, Horne-Thompson A, Donley E, Taylor NF. Not Enough Time or a Low Priority? Barriers to Evidence-Based Practice for Allied Health Clinicians. Journal of Continuing Education in the Health Professions 2014: 34(4):224–231
8. White, J, Grant, K, Sarkies, M Haines T. Translating evidence into practice: a longitudinal qualitative exploration of allied health decision-making. Health Res Policy Syst 2021; 19: 38
9. Slade SC, Philip K, Morris ME. Frameworks for embedding a research culture in allied health practice: a rapid review. Health Res Policy Sys 2018; 16: 29
10. Schweder LJ Forskning er ikke bare en lovpålagt oppgave. Overlegen 2020; (3): 24-25
1. Bismuth H. Discovery and Innovation in Surgery. Chance and Necessity. Ann Surg 2021;274:688–689
2. Gagner M. Pioneers in laparoscopic solid organ surgery. Surg Endosc. 2003 Nov;17(11):1853-4
3. Borel JF. History of the discovery of cyclosporin and of its early pharmacological development. Wien Klin Wochenschr. 2002. 114(12): p. 433-7.
4. Monod J. On Chance and Necessity. In: Studies in the Philosophy of Biology; Springer: 357–75
5. Vieira RM, Tenreiro-Vieira C, Martins IP. Critical thinking: Conceptual clarification and its importance in science education. Science Education International 2011; 22 (1): 43-54
6. Ness RB. Promoting innovative thinking. Am J Public Health. 2015;105 Suppl 1(Suppl 1):S114-8
7. Arksey H. RSI and the experts: The construction of medical knowledge, UCL Press, London, 1998
8. Arroyo NA, Gessert T, Hitchcock M, Tao M, Smith CD, GreenbergC, Fernandes-Taylor S, Francis DO. What Promotes Surgeon Practice Change? A Scoping Review of Innovation Adoption in Surgical Practice. Ann Surg. 2021 Mar 1;273(3):474-482.
9. McCulloch P, Altman DG, Campbell WB, Flum DR, Glasziou P, Marshall JC, et al. No surgical innovation without evaluation: the IDEAL recommendations. Lancet. 2009 Sep 26;374(9695):1105-12.
10. Marusic M, Markulin H, Lukic IK, Marusic A. Academic advancement of authors receiving tutoring from a medical journal. Teach Learn Med. 2006;18(2):126-9.
11. Schulz KF, Altman DG, Moher D, CONSORT Group. CONSORT 2010 Statement: updated guidelines for reporting parallel group randomised trials. BMC Med. 2010 Mar 24;8:18.
12. Liberati A, Altman DG, Tetzlaff J, Mulrow C, Gøtzsche PC, Ioannidis JP, Clarke M, Devereaux PJ, Kleijnen J, Moher D. The PRISMA statement for reporting systematic reviews and meta-analyses of studies that evaluate healthcare interventions: explanation and elaboration. BMJ. 2009 Jul 21;339:
13. Bion J. Financial and intellectual conflicts of interest: confusion and clarity. Curr Opin Crit Care 2009; 15 (6): 583-590
14. Kushner AL, Kyamanywa P, Adisa CA, Kibatala P, Mkandawire N, Coleman P, Kamara TB, Mock CN, Hunter JG. Editorial policy on co-authorship of articles from low- and middle-income countries. World J Surg 2011; 35:2367–2368
15. https://www.icmje.org/recommendations/browse/roles-and-responsibilities/defining-the-role-of-authors-and-contributors.html
16. Haak LL, Fenner M, Paglione L, Pentz E. Ratner H. ORCID: a system to uniquely identify researchers. Learned Publishing 2012; 25:259–264
17. Derish PA, Maa J, Ascher NL, Harris HW. Enhancing the mission of academic surgery by promoting scientific writing skills. J Surg Res. 2007 Jun 15;140(2):177-83.
18. Djulbegovic B, Guyatt GH. Progress in evidence-based medicine: a quarter century on. Lancet 2017;390(10092):415-423
19. Ajiferuke I, Wolfram D. Citer analysis as a measure of research impact: library and information science as a case study. Scientometrics. 2010; 83(3): 623−638
20. Pepe A, Kurtz MJ. A Measure of total research impact independent of time and discipline. PLoS ONE 2012;7(11): e46428.
21. Weart SR. Scientists with a Secret. Physics Today 1976; 29(2): 23–30
22. Tomasoni T, Coats AJS. The Altmetric Attention Score: how science tries to meet social media. Eur J Heart Fail . 2021 May;23(5):693-697.
23. Araujo AC, Vanin AA, Nascimento DP, Gonzalez GZ, Costa LOP. What are the variables associated with Altmetric scores? Syst Rev. 2021 Jun 30;10(1):193.
S238: FORMIDLING AV FORSKNINGEN I MODERNE TID – BEDRE TILGANG, NYE MEDIER OG FAGFELLEROLLEN
1. Cockerill MJ, Norton M. Open-access journals are delivering high impact, and more. Lancet. 2008 Jun 21;371(9630):2084
2. Hagve M. Pengene bak vitenskapelig publisering. Tidsskr Nor Laegeforen. 2020 Aug 17;140(11).
3. https://www.ub.uio.no/skrive-publisere/open-access/dokumenter/
4. https://www.forskningsradet.no/forskningspolitikk-strategi/apen-forskning/publikasjoner/
5. https://research-and-innovation.ec.europa.eu/strategy/strategy-2020-2024/our-digital-future/open-science/open-access_en
6. Toner M, Tompkins RG. Invention, innovation, entrepreneurship in academic medical centers. Surgery. 2008 Feb;143(2):168-71.
7. Medical innovation: science, technology and practice. Edited by Consolo D, Mina A, Nelson RR, Ramlogan R. Taylor & Francis, London/New York: 97
8. Bismuth H. Discovery and Innovation in Surgery. Chance and Necessity. Ann Surg 2021;274:688–689
9. Beall J. Predatory publishers are corrupting open access. Nature 2012; 489: 179.
10. Bohannon J. Who’s afraid of peer review? Science 2013; 342: 60 – 5.
11. Hem E. Se opp for røvertidsskrifter. Tidsskr Nor Legeforen 2014; 134: 1273.
12. Harvey E, Ball CG. Predatory journal publishing: Is this an alternate universe? Can J Surg. 2021 Jun 9;64(3):E358.
13. Kwon D. Open-access journal eLife announces ‘preprint first’ publishing model. Nature. 2020 Dec 15. Online ahead of print.
14. Hem E. På både norsk og engelsk. Tidsskr Nor Legeforen 2012; 132: 1201 – 2.
15. Ruano-Ravina A, Alvarez-Dardet C. Evidence-based editing: factors influencing the number of citations in a national journal. Ann Epidemiol 2012; 22: 649 – 53.
16. Kazaryan AM, Edwin B. PhD-kandidater: Publiser gjerne i Norge! Tidsskr Nor Laegeforen. 2013 Apr 23;133(8):824.
17. Grinberg M, Solimene MC, Barreto MdoC. Why publish in national journals? Arq Bras Cardiol 2012; 98: e62 – 3.
18. Amin M, Mabe M. Impact factors: use and abuse. International journal of environmental sciences and technology 2004; 1(1):1-6.
19. Kazarian AM, Evdokomova IuA. [Work on a scientific medical article]. Klin Med (Mosk). 2002;80(7):43-6 [på russisk].
20. Citrome L. Peer review and Publons - enhancements for the reviewer. Int J Clin Pract. 2016 May;70(5):364.
21. Pritsker M. How video publication of laboratory experiments will solve the reproducibility problem: The Journal of Visualized Experiments. Information Services & Use 2015;35:181–184
22. Anand S, Rahman RA, Jadhav S, Goel P, Jain V, Yadav DK, Dhua AK. Quality Assessment of YouTube Videos on Laparoscopic Pyloromyotomy Using a Validated Tool: An Appeal to Trainees to Follow the Peer-Reviewed Videos for Learning Purposes. J Laparoendosc Adv Surg Tech A. 2022; 32 (2) Online Ahead of Print
23. Mahesh G. The changing face of scholarly journals. Current Science 2017; 113 (10):1813-4
24. Ibrahim AM, Lillemoe KD, Klingensmith ME, Dimick JB. Visual abstracts to disseminate research on social media: a prospective, case-control crossover study. Ann Surg 2017 266(6):e46-e48
25. Thomas RB, Johnson PT, Fishman EK. Social Media for Global Education: Pearls and Pitfalls of Using Facebook, Twitter, and Instagram. J Am Coll Radiol. 2018 Oct;15(10):1513-1516.
26. Kimmons R, Rosenberg J, Allman B. Trends in Educational Technology: What Facebook, Twitter, and Scopus Can Tell us about Current Research and Practice. TechTrends. 2021;65(2):125-136.
27. Li N, Huang Q, Ge X, He M, Cui S, Huang P, Li S, Fung SF. A review of the research progress of social network structure. Complexity. 2021:6692210. 10.1155/2021/6692210
28. Boudry C, Bouchard A. Role of academic social networks in disseminating the scientific production of researchers in biology/medicine: the example of ResearchGate. Med Sci (Paris) 2017;33(6-7):647-652 [Artikkel på fransk]
S246: SCREENING FOR ABDOMINALT AORTAANEURISME ( AAA ) BLANT 65 ÅR GAMLE MENN I OSLO
1. Reimerink JJ, van der Laan MJ, Koelemay MJ, Balm R, Legemate DA. Systematic review and meta-analysis of population-based mortality from ruptured abdominal aortic aneurysm. Br J Surg. 2013;100(11):1405-13
2. Antoniou GA, Antoniou SA, Torella F. Editor’s Choice - Endovascular vs. Open Repair for Abdominal Aortic Aneurysm: Systematic Review and Meta-analysis of Updated Peri-operative and Long Term Data of Randomised Controlled Trials. Eur J Vasc Endovasc Surg. 2020;59(3):385-97.
3. Santiago F. Screening for Abdominal Aortic Aneurysms: The U-Boat in the Belly. JAMA. 1987;258(13):1732. doi:10.1001/jama.1987.03400130046020
4. Cosford PA, Leng GC, Thomas J. Screening for abdominal aortic aneurysm. Cochrane Database Systematic Reviews 2007, Issue 2. Art. No.:Cd002945.
5. Ali MU, Fitzpatrick-Lewis D, Kenny M, Miller J, Raina P, Sherifali D. A systematic review of short-term vs long-term effectiveness of one-time abdominal aortic aneurysm screening in men with ultrasound. J Vasc Surg. 2018;68(2):612-23.
6. Guirguis-Blake JM, Beil TL, Senger CA, Coppola EL. Primary Care Screening for Abdominal Aortic Aneurysm: Updated Evidence Report and Systematic Review for the US Preventive Services Task Force. JAMA. 2019;322(22):2219-38.
7. Rabben T, Mansoor SM, Bay D, Sundhagen JO, Guevara C, Jorgensen JJ. Screening for Abdominal Aortic Aneurysms and Risk Factors in 65-Year-Old Men in Oslo, Norway. Vasc Health Risk Manag. 2021;17:561-70.
8. Mansoor SM, Rabben T, Hisdal J, Jørgensen JJ. Eleven-Year Outcomes of a Screening Project for Abdominal Aortic Aneurysm (AAA) in 65-Year-Old Men. Vasc Health Risk Manag. 2023;19:459-67.
9. Mansoor SM, Jørgensen JJ, Hisdal J, Rabben T. Thirty-Nine Percent of Patients with a Ruptured Abdominal Aortic Aneurysm (AAA) Have an Incidentally Detected AAA Prior to Rupture. Ann Vasc Surg. 2024 Nov;108:148-156.
10. Mansoor SM, Jørgensen JJ, Grønvold T, Hisdal J, Rabben T. Determinants for non-attendance in abdominal aortic aneurysm (AAA) screening. JVS-Vascular Insights, Volume 2, 2024.


Indication: this medicinal product is for diagnostic use only. Carmyne is indicated in adults for the intra-operative detection of suspected ureteral injuries during abdominal and pelvic surgery.
Carmyne 40 mg – Plikttekst for Carmyne 40 mg «Indigokarmin» injeksjonsvæske, oppløsning Reseptgruppe C. Indikasjoner: Kun til bruk ved diagnostiske formål. Indisert hos voksne til intraoperativ påvisning av mistenkte ureterskader under abdominal kirurgi og bekkenkirurgi. Dosering: Anbefalt startdose er 1 ampulle på 5 ml ved langsom i.v. injeksjon. En andre ampulle kan injiseres 20 til 30 minutter etter den første injeksjonen, om nødvendig. Se SPC for spesielle pasientgrupper og administrasjonsmåte. Kontraindikasjoner: Overfølsomhet for innholdsstoffene. Forsiktighetsregler: Kan forårsake en forbigående økning av blodtrykket og refleksbradykardi, spesielt hos pasienter under generell anestesi eller under spinalanestesi. Sjeldne idiosynkratiske reaksjoner med bradykardi og hypotensjon er også rapportert. Det er derfor nødvendig å overvåke hjertefrekvens og blodtrykk under og noen minutter etter injeksjonen. I.v. injeksjon bør stoppes ved følgende symptomer: bradykardi, takykardi, hypotensjon, hypertensjon, utslett eller erytem, luftveissymptomer som dyspné eller bronkospasme. Har ikke blitt studert hos pasienter med GFR <30 ml/min, og bør derfor ikke brukes hos disse. Kan forstyrre puls eller cerebrale oksymetrimålinger. Bør brukes med forsiktighet ved: høyt blodtrykk, lav hjertefrekvens, hjerte- og ledningsforstyrrelser, samtidig bruk av legemidler som induserer bradykardi eller påvirker blodtrykket eller produksjonen av nitrogenoksid, koronare lidelser på grunn av dets perifere vasokonstriktoreffekt. Bruk bør unngås hos pasienter med: hemodynamisk ustabilitet, ukontrollert hjertesvikt, allergiske reaksjoner i anamnesen. Graviditet, amming og fertilitet: Graviditet: Ingen data. Anbefales ikke under graviditet og hos fertile kvinner som ikke bruker prevensjon. Amming: Overgang i morsmelk er ukjent. Risiko for diende barn kan ikke utelukkes. Nytte-/risikovurdering må foretas. Bivirkninger: Svært vanlig: Bradykardi, hypertensjon (forbigående). Svært sjeldne: Anafylaktoide reaksjoner, AV-blokk, bronkial hyperreaktivitet, dyspné, hypotensjon, misfarging av hud, utslett og erytem, takykardi. Overdosering/ Forgiftning: En overdose kan indusere en hypertensiv krise og alvorlig bradykardi. Ved overdosering kan det vurderes behandling med en perifer vasodilator.
For mer informasjon, se Felleskatalogteksten eller preparatomtalen (SPC)Innehaver av markedsføringstillatelsen: SERB S.A., Belgia. Kontaktinformasjon: Telefon: 003227920500. E-post: safety@serb.eu. Basert på SPC godkjent av DMP/EMA: 19.06.2024. Pakninger og priser per 17.07.2024: Ampulle 10 × 5 ml. 4713,00 kr. (priser og ev. refusjon oppdateres hver 14. dag). Refusjon: Ingen refusjon. Utarbeidet 07/2024