Inhoudstafel
Hfst 1. Lipiden
1 Inleiding
2 Lipiden als opslagmoleculen
2.1 Vetuzren
2.2 Triglyceriden
2.3 Wassen
3 Structurele lipiden
3.1 Fosfolipiden
3.2 Glycolipiden
3.3 Sterolen
Hfst 2. Koolhydraten
1 Inleiding
2 Monosachariden
2.1 Classificatie en stereochemie
2.2 Aldosen
2.3 Ketosen
2.4 Configuratie en conformatie
2.5 Suikerderivaten (niet te kennen informatief)
3 Polysachariden
3.1.1 Disachariden
3.1.2 Opslagmoleculen
3.1.3 Structurele polysachariden
3.1.4 Nomenclatuur van polysachariden (globale opbouw van namen, herkenning van namen)
4 Glycoproteïnen
Hfst 3. Nucleïnezuren
1 Inleiding
2 Nucleosiden en nucleotide
Nucleïnezuren
4 Structuur van nucleïnezuren
4.1 DNA structuur
4.2 RNA structuur
5 Chemische eigenschappen van nucleïnezuren
Hfst 4. Eiwitten
1 Inleiding
2 Aminozuren
2.1 Algemene eigenschappen
2.2 20 proteïnogene aminozuren
2.3 Niet proteïnogenen aminozuren (informatief niet te kennen)
3 Primaire structuur van eiwitten
3.1 Peptidebinding
3.2 Lading van peptiden
4 Secundaire structuur van eiwitten
4.1 Het planaire karakter van de peptide binding(informatief naar aanloop van alpha helix…)
4.2 Rotaties rond de bindingen in een polypeptide (informatief naar aanloop van alpha helix…)
4.3 Alpha helix structuur
4.4 Beta vouwblad structuur
4.5 Bochten en lussen
5 Tertiaire en quaternaire structuur van eiwitten
5.1 Fibrillaire eiwitten (ter staving van tertiaire en quaternaire structuur worden hier voorbeelden gegeven, informatief)
5.2 Globulaire eiwitten
6 Denaturatie van eiwitten
6.1 Denaturatie door fysische factoren
6.2 Denaturatie door chemische factoren
7 Industriële toepassingen van eiwitten
7.1 Enzymen (een must, wordt redelijk uitgewerkt)
7.2 Structurele eiwitten: spinnenrag (louter informatief, ook aanzet naar biotech)
Hfst 1. Celmorfologie
1 De prokaryote en eukaryote cel (beetje herhaling sem 1)
2 Rondgang in de eukaryote cel
2.1 Verschil tussen plantaardige en dierlijke cellen: goed afstemmen met vak macro- en microbiologie, niet teveel herhalen!
2.2 De celkern of nucleus: het informatiecentrum
2.3 De ribosomen: eiwitfabrieken
2.4 Het endoplasmatisch reticulum: een biosynthese fabriek
2.5 Het Golgi-apparaat: centrum van dispatching
2.6 Lysozomen: verteringscompartimenten
2.7 Vacuolen: verscheidenheid aan onderhoudscompartimenten
2.8 Mitochondria en chloroplasten: energieomzettingen
3 Het cytoskelet en extracellulaire componenten: mag misschien weg
Hfst 2. Centraal dogma van moleculaire biologie
1 DNA replicatie
2 Transcriptie
3 Eiwitsynthese
Hfst 3. Celcyclus
1 Celcyclus en mitose: ook hier goed afstemmen met biologie, niet 2X in detail zien!
2 Meïose en genetische recombinatie
Hfst 4. Mendeliaanse genetica en evolutie
1 De wetten van Mendel
2 Genetische variabiliteit
3 Introductie tot populatie genetica
Biomoleculen
Hfst 1. Lipiden
1 Inleiding
Lipiden vormen een chemisch diverse groep van biomoleculen waarvan het gemeenschappelijk en bepalend kenmerk de onoplosbaarheid in water is. Het is ook meteen de enige klasse van grote biomoleculen die niet echt polymeren zijn. De biologische functies van de lipiden zijn net zo divers als hun chemische structuren.
Eén van hun belangrijkste rollen is het opslaan van energie onder de vorm van vetten en oliën.
Fosfolipiden en sterolen zijn dan weer belangrijke structurele onderdelen van biologische membranen. Deze membranen bieden niet alleen fysieke bescherming voor de cel, maar reguleren ook de uitwisseling van stoffen en signalen tussen de cel en haar omgeving.
Lipiden vervullen echter meer dan alleen een energieleverende en structurele functie. Ze spelen een rol in signalering, bijvoorbeeld als hormonen of als voorlopers daarvan, zoals steroïden. Daarnaast fungeren lipiden als isolatiemateriaal in dieren, beschermen ze organen tegen mechanische schade, en dragen ze bij aan ontstekingsprocessen en immuunresponsen.
In dit hoofdstuk gaan we dieper in op de chemische eigenschappen van de verschillende typen lipiden, gebaseerd op hun functies in cellen en organismen.
2
Lipiden als opslagmoleculen
2.1
Vetzuren
Vetzuren zijn carboxylzuren met lange koolstofketens (4 à 36). Biologische vetzuren zijn meestal niet-vertakte structuren. Ze kunnen verzadigd zijn (vrij van dubbele bindingen) of verzadigdheden bevatten. In de natuur komen ze zelden voor in vrije vorm. In veresterde vorm in triglyceriden zijn ze belangrijke opslagmoleculen, veresterd in fosfolipiden vormen ze een bouwsteen van membraanlipiden.
In planten en dieren zijn koolstofketens met 16 en 18 C-atomen het meest voorkomend. Ketens korter dan 14 C-atomen of langer dan 20 C-atomen, komen zelden voor. Synthese van vetzuren gebeurt door opeenvolgende condensatie van acetyl-eenheden (2 Cfragmenten). Daardoor hebben vetzuren in de natuur meestal een even aantal C-atomen.
De dubbele binding in enkelvoudig onverzadigde vetzuren bevindt zich meestal na C9 (het 9de C-atoom te beginnen bij het carboxyleinde). Bij meervoudig onverzadigde vetzuren
bevinden de dubbele bindingen zich meestal na C12 en C15 (met arachidonzuur als uitzondering). Dubbele bindingen zijn meestal gescheiden door een methylgroep, het zijn dus meestal geen geconjugeerde dubbele bindingen. Over het algemeen neemt de dubbele binding de Z-configuratie aan (in biochemie nog vaak cis-configuratie genoemd).
Transvetzuren worden gevormd bij fermentatie van dierlijke vetzuren (pens, zuivelproducten).
Vetzuren hebben een triviale naam en een systematische naam. Het is belangrijk inzicht te hebben in de systematische naam, omdat deze vaak gebruikt wordt om verwarring te vermijden.
Bij de systematische naamgeving start de nummering van de C-atomen aan het carboxyl-Catoom, dit C-atoom is het C1-atoom. Het α-C-atoom is het eerstvolgende C-atoom. Het ω-Catoom is het laatste C-atoom in de keten. Dubbele bindingen worden weergegeven door het nummer van het C-atoom waarna de dubbele binding zich bevindt te vermelden voor de naam
Tabel 1 Naamgeving vetzuren
Numerisch symbool
IUPAC nomenclatuur organische (biochemische)
12:0 Dodecaanzuur
14:0 Tetradecaanzuur
16:0 Hexadecaanzuur
16:1 Z-hexadec-9-eenzuur (9-hexadeceenzuur)
18:0 Octadecaanzuur
18:1 (9) Z-octadec-9-eenzuur (cis-9-octadeceenzuur)
18:2(9,12) (9Z,12Z) octadeca-9,12-dieenzuur (cis,cis-9,12-octadecadieenzuur)
18:3(9,12,15) (9Z, 12Z, 15Z) octadeca-9,12, 15trieenzuur (9,12,15-octadecatrieenzuur)
Triviale naam (Ndl)
Triviale naam (Eng)
Laurinezuur Lauric acid
Myristinezuur Myristic acid
Palmitinezuur Palmitic acid
Palmitolinezuur Palmitoleic acid
Stearinezuur Stearic acid
Oleïnezuur Oleic acid
Linolzuur Linoleic acid
(9, 12, 15) Linoleenzuur (9, 12, 15) Linolenic acid
20:0 Icosaanzuur Arachidinezuur Arachidinic acid
20:4(5,8,11,14) (5Z, 8Z, 11Z, 14Z) icosa-5, 8, 11, 14-tetraeenzuur (cis, cis, cis, cis-5,8,11,14icosatetraëenenzuur)
Arachidonzuur Arachidonic acid
• Het eerste deel van de naam geeft aan hoe lang de C-keten is bv palmitinezuur = hexadecaanzuur: hexadeca = 16, dit is een C16 vetzuur
• Het laatste deel is altijd –zuur en geeft aan dat het om een carboxylzuurmolecule gaat, de nummering van de keten start aan het C-atoom van de carbonzure functie
• Het middendeel geeft informatie over de dubbele bindingen -aan: duidt op verzadigde vetzuren: hexadecaanzuur: geen dubbele bindingen -een: duidt op de aanwezigheid van 1 dubbele binding: hexadeceenzuur di- tri- tetra- kunnen ‘-een’ voorafgaan, om aan te tonen dat er meerdere dubbele bindingen aanwezig zijn: bv octadeca-9,12-diëenzuur bevat 2 dubbele bindingen
• Voor de naam wordt de configuratie en eventueel positie van de dubbele bindingen weergegeven
Bij polyonverzadigde vetzuren of ‘PUFA’s’ (= Poly Unsaturated Fatty Acids), dus vetzuren met meer dan 1 dubbele binding, volgt men vaak een ander type nomenclatuur. Hier begint de nummering vanaf het ω-C-atoom en worden dubbele bindingen weergegeven t.o.v. het ω-Catoom.
Figuur 1 Linolzuur of (9Z,12Z) octadeca-9,12-dieenzuur
Bovenaan: officiële IUPAC nummering
Onderaan: triviale nummering PUFA’s
ω-3 en ω-6 vetzuren, zijn dus vetzuren met een dubbele binding na positie 3 of 6 vanaf acyleinde van vetzuur (ω-C-atoom). Deze triviale naamgeving wordt zeker in de gezondheids- en voedingssectoren nog vaak gebruikt.
2.2 Triglyceriden
Vetzuren vormen een belangrijke bron aan energie, maar het zijn zuren. Een te hoge concentratie vetzuren in cellen zou de pH balans kunnen verstoren. Daarom worden vetzuren voornamelijk opgeslagen onder de vorm van triacylglycerolen of triglyceriden. Dit zijn neutrale vetten.
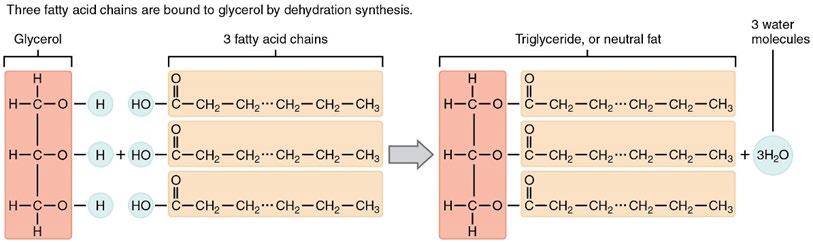
Figuur 2 Structuur van triglyceriden (Organic compounds essential to human functioning, 2020)
In triglyceriden zijn er 3 vetzuren veresterd met glycerol. De polaire groepen van zowel glycerol als van de vetzuren zijn geneutraliseerd door de esterverbinding. Ook triglyceriden zijn dus water onoplosbaar. In de cytosol van cellen vormen ze een aparte fase.
Er zijn een aantal voordelen aan energieopslag onder de vorm van triglyceriden in vergelijking met glycogeen:
• De C-atomen zijn meer gereduceerd dan in koolhydraten, dus oxidatie levert veel meer energie op
• De hydrofobe moleculen zijn niet geassocieerd met water, koolhydraten wel. De associatie met water verhoogt het gewicht dat nodig is voor energieopslag.
In vetweefsel kunnen veel triglyceriden opgeslagen worden die een energievoorraad voor maanden vormen. De voorraad vervat in glycogeen (een koolhydraat), is maar voldoende voor ongeveer één dag.
2.3 Wassen
Wassen zijn esters van lange vetzuurketens (C14 tot C36) met lange keten- alcoholen (C16 tot C30). Ze hebben een hoger smeltpunt dan triglyceriden (60 °C tot 100 °C). In plankton is het de voornaamste opslag van energie.
Wassen hebben ook een belangrijke functie als waterafstotende bescherming bv. in huid, veren, rododendron bladeren.
Bijenwas bevat als belangrijkste component bv. cetylpalmitinezuur, een ester tussen een cetylalcohol (C16-alcohol) en palmitinezuur.
Figuur 3 Structuur van cetylpalmitinezuur
3 Structurele lipiden
Eén van de belangrijkste structurele functie van lipiden, is hun functie in membranen.
Lipiden zijn daarin de belangrijkste moleculen. De meeste membraanlipiden (m.u.v. sterolen) hebben een gelijkaardige structuur.
De indeling in structurele lipiden kan op verschillende manieren gebeuren. Wij gebruiken de indeling volgens de basisstructuur en de bijkomende functionele groepen. Daarnaast bespreken we dan nog een extra groep, nl. de sterolen.
Als basisstructuur bezitten structurele lipiden een glycerol structuur waarop 2 vetzuurketens veresterd zijn of een sfingosine molecule waaraan 1 extra vetzuurketen gebonden is. Verder bezitten ze vaak nog een functionele groep, zoals een fosfaat- of een suikergroep.
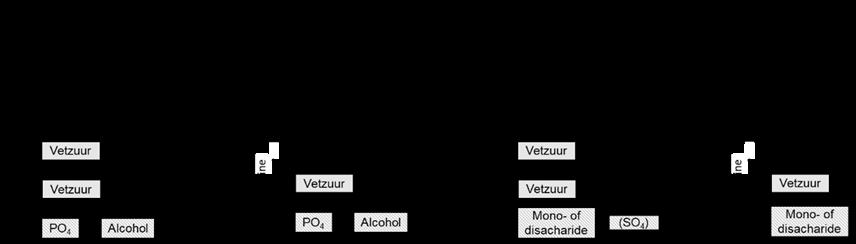
Onderstaande figuur geeft de gevolgde indeling schematisch weer.
Figuur 4 Indeling van structurele lipiden volgens functionele groepen en basisstructuur
3.1 Fosfolipiden
Fosfolipiden kunnen glycerol als basisstructuur hebben (glycerofosfolipiden) of sfingosine als basisstructuur (sfingofosfolipiden).
3.1.1 Glycerofosfolipiden
Glycerofosfolipiden hebben een glycerol basisstructuur. Daarop zitten op positie C1 en positie C2 vetzuren veresterd. Op positie C3 bevindt zich een fosfaatgroep. Dit geheel vormt de basisstructuur van glycerofosfolipiden en wordt fosfatidinezuur genoemd.
5 Structuur fosfatidinezuur (met X = H) (Glycerophospholipids, 2019)
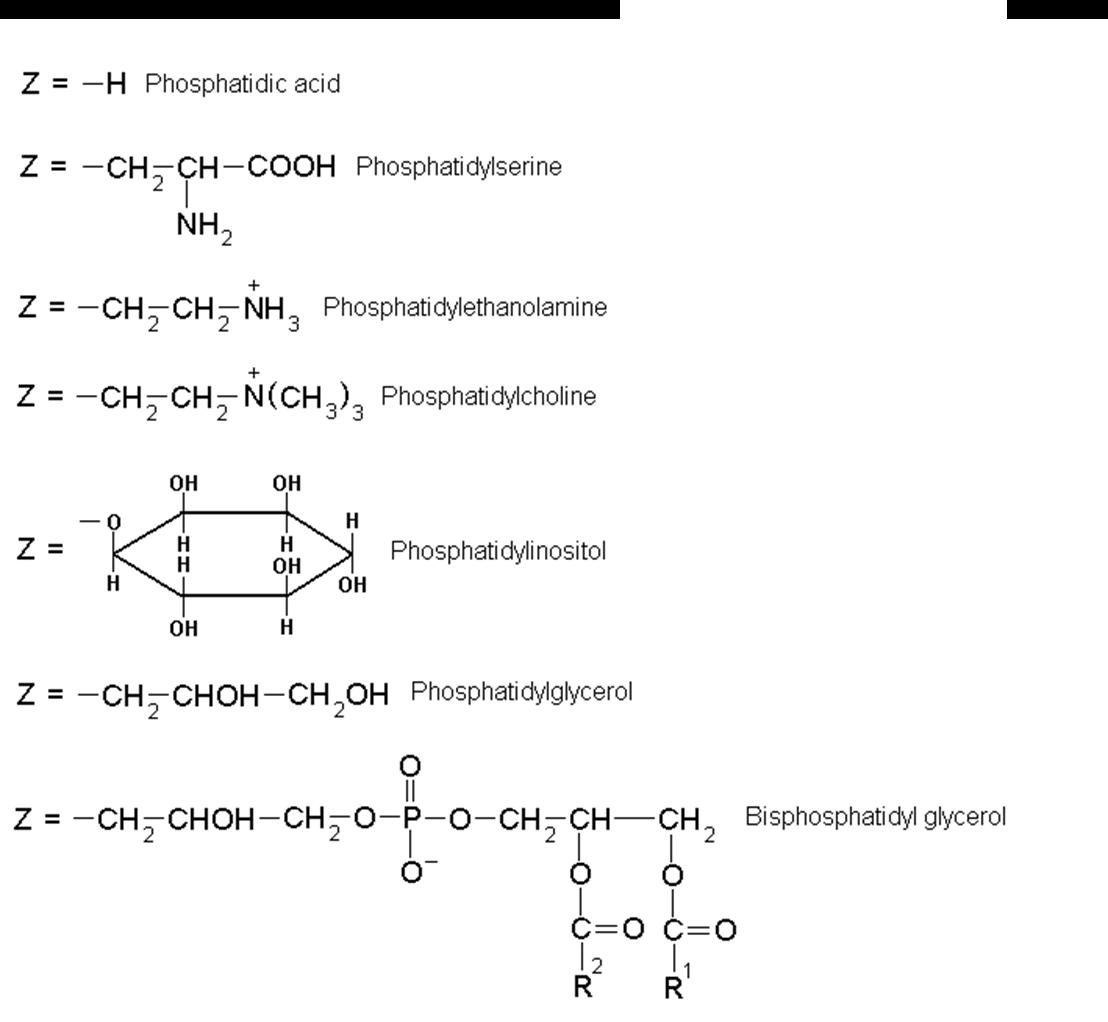
Dit lipide komt maar weinig voor in membranen. Meestal is er aan de fosfaatgroep nog een alcohol veresterd. De naamgeving is gebaseerd op de basistructuur (fosfatidinezuur), met verwijzing naar de polaire alcohol groep die veresterd kan zitten aan de fosfaatgroep.
• Fosfatidylserine bevat bv. serine dat via zijn hydroxylgroep veresterd zit aan de fosfaatgroep in fosfatidinezuur
• Ethanolamine en choline zijn ook vaak voorkomende polaire groepen
Figuur 6 Voorbeelden van nomenclatuur van fosfolipiden en hun functionele groepen (Glycerophospholipids, 2019)
Figuur
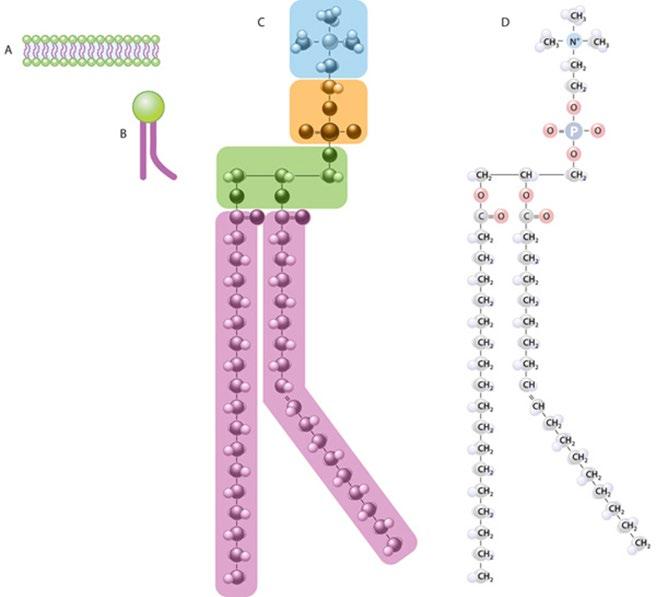
In onderstaande figuur wordt een celmembraan weergegeven en hoe fosfolipiden daar deel van uitmaken
Figuur 7 Lipide membraan samengesteld uit fosfolipden (Nature Education, 2014)
A. Lipidemembraan
B. Schematische voorstelling van een fosfolipide met een polair hoofd en twee hydrofobe vetzuurketens
C. Schematische voorstelling van fosfatidylcholine
D. Structuur fosfatidylcholine, met choline veresterd op glycerol basisstructuur (C3), evenals oleïnezuur (C2) en stearinezuur (C3)
Verschillende vetzuren kunnen aanwezig zijn in een glycerofosfolipide. Maar heel vaak bevindt worden fosfolipiden gekenmerkt door volgende samenstelling:
• een verzadigd vetzuur met 16 of 18 C-atomen op positie 1
• een onverzadigd vetzuur met 18 of 20 C-atomen op positie 2
3.1.2 Sfingofosfolipiden
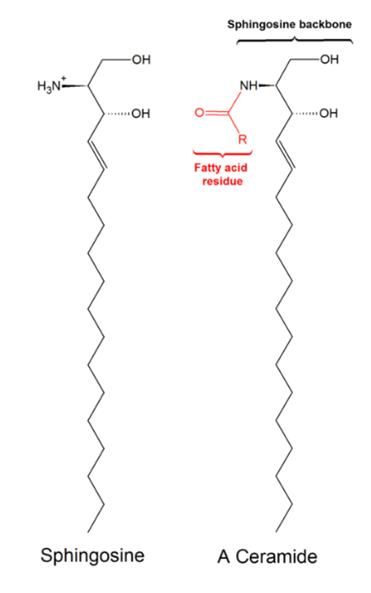
Sfingolipiden bezitten het aminoalcohol sfingosine als basisstructuur (i.p.v. glycerol).
Sfingosine ((2S,3R,4E)-2-Aminooctadec-4-ene-1,3-diol) bestaat uit een lange onverzadigde koolwaterstofketen van 18 koolstofatomen, met twee alcoholfuncties en een aminogroep als substituenten.
8 Sfingosine
In sfingolipiden is ceramide de basisstructuur. Deze bestaat uit:
• Sfingosine
• Vetzuur dat via een amidebinding kan er vetzuurketen gebonden worden op positie C2.
9 Structuur van sfingosine en ceramide (Lipids, 2019)
Figuur
Figuur
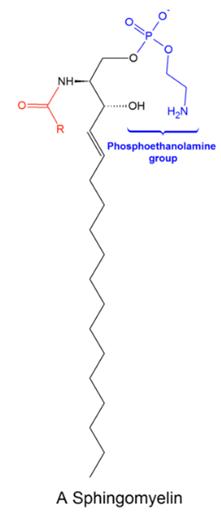
Sfingofosfolipiden worden gekenmerkt door een fosfaatgroep die via een fosfodiësterverbinding gekoppeld is aan de alcoholfunctie op positie C1. Aan deze alcoholfunctie kunnen extra polaire functionele groepen gebonden zijn zoals bv. ethanolamine.
Sfingomyeline is een van de meest gekende sfingolipiden. Het dankt zijn naam aan zijn structuur en aan het feit dat het vaak voorkomt in de myelineschede van zenuwcellen. In onderstaande figuur zie je de structuur die uit volgende componenten bestaat:
• Ceramide basisstructuur
• Fosfaatgroep op C1 positie
• Extra vetzuurketen via amide binding op C2 positie
• Ethanolamine als polaire alcoholfunctie op gefosforyleerd ceramide als basisstructuur
Figuur 10 Structuur van sfingomyeline
Basis van sfingofosfolipide
3.2 Glycolipiden
Ook bij glycolipiden zijn er lipiden met glycerol als ruggengraat en lipiden met sfingosine als ruggengraat.
3.2.1 Glyceroglycolipiden
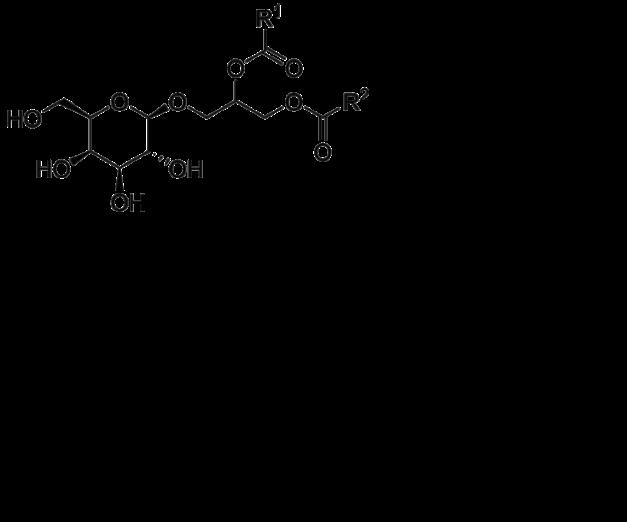
Bij planten komen de glycerol afgeleiden voor. De voornaamste zijn galactolipiden en sulfolipiden.
Galactolipiden komen voor in de thylakoïde membranen van chloroplasten. Daar maken ze 70 % tot 80 % uit van het totaal aan membraan lipiden. De structuur bestaat uit 1 of 2 galactose residu’s die via glycosidische binding op het C3-atoom van 1, 2-diacylglycerol gebonden zijn.
Sulfolipiden hebben als polaire groep een gesulfateerde glucose molecule op de positie C3.
3.2.2 Sfingoglycolipiden
Bij dierlijke organismen vinden we glycolipiden met sfingosine als backbone terug. De koolhydraat-delen bevinden zich vaak aan de buitenzijde van het membraan en spelen vaak een belangrijke rol in cel-cel interacties.
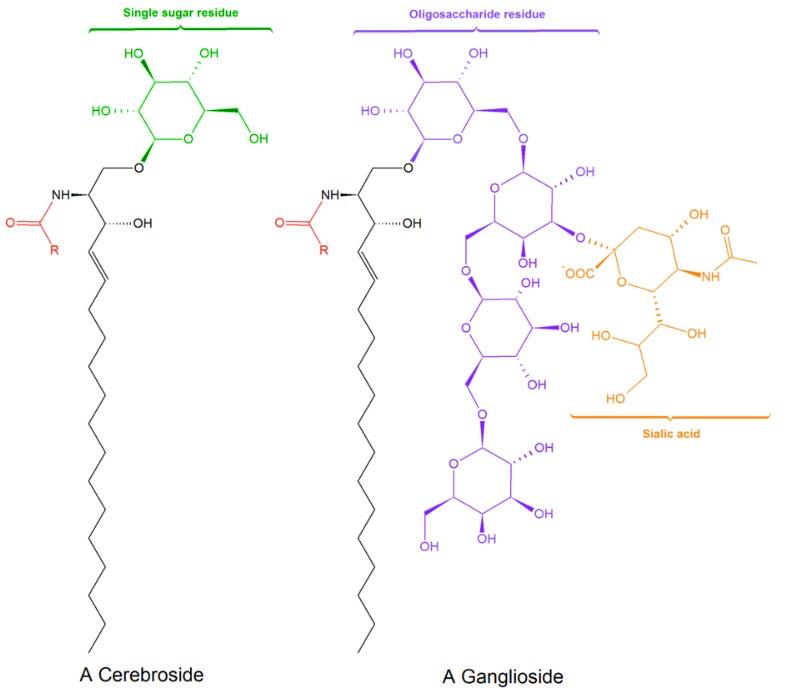
Het eenvoudigste sfingoglycolipide is cerebroside waarbij er 1 koolhydraat residu (glucose of galactose) gebonden zit op de C3 positie en 1 vetzuur via een amidebinding op de C2-positie.
Figuur 11 Structuur van een A. een galactolipide en B. een sulfolipide
Figuur 12 Structuur van sfingo-glycolipiden(Lipids, 2019)
Globosiden zijn sfingoglycolipiden met 2 of meerdere suikerresidu’s, vnl. glucose, galactose of N-acetylgalactosamine
Gangliosiden zijn de meest complexe sfingolipiden met oligosachariden als polaire groep. Op die oligosachariden bevindt zich dan nog minstens 1 N-acetylneuraminezuur-residu (NANA; siaalzuur; vaak eindstandig). Dit geeft de lipiden een negatieve lading bij pH7.
Informatief
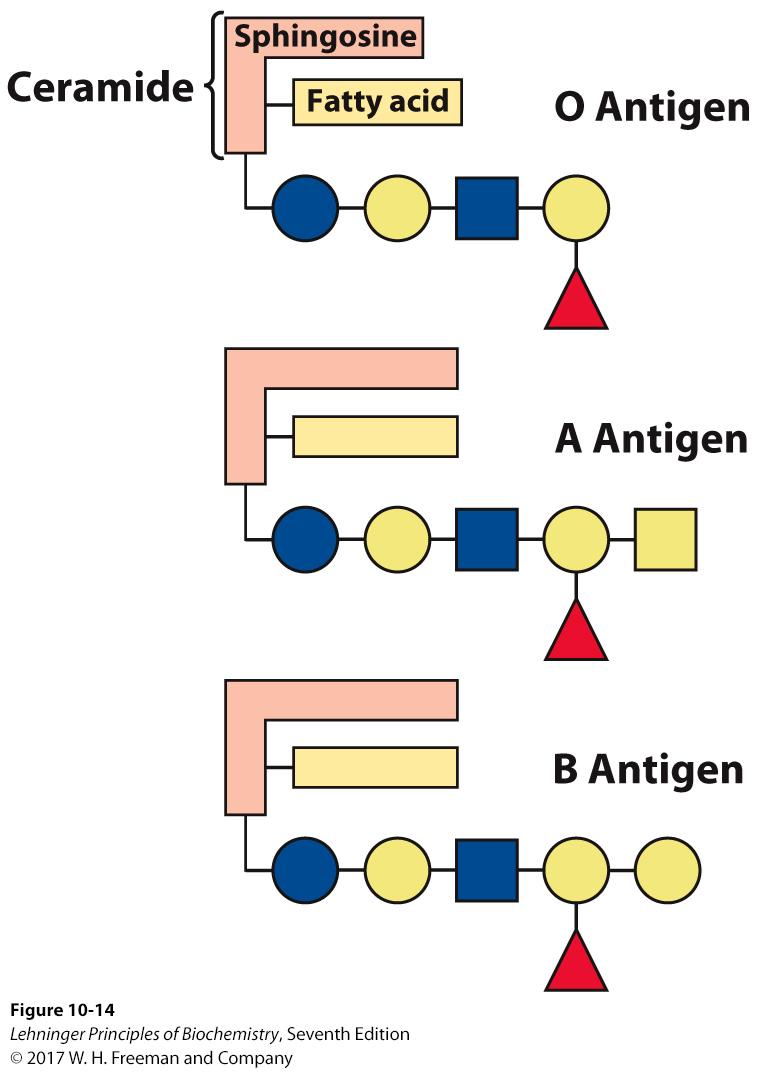
Andere goed gekende glycosfingolipiden zijn de determinanten van bloedgroepen.
Het type bloedgroep wordt deels bepaald door de oligosacharide zijketens van sfingolipiden, waarbij iedere bloedgroep specifieke oligosachariden heeft die gebonden zijn aan het sfingolipide.
Het O-antigen heeft een basisstructuur van oligosachariden die ook in type A en type B aanwezig is. Op deze laatste bevinden er zich bovenop het O-antigen nog andere extra oligosachariden.
3.2.3 Sterolen
Sterolen zijn ook belangrijke membraanlipiden. De basisstructuur verschilt totaal van de andere membraanlipiden.
Sterolen bestaan uit een steroïde kern die bestaat uit 4 ringstructuren : 3 cyclohexaan structuren en 1 cyclopentaan structuur. Dit gedeelte vormt een planaire rigide structuur.
Figuur 13 Basisstructuur van steroïde kern
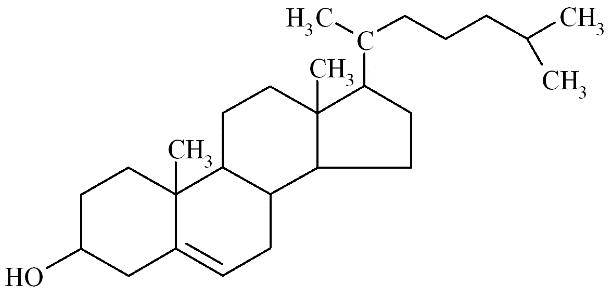
Cholesterol is het belangrijkste sterol in dierlijke weefsels, bij planten is dit stigmasterol en in fungi ergosterol. Bacteriën kunnen zelf geen sterolen aanmaken, maar sommigen incorporeren wel exogene sterolen in hun celmembraan.
Cholesterol is een neutraal lipide met een polaire hydroxylgroep. In membranen komt cholesterol meestal in onveresterde vorm voor.
14 Structuur cholesterol
Figuur
Figuur 20 Vorming van hemi-acetalen en hemi-ketalen (Hemiacetal, 2019)
Bij de circularisatie van koolhydraten zijn dit intramoleculaire reacties tussen een alcoholfunctie en de carbonylfunctie in hetzelfde monosacharide. Zo wordt een cyclisch hemi-acetal of een cyclisch hemi-ketal gevormd.
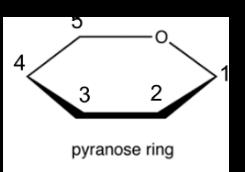
De ringstructuren worden voorgesteld d.m.v. Haworth projecties. De meest voorkomende ringstructuren zijn pyranosen of 6-ring structuren en furanosen of 5-ring structuren.
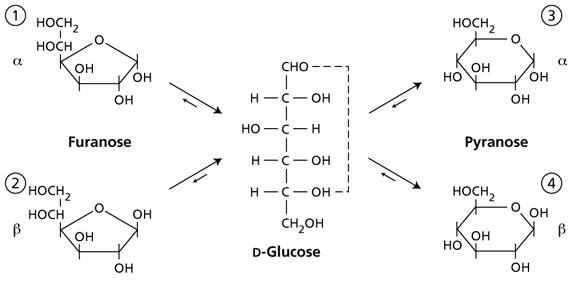
Door de circularisatie wordt het carbonyl-C-atoom een extra asymmetrisch C-atoom: het anomere C-atoom. De stereo-isomeren ter hoogte van dit C-atoom worden anomeren genoemd. Alle cyclische structuren kunnen dus voorkomen in 2 anomere vormen: α of β. Omzetting van de α-vorm naar de β-vorm is mogelijk door mutarotatie (vereist het verbreken van de cyclische structuur).
Figuur 21 Anomere vormen van de furanose en pyranose-configuraties van D-glucose (Taiz & Zieger, 2015)
Onderstaande figuur probeert stapsgewijs duidelijk te maken hoe je van een Fischer projectie kan overgaan naar de Haworth perspectief projectie. In dit geval zal getoond worden hoe je van de Fischer projectie van glucose kan overgaan naar de pyranose of 6-ring structuur.
De belangrijkste start, is een goed inzicht in de vorming van een hemi-acetal, nl. de nucleofiele additie van een alcohol aan een carbonyl-groep. De carbonyl-groep zal hierbij geprotoneerd worden tot een alcohol-functie en het zuurstof atoom van de alcoholfunctie zal verbindingen vertonen met 2 C-atomen. Meer specifiek zal bij deze intramoleculaire hemiacetal-vorming het zuurstof atoom van de alcoholfunctie resulteren in het cyclische Oatoom in de ringstructuur.
We zullen dit nu stapsgewijs doorlopen op onderstaande figuur:
1. In de Fischer projectie is de carbonyl functie aangeduid. Verder is ook de alcoholfunctie aangeduid die de hemiacetalvorming zal doorvoeren
2. De pijl duidt aan op welke positie de nucleofiele additie van de alcoholfunctie zal plaatsgrijpen.
3. In deze structuur werden de functionele groepen op het 6de C-atoom geroteerd naar links. Op deze manier komen alle atomen die in de ringstructuur betrokken zijn op 1 lijn te liggen. In deze structuur kan je de ringstructuur al zien. Het eerste C-atoom zal bij een standaardvoorstelling van de Haworth projectie rechts komen te staan. De daaropvolgende C-atomen bevinden zich dan t.o.v. dat eerste C-atoom links vooraan.
4. Om de positie van de alcoholfuncties in de Haworth perspectief formule weer te geven, kantel je figuur 3 op zijn rechterzijde. De alcoholfuncties die zich in figuur 3 rechts bevinden, zullen in de Haworth perspectief formule onder de ringstructuur terecht komen.
5. Nadat de figuur gekanteld is, kan je zelf de basisstructuur tekenen van de ringstructuur. Teken in deze basisstructuren het laagst genummerde cyclisch Catoom rechts.
Overloop daarna de positie van de alcoholfuncties op de daaropvolgende C-atomen, waarbij de ringstructuur in wijzerzin doorloopt.
6. Als je al deze stappen doorloopt, zou je een correcte Haworth perspectief formule moeten bekomen
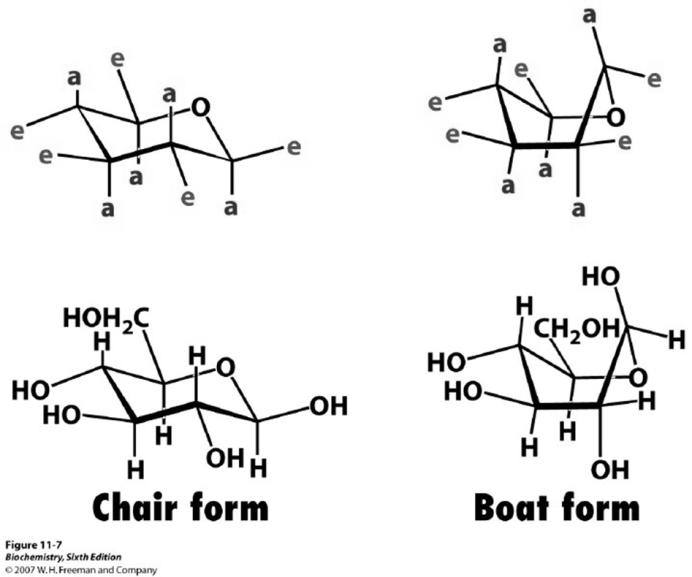
positie bevinden. β-D-glucose is het meest voorkomende suiker. Dit is het enige 6-ring suiker waarbij alle substituenten een sterisch gunstige equatoriale positie kunnen aannemen.
Figuur 24 Stoel en boot-conformaties van pyranose (glucose)
In oplossing kunnen koolhydraten via de lineaire vorm overgaan van de ene cyclische structuur in de andere. Bovendien kunnen ketosen door keto-enol tautomerie omgezet worden in aldosen. Dit wil zeggen dat zolang de monosachariden vrij in oplossing aanwezig zijn, ze de eigenschappen van een aldehyde bezitten, kunnen mutaroteren en kunnen overgaan van pyranose- naar furanosevormen.
2.5 Suikerderivaten
Naast de eenvoudige koolhydraten, komen er in organismen heel vaak afgeleiden van deze vormen voor. In deze afgeleiden is de hydroxylgroep op een van de C-atomen vervangen door een andere groep of is er een oxidatie of reductie opgetreden van de basisstructuur.
2.5.1 Geoxideerde afgeleiden
Aldehyden kunnen een zachte chemische of enzymatische oxidatie ondergaan, zodat er een zuurfunctie gevormd wordt van de aldehydefunctie. De gevormde producten worden aldonzuren genoemd. De naamgeving van deze zuren is overeenkomstig het suiker, met de uitgang: –onzuur. Glucose kan geoxideerd worden, met vorming van gluconzuur. Dit zuur kan een intramoleculaire esterverbinding aangaan, met vorming van een lacton.
De oxidatie-reactie gaat gepaard met reductie van een andere verbinding. Vandaar dat deze suikers reducerende suikers genoemd worden. In de cyclische suikers is het uiteinde waar het anomere C-atoom zich bevindt, het reducerende uiteinde van een suiker.
Ketosen kunnen via keto-enoltautomerie in aldosen worden omgezet en bezitten, vrij in oplossing, dus ook reducerende eigenschappen. Deze eigenschap wordt vaak gebruikt in detectie van koolhydraten.
Ook oxidatie van een primair alcohol in een koolhydraat is mogelijk (bv. C6-OH in glucose).
Deze reactie kan enkel enzymatisch doorgaan en leidt tot de vorming van –uronzuren. De beschikbaarheid van andere hydroxylgroepen, maakt nog steeds circularisatie door vorming van hemiketal of hemiacetal mogelijk. –Uronzuren kunnen dus voorkomen in pyranose- of furanose-ringstructuren.
2.5.2 Gereduceerde vormen
Ketosen en aldosen kunnen onder zachte omstandigheden (bv. m.b.v. NaBH4) reduceren.
Dit leidt tot de vorming van een niet-cyclisch polyhydroxyalcohol: een alditol. De naamgeving van deze producten is opnieuw overeenkomstig het suiker, met de uitgang –itol. In de natuur gebeurt ook deze reductie enkel enzymatisch. Ribitol is bv. een bestanddeel van flavines, die op hun beurt belangrijk zijn bij redox-reacties. Glycerol en cyclisch myo-inositol zijn belangrijke vetbestanddelen. Xylitol is een natuurlijke zoetstof in ‘suikervrije’ kauwgom.
Figuur 25 Geoxideerde vormen van glucose