19 minute read
Columna Internacional IACLE
IACLE
CURSO DE ACTUALIZACIÓN EN CONTACTOLOGÍA PARTE 85
Advertisement
Lic. Opt. Rubén Velázquez Guerrero, FIACLE
Coordinador de IACLE México
os científicos han estado interesados en el estudio de las secreciones de las glándulas de Meibomio desde hace muchos años. Enfermedades asociadas con estas glándulas (por ejemplo, los cánceres, blefaritis posterior) se han observado en la literatura médica, desde la primera parte del siglo XX. Sin embargo, el término “disfunción de las glándulas de Meibomio” (MGD por sus siglas en inglés) fue introducido por Korb y Henríquez en 1980. Se considera que este término es apropiado para describir las alteraciones funcionales de las glándulas de Meibomio; y, más general, el de enfermedad de las glándulas de Meibomio para describir una gama más amplia de los trastornos de éstas, incluyendo neoplasia y enfermedad congénita.
Unidad funcional lagrimal
La unidad funcional lagrimal está compuesta por la película lagrimal, las glándulas que secretan sus componentes, así como los nervios que controlan esta secreción, además de los párpados que son los encargados de la distribución y eliminación de la lágrima; cualquier alteración de alguno de sus componentes puede producir un síndrome de disfunción lagrimal, enfermedad definida en el 2007 por el Taller Internacional sobre Ojo Seco como una enfermedad multifactorial de la película lagrimal y la superficie ocular que causa síntomas de malestar, trastornos visuales e inestabilidad de la película lagrimal con daño potencial en la superficie ocular, que va acompañada por un incremento en la osmolaridad de la película lagrimal e inflamación de la superficie ocular.
Para una comprensión más sencilla, se ha descrito que la película lagrimal está compuesta por 3 capas. La capa superficial se forma sobre la parte acuosa de la misma a partir de las secreciones oleosas de las glándulas de Meibomio (GM) y las glándulas sebáceas accesorias de Zeis y de Moll, las aberturas de las GM se distribuyen a lo largo del borde palpebral, inmediatamente por detrás de los folículos de las pestañas; la capa intermedia es la fase acuosa, que es secretada por la glándula lagrimal principal y las glándulas accesorias de Krause y de Wolfring; y la capa más interna es delgada, mucoide elaborada por células caliciformes de la conjuntiva y también por las criptas de Henle y las glándulas de Manz.
La clasificación más actual del síndrome de disfunción lagrimal está basada en su etiopatogenia y divide la enfermedad en deficiencia acuosa asociada o no a síndrome de Sjogren, y enfermedad de tipo evaporativo, ya sea por una alteración intrínseca como la deficiencia de la secreción de las GM, ya por desórdenes de la alteración de la apertura palpebral o de la frecuencia del parpadeo, así como por interacción medicamentosa especialmente con la isotretinoína (nombres comerciales: Roaccutan®, Neotrex®, Isotrex®, Oratane®, Trevissage®), y una forma extrínseca por deficiencia de vitamina A, el uso de conservadores tópicos o lentes de contacto y enfermedades de la superficie ocular como la alergia.
Glándulas de Meibomio
Las GM son una variante de las glándulas sebáceas situadas en las placas tarsales de los párpados superior e inferior. Estas glándulas son las encargadas de sintetizar y secretar activamente el meibomio, una compleja mezcla de cera, ésteres de colesterol, triglicéridos y fosfolípidos que forman parte de la capa externa de la película lagrimal, fomentando la estabilidad y evitando su evaporación.
Cada GM se compone de múltiples acinos secretores que contienen meibocitos, ductos
laterales, un conducto central y un conducto excretor terminal que se abre en el margen posterior del párpado. La cantidad y volumen de las GM es mayor en el párpado superior (30-40) en comparación con el inferior (20-30), aunque el aporte funcional relativo en la película lagrimal de las glándulas de ambos párpados aún no se ha determinado con exactitud.
Las GM están densamente inervadas y su función está regulada por andrógenos, estrógenos, progestágenos, ácido retinoico, factores de crecimiento, y posiblemente, por neurotransmisores. Las glándulas producen lípidos polares y no polares a través de un proceso complejo y no completamente entendido. Estos lípidos se secretan dentro de los conductos a través de un proceso holocrino; la salida de la secreción sebácea se presenta en los orificios glandulares, los cuales se encuentran situados justo por delante de la unión mucocutánea del borde palpebral, y ésta se produce debido a la contracción muscular durante el movimiento del párpado.
La forma más accesible de evaluar las GM es mediante la exploración con lámpara de hendidura; con esta técnica es posible visualizar cambios anatómicos del borde palpebral como la presencia de telangiectasias, hiperemia, engrosamiento vascular, obstrucción de los orificios de salida, remplazo anterior o posterior de la unión mucocutánea, y mediante la expresión de las GM por presión de los párpados es posible evaluar tanto la calidad como la cantidad de la secreción de las glándulas, cambios que se correlacionan de manera adecuada con la disfunción de las GM.
Disfunción de las glándulas de Meibomio
El término disfunción es el resultado de anormalidades anatómicas o en la secreción de las glándulas de Meibomio. Se usa porque la función de ésta se altera y esto conduce a la disminución de la estabilidad de la película lagrimal (evidenciada por el aumento de la evaporación, de la tensión superficial, la contaminación con sebo, y el no sellado adecuado de los párpados durante el sueño).
El término difuso se utiliza en la definición, ya que el trastorno implica la mayor parte de las glándulas de Meibomio. Las alteraciones localizadas de estas glándulas, como en chalazión, no tienden a causar anormalidades en la película lagrimal o en epitelios de la superficie ocular, y por lo tanto no se consideran dentro del contexto de disfunción de las glándulas de Meibomio (MGD).
La obstrucción del orificio glandular y el conducto terminal se identifica como el aspecto más destacado en esta entidad. Los síntomas subjetivos de irritación de los ojos están incluidos en la definición, ya que son éstos los de mayor preocupación para el paciente, y con frecuencia la mejora de estos síntomas es el objetivo principal en el tratamiento de esta afección. El enigma aún existe en el ojo seco, donde los signos y síntomas frecuentemente muestran disparidad.
El papel de la inflamación en la etiología de la MGD es controvertido e incierto.Aunque la relación causa-efecto no está clara, las asociaciones entre la desaparición de las glándulas de Meibomio y las enfermedades inflamatorias de la superficie ocular, como la blefaritis crónica, la conjuntivitis papilar gigante y el síndrome de Sjögren, han sido reportadas. La observación histopatológica de las glándulas obtenidas en la autopsia ha revelado una inflamación alrededor de los lóbulos de la glándula en el 18,6 % de casos. Clínicamente, el aumento de la vascularización del margen del párpado es una de las señales principales de la inflamación y de la disfunción, y su importancia en el diagnóstico y el tratamiento es ampliamente aceptado; sin embargo, el hallazgo ha demostrado estar relacionado con la edad.
Cuando la MGD se produce con aumento de la secreción de los lípidos, se han utilizado términos como hipersecretora y seborreica. La confusión surge con la dermatitis seborreica, que es una enfermedad crónica con recaídas inflamatorias de la piel en áreas ricas en glándulas sebáceas. Por otro lado, la entidad que nos compete no se asocia regularmente con la secreción excesiva de sebo, ni son las glándulas sebáceas las involucradas. La etiología real puede estar relacionada con la infección por hongos (género Malassezia). Por lo tanto, es más apropiado y comprensible clínicamente utilizar el vocablo hipersecretora. Del mismo modo, el término hiposecretora se utiliza en lugar de disfunción obstructiva. La obliteración de los conductos de las glándulas de Meibomio y la obstrucción del orificio por la
COLUMNA
IACLE
hiperqueratosis es un hallazgo importante en estos casos; sin embargo, la disminución de la secreción de lípidos puede ocurrir debido a anomalías en las glándulas de Meibomio sin obstrucción notable concurrente; por lo que MGD hiposecretora cubre una gama más amplia de las manifestaciones de la enfermedad.
Se ha descrito otra condición llamada queratoconjuntivitis meibomiana (MKC), a menudo asociada con blefaritis anterior, pero los cambios más importantes se han centrado en las glándulas de Meibomio. Por lo general, se asocia con alguna forma de enfermedad de la piel y se caracteriza por la inestabilidad de la película lagrimal, la inflamación de la superficie ocular y el daño de ésta. MKC es una causa importante de los síntomas en la blefaritis crónica.
A lo largo de la historia se han publicado diferentes clasificaciones. La primera fue propuesta en 1921 por Gifford, quien hizo hincapié en la participación de los tejidos adyacentes (por ejemplo, concreciones conjuntivales y tarso). En segundo lugar, en la década de 1980 McCulley y otros utilizaron el término de blefaritis crónica clasificado en cuatro categorías principales, como la blefaritis anterior y posterior: 1) por estafilococos, 2) seborreica, 3) meibomitis primaria y 4) otros (incluyendo atopia, psoriásica y hongos). Este sistema fue observacional y basado en la apariencia, incluyendo la obstrucción de orificios de las glándulas de Meibomio y la inflamación alrededor de las glándulas. Mathers y otros -en 1991- utilizaron tres parámetros: 1) la morfología de las glándulas de Meibomio por meibografía, 2) osmolaridad de la lágrima y 3) prueba de Schirmer. Este método se orientó más hacia los cambios de la película lagrimal en lugar de la función o la anatomía de las glándulas de Meibomio. En el mismo año, Bron y otros se basaron en la observación detallada de los bordes de los párpados; los describieron por biomicroscopia con lámpara de hendidura, y dividieron las enfermedades de las glándulas de Meibomio en cinco categorías principales según los cambios mucocutáneos, los conductos, los acinos y el rendimiento de secreción de la glándula. Cada factor se calificó de manera semicuantitativa. Una variante más reciente fue publicada por Foulks y Bron en 2003 donde se integró la observación de los cambios anatómicos y la expresión de la glándula, con la alteración bioquímica de los lípidos y de la etiología subyacente. Bron y Tiffany presentaron un diagrama circular único sobre las causas de la enfermedad de la glándula de Meibomio y las dividieron en primarias cicatriciales y no cicatriciales, secundarias e hipersecretora. Un esquema de clasificación temprana fue presentado por Foulks y Bron, quienes dividieron la MGD según el nivel de secreciones, en alta y baja producción.
Cualquier sistema de clasificación debe cumplir con las necesidades de los clínicos y de los investigadores. Como bien se ha descrito anteriormente, han sido publicados diferentes esquemas y fue en el Taller Internacional sobre MGD donde se decidió unificar criterios y tomar como parámetros los cambios anatómicos, fisiopatológicos, o la gravedad de la enfermedad. La nueva variante divide los subgrupos sobre la base del nivel de las secreciones y subdivide las categorías por las posibles consecuencias y manifestaciones. De acuerdo con estos criterios, la MGD obstructiva es la más generalizada.
Con bajo nivel de las secreciones de las glándulas de Meibomio, se recogen dos categorías principales: hiposecreción y las condiciones obstructivas. La hiposecreción se caracteriza por la disminución de la liberación de lípidos sin obstrucción de la glándula. Aunque no hay ninguna evidencia publicada y verificada de hiposecreción primaria, este trastorno se asocia clínicamente con atrofia de la glándula. Una disminución en el número de glándulas de Meibomio funcional está asociada con el uso de lentes de contacto, y esta disminución parece ser proporcional a la duración del uso de los mismos. La otra categoría con niveles bajos de secreción es la obstrucción de las glándulas. Esta es probablemente la forma más común de MGD, donde hay cambios histopatológicos que incluyen hipertrofia del epitelio del conducto y la queratinización del epitelio del orificio. El trastorno se observa en los sujetos mayores o después del uso de tratamientos para el acné, la insuficiencia de andrógenos o la falta de receptores de andrógenos también se asocia con la queratinización, la obstrucción y alteración de las secreciones de las glándulas de Meibomio. Las causas obstructivas pueden ser clasificadas como cicatriciales y no cicatriciales.
En la obstructiva no cicatricial los conductos y orificios permanecen en su posición anatómica normal, mientras que en la cicatricial éstos son desplazados posteriormente.
Las causas de la MGD obstructiva cicatricial incluyen: tracoma, penfigoide cicatricial ocular, eritema multiforme y la enfermedad atópica de los ojos. La MGD obstructiva no cicatricial se puede observar en el síndrome de Sjögren, la dermatitis seborreica, el acné rosácea, la atopia y la psoriasis. La inflamación en los tejidos adyacentes se observa con frecuencia; por ejemplo, la blefaritis anterior y la conjuntivitis. Aunque la inflamación se asocia frecuentemente con la obstrucción de las glándulas de Meibomio (el término meibomitis se ha utilizado como sinónimo), aún no queda claro si la inflamación es una causa o una consecuencia de la obstrucción de las glándulas de Meibomio.
La MGD hipersecretora se caracteriza por la liberación de una gran cantidad de lípidos en el borde palpebral en respuesta a la presión sobre el tarso, aunque se ha informado que ésta se asocia con la dermatitis seborreica en el 100 % de los casos. Este trastorno también ocurre en otras enfermedades, como la enfermedad atópica y el acné rosácea (MGD hipersecretora secundaria).
También ha habido casos sin la asociación de otras enfermedades (primaria/MGD hipersecretora idiopática). No está claro si el aumento de lípidos es el resultado de la hipersecreción de las glándulas de Meibomio, o es resultado de represar parte de las secreciones en presencia de una obstrucción leve. El trastorno no se asocia con inflamación activa y no hay cambios notables en la estructura de la glándula por meibografía. Existe una asociación reconocida entre la MGD hipersecretora y el acné, y la evidencia de la posibilidad de aumento de la secreción de lípidos por las glándulas de Meibomio proviene de la constatación del aumento de la secreción de sebo como un factor importante en la fisiopatología del acné.
Una hiperrespuesta de las glándulas a los andrógenos es la explicación más probable para la seborrea. En las mujeres con acné, la tasa de excreción de sebo total es superior a la normal. Aunque la producción de sebo se ve influida por el número de folículos activos y su capacidad individual para excretar el sebo, la gravedad de la seborrea probablemente depende de un aumento de la excreción de sebo por unas pocas glándulas y no de un mayor número de glándulas sebáceas activas.
Estudios clínicos y en animales muestran que la obstrucción de las GM es el resultado de una hiperqueratinización del epitelio ductal, lo que produce una obstrucción de los orificios de salida, dilatación quística del conducto y finalmente una atrofia difusa de los acinos, lo que genera pérdida de las glándula, siendo posible identificar los 2 primeros pasos mediante una exploración con lámpara de hendidura, mientas que los 2 últimos sólo es posible diagnosticarlos mediante estudios de meibografía.
Meibografía
La meibografía es una técnica diagnóstica que permite la evaluación in vivo de la morfología de las GM, ya que éstas no son accesibles a la visualización directa como la mayoría de las estructuras oculares, y se han desarrollado varias técnicas para ello, además de maneras de documentarlas y analizarlas.
Meibografía con luz infrarroja
La meibografía fue descrita en 1977 por Tapie quien utilizó luz ultravioleta para producir la fluroescencia de los ductos de las GM, además de luz infrarroja (IR) para iluminar las glándulas y documentarlas mediante fotografía IR; en 1985 Robin et al. describieron una técnica biomicroscópica de transiluminación del párpado evertido desde la piel y documentación fotográfica IR; y en 1994 Mathers et al. utilizaron el registro mediante video para el seguimiento de estos pacientes; posteriormente, Arita et al. modificaron la técnica a una evaluación de no contacto con documentación videográfica y más recientemente se incluye un análisis computacional de las imágenes adquiridas, lo que la convierte en una técnica objetiva y reproducible.
Existen varios equipos para la realización de la meibografía digital IR, el equipo desarrollado inicialmente por Arita et al. se montaba sobre una lámpara de hendidura equipada con un filtro de transmisión IR (IR 83, Hoya, Tokio, Japón) y una cámara IR acoplada a la lámpara de hendidura (XC-E150, Sony, Tokio, Japón). En el 2012 Pult et al. desarrollaron
COLUMNA
IACLE
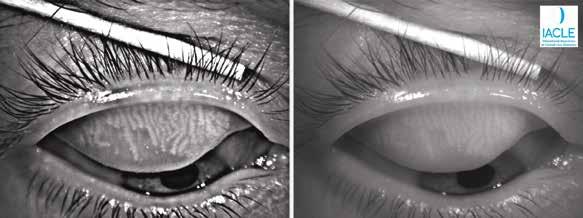
Meibografía con dos diferentes sistemas de infrarrojo.
un meibógrafo portátil usando un video dispositivo de carga acoplada (CCD) IR (802CHA CCD; Shenzhen LYD Technology Co. Ltd. Shenzhan, China) al que se le adaptó un sistema de lentes para observación cercana; además de éstos, otros instrumentos de meibografía IR de no contacto se encuentran disponibles actualmente en el mercado, la compañía CSO (Construzionne Strumenti Oftalmici, Florencia, Italia) la incluye en el tomógrafo de cámara de Sheipglug Sirius®, en la cámara de fondo de ojo Cobra® y el topógrafo de anillos de plácido Antares® que utilizan una iluminación LED IR de 890 nm; la casa comercial Oculus (Wetzlar, Alemania) comercializa en el mercado el Keratograph®27 que utiliza una iluminación IR de 840 nm, equipo con características similares al Antares®, además la compañía Topcon en su modelo TOPCON BG-4M para lámpara de hendidura, incluye un sistema de iluminación IR con una CCD externa para la grabación de la meibografía.
Meibografía con láser confocal
En 2005, Kobayashi et al. demostraron la visualización de las GM utilizando un láser confocal, con la ventaja de poder documentar no sólo la morfología sino también la histología de las glándulas y el tejido que las rodea; en 2008, Matusomoto et al. describieron 2 parámetros objetivos para el diagnóstico de disfunción de las GM mediante la medición de la densidad de acinos glandulares y el diámetro de la unidad acinar, ambos parámetros medidos con un programa incluido en el láser confocal (the Rostock Corneal Software Version 1.2 of the HRTII-RCM Heidelberg Retina Tomograph II- Rostock Cornea Module, Heidelberg Engineering GmbH, Dossenheim, Alemania); posteriormente estos mismos autores describieron la presencia de un infiltrado de células inflamatorias y fibrosis periglandular asociada a la disfunción de las GM, utilizando esta técnica para el seguimiento del manejo antiinflamatorio y reportando una disminución de la infiltración inflamatoria posterior a su uso. La medición de la densidad de acinos, la densidad de la unidad acinar y la infiltración inflamatoria ha demostrado tener una buena sensibilidad y especificidad para diagnosticar disfunción obstructiva de las GM y una buena correlación con otros estudios de dinámica lagrimal y pérdida de las GM; entre las desventajas de esta tecnología se encuentra que es una técnica de contacto ya que requiere el toque del lente al tejido estudiado lo que conlleva mayores molestias para los pacientes, y la poca accesibilidad a la tecnología.
Meibografía con tomografía de coherencia óptica
El uso de la tomografía de coherencia óptica (OCT) para la valoración de las GM fue reportado por primera vez por Bizheva et al. quienes utilizaron un OCT de 1,060 nm de alta resolución para evaluar en 2 y 3 dimensiones in vivo las GM; a diferencia de otras tecnologías, el uso del OCT agrega la posibilidad de evaluar el volumen que ocupa la GM. Más recientemente, Hwang et al. describieron el uso de un OCT de segmento anterior con resultados similares a la meibografía con luz IR. Liang et al. encontraron una disminución del ancho y largo de las GM en pacientes con disfunción de las GM obstructiva en comparación con pacientes sanos.
Análisis de la meibografía
En la meibografía por luz IR, las GM se observan como agregados en forma de racimos de uva con acinos que se dirigen hacia el borde palpebral en línea recta o ligeramente tortuosa y que son hiperreflécticos.
Desde su introducción, la medición de la pérdida de GM se ha cuantificado de diferentes formas. Arita et al. en 2008 desarrollaron un marcador llamado Meiboscore el cual estadificaba la pérdida de GM en 4 pasos (del 0 al 3) de acuerdo al porcentaje alterado, siendo 0 cuando no hay pérdida, 1 cuando la pérdida es menor a un tercio del área, grado 2 entre 1/3 y 2/3 de pérdida y grado 3 cuando la pérdida es mayor de 2/3 del área estudiada; una vez estadificados el párpado superior e inferior se suman para obtener un marcador final, encontrando una buena correlación entre el marcador y la edad, así como las anormalidades del margen palpebral y el tiempo de rotura lagrimal. Pult et al. desarrollaron una escala de 5 grados con el objetivo de aumentar su sensibilidad a cambios más pequeños, estadificando en grado 0 cuando no hay pérdida, grado 1 ≤ 25%, grado 2 del 26-50%, grado 3 del 51-75% y grado 4 > 75%, que al utilizarse mediante un análisis computacional con el programa de edición fotográfico del Instituto Nacional de Salud de los EE. UU. (image editing software Image J National Institute of Health; http:// imagej.nih.gov/ij) presenta un buen acuerdo intra e interobservador. Esta escala es la utilizada en el programa Phoenix de la casa comercial CSO, en la que, a diferencia del equipo Keratograph® donde es necesario utilizar un programa externo, el análisis se realiza en el mismo programa del equipo con una estadificación automática. Más recientemente Arita et al. describieron el uso de un programa computacional para el análisis cuantitativo del área de las GM que mediante filtros que incrementan el contraste y disminuyen el ruido en la imagen identifican la luminosidad de las GM y cuantifican de forma automática el área de pérdida.
Para la meibografía con láser confocal, Ibrahim et al. describieron valores de corte para diagnosticar la disfunción de las GM, siendo de 65 μm para el diámetro más largo del acino, 25 μm para el más corto, 300 células/mm2 para la densidad de células inflamatorias y 70 glándulas por mm2 para la densidad de la unidad acinar, con una sensibilidad y especificidad mayor del 81% para todos los parámetros.
Aplicación clínica
Además de los daños descritos en pacientes con disfunción de las GM, a través de la meibografía se han podido determinar daños en las GM en otras enfermedades como: orzuelo, queratoconjuntivitis atópica, conjuntivitis alérgica, rosácea, enfermedad injerto vs. huésped, parálisis facial, síndrome de Sjögren, orbitopatía de Graves y distrofia granular tipo 2 de la córnea; además, también se ha demostrado daño en las GM en pacientes operados de trabeculectomía, los que utilizan prótesis oculares o lentes de contacto y usuarios crónicos de medicamentos antiglaucomatosos. Finalmente, también se han descrito cambios de la anatomía del borde palpebral y la morfología de las GM asociadas a la edad en pacientes sin disfunción de GM, siendo estos cambios más importantes en los hombres que en las mujeres.
Respuestas correctas al cuestionario del artículo “Película lagrimal II” publicado en la revista anterior:
1. a • 2. b
Cuestionario
1.- ¿Con qué técnica podemos reconocer la obstrucción de las GM, como el resultado de una hiperqueratinización del epitelio ductal? a) Lámpara de hendidura b) Meibografía 2.- La cantidad y volumen de las glándulas de
Meibomio es mayor en el: a) Párpado inferior b) Párpado superior
Bibliografía
1.- Cárdenas Díaz, T. et al. Conceptos actuales en la disfunción de las glándulas de Meibomio. Rev Cubana Oftalmol vol.27 no.2 Ciudad de la Habana abr.-jun. 2014 2.- Garza-Leon,M et al. Meibografía. Nueva tecnología para la evaluación de las glándulas de Meibomio.Revista Mexicana de Oftalmología.Volume 91, Issue 4, July–August 2017, Pages 165-171 3.- H. Pult, J.J. Nichols.A review of meibography.Optom Vis Sci, 89 (2012), pp. E760-E769. 4.- K.L. Menzies, S. Srinivasan, C.L. Prokopich, et al. Infrared imaging of meibomian glands and evaluation of the lipid layer in Sjogren’s syndrome patients and non-dry eye controls. Invest Ophthalmol Vis Sci, 56 (2015), pp. 836-841. 5.- R. Arita, K. Itoh, S. Maeda, et al. Comparison of the long-term effects of various topical antiglaucoma medications on meibomian glands. Cornea, 31 (2012), pp. 1229-1234. 6.- Módulo A1. Anatomy & Physiology of the Anterior Segment. The International Association of Contact Lens Educators (IACLE) 7.- Módulo E6. Advanced Clinical Techniques Instrumentation. The International Association of Contact Lens Educators (IACLE)










