
Edição apoiada por:


Edição apoiada por:

Lidel – edições técnicas, lda. www.lidel.pt
Carlos Calhaz Jorge licenciou-se em Medicina pela Faculdade de Medicina da Universidade de Lisboa em 1975 e concluiu a especialidade de Ginecologia e Obstetrícia em 1985. Doutorou-se em Medicina – Ginecologia com uma tese sobre endometriose –Fatores patogénicos do líquido peritoneal; Implicações clínicas.
Foi Diretor do Departamento de Obstetrícia, Ginecologia e Medicina da Reprodução do Centro Hospitalar Universitário de Lisboa Norte, EPE (CHLN) e é Professor Catedrático Jubilado de Obstetrícia e Ginecologia da Faculdade de Medicina da Universidade de Lisboa. Desde 1985 dedicou a sua atividade profissional à Medicina da Reprodução, tendo sido responsável pela Unidade de Medicina da Reprodução do CHLN desde 1997 até à aposentação em 2021. Publicou numerosos artigos e foi preletor convidado em mais de uma centena de reuniões científicas. Para além de todas as tarefas de organização, gestão e de investigação, manteve uma atividade assistencial intensa ao longo de toda a sua vida profissional.
Desempenhou funções de Presidente da Sociedade Portuguesa de Medicina da Reprodução, de Presidente do Colégio da subespecialidade de Medicina da Reprodução da Ordem dos Médicos e, recentemente, de Presidente da Sociedade Europeia de Reprodução Humana e Embriologia. É membro do Conselho Nacional de Procriação Medicamente Assistida, entidade dependente da Assembleia da República responsável pela regulação a nível nacional da aplicação destas técnicas terapêuticas.
© l idel –e dições t écnicas
Qualquer livro de um único autor espelha inevitavelmente uma visão limitada, potencialmente distorcida pelos seus interesses, tendo em contrapartida assegurada a coerência interna dos conceitos. Este livro tem por base a minha vivência e reflexão sobre várias dimensões da reprodução humana ao fim de quase 40 anos de atividade clínica dedicada a acompanhar e tentar ajudar doentes com dificuldade em concretizar os seus projetos reprodutivos.
Nesse longo intervalo de tempo, assisti a enormes transformações na aplicação à clínica dos conhecimentos de ciências básicas referentes à reprodução, que sofreram um desenvolvimento verdadeiramente exponencial. E acompanhei igualmente uma evolução conceptual na estruturação da especialidade médica que culminou com a criação de uma subespecialidade formal. A este propósito, foi percorrido um longo caminho de progressiva compreensão e valorização desta vertente da atuação ginecológica, desde a designação arcaica “esterilidade”, passando pela denominação “infertilidade”, até à atual, mais abrangente, “Medicina da Reprodução”. No seu conceito lato, pode considerar -se que a Medicina da Reprodução tem duas vertentes, ambas concorrendo para que cada um tenha os filhos que deseja e quando o deseja: 1) a da contraceção, e 2) a da atuação em situações de infertilidade. No entanto, na prática, essa designação é aplicada apenas à segunda dessas áreas e, por isso, é sobre ela que me debruçarei.
Não pretendo fazer uma descrição da evolução histórica dos conhecimentos e/ou das metodologias de diagnóstico ou de terapêutica nesta área, mas aquilo a que assisti e em que participei ao longo dos anos é, certamente, uma base fundamental para o texto que se segue.
Alguns capítulos serão dedicados a aspetos não diretamente clínicos, atrevendo -me a dar a minha perspetiva em áreas para as quais não tenho diferenciação formal. Pedindo a benevolência de algum leitor especializado em qualquer uma delas, considero esses capítulos uma forma de dar maior abrangência ao tema e de propiciar um enquadramento genérico.
Este não é um livro para especialistas, pelo que muitos temas serão abordados de forma menos profunda do que se fossem esses colegas os destinatários. No entanto, sendo dirigido, em princípio, a profissionais de saúde e a estudantes de medicina, a linguagem poderá nem sempre ser de acesso fácil a outros públicos. Mesmo assim, tentei que as explicações dos conceitos fossem o menos complexas possível dentro do razoável.
Numa nota final, não posso deixar de realçar a importância fulcral não só dos meus mestres, mas também de todos os colegas de profissão e não -colegas com quem tive oportunidade (em muitos casos, o privilégio) de me cruzar ao longo da minha vida
profissional; e de dar testemunho de quão enriquecedor foi o contacto com tantos casais inférteis, e do prazer e realização pessoal por ter contribuído para a concretização dos projetos de vida de uma boa parte deles.
Carlos Calhaz Jorgede acordo com a declaração Universal dos direitos Humanos, um dos direitos fundamentais dos indivíduos é o de constituir família, sem limitação devido à raça, à nacionalidade ou à religião. (United nations, 1948)
a evolução de perspetivas sociais e o entendimento lato deste princípio levaram, em muitos países, ao reconhecimento de que o mesmo se aplica a indivíduos sem parceiro ou parceira e a casais de pessoas do mesmo sexo. O que tem óbvias implicações no âmbito da medicina da reprodução.
© l idel –e dições t écnicas
A afirmação contida no título deste capítulo espelha a complexidade da situação, pois é indiscutível que, por um lado, a infertilidade é uma doença, mas, por outro, está muito ligada a comportamentos e opções dos envolvidos.
De facto, a infertilidade conjugal, definida como a incapacidade de conseguir uma gravidez clínica após 12 meses de vida sexual regular, na ausência de qualquer cuidado ou método contracetivo, é considerada uma doença pela comunidade médica e científica há dezenas de anos. Apesar de a Organização Mundial da Saúde (OMS) ter direcionado a sua atenção essencialmente para o problema da sobrepopulação mundial e para a necessidade de difundir metodologias de contraceção, esta instituição reconheceu também a infertilidade como uma doença, que passou a constar, há vários anos, da International Classification of Diseases, publicada por essa organização.
No entanto, como veremos adiante (capítulo 6), nem sempre há situações de doença identificáveis como causa da infertilidade conjugal. Na nossa organização social, é mais do que evidente um fenómeno denominado parentalidade tardia, isto é, a tomada de decisão de procriar em idades mais avançadas. Um dos indicadores habitualmente usados nesta área é a idade feminina no primeiro parto. Em 2020, esta foi de 29,5 anos nos países da União Europeia, e essa tendência crescente é contínua há mais de 20 anos (EUROSTAT, PORDATA).
Embora sejam discutidas potenciais implicações negativas da idade do parceiro masculino para a reprodução, um fator cientificamente inquestionável é o do impacto negativo da idade feminina na eficácia reprodutiva (Figura 1.1). De forma simplificada, é adequado lembrar que a espermatogénese – processo de desenvolvimento e maturação das células reprodutivas masculinas – ocorre em ondas contínuas desde a puberdade, sendo a duração de cada uma (entre o início da diferenciação e a formação final dos espermatozoides) de cerca de 70 dias. De modo completamente diferente, os ovários de uma criança do sexo feminino contêm já todos os ovócitos no momento do nascimento, embora em fase de suspensão do seu processo de desenvolvimento (no estádio diploteno da 1.ª fase da meiose). Ao longo dos anos, não só se reduz continuamente o número de ovócitos (através de um processo de apoptose dos folículos primordiais), como
sucesso de técnicas de PMA usando os ovócitos da própria com as obtidas após recurso a ovócitos de dadora, por definição mulheres jovens (com menos de 35 anos em muitos países).
Pa rto por transferência de embriões (% )
31 32 33 34 35 36 37 38 39 40 41 42 43 44 45 46 47 48 49 >=50
Idade da doente submetida a transferência de embriões (anos)
Com ovócitos da própria Com doação de ovócitos
figura 5.1.1 – taxa de parto de recém‑nascido vivo após transferência de embriões, por idade feminina, em ciclos de fertilização in vitro (fIV)/microinjeção intracitoplasmática de espermatozoides (ICSI) com ovócitos da própria e com ovócitos de dadora. (adaptado de CnPma, 2021)
As informações anteriores espelham também quanto a reprodução humana é um processo pouco eficiente. Pensa -se que as gestações clinicamente visíveis representem menos de metade das situações em que ocorre fecundação. Embora as percentagens exatas sejam impossíveis de confirmar, estima -se que aproximadamente 30% dos embriões sejam perdidos no estado pré -implantação e que cerca de outros 30% se implantem, mas isso se traduza apenas em níveis detetáveis de gonadotrofina coriónica humana (hCG, na sigla em inglês, universalmente usada) no sangue, sem que haja evolução até algo identificável por ecografia. Acresce ainda que 10 a 15% das gestações clínicas terminam em abortos, gestações ectópicas ou mortes fetais in utero (Macklon NS et al., 2002; Nybo Andersen AM et al., 2000) (Figura 5.1.2).
Progesterona Estradiol - 4 -7 0 7 4
lH – hormona luteinizante; fSH – hormona folículo‑estimulante figura 5.2.2 – Variação dos níveis hormonais durante um ciclo menstrual ideal. (fonte: ver final do capítulo)
Conforme já referido, na fase folicular do ciclo menstrual, ocorre o recrutamento de alguns folículos (7 -10) de entre o grande grupo que iniciou, cerca de dois meses antes, um processo de desenvolvimento a partir da fase de folículo primordial, em resposta a estímulos (tanto quanto se pensa, não hormonais) e por mecanismos desconhecidos. Durante esse processo, multiplicam -se as camadas de células da granulosa e aumenta de dimensões o ovócito (que se mantém em estádio diploteno da 1.ª fase da meiose desde a vida intrauterina). Só na fase de folículo secundário surgem nas células da granulosa os recetores para gonadotrofinas que permitem o recrutamento (Figura 5.2.3). Os folículos não recrutados, bem como os recrutados e não selecionados, sofrem, então, um processo de atresia e degeneram.
Células da teca
Folículo secundário
Células da granulosa
Folículo primário
Ovócito
Células da pré-granulosa
Folículo primordial
Células da teca Dependente
figura 5.2.3 – fases do desenvolvimento folicular.
Folículo dominante de Graaf
Antro Folículo pré-ovulatório
fnas
Ovulação
A Figura 5.2.4 representa, graficamente integradas, as modificações fisiológicas que ocorrem ao longo de um ciclo menstrual ideal.
Produção de gonadotrofinas pela hipófise
ovárico
Foliculogénese
Ovulação
Corpo amarelo

Produção de hormonas ováricas
Progesterona Estrogénios
Evolução do endométrio

Menstruação
figura 5.2.4 – modificações ao longo de um ciclo menstrual ideal. (fonte: ver final do capítulo)
A integridade anatómica e funcional dos genitais internos
Esta é uma asserção óbvia. Na ausência de comunicação da vagina com o útero (por agenesia vaginal, presença de septo vaginal transverso completo ou destruição do colo do útero), na ausência de útero ou trompas, nas situações de obstrução tubária bilateral (por doença ou laqueação), é fácil assumir que não poderá ocorrer uma gravidez.
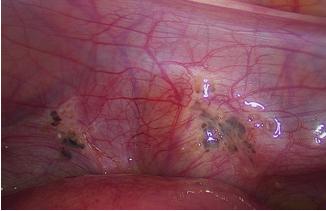
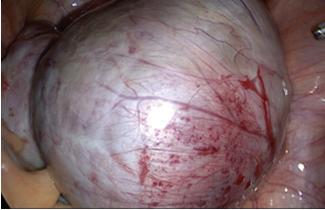

figura 6.4.1 – lesões de endometriose pélvica: a – lesões peritoneais; B – endometrioma do ovário direito; C – processo aderencial pélvico. (Imagens gentilmente cedidas pela dra. filipa Osório)
Se a teoria de Sampson parece uma explicação razoável para as lesões peritoneais (embora questionada pela existência deste tipo de lesões em algumas mulheres com laqueação de trompas), já na génese dos outros tipos de lesões participam, certamente, diversos outros mecanismos ainda em grande parte desconhecidos.
Os quistos dos ovários poderão resultar de invaginação de lesões inicialmente da sua superfície ou resultar de resíduos embrionários ou de corpos amarelos, sendo sempre indispensável a existência de características individuais peculiares das doentes.
Igualmente em condições não esclarecidas, os focos de endometriose podem ser infiltrativos, ocorrendo na espessura de estruturas de músculo liso da pelve, constituindo lesões profundas (assim classificadas por se localizarem mais de 5 mm abaixo da serosa). Outra possibilidade é terem origem em resíduos embrionários na espessura muscular. Aliás, as características comuns e a muito frequente coexistência com a adenomiose sugerem que estas duas entidades possam estar biologicamente relacionadas (Donnez J et al., 2019). As lesões de endometriose profunda podem ser encontradas um pouco por toda a pelve, incluindo o fundo de saco de Douglas/septo retovaginal, ligamentos útero -sagrados, vagina, bexiga, reto, ureter.
Além de sintomatologia resultante de localizações específicas das lesões (por exemplo, na parede da bexiga ou do reto, originando, respetivamente, hematúria ou retorragias catameniais), os sintomas que caracterizam a endometriose pélvica são dor pélvica crónica e infertilidade. Embora os valores variem com as populações avaliadas, é consensual que a endometriose é diagnosticada em 30 a 80% das doentes com dor pélvica crónica e que a prevalência da doença é de 20 a 50% em mulheres com infertilidade.
A dor pélvica pode manifestar -se como dismenorreia, dispareunia profunda ou dor persistente, praticamente contínua. A dismenorreia é habitualmente secundária, isto é, de aparecimento anos depois da menarca, e/ou apresenta -se como um agravamento progressivo da intensidade e/ou duração de dismenorreia
écnicas
e dições
informações sobre as implicações do IMC nas oscilações das fases do ciclo (Bull JR et al., 2019).
Quadro 7.3.1 – dados a obter na história clínica.
Sobre a infertilidade
• Duração da infertilidade
• Frequência das relações sexuais
• Existência de disfunções sexuais (diminuição da libido, disfunções erécteis, disfunções ejaculatórias, vaginismo)
• História de tentativas anteriores de conceção
• Períodos prévios de vida sexual sem contraceção ou usando métodos muito pouco fiáveis
• Avaliações ou tratamentos anteriores para infertilidade
História ginecológica
História menstrual:
• Idade da menarca
• Duração habitual dos ciclos menstruais; duração e características dos fluxos menstruais
• Existência de hemorragias intermenstruais
• Existência de dismenorreia, tipo e intensidade
História ginecológica geral:
• Rastreio de cancro do colo do útero, resultados e tratamentos relacionados (incluindo procedimentos excisionais)
• Tipo de contraceção usada e duração
• Dispareunia ou dor pélvica crónica
• Doenças de transmissão sexual e/ou DIP
História obstétrica
• Número de gestações anteriores (de feto único, de múltiplos) e seu desfecho (abortos clínicos, gravidezes ectópicas, gravidezes de localização desconhecida, interrupções médicas de gravidez, nados-mortos, partos de nado-vivo, tipos de parto)
• Gestações com o parceiro atual e/ou com parceiro anterior
• Complicações obstétricas (diabetes gestacional, doenças hipertensivas da gravidez, doenças da placenta, restrições de crescimento fetal, partos pré -termo)
• Doenças ou malformações congénitas na descendência
História pessoal
• Doenças médicas (especialmente endócrinas, autoimunes, genéticas, psiquiátricas ou oncológicas)
• Medicações crónicas, incluindo suplementos
• Alergias conhecidas a medicamentos e tipos de reação no passado
• Uso de medicações gonadotóxicas ou radioterapia
• Hospitalizações prévias
• Antecedentes cirúrgicos (nomeadamente sobre a pelve)
• Hábitos tabágicos, alcoólicos, drogas
• Exposição (ocupacional ou não) a agentes tóxicos
• Hábitos dietéticos e de exercício físico
• História de traumatismos psicológicos, físicos ou sexuais
(continua)
l idel –e dições t écnicas
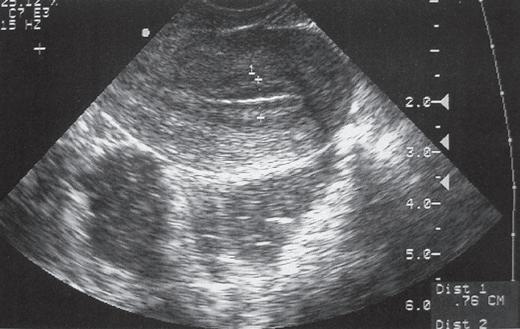

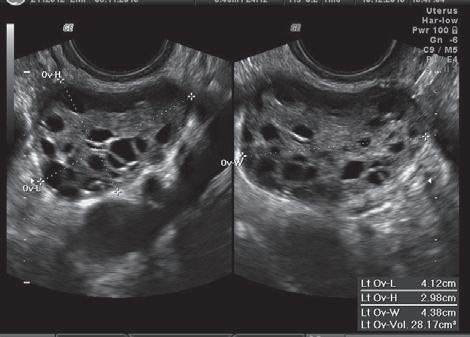
figura 7.3.1 – Imagens de ecografia pélvica usando sonda vaginal: a – corte transversal de útero normal (endométrio trilaminar, de impregnação estrogénica); B – quisto de endometriose do ovário; C – ovários poliquísticos.
Uma situação em que os critérios estão claramente definidos diz respeito aos ovários poliquísticos. Usando sondas vaginais de última geração (8 MHz), os critérios são: 20 folículos medindo 2 -9 mm em cada ovário e/ou um volume ≥10 cc em cada ovário, na ausência de folículo dominante, corpo amarelo ou quisto(s).
Se se tiver acesso apenas a condições técnicas mais antigas ou a sonda abdominal, o critério será um volume ≥10 cc em cada ovário, uma vez que a avaliação do número de folículos muito pequenos é pouco fiável (Teede HJ et al., 2023).
Também os critérios para o diagnóstico ecográfico de adenomiose têm evoluído e, de modo simplificado, podem resumir -se como: aumento da espessura da zona juncional (≥12 mm) e/ou identificação de ilhas hiperecogénicas ou quistos subendometriais e/ou, recorrendo ao Doppler a cores, aumento da vascularização e tortuosidade de vasos no miométrio. No entanto, nem sempre se encontra uma correlação entre estes achados e os resultantes da avaliação histológica (Antero MF et al., 2020).
Outro aspeto que vale a pena acentuar é que a ecografia transvaginal é a técnica padrão para a identificação de endometriomas ováricos, com níveis muito elevados de sensibilidade (93%) e especificidade (97%), quando o exame é efetuado por operador experiente.
O exame ecográfico após instilação de soro fisiológico na cavidade uterina, criando um contraste ultrassonográfico – exame designado por histerossonografia (HSoG) –, é considerado o melhor método para avaliar a cavidade uterina, podendo ser ainda complementado com recurso a ecografia tridimensional (eco 3D, na gíria clínica). É assim possível diagnosticar e caracterizar malformações uterinas (nomeadamente septos uterinos) e sinéquias uterinas, além de formações ocupando espaço na cavidade uterina (pólipos, fibromiomas com componente submucoso).
A ecografia com instilação transcervical de produto concebido especificamente para esse fim tem ganho importância progressiva na avaliação da permeabilidade tubária – histerossonossalpingografia (HSoSG, ou HyCoSy, na literatura anglófila).
A inspeção da pelve possibilita o diagnóstico de alterações uterinas e anexiais que podem já ser suspeitas em resultado de outro tipo de exames, mas, sobretudo, permite a visualização de situações não identificáveis por outros métodos, como é o caso das lesões peritoneais de endometriose (cuja importância causal para a infertilidade continua desconhecida como já foi realçado) e de processos aderenciais (muitas vezes contributo fundamental para a infertilidade) (Figura 7.3.4).
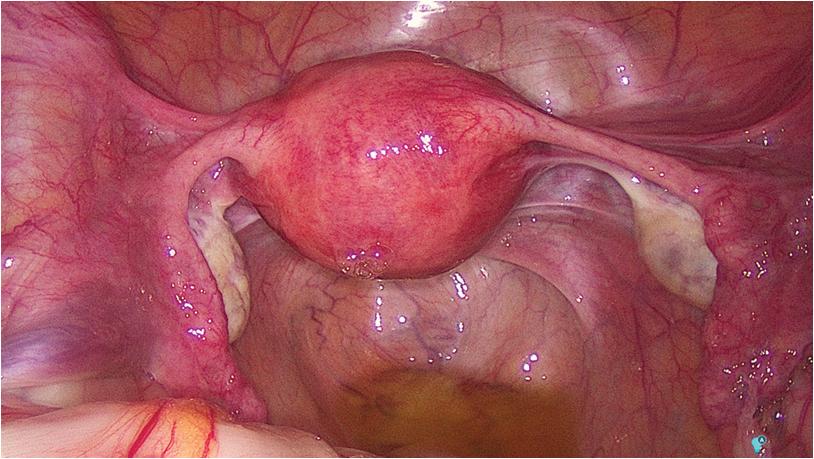
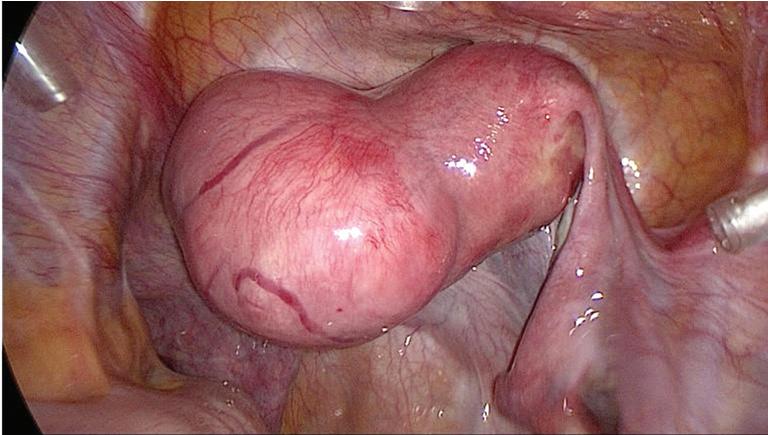
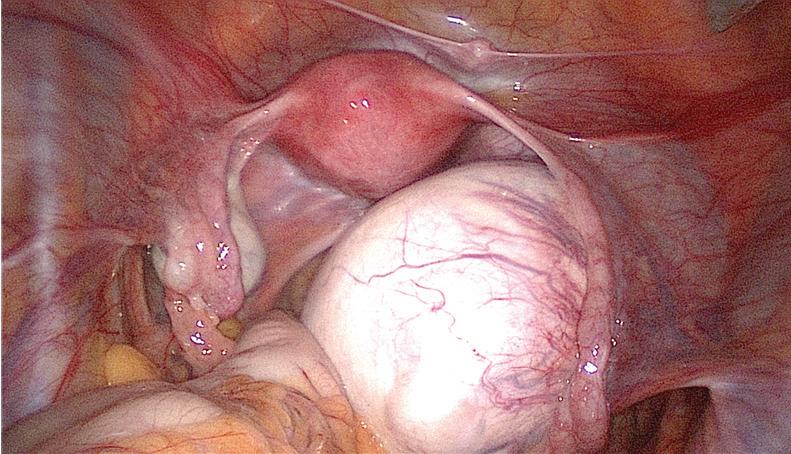
figura 7.3.4 – Imagens de laparoscopia: a – pelve normal; B – fibromioma subseroso; C –quisto do ovário direito. (Imagens gentilmente cedidas pela dra. filipa Osório)
A instilação de um corante vital (habitualmente, o azul de metileno) por via transcervical possibilita a confirmação do estado da permeabilidade tubária e das características das trompas no caso de obstrução uni ou bilateral, fornecendo igualmente informações sobre o prognóstico da sua recuperação cirúrgica. Durante muitos anos, a laparoscopia foi considerada um ato de diagnóstico indicado em todas as doentes com infertilidade. Isso foi posto em causa com a generalização do uso das técnicas de PMA, já que as informações diagnósticas obtidas por laparoscopia e não anteriormente conhecidas através do uso de métodos menos invasivos não motivam modificação na estratégia terapêutica a propor numa proporção significativa de doentes. Assim, há mais de 20 anos, o recurso a laparoscopia é limitado às situações em que exames prévios apontam para a existência de alterações/anomalias passíveis de esclarecimento e/ou resolução cirúrgica.
© l idel –e dições t écnicas
Quadro 9.1.1 – avaliação de casais com abortos de repetição.
avaliações recomendadas
• Colheita crítica de história pessoal e familiar
• Avaliação da função tiroideia
• Avaliação pélvica, imagiológica
• Rastreio de síndrome de anticorpos antifosfolípidos (anticoagulante lúpico, anticorpos anticardiolipina – IgG e IgM –, anticorpos anti -beta 2 glicoproteína I – IgG e IgM) avaliações que podem ser consideradas
• Cariótipo
• Estudo da fragmentação do ADN espermático
• Pesquisa de anticorpos antinucleares
testes não recomendados por rotina*
• Avaliação da reserva ovárica
• Avaliação de resistência à insulina
• Determinação de HLA
• Doseamento de androgénios (nomeadamente testosterona)
• Doseamento de homocisteína plasmática
• Doseamento de progesterona (como teste de insuficiência luteínica)
• Doseamento de prolactina
• Espermograma
• Estudo de células NK (no sangue ou no endométrio)
Hla – antígeno leucocitário humano; nK – natural killer
* testes que não fornecem indicações sobre a causa da situação, não contribuem para a decisão terapêutica e/ou não ajudam no estabelecimento do prognóstico.
Assim, dadas as implicações da função tiroideia na reprodução e a discrepância entre os dados publicados, é recomendado que sejam avaliados os níveis de TSH entre as 7 e as 9 semanas de gestação em mulheres com abortos de repetição e hipotiroidismo subclínico e/ou autoimunidade para a tiroide diagnosticados previamente. Se nessa avaliação for detetado hipotiroidismo (T4 livre diminuída), este deverá ser tratado com levotiroxina.
Em princípio, nas situações de abortos de repetição seria desejável efetuar o estudo cromossómico/genético do produto de conceção. Isso, na prática, é extremamente difícil, quer porque a expulsão do produto ocorre muitas vezes fora de instalações médicas, quer pela necessidade de ter disponível material específico para a sua conservação, quer ainda pela grande dificuldade em excluir contaminação com tecido decidual materno usando as técnicas laboratoriais mais generalizadas. Por isso, nas guidelines referidas, não é recomendada a análise cromossómica/genética de produtos de conceção após perda obstétrica, exceto em âmbito de investigação.
Em relação à avaliação dos membros do casal, e embora noutras séries os valores possam ser diferentes, num grande estudo retrospetivo que incluiu 20 432 casais referenciados para investigação etiológica de abortos de repetição,
