L’evidenza a supporto della scelta.
Esperti a confronto







Conducono:
Armando Santoro (Direttore Humanitas Cancer Center, IRCCS Humanitas Research Hospital, Milano)
Giorgio Vittorio Scagliotti (Direttore SCDU Oncologia Medica, AOU San Luigi Gonzaga, Orbassano, TO)
Intervengono:
Federico Cappuzzo (Direttore Oncologia Medica 2, Istituto Nazionale dei Tumori IRCCS Regina Elena, Roma)
Francesco Grossi (Direttore Oncologia, Ospedale di Circolo di Varese)
Lorenza Landi (Responsabile UOSD Sperimentazioni cliniche: Fase 1 e Medicina di Precisione, Istituto Nazionale Tumori IRCCS Regina Elena, Roma)
Paolo Maione (Dirigente Medico U.O. Oncologia Medica, A.O. «S.G.Moscati», Avellino)
Cemiplimab è un anticorpo monoclonale completamente umano che ha come target il recettore del checkpoint immunitario PD-1 sulle cellule T. Legandosi a PD-1, cemiplimab ha dimostrato di saper impedire alle cellule tumorali il blocco del pathway di PD-1 per sopprimere l’attivazione delle cellule T. Cemiplimab è disponibile in Italia dal 2020 quale prima immunoterapia specifica per il carcinoma cutaneo a cellule squamose (CSCC) in stadio metastatico o localmente avanzato, quando chirurgia e radioterapia non sono più applicabili con intento curativo (vedi su Oncoinfo il commento di Paola Queirolo ai dati presentati ad ASCO 2020). Recentemente, al carcinoma cutaneo squamoso si sono aggiunte due nuove indicazioni oncologiche: il carcinoma basocellulare della cute localmente avanzato o metastatico e il carcinoma polmonare non a piccole cellule (NSCLC), metastatico o localmente avanzato, non candidabile a chemio/radioterapia e con espressione di PD-L1 ≥50%.
Il carcinoma basocellulare è la tipologia più comune di cancro della cute a livello globale e la sua incidenza è in aumento in molti paesi europei. In questa patologia, cemiplimab ha mostrato un beneficio clinico importante nei pazienti con malattia localmente avanzata o metastatica che non tollerano o che vanno in progressione dopo un trattamento di prima linea con inibitori del pathway hedgehog (HHI). Quanto al tumore del polmone, seconda neoplasia più frequente negli uomini dopo il tumore alla prostata e terza più frequente fra le donne dopo il tumore al seno e al colon-retto, quello non a piccole cellule è la forma più comune (80-90% dei casi). La rimborsabilità di AIFA nel NSCLC avanzato/ metastatico si basa sui dati positivi di sopravvivenza globale (OS) e di sopravvivenza libera da progressione (PFS) dello studio EMPOWER-Lung 1, uno studio in aperto, randomizzato, multicentrico di fase 3 presentato all’ESMO 2020 che ha dimostrato
la superiorità di cemiplimab rispetto alla chemioterapia nel setting di pazienti con espressione di PDL1 ≥50% 1 (già commentato a suo tempo su Oncoinfo da Giorgio Scagliotti). Il trattamento in monoterapia di prima linea può essere offerto, oltre ai pazienti in stadio metastatico, anche ai pazienti con malattia in fase localmente avanzata non candidabili alla chemio/radioterapia definitiva, purché esprimano PD-L1 in almeno il 50% delle cellule tumorali e non abbiano alterazioni di EGFR, ALK o ROS1. Al congresso AIOM 2022 si è tenuto un interessante simposio – sponsorizzato da Sanofi – in cui si è discusso, in modalità tavola rotonda, sulla nuova indicazione relativa al NSCLC.
I moderatori, Giorgio Scagliotti e Armando Santoro hanno aperto i lavori presentando cemiplimab, nuovo farmaco immunoterapico che si aggiunge alla lunga lista di trattamenti per il NSCLC destinata senz’altro a crescere nei prossimi anni. Il simposio si è concentrato sui pazienti con espressione di PD-L1 uguale o maggiore al 50%, che oggi rappresentano il 20-30% dei tumori polmonari non a piccole cellule. Quello che ad oggi sappiamo dalle evidenze scientifiche è che l’immunoterapia da sola è più efficace rispetto allo standard degli anni ‘90-‘00, rappresentato dalla chemioterapia con derivati del platino. Farmaci immunoterapici come pembrolizumab e atezolizumab si sono dimostrati superiori alle doppiette di chemioterapia a base di platino nell’ambito di studi randomizzati in cui la superiorità continua ad essere evidente anche al crescere del follow-up (Figura 1).2,3,4 In questo setting di pazienti si deve aggiungere oggi lo studio registrativo EMPOWER-Lung 11 che ha utilizzato cemiplimab, anticorpo monoclonale umano diretto verso il recettore del checkpoint immu-
nitario PD-1 sulle cellule T. Francesco Grossi ha illustrato le caratteristiche di questo studio, dotato di peculiarità molto interessanti (Figura 2).
Tutti i pazienti avevano un NSCLC in stato avanzato o metastatico, non pretrattato, con espressione di PD-L1 maggiore o uguale al 50% e senza le principali alterazioni geniche EGFR, ALK o ROS1. Il Performance Status dei pazienti era 0-1 sec. ECOG; potevano avere metastasi encefaliche clinicamente stabili e trattate e potevano essere positivi per epatite B, C ed HIV, il che rappresenta un criterio di esclusione per la maggioranza degli studi. La randomizza-
zione (1:1) avveniva tra cemiplimab a dose standard (350 milligrammi e.v. ogni 3 settimane per un massimo di 2 anni) e una chemioterapia standard per 4-6 cicli a scelta dell’investigatore. Una peculiarità importante di questo studio, non riscontrata in altri, è che i pazienti in trattamento con cemiplimab potevano, a progressione di malattia, continuare il trattamento con l’immunoterapia in associazione a 4 cicli di chemioterapia. Inoltre, ai pazienti inseriti nel braccio di controllo veniva consentito il crossover a cemiplimab a progressione di malattia. Questo aspetto è molto interessante nell’economia dello
Key Eligibility Criteria
Treatment-naïve advanced NSCLC
PD-L1 ≥50%
No EGFR, ALK, or ROS1 mutations
ECOG performance status 0 or 1
Treated, clinically stable CNS metastases and controlled hepatitis B or C or HIV were allowed
Stratification Factors
Histology (squamous vs non-squamous)
Region (Europe, Asia, or ROW)
Arm A Cemiplimab monotherapy
350 mg IV Q3W Treat until Progressive Disease or 108 weeks
R 1:1
Arm B
4-6 cycles of investigator’s choice chemotherapy
Progressive Disease Progressive Disease
Optional continuation of cemiplimab + 4 cycles of chemotherapy
follow-up
Optional crossover to cemiplimab monotherapy
Primary: OS and PFS
Secondary: ORR (key), DOR, HRQoL, and safety
PD-L1 ≥50% population (N=565†) PD-L1 testing by 22C3 assay performed per instructions for use
ALK, anaplastic lymphoma kinase; CNS, central nervous system; DOR, duration of response; ECOG, Eastern Cooperative Oncology Group; EGFR, epidermal growth factor receptor; HIV, human immunodeficiency virus; HRQoL, health-related quality of life; IV, intravenous; NSCLC, non-small cell lung cancer; ORR, objective response rate; OS, overall survival; PD-L1, programmed cell death-ligand 1; PFS, progression-free survival; Q3W, every 3 weeks; R, randomised; ROS1, c-ros oncogene 1; ROW, rest of the world
studio, poiché il 74% dei pazienti ha ricevuto cemiplimab in seconda linea a progressione dopo chemioterapia.
Le caratteristiche dei pazienti arruolati nello studio meritano alcune considerazioni. Si registra, in primo luogo, una prevalenza di pazienti di sesso maschile (oltre l’80% del totale) e con ECOG PS 1 (73%), criterio, quest’ultimo, abbastanza rispondente alla reallife. La quota di fumatori attuali era pari a circa il 35% del totale, quando normalmente siamo intorno al 20%. Un altro dato interessante è la percentuale di pazienti con istotipo squamoso: di solito questa si aggira intorno al 20-25%, mentre in EMPOWER-Lung 1 la quota ha superato il 40% dei pazienti arruolati. Infine, va rilevato che lo studio con cemiplimab ha arruolato anche una quota (15%) di pazienti con malattia localmente avanzata che, come vedremo, porterà a un risvolto importante in pratica clinica. Analizzando i criteri di inclusione si evince, perciò, che la popolazione prevalente di questo studio è formata da maschi fumatori con istotipo squamoso, caratteristiche che in genere configurano un fenotipo non particolarmente responsivo ai trattamenti e che è meno selezionato rispetto ad altri studi.
I dati di efficacia dello studio sono stati analizzati da Federico Cappuzzo. Dopo il primo anno di followup, secondo quanto pubblicato nel 2021 su Lancet,1 cemiplimab è risultato significativamente superiore alla chemioterapia nei due endpoint primari dello studio (sopravvivenza globale (OS) e sopravvivenza libera da progressione (PFS) ed in alcuni endpoint secondari, come le risposte obiettive (ORR) e la durata della risposta (DoR)(Figura 3).
I dati aggiornati a 3 anni di follow-up, presentati al congresso ESMO 2022,5 hanno confermato gli stessi risultati, con un beneficio significativo a favore di cemiplimab in termini di OS (Hazard Ratio 0,57 – Figura 4a), PFS (Hazard Ratio 0,51 – Figura 4b) e di risposte obiettive (Odds Ratio 3,26 – Figura 4c).
Da notare, nella parte finale delle curve di PFS (Figura 4b), l’elevata quota di pazienti vivi e che continua-
no a beneficiare della terapia con cemiplimab a distanza di tempo dall’inizio del trattamento. I pazienti trattati con cemiplimab vivono significativamente di più rispetto ai pazienti trattati con chemioterapia e vi è un ritardo importante nella comparsa della progressione di malattia. Se volessimo fare un confronto indiretto, in termini puramente numerici, con gli altri immunoterapici attivi nei pazienti con PD-L1 iperespresso, cemiplimab mostra i risultati migliori. Inoltre, nello studio EMPOWER-Lung 1, il braccio di controllo della chemioterapia performa esattamente secondo le aspettative, il che è indice di un dato assolutamente credibile.
Un dato importante che emerge dall’analisi della sopravvivenza è che con cemiplimab, a differenza di quanto in genere accade negli studi di confronto immunoterapia vs chemioterapia, non vi è, all’inizio, un andamento peggiore nei pazienti trattati con immunoterapia. Inoltre, c’è da rilevare che il tasso di risposte obiettive ottenuto da cemiplimab è più che doppio rispetto alla chemioterapia (46,5% vs 21%). Questo è un dato di grande rilevanza poiché, se all’inizio si riteneva che la risposta all’immunoterapia non fosse importante, oggi invece sappiamo che i pazienti lungosopravviventi, di fatto, sono anche quelli che rispondono al trattamento. Il tasso di risposte obiettive diventa, perciò, con cemiplimab, un fattore predittivo di sopravvivenza a lungo termine. Questo aspetto lo vediamo sia con la durata delle risposte, che è significativamente più alta nei pazienti trattati con questo farmaco (23,6 mesi vs 5,9 mesi della chemioterapia), sia con il fatto che le risposte complete nei pazienti trattati con immunoterapia aumentano con il passare del tempo (2,1% dopo 1 anno vs 8,1% dopo 3 anni). Per quanto riguarda l’aggiornamento a 3 anni, si conferma pienamente quello che già era noto dopo i primi 12 mesi di follow-up: l’eventuale effetto confondente del crossover, che solitamente emerge al crescere del follow-up, è superato dall’effetto del cemiplimab somministrato in prima linea. Va sottolineato
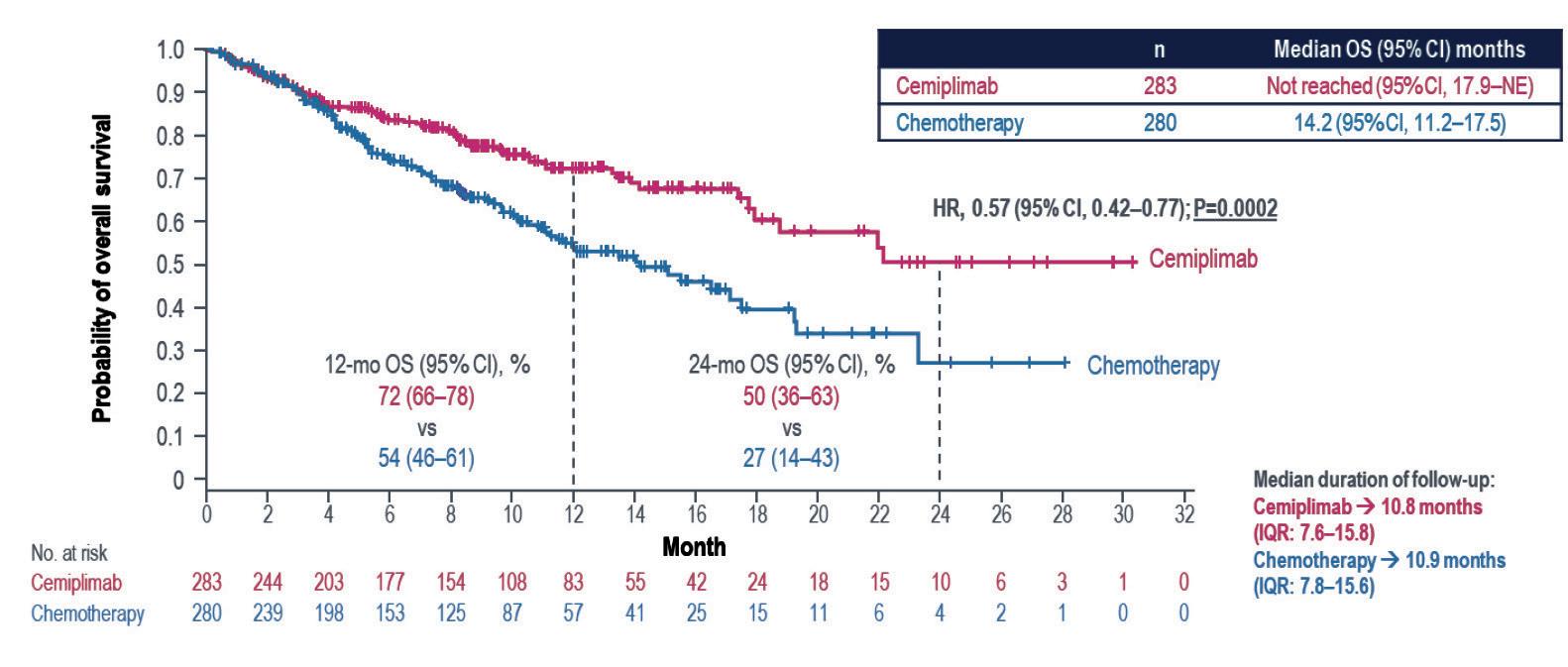
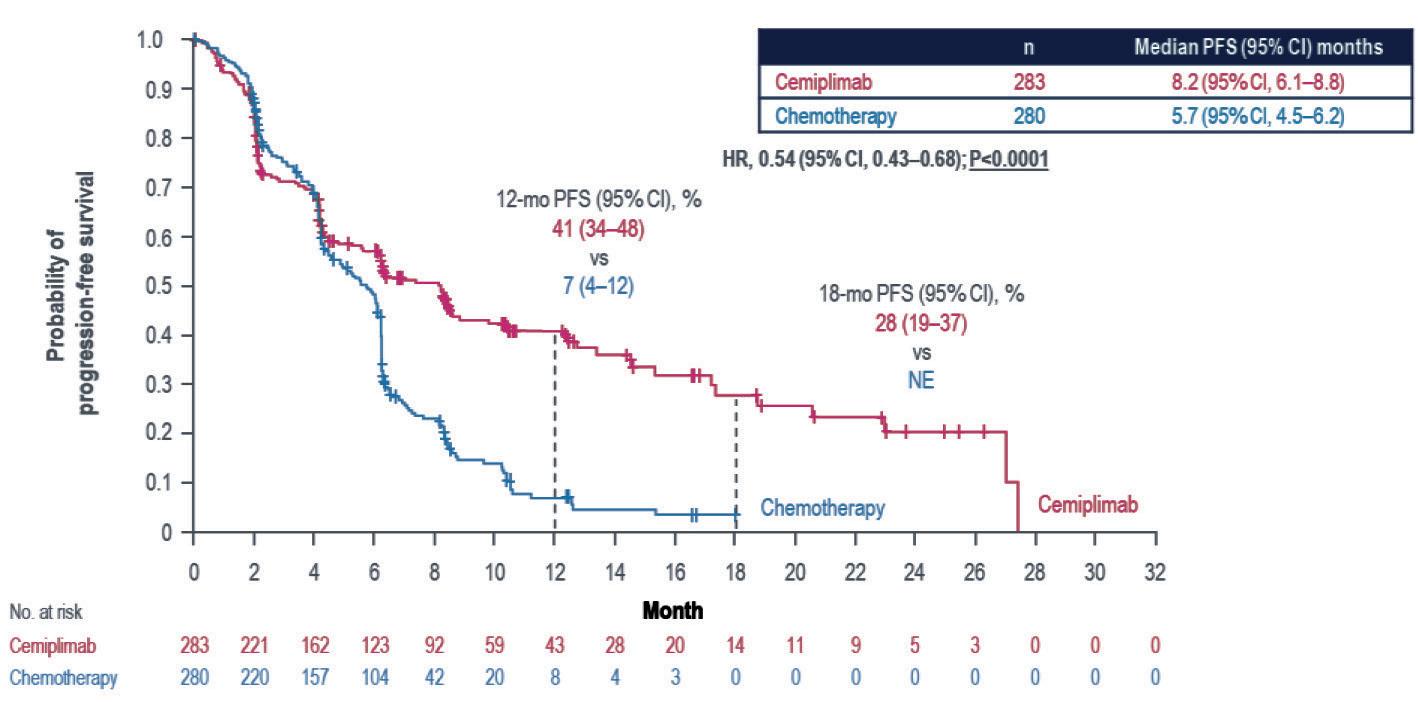
Figura 4a. Studio EMPOWER-Lung 1: curve di OS ad un follow-up di tre anni (mediana 37,1 mesi)
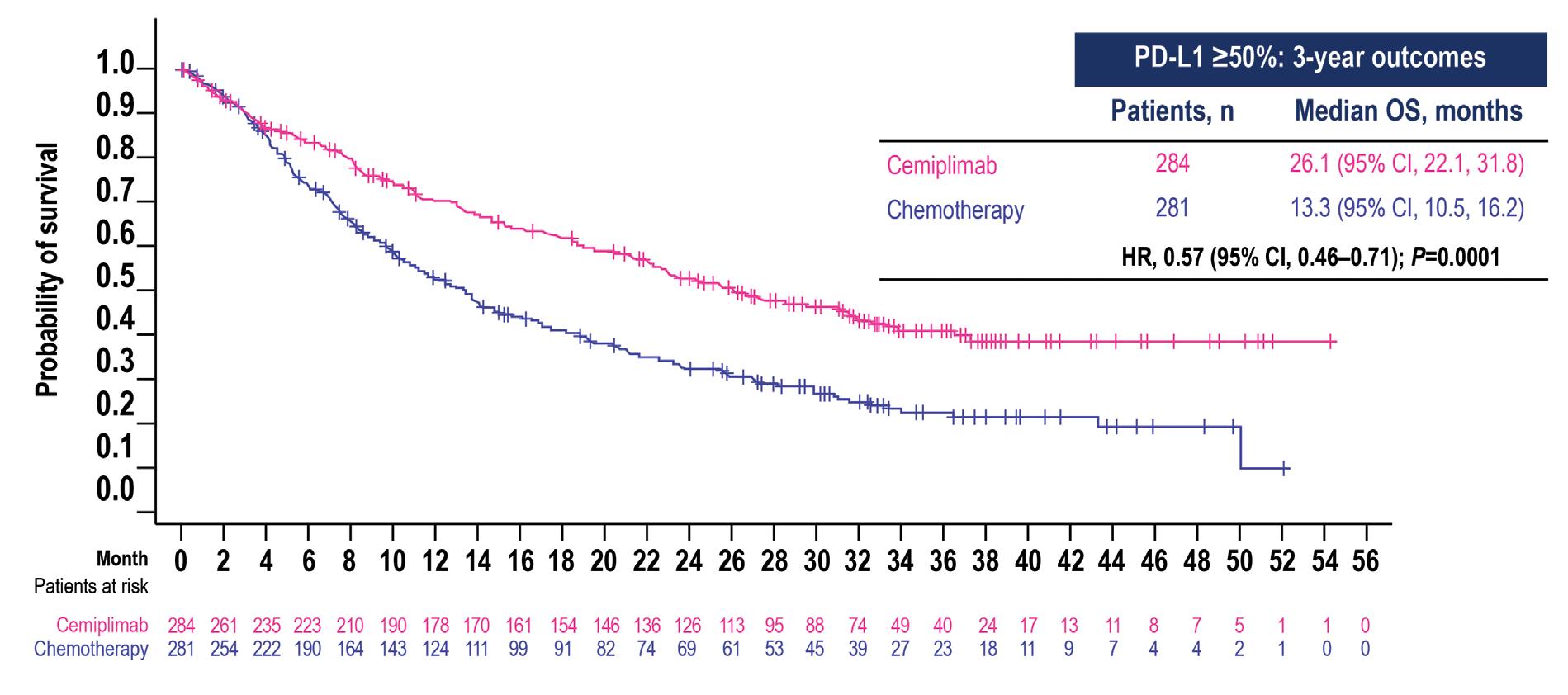
CI, confidence interval; HR, hazard ratio; OS, overall survival; PD-L1, programmed cell death-ligand 1.
Figura 4b. Studio EMPOWER-Lung 1: curve di PFS ad un follow-up di tre anni (mediana 37,1 mesi)
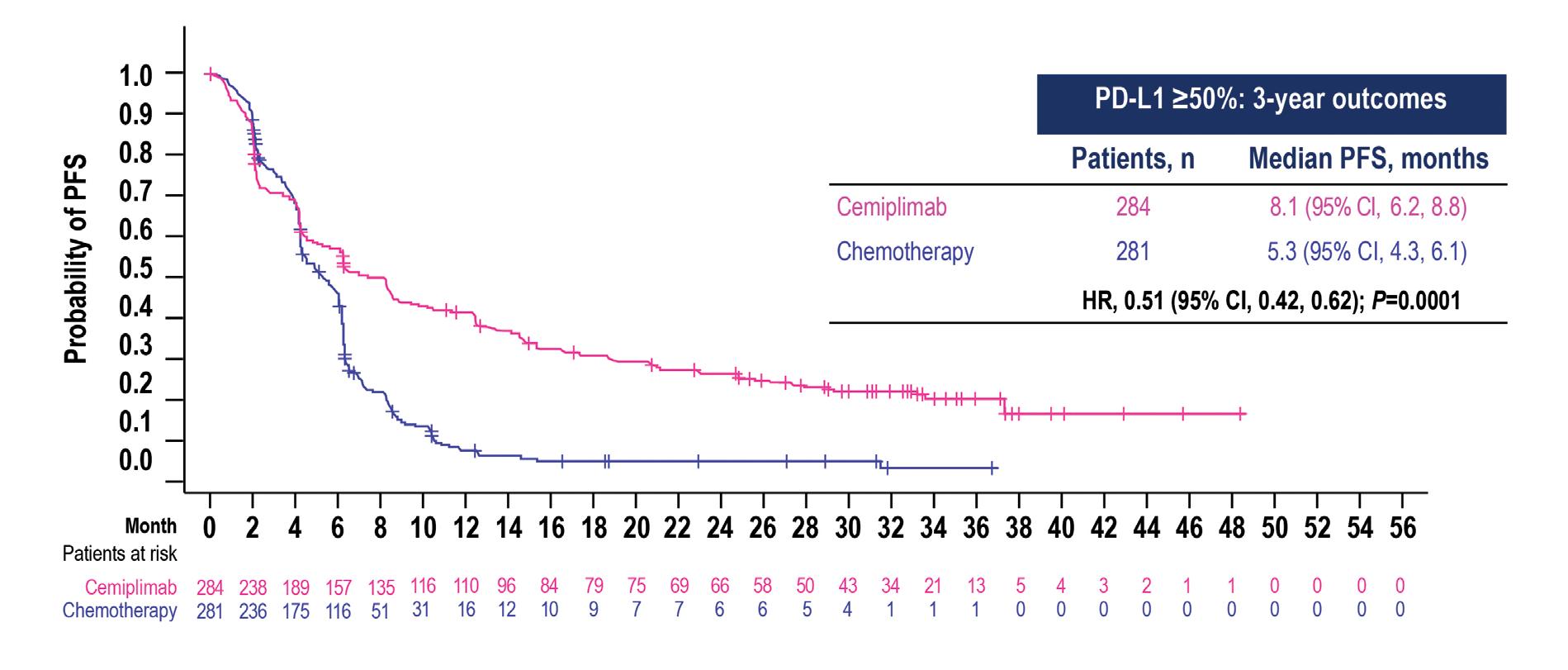
CI, confidence interval; HR, hazard ratio; PFS, progression-free survival; PD-L1, programmed cell death-ligand 1.
quindi ancora una volta che, nei pazienti con espressione PD-L1 di almeno il 50%, l’immunoterapia deve essere offerta immediatamente e il più velocemente possibile. Riservare l’immunoterapia in linee successive, nel NSCLC, può rivelarsi una cattiva strategia terapeutica, perché l’impatto dell’immunoterapia di salvataggio dopo chemioterapia risulta inferiore per diversi motivi. Uno dei principali è che i pazienti trattati in linee successive sono in condizioni generali spesso non ottimali per poter beneficiare del trattamento immunoterapico. Il NSCLC è una malattia evolutiva in cui spesso, già nel passaggio dalla prima alla seconda linea, soprattutto quando non vi sono bersagli molecolari aggredibili con terapia mirata, le condizioni generali tendono a scadere e non si hanno i presupposti per poter beneficiare di ulteriore trattamento.
Armando Santoro, tornando alle curve di sopravvivenza dello studio EMPOWER-Lung 1, fa notare che inizialmente esse non si aprono e solleva il quesito per cui, anche in questa fascia di pazienti con alta
espressione di PD-L1, potrebbe esserci un certo interesse a provare una chemio-immunoterapia di combinazione. Una possibile spiegazione è che alcuni pazienti potrebbero beneficiare di un utilizzo combinato della chemio-immunoterapia, in particolare quelli in cui c’è bisogno di ottenere una risposta rapida e quelli in cui temiamo che un’eventuale non risposta all’immunoterapia possa poi compromettere le possibilità del paziente di ricevere un trattamento efficace.
Figura 4c. Studio EMPOWER-Lung 1: aggiornamento ORR ad un follow-up di tre
Overall Tumor Response, n (%)
Nella seconda parte del simposio si è passati ad analizzare se, all’interno della popolazione arruolata nello studio EMPOWER-Lung 1, potessero esserci dei gruppi di pazienti in grado di beneficiare, più di altri, del trattamento con cemiplimab. Più in dettaglio, si è discusso dei risultati dello studio all’interno dei seguenti sottogruppi di pazienti:
con metastasi cerebrali;
con malattia localmente avanzata non candidabili a chemio/radioterapia;
con istologia squamosa;
con diversi livelli di espressione di PD-L1 oltre il 50%;
che hanno proseguito cemiplimab oltre la progressione.
I pazienti con metastasi cerebrali da NSCLC rappresentano un problema poiché spesso rispondono poco e male ai trattamenti sistemici. Il sistema nervoso centrale (SNC), infatti, è un “santuario” nel quale accedono con difficoltà molti farmaci oncologici sia per le loro caratteristiche molecolari (idrosolubilità vs liposolubilità) sia per i meccanismi di difesa espletati tramite la barriera ematoencefalica. Lorenza Landi ha esposto le caratteristiche e i risultati dello studio EMPOWER-Lung 1 nei pazienti con metastasi al SNC. Lo studio ha arruolato il 12% di pazienti con metastasi encefaliche in entrambi i bracci di trattamento. Queste metastasi dovevano essere trattate e clinicamente stabili prima dell’ingresso in studio, criterio simile a quella che è la nostra pratica clinica quotidiana. In relazione all’obiettivo primario dello studio (OS), dal forest plot si evidenzia un dato straordinario nei pazienti con metastasi encefaliche. Sebbene i numeri siano abbastanza piccoli, il vantaggio in sopravvivenza di cemiplimab rispetto alla chemioterapia si manifesta con un Hazard Ratio pari a 0,17 6 (Figura 5).
Il messaggio, al di là della scarsa numerosità dei pazienti, del fatto che il trial non aveva tra gli endpoint la valutazione dell’attività intracranica e del fatto che i pazienti erano tutti trattati con radioterapia, è che i pazienti con metastasi encefaliche hanno comunque buone probabilità di avere lo stesso beneficio dal trattamento con cemiplimab rispetto ai pazienti che non le hanno. È importante anche porre l’attenzione sul dato di ORR nei pazienti con metastasi al SNC: in relazione a questo parametro, il divario tra il braccio cemiplimab e il braccio chemioterapia è veramente marcato (41.2% vs 8.8%). Attenzione: stiamo parlando non di attività intracranica ma di attività sistemica; tuttavia, in ogni caso, questi pazienti che in teoria sono prognosticamente sfavoriti sembrano beneficiare come e più degli altri dalla terapia offerta. Un problema difficile nella pratica clinica quotidiana è quello relativo ai pazienti con metastasi encefaliche sintomatiche e/o che necessitano di alte dosi di cortisone. In questi casi, come si può conciliare al meglio l’immunoterapia con la radioterapia e con le dosi di cortisone necessarie a ridurre l’edema perilesionale? Questi pazienti, in relazione alla sede di diffusione intracranica e all’entità dell’edema cerebrale, andrebbero eventualmente prima stabilizzati con la radioterapia. D’altronde, il trattamento con gli steroidi non può essere di lungo periodo; essi dopo un po’ vanno sospesi e il problema di interferenza con l’immunoterapia non si pone. I componenti del panel ritengono anche che non vi siano problemi di tollerabilità nel far partire, eventualmente, una radioterapia in contemporanea all’immunoterapia. Un altro setting di pazienti che potrebbe beneficiare dell’immunoterapia è quello dei localmente avanzati non candidabili a trattamento chemio/radioterapico, concomitante o sequenziale. Paolo Maione ha presentato i dati dello studio EMPOWER-Lung 1 relativi a questo sottogruppo di pazienti,7 che potrebbero essere molto utili per la pratica clinica quotidiana. È cosa nota che, nello stadio localmente avanzato, anche in presenza di una espressione PD-L1
Figura 5. Studio EMPOWER-Lung 1: analisi (post-hoc) della OS in pazienti con metastasi encefaliche
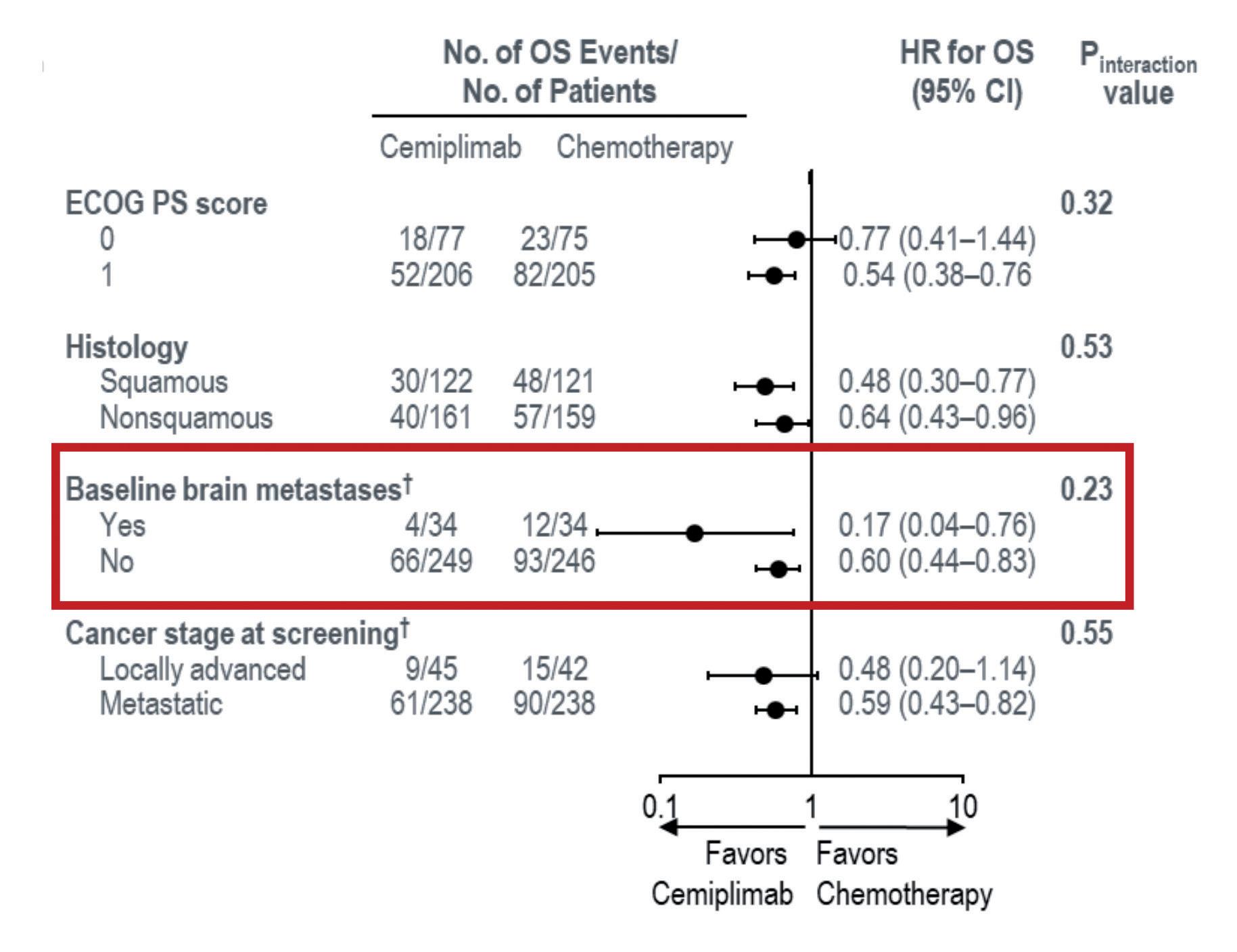
Figura 6. Studio EMPOWER-Lung 1: analisi (post-hoc) della OS nei pazienti con malattia localmente avanzata
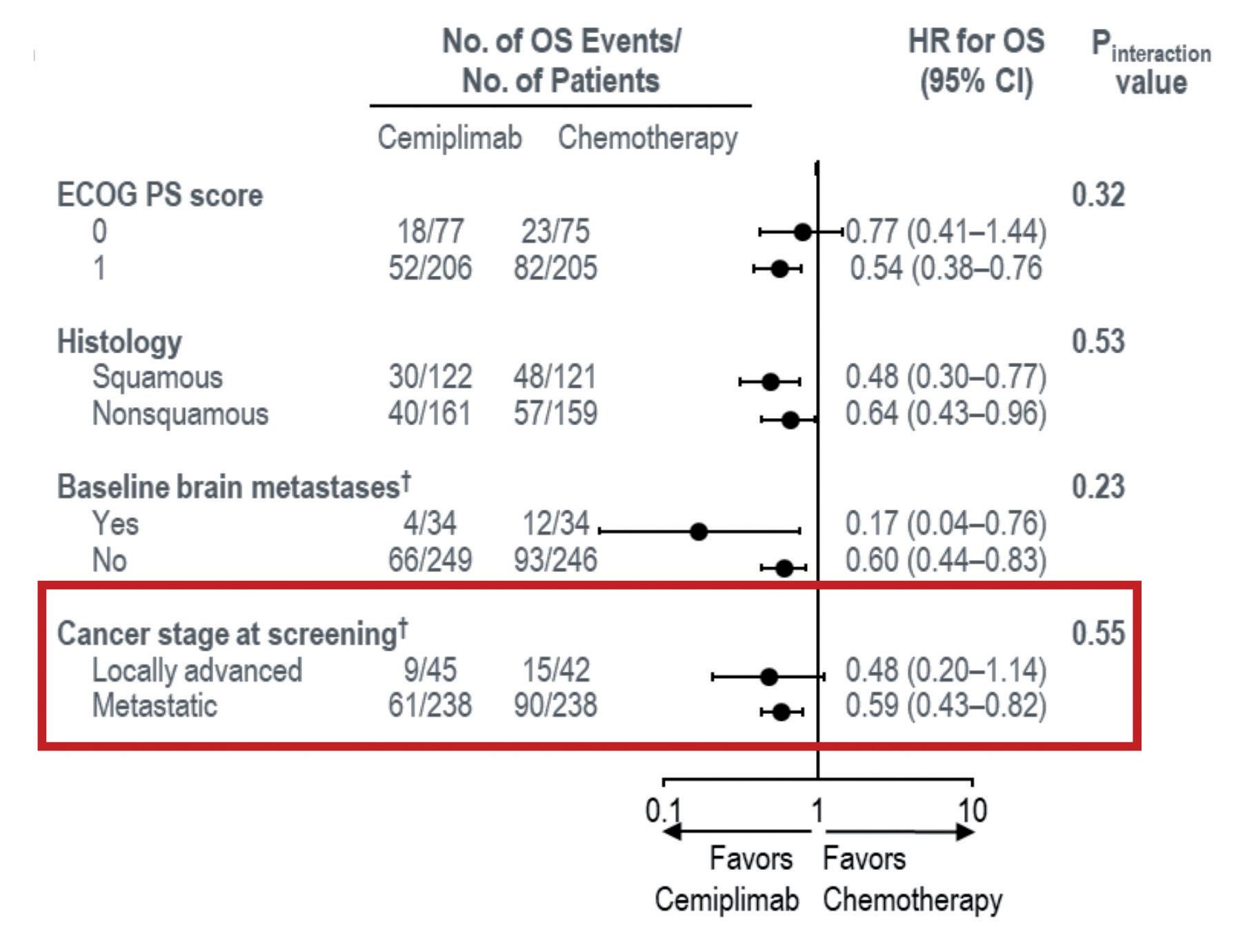
CI, confidence interval; ECOG PS, Eastern Cooperative Oncology Group performance status; OS, overall survival.
†Post-hoc analyses; all others are prespecified exploratory analyses. Limitations: subgroup analysis was not powered to show a statistically significant difference between or within individual subgroups. The small number of events precludes drawing any firm conclusions on the benefit of cemiplimab in these subpopulations (female patients and patients enrolled in Asia).
CI, confidence interval; ECOG PS, Eastern Cooperative Oncology Group performance status; OS, overall survival.
†Post-hoc analyses; all others are prespecified exploratory analyses. Limitations: subgroup analysis was not powered to show a statistically significant difference between or within individual subgroups. The small number of events precludes drawing any firm conclusions on the benefit of cemiplimab in these subpopulations (female patients and patients enrolled in Asia).
uguale o maggiore del 50%, lo standard di cura è rappresentato dalla chemio/radioterapia concomitante, strategia da sempre sottoutilizzata per varie motivazioni: logistiche, compliance dei pazienti, condizioni generali, età e comorbidità. Quando non si riesce a fare la chemio/radioterapia concomitante si può utilizzare la strategia sequenziale, che è sicuramente una valida opzione. Ma c’è anche una quota di pazienti, piccola ma non trascurabile, in cui non ci sono le condizioni per poter erogare una chemioterapia a base di platino oppure una radioterapia, e proprio questi pazienti sono stati trattati in questo studio con cemiplimab o con chemioterapia. Si tratta di una percentuale di pazienti intorno al 15% in entrambi i bracci. Le caratteristiche erano sovrapponibili a quelle della popolazione generale, eccezion fatta per i fumatori attivi, maggiormente rappresentati, e per la percentuale dei tumori squamosi, che è del 60% contro il 40% della popolazione intentionto-treat (ITT). L’analisi (post-hoc) del sottogruppo con
malattia localmente avanzata evidenzia un risultato a vantaggio di cemiplimab nei confronti della chemioterapia, seppur non statisticamente significativo per la ridotta dimensione del campione 6 (Figura 6). In base al risultato di questa analisi di sottogruppo, AIFA ha approvato l’utilizzo di cemiplimab anche nei pazienti localmente avanzati che non possono essere sottoposti a chemio/radioterapia. Si è trattato di una decisione molto apprezzata dagli oncologi poiché ritenuta in grado di cambiare la pratica clinica quotidiana. Con cemiplimab, infatti, si offre un’opzione valida ed efficace ai pazienti non idonei a chemio/radioterapia che, fino ad oggi, non avevano alcuna alternativa terapeutica. L’esame delle curve di sopravvivenza nel sottogruppo con malattia localmente avanzata mostra, a un anno, il 78% di pazienti vivi nel braccio cemiplimab verso il 58% nel braccio chemioterapia (Figura 7).
Si potrebbe obiettare che il braccio di controllo di questo gruppo di pazienti non è la chemio/radiote -
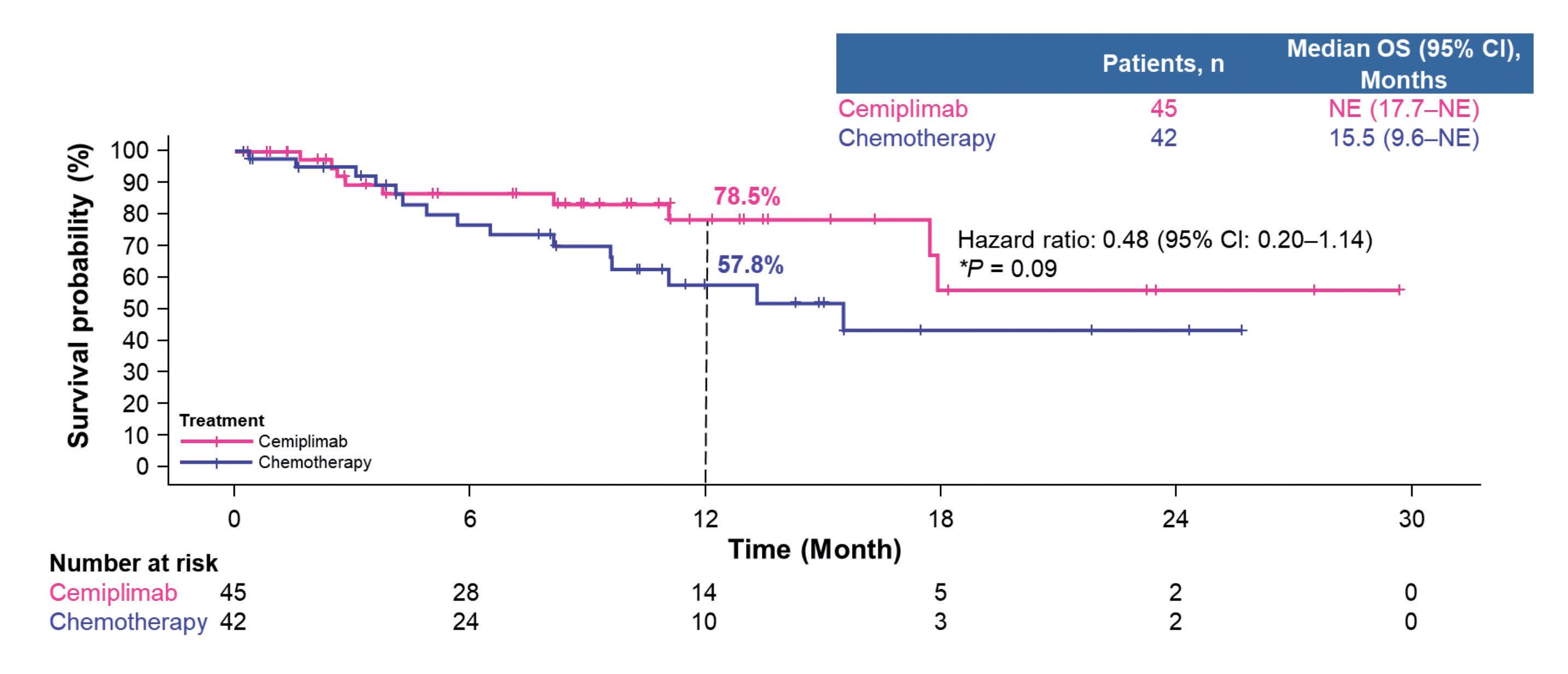
*Nominal P-value. CI, confidence interval; NE, not evaluable; OS, overall survival.
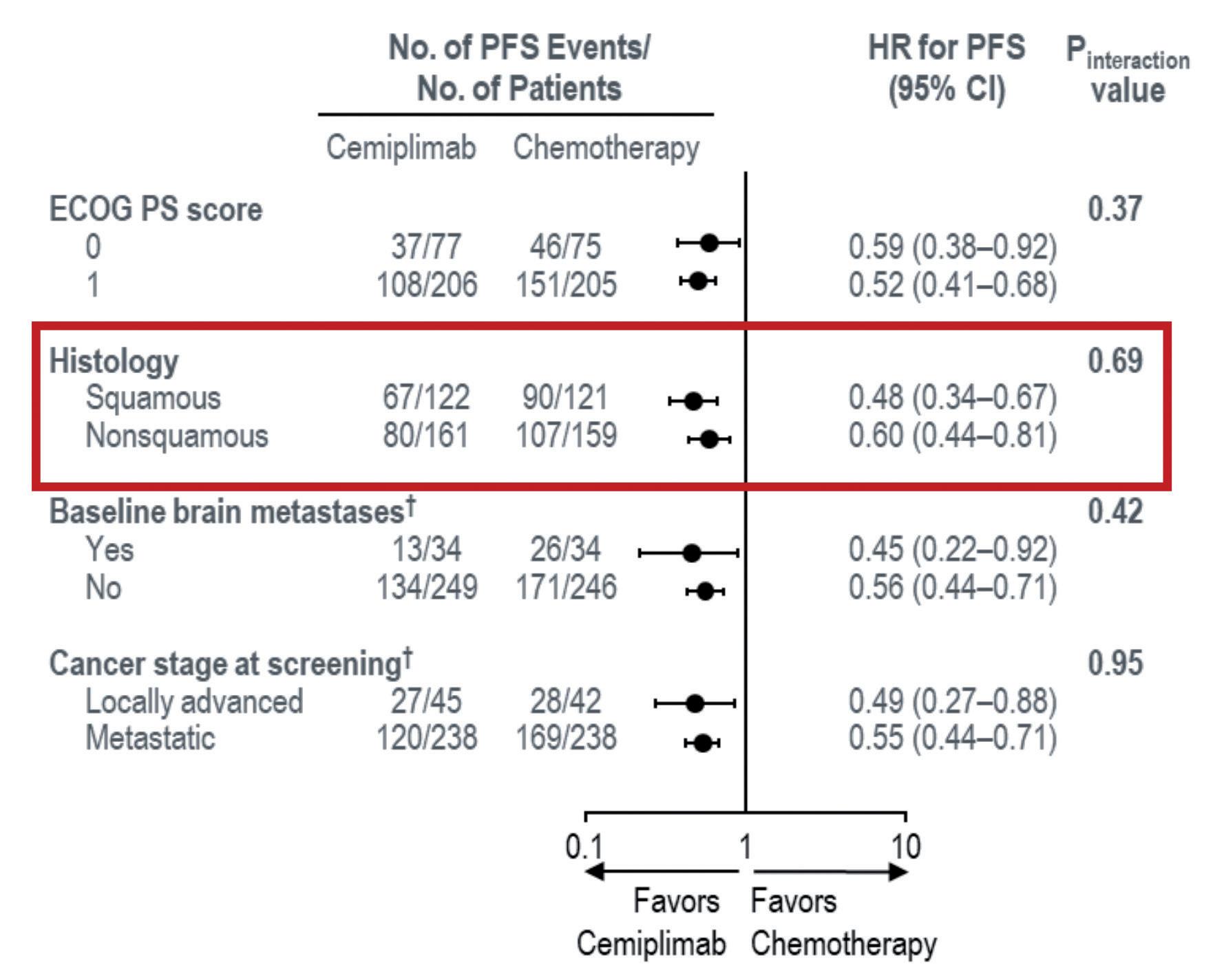
Figura 8a. Studio EMPOWER-Lung 1: analisi post-hoc della OS in pazienti con istologia squamosa
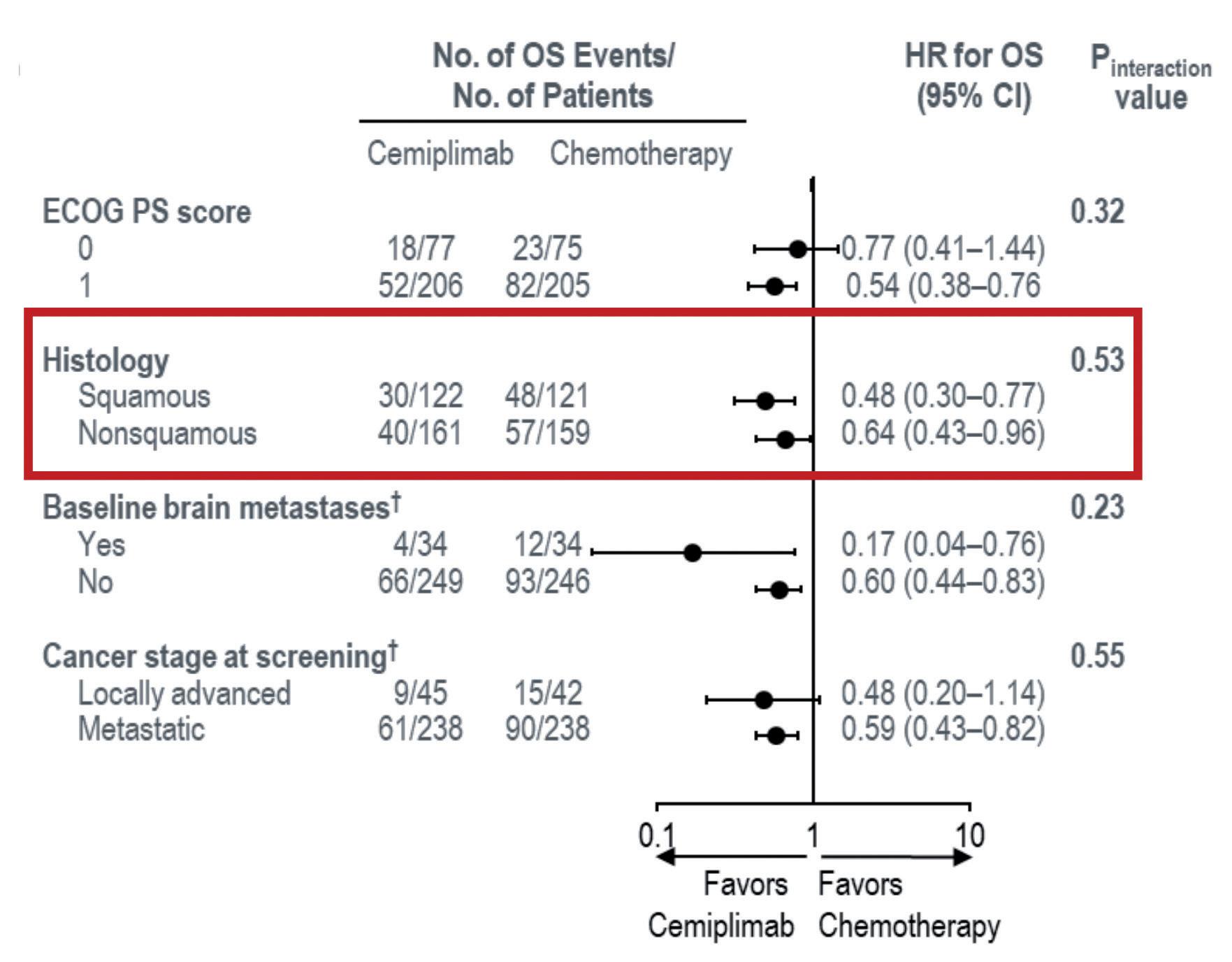
Figura 8b. Studio EMPOWER-Lung 1: analisi (post-hoc) della PFS in pazienti con istologia squamosa
CI, confidence interval; ECOG PS, Eastern Cooperative Oncology Group performance status; OS, overall survival.
†Post-hoc analyses; all others are prespecified exploratory analyses. Limitations: subgroup analysis was not powered to show a statistically significant difference between or within individual subgroups. The small number of events precludes drawing any firm conclusions on the benefit of cemiplimab in these subpopulations (female patients and patients enrolled in Asia).
CI, confidence interval; ECOG PS, Eastern Cooperative Oncology Group performance status; PFS, progression-free survival.
†Post-hoc analyses; all others are prespecified exploratory analyses. Limitations: subgroup analysis was not powered to show a statistically significant difference between or within individual subgroups. The small number of events precludes drawing any firm conclusions on the benefit of cemiplimab in these subpopulations (female patients and patients enrolled in Asia).
rapia ma, certamente, si tratta di un beneficio clinicamente utile per una piccola parte di pazienti. I risultati sono ancora più netti se andiamo ad esaminare la PFS, dove il vantaggio è statisticamente significativo a favore di cemiplimab (38% a 1 anno verso il 6% della chemioterapia), e le ORR (44% cemiplimab verso 3% chemioterapia, non statisticamente significativo). Alla luce del dato relativo alle risposte obiettive si può ipotizzare che, ove ci si trovasse in presenza di una riduzione della malattia localmente avanzata, si dovrebbe comunque valutare la possibilità di inserire, in seconda battuta, un trattamento locale.
L’istologia squamosa è un altro dei sottogruppi che potrebbero beneficiare maggiormente del trattamento con cemiplimab. Bisogna innanzitutto ricordare che cemiplimab ha già una sua storia di efficacia nell’istologia squamosa, in particolare nei carcinomi della cute. Nel trial EMPOWER-Lung 1, come detto, la percentuale di pazienti con istologia squamosa è piuttosto importante, superiore al 40% in entrambi i bracci. Quando guardiamo i dati di sopravvivenza negli altri trial clinici con l’immunoterapia, l’attività nell’istologia squamosa è in genere un po’ più bassa, cosa che sembra invece non suc-
cedere in questo studio. In EMPOWER-Lung 1, infatti, l’analisi post-hoc sembra mostrare un’attività importante di cemiplimab nei pazienti con istologia squamosa, sia in termini di OS (Figura 8a) che di PFS (Figura 8b).
Provando a fare un confronto indiretto che, ricordiamo, può avere valore solo dal punto di vista pratico e non scientifico, rispetto a tutti gli altri studi di immunoterapia cemiplimab sembra avere il vantaggio in OS più evidente nell’istologia squamosa rispetto alla chemioterapia (Figura 9).
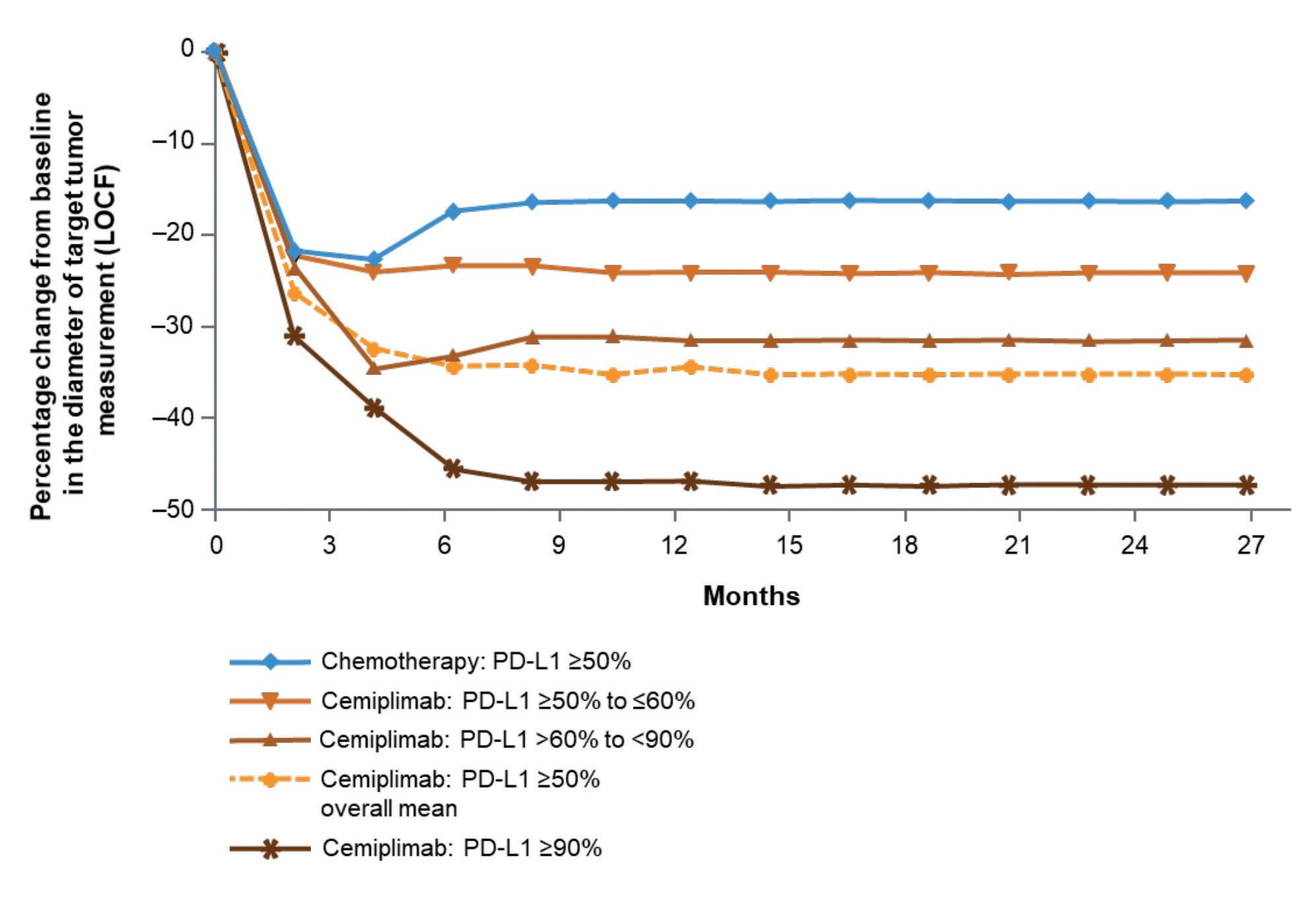
All’interno di EMPOWER-Lung 1 si è provato anche a definire se potesse esserci un beneficio variabile dell’immunoterapia in funzione del livello di espressione di PD-L1. I pazienti arruolati in studio avevano tutti PD-L1 maggiore o uguale al 50% e sono stati stratificati in tre gruppi: i due estremi, abbastanza piccoli (50-59% e >90%), e il gruppo centrale, più numeroso (60-89%). Francesco Grossi sottolinea come, man mano che aumenta l’espressione di PD-L1, si ottiene un maggior beneficio in termini di OS, PFS e risposte obiettive.1 I pazienti che vanno meglio in assoluto sono quelli con espressione maggiore del 90% (ORR 46% vs 32% nei pazienti con espressione 50-59%). La risposta obiettiva è stata ottenuta dopo
la prima rivalutazione, indipendentemente dall’espressione di PD-L1, come si evince dal grafico seguente (Figura 10).
La profondità della risposta, come è facile ipotizzare, risulta più evidente nella curva inferiore, cioè nei pazienti che hanno espressione maggiore del 90%; tuttavia, anche negli altri sottogruppi si può notare una riduzione importante.
Il panel degli esperti ha poi discusso sul fatto che, in relazione all’espressione di PD-L1, da questo studio emerga in maniera più rilevante il valore prognostico o il valore predittivo di PD-L1. Verosimilmente emergono entrambi, ma l’aspetto predittivo
sembra avere importanza maggiore. Infatti, il paziente che ha una forte espressione, superiore al 90%, è quello in cui il beneficio si apprezza in maniera molto più netta. Inoltre, la predittività di PD-L1 nei pazienti in trattamento con cemiplimab è rafforzata dal fatto che non si ottiene lo stesso andamento nel braccio con la chemioterapia. PD-L1, con i suoi difetti, ad oggi resta il marcatore migliore che abbiamo per definire l’efficacia dell’immunoterapia, ed è anche il più facile da ottenere perché ormai arriva contestualmente al referto istologico. Semmai, un problema può essere rappresentato dal fatto che, alcune volte, ci capita di vedere pazienti
con valori di PD-L1 molto elevati (ad esempio 90%) ed il dato di biologia molecolare non ancora disponibile. In questi casi non ci si dovrebbe far prendere dall’euforia di iniziare subito l’immunoterapia ma si dovrebbe attendere, se possibile, il risultato dei test di biologia molecolare. Infatti, è frequente avere pazienti oncogene addicted, soprattutto ROS1 positivi, che presentano elevata espressione di PDL1. Questo dato potrebbe assumere particolare significato nei pazienti con malattia al terzo stadio. Un paziente con queste caratteristiche di malattia, magari sintomatico e con un’istologia squamosa, non candidabile ad un trattamento integrato e con un PD-L1 espresso al 90%, potrebbe giovarsi in prima linea di un trattamento con cemiplimab, rivalutando successivamente un trattamento integrato sulla base della risposta ottenuta. Un altro argomento molto delicato nei pazienti con NSCLC è quello dell’appropriatezza delle richieste di analisi molecolare. Molto spesso, infatti, si abusa con l’uso della Next Generation Sequencing (NGS) e si ripetono esami su esami per ricercare mutazioni in pazienti spesso in terza o quarta linea, senza un criterio ben definito. Un marcatore, per essere applicabile, deve avere una potenzialità terapeutica valida in ogni parte d’Italia, perché altrimenti non è utile per la maggior parte dei pazienti. Riguardo al PD-L1 ancora oggi, dopo anni di studi, probabilmente si ragiona in maniera imperfetta sull’espressione basale del PD-L1 e, cosa ancor più grave, non si ragiona in maniera dinamica. Infatti, nessuno di noi sa cosa succede all’espressione di PD-L1 dopo vari cicli di trattamento ed è una cosa sbagliata poiché il concetto di eterogeneità tumorale esiste anche in questo contesto. A tutt’oggi non sappiamo ancora se PD-L1 è un marcatore dinamico oppure no e, di conseguenza, non sappiamo se molte di quelle risposte complete dopo un prolungato follow-up sono espressione di un cambiamento del microambiente dovuto anche al trattamento. Riallacciandoci a questo aspetto, una suggestione che emerge dal-
lo studio EMPOWER-Lung 1 è quella di continuare cemiplimab oltre la progressione di malattia. Paolo Maione ha riportato brevemente i dati presentati all’ESMO 2022 relativamente a questo aspetto peculiare dello studio. Va sottolineato che, sebbene i dati della sottopopolazione che ha continuato cemiplimab oltre la progressione in aggiunta alla chemioterapia siano molto interessanti, questi non possono essere trasferiti nella pratica clinica in quanto si tratta di un’analisi esploratoria.
Come detto, lo studio prevedeva la possibilità, per i pazienti che andavano in progressione con cemiplimab, di proseguire il farmaco in aggiunta a 4 cicli di chemioterapia. È un disegno molto interessante dal punto di vista pratico poiché, soprattutto nei pazienti con elevata espressione di PDL1 che rispondono all’immunoterapia per lungo tempo con buona qualità di vita, è veramente difficile pensare di sospendere il trattamento, come pure è difficile accettarlo per i pazienti. Spesso, infatti, è prassi comune andare oltre la progressione strumentale quando il beneficio clinico persiste nel tempo. Quando poi, dal punto di vista strumentale e sintomatico, la progressione diventa troppo evidente siamo “costretti” a passare alla chemioterapia. Nel braccio con cemiplimab 64 pazienti su 357 (18%) sono andati in progressione, ed è stata aggiunta la chemioterapia per 4 cicli. Le caratteristiche di questi pazienti erano sovrapponibili a quelli della popolazione generale, tranne che per l’istologia (57% erano squamosi vs 43% non squamosi). I risultati, ovviamente, vanno esaminati con cautela ma sono promettenti.5 In questo gruppo di pazienti, la OS calcolata dalla randomizzazione fino al decesso è pari a 27 mesi, ma se la calcoliamo dall’inizio di cemiplimab + chemioterapia fino al decesso (di fatto, una 2nd-line OS) abbiamo un risultato pari a 15 mesi. Si tratta di un dato interessante, che può stimolare ulteriormente la ricerca in tal senso. Anche la probabilità di essere vivi a 6, 12 e 24 mesi nel periodo della seconda linea è, rispettivamente, del 92%, 60% e 32%. Per quanto
riguarda la PFS, il dato del periodo 1 (solo cemiplimab) e quello del periodo 2 (cemiplimab + chemioterapia) sono più o meno sovrapponibili (6,2 vs 6,6 mesi, rispettivamente), con una probabilità di essere liberi da progressione nel periodo 2 piuttosto alta anche a 18 mesi. Anche le risposte obiettive sono sovrapponibili tra i due periodi (circa 30% per entrambi). Non sono state evidenziate criticità particolari in termini di tossicità associando la chemioterapia a cemiplimab, con un 35% di eventi avversi di grado severo (attesi) ed un 4,7% di pazienti che hanno discontinuato il trattamento per tossicità. I dati relativi alla prosecuzione dell’immunoterapia oltre la progressione non sono ancora così solidi, ma in molti centri c’è una tendenza a proseguire l’immunoterapia nei pazienti con progressione non conclamata, soprattutto se con un’espressione molto alta di PD-L1. Esistono, peraltro, sempre più esperienze in cui, nel medesimo contesto, si combina l’immunoterapia con la chemioterapia e con nuovi farmaci biologici con risultati interessanti. Probabilmente l’immunoterapia, pur essendo caratterizzata da un decremento graduale di efficacia nel corso della malattia, dovrebbe continuare ad essere sfruttata soprattutto in quei pazienti che hanno risposto in modo particolarmente favorevole. In una fase di malattia metastatica peraltro è sempre molto importante, in un’ottica palliativa, rispettare la qualità di vita dei pazienti proponendo trattamenti il meno tossici possibile.
L’ultima parte di analisi dello studio EMPOWER-Lung 1 è stata affidata a Lorenza Landi, che ha presentato e commentato i dati di safety cercando di estrapolare soprattutto notizie utili alla pratica clinica. In caso di un farmaco nuovo come cemiplimab, uno degli aspetti più importanti è l’incidenza di eventi avversi di grado severo e la probabilità di doverlo sospendere a causa di questi ultimi. Il profilo di tollerabilità generale di cemiplimab nello studio EMPOWER-Lung 1 è riportato in figura 11.5 Il primo dato interessante è che la percentuale di discontinuazione del trattamento a causa di eventi avversi di tipo immunomediato è inferiore al 5%, assolutamente comparabile ai trial registrativi di altri farmaci immunoterapici e ai dati della real-life. Esaminando più nel dettaglio gli eventi avversi e confrontandoli con quelli della chemioterapia, emerge chiaramente che i due profili sono differenti e che, probabilmente, questo studio ha goduto favorevolmente della curva d’apprendimento da parte degli sperimentatori nel gestire le tossicità dell’immunoterapia. Una particolarità di questa analisi è che la fatigue, evento avverso soggettivo e perciò difficile da graduare, viene valutata separatamente rispetto all’astenia. Inoltre, iniziano ad essere finalmente raccolte alcune tossicità immunomediate che potremmo definire emergenti ma che in realtà, probabilmente, prima non venivano tracciate, come ad esempio il prurito. Stessa cosa per i dolori articolari e le forme di artrite, cioè quei quadri infiammatori che a volte mimano la riacutizzazione di una patologia degenerativa. Al concetto di evento avverso si correla direttamente la qualità di vita del paziente. Per questo studio esiste un’analisi di qualità di vita, 8 in cui il dato che emerge è a vantaggio dell’immunoterapia rispetto al trattamento chemioterapico.
Treatment-emergent AEs, regardless of attribution, n (%)
AEs, n (%)
immune-related AEs, n (%)
Treatment-emergent AEs in
*Although each pair of neutropenia and decreased neutrophil count; and thrombocytopenia and decreased platelet count might reflect the same condition, they were listed as distinct events for the safety report of the study AEs, adverse events; PD-L1, programmed death-ligand 1
Lo studio EMPOWER-Lung 1 ha portato alla luce l’esistenza e ha dimostrato l’efficacia di un altro farmaco immunoterapico nei pazienti con NSCLC metastatico o localmente avanzato non candidati a chemio/radioterapia ed espressione di PD-L1 uguale o maggiore di 50%, non meno attivo di quelli che avevamo finora a disposizione. Il vantaggio rispetto alla chemioterapia si evidenzia in termini di OS, di PFS, di risposte obiettive, di tollerabilità e di qualità di vita. Sarà importante capire come scegliere, nell’ambito della malattia metastatica, tra farmaci che non hanno e non avranno mai un confronto diretto e che sembrano complessivamente ottenere risultati sovrapponibili e molto più favorevoli rispetto alla chemioterapia. Con tutti i limiti delle analisi per sottogruppi, alcune categorie di pazienti come quelli con metastasi encefaliche stabilizzate e con istologia squamosa sembrerebbero beneficiare dell’uso di cemiplimab in modo particolare. Anche nei pazienti con malattia localmente avanzata che non possono giovarsi di un trattamento chemio-radioterapico, concomitante o sequenziale, cemiplimab rappresenta un’opportunità nei pazienti che iperesprimono PD-L1 Per questo motivo, AIFA ha concesso solamente a cemiplimab la rimborsabilità in questo setting. Più difficile stabilire il ruolo di cemiplimab oltre la progressione di malattia ma anche questa, alla luce dei dati presentati, rappresenta una prospettiva importante in un’ottica di preservazione della qualità di vita nei pazienti metastatici.
1. Sezer A. Kilickap S, Gumus M et al: Cemiplimab monotherapy for first-line treatment of advanced non-small cell lung cancer with PD-L1 of at least 50%: a multicentre, open-label, global, phase 3, randomised, controlled trial. Lancet 2021; 397: 592-604
2. Reck M, Rodríguez-Abreu D, Robinson AG et al: Five-Year Outcomes With Pembrolizumab Versus Chemotherapy for Metastatic Non-Small-Cell Lung Cancer With PD-L1 Tumor Proportion Score ≥ 50. J Clin Oncol 2021; 39(21):2339-2349
3. Jassem J, de Marinis F, Giaccone G et al: Updated Overall Survival Analysis From IMpower110: Atezolizumab Versus Platinum-Based Chemotherapy in TreatmentNaive Programmed Death-Ligand 1-Selected NSCLC. J Thorac Oncol 2021; 16(11):1872-1882
4. Mok TSK, Wu YL, Kudaba I et al: Pembrolizumab versus chemotherapy for previously untreated, PD-L1expressing, locally advanced or metastatic non-smallcell lung cancer (KEYNOTE-042): a randomised, open-label, controlled, phase 3 trial. Lancet 2019; 393(10183):1819-1830
5. Özgüroğlu M, Kilickap S, A. Sezer A et al: Three years survival outcome and continued cemiplimab (CEMI) beyond progression with the addition of chemotherapy (chemo) for patients (pts) with advanced non-small cell lung cancer (NSCLC): The EMPOWER-Lung 1 trial. Proc ESMO 2022, LBA54
6. Özgüroğlu M, Sezer A, Kilickap S et al: Cemiplimab monotherapy as first-line (1L) treatment of patients with brain metastases from advanced non-small cell lung cancer (NSCLC) with programmed cell deathligand 1 (PD-L1) ≥ 50%: EMPOWER-Lung 1 subgroup analysis. Proc ASCO 2021, abstract 9085
7. Bondarenko I, Sezer A, Kilickap S, et al. Clinical benefit of first-line cemiplimab in patients with locally advanced NSCLC: subgroup analysis from EMPOWERLung 1. Presented at: 2021 IASLC World Conference on Lung Cancer; September 8-14, 2021. Abstract FP04.03.
8. Gumus M, Chen IC, Ivanescu C et al: Patient-reported outcomes with cemiplimab monotherapy for first-line treatment of advanced non-small cell lung cancer with PD-L1 of ≥50%: The EMPOWER-Lung 1 study. Cancer 2022; Oct 29. doi: 10.1002/cncr.34477. Online ahead of print
Una pubblicazione de Il Pensiero Scientifico Editore e Think2it
Tutti i diritti riservati Oncoinfo – Anno XII, dicembre 2022


