13 minute read
Kort tarm-syndrom (SBS) hos voksne
from Gastroskopet 1/21
by WebPress
Snorri Olafsson
Forfatter: Snorri Olafsson, overlege dr. med., Medisinsk avdeling Gjøvik, Gastromedisinsk seksjon, Sykehuset Innlandet HF Divisjon Gjøvik – Lillehammer.
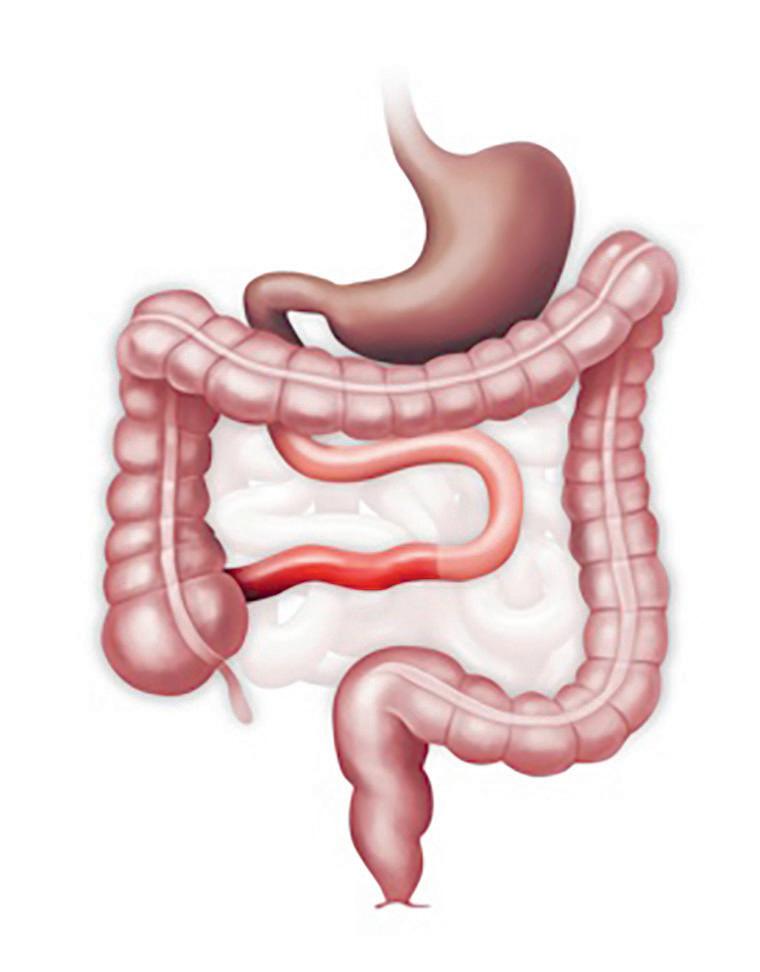
Hva er tarmsvikt og hva er hovedgruppene? Intestinalsvikt (intestinal failure = IF) defineres som reduksjon i tarmfunksjon under minimumskravet for absorpsjon av næringsstoffer og/eller vann og elektrolytter, som fører til behov for intravenøs tilførsel for å opprettholde helse og/ eller vekst [1]. IF er den mest sjeldne typen av alle former for organsvikt. Det er fem hovedårsaker. (Se figur 1)
Hva er kort tarm-syndrom og hvilke årsaker er vanligst? SBS defineres som at mindre enn 200 cm tynntarm er i bruk, men lengden alene er ikke avgjørende for hvor mye symptomer pasienter utvikler. Det er avhengig av flere faktorer, som bl.a. tarmens tilstand, hvilken del av tynntarm og tykktarm som er igjen, om ileocøkalklaffen fortsatt er tilstede, og tilpasningsevnen (adaptasjonen) til gjenværende tarm. Adaptasjon kan skje i opptil to år etter en operasjon.
SBS er en sjelden sykdom. Forekomsten i Norge er ukjent, men hvis man sammenligner med danske tall kan det dreie seg om et sted mellom 160 og 300 pasienter [2, 3]. De vanligste årsakene er: (Se tabell 1) Typer SBS SBS deles ofte i 3 anatomiske grupper [4, 5]:
Type 1 er den vanskeligste å behandle og type 3 den enkleste. (Se bilde 1)
Kliniske funn som kan forekomme ved kort tarm-syndrom • Trøtthet. Vekttap og underernæring kan føre til et lavt energinivå, trøtthet, dårlig konsentrasjonsevne og sløvhet. • Dehydrering, lav urinmengde, tørstefølelse og tørr munn. • Diaré, vanntynn avføring, hasteavføring («urgency»), nattlige tømminger, inkontinens, illeluktende avføring. • Nyrestein. • Leversykdom. • Gallesteiner.
Kort tarmsyndrom (75%)
Tarmfistler (2%) 5 hovedårsaker til tarmsvikt Dysmotilitet (18%)
Obstruksjon Utbredt sykdom i tynntarmen (5%)
Figur 1: Eksempler på utbredt sykdom i tynntarmen er Crohns sykdom og stråleskade etter kreftbehandling. Crohns sykdom Én operasjon øker risikoen for flere operasjoner. Det som er igjen er ikke alltid frisk tarm. Var tidligere den vanligste årsaken.
Komplikasjoner etter annen buk-kirurgi
Mesenterisk iskemi
Skade
Er blitt en av de vanligste årsakene. Utilsiktet traume, skade på blodårer, fistler, infeksjoner, forsnevringer pga. sammenvoksninger. Dette kan skyldes at blodårene til tarmen er innsnevret eller tilstoppet på grunn av åreforkalkning eller blodpropp. For eksempel bilulykke eller skuddskade. Kreft Kirurgisk fjerning av mye svulstvev, «debulking». Postbariatrisk Tilstand etter fedmeoperasjoner. Medfødt Meget sjelden årsak. Kalles «medfødt villusatrofi».
Tabell 1
Illustrasjoner: Takeda AS

Type 1. Ende-jejunostomi Bilde 1 Type 2. Jejuno-colisk anastomose Type 3. Jejuno-ileocolisk anastomose

• Vitaminmangel. • Anemi. • Elektrolyttforstyrrelser. En av de vanligste er magnesiummangel. Lavt magnesium kan gi muskelkramper som eneste symptom, men det kan også gi grov skjelving, nedsatt konsentrasjonsevne, epilepsianfall og hjerterytmeforstyrrelser [6]. Hypokalemi kan bl.a. gi svakhet, trøtthet, ileus og hjertearytmi. Acidose er ikke vanlig, men kan føre til svekket syn, forvirring og snøvlete tale. Tilstanden kan ligne på alkoholpåvirkning.
Hvilke laboratorieprøver kan være aktuelle ved mistanke om kort tarm-syndrom? 1. Hemoglobin, hvite blodlegemer med differensialtelling, blodplater. 2. Elektrolytter og sporelementer: Kreatinin, urea, natrium (Na), kalium (K), magnesium (Mg), fosfat (PO3 −), sink (Zn), krom (Cr), kobber (Cu), mangan (Mn), selen (Se). 3. Leverprøver: ASAT, ALAT, bilirubin, GGT, alkalisk fosfatase, albumin, INR. 4. CRP. 5. Jern, ferritin. 6. Blodsukker. 7. Vitaminer, spesielt fettoppløselige: Totalt vitamin D, vitamin A, vitamin E. Vannoppløselige vitaminer tas opp høyt oppe i tynntarmen, med unntak av vitamin B12 og folat, derfor er det uvanlig med mangel på disse. 8. Fettstoffer: Triglyserider, kolesterol, essensielle fettsyrer. 9. Bukspyttkjertel: Amylase, lipase. 10.PTH (paratyroidea hormon). 11. Surhetsgrad: pH og bikarbonat (HCO3 -) i blodet.
Dehydrering oppdages tidligere ved å måle natrium i spot-urin, enn ved stigning i kreatinin og urea. Hvis spot U-Na er over 20 mmol/liter er man som regel ikke dehydrert, er den lavere er man uttørket.
Målinger Det er 4 ting man bør måle av og til: Drikke, vekt, urinmengde og stomifløde. SBS-pasienter bør produsere over 1200 ml urin/døgn. De som har hatt nyrestein skal lage >1500 ml/d. Urin <800 ml er kritisk lavt. Urinmengde godt over 1 liter hos voksne er den viktigste parameter for å se hvor godt hydrert en pasient er: Stomiflødet ser eventuelt bra ut, men på bekostning av urinmengden slik at de får kronisk nyreskade [7].
Tabellen viser hva som er forventet fløde ved forskjellige type stomier [8].
Tilstand Typisk fløde/avføring per døgn Normal 150-200 ml. avføring Jejunostomi Opptil 6000 ml. Ileostomi Over 1200 ml kort tid etter operasjon. Går med tiden ned til 750 ml. Hvis ileostomifløde er over 1000 ml over tid betegnes det som «diaré». Over 1500 ml er alvorlig («high-output») diaré. Kolostomi 200-600 ml. Hvis kolostomien er på høyre side er avføringen løsere og nærmere 600 ml. Hvis den er på venstre side er den blitt fastere og mengden er omtrent som vanlig avføring, 200 ml.
Tabell 2 Mange har en tendens til å forveksle ileostomi og jejunostomi. Jejunostomi er den typen stomi med størst risiko for alvorlige bivirkninger, og kan føre til alvorlig dehydrering og nyresvikt. Jejunum har minimal evne til adaptasjon.
Når er det behov for parenteral ernæring eller væske? Når en pasient ikke klarer å ernære seg på normalt vis, kan ernæring gis enteralt, til magesekken eller tynntarmen, eller parenteralt (intravenøst). Parenteralt tilskudd kan inneholde væske og kalorier, eller bare væske og eventuelt elektrolytter. Et fellesnavn for de to siste er «home parenteral support», forkortet HPS, og betyr intravenøs støtte. [9]. Hvis en pasient ikke kan oppnå en urinmengde på 1200 ml døgn, kan det være behov for HPS. Urin <800 ml er kritisk lavt, som nevnt ovenfor.
Typer sentralt kateter 1. Sentralt venekateter (SVK), som egner seg til korttidsbruk i opptil 1 uke. 2. «PICC line» (= peripherally inserted central catheter), som kan brukes i opptil 3 måneder. 3. Veneport (VAP, portacath), egner seg godt til cellegiftbehandling som gis med lange mellomrom, men er ikke ideell til daglig HPN (home parenteral nutrition). 4. Tunnelerte katetre, som går delvis under huden (Broviac,
Hickman, Groshong), kan brukes i årevis hvis man tar godt vare på dem [10].
Parenteral væske er en hyperosmolær, irriterende oppløsning som skal gis i en stor vene for å unngå trombose. Det eneste stedet hvor den skal munne ut er vena cava, like utenfor høyre atrium.
Komplikasjoner ved (langvarig) HPN Akutte 1. Vaskulær tilgang. Når katetre settes inn, kan man få pneumothorax eller skade på arterie. 2. Hyperglykemi og hypoglykemi. 3. Reernæringssyndrom.
Kroniske 1. Blodpropp. 2. Kateter-relatert infeksjon. 3. Leverkomplikasjoner. 4. Gallekomplikasjoner. 5. Metabolsk skjelettsykdom. 6. Nyrestein og nyresvikt.
Intestinal rehabilitering Hovedmålet med behandling er å hjelpe pasienter til å få en så normal og selvstendig livsstil som mulig, samt sikre at de får adekvat ernæring, forebygge dehydrering og redusere diaré. Denne prosessen kalles «intestinal rehabilitering». Den deles opp i kosthold, medisiner og kirurgi. I motsetning til i mange andre land finnes det ikke en spesialisert sykehusavdeling for IF eller SBS i Norge, så det er opp til hvert sykehus å behandle disse pasientene.
Kosthold Kosthold er den viktigste delen av SBS behandling. Det er meget gunstig for pasienter med SBS å ha en tett dialog og langtidsoppfølging med en klinisk ernæringsfysiolog (KEF) som er ekspert på SBS.
Væske En naturlig reaksjon på tørste, munntørrhet, redusert urinmengde og svimmelhet er å drikke mer, men det kan gjøre vondt verre hos dem med høyt stomifløde. Dette gjelder ved de fleste typer vanlig drikke som er enten hypotone eller hypertone. Eksempler på hypotone drikker er vann, svart kaffe, sukkerfri te og lettbrus. Hypertone drikker er enda verre og inkluderer fruktjuice, sukkerholdig brus, sportsdrikker, alkohol, søt te, sirup, iskrem, sorbet og søt gelatin. Koffein og alkohol virker vanndrivende og kan føre til dehydrering ved SBS [12]. Korrekt behandling består i å drikke mindre av vanlige drikkevarer (under 1 l/d) og drikke ≥1 l/d av en elektrolyttblanding som inneholder omtrent 75-90 mmol/l natrium samt glukose, såkalte isotone væsker. De kalles også orale rehydreringsvæsker (= oral rehydration solution = ORS). Iblant må man ty til intravenøse væsker.
Oppskrift på hjemmelaget ORS 1 liter vann 2-3 ss sukker 1 ts salt ¼ ts bakepulver Kan tilsettes lime/sitron og søtningsmidler uten sukker Blandes og settes i kjøleskap
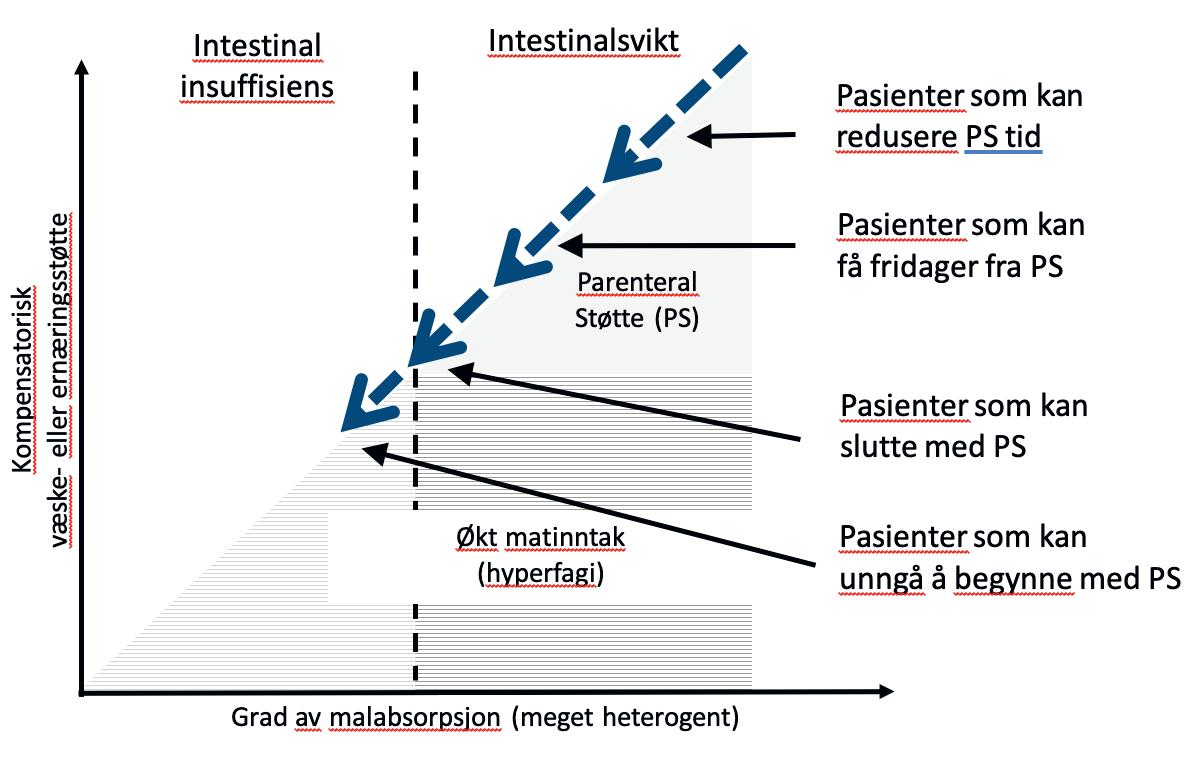
Figur 2: Hva man kan håpe å oppnå ved rehabilitering [11]:
Mat Gjennom avføringen mister friske personer mindre enn 5% av kaloriene de spiser, selv om de spiser veldig mye [13]. Ved SBS mister pasienter mye av energien fordi kalorier ikke blir absorbert og går rett gjennom tarmen. Hvis de mister over 60% av kaloriene kan det være behov for HPS [9]. Pasienter trenger derfor gjerne å øke matmengden med minst 50%, iblant opptil 400%.
Tabell 3 gir en oversikt over anbefalt mat for dem uten tykktarm, med jejunostomi, og de som har tykktarm [14-17].
Energibehov Jejunostomi 35-45 kcal/kg/d. Opp mot 60 kcal/kg/d. Tykktarm til stede 35-45 kcal/kg/d. Opp mot 60 kcal/kg/d.
Karbohydrater 20-40% av totalt energibehov. 50-60% av energi. 96% av energiinnholdet i karbohydrater absorberes, vs. 50% av energiinnholdet i fett og protein.
Protein 1,25-1,5 g/kg/d eller 20-30% av daglig energi. 1,25-1,5 g/kg/d eller 20-30% av daglig energi.
Fett 40-60% av energi. Det er ikke påvist nytte av MCT-fett. 20-30% av energi. MCT-fett 50% av totalfett.
Fiber Lite. Lite eller middels. Kommentar Hyperfagi (= en kraftig økt appetitt). 5-6 måltider fordelt utover dagen.
Begrens enkle karbohydrater (“hyperosmotisk mat”) Bruk komplekse karbohydrater.
Væske Isoton/litt hypoton, saltrik ORS. Isoton/hypoton. Adskill væsker og fast føde. Unngå enkle karbohydrater. Små slurker hele dagen (obs. tannhelse). Hjemmelaget eller kommersiell ORS.
Oksalat Begrensning ikke nødvendig. Lav-oksalat mat (lite spinat, rabarbra, mandler, cashewnøtter, bakte poteter med skall, kakao, rødbeter, pommes frites, bringebær, søtpoteter, te, m.m.). Fruktte er i orden. Mat rik på kalsium eller kalsiumcitrat, for å binde oksalat og gjøre urinen alkalisk (basisk). Bør kartlegge den enkeltes kosthold med tanke på hva som er viktige kilder, og hvordan det ev er lettest for pasienten å redusere inntak. Noen leger begrenser oksalat kun hos dem som har hatt nyrestein.
Laktose Ikke begrens hvis den tåles. Ikke begrens hvis den tåles. Melkeprodukter inneholder protein, jod og kalsium. De fleste melkeprodukter finnes i varianter med redusert innhold av, eller uten, laktose.
Natrium Liberal bruk.
MCT = mellomkjedete fettsyrer Liberal bruk. Pasientene mister mye salt.
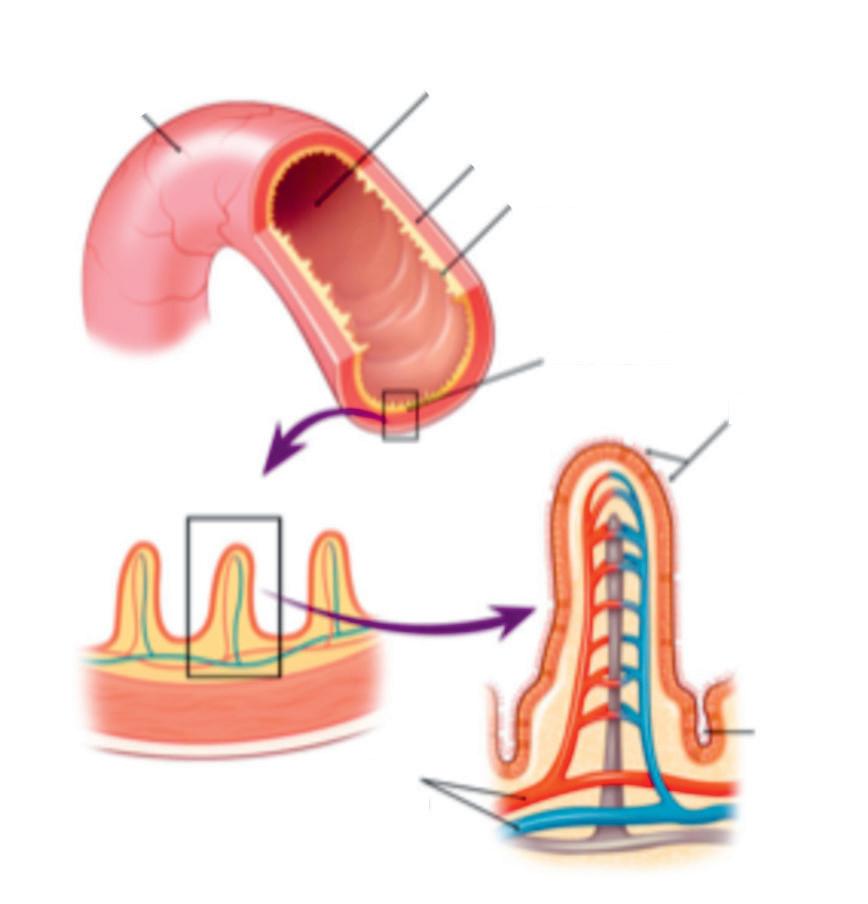
Small intestine
Intestinal villi Lumen
Muscle layers Mucosa
Intestinal villi Microvilli
Bilde 2 Blood vessels Crypt
Medikamenter De kan deles i fire grupper: 1. Medisiner som bremser transittid og reduserer diaré.
Loperamid.
Opioider. Bruken er kontroversiell og ofte unødvendig hvis store nok doser med loperamid gis.
Kolestyramin eller kolestipol. Hjelper bare ved lettere tilfeller av SBS. Brukes sjelden. 2. Redusere GI sekresjon.
Proton-pumpe-hemmere (PPI). 3. Behandle bakteriell overvekst.
Antibiotika i korte perioder. 4. Trofiske midler («hormonterapi»). Medisinen teduglutid kom nylig på markedet og har ført til et paradigmeskifte i behandlingen av SBS. Det er et glucagon-likt peptid (GLP-2), som består av en kjede med 33 aminosyrer.
Mange kan redusere mengde HPN og noen kan slutte helt.
Bilde 2 viser hvordan totter (engelsk: villi) og krypter i tynntarmen ser ut:
Bilde 3 vises en tynntarmsbiopsi fra en enkelt pasient før bruk av teduglutid og 60 uker senere. Tottene blir høyere og kryptene dypere [18]: I tillegg trenger mange pasienter diverse tilskudd. De fleste som slutter med HPN trenger vitaminer og elektrolytter p.o., og dette i større grad enn da de sto på HPN, siden slike stoffer da ble blandet sammen med deres HPN. Alle trenger multivitamin med mineraler. De kan også trenge tilskudd av natriumbikarbonat, fosfat, kaliumklorid, jern (som regel gitt som i.v.-infusjon), kalsium, D-vitamin, A-, E- og K-vitaminer, folat, B12-vitamin, kobber [19] og magnesium [20].
Kirurgi Hvis en del av tynntarm, tykktarm eller magesekk er koblet av (men ikke fjernet) ved en tidligere operasjon, bør man vurdere om det er mulig å ta den i bruk igjen via en ny operasjon [9].
Det er også mulig å utføre tarmtransplantasjon for SBS. Det vurderes spesielt ved livstruende komplikasjoner av HPN, eller når det ikke er mulig med venøs tilgang [12]. Slike operasjoner utføres ikke i Norge og eventuelle pasienter må henvises til utlandet.
Hva slags helsepersonale behandler kort tarm-syndrom? SBS-pasienter har lavere livskvalitet enn folk generelt. De kan trenge hjelp fra klinisk ernæringsfysiolog, psykolog,
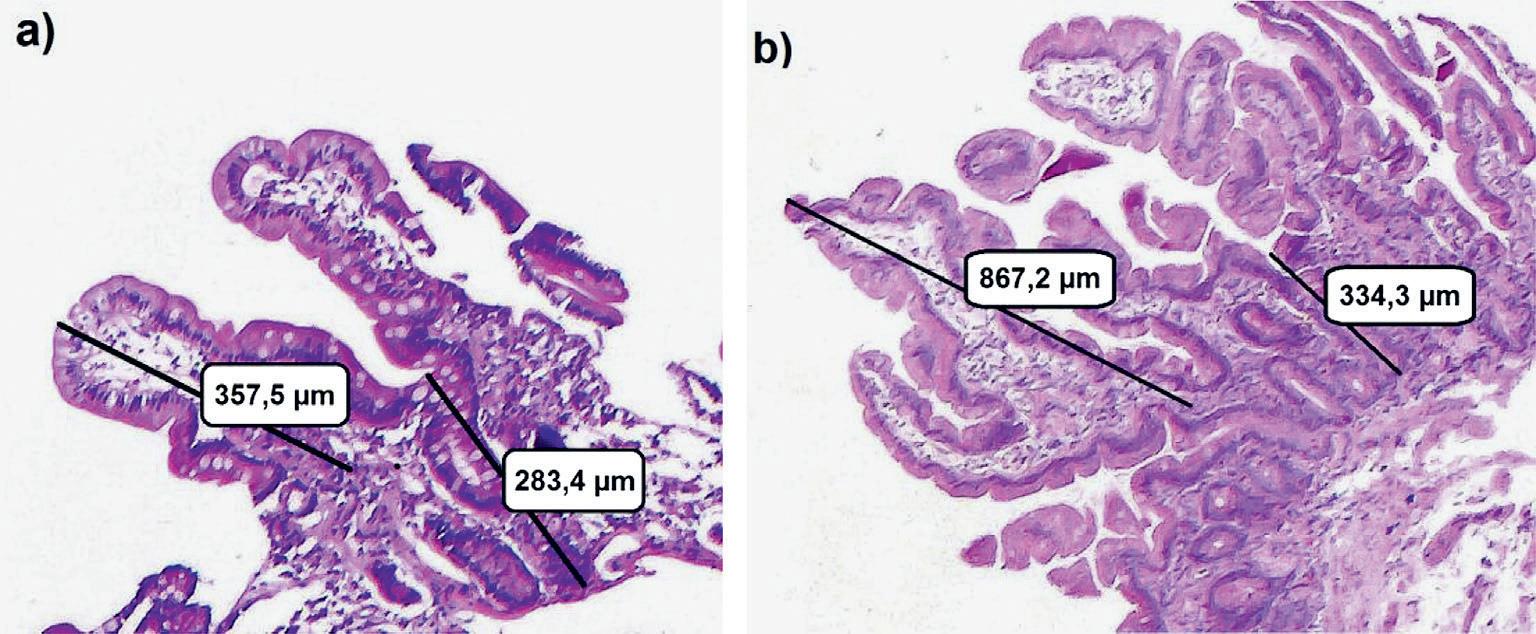
Bilde 3 a) Før bruk av teduglutid Bilde 3 b) Etter 60 uker
fysioterapeut, farmasøyt, lege, stomisykepleier og HPNsykepleier [3]. Blant legespesialister kan det være aktuelt å henvise til en gastroenterolog, gastrokirurg, anestesilege, intervensjonsrøntgenlege, urolog, nyrelege og allmennlege. Sjekklisten er utarbeidet i samarbeid med Takeda. For mer utførlig informasjon henvises det til «Informasjonshefte om kort tarm-syndrom» ved samme forfatter som ferdigstilles i disse dager, og vil ligge på Landsforeningen mot fordøyelsessykdommers (LMF) hjemmesider (www.lmfnorge.no).
Kildehenvisninger 1. Pironi L, Arends J, Bozzetti F, Cuerda C,
Gillanders L, Jeppesen PB et al. ESPEN guidelines on chronic intestinal failure in adults. Clin Nutr 2016;35 2: 247-307. 2. Jeppesen PB. Spectrum of short bowel syndrome in adults: intestinal insufficiency to intestinal failure. JPEN J Parenter Enteral Nutr 2014;38 1 Suppl: 8S-13S. 3. Jeppesen PB. The Long Road to the
Development of Effective Therapies for the
Short Gut Syndrome: A Personal Perspective.
Dig Dis Sci 2019;64 10: 2717-35. 4. Messing B, Crenn P, Beau P, Boutron MC,
Rambaud JC, Matuchansky C. Long-term survival and parenteral nutrition-dependency of adult patients with nonmalignant short bowel. Transplant Proc 1998;30 6: 2548. 5. Messing B, Crenn P, Beau P, Boutron-Ruault MC,
Rambaud JC, Matuchansky C. Long-term survival and parenteral nutrition dependence in adult patients with the short bowel syndrome. Gastroenterology 1999;117 5: 1043-50. 6. Oke S, Nightingale J, Gabe S. Mistakes in short bowel and how to avoid them. UEG Education 2018;18: 7-11. 7. Bridges M, Nasser R, Parrish CR. High Output
Ileostomies: The Stakes are Higher than the
Output. Practical Gastroenterology 2019;43 9: 20-33. 8. Hughes S. Care of the Intestinal Stoma and
Enterocutaneous Fistula. In: Nightingale J ed.
Intestinal failure. London, England; . 2001:53-63. 9. Jeppesen PB, Fuglsang KA. Nutritional Therapy in Adult Short Bowel Syndrome Patients with
Chronic Intestinal Failure. Gastroenterol Clin
North Am 2018;47 1: 61-75. 10. Lappas BM, Patel D, Kumpf V, Adams DW,
Seidner DL. Parenteral Nutrition: Indications,
Access, and Complications. Gastroenterol Clin
North Am 2018;47 1: 39-59. 11. Jeppesen PB. Short bowel syndrome – characterisation of an orphan condition with many phenotypes. Expert Opinion on Orphan
Drugs 2013;1 7: 515-25. 12. Wall E. ORS: The Solutions to Optimize
Hydration in Short Bowel Syndrome. Practical
Gastroenterology 2020: 24-31. 13. Jeejeebhoy KN. Symposium on diarrhea. 1.
Definition and mechanisms of diarrhea. Can
Med Assoc J 1977;116 7: 737-9. 14. Limketkai BN, Hurt RT, Palmer LB eds. The
Aspen Adult Nutrition Support Core
Curriculum: American Society for Parenteral and Enteral Nutrition, 2017. 15. Nordgaard I, Hansen BS, Mortensen PB. Colon as a digestive organ in patients with short bowel. Lancet 1994;343 8894: 373-6. 16. Simko V, McCarroll AM, Goodman S, Weesner
RE, Kelley RE. High-fat diet in a short bowel syndrome. Intestinal absorption and gastroenteropancreatic hormone responses. Dig Dis
Sci 1980;25 5: 333-9. 17. Culkin A. Nutrition support in intestinal failure.
In: Hickson M, Smith S eds. Advanced Nutrition and Dietetics in Nutrition Support: Wiley
Blackwell. 2018:302-12. 18. Pevny S, Maasberg S, Rieger A, Karber M,
Bluthner E, Knappe-Drzikova B et al.
Experience with teduglutide treatment for short bowel syndrome in clinical practice. Clin
Nutr 2019;38 4: 1745-55. 19. Compher C, Boullata JI, Pickett-Blakely O,
Schiavone P, Stoner N, Kinosian BP. Clinical
Management of Patients With Parenteral
Nutrition-Dependent Short Bowel Syndrome
During Teduglutide Therapy. JPEN J Parenter
Enteral Nutr 2016;40 8: 1183-90. 20. Lam K, Schwartz L, Batisti J, Iyer KR. Single-
Center Experience with the Use of Teduglutide in Adult Patients with Short Bowel Syndrome.
JPEN J Parenter Enteral Nutr 2018;42 1: 225-30.










