Fagtidsskrift for Norsk Indremedisinsk Forening

Pulmonary Embolism Respons Team på Akershus Universitetssykehus s. 12

Albumin-kreatinin-ratio (AKR) s. 18

Osteoporose ved kronisk nyresykdom s. 26




Fagtidsskrift for Norsk Indremedisinsk Forening

Pulmonary Embolism Respons Team på Akershus Universitetssykehus s. 12

Albumin-kreatinin-ratio (AKR) s. 18


Osteoporose ved kronisk nyresykdom s. 26



Livtencity (maribavir) er første godkjente behandling for cytomegalovirus (CMV)-infeksjon og/eller -sykdom som er refraktær (med eller uten resistens) mot én eller flere tidligere behandlinger, inkludert ganciklovir, valganciklovir, cidofovir eller foskarnet hos voksne pasienter som har gjennomgått hematopoetisk stamcelletransplantasjon (HSCT) eller organtransplantasjon (SOT).1 Beslutningsforum godkjente i fjor Livtencity for forskrivning på H-resept til behandling av nevnte pasienter.2
Signifikant flere oppnådde CMV-negativitet ved uke 8 med Livtencity3 Primært endepunkt



Viktige behandlingsrelaterte bivirkninger i studien4 FRA SOLSTICE-STUDIEN (FASE 3)* 3:
Ønsker du mer informasjon? Ta kontakt med oss:
Anette Krokaas Frois Commercial Lead anette-krokaas.frois@takeda.com
FOS: foskarnet, GCV: ganciklovir, LIV: Livtencity, VGCV: valganciklovir, konvensjonell terapi: mono- eller kombinasjonsbehandling (≤2 legemidler) med intravenøs (IV) ganciklovir, oral valganciklovir, IV foskarnet, eller IV cidofovir
*SOLSTICE-studien var en multisenter, randomisert, åpen, aktiv kontrollert studie, som undersøkte effekt og sikkerhet av Livtencity sammenliknet med konvensjonell terapi hos stamcelle- (n=141) eller organtransplanterte (n=211) med CMV-infeksjon (med eller uten resistens) som var refraktær mot ganciclovir, valganciclovir, foskarnet eller cidofovir. Deltakerne ble behandlet i 8 uker, med 12 ukers oppfølging. UTVALGT PRODUKTINFORMASJON1:
Det bør tas hensyn til offisielle retningslinjer for riktig bruk av antivirale midler. Livtencity skal ikke brukes samtidig med ganciklovir eller valganciklovir. De vanligste rapporterte bivirkningene var smaksforstyrrelser, kvalme, diaré, oppkast og fatigue. For mer informasjon, se SPC (www.legemiddelsok.no). Reseptgruppe: C. Pakninger og priser: 56 stk tabletter (boks) kr 150 486,30. Refusjon: J05A X10 (Maribavir). Godkjent av Beslutningsforum, inklusive en prisavtale med Sykehusinnkjøp HF, som gjør at reell pris avviker fra den publisert i Felleskatalogen (over).
REFERANSER:
1. Livtencity SPC godkjent 03/2024, kap 4.1, 4.3, 4.8.
2. Protokoll fra Beslutningforum for nye metoder, 12. februar 2024. Hentet fra: https://www.nyemetoder.no/491252/contentassets/1deaee85578f4fc386b34ddd596e593e/beslutningsforum-12022024_ protokoll.pdf. Lest 14.03.2025
3. Avery RK, Alain S, Alexander BD et al. Maribavir for Refractory Cytomegalovirus Infections With or Without Resistance Post-Transplant: Results From a Phase 3 Randomized Clinical Trial. Clin Infect Dis. 2022;75(4):690-701
4. Avery RK, Alain S, Alexander BD et al. Maribavir for Refractory
Dis. 2022;75(4):690-701. Supplementary data table 6
Styret i Norsk indremedisinsk forening:
Trond Vartdal
Leder
Knut Lundin
Nestleder
Cecilie H Nordmo
Styremedlem
Runa Andreassen
Styremedlem
Hamza Nahoui Leder NYI
Stephen Hewitt (ansvarlig redaktør)
OUS Aker
stehewi@online.no
T: 913 72 199
Ole Kristian H. Furulund (assisterende redaktør)
Stephen Hewitt Redaktør Indremedisineren
Maria Seferowicz Høstmøtetkomitéen
Andrea Dobloug Spesialitetskomiteen
Rune Eilertsen Vara
Anita Suntharalingam Vara NYI
Kommuneoverlege i Bærum Maya Bass Akuttmottaket, Bærum sykehus, mctbass@hotmail.com
Fagredaktører:
Bernt Aarli (Lungemedisin)
Haukeland universitetssykehus
Eystein Husebye (Endokrinologi)
Haukeland universitetssykehus
Gunnar Einvik (Lungemedisin) Akershus universitetssykehus/NTNU
Indremedisineren er et fagtidsskrift rettet mot norske leger som arbeider innen fagomådet indremedisin, med dets ulike retninger. Indremedisineren sendes ut til alle medlemmer av Norsk indremedisinsk forening (Nif), som for tiden er ca 3 400, samt til andre med interesse for faget.
Indremedisineren vil presentere
Forsidebilde
Foto:
Utgivelsesplan
Tone Svilaas OUS Aker tosvil@ous-hf.no
Trine Finnes (Endokrinologi) Sykehuset Innlandet/OUS
Guri Hagberg (Geriatri) OUS Ullevål
Camilla Hem (Geriatri) Diakonhjemmet
og fagpolitisk stoff fra norske miljøer, samt noe internasjonalt rettet stoff av allmen interesse. Vi ønsker å legge til rette for at terskel og takhøyde gir rom for en allment engasjert indremedisiner å ytre seg.
Reproduksjon av materiale fra Indremedisineren må skje etter tillatelse fra redaksjon og forfatter.




Bestillingsfrist/ Levering Forfatterfrister Materiellfrist annonsører Posten
Nr. 2 19/5
Annonsepriser 2025
Bakside 24.500,Omslagsside 22.000,Helside 20.500,1/2 side liggende 14.500,-
Årsavtale
Med fire innrykk oppnås min. 20% rabatt.
Annonseformat
Bredde x Høyde
1/1 side 210 mm x 297 mm + 5 mm
1/2 side liggende 210 mm x
1/2 side stående
Bakside 210
Annonsemateriell
Høyoppløste PDF-filer, der fonter og høyoppløste bilder er inkludert.
Layout, produksjon og annonsesalg
Apriil Media AS E-post: ragnar.madsen@apriil.no www.apriil.no Opplag 4 100 eks



Disclaimer






• Informasjon, meninger og synspunkter som utgis i Indremedisineren tilhører forfatterne, og ikke nødvendigvis Norsk indremedisinsk forening eller redaksjonen.
• Publisering av artikler, annonser eller annen informasjon, betyr ikke nødvendigvis støtte eller aksept for disse.
• Redaksjonen og utgiver anstrenger seg for ikke å publisere unøyaktige eller misvisende data, men forfatterne må selv ta ansvar for data,









uttalelser og meninger som blir utgitt på deres vegne.
• Redaksjonenen og utgiver gjør sitt beste for å sikre at legemiddeldoser og andre kvantiteter presenteres nøyaktig, men vi anbefaler leserne å bruke legemidler i samsvar med Felleskatalogen/Norsk legemiddelhåndbok.
• Indremedisineren og/eller utgiver kan ikke holdes ansvarlig for evt. feil eller konsekvenser som oppstår som følge av bruk av informasjon i tidsskriftet.
KRONISK NYRESYKDOM
• FORXIGA reduserte risikoen for det redusert eGFR ≥ 50 %, terminal nyresvikt,
• KUN FORXIGA, blant SGLT2-h, har sekundære endepunktet død uansett
HJERTESVIKT
DIABETES TYPE 2
• FORXIGA reduserte risikoen for det og forverring av hjertesvikt.*1
• KUN FORXIGA, blant SGLT2-h, reduserer alene, uavhengig av ejeksjonsfraksjon.
DIABETES TYPE 2
• FORXIGA reduserte risikoen for det eller sykehusinnleggelse for hjertesvikt UTEN kjent hjerte- og karsykdom.
• FORXIGA økte ikke risikoen for det MACE.*1
• FORXIGA reduserte risikoen for det primære endepunktet vedvarende redusert eGFR ≥ 50 %, terminal nyresvikt, renal eller CV død.*1
• KUN FORXIGA, blant SGLT2-h, har vist å redusere risikoen for det sekundære endepunktet død uansett årsak.**1,3
KRONISK
• FORXIGA reduserte risikoen for det primære endepunktet CV død og forverring av hjertesvikt.*1
• KUN FORXIGA, blant SGLT2-h, reduserer risikoen for CV død alene, uavhengig av ejeksjonsfraksjon.**1,3
HJERTESVIKT
KRONISK NYRESYKDOM
• FORXIGA reduserte risikoen for det primære endepunktet CV død eller sykehusinnleggelse for hjertesvikt hos pasienter MED og UTEN kjent hjerte- og karsykdom.*1
• Forxiga 10 mg skal ikke brukes ved T1D, hos gravide eller ammende.
• FORXIGA økte ikke risikoen for det andre primære endepunktet MACE.*1
• Behandlingen skal avbrytes midlertidig hos pasienter innlagt på sykehus for større kirurgiske inngrep eller ved akutte, alvorlige medisinske sykdommer
•
Referanse: 1. Felleskatalogen.no (20.nov. 2024) 2. Forxiga SPC pkt. 4.1, 4.2, 4.4
det primære endepunktet vedvarende nyresvikt, renal eller CV død.*1
INDIKASJONER:
har vist å redusere risikoen for det uansett årsak.**1,3
Praktisk informasjon:
• Behandling av utilstrekkelig kontrollert diabetes mellitus type 2 (T2D) hos voksne og barn ≥10 år, som tillegg til diett og fysisk aktivitet: Som monoterapi når metformin er uhensiktsmessig pga. intoleranse eller som tillegg til andre legemidler til behandling av T2D.
komplikasjonene ved 1
det primære endepunktet CV død
mg
Forxiga 10 mg skal ikke brukes ved T1D, hos gravide eller ammende. Brukes med forsiktighet ved økt risiko for diabetisk ketoacidose.
• Behandling av kronisk nyresykdom hos voksne.
• Behandling av symptomatisk kronisk hjertesvikt hos voksne.
eduserer risikoen for CV død ejeksjonsfraksjon.**1,3
REFUSJONSBERETTIGET BRUK:
DIABETES TYPE 2
det primære endepunktet CV død hjertesvikt hos pasienter MED og karsykdom.*1
det andre primære endepunktet
Behandlingen skal avbrytes midlertidig hos pasienter innlagt på sykehus for større kirurgiske inngrep eller akutte, alvorlige medisinske sykdommer.
• Som tillegg til annen blodsukkersenkende behandling ved diabetes type 2 (unntatt GLP-1analoger). Refusjonskoder: ICPC: T90 Diabetes type 2. ICD: E11 Diabetes mellitus type 2. Vilkår 264: Refusjon ytes i kombinasjon med metformin til pasienter som ikke oppnår glykemisk kontroll på behandling med metformin. Pasienter med etablert hjerte- og karsykdom og/eller nyresykdom kan starte med SGLT2 hemmer i kombinasjon med metformin som førstevalg.
KRONISK NYRESYKDOM
DOKUMENTERT EFFEKT2
Refusjonskoder
Vilkår
• Behandling av pasienter med kronisk nyresykdom med bekreftet albuminuri (eGFR 25-75 mL/ min/1.73m² og albumin/kreatinin-ratio i urin over 20 mg/mmol). Refusjonskoder: ICPC: U99 Nyresvikt kronisk. ICD: N18 Kronisk nyresykdom.Vilkår 260: Refusjon ytes kun i kombinasjon med optimalisert behandling med RAAShemmer, enten ved bruk av ACE-hemmer eller angiotensin II-reseptorblokker (ARB).
HJERTESVIKT
Praktisk informasjon:
Forxiga 10 mg skal ikke brukes ved T1D, hos gravide eller ammende.
• Behandling av symptomatisk kronisk hjertesvikt hos voksne. Refusjonskoder: ICPC: K77. Hjertesvikt. ICD: I50 Hjertesvikt.
T2D og etablert hjerte- og karsykdom og/eller nyresykdom*
VIKTIG INFORMASJON
Brukes med forsiktighet ved økt risiko for diabetisk ketoacidose.
Metformin
FORXIGA reduserte risikoen for det primære endepunktet vedvarende redusert eGFR ≥ 50 %, terminal nyresvikt, renal eller CV død.*1
FORXIGA + metformin T2D
CKD med min/1.73m uAKR
Behandlingen skal avbrytes midlertidig hos pasienter innlagt på sykehus for større kirurgiske inngrep eller akutte, alvorlige medisinske sykdommer.
Anbefalt dosering: 10 mg 1 gang daglig. Det er ikke anbefalt å starte behandling ved GFR < 25 ml/min. Ved GFR < 45 ml/min skal ekstra glukosesenkende behandling vurderes hos T2D pasienter med behov for ytterligere glykemisk kontroll.
Ved alvorlig nedsatt leverfunksjon er anbefalt startdose 5 mg.
Utvalgt sikkerhetsinformasjon:
• Brukes med forsiktighet ved økt risiko for diabetisk ketoacidose.
KUN FORXIGA, blant SGLT2-h, har vist å redusere risikoen for det sekundære endepunktet død uansett årsak.**1,3
• Pasienter med albuminuri kan ha mer nytte av behandling med Forxiga. Ingen erfaring med behandling av kronisk nyresykdom hos pasienter uten diabetes som ikke har albuminuri.
• Begrenset erfaring med Forxiga i NYHA-klasse IV.
FORXIGA
• Forsiktighet utvises der Forxiga-indusert blodtrykksfall kan utgjøre risiko.
Praktisk informasjon:
2. linje behandling
(Dersom man ikke oppnår glykemisk kontroll med metformin alene)
Forxiga 10 mg skal ikke brukes ved T1D, hos gravide eller ammende.
• Kan gi økt nyreutskillelse av litium. Pasienten skal henvises til forskrivende lege for overvåking av serumkonsentrasjon.
FORXIGA reduserte risikoen for det primære endepunktet CV død og forverring av hjertesvikt.*1
• Kan gi økt hematokrit. Pasienter med uttalte økninger i hematokrit skal overvåkes og undersøkes for underliggende hematologisk sykdom.
Bivirkninger: Svært vanlige: Hypoglykemi (når brukt med sulfonylurea (SU) eller insulin)). Vurder en lavere dose av insulin/ SU for å redusere denne risikoen ved T2D. Vanlige: Genitale infeksjoner, urinveisinfeksjoner. Mindre vanlige: Volumdeplesjon inkl. hypotensjon. Sjeldne bivirkninger: Diabetisk ketoacidose (ved T2D). Svært sjeldne: Fourniers gangren.
Reseptgruppe C.
KUN FORXIGA, blant SGLT2-h, reduserer risikoen for CV død alene, uavhengig av ejeksjonsfraksjon.**1,3
Refusjonskoder Vilkår
T90, E11 264 1. linje behandling
Pakninger og priser: 10 mg: 28 stk. kr 450. 98 stk. kr 1432,30. For mer info. om Forxiga, les FK tekst på www.felleskatalogen.no eller SPC
NO-12728-08-24-CVRM
FORXIGA reduserte risikoen for det primære endepunktet CV død eller sykehusinnleggelse for hjertesvikt hos pasienter MED og UTEN kjent hjerte- og karsykdom.*1

Skann QR-koden for å registrere din e-post slik at du kan motta invitasjoner til møter, e-læringsprogrammer og mer digitalt.
FORXIGA økte ikke risikoen for det andre primære endepunktet MACE.*1
Brukes med forsiktighet ved økt risiko for diabetisk ketoacidose.
Behandlingen skal avbrytes midlertidig hos pasienter innlagt på sykehus for større kirurgiske inngrep eller akutte, alvorlige medisinske sykdommer.
Kalcipos brukes for forebygging og behandling av kalsium og vitamin D-mangel hos eldre.1 osteoporosebehandling hos pasienter med risiko for vitamin D- og kalsiummangel.1 Tablettene er beregnet for voksne over 18 år og doseres daglig.1 Svelges hele med vann. Kan ev. knuses eller deles ved behov.1
Mengde kalsium i preparatet er under vanlig anbefalt daglig inntak.1 Preparatet er derfor primært beregnet til pasienter med behov for vitamin D- tilskudd utover inntak av 500-1000 mg kalsium daglig via maten.1 Kalsiuminntak via maten bør beregnes av forskriver.1

Utvalgt sikkerhetsinformasjon:1
• Kalcipos er kontraindisert ved: Hyperkalsemi, hyperkalsiuri samt sykdommer og/ eller tilstander som fører til hyperkalsemi og/eller hyperkalsiuri (f.eks. myelom, benmetastaser, primær hyperparatyreoidisme), nefrolitiasis, nefrokalsinose, hypervitaminose D, og nyresvikt.
•
• Kalcipos bør forskrives med forsiktighet til pasienter med sarkoidose.

Ved graviditet skal daglig inntak ikke overskride 1500 mg kalsium og 600 IE vitamin D.1 Skal derfor ikke brukes rutinemessig for forebygging av kalsium- og vitamin D-mangel i svangerskapet, men kan brukes til gravide som har stor risiko for å utvikle hypokalsemi, eller som allerede har kalsium- og vitamin D-mangel.1
Kan brukes under amming. Kalsium og vitamin D3 går over i morsmelk.1
Oppbevaring: Oppbevares i originalpakningen for å beskytte mot lys. Hold beholderen tett lukket for å beskytte mot fuktighet.1
Kalcipos (kalsiumkarbonat, vitamin D3): refusjon og pris Reseptgruppe C. Pakninger og priser: 90 tabletter koster: 196,80.2
Kalcipos kan for enkelte diagnoser gis individuell stønad på blå resept, se vedlegg 1, til folketrygdloven § 5-14, blåreseptforskriften.3
Få oversikt over aktuelle diagnosekoder og vilkår i fulltekst på Helsedirektoratets nettsider ved å skanne QR-koden.

Ytterligere informasjon preparatomtalen, SPC: Kalcipos (11.11.2024)

Referanser:
1. Kalcipos SPC (11.11.2024), avsnitt 2., 3., 4,1, 4.2, 4.3, 4.6. og 6.4.
2. Kalcipos, Felleskatalogtekst basert på SPC 11.11.2024
3. Helsedirektoratet, rundskriv, kapittel 5, stønad til helsetjenester, Vedlegg 1 til § 5-14 legemiddellisten, legemidler, kalsiumpreparater Sist faglig oppdatert: 23.04.2024
Viatris AS Hagaløkkveien 26 | Pb 194 – 1371 Asker, Norge infonorge@viatris.com | D-vitaminmangel.no
| 12.2024
Hvilke roller har legene? Jeg regner med at de fleste av dere er kjent med begrepet «felles kompetansemål» (FKM), som ble innført i forbindelse med dagens spesialistforskrift, med full virkning fra 2019. Bakgrunnen er basert på en beskrivelse av de ulike roller som legene naturlig innehar, og hvorav man er innom de fleste av dem i løpet av en vanlig arbeidsdag.
Begrepet «De syv legerollene» ble introdusert gjennom CanMEDSrammeverket utviklet av Royal College of Physicians and Surgeons of Canada. Dette rammeverket dannet så grunnlaget for den norske versjonen; de felles kompetansemålene. Målet er å sikre helhetlig og kvalitetsmessig behandling av pasienter ved å definere de ulike rollene som leger skal fylle: medisinsk ekspert, kommunikator, samarbeidspartner, ledelse, drive forebyggende helse, akademiker og profesjonell. Disse rollene regnes for å være nødvendige for å møte de komplekse og varierende behovene i dagens helsevesen. De syv lege roller er definert i mange land, i alle verdensdeler. Men er tillagt litt ulik betydning i ulike kulturer. De norske er oversatt fra de danske, som ble beskrevet i 2013.
Her følger en kort beskrivelse av de syv rollene. Men jeg anbefaler å lese mer på enten sidene til Sundhedsstyrelsen i Danmark eller Royal College i Canada sine egne sider. Medisinsk ekspert: Selve kjernen i legens rolle og innebærer å både ha nødvendig kunnskap, ferdigheter og holdninger for å kunne diagnostisere, behandle og forebygge sykdom. Det forventes at legen skal holde seg oppdatert på ny forskning og utvikling innen medisinsk vitenskap for å kunne tilby den beste behandlingen. Det forventes at leger baserer sine
valg på den nyeste og mest pålitelige informasjonen. Kommunikator: En leges evne til å kommunisere effektivt med pasienter, pårørende og kolleger er avgjørende for å bygge tillit og forståelse. Gode kommunikasjonsevner kan bidra til bedre pasienttilfredshet, økt etterlevelse av behandling og bedre helseresultater. Spesielt viktig er det å kunne kommunisere godt med pasienter som har ulik kulturell og språklig bakgrunn. Samarbeidspartner: Samarbeid mellom fastleger, spesialister og sykehus er viktig for å sikre god pasientflyt og kontinuitet i behandlingen. Leder: Mange leger innehar lederansvar i løpet av karrieren, enten det er på avdelingsnivå, i prosjekter eller i utvikling av nye behandlingstilbud. Gode lederegenskaper innebærer å kunne ta beslutninger, delegere oppgaver og motivere andre.
Forebyggende helse: Leger har en viktig rolle som helseforkjempere, både på individ- og samfunnsnivå. Dette innebærer å arbeide for å forebygge sykdom og fremme helse gjennom å identifisere og adressere risikofaktorer, samt å påvirke helsepolitikken. Akademiker: Som akademikere skal leger bidra til utviklingen av medisinsk kunnskap gjennom forskning og undervisning. Dette innebærer å delta i forskningsprosjekter, publisere artikler og veilede studenter og kolleger.
Profesjonell: Og til slutt, samfunnet forventer profesjonalitet av legene. Å være profesjonell innebærer å handle med integritet, empati og respekt for pasienter og kolleger. Det innebærer også å være bevisst på egne begrensninger og å søke hjelp og veiledning når det er nødvendig.
FKM er altså læringsmål som spesialistforskriften
beskriver skal dekke disse «… grunnleggende kompetanser alle leger må ha for å fungere optimalt i legerollen». FKM er knyttet til spesialistutdanningen, men i prinsippet blir man aldri ferdig utlært i disse. For eksempel vil etiske vurderinger og refleksjoner endres og modnes over tid, gjennom pasientmøter og diskusjoner med kolleger. I år blir det innført omfattende endringer i FKM, med virkning fra de legene som starter som LIS1 i september 2025, og for LIS2/3 fra mars 2026. Hvordan skal man lære FKM og de syv legeroller? Noe kompetanse kan kanskje læres i klasserom og på kurs, men de fleste ferdighetene skal læres gjennom daglig arbeid, i skjæringspunktet mellom kolleger, annet helsepersonell, pasienter og pårørende. Det kan bli endringer i enkelte av de såkalte lærings aktivitetene, men tanken om at legene har ulike roller vil ikke endres.
Hilsen
Trond Vartdal Leder, Norsk Indremedisinsk forening


Revmatoid artritt: Voksne med revmatoid artritt (RA) i kombinasjon med metotreksat hos de som ikke oppnår tilstrekkelig effekt med metotreksat alene. Autoinflammatoriske periodiske febersyndromer hos voksne, ungdom, barn og spedbarn (≥8 måneder med kroppsvekt ≥10 kg): Cryopyrinassosierte periodiske syndromer (CAPS) inkl. NOMID/CINCA , MWS og FCAS. Familiær middelhavsfeber (FMF), hvis hensiktsmessig i kombinasjon med kolkisin. Stills sykdom: systemisk juvenil idiopatisk artritt (sJIA) og Stills sykdom i voksen alder (AOSD), med aktive systemiske trekk av moderat til høy sykdomsaktivitet, eller ved fortsatt sykdomsaktivitet etter behandling med NSAID eller glukokortikoider.
Kan gis som monoterapi eller i kombinasjon med andre antiinflammatoriske legemidler og DMARD.
Dosering og administrering1
RA: Voksne inkl. eldre: Anbefalt dose er 100 mg 1 gang daglig
CAPS: Voksne inkl. eldre, ungdom og barn ≥8 måneder og ≥10 kg:
Anbefalt startdose 1-2 mg/kg dag.
FMF og Stills sykdom: Anbefalt dose 100 mg/dag ved kroppsvekt ≥50 kg. Ved kroppsvekt <50 kg justeres dosen etter kroppsvekt, med startdose 1-2 mg/kg/dag. Hos barn med utilstrekkelig respons kan dosen økes opptil 4 mg/kg/dag. Kineret skal gis subkutant i daglige injeksjoner.
Utvalgte advarsler og forsiktighetsregler1
Hepatiske hendelser
I kliniske studier har det blitt observert forbigående økning i leverenzymer. Rutinemessig testing av leverenzymer i løpet av den første måneden bør vurderes, særlig hvis pasienten har predisponerende faktorer eller utvikler symptomer som antyder leverdysfunksjon.
Alvorlige infeksjoner
Kineretbehandling skal ikke initieres hos pasienter med aktive infeksjoner. Med nøye overvåking kan behandlingen med Kineret fortsettes også ved en alvorlig infeksjon. Behandling med Kineret for covid 19 kan fortsette til tross for (sekundære) infeksjoner.
Nøytropeni
Kineret bør ikke initieres hos pasienter med nøytropeni (ANC < 1,5 x 109/l).
Annet
Varier injeksjonssted for å unngå tegn og reaksjoner på injeksjonsstedet.
Varenummer: 418642 Styrke: 100mg/0,67 ml
Pakning: 7 x 0,67 ml (ferdigfylt sptøyte)
Pris (AUP): 2875,30 Refusjon: H-resept, R.gr.: C
Swedish Orphan Biovitrum AS Dronning Eufemias gate 16, 0191 Oslo Tlf.: 66 82 34 00 mail.no@sobi.com www.sobi.com/norway
Utvalgte bivirkninger1
Svært vanlige: Reaksjon på injeksjonsstedet Hodepine. Vanlige: Nøytropeni
Trombocytopeni Alvorlige infeksjoner.
For fullstendig oversikt over bivirkninger og forsiktighetsregler: se godkjent SPC på www.felleskatalogen.no
For mer informasjon om Kineret: www.kineret.no eller scan QR-koden

PP-26548 feb 2025
I denne utgaven setter vi søkelys på aktuelle og viktige temaer innen indremedisin, med fokus på både kliniske utfordringer og innovative løsninger. Artiklene favner fra akuttmedisin til forebygging og behandling. Vi får innblikk i hvordan innovative tiltak kan forbedre diagnostikk, behandling og pasientoppfølging.
Akutt lungeemboli (LE) kan være en livstruende tilstand og det er viktig å sikre rett behandling.
Kersti Elisabeth Styren forteller om bakgrunn og hensikt for at de ved Akershus Universitetssykehus (Ahus) har etablert Pulmonary Embolism Response Team (PERT). Hun gjør også rede for hvordan de praktisk har gjennomført dette ved Ahus, samt erfaringer ved Ahus og inter nasjonalt med slike team. Kanskje noe å vurdere også ved andre sykehus?
Obstruktiv søvnapné (OSA) behandles primært med positivt luftveistrykk (PAP), men mange pasienter opplever manglende effekt eller etterlevelse.
Harald Hrubos-Strøm belyser sekundærdiagnostikk av OSA som et viktig verktøy for mer persontilpasset behandling. Metoder som søvnendoskopi og polysomnografi kan identifisere alternative tiltak, inkludert kirurgi eller medikamentell behandling. Artikkelen understreker behovet for grundig utredning før valg av videre behandling.
Angina pectoris forbindes ofte med forsnevrede koronararterier, men mange pasienter har ikke signifikante stenoser. Erik Madssen

beskriver ANOCA, en tilstand der koronar mikrovaskulær dysfunksjon eller spasmer kan forårsake iskemi og symptomer. Diagnosen krever avansert utredning, og behandlingen inkluderer livsstilstiltak og medikamentell terapi. Artikkelen belyser viktigheten av økt bevissthet om ANOCA for bedre pasientbehandling.
Albuminuri er en tidlig markør for nyresykdom og kardiovaskulære skader, spesielt hos pasienter med diabetes og hypertensjon. Sihaam Yasin Ibrahim Ali, Rannveig Skrunes og Hans-Peter Marti beskriver hvordan albumin-kreatinin-ratio (AKR) i urin er en mer presis metode for å vurdere tidlig nyreskade enn tradisjonelle metoder. Forhøyet AKR bør føre til målrettet utredning, slik at underliggende sykdom diagnostiseres og at fokusert behandling kan startes tidlig.
Pasienter med kronisk nyresykdom (CKD) har økt risiko for osteoporose og brudd grunnet forstyrrelser i benog mineralmetabolismen (CKD-MBD). Kiarash Tazmini, Mikkel Pretorius, Hege K. Pihlstrøm og Ruth Strømmen beskriver mekanismene bak denne tilstanden, diagnostiske utfordringer og behandlings alternativer. Artikkelen understreker behovet for tidlig identifikasjon og persontilpasset behandling for å redusere risikoen for skjelettkomplikasjoner hos nyrepasienter.
Redusert hørsel er en av de viktigste modifiserbare risikofaktorene for demens. Christian Myrstad og Bo Engdahl diskuterer i sin artikkel

hvordan hørselstap kan bidra til kognitiv svikt, og de viser til nyere forskning som nyanserer sammenhengen. Selv små forbedringer i hørsel kan redusere demensforekomsten betydelig, men underbehandling er utbredt. Artikkelen understreker behovet for økt bevissthet og tidlig intervensjon for å forebygge kognitiv svikt hos eldre.
På foreningssidene vil vi spesielt trekke frem et innlegg om fadderordning for LIS. Vi kjenner oss igjen med høyt arbeidspress, uforutsigbarhet og manglende opplæring som utfordringer i spesialiseringstiden. Cathrine Kristoffersen skriver hvordan hun fikk etablert en enkel fadderordning, som har spredd seg nasjonalt. Ordningen kan bidra til bedre arbeidsmiljø, lavere turnover og økt trivsel blant nye LIS. Vi kunngjør videre at Norsk nyremedisinsk forening blir ny fast bidragsyter. På foreningssidene redegjør leder Ivar Anders Eide for noen av aktivitetene, og foreningen arrangerer nordisk møte 11-14. juni i Oslo (se oppslag).
Vi takker alle bidragsyterne som formidler verdifulle innsikter, som kan inspirere til refleksjon, faglig utvikling og forbedringer i praksis. En stor takk rettes også til Apriil for deres arbeid med layout og utsendelse. Stor takk også til annonsørene som bidrar til å opprettholde Indremedisineren som en bærekraftig publikasjonsplattform. Vi håper innholdet i denne utgaven gir ny kunnskap og inspirasjon til hverdagen.
Riktig god lesning!


Norske indremedisinere har stor glede og nytte av Indremedisineren (IM). IM bidrar til faglig utvikling og er både et viktig bindeledd i miljøet, og mellom styret i NIF og det enkelte medlem.
Redaksjonen og alle bidragsytere jobber på dugnad. Dere annonsører bidrar til at vi kan utgi et flott IM og at vi kan drifte indremedisineren.no, der trafikken er sterkt økende. Uten deres hjelp hadde det ikke vært mulig.
Vi håper det gode samarbeidet fortsetter, og at dere blir med videre!
























Indikasjon: Tezspire er indisert som tillegg til vedlikeholdsbehandling hos voksne og ungdom i alderen 12 år og eldre med alvorlig astma som er utilstrekkelig kontrollert til tross for høye doser inhalasjonskortikosteroider i tillegg til et annet legemiddel for vedlikeholdsbehandling. Dosering: Anbefalt dose: 210 mg s.c. hver 4. uke. Tezspire er til langtidsbehandling. Forsiktighetsregler: Skal ikke brukes til å behandle akutte astmaeksaserbasjoner. Astmarelaterte symptomer eller eksaserbasjoner kan oppstå. Pasienten bør instrueres om å oppsøke lege hvis astmaen forblir ukontrollert eller forverres. Alvorlige infeksjoner bør behandles før oppstart av behandling. Ved utvikling av alvorlig infeksjon under behandling, bør behandlingen seponeres inntil denne er over. Graviditet og amming: Bruk under graviditet bør unngås med mindre forventet nytte for den gravide oppveier mulig risiko for fosteret. Vanlige bivirkninger: Faryngitt, utslett, artralgi, reaksjon på injeksjonsstedet. Pakninger og priser: Injeksjonsvæske, oppløsning i ferdigfylt penn (210 mg): 1 stk: kr. : 15 053,40. Injeksjonsvæske, oppløsning i ferdigfylt sprøyte (210 mg): 1 stk. kr. : 15 053,40 Reseptgruppe: C. Refusjon: H-resept. Refusjonsberettiget bruk: Der det er utarbeidet nasjonale handlingsprogrammer/nasjonal faglig retningslinje og/eller anbefalinger fra RHF/LIS spesialistgruppe skal rekvirering gjøres i tråd med disse. Vilkår: 216 Refusjon ytes kun etter resept fra sykehuslege eller avtalespesialist. Tezspire inngår i RHF anbefalinger for alvorlig ukontrollert T2-høy astma. Beslutning i Beslutningsforum for nye metoder 18.03.2024. Tezepelumab (Tezspire) innføres som tillegg til vedlikeholdsbehandling ved alvorlig astma med eosinofili hos voksne og ungdom i alderen 12 år og eldre som er utilstrekkelig kontrollert til tross for høye doser inhalasjonskortikosteroider i tillegg til et annet legemiddel for vedlikeholdsbehandling.
For fullstendig informasjon, les mer på www.felleskatalogen.no
AstraZeneca AS - www.astrazeneca.no – P. box 6050 Etterstad - 0601 Oslo
ID: NO-13578-01-2025-TEZ
Tezspire er indisert som tillegg til vedlikeholdsbehandling hos voksne og ungdom i alderen 12 år og eldre med alvorlig astma som er utilstrekkelig kontrollert til tross for høye doser inhalasjonskortikosteroider i tillegg til et annet legemiddel for vedlikeholdsbehandling.1
Utvalgt sikkerhetsinformasjon:
Vanlige bivirkninger er faryngitt, utslett, artralgi, reaksjon på injeksjonsstedet.1 Skal ikke brukes til å behandle akutte astmaeksaserbasjoner.1

Subkutan injeksjon
Et sentralt angrepspunkt i behandlingen av alvorlig astma2,3
TEZSPIRE (tezepelumab) er det første og eneste astmalegemiddelet som blokkerer TSLP* høyt oppe i inflammasjonskaskaden og virker på tvers av fenotyper og uavhengig av biomarkørnivå.2-6**

Vil du lære mer om et sentralt angrepspunkt for behandling av alvorlig astma?
*TSLP =Tymisk stromalt lymfopoietin **f.eks. blodeosinofiler, eosinofiler i luftveislimhinnene, IgE, FeNO, IL-5 og IL-13
Referanser
1. Tezspire SPC 4.1, 5.1, 4.8, 4.4. 2.Corren J, Parnes JR, Wang L et al. Tezepelumab in Adults with Uncontrolled Asthma. N Engl J Med 2017;377:936-46. 3. Menzies-Gow A, Corren J, Bourdin A et al. Tezepelumab in Adults and Adolescents with Severe, Uncontrolled Asthma Supplementary information. N Engl J Med 2021;384:1800-9. 4. Menzies-Gow A, Wechsler ME, Brightling CE. Unmet need in severe, uncontrolled asthma: can anti-TSLP therapy with tezepelumab provide a valuable new treatment option? Respir Res 2020;21:268. 5. Brusselle Guy, Koppelman GH. Biologic Therapies for Severe Asthma. N Engl J Med 2022;386:157-71. 6. Gauvreau GM, Sehmi R, Ambrose CS et al. Thymic stromal lymphopoietin: its role and potential as a therapeutic target in asthma. Expert Opin Ther Targets. 2020;24:777–92.
Akershus underversitetssykehus besluttet i 2022 å opprette Pulmonary Embolism Respons Team (PERT) som et prøveprosjekt. Bakgrunnen for dette var at man så et behov for å få til en mer koordinert og tverrfaglig tilnærming til vurdering og behandling av de dårligste lungeemboli-pasientene.
Kersti Elisabet Styren, Overlege, Akuttmedisinsk Avdeling, Akershus Universitetssykehus

Bakgrunn for PERT Lungeemboli (LE) er en betydelig bidragsyter til morbiditet og mortalitet. Det er den tredje vanligste årsaken til kardiovaskulær død på verdensbasis etter hjerteinfarkt og hjerneslag (1, 2). Samtidig ser man også at insidensen fortsetter å øke (2). Symptomer og klinikk ved lungeemboli er utfordrende ettersom de kan variere fra en asymptomatisk tilstand til en hemodynamisk ustabil situasjon, og i verste fall død. Diagnostikk og behandling av lungeemboli skiller seg fra andre medisinske tilstander ved at den kan involvere både indremedisinske, kirurgiske og radiologiske spesialiteter. Det finnes heller ingen standardisert eller systematisk tilnærming for behandlings- og beslutningsstøtte når pasienter med lungeemboli presenterer med et mer sammensatt bilde (1). Evidensgrunnlaget for behandling av denne pasientgruppen baserer seg i stor grad på ikke randomiserte studier, registerdata og ekspertuttalelser. Samtidig foreligger det også en betydelig heterogenitet i behandlings anbefalinger hos lungeembolipasienter (2). Mangelen på ovenstående samt økt tilgjengelighet av behandlingsmuligheter, herunder systemisk trombolyse, kateterbasert behandling, kirurgisk trombektomi og sirkulasjonsstøttende behandling
som ECMO førte til at det i 2012 ble innført «Pulmonary Embolism Respons Team» (PERT) ved Massachusetts General Hospital (1, 3).
PERT-prinsippet
Prinsippet for PERT bygger på samme konsept som andre multidisiplinære akuttmedisinske team, herunder særlig de amerikanske Heart Team, Stroke Team og Rapid Response Team. Som disse har PERTmodellen til hensikt å ivareta akutte komplekse lungeembolipasienter strømlinjeformet der man gjennom en multidisiplinær tilnærming får en rask og korrekt risikostratifisering, bestemmer den beste terapeutisk tilnærming for hver pasient og mobiliserer nødvendige ressurser for å oppnå dette. Etableringen av PERT er per dags dato en klasse IIa anbefaling i European Society of Cardiology guidelines fra 2019 (4) og håpet er å kunne reduserer mortalitet og morbiditet hos pasienter med en potensielt livstruende og ofte komplisert tilstand (1, 5).
Hensikten med PERT
En særlig viktig rolle for PERT er en rask og nøyaktig risikostratifisering av pasienten, da disse pasientene fort kan bli åpenbart hemodynamisk påvirket eller i fare for hemodynamisk forverring (5). Minst like viktig er en
felles evaluering og beslutningsprosess som bidrar til at man unngår skjevhet i vurderingene fra enkelte spesialiteter eller individer når man planlegger behandling (5). Økt tilgjengelighet av behandlingsvalg gjør det nødvendig med en multidisiplinær tilnærming for å evaluere disse opp mot hverandre i mangel på kontrollerte kliniske studier og anbefalinger utgående fra guidelines (5). Utover dette, vil flere tilgjengelige behandlingstilbud kreve forståelse av styrker og svakheter ved de ulike modalitetene samt en forståelse for hva målet med reperfusjonsbehandling er for hver enkelt pasient. Særlig er det pasientene med høy risiko og intermediær høy risiko lunge emboli som vil gagne på en slik multidisiplinær tilnærming (6).
En gruppe som man de siste årene har valgt å rette et fokus på, er pasientene med intermediær høy risiko. Dette er hemodynamisk stabile pasienter, men hvor man finner ekkokardiografiske holdepunkt for en påvirket høyre ventrikkel og forhøyede troponiner. Nyere studier har vist at nesten 1/3 av pasientene som klassifiseres som intermediær risiko, er i et normotensivt sjokk. Det finnes per dags dato ingen etablert prediksjonsmodell for å indentifisere disse pasientene, men en samlet
Mistanke om lungeemboli
scoring av sjokkparametere kan bidra til å effektivt risikostratifisere disse pasientene (7). Hva gjelder behandling av denne gruppen så viste PEITHO-studien, som per dags dato er den største randomiserte studien gjort på LE-pasienter, ingen forskjell mellom pasientene som fikk actilyse og konvensjonell behandling hvis man så på 30-dagers utfallet, men betydelig økt blødningsrisiko i actilysegruppen (8). Det er nå også gjennomført en multisenter, prospektiv registerstudie – FLASH – som så på 1000 pasienter med høy og intermediær risiko lungeembolisme behandlet med endovaskulær trombektomi. Resultatene fra denne studien er svært lovende og viste tilnærmet umiddelbar hemodynamisk forbedring, signifikant bedring i høyre ventrikkels størrelse og funksjon på ekkokardiografisk-kontroll samt bedring i dyspne etter 48 timer. Samtidig som det ikke forekom noen prosedyrerelaterte dødsfall (9).
Praktisk gjennomføring av PERT på Akershus Universitetssykehus PERT’s sammensetning varierer mellom ulike sykehus ut fra hvilke spesialiteter og ressurser man har tilgjengelig. Ved Akershus Universitetssykehus (Ahus) består PERT av vakthavende anestesiolog/intensivlege, kardiolog, hematolog, inter-
Legevurdering inkl. anamnese, klinisk undersøkelse og biokjemi. EKKO og CT på indikasjon
Vurder å aktiver PERT for tverrfaglig diskusjon om videre behandlingsvalg
Trombemasser forenlig med LE på CT samt hemodynamisk påvirket pasient og/el tegn til hø. belastning på EKKO
vensjonsradiolog samt vakthavende på Medisinsk Overvåkning som raskt kan møtes og gi beslutningsstøtte rundt behandling av pasienter med LE. Per dags dato foreligger det ikke et teamutkall for PERT på lik linje med et medisinsk team eller et traumeteam, men teamet aktiveres av behandlende lege på indikasjon. F.eks. hvis det foreligger tvil om behandlingsstrategi, pasienten forverres under administrering av Actilyse, hemodynamisk stabilisering etter avsluttet Actilyse-behandling ikke er oppnådd eller behandlingseffekt er usikker. Andre pasienttilfeller som anbefales diskutert tverrfaglig er f.eks. normotensive pasienter som har betydelig belastet høyre ventrikkel, er svært O2-krevende og/ eller hvor det foreligger kompensatorisk tachykardi. Teamet skal kunne aktiveres gjennom hele døgnet, men naturlig nok er gjennomføringen utfordrende på natt gitt at flere av spesialistene har hjemmevakt og hvordan man skal optimalisere dette jobbes det med i skrivende stund. Dersom pasienten befinner seg i Akuttmottaket anbefales det at teamet møtes her slik at man får et raskt overblikk over situasjonen, etter dette vil man hovedsakelig samles på Ekkokardiografisk-lab der man tar opp pasientens journal, CT-bilder og den ekkokardiografiske under-
søkelsen. Sammen gjennomgår man disse og tverrfaglig diskuterer videre behandling for pasienten. (figur 1)
Erfaringer fra PERT Internasjonale erfaringer Per dags dato har bare et begrenset antall studier undersøkt fordelene med PERT-implementering. De studiene som er gjort har vist at sykehus som har etablert PERT-team i større grad benyttet seg av mer avanserte behandlingsmetoder, uten at disse har kunnet vise at dette har ført til økt forekomst av komplikasjoner/blødninger, økt overlevelse eller reduserte langtids-komplikasjoner, men flere pågående studier vil etter hvert kunne gi et bedre svar på dette (1, 6, 10, 11).
Det at PERT krever betydelig med ressurser, både personell og utstyr, er problematisert i flere av studiene (6). Det skal også nevnes at de fleste studiene har sine begrensninger i form av at de er ikke-randomisert design utført på singelsenter og de fleste er også retrospektive, noe som ytterligere skaper usikkerhet rundt PERT`s direkte pasientutfall (6).
Anbefalingene for endovaskulær tilnærming har vært begrenset av flere årsaker. Men etter hvert som utstyret blir mer tilgjengelig og utprøvd, vil det etter all sannsynlighet komme mer data på området og anbefalingene vil trolig endres, på samme måte som
Foto: Kamilla Rudberg, Kommunikasjonsavdelingen Ahus
for ST-elevasjonsinfarkt og hjerneslag (12).
Erfaringer fra Akershus Universitetssykehus
På Ahus har det nå gått nesten tre år siden vi etablerte PERT som et forsøksprosjekt. Det pågår systematisk datainnsamling på alle PERT-utkall som skal analyseres og som vi håper gir oss objektive data som under-
Referanser
1. Porres-Aguilar M, et al. Pulmonary embolism response teams: Changing the paradigm in the care for acute pulmonary embolism. J Thromb Haemost 2022;20:2457-64.
2. Rivera-Lebron BN, et al. The pert concept: A stepby-step approach to managing pulmonary embolism. Chest 2021;159:347-55.
3. Brailovsky Y, et al. Pulmonary embolism response team: Additional call burden or a valuable learning opportunity? Journal of the American College of Cardiology 2021;77:1691-6.
4. Konstantinides SV, et al. 2019 esc guidelines for the diagnosis and management of acute pulmonary embolism developed in collaboration with the european
støtter våre erfaringer. Så langt er tilbakemeldingen fra våre kolleger at diskusjonene på PERT-møtene er givende og at man opplever å ha endt opp med en god konklusjon og et bra resultat for pasienten. Tilbakemeldingen fra våre intervensjonsradiologer er at de opplever at man har blitt flinkere på å ta i bruk nye og mer avanserte metoder for fjerning av blodproppene samt i større grad
respiratory society (ers). Eur Heart J 2020;41:543-603.
5. Dudzinski DM, et al. Multidisciplinary pulmonary embolism response teams. Circulation 2016;133:98103.
6. Bejjani A, et al. Pulmonary embolism response teams: Theory, implementation, and unanswered questions. J Clin Med 2022;11.
7. Bangalore S. Prevalence and Predictors of Cardiogenic Shock in Intermediate-Risk Pulmonary Embolism. JAAC, Cardiovaskular Intervention. Volum 16. No. 8 2023.
8. Meyer G. Fibrinolysis for Patiens with Intermediate-Risk Pulmonarsy Embolism. N Engl J Med 2014;370:1402-1411, DOI: 10.1056/NEJMoa1302097, VOL. 370 NO. 15
også benytte seg av de allerede tilgjengelige metodene, som lokal trombolyse. Innføringen av PERT og dermed det økte fokuset på LE, har uten tvil vært den utløsende faktoren for både den raske behandlingen av den aktuelle pasientgruppen, men også den økte bruken av invasiv behandling. Dedikerte tverrfaglige team, med god implementering klinikknært og med tilgjengelighet for de som mottar pasienten hever etter vår mening også kvaliteten og sikkerheten i pasientbehandlingen.
Takk til Ragnar Rosenskiold, May-Liss Hatleskog, Ellen Brodin, Tarjei Øvrebotten og Dan Levi ved Akershus Universitetssykehus for gode innspill og råd.
9. Toma C, Jaber WA, Weinberg MD et al. Acute outcomes for the full US cohort of the FLASH mechanical thrombectomy registry in pulmonary embolism. EuroIntervention 2023; 18: 1201–12
10. Fleitas Sosa D, et al. Impact of pulmonary embolism response teams on acute pulmonary embolism: A systematic review and meta-analysis. Eur Respir Rev 2022;31.of the German Cardiac Society 2022:1-11.
11. Rosovsky R, et al. Pulmonary embolism response teams: Purpose, evidence for efficacy, and future research directions. Res Pract Thromb Haemost 2019;3:315-30
12. Carroll BJ, Larnard EA, Pinto DS et al. Percutaneous Management of High-Risk Pulmonary Embolism. Circ Cardiovasc Interv 2023; 16: e012166.
Primær- og sekundærbehandlingen av obstruktiv søvnapné er positivt luftveistrykk, tonsillektomi, søvnapnéskinne eller posisjonstiltak. Persontilpasset behandling kan tilbys etter standardisert sekundærdiagnostikk i form av endoskopi i kunstig søvn. Endotyping ved hjelp av polysomnografi er også en lovende sekundærdiagnostisk prosedyre.
Hrubos-Strøm, Seksjonsoverlege PhD, Øre- Nese- Halsavdelingen Akershus Universitetssykehus og førsteamanuensis Universitetet i Oslo
Bakgrunn
Obstruktiv søvnapné (OSA) rammer om lag 10% av den voksne befolkningen i Norge1. Sykdommen er knyttet til kardiovaskulær sykdom, søvnighet og nattlige oppvåkninger 2. Positivt luftveistrykk (PAP) er den mest effektive behandlingen av sykdommen, men 25-50% av pasientene er behandlingsresistente i form av manglende etterlevelse eller vedvarende søvnighet3. I nylige publiserte norske anbefalinger for utredning og behandling av OSA hos voksne anbefales rutinemessig å vurdere sekundær «Non-PAP» behandling (tannskinne, vektnedgang, tonsillektomi) i denne gruppen, uten ytterligere diagnostisk vurdering4 Disse tiltakene ansees som mindre effektive enn PAP i uselekterte pasientpopulasjoner, og dessverre gjenstår et stort antall pasienter uten vellykket behandling 5,6 .
Undertegnede og medforfattere beskrev i 2023 begrepet “sekundærdiagnostikk” som et nødvendig instrument for å gi et adekvat tilbud ved behandlingsrefraktær OSA7, og dette er tatt med i nasjonal anbefaling. I denne artikkelen presenteres generelle utfordringer ved behandlingssvikt og rasjonale bak, samt praktisk gjennomføring av sekundærdiagnostikk ved behandlingsresistent OSA.
Behandlingsetterlevelse og pasientperspektiv I moderne medisin er manglende behandlingsetterlevelse assosiert med personlig lidelse, dårligere helseutfall og økte kostnader 8. Ifølge OECD kan 200 000 dødsfall og 125 milliarder € årlig tilskrives manglende behandlingsetterlevelse 9 bare innenfor EU. I gjennomsnitt følger 25 prosent av pasientene ikke opp anbefalinger for forebygging og sykdomshåndtering, som screening, trening, kostholdsendringer, avtale -
C
Akseptabelt symptomnivå Uakseptabel riskiko
planlegging, medisininntak eller bruk av tekniske behandlingsmetoder10 Når behandlingsregimer er komplekse og/eller krever livsstilsendringer, kan manglende etterlevelse være så høy som 70 prosent. Manglende behandlingsetterlevelse har blitt identifisert som en stor barriere for effektiv (selv-)håndtering av kroniske sykdommer 8,11
Majoriteten av primærdiagnostiserte pasienter med OSA er i 30- til 50-årsalderen. Dette er ofte pasientens

D
Uakseptabelt symptomnivå Uakseptabel risiko
A
Akseptabelt symptomnivå Akseptabelt risikonivå B
Uakseptabelt symptomnivå Akseptabelt risikonivå
Figur 1: Mulig beslutningsstøtteverktøy ved utforsking av pasientperspektivet. Figuren er tidligere publisert i referanse 7, norsk oversettelse, trykkes med tillatelse.
Primær- og sekundærbehandling

Pap
Livsstilstiltak
Søvnapnéskinne
Tonsillektomi (ved store mandler)
foreslår eksplisitt å benytte risikoverktøyet «SCORE2» som kartlegger kardiovaskulær risikoprofil14. SCORE2 krever biokjemiske analyser, noe som det ikke er tradisjon for å innhente hos pasienter med OSA.

Sekundærdiagnostikk
Øre- Nese- Halsundersøkelse
Søvndagbok og /eller blodprøver
Endoskopi i kunstig søvn
Polysomnografi


Kombinasjonsbehandling Avansert PAP
Avansert kirurgi
Medikamenter
Persontilpassede treningsprogrammer
Neseseptumplastikk for økt etterlevelse med PAP
¨Behandling av ko-morbid insomnia og OSA (COMISA)
Figur 2: Primære og sekundære behandlingsmetoder, sekundærdiagnostikk og to hovedgrupper av tærtiærbehandling. Figuren er tidligere publisert i referanse 7, norsk oversettelse, trykkes med tillatelse.
første erfaring med en kronisk sykdom som kan kreve en livslang behandling eller livsstilsendring.
En metodikk som kartlegger pasientperspektivet er anbefalt i slike konsultasjoner, men empiri fra daglig drift viser at pasientperspektivet ofte glemmes12. Kartlegging av pasientperspektivet er avgjørende for å oppnå et informert samvalg, der lege og pasient i fellesskap reflekterer mot en beslutning13. Figur 1 fremstiller et beslutnings støtteverktøy inspirert av den modifiserte «Bavenoklassifikasjonen» for bruk ved OSA14 Hvis pasienten angir en høy skår på den visoanaloge skalaen (VAS) på x-aksen, søker man etter fortolkninger av spesifikke symptomer som dagsøvnighet, gjentatte oppvåkninger, nokturi eller en følelse av kvelning under søvn. Man ber også pasientene om å markere på VAS i y-aksen i hvilken grad de aksepterer risiko for hjerte- karsykdom. En slik risikovurdering oppleves ofte vanskelig å gjøre for pasienten. Den modifiserte Bavenoklassifikasjonen
Mange OSA-pasienter sover alene fordi deres sengepartner klager over forstyrrende bevegelser eller lyder. Særlig de sosiale aspektene ved OSA er viktig når pasientperspektivet utforskes15. Allerede fra Sullivans første publikasjon om PAP ved OSA har det vært anbefalt å benytte nesemaske fremfor helmaske16. En helmaske vil kreve stropper som trekker haken bakover og nedover. Dette skaper volumreduksjon i oroog hypopharynx, noe som bidrar til et behov for høyere masketrykk.
Rasjonale for sekundærdiagnostikk
Bruken av sentralstimulerende midler, såkalt «ADHD-medisin» er økende17 Indikasjonen for et slikt medikament, Solriamfetol, er nylig blitt utvidet også til «bedring av våkenhet og reduksjon av uttalt søvnighet på dagtid (EDS) hos voksne pasienter med OSA, hvor EDS ikke har blitt godt nok behandlet med primærbehandling av OSA, slik som pustemaske». Det er avgjørende å kjenne til kunnskapshull i litteraturen omkring diagnostikk og primærbehandling før en vurderer langtidsbehandling med sentralstimulerende legemidler ved OSA7. Balk-rapporten18 har reist nøkkelspørsmål knyttet til dagens objektive diagnostiske metoder ved OSA, inkludert bruk av apné hypopné indeks (AHI). AHI angir alvorlighet av sykdommen målt ved antall respiratoriske hendelser.
Utover sentralstimulerende midler har legemiddelindustrien for alvor rettet fokus mot subgrupper av pasienter med OSA definert etter patofysiologiske virkningsmekanismer19. Disse er det kritiske lukningstrykket (pcrit), oppvåkningsterskel, sentral pusteregulering (såkalt loop gain) og muskelaktivitet, til sammen benevnt PALM-faktorer 20. PALM-faktorene kan observeres ved gradvis å redusere PAP under en titreringsnatt i et eksperimentelt oppsett som inkluderer måling av intratorakalt trykk og muskelaktivitet. Noen
forfattere hevder også at pcrit og nivå for kollaps i de øvre luftveiene kan identifiseres ved polysomnografiundersøkelse21. En prosedyre for segmentering til subgrupper etter PALM-faktorene er per i dag ikke i klinisk bruk, men forskningsfronten nærmer seg. Jeg tror det om fem år eksisterer validerte segmenteringstester for pasienter med OSA, og at tertiærbehandling, enten nonfarmakologisk eller farmakologisk, vil tilbys persontilpasset basert på en slik subklassifisering. Figur 2 oppsummerer primære og sekundære behandlingsmetoder (I), sekundærdiagnostikk (II) og to hovedgrupper av tertiærbehandling (IIIa og IIIb).
Praktisk gjennomføring av sekundærdiagnostikk Øre- nese- halsundersøkelse, søvndagbok og blodprøver Av de fem foreslåtte, sekundærdiagnostiske metodene bør ørenese- halsundersøkelsen være et absolutt minimum. Bruk av søvndagbok og/eller blodprøver vil avhenge av pasientens perspektiv etter bruk av beslutningsstøtteverktøyet vist i figur 1. I tilfeller med symptomer i form av nattlige oppvåkninger eller problemer med å sovne med PAP bør ko-morbid insomni og OSA (COMISA) mistenkes22. COMISA er i løpet av de siste årene innarbeidet som en egen fenotype og det er særlig ved hos disse pasientene at bruk av søvndagbok kan være nyttig. Vi har i vår forskningsgruppe utviklet en elektronisk søvndagbok 23,24. Hos pasienter som i VAS (figur 1) angir uakseptabel risiko ved manglende behandlingsetterlevelse kan blodprøver vurderes for å kunne gi presise risikoestimat.
Søvnendoskopi og polysomnografi Persontilpasset medisin er i Norge definert som «forebygging, diagnostikk, behandling og oppfølging tilpasset biologiske forhold hos den enkelte »25. Endoskopi i kunstig søvn gir unik informasjon om kollapsmønsteret (pcrit) hos hvert individ, og metoden kan bedrer utkomme ved søvnapnékirurgi26. Vi hadde ved utgangen av 2024 utført mer enn 60 slike undersøkelser ved Akershus Universitetssykehus. Indikasjon for undersøkelsen er manglende effekt av behandling med PAP. Innføring av undersøkelsen har medført en
radikal endring av kommunikasjon med pasienter i forhold til problemer med masketoleranse. Figur 3 viser et bilde av en epiglottiskollaps. Nyere forskning indikerer at 15-40% av pasienter som ikke tolererer PAP har en epiglottis som lukker seg over larynx ved behandling med PAP27.
Metoden polysomnografi er under utvikling, og vil sannsynligvis innen kort tid kunne gi kliniker informasjon om oppvåkningsterskel, loop gain og muskelaktivering. I tillegg vil den ko-morbide søvnsykdommen periodiske beinbevegelsessyndrom (PLMS) kunne diagnostiseres og behandles. PLMS bidrar også til søvnighet på dagtid og bør alltid utelukkes før man eventuelt behandler med sentralstimulerende medikamenter.
Tertiærbehandling av OSA basert på sekundærdiagnostikk Tertiærbehandlinger uten bruk av PAP Siden non-PAP behandlinger av OSA alene er mindre effektive enn PAP, er det knyttet spenning til om bruk av segmenteringsverktøy og kombinasjoner av flere behandlinger vil kunne gi sammenliknbar effekt med PAP5,6. Det vil være for
Referanser:
1. Hrubos-Strøm H, Randby A, Namtvedt SK, et al. A Norwegian population-based study on the risk and prevalence of obstructive sleep apnea. The Akershus Sleep Apnea Project (ASAP). Journal of sleep research. 2011;20(1 Pt 2):162-170.
2. Veasey SC, Rosen IM. Obstructive Sleep Apnea in Adults. The New England journal of medicine. 2019;380(15):1442-1449.
3. Craig S, Pépin JL, Randerath W, et al. Investigation and management of residual sleepiness in CPAPtreated patients with obstructive sleep apnoea: the European view. Eur Respir Rev. 2022;31(164).
4. Hrubos Strom H. Nasjonal anbefaling for utredning og behandling av obstruktiv søvnapné hos voksne. Tidsskriftet Søvn. 2024(1):27-37.
5. Randerath W, Verbraecken J, de Raaff CAL, et al. European Respiratory Society guideline on non-CPAP therapies for obstructive sleep apnoea. Eur Respir Rev. 2021;30(162).
6. Jacobowitz O, Afifi L, Alkan U, Penzel T, Poyares D, Kushida C. Endorsement of “European Respiratory Society guideline on non-CPAP therapies for obstructive sleep apnoea” by World Sleep Society. Sleep medicine. 2024;113:293-298.
7. Hrubos-Strøm H, Bergqvist J, Zou D. Longitudinal Management and a Decision-Aid Tool in TreatmentResistant Sleep Apnea. Current Sleep Medicine Reports. 2023.
8. Cutler RL, Fernandez-Llimos F, Frommer M, Benrimoj C, Garcia-Cardenas V. Economic impact of medication non-adherence by disease groups: a systematic review. BMJ open. 2018;8(1):e016982.
9. OECD, Union E. Health at a Glance: Europe 2018. 2018.
10. DiMatteo MR. Variations in patients’ adherence to medical recommendations: a quantitative review of 50 years of research. Medical care. 2004;42(3):200-209.
11. Kim J, Tran K, Seal K, et al. CADTH Optimal Use Reports. In: Interventions for the Treatment of Obstructive Sleep Apnea in Adults: A Health Technology Assessment. Ottawa (ON) aveoTSD. She also participated in the 2015 510(k) process for the Braebon-DentiTrac compliance chip but received no remuneration. Dr. Kendzerska received funding from the ResMed Foundation Research Grant in 2011.: Canadian Agency for Drugs and Technologies in Health
omfattende å redegjøre for de forskjellige kirurgiske teknikkene som kan benyttes ved forskjellige kollapsmønstre i de øvre luftveiene og hvilke kombinasjon av non-PAP som kan vurderes. Vi har ved Akershus Universitetssykehus innført metoden «Barbed Suturer Pharyngoplasty» etter undersøkelse med endoskopi i kunstig søvn28 Denne teknikken rettes mot den bakre tonsillepillaren slik at bredden i svelget økes ved lateral kollaps.
Tertiærbehandlinger med mål om økt PAP-etterlevelse
Hvis årsak til behandlingssvikt ved PAP har vært forhold knyttet til neseanatomi, kan kirurgisk behandling være effektivt for å kunne fortsette med PAP levert gjennom en nesemaske29,30
Kognitiv atferdsterapi for insomni (CBTi) har dokumentasjon for effekt ved behandling av COMISA, og kan se ut til å være en effektiv metode for å øke behandlingsetterlevelse med PAP31. CBTi er dessverre lite tilgjengelig i Norge.
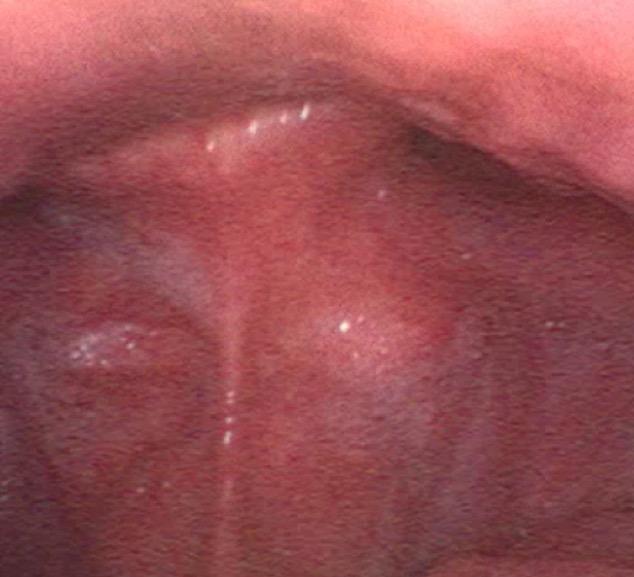
Figur 3: Epiglottiskollaps i ryggleie (foto Harald Hrubos-Strøm)
Konklusjon Sekundærdiagnostikk ved OSA er i rask utvikling og bør gjennomføres før restsøvnighet behandles med sentralstimulerende medikamenter etter primær- og sekundær behandlingssvikt med PAP og non-PAP respektivt. Tertiærbehandling ved behandlingsresistent OSA kan være rettet mot å tolerere PAP bedre, eller være kombinasjoner av non-PAPbehandlingsmetoder.
Copyright © 2017 Canadian Agency for Drugs and Technologies in Health.; 2017.
12. Øverby CT, Sutharshan P, Gulbrandsen P, Dammen T, Hrubos-Strøm H. Shared decision making: A novel approach to personalized treatment in obstructive sleep apnea. Sleep Med X. 2022;4:100052.
13. Ikeda AK, McShay C, Marsh R, et al. Patient Factors and Preferences in Choosing Sleep Surgery for Obstructive Sleep Apnea: A Qualitative Study. Otolaryngology--head and neck surgery : official journal of American Academy of Otolaryngology-Head and Neck Surgery. 2022:1945998221105404.
14. Matthes S, Treml M, Grote L, et al. The modified Baveno classification for obstructive sleep apnoeaDevelopment and evaluation based on the ESADA database. European Respiratory Journal. 2024:2401371.
15. Crawford MR, Espie CA, Bartlett DJ, Grunstein RR. Integrating psychology and medicine in CPAP adherence - New concepts? Sleep medicine reviews. 2013.
16. Sullivan CE, Issa FG, Berthon-Jones M, Eves L. Reversal of obstructive sleep apnoea by continuous positive airway pressure applied through the nares. Lancet. 1981;1(8225):862-865.
17. Hartz I, Madsstuen NHH, Andersen PN, Handal M, Odsbu I. Nationwide trends in the use of ADHD medications in the period 2006-2022: a study from the Norwegian prescription database. BMC Psychiatry. 2024;24(1):767.
18. Balk EM, Adam GP, Cao W, Reddy Bhuma MF, S., Mehta S, Panagiotou ODA, C. Long-Term Health Outcomes in Obstructive Sleep Apnea: A Systematic Review of Comparative Studies Evaluating Positive Airway Pressure and the Validity of Breathing Measures as Surrogate Outcomes. In: Diagnosis and Treatment of Obstructive Sleep Apnea in Adults. Project ID: SLPT0919. (Prepared by the Brown Evidence-based Practice Center under Contract No. 290-2015-00002-I/Task Order No. 75Q80119F32017.) ed. Rockville, MD: Agency for Healthcare Research and Quality.2022.
19. Hedner J, Zou D. Turning Over a New Leaf-Pharmacologic Therapy in Obstructive Sleep Apnea. Sleep Med Clin. 2022;17(3):453-469.
20. Eckert DJ, White DP, Jordan AS, Malhotra A, Wellman A. Defining phenotypic causes of obstructive sleep apnea. Identification of novel therapeutic targets. Am J Respir Crit Care Med. 2013;188(8):996-1004.
21. Op de Beeck S, Vena D, Mann D, et al. Polysomnographic airflow shapes and site of collapse during drug-induced sleep endoscopy. European Respiratory Journal. 2024;63(6):2400261.
22. Sweetman A, Lack L, Bastien C. Co-Morbid Insomnia and Sleep Apnea (COMISA): Prevalence, Consequences, Methodological Considerations, and Recent Randomized Controlled Trials. Brain Sciences. 2019;9(12):371.
23. Thorshov TC, Overby CT, Hansen DD, et al. Experience with the use of a digital sleep diary in symptom management by individuals with insomnia -a pilot mixed method study. Sleep Med X. 2023;6:100093.
24. Thorshov TC, Dammen T, Moen A, Einvik G, HrubosStrøm H. Prevalence of insomnia and feasibility of a nurse-administered digital cognitive behavioural therapy two years after corona virus disease hospitalisation. Sleep medicine. 2024;125:108-113.
25. Helsedirektoratet. Nasjonal strategi for pasienttilpasset medisin i helsetjenesten. In. Oslo2016.
26. Qi Y, Zhao Y, Yan Y, Wu D. Surgical failure guided by DISE in patients with obstructive sleep apnea: a systematic review and meta-analysis. Eur Arch Otorhinolaryngol. 2024.
27. Francia C, Lugo R, Moffa A, et al. Defining Epiglottic Collapses Patterns in Obstructive Sleep Apnea Patients: Francia-Lugo Classification. Healthcare. 2023;11(21):2874.
28. Cammaroto G, Bettini P, Meccariello G, et al. Barbed Repositioning Pharyngoplasty: Tips and Tricks. Otolaryngology--head and neck surgery : official journal of American Academy of Otolaryngology-Head and Neck Surgery. 2024;170(4):1204-1207.
29. Bengtsson C, Grote L, Ljunggren M, Ekström M, Palm A. Nasal polyposis is a risk factor for nonadherence to CPAP treatment in sleep apnea: the population-based DISCOVERY study. J Clin Sleep Med. 2023;19(3):573579.
30. Kempfle JS, BuSaba NY, Dobrowski JM, Westover MB, Bianchi MT. A cost-effectiveness analysis of nasal surgery to increase continuous positive airway pressure adherence in sleep apnea patients with nasal obstruction. The Laryngoscope. 2017;127(4):977983.
31. Sweetman A. Co-morbid Insomnia and Sleep Apnoea (COMISA): Latest Research from an Emerging Field. Current Sleep Medicine Reports. 2023;9(3):180-189.
2025 -02 -17

En betydelig andel pasienter med klinisk angina pectoris har ikke signifikante koronare stenoser ved koronar angiografi og er derfor ikke aktuelle for revaskularisering. Mange av disse pasientene vurderes heller ikke som syke uten angiografifunn. I denne artikkelen presenteres en oppdatert oversikt over angina med ikke-obstruktiv koronarsykdom (engelsk: angina with nonobstructive coronary arteries, ANOCA).
Erik Madssen, overlege, PhD, Klinikk for hjertemedisin, St.Olavs hospital og førsteamanuensis, Institutt for sirkulasjon- og bildediagnostikk, NTNU
Introduksjon
Den patofysiologiske forståelsen av kronisk koronarsyndrom har økt betydelig de siste årene. Koronar iskemi er tradisjonelt oppfattet som en stenosesykdom på aterosklerotisk grunnlag. Nå defineres kronisk koronarsyndrom som «ulike kliniske presentasjoner eller syndromer som oppstår på grunn av strukturelle og/ eller funksjonelle endringer relatert til kroniske sykdommer i koronararteriene og/eller mikrosirkulasjonen» (1). Utvikling av ateromatøse stenoser som begrenser blodstrøm i koronarkar er fortsatt den viktigste mekanismen for koronariskemi, men også andre anatomiske forhold, samt funksjonelle forstyrrelser i arterieog endotelfunksjon står sentralt ( Tabell 1).
Ved angina med ikke-obstruktiv koronarsykdom (ANOCA) er det flere potensielle patofysiologiske
mekanismer som bidrar til iskemi og symptomer. Koronar mikrovaskulær dysfunksjon (engelsk: CMD) står sentralt og inkluderer både endoteldysfunksjon, hyperreaktivitet i vaskulære glatte muskelceller og autonom dysregulering i prearterioler, arterioler og kapillærer (2). Dette medfører nedsatt vasodilatasjon og/eller økt vasokonstriksjon i den koronare mikrosirkulasjonen, redusert blodtilførsel til myokard og således iskemi. Mikrovaskulær angina referer til den kliniske manifestasjonen av myokardiskemi på grunn av CMD. CMD er også anerkjent som en viktig patofysiologisk mekanisme ved andre kardiale tilstander som Takotsubo syndrom (3) og hjertesvikt med bevart ejeksjonsfraksjon (4).
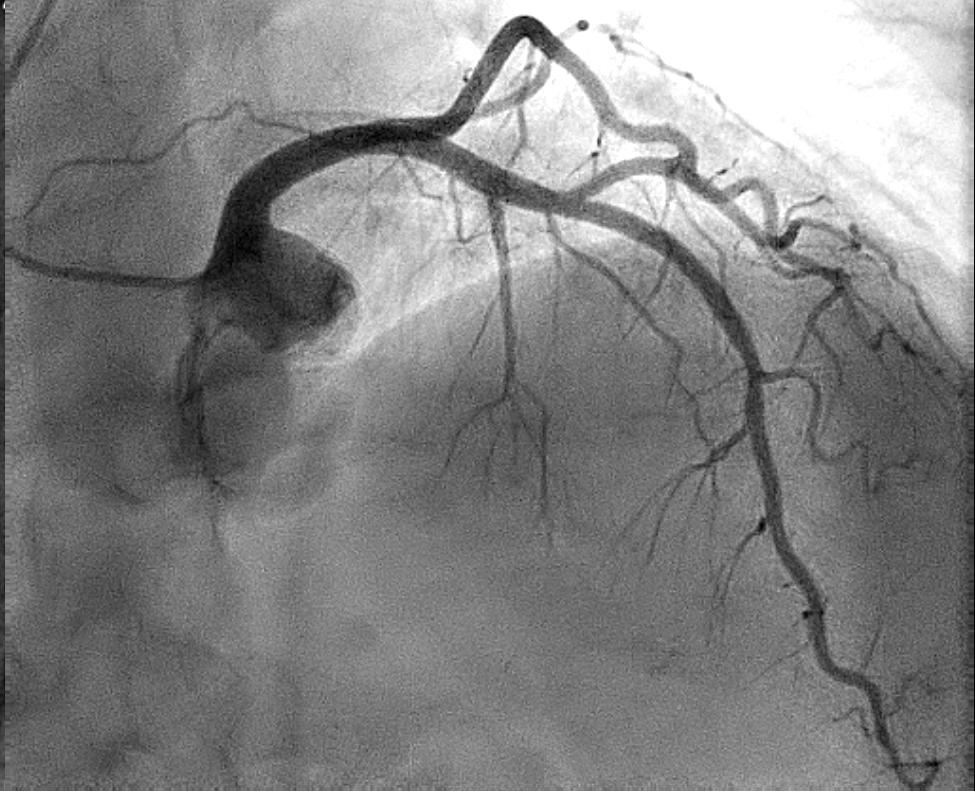
Det er vanlig at ANOCA-pasienter har ikke-signifikante aterosklerotiske plakk i epikardielle arterier ved CT
Tabell 1. Mekanismer ved myokardiskemi.
koronarkar eller koronar angiografi (Figur 1). Dersom man er usikker på om disse forandringene har betydning for koronar blodstrøm, bør det gjøres intrakoronar trykkmåling. Det er heller ikke uvanlig at pasienter som tidligere er revaskularisert har vedvarende symptomer der fornyet utredning viser åpne stenter eller bypassgraft. I slike tilfeller må man mistenke CMD som årsak til symptomene. ANOCA oppstår således over hele spekteret av aterosklerotisk sykdom. Spasmeangina som forårsakes av makrovaskulær spasme i epikardielle arterier inkluderes også i ANOCA-gruppen. Dette er en pasientgruppe som kan være vanskelig å diagnostisere der anamnesen som regel skiller seg fra andre pasienter med kronisk koronarsyndrom (5). Spasmeangina omtales derfor i et eget punkt senere.
Sentrale patofysiologiske mekanismer som fører til myokardiskemi ved kronisk koronarsyndrom
Makrovaskulære
Strukturelle
• Aterosklerose
• Intramuralt hematom
• Myokardiell «brigde»
• Koronararterieaneurysme
Funksjonelle
• Epikardielle vasospasmer
Mikrovaskulære
Strukturelle
• Remodellering i arterioler
• Redusert kapillær tetthet («rarefaction»)
• Mikrovaskulær embolisering («plugging»)
• Perivaskulær fibrose
• Ekstramural kompresjon, f.eks. ved venstre ventrikkelhypertrofi
Funksjonelle
• Redusert vasodilatasjon pga. endoteldysfunksjon eller hyperreativitet i vaskulære glatte muskelceller
• Økt vasokonstriksjon pga. autonom dysregulering
Figuren er bearbeidet basert på data fra European Society of Cardiology retningslinjer for kronisk koronarsyndrom (1).
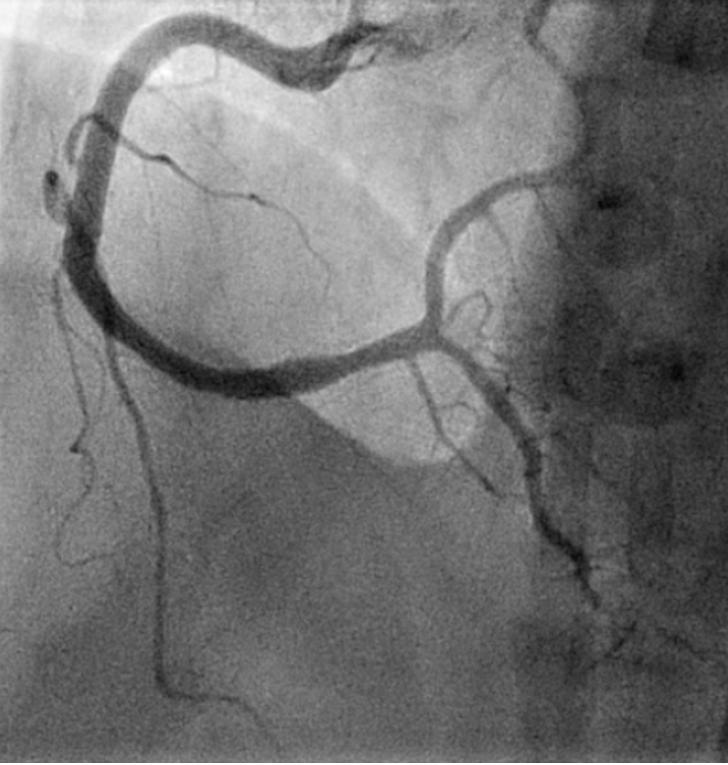
Det er et klart behov for nye studier med mange pasienter som kan undersøke effekten av ulike intervensjoner på mortalitet, kardiovaskulære hendelser og livskvalitet i denne potensielt store pasientgruppen.
Identifisering av pasienter med ANOCA
Hos pasienter med persisterende anginasymptomer etter at obstruktiv koronarsykdom er utelukket ved CT koronarkar eller koronar angiografi bør man mistenke ANOCA. Dette er potensielt en betydelig andel pasienter. I et stort amerikansk materiale som inkluderte nesten 400 000 pasienter var det kun 37.6 % av pasientene som var henvist til koronar angiografi som hadde signifikante koronare stenoser (6). I tilfeller der det var påvist iskemi ved non-invasiv stresstest før angiografi (som f.eks. myokardscintigrafi) økte andelen pasienter med koronare stenoser fra 35 % til 41 %. Et relevant spørsmål blir derfor hvor stor andel av pasienter med ikke-obstruktiv koronarsykdom som faktisk har koronariskemiske symptomer og således ANOCA. Dette mangler man gode tall på. Tidligere studier har vist at opptil 75-90 % av selekterte pasienter med mistenkt ANOCA basert på symptombildet får påvist CMD eller
epikardiell spasme (7). Per nå gjøres slik testing ikke rutinemessig ad hoc i forbindelse med koronar angiografi, men det er aktuelt å vurdere ved en eventuell ny henvisning fordi pasienten har persisterende symptomer.
Før man vurderer ANOCA som aktuell diagnose hos pasienter med persisterende symptomer, er det sentralt å gjennomgå anamnesen på nytt for å vurdere om det er sannsynlig at pasientens symptomer er forårsaket av myokardiskemi. Dette kan være utfordrende. Majoriteten av pasientene har klemmende eller sviende brystsmerter som utløses av fysisk aktivitet eller psykisk stress, men hvilesmerter og andre anginaekvivalente symptomer som funksjonsdyspnoe kan også foreligge. Sistnevnte gruppe er særlig krevende og gjennomgår ofte mange undersøkelser i spesialisthelsetjenesten. Et klinisk poeng er at nitroglycerin til anfallskupering har dårligere effekt hos ANOCA-pasienter enn hos pasienter med obstruktiv koronar-
sykdom, spesielt ved CMD og mikrovaskulær spasme (8). Risikofaktorer for CMD er de samme som for obstruktiv koronarsykdom, med unntak av kjønn, der risikoen for obstruktiv koronarsykdom er høyere hos menn og risikoen for CMD er høyere hos kvinner (9).
Etter en vurdering av pasientens symptomer, bør det vurderes om tidligere utredning med tanke på obstruktiv koronarsykdom er tilfredsstillende, eller om denne bør gjentas. Det er også nyttig å se om det tidligere er påvist myokardiskemi ved non-invasiv testing som f.eks. myokardscintigrafi. Dersom dette er tilfellet, vil det styrke mistanken om ANOCA betydelig, selv om en definitiv diagnose krever ytterligere diagnostikk (10). Dersom muligheten for ANOCA nevnes i henvisningen til invasiv utredning, øker sjansen for at videre utredning med tanke på denne tilstanden gjøres i forbindelse med undersøkelsen.
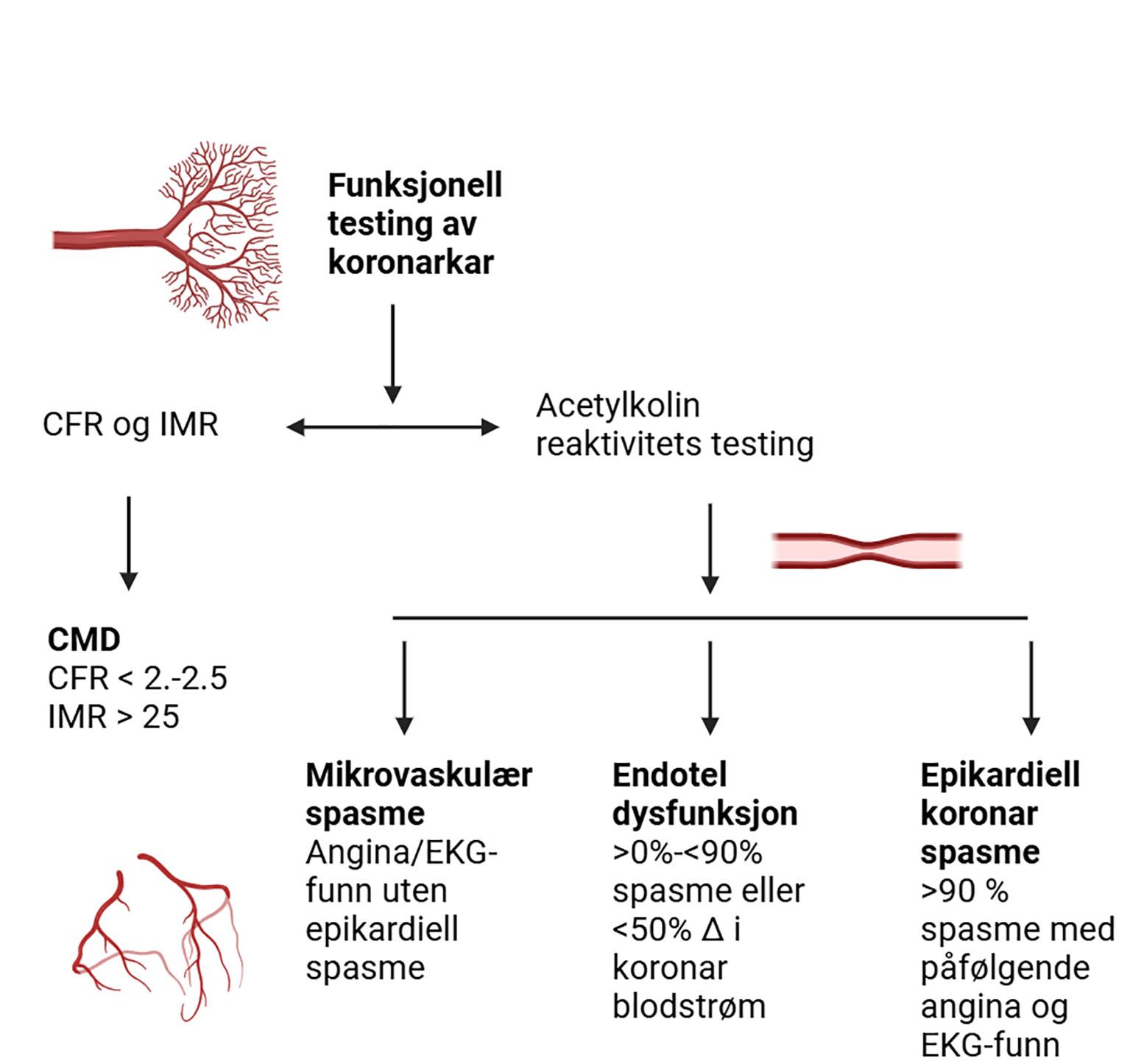
Figur 2. Invasiv testing av ANOCA. IMR = index of myocardial resistance; CMD = koronar mikrovaskulær dysfunksjon; CFR = koronar flow-reserve. EKG-funn refererer til iskemiske endringer i ST-T segmentet. Figur laget med BioRender ®
Aktuell utredning
For å kunne avgjøre om pasienter med anginasymptomer i fravær av obstruktiv koronarsykdom har ANOCA, er det nødvendig å påvise redusert koronar flow-reserve (for holdet mellom maksimal flow og basalflow i et koronarkar) eller induserbar mikrovaskulær- eller makrovaskulær spasme. Invasiv testing hos pasienter med persisterende symptomer og redusert livskvalitet har nå en klasse IB-anbefaling i de nye europeiske retningslinjene for kronisk koronarsyndrom (1). Ved invasiv testing kan man skille mellom ulike patofysiologiske mekanismer (Figur 2) og således potensielt tilby individualisert behandling.
Invasiv utredning av ANOCA inkluderer først en konvensjonell koronar angiografi etterfulgt av validerte tester for CMD, mikrovaskulær spasme, endotel-
dysfunksjon og epikardiell spasme. Testing for CMD gjennomføres først med en endotel-uavhengig vasodilator (som regel adenosin) for å indusere maksimal hyperemi i koronarkar, etterfulgt av testing for endoteldysfunksjon og vasospasme som gjøres med en endotelavhengig vasodilator (som regel acetylkolin i gradvis økende doser). Per nå er Coroflow Cardiovascular System (Coroventis, Abbott) det eneste kommersielle systemet som er tilgjengelig for å måle både trykk og blodstrøm i koronarkar. En fullstendig gjennomgang av testprotokollen er tidligere publisert (11) og omtales ikke her, men kort oppsummert gir systemet informasjon vedrørende to validerte indekser for CMD; koronar flowreserve (CFR) og index of myocardial resistance (IMR). Det er viktig å være klar over at CFR også påvirkes av epikardiell patologi, mens IMR er mer spesifikk for mikrovaskulære forhold.
Tolking av testresultater krever derfor erfaring.
Behandling
Den optimale behandlingen av pasienter med ANOCA er fortsatt omdiskutert på grunn av den heterogene pasientgruppen og mangel på store randomiserte studier. Det er derfor knyttet spenning til resultatene fra pågående større behandlingsstudier (12). Et viktig poeng er at pasienter med ANOCA ofte har flere kardiovaskulære risikofaktorer og bør få råd om livsstilstiltak på samme linje som pasienter med obstruktiv koronarsykdom. Dette inkluderer en klar anbefaling om røykestopp, vektreduksjon ved overvekt eller fedme, samt regelmessig fysisk aktivitet. Erfaringsmessig er det enklere å gi slike råd, og pasientene er mer motiverte når det foreligger påvist patologi ved invasiv testing.
Basert på data fra mindre studier bør medikamentell behandling ved CMD starte med en betablokker (13), ACE-hemmer (14, 15) og statin (16). Behandlingsmål for LDL-reduksjon er ikke godt definert og avhenger av om det er påvist aterosklerose i koronarkar eller andre kargebeter i tillegg. Andrelinje medikamenter inkluderer kalsiumkanalblokkere og ranolazine, hvorav sistnevnte ikke er markedsført i Norge. Mange pasienter bruker også langtidsvirkende nitroglyserinpreparater, men dette er kun anbefalt ved refraktær angina der andre medikamenter er forsøkt. Mer eksperimentell behandling inkluderer ivabradine, L-arginine og phosfodiesterase type-5 inhibitorer (8). Ved endoteldysfunksjon og mikrovaskulær spasme er førstelinjebehandlingen statiner og kalsiumkanalblokkere. Det foreligger få behandlingsstudier i denne pasientgruppen.
Spasmeangina
Pasienter med klassisk spasmeangina får brystsmerter i hvile da tilstanden ikke er assosiert med økt oksygenbehov til myokard. Den opprinnelige publikasjonen fra Prinzmetal beskriver likevel at fysisk aktivitet (varm fase) er trigger hos enkelte pasienter, og at anfall er hyppigere på natt og tidlig morgen (17). Risikofaktorer for tilstanden
Basert på data fra mindre studier bør medikamentell behandling ved koronar mikrovaskulær dysfunksjon starte med en betablokker, ACE-hemmer og statin.
inkluderer røyking, hypomagnesemi, genetisk predisposisjon og systemiske inflammatoriske tilstander (5). Migrene og Raynauds fenomen er identifisert som assosierte tilstander.
Ved mistenkt spasmeanging er det sterkt anbefalt å ta EKG under anfall. Ved hyppige anfall eller ved en kjent trigger kan man også vurdere HolterEKG i et forsøk på å fange dynamiske EKG-forandringer under anfall. Erfaringsmessig er EKG-diagnostikk vanskelig å få til. For en definitiv diagnose spasmeangina, skal alle tre følgende kriterier være oppfylt: 1) nitratresponsiv angina med minst é n av følgende a) hvileangina, b) døgnvariasjon, c) trigger i form av hyperventilasjon eller d) symptomlindring med kalsiumkanalblokker, 2) EKGforandringer under anfall med angina og 3) dokumentert koronarspasme > 90 % under provokasjonstesting eller spontant (18). Hos pasienter med mistenkt spasmeangina og gjentagende episoder med angina i hvile assosiert med ST-forandringer i EKG og som lindres av nitroglyserin eller kalsiumblokker er det en klasse IC-anbefaling for invasiv testing (1).
Referanser
Dette gjøres både for å bekrefte diagnosen og samtidig påvise underliggende koronarsykdom, da kombinasjonen av spasmeangina og obstruktiv koronarsykdom har en dårligere prognose.
Behandling av spasmeangina inkluderer kalsiumkanalblokkere og anfallskuppering med nitroglyserin (8). Det er ikke uvanlig at enkelte pasienter krever høyere doser kalsiumkanalblokker enn det som brukes ved f.eks. hypertensjon. Enkelte argumenterer for at pasienter med spasmeangina også skal behandles med statiner da det ofte foreligger endoteldysfunksjon. Langtidsvirkende nitroglyserin eller en kombinasjon av to ulike kalsiumkanalblokkere (dihydropyridiner og non-dihydropyridiner) er anbefalt som andrelinjebehandling. Kronisk bruk av langtidsvirkende nitroglycerin er assosiert med toleranseutvikling, og pasienter kan få økt vasokonstriksjon ved seponering. Data fra flere retrospektive kohorter antyder også økt forekomst av kardiovaskulære hendelser hos pasienter med spasmeangina som har brukt lang -
1. Vrints C, Andreotti F, Koskinas KC et al. 2024 ESC Guidelines for the management of chronic coronary syndromes. Eur Heart J 2024;00:1-123.
2. Del Buono MG, Montone RA, Camilli M et al. Coronary Microvascular Dysfunction Across the Spectrum of Cardiovascular Disease. J Am Coll Cardiol 2021;78:352-1371.
3. Pellicia F, Kaski JC, Crea F et al. Pathophysiology of Takutsubo syndrome. Circulation 2017;135(24):2426-2441.
4. Shah SJ, Lam CSP, Svedlund SJ et al. Prevalence and correlates of coronary microvascular dysfunction in heart failure with preserved ejection fraction: PROMIS-HFpEF. Eur Heart J 2018;39(37):3439-3450.
5. Jenkins K, Pompei G, Ganzorig N et al. Vasospastic angina: a review of diagnostic approach and management Ther Adv Cardiovasc Dis 2024;18:1-17.
6. Patel MR, Peterson ED, Dai D et al. Low diagnostic yield of elective coronary angiography. N Engl J Med 2010;362:886-895.
7. Samuels BA, Shah SM, Widmer RJ et al. Comprehensive Management of ANOCA, Part 1 – Definition, Patient Population, and Diagnosis J Am Coll Cardiol 2023;82:1245-1263.
8. Smilowitz NR, Prasad M, Widmer JR et al. Comprehensive Management of ANOCA, Part 2 – Program Development, Treatment,
tidsvirkende nitroglyserin (19). Bruken bør derfor begrenses hos denne pasientgruppen. Betablokkere kan potensielt øke koronar vasomotorisk tonus og bør også brukes med forsiktighet ved spasmeangina.
Fremtidsperspektiver Selv om ANOCA nå er inkludert i oppdaterte retningslinjer for kronisk koronarsyndrom er det et klart behov for økt kunnskap om denne pasientgruppen. Dette gjelder ikke minst standardisering av data som registreres og inkluderes i randomiserte studier der invasiv testing er nødvendig for å identifisere ulike subgrupper av pasienter. En spesiell utfordrende gruppe er pasienter med mikrovaskulær spasme og endoteldysfunksjon. Behandlingen hos slike pasienter må individualiseres og dette krever kunnskap og engasjement hos behandlende lege. Det er et klart behov for nye studier med mange pasienter som kan undersøke effekten av ulike inter vensjoner på mortalitet, kardiovaskulære hendelser og livskvalitet i denne potensielt store pasientgruppen.
and Research Initiatives J Am Coll Cardiol 2023;82:1264-1279.
9. Anderson RD, Petersen JW, Mehta PK et al. Prevalence of coronary endothelial and microvascular dysfunction in women with symptoms of ischemia and no obstructive coronary artery disease is confirmed by a new cohort: the NHLBI-sponsored Women’s Ischemia Syndrome Evaluation-Coronary Vascular Dysfunction (WISE-CVD) J Interven Cardiol 2019;2019:7169275.
10. Ong P, Camici PG, Beltrame JF et al. International standardization of diagnostic criteria for microvascular angina Int J Cardiol 2018;250:16-20.
11. Collet C, Yong A, Munhoz D et al. A Systematic Approach to the Evaluation of the Coronary Microcirculation Using Bolus Thermodilution: CATH CMD JSCAI 2024;3(7):101934.
12. Handberg EM, Merz CNB, Cooper-Dehoff RM et al. Rationale and design of the Women’s Ischemia Trial to Reduce Events in Nonobstructive CAD (WARRIOR) trial Am Heart J 2021;237:90103.
13. Di Franco A, Vilano A, Di Monaco A et al. Correlation between coronary microvascular function and angina status in patients with stable microvascular angina Eur Rev Med Pharmacol Sci 2014;18:374-379.
14. Chen JW, Hsu NW, Wu TC et al. Long term angiotensin-converting enzyme inhibition reduces plasma asymmetric dimethylar-
ginine and improves endothelial nitric oxide bioavailability and coronary microvascular function in patients with syndrome X. Am J Cardiol 2002;90:974-982.
15. Pauly DF, Johnson BD, Anderson RD et al. In women with symptoms of cardiac ischemia, non-obstructive coronary arteries, and microvascular dysfunction, angiotensin-converting enzyme inhibition is associated with improved microvascular function: a double-blind randomized study from the National Heart, Lung and Blood Institute Women’s Ischemia Syndrome Evaluation (WISE) Am Heart J 2011;162:678-684.
16. Eshtehardi P, McDaniel MC, Dhawan SS et al. Effect of intensive atorvastatin theraphy on coronary atherosclerosis progression, composition, arterial remodelling, and microvascular function J Invasive Cardiol 2012;24:522-529.
17. Prinzmetal M, Kennamer R, Merliss R et al. Angina pectoris. I. A variant form of angina pectoris; preliminary report. Am J Med 1959;27:375-388.
18. Beltrame JF, Crea F, Kaski JC et al. International standardization of diagnostic criteria for vasospastic angina Eur Heart J 2017;38:2565-2568.
19. Takahashi J, Nihei T, Takagi Y et al. Prognostic impact of chronic nitrate therapies on long-term clinical outcomes of patients with vasospastic angina: multicentre registry of the Japanese coronary spasm association Eur Heart J 2015;36:228-237.

Artikkelen gjennomgår viktige generelle aspekter, og tar spesielt for seg vurdering og kvantifisering av albuminuri ved hjelp av albumin-kreatinin-ratio i urin.
Sihaam Yasin Ibrahim Ali1, Rannveig Skrunes 2 og Hans-Peter Marti2,3
1 Medisinstudent, Universitetet i Bergen.
2 Overlege, Nefrologisk seksjon, Medisinsk klinikk, Haukeland universitetssykehus.
3 Professor i nefrologi, Universitetet i Bergen.
Introduksjon
Proteinuri med eller uten hematuri er et vanlig funn som vi kan se i allmennpraksis, i poliklinisk setting eller hos innlagte sykehuspasienter (1, 2). Isolert proteinuri, særlig albuminuri, kan være et tegn på tidlig nyresykdom, men også generelle kardiovaskulære skader, spesielt i forbindelse med diabetes og hypertensjon (3). Når vi ser redusert nyrefunksjon i blodprøvene (kreatinin og eGFR), er allerede store deler av nyrevevet gått tapt, Figur 1.


Med medikamenter kan vi forsinke, og til og med stoppe utviklingen av begynnende nyreskade - om den oppdages tidlig nok. Kvantitering av albuminuri ved urinstix er en grov, og ofte unøyaktig målemetode. Når urin albumin-kreatinin-ratio (AKR) utføres, deles albuminfraksjon på urin kreatinin, som gir en mer nøy aktig vurdering av grad av tap av albumin i urinen. Metoden er pålitelig i spoturin, og gjør døgnsamling av urin unødvendig. Hvis det i tillegg til albuminuri også kan påvises hema turi, støtter det mistanken om nyre sykdom (1, 4).
Betydning og forekomst av albuminuri
Proteinuri, særlig albuminuri, er ofte første tegn til nyreskade (5), og kan oppstå allerede før kreatinin stiger og eGFR faller (Figur 1). Forhøyet utskillelse av albumin i urinen kan også indikere generell karsykdom, inkludert hjertesykdom (6).
Proteinuri defineres som funn av proteiner i urinen, utover det som ansees som normalt (7). Kun små mengder proteiner – særlig de minste plasmaproteinene som albumin – vil bli filtrert gjennom filtrasjonsbarrieren i en normal glomerulus. Disse proteinene vil reabsorberes i proksimale tubuli i en sunn nyre. Ved glomerulære skader øker proteinurien, særlig albuminurien, betydelig. Pasienter med nefrotisk syndrom viser tap av albumin, men også av immunglobuliner og andre plasmaproteiner i urinen. Hos en frisk person
vil det meste av utskilte proteiner komme fra tubulusceller, de såkalte Tamm-Horsfall proteiner.
Lavgradig albuminuri med forhøyet AKR kan sees før urin proteinkreatinin-ratio (PKR) begynner å stige. Forhøyet urin-AKR er en prognostisk skademarkør angående endotelskade, særlig for glomerulær nyreskade, og benyttes sammen med urin-PKR som ledd i utredning av nyresykdom, diabetes og hjerte- og karsykdom, inkludert hypertensjon. Tabell 1 viser prognose for kronisk

Figur 1. Utvikling av proteinurisk (albuminurisk) nyresykdom. Albuminuri (økt AKR) oppstår før detekterbar nyresvikt (nedsatt eGFR og økt kreatinin). Viktige risikofaktorer er diabetes, hjertesykdom, karsykdom, fedme, høyt blodtrykk og positiv familiehistorie. AKR: Albumin-kreatinin-ratio, eGFR: estimert glomerulær filtrasjonsrate.
nyresykdom basert på estimert glomerulær filtrasjonsrate (eGFR) og albuminurikategorier (5, 8).
Proteinuri eller albuminuri trenger ikke alltid å være patologisk, og kan noen ganger være forbigående. Vi kan eksempelvis se tilfeller av proteinuri ved hard fysisk aktivitet, urinveisinfeksjoner, feber, eller dersom urinen er forurenset av vaginalsekret. Vedvarende proteinuri og albuminuri er imidlertid et tegn på nyresykdom, og må undersøkes videre (9, 10).
Tilstedeværelsen av både proteinuri/ albuminuri og hematuri gir mistanke om nyrepatologi som glomerulonefritt (f.eks. IgA-nefropati) eller systemiske sykdommer som vaskulitt eller autoimmun sykdom. Hematuri diagnostiseres vanligvis ved bruk av urinstrimmel, som i en sykehussetting ideelt sett bekreftes med urinmikroskopi. Protein-/albuminuri med samtidig hematuri er forbundet med dårligere prognose og risikoen for tap av nyrefunksjon over tid øker. Ved nefrotiske tilstander med hematuri som minimal change disease, fokal og segmental glomerulosklerose eller membranøs nefropati kan sannsynligheten for komplett remisjon av proteinuri reduseres (11).
AKR er avgjørende når det gjelder vurdering av pasienter med nyre sykdom relatert til diabetes. Pasienter med diabetes er også en viktig gruppe angående utvikling av hematuri med samtidig albuminuri. En studie har vist at hematuri forekommer hyppigere hos pasienter med diabetes type 2 med forhøyet AKR, spesielt moderat/ alvorlig albuminuri, sammenlignet med pasienter med normal/moderat albuminutskillelse (12).
Hvorfor er AKR bedre enn PKR eller urinstrimmel?
Hva skal man måle i urinen: protein (totalprotein) eller albumin? Med tanke på tidlig nyresykdom, spesielt ved diabetes og hjerte- karsykdommer (inkludert hypertension) er albumin best (6, 10). AKR har større sensitivitet for lave nivåer av protein-
Tabell 1: Prognose for kronisk nyresykdom basert på glomerulær filtrasjonsrate (GFR) og albuminurikategorier (5, 8)
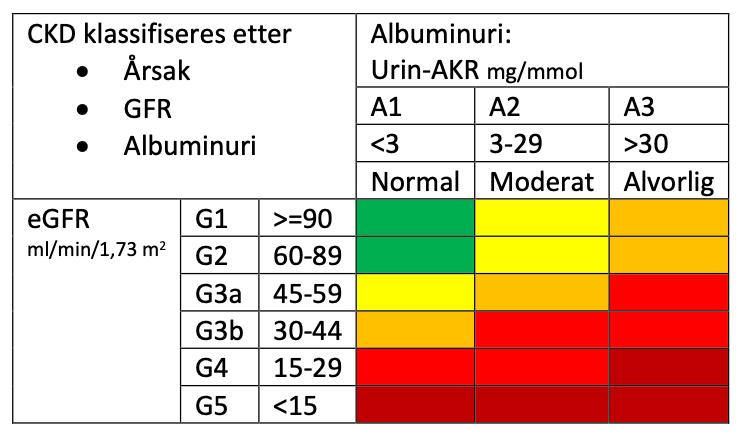
Grønn: lav risiko (hvis ingen andre markører for nyresykdom, ingen kronisk nyresyndom); Gul: moderat økt risiko; Oransje: høy risiko; Rød: svært høy risiko. Figuren er gjengitt (5) med tillatelse fra Norsk Nyremedisinsk Forening. AKR: Albumin-kreatinin-ratio, eGFR: estimert glomerulær filtrasjonsrate.
Grad av proteinuri Normal (-mild) Moderat Alvorlig
Spot urin AKR <3 mg/mmol 3-29 mg/mmol >30 mg/mmol
Spot urin PKR <15-30 mg/mmol ca. 30-300 mg/mmol >300-500 mg/mmol
Urinstrimmel spor - 1+ 1+ ≥2+
Definisjonen av normale/patologiske verdier for proteinuri er generelt mindre veldefinerte enn for albuminuri. Ved bruk av urinstix avhenger resultatene av type urinstrimmel (f. eks. skalering) og konsentrasjonen av urinprøven. AKR: albuminkreatinin-ratio, PKR: protein-kreatinin-ratio (5, 7, 8).
uri enn PKR (13). Proteinkvantitering (totalprotein) ved PKR kan ofte ikke oppdage lav/moderat albuminuri (<30 mg/mmol), som er en tidlig markør for nyreskade (14); i tillegg anses PKR verdier av <15-30 mg/mmol for å være normale (Tabell 2) og AKR på 30 mg/mmol tilsvarer omtrent PKR på 50 mg/mmol. Albumin er dessuten hovedkomponenten av protein i urinen ved de fleste nyresykdommer, og epidemiologiske data viser en sterk sammenheng mellom albuminmengden i urin og økt risiko for nyre- og kardiovaskulære sykdommer (8).
En studie viste at median albumintil-protein prosent øker fra <30% ved lav proteinuri (AKR<3 mg/mmol) til >60% ved høy proteinuri (AKR>30 mg/mmol), og at sammenhengen mellom AKR og PKR ble mer lineær med mindre spredning ved høy og spesielt ved nefrotisk proteinuri (15).
Hos pasienter med klinisk betydelig albuminuri (AKR >70 mg/mmol), særlig nefrotisk albuminuri, vil PKR derfor alltid være påvirket (13, 15).
Måling av AKR er anbefalt, og foretrukket fremfor PKR, i nefrologiske retningslinjer (5, 8). I tillegg til en bedre standardisering av AKR, har AKR bedre og mer etablert prediktiv verdi for kardiovaskulære og renale utfall sammenlignet med PKR. Ved noen sjeldne tilstander (f.eks. lettkjedesykdom og myelomatose pluss noen ganger ved tubulointerstitiell nefritt) kan ikke-albumin dominere i urinen, men dette er unntak. Ved disse tilstandene kan man ha nytte av å måle både AKR og PKR hvor man da vil se at PKR >> AKR , men lettkjedesykdom og myelomatose krever spesifikk måling av paraproteiner, inkludert lette kjeder, i urinen.
Tabell 3. Viktige indiksjoner for bruk av AKR som diagnostisk, terapeutisk og/eller prognostisk biomarkør.
Viktige indikasjoner for AKR-måling
Kronisk eller akutt nyresykdom (inkl. positiv familie historie)
Hjertesykdom
Diabetes type I og II
Hypertensjon
Karsykdom
Systemiske sykdommer med potensiell nyrepåvirkning - for eksempel systemisk lupus erythematosus (SLE)
Overvekt/fedme (BMI>30)
Påvisning av hematuri
Vurdering av behandlingseffekt mot albuminuri
AKR: albumin-kreatinin-ratio.
AKR-testen måler mengde albumin i urinen i forhold til mengde kreatinin i en spoturinprøve. Forholdet mellom disse gir et pålitelig estimat av albuminutskillelsen, justert for urinkonsentrasjon som reflekteres av kreatininkonsentrasjonen. Urinsamling i en definert tidsperiode blir unødvendig. Derfor er AKR mer pålitelig enn enkle urinstrimmelanalyser som ikke tar hensyn til urinkonsentrasjonen direkte. Det samme gjelder for PKR-analysen.
I tillegg er urinstrimmelen ofte ikke sensitiv nok til å detektere lavgradig/ moderat albuminuri (AKR <30 mg/ mmol kreatinin), særlig ved lav urin-osmolalitet (7, 16). En nylig undersøkelse fant imidlertid at svært få pasienter med unormale urinstrimmelresultater fikk oppfølging med kvantifisering av albuminuri som anbefalt av kliniske retningslinjer (17).
I enkelte tilfeller kan man benytte seg av en presis 24-timers urinprøve for mer nøyaktige målinger, men generelt sett er det mer hensiktsmessig å benytte seg av AKR eller PKR basert på spoturin (4). En nylig studie som sammenligner AKR, PKR og 24-timers urinsamling ved kronisk nyresykdom som IgA-nefropati viser at AKR er best som prognostisk faktor (18).
Hvordan måle albuminuri med AKR?
Grad av albuminuri er stillingsavhengig. I samsvar med internasjonale anbefalinger og retningslinjer brukes derfor fortrinns-
vis første gangs morgenurinprøve for å estimere utskillingen av protein - særlig albumin - med hjelp av AKR og/eller PKR (5, 6, 8). Om første eller andre gangs morgenurin ikke er mulig, er ofte en spoturinprøve på tilfeldig tidspunkt akseptabelt (7, 8). Bekreftelse bør gjøres ved hjelp av en påfølgende morgenurin når AKR er omtrent mellom 3-70 mg/mmol på et slikt tilfeldig tidspunkt (13). Hvis to av tre prøver har forhøyet AKR i løpet av tre måneder eller mer, har pasienten påvist forhøyet albuminuri (19).
Døgnutskilling av kreatinin er omtrent 10 mmol hos voksne, man kan dermed få et omtrentlig estimat for protein- eller albuminutskilling per døgn i milligram ved å multiplisere ratioen (PKR eller AKR) med en faktor på 10 (10).
De nøyaktige normale og patologiske verdiene for proteinuri er generelt mindre veldefinert enn for albuminuri. En protein- eller albuminutskillelse på ≥150-200 mg eller ≥30 mg i løpet av 24 timer (tilsvarende en PKR på ≥1530 mg/mmol og AKR ≥3 mg/mmol) ansees som unormalt; se Tabell 2. Ved betydelig forhøyet AKR (≥300 mg/mmol) - omtrent tilsvarende til PKR >300-500 mg/mmol - handler det om en nefrotisk albuminuri (proteinuri) som er et sikkert tegn på glomerulær skade (8, 10, 20).
Indikasjon for å måle albuminuri med AKR Klinisk forskning viser til at AKR selv innenfor normalområdet ikke bare har god prediktiv verdi for kardio -
vaskulære og renale utfall, men også for generell overlevelse, «all causemortality». Dette underbygger betydningen til AKR, da forhøyet AKR kan benyttes til å identifisere pasienter med forhøyet risiko for både nyresykdom og kardiovaskulær sykdom tidlig (6, 21).
Proteinuri og albuminuri indikerer nyreskade, og graden av proteinuri/ albuminuri er ofte sammenhengende med alvorlighetsgraden av nyreskaden. Denne sammenhengen kan brukes til å overvåke videre sykdomsforløp.
Beregning av AKR burde utføres rutinemessig, særlig hos pasienter med hjertekarsykdom (inkludert hypertensjon), diabetes, øket risiko for nyresykdom, pluss hos pasienter med allerede kjent nyresykdom, som beskrevet i Tabell 3. Monitorering av AKR kan eksempelvis brukes for å vurdere effekt av tiltak mot albuminuri. Risikofaktorer for nyresykdommer inkluderer blant annet diabetes, hypertensjon, hjertesvikt, karsykdom, fedme (BMI>30) og positiv familiehistorie for nyresykdom (3, 20).
AKR er også viktig ved utredning av akutt eller subakutt nyreskade i sykehus. Albuminuri, spesielt med samtidig mikroskopisk hematuri, er et tydelig tegn på glomerulær skade. Ved debut av en akutt glomerulonefritt (f.eks. post-streptokokk glomerulonefritt), systemiske vaskulitter eller autoimmune sykdommer, (f.eks. ANCA-assosiert vaskulitt, anti-GBM sykdom, eller systemisk lupus eryt-
hematosus (SLE)), kan kombinasjonen av forhøyet AKR og mikroskopisk hematuri være det første tegnet på akutt/subakutt nyreskade. Ved diabetesnefropati eller kroniske glomerulonefritter, vil forhøyet AKR og mikroskopisk hematuri være et uttrykk for pågående nyreskade over tid.
Utredning av pasienter med albuminuri ± hematuri
Generelt ved en AKR >30 mg/mmol (A3) anbefales henvisning til nefrolog (5). Ved lav/moderat albuminuri (A1, A2) er det ofte ikke behov for videre henvisning; unntak kan være pasienter med uklar diagnose og pasienter med mistanke om vaskulitt eller autoimmun sykdom.
Faktorer som høy alder, stabil nyrefunksjon, lav/moderat albuminuri (A1, A2) pluss velregulert hypertensjon eller diabetes kan godt indikere langsom progresjon av sykdom og kan derfor håndteres i primærhelsetjenesten (5).
Normale/lave proteinuri- og albuminuriverdier (under referansenivå) kan også være tegn på nyresykdom hos for eksempel pasienter med samtidig hematuri, hypertensjon, diabetes, hjerte/karsykdom -
Referanser
1. Imam AA, Saadeh SA. Evaluation of Proteinuria and Hematuria in Ambulatory Setting. Pediatr Clin North Am. 2022;69(6):1037-49.
2. Pruijm MT, Madeleine G, Riesen WF, Burnier M, Bovet P. Prevalence of microalbuminuria in the general population of Seychelles and strong association with diabetes and hypertension independent of renal markers. J Hypertens. 2008;26(5):871-7.
3. Haider MZ, Aslam A. Proteinuria. StatPearls. Treasure Island (FL)2024. Publishing; 2024 Jan–. PMID: 33232060.
4. Avellino GJ, Bose S, Wang DS. Diagnosis and Management of Hematuria. Surg Clin North Am. 2016;96(3):503-15.
5. Norsk nyremedisinsk forening. Veileder for samhandling om pasienter med kronisk nyresykdom 2024 (updated April 2024). Available from: http://nephro.no/ veileder/CKD_veileder_fastleger_v2%20NNF_NFA_ april_2024.pdf.
6. Barzilay JI, Farag YMK, Durthaler J. Albuminuria: An Underappreciated Risk Factor for Cardiovascular Disease. J Am Heart Assoc. 2024;13(2):e030131.
7. Bergen H. Analyseoversikten: Haukeland universitetssjukehusa; 2019 Available from: https://analyseoversikten.no/analyser/209.
8. Kidney Disease: Improving Global Outcomes CKDWG. KDIGO 2024 Clinical Practice Guideline for the Evaluation and Management of Chronic Kidney Disease. Kidney Int. 2024;105(4S):S117-S314.
9. Johansen IH, Blinkenberg J, Arentz-Hansen C, Moen
mer, vaskulitt, autoimmun sykdom (særlig SLE) med mer (20).
Med tanke på urinstrimmel, kan en positiv test på 1+ eller mer være en god nok indikasjon for videre undersøkelser, inkludert AKR (20).
Personer med forhøyet AKR bør vurderes klinisk med tanke på hypertensjon, perifere ødemer og vaskulitt i hud (4, 9, 10). Videre utredningsprøver bør inkludere kreatinin, eGFR, CRP, albumin, HbA1C, glukose og et vanlig hematogram som et minimum (9). Hos pasienter med mistanke om systemsykdom som årsak til albuminuri/proteinuri, bør det også måles autoantistoffer. Eksempelvis bør PLA2R-antistoff måles ved mistanke om membranøs nefropati, ANCA, ANA, anti-DNA og anti-dsDNA bør måles ved mistanke om ANCAassosiert vaskulitt eller SLE. Ultralyd urinveier og urinmikroskopi er ofte nyttig i utredning av nyresykdom. For å stille en endelig diagnose kan en nyrebiopsi være nødvendig.
Fordi vedvarende albuminuri er en viktig risikomarkør for sykdom, er målrettet behandling viktig. Behandling med ACEI/ARB og SGLT2i er særlig viktig for å bremse tap av nyrefunksjon hos pasienter med
albuminuri og kronisk nyresykdom (5, 8). Forhøyet albuminuri (AKR) kan potensielt reverseres dersom man kommer tidlig til med behandling.
Sammendrag og konklusjon
AKR er et praktisk verktøy for kvantifisering av albuminuri hos pasienter med nyresykdom, diabetes og hjerte- karsykdommer inkludert hypertensjon, med tanke på diagnose, behandling og prognose. AKR kan være forhøyet selv om urinstix er negativ og urin PKR samt eGFR er innenfor normalområdet. Urin AKR i spoturin er derfor en enkel måte å oppdage nyresykdom med proteinuri tidlig (17, 18, 22), slik at utredning og behandling kan startes i rett tid.
Interessekonflikter
Forfatterne oppgir ingen interessekonflikter.
K. Proteinuri: Gyldendal; 2024 (cited 2024). Available from: https://www.lvh.no/symptomer-og-sykdommer/ urinveier-og-nyrer/proteinuri.
10. Hartmann A, Jenssen T, Midtvedt K, Reisaeter AV, Fauchald P, Henriksen T, et al. [Protein-creatinine ratio--a simple method for proteinuria assessment in clinical practice]. Tidsskr Nor Laegeforen. 2002;122(22):2180-3.
11. Marchel D, Trachtman H, Larkina M, Helmuth M, Lai Yee JY, Fermin D, et al. The Significance of Hematuria in Podocytopathies. Clin J Am Soc Nephrol. 2024;19(1):56-66.
12. Shen FC, Lee CT, Sun CK, Chung MS, Lee JJ, Chang HW, et al. Prevalence of haematuria positively associated with urine albumin excretion in Type 2 diabetes. Diabet Med. 2012;29(9):1178-83.
13. NICE guideline NG 203: Chronic kidney disease. August 2021; https://www.nice.org.uk/guidance/ ng203/evidence/b-accuracy-of-albumin-creatinineratio-versus-protein-creatinine-ratio-measurementsto-quantify-proteinuria-inchildren-and-young-peoplewith-ckd-pdf-9204445983.
14. Sumida K, Nadkarni GN, Grams ME, Sang Y, Ballew SH, Coresh J, et al. Conversion of Urine ProteinCreatinine Ratio or Urine Dipstick Protein to Urine Albumin-Creatinine Ratio for Use in Chronic Kidney Disease Screening and Prognosis : An Individual Participant-Based Meta-analysis. Ann Intern Med. 2020;173(6):426-35.
15. Weaver RG, James MT, Ravani P, Weaver CGW, Lamb EJ, Tonelli M, et al. Estimating Urine Albumin-toCreatinine Ratio from Protein-to-Creatinine Ratio:
Development of Equations using Same-Day Measurements. J Am Soc Nephrol. 2020. Mar;31(3):591-601. doi: 10.1681/ASN.2019060605. Epub 2020 Feb 5. Erratum in: J Am Soc Nephrol. 2020 May;31(5):1140. doi: 10.1681/ASN.2020030291. PMID: 32024663; PMCID: PMC7062208.
16. Lim D, Lee DY, Cho SH, Kim OZ, Cho SW, An SK, et al. Diagnostic accuracy of urine dipstick for proteinuria in older outpatients. Kidney Res Clin Pract. 2014;33(4):199-203.
17. Xu Y, Shin JI, Wallace A, Carrero JJ, Inker LA, Mukhopadhyay A, et al. Shortfalls in Follow-up Albuminuria Quantification After an Abnormal Result on a Urine Protein Dipstick Test. Ann Intern Med. 2024. Nov;177(11):1593-1595. doi: 10.7326/ANNALS-24-00549. Epub 2024 Oct 1. PMID: 39348706.
18. Yu G, Cheng J, Li H, Li X, Chen J. Comparison of 24-h Urine Protein, Urine Albumin-to-Creatinine Ratio, and Protein-to-Creatinine Ratio in IgA Nephropathy. Front Med (Lausanne). 2022;9:809245.
19. National kidney foundation. Albuminuria (proteinuria) 2023 [Available from: https://www.kidney.org/kidneytopics/albuminuria-proteinuria.
20. Haynes J, Haynes R. Proteinuria. BMJ. 2006;332(7536):284.
21. Mahemuti N, Zou J, Liu C, Xiao Z, Liang F, Yang X. Urinary Albumin-to-Creatinine Ratio in Normal Range, Cardiovascular Health, and All-Cause Mortality. JAMA Netw Open. 2023;6(12):e2348333.
22. Sethi S, De Vriese AS, Fervenza FC. Acute glomerulonephritis. Lancet. 2022;399(10335):1646-63.




Kronisk nyresykdom øker risiko for osteoporose og benbrudd på grunn av forstyrrelser i ben- og mineralmetabolismen. Tidlig diagnostikk og målrettet behandling kan redusere risikoen for skjelettkomplikasjoner. Artikkelen beskriver underliggende mekanismer, diagnostiske utfordringer og behandlingsmuligheter.
Kiarash Tazmini, Overlege, PhD1, Mikkel Pretorius, Overlege, PhD1,2, Hege K Pihlstrøm, Overlege, PhD 3, Ruth Strømmen, LIS 3 i nefrologi og PhD kandidat 3 1 Endokrinologisk Avdeling, ESF, Oslo Universitetssykehus, 2 Medisinsk Fakultet, Universitetet i Oslo, 3 Nyremedisinsk avdeling, Oslo Universitetssykehus Korrespondanse: Kiarash Tazmini, kiataz@ous-hf.no
Bakgrunn
Osteoporose er en systemisk skjelettsykdom med redusert bentetthet og endringer av benvevets mikroarkitektur, som fører til økt bruddrisiko1. Osteoporotiske brudd er vanlige og affiserer omtrent en av to postmenopausale kvinner samt en av fem menn over 50 år 2 Kronisk nyresykdom (CKD) (tabell 1) er en uavhengig risikofaktor for osteoporose. På verdensbasis er prevalensen av CKD 10-15%, og den øker med økende alder og er vanligere blant kvinner1–3. Pasienter med estimert glomerulær filtrasjonsrate (eGFR) < 60 ml/min har minst dobbelt så høy risiko for osteoporose1, og nyretransplanterte har opptil fire ganger høyere risiko for fraktur sammenlignet med den generelle befolkningen4,5
Patogenese
En ubalanse mellom benformasjon og benresorpsjon starter tidlig ved fallende nyrefunksjon og bentapet er multifaktorielt1. Begrepet CKD- MBD (mineral-og bensykdom ved CKD) ble innført av den globale nyreorganisasjonen KDIGO i 2005, for å synliggjøre at det dreier seg om en systemisk patologisk tilstand karakterisert av forstyrrelser i blant annet kalsium og fosfat-metabolismen, skjelettpatologi og kalsifisering av kar og bløtvev (figur 1 og 2). I tillegg til å øke risiko for benbrudd, resulterer CKD-MBD i økt risiko for kardiovaskulære hendelser og økt mortalitet1–3
Sekundær hyperparatyreoidisme ved CKD er en følge av lave nivåer av aktivt vitamin D, økende fibroblast vekstfaktor 23 (FGF-23), hypokalsemi og hyperfosfatemi7. Tertiær hyperparatyreoidisme ( persisterende høy PTH og hyperkalsemi) skyldes
1 Nyreskade med normal GFR ≥ 90
2 Nyreskade med lett redusert GFR 60-89
3 Moderat redusert nyrefunksjon 30-59
4 Alvorlig redusert nyrefunksjon 15-29
5 Nyresvikt i endestadiet < 15
GFR: glomerulær filtrasjonsrate
Nyreskade definert som strukturelle avvik ved nyrer eller vedvarende unormal proteinutskillelse i urinen
utvikling av autonom PTH-sekresjon hos personer som har hatt sekundær hyperparatyreoidisme i lengre tid1,7
Vitamin D-mangel (25-OH-D <50 nmol/L) er vanlig ved CKD og medfører redusert benformasjon, økt benresorpsjon og redusert mineralisering uavhengig av nivå på PTH og aktivt vitamin D (kalsitriol (1,25-OH-vitamin D) )1. Suboptimal vitamin D-status er også assosiert med sekundær hyper paratyreoidisme og lav bentetthet hos pasienter med CKD inklusive dialysepasienter 6
I tillegg til forstyrrelsene knyttet til CKD-MBD vil bruk av legemidler som forstyrrer benmetabolismen, som glukokortikoider, diuretika og protonpumpehemmere forverre skjeletthelsen. I tillegg til glukokortikoidenes effekt på benvev og kalsium-utskillelse, kan de føre til hypogonadisme som også har negativ effekt på benomsetningen4,5
Etter nyretransplantasjon, har det vært dokumentert signifikant tap av bentetthet de første 6 månedene etter transplantasjon. Etablert CKDMBD før transplantasjon, behandling med glukokortikoider og kalsinevrinhemmere (ciklosporin, takrolimus) og vedvarende forstyrrelser i mineralmetabolismen postoperativt
er medvirkende årsaker. Så mange som 90% av pasientene får hypofosfatemi4,6 som over tid kan føre til osteomalasi og progressiv demineralisering4. Suboptimal vitamin D-status (25-OH-vitamin D < 50 nmol/L) ses hos opptil 80% innen de tre første månedene og kan gi hypokalsemi og fall i bentetthet6. Hyperparatyreoidisme normaliseres kun hos 30% i løpet av første året og hos 57% i løpet av to år4,6. Persisterende høy PTH ved god transplantat funksjon skyldes i hovedsak tertiær hyperparatyroidisme.
Moderne medikamentprotokoller med lavere steroiddoser har bidratt til at bentapet er mindre uttalt nå enn tidligere.
Risikofaktorer for osteoporose
• Tradisjonelle faktorer: Kvinne, høy alder, lav kroppsvekt (KMI < 19 kg/m2), immobilisering, kalsium- og vitamin D-mangel, tidlig menopause, tidligere lavenergifraktur, arvelig disposisjon (førstegradsslektninger), alkoholinntak > 3 enheter per dag, røyking, legemidler som glukokortikoider samt en rekke tilstander som disponerer for sekundær osteoporose1,3
• Spesifikke faktorer knyttet til moderat/alvorlig CKD (CKD 3-5D): CKD-MBD med forstyrrelser i kalsium- og fosfatmetabolismen, D-vitaminmangel og sekundær/tertiær hyperparatyreoidisme, tid i dialyse, under- eller feilernæring, fysisk inaktivitet behandling med glukokortikoider og andre immunsuppressiva 2,6
Klinikk
Osteoporose uten brudd gir ingen symptomer. Lavenergibrudd (fall fra egen høyde eller lavere) er imidlertid diagnostisk for osteoporose. Vertebrale brudd kan gi ryggsmerter, men er ofte asymptomatiske, med høydetap og utvikling av kyfose som typiske funn. De fleste kompresjonsfrakturer oppdages ikke, da de kan forekomme uten fall eller de vanlige symptomer og tegn ved akutt fraktur1
Diagnostikk
Bentetthetsmåling Bentetthetsmåling ved dual energy x-ray absorptiometri (DXA) er anbefalt hos pasienter med CKD 3-5D som har etablert CKD-MBD og/eller andre risikofaktorer for osteoporose, samt etter nyretransplantasjon (1). Hos postmenopausale kvinner og menn over 50 år uten brudd er T-skår ≤ -2,5 ved DXA i columna eller hofter diagnostisk for osteoporose 3,7. DXAmåling av underarm med radius 33% anbefales ved hyperparatyreoidisme og når måling i columna eller hofter er vanskelig å tolke 3
I tillegg til de vanlige feilkildene ved DXA er det viktig å være klar over at kaliumbindere kan påvirke verdier målt i columna3,8, og at bentetthet i underarm med AV-fistel kan være falsk lav 9,10
Vertebral Fracture Assessment (VFA), sidebilde av lumbal- og torakalcolumna, er anbefalt hos pasienter med CKD 3-5D, ved høydetap > 4 cm, tidligere vertebralt brudd, og/ eller ved glukokortikoidbehandling av mer enn 3 mnd varighet3
Blodprøver Hos pasienter med CKD eller nyretransplanterte anbefales følgende blodprøver: Hb, natrium, kalium, magnesium, fritt kalsium, fosfat,
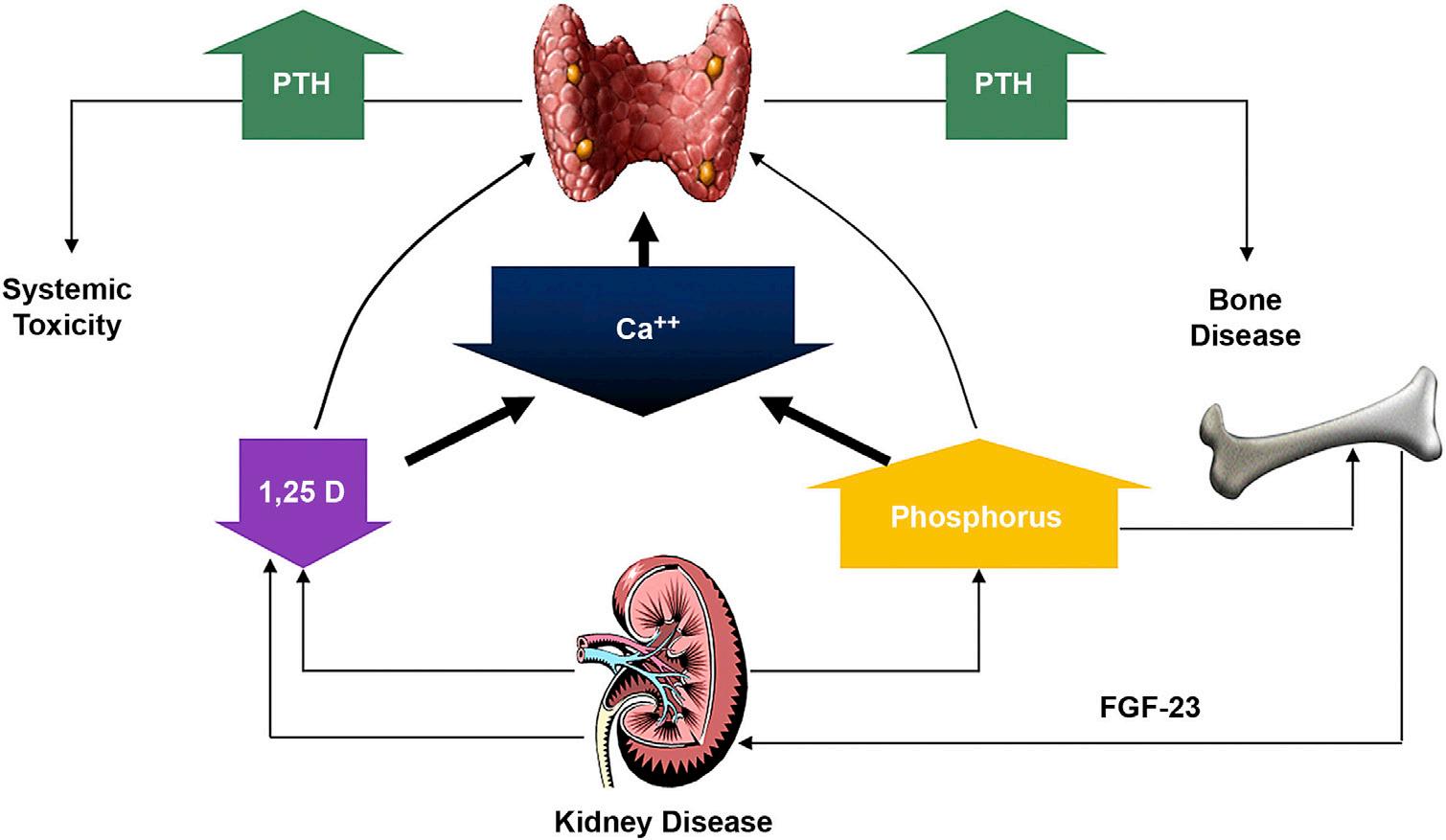
Figur 1. Patofysiologisk mekanisme for kronisk nyresykdom – mineral og bensykdom. 1,25 D, 1- α-hydroksylering av 25-hydroksy vitamin D; Ca++, fritt kalsium; FGF-23, fibroblastvekstfaktor 23; PTH, paratyreoideahormon. Gjengis fra Beto J. et al. J Ren Nutr. 2019 (trykkes med tillatelse).
PTH, 25-OH-vitamin D, kreatinin (ev. cystatin C), venøs syre-base-status, benspesifikk alkalisk fosfatase (bALP) og prokollagen type 1 N-terminal propeptid (P1NP).
Ved vurdering av PTH bør trenden (persisterende høy eller progressiv stigende) vektlegges og ikke enkeltmålinger7
Hos pasienter med CKD stadium 4-5 og hos nyretransplanterte pasienter bør osteomalasi (mineraliseringsdefekt) mistenkes ved vitamin D mangel, muskel-skjelettsmerter og høy bALP.
Benomsetningsmarkører er enten kollagenfragmenter eller enzymer fra benceller som frigjøres til blodbanen og kan gi et «øyeblikksbilde» av benremodelleringsprosessen2. I klinisk praksis bruker vi benformasjonsmarkørene P1NP og bALP. CTX-1 er en benresorpsjonsmarkør som er mindre egnet i klinisk praksis siden den har døgnvariasjon, må tas fastende og er avhengig av nyrefunksjon. Etter fraktur kan man se økning i benomsetningsmarkører inntil 12 måneder (høyest etter 2-3 måneder). Menopause, malignitet i skjelettet, sykdommer med høy benomsetning (f.eks. hyperparatyreoidisme) og legemidler som øker benomsetning (aromatasehemmere, tyroksin, teriparatid, romosozumab) øker også nivået av disse markø -
rene2,11. Ved bruk av glukokortikoider faller bALP og P1NP12. Mens bALP er uavhengig av nyrefunksjon kan total P1NP bli forhøyet ved redusert nyrefunksjon (eGFR ≤ 44 ml/min.)13. Intakt P1NP (tredje-generasjon) skal ikke påvirkes av nyrefunksjon, men dette måles per dags dato ikke i klinisk praksis i Norge.
Andre metoder som brukes for å vurdere bruddrisiko: Siden DXA er en kvantitativ analyse og tilgjengelige benomsetningsmarkører i hovedsak reflekterer benmetabolismen innenfor et begrenset tidsrom, er det behov for tilleggsverktøy for å vurdere bruddrisiko hos nyrepasienter, inkludert analyser som gir informasjon om benkvalitet
FRAX (Fracture Risk Assessment Tool) er en risikokalkulator som kan brukes til både å predikere frakturrisiko og avklare behov for DXA-måling. FRAX har flere svakheter, blant annet tar den ikke høyde for varighet og alvorlighetsgrad av risikofaktorene. Selv om FRAX ikke inkluderer CKD som en av risikofaktorene1,3 kan verktøyet trolig brukes hos pasienter med CKD og nyretransplanterte 3. Se FRAX Norge.
Trabekulær benskår (TBS) er et surrogatmål for benvevets mikroarkitektur i lumbalcolumna og måles med et eget software i DXA-apparater ved bentetthetsmåling. TBS ser ut
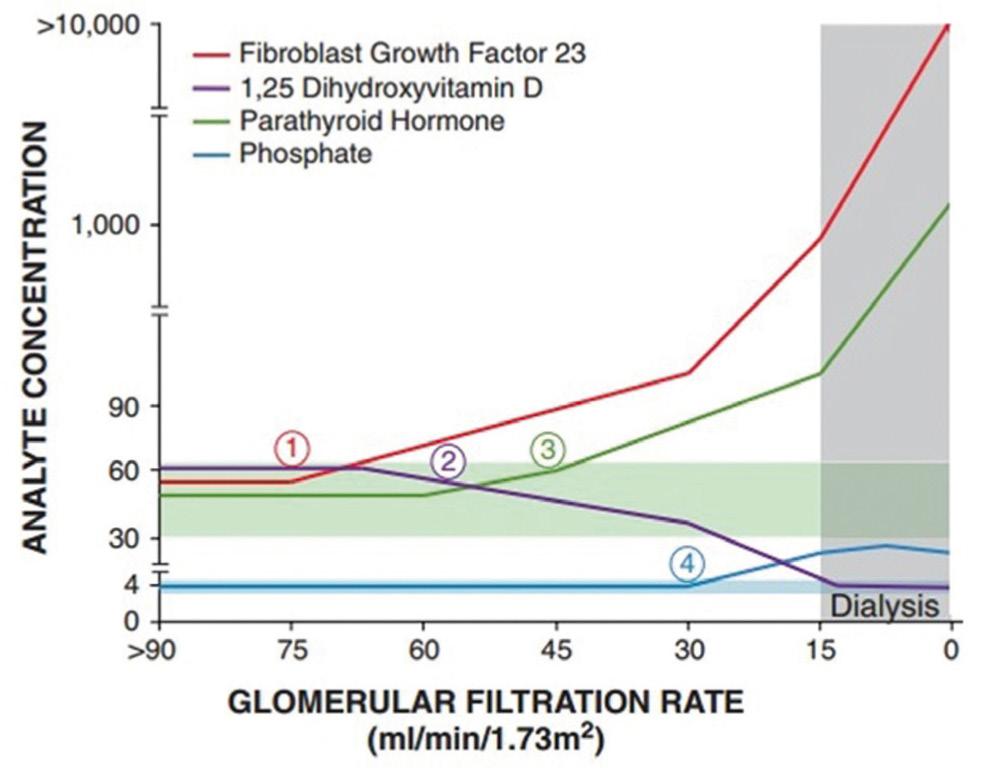
Figur 2. Nivåer av fibroblast vekstfaktor 23 (1), 1,25-dihydroksyvitamin D (2), parathyreoideahormon (3) og fosfat (4) i forhold til glomerulær filtrasjonshastighet. Gjengis fra Diniz H. & Frazao J.M. Nefrologia. 2013 (trykkes med tillatelse).
til å predikere frakturrisiko ved CKD, men den bør ikke brukes alene ved beslutninger om behandling av lav bentetthet1,2
Benbiopsi betraktes fortsatt som gullstandard for evaluering av skjelettmetabolismen, jmf. Internasjonale retningslinjer14. Både statiske og dynamiske parametere for benmodellering samt grad av mineralisering kartlegges. Kortikalt og trabekulært benvev vurderes hver for seg. Metoden er imidlertid invasiv, tidkrevende og avhengig av trent personell. I skrivende stund gjøres det ikke benbiopsier rutinemessig på klinisk indikasjon i Norge.
Behandling Hos pasienter med CKD stadium 1-3 anbefales samme behandling for osteoporose som for pasienter uten CKD3,7. Der dokumentasjonen bak råd om bruddforebyggende behandling er god for pasienter med CKD stadium 1-3, er den mindre omfattende og usikker for nyresykdom stadium 4-5D7. Det introduserer usikkerhet, samtidig som potensiale for skade ved aktiv behandling er større i denne gruppen. Det er derfor ekstra viktig med dialog med pasienten før oppstart av aktiv behandling.
Ikke-farmakologisk behandling (bør tilbys alle)
• Generelle anbefalinger om røykestopp, begrenset alkoholinntak, mosjon i form av vektbærende
fysisk aktivitet, tidlig mobilisering etter operasjon og fallforebyggende tiltak gjelder også for nyresyke med økt bruddrisiko1–3
• Det anbefales reduksjon til minste effektive dose av glukokortikoider og om mulig seponering. Medikamenter som kan føre til døsighet eller ustøhet bør unngås1,3.
• Pasienter bør ha adekvat inntak av kalsium (1000 mg daglig) helst igjennom kosten, ev. som kosttilskudd. De bør ha daglig inntak av vitamin D på 800 E (20 µg) og 25-OH-vitamin D bør være over 50 nmol/L, men fortrinnsvis over 75 nmol/L gjennom hele året 2,3 25-OH-vitamin D > 50 nmol/L bør sikres før oppstart av ev. antiresorptiv terapi. Kalsiuminntak gjennom kosten kan kalkuleres på melk.no/kalsiumkalkulator
- Ved osteomalasi (vitamin D-mangel, lav eller grenselav kalsium og fosfat, samt høy PTH og bALP) bør optimalisering av kalsium og vitamin D tilskudd forsøkes i minimum 12 måneder før ev. etterfølgende benspesifikk behandling15
Optimal behandling av CKD-MBD (bør tilbys alle). Behandling for hyperparatyroidisme, forstyrrelser i mineralbalansen og syre- baseforstyrrelser bør optimaliseres før spesifikk behandling for osteoporose er aktuelt3,7
• Fosfat: S-fosfat bør så langt det er mulig holdes innenfor referanseområdet ved CKD. Fosfatreduserende behandling inkluderer fosfatredusert kost, fosfatbindende behandling og lengre/oftere dialyse7,16 Hypofosfatemi er vanlig etter nyretransplantasjon og krever sjelden substitusjonsbehandling med mindre pasienter utvikler alvorlig (s-fosfat < 0,3 mmol/L) eller symptomatisk hypofosfatemi4
• Kalsium: Hyperkalsemi ved CKD er oftest resultat av vedvarende hyperparatyroidisme eller for høyt dosert behandling med vitamin D og bør unngås7,16. Det er dog anbefalt at 25-OH-vitamin D holdes > 50 nmol/L.
• PTH: hos pasienter med CKD 4-5 bør PTH ligge innenfor referanseområdet eller lett
forhøyet mens det tillates 2-9 x øvre referansegrense hos pasienter med CKD57,16. Medikamentell behandling (cinacalcet, aktivt vitamin D, syntetisk vitamin D-analog) er anbefalt før ev. paratyreoidektomi7. Indikasjon for paratyreoidektomi ved sekundær hyperparatyreoidisme er manglende effekt av medikamentell behandling, mens ved tertiær hyperparatyreoidisme er kirurgisk behandling indisert og bør alltid vurderes for å unngå bentap sekundært til høy benomsetning1,7 Persisterende hyperparatyroidisme er i tillegg assossiert med redusert graftoverlevelse hos nyretransplanterte. Siden paratyroidektomi medfører risiko for svekket transplantatfunksjon, bør slik kirurgi vurderes gjennomført i forkant av nyretransplantasjon17
Spesifikk osteoporose behandling ved CKD 4-5D2,6
Medikamentell behandling av osteoporose ved langtkommen nyresvikt er en spesialistoppgave som i flere tiår har hatt lav prioritet. Generelt er det svak evidens for effekt av slik behandling, da pasienter med CKDMBD regelmessig har vært utelatt fra større medikamentstudier. Med økende fokus på persontilpasset medisin, er det viktig å vurdere sannsynlig nytte av osteoporosebehandling opp mot risiko, helst i samforståelse med pasienten. Pasienter med lavenergifraktur bør vurderes for spesifikk osteoporotisk behandling uavhengig av bentetthetsmåling.
Antiresorptive legemidler hemmer den osteoklastiske benresorpsjonen. De mest potente er bisfosfonater og denosumab2. Ved bruk av bisfosfonater ved eGFR < 30 ml/min. bør forsiktighet utvises pga. manglende sikkerhetsdata. Bisfosfonater kan vurderes hos pasienter med CKD 4-5D etter konferering med endokrinololog/nefrolog2,3. Det bør da vurderes å gi halv dose av legemidlet og ved valg av zoledronsyre bør infusjonstiden dobles (ca. 40 minutter). Bisfosfonater blir dialysert og bør derfor gis rett etter dialyse2 Behandlingspause bør overveies etter 5 års behandling med alendronat eller 3 år med zoledronsyre, dersom bentetthetsmålinger ligger høyere
enn -2,5, og det ikke er oppstått nye frakturer. Hvis fortsatt T-score ≤ -2,5 anbefales 6 infusjoner eller 10 års peroral behandling før pause. Kontinuerlig behandling utover dette anbefales generelt ikke. Under behandlingspause kan bentetthet måles hvert 2.-3. år og bALP en gang årlig. Ved nytt lavenergibrudd eller signifikant fallende bentetthetsmåling er det aktuelt å starte med bisfosfonat igjen eller skifte til annen behandling22,23
Denosumab foretrekkes ofte ved eGFR < 30 ml/min da den er uavhengig av nyrefunksjon. Man bør være oppmerksom på at risikoen for hypokalsemi øker med redusert nyrefunksjon og behandling med kalsimimetikum, noe som kan forekomme hos opptil 25% av pasienter 2. Det er viktig at pasientene har adekvat kalsium tilskudd og vitamin D status. Fritt kalsium bør følges etter oppstart av denosumab ved CKD 4-5, og nadir verdi forekommer 2-8 uker etter administrering2. Seponering av denosumab er assosiert med økt risiko for vertebrale frakturer (opptil 30% hos postmenopausale kvinner) og må etterfølges av annen antiresorptiv behandling2. Teriparatid (syntetisk PTH) er anabol behandling som øker antall osteoblaster ved å redusere apoptose og øke modning og aktivering av osteoblaster og preosteoblaster4. Medikamentet brukes maksimalt i to år og kan forårsake hyperkaslemi. Det er kontrindisert ved alvorlig nyresvikt og hyperparatyreoidisme. Romosuzumab virker både anti-resorbtivt og anabolt, men er
foreløpig lite studert hos pasienter med CKD grunnet risiko forbundet med hjerte- karsykdom.
Måling av PTH og bALP kan være veiledende i valget mellom antiresorptiva eller anabol behandling. Ved PTH > 2 x øvre referansegrense og bALP > øvre referansegrense eller normal benomsetning, anbefales som regel bisfosfonat eller denosumab. Ved lav benomsetning definert ved PTH < 2 x øvre referansegrense og bALP < nedre referansegrense kan teriparatid vurderes. Internasjonalt gjøres benbiopsi ved noen sentra ved grenseverdier.
Spesifikk osteoporotisk behandling etter nyretransplantasjon. Selv om de fleste metabolske abnormiteter er reversible etter nyretransplantasjon, kan det være utfordrende med korrigering av CKD-MBD1. Pasienter med osteoporose etter nyretransplantasjon som har normale elektrolytter og nyrefunksjon, kan i stor grad behandles som ved primær osteoporose.
• Glukokortikoider bør trappes ned så raskt som mulig til minste effektive dose 4–6
• Nyretransplanterte med T-skår ≤ -2,5 ved DXA bør tilbys spesifikk behandling7,16
- Bisfosfonat er førstevalg til pasienter med stabil eGFR ≥ 30 ml/min., forslagsvis alendronat 70 mg/uke per oralt eller zoledronsyre 5 mg intravenøst hver 12. mnd.7,16,18,19
- Ved eGFR < 30 ml/min. foretrekkes denosumab 60 mg s.c. hver 6. måned5,6
- Antiresorptiv behandling bør kombineres med vitamin D-tilskudd og inntak av minst 1000 mg kalsium daglig (helst via kosten)4,20
- Dokumentasjonen for osteoanabol behandling er svært begrenset etter nyretransplantasjon5,6,21.
Oppfølging
CKD-MBD følges i hovedsak av nyreleger i forbindelse med oppfølging av grunnlidelsen. Ved oppstart av spesifikk osteoporosebehandling vil det noen ganger være nødvendig å konferere endokrinolog. For å evaluere bivirkninger, terapeutisk respons, pasientetterlevelse, og for å vurdere reoppstart av behandling etter en behandlingspause bør følgende blodprøver kontrolleres minst en gang årlig3: Fritt kalsium, PTH, 25-OH-vitamin D, bALP, P1NP, fosfat, magnesium og kreatinin.
• Behandling med denosumab er som hovedregel livslang og bør ikke seponeres uten å konferere med endokrinolog/nefrolog22,23
• Generelt tar det tid før signifikante endringer i skjelettet kan detekteres med DXA-måling. Bentetthetsmåling anbefales hver 2.-3. år eller sjeldnere avhengig av klinikk hos pasienter med CKD3 Etter nyretransplantasjon måles bentetthet etter 8 uker og 1 år ved Rikshospitalet. Videre anbefales bentetthetsmåling hvert 5. år hos transplanterte med normal bentetthet i initialforløpet, og hvert 2.-3. år ved osteoporose/osteopeni.
Zirconium Cyclosilicate. J Clin Densitom 24, 281–286 (2021).
Referanser:
1. Abdalbary, M. et al. Management of osteoporosis in patients with chronic kidney disease. Osteoporosis Int 1–16 (2022) doi:10.1007/s00198-022-06462-3.
2. Hampson, G., Elder, G. J., Cohen-Solal, M. & Abrahamsen, B. A review and perspective on the assessment, management and prevention of fragility fractures in patients with osteoporosis and chronic kidney disease. Endocrine 73, 509–529 (2021).
3. Evenepoel, P. et al. European Consensus Statement on the diagnosis and management of osteoporosis in chronic kidney disease stages G4–G5D. Nephrol Dial Transpl (2020) doi:10.1093/ndt/gfaa192.
4. Torregrosa, J.-V., Ferreira, A. C., Cucchiari, D. & Ferreira, A. Bone Mineral Disease After Kidney Transplantation. Calcified Tissue Int 108, 551–560 (2021).
5. Jurdi, A. A., Martins, J. D. S. & Riella, L. V. Mineral Bone Disorders in Kidney Transplantation. Semin Nephrol 41, 168–179 (2021).
6. Khairallah, P. & Nickolas, T. L. Bone and Mineral Disease in Kidney Transplant Recipients. Clin J Am Soc Nephro 17, CJN.03410321 (2021).
7. Ketteler, M. et al. Executive summary of the 2017 KDIGO Chronic Kidney Disease–Mineral and Bone Disorder (CKD-MBD) Guideline Update: what’s changed and why it matters. Kidney Int 92, 26–36 (2017).
8. McCarney, B., Binkley, N. & Krueger, D. A Newly Recognized DXA Confounder: The Potassium-Binding Medication Sodium
9. Muxí, Á. et al. Arteriovenous Fistula Affects Bone Mineral Density Measurements in End-Stage Renal Failure Patients. Clin. J. Am. Soc. Nephrol. 4, 1494–1499 (2009).
10. Walder, A. et al. The effect of a previous created distal arteriovenous-fistula on radial bone DXA measurements in prevalent renal transplant recipients. PLoS ONE 13, e0200708 (2018).
11. Evenepoel, P. et al. Diagnosis and management of osteoporosis in chronic kidney disease stages 4 to 5D: a call for a shift from nihilism to pragmatism. Osteoporosis Int 1–9 (2021) doi:10.1007/ s00198-021-05975-7.
12. Devogelaer, J.-P., Durnez, A., Gruson, D. & Manicourt, D. H. Biomarkers in Bone Disease. Biomarkers Dis Methods Discov Appl 905–932 (2017) doi:10.1007/978-94-007-7693-7_23.
13. Tridimas, A., Milan, A. & Marks, E. Assessing bone formation in patients with chronic kidney disease using procollagen type I N-terminal propeptide (PINP): The choice of assay makes a difference. Ann Clin Biochem 58, 528–536 (2021).
14. Group, K. KDIGO 2017 Clinical Practice Guideline Update for the Diagnosis, Evaluation, Prevention, and Treatment of Chronic Kidney Disease–Mineral and Bone Disorder (CKD-MBD). Kidney Int Suppl 7, 1–59 (2017).
15. Cianferotti, L. Osteomalacia Is Not a Single Disease. Int. J. Mol. Sci. 23, 14896 (2022).
17. Cianciolo, G. et al. A roadmap to parathyroidectomy for kidney transplant candidates. Clin. Kidney J. 15, 1459–1474 (2022).
18. Hauck, D. et al. Bisphosphonates and bone mineral density in patients with end-stage kidney disease and renal transplants: A 15-year single-centre experience. Bone Reports 16, 101178 (2022).
16. Isakova, T. et al. KDOQI US Commentary on the 2017 KDIGO Clinical Practice Guideline Update for the Diagnosis, Evaluation, Prevention, and Treatment of Chronic Kidney Disease–Mineral and Bone Disorder (CKD-MBD). Am J Kidney Dis 70, 737–751 (2017).
19. Ali, M. S. et al. Alendronate use and bone mineral density gains in women with moderate-severe (stages 3B–5) chronic kidney disease: an open cohort multivariable and propensity score analysis from Funen, Denmark. Arch Osteoporos 15, 81 (2020).
20. Tsujita, M. et al. Cholecalciferol Supplementation Attenuates Bone Loss in Incident Kidney Transplant Recipients: A Prespecified Secondary Endpoint Analysis of a Randomized Controlled Trial. J Bone Miner Res 37, 303–311 (2022).
21. Chen, C.-H. et al. Efficacy of Osteoporosis Medications for Patients With Chronic Kidney Disease: An Updated Systematic Review and Network Meta-Analysis. Front Pharmacol 13, 822178 (2022).
22. Shoback, D. et al. Pharmacological Management of Osteoporosis in Postmenopausal Women: An Endocrine Society Guideline Update. J Clin Endocrinol Metabolism 105, 587–594 (2020).
23. Camacho, P. M. et al. American association of clinical endocrinologists/American college of endocrinology clinical practice guidelines for the diagnosis and treatment of postmenopausal osteoporosis - 2020 update. Endocr Pract 26, 1–46 (2020).
Norske indremedisinere har stor glede og nytte av Indremedisineren (IM). IM bidrar til faglig utvikling og er både et viktig bindeledd i miljøet, og mellom styret i NIF og det enkelte medlem.
Redaksjonen og alle bidragsytere jobber på dugnad. Dere annonsører bidrar til at vi kan utgi et flott IM og at vi kan drifte indremedisineren.no, der trafikken er sterkt økende. Uten deres hjelp hadde det ikke vært mulig.
Vi håper det gode samarbeidet fortsetter, og at dere blir med videre!







































Familiær hyperkolesterolemi* FH – sekundærprevensjon LDL-C >2,6 mmol/l, FH – primærprevensjon (barn og voksne fra og med 8 år) LDL-C >3,6 mmol/l
Hyperkolesterolemi ved etablert aterosklerotisk sykdom** (sekundærprevensjon) med en av følgende risikofaktorer: tidligere hjerteinfarkt, med tilbakevendende CV-hendelser, diabetes mellitus LDL-C >2,6 mmol/l, uten tilleggsrisiko LDL-C >3,6 mmol/l
Krav til tidligere behandling: Refusjon ytes når alirokumab brukes som tillegg til statin og/eller ezetimib hos pasienter som ikke oppnår LDL-nivåer under grenseverdiene nevnt ovenfor. Se følgende krav ***
Spesialistkrav: Forskrivning skal være instituert av spesialist i indremedisin, kardiologi, endokrinologi, geriatri, pediatri, nevrologi eller av lege ved tilsvarende sykehusavdeling.
* Gentest må være utført
** Sekundærprofylakse etter akutt koronarsykdom (hjerteinfarkt, ustabil angina med sykehusinnleggelse), koronar- eller annen arteriell revaskularisering, angina pectoris, iskemisk hjerneslag eller symptomatisk perifer arteriell sykdom
*** For brukere som tåler statiner: Høyeste tolererbare dose statin i kombinasjon med ezetimib. For brukere som ikke tåler statiner (statinintoleranse): Minst to forskjellige statiner i laveste dose i kombinasjon med ezetimib. Intoleranse må dokumenteres i journal av forskrivende lege. Ved absolutt kontraindikasjon mot statiner: ezetimib i monoterapi.
Refusjonskoder ICD: -26 etablert aterosklerotisk sykdom (sekundærprevensjon) og E78 ren hyperkolesterolemi. ICPC: -26 etablerte atersklerotisk sykdom og T93 hyperkolesterolemi
Referanser:
1. https://www.dmp.no/nyheter/forhandsgodkjent-refusjon-for-to-pcsk9-hemmere-fra-1.-januar-2025 ( 06.02.2025)
2. Praluent SPC 18.11.2024 pkt 4.2.
3. https://www.felleskatalogen.no/medisin/blaarev-register/c10ax14-1 (06.02.2025).
MAT-NO-2500048 v1.0, 02.2025
sanofi-aventis Norge AS - Pb 133, 1325 Lysaker - Tel.: 67 10 71 00 www.sanofi.no

Les mer om anbudet her

C Praluent «sanofi-aventis»
Lipidmodifiserende middel, humant monoklonalt antistoff (IgG1).
ATC-nr.: C10A X14
INJEKSJONSVÆSKE, oppløsning 75 mg/ml, 150 mg/ml og 300 mg/2 ml: Hver ferdigfylt penn inneh.: Alirokumab 75 mg, 150 mg resp. 300 mg, histidin, sukrose, polysorbat 20, vann til injeksjonsvæsker.
PRALUENT er indisert ved: Primær hyperkolesterolemi eller blandet dyslipidemi: Til voksne med primær hyperkolesterolemi (heterozygot familiær og ikke-familiær) eller blandet dyslipidemi, og hos pediatriske pasienter >8 år med heterozygot familiær hyperkolesterolemi (HeFH) som tilleggsbehandling til diett: I kombinasjon med et statin eller statin med annen lipidsenkende behandling hos pasienter som ikke oppnår LDL-kolesterol (LDL-C)-mål med høyeste tolererte dose av et statin, eller alene eller i kombinasjon med annen lipidsenkende behandling hos pasienter som er statinintolerante, eller der et statin er kontraindisert.
Påvist aterosklerotisk kardiovaskulær sykdom: Til voksne med påvist aterosklerotisk kardiovaskulær sykdom for å redusere kardiovaskulær risiko ved å senke LDL-C-nivåene, som tillegg til korreksjon av andre risikofaktorer: I kombinasjon med den maks. tolererte dosen av et statin med eller uten andre lipidsenkende behandlinger, eller, alene eller i kombinasjon med andre lipidsenkende behandlinger hos pasienter som er statinintolerante, eller der et statin er kontraindisert. For informasjon om studieresultater i forhold til effekt på LDL-C, kardiovaskulære hendelser og studerte pasientgrupper, se SPC. Dosering: Vanlig oppstartsdose er 75 mg 1 gang hver 2. uke. Hvis ønsket LDL-C-reduksjon er >60%, gis 150 mg 1 gang hver 2. uke, eller 300 mg 1 gang hver 4.uke (månedlig).
Utvalgt sikkerhetsinformasjon:
Bivirkninger: Vanlige (≥1/100 til <1/10): Generelle: Reaksjon på injeksjonsstedet inkl. erytem/rødhet, kløe, hevelse, smerter/ømhet. Hud: Kløe. Luftveier: Tegn og symptomer fra de øvre luftveiene inkl. smerter i orofarynks, rhinoré, nysing. Sjeldne (≥1/10 000 til <1/1000): Hud: Nummulært eksem, urtikaria. Immunsystemet: Overfølsomhet, overfølsomhetsvaskulitt. Ukjent frekvens: Generelle: Influensalignende sykdom. Hud: Angioødem. Kontraindikasjoner: Overfølsomhet for innholdsstoffene. Forsiktighetsregler: Brukes med forsiktighet ved alvorlig nedsatt lever- eller nyrefunksjon. Interaksjoner: Klinisk relevante interaksjoner forventes ikke. Pakninger og listepriser: 75 mg/ml: 2 stk. kr 4334,60. 6 stk. kr 12931,20. 150 mg/ml: 2 stk. kr 4334,60. 6 stk. kr 12931,20. 300 mg/2 ml: 3 stk. kr 12931,20. Refusjonsprisen er rabattert: Anbudskode: 2580. For fullstendig informasjon les godkjent FK-tekst eller SPC for Praluent. Praluent «Sanofi» - Felleskatalogen Basert på Praluent SPC godkjent av DMP/EMA 18.11.2024.
sanofi-aventis Norge AS - Pb 133, 1325 Lysaker - Tel.: 67 10 71 00 www.sanofi.no


Redusert hørsel regnes som en av de viktigste modifiserbare risikofaktorene for demens. Grunnet den svært høye forekomsten av redusert hørsel vil selv en liten bedring av hørsel i samfunnet kunne føre til en kraftig reduksjon i demensforekomsten. Kunnskap og bevissthet blant leger om sammenhengen er nødvendig for å redusere underbehandling av redusert hørsel.
Christian Myrstad, geriater og stipendiat, Sykehuset Levanger og Nasjonalt senter for aldring og helse/UiO. Bo Engdahl, forsker/Ph.D., Folkehelseinstituttet.
Redusert hørsel
Hørselsnedsettelse er en tilstand hvor evnen til å oppfatte lyder svekkes. Dette kan skyldes en rekke faktorer, inkludert aldersrelaterte endringer (presbyacusis), støyskade, genetiske faktorer (arv), sykdommer og medikamenter (1). Audiometriske tester brukes for å diagnostisere tilstanden ved å måle i decibel (dB) terskelen for hørbarhet i forskjellige frekvensområder (kHz). Som risikofaktor for demens er redusert hørbarhet for talefrekvensene (0,5-4 kHz) mest relevant. Hørselstap har mange definisjoner, men klassifiseres ofte som mildt (25-39 dB), funksjonsnedsettende (≥35 dB), moderat og alvorlig (≥40 dB), eller døvhet. Se Tabell 1.
Hørselstap er en vanlig tilstand spesielt blant eldre, men med økende forekomst fra 40-årsalderen og forekomsten globalt er 25% hos personer over 60 år (≥20 dB) (2). Ifølge WHO er omtrent 1,5 milliarder (20%) av verdens befolkning berørt av hørselsnedsettelse, hos 430 millioner (5%) er det et funksjonsnedsettende tap (>35 dB), og 20% bor i høyinntektsland. En studie av forekomsten av hørselstap (≥20 dB) i HUNT2 og HUNT4 (55% hos personer >64 år, 2017-2019) viser at redusert hørsel er utbredt i den eldre befolkningen i Norge, men at den har falt med 10% de siste 20 årene til 18% i 2018 (3).
Ifølge Hørselhemmedes landsforbund har 1 million nordmenn nedsatt hørsel og 300.000 har hørselskorrigerende behandling som høreapparat (4).
Demens
Anslagsvis lever 55 millioner mennesker med demens, ca. 100.000 av dem i Norge. Antallet anslås å tredobles innen 2050 (5, 6). Demens er en samlebetegnelse for flere sykdommer som kjennetegnes av en progressiv reduksjon i kognitive funksjoner, inkludert hukommelse, resonnering og evnen til å utføre daglige aktiviteter (6). Forekomsten av demens i Norge ble grundig kartlagt i 2021 etter studien HUNT4 70+. Standardisert prevalens i Norge var 15% blant personer fra 70 år (5). Antall personer med demens forventes å stige betraktelig grunnet økende levealder, men med en forskyvning av debuttidspunkt til høyere aldre.
Sammenheng mellom hørsel og demens
Siden det ikke er mulig å studere om redusert hørsel forårsaker demens i randomiserte kontrollerte studier er studier av observerte sammenhenger i kohortstudier det beste vi har. En hovedutfordring ved forskning på hørsel og demens er at sammenhengen kan fremstå kunstig høy på grunn av revers årsaksforklaring.
≥40 dB Moderat/alvorlig Høreapparat nødvendig
dB: Decibel; WHO: Verdens helseorganisasjon.
Nevrodegenerasjon i auditive assosiasjonsbaner i hjernen påvirker bearbeidelsen av hørselsinntrykkene og redusert hørsel kan dermed være et symptom på slik nevrodegenerasjon ved demens. Patologiske forandringer kan starte mer enn 20 år før man får demensdiagnose, så for å unngå revers kausalitet må oppfølgingstiden være tilsvarende (7). Foreløpig er HUNT alene i verden om å tilby både en slik oppfølgingstid, audiometrisk hørselsdata og demensdiagnoser stilt av et ekspertpanel (5, 8). En metaanalyse presentert av ekspertgruppen som gjennomgikk demenslitteraturen for The Lancet i 2017 inkluderte tre kohortstudier med audiometrisk hørselstap ved inklusjon, mer enn 5 års oppfølgingstid (9-17 år) og justering for relevante konfunderende faktorer inkludert kardiovaskulær sykdom.(9) En annen metaanalyse fra samme år viser at det på tidspunktet fantes minst 26 tverrsnittstudier og 6 kohortstudier som ikke oppfylte disse kravene. Studiene i Lancet-rapporten var konsistente (I2 = 29%) og viste en nesten doblet risiko for demens for personer med redusert hørsel (relativ risiko [RR] 1,94, 95% konfidensintervall [KI] 1,38-2,73). Rapporten konkluderte med at 9% (population attributable fraction, PAF) av demensforekomsten var forårsaket av redusert hørsel, og at hørsel dermed var den mest utslagsgivende risikofaktoren for demens. Det store utslaget redusert hørsel utgjør er ikke på grunn av størrelsen på risikoen, men grunnet den svært høye forekomsten av redusert hørsel i samfunnet. Selv få års utsettelse av redusert hørsel gjennom forebygging, eller behandling som utsetter konsekvensene redusert
hørsel fører med seg, skal derfor gi en kraftig reduksjon i forekomsten av demens. Størrelsen på PAF-verdien for hørsel er imidlertid omdiskutert, ettersom utregningen inkluderte forekomsten av mildere hørseltap, som ikke ble inkludert i studiene av risiko (10).
Forskning de siste årene svekker imidlertid sammenhengen noe. Tar vi utgangspunkt i de seks siste studiene som er inkludert i den siste Lancet-rapporten (2024) og legger til ytterligere to ferske studier med like inklusjonskriterier, viser vår metaanalyse en 27% økt risiko (RR 1,27, 95% KI 1,01-1,58), dvs. en tredel av risikoen fra Lancet-rapporten i 2017, og betydelig inkonsistens (I2 = 91%) (11-13). Se Figur 1. I studien av sammenhengen mellom redusert hørsel og demens med data fra HUNT (Myrstad et al, 2023), med den hittil største populasjonen og den lengste oppfølgingstiden, var sammenhengen svak og kun signifikant i gruppen under 85 år (RR 1,36, 95% KI 1,11-1,67), det siste antakelig fordi de aller eldste med demens falt ut av studien grunnet død før oppfølgingstidspunktet (12).
Behandling av redusert hørsel og effekt på demensrisikoen Rasjonalet bak hørselskorrigerende behandling som et tiltak for å redusere demensforekomsten baserer seg på flere årsaksforklaringer (14). Redusert sensorisk stimuli gir redusert dannelse av nye nevroner og synapser og påvirker direkte hjernevolumet. Indirekte er redusert hørsel årsak til sosial isolasjon og i noen tilfeller depresjon, som i tillegg til å
Referanser
1. Engdahl B. Fakta om hørselstap fhi.no: Folkehelseinstituttet; 2024 [updated 2024-12-20]. Available from: https:// www.fhi.no/kl/stoy/om-horselstap/?utm_source=chatgpt. com#risikofaktorer-for-hrselstap.
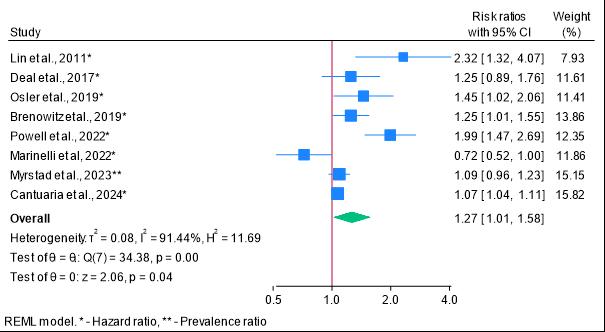
Figur 1 Relativ risiko for demens for personer med redusert hørsel ved baseline sammenlignet med personer uten redusert hørsel (12).
forsterke den direkte mekanismen også er individuelle risikofaktorer for demens. Redusert hørsel gir i tillegg økt bruk av kognitive ressurser for auditiv prosessering, som gir reduserte kognitive reserver til andre kognitive funksjoner. Til slutt finnes en lang rekke felles risikofaktorer for redusert hørsel og demens som er viktig å ta hensyn til ved forskning på sammenhengen (15).
Den vanligste behandlingsmetoden er høreapparat, men avhengig av årsak gjøres også fjerning av ørevoks, kirurgi, ossikkeltransplantasjon ved kalsifikasjon i mellomøret og implantasjon av cochleaimplantat. Flere studier har vist en sammenheng mellom bruk av høreapparat og redusert risiko for demens. I en metaanalyse i 2022 var bruk av høreapparater assosiert med 19% lavere risiko for demens sammenlignet med de med ukorrigert hørselstap.(16) En randomisert kontrollert studie over tre år viste imidlertid ingen redusert risiko for demens ved bruk av høreapparater, annet enn i en sensitivitetsa-
2. World Health Organization (WHO). Deafness and hearing loss Geneva: World Health Organization2024 [updated 2024-02-02; cited 2024 2024-11-12]. Available from: https://www.who.int/ news-room/fact-sheets/detail/deafness-and-hearing-loss.
3. Engdahl B, Strand BH, Aarhus L. Better hearing in Norway. A comparison of two HUNT cohorts 20 years apart.: Erratum. Ear and Hearing. 2022;43(4).
4. Hørselshemmedes Landsforbund. Norge mangler minst 150 audiografer hlf.no: Hørselhemmedes Landsforbund; 2025 [updated 2024-11-11.
5. GjOra L, Strand BH, Bergh S, Borza T, Braekhus A, Engedal K, et al. Current and Future Prevalence Estimates of Mild Cognitive Impairment, Dementia, and Its Subtypes in a Population-Based Sample of People 70 Years and Older in Norway: The HUNT Study. J Alzheimers Dis. 2021;79(3):1213-26.
6. World Health Organization (WHO). Dementia: Key Facts 2023 [Available from: https://www.who.int/news-room/fact-sheets/ detail/dementia.
nalyse med personer med økt risiko for kognitiv svikt ved baseline (17). I Norge har vi behovsprøvd refusjon for høreapparater, men stigma knyttet til bruk, manglende bevissthet og for sen oppstart av behandling er hyppige årsaker til underbehandling (18).
Oppsummering Redusert hørsel er en vanlig tilstand som øker med alderen og er en viktig risikofaktor for demens. Sammenhengen mellom hørselstap og demens er godt dokumentert, men nyere forskning antyder at risikoøkningen ikke er like stor som tidligere antatt. Tidlig diagnostisering og behandling av hørselstap, spesielt gjennom bruk av høreapparater, kan redusere risikoen for demens og forbedre livskvaliteten for eldre. Funnene understreker viktigheten av å inkludere hørselsscreening som en del av forebyggende helsearbeid for å bedre livskvaliteten i befolkningen og redusere unødvendig ressursbruk.
8. Yu RC, Proctor D, Soni J, Pikett L, Livingston G, Lewis G, et al. Adult-onset hearing loss and incident cognitive impairment and dementia - A systematic review and meta-analysis of cohort studies. Ageing Res Rev. 2024;98:102346.
9. Livingston G, Sommerlad A, Orgeta V, Costafreda SG, Huntley J, Ames D, et al. Dementia prevention, intervention, and care. Lancet. 2017;390(10113):2673-734.
10. Engdahl B. Reflections on The Lancet’s Commission on dementia prevention, intervention, and care. The Lancet. 2025;405(10479):624.
11. Livingston G, Huntley J, Liu KY, Costafreda SG, Selbæk G, Alladi S, et al. Dementia prevention, intervention, and care: 2024 report of the Lancet standing Commission. Lancet. 2024;404(10452):572-628.
12. Myrstad C, Engdahl BL, Costafreda SG, Krokstad S, Lin F, Livingston G, et al. Hearing impairment and risk of dementia in The HUNT Study (HUNT4 70+): a Norwegian cohort study. EClinicalMedicine. 2023;66:102319.
13. Cantuaria ML, Pedersen ER, Waldorff FB, Wermuth L, Pedersen KM, Poulsen AH, et al. Hearing Loss, Hearing Aid Use, and Risk of Dementia in Older Adults. JAMA Otolaryngol Head Neck Surg. 2024;150(2):157-64.
14. Fortunato S, Forli F, Guglielmi V, De Corso E, Paludetti G, Berret-
7. Jack CR, Jr., Knopman DS, Jagust WJ, Shaw LM, Aisen PS, Weiner MW, et al. Hypothetical model of dynamic biomarkers of the Alzheimer’s pathological cascade. Lancet Neurol. 2010;9(1):11928.
tini S, et al. A review of new insights on the association between hearing loss and cognitive decline in ageing. Acta otorhinolaryngologica Italica : organo ufficiale della Societa italiana di otorinolaringologia e chirurgia cervico-facciale. 2016;36(3):15566.
15. Myrstad C. Directed acyclig graph mapping the associations between hearing impairment, covariates and the MoCA score: DAGitty; 2024 [Available from: https://dagitty.net/mp6zDj58w.
16. Yeo BSY, Song H, Toh EMS, Ng LS, Ho CSH, Ho R, et al. Association of Hearing Aids and Cochlear Implants With Cognitive Decline and Dementia: A Systematic Review and Meta-analysis. JAMA Neurol. 2023;80(2):134-41.
17. Lin FR, Pike JR, Albert MS, Arnold M, Burgard S, Chisolm T, et al. Hearing intervention versus health education control to reduce cognitive decline in older adults with hearing loss in the USA (ACHIEVE): a multicentre, randomised controlled trial. Lancet. 2023;402(10404):786-97.
18. Helsedirektoratet. Mangelfullt system for identifisering av hørselstap 2020 [updated 2020-09-27. Available from: https:// www.helsedirektoratet.no/rapporter/utredning-av-tilbud-tilhorselshemmede/utfordringer-og-behov-for-videre-innsats/ mangelfullt-system-for-identifisering-av-horselshemming?utm_ source=chatgpt.com.
Olympus is the only gastroenterology solution provider that combines the entire clinical process with state-of-theart medical technology and precision manufacturing capabilities. From diagnosis and therapy to documentation, processing and training, this support allows medical professionals to strengthen their skills and optimize workflows, and thus aiming to achieve best possible outcomes for their patients.



















Whether it is a diagnostic or therapeutic endoscopic procedure — ranging from basic to advanced — our unique and comprehensive endoscopic product portfolio ensures the right solution for all clinical needs.

Using the right ERCP tools during interventions with pancreatobiliary disorders allows you to effectively exchange devices during the procedure. The Olympus ERCP portfolio contains, among others, our VisiGlide guidewires, the CleverLock guidewire locking device and the CleverCut 3 V preloaded sphincterotomes to help ensure smooth procedures.




Respiratory Endoscopy
ESD is an effective technique for removing cancerous or other abnormal tissues from the digestive tract. Olympus has pioneered the development of the ESD technique and developed devices like the DualKnife J, HookKnife J, and the TriangleTipKnife J to ease the operations. The Coagrasper hemostatic forceps allow for reliable hemostasis during ESD procedures.
POEM is an endoscopic procedure to cure achalasia, an esophageal motility disorder with symptoms like dysphasia. Olympus offers excellent products for POEM procedures such as the dedicated TriangleTipKnife J and the NeedleMaster injection needles.
EUS combines the advantages of endoscopy and ultrasonography. Olympus EZShot 3 and EZShot 3 Plus EUS needles provide superior flexibility that helps smooth access and targeting for EUS-FNB and EUS-FNA. Consequently, tissue can be obtained from difficult scope positions.
In the respiratory field, Olympus provides a wide range of innovative solutions and advanced equipment to support respiratory diagnosis and treatment. These include a versatile lineup of instruments for endobronchial ultrasound, transbronchial needle aspiration, peripheral bronchoscopy and valves for emphysema and air leak treatment.
Read More ... www.olympus.eu/endotherapy

ProjectedImpactandCost-EffectivenessofNovelMolecularBloodBasedorStool-BasedScreeningTestsforColorectalCancer UriLadabaum,MD,MS;AjithaMannalithara,PhD;RobertE.Schoen,MD,MPH;JasonA.Dominitz,MD,MHS;and
0.25(0.23to0.27),0.28(0.27to0.30),0.28(0.26to 0.30),0.44(0.42to0.47),and0.46(0.44to0.49), respectively.Thecf-bDNAtest(Shield;listprice $1495)cost$89600($74800to$102300)perQALY gainedversusnoscreening;alternativeswereless costlyandmoreeffective.

Annals of Internal Medicine utropte ved inngangen til dette året de 10 mest innflytelsesrike artiklene fra 2024. Redaksjonen gir her en kort oppsummering av 8 av disse, som vi tenker er mest aktuelle for norske lesere.
ResultsofSensitivityAnalysis:
Incrementalcosts exceededincrementalbenefitswhennoveltestintervalswereshortenedto2or1years.Thecf-bDNAtest matchedFIT’simpactonCRCmortalityat1.35(1.30to 1.40)-foldFIT ’suptakerate,assumingequalcolonoscopy follow-up.Ifpersonswhoacceptcolonoscopyorstool testsshiftedtocf-bDNA,CRCdeathsincreased.This adverseeffectwasovercomeifevery3suchsubstitutionswerecounterbalancedbycf-bDNAuptakeby 2ormorepersonsrefusingalternatives,assuming equalcolonoscopyfollow-up.
NovelversusestablishedCRCscreenIncidenceandmortalityofCRC, Forcolonoscopyevery 10years,annualfecalimmunochemicaltest(FIT), andtriennialnext-generationmultitargetstoolDNA, FIT-RNA,cf-bDNA(GuardantShield),orcf-bDNA (Freenome),therelativerates(RRs)and95%uncertaintyintervals(UIs)versusnoscreeningforCRC incidencewere0.21(0.19to0.22),0.29(0.27to 0.31),0.33(0.32to0.36),0.32(0.30to0.34),0.58 (0.55to0.61)and0.58(0.55to0.60),respectively; theRRsforCRCdeathwere0.19(0.17to0.20),

Hewitt, Ole Kristian Furulund, Maya Bass og Tone Svilaas Redkasjonen i Indremedisieneren
Differentiation of Prior SARS-CoV-2 Infection and Postacute Sequelae by Standard Clinical Laboratory Measurements in the RECOVER Cohort
Limitation: Longitudinaltest-specificparticipationpatternsareunknown.

Conclusion: First-generationcf-bDNAtestsmaydeliver netbenefitorharm,dependingonthebalance betweenachievingscreeninginpersonswhodecline alternativesversussubstitutingcf-bDNAformore effectivealternatives. PrimaryFundingSource:TheGorrindoFamilyFund.
Erlandson KM et al. Ann Intern Med 2024; 177: 1209-1221
Denne studien undersøkte kliniske laboratoriemarkører for SARSCoV-2 og post-akutte senfølger av infeksjonen (PASC). Forskerne benyttet en propensitetsskår vektet lineær regresjonsmodell for å evaluere forskjeller i gjennomsnittlige laboratorie målinger før infeksjon og gjennom en PASC-indeks. Studien inkluderte 10 094 deltakere, hvorav 8 747 hadde tidligere SARS-CoV-2 infeksjon. Resultatene viste at
AnnInternMed.
Forauthor,article,anddisclosureinformation,seeendoftext.2024;177:1610-1620.doi:10.7326/ANNALS-24-00910

Thisarticlewaspublishedat Annals.org on29October2024.
pasienter med tidligere infeksjon hadde lavere gjennomsnittlig antall blodplater og høyere gjennomsnittlig HbA1c-nivå og urin albuminkreatinin ratio sammenlignet med ikke-infiserte deltakere. Forskjellene var imidlertid av begrenset klinisk betydning. Blant deltakere med tidligere infeksjon var det ingen meningsfulle forskjeller i gjennomsnittlige laboratorieverdier mellom de med høy PASC-indeks
og de med lav PASC-indeks.
Studien konkluderte med at ingen av de 25 laboratorieverdiene kunne tjene som en klinisk nyttig biomarkør for PASC. Begrensninger ved studien inkluderer manglende evne til å avgjøre om forskjellene i laboratorie målinger er konsekvenser av SARS-CoV-2 eller risikofaktorer for infeksjonen.
Projected impact and Cost-Effectiveness of Novel Molecular Blood-Based or Stool-Based Screening Tests for Colorectal Cancer
Ladabaum U, et al. Ann Intern Med. 2024 Dec; 177 (12): 1610-1620
Denne studien analyserte de kliniske og økonomiske effektene av et nytt screeningsprogram for kolorektalkreft ved bruk av cf-bDNA (cell-free DNA blodprøve). Forskerne sammenlignet den nye metoden med konvensjonelle metoder for screening, inkludert fekal immunokjemisk test (FIT), koloskopi og fekalprøver. Studien ble utført i USA og inkluderte personer i alderen 45 til 100 år. Endepunktene var insidens og mortalitet for
creeningsubstantiallydecreasescolorectalcancer (CRC)incidenceandmortalitythroughdetection ofCRCprecursorsandearly-stageCRC(1,2).TheU.S. PreventiveServicesTaskForce(USPSTF)providesa gradeArecommendationforCRCscreeningforages 50to75yearsandagradeBrecommendationforages 45to49years(3).DespitetheeffectivenessofCRC screening,approximately40%ofeligiblepersonsare notuptodatewithCRCscreeningintheUnitedStates. (4).Accesstoscreeningandpatientpreferences,includingtheacceptabilityofavailabletests,suchasthefecal immunochemicaltest(FIT),themultitargetstoolDNA test(MT-sDNA),orcolonoscopy,arepowerfuldeterminantsofscreeningparticipation(5,6).Emergingblood-basedandstool-basedtestscould altertheCRCscreeninglandscape(7).In2021,the CentersforMedicare&MedicaidServices(CMS) announcedtheywouldcoverCRCscreeningevery 3yearswithU.S.FoodandDrugAdministration (FDA)-approvedblood-basedtestswithsensitivity of74%ormoreandspecificityof90%ormorefor CRC(8).TheFDAapprovedanovelcell-freeDNA bloodtest(cf-bDNA;GuardantShield)forCRCscreeningon29July2024(9).Thistest,whichhashighsensitivityforCRCstagesIItoIVbutnotstageI(65%)orCRC precursors(10),becamecommerciallyavailableatalist priceof$1495on1August2024(11).Inthischanging landscape,tradeoffsemergebetweentests ’ abilitiesto
kolorektalkreft, QALY’s (qualityadjusted life years) og kostnader.
Resultatene viste at cf-bDNAtesten var dyrere og mindre effektiv enn de konvensjonelle metodene. Selv om cf-bDNAtesten var gunstig sammenlignet med ingen screening, ga den dårligere utkomme (mortalitet) sammenlignet med de konvensjonelle screeningsmetodene. Studien impliserer at klinikere bør fortsette å tilby alle metoder for kolorektal
Downloadedfromhttps://annals.orgbyUniversiteetsbiblIOsloon03/03/2025.
diagnostikk og ha samtaler med pasienten vedrørende preferanser for screeningsmetode.
Ytterligere analyser viste at cf-bDNA-testen kostet $90,000 per QALY oppnådd sammenlignet med ingen screening, mens alternative metoder var mindre kostbare og mer effektive. Studien konkluderte med at første generasjons cf-bDNA-tester kan gi netto nytte eller skade, avhengig av alternative screeningtiltak.
Background:Cell-freeDNAbloodtests(cf-bDNA)and next-generationstooltestscouldchangecolorectal cancer(CRC)screening.
of
Objective: impactsofnovelCRCscreeningtests.ToestimatetheclinicalandeconomicDesign: Cost-effectivenessanalysisusingMOSAIC (ModelofScreeningandSurveillanceforColorectal Cancer).
ProjectedImpactandCost-EffectivenessofNovelMolecularBloodBasedorStool-BasedScreeningTestsforColorectalCancer
Wang W et al. Ann Intern Med 2024; 177: 1016-1028
UriLadabaum,MD,MS;AjithaMannalithara,PhD;RobertE.Schoen,MD,MPH;JasonA.Dominitz,MD,MHS;and
Denne artikkelen undersøkte sammenhengen mellom bruk av semaglutid og forekomsten av medisinske intervensjoner forårsaket av tobakk-avhengighet hos pasienter med diabetes type 2. Forskerne analyserte elektroniske journaler til 222 942 nye brukere av antidiabetisk medikasjon, deriblant 5967 som brukte semaglutid. Resultatene viste at semaglutid-brukere hadde færre konsultasjoner relatert til sin tobakk-avhengighet
Datasources: Publisheddata.TargetPopulation:Average-riskpersons. TimeHorizon:Ages45to100years. Perspective: Healthsector. Intervention: NovelversusestablishedCRCscreen- ingtests.
enn de som brukte andre antidiabetika. I tillegg fikk pasientene i semaglutid-gruppen færre resepter på røykesluttmedisiner og hadde mindre behov for røykesluttveiledning. Disse funnene var uavhengige av fedme. For de fleste var reduksjonen synlig innen 30 dager etter oppstart behandling med semaglutid.
OutcomeMeasures: quality-adjustedlife-years(QALYs),costs.IncidenceandmortalityofCRC, ResultsofBase-CaseAnalysis:Forcolonoscopyevery 10years,annualfecalimmunochemicaltest(FIT), andtriennialnext-generationmultitargetstoolDNA, FIT-RNA,cf-bDNA(GuardantShield),orcf-bDNA (Freenome),therelativerates(RRs)and95%uncertaintyintervals(UIs)versusnoscreeningforCRC incidencewere0.21(0.19to0.22),0.29(0.27to 0.31),0.33(0.32to0.36),0.32(0.30to0.34),0.58 (0.55to0.61)and0.58(0.55to0.60),respectively; theRRsforCRCdeathwere0.19(0.17to0.20),
0.25(0.23to0.27),0.28(0.27to0.30),0.28(0.26to 0.30),0.44(0.42to0.47),and0.46(0.44to0.49), respectively.Thecf-bDNAtest(Shield;listprice $1495)cost$89600($74800to$102300)perQALY gainedversusnoscreening;alternativeswereless costlyandmoreeffective.
Disse funnene antyder at semaglutid kan ha en positiv effekt for å
oppnå røykeslutt, men ytterligere kliniske studier er nødvendige for å bekrefte dette. Studien konkluderte med at semaglutid-brukere hadde signifikant færre konsultasjoner relatert til tobakk-avhengighet, noe som kan indikere en potensiell nytteverdi av semaglutid i behandlingen av tobakk-avhengighet hos pasienter med diabetes type 2.
ResultsofSensitivityAnalysis: Incrementalcosts exceededincrementalbenefitswhennoveltestintervalswereshortenedto2or1years.Thecf-bDNAtest matchedFIT’
A Clinical
Qaseem A et al. Ann Intern Med 2024; 177: 658-666
Denne kliniske retningslinjen fra American College of Physicians (ACP) oppdaterer anbefalingene for nyere farmakologisk behandling av type 2 diabetes. Retningslinjen er basert på en systematisk gjennomgang av effekt og sikkerhet av nyere legemidler som glukagon-liknende peptid-1 (GLP1) agonister, en GLP-1 agonist og glukose-avhengig insulinotrofisk polypeptid (GIP) agonist, natriumglukose cotransportør-2 (SGLT-2) hemmere, dipeptidyl peptidase-4 (DPP-4) inhibitorer, og langtidsvirkende insulin. Disse legemidlene ble vurdert både som monoterapi og i kombinasjon med andre medisiner.
1.40)-foldFITsimpactonCRCmortalityat1.35(1.30to ’ suptakerate,assumingequalcolonoscopy follow-up.Ifpersonswhoacceptcolonoscopyorstool testsshiftedtocf-bDNA,CRCdeathsincreased.This adverseeffectwasovercomeifevery3suchsubstitutionswerecounterbalancedbycf-bDNAuptakeby 2ormorepersonsrefusingalternatives,assuming equalcolonoscopyfollow-up.
Retningslinjen prioriterte utfall som total-mortalitet, alvorlige kardiovaskulære hendelser, hjerteinfarkt, hjerneslag, sykehusinnleggelse grunnet hjertesvikt med stuvning, forverring av kronisk nyresykdom, alvorlige bivirkninger og alvorlig hypoglykemi. Prosentandelen av deltakere som oppnådde minst 10% vekttap var også et prioritert utfall, men data var ikke tilstrekkelig til metaanalyser og ble ikke gradert utfra GRADE-kriteriene.
Limitation: Longitudinaltest-specificparticipationpatternsareunknown.
PrimaryFundingSource:TheGorrindoFamilyFund. AnnInternMed.
Conclusion:First-generationcf-bDNAtestsmaydeliver netbenefitorharm,dependingonthebalance betweenachievingscreeninginpersonswhodecline alternativesversussubstitutingcf-bDNAformore effectivealternatives.
Forauthor,article,anddisclosureinformation,seeendoftext.2024;177:1610-1620.doi:10.7326/ANNALS-24-00910 Thisarticlewaspublishedat Annals.org on29October2024. creeningsubstantiallydecreasescolorectalcancer (CRC)incidenceandmortalitythroughdetection ofCRCprecursorsandearly-stageCRC(1,2).TheU.S. PreventiveServicesTaskForce(USPSTF)providesa gradeArecommendationforCRCscreeningforages 50to75yearsandagradeBrecommendationforages 45to49years(3).DespitetheeffectivenessofCRC screening,approximately40%ofeligiblepersonsare notuptodatewithCRCscreeningintheUnitedStates. (4).Accesstoscreeningandpatientpreferences,includingtheacceptabilityofavailabletests,suchasthefecal immunochemicaltest(FIT),themultitargetstoolDNA test(MT-sDNA),orcolonoscopy,arepowerfuldeterminantsofscreeningparticipation(5,6).
ACP anbefaler å legge til SGLT-2 inhibitor eller GLP-1 agonist til metformin og livsstils-modifisering hos voksne med type 2 diabetes med utilstrekkelig glykemisk
Medication-Induced Weight Change Across Common Antidepressant Treatments
Petimar J, et al. Ann Intern Med 2024; 177: 1209-1221
kontroll. Bruk av SGLT-2 hemmer reduserer risikoen for total-mortalitet, alvorlige kardiovaskulære hendelser, forverring av kronisk nyresykdom og sykehusinnleggelse på grunn av hjertesvikt med stuvning. Bruk av GLP-1 agonist reduserer risikoen for totalmortalitet, alvorlige kardiovaskulære hendelser og hjerneslag. ACP fraråder å legge til DPP-4 inhibitor til metformin og livsstilsmodifisering hos voksne med diabetes type 2 og utilstrekkelig glykemisk kontroll for å redusere morbiditet og mortalitet.
Emergingblood-basedandstool-basedtestscould altertheCRCscreeninglandscape(7).In2021,the CentersforMedicare&MedicaidServices(CMS) announcedtheywouldcoverCRCscreeningevery 3yearswithU.S.FoodandDrugAdministration (FDA)-approvedblood-basedtestswithsensitivity of74%ormoreandspeci
Denne studien undersøkte endringer i vekt som følge av behandling med ulike førstelinje antidepressiva. Forskerne analyserte helsejournalene til 183 118 pasienter som hadde startet behandling med ett av åtte vanlige antidepressiva. Resultatene etter seks måneder viste at sertralin var
ficityof90%ormorefor CRC(8).TheFDAapprovedanovelcell-freeDNA bloodtest(cf-bDNA;GuardantShield)forCRCscreeningon29July2024(9).Thistest,whichhashighsensitivityforCRCstagesIItoIVbutnotstageI(65%)orCRC precursors(10),becamecommerciallyavailableatalist priceof$1495on1August2024(11).Inthischanging landscape,tradeoffsemergebetweentests’ abilitiesto
Downloadedfromhttps://annals.orgbyUniversiteetsbiblIOsloon03/03/2025.
assosiert med minst vekt økning, mens bupropion var assosiert med en liten vektnedgang. Andre antidepressiva som escitalopram, paroksetin, duloksetin, venlafaksin og citalopram viste en noe høyere vektøkning enn sertralin, mens fluoksetin hadde samme effekt. Studien konkluderte med at det
var små forskjeller mellom de åtte studerte førstelinje antidepressiva, men at bupropion konsekvent kom best ut mhp vekt. Ved oppstart av antidepressiv behandling bør klinikere vurdere potensialet for vektøkning og overvåke vektendringer hos pasientene.
ProjectedImpactandCost-EffectivenessofNovelMolecularBloodBasedorStool-BasedScreeningTestsforColorectalCancer UriLadabaum,MD,MS;AjithaMannalithara,PhD;RobertE.Schoen,MD,MPH;JasonA.Dominitz,MD,MHS;and
Artificial Intelligence in the Provision of Health Care: An American College of Physicians Policy Position Paper
Daneshvar N, et al. Ann Intern Med 2024; 177: 964-967
NovelversusestablishedCRCscreenIncidenceandmortalityofCRC, Forcolonoscopyevery 10years,annualfecalimmunochemicaltest(FIT), andtriennialnext-generationmultitargetstoolDNA, FIT-RNA,cf-bDNA(GuardantShield),orcf-bDNA (Freenome),therelativerates(RRs)and95%uncertaintyintervals(UIs)versusnoscreeningforCRC incidencewere0.21(0.19to0.22),0.29(0.27to 0.31),0.33(0.32to0.36),0.32(0.30to0.34),0.58 (0.55to0.61)and0.58(0.55to0.60),respectively; theRRsforCRCdeathwere0.19(0.17to0.20), 0.25(0.23to0.27),0.28(0.27to0.30),0.28(0.26to 0.30),0.44(0.42to0.47),and0.46(0.44to0.49), respectively.Thecf-bDNAtest(Shield;listprice $1495)cost$89600($74800to$102300)perQALY gainedversusnoscreening;alternativeswereless costlyandmoreeffective.
Denne artikkelen er et synopsis fra American College of Physicians (ACP) sitt position paper, som ble utarbeidet etter en bred gjennomgang av kunstig intelligens (KI) innen indremedisin. ACP anerkjenner at KI og maskinlæring har vært i utvikling siden 1970-tallet, og at bruken og interessen har økt betydelig siden 2020, spesielt etter introduksjonen av ChatGPT. KI har blitt utprøvd og integrert i økende grad i ulike deler av helsevesenet, og ACP ser at det kan være et nyttig supplement til beslutningsstøtte.
ResultsofSensitivityAnalysis: Incrementalcosts exceededincrementalbenefitswhennoveltestintervalswereshortenedto2or1years.Thecf-bDNAtest matchedFIT’simpactonCRCmortalityat1.35(1.30to 1.40)-foldFIT ’suptakerate,assumingequalcolonoscopy follow-up.Ifpersonswhoacceptcolonoscopyorstool testsshiftedtocf-bDNA,CRCdeathsincreased.This adverseeffectwasovercomeifevery3suchsubstitutionswerecounterbalancedbycf-bDNAuptakeby 2ormorepersonsrefusingalternatives,assuming equalcolonoscopyfollow-up.
ACP har utarbeidet 10 anbefalinger for bruk av KI i helsevesenet. Disse inkluderer at KI-teknologi bør supplere og ikke erstatte klinikerens logikk og beslutningstaking, at utvikling, testing og bruk av KI må følge medisinsk etiske prinsipper, og at det trengs åpenhet innen dette feltet for å fremme et godt pasient-lege-forhold. Videre må alle ledd fremme personvern og konfidensialitet, og valører som klinisk sikkerhet, effekt, samt helselikhet må ha topp-prioritet. ACP understreker at KI bør minske fremfor å forsterke ulikheter innen
Limitation: Longitudinaltest-specificparticipationpatternsareunknown.
helse og helseomsorg, og at utviklere må stå til ansvar for sine modellers prestasjon. Alle trinn i utvikling og bruk bør designes for å redusere den kliniske byrden, og opplæring må gis på alle nivåer av medisinsk utdanning. Til slutt må miljømessige sider vurderes.
ACP konkluderer med at utstrakt forskning er nødvendig for å kartlegge risikoaspekter og nytteverdi av KI på kort og lang sikt.
Conclusion: First-generationcf-bDNAtestsmaydeliver netbenefitorharm,dependingonthebalance betweenachievingscreeninginpersonswhodecline alternativesversussubstitutingcf-bDNAformore effectivealternatives. PrimaryFundingSource:TheGorrindoFamilyFund.
Barry H, et al. Ann Intern Med. 2024 Jul;177(7):901-910
AnnInternMed.
Denne studien undersøkte effekten av ekstrem varme på blodstrøm i myokard og kardiovaskulær funksjon. Ekstremvarme og hetebølger er assosiert med økt risiko for kardiovaskulær død, og formålet med studien var å kvantifisere behovene for myokardial blodstrøm ved ekstremvarme. Studien ble utført på 61 deltakere: 20 friske unge voksne (gjennomsnittsalder 28 år), 21 friske eldre voksne (gjennomsnittsalder 67 år) og
20 eldre voksne med koronarsykdom (gjennomsnittsalder 70 år). Deltakerne ble varmet opp til kjernetemperaturen hadde økt med 1,5 °C, og myokardial blodstrøm ble målt med positron emisjons tomografi før varme-eksponering og for hver 0,5°C økning i kjernetemperatur.
Resultatene viste en nesten dobling i myokardial blodstrøm ved en økning i kjernetemperatur
Forauthor,article,anddisclosureinformation,seeendoftext.2024;177:1610-1620.doi:10.7326/ANNALS-24-00910 Thisarticlewaspublishedat Annals.org on29October2024. creeningsubstantiallydecreasescolorectalcancer (CRC)incidenceandmortalitythroughdetection ofCRCprecursorsandearly-stageCRC(1,2).TheU.S. PreventiveServicesTaskForce(USPSTF)providesa gradeArecommendationforCRCscreeningforages 50to75yearsandagradeBrecommendationforages 45to49years(3).DespitetheeffectivenessofCRC screening,approximately40%ofeligiblepersonsare notuptodatewithCRCscreeningintheUnitedStates. (4).Accesstoscreeningandpatientpreferences,includingtheacceptabilityofavailabletests,suchasthefecal immunochemicaltest(FIT),themultitargetstoolDNA test(MT-sDNA),orcolonoscopy,arepowerfuldeterminantsofscreeningparticipation(5,6).Emergingblood-basedandstool-basedtestscould altertheCRCscreeninglandscape(7).In2021,the CentersforMedicare&MedicaidServices(CMS) announcedtheywouldcoverCRCscreeningevery 3yearswithU.S.FoodandDrugAdministration (FDA)-approvedblood-basedtestswithsensitivity of74%ormoreandspecificityof90%ormorefor CRC(8).TheFDAapprovedanovelcell-freeDNA bloodtest(cf-bDNA;GuardantShield)forCRCscreeningon29July2024(9).Thistest,whichhashighsensitivityforCRCstagesIItoIVbutnotstageI(65%)orCRC precursors(10),becamecommerciallyavailableatalist priceof$1495on1August2024(11).Inthischanging landscape,tradeoffsemergebetweentests ’ abilitiesto
på 1,5°C. Endringene i blodstrømmen var ikke forskjellige for alder eller koronar sykdom, men hos noen eldre med koronarsykdom kunne det observeres asymptomatisk myokardiskemi. Forfatterne konkluderte med at passiv ekstrem varmeksponering øker myokardial blodstrøm og kan predisponere noen eldre voksne med koronarsykdom for asymptomatisk myokardiskemi.
Artificial intelligence-Assisted Colonoscopy for Polyp Detection
Soleymanjahi, et al. Ann Intern Med 2024; 177: 1652-1663
Kolorektal kreft er den fjerde hyppigste krefttypen i USA og den nest ledende årsaken til kreftdød. Koloskopi står her sentralt i diagnostikk og terapi, og flere studier har undersøkt bruk av data assistert koloskopi med KI-teknologi. Denne systematiske oversiktsartikkelen og meta analysen sammenlignet dataassistert koloskopi med konvensjonell koloskopi i randomiserte kontrollerte studier. Etter omfattende litteratursøk inkluderte metaanalysen 36 201 deltakere i 44
studier. Med data-støttet koloskopi ble det identifisert flere adenomer (0,98 versus 0,78) per koloskopi, og koloskopiene hadde en høyere deteksjonsrate (45% versus 37%). Det var små forskjeller med hensyn til funn av avansert neoplasi per koloskopi (0,16 og 0,15), men KIstøtte viste litt høyere deteksjonsrate (12,7% versus 11,5%). Videre fant man to ikke-neoplastiske polypper per ti koloskopier, og tilbaketrekkingstiden var litt lenger (0,53 min). Studiene viste signifi-
Downloadedfromhttps://annals.orgbyUniversiteetsbiblIOsloon03/03/2025.
kant heterogenitet for kvalitet og utvalgstørrelse.
Forfatterne konkluderte med at KI-støttet koloskopi forbedrer deteksjonsraten for adenomer og polypper, med litt lenger prosedyretid, mens effekten på neoplasier var begrenset. Deteksjonsraten var høyere i noen enkeltstudier, eldre studier og fra Kina. Fremtidige studier anbefales å fokusere på viktige kliniske utfall, og at studiene randomiserer leger fremfor pasienter.

Helsedirektoratet anbefaler at DIFICLIR vurderes til behandling av C. difficileinfeksjon (CDI) hos pasienter på sykehus og med høy risiko for residiv

Vennligst se retningslinjer for fullstendig behandlingsanbefaling
Elektronisk søknadsløsning for individuell refusjon, scan her
200 mg tabletter og granulat til mikstur, 40 mg/ml
Indikasjoner: For behandling av Clostridioides difficile-infeksjoner (CDI), også kjent som C. difficile-assosiert diaré (CDAD). Tabletter: Hos voksne og pediatriske pasienter med en kroppsvekt på minst 12,5 kg. Granulat: Hos voksne, ungdom og barn 0 - < 18 år. For både tabletter og granulat skal det tas hensyn til offisielle retningslinjer for korrekt bruk av antibakterielle midler. Vanligste bivirkninger: Vanlige: Forstoppelse, kvalme, oppkast Vanligste alvorlige bivirkninger: Overfølsomhetsreaksjoner inkl. alvorlig angioødem. Interaksjoner: Forsiktighet utvises ved samtidig bruk av potente P-gp-hemmere. Kontraindikasjoner: Overfølsomhet for innholdsstoffene. Forsiktighetsregler: Fidaksomicin bør brukes med forsiktighet ved kjent allergi mot makrolider. Hvis det oppstår en alvorlig allergisk reaksjon, skal legemidlet seponeres og egnede tiltak igangsettes. Bør brukes med forsiktighet ved pseudomembranøs kolitt eller fulminant eller livstruende CDI, ved nedsatt lever- og nyrefunksjon. Granulat bør brukes med forsiktighet hos spedbarn < 6 måneder/< 4 kg. Graviditet, amming og fertilitet: Graviditet: Det anbefales å unngå bruk under graviditet. Amming: Det må tas en beslutning om amming skal opphøre eller behandling avstås fra, basert på nytte-/risikovurdering. Fertilitet: Dyrestudier indikerer ingen effekt på fertilitet. Dosering: Tabletter: Standard dosering: Voksne og barn ≥12,5 kg: Anbefalt dose er 200 mg (1 tablett) administrert 2 ganger daglig (1 tablett hver 12. time) i 10 dager. Utvidet pulsdosering: Voksne: 200 mg tabletter administreres to ganger daglig for dag 1–5 (ingen tablett på dag 6) og deretter én gang daglig annenhver dag for dag 7–25. Hvis en dose blir glemt, skal den glemte dosen tas så snart som mulig, men hvis det snart er tid for neste dose, skal tabletten hoppes helt over. Granulat: Voksne: Standard dosering: Anbefalt dose er 200 mg (5 ml) 2 ganger daglig (5 ml hver 12. time) i 10 dager Utvidet pulsdosering: Tas 2 ganger daglig på dag 1-5 (ingen dose på dag 6) og deretter 1 gang daglig annenhver dag på dag 7-25. Ungdom og barn 0 - < 18 år: Anbe falt dose baseres på kroppsvekt og tas 2 ganger daglig (1 dose hver 12. time) i 10 dager. Administrering: Tabletter: Kan tas med eller uten mat. Svelges hele sammen med et glass vann. Granulat: Rekonstitueres av farmasøyt eller helsepersonell. Tas peroralt, med eller uten mat, eller ved behov via en enteral sonde med sprøyte. Pakninger og priser: Tabletter 20 stk. (blister) kr 18 099,90. Granulat til mikstur: 1 stk. (glassflaske) kr 18 288,90. Reseptgruppe C. DIFICLIR er tilgjengelig til rabattert pris via LIS-anbud og er gjenstand for individuell refusjon for blå resept, for mer informasjon; se Helsedirektoratets hjemmeside. Basert på SPC godkjent av DMP/EMA: 01.12.2023.
For utfyllende informasjon om dosering, forsiktighetsregler, interaksjoner og bivirkninger - se felleskatalogen.no
Referanse: 1. https://www.helsedirektoratet.no/retningslinjer/antibiotika-i-sykehus/infeksjoner-i-abdomen#clostridioides-difficile-infeksjon. Sist faglig oppdatert 01.03.2022.
Tillotts Pharma AB | Gustavslundsv. 135, 167 51 Bromma, Sverige | Tel: +46 8-704 77 40 | nordicinfo@tillotts.com

Som nordmann har jeg alltid syntes det var litt flaut å innrømme at det lengste nord jeg har vært, er Molde. Heldigvis ga den indremedisinske vinterskolen meg ikke bare muligheten til å øke rekorden, men også knytte nye vennskap og lære enda mer om indremedisin.
Jostein Ibsen, Lege og Ph.d. kandidat ved OUS Rikshospitalet Bilder er tatt av arrangør og skolens deltakere. Trykkes med tillatelse
Årets Vinterskole tok meg med til Björkliden i Sverige, like over grensen fra Narvik. Her var 60 unge indremedisinere fra hele Europa samlet. Som eneste nordmann var det en spesiell opplevelse å legge ut på reisen, med en viss usikkerhet om hvordan uken ville bli. Før jeg forteller mer om mine egne opplevelser, kan det være nyttig med litt bakgrunnshistorie. Vinterskolen har vært et årlig tilbud fra European School of Internal
Medicine (ESIM) siden 2011. Den ble etablert etter suksessen til ESIMs sommerskole, som har røtter helt tilbake til 1998. Vinterskolen varer i syv dager og kombinerer undervisning, kurs og sosiale aktiviteter. Den er rettet mot yngre leger i spesialisering. Hvert tredje år flyttes den til et nytt vertsland i Europa. Årets vinterskole var den tredje og siste i rekken i Sverige.
Et sterkt faglig innhold
Dagene på vinterskolen var tettpakket med innhold. Et fantastisk program bestående av foredrag, workshops og diskusjoner var satt sammen av den svenske indremedisinske foreningen. Vi ble undervist i hvordan vi burde presentere forskning, utføre ultralyd undersøkelse, vurdere toxidromer, og så utrolig mye mer! Det er alltid vanskelig å trekke fram noen spesifikke høyde -


punkter når hele programmet var så godt satt sammen, men for meg som ung lege var det noen foredrag jeg kommer til å ta med meg videre mot en spesialisering. Aime Burbridge fra Storbritannia holdt en helt fantastisk og minneverdig presentasjon om det å gjøre feil som lege. Lærdommene og de erfaringene hun delte kommer både jeg og veldig mange av deltakerne til å huske.
Medisinske kasustikker var et fast innslag hver kveld gjennom hele uken. Deltakerne fra hvert land skulle også presentere en medisinsk case som man kunne ta lærdom av. Siden jeg var den eneste fra Norge, fikk jeg samarbeide med den svenske delegasjonen. Sammen presenterte vi en lærerik case om hjerneødem etter et lillehjerneinfarkt, som i
starten ble maskert av opioid smertestillende. Det var en god blanding av kasustikker - alt fra vanlige sykdommer som pneumothroax til sjeldne tilstander som hemofagocytisk lymfohistiocytose (HLH), og til og med noen ganske morsomme caser som cerebral vasospasme utløst av Carolina Reaper (kraftig chili).
Ulikhetene i helsevesenet Noe av det mest interessante man får oppleve ved å tilbringe en uke sammen med leger fra resten av Europa, er alle ulikhetene - både på godt og vondt. Blant annet ble jeg svært fascinert av hvor praktisk Sveriges løsning med en digital reseptformidler på mobilen var. Hvor enkelt og behagelig det var å kunne forskrive et legemiddel og deretter bekrefte med BankID.




Diskusjonen under workshopen om frailty (skrøpelighet) brakte også frem mange kontraster. Her dreide samtalen seg om hva som er etisk riktig og hvordan pasienter i livets siste faser bør behandles. Det var stor forskjell fra land til land på om målet var å gi pasienter et lengst mulig liv, eller om mest mulig livskvalitet og en verdig slutt skulle stå i sentrum. Det var spesielt å se hvordan enkelte land, både på grunn av lovverk og forventninger fra pasienters familie, var langt mer tilbakeholdne med å avslutte behandling hos skrøpelige pasienter - også i tilfeller der pasienten selv ikke ønsker livsforlengelse.
Noen foredrag var kanskje mer relevante for legene som kom enda mer sørfra enn meg, slik som “Living in cold climate”. Her må det vel være lov å si at det meste allerede var ganske kjent og hverdagslig.
Venner for livet:
Nå må det ikke glemmes at det sosiale også sto sterkt under årets vinterskole. Når man samler 60 leger som ikke kjenner hverandre fra før, skapes
det en unik mulighet til å bygge nye vennskap og samarbeid. Det er lett å si at vinterskolen ikke hadde vært det samme uten de andre fantastiske deltakerne. Vinterskolen hadde ikke bare et tettpakket faglig program, men også et sosialt program fullt av opplevelser. Allerede på mandagen startet vi med trugevandring og snøballkrig. På programmet sto også sauna, isbading, karaoke, ski, salsaog så utrolig mye mer!
Nordlys vandring:
En av de første beskjedene vi fikk etter å ha ankommet Bjørkliden var fra vår nordlysguide: “Jeg må bare være ærlig, utsiktene for nordlys denne uken er helt forferdelig!”. Heldigvis kan selv eksperter ta feil, for allerede to timer senere så vi ukens første nordlys. Resten av uken skuffet heller ikke! Hver kveld virket nordlyset bare sterkere og sterkere, og vi fikk oppleve helt spektakulære farger over hele nattehimmelen. Som sørlending var det en helt fantastisk opplevelse å få på sin første uke så langt nord!

Minner for livet
Før jeg reiste på ESIMs vinterskole 2025, tenkte jeg at en uke med fremmede kanskje var litt i lengste laget. På vei hjem igjen tenkte jeg bare: En uke med nye venner er alt for kort tid. Det fellesskapet og vennskapene vi skapte den uken, er noe vi vil ta med oss videre i arbeidslivet. Allerede er det gjort mange avtaler om å treffes igjen på tvers av landegrensene.
Vinterskolen har vært en uke der jeg har utviklet meg mye som lege, med
nye lærdommer og perspektiver jeg ikke har hatt tidligere. Jeg vil rette en stor takk til Norsk Indre medisinsk Forening for at jeg fikk denne muligheten! Jeg kan på det varmeste anbefale alle yngre og fremtidige indremedisinere å delta! Dette er ikke en opplevelse dere vil gå glipp av, og allerede om ett år kommer en ny mulighet. Kanskje neste års delegasjon blir enda større!



Som LIS kjenner vi utfordringer med arbeidspress, arbeidsbelastning, uforutsigbarhet, opplæring og utdanning, og tilbakemeldinger. Disse temaene fikk bred oppmerksomhet i både offentlige og sosiale medier i forbindelse med aksjonen #Legermåleve i 2023. Helseledere og arbeidstakere vil endre, men hva, og hvordan skal vi gjøre det?
Cathrine Kristoffersen, lege i spesialisering geriatri, Sykehuset i Vestfold og prosjektleder for innovasjonsprosjektet «Velkommen til oss – Fadderordning for LIS» i regi av HSØ. – cathkr@siv.no
Etter å ha jobbet som LIS i medisin siden 2018, har opplevelsen fra LISrollen vært todelt; på den ene siden med gode kollegaer og et spennende fag, og på den andre siden svært belastende og utfordrende arbeidsforhold. I april 2022 var jeg utbrenthet og ble langtidssykemeldt. Likevel var ønske om å komme tilbake til jobb stort, men da måtte noe endres.
Refleksjonene mine rundt hva som kunne endres startet for alvor i november 2021, da 19 av mine 30 kollegaer hadde sluttet i løpet av de siste 14 månedene. Hva kunne gjøres «her og nå» som ikke ville kreve lange
utredningsprosesser eller arbeidsgrupper? Ett av svarene kom fort – sørge for god velkomst, innføring og informasjon om rollen som LIS og sørge for kollegial støtte – alt det jeg selv manglet, og helt fra start.
Starten på fadderordningen Som et resultat startet vi derfor i mars 2023 en fadderordning for LIS2/3 ved medisinsk avdeling. Ordningen ble formet etter innspill fra LIS-gruppen og bygget på prinsippet «for LIS, av LIS og med LIS». Jeg ble «fadderansvarlig» og ledet ordningen i en 5 % frikjøpt stilling. Mine LIS-kollegaer stilte
frivillig som faddere. De fikk fri for å ta imot nyansatte på deres første arbeidsdag, og skulle følge opp etter to uker og seks måneder. Rådgiverne våre (tidligere kalt lederstøtte) skulle bidra med å fordele fadder til ny LIS og sende velkomstbrev med fadders og veileders kontaktinfo. Lederen vår fikk ingen direkte rolle, men var selvsagt godt orientert om ordningen.
Fadderordningens 4 deler
Del 1: Fadderansvarlig ringer til ny LIS ca. 14 dager før oppstart med informasjon om bakgrunn og hensikt med fadderordningen, informasjon om fadders rolle og første
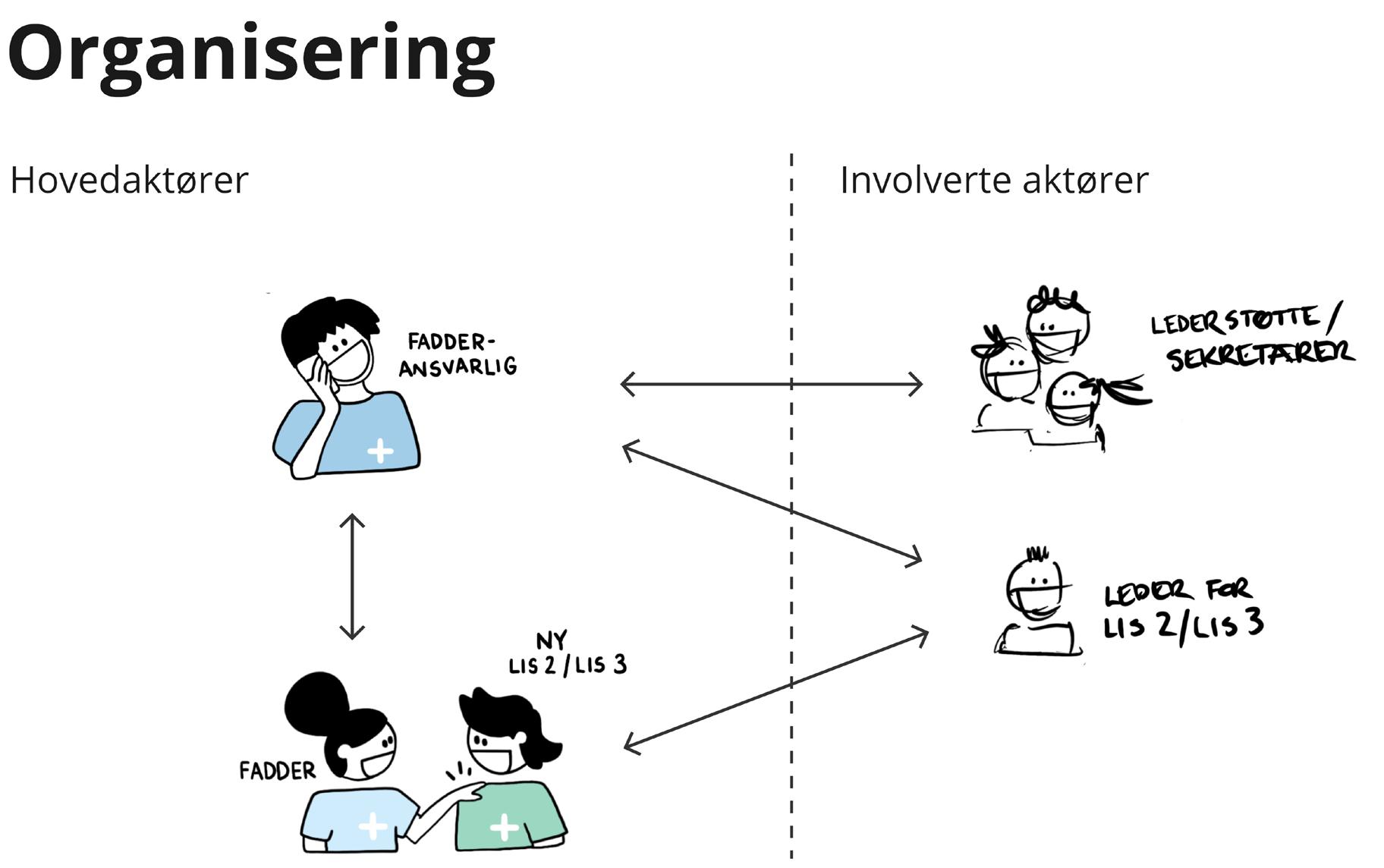
1. Organisering av involverte aktører. Illustratør Ida Husjord v/Sykehuset i Vestfold. Trykkes med tillatelse.
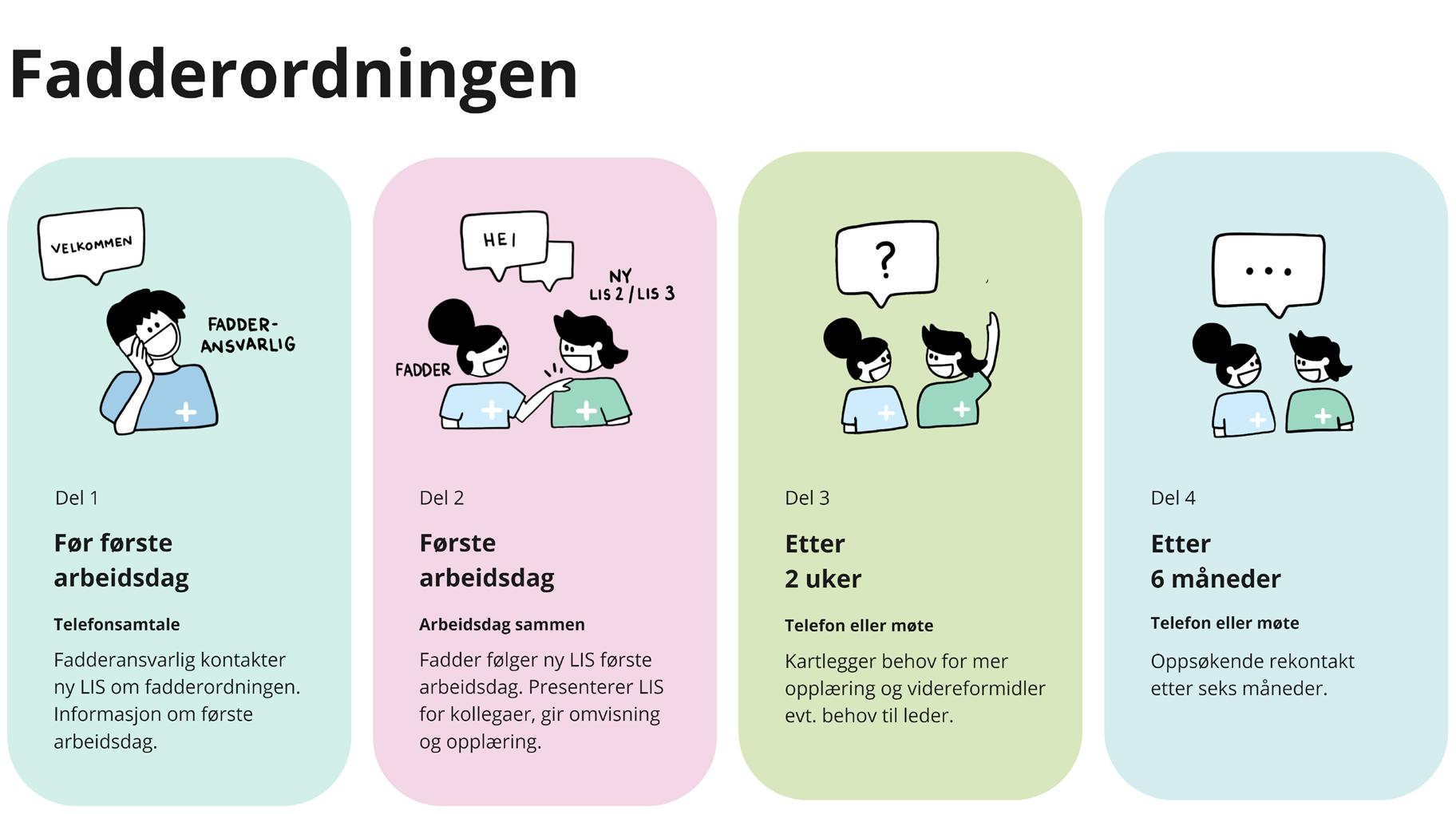
arbeidsdag. Forklarer at fadder er en støttende kollega man kan spørre om smått og stort, men som ikke erstatter tillitsvalgt, veileder eller leder.
Del 2: Første arbeidsdag. Hele første arbeidsdag tilbringes sammen med fadder. De følger en prosedyre for gjennomføring av dagen, slik at den blir lik uavhengig fadder. Prosedyren inneholder en mal for introduksjon, omvisning og gjennomgang av relevant informasjon om rollen som LIS2/3.
Del 3: Fadder tar kontakt med ny LIS mot slutten av opplæringsperioden på 14 dager, for å høre hvordan det har gått og forhører seg om behov for mer opplæring.
Del 4: Fadder har siste oppsøkende kontakt etter 6 måneder for å høre «hvordan går det, hvordan har du det, er det noe som er utfordrende eller vanskelig?».
Etter 1,5 år hadde vi ønsket 29 nye LIS velkommen. Kun seks av dem sluttet i samme periode. Arbeidsmiljøet ble merkbart bedre, turnoveren sank, og de nyansatte var overrasket over hvor godt de ble tatt
imot. Det at vi klarte å ansette nye og beholde disse medførte igjen lavere arbeidsbelastning for alle. Det var flere andre gode tiltak i samme periode, som egen leder for LIS, veiledning satt i system og et flott kontorlokale som samlingspunkt for LIS. Likevel tør jeg påstå at fadderordningen var sterkt medvirkende til den positive utviklingen. Det var utelukkende positive tilbakemeldinger.
Fra lokal løsning til nasjonal interesse
I oktober 2023 var fadderordningen ved SIV førstesideoppslag i Aftenposten (1). Dette førte til at Helse Sør-Øst RHF åpnet muligheten for at jeg kunne arbeide 50 % som prosjektleder for innovasjonsprosjektet «Velkommen til oss – Fadderordning for LIS» fra april 2024. Målet var å etablere fadderordning ved 50 % av medisinske avdelinger i løpet av første året, og ved voksenpsykiatrien andre året. Alle 20 medisinske avdelinger i HSØ var med i prosjektet allerede etter to måneder. I september 2024 hadde 14 av 20 sykehus tatt imot nye LIS med fadder. Interessen for prosjektet var langt større enn forventet.
Per januar 2025 har 3 av 9 aktuelle helseforetak i HSØ bekreftet at de vil etablere fadderordning for sine LIS2/3 på samtlige avdelinger (Syke huset Østfold HF, Sykehuset i Vestfold HF, Vestre Viken HF), og Lovisenberg Diakonale planlegger å bredde ordningen til flere avdelinger. Akershus universitetssykehus HF har som første sykehus startet fadderordning ved kirurgiske avdelinger.
Helse Nord RHF planlegger etablering av fadderordning for alle sine LIS, og jeg blir stadig kontaktet av andre som ønsker å etablere fadderordning. Prosjektdirektør Andreas Moan i Helse Sør-Øst har mange års erfaring innen helseinnovasjon og sier at han aldri før har sett et innovasjonsprosjekt spre seg så fort (3).
Hvordan står det egentlig til? Hvorfor har interessen for fadderordningen vært så stor? Min hypotese er at mange års effektivisering og stramme budsjetter har fjernet viktige elementer for et godt arbeidsog læringsmiljø, og at stadig mer komplekse pasientforløp har bidratt til ytterligere forverring. Mester har ikke lenger tid til sin svenn. Jeg tror også kulturen og holdningene som eksisterer blant oss leger, og andre
At en ny LIS opplever at arbeidsplassen har investert i en god start, sender et klart signal om hvordan arbeidsplassen verdsetter sine ansatte
helsearbeidere, stammer fra en ganske annen epoke og er utdatert. Men gammel vane er vond å vende, og jeg tror mange leger har opplevd å tilpasse seg en viss kultur, selv om det kan stride imot ens egen fornuft.
Hvis jeg som vakthavende lege får en telefon om en delirisk pasient, ville det være naturlig å spørre om miljøtiltakene og de basale behovene er på plass. Hvis ikke, må dette tas tak i først. Jeg tror helselederne, og vi som arbeidsgruppe, må ta et steg tilbake og reflektere: Ivaretar vi de basale behovene for oss ansatte som skal til for et godt lærings- og arbeidsmiljø? Og dersom det finnes planer eller prosedyrer for dette, hvordan oppleves de i praksis? Spesialisthelsetjenesteloven spesifiserer at sykehusene har fire hovedoppgaver (2), hvor én av dem er utdanning. Blir dette faktisk prioritert i den størrelsesorden som loven forutsetter? Hva slags tilbakemeldingskultur har vi, og i hvilken grad legger vi til rette for at ansatte kan bidra til positiv endring?
Helge Stene-Johansen, administrerende direktør ved sykehuset i Østfold, siteres i en NRK-artikkel (3) om fadderordningen, hvor journalisten spør om hvorfor det har tatt så lang tid før det har blitt gjort noe for de nyansatte legene og sier: «Det har med tradisjon å gjøre. Leger har bare fått inngangskortet i handa og blitt kasta rett ut i jobben». Jeg vil berømme han, som helseleder, som tør å kalle en «en spade for en spade», og som forsøker å skape endring
Alle leger skal ha opplæring. Travelt mottak eller ventelister på poliklinikk kan ikke gå foran.
Vi må selv skape endringen vi ønsker oss
Fadderordningen alene vil ikke løse «legekrisen», men jeg tror det er et godt sted å starte. Kultur og holdninger ved en arbeidsplass formes i stor grad av arbeidstakerne selv. Å legge premissene for en god kultur og gode holdninger allerede fra første arbeidsdag kan bidra til å snu en negativ trend eller motvirke ukultur. At en ny LIS opplever at arbeidsplassen har investert i en god start, sender et klart signal om hvordan arbeidsplassen verdsetter sine ansatte, og står i sterk kontrast til opplevelsen av å kun få «et inngangskort i handa og bli kasta rett ut i jobben».
Gjennom prosjektet mitt har jeg fått innsikt i flere utfordrende forhold for LIS-leger. Paradoksalt nok har jeg blitt noe fremtidspositiv, fordi mange av utfordringene jeg har hørt om kan løses – og de kan løses uten lange utredningsprosesser. Jeg har også sett at etablering av fadderordning kan fungere som en katalysator for andre gode tiltak, og at det finnes mange engasjerte og løsningsorienterte LIS og ledere. At tiltaket etableres og drives av de den skal gjelde for tror jeg er essensielt. Vi som står i utfordringene, vet best hvor skoen trykker, og derfor hvilken endring vi ønsker oss. Små, målrettede tiltak kan gjøre en stor forskjell, og det er nettopp derfor det er viktig at vi får være med på å forme løsningene.
Den samfunnsøkonomiske kostnaden knyttet til dårlig arbeidsmiljø ble i 2018 estimert til 75 milliarder kroner for Norge som helhet (4). Det ikke urealistisk å anta at kostnaden for et dårlig arbeidsmiljø ved våre sykehus også er betydelig. Derfor må vi sørge for et bærekraftig og godt arbeidsmiljø. En 5% frikjøpt stilling for en engasjert LIS som ønsker å bidra til dette bør derfor ikke være vanskelig å prioritere.
Jeg håper at dagens ledere tør å investere i tiltak som kan fremme gode arbeids- og læringsmiljø, positiv tilbakemeldingskultur og mer tid til utdannelse. Jeg tror også det kan være lurt å sørge for dette tidlig i arbeidsforholdet, for å legge gode premisser for fremtiden.
Jeg fryder meg over å jobbe i prosjektet, mest av alt fordi jeg blir så inspirert av alle menneskene jeg møter, som ønsker å bidra til positiv endring. Tenk hvilke enorme ressurser som finnes blant oss. Vi må legge til rette for at de kan bli brukt på en god måte.
Referanser
1 Sykehuslegen gikk rett i veggen. Mottrekket hennes kan redde liv, mener sjefen.
2 Sykehusenes hovedoppgaver - regjeringen.no
3 Korleis fadderordning kan redusere legemangel på sjukehus – NRK Østfold – Lokale nyheter, TV og radio
4 Samfunnsnytten-av-bedriftshelsetjenesten.pdf
Mens interessegruppene i Norsk endokrinologisk forening (NEF) kun har eksistert i fire år, så har en tverrfaglige Norsk tyroideagruppe (NTG) en lengre historie. Interessegruppene har som hovedoppgaver å bistå styret i NEF med høringsinnspill, aktivt bidra med forslag til aktiviteter i NEF regi, inkludert kurs og møter innenfor interessegruppens fagområde, og å arbeide for samordning og samarbeid med relevante spesialiteter. Dette siste gjordet NTG til fulle på Radiumhospitalet den 31.1.25 med et Nasjonalt Tyreoidea Symposium. Sara Hammerstad, Åse Tangerud og Eva Sigstad utgjorde arrangements- og programkomite og hadde satt sammen et rikholdig og aktuelt program.
Sara Hammerstad, Trine Finnes, Therese Weider
Over 100 deltakere møtte opp i M-auditoriet i forskningsbygget. Spesielt gledelig var den store andelen tilreisende og det tverrfaglige engasjementet. Her møtte både nukleærmedisinere, patologer, endokrinologer, fostermedisiner, øyeleger, nevrologer, barneleger og endokrine kirurger. Videreutvikling av faget uten pasienten i sentrum er meningsløst, og det var derfor også særlig prisverdig at også Stoffskifteforbundet ved generalsekretær
Mette Kaaby fikk frem sitt perspektiv på hva som rører seg og ikke rører seg innen forskning og behandling av tyreoidea sykdommer. Brukerrepresentasjon bør bli en selvfølge for fremtidige møter.
Det blir vanskelig å trekke frem noen høydepunkter fra programmet som strakk seg fra kombinasjonsbehandling ved hypotyreose ved Prof. Birte Nygaard Herlev-Gentofte
Sykehus og debatt om monobehandling med trijodtyronin til nye eksperimentelle kirurgiske metoder og stoffskiftesykdom i svangerskapet. Vi velger her å trekke frem oppsummeringen fra siste American Thyroid Association (ATA) møte 2024 i Chicago. Elin Naderi fra Oslo Universitets sykehus sto for rapporteringen. Der ble lagt hovedvekt på å presentere hva som er nytt i snarlig ventede oppdateringer av ATA- retningslinjer innen skjoldbruskkjertelkreft. Den gjeldende retningslinjen for håndtering av voksne pasienter med skjoldbruskkjertelknuter og differensiert skjoldbruskkjertelkreft vil deles opp i to separate retningslinjer. Retningslinjen for knutediagnostikk vil inneholde et revidert klassifikasjonssystem med tilhørende estimat for malignitetsrisiko og utvidet atlas. Retningslinjen for differensiert skjoldbruskkjertelkreft vil bl.a. inneholde nye anbe -
falinger for aktiv over våkning, omfang av kirurgi, tabeller for risikostratifisering og algoritmer for systemisk tumorrettet behandling. Den gjeldende retningslinjen for håndtering av medullær skjoldbruskkjertelkreft vil i første omgang oppdateres kun for kapittelet om systemisk tumorrettet behandling. Alle oppdateringer forventes publisert i løpet av det kommende året, og det var svært nyttig å få dette presentert muntlig i god tid med alle involverte faggrupper tilstede.
Vi håper at tverrfaglig Nasjonalt Tyreoidea Symposium i januar nå igjen er blitt en tradisjon, slik det var i pre-covid-tid.
Vennlig hilsen
Sara Hammerstad
Trine Finnes
Therese Weider





Norsk Nyremedisinsk Forening (NNF) teller 320 medlemmer. Vi er en liten, men stolt forening som nylig har rundet 50 år. Den interesserte leser vil lære mye om nyrefaget og om foreningen ved å gå inn på vår hjemmeside nephro.no.
Ivar Anders Eide, Leder Norsk Nyremedisinsk Forening

Norsk nyremedisin har omsider valgt å verve seg som fast bidragsyter til Indremedisineren. Det er økt oppmerksomhet om behovet for å screene risikopopulasjoner for proteinuri, økt bevissthet rundt samspillet mellom nyre og andre organer og ikke minst: Mange nye medikamenter i nyreverktøykassen de senere år. Bidrag til Indremedisineren er en fin mulighet til å formidle disse framskritt på til våre kolleger og en mulighet til å poengtere hva vi nyreleger vektlegger i utredning og behandling. Lovnad om faste bidrag gjør at vi også får lov å dele foreningsnytt. Til sist, og ikke minst, nyreleger er indremedisinere med bred faglig interesse. Norsk nefrologi hører derfor til i Indremedisineren!
Vårmøte og 50-års jubileum 2024 NNF avholder sitt Vårmøte annethvert år. Møtet i Trondheim juni 2024 var større og flottere enn vanlig: Vi hadde nemlig et 50-års lag å feire. Oppmøtet var stort og store internasjonale navn og flere norske nefrologer ga flotte bidrag til møtet. Jubileumsmiddagen ble avholdt på Rockheim etter en kvikk omvisning i museet. Den som ønsker å mimre og den som ønsker å vite mer vil finne at lenken «Historien til norsk nyremedisin» på vår hjemmeside er blitt oppdatert med et jubileumsskriv. Ålesund gjør seg klar for innrykk av norske nefrologer våren 2026.

Anders Hartmann utnevnt som æresmedlem Årsmøtet i november hadde privilegiet av å utnevne Professor Anders Hartmann som det tiende æresmedlem i NNF. Anders har hatt en enorm betydning for vår forening. Han er den lengstsittende lederen av foreningen, ga ut foreningens eget lille tidsskrift Nefrologisk Forum i en årrekke og sørget for at foreningen endret navn fra Norsk forening for nyresykdommer - vi er tross alt mot nyresykdommer – til dagens NNF. Anders har vært en bauta i norsk nefrologi. Han er en nestor i transplantasjonsmedisin med en stor vitenskapelig produksjon og en lang karriere som professor ved UiO og OUS Rikshospitalet bak seg. Mer enn noe annet: Anders har vært en vennlig, varm, tålmodig og samlende person i norsk nefrologi.
Nordiske nyredager i Oslo juni 2025
Hvert tiende år er det Norges tur til å være vertskap for den nordiske nyrekongressen NSN. I år er det igjen vår tur. Kongressen avholdes på Radisson Blu Scandinavia hotell ved Holbergs plass i Oslo fra onsdag 11. til lørdag 14. juni. Vi regner med rundt 400 besøkende. De kan se fram til store internasjonale navn, fremtredende nordiske forskere og et omfattende sosialt program. Kongressen er åpen for alle som er interessert i nyremedisin og du kan velge deltakelse en dag eller hele kongressen. Det er early bird påmelding med rabattert pris ut mars måned. Du finner mer om kongressen på NSN Oslo 2025





som tillegg til diett med redusert kaloriinntak og økt fysisk aktivitet1
gjennomsnittlig vektreduksjon opprettholdt i 2 år*2,3
Mer enn 1/3 av pasienter gikk ned 20 % eller mer med Wegovy®**2,3
Les mer på www.wegovy.no
* STEP 5: -2,6 % for placebo og -15,2 % for Wegovy®, som tillegg til diett med redusert kaloriinntak og økt fysisk aktivitet for begge grupper (500 kcal/dag + 150 min/ uke fysisk aktivitet + individuell oppfølging hver 4. uke) 12,6 % forskjell fra placebo, [KI 95 % -15,3; -9,8], p < 0,0001.2,3
** STEP 5: I uke 104 etter baseline oppnådde 74,7 % av pasientene et vekttap på ≥ 5 % (primært endepunkt), 59 % et vekttap på ≥ 10 % og 50 % et vekttap på ≥ 15 % (bekreftende sekundære endepunkt). 36 % av pasientene oppnådde et vekttap på ≥ 20 % ( supporterende sekundært endepunkt)2,3
Novo Nordisk Norway AS Nydalsveien 28 · NO-0484 Oslo Telefon: + 47 22185050 · Kundeservice: +47 2218 5051 · www.novonordisk.no
Indikasjon:
Voksne: Tillegg til diett med redusert kaloriinntak og økt fysisk aktivitet for vektkontroll, inkl. vekttap og vedlikehold av vekt, hos voksne med initial BMI ≥ 30 kg/m2 (fedme), eller ≥ 27 til < 30 kg/m2 (overvekt) ved forekomst av minst én vektrelatert komorbiditet, som dysglykemi (prediabetes eller diabetes mellitus type 2), hypertensjon, dyslipidemi, obstruktiv søvnapné eller kardiovaskulær sykdom.
For resultater fra studier vedrørende kardiovaskulær risikoreduksjon, fedmerelatert hjertesvikt og populasjoner som ble undersøkt, se pkt. 5.1 i Wegovy ® preparatomtale.
Ungdom (≥ 12 år): Tillegg til diett med redusert kaloriinntak og økt fysisk aktivitet for vektkontroll hos ungdom ≥ 12 år med fedme1 og kroppsvekt > 60 kg. Behandling skal seponeres og reevalueres etter 12 uker dersom ungdomspasienten ikke oppnår en reduksjon i BMI på minst 5 % etter 12 ukers behandling med (Wegovy ®) 2,4 mg eller maks. tolererte dose.1
Fedme (BMI ≥ 95-prosentil) som definert i kjønns- og aldersspesifikk BMI-vekstkurve (CDC.gov).
Wegovy® – utvalgt sikkerhetsinformasjon
De hyppigst rapporterte bivirkningene var gastrointestinale (svært vanlige, ≥ 1/10), inkludert kvalme, diaré, forstoppelse, oppkast og magesmerter. Generelt milde eller moderate i alvorlighetsgrad, og av kort varighet. Årsak til seponering hos 4,3 %. Kan forårsake dehydrering som i sjeldne tilfeller kan forverre nyrefunksjon. Unngå væskemangel
• Andre svært vanlige (≥ 1/10) bivirkninger: Hodepine, fatigue
• Andre vanlige (≥ 1/100 til < 1/10) bivirkninger: Dysestesi, dysgeusi, svimmelhet, gastritt, gastroøsofageal reflukssykdom, dyspepsi, raping, flatulens, abdominal distensjon, gallestein, hårtap, reaksjoner på injeksjonsstedet. Hos pasienter med diabetes type 2: hypoglykemi (særlig i kombinasjon med insulin eller sulfonylurea), retinopati
Gallestein: Vanlig bivirkning ved bruk av semaglutid. Ble rapportert hos 1,6 % av de som fikk semaglutid og 1,1 % hos de som fikk placebo. Førte til kolecystitt hos 0,6 % og 0,3 % hos de som fikk henholdsvis semaglutid og placebo
• Pankreatitt: 0,2 % for semaglutid og < 0,1 % for placebo. I den kardiovaskulære endepunktsstudien SELECT var frekvensen av akutt pankreatitt, bekreftet ved avklaring (adjudikering), 0,2 % for semaglutid og 0,3 % for placebo. Ved mistanke bør semaglutid seponeres. Semaglutid skal ikke gjenopptas etter bekreftet pankreatitt. Forsiktighet bør utvises hos pasienter som tidligere har hatt pankreatitt
• Tarmobstruksjon: En alvorlig form for forstoppelse med tilleggssymptomer som magesmerte, oppblåsthet og oppkast. Rapportert med ukjent frekvens etter markedsføring
Puls: Gjennomsnittlig økning på 3 slag per minutt observert
• Skal ikke brukes av gravide eller ved amming. Semaglutid skal på grunn av den lange halveringstiden seponeres minst 2 måneder før en planlagt graviditet
• Forsiktighet bør utvises hos pasienter med inflammatorisk tarmsykdom eller gastroparese Ungdom (12 - < 18 år): Generelt var frekvens, type og alvorlighetsgrad av bivirkninger hos ungdom tilsvarende det som sees hos voksne. Gallestein ble sett hos 3,8 % av pasientene behandlet med Wegovy® og 0 % behandlet med placebo. Ingen effekt på vekst eller pubertetsutvikling ble funnet etter 68 uker med behandling
Dosering – én gang per uke
Alder
Nyrefunksjon
Hjertesvikt
Leverfunksjon
Kan benyttes uten dosejustering
Voksne og ungdom ≥ 12 år
Begrenset erfaring hos pasienter ≥ 85 år
Lett og moderat nedsatt eGFR > 30 ml/min 1,73m2
Anbefales ikke
Barn/ungdom under 12 år
Alvorlig nedsatt, eller terminal nyresykdom eGFR < 30 ml/min 1,73m2
NYHA klasse I-III NYHA klasse IV
Lett og moderat nedsatt Forsiktighet bør utvises
Alvorlig nedsatt
Diabetes Diabetes type 2 Diabetes type 1
Wegovy® skal injiseres subkutant i abdomen, i låret eller i overarmen og administreres én gang per uke når som helst i løpet av dagen, til måltid eller utenom måltid. For å redusere sannsynligheten for gastrointestinale symptomer bør dosen trappes opp i løpet av en 16-ukers periode til en vedlikeholdsdose på 2,4 mg én gang per uke.
For ungdom i alderen 12 år og eldre benyttes samme doseopptrappingsplan som for voksne. Dosen bør økes opptil 2,4 mg, eller til maksimalt tolererte dose oppnås. Se preparatomtale for mer informasjon om dosering.
Reseptgruppe og pris
Legemiddelgruppe: GLP-1-analog Reseptgruppe: C ATC-nr.: A10B J06
Pakninger og priser: 0,25 mg: 1,5 ml (ferdigfylt penn) kr 1773,50. 0,5 mg: 1,5 ml (ferdigfylt penn) kr 1773,50. 1 mg: 3 ml (ferdigfylt penn) kr 1773,50. 1,7 mg: ml (ferdigfylt penn) kr 2597,20. 2,4 mg: 3 ml (ferdigfylt penn) kr 3189,40 (Priser per desember 2024).
Behandling med Wegovy® er ikke refundert og kan ikke skrives på blå resept
For individuell stønad se vedlegg 1 til folketrygdloven § 5-14 (legemiddellisten) på www.helsedirektoratet.no4
Referanser 1. Wegovy® SPC, avsnitt 4.1 2. Wegovy® SPC, avsnitt 5.1 3. Garvey WT, Batterham RL, Bhatta M, et al. Two-year effects of semaglutide in adults with overweight or obesity (STEP 5) Nature medicine 2022; 28(10), 2083-2091 4. Informasjon om vilkår for individuell refusjon er hentet fra: https://www.helsedirektoratet.no/rundskriv/kapittel-5-stonad-vedhelsetjenester/vedlegg-1-til--5-14- legemiddellisten/virkestoffer/semaglutid (Lest 06.12.2024)
ATTR-CM behandling med fem års overlevelsesdata3
TRANSTYRETIN AMYLOID KARDIOMYOPATI (ATTR-CM) ER EN UNDERDIAGNOSTISERT ÅRSAK TIL HJERTESVIKT1,2
Etter 30 måneder reduserte Vyndaqel risiko vs. placebo for 4,‡:
Død uansett årsak

Kardiovaskulære sykehusinnleggelser


HR: 0,70 (95 % KI: 0,51-0,96)



Relativ risikoratio: 0,68 (95 % CI 0,56-0,81)
Etter fem år var relativ risikoreduksjon for død uansett årsak 41 % (HR: 0,59 (95% KI: 0,44-0,79))3
Se et variert utvalg av foredrag som dekker ulike emner innen kardiologi
▼Vyndaqel® (tafamidis) 61 mg er indisert til behandling av villtype eller arvelig transtyretin amyloid kardiomyopati (ATTR-CM). Anbefalt dosering er 1 kapsel 1 gang daglig. Forsiktighet anbefales ved alvorlig nedsatt leverfunksjon. Kan gi interaksjoner ved klinisk relevante konsentrasjoner med BCRP-substrater (f.eks. metotreksat, rosuvastatin, imatinib). Utvalgte bivirkninger: Økte verdier i leverfunksjonsprøver og reduksjon i tyroksin kan forekomme. Pris: Det er fremforhandlet en konfidensiell, kostnadseffektiv pris til norske helseforetak og enkelte private sykehus. Denne er betydelig lavere enn maksimal utsalgspris i apotek, som er kr 129 737,10.
Pakning: Myke kapsler, 30 stk. Reseptgruppe: C. Refusjon: H-resept. ICD10: E85
Kriterier for forskrivning på H-resept:
1. Oppstart av behandling kan kun gjøres av kardiolog med erfaring i behandling av transtyretin amyloidose (ATTR), ansatt ved universitetssykehus eller annet helseforetak med kardiologisk enhet med kompetanse på behandling for denne pasientgruppen.Pasienten må ha en sikkert diagnostisert ATTR kardiomyopati, vanligvis med nukleærmedisinsk påvist amyloid i myokard. Pasienten skal ved oppstart være i NYHA-klasse I eller II.
2. Pasienten må ha en sikkert diagnostisert ATTR kardiomyopati, vanligvis med nukleærmedisinsk påvist amyloid i myokard. Pasienten skal ved oppstart være i NYHA-klasse I eller II.
3. Pasienten skal ha en forventet gjenstående levetid betydelig over 18 måneder.
4. Ved progresjon til vedvarende (minst 6 måneder) NYHA-klasse III, skal beslutning om å fortsette behandlingen tas i samråd med kardiolog med erfaring i behandling av ATTR, ansatt ve universitetssykehus eller annet helseforetak med kardiologisk enhet med kompetanse på behandling for denne pasientgruppen.
5. Ved rask progresjon til vedvarende NYHA-klasse III i løpet av 6 måneder etter initiert behandling, bør behandlingen avsluttes.
Før forskrivning, konsulter preparatomtalen på www.legemiddelsok.no
‡Hjertetransplantasjon, kombinert hjerte- og levertransplantasjon og hjertemekanisk hjelpemiddelimplantasjon (CMAD) ble behandlet som likeverdig med død i denne analysen. ATTR-ACT=Tafamidis in Transthyretin Cardiomyopathy Clinical Trial; TTR=Transtyretin; HR=Hazard ratio Referanser: 1. Witteles RM, et al. JACC Heart Fail. 2019;7(8):709-716. 2. Maurer MS, et al. J Am Coll Cardiol. 2016;68(2):161-172. 3. Eliott P, et al. Long-term survival with tafamidis in patients with transthyretin amyloid cardiomyopathy. Circ Heart Fail. 2022;15:4-11. 4. Maurer MS, et al. N Engl J Med. 2018;379(11):1007-1016.