MEDICINA LABORATORIAL
Da Prescrição à Interpretação Clínica





Rui Abrantes Pimentel
Licenciado em Medicina pela Faculdade de Medicina da Universidade de Lisboa; Internato Complementar de Patologia Clínica no Serviço de Patologia Clínica do Hospital de São José; Grau de Assistente Hospitalar de Patologia Clínica pelo Hospital Curry Cabral, EPE; Especialista em Patologia Clínica pela Ordem dos Médicos; Consultor de Patologia Clínica da Carreira Médica Hospitalar no Centro Hospitalar Vila Nova de Gaia/Espinho, EPE – Unidade do Monte da Virgem; Foi responsável pela Coordenação do Controlo da Qualidade Analítica e pela Área Core Laboratorial no Dr. Joaquim Chaves, Laboratório de Análises Clínicas SA; Foi Diretor Técnico Substituto no Dr. Joaquim Chaves, Laboratório de Análises Clínicas SA; Esteve envolvido na atividade docente da cadeira de Farmacologia da Faculdade de Medicina da Universidade de Lisboa; Foi convidado para fazer parte de vários grupos de trabalho.
A todos aqueles que foram, e muitos continuam a ser, os meus mestres, colegas e amigos, e que me têm acompanhado e acrescentado valor à minha formação pessoal, académica e profissional, em particular ao Doutor Joaquim Chaves pela confiança que sempre depositou em mim, pela sua amizade e por todas as oportunidades que me concedeu.
Ao senhor Professor Doutor Joaquim Augusto da Silveira Sérgio, uma das minhas grandes referências como Homem, profissional e, sobretudo, como amigo inestimável com quem tive a honra e o privilégio de trabalhar sob a sua direção. Agora, alguns anos depois, pelo incentivo, entusiasmo e motivação que manifestou pela divulgação deste trabalho, assim como pela generosidade com que se disponibilizou e contribuiu para o tornar melhor na sua estrutura e ordenação dos temas abordados.
Edições Técnicas, Lda.
Lidel –
Tenho a honra de prefaciar, novamente, um volume desta coleção de Patologia Clínica do Doutor Rui Abrantes Pimentel, Medicina Laboratorial, desta vez abordando os vastos temas da Química Clínica, antecedidos por um capítulo de verdadeira Semiótica Laboratorial, que pode passar despercebido a olhos menos inquisitivos. Neste capítulo, são levantados os problemas que subjazem a interpretação e a correlação dos resultados, sobretudo aqueles que sejam resultantes de fatores interferenciais e que necessitem da correspondente correção, sob pena de, ao serem “apreciados” aquém ou além dos reais valores, poderem conduzir a gestos terapêuticos menos adequados, comprometendo a situação do doente.
Tal como dissera no anterior prefácio, do volume Estados Inflamatórios, e na sequência do atrás descrito, o autor não se limita a fazer uma mera análise de considerandos técnico-laboratoriais, uma vez que invade, com todo o direito, como médico que é, os campos da Clínica, procurando neles a racionalidade bijetiva dos resultados. Ou seja, é como se os sinais e os sintomas se traduzissem por valores observáveis e quantificáveis, a maioria deles no plano da interação molecular. Mutatis mutandis, e repescando o que Hermes Trismegisto putativamente afirmara – “o que se passa em cima é igual ao que se passa em baixo, e vice-versa”.
Deixando de parte, por ora, estes estudos arcanos, para continuarmos na análise do exposto no presente volume, podemos afirmar que a importância da avaliação dos produtos nitrogenados advém das múltiplas e complexas funções proteicas, desde a replicação do ácido desoxirribonucleico (ADN), passando pelas enzimas – catalisadoras de grande especificidade das reações metabólicas, sem as quais tais reações muito dificilmente se fariam e, a serem efectuadas, registar-se-ia um enorme gasto energético –, até ao campo estrutural –; do citosqueleto (que compreende, de entre as demais proteínas intracelulares, a actina, a miosina e a tubulina) às estruturas ósteo-cartilagíneas – já para não mencionar outras, também no âmbito do conectivo, que conformam os diversos órgãos e aparelhos, a par das que subjazem à arquitetura da beleza, ou da fealdade, com que os corpos humanos se apresentam e interagem entre si. Mas aqui, há que dizê-lo, para manter a rigidez da estrutura proteica, é necessário contar com os tão “perseguidos” hidratos de carbono, pois, sem eles, dificilmente se alcançaria uma postura ereta, nem haveria capacidade para se fixar grande parte dos sais minerais (e, quiçá, a funcionalidade enzimática) passando o ser humano, caso existisse, a ter de se contentar com uma morfologia de aspeto discoide ou similar, com graves implicações no desenvolvimento cerebral e... é só deixar correr a imaginação. Dito por outras palavras, não existiríamos como somos.
Ainda, e dentro das substâncias nitrogenadas, é descrito o doseamento das complexas moléculas glicoproteicas (mais uma vez, o casamento persiste), como as que se encontram na estrutura, entre outras, das diversas frações do complemento e das globulinas da resposta imunitária, reveladoras do nosso estado de prontidão defensiva. Este capítulo, tal como se encontra desenvolvido, é bem o exemplo da importância deste volume na atualidade, perante, por um lado, as questões advindas das alterações ambientais e, por outro, as pandemias que vão surgindo, tal como os fogos de verão, com a ajuda do (mau) engenho humano. Daí que o autor descreva e justifique, com certo pormenor, a pesquisa de marcadores dos processos inflamatórios, com realce para as proteínas de fase aguda, sobretudo relevantes na monitorização da evolução clínica, tendo em conta que a resposta é multifatorial, dado envolver não só os metabolitos, como também as estruturas celulares e respetivos produtos por elas produzidos, como é o caso das interleucinas.
Não deixa de ser admirável verificar-se que a diferenciação humana depende do arranjo sequencial dos ácidos aminados, comandado pelo posicionamento, segundo uma dada ordem, das bases azotadas, cada uma delas ligada, como não podia deixar de ser, a uma molécula açucarada – uma ribose – com ou sem oxigénio, respetivamente no ácido ribonucleico (ARN) e no ADN, cujo comportamento catabólico das bases purínicas (adenina e guanina) pode ser perscrutado através do doseamento do ácido úrico.
No aspeto metabólico de base, dois grandes capítulos se impõem. O capítulo relacionado com as disfunções dos hidratos de carbono e o referente às perturbações lipídicas, substâncias que sustentam o metabolismo energético. As disfunções destas duas interligadas famílias metabólicas repercutem-se, na sua essência, na deterioração do sistema cardiovascular, cujas consequências incapacitantes são amplamente conhecidas. Deste modo, dever-se-ia pensar em propor, para além do estudo das lipoproteínas, as provas de tolerância à glucose oral (PTGO) e o doseamento da adiponectina, como análises preditivas a incorporar, as provas de “rotina”, a fim de ajudar na prevenção de situações que todos nós lamentamos. Na continuidade do estudo analítico das funções metabólicas, o fígado é visto como o órgão-fábrica, reformulador da generalidade das substâncias assimiladas de que o organismo necessita para cumprir as suas funções e, concomitantemente, como depurador ou reciclador — por um lado, dos catabolitos resultantes desse funcionamento e, por outro, como segregador de uma parte desses produtos, através da bílis, os quais acabarão por serem eliminados através do intestino. No âmbito da sua ação catabólica, sendo o fígado ajudado pelos rins, compreende-se a existência de uma biunivocidade fisiológica, facilmente verificada pelo facto de a disfuncionalidade que haja num deles se vir a repercutir no outro. Daí que se justifique, aquando da pretensão de estudar a funcionalidade num dos sistemas, que seja obrigatória a análise referente aos parâmetros do outro, sob pena de a avaliação clínica pecar por defeito. Na verdade, não se trata de um exagero prescritivo, mas sim de uma praxis correcta.
Outro estudo sobre o qual o autor se debruça, diz respeito aos — por vezes tão esquecidos — equilíbrios hemodinâmicos e ácido-básico. Ainda que ambos tenham como função-alvo principal a renal, deve acrescentar-se a responsabilidade pulmonar. Se na segunda funcionalidade se torna evidente o seu controlo, na primeira há que lembrar a importante enzima conversora da angiotensina (ECA) hepática, existente em vários endotélios orgânicos, entre os quais o do pulmão, que a transforma em angiotensina II, para que esta atue sobre as glândulas suprarrenais para a libertação da aldosterona.
O doseamento das “drogas de abuso” que se tem vindo, infelizmente, a impor, dado não só o uso acrescido das mesmas, mas, igualmente, devido à sua interferência funcional multiorgânica com repercussão nas atitudes terapêuticas, quer seja no campo clínico-medicamentoso, que seja no anestésico-cirúrgico. Neste último, recordo-me de várias situações que deixaram um sabor amargo na boca, quando, no dealbar da década de 1980, grande parte dos clínicos ainda se encontrava na penumbra deste conhecimento. Deste modo, felicito a sua inclusão neste volume.
Se o estudo das hormonas – essas substâncias que, a seguir ao sistema nervoso central (SNC) — e a ele ligado —, são as que mais determinam o comportamento fisiológico do organismo, que já vem sendo descrito há vários anos, o que não se pode dizer dos marcadores tumorais que, recentemente, têm sofrido um acréscimo muito positivo, que está de acordo com a prática de uma Medicina cada vez mais preventiva. Na verdade, existe uma unanimidade clínica no que respeita ao diagnóstico precoce da recidiva e à monitorização da evolução terapêutica deste tipo de patologia. Ainda que, em determinados casos, as avaliações possam ter um custo financeiro elevado, deve comparar-se esse custo com o a posteriori das medidas então utilizadas para debelar a doença, já para não falar do preço de se salvar, atempadamente, uma vida humana.
Antes de terminar este acerto de palavras, permitam-me uma chamada de atenção para o capítulo dedicado aos parâmetros do metabolismo ósseo, tão importante na atualidade, perante o aumento da esperança de vida. Este capítulo encontra-se antecedido (muitas páginas atrás, é certo) pelo doseamento das enzimas referentes ao estado dos músculos estriados. Mas, só por se tratar de enzimas, e se encontrarem referenciadas no capítulo homónimo, não significa que o seu estudo não deva ser feito em conjunto com o dos parâmetros ósseos.
Cumpre-me, por último, agradecer ao meu colega e amigo, Doutor Rui Abrantes Pimentel, por me ter proporcionado esta longa, mas agradabilíssima viagem de revisitação ao conhecimento da atual ars medicinae
Bem-hajas, Rui.
Doutor Joaquim Silveira Sérgio Licenciado em Medicina e Cirurgia pela Faculdade de Medicina da Universidade de Lisboa, Especialista em Ortopedia, Chefe de Clínica/Consultor de Ortopedia da Carreira Médica Nacional. Professor Jubilado.
O presente trabalho é, essencialmente, uma compilação modulada de boas práticas no âmbito da prescrição médica, de todas as fases do processo laboratorial (pré-analítico, analítico e pós-analítico) e da interpretação dos resultados analíticos baseadas na minha experiência clínica e laboratorial, que foram sendo adquiridas e amadurecidas ao longo de mais de quatro décadas, mais de metade das quais na Dr. Joaquim Chaves, Laboratório de Análises Clínicas, e nas evidências publicadas na literatura científica das diversas especialidades médicas.
Aceitei o desafio proposto pelas minhas colegas e amigas, Catarina Rombo, Marina Pires e Rute Pereira, e pela minha mulher, Margarida Ponte, de publicar Medicina Laboratorial: Da Prescrição à Interpretação Clínica, por estar convencido de que a partilha em todas as áreas do conhecimento, na qual se inclui a Medicina Laboratorial, é uma janela de oportunidade imperdível, por permitir criar as condições necessárias para explicar a importância da relação entre a clínica e o laboratório, cujo diálogo entre pares deve ser permanente, assim como o significado de muitos sinais do âmbito da Patologia Clínica. Estou convicto de que constitui um importante contributo para melhorar a sua compreensão e o processo de interpretação dos resultados dos mensurandos prescritos, uma vez que é neles que se baseiam entre 60 e 70% das decisões médicas, que condicionam a qualidade de vida das pessoas e, muitas vezes, o seu tempo de sobrevida.
Revisitada a literatura médica publicada, quer em livros de texto, quer em artigos científicos, nacionais e internacionais, é evidente a existência de uma enorme lacuna, que se vem traduzindo pela insuficiência de articulação, cooperação e coordenação de esforços interdisciplinares. É patente, também, um afastamento cada vez maior entre o que é pretendido e tomado como necessidade por cada uma das especialidades médicas e cirúrgicas, e as limitações e potencialidades do estado da arte da Medicina Laboratorial, que importa conhecer e colmatar.
Só há uma Medicina. A Medicina como a Arte Maior de ajudar as pessoas a ter a melhor qualidade de vida (bem-estar físico, psíquico e social) durante o máximo de tempo possível.
No âmbito da Química Clínica e da Endocrinologia, Medicina Laboratorial faz uma abordagem prévia aos processos de validação e de interpretação dos resultados laboratoriais, e são caracterizados, ao longo dos diferentes capítulos, os parâmetros laboratoriais (mesurandos) com maior valor semiológico no contexto do rastreio, do diagnóstico, da monitorização da evolução clínica e resposta ao tratamento, e da estratificação do risco (prognóstico) das diferentes entidades nosológicas, assim como a sua sensibilidade e especificidade, tendo em consideração o estado da arte atual. Em relação a cada mesurando também são referidas e descritas as condições potenciais de interferência analítica mais frequentes, que importa reconhecer para se poder minimizar o seu impacto negativo na utilidade clínica dos resultados.
Técnicas, Lda.
Edições
Lidel –
©
Os médicos recorrem às análises clínicas quer para efetuar diagnósticos, estratificar o risco de morbilidade e de mortalidade, identificar recaídas ou recorrências e monitorizar a evolução clínica e a resposta ao tratamento de diversas entidades nosológicas, quer para despistar a presença destas entidades em indivíduos aparentemente saudáveis.
A principal responsabilidade da Medicina Laboratorial é contribuir para melhorar de forma consistente a qualidade de vida das pessoas (estado de completo bem-estar físico, psíquico e social) durante o máximo tempo possível, devendo, para isso, garantir que, de forma sustentada, todos os resultados reportados se caracterizem pelos seguintes aspetos:
• Não estejam comprometidos por enviesamentos inaceitáveis em relação ao valor real (in vivo);
• Sejam clinicamente úteis para permitir a tomada de decisões médicas mais adequadas;
• Sejam reportados em tempo útil.
Tem sido evidenciado que até 25% dos erros de avaliação clínica relacionados com os resultados laboratoriais afetam o processo de decisão médica, tendo como consequência atrasos na prestação dos cuidados de saúde mais adequados em tempo útil (Lippi, G. et al., 2008).
A caracterização da variabilidade fisiológica, fisiopatológica e iatrogénica, e a identificação e monitorização da variabilidade que decorre do processo analítico, assim como a garantia de que se mantém dentro de limites clinicamente aceitáveis, são fundamentais para que as informações veiculadas pelos resultados reportados não induzam os clínicos prescritores a cometer erros de julgamento em relação a um diagnóstico, prognóstico (estratificação do risco) ou tratamento e, assim, diminuindo a qualidade de vida dos pacientes.
A variabilidade dos resultados laboratoriais está relacionada com diversos fatores e condições, dos quais se destacam, de acordo com a sua origem, os seguintes:
• A variabilidade biológica intraindividual específica de cada mesurando (equilíbrio homeostático);
• As alterações do estado de saúde dos indivíduos (variabilidade fisiopatológica);
• As alterações decorrentes de atos ou de intervenções no âmbito da terapêutica ou do diagnóstico (variabilidades iatrogénicas);
• O processo pré-analítico, analítico e pós-analítico, designadamente a competência dos profissionais envolvidos (fatores humanos) e a qualidade do desempenho dos diferentes procedimentos de medida e ensaios instalados no laboratório (exemplos: precisão e exatidão próprias do método, intervalo de medição e linearidade, limites de deteção e especificidade analítica);
• A estabilidade dos mesurandos (analitos e parâmetros) nas amostras biológicas em função das suas características, da preparação pré-analítica efetuada e das condições de colheita, de conservação e do seu processamento;
• As interferências analíticas positivas ou negativas que se traduzem pela diferença entre o resultado obtido e o seu valor real (in vivo).
Antes de ser tomada uma decisão perante resultados laboratoriais anormais ou discordantes, seja através da história clínica, epidemiológica ou ambas, seja com recurso a critérios interparamétricos, ou ainda através dos resultados obtidos em colheitas anteriores, é importante que o processo de interpretação, tanto a nível laboratorial como clínico, permita determinar se estes resultados estão relacionados
com o estado de saúde dos pacientes ou se são resultantes de variáveis pré-analíticas, analíticas ou pós-analíticas, nas quais se incluem as interferências.
O impacto negativo que os resultados incorretos podem ter para os pacientes está relacionado com os seguintes fatores:
• Estado de saúde e características das patologias que o condicionam;
• Sensibilidade e especificidade diagnósticas (valor semiológico) dos mesurandos objeto de análise;
• Grandeza da diferença entre o resultado reportado e o seu valor real (in vivo);
• Competência e experiência, quer dos profissionais do laboratório, quer dos médicos prescritores, em identificar e lidar com este tipo de resultados, visando minimizar a gravidade do dano.
Técnicas, Lda.
Edições
Lidel –
Os resultados analíticos, de um modo geral, designadamente os quantitativos e semiquanti tativos, têm um enviesamento em relação a um valor de tendência central e uma variabilidade que resulta da presença de duas componentes constantes e de grandeza variável: a biológica, própria de cada indivíduo, e a analítica, caracte rística de cada sistema analítico/ensaio. A estas duas componentes está associada frequentemen te uma terceira, indesejável quando é estatística e/ou clinicamente excessiva, que corresponde à interferência analítica, cuja natureza pode ser en dógena e/ou exógena.
De um modo geral, a interpretação e a valori zação clínica dos resultados laboratoriais fazem‑se com base na sua verosimilhança, correlação inter paramétrica e concordância com a história clínica dos pacientes, com os dados e os fatores epidemio lógicos da população a que pertencem, e por com paração quer com os intervalos de referência, quer com os níveis de decisão clínica (NDC) ou cutoff, quer ainda com os resultados obtidos em colheitas anteriores (exemplo: monitorização da evolução clínica ou da resposta ao tratamento assentes na análise do histórico dos resultados dos mensuran dos, principalmente daqueles que têm um elevado índice de individualidade).
Os intervalos de referência e os NDC são deter minados de acordo com protocolos padronizados rígidos, a partir de populações e subpopulações bem caracterizadas, em que os indivíduos selecio nados, além de não estarem a fazer qualquer tipo de terapêutica e de não consumirem nem estarem expostos a substâncias psicoativas ou a tóxicos, estão, no momento em que é efetuada a colhei ta das amostras biológicas, nas condições basais ideais requeridas para a determinação do mensu rando específico (exemplos: jejum e repouso).
Os resultados laboratoriais são valorizados por comparação com critérios fixos (exemplos: intervalos de referência e NDC), determinados em função das seguintes variáveis e fatores:
• Características dos ensaios (exemplos: preci são própria do método, sensibilidade e espe cificidade analíticas);
• Variabilidade biológica intraindividual e interindividual (Cvb%): variação ou flutu ação fisiológica da atividade, concentração ou propriedades de um determinado men surando, que ocorre em volta de um valor homeostático central ou basal (equilíbrio dinâmico intraindividual e interindividual);
• Índice de individualidade dos mensurandos;
• Valor semiológico dos mensurandos.
Os limites de decisão usados no processo de validação e de interpretação dos resultados po dem ser de diferentes tipos, designadamente:
• Limite inferior e superior do intervalo de referência: reservado para os mensuran dos que têm um índice de individualidade baixo. Os intervalos de referência podem ser unidirecionais [exemplo: percentil 99 –P99)] ou bidirecionais, cuja amplitude está diretamente relacionada com a variabilida de analítica própria do método e a biológica (intraindividual e interindividual). Para os mensurandos cuja distribuição de frequên cias dos resultados dos pacientes saudáveis é gaussiana, são utilizados habitualmente os intervalos de 95%, que correspondem a 2 SD, ou de 99%, que correspondem a 3 SD. Para aqueles cuja distribuição de frequências dos resultados não é gaussiana, são utiliza dos frequentemente os intervalos de referên cia entre os P2,5 e P97,5;
• Índice de individualidade: a valorização clí nica correta dos resultados dos mensuran dos que têm um índice de individualidade elevado deve ser efetuada preferencialmente em função das diferenças estatisticamente significativas entre 2 resultados obtidos em amostras colhidas em dias diferentes (dife rença crítica);
Ménétrier ou gastropatia hipertrófica, colite ulcerosa, doença de Crohn, enterite regional, lipodistrofia intestinal de Whi pple, obstrução linfática, linfangiectasia intestinal, insuficiência cardíaca conges tiva por valvulopatias direita ou por peri cardite constritiva, hipogamaglobuline mia congénita, gastroenteropatia alérgica, intolerância ao leite de vaca, Sprue tropical e neoplasias do aparelho gastrointestinal).
– Cutâneas: grandes queimados.
É uma condição benigna revelada na separa ção eletroforética das proteínas do soro e que se traduz por um padrão característico em que a albumina aparece, com maior ou menor nitidez, desdobrada em duas frações — ver Figura 2.1. Pode ter origem genética (persistente; a in cidência da heterozigotia varia entre 1 por mil ou 10 mil habitantes por ano) ou ser adquirida (transitória ou autolimitada) não sendo revela dora, por si só, de qualquer patologia maligna.
A alteração genética que se acompanha fre quentemente por outras alterações laboratoriais é a hipertiroxinemia bisalbuminémica familiar [mutações no gene ALB (albumin) de transmis são autossómica dominante], cuja albumina anormal tem uma afinidade aumentada para a tiroxina, cujos pacientes são clinicamente euti roideus e que se traduz por valores no soro ou no plasma de tiroxina (T4) total e de T4 livre ele vados, com concentrações normais da hormona tirotrófica (hTSH, do inglês human thyroid sti mulatory hormone).
A bisalbuminemia adquirida pode aparecer nos doentes a fazer tratamento com agentes anti

microbianos β‑lactâmicos ou com aminoglicosi dos, na pancreatite aguda em que ocorreu rutura de pseudoquistos, na presença de proteína M, síndroma nefrótica, insuficiência renal crónica, DM, sarcoidose e doença de Alzheimer.
O principal valor semiológico da determina ção da albumina no soro ou plasma, na urina, no líquor e no derrame de serosas é o que a seguir se refere para cada uma destas amostras biológicas:
• Soro ou plasma: avaliação do estado nutri cional dos indivíduos e do grau de insufi ciência hepática (marcador bioquímico da reserva funcional dos hepatócitos), assim como na monitorização da evolução clínica e da resposta ao tratamento das patologias que deram origem à hipoalbuminemia;
• Urina: identificação precoce dos doentes com deterioração da função renal, estra tificação do risco de evolução para doença renal crónica e monitorização da evolução clínica e da resposta ao tratamento das pato logias renais;
• Líquor (QAlb): caracterização da disfunção da barreira hematoencefálica e monitoriza ção da evolução clínica e da resposta ao tra tamento das lesões do SNC que lhe deram origem;
• Derrame de serosas (SAAG: albumina do soro ‑ albumina do derrame): diagnóstico diferencial entre a ascite secundária a hiper tensão portal e a que é devida a outros pro cessos não relacionados com o aumento da pressão ao nível dos sinusoides hepáticos:
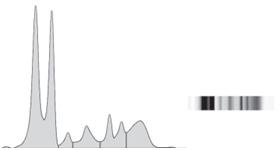
Figura 2.1 • Exemplos de padrões eletroforéticos de bisalbuminemia [Eletroforese capilar de zona (ECZ) – Capillarys 2 Sebia].
A avaliação do estado nutricional (MUST, do inglês Malnutrition Universal Screening Tool) e a atribuição do score correspondente, pode ser efetuada com base na combinação dos valores do IMC, perda de peso não intencional e da pre sença ou ausência de doença aguda associada a diminuição da ingestão alimentar de acordo com a Tabela 3.2.
3.1. reação de fase aguda
A APR é essencial para que o organismo possa responder de forma eficaz aos agentes patogéni cos, sejam de origem interna ou externa. É, no sentido lato, uma resposta sistémica à inflamação de qualquer natureza.
As reações agudas e subagudas caracterizam ‑se por serem autolimitadas e reversíveis. Contu do, a persistência dos estímulos evolui para um estado de inflamação sistémica crónica de grau variável, ao qual se pode associar lesão tecidular permanente, disfunção de órgão e doença (se quelas).
A APR é habitualmente um processo fisioló gico protetor que envolve a resposta imune inata e é acompanhado por múltiplas alterações meta bólicas. Na APR os pontos de equilíbrio home ostáticos normais são substituídos por outros, visando eliminar ou controlar o agente ou os es tímulos patogénicos e colaborar com os proces sos envolvidos na reparação molecular, celular e tecidular (preservação da integridade).
As APR podem ser identificadas, quer nos in divíduos imunocompetentes quer nos doentes imunocomprometidos, por patologias primá rias, secundárias ou adquiridas iatrogenicamente (exemplo: quimioterapia antineoplásica intensiva).
As manifestações clínicas da APR estão di retamente relacionadas com a sua gravidade e persistência no tempo, e caracterizam‑se por al terações de naturezas diversas, designadamente:
• Metabólicas:
– Aumento do catabolismo proteico, dimi nuição da massa muscular (sarcopenia) e da massa óssea (osteoporose);
– Aumento da síntese das APP positivas e diminuição das negativas;
– Desequilíbrio quantitativo entre as con centrações das citocinas pró‑inflamatórias (exemplos: IL‑6, TNF‑α, IL‑1β, IL‑8 e IFN‑γ), que estão aumentadas, e as anti ‑inflamatórias [exemplos: IL‑10, IL‑4, IL‑13 e transforming growth factor‑β (TGF‑β)], que estão relativamente diminuídas;
– Aumento da lipogénese hepática e da lipó lise ao nível do tecido adiposo, diminuição da atividade da lipoproteína lípase ao nível do fígado e do tecido adiposo, diminuição da gliconeogénese;
– Sarcopenia, caquexia;
– Amiloidose secundária.
• Neuroendócrinas:
– Febre, anorexia, sonolência e letargia;
– Aumento da hormona adrenocorticotrófica (ACTH, do inglês adrenocorticotropic hor mone) e do cortisol (atinge o valor máximo cerca de 6 horas depois do início da APR), assim como das catecolaminas [adrenalina (ADR) e noradrenalina (NA)], AVP (induz
Tabela 3.2 • Tabela usada para avaliação do estado nutricional (MUST)
Ferramenta universal de pesquisa/identificação de uma condição de má nutrição (MUST)
IMC (kg/m2)
Perda de peso não intencional nos últimos 3 a 6 meses
Doença aguda com diminuição da ingestão alimentar durante ≥ 5 dias
(quer do seu gradiente, quer das suas concentra ções). Exemplos:
• Hipocalemia (clinicamente significativa: < 3,0 mmol/L; grave: < 2,7 mmol/L): fraqueza, irritabilidade e paralisia muscular; taquicar dia, arritmias e paragem cardíaca em sístole;
• Hipercalemia (clinicamente significativa: >5,8 mmol/L; grave: > 6,0 mmol/L): confu são mental, fraqueza muscular, parestesias, paralisia flácida dos músculos respiratórios e periféricos, bradicardia e arritmias. Quando os valores do K+ são > 7,0 mmol/L pode dar origem a colapso vascular periférico e para gem cardíaca em diástole (assistolia).
O K+ no soro ou no plasma tem caracteristica mente uma variabilidade fisiológica, apresentan do um coeficiente de variação biológico intrain dividual no soro ou no plasma entre 3,0 e 5,4% (mediana 3,9%) e interindividual entre 1,1 e 9,7% (mediana 5,3%). Na urina é de 24,4% e de 22,2%, respetivamente.
1.4.1. Situações clínicas em que a concentração do potássio está diminuída no soro ou no plasma
A hipocalemia caracteriza‑se pela concentra ção do K+ < 3,5 mmol/L. Seguidamente são re feridas algumas condições clínicas que se acom panham por hipocalemia (ver ainda Caixa 6.1):
• Redistribuição do potássio do espaço extracelular para o intracelular:
– Insulinoterapia;
– Alcalose metabólica;
– Pseudo‑hipocalemia (exemplos: hiper leucocitose e administração de fatores de crescimento mielopoiéticos);
– Hipotermia, paralisia periódica hipocali émica, atividade β2‑adrenérgica e síndro ma paraneoplásica por produção ectópica de ACTH (exemplos: tumor de pequenas células do pulmão, feocromocitoma, insu linoma e tumor medular da tiroide).
Caixa 6.1 • Algoritmo de abordagem dos doentes com hipocalemia
• K+ urina < 18 mmol/g creatinina:
– Ausência de desequilíbrio ácido-base: entrada aguda de K+ para dentro das células
– Acidose metabólica: diarreia
– Alcalose metabólica:
- Perda de K+ extrarrenal: diarreia com espoliação de cloretos, abuso de laxantes, perdas cutâneas e fibrose quística
- Perda de K+ renal: diuréticos (exemplos: furosemido e tiazidas) e alguns doentes com vómitos
• K+ urina > 18 mmol/g creatinina:
– Acidose metabólica hiperclorémica: diarreia, acidose tubular renal (RTA) distal, RTA proximal tratada com doses elevadas de bicarbonato de sódio (NaHCO3), tratamento com inibidores da anidrase carbónica (exemplos: acetazolamida e topiramato), hiperprodução de um ácido com excreção urinária dos seus aniões com o K+
– Alcalose metabólica com volemia arterial:
- Diminuída ou normal: vómitos (cloretos na urina diminuídos), síndroma de Bartter e síndroma de Gitelman hereditários ou adquiridos (cloretos na urina persistentemente aumentados) e diuréticos (cloretos na urina intermitentemente aumentados)
- Aumentada: condições associadas com efeito mineralocorticoide primário elevado (exemplos: hiperaldosteronismo hiperreninémico primário como a estenose da artéria renal e os tumores secretores de renina, hiperaldosteronismo primário como adenoma adrenal, hiperplasia adrenal bilateral e hiperaldosteronismo que responde ao tratamento com glucocorticoides, condições em que o cortisol atua como mineralocorticoide como síndroma mineralocorticoide aparente, ingestão de compostos contendo ácido glicirrízico que inibe 11-β-hidroxisteroide desidrogenase -2, tumores produtores de ACTH, e canal do sódio epitelial constitutivamente ativo como a síndroma de Liddle
Urina:
• O GHB é quase todo metabolizado em água e dióxido de carbono pela ADH;
• Entre 1 e 5% do GHB consumido é excreta do na forma livre pela urina;
• A gama‑butirolactona (GBL) e o 1,4‑butanodiol (BD) depois de consumidos são rapidamente metabolizados em GHB;
• Janela de deteção (na urina): até 12 horas (concentração máxima cerca de 4 horas após oúltimo consumo).
Sangue total e soro ou plasma:
• T½: GHB é de 20 a 60 minutos;
• Concentrações máximas (pico) após consu mo:
– Oral: aos 20 a 45 minutos deixando de ser detetável a partir de 6 a 8 horas; – IV: aos 15 minutos;
• Relação sangue ÷ plasma: ½;
• A concentração normal do GHB endógeno é < 1 mg/L;
• NDC usado para fazer o diagnóstico diferen cial entre o GHB administrado no âmbito tera pêutico e o consumo abusivo: < 10 mg/L ≥.
Metabolismo:
A cetamina é metabolizada no fígado princi palmente pela via da N‑desmetilação (citocromo P450) dando origem à norcetamina (metabolito ativo).
T½ plasma:
• Cetamina: 2,3±0,5 horas;
• Norcetamina: 240 minutos.
Janela de deteção na urina: até 3 dias. Não existem imunoensaios disponíveis. A identi ficação da cetamina, norcetamina e di‑hidro ‑norcetamina no sangue ou na urina é efetuada por GC‑MS ou por HPLC‑MS).
Os seus metabolitos urinários mais importan tes são o 2 oxo 3 hidroxi LSD e o nor LSD.
T½ plasma: 2,5 a 4 horas.
Janela de deteção na urina: até 5 dias.
Metabolismo (principais metabolitos):
• Metaqualona‑N‑óxido;
• 4’‑hidroxi‑metaqualona glucuronido;
• 2’‑hidroxi‑metil‑metaqualona glucuronido;
• 3‑hidroxi‑metaqualona;
• 2‑hidroxi‑metil‑metaqualona glucuronido;
• 6‑hidroxi‑metaqualona glucuronido.
T½ plasma: 20 a 60 horas.
Janela de deteção na urina: 3 a 4 dias.
Metabolismo:
• É rapidamente metabolizado em ácido rita línico inativo;
• Metilfenidato (Ritalina®):
– Cerca de 80% é excretada em 24 horas, menos de 1% na forma livre (pode ser maior nas urinas ácidas), 60 a 81% como ácido rita línico e 5 a 12% como 6‑oxo‑ácido ritalínico;
– O etilfenidato pode ser identificado nos consumidores de etanol.
T½ plasma: entre 1,4 e 4,2 horas.
Janela de deteção na urina: até 24 horas.
Os metabolitos mais importantes presentes na urina são os que a seguir se referem:
• N‑benzilpiperazina (BZP): BZP na forma livre ±6% e vestígios (0,11%) de 3’‑hidroxi‑BZP e de 4’‑hidroxi‑BZP;
• Derivados da BZP [1‑(3,4‑metilenedioxi benzil)‑piperazina (MDBP), 1‑(4‑metoxife nil)‑piperazina (MeOPP), 1‑(3‑trifluorme
Vol. 4
Esta coleção de 5 volumes apresenta as fases da prescrição médica, do processo laboratorial (pré-analítico, analítico e pós-analítico) e da interpretação dos resultados analíticos. É explicada e evidenciada a importância da relação entre a clínica e o laboratório, cujo diálogo entre pares deve ser permanente, e clarificado o significado de muitos sinais do âmbito da Patologia Clínica, que são representados e se traduzem nas diferentes formas como os resultados dos parâmetros laboratoriais prescritos podem ser reportados e devem ser interpretados.
Destina-se a internos e especialistas em Patologia Clínica; estudantes de Medicina; médicos de diversas especialidades que, na prática clínica diária, prescrevem análises clínicas e interpretam os seus resultados; estudantes e profissionais das áreas de Ciências Farmacêuticas, Ciências Biomédicas, Biologia e Bioquímica em formação e especialistas em Análises Clínicas; interessa também a técnicos de análises clínicas e saúde pública.
Química Clínica e Endocrinologia
Neste volume, , é feita uma abordagem prévia aos processos de validação e interpretação dos resultados laboratoriais, e são caracterizados os parâmetros laboratoriais (mensurandos) com maior valor semiológico no contexto do rastreio, do diagnóstico, da monitorização da evolução clínica e da resposta ao tratamento, e da estratificação do risco (prognóstico) das diferentes entidades nosológicas, assim como a sua sensibilidade e especificidade, tendo em consideração o estado da arte atual. Em relação a cada mensurando, também são referidas e descritas as condições potenciais de interferência analítica mais frequentes, que importa reconhecer para se poder minimizar o seu impacto negativo na utilidade clínica dos resultados

Edição apoiada por:
