













G. Covelli
Impianto di IOL telescopiche SING-IMT in pazienti affetti da degenerazione maculare
F. Serino, F. Franco, F. Giansanti
Approfondimenti
Board
M. Borgioli
L. Menabuoni
S. Zuccarini
G. Covelli
F. Franco
F. Giansanti
G.R. Tedesco
L. Vigo
F. Serino
Editore
FGE S.r.l
Fabiano Gruppo Editoriale
Redazione: Strada 4 Milano Fiori, Palazzo Q7 20089 Rozzano (MI) Sede legale: Regione Rivelle, 7 14050 Moasca (AT) Tel. 0141 1706694 - Fax 0141 856013
Pubblicità info@fgeditore.it tel. 0141 1706694
Direttore responsabile
Ferdinando Fabiano f.fabiano@fgeditore.it
Registrazione presso il Tribunale di Asti N. 02/2024 in data 14 marzo 2024
© Copyright FGE srl È vietata ogni riproduzione totale o parziale di testi e immagini






Cari lettori,
Siamo entusiasti di presentarvi il terzo numero della nostra rivista! Il nostro viaggio fino a qui non è stato facile; dedicare tempo alla creazione di contenuti di alta qualità richiede sacrifici da parte di ciascuno di noi, ma il risultato è una pubblicazione che ci riempie di orgoglio.
In questo numero troverete articoli che spaziano su vari argomenti, tutti scelti con cura per la loro rilevanza e qualità. Siamo particolarmente felici di offrirvi un’intervista esclusiva con Simone Bagaglia, un giovane pieno di entusiasmo e già ricco di esperienze da condividere con noi. Grazie a Simone per la sua disponibilità!
Inoltre, abbiamo in serbo per voi un’intervista con un maestro di grande esperienza. Non sveleremo il suo nome per ora, ma vi promettiamo che le sue parole sapranno catturare la vostra attenzione e il vostro interesse.
Un momento cruciale accompagna questa pubblicazione: la storica unificazione di AIMO e SISO, una fusione che promette di creare una forte comunità di oculisti italiani. Questo è il frutto di un'attesa di 15 anni, e non vediamo l'ora di vedere quali opportunità si presenteranno in questa nuova fase. Il congresso AIMO, che si svolgerà per l’ultima volta “in collaborazione con SISO”, sarà certamente un’occasione imperdibile.
Prepariamoci, quindi, a un nuovo inizio e a leggere insieme la nostra rivista. Domani si prospetta un giorno di grandi novità!
Un caloroso saluto da Luca, Marco e Silvio.
Giovanni Roberto Tedesco
Centro Oculistico Tedesco STP srl
L’occhio secco è una delle patologie più frequenti al mondo con il 5-35% della popolazione mondiale affetta da dry eye.
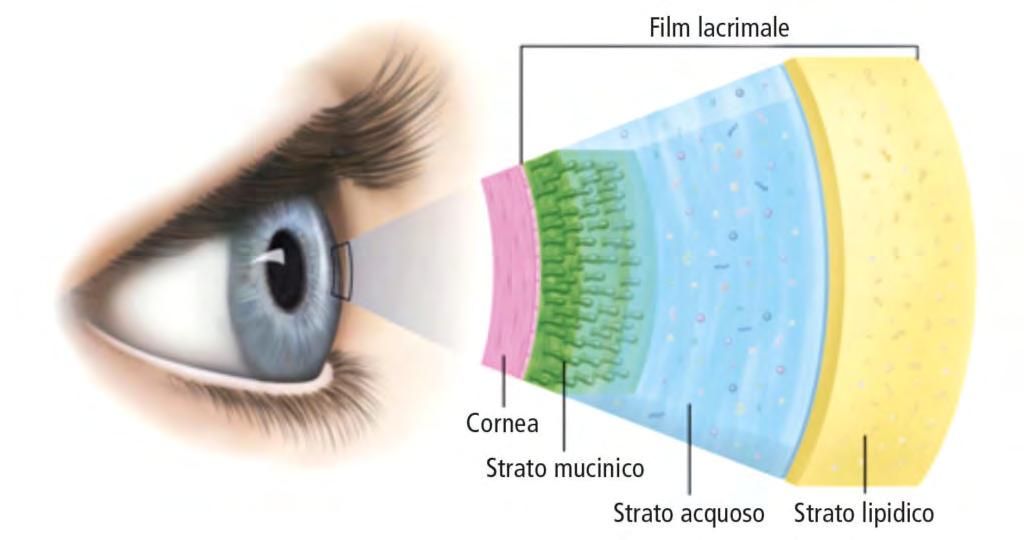
Il film lacrimale è una pellicola che riveste la superficie oculare ed è composto da tre strati: uno strato esterno (lipidico), uno strato intermedio (acquoso) e uno strato interno (mucinico). (Fig. 1)
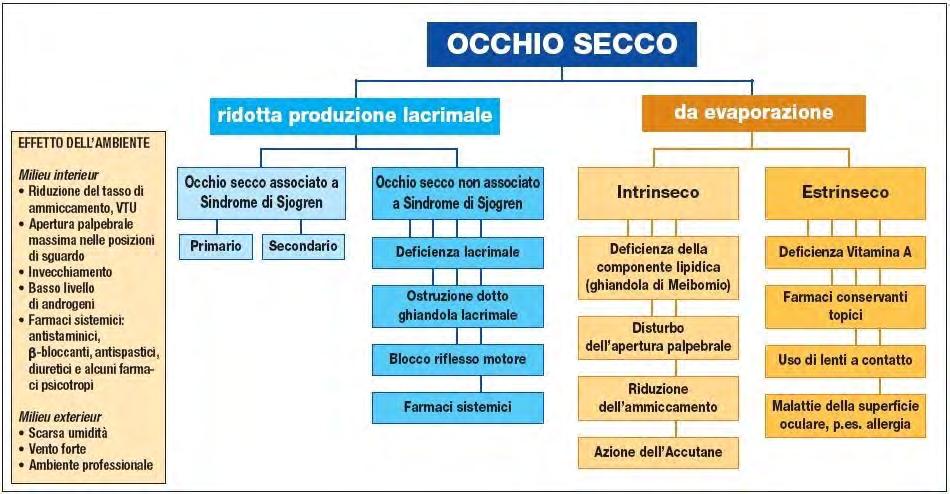
L’occhio secco si distingue in iperevaporativo, iposecretivo e/o misto.
La forma iperevaporativa è la più frequente tra le forme di secchezza oculare ed è più frequentemente legato a una patologia a carico delle ghiandole di meibomio, che sono responsabili della secrezione del mebo. La fluidità del mebo è fondamentale nella costituzione dello strato lipidico del film lacrimale. La forma di secchezza oculare iposecretiva invece è più frequentemente legato alla sindrome di Sjogren. Le forme miste di secchezza oculare sono caratterizzati dalla combinazione di forma iposecretiva e for-

ma iperevaporativa. (Fig. 2)
La diagnostica dell’occhio secco ha un ruolo fondamentale nel distinguere le varie forme di secchezza oculare.
Nella pratica clinica spesso si usano strumenti high tech che consentono una più rapida acquisizione dei parametri, che risultano alterati in caso di occhio secco, quali tempo di rottura non invasivo (NIBUT) e meibografia (valutazione della morfologia e dell’anatomia delle ghiandole di meibomio).
Il NIBUT va considerato patologico quando è inferiore ai 5 secondi, mentre valori superiori ai 10 secondi sono da considerarsi normali.
Un test di fondamentale importanza per una diagnosi quantitativa di occhio secco è il test di schirmer ed è consigliabile eseguirlo dopo instillazione di anestetico topico 5 minuti prima dell’esecuzione dell’esame. Il test di schirmer va considerato patologico quando è inferiore ai 5 mm, mentre sopra i 10 mm è nella norma.
L’ultimo esame che va eseguito per avere una valutazione completa dell’occhio secco è l’interferometria che misura lo spessore dello strato lipidico, che risulta nella norma per valori tra i 100 e i 75 nm, mentre valori inferiori ai 50 nm sono patologici.
Spesso risulta importante valutare la sensibilità corneale che può essere alterato in caso di occhio secco cronico.
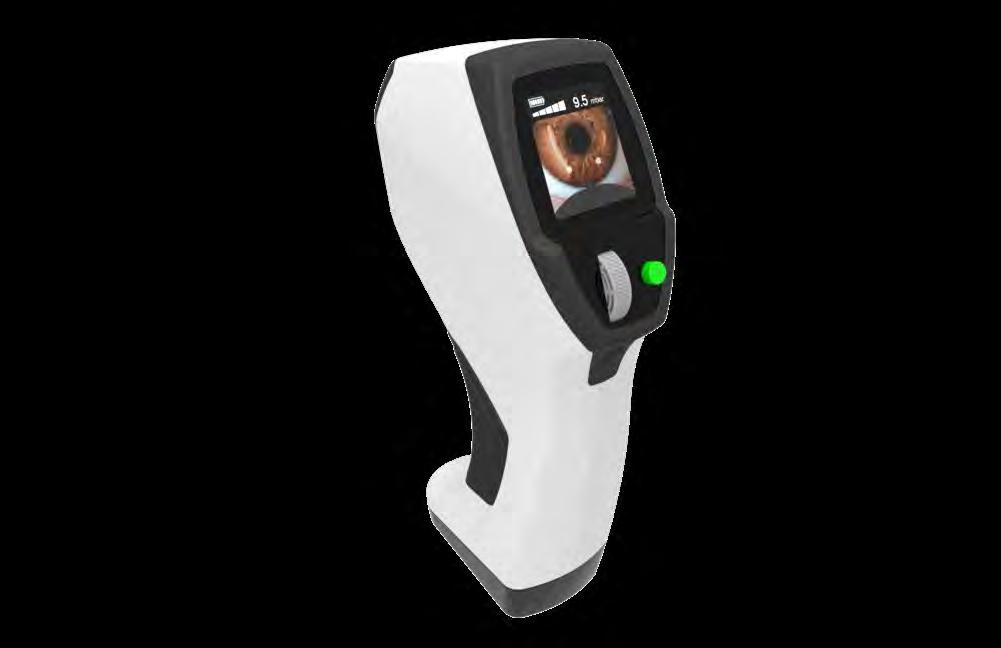
Un nuovo strumento che consente la valutazione della sensibilità corneale è l’estesiometro non a contatto. Si tratta di un dispositivo portatile che emette un getto d’aria e che presenta sei livelli di soglia.
I livelli di normalità corrispondono al secondo e al terzo impulso d’aria; Il livello 1 corrisponde a una ipersensibilità corneale, mentre i livelli 4 e 5 a una sensibilità corneale ridotta.
Infine il livello di soglia 6 è segno di una severa ipoestesia corneale. (Fig. 3)
I risultati dell’interferometria, del NIBUT, della mei-
bografia e del test di schirmer ci consentono di eseguire una diagnosi qualitativa e quantitativa di occhio secco, in modo da poter instaurare una terapia mirata.
In caso di occhio secco iperevaporativo si possono usare lacrime artificiali a base di acido ialuronico associato a idrocortisone a basso dosaggio, oppure associato a trealosio, oppure associato a xanthan gum e sostanze ad azione osmoprotettiva, oppure associato a trealosio e a fosfolipidi (lacrima a tre componenti), infine si può valutare anche l’uso di una lacrima a base di perfluoroesilotta-
In caso di occhio secco iperevaporativo associato a blefarite anteriore si possono associare ai colliri precedenti un un-
guento a base di tetracicline per uso palpebrale oppure un collirio a base di azitromicina.
Se, invece l’occhio secco iperevaporativo si dovesse associare a meibomite, alle lacrime artificiali, di cui abbiamo parlato in precedenza, sarebbe il caso di associare un unguento a base di tetracicline e corticosteroidi per uso palpebrale, impacchi caldi oppure maschere riscaldanti e/o tetracicline per via sistemica per 15 gg, onde evitare terapie più durature tali da alterare il microbioma intestinale, associandolo all’uso di probiotici per almeno 60 giorni.
La terapia dell’occhio secco iposecretivo è caratterizzato dall’uso di lacrime artificiali a base di acido ialuronico ad alto peso molecolare in formulazione più viscosa.
Altre possibili terapie sono l’utilizzo di ciclosporina all’1-2% in collirio da instillare 2 volte al die, l’utilizzo del siero autologo in collirio, l’utilizzo del PRP (plasma ricco di piastrine) sempre in collirio, l’utilizzo di formulazioni gelatinose o in ungento.
Esistono anche altre terapie che non sono attuabili in Italia quali l’uso del Liftegrast coll o della Vareniclina spray nasale.
Nel caso di una forma di secchezza oculare mista si possono combinare le due terapie precedentemente descritte.
Esiste un ulteriore caso di secchezza oculare, ossia quando c’è un’alterazione dello strato mucinico e in questo caso si possono utilizzare: lacrime artificiali iperviscose associato a ungento serale a base di Vit. A, mucolitici in collirio o per via sistemica, Diquafasol (non in commercio in Italia), Rebamipide (non in commercio in Italia) e infine Resolvine (in studio). In caso, invece di assenza di segni clinici di dry eye e di presenza di sintomatologia di occhio secco con alterazione della sensibilità corneale (più frequentemente di ipersensibilità) si può usare un collirio a base di GlicoPro (complesso multimolecolare a base di proteine, glicosaminoglicani solforati e non solforati veicolati da una base mucinica costituita da Idrossipropilmetilcellulosa) da instillare 3-4 volte al die, magari associandolo a una terapia sistemica a base di Pregabalin da 150 mg da assumere 2 volte al die per 30 giorni e poi a scalare una volta al die per altri 30 giorni.
Una volta iniziata una terapia mirata per l’occhio secco risulta fondamentale seguire il paziente nel tempo, valutando i vari parametri dell’occhio secco quali test di schirmer, NIBUT, interferometria e OSDI (ocular surface disease index), che è un questionario da somministare al paziente e che indica il grado di severità della sintomatologia dell’occhio secco.
L’OSDI risulta nella norma per un scorse inferiore a 11, lieve per uno score tra 12 e 22, moderato tra 23 e 32 e infine severo per uno score tra 33 e 100. I pazienti vanno controllati a 30-60-90 gg almeno per poi ricontrollarli a 3-6 mesi in funzione della risposta alla terapia.
Nel caso in cui la terapia topica e/o sistemica dovesse fallire nel migliorare i segni e i sintomi dell’occhio secco, è possibile integrare la terapia topica e/o sistemica con un trattamento elettromedicale.
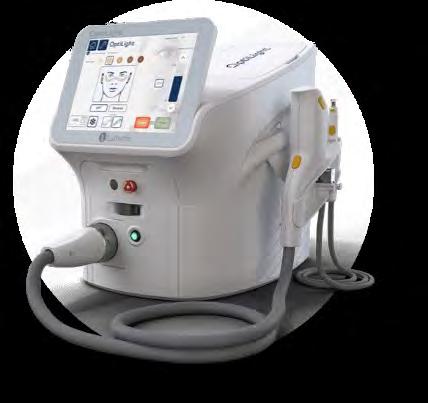
Se il trattamento risulta refrattario alla terapia topica/o sistemica in caso di occhio secco iposecretivo oppure iperevaporativo associato a marcata atrofia delle ghiandole di meibomio, il trattamento che propongo al paziente è il QMR (quantum molecular resonance), che è uno strumento elettromedicale che sfrutta l’energia a bassa potenza e ad alta frequenza. (Fig. 4)
Il QMR si esegue mediante applicazione di una mascherina per 20 minuti a seduta variando la potenza da 3 a 10 a secondo della sensibilità della paziente. Il QMR va eseguito una volta alla settimana per 4 settimane.
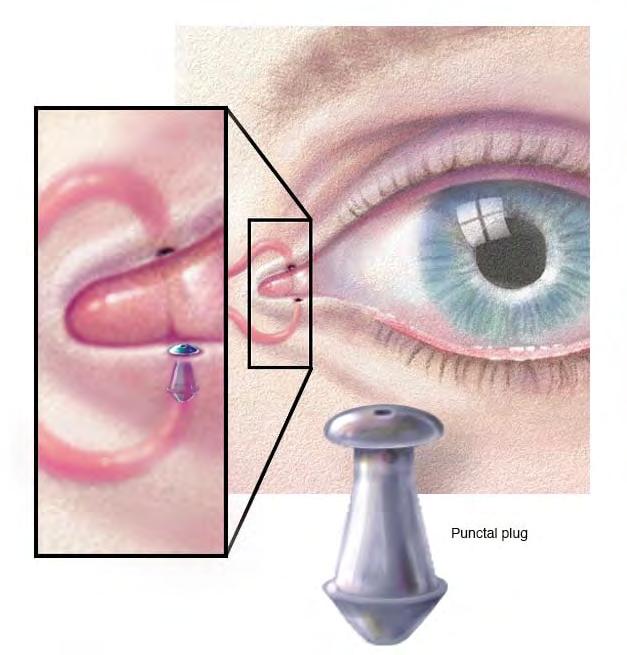
Qualora, dopo 2 mesi dal trattamento, la produzione acquosa del film lacrimale non dovesse essere suf-

ficiente mediante valutazione con test di schirmer, propongo di impiantare i punctum plug nei puntini lacrimali inferiori di entrambi gli occhi e di lasciare una terapia topica a base di un collirio all’acido ialuronico e idrocortisone, da instillare 3 volte al die. (Fig. 5)
In caso di secchezza oculare iperevaporativo con una buona anatomia delle ghiandole di meibomio si può valutare di eseguire un ciclo di trattamento con la luce pulsata, eseguendo dalle 3 alle 4 sedute a intervalli di 15 gg; alla fine di ogni seduta di luce pulsata è consigliabile eseguire la spremitura delle ghiandole di meibomio con una pinza o un forcipe da “squeezing”.
Il protocollo di luce pulsata che consiglio di utilizzare è quello di Toyos con 50 spot tra palpebra superiore e inferiore. (Fig. 6)
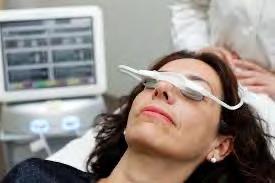
In alternativa, sempre in caso di secchezza oculare iperevaporativa con conservazione della morfologia delle ghiandole di meibomio, si può eseguire una seduta singola di Lipiflow della durata di 12 minuti. (Fig. 7)
Le forme di secchezza oculare miste vanno trattate combinando QMR e luce pulsata o Lipiflow. In questi casi consiglio di eseguire una prima seduta
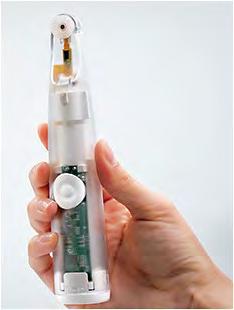
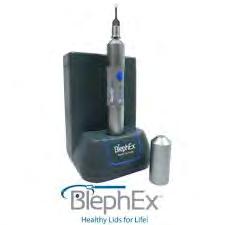
di QMR associata a una seduta di luce pulsata con conseguente spremitura delle ghiandole di meibomio, una seconda seduta solo di QMR, una terza seduta di QMR associato a luce pulsata ed espressione delle ghiandole di meibomio, una quarta seduta solo di QMR e infine una quinta seduta solo di luce pulsata ed espressione delle ghiandole di meibomio. In caso di blefarite anteriore refrattaria alla terapia topica e/o sistemica si può eseguire un trattamento palpebrale con Nulids (Fig. 8) oppure Blephex (Fig. 9) con soluzione a base di tea tree oppure ozonizzante liposomiale.
In caso di blefarite anteriore e/o posteriore si può ricorrere a una terapia domiciliare prolungata con cicli di 10 giorni 2 volte al die di igiene palpebrale con schiume a base di Tea Tree associate o meno a Mela-
tonina oppure a base di olio ozonizzante liposomiale oppure spray a base di Ipoclorito di Sodio più ma schera riscaldante o massaggiatore oculare elettroni co combinato al calore (Fig. 10)
Infine, in caso di dry eye iperevaporativo, si pùò cer care di disostruire le ghiandole di meibomio ostruite utilizzando il jet plasma mediante trattamenti setti manali della durata di 12 minuti per 4 settimane con sonda d’argento mentre nelle forme severe si può usa re la sonda d’oro e in questo caso è sufficiente una sola seduta previa anestesia loco-regionale.
Una volta eseguita la decheratinizzazione del bor do palpebrale si deve procedere all’espressione delle ghiandole di meibomio.
Alcune volte è necessario eseguire prima dell’espres sione delle ghiandole di meibomio il Probing con sonda di Maneskin.
Bibliografia
– Talking on Dry Eye. L. Marino. Protocollo soggettivo del Dry Eye: relazione AIMO 2023 corso IDEA Tedesco Giovanni Roberto
– Stonecipher K, Potvin R. Low level light therapy for the treatment of recalcitrant chalazia. Clinical Ophthalmology 2019;13:1727-1733.

РCraig JP, Chen Y-H, Turnbull PRK. Prospective Trial of Intense Pulsed Light for the Treatment of Meibomian Gland Dysfunction. Investigative Ophthalmology & Visual Science 2015;56:1965–70.
Pult H. Intense Pulse Light and Low-Level Light Therapy in the Treatment of Meibomian Gland Dysfunction. IOVS 2020; ARVO abstract.
– J Optom, 2023 vol. 16(2) pp. 128-134. Evaluating the efficacy of Quantum Molecular Resonance (QMR) electrotherapy in mixed-type dry eye patients
– Trivli, A; Karmiris, E; Dalianis, G; Ruggeri, A; Terzidou, C. Ocul Surf, 2019 vol. 17(2) pp. 250-256
Incidence, demographics, types and risk factors of dry eye disease in India: Electronic medical records driven big data analytics report I Donthineni, PR; Kammari, P; Shanbhag, SS; Singh, V; Das, AV; Basu, S. (da cui preso fig. 1)
Atlante di diagnostica oculare
Guida alla interpretazione delle immagini: Ecografia, OCT, OCTA, Fluorangiografia
Luisa Pierro








1 mg/ml desametasone + 5 mg/ml levofloxacina, collirio, soluzione
DUCRESSA “1 mg/ml + 5 mg/ml, collirio,soluzione”
1 flacone in LDPE da 5 ml con contagocce (AIC n. 047874019)
Classe ai fini della rimborsabilità: Classe C
Prezzo al pubblico (IVA inclusa): € 19,90
Bibliografia: Classificazione ai fini della fornitura: RR - medicinale soggetto a prescrizione medica
1) Bandello F. et al. Eye (Lond). 2020 May 4. doi: 10.1038/s41433-020-0869-1. Online ahead of print.
2) RCP Ducressa.




La combinazione fissa Levofloxacina / Desametasone indicata per la prevenzione e il trattamento dell’infiammazione e per la prevenzione dell’infezione associata all’intervento chirurgico per la cataratta 2




Ducressa fornisce l’efficacia antibatterica con una sola settimana di trattamento dopo l’intervento di cataratta 1
Luca Vigo
Direttore medico - Specialista in Chirurgia refrattiva, Disturbi della lacrimazione e Oftalmologia pediatrica
I problemi di lacrimazione sono oggi molto frequenti ed in continuo aumento.
Problematiche endogene (patologie o disequilibri ormonali, metabolici od immunologici) sono sicuramente la causa principale dei problemi di lacrimazione (dry eye disease) che però vengono ulteriormente aggravati e peggiorati nelle manifestazioni sintomatologiche da condizioni ambientali oggi molto comuni quali l’uso eccessivo di schermi, tablet, smartphone o la permanenza in ambienti molto secchi con aria condizionata/riscaldata.
Per arrivare alla giusta diagnosi, inquadrare al meglio il nostro paziente, dobbiamo partire dalla definizione di dry eye e valutare tutti i dati che sono alla base della patologia per poter classificare il paziente all’interno di una delle forme di occhio secco e poter impostare una terapia specifica ed efficace per risolvere o almeno ridurre la sintomatologia. I tre gruppi principali
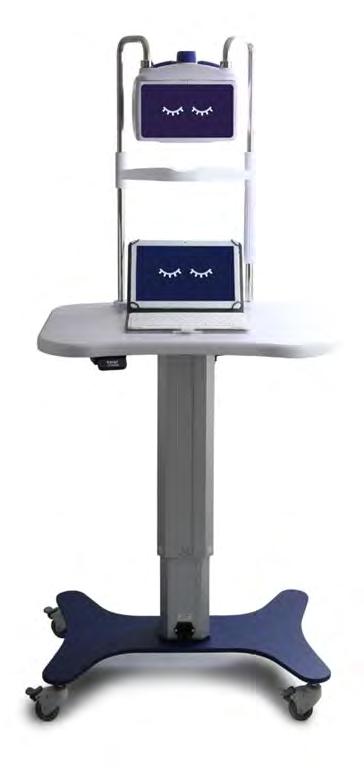

in cui possiamo classificare il paziente con problemi di lacrimazione sono: dry eye iposecretivo per interessamento della ghiandola lacrimale e scarsa produzione della componente acquosa, dry eye evaporativo per eccessiva evaporazione del film lacrimale con disfunzione delle ghiandole di Meibomio per ridotta produzione dello strato lipidico e dry eye misto in cui si ha un coinvolgimento sia della ghiandola lacrimale che delle ghiandole di Meibomio. In ciascun gruppo ovviamente ci possono essere diversi gradi di severità, da definire bene per poter intervenire in modo più o meno incisivo nel trattamento del paziente.
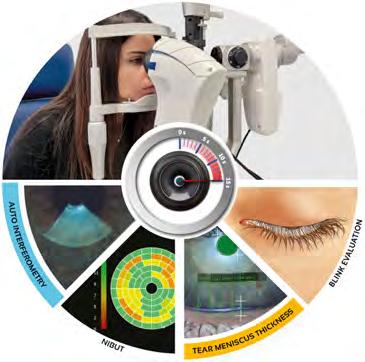
Data quindi la complessità della definizione e della problematica alla base dei disturbi di lacrimazione ritengo che la sola esperienza clinica, sebbene importantissima, non sia sufficiente per arrivare ad una corretta e precisa diagnosi ed inquadramento dei nostri pazienti e da qui la necessità di utilizzare strumenti ed esami che possono aiutare a finalizzare il percorso diagnostico (Fig. 1).
Pur rimanendo indispensabile un’anamnesi accurata per identificare le cause predisponenti sia or-



ganiche che ambientali, è necessario anche valutare la severità della sintomatologia per mezzo di questionari che attraverso domande specifiche possano farci capire quanto la problematica sia fastidiosa o addirittura invalidante per il paziente durante la quotidianità (Fig. 2).
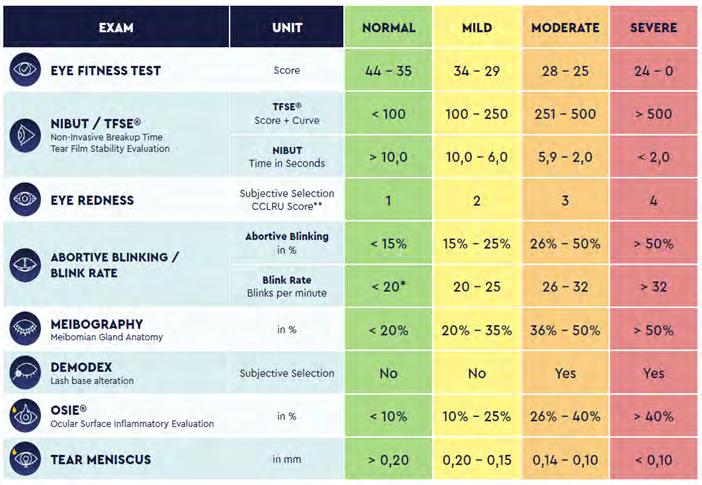
Come primo esame, l’esame dell’osmolarità (Fig. 3) ci permette di dividere i pazienti con problemi di lacrimazione da quelli con una sintomatologia simile ma non correlata con il dry eye: pazienti con un’elevata osmolarità (superiore a 310 mOsm/ litro) o con una differenza tra i due occhi oltre le 8 mOsm/litro hanno sicuramente problemi di lacrimazione e la sintomatologia riferita può essere associata al dry eye; pazienti invece con un’osmolarità nella norma possono manifestare una sintomatologia anche importante ma che potrebbe essere invece correlata ad altri problemi oculari (congiuntiviti atopiche distrofia della membrana
basale epiteliale, alterata sensibilità corneale per uso eccessivo di lenti a contatto...).
La ricerca della metalloproteinasi MMP-9 all’interno del film lacrimale con il test ‘Inflammadry’ (Fig. 4) ci permette inoltre di sapere se è già presente un’infiammazione della superficie oculare, correlata con il dry eye e quindi di suggerire al paziente una terapia antinfiammatoria steroidea o a base di ciclosporina specifica e/o di lunga durata.
Con la valutazione alla lampada a fessura ci accor-
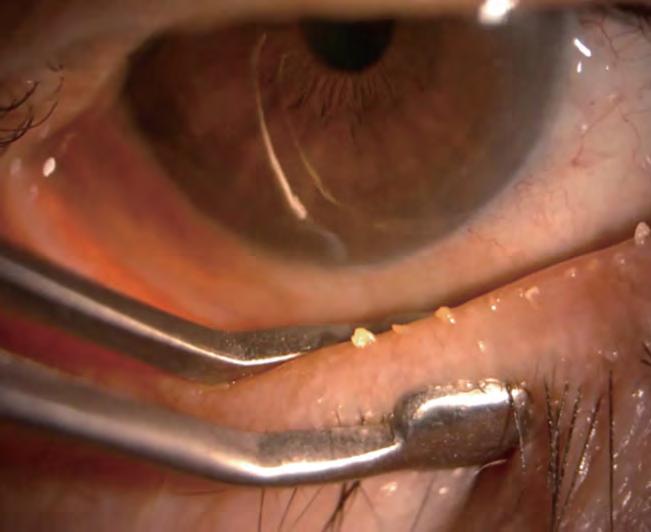
giamo subito se un paziente ha un ammiccamento (blinking) molto frequente o raro ma conoscere se a ciascun ammiccamento corrisponde una efficace spremitura delle ghiandole può non essere così intui-
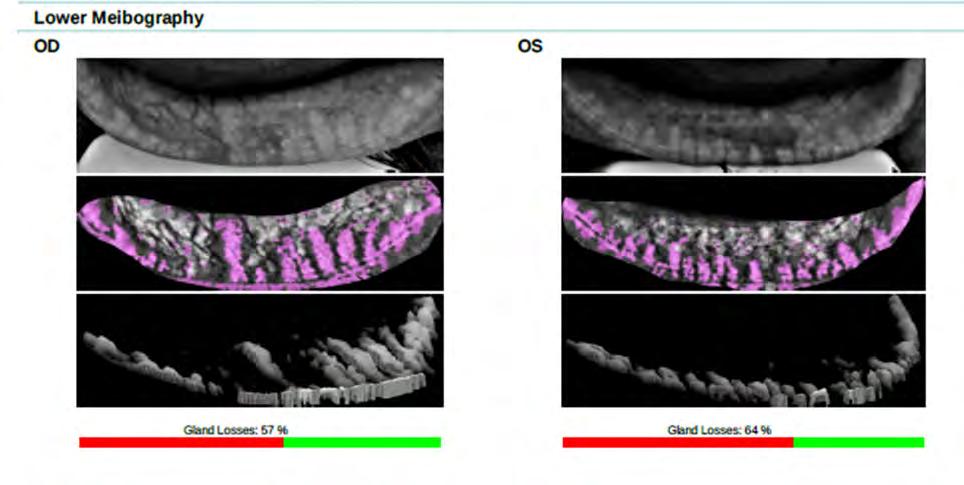
tivo: alcuni dispositivi ci permettono di avere questa informazione che associata ad altre ci conduce ad una corretta diagnosi. Possiamo inoltre spremere le ghiandole di Meibomio (Fig. 5) per capire la qualità e/o quantità del secreto prodotto ma come e quanto le ghiandole siano compromesse lo rileviamo solamente da una meibomiografia (Fig. 6).
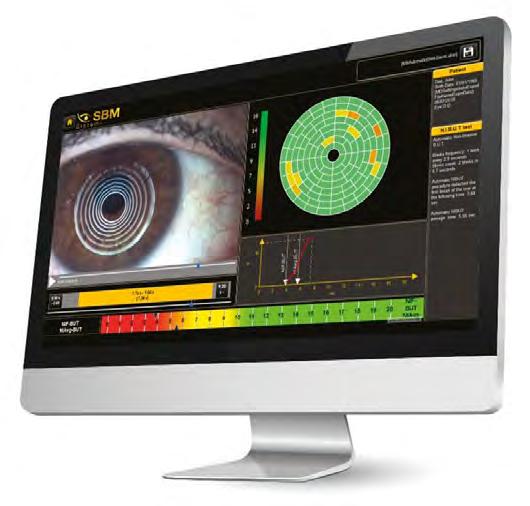
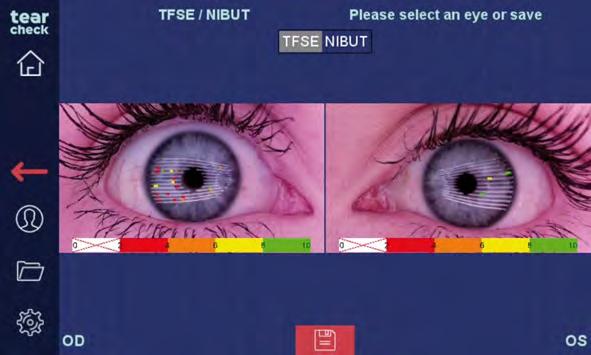
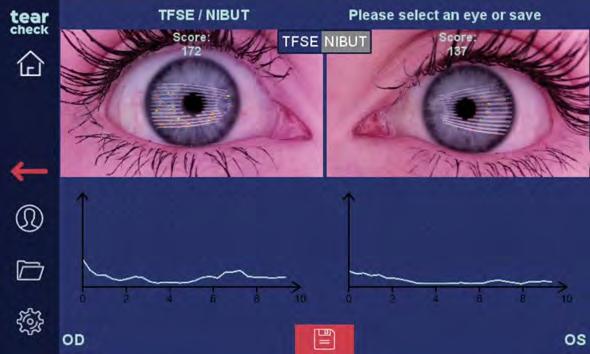
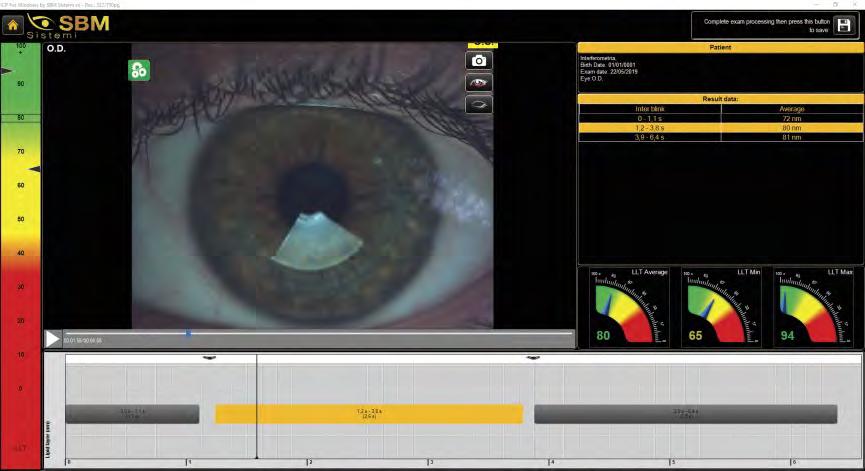
La maggior parte degli strumenti diagnostici del film lacrimale è in grado di darci questa valutazione attraverso una telecamera ad infrarossi e di farlo in modo automatico, sia per la palpebra inferiore che per quella superiore. Siamo in grado in tal modo di conoscere la percentuale di perdita o mal funzionamento delle ghiandole e capire se sono atrofiche, dilatate od ostruite. Questo esame è fondamentale se associato al BUT (Break Up Time) o al NIBUT (Not Invasive Break Up Time) (Fig. 7) e alla misurazione dello strato lipidico attraverso l’interferometria (Fig. 8) o alla valutazione del grado di stabilità ed omogeneità del film lacrimale sulla superficie dell’occhio (TFSE) (Fig. 9). Conoscere dopo quanti secondi e dove si spezza il
film lacrimale sulla cornea è fondamentale per sapere se si tratta di un dry eye evaporativo e grazie alla meibomiografia se questa evaporazione eccessiva è dovuta ad un mal funzionamento delle ghiandole, ad una loro ostruzione o addirittura ad una atrofia. Contare alla lampada a fessura i secondi prima che il film lacrimale si rompa dopo aver colorato la cornea con fluorescina è possibile e semplice ma avere questi dati in modo automatico, senza interpretazione soggettiva è ancora più utile e facile per fare una diagnosi precisa ed impostare una terapia efficace. I dispositivi diagnostici tecnologicamente avanzati ci danno questi valori permettendoci di misurare i tempi di rottura istantanei, medi e le aree dove questa avviene per mezzo di mappe colorate.
La colorazione della superficie oculare (staining) alla lampada a fessura ci permette di valutare se ci sono aree sofferenti, dove l’epitelio è degenerato; grazie agli strumenti diagnostici possiamo analizzare la percentuale di aree compromesse e paragonare i risultati dopo una terapia.
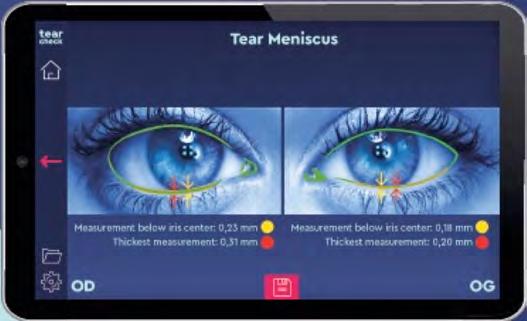
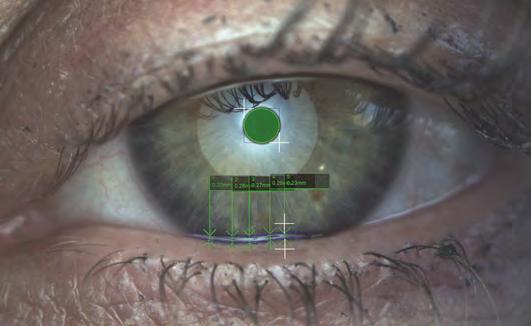
Dopo tutti questi esami sappiamo se il paziente ha un problema di lacrimazione e se può essere associato ad eccessiva evaporazione e ad un problema delle ghiandole di Meibomio ma la valutazione del menisco lacrimale e della produzione acquosa è indispensabile per capire se siamo di fronte anche ad un problema iposecretivo con disfunzione della ghiandola lacrimale oppure solo evaporativo. Il test di Shirmer
rimane sicuramente un esame efficace e preciso ma con la variabile dell’esecuzione e del grado di sensibilità corneale. Grazie agli strumenti high tech possiamo valutare il menisco lacrimale (Fig. 10) senza toccare l’occhio del paziente e correlare questo valore alla produzione della componente acquosa così come facciamo con il test di Shirmer.
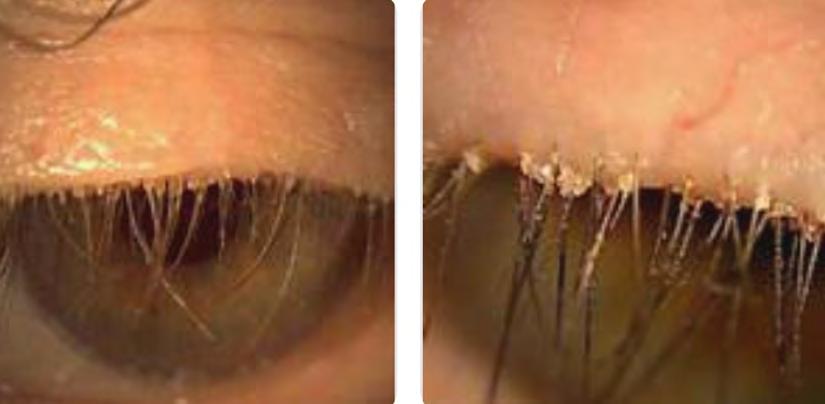
La ricerca dei collaretti alla base delle ciglia (Fig. 11),
delle teleangectasie sul bordo palpebrale, delle secrezioni completano la valutazione dei pazienti alla lampada a fessura per associare al problema di lacrimazione una patologia palpebrale come la blefarite o la blefarocongiuntivite
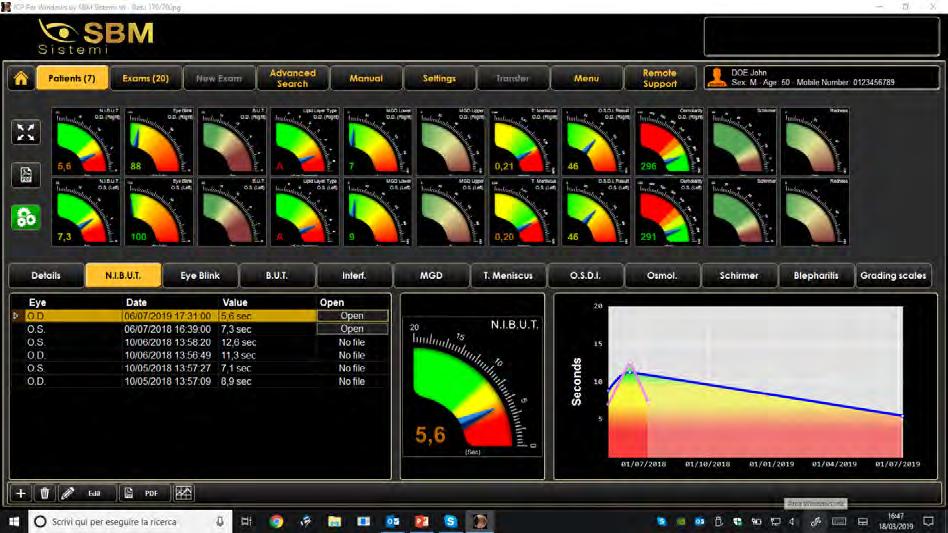
La nostra esperienza clinica rimane quindi importantissima per la classificazione e la diagnosi dei pazienti ma l’utilizzo di strumenti diagnostici sofisticati ci aiuta e semplifica molto l’iter diagnostico. L’insieme di tutti i dati, la loro rappresentazione su un file (Fig. 12), la possibilità di mostrare i risultati ai pazienti ci permette inoltre di affinare e rendere più precisa la nostra diagnosi e di poter proporre più facilmente, anche a pazienti molto preparati ed esigenti, una specifica terapia sia farmacologica che strumentale.
Poter inoltre comparare i risultati in momenti diversi ci permette più facilmente di capire e far compren-
dere al paziente se la terapia è efficace e sta dando i risultati previsti.
In conclusione, data l’importanza e la frequenza dei problemi di lacrimazione, del loro continuo aumento e della correlazione tra problemi di lacrimazione (dry eye) e chirurgia del segmento anteriore (cataratta e refrattiva) risulta importante non solo saper diagnosticare pazienti sintomatici ma essere anche in grado di individuare pazienti ancora asintomatici ma che potrebbero manifestare una sintomatologia importante dopo un intervento chirurgico. Per tale motivo la nostra esperienza pur essendo imprescindibile per la valutazione dei pazienti deve essere associata all’utilizzo di apparecchi sofisticati che siano in grado di fornirci dati più precisi, attendibili e ripetibili per arrivare ad una diagnosi più accurata e di conseguenza ad una terapia più efficace.
Ulrich Spandau - Edizione italiana a cura di Alfonso Anania
NOVITÀ EDITORIALE
Ulrich Spandau
Edizione italiana a cura di Alfonso Anania
Presentazione del Prof. Stanislao Rizzo



FABIANO GRUPPO EDITORIALE
Redazione: Strada 4 Milano Fiori, Palazzo Q7 – 20089 Rozzano (MI)
Sede operativa: FGE srl – Regione Rivelle 7/F – 14050 Moasca (AT) Tel. 0141 1706694 – Fax 0141 856013 – e-mail: info@fgeditore.it – www.fgeditore.it
Gianpiero Covelli
Ospedale
Sant'Andrea - Università Sapienza di Roma
L’astenopia è riconosciuta da oculisti medici del lavoro e medici legali come una sindrome a tal punto che nelle linee guida della SIMLI sulla ergoftalmologia (Società Scientifica dei Medici del Lavoro) è rubricata come sindrome non perimetrabile giuridicamente e quindi non malattia professionale.
– Una sindrome per definizione è un insieme di sintomi che definiscono un corteo sintomatologico individuabile nel suo insieme.
– Una malattia per definizione è una lesione di una funzione che produce dei sintomi.
– L’apparato accomodazione convergenza dell’occhio regolato da un muscolo liscio il muscolo ciliare o muscolo di Riolano a forte componente di fibre lisce e la sua azione consiste nel cambiamento di forma del cristallino e nel processo dell’accomodazione che è funzionale a mettere a fuoco gli oggetti vicini e lontani.
– Un affaticamento oculare dovuto a più situazioni convergenti e coinvolgenti la postazione di lavoro determina una anomalizzazione di una funzione quella dell’apparato accomodazione e convergenza per anomale contrazioni del muscolo ciliare che non assolve più la sua funzione di modifica delle dimensioni del cristallino. I risvolti clinici DI QUESTO DEFAULT sono sfuocamenti di immagini miopizzazioni transitorie, cefalee a volte paresi vere proprie del muscolo irritazione oculare fino ad un occhio secco minore e manifestazioni sistemiche come insonnia, mal di stomaco, nausea ed altre situazione patologiche da somatizzazione.

Covelli
Da cui sembra essere intuitiva a fronte di questa distinzione nosologica, la reale collocazione di questa patologia. Sembra inverosimile e forse improbabile ma da questa piccola sindrome dipendono tante cose con un effetto a cascata su situazioni di rilevante importanza sociale. Un mio carissimo amico direbbe diritti civili e sociali??... fiumi di inchiostro versati. Ci vorrebbe a nostro giudizio una rivisitazione della patologia astenopeica che andrebbe riragionata e si dovrebbe attualizzare un percorso (realmente fantascientifico...) di quantificazione del danno con una valutazione di insieme omnicomprensiva della situazione sistemica e poi instaurare un dialogo con l’inail per un riconoscimento realmente fattivo.
Sarebbe cosa buona e giusta ma politicamente e improbabile e forse un carico eccessivo (ironico) sul bilancio di sistema... quanti sperperi fanno trascurando queste cose che la contrario e con ragionamento inverso farebbero risparmiare il sistema.
L’astenopia non è valutata patologia da tecnostress dall’Inail e dall’0ms ma secondo una nostra improbabile e bislacca ipotesi teorica il meccanismo fisiopatogenetico che ne è alla base risponde a stimoli stressogeni e fa riferimento al sistema parasimpatico. Esempio di percorso di stimolo: situazione anomala e stressogene (e quante ve ne sono)... imput del parasimpatico sul muscolo ciliare, modifica del sistema accomodazione convergenza... anomalo spostamento del cristallino nella messa fuoco degli oggetti. Per cui la potremmo rubricare in maniera improbabile ed eretica come “malattia da tecno stress”.
1. DENOMINAZIONE DEL MEDICINALE Ducressa 1 mg/ml + 5 mg/ml, collirio, soluzione
2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Un ml di collirio, soluzione contiene desametasone sodio fosfato, equivalente a 1 mg di desametasone e levofloxacina emiidrato, equivalente a 5 mg di levofloxacina. Una goccia (circa 30 microlitri) contiene circa 0,03 mg di desametasone e 0,150 mg di levofloxacina. Eccipienti con effetti noti: Un ml di collirio soluzione contiene 0,05 mg di benzalconio cloruro e una goccia contiene circa 0,0015 mg di benzalconio cloruro. Un ml di collirio soluzione contiene 4,01 mg di fosfati e una goccia contiene 0,12 mg di fosfati. Per l’elenco completo degli eccipienti, vedere paragrafo 6.1.
3. FORMA FARMACEUTICA Collirio, soluzione (collirio). Soluzione limpida, giallo-verdastra, praticamente priva di particelle con un pH di 7,0-7,4 e osmolalità di 270-330 mOsm/Kg. Le gocce erogate appaiono trasparenti ed incolore.
4. INFORMAZIONI CLINICHE 4.1 Indicazioni terapeutiche Ducressa collirio, soluzione è indicato per la prevenzione e il trattamento dell’infiammazione e per la prevenzione dell’infezione associata all’intervento chirurgico per cataratta negli adulti. Tenere in considerazione le linee guida ufficiali sull’uso appropriato degli agenti antibatterici. 4.2 Posologia e modo di somministrazione Posologia Dopo l’intervento chirurgico, instillare una goccia nel sacco congiuntivale ogni 6 ore. La durata del trattamento è di 7 giorni. Fare attenzione a non interrompere anticipatamente la terapia. Se si dimentica una dose, il trattamento deve essere proseguito assumendo la dose successiva come pianificato. Dopo una settimana di trattamento con Ducressa collirio si raccomanda di rivalutare il paziente per stabilire se è necessario proseguire con la somministrazione di un collirio a base di corticosteroidi in monoterapia. La durata di questo trattamento può dipendere dai fattori di rischio del paziente e dall’esito dell’intervento chirurgico e deve essere stabilita dal medico dopo un esame con lampada a fessura e in base alla gravità del quadro clinico. Un trattamento di follow-up con collirio a base di steroidi non dovrebbe di norma superare le 2 settimane. Fare comunque attenzione a non interrompere anticipatamente la terapia. Popolazione pediatrica: La sicurezza e l’efficacia di Ducressa nei bambini e negli adolescenti di età inferiore a 18 anni non sono state stabilite. Non ci sono dati disponibili. L’uso di Ducressa non è raccomandato nei bambini e negli adolescenti di età inferiore a 18 anni. Pazienti anziani: Non c’è necessità di modificare la dose nei pazienti anziani. Uso nella compromissione renale/ epatica Ducressa non è stato studiato nei pazienti con compromissione renale/epatica e pertanto, Ducressa deve essere utilizzato con cautela in questi pazienti. Modo di somministrazione Uso oftalmico. Una goccia deve essere somministrata nel canto laterale applicando, nel contempo, una pressione a livello del canto mediale per evitare il drenaggio delle gocce. I pazienti devono essere istruiti a lavarsi le mani prima dell’uso e a evitare il contatto con la punta del contenitore e l’occhio o le aree circostanti, in quanto ciò potrebbe causare lesioni oculari. Inoltre, è necessario informare i pazienti che le soluzioni oftalmiche, se maneggiate in modo improprio, possono venire contaminate da batteri comuni in grado di causare infezioni oculari. L’uso di soluzioni contaminate può arrecare gravi danni all’occhio e successiva perdita della vista. L’occlusione nasolacrimale mediante compressione dei dotti lacrimali può ridurre l’assorbimento sistemico. In caso di trattamento concomitante con altri colliri, le instillazioni devono avvenire a distanza di 15 minuti. 4.3 Controindicazioni • Ipersensibilità al principio attivo levofloxacina o ad altri chinoloni, al desametasone o ad altri steroidi, o ad uno qualsiasi degli eccipienti elencati al paragrafo 6.1; • Cheratite da herpes simplex, varicella e altre malattie virali della cornea e della congiuntiva; • Infezioni oculari da micobatteri causate, ad esempio, da bacilli acido-resistenti quali Mycobacterium tuberculosis, Mycobacterium leprae o Mycobacterium avium; • Micosi delle strutture oculari; • Infezioni oculari purulente non trattate. 4.4 Avvertenze speciali e precauzioni di impiego Effetti oculari: Ducressa è esclusivamente per uso oftalmico. Ducressa non deve essere somministrato per iniezione sottocongiuntivale. La soluzione non deve essere introdotta direttamente nella camera anteriore dell’occhio. L’uso prolungato può indurre resistenza agli antibiotici con conseguente proliferazione di organismi non sensibili, inclusi i miceti. In presenza di infezioni è necessario interrompere il trattamento e adottare una terapia alternativa. Ogni qual volta richiesto dal giudizio clinico, il paziente deve essere esaminato mediante visualizzazione ingrandita, ad esempio tramite biomicroscopia con lampada a fessura ed eventualmente colorazione con fluoresceina. L’uso prolungato di corticosteroidi per uso topico oftalmico può causare ipertensione oculare/glaucoma, il verificarsi di tale evenienza è, tuttavia, improbabile se Ducressa viene utilizzato per il periodo di trattamento raccomandato (7 giorni). È in ogni caso consigliabile un controllo frequente della pressione intraoculare. Il rischio di innalzamento della pressione intraoculare indotto da corticosteroidi è maggiore nei pazienti predisposti (per es. i diabetici). Con l’uso di corticosteroidi sistemici e topici possono essere riferiti disturbi della vista. Se un paziente si presenta con sintomi quali visione offuscata o altri disturbi visivi, è necessario considerare la visita con un oftalmologo per la valutazione delle possibili cause che possono essere collegate a complicanze postoperatorie, allo sviluppo di glaucoma o a patologie rare, quali la corioretinopatia sierosa centrale (CSC), che sono state segnalate dopo l’uso di corticosteroidi sistemici e topici. I corticosteroidi per uso topico oftalmico possono rallentare la guarigione delle ferite corneali. È noto che anche i FANS per uso topico oftalmico possono rallentare o ritardare la guarigione. L’uso concomitante di FANS e steroidi per uso topico oftalmico può aumentare il rischio di problemi di guarigione. Nei pazienti con patologie che causano assottigliamento della cornea o della sclera, è stato riscontrato che si verificano perforazioni con l’uso di corticosteroidi topici. Effetti sistemici I fluorochinoloni sono stati associati a reazioni di ipersensibilità anche dopo una singola dose. In presenza di una reazione allergica alla levofloxacina, interrompere il trattamento. Durante la terapia sistemica con fluorochinoloni, compresa la levofloxacina, possono verificarsi l’infiammazione e la rottura dei tendini, in particolare nei pazienti più anziani e in quelli trattati contemporaneamente con corticosteroidi. È, pertanto, necessario essere cauti e interrompere il trattamento con Ducressa ai primi segni di tendinite (vedere paragrafo 4.8). La Sindrome di Cushing e/o soppressione surrenalica associate con l’assorbimento sistemico di desametasone oculare possono verificarsi dopo terapia intensiva o continuata per lunghi periodi in pazienti predisposti, compresi bambini e pazienti trattati con inibitori del CYP3A4 (compresi ritonavir e cobicistat). In questi casi, il trattamento dovrebbe essere sospeso progressivamente. Effetti sul sistema immunitario L’uso prolungato (in genere si osservano entro le 2 settimane di trattamento) può anche causare infezioni oculari secondarie (batteriche, virali o micotiche), dovute alla soppressione della risposta dell’ospite o a un ritardo nella guarigione. Inoltre, i corticosteroidi per uso topico oftalmico possono favorire, aggravare o mascherare i segni e i sintomi di infezioni oculari causate da microrganismi patogeni. Il verificarsi di tali patologie è limitato se il trattamento con corticosteroidi è di breve durata, come quello suggerito con Ducressa. Eccipienti Benzalconio cloruro: Sono stati riportati casi di irritazione agli occhi, occhio secco, alterazione del film e della superficie corneali a seguito di somministrazione oftalmica di benzalconio cloruro. Da usare con cautela nei pazienti con occhio secco e con compromissione della cornea. I pazienti devono essere monitorati in caso di uso prolungato. Dopo l’intervento di cataratta, i pazienti non devono portare lenti a contatto per tutta la durata del trattamento con Ducressa. 4.5 Interazioni con altri medicinali e altre forme di interazione Non sono stati effettuati studi di interazione. Dato che dopo somministrazione oculare le concentrazioni massime nel plasma di levofloxacina e desametasone sono almeno 1000 volte inferiori a quelle riferite dopo dosi orali standard, è improbabile che le interazioni con altri prodotti per uso sistemico siano clinicamente rilevanti. L’uso concomitante di probenecid, cimetidina o ciclosporina con levofloxacina ha alterato alcuni parametri farmacocinetici della levofloxacina, ma non in misura clinicamente significativa. L’uso concomitante di steroidi topici e FANS topici può aumentare il rischio di problemi di guarigione della cornea. Gli inibitori del CYP3A4 (inclusi ritonavir e cobicistat) possono ridurre la clearance del desametasone potenziandone gli effetti. La combinazione deve essere evitata, a meno che il beneficio non sia superiore al rischio aumentato di effetti collaterali sistemici causati dal corticosteroide, nel qual caso i pazienti devono essere monitorati per tali effetti sistemici. 4.6 Fertilità, gravidanza e allattamento Gravidanza I dati relativi all’uso di desametasone e levofloxacina in gravidanza non sono disponibili o sono in numero limitato. I corticosteroidi attraversano la placenta. L’uso prolungato o ripetuto di corticosteroidi durante la gravidanza è stato associato a un maggiore rischio di ritardo di crescita intrauterina, a un minor peso alla nascita e al rischio di ipertensione, disturbi vascolari e insulino-resistenza in età adulta. I lattanti nati da madri che hanno assunto dosi considerevoli di corticosteroidi durante la gravidanza devono essere sottoposti ad accurati controlli per rilevare eventuali segni di iposurrenalismo. Negli studi condotti sugli animali i corticosteroidi hanno mostrato tossicità riproduttiva ed effetti teratogeni (tra cui palatoschisi; vedere paragrafo 5.3). Dato che non può essere esclusa un’esposizione sistemica rilevante ai corticosteroidi conseguente alla somministrazione oculare, il trattamento con Ducressa non è raccomandato durante la gravidanza, in particolare durante i primi tre mesi, e dovrebbe essere impiegato solo dopo un’attenta valutazione dei rischi e dei benefici. Allattamento La levofloxacina e i corticosteroidi sistemici vengono escreti nel latte materno. Non vi sono dati disponibili per stabilire se nel latte materno possano passare quantità di desametasone tali da produrre effetti clinici nel lattante. Un rischio per il lattante non può essere escluso. È necessario decidere se interrompere l’allattamento con latte materno o interrompere/sospendere la terapia con Ducressa, valutando il beneficio per il bambino derivante dall’allattamento con latte materno e il beneficio per la donna derivante dal trattamento. Fertilità I corticosteroidi somministrati per via sistemica possono compromettere la fertilità maschile e femminile influenzando la secrezione ormonale dell’ipotalamo e dell’ipofisi, come pure la gametogenesi nei testicoli e nelle ovaie. Non è noto se il desametasone per uso oftalmico comprometta la fertilità umana. La levofloxacina non ha causato alcuna compromissione della fertilità nei ratti, a livelli di esposizione notevolmente più elevati rispetto all’esposizione massima nell’uomo dopo la somministrazione oculare. 4.7 Effetti sulla capacità di guidare veicoli e sull’uso di macchinari Come con qualsiasi altro collirio, un offuscamento transitorio della vista o altri disturbi visivi possono pregiudicare la capacità di guidare veicoli e di usare macchinari. In caso di offuscamento della vista, il paziente deve attendere che la vista ritorni nitida prima di mettersi alla guida o usare macchinari. 4.8 Effetti indesiderati Riassunto del profilo di sicurezza 438 pazienti sono stati trattati con Ducressa nell’ambito degli studi clinici. Non si sono verificate reazioni avverse gravi. Le reazioni avverse non gravi più comunemente riportate sono irritazione dell’occhio, ipertensione oculare e cefalea. Elenco tabulare delle reazioni avverse Le seguenti reazioni avverse correlate a Ducressa sono state riportate nel corso di studi clinici in cui sono stati arruolati pazienti sottoposti a intervento chirurgico di cataratta (all’interno di ciascuna categoria di frequenza, le reazioni avverse sono presentate in ordine di frequenza decrescente).
LOREM IPSUM La frequenza delle possibili reazioni avverse di seguito elencate è stata definita sulla base della seguente convenzione:
molto comune
≥1/10 comune
≥1/100, <1/10 non comune
≥1/1.000, <1/100 rara
≥1/10.000, <1/1.000 molto rara
≤1/10.000 non nota
La frequenza non può essere definita sulla base dei dati disponibili
Ducressa (combinazione di levofloxacina/desametasone)
Classificazione per sistemi e organiFrequenza Reazioni avverse
Patologie del sistema nervoso Non comuneCefalea, disgeusia.
Patologie dell’occhio Non comuneIrritazione dell’occhio, sensazione anomala all’occhio, ipertensione oculare. Patologie della cute e del tessuto sottocutaneo Non comunePrurito.
Esami diagnostici Non comunePressione intraoculare aumentata (*). (*) > 6 mmHg che significa aumento significativo della pressione intraoculare
Le reazioni avverse osservate con i singoli principi attivi per uso oftalmico (levofloxacina o desametasone) e che possono potenzialmente manifestarsi anche con Ducressa sono riportate di seguito:
Levofloxacina
Classificazione per sistemi e organiFrequenza Reazioni avverse Disturbi del sistema immunitario Rara
Patologie del sistema nervoso
Reazioni allergiche extraoculari, incluso rash cutaneo.
Molto rara Anafilassi.
Non comuneCefalea.
Patologie dell’occhio Comune Bruciore agli occhi, diminuzione della vista e produzione di filamenti mucosi.
Non comuneFormazione di croste sul margine palpebrale, chemosi, reazione papillare congiuntivale, edema palpebrale, fastidio oculare, prurito oculare, dolore oculare, iperemia congiuntivale, follicoli congiuntivali, secchezza oculare, eritema palpebrale e fotofobia.
Patologie respiratorie, toraciche e mediastiniche
Desametasone
Non comuneRinite.
Molto rara Edema laringeo.
Classificazione per sistemi e organiFrequenza
Patologie dell’occhio
Reazioni avverse
Molto comuneAumento della pressione intraoculare*. Comune Fastidio*, irritazione*, bruciore*, dolore puntorio*, prurito* e visione offuscata*. Non comuneReazioni allergiche e di ipersensibilità, ritardata guarigione delle ferite, cataratta capsulare posteriore*, infezioni opportunistiche, glaucoma*.
Molto rara Congiuntivite, midriasi, ptosi, uveite indotta da corticosteroidi, calcificazioni corneali, cheratopatia cristallina, alterazioni dello spessore corneale*, edema corneale, ulcera corneale e perforazione corneale.
Patologie della cute e tessuto sottocutaneoMolto rara Edema facciale.
Patologie endocrine Frequenza non notaSindrome di Cushing, soppressione surrenalica. * vedere il paragrafo Descrizione di alcune reazioni avverse
Descrizione di selezionate reazioni avverse Aumento della pressione intraoculare Possono manifestarsi aumento della pressione intraoculare (PIO) e glaucoma. L’uso prolungato di corticosteroidi può comportare ipertensione oculare/glaucoma (in particolare nei pazienti con precedente PIO elevata indotta da steroidi o con PIO elevata o glaucoma preesistenti). Bambini e anziani possono essere particolarmente suscettibili all’insorgere di PIO indotta da steroidi (vedere paragrafo 4.4). Anche i diabetici sono più soggetti a sviluppare cataratte sottocapsulari dopo somministrazione prolungata di steroidi topici. Reazioni avverse post-procedurali Nel corso degli studi clinici sono stati segnalati disturbi oculari (per es. edema corneale, irritazione dell’occhio, sensazione anomala all’occhio, aumento della lacrimazione, astenopia, disturbi della cornea, secchezza oculare, dolore oculare, fastidio oculare, uveite, visione offuscata, luminosità visiva, congiuntivite) e nausea. Queste reazioni sono generalmente lievi e transitorie e si reputa siano connesse all’intervento stesso di cataratta. Possibili reazioni avverse connesse alla cornea Nelle patologie che causano assottigliamento della cornea, l’uso topico di steroidi può talora comportare perforazione corneale (vedere paragrafo 4.4). Molto raramente sono stati riportati casi di calcificazione della cornea associati all’uso di colliri contenenti fosfati in pazienti con cornea significativamente danneggiata. Ulteriori reazioni avverse osservate con l’uso prolungato del principio attivo levofloxacina che possono potenzialmente verificarsi anche con Ducressa Rotture dei tendini della spalla, della mano, del tendine di Achille e di altri tendini, che hanno richiesto una riparazione chirurgica, o hanno comportato un’invalidità prolungata, sono state riferite in pazienti trattati con fluorochinoloni per via sistemica. Studi ed esperienze post-marketing con i chinoloni per via sistemica indicano che il rischio di tali rotture può essere aumentato nei pazienti trattati con corticosteroidi, in particolare nei pazienti geriatrici e nei tendini sottoposti a sollecitazioni elevate, incluso il tendine di Achille (vedere paragrafo 4.4). Segnalazione delle reazioni avverse sospette La segnalazione delle reazioni avverse sospette che si verificano dopo l’autorizzazione del medicinale è importante, in quanto permette un monitoraggio continuo del rapporto beneficio/rischio del medicinale. Agli operatori sanitari è richiesto di segnalare qualsiasi reazione avversa sospetta tramite il sistema nazionale di segnalazione all’indirizzo www.aifa.gov.it/content/segnalazioni-reazioni-avverse 4.9 Sovradosaggio La quantità totale di levofloxacina e desametasone 21-Fosfato contenuta nel flaconcino di Ducressa è troppo esigua per indurre effetti tossici dopo un’assunzione accidentale.
a cura di In caso di sovradosaggio topico il trattamento deve essere interrotto. In caso di irritazione prolungata, sciacquare l’occhio/gli occhi con acqua sterile. La sintomatologia dovuta a ingestione accidentale non è nota. Il medico può considerare la lavanda gastrica o l’emesi. 5. PROPRIETÀ FARMACOLOGICHE 5.1 Proprietà farmacodinamiche Categoria farmacoterapeutica: agenti antinfiammatori e antinfettivi in combinazione, corticosteroidi e antinfettivi in combinazione. Codice ATC: S01C A01. Ducressa è una combinazione fissa di due principi attivi: levofloxacina e desametasone. Levofloxacina: Meccanismo d’azione: La levofloxacina, L-isomero attivo dell’ofloxacina, è un agente antibatterico della classe dei fluorochinoloni che inibisce le topoisomerasi batteriche di tipo II: DNA girasi e topoisomerasi IV. I target della levofloxacina sono principalmente la DNA girasi nei batteri Gram-negativi e la topoisomerasi IV nei batteri Gram-positivi. Lo spettro di attività contro i patogeni oculari include microrganismi aerobi Gram-positivi (per es. S. aureus MSSA, S. pyogenes, S. pneumoniae e gli streptococchi del gruppo viridans), batteri aerobi Gram-negativi (per es. E. coli, H. influenzae, M. catarrhalis, isolati ambientali di P. aeruginosa) e altri organismi (per es. Chlamydia trachomatis). Meccanismo di resistenza La resistenza batterica alla levofloxacina può svilupparsi principalmente attraverso due meccanismi principali: una riduzione della concentrazione intrabatterica del farmaco o alterazioni dei suoi enzimi target. L’alterazione del sito target deriva da mutazioni dei geni cromosomici che codificano la DNA girasi (gyrA e gyrB) e la topoisomerasi IV (parC e parE; grlA e grlB nello Staphylococcus aureus). La resistenza dovuta a una bassa concentrazione intrabatterica del farmaco può essere legata a un’alterazione delle porine della membrana esterna (OmpF), con conseguente riduzione del passaggio dei fluorochinoloni all’interno dei batteri Gram-negativi, oppure alle pompe di efflusso. La resistenza mediata dalle pompe di efflusso è stata descritta in pneumococchi (PmrA), stafilococchi (NorA), anaerobi e batteri Gram-negativi. Infine, una resistenza ai chinoloni mediata dai plasmidi (determinata dal gene qnr) è stata descritta nella Klebsiella pneumoniae e nell’E. coli Resistenza crociata Può verificarsi una resistenza crociata tra i fluorochinoloni. Le singole mutazioni possono non comportare resistenza clinica, tuttavia le mutazioni multiple generalmente comportano resistenza clinica a tutti i farmaci appartenenti alla classe dei fluorochinoloni. Le porine alterate della membrana esterna e i sistemi di efflusso possono avere un’ampia specificità di substrato, individuando diverse classi di agenti antibatterici, con conseguente resistenza multipla. Criteri interpretativi dei saggi di sensibilità Non ci sono criteri interpretativi. Desametasone: Meccanismo d’azione: I corticosteroidi come il desametasone sopprimono l’espressione delle molecole di adesione delle cellule endoteliali vascolari, delle ciclossigenasi I o II e delle citochine. Tale azione culmina in un’espressione ridotta dei mediatori proinfiammatori e nella soppressione dell’adesione dei leucociti circolanti all’endotelio vascolare, impedendo pertanto la loro migrazione nel tessuto oculare infiammato. Il desametasone esercita una spiccata attività antinfiammatoria con un’attività mineralcorticoide limitata rispetto ad alcuni altri steroidi, ed è uno dei più importanti agenti antinfiammatori. Efficacia clinica: L’efficacia di Ducressa è stata indagata in uno studio controllato per valutare la non inferiorità di Ducressa rispetto al trattamento standard con una formulazione commerciale di tobramicina (0,3%) e desametasone (0,1%) in gocce oculari, per la prevenzione e il trattamento dell’infiammazione e per la prevenzione delle infezioni associate all’intervento chirurgico per cataratta negli adulti. Allo Sperimentatore addetto alla valutazione dei parametri dello studio non è stata resa nota l’assegnazione del trattamento. I pazienti che dopo l’intervento di cataratta non presentavano complicanze sono stati assegnati a Ducressa collirio, 1 goccia 4 volte al giorno per 7 giorni, seguito da desametasone 0,1% collirio, 1 goccia 4 volte al giorno, per altri 7 giorni, o al trattamento di riferimento con tobramicina + desametasone collirio, 1 goccia 4 volte al giorno per 14 giorni. I dati di efficacia sono disponibili in 395 pazienti trattati con Ducressa e in 393 pazienti trattati con il prodotto di riferimento dopo l’intervento di cataratta. Dopo 14 giorni di trattamento, la percentuale di pazienti che non presenta segni di infiammazione (endpoint primario dello studio) nel gruppo Ducressa seguito da desametasone è del 95,19%, rispetto al 94,91% del gruppo tobramicina + desametasone. La differenza tra le due percentuali è di 0,0028 (IC al 95%: [-0,0275; 0,0331]), dimostrano pertanto la non inferiorità del regime di trattamento sperimentale rispetto a quello di riferimento. Nel corso dello studio l’endoftalmite non è stata riscontrata in nessuno dei due gruppi. Nel braccio Ducressa, i segni di infiammazione della camera anteriore sono risultati assenti nel 73,16% dei pazienti al giorno 4 e nell’85,57% dei pazienti al giorno 8 successivi all’intervento chirurgico. Nel braccio tobramicina + desametasone, i segni di infiammazione della camera anteriore sono risultati assenti nel 76,84% dei pazienti al giorno 4 e nell’86,77% dei pazienti al giorno 8. L’iperemia congiuntivale è già assente al giorno 4 nell’85,75% dei pazienti del braccio Ducressa rispetto all’82,19% del braccio tobramicina + desametasone. Il profilo di sicurezza è risultato simile in entrambi i gruppi. Popolazione pediatrica L’Agenzia europea per i medicinali ha previsto l’esonero dall’obbligo di presentare i risultati degli studi con Ducressa in tutti i sottogruppi della popolazione pediatrica per la prevenzione e il trattamento dell’infiammazione e per la prevenzione delle infezioni associate all’intervento chirurgico per cataratta (vedere paragrafo 4.2 per informazioni sull’uso pediatrico). 5.2 Proprietà farmacocinetiche L’instillazione oculare di Ducressa comporta l’assorbimento di entrambi i principi attivi nei tessuti oculari e, in misura molto minore, nella circolazione sistemica. Nei conigli, dopo instillazione oculare, le concentrazioni plasmatiche di levofloxacina aumentano con la dose, sia dopo somministrazione singola, sia dopo somministrazione ripetuta. I livelli di desametasone sodio fosfato misurati nel plasma sono bassi. Infatti, il desametasone sodio fosfato viene rapidamente metabolizzato in vivo in desametasone, che è il metabolita attivo. L’esposizione al desametasone aumenta con la dose e dopo dosi ripetute è evidente un lieve accumulo sia di levofloxacina sia di desametasone. Nei tessuti oculari (umore acqueo, cornea e congiuntiva) i livelli di levofloxacina e di desametasone risultano superiori ai livelli massimi plasmatici dopo dosi singole e ripetute. In particolare, dopo 28 giorni di trattamento i livelli di levofloxacina e desametasone nei tessuti oculari sono superiori alla Cmax plasmatica da 50 a 100 volte e da 3 a 4 volte, rispettivamente. Centoventicinque pazienti sottoposti a intervento chirurgico di cataratta sono stati assegnati in modo casuale a 3 gruppi: levofloxacina, desametasone e Ducressa. Una goccia di ciascun farmaco è stata somministrata 90 e 60 minuti prima della paracentesi limbare. La media dei valori osservati per la concentrazione di levofloxacina era di 711,899 ng/ml (IC al 95%: 595,538; 828,260) nel gruppo Ducressa, e di 777,307 ng/ml (IC al 95%: 617,220; 937,394) con somministrazione della sola levofloxacina. Le concentrazioni di levofloxacina nell’umore acqueo sono ben al di sopra delle concentrazioni minime inibitorie per i patogeni oculari nello spettro di attività della levofloxacina. Quando Ducressa è stato somministrato con desametasone si è raggiunta una concentrazione nell’umore acqueo di 11,774 ng/ml (IC al 95%: 9,812; 13,736) rispetto ai 16,483 ng/ml (IC al 95%: 13,736; 18,838) con somministrazione del solo desametasone. Sia la levofloxacina sia il desametasone vengono eliminati con le urine. 5.3 Dati preclinici di sicurezza Gli studi sulla tossicità oculare per dosi ripetute condotti nei conigli con la combinazione fissa di levofloxacina/desametasone per un periodo di 28 giorni hanno evidenziato tossicità sistemiche attribuibili a effetti farmacologici esagerati del desametasone (necrosi focale delle cellule tubulari e glomerulopatia con necrosi e/o depositi ialini nei reni, ipertrofia epatica con inclusioni ialine intracellulari e necrosi di singole cellule, atrofia della corteccia surrenale e diminuzione dei linfociti dovuta ad atrofia della milza, del timo e dei linfonodi). Tali effetti sono stati osservati solo a esposizioni circa 3 volte superiori rispetto a quelle raggiunte alla massima dose oftalmica raccomandata per l’uomo, a indicare la scarsa rilevanza nell’uso clinico. Gli studi condotti sugli animali hanno dimostrato che gli inibitori della girasi causano disturbi nella crescita delle articolazioni portanti. Nel ratto e nel cane la levofloxacina, come altri fluorochinoloni, ha mostrato effetti sulla cartilagine (formazione di vesciche e cavità) dopo dosi elevate per via orale. Genotossicità e cancerogenicità Il desametasone e la levofloxacina non rivelano alcun potenziale genotossico o cancerogeno clinicamente rilevante. Tossicità riproduttiva: La levofloxacina non ha influenzato la fertilità e ha compromesso lo sviluppo embrio-fetale negli animali solo a esposizioni notevolmente più elevate di quelle raggiungibili con la dose terapeutica per via oftalmica raccomandata per l’uomo. La somministrazione topica e sistemica di desametasone ha compromesso la fertilità maschile e femminile e indotto effetti teratogeni che comprendono formazione di palatoschisi, ritardo di crescita intrauterina e mortalità fetale. È stata osservata anche una tossicità peri- e postnatale del desametasone. Potenziale fototossico: Gli studi nel topo, dopo dosaggio sia orale sia endovenoso, hanno mostrato che la levofloxacina svolge un’attività fototossica solo a dosi molto elevate.
6. INFORMAZIONI FARMACEUTICHE 6.1 Elenco degli eccipienti Sodio diidrogeno fosfato monoidrato, Disodio fosfato dodecaidrato, Sodio citrato, Benzalconio cloruro, Sodio idrossido/acido cloridrico (per la correzione del pH), Acqua per preparazioni iniettabili 6.2 Incompatibilità Non pertinente. 6.3 Periodo di validità 3 anni. Eliminare entro 28 giorni dopo la prima apertura. 6.4 Precauzioni particolari per la conservazione Questo medicinale non richiede alcuna precauzione particolare per la conservazione. 6.5 Natura e contenuto del contenitore Flacone da 5 ml in polietilene a bassa densità (LDPE), con un contagocce in LDPE e un tappo a vite in polietilene ad alta densità (HDPE). Confezione da: 1 flacone x 5 ml 6.6 Precauzioni particolari per lo smaltimento L’antibiotico non utilizzato o la soluzione antibiotica residua e i materiali utilizzati per la somministrazione devono essere smaltiti in conformità alla normativa locale vigente.
7. TITOLARE DELL’AUTORIZZAZIONE ALL’IMMISSIONE IN COMMERCIO SANTEN OY Niittyhaankatu 20 33720 Tampere Finlandia
8. NUMERO(I) DELL’AUTORIZZAZIONE ALL’IMMISSIONE IN COMMERCIO AIC n. 047874019 - “1 MG/ML + 5 MG/ML COLLIRIO, SOLUZIONE” 1 FLACONE IN LDPE DA 5 ML CON CONTAGOCCE
9. DATA DELLA PRIMA AUTORIZZAZIONE/RINNOVO DELL’AUTORIZZAZIONE Data della prima autorizzazione: 15 ottobre 2020. Data del rinnovo più recente:
10. DATA DI REVISIONE DEL TESTO 07/2022
DUCRESSA “1 mg/ml + 5 mg/ml, collirio, soluzione” 1 flacone in LDPE da 5 ml con contagocce (AIC n. 047874019). Classificazione ai fini della fornitura: RR - medicinale soggetto a prescrizione medica. Classe ai fini della rimborsabilità: classe C. Prezzo al pubblico (IVA inclusa): € 19,90
F. Serino, F. Franco, F. Giansanti
SOD oculistica - Azienda Ospedaliero Universitaria Careggi
La degenerazione maculare senile legata all’età (DMLE) è una delle principali cause al mondo di perdita permanente dell’acuità visiva nelle persone con età superiore a 50 anni. Circa l’8.7% della popolazione mondiale ne è affetta, con numeri destinati a crescere in conseguenza all’invecchiamento della popolazione.
Nonostante il successo delle terapie con farmaci intravitreali che inibiscono il fattore di crescita dell’endotelio vascolare (in inglese vascular endothelial growth factor, da cui la sigla VEGF), una cospicua percentuale di pazienti progredisce a fasi di malattia avanzate, con gravi riduzioni del visus (ipovisione) finanche alla cecità bilaterale.
La riabilitazione dell’ipovisione ha lo scopo di consentire a pazienti con malattia avanzata di recuperare o mantenere alcune attività della vita quotidiana
vi esterni presentano una serie di limiti, dall’aspetto puramente estetico alla riduzione marcata del campo visivo e alle limitazioni muscoloscheletriche e di coordinazione.
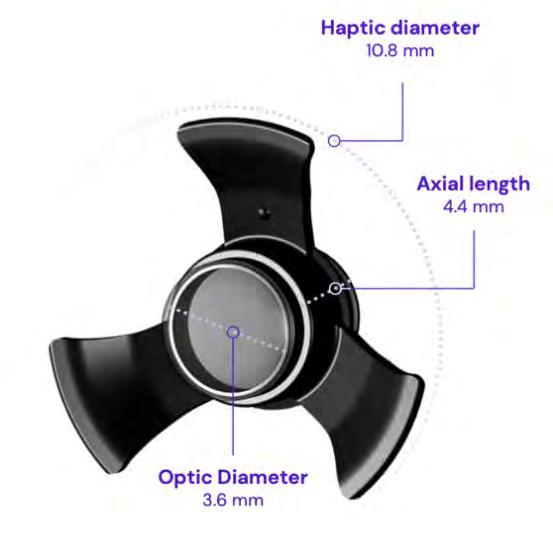

Da qui l’idea di utilizzare delle lenti intraoculari (IOL) con capacità di ingrandire l’immagine. La lente Small Incision New Generation IMT (SING-IMT) è stato approvata dalle autorità europee nel 2020(1-4) (Fig. 1). Funziona come un telescopio galileiano, con un potere di magnificazione 2.7x (Fig. 2). Induce una riduzione del campo visivo a 20°-24°, rendendo possibile l’impianto in un solo occhio (l’altro verrà usato per l’orientamento). Il grande vantaggio rispetto alla generazione di lenti precedente (IMTTM - Vision Care Ophthalmic Technologies, Saratoga, CA), è che si presenta precaricata nel suo iniettore, grazie alle aptiche in silicone pieghevoli che riprendono immediatamente forma una volta che il SING IMT è iniettato nel sacco capsulare.
Sono elegibili ad intervento pazienti con DMLE avanzata bilaterale stabile (in assenza di trattamento anti VEGF da oltre 6 mesi) ed età superiore a 55 anni. Le controindicazioni all’impianto sono stringenti: malattie retiniche di qualsiasi natura ad eccezione della DMLE, glaucoma cronico non controllato (o IOP > 22 mmHg), patologie corneali (comprese le guttae), miopia >6D oppure ipermetropia >4D.
Particolare attenzione deve essere prestata durante lo screening dei pazienti. La valutazione di idoneità
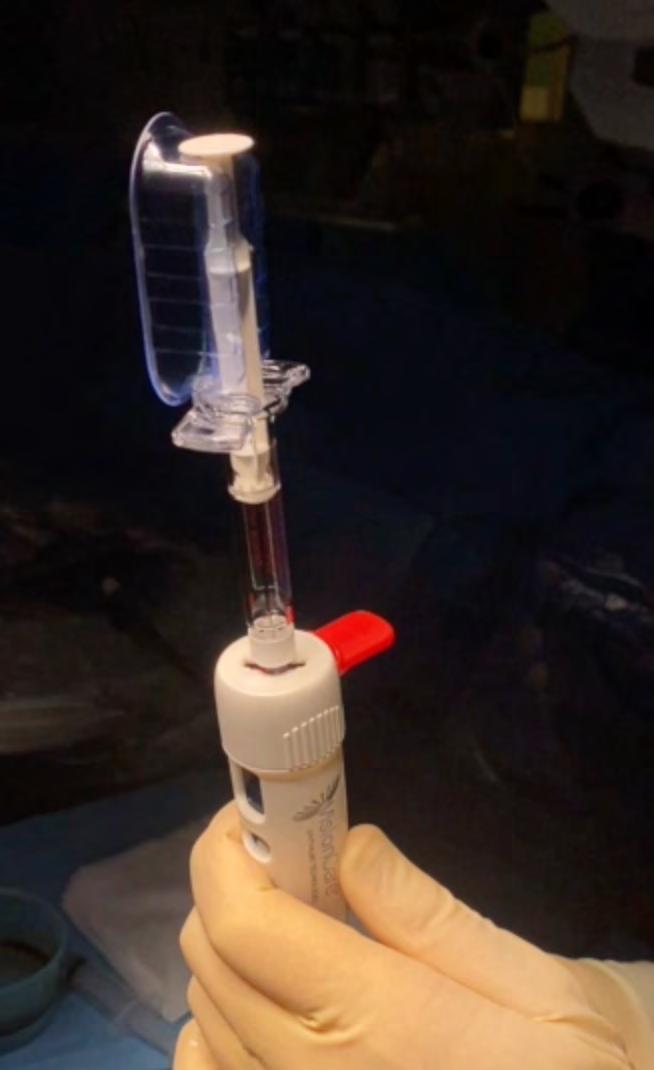
all’impianto deve essere volta ad appurare non solo la presenza delle caratteristiche anatomiche necessarie ad una procedura sicura (profondità della camera anteriore ≥ 2.5 mm, lunghezza assiale AL > 21 mm e conta endoteliale > 1600 cell/mm2), ma anche a valutare le caratteristiche cognitive del paziente, le sue motivazioni, la capacità di comprendere i limiti e gli obiettivi dell’impianto e della necessità di un percorso riabilitativo post-operatorio. Al fine di simulare l’effetto di magnificazione, di minimizzazione dello scotoma, ma anche di riduzione del campo visivo, durante la visita di screening viene effettuata una valutazione (monoculare) con un telescopio esterno ingrandente 3x.
Presso la Clinica Oculistica in AOU Careggi di Firenze abbiamo eseguito l’impianto di SING IMT in sette pazienti affetti da AMD bilaterale stabile. Abbiamo complessivamente registrato un incremento nelle capacità visive, per lontano ma soprattutto per vicino (acuità di lettura). Tali miglioramenti si sono avuti dal primo mese post chirurgia, momento a partire dal quale il paziente iniziava le sedute di riabilitazione con l’ortottista dedicata. La procedura si è dimostrata al contempo sicura dal momento che non si
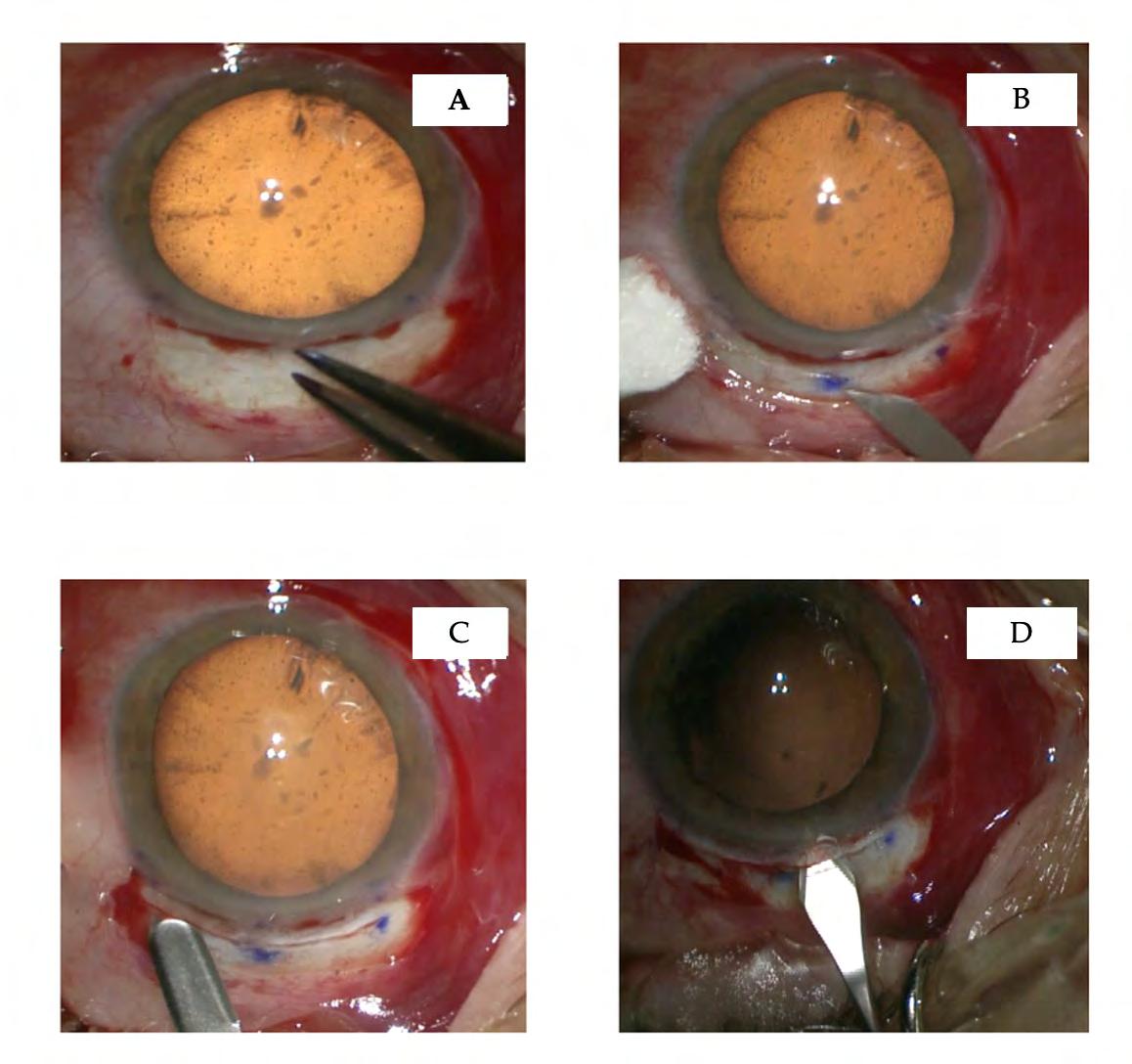



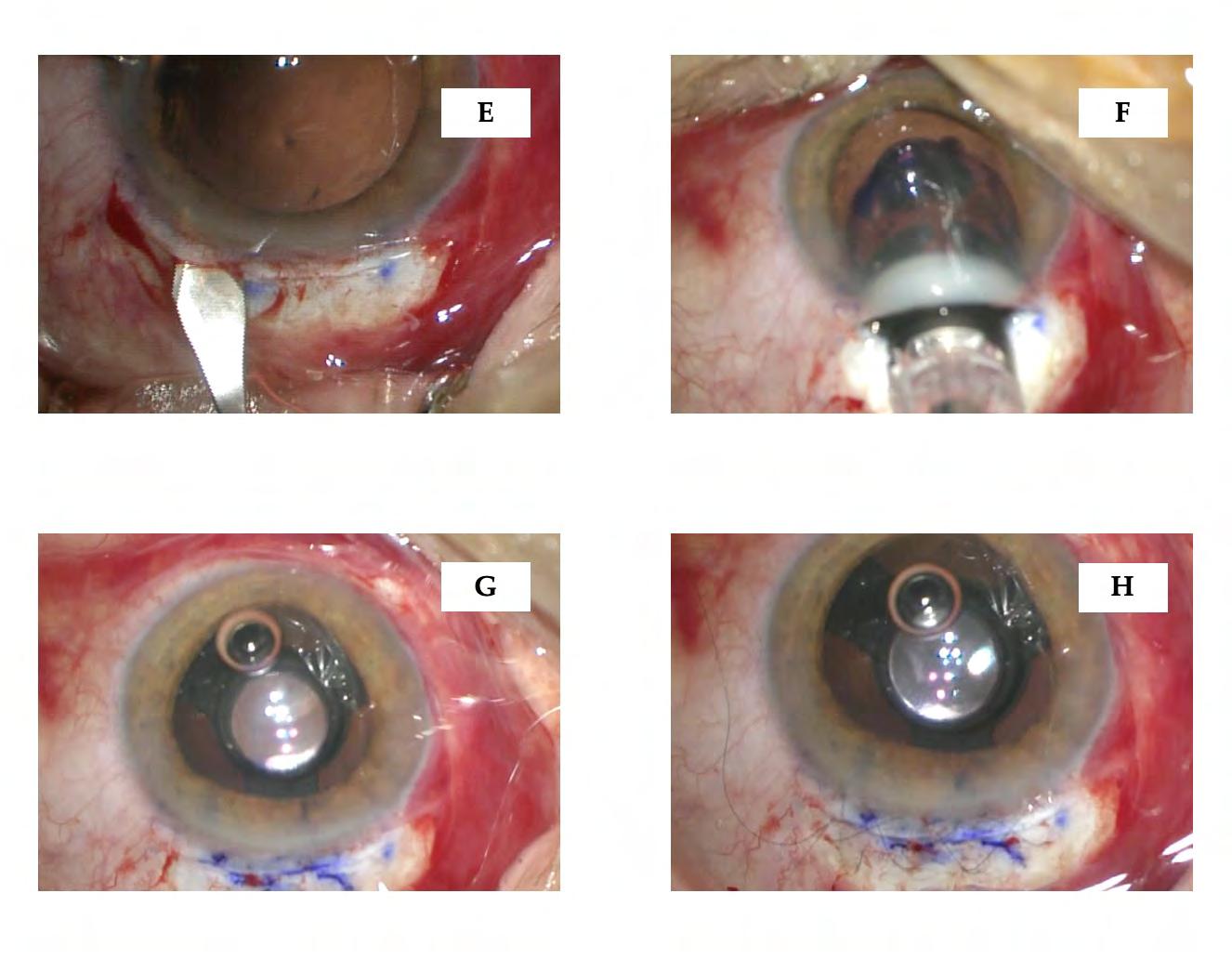

Figura 5. Fasi dell’impianto: allargamento del taglio sclerale (E); ingresso del cartridge caricato con il dispositivo: risulta fondamentale ai fini di una buona riuscita chirurgica che la punta dell’iniettore raggiunga il piano della capsuloressi (F); SING IMT nel sacco capsulare (G); sutura del taglio sclerale con Nylon 10-0 e controllo intraoperatorio dell’astigmatismo indotto con il cheratoscopio integrato nel microscopio operatorio (H).


lule endoteliali corneali. L’effetto collaterale più frequente (2 pazienti su 7) è stato la formazione di una membrana di fibrina in campo pupillare nelle prime settimane postchirurgiche, risoltesi con trattamento steroideo topico.
Dalla nostra esperienza si evince che nonostante i ri-
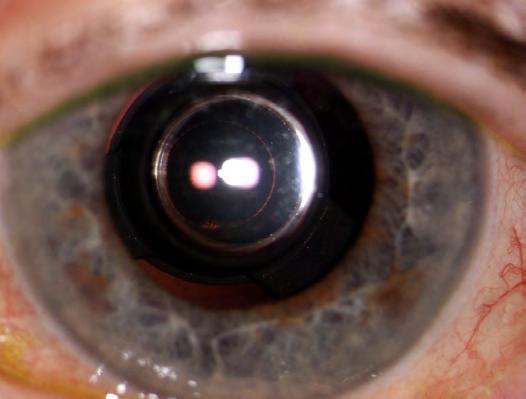
6. Occhio di un paziente impiantato con SING IMT nella prima giornata post-operatoria.
sultati tendenzialmente positivi in termini di capacità visiva monoculare, tuttavia 3 dei 7 pazienti sono stati sottoposti ad esianto del dispositivo rispettivamente a 1, 2 e 6 mesi dalla chirurgia. Tali pazienti hanno lamentato intollerabile adattamento alla visione monoculare, con gravi deficit nell’orientamento dato dalla riduzione campimetrica indotta dall’impianto. Gli interventi di espianto si sono svolti in sicurezza, concludendosi con impianto di IOL monofocale. L’estrazione della IOL telescopica mantenendo integro il sacco capsulare è stata possibile dal momento che, anche a 6 mesi dalla prima chirurgia (come nel caso 2), non erano presenti aderenze significative tra le aptiche (in silicone), il telescopio (in vetro) e la capsula. In letteratura è riportato una percentuale di espianto del 5.2% (5) e 16% (6). Nella nostra serie la percentuale è stata invece del 40%.
Considerate le percentuali riportate, la nostra esperienza fa luce sulla necessità di chiarire ed approfondire gli aspetti psicologici che possono conseguire da questa tipologia di procedura, al fine di migliorare il processo di selezione del paziente ed evitare la necessità di un reintervento.
Bibliografia
1. Hudson, H.L.; Lane, S.S.; Heier, J.S.; Stulting, R.D.; Singerman, L.; Lichter, P.R.; Sternberg, P.; Chang, D.F.; IMT-002 Study Group. Implantable miniature telescope for the treatment of visual acuity loss resulting from end-stage age-related macular degeneration: 1-year results. Ophthalmology 2006, 113, 1987–2001.
2. Hudson, H.L.; Stulting, R.D.; Heier, J.S.; Lane, S.S.; Chang, D.F.; Singerman, L.J.; Bradford, C.A.; Leonard, R.E.; IMT002 Study Group. Implantable telescope for end-stage age-related macular degeneration: Long-term visual acuity and safety outcomes. Am. J. Ophthalmol. 2008, 146, 664–673.e1
3. Toro, M.D.; Vidal-Aroca, F.; Montemagni, M.; Xompero, C.; Fioretto, G.; Costagliola, C. Three-Month Safety and Efficacy Outcomes for the Smaller-Incision New-Generation Implantable Miniature Telescope (SING IMT™). J. Clin. Med. 2023
4. Savastano, A.; Ferrara, S.; Sasso, P.; Savastano, M.C.; Crincoli, E.; Caporossi, T.; De Vico, U.; Vidal Aroca, F.; Francione, G.; Sammarco, L.; et al. Smaller-Incision new-generation implantable miniature telescope: Three-months follow-up study. Eur. J. Ophthalmol. 2023
5. Boyer, D.; Freund, K.B.; Regillo, C.; Levy, M.H.; Garg, S. Longterm (60-month) results for the implantable miniature telescope: Efficacy and safety outcomes stratified by age in patients with end-stage age-related macular degeneration. Clin. Ophthalmol. 2015, 9, 1099–1107.
6. Mastropasqua R, Gironi M, D'Aloisio R, Pastore V, Boscia G, Vecchiarino L, Perna F, Clemente K, Palladinetti I, Calandra M, Piepoli M, Porreca A, Di Nicola M, Boscia F. Intraoperative Iridectomy in Femto-Laser Assisted Smaller-Incision New Generation Implantable Miniature Telescope. J Clin Med. 2023 Dec 22;13(1):76. doi: 10.3390/jcm13010076
ATLANTE DELLE INFIAMMAZIONI OCULARI NOVITÀ EDITORIALE


ATLANTE DELLE INFIAMMAZIONI OCULARI PARTE II - SEGMENTO POSTERIORE NOVITÀ EDITORIALE Parte I Segmento anteriore Parte II Segmento posteriore


FABIANO GRUPPO EDITORIALE
Redazione: Strada 4 Milano Fiori, Palazzo Q7 – 20089 Rozzano (MI) Sede operativa: FGE srl – Regione Rivelle 7/F – 14050 Moasca (AT) Tel. 0141 1706694 – Fax 0141 856013 – e-mail: info@fgeditore.it – www.fgeditore.it Atlante delle infiammazioni oculari
Parte III Multimodal Imaging

Volume 1
Ophthalmology up-to-date

Volume 2

FABIANO GRUPPO
EDITORIALE
Redazione: Strada 4 Milano Fiori, Palazzo Q7 – 20089 Rozzano (MI) Sede operativa: FGE srl – Regione Rivelle 7/F – 14050 Moasca (AT) Tel. 0141 1706694 – Fax 0141 856013 – e-mail: info@fgeditore.it – www.fgeditore.it
approfondimenti in collaborazione con le Aziende del settore
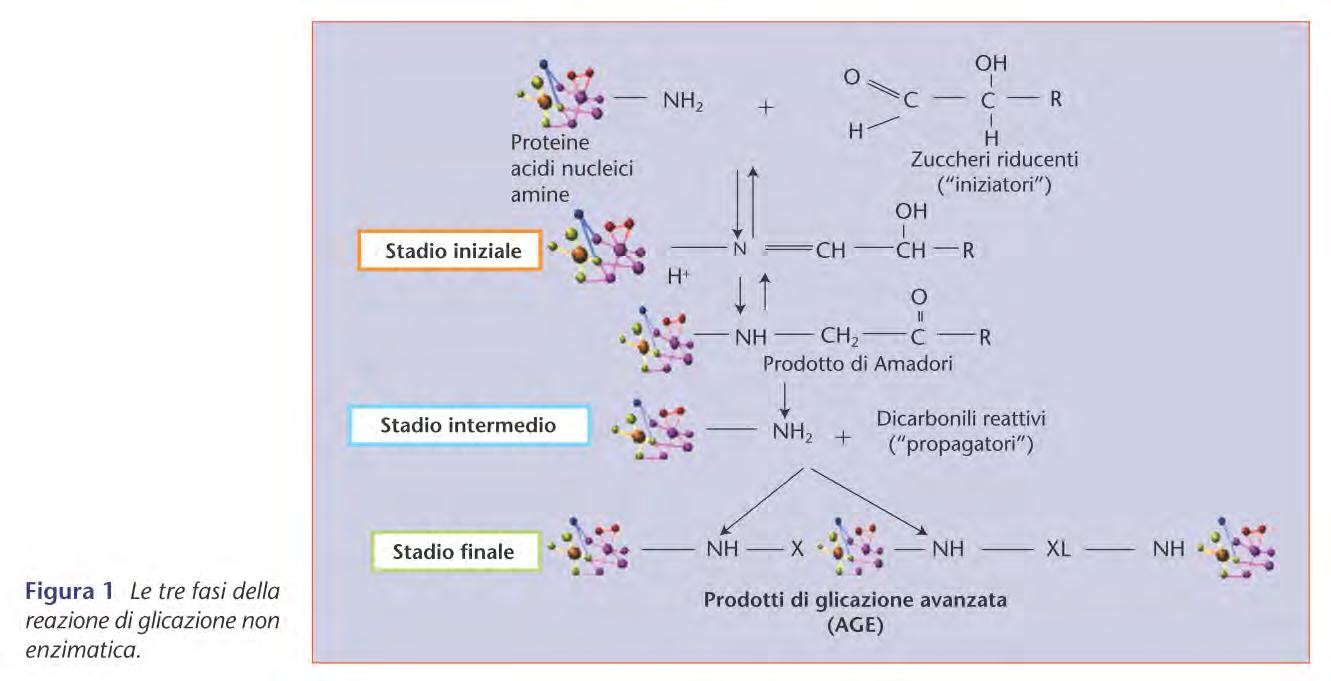
Il diabete mellito è caratterizzato da un’iperglicemia che determina uno stato infiammatorio cronico conseguente alla alterata omeostasi cellulare. Tutto ciò si riflette in un danno vascolare e disfunzionale multiorgano, che a livello della retina si può presentare con complicanze microvascolari e danno alla neuroretina. L’eccesso dei prodotti di glicazione avanzata (AGE), innesacata da specie reattive dell’ossigeno (ROS), è uno dei meccanismi più importanti coinvolti nella fisiopatologia delle complicanze croniche del diabete, come le microemorragie retiniche.
ERREDI e la protezione dei capillari nella retinopatia diabetica non proliferante Esistono alcuni particolari micronutrienti vegetali che presentano capacità protettive nei confronti dei capillari retinici, ma affiché essi possano contribuire al
mantenimento dell’integrità capillare, è necessario che possano garantire una serie di proprietà quali.
1. Contrastare la formazione degli AGE
2. Migliorare le tolleranza al glucosio
3. Neutralizzare lo stress ossidativo tramite inibizione dei radicali liberi dell’ossigeno (ROS)
4. Inter venire riducendo i fenomeni infiammatori.
L’Acido Oleanolico (OA), agisce inibendo le tre fasi della glicazione avanzata, che portano alla formazione dei prodotti finali, gli AGE.
La Quercetina (Quercefit®), riduce l’assorbimento intestinale del glucosio ed incrementa l’assorbimento del glucosio nei muscoli scheletrici, contribuendo in tal modo al controllo della glicemia.
I beta-glucani contenuti in Betavia™ Complete, polisaccaridi derivati da una particolare microalga, l’Euglena gracilis, presentano proprietà antiossidanti, immunomodulanti ed antitumorali.
Una caratteristica dei beta-glucani è quella di stimolare i meccanismi di difesa, principalmente l'attivazione dei granulociti, monociti, macrofagi e cellule killer naturali.
Al tempo stesso, come catene polimeriche di glucosio, i beta-glucani alimentano e supportano la crescita di Lactobacillus e Bifidobacteria nell'intestino, i batteri probiotici che costituiscono la flora intestinale dell’organismo, agendo sull’asse intestino-retina: una nuova prospettiva nella prevenzione e nel trattamento della retinopatia diabetica.
Gli estratti della Boswellia serrata contengono gli Acidi Boswellici, che posseggono significative proprietà antinfiammatorie.
ERREDI costituisce un valido contributo nel prevenire i fenomeni microemorragici della retina nella retinopatia diabetica non proliferante.
1. Huafang Ding et al; The inhibition of oleanolic acid on protein non-enzymatic glycation. LWT - Food Science and Technology 125 (2020) 109253
2. Priya Mijgar and Uday Deokate. Antidiabetic Potential of Quercetin. DOI: http://dx.doi. org/10.5772/intechopen.1003171.
3. Anna Ciecierska et al; NUTRACEUTICAL FUNCTIONS OF BETA-GLUCANS Rocz Panstw Zakl Hig 2019;70(4):315-324. https://doi.org/10.32394/rpzh.2019.0082
4. M.Z. Siddiqui. Boswellia Serrata, A Potential Antiinflammatory Agent: An Overview. Indian Journal of Pharmaceutical Sciences May-June 2011

Il sistema completo per la gestione della miopia nei bambini












Scopri perche` e` importante controllare gli occhi sin dai primi anni di vita!
lui è Pigrocchio
Puoi chiedere 50 copie gratuite da mettere a disposizione dei tuoi pazienti nella sala d'attesa


Richiedi gli opuscoli a info@fgeditore.it

Le lenti Essilor®
Stellest® rallentano

Le Lenti Stellest® sono la soluzione visiva di Essilor® progettata per contrastare la miopia dei tuoi bambini. Rallentano in media del 67%(1) la progressione della miopia rispetto alle lenti monofocali, se indossate 12 ore al giorno