АНТИБИОТИЦИ И АНТИБИОТИЧНА РЕЗИСТЕНТНОСТ

СТР. 04
АЛТЕРНАТИВНИ НАЧИНИ ЗА ОТКАЗ ОТ ТЮТЮНОПУШЕНЕ
СТР. 32
СРАВНЕНИЕ МЕЖДУ РОБОТИЗИРАНА И ЛАПАРОСКОПСКА ГАСТРЕКТОМИЯ
СТР. 46
СПЕЦИАЛИЗИРАНО ИЗДАНИЕ ЗА ЛЕКАРИ
БРОЙ 108 / 01.2023
Д-р Калин Лисички, д-р Веселина Кендерова:
ОСТРИ РЕСПИРАТОРНИ ИНФЕКЦИИ В ДЕТСКА ВЪЗРАСТ
WWW.MEDMAG.BG БРОЙ 108| 01.2023
ИНФЕКЦИИ И УНГ ПУЛМОЛОГИЯ ХИРУРГИЯ

Изпълнителен директор Главен редактор Отговорен редактор
Редакционна колегия
редакционен
екип
Кристиан Лечев
Проф. д-р Георги Христов
Нели Христова 0894 39 99 50
Проф. д-р Анастас Баталов
Проф. д-р Ваня Юрукова
Проф. д-р Диана Попова
Проф. д-р Диляна Вичева
Проф. д-р Димитър Масларов
Проф. д-р Иван Стайков
Проф. д-р Лъчезар Трайков
Проф. д-р Мери Ганчева
Проф. д-р Милена Станева
Проф. д-р Пенка Илиева
Проф. д-р Петър Петров
Проф. д-р Соня Марина
Проф. д-р Цветомир Димитров
Проф. д-р Цеца Дойчинова
Доц д-р Асен Куцаров
Доц. д-р Аспарух Николов
Доц д-р Борис Тилов
Доц. д-р Валентин Вълчев
Доц д-р Гриша Матеев
Доц. д-р Десислава Тодорова
Доц д-р Желязко Арабаджиев
Реклама
Разпространение
Предпечат и дизайн
Коректор Фотограф Печат
Доц. д-р Иван Цинликов
Доц д-р Ирена Велчева
Доц. д-р Любомир Дурмишев
Доц д-р Мария Атанасова
Доц. д-р Петко Карагьозов
Доц д-р Пламен Павлов
Доц д-р Стоянка Динева
Доц д-р Тодор Попов
Доц. д-р Цветелина Михайлова
Доц. д-р Христина Видинова
Доц. д-р Цветелина Тотомирова
Д-р Александър Алексиев
Д-р Александър Носиков
Д-р Анелия Гоцева
Д-р Борислав Дангъров
Д-р Диана Димитрова
Д-р Екатерина Куртева
Д-р Иво Димитров
Д-р Ина Генева
Д-р Силвия Скелина
Петя Дулева adv@medmag bg
0894 399 948
Ивомир Коларов
Даниела Петрова
Ива Лалова
Мартин Минев IFO DESIGN
Изисквания за авторите, желаещи да публикуват
в сп. MEDICAl Magazine

1. Оригиналните авторски статии да са оформени по следния начин: под заглавието се изписват имената на автора
или авторския колектив с инициали за първо име и пълно -
то фамилно име, с пореден брой цифри Статиите да имат обем до 8 страници, включващи таблиците и илюстрациите, литературните източници и резюметата.
2. Обзорите трябва да имат обем до 8 страници и литературни източници до 20 заглавия
3. Казуистика - клинични случаи трябва да имат обем до
4 страници, без резюме, литерат урни източници до 10 заглавия
4. Резюметата да съдържат текст на български език - до 200-250 думи и до 6 ключови думи, подредени по азбучен ред
5. Онагледеният материал - таблици, фигури и диаграми да
се упоменава в скоби, непосредствено след параграфа, за
който се отнася. Снимковият материал трябва да се представи в оригинал, не по-голям от формат А4 или като файлове с разширение. tif или. jpg, с не по-малка разделителна
способност от 150 dpi
Списанието не носи отговорност за автентичността на онагледения материал.
6. В края на статията могат да се изказват благодарности
към съвета, разгледал и подпомогнал оформянето на статията, към научния ръководител, сътрудници, лаборатории и др
7. Книгописът се дава на отделна страница
8. След книгописа се посочва адресът за кореспонденция
- на български език Той трябва да включва пълния пощ ен-
ски адрес и по възможност телефон за контакт на отговорния автор
Редакционната колегия си запазва правото: да публикува само материали, които счита за подходящи да публикува мнения, становища и въпроси към публикуваните материали
Материалите се рецензират от членовете на редколегията и Редакционния съвет, а при необходимост и от поканени рецензенти
БРОЙ 108
ЯНУАРИ 2023
ISSN: 1314-9709
Адрес на редакцията : София 1407, п. к.177, телефон: 02) 868 82 95
Списание Medical Magazine е запазена марка на фирма „Ел Креатив“ ООД. Никаква част от това издание не може да бъде възпроизвеждана и/или публикувана без изричното писмено съгласие на издателя.
e-mail:
Списанието се обработва в БД „Българска медицинска литература "
Мненията и изявленията, изложени в материалите, принадлежат на авторите на съответните публикации и не са задължително споделяни от редакционния екип и издателите на списанието. Редакцията на списанието не се обвързва с рекламираните в него продукти, както и не дава гаранция за достоверността на информацията, изложена в съответните реклами, като не носи отговорност по предявени
Всички материали се изпращат на адрес: office@medmag.bg или
сп Medical Magazine, 1164 София , ул „Плачковица“ 11
www.medmag bg
повод
„Ел Креатив” ООД е собственост на Кристиан Лечев и Петя Лечева. ПУБЛИКУВАНЕ ИНФЕКЦИИ И УНГ ПУЛМОЛОГИЯ ХИРУРГИЯ Д-р Калин Лисички, д-р Веселина Кендерова: ОСТРИ РЕСПИРАТОРНИ ИНФЕКЦИИ В ДЕТСКА ВЪЗРАСТ
по този
искания.
СЪДЪРЖАНИЕ
04 АНТИБИОТИЦИ И АНТИБИОТИЧНА РЕЗИСТЕНТНОСТ Разговор с доц. Цветан Велинов
08 ОСТРИ РЕСПИРАТОРНИ ИНФЕКЦИИ В ДЕТСКА ВЪЗРАСТ К. Лисички, В. Кендерова
14 КЛЮЧОВИ ФАКТИ И ТЕНДЕНЦИИ В ПРОФИЛАКТИКАТА НА ГРИПНАТА ИНФЕКЦИЯ М. Атанасова
18 ИНФЕКЦИИ НА ГОРНИТЕ ДИХАТЕЛНИ ПЪТИЩА В ДЕТСКА ВЪЗРАСТ П. Масларски
22 ОСТРИ РЕСПИРАТОРНИ ЗАБОЛЯВАНИЯ И ВИРУСНИ ИНФЕКЦИИ – УСЛОЖНЕНИЯ И ПРЕВЕНЦИЯ
И. Георгиева, С. Ангелова, С. Волева, И. Трифонова, Н. Корсун
ПУЛМОЛОГИЯ
28 ПНЕВМОНИИ, ПРИДОБИТИ В ОБЩЕСТВОТО – СЪВРЕМЕННИ РЕШЕНИЯ В КЛИНИЧНАТА ПРАКТИКА П. Павлов
32 АЛТЕРНАТИВНИ НАЧИНИ ЗА ОТКАЗ ОТ ТЮТЮНОПУШЕНЕ Е. Стаменова
36 БЕЛОДРОБНАТА ТУБЕРКУЛОЗА ПО ВРЕМЕ НА ПАНДЕМИЯТА ОТ COVID-19 С. Испир, Д. Митева ХИРУРГИЯ
40 ХОЛАНГИОГРАФИЯ В ХОДА НА ЛАПАРОСКОПСКА ХОЛЕЦИСТЕКТОМИЯ Г. Костов
44 ИНСУФИЦИЕНЦИЯ НА АНАСТОМОЗАТА СЛЕД НИСКА ПРЕДНА РЕЗЕКЦИЯ Г. Костов
46 СРАВНЕНИЕ МЕЖДУ РОБОТИЗИРАНА И ЛАПАРОСКОПСКА ГАСТРЕКТОМИЯ Г. Костов
50 КОРЕМНА ТРАВМА Й. Ценовски, А. Червеняков
56 ПЕРФОРАЦИЯ НА СТОМАШНА И ДУОДЕНАЛНА ЯЗВА Й. Ценовски
2 І Medical Magazine | януари 2023 СЪДЪРЖАНИЕ
ИНФЕКЦИИ И УНГ






Антибиотици и антибиотична
резистентност
Разговор с доц. Цветан Велинов
СМДЛ "ВЕЛИНОВ
ДИАГНОСТИКА" ЕООД е лечебно заведение за извънболнична помощ, което предлага съвременни и ефективни решения в областта на медицинската лабораторна диагностика. Лабораторията е създадена и се ръководи от доц. д-р Цветан Велинов, д.м., специалист с 30-годишен опит в диагностично-лабораторната дейност. Модерното и надеждно оборудване се допълва със стандартизирани и верифицирани в съответствие с най-добрите международни практики технологични процеси, което позволява да се гарантира точност на резултатите и високо ниво на безопасност за пациентите и медицинския персонал. За удобство на пациентите лабораторията предлага ONLINE консултация с доц. д-р Цветан Велинов за разчитане на резултати от проведено изследване, поставяне на диагноза и назначаване на адекватно и ефективно лечение. Лабораторията предлага широк спектър лабораторни изследвания, които може да разгледате на сайта на лабораторията www.velinovlab.bg
Доц. Велинов, да поговорим за антибиотиците – какво представляват, какво лекуват и какво не лекуват, и
защо е важно да се приемат само при необходимост?
Думата антибиотик (от старогръцки „срещу“ „живот“) е използвана за пръв път от Селман Ваксман, откривателя на стрептомицина. Днес това понятие е добило гражданственост
за средства, които убиват или спи-
рат растежа на бактериите, и имен-
но затова се използват за лечение на
бактериални инфекции. Антибиоти-
ците не действат на вирусите и е гру-
ба грешка на медицинското изкуство
да се използват за лечение на вирус-
ни инфекции. Наред с безспорната
полза, която имаме от тях, провере -
на през годините, употребата на ан-
тибиотици води и до развитието на
резистентност. Това е биологичен фе -
номен, при който бактериите продъл-
жават развитието си в присъствието на антибиотик, който е в концентра-
ции, по-високи от терапевтичните, т.е. антибиотиците са основният мутагенен фактор за резистентността. Освен това, антибиотиците действат и на нормалната ни флора, микробиома ни, като убиват чувствителните там бактерии и селектират само тези, които притежават резистентни гени. Възможността бактериите да си предават тази информация, имам предвид резистентните гени, създава огромния ни проблем с разпространението на антибиотичната резистентност.
Защо хората трябва да се тревожат за антибиотичната резистентност? Антибиотичната или микробна резистентност, двете понятия са синоними, ни поставя пред проблема да не можем да лекуваме болести, които довчера са били лечими. Тези пациенти, които са инфектирани с резистентни бактерии, се нуждаят от по-дълги антибиотични курсове, много често при тях се предписват
комбинации от антибиотици, удължава се болничният престой и много често те се инвалидизират. Този антибиотичен натиск, както споменах и по-горе, е основният фактор за развитието на резистентност. Друг много неприятен ефект от резистентността е леталният изход при голяма част от пациентите, особено тези в имунен дефицит.
Скорошно проучване, публикувано в The Lancet, изчисли, че 1,27 милиона смъртни случая се дължат на инфекции, причинени от резистентни бактерии. Смятате ли, че настоящите действия са достатъчни за справяне с проблем от такъв мащаб? Това е огромен проблем и държавите с развита медицинска и социална система от години алармират за него. Колкото и да ми е неприятно, трябва да кажа, че в България този проблем е силно неглижиран. От години отделни институции и лека -
4 І Medical Magazine | януари 2023
ИНФЕКЦИИ И УНГ
„Лабораторните изследвания са изключително важни преди стартирането на антибиотичното лечение, защото ни дават възможност да проведем правилно терапевтичния курс“
ри алармираме за проблема, но е като глас в пустиня. Тук сме много далеч от мащабните
кампании и ангажираността на много специалисти от различни сфери, лекари, фармацевти, държавни служители, ветеринари, които наблюдаваме в останалите страни от ЕС.
Данните, които цитираме, са наистина стряс -
кащи и това са данни от държави, в които от години се гледа сериозно на този проблем.
Така че, отговорът ми на този въпрос е - Не.
Действията са категорично недостатъчни.
Кои според Вас са най-големите препятствия
за преодоляване на микробната резистент-
ност?
На първо място това е неправилната употреба
на антибиотици, свързана с грешно поставе -
на диагноза. Практика е в нашата страна, ди-
агнозите да се поставят основно по клинич-
ни белези, но трябва веднага да подчертая, че през последните години се наблюдава промяна в патоморфозата на инфекциозните заболявания. Това се дължи както на фактори от околната среда, така и на медицинската намеса и употребата на различни лекарствени средства, антибиотици, ваксини, хранителни добавки и пр. Започнахме да диагностицира-
ме все повече „нови“ патогенни микроорганизми. Казвам в кавички, защото напредъкът в диагностичните методи ни позволи да открием тези патогени, които много често са с нетипична чувствителност към антибиотици. Примерът с COVID-19 е много показателен в това отношение. Когато няма поставена етиологич-
на диагноза и се стартира емпирична терапия, тя най-често е с широко-спектърен антибиотик или с комбинация от няколко антибиотика, при неуспех до втори-трети ден се изписва нов антибиотик. Този антибиотичен натиск е водеща причина да се генерира резистентност, която след това бактериите лесно предават помежду си, използвайки различни генетични механизми. Именно поради тези причини, лабораторните изследвания са изключително важни, вземането на проби за микробиологични анализи преди стартирането на антибиотичното лечение ни дава възможност да проведем правилно терапевтичния курс.
Споменахте за пандемията от COVID-19, как се отрази тя на микробната резистентност?
По време на епидемията бяха взети много строги мерки за ограничаване разпространението на вируса и тези мерки до голяма степен пречат на разпространението и на резистентните микроорганизми. Надеждата ни
тогава беше, че покрай тези мерки и поради факта, че вирусни инфекции не се лекуват с антибиотици, ще имаме задържане, а може би и спад на резистентността. В световен мащаб това се наблюдава в отделни сектори. Като консумация на антибиотици всички страни от ЕС регистрираха такъв спад, 18% за 2020 г. Тъжното е, че България е единствената страна от ЕС, в която не само няма спад на антибиотичната консумация, но бележим близо 20% ръст. Клиничната несигурност, породена от липсата на ефективна диагностика, практикуването на телефонна медицина и липсата на пряк контакт с пациента, доведоха до изписването на антибиотици за всеки случай, много често и в неподходящи комбинации. Това естествено се отрази и като ръст на резистентноста в страната ни.
Търсят ли се микробиологичните изследвания преди изписване на антибиотици и защо те са важни?
Много рядко. Това до голяма степен се дължи на факта, че редица микробиологични лаборатории съобщават резултатите след 3 дни, а понякога и по-късно. Това е време, през което клиницистът е назначил емпиричната терапия, а когато тя не върви, дори я е сменил. Това забавяне на резултатите, през последните години се стремим да компенсираме с подобряване на диагностичните методи. Въвеждането на редица генетични анализи, използването на имуно-хроматографските, т.нар. бързи тестове, използването на мас-спектрометричния анализ ни позволява да съкратим диагностиката до няколко часа, максимум два дни, а когато говорим за бързите тестове - и до минути. В нашата лаборатория използваме всички тези възможности за ускорена диагностика и резултатите много рядко се забавят повече от 48 часа. Микробиологичната диагноза има няколко основни предимства. На първо място, тя е етиологичната диагноза на инфекцията. При стартирана емпирична терапия и предварително взета проба за микробиология, когато излязат резултатите, терапията може да се коригира с точния антибиотик, т.нар. де-ескалираща терапия, препоръчана от всички специалисти в областта на инфекциозната патология. И не на последно място, от микробиологичните резултати се натрупват данните за водещите микробни причинители при отделните заболявания и нивата им на резистентност в дадения географски регион, което е база за правилната емпирична терапия.
[www.medmag.bg ] 5
Как диагностичните новости могат
да намалят употребата на антиби -
отици, без това да се отрази върху
здравето на пациента?
Имуно-хроматографските тестове, с
които разполагаме в лабораторията,
са изключително полезни в тази на-
сока, а именно защото са бързи. Ре -
зултатите излизат в рамките на 20-
30 минути, време, за което може да
се отложи предписването на антиби-
отик и да се предприеме лечение на
база резултата от теста. Такива тесто -
ве има за различни вируси, като рес-
пираторни, които са популярни през
есенно-зимния сезон, така и за чрев-
ни, характерни за лятото. Има те -
стове и за най-честите бактериал-
ни причинители, като Streptococcus
pneumoniae, Streptococcus pyogenes, Helicobacter pylori, Clostridium difficile, Campylobacter и др. Гамата се увели-
чава постоянно. Генетичните тесто -
ве също са от голяма полза, особено
за бавно растящите и трудно или не -
култивируеми микроорганизми. При
тях диагнозата се поставя в рамките
на 2 до 4 часа, време, през което също
може да се изчака и след това да се
приложи прицелна терапия, често без
антибиотик, разбира се, когато се ка-
сае за вирусна инфекция.
Каква е ролята на генетичните тестове за диагностиката и лечението на инфекциозните болести?
Без да преувеличавам, огромна. Това е най-бързо развиващото се направление в диагностичната дейност.
Благодарение на тези тестове, ние днес знаем за съществуването на ми -
кроорганизми, за които преди само
подозирахме, че могат да участват
в инфекциозния процес. Благодаре -
ние на генетичните тестове се разкри
и огромното разнообразие от ми -
кроорганизми, които ни населяват
т.нар. микробиом, без който не мо -
жем да съществуваме. Ползите ни от
тази симбиоза са безспорни. Но да
се върна на генетичните тестове за
диагностика на инфекциозни патогени. Разнообразието и тук е много
голямо. Повечето от рутинно използваните са на базата на полимеразно-верижната реакция в реално вре -
ме. Използването на мултиплексни PCR тестове ни дава възможност в една проба да докажем повече от 20 микробни вида и да направим количествена оценка на тези микроби. Разполагаме с такива тестове както за респираторната система, където в рамките на 2-3 часа можем да кажем кой е причинителят на респираторната инфекция и как най-правилно да се стартира терапията, така и с тестове за уро-гениталната система. Количественият анализ, например за човешкият папилома вирус, ни дава възможност да проследим броя вирусни копия и съответно напредъка на болестта или ефекта от проведеното лечение. Изключително полезни са и за откриването на гени на резистентността. Тази информация
също ни насочва при избора на антибиотично лечение. Ползите са много.
Повлиява ли се микробиомът ни от антибиотиците?
Микробиомът ни играе важна роля в нашия живот. Една от задачите му е да ни пази, като пречи да се колонизираме с патогенни микроорганизми. Участва в метаболизма, където без определени микробни видове, ние не можем да усвоим фибрите в храната, които са важни за производството на късо-верижни мастни киселини, като бутириновата и пропионовата, произвеждат редица витамини и пр. Ролята му в метаболизма ни е сравнима, даже по-голяма от тази на черния дроб. Като добавим и ролята му в изграждането на имунната система, разбираме защо микробиомът ни е толкова важен за самото ни съществуване. Всяка употреба на антибиотик влияе върху алфа-разнообразието от микроорганизми и зависи от спектъра на действие на антибиотика. Колкото по-широкоспектърен е той, толкова повече полезни бактерии ще унищожи. Това е и причината да говорим за прицелна и де-ескалираща терапия, защото възстановяването на микробиома е трудна и продължителна задача, а за да можем
да приложим гореспоменатите тера -
пии ни е нужен резултат от микробиологичния анализ.
Бихте ли ни казали какво е лечение, определено за конкретен пациент, т. нар. персонализирана медицина?
Често се шегуваме с колегите, че ние, микробиолозите, първи сме въвели персонализираната медицина и това не е далеч от истината. Микробиологичният резултат ни дава информация за причинителя на инфекцията при конкретния пациент и кои антибиотици са подходящи за него - това е персонализиран подход. Човечеството е на прага на технологична революция, ĸoятo щe пpeдизвиĸa фyндaмeнтaлнa пpoмянa в нaчинa ни нa живoт, и ние тpябвa дa ce пoдгoтвим зa нeя. На преден план излиза задълбоченият индивидуализиран подход към пациента и желанието за предотвратяване на заболяването. Този подход може значително да подобри качеството и ефективността на медицинската помощ. Така на мястото на патерналистната медицина (еднолично вземане на решение, в името на "доброто", както го разбира лекарят) идва медицината на взаимодействието между пациента и лекаря (партисипативна медицина).
Благодарение на мащабните открития в областта на генетиката и клетъчната биология, днес медицината разполага с тестове, които ни дават информация за гените, за микробиома и междинните продукти на метаболизма (метаболом). Така се разкрива информация за здравето на пациента, вероятните рискове, предиспозицията и „слабостите” на тялото пред лекаря. По този начин стана възможно да се "прогнозират" патологии и заболявания, които с голяма вероятност ще възникнат при пациента в бъдеще. Съвременната медицина се движи в посока ранна диагностика - колкото по-рано е диагностицирана болестта, толкова по-лесно и евтино е да се справим с нея.
Този подход сме възприели и ние във "Велинов Диагностика", разполагаме с голям набор от подобни тестове и необходимия капацитет да ги приложим и да дадем съответната консултация.
6 І Medical Magazine | януари 2023
ИНФЕКЦИИ И УНГ

К. Лисички, В. Кендерова
АСК УМБАЛ Токуда, София, Клиника по педиатрия
Остри респираторни инфекции в детска възраст
Острите респираторни инфекции (ОРИ) са основна причина за заболеваемост и смъртност в световен мащаб. Всяка година около 1.3 милиона деца под 5 години умират от тях[1]. Ежегодно се регистрират над
Съобразно анатомичната локали -
зация се класифицират като:
• Инфекции на горните дихател -
ни пътища – засягането е от ноздрите до гласните струни на ларинкса, включително параназалните синуси и средното ухо (ринит, тонзилофарингит, епиглотит, ларингит, отит, синуит).
• Инфекции на долните дихателни пътища - обхващат продължението на дихателните пътища от трахеята и бронхите до бронхиолите и алвеолите (трахеит, бронхит, бронхиолит, пневмония)[23] .
В етиологичен план острите респи -
раторни инфекции се причиняват
най-често от вирусни и/или бакте -
риални агенти и по-рядко от някои
видове гъбички, паразити, протозои. Най-често срещаните вируси, предизикващи респираторни симптоми са грипните (тип А и В), респираторно синцитиален вирус, парагрип, риновируси, ентеровируси, аденовируси, коронавируси и др. От бактериалните патоге -
ни, причиняващи ИГДП, най-често се установяват Streptococcus pneumoniae, Streptococcus pyogenes, Haemophilus influenzae, Moraxella catarrhalis, Mycoplasma pneumoniae и други [3]
Имунният отговор към инфекциоз -
ни агенти включва следните елементи:
• Вродена имунна защита – кожно-лигавична бариера, неутрофилни фагоцити, NK-клетки (естествени клетки убийци), интерферон тип I, лизозим, стомашна киселина. Характерно за този тип имунна защите е, че тя не е антиген-специфична.
• Адаптивен имунен отговор –участват различни класове и
субкласове на Т- и В-лимфоцитните популации и редица цитокини, чрез които се осъществява антиген-специфичен имунен отговор.
Както вроденият, така и адаптив -
ният имунен отговор играят клю -
чова роля в контролирането на
вирусните инфекции, като те са неразривно свързани [4]
Цитокините са ключови участници в осъществяването и модулирането на имунните и възпалителните реакции в човешкия организъм [5]
Те могат да бъдат както антиинфламаторни, така и проинфламаторни за макроорганизма [24] . Така например, при инфекции от респираторно синцитиален вирус се наблюдава увеличаване на възпалителните IL-1, IL-6 и намаляване на противовъзпалителните IL10 и IFN-γ [5] . При грипни инфекции участват IL-6, TNF-α, IL-10, IL-8, IP10 (интерферон γ-индуциран протеин), IFN-γ, които варират в зависимост от циркулиращите грипни щамове - например е установено, че щамовете H5N1 индуцират високи серумни нива на IP-10 и монокин, индуцирани от интерферон-γ, както и по-високи нива на TNF-α и IFN-β, в сравнение с щамовете H3N2 или H1N1. Съобщава се за значителна корелация между тежестта на грипното заболяване и
8 І Medical Magazine | януари 2023
ИНФЕКЦИИ И УНГ
12 милиона хоспитализации на деца под 5 години, поради ОРИ[2]. Те са много често срещан проблем сред бебета, деца и възрастни хора и представляват около 9% от всички консултации при общопрактикуващия лекар[3].
високите нива на IL-6, IL-10 и IL-15 и за раз -
лика от тях, IL-17 е по-нисък при пациен -
ти в по-тежко състояние [6] . При инфекция с HRV, част от цитокините, които произвеж -
дат епителните клетки на дихателните пъ -
тища са IL-1, IL-6, IL-8, TNF-α, IL-10, IL-11[16]
Възможностите за терапевтично повлияване на острите респираторни инфекции
при децата зависят основно от етиологичния причинител. В тази връзка при бактериално провокирани ОРИ на първо място в терапевтичния план стоят антибактериал -
ните медикаменти. Не така стои въпросът
при вирус-индуцираните респиратони инфекции. Понастоящем медицината разпо -
лага с твърде ограничен набор антивирус -
ни медикаменти. В тази връзка се търсят
нови подходи за терапевтично повлиява -
не на вирусните инфекции на горните и до -
лни дихателни пътища. През последните
години се появяват все повече проучвания, свързани с използването на пробиотиците
при различни здравословни състояния. Установено е, че пробиотичните щамове по -
влияват имунния отговор по следния на -
чин:
• Имуномодулация на локалния имунитет
(чрез поддържане целостта на чревната
стена).
• Повлияване на вродения имунен отго -
вор.
▪ Повишават фагоцитния капацитет на левкоцитите в периферната кръв (полиморфонуклеари и моноцити).
▪ Подобряват фагоцитната активност. Гранулоцитите показват повишена фагоцитна клетъчна функция, в сравнение с моноцитите.
▪ Значително повишават експресията на рецептори (CR1, CR3, FccRI и FcaR), участващи във фагоцитозата, фагоцитния индекс, оксидативния взрив.
▪ Увеличават активността и процентното съдържание на NK-клетки в периферна кръв.
• Влияние върху адаптивния имунен отговор.
▪ Значително по-високи специфични IgG, IgA и IgM.
▪ Увеличават синтеза на цитокини (напр. IL-1, IL-2, IL-6, IL-10, IL-12, IL-18, TNF-α, интерферон-α)[7]
Познанията за влиянието на чревната микробиота за здравето се развиват бързо и броят на публикуваните научни статии за ползите от нейните модификации нараства експоненциално. Ето защо не е изненадващо, че медицинската общност и широката общественост искат базирани на доказателства отговори за това кога и как да се промени чревната микробиота, за да се подобри здравето като цяло.
Способността за промяна на състава и метаболитните свойства на нашата чревна микробиота е добре позната от десетилетия, а именно чрез използването на пробиотици, пребиотици и комбинацията между тях, известни като синбиотици. Валидната към момента дефиниция за пробиотици е тази от 2014 г., на СЗО и Международната научна асоциация за пробиотици и пребиотици, а именно, че „пробиотиците са живи микроорганизми, които, когато се прилагат в адекватни количества, предоставят ползи за здравето на гостоприемника“ [8] .
Напоследък се дискутират много факти относно оста черва – бял дроб. Дихателната система има собствена микробиота и възпалението на белите дробове може да доведе до чревна дисбиоза, която от своя страна може да засегне имунитета на белите дробовe [26] . „Пропускащите” черва позволяват транслокация на бактериални продукти и антигени в кръвообращението, което води до изостряне на заболяването [9]
В резултат на редица проучвания е установено, че Lactobacillus rhamnosus GG:
• Eфективно прилепва към лигавицата на дебелото черво и оказва противовъзпалително действие както ex vivo, така и in vivo [10] .
• Предотвратява индуцирана от цитокини апоптоза в чревните епителни клетки, in vitro [11]
• Намалява TNF-индуцираното активиране на NF-kB in vitro, увеличава производството на IL-10, IL-12, IL-18 [12,13] .
• Стимулира производството на интерферон (IFN)-γ [13]
• При концентрации от 10 6 и 10 8 cfu/L, жив
[www.medmag.bg ] 9
LGG инхибирa (p<0.01) TNF-индуцирана IL-8 секреция [14]
• В сравнение с плацебо, LGG значимо намалява продължителността на инфекциите на дихателните пътища (3 рандомизирани контролирани проучвания, n = 1295 деца от 3 месеца до 7 години)[12]
Установено е, че приложението на Lactobacillus rhamnosus GG и
Bifidobacterium lactis Bb-12 намалява тежестта при ИГДП[17] , подобрява качеството на живот на болните [17] . Отчетено е, че Bifidobacterium sp. и Lactobacillus sp. намаляват употребата на антибиотици при бебета и деца [18] . Lactobacillus rhamnosus GG се съдържа в хранителната добавка Линекс Комплекс , като формулата е обогатена с витамини B1, B2, B6 и цинк. Може да се прилага на деца над 6-год. възраст [21]
Част от комплексната симптоматична терапия при острите респираторни инфекции е приложението на локални антисептични средства в устната кухина. Хлорхексидинът е едно от тях. Той представлява катийон-активен антисептичен агент и притежава бактерициден ефект спрямо грам-позитивни и грам-негативни бактерии, има антимикотичен и противовирусен ефект срещу някои гъбички и вируси. Хлорхексидин се свързва с отрицателно заредените повърхности на оралната мукоза, зъбите и интраоралната плака, като това спомага за дълготрайната наличност на хлорхексидин в устната кухина. Около 30% от хлорхексидин се запазва след изплакване на устната кухина, като след това постепенно се излъчва в слюнката [22] . Провеждани са проучвания за ефекта от приложението на хлорхексидин при пациенти със SARS CoV-2 инфекция. Установено е, че при пациенти, инфектирани със SARS CoV2 след 4 дни локална употреба на хлорхексидин в устната кухина настъпва елиминиране на вируса от орофаринкса в 62.1% от случаите, в сравнение с 5.5% от пациентите в контролната група, а при комбинирано приложение на орална вода и орофарингеален спрей вирусната ерадикация е 86%. В тази връзка може да се направи изводът, че хлорхексидинът е лесно приложимо допълнение към симптоматична -
та терапия при COVID-19 и може да играе роля за намаляване на разпространение -
то на вируса [19] Ангал е комбиниран препарат, съдържащ хлорхексидин и лидокаин. Предлага се под формата на таблетки (с вкус на мед, лимон, ментол и ягода) и орофарингеален спрей (лимон и ментол).
Прилага се при деца над 6-год. възраст за локално лечение на възпалено гърло, фарингит, гингивит, стоматит, афти. Лидокаинът води до бързо облекчение на болката.
Дозировката е между 3 и 5 таблетки днев -
но при пациенти над 6-годишна възраст и
6-10 таблетки дневно при пациенти над 12
години. Ангал спрей се прилага от 2 до 3
впръсквания 3-5 пъти дневно при пациенти над 6-годишна възраст и 3 до 5 впръсквания 6-10 пъти дневно при пациенти над 12 години [22] .
Образуването на мукус е първата линия на защита на епитела в нашето тяло срещу вредни патогени. Неговите защитни свойства се дължат както на съчетание от протеини като имуноглобулини, различни гликопротеини и някои антимикробни ензими като лизозим, така и на кръстосаното свързване на полимерни гел-образуващи муцини, които като цяло определят биофизичните свойства на мукуса. Този слой осъществява защитата срещу бактериалните агенти чрез инхибиране на бактериалния растеж, а също така работи и като физическа бариера срещу респираторни дразнители и предотвратява загубата на течности.
При някои болестни състояния като ХОББ и астма хроничното възпаление на дихателните пътища води до хиперсекреция на слуз. Прекомерното производство на мукус води до свръхнатоварване на механизмите на мукоцилиарния клирънс, като по този начин води до прекомерното му натрупване. Това води до образуване на слузни тапи, които допълнително намаляват клирънса. Дихателните пътища реагират чрез отделяне на излишък от възпалителни медиатори в опит да изчистят обструкцията. За съжаление, това само влошава състоянието, тъй като вискозитетът на мукуса се увеличава, което води до допълнително намаляване на клирънса и задълбочаване на възпалението [20]
10 І Medical Magazine | януари 2023
ИНФЕКЦИИ И УНГ
В тези случаи е уместна употребата на муколитици. Те се разделят
в две основни групи: класически
муколитици и пептидни муколитици. Основен представител на класическите муколитици е N-ацетилцистеин. Свободната тиолова
група в неговата структура хидролизира дисулфидните връзки, свързани с цистеиновите остатъци, които са съставна част на муцина (основния белтък в бронхиалната слуз). Тази реакция нарушава 3-D
рамката на слузта чрез редуциране на S-S връзката до S-H (сулфхидрилна) връзка. Освен този муколитичен ефект, N-ацетилцистеин притежава противовъзпалителни
и антиоксидантни свойства чрез
намаляване на свободните кислородни радикали и възпалителни
медиатори на мястото на бронхиалното възпаление. По този начин, с тройното си действие, ацетилцистеин спомага за намаляване продължителността на заболяването на пациентите, страдащи от бронхит и белодробни инфекции [20,25] . Друг много важен ефект е намаляването на бактериалните биофилми [15] , което увеличава ефективността на антибиотичната терапия [25] . Представител на ацетилцистеин е АЦЦ сироп. Той съдържа 20 мг ацетилцистеин в 1 мл. Подходящ е за приложение при деца над 2-год. възраст (200-300 мг дневно), и възрастни и юноши над 14 год., като при тях дневната доза е 400-600 мг дневно [15] .
В
може да се отбеле -
жи, че терапевтичната стратегия при вирус-провокираните респираторни инфекции включва комплексно симптоматично лечение, включващо антипиретици, назални деконгестанти, локални противовъзпалителни средства за приложение в устната кухина, противокашлични медикаменти. Антибиотиците намират приложение само, ако се насложи вторична бактериална суперинфекция или при първоначално бактериално остро респираторно заболяване. Провеждането на все повече проучвания, доказващи ефекта от приложението на пробиотични щамове като имуномодулатори, дават все по-голямо основание за тяхната употреба и благоприятен ефект като добавка към терапията на респираторни инфекции.
1. Organization WH, UNICEF. Ending preventable child deaths from pneumonia and diarrhoea by 2025: the integrated global action plan for pneumonia and diarrhoea (GAPPD). 2013.
2. Nair H, Simoes EA, Rudan I, Gessner BD, Azziz-Baumgartner E, Zhang JS, et al. Global and regional burden of hospital admissions for severe acute lower respiratory infections in young children in 2010: a systematic analysis. Lancet (London, England). 2013;381 (9875):1380–90. 10.1016/S0140-6736(12)61901-1
3. Strauss, M.; Mičetić-Turk, D.; Pogačar, M.Š.; Fijan, S. Probiotics for the Prevention of Acute Respiratory-Tract Infections in Older People: Systematic Review. Healthcare 2021, 9, 690. https:// doi.org/10.3390/healthcare9060690
4. Whitton JL, Slifka MK, Liu F, Nussbaum AK, Whitmire JK. The regulation and maturation of antiviral immune responses. Adv Virus Res. 2004;63:181-238. doi: 10.1016/S0065-
3527(04)63003-X. PMID: 15530562; PMCID: PMC7125551.
5. Bohmwald K, Gálvez NMS, CanedoMarroquín G, Pizarro-Ortega MS, Andrade-Parra C, Gómez-Santander F and Kalergis AM (2019) Contribution of Cytokines to Tissue Damage During Human Respiratory Syncytial Virus Infection. Front. Immunol. 10:452. doi: 10.3389/fimmu.2019.00452
6. Cohen L, Fiore-Gartland A, Randolph AG, Panoskaltsis-Mortari A, Wong S-S, Ralston J, Wood T, Seeds R, Huang QS, Webby RJ, Thomas PG and Hertz T (2019)
A Modular Cytokine Analysis Method Reveals Novel Associations With Clinical Phenotypes and Identifies Sets of Cosignaling Cytokines Across Influenza Natural Infection Cohorts and Healthy Controls. Front. Immunol. 10:1338.
7. Hao Q, Dong BR, Wu T. Probiotics for preventing acute upper respiratory tract infections. Cochrane Database Syst Rev. 2015 Feb 3; (2):CD006895. doi: 10.1002/14651858.CD006895.
pub3. Update in: Cochrane Database Syst Rev. 2022 Aug 24;8: CD006895. PMID: 25927096.
8. Hojsak, I., Fabiano, V., Pop, T.L., Goulet, O., Zuccotti, G.V., Çokuğraş, F.C., Pettoello-Mantovani, M. and Kolaček, S. (2018), Guidance on the use of probiotics in clinical practice in children with selected clinical conditions and in specific vulnerable groups. Acta Paediatr, 107: 927-937. https://doi. org/10.1111/apa.14270
9. Hussain et al. Frontiers in Immunology |October 2021 | Volume 12
| Article 765965
10. Pagnini C. et al., World J Gastroenterol 2018 November 7; 24(41): 4652-4662
11. Fang Yan‡ and D. Brent Polk, J Biol Chem. 2002 December 27_277(52) 50959–50965 3.
12. Capurso L, J Clin Gastroenterol, Volume 53, Supp. 1, March 2019
13. Segers and Lebeer Microbial Cell Factories 2014, 13
14. Zhang L et al., 0022-3166/05
$8.00 © 2005 American Society for Nutritional Sciences.
15. Кратка характеристика на АЦЦ сироп
16. Kimura et al. Frontiers in microbiology September 2013 | Volume4 | Article 276
17. Smith TJ, Rigassio-Radler D, Denmark R, Haley T, Touger-Decker R. Effect of Lactobacillus rhamnosus LGG(r) and Bifidobacterium animalis ssp. lactis bb-12(r) on health-related quality of life in college students affected by upper respiratory infections. Br J Nutr. 2013;109:1999–2007.
18. King S, Tancredi D, LenoirWijnkoop I, Gould K, Vann H, Connors G. Does probiotic consumption reduce antibiotic utilization for common acute infections? A systematic review and meta-analysis. Eur J Public Health. 2019;29:494–499.
19. Huang YH, Huang JT. Use of chlorhexidine to eradicate
oropharyngeal SARS ‐ CoV‐2 in COVID ‐19 patients. J Med Virol. 2021;1‐ 4. https:// doi.org/10.1002/jmv.26954
20. Gupta R, Wadhwa R. Mucolytic Medications. [Updated 2022 Jul 4]. In: StatPearls [Internet]. Treasure Island (FL): StatPearls Publishing; 2022 Jan-. Available from: https://www.ncbi.nlm. nih.gov/books/NBK559163/
21. Листовка за потребителя Линекс Комплекс
22. Кратка характеристика на продуктите Ангал
23. Eric A. Acute Respiratory Infections in Children - Disease Control Priorities in Developing Countries - NCBI Bookshelf
24. Md. Abul Kalam Azad , Manobendro Sarker and DanWan, BioMed Research International, Volume 2018, Article ID 8063647
25. Chalumeau M, et al. Cochrane Database of Systematic Reviews 2013, Issue 5. Art. No.: CD003124.
26. De Oliviera. Front. Immunol. 2021 12_635471
[www.medmag.bg ] 11
заключение
ИЗПОЛЗВАНА ЛИТЕРАТУРА:
Материалът е подготвен с подкрепата на „Сандоз България“ КЧТ с адрес: София 1407, бул. Никола Вапцаров 55, сграда 4, ет. 4, тел.: 02/9704747, факс: 02/9704757.
BG2211229100/22-Nov-2022








М. Атанасова КАИЛ, УМБАЛ „Св. Анна“ - София
Ключови факти и тенденции
в
профилактиката на
грипната инфекция
Ключови думи: грип, епидемиологична характеристика, ваксинопрофилактика.
Грипът е остра вирусна инфекция, която се разпространява лесно от човек на човек във всяка възрастова група и която може да причини сериозни усложнения при определени рискови групи. В допълнение към сезонните епидемии грипната пандемия може да възникне, когато възникне нов подтип на грипния вирус или когато грипният вирус на животните започне да се разпространява сред хората. Надеждна профилактика на заболяването се постига чрез прилагането на ваксини.
Грипът е една от най-контагиозните респиратрни инфекции. Причинява се от грипни
вируси, чиято изменчивост променя непрекъснато епидемиологичната картина. При на -
деждно наблюдение на сезонния
грип степента на риска може да бъде
предвиден[6]. Грипните вируси могат
да причинят от леко до тежко забо -
ляване и да доведат до хоспитализа -
ция или фатален край. Възрастните
хора, малките деца и хората с опре -
делени здравословни проблеми са
изложени на по-висок риск от услож-
нения. След откриването на вирусите
са разработени убити и живи вакси -
ни, които през годините се усъвър -
шенстват. В съвременните условия
широко приложение в имунизацион -
ната практика заемат убитите вакси -
ни. През втората половина на ХХ век са приложени и противовирусни медикаменти - М2-инхибитори и невраминидазни (NA) инхибитори[1,2]
ЕТИОЛОГИЯ
Грипният вирус (Influenza virus) принадлежи към род Influenzavirus на сем. Orthomyxoviridae. Антигенни
особености разпределят грипните вируси на три типа - А, В и С. Грипният вирус се характеризира с висока изменчивост. С антигенен шифт се отбелязват драстични промени в структурата на повърхностните антигени, което води до появата на нов подтип, водещ до пандемия. Го -
лемите промени са резултат от пренареждане на гени, осъществяващо се между два различни щама вируси, вероятно при условия на смесена инфекция (например инфектиране в един организъм с човешки и птичи вирус). Така могат да възникнат по-вирулентен щам, който е по-смъртоносен, и се разпространява по-бързо. Към него населението няма имунитет. Антигенен дрифт са по-слаби промени, напр. точкови мутации, които водят до появата на епидемични щамове, с което се обяснява възникването на грипни епидемии в интервал от 1-2 години. Механизмът на антигенния дрифт се свързва с постепенно натрупване на промени в един или от петте идентифицирани основни антигенни участъци на молекулата на НA. Сравняването на хемаглутининовите секвенции
на грипните вируси, изолирани последните години, показват определени различия за хемаглутинина (НА) между А, В и С вируси. При хората циркулират една или относително малки линии на А вирус, а натрупването на точкови мутации на НА линеино до формиране на нов щам, който замества предходния циркулиращ щам. Тези данни са по характерни за щам Н3, докато при С вирус циркулират множество линии. Грипен вирус тип В е с относително малко циркулиращи линии на гена НA. Сходни са механизмите и при NА. Циркулацията на нови антигенни варианти от даден подтип води до създаване на имунитет и невъзприемчивост на населението. Едновременно при грипна епидемия могат да циркулират грипни вируси А и В.
ЕПИДЕМИОЛОГИЯ Грипните вируси са свързани с повишена заболяемост и смъртност. Неблагоприятният изход на заболяването с неговите усложнения е в пряка зависимост и с циркулиращия щам за различните грипни епидемии. През ХХ век са описани няколко пандемии
14 І Medical Magazine | януари 2023
ИНФЕКЦИИ И УНГ
- „Испански грип” А (Н1N1) - 1918-1919 г. - починали 40 млн.; „Азиатски грип” А (Н2N2)1957 г. – починали 2 млн.; „Хонгконгски грип”
А (Н3N2) - 1968 г. - починали 1 милион; 1972, 1973, 1974, 1975, 1975, 1976, 1977, 1978, 1982
г. се характеризират с пандемично разпрос -
транение на А (Н3N2). През 1997 г. е регистри -
ран първият случай на заразен човек с пти -
чи грипен вирус А (Н5N1)[1]. През април 2009
г. нов грипен щам еволюира, като комбини -
ция от гени на човека, свине и птици. Пър -
воначално е наречен „свински грип“ и също
така е известен като грип A (H1N1. Появява
се първоначално в Мексико, САЩ и някол -
ко други страни. Фатално завършили - около
500 000. Последните наблюдения позволя -
ват да се коментират две теории за резерво -
ар на вируса. Според антропонозната теория
човешката популация е единствен резервоар
на грипните вируси. Промените в антигенна -
та им структура се формират под въздействи -
ето на противогрипния имунитет на населе -
нието. Според зоонозната теория се приема, че излезлите от циркулация сред хората гри -
пни вируси успяват да преживяват в различ -
ни видове животни. При определени усло -
вия някои от тях попадат отново сред хората.
Тук обаче се сформират нови вируси, посредством рекомбинация между човешките и жи -
вотинските вируси. През 2015 г. има съобще -
ния за заразяване с птичи грип тип A(H7N9). В
съвременните условия масовото разпростра -
нение на грипните вируси се улеснява от въздушния и сухопътен транспорт[4,10]
Грипните вируси се разпространяват главно
от малки капчици, създадени, когато хората
с грип кашлят, кихат или говорят. Тези капчици могат да се „приземят“ в устата или носа
на хората, които са наблизо. По-рядко човек
може да получи грип, като докосне повърхност или предмет, който има грипен вирус
върху него, и след това докосва собствената си уста, нос или евентуално очите си. Хората с грип са най-заразни през първите 3-4 дни след началото на заболяването си, като малките деца и хората с отслабена имунна систе -
ма биха могли да заразяват по-дълго време.
СИМПТОМИ НА ГРИП Инфектираните с грипен вирус съобщават за внезапно настъпила треска, кашлица, възпалено гърло, запушен нос, болки в мускулите, главоболие, умора. Повръщане и диария се среща по-често при малките деца. Според някои проучвания грип А протича по-ле -
ко, а грипният вирус тип В води по-често до усложнения от страна на дихателна, сърдечно-съдова и нервна система. Тежката първична грипна пневмония протича със силно изразена токсикоза, диспнея, цианоза, тахикардия. Аускултаторната находка е по-често негативна. Рентгеновото изследване установява двустранни белодробни изменения, характерни за респираторен дистрес синдром, но без консолидиране. Състоянието на болните не се повлиява от антибиотичната терапия. Може да доведе до фатален изход както при деца, така и при възрастни. Вторичната бактериална пневмония често се предизвиква от пневмококи, стафилококи и други бактерии[7,9]. За нея се мисли при повишаване на температурата след около 10 дни след началото на грипна инфекция. Налице са аускултаторна находка в белите дробове и рентгенови изменения. Антибиотичното лечение повлиява благоприятно общото състояние и локалните промени в белодробния паренхим. Възможна е и смесена пневмония. Усложненията са чести при болни с хронични белодробни, сърдечни и метаболитни заболявания, при имуносупресирани лица. Немалко от тези групи болни показват резистентност към антивирусните медикаменти. В детска възраст като усложнение често се среща грипозния круп. Протича с дрезгава, лаеща кашлица, затруднено дишане, неспокойствие. По-често се причинява от парагрипен вирус тип 1 или 3 или респираторно-синцитиален вирус[1]
На второ място по честота са усложненията на сърдечно-съдова система: миокардити, перикардити, флебити, тромбози, с които се обясняват фатално завършилите случаи на грип. Усложненията на ЦНС са свързани с развитие на грипен енцефалит при деца и възрастни. Заболяването протича тежко с промени в съзнанието, вариращи от сопор до кома, гърчове и неблагоприятен изход. По-рядко се описват миозити, миелити, синдром на Рей, токсичен шок синдром, свързан с наслоена инфекция от токсин произвеждащи бактерии[1]
Оздравителният процес се свързва с развитието на клетъчно-медииран имунитет. Освен активирането на СД4 Т лимфоцити, важна роля имат и цитотоксичните СД8 Т лимфоцити. Те разпознават НA в мембраните на заразените клетки и ги убиват, с което преустановяват вирусната репликация на
[www.medmag.bg ] 15
етап сглобяване на вирионите. Оз -
дравителният процес често предше -
ства появата на антитела в органи -
зма. Инфекцията с грипните вируси
води до развитие на локален (синтез
на секреторен IgA) и системен хумо -
рален както към НA и NA, така и към
структурните протеини. Антитела -
та се появяват към края на първа -
та седмица, достигат максимума си
около 2-3 месец, след което титрите
на серумните им нива бавно нама -
ляват. Те осигуряват типово специ -
фичната защита, като блокират из -
вън клетъчното разпространение на
вирусите чрез инхибиране на адхе -
зията му към специфичните клетъч -
ни рецептори. Те могат да предпа -
зят от заразяване с вируси от същия
НA подтип, видоизменен в резултат
на антигенен дрифт. НA антителата,
които присъстват в ниски титри са
насочени към хетероложни щамо -
ве от същия подтип и са в състояние
само да модифицират тежестта на
заболяването, но не и да го предотвратят. Специфичните NA антитела
нямат вирусонеутрализиращ ефект, но високите им серумни нива намаляват интензитета на излъчване на вируса[2,3]
Терапевтичният подход при грип включва прилагане на антивирусни препарати. Те водят до съкращаване на продължителността на заболяването и намаляване на риска от ус -
ложнения, особено при децата под 2-годишна възраст, възрастни над 65 години, хора с хронични заболявания, като астма, хронична белодробна болест, сърдечна недостатъчност, диабет и затлъстяване, както и болни от СПИН. Проучванията показват, че антивирусните препарати са високо ефективни, когато са приложени още в самото начало на заболяването. Но започването им по-късно може да бъде полезно, особено ако болният е изложен на висок риск от сериозни грипни усложнения или инфекцията протича тежко. Препоръчаните за лечение на грип антивирусни препарати са: Inosine acedoben dimepranol (търговско наименование Isoprinosine®), Oseltamivir (наличен под търговското наименование Tamiflu®), Zanamivir (търговско наименование Relenza®).
ПРОФИЛАКТИКА
Грипът има сезонен характер - преобладава през зимните месеци. Ваксинирането на възприемчиви лица и рискови контингенти следва да се прилага преди епидемичния период. За Северното полукълбо грипният сезон е от ноември до април. Достъпните на пазара ваксини се инжектират мускулно, подкожно или интрадермално еднократно в делтоидния мускул. Месеците октомври и началото на ноември са най-подходящи за поставяне на противогрипна
ваксина по две причини: организмът има достатъчно време да изгради имунитет и хората са все още здрави, което е задължително условие за ваксинация. Продължителността на имунитета е около една година, като най-силен е през първите шест месеца от поставяне на ваксината.
Ежегодните имунизации увеличават колективния имунитет на населението и намаляват риска от епидемично разпространение на инфекцията.
ЗАКЛЮЧЕНИЕ
Епидемиите от грип и пандемиите причиняват значителна заболяемост и смъртност, разходи за здравни услуги и икономически загуби. Световната здравна организация (СЗО), Европейският център за профилактика и контрол на заболяванията, Центровете за контрол и превенция на заболяванията в САЩ и центровете за сътрудничество на СЗО имат за цел да намалят заболяемостта и смъртността, свързани с грип, чрез: засилване на вирусологичното и епидемиологичното наблюдение на лекия и тежък грип; използване на данни от наблюдението за оценка на тежестта на грипа, за да се даде приоритет на националните програми за ваксинация срещу грип; и поддържане и засилване на дейностите по подготовка за пандемия на национално равнище.
1. Илиев Б., Г. Митов, М. Радев. Инфектология, АИ „Проф. М. Дринов’, 2001, 189-198.
2. Илиева П., Грип. Инфекциозни болести и епидемиология. Медицина и физкултура. София, 2013, 217-221.
3. Belser J, D. Wadford, C. Pappas et al. Pathogenesis of Pandemic Influenza A
(H1N1) and Triple-Reassortant Swine Influenza A (H1) Viruses in Mice. J. Virol. May 2010 vol. 84 no. 9 4194-4203
4. Browne A, St-Onge Ahmad S, Beck CR, et al. The roles of transportation and transportation hubs in the propagation of influenza and coronaviruses: a systematic review. J Travel Med. 2016 Jan 18;23(1).
5. Chung JR, Flannery B, Thompson MG, et al. Seasonal Effectiveness of Live Attenuated and Inactivated Influenza Vaccine. Pediatrics. 2016 Jan 5. pii: peds.2015-3279.
6. Fox SJ, Miller JC, Meyers LA. Seasonality in risk of pandemic influenza emergence. PLoS Comput Biol. 2017 Oct
19;13(10):e1005749.
7. Morens, D. M., Taubenberger, J. K. & Fauci, A. S. Predominant role of bacterial pneumonia as a cause of death in pandemic influenza: implications for pandemic influenza preparedness. J. Infect. Dis. 198, 962–970 (2008).
8. Skowronski DM, Chambers C, Gustafson
R et al. Avian Influenza A(H7N9) Virus Infection in 2 Travelers Returning from China to Canada, January 2015(1). Emerg Infect Dis. 2016 Jan;22(1):71-4.
9. http://www.cdc.gov/flu/.
11. Zambon M. Epidemiology and pathogenesis of influenza. J. Antimicrob. Chemother. 1999; 44, suppl 2 3-9.
16 І Medical Magazine | януари 2023
ИЗПОЛЗВАНА ЛИТЕРАТУРА:
ИНФЕКЦИИ И УНГ
сила сила




















































имуномодулираща
допълнителна информация: Eвофарма ЕООД 1618 София, ул. „Пирински проход“ 24, Tел.: (02) 962 12 00, Факс: (02) 868 39 68 info@ewopharma.bg, www.ewopharma.bg Лекарствен продукт по лекарско предписание. За възрастни и деца на 1 год. KХП 51290/06.08.2020; 56264/08.10.2021; 51288/06.08.2020 ИАЛ 41545/25.09.2019 Информация, относно това как Евофарма събира, обработва и съхранява лични данни може да получите тук: https://www.ewopharma.bg/politika-za-poveritelnost/ Двойната
срещу респираторните
ISO_Add-HCPs-BG-Ver.2_24.01.2022
антивирусна За
инфекции
П. Масларски, педиатър
Аджибадем Сити Клиник - София
Инфекции на горните
дихателни
пътища в
детска възраст
Инфекциите на горните дихателни пътища обединяват група заболявания, които се характеризират с инфекциозно възпаление на лигавицата на носа, фаринкса, ларинкса и свързаните с тях околоносни кухини и средното ухо. При малките деца инфекцията рядко се локализира само в един орган и се налага използването на диагнози като ринофарингит, тонзилофарингит. В англоезичната медицинска литература се използва терминът common cold, който заменя диагнозата остра вирусна инфекция, засягащ лигавицата на носа и фаринкса. Този термин не е възприет у нас и заболяванията се означават в зависимост от болестните промени в различните отдели на горните дихателни пътища.
ЕПИДЕМИОЛОГИЯ
Касае се за най-честите заболява -
ния, от които страдат децата. Засег-
ната е обикновено възрастта между 1 и 6 години. Кърмачетата страдат относително пo-рядко поради пасивния имунитет, получен от майката.
След 6-ата година заболяванията постепенно намаляват поради усъвършенстването на локалната защита на горните дихателни пътища.
Статистическите данни показват, че при децата от ранна и предучилищна
възраст 63% от инфекциите са на гор -
ните дихателни пътища. Тези заболявания зачестяват през есенно-зим -
но-пролетния период и неправилно
се означават като простудни заболя -
вания, тъй като няма доказателства
за етиологичната роля на простуда -
та. Заболяемостта е по-висока сред
децата, отглеждани в колективи, където възможността за инфектиране
нараства многократно.
ЕТИОЛОГИЯ Основен етиологичен фактор при инфекциите на горните дихателни пътища са вирусите. По-малка е ролята на бактериите и микоплазмите. Бактериите могат да предизвикват първични заболявания, но по-често усложняват вторично вирусните инфекции. Проучванията показват, че в ранна и предучилищна възраст вирусите причиняват над 90% от инфекциите на горните дихателни пътища. В училищна възраст ролята на бактериите нараства и те биват изолирани в 20-25% от болните. Бактериите са основен етиологичен агент на усложненията на инфекциите на горните дихателни пътища: синузит, отит, шиен лимфаденит.
Въведените нови методи за идентифициране на вирусите - имуно-флуоресценция и ELISA, дават възможност
да се изясни значението на различ -
ните вируси за възникване на инфекциите на горните дихателни пътища. Бактериологичното изследване на секрети от горните дихателни пътища е рутинна практика, но резултатите се получават късно - след 48-72 часа, а това намалява тяхната практическа стойност. Експресните методики за доказване на бактерии, и по-специално на хемолитичния стрептокок, са с висока специфичност, но за съжаление имат ниска чувствителност.
ПАТОГЕНЕЗА Инфекциозните причинители попадат в горните дихателни пътища по аерогенен път. След като вирусите преодоляват местната защита, проникват в клетките на мукоциларния епител и ги увреждат или унищожават. Лигавицата е хиперемирана, оточна, жлезите й обилно секретират. Това обуславя клиничните изяви и създава условия за бактериална ин -
18 І Medical Magazine | януари 2023
ИНФЕКЦИИ И УНГ
вазия, която е в основата на усложненията.
КЛИНИЧНА КАРТИНА
Общите клинични прояви на инфекциите на горните дихателни пътища се изразяват в:
• Повишената телесна температура
е почти постоянен симптом, чес -
то предхождащ локалните прояви.
Повишаването й у децата на въз -
раст между 6 и 48 месеца може
да предизвика фебрилни гърчо -
ве, които да се съпровождат с по -
вишен вътречерепен натиск и менинго-радикулярно дразнене (менингизъм).
• Безапетитието съпътства фебрилния период на заболяването, но
често продължава и по време на реконвалесценцията.
• Повръщането е често още в на -
чалото на заболяването и може да бъде проява на менингизъм,
израз на токсично и инфекциозно дразнене на окончанията на
п. vagus във фаринкса, засилва се при хранене.
• Диарията е честа проява на инфек-
циите на горните дихателни пъти -
ща, особено когато са причинява -
ни от вируси.
• Коремната болка може да бъде
основно оплакване у деца от ран -
на детска възраст. Често е резул -
тат на мезентериален лимфаденит, причинен от аденовируси.
• Неспокойствието и нарушението
на съня се дължат на затрудненото дишане поради блокада на носните ходове и/или хипертрофия на тонзилите, както и при обструкция на ларинкса.
Малките деца, дори и тези от предучилищна възраст, рядко се оплакват от болки в гърлото.
РИНИТ И РИНОФАРИНГИТ Ринитът се причинява най-често от риновируси. Инкубационният период е къс - 1-2 дни. Основният симптом е затрудненото дишане през носа, което принуждава детето да диша през устата с отметната назад глава. Носната секреция в началото е оскъд-
на и детето сумти. По-късно тя става по-обилна, серозна и предизвиква кихане. Постепенно секрецията придобива слузен или слузно-гноен характер. Температурата е повишена. При обективното изследване се открива зачервена оточна лигавица на носа и обилен секрет в носните ходове. Тази клинична картина се среща при no-големите деца. У по-малките деца инфекцията се разпространява към назо- и орофаринкса и има основание да се постави диагнозата ринофарингит.
Причинителите на ринофарингита са също вируси, но тук наред с риновирусите етиологична роля играят и парагрипните вируси, респираторно-синцитиалният вирус и по-рядко адено- и ентеровирусите. Изброените вирусни причинители са представени в над 100 щама.
У no-големите деца поради набъбване на лигавицата и обилния секрет е налице назална обструкция. Добавят се общо неразположение безапетитие, главоболие, сухота в гърлото, кихане и рядка кашлица. Кашлицата
се дължи на аспирация или стичане на секрет от фаринкса към ларинкса, поради което тя се засилва, когато детето ляга. Температурата обикновено е повишена.
Обикновено се установяват хиперемия на носната лигавица, обилен секрет в носните ходове, понякогаfoetor ех ore. Фарингеалната стена е също зачервена и се вижда стичащ се от назофаринкса секрет. Лимфните фоликули във фарингеалната стена се увеличават и проминират над лигавицата. Могат да се опипат субмандибуларни и шийни лимфни възли. Рутинните лабораторни изследвания обикновено не показват отклонения.
У кърмачетата и малки деца инфекциозният синдром е силно изявен. Наред с горепосочените симптоми е налице и висока температура - над 38°С, която може да предизвиква фебрилни гърчове. Децата са
неспокойни, сънят е нарушен, храненето - затруднено. Повръщане и пo-рядко диария съпровождат проявите от страна на горните дихателни пътища.
Диагнозата се поставя въз основа на клиничната картина и данните за епидемиологичен контакт. С помощта на имунофлуоресцентна техника може да се идентифицира причинителят. В диференциалнодиагностичен аспект трябва да се имат предвид алергичните ринити. С ринофарингит започват обривните заразни болести – mоrbili, rubeolla, varicella.
Лечението с антибиотици предвид вирусната етиология на ринита и ринофарингита не е ефективно и не намалява опасността от бактериална суперинфекция. Патогенетичното лечение с антнхистаминови препарати е също неефективно. Големите дози витамин С не облекчават субективните оплаквания. Още по-малко основание има локалното приложение на витамин С под формата на капки в носа - практика, възприета от някои наши лекари.
Лечението е насочено преди всичко към намаляване на обструкцията
на носните ходове, която е причинена от обилната секреция и набъбналата лигавица. Извършва се внимателно механично почистване на носа и накапване на физиологичен серум. За отбъбване на носната лигавица се използва 2% разтвор на Ephetomin (Ephedrin) или 0,25% на Vasoton (Sympatol). Добре действат и препаратите на колоидално сребро Collargol (Protargol), които като 2% разтвор имат и антисептични свойства.
Многобройните препарати, които съдържат по-активни и по-продължително действащи деконгестанти, трябва да се избягват при малки деца, тъй като причиняват възбуда или депресия, а и други, по-тежки прояви на интоксикация. Капките, съдържащи етерични масла, и мехле -
[www.medmag.bg ] 19
мите за мазане на носните ходове
крият опасност от аспирация и раз -
витие на пневмония. Носните капки
трябва да се прилагат 10-15 минути
преди хранене, като се препоръчва
двукратно накапване - първите 1-2
капки отбъбват лигавицата на ноз -
дрите, след 5 минути - нови 1-2 кап -
ки, които проникват по-дълбоко в
носните ходове.
При повишена температура, която
безпокои детето, се използват антипиретици.
Затрудненото хранене на децата,
особено на малките кърмачета, изис -
ква търпение и настойчивост. Пред-
лагат се течности под форма на чай, плодови сокове. Диетата е млеч -
но-плодова, като храната се дава
по-често, на малки порции. Режимът е домашен.
Прогнозата на ринофарингита е добра. Децата оздравяват за 5-7 дни, но носната секреция може да бъде и по-продължителна. Прогнозата се
помрачава от честите рецидиви при
наличието на неблагоприятни екзо-
и ендогенни фактори - при т.нар.
често боледуващо дете. Прогнозата
зависи и от възникване на усложне -
ния: sinusitis, otitis, шиен лимфаде -
нит и десцендиране на инфекция -
та към ларинкса, бронхите и белия
дроб.
Гърлен секрет – има важно значение
за поставяне на диагнозата при чести инфекции на ГДП, изолиране на контактните деца при заразните инфекциозни заболявания (скарлатина), определяне на терапията и необходимостта от включване на антибиотична и/или друга симптоматична терапия.
Антибиограма - задължителна е при бактериалните инфекции за определяне на антибиотичната терапия и
продължителност на лечението.
СРЕДЕН ОТИТ В практиката едно от най-често диагностицираните усложнения на ин -
фекциите на ГДП е средният отит. Най-често диагностициран е във възрастта от 6-36 месеца. На 3 години 60% от всички деца са преболедували 1 път от среден отит, а 30%три пъти.
ЕТИОЛОГИЯ Пневмококи - 30%, Хемофилус инфлуенце - 20%, Стрептококи гр. А10%, Мораксела катаралис - 10%, по-рядко микоплазма и вируси.
РИСКОВИ ФАКТОРИ
Недоносени деца или деца с ниско тегло при раждането, алергична предиспозиция, компрометиран имунитет, краниофациални аномалии, нервно-мускулни заболявания, деца с по-къса и широка Евстахиева тръба, деца с хронични инфекции на ГДП, неблагоприятни фактори на околната среда и условията на живот, есеннозимен сезон.
ПАТОФИЗИОЛОГИЯ Острият среден отит обикновено възниква като усложнение на вирусна инфекция на ГДП, нарушаваща цилиарната активност и намаляваща проходимостта на Евстахиевата тръба. Това води до серозен излив в средното ухо, вторична бактериална инфекция, задебеляване на тъпанчевата мембрана и възпаление с катарален, хеморагичен, гноен или некротичен механизъм. В кърмаческата възраст и при малките деца Евстахиевата тръба е със склонност към дисфункция, поради непълноценен хрущял и слаб m. tensor veli palatine.
КЛИНИЧНА КАРТИНА Температура, плач и възбуда, болка, отказ от храна, гастроинтестинални симптоми.
УСЛОЖНЕНИЯ
Излив в средното ухо и персистираща глухота с последващо смущение в нервно-психическото развитие, говор и обучение. Мастоидит, менингит, тромбози, перфорация на мембраната, обикновено в задния й долно-задния й квадрант.
ДИАГНОЗА
Гърлените и носните секрети не корелират с етиологията на отита. Отоскопия - основен диагностичен метод. Допълнителни сведения могат да бъдат получени чрез тимпанометрията, пневматичната отоскопия.
Клиничната диагноза може да бъде потвърдена с кръвна картина и парацентеза.
ЛЕЧЕНИЕ
Насочено е към повлияване на болката - с локални медикаменти.
Дрениране на Евстахиевата тръбакапки за нос, при деца под 6 месеца дори само при съмнение за среден отит се започва незабавно антибиотично лечение.
При деца над 6 м. антибио тично лечение се започва само при сигурна диагноза и тежко протичане на заболяването. При неповлияване
на симптомите до 72 часа се започва антибиотично лечение. Като първа позиция при оралната антибиотична терапия са Пеницилиновите, Цефалоспорини – втора генерация и Макролиди.
Важна роля играят противовъзпалителните, обезболяващите и антипиретични медикаменти - от групата на ибупрофен, нурофен и др.
ПРОФИЛАКТИКА
При рисковите деца се препоръчва, освен общите профилактични мерки като закаляване, хранене, оптимизация на средата, приложение на ваксини за Str. Pneumonia, поради огромното етиологично значение на този микроорганизъм. Адекватна е имунопрофилактиката за Haemophilus influence.
20 І Medical Magazine | януари 2023
ИНФЕКЦИИ И УНГ


BG-DEF-1222-001 Informacije za uporabnike Витамин D и Цинкът играят роля за функционирането на имунната система. Хранителната добавка не е заместител на балансираното и разнообразно хранене НОВО ВКУСНИ ДЪВЧАЩИ ТАБЛЕТКИ ЗА ИМУНИТЕТА на Вашите деца 1, 2, 3 таблетката сдъвчи
И. Георгиева, С. Ангелова д.б., С. Волева, И. Трифонова, Н. Корсун
Национална референтна лаборатория „Грип и
ОРЗ“, Национален център
по заразни и паразитни
болести - София
Остри респираторни заболявания
и
вирусни инфекции – усложнения
и превенция
Респираторните заболявания са най-често срещаните заболявания при човека. Те имат голямо социално-икономическо въздействие, причинявайки милиардни парични загуби като преки разходи за здравните системи и пропуснати икономически ползи поради неоползотворени работни и учебни дни. Подценяването на респираторните инфекции и тяхната диагностика води до ненавременно и некоректно лечение и често до възникване на усложнения. А неправилната употреба на антибиотици е причина за развитието на антибиотично-резистентни бактериални щамове, което представлява все по-сериозен проблем за общественото здраве в Европа и света.
Причинителите на остри
респираторни заболява -
ния (ОРЗ) могат да бъдат
както вирусни, така и бак-
териални или паразит-
ни агенти, като вирусите са отговор -
ни за преобладаващия брой случаи. Множество вируси от различни семейства причиняват ОРЗ, но едни от най-честите патогени на дихателната система са грипните вируси, респираторно-синцитиалният вирус (РСВ) и риновирусите.
В страните с умерен климат, каквато е България, грипните вируси тип А и
В предизвикват ежегодни епидемии
през зимния сезон. Инкубационни -
ят период на заболяването грип е 1-5 дни (средно 2 дни). Началото е остро, дори внезапно с клинични прояви от
страна на дихателните пътища - възпалено гърло, ринорея, назална конгестия, кашлица. При някои пациенти (главно малки деца) се наблюдават гастро-интестинални симптоми (га -
дене, повръщане, диария). Системните прояви включват висока температура, главоболие (предимно в челната и задочна област), миалгия, артралгия, отпадналост. Фебрилитетът продължава 3-5 дни; кашлица и отпадналост се наблюдават няколко седмици. Токсикоинфекциозният синдром при грипа е по-силно изразен, в сравнение с другите ОРЗ. Грипните вируси рядко се асоциират с асимптомни инфекции.
Усложненията на грип включват отит на средното ухо (при деца), синуит, ларинготрахеобронхит (круп), вирусна пневмония, вторична бактериална пневмония, бронхиолит, обостряне на хронични белодробни и сърдечни заболявания, миозит (вкл. рабдомиолиза), неврологични усложнения (фебрилни гърчове, енцефалопатия, енцефалит, миоперикардит, смърт). Рискови групи за тежко протичащ грип и усложнения са: деца <2 год.; възрастни ≥65 год.; лица със съпро -
вождащи хронични заболявания: бронхо-белодробни, сърдечно-съдови, бъбречни, чернодробни, неврологични, метаболитни (диабет), хемоглобинопатии, имунен дефицит и др.; бременни; лица с висока степен на затлъстяване (BMI≥40).
За лечение и профилактика на грип в Европа и България има лицензирани 4 препарата от два класа: инхибитори на йонните канали М2 (Аmantadin и Rimantadin) и невраминидазни инхибитори - oseltamivir (Tamiflu), zanamivir (Relenza). Адамантаните (инхибиторите на М2) са ефективни само срещу грипни вируси тип А, докато невраминидазните инхибитори проявяват активност спрямо тип А и В вируси. Препаратите са най-ефективни, когато се прилагат в първите 48 часа от началото на заболяването. Широко разпространената резистентност на циркулиращи през последните години грипни вируси спрямо инхибиторите на йонни -
22 І Medical Magazine | януари 2023
ИНФЕКЦИИ
И УНГ
те канали М2 обаче, прави неефективно тяхното използване за лечение и профилактика.
По отношение на невраминидазните инхибитори за сега са доказани сравнително малък брой резистентни вируси.
Основен инструмент за превенция и контрол на грипа са ваксините. Световната здравна организация препоръчва ежегодна имунизация на деца на възраст 6-59 мес., възрастни ≥65 год., лица с определени хронични заболявания, бременни, здравни работници и др. Ефективността на противогрипните ваксини е 60-80% и зависи от антигенното родство между ваксиналните и епидемичните щамове, възрастта и здравния статус на ваксинираните лица. Една от най-важните ползи на молекулярната диагностика е именно събиране на детайлна информация за циркулиращите вирусни щамове, което е в основата на подбора на компонентите на противогрипната ваксина.
РСВ е повсеместно разпространен, силно заразен респираторен патоген. Човекът е единствен естествен гостоприемник за този вирус.
Инфектирането с РСВ става по въздушно-капков път, чрез вдишването на големи капчици респираторни секрети, отделяни от болния при кихане, кашляне или говор. Тези секрети могат да контаминират повърхностите на околните предмети. Друг възможен начин на заразяване е контактният път, чрез докосването на носа, очите или устата с мръсни ръце (Hall, 2007). РСВ причинява респираторни инфекции при лица от всички възрасти, но тежестта на заболяванията е най-голяма при деца в кърмаческа и ранна възраст - под 5 год. Първичната инфекция с РСВ е обикновено симптоматична, като 25-40% от първичните инфекции протичат със засягане на долните дихателни пътища с развитие на трахеобронхит, бронхиолит и пневмония. При около 10% от тези заболявания се налага болнично лечение (Nair и съавт., 2010). Рискови групи за тежко протичащи инфекции с РСВ са недоносените деца, малките деца (възраст под 2 г.), деца с хронични белодробни заболявания, особено бронхопулмонална дисплазия; вродени сърдечни заболявания; имунен дефицит, както и лица в напреднала възраст (Resch, 2012).
[www.medmag.bg ] 23
У нас и в Европа, в страните с умерен климат, РСВ причинява епидемични взривове със сезонен пик през студените месеци - есента, зимата и ранната пролет (месеците от ноември до април), но не и през лятото. Взривовете съвпадат с епидемичното разпространение на грипните вируси. РСВ е водещ причинител на вътреболнични респираторни инфекции (French и съавт., 2016). Инкубационният период на инфекцията с РСВ е 2-8 дни (средно около 4 дни), продължителността на заболяването – 8-15 дни. Типични клинични прояви са невисок фебрилитет, ринорея, кашлица, учестено дишане (тахипнея), цианоза, хрипове, сепсис-подобни прояви или апнотични епизоди. В резултат на първичната инфекция с РСВ не малък процент от инфектираните деца в кърмаческа или ранна възраст развиват бронхиолит или пневмония, а поне 0,5-2% от случаите изискват хоспитализация. Макар и сравнително нисък в индустриалните страни, съществува риск от развитие на вторична бактериална пневмония при деца, хоспитализирани с инфекция с РСВ. Екстрапулмонарните прояви са редки – описани са случаи на фебрилни гърчове, енцефалит, миокар -

дит (Eisenhut, 2006). Абнормалната пулмонарна функция често се наблюдава след бронхит или пневмония, причинени от РСВ. Нещо повече, може да персистира 7-10 години след заболяването, дори до зряла възраст (Sigurs и съавт., 2010; Noble и съавт., 1997). Инфекция с РСВ може да причини екзацербация на астма или ХОББ при деца и възрастни (Kurai и съавт., 2013).

Към момента има само два препарата за борба с заболяванията, причинени от РСВ – паливизумаб за превенция и рибавирин за лечение (Griffiths и съавт., 2017). Рибавирин е синтетичен нуклеозиден аналог с широк спекър на антивирусно действие, лицензиран е за аерозолно приложение за лечение на тежки инфекции с РСВ под търговското име Virazole. Използването на рибавирин обаче няма ясен ефект за редуциране на честотата на хоспитализациите и смъртността.
се прилага ограничено при лица със сериозни рискови фактори (имунокомпрометирани пациенти, деца със сърдечни и белодробни заболявания, водещи до значителни нарушения на хемодинамиката) и не се използва
24 І Medical Magazine | януари 2023
И УНГ
ИНФЕКЦИИ
Той

рутинно при предишно здрави деца
с пневмония или бронхиолит (Ventre
и Randolph, 2004). Към настоящия
момент няма лицензирани ваксини
срещу РСВ.
Възприемчивостта на човека към ри -
новирусна инфекция е висока и зависи от възрастта, имунния статус, температурата на околната среда.
Стресът, недостатъчният сън, охлаждането, дефицитът на витамин D, по -
вишават чувствителността на организма. Неблагоприятни фактори са
тютюневият дим и други замърси -
тели на въздуха. Честотата на риновирусните инфекции е най-голяма в
кърмаческа и ранна детска възраст и намалява пропорционално с напредване на възрастта. Риновирусните
инфекции се срещат през цялата година, но тяхната честотата е най-голяма през ранна есен (септември-октомври) и ранна пролет (март-април).
Те причиняват 50-75% от случаите на „простудна хрема“ и от 1/3 до 1/2
от всички остри респираторни забо -
ИЗПОЛЗВАНА ЛИТЕРАТУРА:
1. Корсун, Н. (2009). Ентеровирусни инфекции. София: Любомъдрие.
2. Hall, C. (2007). The spread of inluenza and other respiratory viruses: complexities and conjectures. Clin Infect Dis(45), 353-359
3. Resch, B. (2012). Burden of respiratory syncytial virus infection in young children. World J Clin Pediatr(1), 8-12.
4. French, C., McKenzie, B., Coope, C., & al, e. (2016). Risk of nosocomial respiratory
лявания (ОРЗ). По време на есенния епидемичен сезон (септември-октомври) те са отговорни за около 90% от случаите на ОРЗ.
Риновирусите предизвикват широк
спектър клинични прояви - от асимптомни инфекции до тежки заболявания на долните дихателни пътища.
Най-често инфекцията протича със засягане на горния отдел на дихателния тракт. Инкубационният период
варира от 1-2 дни до 6 дни. Симптомите започват остро и достигат максимум на 24-48 час. Най-характерни клинични прояви са ринорея с обилни слизесто-воднисти секрети, които по-късно стават мукоидни или пурулентни, назална конгестия и възпалено гърло. Често се наблюдават кихане, инфекция на конюнктивите и склерите със сълзотечение, умерена непродуктивна кашлица, главоболие, тежест в лицето и синусите. По-рядко се съобщава за леко повишена температура, отпадналост, липса на апе -
syncytial virus infection and effectiveness of control measures to prevent transmission events: a systematic review. Influenza and Other Respiratory Viruses(10), 268-290. doi:10.1111/irv.12379.
5. Nair, H., Nokes, J. D., Gessner, B. D., Dherani, M., Madhi, S. A., Singleton, R. J., и др. (2010). Global burden of acute lower respiratory infections due to respiratory syncytial virus in young children: a
тит, общо неразположение, миалгия. Общото състояние е слабо засегнато, токсичните явления са леко изразени. Средната продължителност на заболяването е най-често една седмица, но при 25% от заболелите то продължава 2 седмици и повече. При пушачи кашлицата може да персистира по-дълго.
Към настоящия момент няма лицензирани препарати с антивирусно действие и ваксини срещу риновирусите.
Ранната диагностика на причинителя на дадено респираторно заболяване е от изключителна важност за определяне на правилната стратегия за лечение на пациента. Освен това чрез диагностиката се събират данни за разпространението на различните вирусни патогени. За диагностика на вирусни инфекции на дихателните пътища се използват различни клинични проби: назофарингеални секрети /аспирати; носогърлени секрети/ аспирати/; промивни течности; трахеални аспирати, бронхоалвеоларен лаваж; храчка; при смъртен случай - трупни материали (трахея, бял дроб). Тези проби са подходящи за изолация на вирус или за доказване на вирусни антигени/нуклеинови киселини. Важно е пробите да бъдат събрани в първите 3 дни след началото на симптомите. За серологично изследване се използват двойни серумни проби, взети в острата (до 7-мия ден) и реконвалесцентната фаза на заболяването (след 2-4 седмици). Правилното съхранение и транспортиране на пробите е много важно поради изключителната лабилност на някои от вирусите, като РСВ.
systematic review and meta-analysis. Lancet, 375: 1545–55
6. Eisenhut, M. (2006). Extrapulmonary manifestations of severe respiratory syncytial virus infection – a systematic review. Critical Care(10(4)), R107, doi:10.1186/cc4984.
7. Sigurs, N., Aljassim, F., Kjellman, B., Robinson, P. D., Sigurbergsson, F., Bjarnason, R., и др. (2010). Asthma and allergy patterns over 18
years after severe RSV bronchiolitis in the first year of life. Thorax(65), 1045–52.
8. Noble, V., Murray, M., Webb, M., & al., e. (1997). Respiratory status and allergy nine to 10 years after acute bronchiolitis. Arch Dis Child(76), 315-319.
9. Kurai, D., Saraya, T., Ishii, H., & Takizawa, H. (2013). Virus-induced exacerbations in asthma and COPD. Frontiers in Microbiology, 293(4), doi:10.3389/fmicb.2013.00293.
10. Griffiths, C., Drews, S., & Marchant, D. (2017). Respiratory syncytial virus: infection, detection, and new options for prevention and treatment. Clin Microbiol Rev(30), 277-319
11. Ventre, K., & Randolph, A. (2004). Ribavirin for respiratory syncytial virus infection of the lower respiratory tract in infants and young children. Cochrane Database Syst Rev, CD000181.
26 І Medical Magazine | януари декември20232022
ИНФЕКЦИИ И УНГ

П. Павлов Медицински Университет - Плевен
Пневмонии, придобити в обществото – съвременни
решения в клиничната практика
Ключови думи: Пневмонии, тенденции, поведение.
Пневмонията е едно от най-големите открития на клиничната медицина. Диагнозата и лечението й в днешно време се усложняват от появата на нови, непознати патогени, разширяващата се антибиотична резистентност, увеличаващата се популация на имунокомпрометирани пациенти, модерни диагностични методи и антимикробни средства.
Пневмонията, придобита в обществото (ППО) остава често срещана и досега, определя се като едно от тежките инфекциозни заболявания в западния свят, чиито еволюция и изход варират в широки граници. Отличава се със значима заболяемост и смъртност. Регистрират се средно 5.6 милиона случаи годишно, 1.1 милиона се хоспитализират. Смъртността при лекуваните амбулаторно е 1-5%, според последни проучвания при хоспитализирани достига до 13%, а при тежките пневмонии - до 35%[1]
Повече от 100 микробни агента могат да причинят ППО. Няколко основни фактора, цитиращи се напоследък в популационно базираните проучвания, оказват влияние при откриване на причинителя: възраст, приложение на противогрипна и пневмококова ваксина, антибиотична терапия,
ПУЛМОЛОГИЯ
28 І Medical Magazine | януари 2023
Страна регион β-лактам Макролид Тетрациклин Хинолон β-лактам + Макролид β-лактам + Тетрациклин
ERS/ESCMID + (+) (+) (+) (+)
Франция + (+) + (+) (+) UK + (+) (+)
Германия +
Португалия +
алкохолизъм, имуносупресия, коморбидност, особено малигнени заболявания. Значение имат безспорно и чувствителността на методите за диагностика, както и свойствата на патогенните микроорганизми. Водеща остава ролята на S. pneumoniaе. S. aureus, Legionella
и Gram-отрицателните бактерии от клас Enterobacteriaceae са по-рядко срещани, но
показват прогресивно нарастване на честотата, корелираща с тежестта на пневмониите[2].
В наше проучване при 110 хоспитализира -
ни пациенти с ППО с най-голям относителен
дял са били щамовете от Enterobacteriaceae (42.7%), следвани от S. aureus (19.1%)[3]. H.
influenzaе се среща по-често при лица с подлежаща хронична обструктивна белодробна
болест (ХОББ). Етиологичната роля на вирусите все още не е достатъчно изяснена. Атипични микроорганизми (M. pneumoniae, C. pneumoniae) се описват като водещи всред причинителите на ППО с географски различия в честотата[4].
Антибиотичната резистентност, най-вече при S. pneumoniae, остава важен и нарастващ феномен. Клиничните й изяви все още не са достатъчно проучени. Много от респираторните патогени, особено S. pneumoniae, GroupA streptococcus и S. аureus се променят постоянно в съответствие с променящата се антибиотична резистентност. ППО при метицилин резистентни S. Аureus (MRSA) остава рядко срещана, но се очаква да бъде проблемна за лечение[5]. MRSA – инфекцията, придобита в обществото (CA-MRSA), обикновено се установява при предшестващо здрави лица и се представя с тежка некротизираща пневмония. Инфекцията с резистентните
щамове на ESBL продуциращите щамове на K. pneumoniae е свързана с висока смъртност.
Честотата на респираторните патогени и отчитането на местните нива на антибиотична резистентност би трябвало да се вземат предвид при лечението на ППО. В постоянно обновяващите се насоки за третиране на пациентите с пневмонии са отразени познатите скали на Fine, CURB 65 (Confusion, Urea, Respiratory rate ≥30, Systolic blood pressure <90 mm Hg or Diastolic blood pressure <60 mm Hg) и CRB 65. Техният дизайн включва определяне на нискорискови пациенти, кандидати за амбулаторно лечение и високорисковите по отношение на смъртен изход. Актуализирана клинична информация относно ППО посочва значимостта и на по-малко изследвани рискови фактори за развитието и тежестта й: пасивно тютюнопушене, контакт с деца, с домашни животни, употреба на инхалатори[7]. Съпътсващи болести, употреба на антибиотици също би трябвало да се имат предвид. Нашето проучване показва, че близо половината от изследваните пациенти с ППО са лекувани с антибиотик в предходните три месеца преди хоспитализацията, а 60% са били с коморбидитети[3]
Водещи са били кардиоваскуларните заболявания, следвани от захарен диабет и мозъчно-съдова болест[3]
Опасността от влошаване при високорискови пациенти в горепосочените скали остава недооценена. Във връзка с това все повече данни в литературата напоследък подкрепят ранната и проследяваща оценка на клиничните маркери на дихателна недостатъчност, свързаната със сепсис, органна дисфункция,
Табл. 1
Емпирично антибиотично
лечение на средно тежка
ППО – вариации в Европа + антибиотик на първи
избор; (+) алтернативен избор ERS - European Respiratory Society
ESCMID - European Society of Clinical Microbiology and Infectious Diseases.
[www.medmag.bg ] 29
(+) (+) (+) (+) (+)
(+)
Испания (+) + (+)
(+) (+) (+) (+)
или декомпенсирането на подлежащи коморбидности[1]. В светлината на съвременния подход за индивидуализирана медицина, това предполага и дефиниране на лечеб -
ните цели при всеки отделен паци -
ент с пневмония. Инфламаторните
маркери C-реактивен протеин (CRP), прокалцитонин (PCT) и цитокините
IL-6, TNFα имат допълнителна прог-
ностична стойност относно смърт-
ността и тежестта на пневмонията.
Подходящото антибиотично лечение
и добрата прогноза се асоциират със
снижаване нивата на CRP и PCT след
няколкодневно лечение. Кардио -
васкуларните и свързани със стреса биомаркери – копептин, мидрегионалния проадреномедулин (MR-proADM), мидрегионалния натриуретичен пептид (MR-pro-ANP), кортизол, D-димер, доказват връзката си с хода и изхода при ППО в обсервационни проучвания и се явяват обещаващ инструмент за персонална преценка на риска при ППО[8,9]. Препоръчвани са основно при третиране на хоспитализирани пациенти[10,11]
Антибиотичното лечение на ППО е базирано на медицината на доказателствата и е съобразено с вариаци -
ите на различни фактори. Провеждането на антибактериална терапия е тясно свързана с антибиотичната резистентност, тъй като тя винаги интерферира с ефективността на лечението. Засега няма достатъчно доказателства за приемане на „златен стандарт” в емпиричното антибиотично лечение на пневмониите[12,13].
Основни елементи на емпирична терапия, препоръчани от консенсусните документи в различни страни в Европа, са представени на Табл. 1
Съвременните насоки за третиране на пациенти с ППО са отражение на стремежа към унифициран подход в диагностиката и лечението им. Въпреки че повече от лекарите приемат гайдлайните и ги считат за полезни, приложението им в клиничната практика остава незадоволително[14,15] Клиничното решение за диагнозата, тежестта на пневмонията, мястото на лечението и самото лечение не винаги е лесно. То изисква персонализиран подход, отчитане на много фактори и отговор на важни въпроси – очакван причинител и нива на резистентност, съпъстващи фактори, влияещи върху хода на болестта; емпирична или етиологично насочена терапия; свойства на антибиотиците, отчитане на странични действия, цена на лечението, социален статус на пациента. Всички тези въпроси оказват съществено влияние върху нашия реален клиничен избор при третиране на пациентите с ППО.
1. Kolditz M., EwigS., Ho¨ffkenG. Management-based risk predictionin community-acquired pneumonia byscores and biomarkers. Eur Respir J. 2013; 41(4): 974–984.
2. Woodhead M. Community-acquired pneumonia in Europe: causative pathogens and resistance patterns.Eur Respir J 2002; 20: Suppl. 36, 20s–27s.
3. Глоговска П. Клинично значение на резистентността при инфэекции на
долните сихателни пътища, придобити в обществото. Фармакоикономически анализ. Докт. дис. 2010.
4. DharR. Pneumonia: Review of
Guidelines.JAPI 2012; suppl. vol. 60, 25 -28.
5. Goossens H., FerechM.et al. Outpatient antibiotic use in Europe and association with resistance: a crossnational database study.Lancet 2005; 365(9459):548-9.
6. Ewig S., GatermannS. Pathogen directed antimicrobial treatment of pneumonia In: Community-Acquired Pneumonia: strategies for management, ed. by Torres A., Menendez R. 2008. John Wiley & Sons, Ltd. 64.
7. Almirall J., Bolı´bar I., Serra-Prat M. et al. New evidence of risk factors
forcommunityacquiredpneumonia: a population-basedstudy.Eur Respir J. 2008; 31:1274–1284.
8. Ramirez P., Ferrer M., Marti V. et al. Inflammatory biomarkers andprediction for intensive care unit admission in severe communityacquiredpneumonia. Crit Care Med 2011; 39: 2211–2217.
9. Kruger S., Ewig S., Giersdorf S. et al. Cardiovascular andinflammatory biomarkers to predict short- and longtermsurvival in community-acquired pneumonia: results from theGerman Competence Network, CAPNETZ. Am J Respir Crit CareMed 2010; 182: 1426–1434.
10. Mandel L. et al., Infectious Diseases Society of America/American Thoracic Society, Consensus guidelines on the management of community-acquired pneumonia in adults. Clinical Infectious diseases 2007; 44: S27-72.
11. Woodhead M.et al., Guidelines for the management of adult lower respiratory tract infections, ERS task force in collaboration with ESCMID, Eur Respir. J. 2005; 26: 1138–1180.
12. Garau J. Why do we need to eradicate pathogens in respiratory tract infections?, Int. J. Infect. Dis. 2003, 7: Suppl.1, S5-S12.
13. Aspa J. et al., Empirical treatment of
community-acquired pneumonia: current guidelines In: Community-acquired pneumonia: strategies for management, ed. by Torres A., R. Menendez, 2008, John Wiley & Sons, Ltd 64.
14. Heselmans A. et al. The attitude of Belgian social insurance physicians towards evidence-based practice and clinical practice guidelines. BMC Fam Pract 2009;10:64.
15. Dambrava P., Torres A. et al.Adherence to guidelines’ empiricalantibiotic recommendations andcommunityacquired pneumonia outcome. Eur Respir J 2008; 32: 892–901.
30 І Medical Magazine | януари 2023 ПУЛМОЛОГИЯ
ИЗПОЛЗВАНА ЛИТЕРАТУРА:






Е. Стаменова УМБАЛ „Св. Анна“ - София, Медицински център „Инспиро“ - София
Алтернативни начини за отказ от тютюнопушене
По същество тютюнът е единственият по рода си опасен за консумация, свободно продаван продукт, водещ до тежки здравни последствия. По целия свят той е една от най-големите причини за инвалидизиране, заболяване и преждевременна смърт. Тютюнопушенето е тежък порок, който повишава риска от развитие на редица заболявания и нерядко се явява водещ фактор. Единственият начин за преустановяване на влиянието му върху здравето на човека е неговият пълен отказ.
Не е известно от кого е от-
крито тютюневото рас -
тение, но се знае, че
родината на тютюна е
Америка. Тютюнопу -
шенето е ритуал, който съществу -
ва още от древни времена (първи -
те доказателства датират от VII-XI
в. преди н.е. от Гватемала). В древ -
ните цивилизации на тютюневия
дим са приписвани магически свой -
ства, а вдишването му приравня -
вали към връзката с Бог. Тютюнът
се е отглеждал само в Централна и
Южна Америка, преди пътешестви -
ето на Колумб. Счита се, че рожде -
ното място на тютюна е именно там
– в Новия свят.
По същество тютюнът е единственият
по рода си опасен за консумация, сво -
бодно продаван продукт, водещ до
тежки здравни последствия. По целия свят той е една от най-важните причини за инвалидизиране, страдание и преждевременна смърт.
В световен мащаб около 47% от мъжете и 15% от жените са пушачи. Епидемиологични данни сочат, че рискът един пушач да развие заболяване, свързано с тютюнопушенето, нараства с течение на времето. Следователно, най-сигурният начин да се намали рискът е спиране на тю -
тюнопушенето. По данни на Американското торакално дружество (ATS)
половината от пушачите умират поради навика си!
ХАРАКТЕРИСТИКИ НА ТЮТЮНЕВИЯ ДИМ
Цигареният дим уврежда дихателните пътища и белия дроб както чрез химическите си характеристики (оксиданти, нитрозамини, феноли), така и чрез физическите си характеристики – висока температура и предизвикани термоувреждания на дихателния епител.
Доказано е, че веществата, съдържащи се в тютюневия дим имат цитотоксични, мутагенни и канцерогенни свойства. Установени са над 6 000 химични вещества, като над 100 от тях се класифицират като потенциално вредни. По-известни на широката аудитория са: въглероден оксид, азотен оксид, циановодород, бензол, толуен, формалдехид и много, много други.
СЗО отнася към най-опасните канцерогени 44 вещества, 10 от които присъстват в цигарения дим. Това са олово, кадмий, никел, хром, арсен, полоний, берилий и др. Плашещо е откритието, че пушач, който пуши по 1 кутия цигари на ден за една година
получава доза радиация, равняваща се на 1 000 рентгенови снимки!
Много от съставките на тютюневия дим генерират кислородни радикали. Те причиняват разкъсване на ДНК-веригите и хромозомни аберации.
Предизвикват оксидативен стрес и участват в патогенезата на редица болести, сред които ХОББ, атеросклероза и др. Свободните радикали повлияват най-активно горните дихателни пътища, предизвиквайки възпаление и атрофия на лигавицата на фаринкса и трахеята. Оксидантите се образуват не само в момента на горене на тютюна, но и при контакт на твърдите частици с клетъчната мембрана на алвеоларните макрофаги.
Процесът на горене се характеризира с включване на високи енергии, например температури от над 600°С. При вдишване температурата на върха на пламъка се повишава и достига 850°С. Това термично въздействие уврежда епителния слой на дихателните пътища и осигурява благоприятен терен за развитие на редица инфекции.
За да се поддържа горенето е необходим окислител, например кислород от въздуха. Хартиената обвивка на ци-
32 І Medical Magazine | януари 2023
ПУЛМОЛОГИЯ
гарата се възпламенява и се образуват твър -
ди частици, базирани на въглерод, които при дръпването от цигарата попадат в горните дихателни пътища, действат като „чуждо тяло“ и
засилват вече развилото се възпаление.
ЗАЩИТНИ МЕХАНИЗМИ НА ДИХАТЕЛНАТА СИСТЕМА
В белия дроб съществува защитна система, която в определени граници намалява ефектите на инхалираните токсини. Въпреки това при продължително инхалиране на токсични
вещества се наблюдават адаптивни промени, включващи хиперплазия на цилиндричните и гоблетовите клетки, преходна и плоскоклетъчна метаплазия. Крайният резултат е трансформация на епитела в кубичен.
Основен защитен механизъм е мукоцилиарни-
ят клирънс, състоящ се от постоянното треп-
тене на цилиите на ресничестия епител на дихателните пътища. Бронхиалните жлези и
секреторните цилиндрични клетки секретират мукусен слой в посока към ларинкса. В този
фин слой, покриващ епитела, се разтварят инхалираните частици и така лесно могат да бъдат отделени навън от дихателните пътища чрез кашлицата.
Алвеоларните макрофаги също се борят с „нашествениците“ от цигарения дим. Те са постоянни обитатели на алвеолите и фагоцитират инхалираните частици. След това чрез мукуса навлизат в лимфните съдове и достигат дрениращите лимфни възли, където представят обработения чужд генетичен материал на дендритните клетки и лимфоцитите за стартиране на имунна реакция.
Различни групи ензими взаимодействат с веществата в тютюневия дим с цел да ги неутрализират, защитават клетките от увреждане на ДНК и злокачествена трансформация.
НИКОТИНОВА ЗАВИСИМОСТ Никотинът е безцветен, силно отровен алкалоид, съдържащ се в листата на тютюневите растения. Достига мозъчните никотинови рецептори за 10 сек. след инхалиране, което е три пъти по-бързо от скоростта при венозното му приложение. Установен е силно изразен пристрастяващ ефект. Зависимост настъпва само при пушачи, т.е тя е следствие от употребата на тютюн. Зависимостта засяга личността като цяло – на психическо, физическо и социално ниво. Интересен е фактът, че Между-
народната агенция за изследване на рака НЕ класифицира никотина към клас канцерогенни, но той подпомага развитието на злокачествените процеси!
АЛТЕРНАТИВНИ НАЧИНИ ЗА ОТКАЗ ОТ ТЮТЮНОПУШЕНЕ Основна цел е преодоляването на никотиновата зависимост, т.е. прекъсване автоматизма на пушене и патологичния условен рефлекс. Изисква се комплексен подход, който въвлича редица специалисти: общопрактикуващи лекари, психолози, пулмолози, психиатри, медицински специалисти от специализирани кабинети, близки и познати на съответния пациент. Той трябва да почувства, че е проявен интерес към неговия проблем, да усети, че има рамо, на което да се опре. Тази мотивационна работа изисква време, отдаденост и ангажираност на различните специалисти. Освен риска от пристрастяване, никотинът има и други ефекти: подобрява концентрацията (за кратко), намалява апетита, повдига настроението. Важна роля имат и ритуалите, свързани с тютюнопушенето (кафе с цигара, цигара след хранене, първата сутрешна цигара).
Електронни цигари – системи за доставка на никотин, които навлязоха на българския пазар преди около 10 години. Въпреки че спечелиха бърза популярност, липсват научни доказателства за ефекта им върху здравето. Те са алтернатива на традиционните цигари и употребата им би могла да доведе до намаляване на тютюнопушенето, съответно на болестите, причинени от него. Но имат краткосрочен ефект и голяма част от потребителите се връщат към тютюнопушенето. Не е установено подобрение на белодробната функция. Няма единна директива, която гарантира качество и безопасност на продуктите. Поради опасенията за сблъсък на FDA не се продават като средства за спиране на тютюнопушенето.
Системи за нагряване на тютюна (СНТ) – високотехнологична система, която осигурява прецизно контролиране на температурата на нагряване на тютюна, като по този начин се избягва процесът на горене. С премахване на горенето вместо дим, пепел и катрани, се отделя аерозол, който съдържа вода, никотин, глицерол и аромати. Отделеният мирис е в пъти послаб в сравнение с конвенционалната цигара. Концентрацията на вредни вещества е сведена до минимум, като пушачите получават чист никотин от висококачествен тютюн. По този
[www.medmag.bg ] 33
начин те задоволяват никотиновите си нужди, а едновременно с това
е намалена токсичността. Според по -
следните проучвания употребата на
такъв тип системи води до подобре -
ние на
белодробната функция и нама-
ляване обема на атеросклеротичните
плаки в съдовете. Предстои да про -
следим ефектите на този нов продукт, тъй като той се появи на българския
пазар съвсем скоро (ноември 2017 г.).
Никотинови лепенки – непосредстве -

но след апликацията има бърз транс-
фер на никотина от пластира към ко -
жата, която се превръща в резервоар
за него, с бавно освобождаване на ве -
ществото в системната циркулация.
Мястото на апликация се променя
всекидневно, като не се повтаря поне за една седмица. Потребителите съ-
общават за нежелани ефекти: локални кожни реакции, нарушения в съня, гадене, повръщане. Освен това не задоволяват рефлекса за допир до цигарата, нарушен е тактилният усет на пръстите.
Никотинови дъвки – първата използвана никотин-заместителна терапия. Дъвката съдържа 2 мг или 4 мг. никотин и не се дъвче като оригинално произвежданите дъвки, а с прекъсване – държи се в устата за около 30 мин., при което се освобождава 90% от наличния никотин. Неудобство за потребителя е избягването на някои храни и напитки (кафе, плодов сок, газирани безалкохолни напитки и храни с висока киселинност), които намаляват обсорбцията на никотина. Като странични ефекти се наблюдават хъл-
цане, гадене, единични случаи на астматичен пристъп.
Препарати от растителен произход – разработени са на базата на алкалоида цитизин, който има свойства, неразличими от тези на никотина. Потиска абстинентния синдром при рязко спиране на тютюнопушенето като намалява броя на никотиновите рецептори средно с 25%. Данни от направени проучвания показват добра ефективност на продуктите като помощно средство за отказ от тютюнопушене.
Рефлексотерапия, акупунктура –действат на точно определени точки като въздействат върху различни отдели на централната нервна система. Установено е, че имат временен ефект – балансират процесите на потискане и възбуждане.
ЗАКЛЮЧЕНИЕ
Тютюнопушенето е тежък порок, който повишава риска от развитие на редица заболявания и нерядко се явява водещ фактор. Единственият начин за преустановяване на влиянието му върху здравето на човека е неговият пълен отказ. Това се постига със силна вяра, позитивно мислене и оказана помощ. Да откаже цигарите е най-хубавото нещо, което един пушач може да направи не само за себе си, но и за всички хора около него! Ако той не в състояние да го направи, трябва да получи подходяща алтернатива.
1. Graham A. Colditz, M.D. Smoke control P 665, The New England Journal of Medicine, 2015
2. American Thoracic Society. Cigarette smoking and health. Am J Respir Crit Care Med 1996; 153: 861-865
3. Blasi F., Ward B. – Eur Respir J 2014; 44: 585–588

4. Wang GF, Lai MD, Yang RR, et al. Histological types and significance of bronchial epithelial dysplasia. Mod Pathol 2006; 19: 429–437
5. Popper H.H., Timens W. Smoking-induced lung disease. Eur Respir Mon 2007; 39: 134–152

6. Paolini M, Perocco P, Canistro D, et al. Induction of cytochrome P450, generation of oxidative stress and in vitro cell-transforming and DNA-damaging activities by glucoraphanin, the bioprecursor of the chemopreventive agent sulforaphane found in broccoli. Carcinogenesis 2004; 25: 61–67
7. Department of Health and Human Services.Preventing tobacco use among youth and young adults: a report of the Surgeon General, 2012 (http://www.surgeongeneral.gov/library/reports/preventing-youth-tobacco-use/#Full%20Report)
8. Ангелова С. Тютюнопушене-последици и лечение, 2016
34 І Medical Magazine | януари 2023
ИЗПОЛЗВАНА ЛИТЕРАТУРА:
ПУЛМОЛОГИЯ
Living Every Breath
Фиксирана тройна комбинация за превенцията на средно тежки и тежки екзацербации при
Двукратен дневен прием в познато pMDI устройство 1 за облекчаване на симптомите през деня и нощта5
Extrafine частици със среден аеродинамичен размер на масата MMAD<2 µm, чрез които се постига депозиция в големите и малките дихателни пътища1,6


Преди да изпишете Trimbow®, моля запознайте се с кратката характеристика на продукта (КХП).
Пълна информация можете да получите от: Киези България ЕООД
София 1330, ул. Гюешево 83
БЦ „Сердика“, офис 103-105 , тел. 02 9201205
Източници:
1. Trimbow, КХП Април, 2021 (https://www.ema.europa.eu)

2. Singh et al. The Lancet, 2016, 388.10048: 963-973.
3. Papi et al.The Lancet, 2018, 391.10125: 1076-1084.
ПО ЛЕКАРСКО ПРЕДПИСАНИЕ
Притежател на разрешение за употреба: Chiesi Pharmaceutici S.pA Via Palermo 26/A

43122 Parma, Италия
4. Vestbo et al.The Lancet, 2017, 389.10082: 1919-1929.
5. Singh, D. .Expert opinion on pharmacotherapy, 2018, 19.11: 1279-1287.
6. Singh et al. International journal of chronic obstructive pulmonary disease, 2017, 12: 2917.
BG.TRI.21.07.07
ИАЛ 34754/15.07.2021
2,3,4 87 микрограма beclometasone dipropionate 5 микрограма formoterol fumarate dihydrate 9 микрограма glycopyrronium разтвор под налягане за инхалация
ХОББ
С. Испир1 , Д. Митева2
1Клиника по вътрешни бо -
лести, УМБАЛ “Св. Марина“ - Варна, Катедра по пропедевтика
на вътрешните болести, Медицински университет - Варна
2Клиника по пневмология
и фтизиатрия, УМБАЛ
Белодробната туберкулоза
по време на пандемията
от COVID-19
“Св. Марина“ - Варна, УС по белодробни болести и алергология, Медицински университет - Варна Белодробната туберкулоза е сред водещите причини за смъртност в световен мащаб, въпреки че през последното десетилетие заболеваемостта и смъртността от туберкулоза бавно намаляват. Световната пандемия от COVID-19 доведе до преразпределение на икономически и здравни ресурси, което рефлектира върху контрола, профилактиката, диагностиката и лечението на туберкулозата, компрометирайки крехкия успех до момента. Наблюдават се случаи на ко-инфекция между двете заболявания, като всяко от тях потенцира възникването и влошава прогнозата на другото заболяване. Двете заболявания се проявяват като синдемия, за овладяването на която са необходими координирани усилия както на клиничните специалисти, така и на здравеопазните системи като цяло.
Ключови думи: Туберкулоза, COVID-19, ко-инфекция.
Н
а 11.03.2020 г. СЗО обя -
ви глобална пандемия от COVID-19. В рамките на по -
вече от две години пандемията доведе до преразпределение на икономически, социални и здравни ресурси, които бяха пренасочени предимно към овладяване на пандемията. Това от
своя страна рефлектира върху контрола, профилактиката, диагностиката и лечението на редица други заболявания, включително туберкулоза (TB). В годишния си доклад от 2021 г. (Фиг. 1). СЗО съобщава за 18%
спад на новодиагностицираните и
съобщени случаи на TB през 2020 г.
в сравнение с 2019 г. (5.8 милиона за
2020 г. срещу 7.1 милиона за 2019 г.), като се счита, че 21% от хората, заразени с TB за 2020 г. са останали недиагностицирани. Затрудненият достъп до диагностика и лечение на TB резултира в увеличение на смъртните случаи. За 2020 г. се съобщават 1.3 милиона смъртни случаи сред HIV-негативни лица (увеличени в сравнение с 1.2 милиона за 2019 г.) и допълнително 214 000 смъртни случая сред HIV-позитивни лица (увеличени в сравнение с 209 000 за 2019 г.). Нивото на BCG ваксинация в някои части на света е спаднало с до 60%, което в бъдеще вероятно ще доведе до увеличение на детската болестност и смъртност. Разходите за диаг-
ностика, лечение и превенция на TB също са спаднали от 5.8 милиарда на 5.3 милиарда US$, или по-малко от половината от сумата, която е необходима. Всички тези данни сочат отстъпление от стратегията на СЗО за "Край на туберкулозата"[1]
Двете заболявания ТВ и COVID-19 показват някои сходства в клиничното си протичане, както и значими различия. Ако COVID-19 е новата модерна болест, първите следи за наличие на ТВ датират от преди повече от 9000 години в Atlit Yam, град по крайбрежието на Израел[2]. На 24.03. 1882 г. Robert Koch оповестява откриването на Mycobacterium tuberculosis и
36 І Medical Magazine | януари 2023
ПУЛМОЛОГИЯ
днес денят е обявен от СЗО за Световен ден за борба с туберкулозата. И двете заболявания се разпространяват по въздушно-капков път, поразяват основно дихателната система, но могат да ангажират и редица други органи. Респираторните симптоми като кашлица, еспекторация, фебрилетет могат да се припокриват при двете заболявания, но клиничният ход при COVID-19 е остър, докато при ТВ е налице хронично протичане. Въпреки че по-дълготрайни симптоми като хемоптое, нощни изпотявания и загуба на тегло са по-характерни за ТВ, трябва да се отбележи, че давността на симптомите не може да бъде надежден критерий за разграничаване

на двете заболявания и симптоми с давност
под 14 дни не изключват ТВ. Някои комор -
бидности като захарен диабет и имуносупресивни състояния крият повишен риск за теж-
ко протичане и на двете зболявания, докато
други като обезитет и хипертонична болест са особено рискови за прогресия на COVID-19. Различна е и рентгеновата картина, като при COVID-19 типични са периферните инфилтрати тип "матово стъкло", докато при ТВ са наблюдават консолидации с кавитации, предоминантно върхово разположени[3] .
Ко-инфекцията между ТВ и COVID-19 представлява истинско предизвикателство за клиницистите, като клиничните и имуно-патологични взаимовръзки между двете заболявания
се нуждаят от допълнително осветляване.
Редица проучвания изследват ко-инфекцията между двете заболявания, като се уста -
новява, че всяко едно от тях потенцира възникването и влошава прогнозата на другото заболяване. Така например, пациентите с ТВ, както и тези с грип имат над 2 пъти повишен риск за смъртност при ко-инфекция със SARSCoV-2[4]. COVID-19 може да възникне преди, едновременно или след диагностицирането на ТВ. В ендемични за туберкулоза райони сред хоспитализирани пациенти с COVID-19 делът на тези с активна или прекарана TB варира между 2-8% [5]. По данни от клинични случаи, серии от случаи и мета-анализ Song и съавтори съобщават за 23.46% смъртност при пациенти с COVID-ТВ ко-инфекция, като починалите пациенти са по-възрастни, по-често имат хипертония като придружаващо заболяване, двустранни инфилтрати, промени тип "цъфнала клонка" и по-висок левкоцитен брой[6]. Голямо проучване върху двойната COVID-ТВ инфекция е проведено от TB/ COVID-19 Global Study Group. Проучването об -
хваща 767 пациента с активна или прекарана туберкулоза и COVID-19 от 172 центъра в 34 страни. При по-голямата част от тях (74%) ТВ е диагностицирана преди COVID-19, а при 16.5% двете заболявания са диагностицирани в рамките на една седмица. Смъртността
в изследваната група е 11.08%, като причината за смъртта при около половината от смъртните случаи е COVID-19, при друга част като причина за смъртта са приети двете заболявания и само при един човек като причина за смърт та е приета туберкулозната инфекция. При мултивариантен анализ факторите, свързани с повишена смъртност, са възраст, мъжки пол и необходимост от инвазивна вентилация. Авторите заключават, че ТВ трябва да се разглежда като рисков фактор за тежък COVID-19 и пациентите с ТВ изискват засилени превантивни мерки, включително ваксинация срещу SARS-CoV-2[7]. Диагностиката на двете едновременно протичащи заболявания не винаги е лесна. При ко-инфекция между COVID-19 и активна ТВ, в немалка част от случаите образните методи, включително компютърна томография могат да покажат картина, характерна за COVID-19 и да пропуснат активна ТВ. Диагнозата на ТВ се затруднява също от липсата на експекторация при част от пациентите и избягване провеждането на ФБС или провокирана храчка по време на активна инфекция със SARS-CoV-2[5]
Бихме искали да споделим наблюдаван от
Фиг. 1
Доклад на СЗО за туберкулоза -2021г.
[www.medmag.bg ] 37
Фиг. 2
Рентгенография на пациентка с ко-инфекция
ТВ-COVID-19
Архив: УМБАЛ "Св. Марина"
нас случай на COVID-19 и съпътстваща белодробна туберкулоза. Касае се за пациентка на 27 години с малцинствен произход, с едномесечни оплаквания от продуктивна кашлица с гноевидна експекторация и фебрилитет. Хоспитализирана е с положителен РСR тест за SARSCoV-2, но отказва лечение и напуска болницата по собствено желание. Две седмици по-късно отново е хоспитализирана, вече в тежко общо състояние, с кахексия и прояви на остра дихателна недостатъчност. Рентгенографията на гръдна клетка показва двустранни кавитиращи лезии (Фиг. 2). РСR тестове за SARS-CoV-2 (носогърлен секрет) и за Mycobacterim tuberculosis (храчка) са положителни, като впоследствие е получен и положителен резултат от посявка в среда на Löwenstein–Jensen. Започната е кислородотерапия, антибактериална, кортикосте -
роидна и туберкулостатична терапия. Антивирусна терапия с remdesivir не е провеждана поради голямата давност на COVID-19. Въпреки така провежданата терапия на 5-ия ден от хоспитализацията е регистриран летален край. Имайки предвид клиничната картина с давност на оплакванията повече от месец и рентгеновата картина, смятаме, че това е един от редките случаи на ко-инфекция ТВ-COVID-19, при който най-вероятната причина за смъртта е именно запуснатата туберкулозната инфекция, а COVID-19 играе ролята на допълнителен, утежняващ нейното протичане фактор.
Тежко протичащият COVID-19 по -
вишава риска за реактивация на латентна туберкулоза и разви -
тие на активна болест. Значение за това най-вероятно има потис -
кането на клетъчния имунитет от SARS-CoV-2, както и използ -
38 І Medical Magazine | декември 2022 ПУЛМОЛОГИЯ
ваните в лечението на COVID-19 имуносупресивни и имуномодулаторни терапии. Употребата на кортикостероиди, например, има доказани ползи в лечението на тежък COVID-19, но едновременно с това повишава риска за опортюнистични бактериални, гъбичкови и вирусни заболявания[8].
Това налага прецизиране употребата на кортикостероиди само до показаните за това пациенти с COVID-19, както и избягване на ненужно високи дози и продължителни курсове.
Клиницистите, лекуващи хоспитализирани пациенти с COVID-19, тряб -
ва да бъдат внимателни по отноше -
ние реактивацията на ТВ, тъй като в
част от случаите наличието на новопоявили се инфилтрати на контролна рентгенография би могло да се
приеме да бактериална нозокомиална пневмония, с което диагностиката на ТВ да се забави. Най-вероятно обаче активирането
това тепърва ще се изявяват. Интерес представлява въпросът за лечението на COVID-19 при налична ко-инфекция с активна ТВ. Обикновено се провежда стандартно лечение, но трябва да се имат пред вид някои междулекарствени взаимодействия. Така например когато е необходимо приложение на кортикостероид при тежък COVID-19, дозата му трябва да се удвои поради индуциращия ефект върху чернодробните ензими на rifampicin. Подобно действие има rifampicin върху някои антивирусни препарати, включително remdesivir, чиито серумни нива намаляват при съвместна употреба[5]. Отново трябва да се отбележи обаче риска от прекалено високите дози и дълги курсове кортикостероиди, които не само могат да влошат протичането на ТВ, но да доведат до активация на гъбичкови инфекции, включително редки такива като мукормикоза.
на латентна
ТВ вследствие прекаран COVID-19 настъпва по-късно и последствията от
двете заболявания ТВ и COVID-19 действат като синдемия. Терминът синдемия се дефинира като съвкупност от две или повече едновременни епидемии или групи от болести, протичащи при определени социални условия, които изострят прогнозата и тежестта на заболяванията. Терминът е разработен от Мерил Сингър в средата на 90-те. Туберкулозата и COVID-19 се съчетават още с редица незаразни болести, добили епидемичен характер- хипертонична болест, затлъстяване, захарен диабет, сърдечно-съдови болести, хронични белодробни болести, рак. Двете заболявания се развиват в условия и на социални рискови фактори като бедност и недоверие в здравеопазните системи и институциите, с което се затруднява провеждането на ваксинационните програми и спазването на противоепидемичните мерки. Успешната борба с ТВ и COVID-19 изисква интегриран подход в разбирането и лечението на болестите.
1. https://www.who.int/publications/i/item/9789240037021
2. Viscaa D. Ong CMV, Tiberie S et al. Tuberculosis and COVID-19 interaction: A review of biological, clinical and public health effects. Pulmonology 2021 Mar-Apr;27(2):151-165. doi: 10.1016/j.pulmoe.2020.12.012
3. Gopalaswamy R, Subbian S. Corticosteroids for COVID-19 therapy: potential implications on tuberculosis. Int J Mol Sci 2021; 22: 3773.
4. Sarkar S, Khanna P, Singh AK. Impact of COVID-19 in patients with concurrent co-infections: A systematic review and meta-analyses. J Med Virol 2021; 93: 2385–2395.
5. Dheda K, Perumal T, Moultrie H et al. Tuberculosis in the time of COVID-19 1. The intersecting pandemics of tuberculosis and COVID-19: population-level and patient-level impact, clinical presentation, and corrective interventions. Lancet Respir Med 2022; 10: 603–22
6. Song W-m, Zhao J-y, Zhang Q-y, Liu S-q et al. COVID-19 and Tuberculosis Coinfection: An Overview of Case Reports/Case Series and Meta-Analysis. Front. Med. 2021; 8:657006. doi: 10.3389/fmed.2021.657006
7. The TB/COVID-19 Global Study Group. Tuberculosis and COVID-19 co-infection: description of the global cohort. Eur Respir J 2022; 59: 2102538 [DOI: 10.1183/13993003.02538-2021].
8. Shariq
COVID-19 and tuberculosis: the double whammy of respiratory pathogens. Eur Respir Rev 2022; 31: 210264 [DOI: 10.1183/16000617.0264-2021].
ИЗПОЛЗВАНА ЛИТЕРАТУРА:
M, Sheikh JA, Quadir N, et al.
В заключение може да се каже, че
Г. Костов, д.м. Медицински Универстет – Пловдив, Медицински факултет, Катедра „Специална хирургия“, УМБАЛ „Каспела“, Клиника по хирургия
в хода на лапароскопска холецистектомия
Ключови думи: Холангиография, експлорация на жлъчни пътища.
Въведение: След масовото навлизане на миниинвазивната хирургия, лапароскопската холецистектомия се наложи като златен стандарт при лечението на хирургичните заболявания на жлъчния мехур. Като всяка една хирургична метода и тази се характеризира със своите специфични усложнения. Последните са асоциирани с повишен морталитет, морбидитет, влошено качество на живот на пациентите, повишени болнични разходи. Един от методите за справяне с тази компликация е използването интраоперативна холангиография.
Цел: Да разгледаме предимствата и недостатъците на интраоперативната холаниография в хода на холецистектомия и ги сравним със собствените резултати. Материали и методи: В проучването бяха включени всички пациенти с осъществена интра оперативна холангиография в хода на холецистектомия в Клиниката по Хирургия на УМБАЛ “Каспела“ през периода 2014-2021 г. Резултати: За посочения период са осъществени n=2587 холецистектомии. Половото разпределение е както следва: жени n=1884, мъже n=703. От тях лапароскопски n=2573, конвенционални n=14. При n=264, извършена ИОХ поради суспекция за конкременти или неясна анатомия, доказана холедохолитиаза при n=135 пациента. Осъществена интраоперативна холангиография при n=687 оперирани. Установени асимптомни конкременти при n=101 пациента, от тях при n=83 на фона на неразширен холедох, само при n=18 хепатохоледоха бе с размер над 9 мм. Заключение: Интраоперативната холангиография предоставя възможност за детайлизиране анатомията на жлъчните пътища, подпомагайки младите хирурзи в периода на тяхното обучение, спомага за откриване на асимптоматична холедохолитиаза, като същевременно притежава нисък процент на усложнения.
След масовото навлизане на миниинвазивната хирургия лапароскопската холецистектомия се наложи, като зла-
тен стандарт при лечението
на хирургичните заболявания на жлъч-
ния мехур[1]. Като всяка една хирургич-
на метода и тази се характеризира със
своите специфични усложнения - нара-
няване на жлъчните пътища. Послед-
ните са асоциирани с повишен морталитет, морбидитет, влошено качество
на живот на пациентите, повишени болнични разходи[2,3]. Един от методи-
те за справяне с тази компликация е използването интраоперативна холангиография. Използването на последната в хода на холецистектомия остава противоречиво. Операторите против регулярната й употреба считат, че прилагането й с цел избягване нараняване на жлъчните пътища не е препоръчително поради наличието и на други методи, способстващи изясняването на билиарната анатомия. Повечето от автори са на мнение, че безсимптомни конкременти се откриват рядко. Те асоциират процедурата с удължаване
на оперативното време, лъчево натоварване на пациента, възможни фалшиво позитивни резултати, вероятни ятрогенни увреди и повишаване на медицинските разходи[4,5]
На другия полюс стои възможността за изясняване анатомията на екстрахепаталните жлъчни пътища и избягване на тяхната увреда, което предоставя значителна сигурност особено при хирурзи с малък опит, спомага за идентифициране на асимптомни конкременти и ограничава използването на предо-
40 І Medical Magazine | януари 2023
Холангиография
ХИРУРГИЯ
перативна ERCP, която също е асоцирана с възможни различни по вид и тежест усложнения[6].
Цел: На база на изложеното по-горе си поставихме за цел да разгледаме предимствата и недостатъците на рутинната интраоперативна холаниография в хода на холецистектомия и ги сравним със собствените резултати.
Материали и методи: В проучването бяха включени всички пациенти с осъществена рутинна интра оперативна холангиография в хода на холецистектомия в Клиниката по Хирургия на УМБАЛ "Каспела" през периода 2014-2021 г.
Информацията бе събрана от История на заболяването на пациентите и оперативните журнали. Изключващи критерии: диаметър на общия жлъчен канал >10 mm, ASAT, ALAT > два пъти, алкална фосфатаза >280 U/I, анамнеза за пожълтяване, преживян остър панкреатит, повишени стойности на общия и директен билирубин. При наличие на тези обстоятелства интраоперативната холатгиография е задължителна.
Оперативната метода включваше щателна дисекция на d.cysticus и a.cystica в триъгълника на Kalot, с поставяне титаниев клипс максимално
[www.medmag.bg ] 41
ХИРУРГИЯ
високо в проксимално направление в близост до инфундибуларно цистичната зона с цел осигуряване повече дължина на цистикуса. Впоследствие се осъществява малка дуктотомия, през която се въвежда холангиографски катетър, същият се позиционира с титаниев клипс. Проверяваме проходимостта му с физиологичен разтвор, след което въвеждаме контрастната материя. Визуализираме анатомията на интра- и екстрахепаталните жлъчни пътища, наличието на конкременти, тумори или кистични формации, както и преминаването на контраста в дуоденума.
Резултати: За посочения период са осъществени n=2587 холецистектомии. Половото разпределение е, както следва: жени n=1884, мъже n=703. От тях, лапароскопски n=2573, конвенционални n=14. При n=264 извършена ИОХ поради суспекция за конкременти или неясна анатомия, доказана холедохолитиаза при n=135 пациента. Осъществена рутинна интраоперативна холангиография при n=687 оперирани. Установени асимптомни конкременти при n=101 пациента, от тях при n=83 на фона на неразширен холедох, само при n=18 хепатохоледоха бе с размер над 9 mm. Нямахме случай на нараняване на жлъчните пътища в тази група. Средната продължителност на операцията при конвенционална холецистектомия68 мин., при миниинвазивна намеса - 41 мин., при лапароскопска холицистектомия с ИОХ - 54 мин. Времето се измерва от първия разрез до последния конец. Лезия на жлъчните пътища при оперираните „със“ и „без“ ИОХ, съответно n=0 и n=3. Удължаване на оперативното време при оперираните с осъществена ИОХ - средно с 13 мин. Увеличаване на медицинските разходи в същата група с 46 лв.
Нямахме нито едно нараняване на жлъчен път в хода на осъществяване на РИОХ, в случаите с къс цистикус поставяхме холангиографския катетър през отвор в инфундибуларната част на жлъчния мехур.
Дискусия: Установено, е че „златен стандарт“ за установяване на конкременти в жлъчните пътища са ERCP и интраоперативната холангиография. Дебатът относно рутинното изпълнение на последната съществува. Множество автори се опитват да създадат предиктивна скорова система, която да категоризира пациентите с риск от налични конкрменти и необходимост от ИОХ. Според редица студия холедохолитиаза се среща в до 77% от случаите при
наличието на разширени жлъчни канали, повишени стойности на АСАТ, АЛАТ, ГГТ, АФ, билирубин. Според същите необходимостта от ИОХ при болни с показатели в границите на нормата изчезва предвид възможността за използване на ендо Ехо и Магнитно-резонансна холангиопанкреатография. Според някои автори ИОХ води до увеличаване на медицинските разходи, необходимост от скъпоструваща апаратура
и специално обучен персонал в сферата на образната диагностика[7]. Нещо повече те считат, че в определени случаи тя е безполезна или дори опасна: при къс, фибротично променен от възпалителния процес или дори изчезващ
такъв, както е при синдрома на Mirizzi. В такъв случай опита за осъществяване на холангиография може да доведе до нараняване на предната или задната стена на общия жлъчен канал[8,9]
Според други автори тук е важен индивидуалният опит на хирурга, развил своите лапароскопски умения и интрабдоминална ориентация с възможност за въвеждане на катетъра през инфундибуларната част на жлъчния мехур или преценка за неосъществяване на холангиография „на всяка цена“.
Холангиографията от своя страна намалява риска от увреда при неразпозната аномалия на билиарното дърво, като например рядко срещаното наличие на десен сегментен аберентен жлъчен канал, спомага за визуализиране на вече получено нараняване в хода на дисекция и възможност за симултанно възстановяване на лезията при наличието на опитен хирург[10] Голяма част от изследователските колективи са на мнение, че интраоперативната холангиография задължително трябва да се използва от младите хирурзи до натрупване на опит в хирургичната анатомия[11].
Освен това, изследването на жлъчните пътища предоставя възможност за едномоментно решаване на проблема при доказването на асимптомни конкременти, било то чрез интраоперативна ERCP, или ревизия на жлъчните пътища в зависимост от индивидуалните предпочитания и възможности на хирурга. Този подход премахва необходимостта от повторна хоспитализация и намаляване на медицинските разходи[12,13]. Vezakis et al. съобщават за значително редуциране броя на предоперативните ERCP от 20% на 7% при извършването на рутинна ИОХ и в резултат снижаване процента на усложненията, възникнали в резултат на ERCP[14]. Към това трябва да се има предвид
42 І Medical Magazine | януари 2023
и факта, че 1/3 от случайно откритите безсимптомни конкременти в жлъчните пътища преминават спонтанно през папилата в рамките на 6 седмици[15]. Удълженото оперативно вре -
ме, като причина за въздържание от ИОХ, не е сериозен довод, според ре -
дица проучвания и мета анализи то
е с не повече от 18 мин., и ако бъде приравнено към времето, необходи-
мо за постигане на висок „Critical view of safety score“, вземе се под внима-
ние по-малкото лъчево натоварване
в сравнение с ERCP, избягване на потенциално нараняване на жлъчното дърво или своевременно установява-
не на получени лезии в хода на дисек-
ция, се вижда, че това така наречено „удължаване“ е незначимо[16]. В този
контекст не може да не засегнем и темата за повишаване на медицински-
те разходи, но за да бъде обективен въпросът би трябвало да се сравни показателят цена/ефективност. Американско проучване показва себе -
стойност на РИОХ варираща от 77-738 usd, усреднено 122 usd. А разходите при възникване на нараняване на жлъчните пътища и лечение в по-късен етап варира между 60000-87000 usd, без да са включени евентуални компенсации за пациента, вариращи между 250000-500000 usd[17,18]. От изложените по-горе данни ясно се вижда, че все още не съществува единно становище относно използването на ИОХ[19]
Заключение: Интраоперативната холангиография предоставя възможност за детайлизиране анатомията на жлъчните пътища, подпомагайки младите хирурзи в периода на тяхното обучение, спомага за откриване
на асимптоматична холедохолитиаза, като същевременно притежава нисък процент на усложнения. Тъй като е ефективна, безвредна, лесна за усвояване и евтина може да се използва рутинно в хирургичната практика.
1. Sicklick JK, Camp MS, Lillemoe KD, Melton GB, Yeo CJ, Campbell KA, et al. Surgical management of bile duct injuries sustained during laparoscopic cholecystectomy: perioperative results in 200 patients. Ann Surg 2005;241:786-792.

2. Strasberg SM, Hertl M, Soper NJ. An analysis of the problem of biliary injury during laparoscopic cholecystectomy. J Am Coll Surg 1995;180:101-125.
3. de Reuver PR, Sprangers MA, Rauws EA, et al. Impact of bile duct injury after laparoscopic chole¬cystectomy on quality of life: a longitudinal study after multidisciplinary treatment. Endoscopy 2008; 40(8):637–643.
4. Wenner DE, Whitwam P, Turner D, et al. Laparoscopic cholecystectomy and management of biliary tract stones in a
freestanding ambulatory surgery center. JSLS 2006;10:47–51.
5. Nickkholgh A, Soltanivekta S, Kalbasi
H. Routine versus selective intraoperative cholangiography during laparoscopic cholecystectomy: a survey of 2,130 patients undergoing laparoscopic cholecystectomy. Surg Endosc 2006;20:868–874.
6. Ding GQ, Cai W, Qin MF. In intraoperative cholangiography necessary during laparoscopic cholecystectomy for cholelithiasis? World J Gastroenterol. 2015;21:2147–2151.
7. Williams EJ, Green J, Beckingham I, Parks
R, Martin D, Lombard M. Guidelines on the management of Common Bile Duct stones. Gut 2008;57:1004e21.
8. Lill S, Rantala A, Pekkala E, et al. Elective laparoscopic cholecystectomy without
routine intra-operative cholangiography: a retrospective analysis of 1101 consecutive cases. Scand J Surg. 2010;99:197–200
9. White TT, Hart MJ. Cholangiography and small duct injury. Am J Surg 1985;149:640–643.
10. Carroll BJ, Friedman RL, Liberman MA, Phillips EH. Routine cholangiography reduces sequelae of common bile duct injuries. Surg Endosc 1996; 10: 1194-7.
11. Olsen D. Bile duct injuries during laparoscopic cholecystectomy. Surg Endosc 1997; 11: 133-8.
12. K. T. Buddingh, V. B. Nieuwenhuijs, L. van Buuren, J. B. F. Hulscher, J. S. de Jong, and G. M. van Dam, “Intraoperative assessment of biliary anatomy for prevention of bile duct injury: a review of current and future patient safety interventions,” Surgical Endoscopy,
vol. 25, pp. 2449–2461, 2011
13. Wu SC, Chen FC, Lo CJ. Selective intraoperative cholangiography and singlestage management of common bile duct stone in laparoscopic cholecystectomy. World J Surg 2005; 29: 1402-8.
14. Vezakis A, Davides D, Ammori BJ, Martin IG, Larvin M, McMahon MJ. Intraoperative cholangiography during laparoscopic cholecystectomy. Surg Endosc 2000; 14: 118-1122.
15. Collins C, Maguire D, Ireland A, Fitzgerald E, O’Sullivan GC. A prospective study of common bile duct calculi in patients undergoing laparoscopic cholecystectomy: natural history of choledocholithiasis revisited. Ann Surg 2004;239: 28e33.
16. Flum DR, Koepsell T, Heagerty P, Sinanan M, Dellinger P. Common bile duct injury
during laparoscopic cholecystectomy and the use of intra-operative cholangiography. Arch Surg. 2001;136:1287–1292.
17. Flum DR, Flowers C, Veenstra DL. A costeffectiveness analysis of intraoperative cholangiography in the prevention of bile duct injury during laparoscopic cholecystectomy. J Am Coll Surg 2003;196:385–393.
18. Podnos YD, Gelfand DV, Dulkanchainun TS, et al. Is intraoperative cholangiography during laparoscopic cholecystectomy cost effective? Am J Surg 2001;182:663–669.
19. Nies C, Bauknecht F, Groth C, Clerici T, Bartch D, Lange J, et al. Intraoperative cholangiography as a routine method? A prospective, controlled, randomised study. Chirurgia 1997;68:892e7.
[www.medmag.bg ] 43
ИЗПОЛЗВАНА ЛИТЕРАТУРА:
Г. Костов, д.м. Медицински Универстет – Пловдив, Медицински факултет, Катедра „Специална хирургия“, УМБАЛ „Каспела“, Клиника по хирургия
Ключови думи: Инсуфициенция на анастомозата, ниска предна резекция, карцином на ректума.
на анастомозата след ниска предна резекция
Въведение: Инсуфициенцията на анастомозата при НПР е актуален проблем според различни студия, вариращ между 3-20%. От практическа гледна точка инсуфициенцията е комуникация между интра и екстралуменния компартимент на червото, причинен от нарушаване целостта на интестиналната стена в зоната на анастомозата между колона и ректума. Цел: Да разгледаме основните методи, използвани при диагностицирана инсуфициенция на анастомозата при ниски предни ректални резекции. Материали и методи: За симптоми на инсуфициенция приехме: фебрилитет, левкоцитоза, поява на болка в корема, пролонгиран следоперативен илеус, тахикардия, тахипнея, повишена секреция от коремните дренове, повишаване на С-реактивен протеин, нарушение на бъбречната функция. Наличието на перитонеално дразнене и изтичане на фекулентно съдържимо от абдоминалните дренове потвърждаваше усложнението. Резултати: За посочения период в клиниката са осъществени общо 414 ниски предни резекции. От тях инсуфициенция се наблюдаваше при n=33 (8.03%). При n=22 (66.6%) тя бе класифицирана, като Grade С, изискващ спешна реоперация. При n=11 (33.4%) инсуфициенцията се класифицира, като Grade В. Заключение: Инсуфициенцията на анастомозата след ниски предни резекции продължава да е проблем в световен мащаб поради неблагоприятните последствия до които води, а именно високшият морбидитет и морталитет, влошеното качество на живот на пациентите, сигнификантното повишаване на медицинските разходи.
Ниската предна резекция (НПР) е стандартна операция при дистален ректален карцином, позволяваща осъществяването на анастомоза и съхраняване на аналните сфинктери[1]. Инсуфициенцията на анастомозата (ИА) при НПР е актуален проблем според различни студия, вариращ между 3-20%[2]. От практическа гледна точка инсуфициенцията е комуникация между интра и екстралуменния компартимент на червото, причинен от нарушаване целостта на интестиналната стена в зоната на анастомозата между колона и ректума[3]
Последната от своя страна повишава
морталитета, морбидитета, болничния
престой и влияе негативно върху качеството на живот на пациентите[4]
ФАКТОРИ, ПОВИШАВАЩИ РИСКА ОТ ИНСУФИЦИЕНЦИЯ
Нарушение в кръвоснабдяването на колона и/или ректалния остатък: напрежение на конструираната анасто-
моза[5]; кумулация на течност в малкия таз и/или сформиране на пресакрален хематом, които впоследствие може да се инфектират и да компрометират заздравяването на анастомозата[6];
През последните десетилетия няколко проучвания са се фокусирали върху проблема относно рисковите фактори за инсуфициенция при ниска резекция. Всички резултати се обединяват около тезата, че основният рисков фактор е височината на анастомозата. Като различните авто ри посочват и различни рискови отстояния от линеа анораекталис: Vignali 7 cm, Karanjia <6 cm, Rullier <5 cm и Eriksen <3 cm.
От друга гледна точка ниските анастомози и мъжкият пол са независими фактори, повишаващи риска от инсуфициенция[7]. Тук трябва да се имат предвид и липсата на дренаж в малкия таз[8]; интраоперативна хеморагия повече от 500 ml[9]; продължителност на оперативната интервенция над
200 минути[10] интра- или периоперативна трансфузия на кръв или кръвни продукти[11]; BMI >27[12]; висок ASA score[13]; употребата на нестероидни противовъзпалителни средства[14]; неадювантна лъче и/или химиотерапия[15]; тютюнопушене[16]; употребата на алкохол[16]; напреднала възраст[17]
Относно начина на конструиране на анастомозата проведени проучвания не намират сигнификантна разлика в честотата на инсуфициенция при ръчно или механично конструирана такава[18]
Цел: Да разгледаме основните методи, използвани при диагностицирана инсуфициенция на анастомозата при ниски предни ректални резекции. Материали и методи: В настоящото изследване бяха включени всички пациенти с осъществена ниска предна резекция по повод ректален карцином и проявена инсуфициенция на
44 І Medical Magazine | януари 2023
Инсуфициенция
ХИРУРГИЯ
анастомозата в Клиниката по Хирургия на УМБАЛ "Каспела" през периода 2011-2020 г. Информацията бе събрана от история на заболяването на па-
циентите, оперативните журнали и журналите от журналите за проведените контролни прегледи. За симптоми на инсуфициенция приехме: фебрилитет, левкоцитоза, поява на болка
в корема, пролонгиран следоперативен илеус, тахикардия, тахипнея, повишена секреция от коремните дренове, повишаване на CRP (С-реактивен протеин), нарушение на бъбречната
функция. Наличието на перитонеал-
но дразнене и изтичане на фекулент-
но съдържимо от абдоминалните дре-
нове потвърждаваше усложнението.
При тези пациенти освен физикалния
преглед и лабораторните изследвания
за потвърждавнане на компликацията
използвахме рентгенография, Компютър томография (КТ) със или без контраст, ректоскопия за визуално потвърждаване и оценка големината й.
Резултати: За посочения период в клиниката са осъществени общо 414 ниски предни резекции. Половото разпределение е, както следва: мъже 220 (53.15%), жени 194 (46.85%).
От тях инсуфициенция се наблюдава-
ше при n=33 (8.03%). При n=22 (66.6%) тя бе класифицирана, като Grade С изискващ спешна реоперация. Лаваж с надшиване на дефекта и извеждане на протективна илеостомия се осъществи при n=7 (31.81%) пациенти, при тях инсуфициенцията заемаше по-малко от 1/3 от циркумференцията й. При останалите n=15 (68.19%) поради тотална дехисценция, проксималният край на дебелото черво се изведе, като колостома и се осъществи ампутация на аналния остатък.
При n=11 (33.4%) инсуфициенцията се класифицира, като Grade В. Терапев-
тичният ни арсенал в тази група включ-
ваше консервативно лечение с при-
лагане на антибиотици, поставяне на перкутанен дренаж под ехографски контрол и трансанален лаваж. За съжаление при n=5 (45.46%) от болните се получи влошаване на състоянието им и преминаване в Grade С, което наложи оперативна ревизия, при нея се намери тотална дехисценция на анастомозата, проксималният край на колона след опресняване се изведе, като колостома с ампутация на аналния остатък. Пациентите бяха оставени на лапаростома с неколкократни последващи ревизии.
Обсъждане: Честотата на ИА при ниска предна резекция остава висока и е най-опасното усложнение в следоперативния период и е отговорна за 1/3 от морбидитета в следоперативния период, повишаване на болничния престой и увеличаване на медицинските разходи[19]. Обикновенно се проявява между 5-8 ден[20]. След диагностицирането й мерките, които ще се вземат, зависят от клиничното й проявление. Лечебните действия варират в широк диапазон, включващ консервативно лечение - антибиотична терапия, перкутанни дренажи, трансанален дренаж, стентиране или реоперация. International Study Group of Rectal Cancer е предложила система за класифициране и поведение: Ако инсуфициенцията е малка и няма клинични данни за развитието на перитонеално дразнене и акумулиране на течност в коремната кухина, а данните за ИА са параклинични и рентгенографски, тогава тя се класифицира като Grade A и подлежи на консервативно лечение и наблюдение. В нашето проучване нямахме такива пациенти. Когато състоянието на пациента изисква активна, но неоперативна намеса се класифицира, като Grade В, той изисква използването на антибиотици, поставяне на транскутанни дренажи под ехографски или скенеграфски кон-
трол и/или трансанален лаваж. Имахме единадесет болни в тази група, като при петима се наблюдава прогресия на симптоматиката с изява на перитонит налагащ оперативна ревизия. При наличието на физикални и рентгенови данни за дифузен перитонит с характерна параклинична картина състоянието се класифицира, като Grade С, изискващо спешна реоперация – лаваж, надшиване на анастомозата, ако лезията заема до 1/3 от циркумференцията с извеждане на протективна илеостомия, а при тотална инсуфициенция извеждането на колостома. При двадесет и двама от нашите болни се осъществи реоперация, като оперативния обем варираше от надшиване на дефекта и извеждане на протективна илеостомия до ампутация на аналния остатък и извеждане на колостома, като при всички тези случай коремната кухина поради фекулентния перитонит бе оставена на лапаростома, с последващи ревизии и етапни лаважи.
Заключение: Инсуфициенцията на анастомозата след ниски предни резекции продължава да е проблем в световен мащаб поради неблагоприятните последствия до които води, а именно високият морбидитет и морталитет, влошеното качество на живот на пациентите, сигнификантното повишаване на медицинските разходи. Методиките за разпознаване на субклинично проявена такава включват стриктно наблюдение на неспецифичните оплаквания в ранния следоперативен период, резултатите от образните и лабораторни изследвания. При възникване на това усложнение от значение е ранното му разпознаване, стриктното проследяване и адекватното своевременно лечение, съобразно тежестта на симптоматиката с
целия познат арсенал, включващ консервативни, мининвазивни и хирургични методи.
1.Griffen FD, Knight CD, Whitaker JM, Knight CD. The double stapling technique for low anterior resection. Results, modifications, and observations. Ann Surg 1990; 211: 745751; discussion 751-752 [PMID: 2357137]
2. Bruce J, Krukowski ZH, Al-Khairy G, Russell
EM, Park KG. Systematic review of the definition and measurement of anastomotic leak after gastrointestinal surgery. Br J Surg 2001; 88: 1157-1168 [PMID: 11531861 DOI: 10.1046/ j.0007-1323.2001.01829.x]
3. Rahbari NN, Weitz J, Hohenberger W,
Heald RJ, Moran B, Ulrich A, Holm T, Wong WD, Tiret E, Moriya Y, Laurberg S, den Dulk M, van de Velde C, Büchler MW. Definition and grading of anastomotic leakage following anterior resection of the rectum: a proposal by the International Study
Group of Rectal Cancer. Surgery 2010; 147: 339-351 [PMID: 20004450 DOI: 10.1016/j. surg.2009.10.012
4. McArdle CS, McMillan DC, Hole DJ. Impact of anastomotic leakage on long-term survival of patients undergoing curative
resection for colorectal cancer. Br J Surg 2005; 92: 150-1154 [PMID: 16035134 DOI: 10.1002/bjs.5054 Пълната библиографската справка съдържа 20 източника и е на разположение в редакцията при поискване.
[www.medmag.bg ] 45
ИЗПОЛЗВАНА ЛИТЕРАТУРА: ИЗПОЛЗВАНА ЛИТЕРАТУРА:
Г. Костов, д.м. Медицински Универстет –Пловдив, Медицински факултет, Катедра „Специална хирургия“, УМБАЛ „Каспела“, Клиника по хирургия
ХИРУРГИЯ
Сравнение между роботизирана и лапароскопска
гастректомия
Ключови думи: Роботизирана гастректомия, гастректомия, D2 лимфна дисекция.
Въведение: Роботизираната хирургия е създадена с цел да преодолеe в известна степен недостатъците или по-точно ограниченията на лапароскопската хирургия. В литературата ролята на роботизираната хирургия при лечението на онкологичните заболявания на стомаха по-рядко е обект на обсъждане.
Цел: Нашето проучване има за цел да сравни роботизирания и лапароскопски метод при осъ
-
Методи: тридесет и четири пациенти с рак на стомаха, претърпели роботизирана гастректомия (DaVinchi) от март 2021 г. до юни 2022 г., са сравнени с последните 32 пациенти, подложени на лапароскопска гастректомия и D2 дисекция от един и същи екип. Всички оперирани включени в проучването са с тотална гастректомия и D2 лимфна дисекция с конструиране на езофаго-йеюно анастомозата с циркулярен ушивател тип Орвил на повдигната йеюнална бримка по Roux сутурирана на два етажа Y анастомоза интракорпорална в роботизираната и екстракорпорална в лапароскопски асистираната група. Резултати: Общото оперативно време при роботизираните операции бе средно 255 мин. (190306 мин.), като конзолното е 180 (148-240 мин.). Продължителността на интервенцииите при лапароскопски асистираните ни гастректомии е 190 мин. (158-285мин.). Броят на отстранените лимфни възли е съответно 35.4 +/- 10.5 в първата и 33.4 +/- 17.1 във втората група. Болничният престой съответно 5.6 и 7.4 дни. Следоперативни усложнения се наблюдаваха при четирима пациенти в роботизираната и също толкова в лапароскопски асистираната група. Заключение: С натрупването на повече данни се установява, че роботизираната хирургия използвана при лечението на злокачествените новообразувания на стомаха е безопасна и предлага онкологични резултати идентични с лапароскопската, и конвенционална такава. Нейни недостатъци са увеличената продължителност на оперативните намеси и високата себестойност.
навлизането на минимално инвазивните подходи през последните години започна една нова ера в лечението на бенигнените и малигнени заболявания в коремната кухина. Тези методи вече се използват рутинно при лечението злокачествените новообразования на стомаха. Характерни за тях са предимствата, които притежават пред конвенционалната хирургия, а именно: по-нисък риск от усложне -
ния, особено от страна на оперативната рана, редуцирана кръвозагуба, намалени болеви раздрази, водеши до намалена нужда от обезболяване в следоперативния период, ранна вертикализация на пациента в резулта на това значително се скъсява болничният престой и се редуцират медицинските разходи[1]
Роботизираната хирургия е одобрена, като асистираща хирургичните операции система (daVinci

С
intuitive) през 1997 г., а няколко години по-късно през 2000 г. получава сертифициране от FDA (Federal Drug Agency) за осъществяването на самостоятелни оперативни намеси с нея. Кумулирането на опит и усъвършенстването на роботизираните системи продължава. Благодарение на своите предимства роботизираните системи преодоляват някой от ограниченията и недостатъците на другите мининвазивни подходи и в частност на лапароскопската хирур46 І Medical Magazine | януари 2023
ществяването на тотална гастректомия и D2 лимфна дискеция при пациентите със стомашен карцином.

[www.medmag.bg ] 47
гия, те повишават прецизността на движенията, редуцират тремора, подобряват детайлизирането на образа, а мобилността на инструментите позволява сигурно манипулиране в тесни пространства недостъпни за лапароскопския инструментариум. Не на последно място стой и ергономията на оператора управляващ действията на роботизираната система от своята конзола, далеч и в същото време близо до оперативното поле с възможност за непрекъсната комуникация и бързо конвертиране при необходимост [2] . Въпреки това редица въпроси свързани с високата себестойност на оперативните намеси, както и онкологичните резултати при авансиралия стомашен карцином остават нерешени[3,4]
Цел: Да оценим преимуществата на роботизираната система при осъществяването на гастректомия и Д2 лимфна дискеция при лечението на стомашния карцином на база нашият опит.
Материали и методи: Тридесет и четири пациенти с рак на стомаха, претърпели роботизирана гастректомия (DaVinchi) от март 2021 г. до юни 2022 г., са сравнени със същия брой пациенти, подложени на лапароскопска гастректомия и D2 дисекция от един и същи екип.
Статистически методи: Променливите фактори бяха разгледани с помощта на теста на Фишер и хи-квадрат. Непрекъснатите променливи бяха оценени с помощта на Т-тест или U-тест на Ман-Уитни. Стойността на р по-малка от 0,05 приехме за статистически значими. Всички статистически анализи бяха извършени с помощта на IBM SPSS Statistics v. 22.
Резултати: При сравняване на посочените фактори установихме следните резултати. Общото оперативно време при роботизираните операции бе средно 255 мин. (190-306 мин.), като конзолното e 180 (148-240 мин.) Продължителността на интервенцииите при лапароскопски асистираните ни гастректомии е 190 мин. (158-285 мин.). Броят на отстранените лимфни възли е съответно 35.4 +/- 10.5 в първата и 33.4 +/- 17.1 във втората група. Болничният престой съответно 5.6 и 7.4 дни. Обемът на кръвозагубата в първата група бе 100 мл (90-190), а във втората 120 мл (100-210). Усложнения изразяващи се в
инсуфициенция на езофаго йеюналната анастомоза наблюдавахме при четирима пациенти в роботизираната и също толкова в лапароскопски асистираната група, като при трима в първата група се касаеше за частична инсуфициенция на анастомозата третирана с консервативни средства и посредством консервативна терапия при двама и налагане на ендоскопски клипси също при двама в лапароскопската група.
Дискусия: Оперативното време е един от основните сравняващи се фактори при всяка хирургична метода предвид рисковите, които то крие за възникване на компликации в следоперативния период особенно при пациенти с изразен ко-морбидитет. От резултатите ни наблюдаваме сигнификантно по-дълга продължителност на оперативната намеса в роботизираната група, идентични са резултатите и на други автори, като техните времена са в диапазона 202-439 мин. в роботизираната и съответно 171-361
мин. лапароскопската група[5]. Редица проучвания се опитват да асоциират удълженото оперативно време с докинга и подготовката за него[6]. Установено, че сигнификантно редуциране на оперативното време се наблюдава при кумулиране на достатъчно опит в роботизираната хиругия, който намалява основно конзолното време и разбира се несигнификантно докинга[7]. Ако се фокусираме само върху конзолното време то продължителността на оперативните намеси в двете наши групи е практически еднаква.Множество изследвания и метаанализи показват значително редуцирана кръвозагуба в роботизираните групи със стойности вариращи между 50-180 мл. и 34-220 мл. в лапароскопските. Според тях тези разлики вероятно се дължат на Боди мас индекса на пациентите, който корелира с повишен риск от кървене при извършване на лимфната дисекция. А според други тази разлика е реална и е породена от предимствата на роботизираните системи включващи по-добра 3D визуализация на структурите, липсата на тремор, подобрен достъп при дисекция в резултат на маневреността на инструментите[8,9]. В нашето изследване не наблюдавахме сигнификантана разлика по този показател (р=0.10). По критерия болничен престой повечето учени също не намират разлика в двете групи[10,11]. В нашето изследване съществува разлика между сравняваните групи съответно 5.7 в Роботизираната и 7.7 в лапа -
48 І Medical Magazine | януари 2023
ХИРУРГИЯ
роскопски асистираната група. Тази разлика обясняваме с наличието на
по-голям разрез на предна коремна стена свързан с по-изразени боле -
ви раздрази, по-бавната вертикали -
зация на пациента и възвръщане -
то към ежедненвните му дейности.
Като разбира се съобразяваме с
факта, че удължаването на болнич -
ния престой в двете групи поради възникнала инсуфициенция е почти идентичен 15/13 дни. Относно компликациите проспективно мултицентрично проучване на Kim et al.[7]
установява честота на усложненията 11.9% в роботизираната и 10.3%
в лапароскопската група. При нашите болни също не открихме разлика в усложненията-по едно във всяка група. Съществуват и доклади, които изнасят сигнификантно по-рядко компликации при роботизираните намеси обяснявани с по-малкото травмиране на панкреаса в хода на оперативната намеса и особено в
хода на лимфната дисекция с произтичаща от това намалена честота на следоперативните панкреатити и панкреатични фистули[10]. По отношение на броят отстранени лимфни възли повечето автори същи не откриват сигнификантна разлика между двете методи[6]. Такива са и нашите резултати. Разбира се съществуват и хирурзи, които считат, че роботизираната хирургия притежава предимство и по този показател, дължащо се отново на по-добрата и триизмерна визуализация, както и достъпността до всички групи възли[12]. Сравняването на двете методики не би било пълно, ако не добавим и критерия цена ефективност. Безспорно по-скъпият метод, чиято себестойност многократно надвишава конкурента си е роботизираната хируригия. Тук освен големият начален разход за закупуване на роботизираната система, ежемесечната такса за подръжка и ак-
туализация на софтуерът й, влизат и сигнификантно по-скъпите инструменти и консумативи в сравнение с лапароскопската група[13]. При нашите болни установяваме оскъпяване на цената на оперативната намеса почти двойно в сравнение с лапароскопсаката група, като тук не са взимани под внимание цените за стаплери и ушиватели, които са идентични.
Заключение: С кумулирането на данни се установява, че роботизираната хирургия използвана при злокачествените новообразувания на стомаха е безопасна и с идентични онкологични резултати с лапароскопсата, и конвенционалната, като притежава и редица предимства пред тях. Едни от често коментираните й недостатъци са продължителността на оперативните намеси и тяхната себестойност.
1. Son T, Hyung WJ. Laparoscopic gastric cancer surgery: current evidence and future perspectives. World J Gastroenterol. 2016; 22:727–35.
2. Marano A, Choi YY, Hyung WJ, Kim YM, Kim J, Noh SH. Robotic versus laparoscopic versus open gastrectomy: a meta-analysis. J Gastric Cancer. 2013;13:136–48.
3. Song J, Kang WH, Oh SJ, Hyung WJ, Choi SH, Noh SH. Role of robotic gastrectomy using da Vinci system compared with laparoscopic gastrectomy: initial experience of 20 consecutive cases. Surg Endosc 2009;23:1204-11.
4. Son T, Hyung WJ. Robotic gastrectomy for gastric cancer. J Surg Oncol.
2015;112:271–8.
5. Pugliese R, Maggioni D, Sansonna F, et al. Subtotal gastrectomy with D2 dissection by minimally invasive surgery for distal adenocarcinoma of the stomach: results and 5-year survival. Surg Endosc.
2010;24:2594–602.
6. Huang KH, Lan YT, Fang WL, Chen JH, Lo SS, Li AF, Chiou SH, Wu CW, Shyr YM. Comparison of the operative outcomes and learning curves between laparoscopic and robotic gastrectomy for gastric cancer. PLoS One 2014;9:e111499.
7. Kim HI, Han SU, Yang HK, Kim YW, Lee HJ, Ryu KW, Park JM, An JY, Kim MC, Park S, Song KY, Oh SJ, Kong SH, Suh BJ, Yang DH, Ha TK, Kim YN, Hyung WJ. Multicenter prospective comparative study of robotic versus laparoscopic gastrectomy for gastric adenocarcinoma. Ann Surg 2016;263:103-9.

8. Eom BW, Yoon HM, Ryu KW, Lee JH, Cho SJ, Lee JY, Kim CG, Choi IJ, Lee JS, Kook MC, Rhee JY, Park SR, Kim YW. Comparison of surgical performance and short-term clinical outcomes between laparoscopic and robotic surgery in distal gastric cancer. Eur J Surg Oncol 2012;38:57-63.
9. Shen W, Xi H, Wei B, et al. Robotic versus laparoscopic gastrectomy for gastric cancer: comparison of short-term surgical outcomes. Surg Endosc. 2016;30:574–80.
10. Suda K, Man-I M, Ishida Y, Kawamura Y, Satoh S, Uyama I. Potential advantages of robotic radical gastrectomy for gastric adenocarcinoma in comparison with conventional laparoscopic approach: a single institutional retrospective comparative cohort study. Surg Endosc. 2015;29:673–85.
11. Greenleaf EK, Sun SX, Hollenbeak CS, Wong J. Minimally invasive surgery for
gastric cancer: the American experience. Gastric Cancer 2017;20:368-78.
12. Nakauchi M, Suda K, Susumu S, Kadoya S, Inaba K, Ishida Y, Uyama I. Comparison of the long-term outcomes of robotic radical gastrectomy for gastric cancer and conventional laparoscopic approach: a single institutional retrospective cohort study. Surg Endosc 2016;30:5444-52
13. Yang SY, Roh KH, Kim YN, Cho M, Lim SH, Son T, Hyung WJ, Kim HI. Surgical outcomes after open, laparoscopic, and robotic gastrectomy for gastric cancer. Ann Surg Oncol 2017;24:1770-7.
[www.medmag.bg ] 49
ИЗПОЛЗВАНА ЛИТЕРАТУРА:
Й. Ценовски, А. Червеняков МБАЛСМ
Коремна травма
“Н. И. Пирогов“ - София Характерна черта на „травматичната епидемия” в съвременния свят е наличието на многообразни, тежки травматични увреждания, които много често са несъвместими с живота на пострадалия. Според Световната здравна организация, в света ежегодно около 10 000 000 души получават различни травматични увреди, като 250 000 от тях умират. За да се подобрят резултатите трябва да има диагностично-терапевтичен алгоритъм за травма, подготвен координиран екип – парамедици, лекари, адекватен транспорт, високоспециализирано лечебно заведение, наличие на противошокова зала, специализиран екип – хирурзи, травматолози, неврохирурзи, уролози, реаниматори, диагностици, интензивно отделение.
Ключови думи: Алгоритъм, коремна травма, лапаротомия, съчетана травма.
Kласификация на травмата е
определена от нуждата от
единен подход, тя трябва
да отговаря на определени
принципи да има практиче -
ска значимост. Единният подход оп-
ределя тактиката от мястото на зло -
полуката и продължава до пълното
оздравяване, важно е и оптимално
лечение в съкратени срокове. Меди-
цинската наука и в частност спешна-
та хирургия се доближава до точните
науки. От изключително значение за
спешните състояния са въвеждането
на алгоритми за лечение. Алгоритъм
е стъпка по стъпка процедура за пресмятане, обмисляне и преценка за из-
вършване на действие. Той опреде -
ля добре дефинирани инструкции за преценка и действие.
ВИДОВЕ ТРАВМИ, ВКЛЮЧВАЩИ
КОРЕМНАТА
Съчетана травма е едновременно ув-
реждане на органи от различни об -
ласти и системи на организма, причи-
нено от механичен травмиращ агент.
Засегнати са две, три и повече анато -
мични области едновременно. В ком-
плекса от увреди една от тях заема
водещо място – глава, гръден кош, корем, таз, крайници.
Множествена травма е едновремен-
но нараняване на няколко органа
от една и съща система или кухина, напр. две или три кости на крайници,
едновременно засягане на повече от един вътрегръден или вътрекоремен орган и др.
Комбинирана травма са увреждания,
настъпили едновременно от различни нараняващи фактори, напр. механична травма, съчетана с термично увреждане, поражение от йонизираща радиация и др.
КЛИНИЧНА КАРТИНА
Симптоми на перитонеално дразнене има при увреда на кух коремен орган, симптоми на кървене има при увреда на паренхимен орган. Въпреки това, големи количества кръв могат да се натрупват в перитонеалната и тазовата кухини, без да се доловят с ранните промени в резултатите от физикалното изследване. Брадикардията може да покаже наличие на интраперитонеално кръв или билиум.
ДИАГНОСТИКА Оценката на хемодинамичната стабилност е най-важният първоначален момент в диагностиката на пациент с тъпа коремна травма. При хемодинамично нестабилни бърза оценка
за хемоперитонеум може да се осъществи с помощта на диагностична перитонеална промивка (DPL) или фокусирана оценка със сонография за травми (FAST). Рентгенографски изследвания на корема са посочени при стабилни пациенти, когато резултати-
те от физикалното изследване са неубедителни.
Диагностичната перитонеална промивка е показана за следните пациенти в определянето на тъпи коремни травми[1]:
• Пациенти с увреждане на гръбначния мозък
• Пациенти с множество наранявания и необясним шок
• Пациенти с притъпена чувствителност (от придружаващи заболявания), при които се предполага коремна травма
• Интоксикирани пациенти или пациенти в нетрезво състояние, при които се предполага коремна травма
• Пациенти с потенциални интраабдоминални наранявания, които ще претърпят продължителна анестезия за друга процедура
Един от водещите методи за изследване на коремната травма е Focused Т - Abdominal Sonography for Trauma (FAST) – ехография. Този метод демонстративно показва свободна интраабдоминална течност, дава оценка на състоянието на солидните коремни органи. Притежава предимства от прилагането му, като липса на риск от замърсяване и радиация, неинвазиен е, дава бързи резултати, удобен е за многократно използване. Относителните недостатъци са
50 І Medical Magazine | януари 2023
ХИРУРГИЯ
трудна оценка на висцерални перфорации, зависят от оператора и квалификацията му, ретроперитонеалните структури са трудни за диагноза. Въпреки това, някои проучвания
са показали, че дори начинаещите оператори могат да определят свободно интраабдоминална течност, особено ако има повече от 500 мл течност. Чувствителността и специфичността на проучванията варира от 85% до 95%[2,3,4,5,6].
Оглеждат се 4 акустични прозорци, съответно региони (перикардиален, перихепатален, перилиенален, тазов), при легнало положение на пациента. С тази методика се откриват и съпътстващи увреди. При перикардния прозорец може да се диагностицира хемоперикард. При перихепаталния и перилиеналния прозорец травматични увреди на бъбреците, хемоторакс от същата страна, руптури на диафрагмата, излив във субфреничните пространства. Прегледът се тълкува като положителен, ако свободна течност се намира в някой от 4-те акустични прозорци, отрицателен, ако не се вижда течност и неопределен, ако някои от прозорците не могат да бъдат адекватно оценени[1].
При рентгенография на корема може да се диагностицира свободен въздух под диафрагмалните куполи при перфорация на интраперитонеален кух коремен орган, въздух в ретроперитонеума при дуоденална перфорация, фрактури на лумбалния отдел на гръбначния стълб[1]
Компютърната томография (СТ) осигурява най-детайлните изображения на травматична патология и може да помогне при определяне на оперативната интервенция[7,8,9,10]. За разлика DPL или FAST, CT може да определи източника на кръвоизлив. Компютърна томография е стандарт за откриване на наранявания на масивен орган. Тя осигурява отлично възпроизвеждане на изображения на панкреаса, дванадесетопръстника, и пикочно-половата система. Тези ретроперитонеални увреди може да не се диагностицират с DPL или FAST. В допълнение, КТ на корема може да разкрие други травми, свързани с коремната, като прешленни и тазови фрактури и наранявания в гръдния кош. Недостатък на метода е загубата на време при транспортиране
на пациента към рентгеновото отделение и е неприложим при хемодинамично нестабилни пациенти.
Диагностичната
лапароскопия е била най-полезна при оценката на възможните диафрагмална наранявания, особено при проникващи торако-абдоминални наранявания на лявата страна[11,12,13] при тазови фрактури. При тъпи травми този метод все още няма ясни предимства пред по-малко инвазивни изследвания като DPL и CT сканиране. Нещо повече, усложнения могат да се появат като резултат от неправилно поставен троакар. Хемодинамично стабилни пациенти с отрицателни бързи резултати от FAST изискват внимателно наблюдение, серийни коремни прегледи и повторно FAST проследяване. Въпреки това, да се обмисли извършването на КТ, особено ако пациентът е в нетрезво състояние или има други свързани наранявания.
Хемодинамично нестабилни пациенти с отрицателни бързи резултати са диагностично предизвикателство. Опциите включват DPL, експлоративна лапаротомия и, евентуално, КТ след агресивна реанимация.
Експлоративна лапаротомия е индицирана при нестабилна хемодинамика с диагностични или клинични данни за вътрекоремна хеморагия, при закрита травма на корема с положителна лапароцентеза, при нестабилна хемодинамика и проникващо нараняване в корема или над ребрена дъга, при огнестрелно нараняване в областта на корема, при данни за свободен газ под диафрагмалните куполи от рентгеновото изследване, при руптура на диафрагмата. Тук задължително трябва да има достатъчна експлорация (ксифопубична).
Показанията за лапаротомия включват към тези за експлоративната и клинични и параклинични данни за перитонит, данни за хемоперитонеум при DPL, FAST или CT сканиране, клинично влошаване по време на наблюдението.
Ревизията на ретроперитонеалното пространство е в зависимост от механизма на травмата, локализацията и находката. Прави се при всяко съмнение за увреда на подлежащия орган дуоденум, панкреас, бъбреци. Обособяват се 3 зони на хирургична намеса:
• централен/зона 1 – ревизия (аорта, целиачен ствол, куха вена, проксимална част на бъбречни съдове);
• латерален/зона 2 – ревизия при пулсации и нарастване (бъбреци, съдов педикул);
[www.medmag.bg ] 51
Фиг. 1
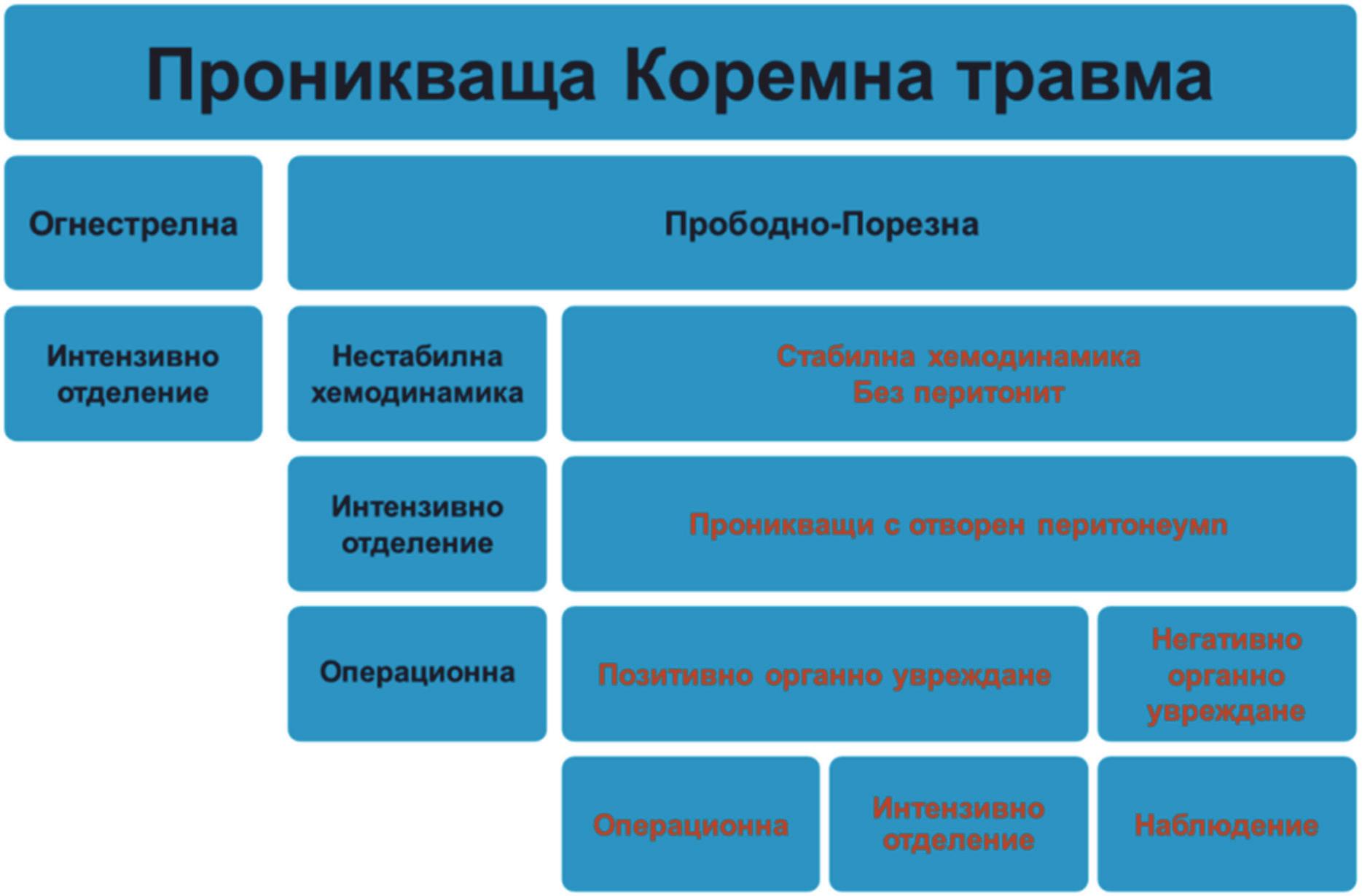
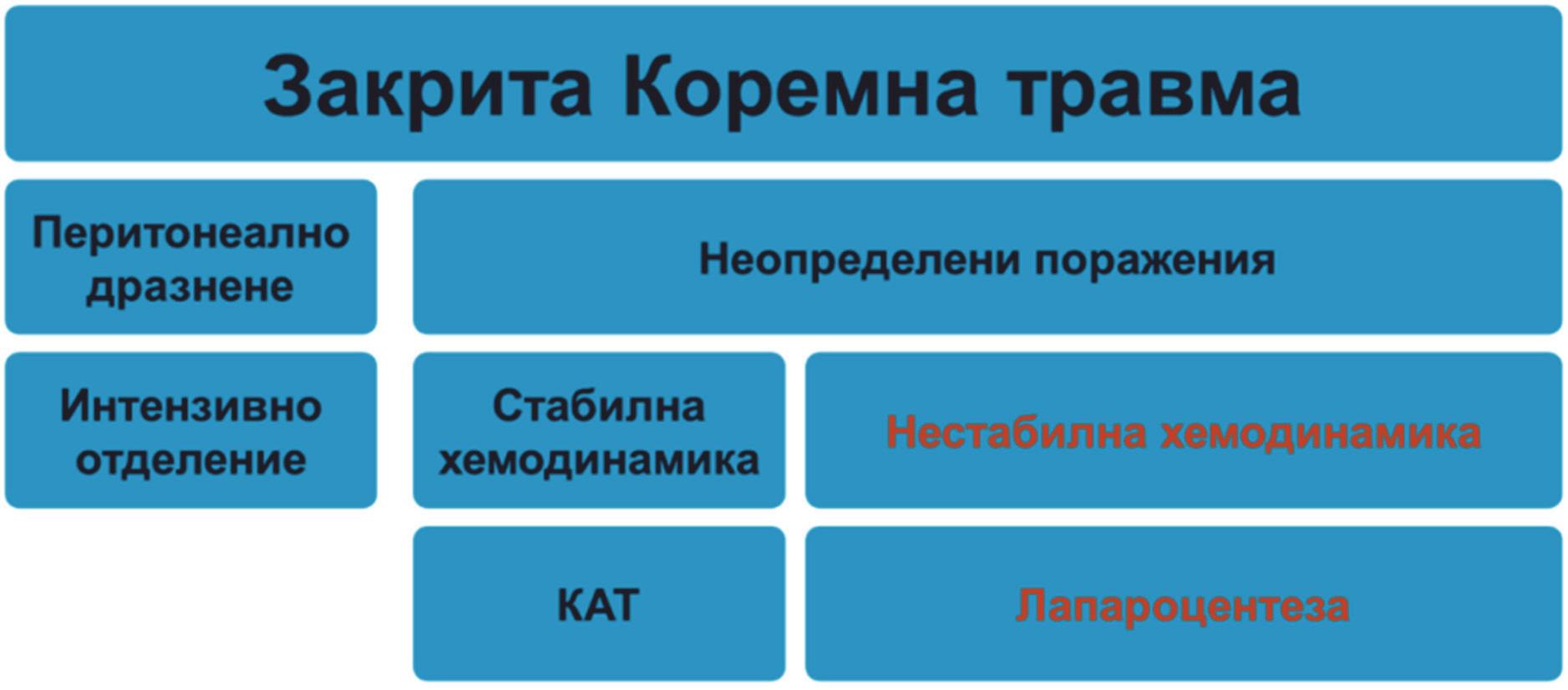
Алгоритъм при закрита коремна травма
Фиг. 2 Алгоритъм при проникваща коремна травма
• малкотазов/зона 3 – експлорация в краен случай при проникващо нараняване (увреда на дебело черво, илиачни съдове, уретери).
На Фиг. 1 и Фиг. 2 показваме диагностичния и терапевтичния алгоритъм при закрита и проникваща коремна травма.
Доболничната помощ се фокусира върху бързо оценяване животозастрашаващия проблем, започване реанимационни мерки, както и бързото транспортиране до болничното заведение[14,15]. По пътя се инфузира болус Рингер лактат или физиологичен разтвор при пациенти с данни за шок[16,17]. Това трябва да се титрира до систолно кръвно налягане от 90-100 mm

52 І Medical Magazine | януари 2023 ХИРУРГИЯ 1
Hg. Тази практика следва да доведе средното кръвно налягане, необходимо за поддържане на перфузията на жизненоважни органи.
При тежки съчетани травми с участие на коремната, тактиката е по-различна от стандартната. Тук важат принципите на хирургията, контролираща уврежданията.
Принципи за определяне на контрол на уврежданията
• pH <7.2
• ниво на серумен бикарбонат <15 mEq/L
• телесна температура <340 C
• трансфузия на еритроцитна маса >4000 ml
• хемотрансфузия >5000 ml
• общо водносолеви разтвори >12 000 ml
При 1 фактор – контролирана от уврежданията хирургия.
При всички фактори – летален изход. Леталната триада - хипотермия, ацидоза, коагулопатия.
Принципи на хирургията, контролираща уврежданията, са контрол на хеморагията, предпазване от замърсяване и да се избегнат допълнителни увреди. При хирургията, контролираща уврежданията трябва минимализиране на доболничната и спешната болнична помощ, да се извършат животоспасяващи процедури ABCDE (азбука на реанимацията), без излишни изследвания. Извършва се бърз транспорт до операционна (без повтарящи се опити за възстановяване на циркулацията) за хирургично спиране на хеморагията с активна ресусцитация.
Първият стадий на хирургията, контролираща уврежданията изисква незабавна лапаротомия, идентифициране на източника на кървене, периферно тампониране. Малките гастро и ентеротомии подлежат на бързо затваряне. Ресецират се невитални черва и се затварят на глухо. Минимални панкреасни лезии да се оставят без хирургична обработка. Дистални увреди на панкреаса и увреждания на ductus pancreaticus налагат дистална панкреатектомия. НЕ се извършва панкреатодуоденална резекция. Затварянето на корема е бързо и временно. Ако има съмнение за Компартмент синдром се оставя отворен.
Вторият стадий на хирургията, контролираща уврежданията започва в Интензивно отделение, като следващите 24-48 ч. са критични.
Тук се извършва дихателна поддръжка, корекция на метаболитните увреди, затопляне на тялото, корекция на нарушената коагулация, корекция на ацидозата, дентификация на окултни увреди. В третия стадий на хирургията, контролираща уврежданията са планирани реоперации, като прозорец за възможно лечение 24-48 ч. след травмата, между корекцията на метаболитните нарушения и развитие на SIRS и полиорганна недостатъчност. Извършва се премахване на коремна тампонада след 48-72 ч., налагане на чревни анастомози, лаваж, санация и затваряне на коремната стена. Може да се наложи ранна непланирана реоперация при пациенти с нарастваща хеморагия, перитонит или коремен Компартмент синдром. Прозорец за възможна дефинитивна остеосинтеза е 5-10 дни след травмата.
Хирургия, контролираща уврежданията ( ХКУ/ DCS ) е лечебен метод. Тя е една от водещите оперативни техники за последните 20 г. и е световно признат метод за лечение на травматично болни (ISS≥35). Понастояшем се прилага рутинно в УМБАЛСМ “Пирогов”, като намалява леталитета при тежките гръдни и коремни травми.
Усложненията на ХКУ са супурация на раната, дехисценция на раната, формиране на фистули, нозокомиални инфекции, органни увреди, кожни усложнения, коремен компатр -
мент синдром.
Показанията за лапаротомия при пациент с изолирана тъпа коремна травма, включват следното[1]:
• Признаци на перитонит
• Неконтролиран хеморагичен шок
• Клинично влошаване по време на наблюдението
• Констатация на хемоперитонеум от FAST или DPL ЧЕРНОДРОБНА И ЛИЕНАЛНА ТРАВМА Чернодробната и лиенална травма се получават при тъпа или проникваща травма. Леталитетът е 10-20%. Асоцирана е с фрактури на долни ребра. Симптомите са болка в дясно подребрие, дефанс, колапс. Мониторирането в интензивно отделение включва ултразвук, КАТ и контрол на хемодинамиката.
Показания за оперативно лечение възникват при хемодинамично нестабилен пациент, при
[www.medmag.bg ] 53
данни за лезия или перитонеален излив, при неефективно кръвопреливане. Дава се предимство на органосъхраняващите операции, особено при деца. При спленектомия може да възникнат инфекциозни усложнения, ранева инфекция, субдиафрагмален абцес, белодробни усложнения, хиповолемичен шок, травми на колон и ректум, емболизация, налагат се постоперативни ваксинации.
ТРАВМА НА СТОМАХА И ТЪНКИТЕ ЧЕРВА Травмата на стомаха и тънките черва също се
получава при тъпа или проникваща травма. Диагнозата се поставя при пневмоперитонеум или свободна течност (КАТ, Ехо), лапароцентеза, лапароскопия, лапаротомия. Лечението включва първичен шев или резекция.
ТРАВМА НА ДЕБЕЛОТО ЧЕРВО И РЕКТУМА Tравма на дебелото черво се диагностицира по пневмоперитонеума или свободна течност, лапароцентеза, лапароскопия, лапаротомия. Лечението е шев със или без колостомия. При интраперитоеална увреда на ректума поведе -
54 І Medical Magazine | януари 2023 ХИРУРГИЯ
нието е както при дебелочревна травма. При екстраперитонеална увреда - с противоестествен анус и пресакрален дренаж.
ТРАВМА НА ПАНКРЕАСА И ДУОДЕНУМА
Диагнозата при увредата на панкре -
ас и дуоденум често е късна, възмож-
но е едновременно увреда на два-
та органа. Възниква при контузия при тъпа травма. Ехография и КАТ, лапароскопия, лапаротомия са инструменталните езследвания. При интрамура-
лен хематом в стената на дуоденума
се изявява болка, метеоризъм, стомашно дуоденално повръщане. Ле-
чението при травма на панкреаса е консервативно (при закрита травма)
и включва назогастична сонда, очистителни клизми, наблюдение, мониториране, 3 седмици тотално парентерално хранене. Усложненията при консервативно лечение са панкреатична фистула, кисти. Оперативно лечение се предприема при болка, перитонит, висока температура, илеус, увеличение на серумната амилаза.
За хематом при дуоденална травма
се включва назогастрична сонда, наблюдение (периодично физикално изследване), мониториране, контрол на инфекцията. При проблеми се из-
вършва 3 седмици тотално парентерално хранене за отбременяване на пасажа.
При перфорация се предприема първичен шев с ексцизия и еферентно/ аферентно дуоденално дрениране.
ТАЗОВИ УВРЕЖДАНИЯ При тазовите увреждания има значителна кръвозагуба, промените са ретроперитонеално. Те са 2-ра по честота причина за травматичен леталитет (леталитет 8-50%). Съставляват 3% от фрактурите. Признаците и симптомите включват нестабилност на таза, болка (надпубисна), крепитации, кървав меатус, невроваскуларни дефицити. Да се търсят интра и ретроперитонеални увреди на пикочния мехур, а така също и увреди на уретрата. При тазови увреждания интервенции се провеждат при стабилизиран пациент, като се извършва обезболяване и фиксиране. При нестабилни пациенти се извършва имобилизация, външна фиксация, ангиография и емболизация. Тактиката е като при хематом с фрактура на таза, и ако пациентът продължава да губи кръв след външното фиксиране, трябва да се извърши артериография с емболизация, за да спре малкият процент
на артериално кървене намерено в тазовите фрактури.
НЕОПЕРАТИВНО ЛЕЧЕНИЕ Неоперативните стратегии за управление се основават на СТ сканиране диагностика и хемодинамична стабилност на пациента, както следва[1]: - В по-голямата си част, децата могат да бъдат съживени и лекувани неоперативно; някои детски хирурзи често преливат до 40 мл/кг кръвни продукти с цел да се стабилизира детето. Ако то остава хемодинамично нестабилно,тогава е показана лапаротомия,като се отдава предпочитание на органосъхраняващите операции.
- Хемодинамично стабилни възрастни с увреждания на паренхимни
органи, най-вече тези, на черния дроб и далака, могат да бъдат кандидати.
- Емболотерапия на лиеналната артерия, въпреки че не е стандартна терапия, може да се използва за възрастни с тъпа контузия на слезката.
Неоперативното лечение включва внимателно следене на жизнените показатели и често повтаряне на физикалния преглед и компютър томографии.
1.Eric L Legome, John Geibel, Blunt Abdominal Trauma-E-medscape
2. Blaivas M, Brannam L, Hawkins M, Lyon M, Sriram K. Bedside emergency ultrasonographic diagnosis of diaphragmatic rupture in blunt abdominal trauma. Am J Emerg Med. 2004 Nov. 22(7):601-4.
3.Branney SW, Moore EE, Cantrill SV, Burch JM, Terry SJ. Ultrasound based key clinical pathway reduces the use of hospital resources for the evaluation of blunt abdominal trauma. J Trauma. 1997 Jun. 42(6):1086-90.
4.Kornezos I, Chatziioannou A, Kokkonouzis I, Nebotakis P, Moschouris H, Yiarmenitis S, et al. Findings and limitations of focused ultrasound as a
possible screening test in stable adult patients with blunt abdominal trauma: a Greek study. Eur Radiol. 2010 Jan.
20(1):234-8.
5.Kendall JL, Faragher J, Hewitt GJ, Burcham G, Haukoos JS. Emergency Department Ultrasound Is not a Sensitive Detector of Solid Organ Injury. West J Emerg Med. 2009 Feb. 10(1):1-5.
6.Rozycki GS, Ochsner MG, Schmidt JA, Frankel HL, Davis TP, Wang D, et al. A prospective study of surgeon-performed ultrasound as the primary adjuvant modality for injured patient assessment. J Trauma. 1995 Sep. 39(3):492-8; discussion
498-500.
7.Brasel KJ, Olson CJ, Stafford RE, Johnson TJ. Incidence and significance
of free fluid on abdominal computed tomographic scan in blunt trauma. J Trauma. 1998 May. 44(5):889-92.
8.Holmes JF, Offerman SR, Chang CH, Randel BE, Hahn DD, Frankovsky MJ, et al. Performance of helical computed tomography without oral contrast for the detection of gastrointestinal injuries. Ann Emerg Med. 2004 Jan. 43(1):120-8.
9.Christiano JG, Tummers M, Kennedy
A. Clinical significance of isolated intraperitoneal fluid on computed tomography in pediatric blunt abdominal trauma. J Pediatr Surg. 2009 Jun. 44(6):1242-8.
10.Shanmuganathan K. Multi-detector row CT imaging of blunt abdominal
trauma. Semin Ultrasound CT MR. 2004 Apr. 25(2):180-204.
11.Fabian TC, Croce MA, Stewart RM, Pritchard FE, Minard G, Kudsk KA. A prospective analysis of diagnostic laparoscopy in trauma. Ann Surg. 1993 May. 217(5):557-64; discussion 564-5.
12.Ivatury RR, Simon RJ, Weksler B, Bayard V, Stahl WM. Laparoscopy in the evaluation of the intrathoracic abdomen after penetrating injury. J Trauma. 1992 Jul. 33(1):101-8; discussion 109.
13.Ortega AE, Tang E, Froes ET, Asensio JA, Katkhouda N, Demetriades D. Laparoscopic evaluation of penetrating thoracoabdominal traumatic injuries. Surg Endosc. 1996 Jan. 10(1):19-22.
14.Cryer HG, Larmon B. Patient care
phase: prehospital and resuscitation care. In: Greenfield LJ, Mulholland MW, Oldham KT, Zelenock GB, Lillemoe KD, eds. Surgery: Scientific Principles and Practice. Philadelphia: Lippincott-Raven;. 1997:280-4.
15.Pryor JP, Pryor RJ, Stafford PW. Initial phase of trauma management and fluid resuscitation. Trauma Reports. 2002;3(3):1-12.
16.Perel P, Roberts I. Colloids versus crystalloids for fluid resuscitation in critically ill patients. Cochrane Database Syst Rev. 2007 Oct 17. CD000567.
17.Bunn F, Trivedi D, Ashraf S. Colloid solutions for fluid resuscitation. Cochrane Database Syst Rev. 2008 Jan 23. CD001319.
[www.medmag.bg ] 55
ИЗПОЛЗВАНА ЛИТЕРАТУРА:
Й. Ценовски I-ва хирургическа клиника УМБАЛСМ „Н. И. Пирогов“ - София
Перфорация на стомашна
и дуоденална язва
Перфорацията е най-тежкото и смъртоносно усложнение на пептичната язва. Среща се в 5-10% от болните и може да бъде първа проява на болестта. По-често перфорират язвите по предната стена на дванадесетопръстника и предимно в следобедните часове. Честотата на пенетрацията (в панкреаса и съседните органи) е също 5-10%. Причина за тези усложнения са изострянето на процеса в съчетание с психотравми, диетичните грешки и злоупотребата с алкохол и някои медикаменти[1].
Пробивът може да бъде в свободната коремна кухина (80-85%), пробив с формиране на сраствания и
субфренични абсцеси (4-5%) и покрита перфорация. Пенетрации -
те (проникване) са по-чести при
язви по задната стена на дуодену -
ма и при постбулбарните язви с ви -
сока стомашна киселинност и чести рецидиви. Те проникват към задстомашната жлеза, по-рядко към черния дроб, жлъчните пътища или дебелото черво.
ЕТИОЛОГИЯ И ПАТОГЕНЕЗА
Пептичните язви са резултат от дисбаланс между фактори, които
могат да навредят на гастродуоде -
налната лигавица, и защитни механизми, които нормално ограничават
увреждането. При нормални условия съществува физиологичен баланс
между секрецията на стомашна киселина и гастродуоденалната мукозна
защита. Увреждане на лигавицата и
съответно пептична язва възниква, когато се наруши равновесието между агресивните фактори и защитните механизми. Агресивните фактори, като НСПВС (нестероидни противовъзпалителни средства), инфекция с H. pylori, алкохол, жлъчни соли, ки -
селина и пепсин, могат да променят защитата на лигавицата, като позволяват обратна дифузия на водородните йони и последващо увреждане на епителната клетка. Защитните механизми включват тесни междуклетъчни връзки, слуз, приток на кръв в лигавицата, клетъчно възстановяване и подновяване на епитела. Като цяло, дуоденалните язви са резултат от свръхсекреция на стомашна киселина, свързана с инфекция с H. pylori (при повечето случаи), докато секрецията е нормална или намалена при пациенти със стомашна язва. Хроничната исхемия на стомаха е в основата на стрес индуцираните язви при пациенти в интензивно отделение[2].
ПАТОЛОГОАНАТОМИЯ
Язвената болест е остър или хронично повтарящ се дефект (лезия) на лигавицата на стомаха или дуоденума, получаваща се вследствие на разяждащото действие на солната киселина, която се произвежда в стомаха. За язва се приема, когато дефектът преминава l. muscularis mucosae и е навлезнал по-дълбоко в стената на стомаха. Има дефекти на лигавицата, които не преминават l. muscularis mucosae, и тогава се гово -
ри за ерозия[2]. Когато язвата пенетрира и проникне през всичките слоеве на стомашната стена се получава перфорация - пробив през стената на органа, в който се намира язвата. Острата перфорация е най-тежкото усложнение на язвената болест. При него се получава изтичане на стомашно или дуоденално (от дванадесетопръстника) съдържимо в перитонеалната (коремната) кухина, вследствие на което се развива остър перитонит (инфекция на коремната кухина).
КЛИНИКА
1. Внезапна, жестока болка високо в корема.
2. Контрактура на цялата коремна стена.
3. Определени стомашни предшественици и предишни симптоми на язвената болест преди перфорацията.
Болка
а/ интензитет: внезапна, жестока, като удар с нож, пациентът се превива на две, може да колабира от болка, вика.
б/ локализация на болката: на стомашната язва - е в епигастриу-
56 І Medical Magazine | януари 2023
ХИРУРГИЯ
ма, дуоденалната – в епигастриум, дясно
подребрие, дясна илиачна област.
в/ ирадиация: към дясна илиачна област,
при дуоденалните може и вляво. Дру-
ги, по-редки локализации - клавикулар -
на, надключична, акромиална, скапулар -
на, интерспинална, към гръбначния стълб.
Симптом
на Олекер - болка в рамото. За да
се появи този симптом - трябва контакт на
колекцията с диафрагмата. Понякога е двустранна.
Контрактура на коремната стена Коремът не участвува при дишането, плосък, контрахиран. Контрактурата се явява още в началото, заедно с болката, тя намалява с прогресирането на перитонита и балониране -
то се увеличава, докато тя изчезва - към 10-12 час. В първите часове – контрактурата е над
пъпа, локализирана или сегментарна, понякога обхваща цялата коремна стена, но нейният максимум си остава в епигастриума, в дясно подребрие или вляво. Липсата на контрактура в първите часове е рядка (може да няма при дуоденална язва – дуоденалният сок е неутрален или алкален и е по-малко дразни). Тя е
причинена от рефлекторното дразнене на пе -
ритонеума от солната киселина.
Стомашни предшественици
а/ може да перфорира язва, латентна дотогава - това се случва в 1 от 10 случая.
б/ пациентът е имал преди гастритни оплаквания (болка след ядене, хематемеза, мелена, повръщане). Продроми - болки, придружени с гадене и повръщане, субфебрилно състояние[3]
Допълнителни (второстепенни) признаци
• Повръщания - те са ранни - от самото начало. Повръщанията са: мукозни, жлъчни, хранителни - не много обилни (според последното хранене) - 2-3 повръщания със средна обилност. По-чести са при дуоденалната язва, тъй като стомахът в този случаи е интактен, той се изпразва чрез повръщане, докато при стомашната перфорция стомахът се изпразва чрез перфорацията.
• Хематемеза - рядко.
• Стоп на газове и изпражнения - още от началото и не чака перитонита.
• Жажда.
• Студена, лепкава пот[3]
При наличие на такива оплаквания трябва незабавно да се потърси медицинска по -
мощ, тъй като може да се касае за перфорация и тогава е необходимо да се предприеме спешно оперативно лечение. Перфорацията е по-рядко усложнение при язва, но е най-тежкото и смъртоносно. При перфорация язвата извършва пробив през стената на органа, като съдържимото му се излива в коремната кухина. Бактерии и частично смляна храна могат да попаднат в перитонеума. Перфорирана язва може да доведе до перитонит. При перитонит инфекцията може бързо да се разпространи в кръвта, причинявайки сепсис. Това носи риск от полиорганна недостатъчност и може да бъде фатално, ако не се лекува.
Има три фази:
• І фаза - на шока.
• ІІ фаза - лъжливо благополучие.
• ІІІ фаза - фаза на перитонита.
Симптомите на перфорацията се характеризира с внезапна, много силна болка в горната половина на корема, с излъчване към гърба и плешката, която след няколко часа се разстила по целия корем. Болката се обуславя от химичното дразнене на корема от солната киселина. В някои случаи след тази остра фаза за час-два се наблюдава т.нар. мнимо благополучие - болките отслабват и лицето се зачервява. У изтощени и стари хора клиниката може да протече нетипично - липсват остри болки, дефанс, левкоцитоза[1]. Бързо се развива перитонит и остър хирургически корем, ригидност и мускулна защита на коремната стена, гръдно дишане, щадящо корема положение, тахикардия, колапс, напредваща интоксикация.
ОБЕКТИВНО ИЗСЛЕДВАНЕ Обективно болните лежат с прегънати към корема крака, избягват движения, кашлица и допир, дишат учестено и повърхностно. Езикът е сух и обложен с белезникав налеп. Установяват се силна болка при палпация и изразен мускулен дефанс в епигастриума, който постепенно обхваща целия корем. Поради стичане на стомашно съдържимо в илео-цекалната област дефансът понякога е най-изразен там. Чернодробното притъпление изчезва вследствие на проникване на въздух в коремната кухина. Появяват се метеоризъм, отслабване и изчезване на чревната перисталтика, затруднена дефекация. В началото е налице брадикардия (дразнене на n. vagus), която скоро се сменя с тахикардия[3].
[www.medmag.bg ] 57
ХИРУРГИЯ
Дифузният перитонит се появява 6-8 часа след перфорацията. Той се манифестира с хълцане, повръщане, студена и лепкава пот, изостряне на чертите на лицето, подуване на корема (мускулният дефанс намалява), силно ускорен и слабо напълнен пулс, артериална хипотония, висок фебрилитет и левкоцитоза със силно олевяване. Предизвиква се от попадане на чревна флора в перитонеалната кухина[1]. Понякога перфорацията се припокрива от оментума и съседните органи (Perforatio tecta). В началото се наблюдава картината на перфорация, но понеже не настъпва дифузен перитонит, постепенно острите болки изчезват спонтанно, а мускулният дефанс се ограничава в определен участък, където се задържа до 2-3 денонощия.
ФИЗИКАЛНИ СИМПТОМИ - ЛОКАЛЕН
СТАТУС[3]
1. Оглед на корема - коремът не участвува при дишането - под нивото на гръдния кош - плосък, ригиден - често при дуоденалната перфорация има балониране на левия
долен квадрант.
2. Палпация на корема а/ болка - най-силна в епигастриума, в дясно подребрие или вляво, а по-късно по целия корем, като пунктум максимум си остава горе. б/ симптом на Блумберг - положителен. в/ хиперестезия.
3. Перкусия на корема а/ чернодробното притъпление изчезва – в 60% трябва да се различи от по-късното, дължащо се на раздуването на колона при перитонита. б/ притъпление във флантовете (в резултат на излива).
4. Ректално туширане - чувствителен Дуглас (от излива).
5. Аускултация на корема а/ гробна тишина в корема още от началото (в резултат на чревна парализа). б/ Hustin – описва три симптома при аускултация - пропагация на гръдни шумове до пъпа - сърдечни шумове - перитонеално триене, свързано с наличие на ексудат (подобно на плевралното триене между органите) – шум с метален отзвук, свързан с преминването на мехурчета през перфорацията.
ОБЩИ ПРИЗНАЦИ[3]
1. Шоково състояние - бледост на лицето, пот, студени крайници, инертност, температура, по-ниска от нормалната, слаб, учестен пулс. В 30% от случаите - шок. 2. Пулс - в началото е леко забавен, по-къс -
но се учестява. 3. Темпертурата – нормална или по-ниска. Понякога перитонеалната болка се е успокоила - пертонитът се е локализирал - възниква абсцес - това става 1, 2, 3 или повече седмици след перфорацията. Симптоми: липса на апетит, безсъние, леки втрисания, температурата става висока, осцилираща, левкоцитоза, локализирана болка и локална мускулна защита. Абсцесите биват: субфренични, интеринтестинални, перигастрични, тазови. Рядко – интрависцерални (черен дроб, панкреас, слезка). Абсцесите биват единични или множествени.
ДИАГНОСТИКА
Все пак основният проблем си остава срокът, изтекъл от поставянето на диагнозата, тъй
като при 20-30% от болните не се установява
наличието на свободен газ под диафрагмата.
Почти 1/2 от екзитусите се падат на тази група. Много опасна в това отношение е стомашната язва, перфорирала в bursa omentalis, тъй като рентгеновите признаци при тези случаи могат да са неуловими. Диагнозата се потвърждава от наличието на свободен газ под диафрагмата, установено с обзорна рентгенография на корема. При отрицателен резултат може да се постави назо-гастрична сонда и да се инсуфлира възух под наляганетака при повторното рентгеново изследване се потвърждава диагнозата. При т.нар. „покрита“ перфорация може да е от полза рентгеново изследване на стомаха с течен контраст. При отрицателен резултат от горните изследвания и персистиращо съмнение за перфорация, е необходимо извършването на компютърна томография (КТ) на корема. Понякога само с КТ може да се открият промени в стомашната стена, прилежащо възпаление, минимално количество газ или течност като доказателство за перфорацията. С КТ се откриват и някои последствия на перфорацията в областта на срастванията като флегмон и субфреничен абсцес[4]. Лечението започва с интравенозни ИПП (80 mg болус и по 8 mg/ час), антибиотици (цефалоспорини, метронидазол, карбапенеми) и незабавно хирургическо лечение. Алтернатива е ендоскопският клипсинг, заедно с ИПП и антибиотици[4]
ЛЕЧЕНИЕ Лечението е оперативно. То се извършва по спешност, тъй като леталитетът нараства стръмно с часове: 2% до 6-ия час от началото на перфорацията, след 24 часа - 60% и по -
58 І Medical Magazine | януари 2023
вече. Общо смъртността при перфорация на стомашна язва е по-висока (10-40%), отколкото при дуоденалната (5-15%). Поведението при префоративната язва се определя от анамнестичните данни за еволюцията на заболяването, общото състояние на болния и степента на бактериалната контаминация
на перитонеума. Все пак, с използването на мощно киселинно потискащо лечение и ередикацията на Helicobacter Pylori, необходимостта от радикална операция рязко намаля. Хирургичното лечение най-често включва
зашиване на перфорацията, ексцизия на яз -
вата със или без пилоропластика, съчетани с
обилен перитонеален лаваж и много по-ряд-
ко стомашна резекция. В съвременен аспект
някои автори считат, че неоперативното ле -
чение следва да се има предвид при онези пациенти, които имат тежки съпътстващи заболявания, които правят риска от операцията толкова голям, че се забранява извършването й при условие обаче, че не изтича повече стомашно съдържимо рентгенографски (с водноразтворим контраст) и ако са
налице и другите критерии на L. Rosoff и С. Berne (1977), т.е. ако абдоминалната наход-
ка се подобрява в 3-5 ч., пневмоперитонеу-
мът не се увеличава и няма влошаване след период на подобрение. Трябва да се знае, че ако фибриновата „кръпка" се отлепи и падне, последиците са катастрофални[5]
Още с отварянето на перитонеума се взема течност за оцветяване по Gram и за посявка.
След откриването на перфорационното отверстие се преценява кой е най-добрият метод за затваряне, ръководейки се от принципа, че шевовете трябва да се налагат в нормална тъкан, тоест трябва да се изреже променената калозна тъкан - това определя дали само шев, или ексцизия с шев, или резекция.
СТОМАШНА ЯЗВА Ако един болен е бил лекуван за язвено-пептична болест преди перфорацията, като добавка към надшиването или ексцизията може да се извърши проксимална селективна ваготомия, стига общото състояние да е добро, да няма стеноза и контаминацията да е минимална. В последно време това не се прави, смятайки се, че медикаментозната химическа ваготомия следоперативно е достатъчна. При други обстоятелства е за предпочитане простото надшиване на язвата или ексцизията със сутурата. При перфорация на
стомашна язва, ако контаминацията е минимална и болният е в добро общо състояние, се препоръчва извършването на анатомична антректомия - при стари калозни язви, които силно деформират органа и другите два метода могат да доведат следоперативно до смущение в пасажа[5] ДУОДЕНАЛНА ЯЗВА Повечето перфорации на дуоденума са относително малки и могат да бъдат затворени с двуетажен шев, наложени успоредно на надлъжната ос на дуоденума. Макар и рядко, ръбовете на перфорацията могат да бъдат некротични и тогава се ексцизират. Способът на Graham за оментопексия е рядко приложим, ако изобщо следва да се прилага, и може да бъде рискован, ако се използва при широки перфорации. Състои се в прикрепяне с шевове на оментум на краче над перфорационното отвърстие, без да се прави опит да се съберат или приближат ръбовете му. В около 50% от болните, третирани по този начин, впоследствие се развива стеноза, изискваща реоперация. Когато е налице широка перфорация или дуоденалната стена е ръбцово изменена, което прави трудно надшиването, за препоръчване е изборът между две методики. Едната е да се превърне перфорацията в пилоропластика по Heineke-Miculicz, при което ръбцовите ръбове на язвата се ексцизират. Другата е ексцизията на язвата на дуоденума, като полученият дефект се затваря. Може да се направи серозна "кръпка" посредством повдигане на гънка от проксималния йеюнум (подобен способ е необходим само при извънредни обстоятелства). Независимо от способа на затваряне, се използва оментум на краче за покриване на линията на шевовете. Когато затварянето на дуоденума е незадоволително, т.е. ако се счита, че самото затваряне е причинило стеноза или ако такава е налице отпреди перфорацията, следва да се направи и гастро-йеюностомия. В много рядката ситуация на пълно прекъсване на предната дуоденална стена е много по-лесно да се пререже дуоденумът дистално от язвата и да се премине към антректомия със или без ваготомия[5]
Около 5% от болните след надшиване на перфоративна язва кървят в следоперативния период. Кървенето се дължи най-често на синхронна задна язва (целуващи се язви).
В полза на такава втора язва говори наличието на предоперативна гастроинтестинал -
[www.medmag.bg ] 59
на хеморагия. При все че последната
може да се дължи на самата перфо -
рация, синхронната задна язва тряб -
ва да бъде съответно третирана.
ПЕПТИЧНА ЙЕЮНАЛНА ЯЗВА
Независимо от степента на контами -
нацията и общото състояние, пер -
фориралата маргинална язва (ulcus
pepticum jejuni) следва да бъде тре -
тирана с просто надшиване, стига да
няма стенотично запушване на ана -
стомозата. Интензивното следопе -
ративно противорецидивно лечение
позволява да се спечели време за оп -
ределяне на етиологията на рециди -
ва и да се подбере съответно опера -
тивно лечение в планов порядък[5]
Перфориралата пептична язва на сто -
маха и дуоденума изисква незабав -
но оперативно лечение. Консерва -
тивният метод на Тейлър (аспирация
на стомашното съдържимо през на -
зо-гастрична сонда, антибиотици, на -
блюдение) дава висока смъртност (90-100%) и може да бъде приложен
единствено в случаите на категори -
чен отказ за операция от страна на
пациента. При напреднал перитонит
или тежко състояние на болните (на -
преднала възраст, наличие на тежки придружаващи заболявания) се извършва минимална оперативна намеса - просто зашиване на язвата. В останалите случаи поведението е различно:
- перфорирала калозна язва на стомаха - резекция на стомаха (опасност от пропускане на скрит карцином - 8%, рецидиви след просто зашиване - 40%);
- перфорирала пилорна и препилорна язва - ексцизия с пилоропластика евентуално с ваготомия или последваща медикаментозна ерадикация на ХП (хеликобактер пилори);
- перфорирала дуоденална язва без стеноза или пенетрация - същото
поведение както при пилорните язви;
- перфорирала дуоденална язва със стеноза или с пенетрация – резекция на стомаха.
Доказано е наличието на ХП (хеликобактер пилори) при перфориралата
пептична язва на стомаха и дуоденума в 85 до 95% от случаите. Лечение -
то на перитонита се провежда по установените правила.
Лечението на перфориралата язва може да се извърши лапароскопски в 85% от случаите, което допринася да се избегнат усложненията на срединната лапаротомия. В слу-
чай на сепсис, обаче, създаването на пневмоперитонеум крие рискове от хиперкапния, поради увеличения пермеабилитет на увредения перитонеум и бактериемия - повишеното вътрекоремно налягане води до бактериална транслокация.
Лапароскопският метод при перфорирала пептична язва има същите предимства, както за по-голямата част от лапароскопските процедури - добър козметичен ефект, по-малка по обем тъканна дисекция, по-слаба следоперативна болка, минимална честота на усложненията, ранно завръщане към обичайната активност.
Противопоказания за лапароскопия са високорискови пациенти, масивни интраабдоминални адхезии, напреднал гноен перитонит, хирург с малък опит в лапароскопската хирургия, съмнение за перфорирал рак на стомаха.
ИЗПОЛЗВАНА ЛИТЕРАТУРА:
1. Перфорация и пенетрация на язва. E zdravo tialo
2. Петров А. Язва-Е Фармар
3. Узунова В., Учикова Е., Присадов Г-Ръководство по спешна хирургия- стр.30-36
4. Коцев И. Пептична язвена болест. Е Мedinfo
5. Баев Ст. Перфоративна язва-E My surgery Bg
60 І Medical Magazine | януари 2023
ХИРУРГИЯ



























































































































Център за медицина на съня тел. 0878 67 98 98 www.inspiro.bg Полисомнография, Полиграфия, Актиграфия, СРАР титрация









































































































































































































