НОВОСТИ В ДИАГНОЗАТА НА АТИПИЧНИТЕ ПАРКИНСОНОВИ
СИНДРОМИ
СТР. 18
СПЕЦИАЛИЗИРАНО ИЗДАНИЕ ЗА ЛЕКАРИ

СМЯНА НА ПАРАДИГМАТА ПРИ ЛЕЧЕНИЕ НА ШИЗОФРЕНИЯ СТР. 26
РИТЪМНИ И ПРОВОДНИ
НАРУШЕНИЯ ПРИ СЪРДЕЧНА НЕДОСТАТЪЧНОСТ
СТР. 52
БРОЙ 114 / 07.2023
WWW.MEDMAG.BG БРОЙ 114| 07.2023
НЕВРОЛОГИЯ ПСИХИАТРИЯ
НЕФРОЛОГИЯ КАРДИОЛОГИЯ
НЕВРОЛОГИЯ
ПСИХИАТРИЯ НЕФРОЛОГИЯ КАРДИОЛОГИЯ

редакционен
екип
Изпълнителен директор Главен редактор Отговорен редактор
Редакционна колегия
Изисквания за авторите, желаещи да публикуват
в сп. MEDICAl Magazine
Кристиан Лечев
Проф. д-р Георги Христов
Нели Христова 0894 39 99 50
Проф. д-р Анастас Баталов
Проф. д-р Ваня Юрукова
Проф. д-р Диана Попова
Проф. д-р Диляна Вичева
Проф. д-р Димитър Масларов
Проф. д-р Иван Стайков
Проф. д-р Лъчезар Трайков
Проф. д-р Мери Ганчева
Проф. д-р Милена Станева
Проф. д-р Пенка Илиева
Проф. д-р Петър Петров
Проф. д-р Соня Марина
Проф. д-р Цветомир Димитров
Проф. д-р Цеца Дойчинова
Доц д-р Асен Куцаров
Доц. д-р Аспарух Николов
Доц. д-р Борис Тилов
Доц. д-р Валентин Вълчев
Доц. д-р Весела Карамишева
Доц. д-р Гриша Матеев
Доц. д-р Десислава Тодорова
Доц. д-р Желязко Арабаджиев
Реклама
Разпространение
Предпечат и дизайн
Коректор Фотограф
Печат
Доц. д-р Иван Цинликов
Доц д-р Ирена Велчева
Доц. д-р Любомир Дурмишев
Доц. д-р Мария Атанасова
Доц. д-р Мария Димитрова
Доц. д-р Петко Карагьозов
Доц. д-р Пламен Павлов
Доц. д-р Стоянка Динева
Доц. д-р Тодор Попов
Доц. д-р Цветелина Михайлова
Доц. д-р Христина Видинова
Доц. д-р Цветелина Тотомирова
Д-р Александър Алексиев
Д-р Александър Носиков
Д-р Анелия Гоцева
Д-р Борислав Дангъров
Д-р Диана Димитрова
Д-р Екатерина Куртева
Д-р Иво Димитров
Д-р Ина Генева
Д-р Мария Калинкова
Д-р Силвия Скелина
Петя Дулева adv@medmag bg
0894 399 948
Ивомир Коларов
Даниела Петрова
Ива Лалова
Мартин Минев IFO DESIGN
1. Оригиналните авторски статии да са оформени по следния начин: под заглавието се изписват имената на автора
или авторския колектив с инициали за първо име и пълно -
то фамилно име, с пореден брой цифри Статиите да имат обем до 8 страници, включващи таблиците и илюстрациите, литературните източници и резюметата.
2. Обзорите трябва да имат обем до 8 страници и литературни източници до 20 заглавия
3. Казуистика - клинични случаи трябва да имат обем до
4 страници, без резюме, литературни източници до 10 заглавия
4. Резюметата да съдържат текст на български език - до 200-250 думи и до 6 ключови думи, подредени по азбучен ред
5. Онагледеният материал - таблици, фигури и диаграми да се упоменава в скоби, непосредствено след параграфа, за
който се отнася. Снимковият материал трябва да се представи в оригинал, не по-голям от формат А4 или като файлове с разширение. tif или. jpg, с не по-малка разделителна способност от 150 dpi
Списанието не носи отговорност за автентичността на онагледения материал.
6. В края на статията могат да се изказват благодарности
към съвета, разгледал и подпомогнал оформянето на статията, към научния ръководител, сътрудници, лаборатории и др
7. Книгописът се дава на отделна страница
8. След книгописа се посочва адресът за кореспонденция
- на български език Той трябва да включва пълния пощенски адрес и по възможност телефон за контакт на отговорния автор
Редакционната колегия си запазва правото: да публикува само материали, които счита за подходящи да публикува мнения, становища и въпроси към публикуваните материали
Материалите се рецензират от членовете на редколегията и Редакционния съвет, а при необходимост и от поканени рецензенти
БРОЙ 114
ISSN: 1314-9709
Адрес на редакцията: София 1407, п. к.177, телефон: 02) 868 82 95
Списание Medical Magazine е запазена марка на фирма „Ел Креатив“

ООД. Никаква част от това издание не може да бъде възпроизвеждана и/ или публикувана без изричното писмено съгласие на издателя. e-mail:
Списанието се обработва в БД „Българска медицинска литература " Мненията и изявленията, изложени в материалите, принадлежат на авторите на съответните публикации и не са задължително споделяни от редакционния екип и издателите на списанието. Редакцията на списанието не се обвързва с рекламираните в него продукти, както и не дава гаранция за достоверността на информацията, изложена в съответните реклами, като не носи отговорност по предявени по този повод искания. „Ел Креатив”
Всички материали се изпращат на адрес: office@medmag.bg или
сп Medical Magazine, 1164 София , ул „Плачковица“ 11
www.medmag bg
ООД е собственост на Кристиан Лечев и Петя Лечева. ЮЛИ 2023 ПУБЛИКУВАНЕ НЕВРОЛОГИЯ ПСИХИАТРИЯ НЕФРОЛОГИЯ КАРДИОЛОГИЯ КАРДИОЛОГИЯ
НЕВРОЛОГИЯ
04 РЯДЪК КЛИНИЧЕН СЛУЧАЙ НА
ПАРАНЕОПЛАСТИЧЕН МИОЗИТ
ПРИ ПАЦИЕНТКА С ОВАРИАЛЕН
КАРЦИНОМ
Н. Христов, В. Цветкова, Р. Стоянов, М. Димитрова
09 „МУЛТИДИСЦИПЛИНАРНАТА
РАБОТА Е ОТ ИЗКЛЮЧИТЕЛНО
ЗНАЧЕНИЕ И ТРЯБВА ДА ИМАШ
КОЛЕГИ, НА КОИТО ДА РАЗЧИТАШ“
Разговор с доц. Мария Димитрова, д.м., завеждащ Клиника по нервни болести, УМБАЛСМ "Н. И. Пирогов"
12 КЛИНИЧЕН СЛУЧАЙ НА
24-ГОДИШНА ПАЦИЕНТКА С
ОКЛУЗИЯ НА М2/М3 СЕГМЕНТА
НА СРЕДНА МОЗЪЧНА АРТЕРИЯ-
ВЪЗМОЖНИ ТЕРАПЕВТИЧНИ
ПОДХОДИ
Р. Стоянов, М. Димитрова, М. Петров, Н. Велинов, Н. Габровски
14 РЯДЪК КЛИНИЧЕН СЛУЧАЙ
НА ПАЦИЕНТ С БАКТЕРИАЛЕН
МЕНИНГОЕНЦЕФАЛИТ С
ИЗОЛИРАН ПРИЧИНИТЕЛ LISTERIA
MONOCYTOGENES
И. Балтова, Дж. Башчобанов, В. Цветкова, М. Димитрова
16 „В НАШАТА СТРАНА СА
ВЪВЕДЕНИ СЪВРЕМЕННИТЕ
МЕТОДИ ЗА ДИАГНОСТИКА И
ЛЕЧЕНИЕ НА МОЗЪЧНОСЪДОВИТЕ
ЗАБОЛЯВАНИЯ“
Разговор с доц. Ирена Велчева,
председател на Българска асоциация
по невросонология и мозъчна
хемодинамика
18 НОВОСТИ В ДИАГНОЗАТА НА
АТИПИЧНИТЕ ПАРКИНСОНОВИ
СИНДРОМИ
М. Клисурски
ПСИХИАТРИЯ
26 СМЯНА НА ПАРАДИГМАТА ПРИ
ЛЕЧЕНИЕ НА ШИЗОФРЕНИЯ
Е. Хараланова, Св. Хараланов
30 ПСИХОФАРМАКОТЕРАПИЯ:
КРОС-КУЛТУРАЛНИ И ЕТНИЧЕСКИ СЪОБРАЖЕНИЯ А. Бешков, П. Въргов, К. Акабалиева, В. Акабалиев
34 ТРЕВОЖНИЯТ СИНДРОМ - НАЙЧЕСТО СРЕЩАНОТО, НО И НАЙНЕСПЕЦИФИЧНОТО ОПЛАКВАНЕ В АМБУЛАТОРНАТА ПСИХИАТРИЯ М. Ганчев НЕФРОЛОГИЯ
СЪДЪРЖАНИЕ
38 РОЛЯ НА МАСТНОРАЗТВОРИМИТЕ ВИТАМИНИ ПРИ ПАЦИЕНТИ НА ДИАЛИЗНО ЛЕЧЕНИЕ Б. Борисов
КАРДИОЛОГИЯ
42 КЛИНИЧЕН СЛУЧАЙ НА ФУЛМИНАНТЕН МИОКАРДИТ С БЛАГОПРИЯТЕН ИЗХОД СЛЕД ИМУНОСУПРЕСИВНО ЛЕЧЕНИЕ Г. Господинова, И. Даскалов, Л. Демиревска
46 ЛЕЧЕНИЕ НА АРТЕРИАЛНАТА ХИПЕРТОНИЯ: ПРЕПОРЪКИ В ПРАКТИКАТА НА СПЕЦИАЛИСТА КАРДИОЛОГ Л. Золумова, И. Желева, В. Гелев
52 РИТЪМНИ И ПРОВОДНИ
НАРУШЕНИЯ ПРИ СЪРДЕЧНА НЕДОСТАТЪЧНОСТ К. Костов
56 АОРТО-КОРОНАРЕН БАЙПАС
С ПОВЕЧЕ ОТ ЕДИН АРТЕРИАЛЕН
ГРАФТ - ОПИТЪТ НА „АДЖИБАДЕМ
СИТИ КЛИНИК“ - СОФИЯ
В. Янчева, А. Неутов, С. Казаков, С. Иванова, А. Келчев
2 І Medical Magazine | юли 2023
СЪДЪРЖАНИЕ

Н. Христов¹,² , В. Цветкова² , Р. Стоянов² , М. Димитрова² ¹Медицински университет – София
²Клиника по нервни болести, УМБАЛСМ
„Н. И. Пирогов“ – София
Рядък клиничен случай на
паранеопластичен миозит при
пациентка с овариален карцином
Паранеопластичният синдром засяга по-малко от 1% от пациентите с онкологични страдания. Цел: Да се представи рядък клиничен случай на паранеопластичен миозит при пациентка с овариален карцином и да се направи литературна справка за поведението в такива случаи. Клиничен случай: Касае се за пациентка на 54 г., хоспитализирана с оплаквания от болки в мишниците и болка в двете бедра до силно затруднена походка. Оплакванията са се появили няколко дни преди реоперация по повод на овариален тумор (първата интервенция 2016 г.). Проведоха се диференциално-диагностични изследвания, които отхвърлиха да се касае за друга причина и се прие диагнозата паранеопластичен миозит. Назначи се лечение с кортикостероид по схема със значително подобрение на симптомите. Заключение: Паранеопластичният полимиозит протича със същата клинична картина като полимиозита без карцином, което значително затруднява диагнозата при пациенти с непроявено онкологично страдание до момента.
ВЪВЕДЕНИЕ
Паранеопластичният синдром засяга по-малко от 1% от пациентите с онкологични страдания. Появата на паранеопластичен синдром може да предшества или да се появи по време на диагностициране и лечение на тумора. Миозитът протича най-често със слабост, подуване и болка. Диагнозата на паранеопластичен синдром с неврологично засягане изисква скрининг за подлежащо злокачествено заболяване, включително пълна анамнеза, физикален преглед и образни изследвания. Лечението често води до стабилност на симптомите, вместо до подобрение. Неврологичните симптоми могат да персистират дори след лечението на злокачественото заболяване.
Полимиозитът принадлежи към хетерогенна група автоимунни заболявания, наречени инфламаторни
мио патии, които се характеризират със слабост на проксималната
скелетна мускулатура, кожни прояви, повишена активност на серум -
ната креатинкиназа и възпалителни клетки в мускулния биоптат. Полимиозитът е клетъчно-медиирано автоимунно заболяване[1]. Първата докладвана връзка между злокачествено заболяване и миозит е направена от Stertz G et al през 1916 г.[2]. Докладваната честота на възпалителен миозит варира от 0.5 до 0.89 на 100 000 на година[3]
Проучванията показват, че съпътстващи заболявания като белодробна фиброза, дисфагия, тежест на мускулното заболяване, стадий на тумора и възраст на пациента влияят върху прогнозата на пациенти с възпалителен миозит. Възпалителната миопатия може да продължи или да стане очевидна след диагностицирането на злокачествено заболяване. Клиничното изражение на паранеопластичния полимиозит е същото
като това на полимиозит без рак[4]
Полимиозитът се диагностицира
чрез използването скоростта на утаяване на еритроцитите и серумните нива на мускулните ензими, заедно с
миогенните признаци на електромиография[4]
Имунната дисфункция е централна за патофизиологията, лежаща в основата на паранеопластичния синдром. Имунологичен отговор се предизвиква от ектопичната експресия на вътре- или извънклетъчни невронни антигени от тумора[5], което води до кръстосана реактивност между туморните клетки и компонентите на нервната система. Това създава антитуморни антитела и свързани онконевронални антиген-специфични Т лимфоцити, които атакуват нервната система, предизвиквайки неврологични симптоми.
ЦЕЛ
Да се представи рядък клиничен случай на паранеопластичен миозит при пациентка с овариален карцином и да се направи литературна справка за поведението в такива случаи.
МАТЕРИАЛИ И МЕТОДИ
Касае се за пациентка на 54 г., хоспи -
4 І Medical Magazine | юли 2023
НЕВРОЛОГИЯ
тализирана с оплаквания от болки в мишни -
ците и болка в двете бедра до силно затруднена походка. Болката ирадиира към двете
рамена и плешки. Оплакванията са с давност
около 2 седмици, съпроводени от слабост
и лесна уморa, по-изразени за горни крайници. Оплакванията са се появили няколко
дни преди реоперация по повод на овариален тумор (първата интервенция 2016 г.). По
време на пролежаването в гинекологично
отделение оплакванията прогресират. Хистологичната находка кореспондира с умеренодиференциран аденокарцином на яйчника. Проведен МРТ на шия с начални дегенеративни промени. При постъпването в неврологично отделение обективно пациентката е с проксимална мускулна слабост, по-изразена
в горни крайници, с оток на двете предмишници. Проведени с оглед диференциална ди -
агноза: лумбална пункция с данни за нормален белтък без наличие на клетки, с което се отхвърли възпалителна генеза на оплакванията, КТ на гръден кош и корем - без патологични промени, предимно с цел да се изключи вторична дисеминация на процеса и наличие на vena cava superior syndrome, предвид анамнезата за оток в областта на раменния пояс. От проведено ЕМГ има данни за миогенна увреда.
От параклиниката се установи наличие на високи стойности на креатинфосфокиназа (6551 U/L) и миоглобин (800.2 mg/l), както и маркери за възпаление (С-реактивен протеин – 5.65 mg/l и СУЕ – 75 mm/h). Изследва се паранеопластичен и миозитен панел, чиито резултати позитивираха анти-Ro 52 антитяло.
Започна се терапия с кортикостероид (Urbazone) в доза 60 mg (1 mg/kg), НСПВС (Dexofen) i.v. – 50 mg/ден, антибиотик (Medaxon) в доза 2 х 2 g/ден, Н2-рецепторен блокер (Quamatel), вливания с водно-солеви разтвори, ниско-молекулен хепарин (Clexane) в доза 0.4 ml (40 mg), хепатопротектори –Transmetil в доза 2 х 500 mg и HepaMerz в доза 2 х 1 амп. с добър клиничен ефект. След дехоспитализацията пациентката беше представена на онкологична комисия за последваща химио- и лъчетерапия, назначена терапия с перорален кортикостероид по схема в намаляваща доза и гастропротектор.
ОБСЪЖДАНЕ Систематичен преглед на литературата прави връзка между дерматомиозит (ДМ), по -
лиомиозит (ПМ) и карцином на яйчниците. Според резултатите от това проучване заболяванията в повечето случаи съществуват едновременно и трябва да се обмисли пълен скрининг за овариален карцином при пациенти с миозит. Въпреки че броят на статиите, включени в проучването не е голям, броят на пациентите, които са изследвани е значителен, в сравнение с епидемиологичните данни
за миозит и съпътстващ овариален карцином в литературата[6].
В проучване на Cherin et al., при 76 жени миозитът се проявява първо, в сравнение с 36 пациентки с рак на яйчниците, които по-късно са диагностицирани с паранеопластичен дерматомиозит или полиомиозит. Диагнозата се основава на клиничните характеристики и повишената серумна креатинин киназа, която има средни стойности от 886 U/l, както и наличието на автоантитела, които са открити положителни при 25 жени.
Независимо от напредналия стадий, по-голямата част от пациентите 78 (70.9%) са лекувани чрез хирургично лечение, последвано от химиотерапия или лъчетерапия при 64 от тях (58.2%), докато останалите пациенти са лекувани основно с химиотерапия, самостоятелно или с последваща операция. Tembe et al. в проучване на 10 пациенти с паранеопластичен ДМ и ПМ, съобщава за 3 случая с овариален аденокарцином в напреднал стадий, всички лекувани с химиотерапия, които изискват терапия след лечението с комбинация от метотрексат, азатиоприн и стероиди[7]
Последните клинични указания показват в допълнение към нивата на Ca-125, преглед на таза и трансвагинален ултразвук на всеки 6–12 месеца в продължение на 2–5 години след поставяне на диагнозата дерматомиозит[8]. Независимо от това, трябва да се направят по-големи проучвания, за да се формират универсални насоки по отношение на скрининга за рак при пациенти със ДМ/ ПМ.
Hong et al., 2015 и Nakanishi et al., 1999, докладват за 35 случая на паранеопластичен миозит, появил се след овариален карцином, повечето от които са лекувани хирургично, или с първично отстраняване на обема, или с двустранна салпингооофоректомия. Миозитът протича паралелно на рака на яйчниците.
Пълното отстраняване на тумора обикновено
[www.medmag.bg ] 5
води до подобряване на симптомите и биомаркерите на миозита.
Според публикуваните доклади, ди -
агнозата рак на яйчниците се поста -
вя малко след диагностицирането на
миозит. След диагностицирането на
миозит рискът от диагностициране -
то на рак на яйчниците е 16.7% през
следващите 5 години (Sigurgeirsson et al., 1992). Един случай съобщава за
рак на яйчниците, диагностициран 6
години след откриването на миозит (Scheinfeld, 2008). С увеличаване на
интервала от време между двете ди -
агнози става все по-трудно да се раз -
граничи първичният от паранеоплас-
тичния миозит.
По-голямата част от пациентите са
лекувани с курс стероиди, които ми -
нимално подобряват слабостта и
болката, и при които се установяват
двустранни образувания на яйчници -
те при проведени графии.
Паранеопластичният миозит обик-
новено е резистентен на класическа -
та терапия за лечение на миозит и
обикновено ремитира, само когато подлежащото злокачествено заболяване е лекувано.
Според доклад на P-O Carstens, J Schmidt, лечението започва с пулсова интравенозна терапия с глюкокортикостероиди, в дози 250–1000 mg
преднизолон на ден за 3–5 дни (Фиг. 1). Последващата стандартна перорална терапия се състои от преднизон 1 mg/kg/ден. Тази доза обикновено се прилага най-малко 4 седмици.
След първоначално стабилизиране,
което може да отнеме 4-12 седмици, дозата може да се титрира на все -
ки 1 или 2 седмици с 10 mg до дос -
тигане на 20 mg/ден. Впоследствие
дозата се намалява до достигане на
поддържаща терапия от 5 mg/ден.
Терапията се основава на предиш -
ни доклади, предполагащи положи -
телен ефект на кортикостероидите
върху мускулната сила[9], въпреки че
тези ефекти никога не са били офи -
циално доказани в проспективно двойно-сляпо проучване. Степента
на намаляване на дозата зависи от отговора на пациента и в случай на екзацербация намаляването трябва да бъде прекратено или забавено, или дори дозата да бъде увеличена. Алтерниращият дневен режим може да помогне за намаляване на страничните ефекти. Месечните 4-дневни курсове с 40 mg дексаметазон като „перорална пулсова терапия“ показват ефикасност, сравнима с ежедневния прием на преднизон, но със значително по-малко странични ефекти[10]. Рискът от фрактура се повишава при терапия с преднизон в дневна доза над 5 mg или с продължителност над 3 месеца. Препоръчва се съпътстващо лечение с 1000 mg калциев карбонат и 500 IU витамин D на ден[11]. Индуцираната от стероиди миопатия е важен страничен ефект на глюкокортикостероидите, с бавно прогресираща проксимална мускулна слабост, която може да имитира рецидив[12]. Остри промени в ЕМГ обикновено се очакват при рецидив
и могат да помогнат за разграничаването на едното от другото.
Допълнителна имуносупресив -
на терапия може да започне едновременно, освен ако не са налице леки симптоми. Това лечение налага прилагането на по-малка доза преднизон. Шест проучвания сравняват терапията с имуноглобулин (IVIG), етанерцепт, екулизумаб, инфликсимаб, азатиоприн или левкофореза с плацебо, като значително подобрение на мускулната сила е установено само за IVIG. Други четири проучвания сравняват ефекта от две имуносупресивни терапии и не е открита статистически значима разлика. Може да се обобщи, че няма убедителни доказателства за ефикасността на често използваните имуносупресивни средства при миозит като метотрексат (MTX), азатиоприн и микофенолат мофетил (MMF). Въпреки това, с оглед на имунопатогенезата, международен консенсус от експерти препоръчва използването на имуносупресори. Необходими са повече проспективни и контролирани проучвания с
подходящ размер на кохортата.
IVIG може да се използват като алтернатива, когато страничните ефекти от имуносупресорите превишават тяхната клинична полза. Може да се използват и като допълнително лечение по време на рецидив или когато имуносупресорите не са достатъчно ефективни. В допълнение, IVIG са възможност за лечение, когато не е желана имуносупресия, напр. при жени в детеродна възраст или при юноши. Обикновено първоначално се прилага обща доза от 2 g/ kg. Терапията се повтаря редовно на всеки 4–8 седмици с доза от 1 g/kg, като постепенното намаляване зависи от ефекта от лечението. Съответните странични ефекти са повишен риск от тромбоза, треска и алергични реакции/анафилаксия[13]. Рискът от алергична реакция е повишен при пациенти с дефицит на имуноглобулин (Ig)A, който трябва да се изключи преди започване на лечението. Жените с детероден потенциал могат да бъдат лекувани с IVIG като безопасен вариант[14]. MTX, азатиоприн и MMF са потенциално тератогенни, което прави ефективната контрацепция от съществено значение[15] Бременност не трябва да се планира преди спиране на имуносупресорите за няколко месеца, тъй като активните метаболити могат да персистират в тъканите в продължение на няколко седмици[16]
Други вещества, като циклоспорин или циклофосфамид, се използват по-рядко, отчасти поради по-високия риск от странични ефекти. Въпреки това, тези лекарства могат да бъдат много полезни за ескалираща терапия при отделни пациенти, особено когато всички други лечения са неуспешни.
Въз основа представения клинични данни пациентите са лекувани с 1 mg/kg перорален преднизон дневно. При подобрение, напр. след 6-8 седмици дозата се намалява бавно и се включва азатиоприн от 50-150
6 І Medical Magazine | юли 2023 НЕВРОЛОГИЯ
При липса на ефект/ влошаване:
• Rituximab
• Cyclophosphamide
mg/ден. MMF и MTX се приемат за втори или трети избор, напр. в случай на странични ефекти от азатиоприн. Ако лечението само с някое от тези лекарства е неефективно, допълнително се прилагат интравенозни имуноглобулини. Възможностите за ескалация на лечението включват блокада на CD20 с ритуксимаб или максимална имуносупресия с циклофосфамид.
Допълнителна/ алтернативна терапия:
• IVIG – 1 g/kg на всеки 4-8 седм.
• Cyclosporine – 150 mg/ден
Имуносупресивна терапия, напр. в комбинация с Prednisone:
• Methotrexate 10-20 mg/седм.
• Azathioprine 2-3 x 50 mg/ден
• Mycophenolate mofetil 2 x 0.5-1 g/ден
Терапия с Prednisone:
• 1 mg/kg до стабилност, напр. 4-12 седм. или повече
• Първоначална интравенозна пулсова терапия с 0.5-1 g/ден за 3-5 дни
• Редукция с 10 mg на всеки 1-2 седм.; от 20 mg/ден титрирането е забавено
до 2.5-5 mg/ден в рамките на 1-2 седм.
• Поддържаща доза от 5 mg/ден често е необходима
Фиг. 1. Лечение на дерматомиозит, полимиозит и некротизираща миопатия. Дозата трябва да се адаптира за всеки отделен случай. Адаптирано от Schmidt J, Vorgerd M. Standard treatment for myositis and muscular dystrophies. Nervenarzt 2011; 82:723–732, с разрешение на Springer Science and Business Media
1. Buchbinder R, Forbes A, Hall S et al.. Incidence of malignant disease in biopsyproven inflammatory myopathy. A population-based cohort study. Ann Intern Med 2001; : 1,087–1,095.
2. Stertz G. Polymyositis. Berl Klin Wochenschr 1916; : 489.
3. Christie A, McKay N, Nussey F. Dermatomyositis as presenting feature of ovarian cancer, treated with neo-adjuvant chemotherapy and interval debulking surgery. Gynecol Oncol Case Rep 2013; : 13–15.
4. Croce S, Guèye M, Korganow AC et al..
ЗАКЛЮЧЕНИЕ Паранеопластичният полимиозит протича със същата клинична картина като полимиозита без карцином, което значително затруднява диагнозата при пациенти с непроявено онкологично страдание до момента. Проведени са проучвания за наличието на анти-Ro 52 антитела при пациентки с овариални карциноми и се описва, че наличието им се свързва благоприятна прогноза за лечението на заболяването. Този случай илюстрира сложността, свързана с бързата диагностика на необичаен случай на паранеопластичен полимиозит. Ключов момент в представения случай е необяснимият случай на миозит при възрастен, който трябва да повдигне подозрение за връзката на миозит със злокачественото заболяване, което изисква подробен мултидисциплинарен подход. Развитието на миозит като паранеопластичен синдром може да бъде синхронизирано с подлежащото злокачествено заболяване или да се появи месеци до години преди клиничната проява на рак.
Paraneoplastic polymyositis associated with breast cancer: a therapeutic emergency. Breast Cancer Res Treat 2011; : 811–814.
5. de Beukelaar JW, Sillevis Smitt PA. Managing paraneoplastic neurological disorders. Oncologist 2006; : 292–305.
6. Trallero-Araguás E, Rodrigo-Pendás JÁ, Selva-O’Callaghan A, et al.. Usefulness of anti-p155 autoantibody for diagnosing cancer-associated dermatomyositis: a systematic review and meta-analysis. Arthritis Rheum 2012; 64: 523-532
7. Tembe AG, Ramteke S, Joshi VR,
Balakrishnan C. Dermatomyositis/ polymyositis associated with malignancy: our experience with ten patients and review of relevant literature. Int J Rheum Dis 2008;
11: 269-273.
8. Field C, Goff BA. Dermatomyositis–key to diagnosing ovarian cancer, monitoring treatment and detecting recurrent disease: Case report. Gynecol Oncol Rep 2017; 23: 1-3.
9. Micks RH, Mullaney J. Dermatomyositis successfully treated by prednisone. Ir J Med Sci 1958; 33:333–334.
10. van de Vlekkert J, Hoogendijk JE, de
Haan RJet al. Oral dexamethasone pulse therapy versus daily prednisolone in subacute onset myositis, a randomised clinical trial. Neuromuscul Disord 2010; 20:382–
389.
11. Pereira RM, Carvalho JF, Paula APet al. Guidelines for the prevention and treatment of glucocorticoid-induced osteoporosis. Rev Bras Reumatol 2012; 52:580–593.
12. Batchelor TT, Taylor LP, Thaler HT, Posner JB, DeAngelis LM. Steroid myopathy in cancer patients. Neurology 1997; 48:1234–1238.
13. Nydegger UE. Safety and side effects of i.v. immunoglobulin therapy. Clin Exp Rheumatol 1996; 14 (Suppl. 15):S53–S57.
14. Lidar M, Langevitz P. Pregnancy issues in scleroderma. Autoimmun Rev 2012; 11:A515–A519.
15. Makol A, Wright K, Amin S. Rheumatoid arthritis and pregnancy: safety considerations in pharmacological management. Drugs 2011; 71:1973–1987.
16. Ostensen M, Forger F. Management of RA medications in pregnant patients. Nat Rev Rheumatol 2009; 5:382–390.
[www.medmag.bg ] 7
ЛИТЕРАТУРА:
ИЗПОЛЗВАНА
изключително
и трябва да имаш колеги, на които да разчиташ“
Разговор с доц. Мария
Доц. Димитрова, моля представете Отделението по Нервни болести, което завеждате.
Отделението по нервни болести до 2018 г. е съществувало с предимно
консултантивна дейност. През 2018 г.
структурата се трансформира и заработи с изцяло нов екип за работа със спешни неврологични състояния и не само. Създаването на тази органи -
зация съвсем не беше едноетапно и
лесно, а беше процес от набиране на
лекари и сестри, създаване на спе -
шен неврологичен кабинет, обуче -
ние на специализанти, обучение на
целия екип да действа при спешни
неврологични състояния и особено при пациенти с остри инсулти, създа -
Доц. д-р Мария Димитрова завършва медицина през 2007 г. През 2008 г. след конкурс е зачислена за специализант клинична ординатура в Клиника по нервни болести на Военномедицинска академия. Придобива специалност по нервни болести през 2013 г. През 2018 г. защитава дисертационен труд на тема „Невропсихологични нарушения при обструктивна сънна апнея“ с научен ръководител проф. Красимир Генов. От 2018 г. е началник на Отделение по нервни болести в УМБАЛСМ "Н. И. Пирогов". От 2021 г. е доцент по нервни болести. Работи в областта на невросонологията. Член на БЛС, Българско дружество по неврология, Българска асоциация по невросонология и мозъчна хемодинамика, Българско дружество по сомнология, европейски неврологични асоциации. Автор на монографията "Диагностични и терапевтични подходи при криптогенен мозъчен инсулт" и на редица публикации в български и международни периодични издания.
ване на център за лечение на инсулти. За щастие, за по-малко от 5 години успяхме да съберем и да обучим един добър екип и съм много благодарна на хората, които ми повярваха. Вече имаме 18 лекари, за този период първите ни лекари-специализанти завършиха курса си на обучение и успешно положиха изпита си за специалност, така че вече можем да се похвалим с първите специалисти невролози, обучавани в Пирогов. Преди броени дни, с новото разрешение за лечебна дейност, Отделението по нервни болести се трансформира в Клиника по нервни болести с две отделения - общо и интензивно. Бих казала, че съм много доволна от по -

стигнатото, но то е само основата за бъдещите ни планове.
С какви патологии се срещате в ежедневната си дейност най-често? Разкажете ни за някой рядък случай. Естеството на работа на лечебното заведение, като спешен център, предполага да се акцентира на спешната неврологична патология. Основната патология е остри нарушения на мозъчното кръвообращение. Такова беше очакването при създаването на Отделението, да се създаде център за лечение на мозъчни инсулти. Лекуваме и пациенти с епилепсия, възпалителни заболявания на ЦНС -
8 І Medical Magazine | юли 2023
„Мултидисциплинарната работа е от
значение
Димитрова, д.м., завеждащ Клиника по нервни болести, УМБАЛСМ "Н. И. Пирогов"
НЕВРОЛОГИЯ
менингити, енцефалити, енцефалопатии, миастения и миастенни кризи, остри полиневропатии - тип синдром на Гилен-Баре.
Всеки лекар има случаи, които помни. И нашият екип има емблематични казуси, такива, за които сме се чували денонощно и сме
вложили много енергия, пък и страх какъв ще бъде изходът. За мен, а и за всички нас, за -
помнящ ще си остане един млад мъж с тромботична тромбоцитопенична пурпура, синдром на Мошковиц. Много рядко заболяване, което за първи път клинично се изяви с неврологична симптоматика, което също е рядко. Всичко беше голямо предизвикателство, от поставянето на диагнозата, през лечението с плазмафереза, в което се наложи да се включат колеги от Националната болница по хематология до изхода от лечението. Буквално за един ден трябваше да се организираме, апаратурата от хематологията беше докарана
с фирма за хамалски услуги, колегите хематолози бяха изключително съдействащи. Статистически голям процент от пациентите за -
гиват, но нашият пациент оцеля след месеци
в реанимация и неврология. Ще представим
и един случай в този брой на Вашето списа -
ние на 24-годишна жена с инсулт, в този слу-
чай съвместно работихме с ендоваскуларния
екип от Клиника по неврохирургия. Няколко
дни всички бяхме ангажирани денонощно с
тази млада жена, но я изписахме без дефи -
цит. Като цяло, винаги най-страшно е, когато сериозни заболявания се случват на мла -
ди хора, когато състоянието е статистически неочаквано. Но има и друго важно в такива случаи, мултидисциплинарната работа е от изключително значение и трябва да имаш колеги, на които да разчиташ.
Как е организирана работата Ви в структурата на най-голямата болница за спешна помощ и с кои Отделения най-често сте в колаборация?
В спешната болница кипи живот и активност 24∕7. В спешното отделение има пациенти, консултации и динамика. Има триажна зала, в която младите колеги дават разположения.
В спешното звено е мястото, където трябва да се прецени възможно най-бързо как да се менажира всеки болен, накъде да се насочи пациентът, за да му се помогне най-бързо и най-добре. Това е добра възможност, особено за младите колеги, да добият опит и увереност, да вземат решения бързо, да видят случаи, които рядко се виждат. „Пирогов“ е
болница с денонощна образна диагностика и лаборатория, което е от изключително значение за диагностиката на пациентите. Огромна подкрепа имаме от колегите от образна диагностика, непрекъснато се чуваме, обсъждаме пациентите. Като център за специфично лечение за инсулти, повече си сътрудничим със структурите, ангажирани в посока на диагностика, уточняване и лечение на съдови заболявания. Поради това естество на работата, най-често си колаборираме с Клиниката по неврохирургия и особено с ендоваскуларния екип, доц. Николай Велинов и д-р Михаил Петров. Много добра комуникация имаме и с Клиниката по кардиология, пациентите с мозъчно-съдови заболявания подлежат задължително на кардиологична оценка. Разкажете повече за организацията на работа по отношение на мозъчните инсулти и т.нар. „златен час“. Лечението на исхемичните инсулти бива специфично с интравенозна тромболиза и ендоваскуларно лечение до 6-ти час от началото на симптомите и неспецифично - след това време. Затова е изключително важно да се бърза, от вземането на пациента от дома му до обработването му в болницата, като тези времена се оценяват, използвайки показате -
ли като време „врата до игла“, време „врата до пункция“. В УМБАЛСМ имаме възможност да проведем специфично лечение на нашите болни и функционира т.нар. Stroke unit. Екипът ни е обучен, проследяваме количествени и качествени показатели, които Европейската асоциация по инсулти е определила. Данните се въвеждат в регистъра RES-Q от центрове от Европа. В последната една година успяхме да покрием критериите за сертифициране. Преминахме през златен статут в началото, а вече имаме платинен статут по програмата Angels на ESO. Това означава, че над 15% от пациентите с инсулти, които постъпват при нас са лекувани с тромболизи и ендоваскуларно лечение, като тези пациенти са обработени в болничното заведение много бързо и са направени всички необходими диагностични процедури да се уточни причината за инсулта. Въпреки тези резултати, мога да отбележа, че статистиката изобщо не е добра, броят на пациентите, лекувани специфично в България остава много нисък, сравнено със статистиката по света.
Вие сте сертифициран специалист по невросонология и работите в областта на сом -
[www.medmag.bg ] 9
нологията. Оказва се, че между 20 и 30% от населението на света страда от нарушения на съня - доказани рискови фактори за заболявания като инфаркти и инсулти. Изключително важно е да се уточняват рисковите фактори за инсулти.
Ние си имаме алгоритъм за диагностициране на причината за инсулта при нашите пациенти. Невросонологичното изследване на каротидни и вертебрални артерии е сред
първите и най-важни изследвания.
Сред рисковите фактори за инсулт
са и дихателните нарушения по време на сън, като обструктивната сън -
на апнея, например. При съмнение
за такъв фактор провеждаме респираторна полиграфия или полисомнография според показанията.
Какво можете да споделите по отношение на терапията на проблеми като безсънието и синдрома на неспокойните крака, например. Има ли достатъчно „арсенал“ за повлияването им?
Безсънието е изключително тежък социален проблем, доста често се среща, за съжаление. Най-страшното е, че се нарушава функционирането на пациентите през деня, трудно се справят с дейностите си. Много е трудно за лечение и повлияване понякога. В повечето случаи е уместно в лечението да се включи и психиатър, особено когато безсънието е вследствие на тежки депресивни симптоми. Синдромът на неспокойните крака и другите двигателни нарушения по време на сън са състоя -

ния, които доста често съпътстват налични полиневропатии или някои соматични заболявания. Лечението е с допаминергични медикаменти и пациентите получават облекчение.
На изминалия XXII Конгрес по неврология имаше забележимо присъствие от Отделението Ви със значителен брой представени Клинични случаи в постерната сесия. Поздравления! Бихте ли споделили Вашите впечатления от дните на Конгреса?
Националният конгрес е мястото, на което се събират специалистите от цялата страна, най-мащабното неврологично събитие. И наистина е важно да се представи работата, която е свършена през изминалата годи -
10 І Medical Magazine | юли 2023 НЕВРОЛОГИЯ
на. Ние представихме някои клинични случаи от практиката, както и две проучвания за резултатите от проведените тромболизи и ендоваску-
ларно лечение за период от една година. В последните години имаме студенти, които работят при нас като болногледачи и им даваме възможности да направят първи стъпки в подготовката и представянето на постерна презентация. Работата на д-р Грънчарова и д-р Кади беше отличена с грамота. Освен, че представихме нашия труд, чухме и представянията на колегите, което си е безценна обмяна на опит.
Какви са новостите от изминалото събитие по отношение на диагностиката, терапията и превенцията
на социално-значимите неврологични заболявания?
Има новости всяка година, както и гостуващи чуждестранни лектори. За поредна година гостува проф. Коми, който е сред най-изтъкнатите специалисти в сферата на диагностиката и лечението на множествена склероза. Проф. Коми представи нови медикаменти за лечение на множествена склероза и резултати от проучвания за вече познати медикаменти.
За мен изключително интересно беше представянето на медикамента efgartigimod за лечение на миастения гравис, който се очаква в България в началото на следващата година, което беше направено от акад. Миланов
и проф. Григориадис. Друг нов медикамент, Римегепант, имаме за лечение на мигрена, който е различен от досегашните медикаменти по това, че може да се използва и за профилактика и за пристъп на заболяването. Имаше и много други презентации, винаги може да се чуе и научи нещо ново.
Нещо, което желаете да споделите с читателите на списанието?
Работата на медика не е работа за индивидуалисти. Много е важно да имаш екип, на който да разчиташ
и си мисля, че най-важното е да се стараем да се ображдаме с мислещи и търсещи хора. Аз имам такива около себе си и наистина много се радвам.

[www.medmag.bg ] 11
Р. Стоянов¹, М. Димитрова¹, М. Петров², Н. Велинов², Н. Габровски²
¹Клиника по нервни болести, УМБАЛСМ "Н. И. Пирогов" – София
²Клиника по неврохирургия, УМБАЛСМ "Н. И. Пирогов" - София
Клиничен случай на 24-годишна
пациентка с оклузия на М2/М3
сегмента на средна мозъчна артериявъзможни терапевтични подходи
Въведение: Мозъчният инфаркт (МИ) е остро разстройство на мозъчното кръвообращение. Интравенозната тромболиза и ендоваскуларното лечение са златен стандарт в лечението на пациентите с остри исхемични инсулти. Исхемичният мозъчен инсулт според СЗО е една от най-честите причини за заболеваемост и смъртност в световен мащаб. Всяка година около 15 000 000 милиона души по света получават исхемичен мозъчен инсулт. За успешното му лечение е необходима спешна хоспитализация, незабавно започване на диференциращо лечение. Цел: Да се представи рядък случай на пациент в млада възраст с исхемичен мозъчен инсулт извън терапевтичен прозорец за провеждане на интравенозна тромболиза с проведена интраартериална тромболиза с пълно обратно развитие на неврологичната симптоматика, както и да се направи обзор на възможните терапевтични подходи за лечението в рамките на времевия прозорец и възможностите на интраартериалната тромболиза.
КЛИНИЧЕН СЛУЧАЙ
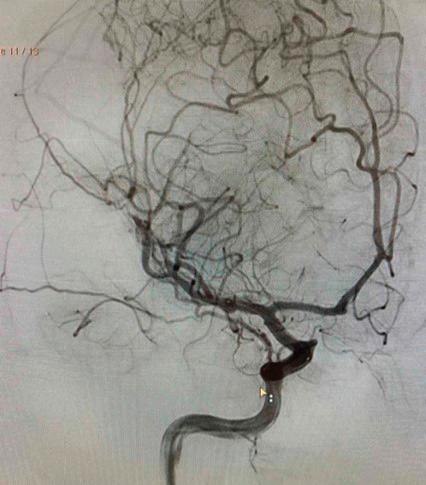
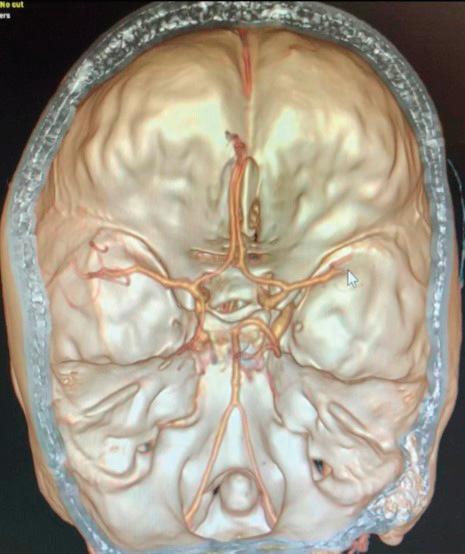
Пациентка на 24 години, постъпила по спешност по повод на оплаквания от нарушение на говора. Без анамнеза за придружаващи заболявания. При прегледа се установява левостранна централна хемипареза с участието на VII, XII КН вляво и левостранна хемихипестезия. След направен КТ на глава с КТ-ангиография (Фиг. 1) се установи оклузия на М2/М3 сегмента на церебри медия в дясно, без данни за исхемични промени.
Пациентката беше с противопоказа -
ние за провеждане на интравенозна тромболиза, начало на симпто -
матиката преди повече от 4.5 ч., но с установена оклузия на ДСМА. Пора -
ди това пациентката бе консултира -
на с интервенционален неврохирург.
След клинично обсъждане се прецени, че подлежи на конвенционална ангиография и след потвърждаване на оклузията на М2-М3 сегмент се премина към интраартериална тром -
болиза в спешен порядък. При NIHSS – 7 т., стабилна хемодинамика, АН110/70 mmHg, INR - 1.26 се проведе
интервенционално лечение с Актилизе 6 mg и.а.
Контролната конвенционална ангиография показа частична реканализация на М2-М3 сегмент TICI II А (Фиг. 2 и 3).
Пациентката понесе добре проведената процедура. Контролният КТ на главен мозък показа исхемични промени в басейна на дясната СМА темпорално и базално. Проведоха се изследвания с оглед уточняване на рисков фактор за исхемичен инсулт в млада възраст: ехокардиография с данни за междупредсърден дефект; скрининг за тромбофилия с данни за понижени нива на протеин С (43.9%) и леко завишени стойности на хомоцистеин (12.8 umol/l). Понижени нива на протеин C се свързват по-често с БТЕ, но при млади лица се срещат артериални исхемични събития (вкл. ИМИ). Пациентката се изписа с подобрение. NIHSS - 0 т.
ОБСЪЖДАНЕ
Постигнат е голям напредък в превенцията, лечението и рехабилитацията на инсулта. За пример, тромбо -
литичната терапия може да ограничи степента на неврологичното увреждане от исхемичен инсулт, но наличното време за лечение е ограничено. Съгласно действащите консенсуси за лечение на ИМИ, тромболизата може да бъде извършена при остър исхемичен инсулт в рамките на 4.5 часа, като съществуват абсолютни и относителни противопоказания за провеждането й. Механичната тромбектомия се препоръчва при исхемичен инсулт в рамките на 6 часа от „последното известно добре“. За осъществяването й се използват стент ретриивъри. При някои условия до 24 часа от последната известна норма. Интраартериалната тромболиза се осъществява чрез въвeждане на тромболитика или в самия тромб, или проксимално от него.
Според Националния консенсус за профилактика и лечение на мозъчно-съдови заболявания, интраартериалната тромболиза:
• се прилага само при подбрани пациенти с големи исхемични ин -
12 І Medical Magazine | юли 2023
НЕВРОЛОГИЯ
султи с давност под 6 часа, предизвикани от оклузия на средната мозъчна артерия (клас I, ниво B-R).
• алтернатива е при пациенти, които имат противопоказания за прилагане на интравенозна тромболиза, като скорошна оперативна интервенция (клас IIb, ниво C).
• препоръчва се при пациенти с
остра базиларна оклузия до 6-ия
час от нейното възникване (клас III, ниво B).
• rtPA няма одобрени дози за интраартериално приложение и
се препоръчва само при болни, включени в международни мултицентрови проучвания или национални програми[1]
Кастро и сътрудници съобщават, че средният резултат на пациентите, приети с оклузия на М2 сегмента, е
около 16 по NIHSS скалата. При провеждане на интраартериална тромбектомия степента на реканализа -
ция е TICI 2b/3 при 90% и 2c/3 при
60% от пациентите. Пълна реканали -
зация на М2 сегмента е постигната
при 53% от пациентите. Честотата на
sICH е 6.6%, смъртността е 30%, а добър функционален резултат (mRS ≤2)
се наблюдава при 50% от пациентите. По отношение на мястото на М2
оклузии, 74% от пациентите са имали проксимални М2 оклузии[2]. TICI (Thrombolysis In Cerebral Infaction) е скала, описана от Higashida и съавтори през 2003 г., за да се оценява отговорът на тромболитична терапия при исхемични инсулти, като има следните степени на TICI - Степен 0: без перфузия; Степен 1: преминаване на потока, но с минимална перфузия; Степен 2: частична перфузия; Степен 2А: от цялата съдова територия се
визуализира само частично изпълване на съдовете (по-малко от две трети); Степен 2B: визуализира се изпълването на цялата очаквана съдова територия, но изпълването е по-бавно от нормалното; Степен 3: пълна перфузия[3]
Няма единно мнение и консенсус за дозировката на rtPA: За артериални оклузии се описва прилагане в доза 0.05-0.1 mg/kg за 1 до 8 часа или до лизиране на тромба[4], Rejane C[5] и сътрудници съобщават за доза между 20-60 mg, а Alicia C[6] и сътрудници съобщават за най-често използвани в практиката дозировки между 2 и 20 mg.
Кереши и сътрудници осъшествяват проучване, в което съобщават за последователно по-добра преживяемост и намален неврологичен дефицит при пациентите, претърпяли интервенционално лечение, в сравнение с пациентите, на които е извършена интравенозна тромболиза[7]. При анкетен метод чрез запитване на интервенционални невролози и неврохирурзи е установено, че повечето от тях при оклузии предимно на дисталните клонове на артериите продължават да използват ИАТ, въпреки наличието на стент ретрийвъри[6]
ЗАКЛЮЧЕНИЕ Предвид четрикратно по-големия риск от смърт при млади пациентите с исхемичен мозъчен инсулт, уместно е да се търсят насочено причините, довели до инцидента, с цел превенция на усложненията и последващи мозъчно-съдови инциденти[7]
мозъчносъдовите заболявания под редакцията на Акад. проф. д-р Ив. Миланов и проф. д-р П. Стаменова 2020 г.
2. Luís Henrique de Castro Afonso Thrombectomy for M2 occlusions and the role of the dominant branch. Interv Neuroradiol. 2019 Dec; 25(6): 697–704

3. Higashida RT, Furlan AJ, Roberts H et-al. Trial design and reporting standards for intra-arterial cerebral thrombolysis for acute ischemic stroke. Stroke. 2003;34 (8): e109-37
4. https://reference.medscape.com/drug/activase-tpa-alteplase-342287#0
5. Rejane C. Lisboa, Borko D. Jovanovic and Mark J. Alberts Analysis of the Safety and Efficacy of Intra-Arterial Thrombolytic Therapy in Ischemic Stroke Stroke. 2002;33:2866–2871
6. Alicia C. Castonguay, Mouhammad A. Jumaa, Osama O. Zaidat, Diogo C. Haussen, Ashutosh Jadhav, Hisham Salahuddin and Syed F. Zaidi Insights Into Intra-arterial Thrombolysis in the Modern Era of Mechanical Thrombectomy. Front Neurol. 2019 Nov 13;10:1195
7. Jose F. Varona* Stroke Res Treat. 2011; 2011: 879817. Published online 2010 Dec 20.
[www.medmag.bg ] 13
ИЗПОЛЗВАНА ЛИТЕРАТУРА: 1. Национален консенсус за профилактика, диагноза и лечение на
Фиг. 1 Фиг. 2 Фиг. 3
НЕВРОЛОГИЯ
И. Балтова1,2 , Дж. Башчобанов1,2 , В. Цветкова2 , М. Димитрова2
1Медицински Факултет, Медицински Университет - София
2Клиника по нервни болести, УМБАЛСМ “Н. И. Пирогов”
Рядък
причинител Listeria monocytogenes
Листериозата е инфекциозно заболяване, причинено от Listeria monocytogenes. L. monocytogenes (Lm) е грам-позитивнa, факултативно анаеробнa, интрацелуларна бактерия. Може да бъде изолирана от месото, почвата, водите и някои растения, което обяснява широкото ѝ разпространение в човешката популация[1] Най-често заразяваното става чрез контаминирани храни, чрез които попада в стомашно-чревния тракт (СЧТ), което дава възможността да премине през мукозата и да попадне в системното кръвообращение. Проучвания в семейства с доказана листериоза показват
21% честота на носителство в СЧТ[2]. Микроорганизмът
се изолира от изпражненията на 5% от здравите индивиди. Малко проучване доказва, че колонизацията от един и същи серологичен тип листерия не се задържа за повече от 2 месеца[3]. Демографските показатели сочат, че листерозата се среща най-често при новородени до 30 ден, бременни жени, при хора над 65-годишна възраст и при хора с имунен дефицит - пациенти с HIVинфекция, подложени на имуносупресивна или имуномодулираща терапия, облъчване и хора с автоимунни заболявания[4]. Тези демографски данни и фактът, че
КЛИНИЧЕН СЛУЧАЙ
Касае се за мъж на възраст 69 години, постъпил с оплаквания от силно
главоболие, фебрилитет - 38-39 гра -
дуса, намален апетит и дезориентация. Пациентът редовно употребя -
ва алкохол (постъпва с 0,09 промила етанол при направен кръвен тест).
Анамнестичните данни сочат за
пред ходно извършена оперативна интервенция - поставяне на езофагеален стент. Имал е микотична инфекция на хранопровода. Перфорирала язва на дуоденума и направена гастроенетроанастомоза. Има данни за исхемична болест на сърцето и поставени 3 стента. Пациентът е с хипертония III степен.
Неврологичният статус показва
синдром на менинго-радикулерно
дразнене положителен, Керниг положителен, латентна левостранна хе -
здрави индивиди могат да бъдат носители на микроорганизма, без да развият клинична картина на самото заболяване, са в подкрепа на твърденията, че листерозата засяга имунокомпрометирани пациенти[5]. Lm има тропизъм към нервната система. Засягането на нервната система се изразява в менингоенцефалит, менингит, прогресивна левкоенцефалопатия, абсцес, церебрит. Най-често засегнатите краниални нерви са VI и VII. Lm показва и известен тропизъм към структурите на мозъчния ствол[6]
При небременни пациенти със системно бактериално разпространение клиничната картина се характеризира с фебрилитет, болки в мускулите и ставите, вратна ригидност, главоболие, конфузия, загуба на баланс, припадъци, нарушени когнитивни функции, неврологичен дефицит[7].
Цел: Целта ни е да се представи рядък клиничен случай на пациент с менингоенцефалит, с изолирана причинител - Lm. Както и да се направи сравнение с публикуваните в световната база данни подобни случаи.
мипареза и Бабински положителен вляво и централно левостранно засягане на VII и ХII черепно-мозъчни нерви.
Кръвните изследвания показаха анемичен синдром (желязо-дефицитна анемия) и промени от реактивен тип - характерна находка при инфекциозни заболявания.
Бяха проведени следните диагностични изследвания - компютърна томография (КТ) на глава, лумбална пункция и магнитно-резонансна томография (МРТ) на главен мозък. При разчитането на КТ на глава не бяха установени данни за огнищни или дифузни промени, нетипични за възрастта (Фиг. 1).
При лумбална пункция, резултатите показаха изразена протеинрахия,
хипогликорахия, плеоцитоза с превалиране на неутрофили. Тези данни сочат за бактериално инфектиране, поради което бяха проведени PCR (polymerase chain reaction) изследвания за Mycobacterium tuberculosis, Lysteria monocytogenes, Haemophilys influenzae, Neisseria meningitis, Streptococcus pneumoniae. Чрез PCR се установи инфекция с Listeria monocytogenes.
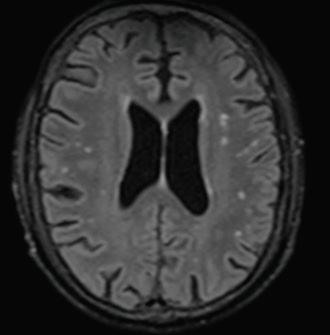
Беше проведен и МРТ на главен мозък, при която се установи разпространена левкоенцефалопатия и пролабиране на хиазмалната цистерна инстраселарно - частично "празна села", Фиг. 2
След консултация със специалист по вътрешни болести, започна провеждането на антибиотична терапия с ампицилини и амикацин в про -
14 І Medical Magazine | юли 2023
клиничен
случай на пациент с бактериален менингоенцефалит с изолиран
дължение на 10 дни и продължение
на терапията до 14 дни, ако при контролна лумбална пункция се установи същият причинител. Контролната лумбална пункция показа подобрение в плеоцитозата. Пациентът бе изписан с липса на симптоматика за персистираща невроинфекция с препоръки за продължаване на антибиотичното лечение.
ОБСЪЖДАНЕ
Едни от изявите на инфекцията с L. monocytogenes е прогресивната левкоенцефалопатия и менингоенцефа -
лит. Два случая са докладвани след предходна бъбречна транспланта -
ция. Единият - завършил със смърт след обостряне на неврологичната
симптоматика, а другият е лекуван с антибиотици до негативен микробиологичен резултат от ликвора, но
2 години по-късно неврологичната симптоматика силно се обостря и за -
вършва със смърт[8].
Според проучване, направено в Лондон, включващо 54 листериозно болни със засягане на нервната система, по-тежка прогноза имат случаите с изолиран менингит, в сравнение с тези с менингоенцефалит. Смъртността е 52%, въпреки антибиотичната терапия (най-често е предписван ампицилин), като от групата незагинали пациенти при 20% персистира резидуален неврологичен дефицит. Докладва се за обратно развитие в парезите на VI и VII ЧМН, моноплегията и ипсилатералните оживени рефлекси[9].
От голямо значение е не само видът на антибиотичната терапия, но и продължителността на приема - показва проучване, продължаващо 33 години. Рецидивите на неврологичния дефи-
ИЗПОЛЗВАНА ЛИТЕРАТУРА:
1. McLauchlin J. Human listeriosis in Britain, 1967–85, a summary of 722 cases. 2. Listeriosis in non-pregnant individuals, a changing pattern of infection and seasonal incidence.Epidemiol. Infect.1041990191-201
2. Farber JM, Peterkin PI: Listeria monocytogenes: a food-borne pathogen. Microbiol Rev 1991, 55:476–511.
цит са значително повече при пациенти, приемали антибиотична терапия за 14 или по-малко дни. Препоръчва
се лечението да е между 15-21 дни, а за пациенти с фокални неврологични дефицити дори по-дълго, поради откриването при аутопсията на формирали се микроабсцеси. При добавяне
на аминогликозид в началото на основното лечение (първите 7-10 дни) с бета-лактамни антибиотици се наблюдава най-добър изход с най-малко рецидиви на инфекцията[7]
В България заболелите от листериоза са 6-7 човека годишно, като броят на неврологичните усложения са по-редки. Неспецифичната клинична картина затруднява навременното диагностициране, а стандартните микробиологични изследвания са често недостатъчни, което налага използване на по-специализирани методи за откриване на причинителя.
Lm е трети по честота причинител на бактериален менингит при пациенти над 65 години. Тя води до заболяване най-често при имунокомпрометирани пациенти и такива с наранена лигавица на стомашно-чревния тракт, което прави разпространението на микроорганизма по-лесно. В нашия случай се касае за пациент на 69-годишна възраст, който има редовен прием на алкохол, с поставен езофагеален стент и анамнеза за перфорирана дуоденални язва с последваща гастроентеростомоза преди около 10 години. Това го поставя в групата на пациенти с риск от клинично изявена листериоза.
ЗАКЛЮЧЕНИЕ
Листерозата е рядко срещана, но животозастрашаваща инфекция с висо -
3. Schuchat A, Deaver K, Hayes PS, et al.: Gastrointestinal carriage of Listeria monocytogenes in household contacts of patients with listeriosis [letter]. J Infect Dis 1993, 167:1261.
4. Drevets DA, Jelinek TA, Freitag NE. Listeria monocytogenes-infected phagocytes can initiate central nervous system infection in mice.
Фиг. 1
Нормално
Infect Immun. 2001 Mar;69(3):1344-50.
5. Drevets DA, Jelinek TA, Freitag NE. Listeria monocytogenes-infected phagocytes can initiate central nervous system infection in mice. Infect Immun. 2001 Mar;69(3):1344-50.
6. Rogalla D, Bomar PA. Listeria Monocytogenes. 2022 Jul 4. In: StatPearls [Internet]. Treasure Island (FL): StatPearls Publishing; 2023 Jan.
ка смъртност. Поради което трябва да бъде включена в диференциално-диагностичен план при пациенти, попадащи в рисковата група за невроинфекция с Lm, с бактериален менингит и/или с изразен неврологичен дефицит в хода на инфекциозно заболяване. Познаването на историята на пациента и правилното интерпретиране на клиничните изследвания са от изключителна важност за поставянето на правилната диагноза и последващото правилно лечение.
7. Mylonakis E, Hohmann EL, Calderwood SB. Central nervous system infection with Listeria monocytogenes. 33 years' experience at a general hospital and review of 776 episodes from the literature. Medicine (Baltimore). 1998 Sep;77(5):313-36.
8. Reznik M, Halleux J, Urbain E, Mouchette R, Castermans P, Beaujean M. Two cases of
progressive multifocal leukoencephalopathy after renal transplantation. Acta Neuropathol Suppl. 1981;7:189-91.
9. Pollock SS, Pollock TM, Harrison MJ. Infection of the central nervous system by Listeria monocytogenes: a review of 54 adult and juvenile cases. Q J Med. 1984 Summer;53(211):331-40.
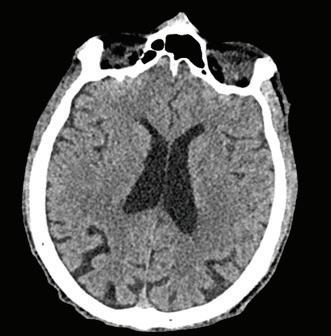
[www.medmag.bg ] 15
КТ на главен мозък за възрастта Фиг. 2 МРТ на главен мозък (Т2-режим) с данни за съдова левкоенцефалопатия
Разговор с доц. д-р Ирена Велчева, Председател на Българска
асоциация по невросонология и мозъчна хемодинамика
Доц. д-р Ирена Велчева е завършила Медицинска академия, София. Специалист по нервни болести.
От 1990 г. е доцент, ръководител на неврологично отделение, а от 2001 г. – на неврологична клиника в Университетската специализирана болница по неврология и психиатрия „Св. Наум“ ЕАД, София. В периода 1993–2001 г. е медицински директор на същата болница. От 2016 г. е началник на Клиника по нервни болести в МБАЛ „Уни Хоспитал“. Медицински експерт към МЗ и МОН. Дългогодишен национален консултант по нервни болести. Автор и съавтор на над 200 научни публикации, 22 монографии и 15 учебника по нервни болести. Основните ѝ научни и професионални интереси са в областта на мозъчно-съдовата болест – хемореологични промени и функционални невросонографски изследвания, заболявания на автономната нервна система, главоболие, епилепсия, заболявания на периферната нервна система. Ръководител на докторанти и специализанти по нервни болести.
Доц. Велчева е член на бордовете на национални и международни организации и фондации: European Society of Clinical Hemorheology and Microcirculation, International Danube Association for Neurology and Psychiatry, Фондация Балкански медицински съюз, Фондация Предпазване от мозъчни инсулти. Член е на ръководството на Научната група по автономна нервна система към European Academy of Neurology. Дългогодишен научен секретар на Българско дружество по неврология. Председател е на секция „Медицински науки“ към Съюза на учените в България. Представител е на България в Борда по неврология ня Съюза на Европейските медицински специалисти и в Световната федерация по неврология. Носител на почетен знак „Български лекар”, „За принос в развитието на медицината”, „За принос към развитието на МБАЛ „Св. Наум”, „За принос към червенокръстката кауза”.
Доцент Велчева, Българската асоциация по невросонология и мозъчна хемодинамика (БАНМХ) е създадена през 2005 г. в София.
Какво постигнахте през годините в Асоциацията?
БАНМХ беше основана през 2005 г. по подобие на Европейското дру -
жество по невросонология и мозъчна хемодинамика по инициатива на акад. проф. Екатерина Титянова, дългогодишен Председател на Управителния съвет, която ни напусна внезапно в началото на 2022 г. През годините Асоциацията разви активна научна, об -
разователна и издателска дейност. За периода 2005 – 2022 г. са организирани 9 научни срещи и 8 национални конгреси с международно участие, над 40 научни симпозиуми, краткосрочни курсове и учебно-практически семинари, Световен форум по невро -

16 І Medical Magazine | юли 2023
НЕВРОЛОГИЯ
„В нашата страна са въведени съвременните методи за диагностика и лечение на
мозъчно-съдовите заболявания“
сонология на Световната федерация по неврология (2013 г.), два регионални обучителни курса на Европейската академия по неврология (2014, 2017 г.), международен семинар „Ултразвуковите технологии – предизвикателства сред младите медици“ от програма на Европейската комисия (2013 г.). Подпомага се участието на сту -
денти, докторанти и млади учени в раз -
лични национални и международни научни форуми и проекти.
БАНМХ издава специализирано двуезично (на български и английски език) списание с
международен редакционен съвет, включено в Web of Science и Emerging Sources
Citation Index. Със съдействие на Асоциацията са издадени учебни помагала по невросонология и неврология: „Ултразвукова диагностика в неврологията“, „Атлас по невросонология“, “Национален консенсус по ултразвукова диагностика и поведение при екстракраниална каротидна патология“ с актуализирана интердисциплинарна версия през 2020 г.
Моля споделете какви са акцентите, на които обръщате внимание и кое за Вас е на преден план в работата ви като председател на Асоциацията?
През изминалите години БАНМХ създаде съвременна школа по невросонология, утвърди традиции в изграждането на висококвалифицирани и европейски сертифицирани специалисти в областта на диагностичния и терапевтичния ултразвук в неврологията и се ползва с национално и международно признание.
В работата ми като председател се стремя да поддържам високо професионално
и научно ниво на образователните инициативи и на печатния орган на Асоциацията, както и ползотворни контакти със сродни български и международни организации.
Какви предизвикателства стоят пред вас?
На изминалия 8-ми конгрес на БАНМХ акценти бяха поставени върху приложението на ендоваскуларното и тромболитичното лечение при остър исхемичен мозъчен инсулт, както и върху ролята на ултразвуковата диагностика и рехабилитацията при мозъчносъдовите заболявания.
Бихте ли очертали къде стои нашата страна, в сравнение с останалите европейски държави по отношение на представените диагностични методи и лечение?
В нашата страна са въведени съвременните методи за диагностика и лечение на мозъчносъдовите заболявания. Изминалият 8–ми конгрес на БАНМХ (21–23 октомври 2022 г.) беше по традиция интердисциплинарен, с участието на невролози, ангиолози, инервенционални специалисти, кардиолози, неврохирурзи, съдови хирурзи, специалисти по медицинска рехабилитация и ерготерапия и по кинезитерапия. На конгреса водещи български специалисти представиха своя опит в приложението на тромболизата при остър исхемичен инсулт и на ендоваскуларното лечение на каротидни стенози и артериовенозни малформа -
ции при различни форми на мозъчносъдова болест. Резултатите са обещаващи, но тези съвременни методи се прилагат в ограничен брой центрове с неравномерно разпределение в страната.
Представени бяха и съвременни технологии за генериране на триизмерни модели на мозъчното кръвообращение. На конгреса беше разгледана както от българските специалисти, така и от чуждестранните лектори ролята на невросонологията в диагностичния и терапевтичния алгоритъм при остри инсулти и при екстракраниална съдова патология.
Голям брой доклади и постери бяха посветени на съвременните форми на рехабилитация при неврологични заболявания. Творби на болни с тези заболявания бяха представени в изложба по инициативата „Арт терапия“. Организиран бе и симпозиум в сътрудничество с БАНИ на тема „Иновации в медицината“.
Какви инициативи организирате и към кого са насочени усилията ви? Основно събитие на 2023 г. ще бъде предстоящия 9–ти национален конгрес, на 27–29 октомври, който ще бъде традиционно интердисциплинарен и с международно участие, с представяне на нови технологии в невросонологията, практически семинари и дискусии върху актуални проблеми на мозъчносъдовите заболявания.
[www.medmag.bg ] 17
М. Клисурски, д.м. Медико Диагностичен Център "СПЕКТЪР"
ЕООД - София
НЕВРОЛОГИЯ
Новости в диагнозата на
атипичните паркинсонови
синдроми
Целта на статията е да се представи информация за диагнозата на най-често срещаните атипични паркинсонови синдроми (АПС) – прогресивна супрануклерна парализа (ПСП), мултисистемна атрофия (МСА), кортикобазалния синдром или дегенерация (КБД), деменция с телца на Леви (ДТЛ) – и да се очертаят новите невроизобразителни подходи и диагностични биомаркери при диференцирането им от идиопатичната болест на Паркинсон (БП). През последните няколко години се наблюдава значителен прогрес в разработване на образни и лабораторни методи за диагноза при ПБ и АПС. Нововъведения са мултимодалното МРТ и ПЕТ невроизобразяване на дегенеративния процес и комплексният подход при използване на различните флуидни биомаркери, което превъзхожда единичните методи. Молекулярното ПЕТ изобразяване на алфа-синуклеина и тау-протеина чрез нови лиганди, както и регистрирането на мозъчния глюкозен метаболизъм предоставят отлична възможност за вникване в патогенезата на паркинсонизма и разпределението на патологичната протеинова агрегация в мозъка. Базираните на изкуствен интелкт техники на машинно обучение за усвояване на образни диагностични алгоритми и анализи са в ход на проучване. Клиничното приложение на иновативните техники все още е ограничено и тяхната стандартизация предстои. Предложеният наскоро от International Parkinson and Movement Disorder Society „Прагматичен подход при използване на невроизобразителни техники в диференциалната диагноза на паркинсонизма“ е реално изпълнима стратегия[37], която може да подобри рутинната неврологична практика в нашата страна.
Болестта на Паркинсон и
АПС са прогресивни невродегенеративни заболява -
ния с различна етиопатогенеза, които независимо от разнообразната си фенотипна презентация често се припокриват с клиниката на БП, но са отделни клиникопатологични единици. Тяхното разграничаване се базира на консенсусни международно утвърдени критерии, но поради голямата хетерогенност все още това е значително предизвикателство, особено в ранната фаза на болестта. Съвременните критерии за МСА, КБД и ПСП все още нямат позитивната предиктивна стойност на патоанатомичната диагноза, която засега остава златен стандарт. Погрешни диагнози са
наблюдавани и при дълго проследявани пациенти. Ето защо се разработват и усъвършенстват множество невроизобразителни, ликворни, молекулярни и генетични биомаркери, които in vivo да диференцират АПС със сходен фенотип от ПБ. Стремежът е от подкрепящи критерии те да станат бъдещи високо сензитивни и директни диагностични индикатори[41,42]. Патологичната протеинова агрегация в мозъка при АПС е комплексна, но два типа протеинопатии са водещи[8,16,22,24,32,43]:
1) алфа-синуклеинопатии – към които спадат ПБ, МСА и ДТЛ, и 2) тау-патии - ПСП, КБД, и някои варианти на фронто-темпоралната деменция (ФТД).
Идиопатичната БП е второто най-чес -
то срещано невродегенеративно заболяване след болестта на Алцхаймер (БА), при около 2% от хората над 60 г., до 4% при тези над 80 г. Среша се при 8 до 18 души на 100.000 (5) . Обновени диагностични критерии за БП са предложени през 2015 от International Parkinson and Movement Disorders Society[38]. АПС или т.нар. Паркинсон-плюс синдроми се срещат сравнително рядко - 0.4-5/100.000 души. Медикаментозният паркинсонизъм заема второ място по честота след ИБП.
ПСП е тау-патия с интрацеребрално натрупване (агрегиране) на микротубулно асоциирани тау-протеини, предимно на изоформи с четири повторения (4R-tau) в неврофибри -
18 І Medical Magazine | юли 2023
1. Бързо прогресивно увреждане на походката, налагащо използване на количка в рамките на 5 години от началните прояви;
2. Липса на прогресия на моторните симптоми или белези след 5 или повече години, освен ако клиничната стабилност не е свързана с полза от лечението;
3. Ранна булбарна дисфунцкция: тежка дисфония и дизартрия (трудноразбираема реч) или тежка дисфагия (налагаща използване на течнокашава храна, назогастрална сонда, или гастростома) в рамките на първите 5 години;
4. Инспираторна дисфунцкция: дневен или нощен инспираторен стридор или чести инспираторни смушения;
5. Тежка автономна увреда в първите 5 години на болестта. Ортостатична хипотония или тежка уринарна ретенция, или инконтиненция през първите 5 г., (при мъжете – несвързана със заболяване на простатата и асоциирана с еректилна дисфункция);
6. Многократни (>1/годишно) падания, поради нарушен баланс още в първите 3 години от началото;
7. Непропорционален антероколис (дистоничен) или наличие на контрактури на ръцете и краката през първите 10 години;
8. Липса на обичайните за ПБ немоторни симптоми за предшестващите 5 години (поведенчески нарушения
по време на REM сън), автономна дисфункция, хипосмия, или психични прояви (като депресия, тревожност, халюцинации);
9. Необясними пирамидни белези, слабост, парези, патологична хиперрефлеския;
10. Двустранно симетричен паркинсонизъм.
лерни вретена, олигодендроцитни спирали и специфични астроцитни снопчета/туфи[25]. Невродегенерацията обхваща субкортикални структури като субстанция нигра, нуклеус субталамикус и мезенцефалона[28,40]. Предложените клинични критерии за ПСП (NINDSSPSP) са най-широко използваните за диагноза антемортем[28,39]. Актуализираните критерии на MDS-PSP, разработени от експерната група на MDS-PSP предлагат тристепенен подход[11,19]. Установени са осем различни варианта на ПСП, с класически фенотип, познат като синдром на Steele-RichardsonOlszewski. Той презентира с аксиален акинетично-ригиден паркинсонизъм, със слаб или лош отговор на лечение с леводопа, и постурални нарушения (хиперекстензия на главата и торакса, ретроколис, за разлика от камптокорнията при БП), абнормна походка (на широка основа и епизоди на замръзване), постурална нестабилност и падания от началото на болестта (отколкото в късните стадии при БП). Много специфичен синдром е супрануклеарната вертикална погледна пареза, липсваща при БП. Други белези на окуломоторна дисфункция са забавените вертикални сакадични движения (особено надолу), апраксията на отваряне на клепачите (водеща до компенсаторна свръхактивност на фронталните мускули и лицев израз на „изненада“). Вести -
було-окуларният рефлекс е съхранен, поради супрануклеарната локализация на увредата. Допълнително има псевдобулбарни прояви, субкортикален тип деменция, префронтални или премоторни рефлекси, моторна персеверация, (обикновено липсващи при БП). Характерен белег при болните с ПСП е и “моторната необмисленост”, определяна като невнимание при ходене, ставане или движение, въпреки липсата на баланс и чести падания[19,28]
МСА е спорадично, прогресивно невродегенеративно заболяване, което се проявява с различна степен на акинетично-ригиден, сравнително симетричен паркинсонизъм, церебеларна дисфункция (дизартрия, дисметрия, нистагъм и атаксия), пирамидна увреда, ранни автономни нарушения (уро-генитални и сърдено-съдови – ортостатична хипотония, синкопи, постурално вертиго) и др.[8,22, 48]. Пациентите с МСА също слабо се повлияват от терапия с леводопа и ДА2-агонисти. Възможна е окуломоторна дисфункция (нарушени плавни проследяващи движения, дисметрични сакади, супресия на окуловестибуларния рефлекс). Треморът в покой е рядкост, но пациентите могат да имат миоклонус, антероколис или ретроколис, орофациална дистония, особено като страничен ефект на ле -
Табл. 1
Някои разграничителни
белези при диференциране на ПБ от АПС[38]
[www.medmag.bg ] 19
водопа терапията. Респираторният стридор, и дихателните нарушения по време на сън са сериозни компликации. Деменция се наблюдава в крайните фази на болестта. Главна патоанатомична характеристика е разпространеното натрупване на aлфа-синуклеин в олигодендроглията, като цитоплазматични глиални или невронални нуклеарни включвания. Невроналната загуба е предимно в стриатонигралната и оливо-понто-церебеларната система[48,31,46].
При КБД за разлика от ПБ има асиметрична моторна симптоматика: ригидност, брадикинезия в един крайник, както и дистония или дистален миоклонус[1]. Характерен синдром при около 50% от пациентите е т.нар. “alien limb phenomenon”: ръката заема неволеви пози, хваща обекти неправилно или интерферира неадекватно с движенията на другия незасегнат крайник. Треморът е рядко срещан, или ако го има, е акционен или постурален, но не и в покой. Кортикалните белези включват деменция и фронтални и париетални кортикални нарушения, апраксии и агнозии, също липсващи при БП. Клиничната презентация при КБС е много вариабилна и се припокрива с много други заболявания – БА, ПСП, ФТД, прионопатии - ето защо клиничната й диагностична точност е по-ниска[1,43]. Патологоанатомично КБД или КБС е тау-патия, с наличие на “астроцитни плаки”; предимно засягане на субстанция нигра и фронтопариеталния кортекс[24,43]. Комплексното ПЕТ изобразяване за амилоид чрез 11C-PiB, за тау чрез 18F-flortaucipir, и за глюкоза чрез 18F-FDG може да диференцира БА с КБС от КБД[33]
Главните клинични синдроми на деменцията с телца на Леви (ДТЛ, DLB) са когнитивни нарушения с флуктуираща будност и внимание, паркинсонизъм, зрителни халюцинации и нарушения по време на РЕМ съня[16,13]. Паркинсонизъм имат около 85% от болните, който е в по-лека форма, в сравнение с другите АПС и БП. Наблюдава се постурална нестабилност, но тремор почти липсва. Когнитивните промени започват паралелно или в рамките на една година от проявите на паркинсонизъм[21]. Страдат екзекутивните функции и зрително-пространствените способности, има дефицит на вниманието, докато паметта и езиковите функции са относително съхранени. Други клинични прояви са вегетативните смущения, честите падания, изразената днев -
на сънливост, особената чувствителност към невролептици, хипосмията и промените в настроението. Халюцинациите са доста живи и детайлни. ДТЛ е синуклеинопатия; с характерните невронални включвания (телца или Lewy neurites) и невронална дегенерация. При ДТЛ има 3 варианта на алфа-синуклеинова патология: с доминиращо засягане на мозъчния стовол, на лимбичната система (транзиторна) или на неокортекса[16].
АПС могат да се подозират или разграничават от спорадичната идиопатична БП, при наличие на особени клинични белези („red flags”, Табл. 1)[2,19,31,32]. Тук не говорим за фамилните или генетични форми на БП. Не става въпрос и за хередитарни невродегенеративни заболявания (болест на Wilson, Huntington, Kufor-Rakeb синдром, SCA3, Dopa-responsive dystoniа, X-linked parkinsonism dystonia), които първоначално или вторично включват прояви на хипокинезия, ригидност, дистония, тремор и др. Към АПС не се включват и заболяванията с вторичен паркинсонизъм, причинени от съдова, възпалителна, автоимунна, токсична, травматична или друга етиология, напр. нормотензивна хидроцефалия.
При DATSCAN или DAT-SPECT изследването се маркира допаминовия (ДА) транспортер-протеин, чието намалено или асиметрично натрупване отразява денервацията или дегенерация на нигростриарната система, особено в задната част на путамена. Тестът е одобрен от FDA за рутинна клинична употреба, за разграничаване на ПБ от есенциален тремор (95% сензитивност и 93% специфичност[32,35, 38,42]. Това изследване е особено полезно при диференциране на случаите с невролептичен, съдов или друг вторичен недегенеративен паркинсонизъм. Но така не може да определи дали се касае за МСА, ПСП или КБС. Макар и рядко са докладвани фалшиво позитивни или фалшиво негативни резултати.
Нови образни биомаркери при АПС (Табл. 2) са: (1) структурна МРТ морфометрия; (2) дифузионни и diffusion tensor-техники; (3) функционален МРТ (resting-state; task-based); (4) протонна МР спектроскопия; (5) степен на възпаление (невроинфламация; (6) методи за пресинаптично и постсинаптично СПЕКТ маркиране за оценка на ДА система и мозъчна перфузия; (7) ПЕТ за количествена оценка на нигростриарните функции; глюкозен метаболизъм; (8) ПЕТ молекулярно изобразяване
20 І Medical Magazine | юли 2023
НЕВРОЛОГИЯ
за амилоид, тау-протеин и aлфа-синукелин с нови лиганди; (9) транскраниална сонография
за определяне на ехогенната плътност на субстанция нигра и лентиформното ядро[41,42,3]
Иновативни ПЕТ лиганди (изотопи) са в процес на задълбочено изследване[33]. Молекулярното изобразяване предоставя отлична възможност за разбиране на патогенезата
на паркинсонизма и рапределението на патологичната протеинова агрегация в мозъка.
По подобен начин, регистрирането на мозъчния глюкозен метаболизъм чрез [18F]FDG-PET
е подкрепящ критерий за диагноза на ПСП и на МСА[37,38]. Изследванията с [18F]FDG-PET
са важни за откриване на различните прояви
на мозъчен хипометаболизъм и предоставят
значими “образно-клинични” корелации при невродегенеративните заболявания[34]. Тен -
хиката дава количествена оценка на мрежовите нарушения по един образно-специфи -
чен начин. Изследванията с [18F]FDG-PET
демонстрират превъзходство пред D2/D3SPECT при разграничаването на БП от АПС. Последните критерии на Movement Disorder Society подкрепят употребата на FDG-PET за тази цел[38,19]. Един нов ПЕТ-изотоп (радиотрейсер) - [11C]UCB-J - се свързва с пресинаптичния везикулен протеин SV2A. Той е широ -
ко разпространен в мозък и е валидиран през
2017 г. като първи in vivo универсален маркер
за синаптична плътност при хора. Потвърдена е отличната линейна корелация между SV2A и “златния стандарт” синаптичния маркер синаптофизин [18F]FDG PET предоставя информация за клетъчната хексокиназна активност, което отразява поемането на глюкозата. Необходимостта от глюкоза за невроните отчасти е свързана с генерирането на АТФ от синаптичните терминали за синтез, освобождаване и рециклиране на невротрансмитерни молекули. Ето защо, [18F]FDG PET предоставя валидирано измерение за невроналното функциониране[4].
Пресинаптично допаминово сканиране
(DATscan-F-DOPA PET) може да бъде особе -
но полезно в съчетание с постсинаптично
ДА изобразяване за диференциална диагноза на БП и АПС. Наличността на ДА-рецептори обикновено е намалена при МСА и ПСП за разлика от ПБ, където D2-рецепторите са нормално представени или увеличени[41,42]. Съединенията за това рецепторно изобразяване не са одобрени за клинична потреба от FDA, а и повечето центрове не могат да прилагат
тази комбинация. Пресинаптичното ДА-сканиране диференцира дегенеративните от недегенеративните форми на паркиносонизъм, а комбинацията от пресинаптично сканиране плюс FDG-PET е особено полезна за ДД между БП и АПС. За документиране на пресинаптичен ДА дефицит е идеална комбинацията F-DOPA или FP-CIT PET (с по-добро съотношение сигнал-шум отколкото DaTscan) плюс метаболитното изобразяване. За тази цел също може да се използва и resting state-fMRI, на база алгоритми за образно базирани решения.
Ролята на новите тау-ПЕТ лиганди, особено важни при БА, все още се уточнява при ПБ и АПС [42]. Tау-ПЕТ е най-вълнуващата област в образната диагноза на паркинсонизма, която се развива като in vivo модалност за индивидуална диагноза на ПСП. Това става най-добре с използване на изотопи от второ поколение[33]. Напр. [18F]-PI-2620 демонстрира висок афинитет на свързване с натрупаните 4-повторни изоформи на тау-протеина, без значимо off-target-свързване с бета-амилоида или MAO-A, или B. Пациентите с ПСП-RS, но не и здравите контроли, натрупват значимо маркера в специфичните за болестта региони.
Стандартната МРТ не е полезна за диагнозата на ПБ, но може да изобрази добре съдово исхемичните, възпалителни, неопластични и др. етиологии[41,18,17,20]. Протоколите
за МРТ с по-мощно магнитно поле >3Т предоставят техники за изобразяване на различните маркери за невродегенерация – напр. невромеланин (НМ) и дорзален нигрален хиперинтензитет[17]. Те идентифицират протичащия невродегенеративен процес, загубата на ДА неврони и намаление в сигнала за невромеланин. Техниките, чувствителни за натрупване на желязо, т.нар. susceptibility weighted imaging, регистрират сигналното намаление в путамена при АПС, където натрупването на железни йони е преобладаващо и по-тежко при ПСП в сравнение с MSA-P. Демонстрира се нарастваща точност за диференциране на АПС при комбиниране на тези методики. Нигрозома -1 може да бъде визуализирана чрез МРТ като хиперинтенза овоидна зона, неречена дорзален нигрален хиперинтензитет (ДНХ), (симптом на „лястовичата опашка”, “swallow tail”). Нигрозома -1 е малко струпване на ДА-съдържащи неврони в субстанция нигра, най-добре видима при т.нар.
[www.medmag.bg ] 21
susceptibility map-weighted техника, и е значимо променена при болните с БП. При МРТ изобразяването на НМ - субстанция нигра се вижда като зона на висок сигнален интензитет при здрави лица. При болните с БП обаче, има намаление на този интензитет в задната и латерална част на субстанцията. НМ е грануларен интрацелуларен пигмент, който се открива в катехоламинергичните неврони на субстанция нигра и локус церулеус. Той има протектираща роля върху ендогенния допамин, особено чувствителен към оксидативен стрес[37]. Загубата на НМ в парс компакта на субстанция нигра и в локус церулеус са кардинални увреди за БП. Eкстрацелуларният НМ отключва инфламаторна каскада, усилваща невродегенерацията. Ето защо, проследяването на динамиканата на НМ чрез МРТ е особено важно за клиниката[20]
МРТ предоставя други белези и морфологични критерии (Табл. 3) за разграничаването на АПС от БП[2]: 1) атрофия и сигнални промени в путамена и T2-хиперинтензи промени в понса (“hot cross bun” sign) и в средните церебеларни крачета при МСА; 2) специфичната атрофия на мезенцефалона спрямо понса (“hummingbird” sign) при ПСП, или 3) асиметрична фронтална или париетална атрофия при КБД. Ограничение на метода е сензитивността, защото половината от болните с АПС нямат тези белези в ранната фаза на болестта[3,30,48,42,37,29]. Мозъчната морфометрия засега има малко практическо значение в ежедневната практика. Те е приложима за изследователски цели и клинични проучвания. Методът resting state-fMRI е разработен като алтернатива на FDG-PET за вероятностна образна диагноза[10], една по-достъпна методика, неизискваща радиоизоп. Като маркери на функционалната мрежова активност в целия мозък, методите resting state-fMRI и FDGPET се допълват много добре за доказване на in vivo нигростриарна ДА дисфункция. Т.нар. diffusion tensor imaging МРТ е индиректен показател за ДА дегенерация в субстанция нигра и потанциално неинвазивен ранен биомаркер за БП (100% Se и Sp);
Новите нахлуващи технологии, като хибридния ПET/МРТ скенер, включват предимствата на МРТ за подобряване на пространствената и времева резолюция[45]. Базираните на изкуствен интелкт техники на машинно обучение за усвояване на образни диагностични алгоритми и анализи са в ход на проучване.
Използват се МРТ атласи за автоматизирано сегментиране при диференциална диагноза на ПБ и АПС. Смята се, че съчетаването
на различни модалности от ПЕТ и МРТ заедно с автоматизираните компютърни алгоритми ще усъвършенстват значимо диагнозата на невродегенеративните болести и ще способстват за вникване в патогенезата на техните комплексни промени.
Разбира се, че клиничното приложение на такива иновативни или допълнителни техники (Табл. 2 и 4) е все още ограничено и тяхната стандартизация предстои[35,41,42]. Ето
защо наскоро Peralta et al, публикуваха в Mov Disord Clin Pract, 2022 един „Прагматичен подход при използване на невроизобразителни техники в диференциалната диагноза на паркинсонизма“, методика, която е реално изпълнима понастоящем[37]. Тя може да подобри рутинната неврологична практика при диференциране на подобни пациенти и у нас. Сега диагностичните критерии за БП на International Parkinson and Movement Disorder Society включват “абсолютни изключващи критерии” (нормален пресинаптичен допаминов терминал) и “подкрепящи критерии” (миокардна симпатикова денервация)[38]. Първо е важно чрез МРТ да се разграничат вторичните, симптоматични форми на паркинсонизъм и да се определят специфичните морфологични параметри за атрофия на мозъчни структури (напр. при ПСП или МСА). Ако не е ясно, че се касае за дегенеративен паркинсонизъм, да се използват техниките за оценка на невромеланин и нигрален хиперинтензитет или за дифузия. Второ, ако от ДаТСкан изследването има данни за ДА-стриарна дегенерация (изключен е ЕТ, невролептичен или съдов паркинсонизъм) - но има клинични белези за АПС
- да се проведе [18F]FDG-PET изобразяване за глюкозен метаболизъм, чрез което може да определим дали се касае за ПСП, КБД или МСА [37]
Практическо значение за оценка на симпатиковата денервация на сърцето има миокардната сцинтиграфия чрез мetaiodobenzylguanidine. Методът предоставя информация за диференциране на ПБ от АПС и ДТЛ от МСА и ПСП[36,6,35]. При невродегенеративната МСА и съдовия паркинсонизъм се наблюдава нормално натрупване (или леко намаление) на изотопа за разлика от БП, където има значимо намалено миокардно
22 І Medical Magazine | юли 2023
НЕВРОЛОГИЯ
• Пресинаптично ДА изобразяване – SPECT [123I]FP-CIT; DaTscan, [123I] beta-CIT
• Постсинаптично ДА изобразяване - измерва D2/D3-активността
• ПЕТ - F-dopa, маркер за ДА синтеза; редукцията на F-dopa захвата главно в путамена диференцира БП от МСА и ПСП
• Глюкозен метаболизъм: [18F] Fluorodeoxyglucose (FDG)-PET, мозъчен хипометаболизъм
• Тау-ПЕТ: изотопи първо поколение [18F]-AV1451; второ поколение изотопи с по-добра специфичност са [18F]-PI2620, [18F]-MK- 6240, [18F]-RO -948, [18F]-PM-PBB3
• Амилоид-ПЕТ: 11C-PIB (Pitsburg compound B) - БП < БП-ЛКН < ПДД < ДТЛ
• Синуклеин-ПЕТ: надежди за диагностичен пробив, но все още неосъществен
• Базирани на образи модели за машинно обучение
• Структурна / МРТ морфометрия
• Изобразяване за невромеланин
• МРТ изобразяване за натрупване на желязо: SWI и QSM техники;
• Протонна МР спектроскопия при ПСП
• Diffusion Tensor Imaging
• Функционална MРТ
• MРТ за невроинфламаторни промени
• Хибриден ПЕТ/MРТ скенер
• Субстанция нигра: редуциран НМ и загуба на ДНХ
• Белези на колибрито „Hummingbird“ и утринната слава „Morning glory“
• M/P съотношение: обикновено <0,215 спрямо БП и МСА-П
• MRPI index: увеличен > 13,6 спрямо БП и ЗК; спрямо 12,9 при МСА-П
• Атрофия на горно малкомозъчно краче - типично 2 мм
• Ширина на трети вентрикул - увеличен, cut- off стойност ≥2.91
• Фронтален кортекс – разширени сулкуси; Путамен – нормален
• MRPI диференциара ПСП - Паркинсонизъм от ПБ със Se 73.5% и Sp 98.1%,
• MRPI 2.0 показва висока Se 100% и сходна Sp 94.3% при разграничаване на двете групи
маркиране (поради загуба на ДА транспортер). Главен недостатък на [123I]MIBG/SPECT е ниската специфичност (37.4%), при относителноо висока сензитивност (87.7%) (клас II доказателсво).
Транскраниалното ултразвуково паренхимно изобразяване е по-стар подкрепящ метод, отпреди 10 години, чрез който може да се регистрира абнормна ехогенност (хипер- или хипо-)
в областта на субстанция нигра, рафе нуклеи и базалните ганглии при болните с БП АПС. Изразената хиперехогенност на субстанция нигра в комбинация с нормална ехогенност на нуклеус лентикуларис диференцира БП от МСА и ПСП с позитивна предиктивна стойност от 90%. Методът обаче изисква съответна настройка на апарата и е зависим от опитността на оператора, но неговата сензитивност и специфичност при болни с БП са субоптимални
Табл. 2
Методи за невроизобразяване при АПС (адаптирано по 37, 42)
Табл. 3
Невроизобразяване при ПСП и МСА – визуален анализ[2,8,37,38,39,29,18,30]
[www.medmag.bg ] 23
Табл. 4 Допълнителни биомаркери при БП и АПС (според направения обзор, 1-50)
• Ликворни и кръвни (флуидни) биомаркери: алфа-синуклеин; Aмилоид-бета и Tau; Неврофиламенти с леки вериги; Mикро-РНК; Автоантитела
• Специфични ликворни изследвания: RT-QuIC и Protein Misfolding Cyclic Amplification
• Генетични тестове за някои генни мутации: alpha-synuclein (SNCA), leucine-rich repeat kinase 2 (LRRK2), glucocerebrosidase (GBA), parkin (PARK2), PINK1 (PARK6) and DJ-1 (PARK7), ATP13A2 (PARK9), PLA2G6 (PARK14), FBXO7 (PARK15)
• Тестове с медикаментозна провокация
• Невропатологични и имунохистохимични биопсични техники
• Изобразяване на миокардната симпатикова инервация
• Алфа-синуклеин кожна имунофуоресценция
• Вегетологични методики: Олфакторен тест; Потна секреция, Нарушен аксон-рефлекс на потене при БП и МСА (не разграничат дефинитивно ПБ от МСА)
• Неврофизиологични тестове; напр. кинематични техники за анализ на брадикинезията
• Мониториране на нарушенията на съня; ЕЕГ техники[26]
• Невроофталмологични и отоневрологични методики
• Мултимодален подход
(съответно, 75% и 70% при АПС; и 78% и 85% при есенциален тремор)[47,9,12].
Необходимостта от надежден, репродуктивен и нескъп маркер за патологично натрупване на периферния фофорилиран алфа-синуклеин е дългогодишна изследователска одисея. Детекцията му в кожата е обещаващо направление за болестен процес, но проучванията досега имаха противоречив данни. Ето защо алфа-синуклеиновата кожната имунофлуорисценция е един практически лесно осъществим метод за доказване на протеинопатия. Установяването на дермални депозити от алфа-синуклеин служи като биомаркер при БП, за разлика от пациентите с тау-патии или здрави контроли [7,15,14] .
Също така, особено задълбочено се проучва кой е най-надеждният единичен биомаркер от плазмата или ликвора, и кои са оптималните панели от биомаркери за диренциране на различните АПС един от друг и от съответните здрави контроли[27,23]. Засега като най-важен отделен маркер за разграничаване на БП от АПС е установяването на неврофиламенти с леки вериги. В ликвора това е комплексия панел: NFL, Ab42, p-tau, t-tau, и t-a-synclein[49]
Той има сензитивност 85% и специфичност 92% в диагнозата на БП от тези с ПСП, МСА и КБС.
Други два много важни лабораторни метода за директно доказване наличето на патологичен ултраструктурен компонент (и при АПС) са т.нар „Seeding amplification assays“[50]. Това са Real-time quaking induced conversion (RTQuIC) и Protein misfolding cyclic amplification (PMCA), все още липсващи в нашата страна. По време на всеки цикъл, чрез специфичен флуорофор се мониторира експоненциалното нарастване на патологичните алфа-синуклеин или тау-агрегати в биологичната проба. [44]. При PMCA, в биологичните течности директно се регистрират патологино нагънатите протеинови агрегати. В многнао държави RT–QuIC вече е валиран диагностичен метод, официален критерий за диагноза на прионова болест (прионова енцефалопатия). През последните години се равива интензивно този подход за in vivo диагноза и биомаркиране от ликвора и тъканите на други прионо-подобни заболявания като синуклеинопатии и тау-патии.
ЗАКЛЮЧЕНИЕ
През последните няколко години се наблюдава значителен прогрес в разработване на методи за диагноза при ПБ и АПС. Нововъведения са мултимодалното невроизобразяване на дегенеративния процес и комплексният подход при използване на различните флуидни биомаркери, което превъзхожда единичните модални методи. Търсят се доказател -
24 І Medical Magazine | юли 2023
НЕВРОЛОГИЯ
ства за това кой е най-добрият метод за молекулярно изобразяване или директно протеиново отктиване. Новите лиганди не са валидирани при големи независими кохорти за еже -
дневна клинична употреба. Ролята на изкуствения интелект за анализ на образните патерни с предложения на клинични решения все повече нараства. Идващото поколение клинич -
ни невролози предстои да получи надеждни биомаркери за рутинна и ранна диагноза и диференциране на АПС и следователно разширени терапевтични възможности.
1. Alexander SK, Rittman T, Xuereb JH, et al. Validation of the new consensus criteria for the diagnosis of corticobasal degeneration. J Neurol Neurosurg Psychiatry 2014; 85:925–929.
2. Alster P, Nieciecki M, Migda B, Kutyłowski M, Madetko N, Duszyńska-Wąs K, Charzyńska I, Koziorowski D, Królicki L, Friedman A. The Strengths and Obstacles in the Differential Diagnosis of Progressive Supranuclear Palsy-Parkinsonism Predominant (PSP-P) and Multiple System Atrophy (MSA) Using Magnetic Resonance Imaging (MRI) and Perfusion Single Photon Emission Computed Tomography (SPECT). Diagnostics (Basel). 2022; 12(2):385.
3. Aludin S, Schmill LA. MRI Signs of Parkinson's Disease and Atypical Parkinsonism. Rofo. 2021 Dec;193(12):1403-1410.
4. Andersen KB, Hansen AK, Schacht AC, Horsager J, Gottrup H, Klit H, Danielsen EH, Poston KL, Pavese N, Brooks DJ, Borghammer P. Synaptic Density and Glucose Consumption in Patients with Lewy Body Diseases: An [11 C]UCB-J and [18 F]FDG PET Study. Mov Disord. 2023; 38(5):796-805.
5. Balestrino R, Schapira AHV. Parkinson disease. Eur J Neurol. 2020; 27(1):27-42.
6. Berardelli e al. EFNS/MDS-ES recommendations for the diagnosis of Parkinson’s disease. Eur J Neurol 2013; 20(1): 16–34.
7. Doppler K. Detection of Dermal AlphaSynuclein Deposits as a Biomarker for Parkinson's Disease. J Parkinsons Dis. 2021;11(3):937-947.
8. Fanciulli A, Wenning GK. Multiple-system atrophy. N Engl J Med. 2015; 372(3):249-63.
9. Favaretto S., Walter U, Baracchini C, Cagnin A. Transcranial Sonography in Neurodegenerative Diseases with Cognitive Decline. J Alzheimers Dis. 2018; 61(1):29-40.
10. Filippi M, Sarasso E, Agosta F. Restingstate Functional MRI in Parkinsonian Syndromes. Mov Disord Clin Pract. 2019; 6(2):104-117.
11. Frank A, Peikert K, Linn J, Brandt MD, Hermann A. MDS criteria for the diagnosis of progressive supranuclear palsy overemphasize Richardson syndrome. Ann Clin Transl Neurol. 2020; 7(9):1702-1707.
12. Fujita H, Suzuki K, Numao A, Watanabe Y, Uchiyama T, Miyamoto T, Miyamoto M, Hirata K. Usefulness of Cardiac MIBG
Scintigraphy, Olfactory Testing and Substantia Nigra Hyperechogenicity as Additional Diagnostic Markers for Distinguishing between Parkinson's Disease and Atypical Parkinsonian Syndromes. PLoS One. 2016; 11(11):e0165869.
13. Galasko D. Lewy Body Disorders. Neurol Clin. 2017; 35(2):325-338.
14. Giannoccaro MP, Avoni P, Rizzo G, Incensi A, Infante R, Donadio V, Liguori R. Presence of Skin α-Synuclein Deposits Discriminates Parkinson's Disease from Progressive Supranuclear Palsy and Corticobasal Syndrome. J Parkinsons Dis. 2022; 12(2):585-591.
15. Gibbons CH, Freeman R, Bellaire B, Adler CH, Moore D, Levine T. SynucleinOne study: skin biopsy detection of phosphorylated α-synuclein for diagnosis of synucleinopathies. Biomark Med. 2022; 16(7):499-509.
16. Gomperts SN. Lewy Body Dementias: Dementia With Lewy Bodies and Parkinson Disease Dementia. Continuum (Minneap Minn). 2016; 22(2 Dementia):435-463.
17. Grossauer A, Müller C, Hussl A, Krismer F, Schocke M, Gizewski E, Mahlknecht P, Scherfler C, Wenning GK, Poewe W, Seppi K, Heim B. Dorsolateral Nigral Hyperintensity on 1.5 T Versus 3 T SusceptibilityWeighted Magnetic Resonance Imaging in Neurodegenerative Parkinsonism. Mov Disord Clin Pract. 2023; 10(6):914-921.
18. Heim B, Krismer F, De Marzi R, Seppi
K. Magnetic resonance imaging for the diagnosis of Parkinson's disease. J Neural Transm (Vienna). 2017; 124(8):915-964.
19. Höglinger GU, Respondek G, Stamelou M, Kurz C, Josephs KA, Lang AE, Mollenhauer B, Müller U, Nilsson C, Whitwell JL, Arzberger T, Englund E, Gelpi E, Giese A, Irwin DJ, Meissner WG, Pantelyat A, Rajput
A, van Swieten JC, Troakes C, Antonini A, Bhatia KP, Bordelon Y, Compta Y, Corvol JC, Colosimo C, Dickson DW, Dodel R, Ferguson
L, Grossman M, Kassubek J, Krismer F, Levin J, Lorenzl S, Morris HR, Nestor P, Oertel WH, Poewe W, Rabinovici G, Rowe
JB, Schellenberg GD, Seppi K, van Eimeren
T, Wenning GK, Boxer AL, Golbe LI, Litvan
I; Movement Disorder Society-endorsed
PSP Study Group. Clinical diagnosis of progressive supranuclear palsy: The movement disorder society criteria. Mov Disord. 2017; 32(6):853-864.
20. Hwang KS, Langley J, Tripathi R, Hu XP, Huddleston DE (2023) In vivo detection of substantia nigra and locus coeruleus volume loss in Parkinson’s disease using neuromelaninsensitive MRI: Replication in two cohorts. PLoS ONE 18(4): e0282684.
21. Jellinger KA. Dementia with Lewy bodies and Parkinson's disease-dementia: current concepts and controversies. J Neural Transm (Vienna). 2018; 125(4):615650.
22. Jellinger KA. Multiple system atrophy - a clinicopathological update. Free Neuropathol. 2020; 1:1-17.
23. Jiménez-Jiménez FJ, Alonso-Navarro H, García-Martín E, Agúndez JAG. Cerebrospinal and blood levels of amino acids as potential biomarkers for Parkinson's disease: review and meta-analysis. Eur J Neurol. 2020; 27(11):2336-2347.
24. Koga S, et al. Neuropathology and emerging biomarkers in corticobasal syndrome. J Neurol Neurosurg Psychiatry 2022; 93:919–929.
25. Kovacs GG, Lukic MJ, Irwin DJ, Arzberger T, Respondek G, Lee EB, Coughlin D, Giese A, Grossman M, Kurz C, McMillan CT, Gelpi E, Compta Y, van Swieten JC, Laat LD, Troakes C, Al-Sarraj S, Robinson JL, Roeber S, Xie SX, Lee VM, Trojanowski JQ, Höglinger GU. Distribution patterns of tau pathology in progressive supranuclear palsy. Acta Neuropathol. 2020; 0(2):99-119.
26. Kunz D, et al. Prognostic biomarkers in prodromal α-synucleinopathies: DAT binding and REM sleep without atonia.
J Neurol Neurosurg Psychiatry 2023; 94:532–540.
27. Li Q, et al (2022) A Panel of Plasma Biomarkers for DDx of Parkinsonian Syndromes. Front. Neurosci. 16:805953
28. Litvan I, Agid Y, Calne D, Campbell G, Dubois B, Duvoisin RC, Goetz CG, Golbe LI, Grafman J, Growdon JH, Hallett M, Jankovic J, Quinn NP, Tolosa E, Zee DS. Clinical research criteria for the diagnosis of progressive supranuclear palsy (SteeleRichardson-Olszewski syndrome): report of the NINDS-SPSP international workshop. Neurology. 1996; 47(1):1-9.
29. Madetko N, Alster P, Kutyłowski M, Migda B, Nieciecki M, Koziorowski D, Królicki L. Is MRPI 2.0 More Useful than MRPI and M/P Ratio in Differential Diagnosis of PSP-P with Other Atypical Parkinsonisms? J Clin Med. 2022; 11(10):2701.
30. Massey LA, Jäger HR, Paviour DC, O'Sullivan SS, Ling H, Williams DR, Kallis C, Holton J, Revesz T, Burn DJ, Yousry T, Lees AJ, Fox NC, Micallef C. The midbrain to pons ratio: a simple and specific MRI sign of progressive supranuclear palsy. Neurology. 2013; 80(20):1856-61.
31. McFarland NR, Hess CW. Recognizing Atypical Parkinsonisms: "Red Flags" and Therapeutic Approaches. Semin Neurol. 2017; 37(2):215-227.
32. McFarland NR. Diagnostic Approach to Atypical Parkinsonian Syndromes. Continuum (Minneap Minn). 2016; 22 (4 Movement Disorders):1117-42.
33. Mena AM, Strafella AP. Imaging pathological tau in atypical parkinsonisms: A review. Clin Park Relat Disord. 2022; 16;7:100155.
34. Meyer PT, Frings L, Rücker G, Hellwig S. (18)F‐FDG PET in parkinsonism: differential diagnosis and evaluation of cognitive impairment. J Nucl Med 2017; 58(12):1888–1898.
35. Mortezazadeh et al. Imaging modalities in differential diagnosis of Parkinson’s disease: opportunities and challenges. Egyptian Journal of Radiology and Nuclear Medicine (2021) 52:79.
36. Orimo S, Suzuki M, Inaba A, Mizusawa H. 123I-MIBG myocardial scintigraphy for differentiating Parkinson's disease from other neurodegenerative parkinsonism: a systematic review and meta-analysis. Parkinsonism Relat Disord 2012; 18: 494–500.
37. Peralta et al. Pragmatic Approach on Neuroimaging Techniques for the DDx of Parkinsonism. Movment Disord Clin Pract, 2022; 9(1): 6–19.
38. Postuma RB, Berg D, Stern M, et al. MDS clinical diagnostic criteria for Parkinson's disease. Mov Disord 2015; 30(12):15911601.
39. Respondek G, Roeber S, Kretzschmar H, Troakes C, Al-Sarraj S, Gelpi E, Gaig C, Chiu WZ, van Swieten JC, Oertel WH, Höglinger GU. Accuracy of the National Institute for Neurological Disorders and Stroke/ Society for Progressive Supranuclear Palsy and neuroprotection and natural history in Parkinson plus syndromes criteria for the diagnosis of progressive supranuclear palsy. Mov Disord. 2013; 28(4):504-9.
40. Respondek G, Stamelou M, Kurz C, Ferguson LW, Rajput A, Chiu WZ, et al.
The phenotypic spectrum of progressive supranuclear palsy: a retrospective multicenter study of 100 definite cases. Mov Disord. 2014; 29:1758–1766.
41. Saeed U, Compagnone J, Aviv RI, Strafella AP, Black SE, Lang AE, Masellis M. Imaging biomarkers in Parkinson's disease and Parkinsonian syndromes: current and emerging concepts. Transl Neurodegener. 2017; 6:8.
42. Saeed U, Lang AE and Masellis M. Neuroimaging Advances in Parkinson’s Disease and Atypical Parkinsonian Syndromes. Front. Neurol. 2020; 11:572976.
43. Shir D, Thu Pham NT, Botha H, Koga S, Kouri N, Ali F, Knopman DS, Petersen RC, Boeve BF, Kremers WK, Nguyen AT, Murray ME, Reichard RR, Dickson DW, Graff-Radford N, Josephs KA, Whitwell J, Graff-Radford J. Clinicoradiologic and Neuropathologic Evaluation of Corticobasal Syndrome. Neurology. 2023: 10.1212/WNL.0000000000207397.
44. Srivastava A, Alam P, Caughey B. RTQuIC and Related Assays for Detecting and Quantifying Prion-like Pathological Seeds of α-Synuclein. Biomolecules. 2022;12(4):576.
45. Tondo G, Esposito M, Dervenoulas G, Wilson H, Politis M, Pagano G. Hybrid PETMRI Applications in Movement Disorders. Int Rev Neurobiol. 2019; 144:211-257.
46. Virameteekul et al., Pathological Validation of the MDS Criteria for the Diagnosis of Multiple System Atrophy. Movement Disorders, 38, 3, 2023; 444-452.
47. Walter U, Behnke S, Eyding J, Niehaus L, Postert T, Seidel G, Berg D. Transcranial brain parenchyma sonography in movement disorders: state of the art. Ultrasound Med Biol. 2007; 33(1):15-25.
48. Wenning et al., The Movement Disorder Society Criteria for the Diagnosis of Multiple System Atrophy. Movement Disorders, 37, 6, 2022; 1131-1148.
49. Yang J, Idowu A, Rosenthal L, Mao X. Parkinson's disease fluid biomarkers for differential diagnosis of atypical parkinsonian syndromes. Clin Trans Disc, 2023; 3:e150.
50. Yoo D, Bang JI, Ahn C, Nyaga VN, Kim YE, Kang MJ, Ahn TB. Diagnostic value of α-synuclein seeding amplification assays in α-synucleinopathies: A systematic review and meta-analysis. Parkinsonism Relat Disord. 2022; 104:99-109.
[www.medmag.bg ] 25 ИЗПОЛЗВАНА ЛИТЕРАТУРА:
Е. Хараланова, д.кл.пс. Св. Хараланов, д.м. Първа психиатрична
клиника, УМБАЛНП
„Св. Наум” - София
Смяна на парадигмата
при лечение на шизофрения
След откриването на първите антипсихотици лечението на шизофренията се фокусира върху проявите на шизофренната психоза, пренебрегвайки непсихотичните шизофренни симптоми. В последните години обаче все повече се изяснява, че психотичният епизод е само косвено, преходно и относително краткотрайно следствие от шизофренния процес, докато препсихотичните и постпсихотичните дефицитни („а“-) симптоми са негова пряка и персистираща проява, лежаща в основата на трайната (нерядко прогресираща) социална дезадаптация на пациентите. Този фокус върху непсихотичните шизофренни симптоми коренно променя базисната концепция за болестта и създава предпоставки за смяна на парадигмата при нейното лечение.
ВЪВЕДЕНИЕ
Шизофренията е най-значимата болест в психиатрията[1]. На нея са пос -
ветени над сто хиляди научни публикации, от които десетки монографии, както и няколко специализирани
международни списания[2]. За лечение и рехабилитация на шизофренно
болни ежегодно се отделят милиарди долари, а още толкова се изразходват за фундаментални и приложни научни изследвания[3]. Но въпреки огромните разходи на средства, време и енергия, болестта и до днес остава неразгадана и енигматична. В
опитите за нейното лечение истори -
чески са доминирали разнопосоч -
ни и дори противоположни подходи,
които все още не са интегрирани в
цялостна концепция[4]
Болестта е обособена и описана
за първи път от родоначалника на
съвременните психиатрични класификации Emil Kraepelin (1896), който й
дава названието „dementia praecox”
с презумпцията, че се касае за ранен
вариант на невродегенеративна пре -
сенилна деменция с психотичен де -
бют, но малко по-късно я концептуализира и като ендогенна психоза,
разграничавайки я от манийно-депресивната болест и разделяйки обособената преди него единна ендогенна психоза в две нозологични категории (Крепелинова дихотомия) [1]. Аргументът му за разграничаването е, че при dementia praecox мозъчната патология прогресивно се засилва, което прави болестта практически неизлечима[4]
Съвременното название „шизофрения” (раздвоена психика) е дадено от Eugen Bleuler (1911), който оспорва неизбежността на крайния изход в деменция и изтъква значението на раздвояването (разцепването) на психичните функции[1]. Според концепцията му болестният процес в мозъка пряко обуславя фундаментални (първични) дефицитни симптоми, а косвено активира допълнителни (вторични) защитни механизми, лежащи в основата на психотичните симптоми[1,2]. Тази Блойлерова дихотомия в най-общи линии би могла да се приеме за първообраз на съвременната биполярност между негативни (дефицитни) и позитивни (продуктивни) шизофренни симптоми[3,4].
В нея се обосновава, че диагнозата се определя от фундаменталните симптоми, а психотичните симптоми не са задължителни и може да липсват (латентна и проста шизофрения). Bleuler не споделя терапевтичния нихилизъм на Kraepelin и допуска, че фундаменталните симптоми най-вероятно са свързани с функционални мозъчни (вкл. неврохимични) дефицити, които с бъдещото развитие на фармакологията биха могли да бъдат успешно лекувани. Под влияние на своя асистент Carl-Gustav Jung (1907) той приема, че предизвикана от шизофренния процес слабост на Аза води до нахлуване на несъзнавани афективни комплекси в съзнанието и до активиране на патологични защити на Аза (“психотични защити” по Sigmund Freud), обуславящи психотичните симптоми[2,3]. Ето защо счита, че тези симптоми биха могли да бъдат лекувани и с психологични методи[3,4]
Коренно различен е прагматичният подход на представителя на феноменологичната психиатрия Kurt Schneider (1939), който в противоре -
26 І Medical Magazine | юли 2023
ПСИХИАТРИЯ
чие с Bleuler и Kraepelin пренебрегва негативните (препсихотични и постпсихотични) шизофренни симптоми и се фокусира върху позитивните (психотични) параноидни симпто -
ми, които разделя на такива от I-ви и от II-ри ранг в зависимост от приписваната им диагностична специфичност[1,2,3,4]. Той приема първия психотичен епизод за начало на болестта, от което следва, че лечението на шизофренията трябва да е насоче -
но към психотичните й симптоми[4]
Когато се откриват първите невро -
лептици и става ясно, че те лекуват
именно тези симптоми, теоретично -
то мислене трайно се измества към
тях и към техните механизми[4]. Кри -
териите на Schneider започват повсе -
местно да се прилагат в клиничната практика и в научните изследвания, а концепцията на Bleuler остава в историята[1,4]
ДОМИНИРАЩА ПАРАДИГМА ПРИ ЛЕЧЕНИЕ НА ШИЗОФРЕНИЯ Центрираната върху психозата парадигма продължава да доминира и досега. Тя разглежда шизофренията
като ендогенна психоза, а лечението й − като антипсихотично. Аргументът
е, че психотичните симптоми опре -
делят както диагнозата, така и лечението на болестта, а ефективността
на самото лечение се измерва чрез степента на трайното им потиска -
не. Фактът, че те се повлияват благоприятно от медикаментозна терапия убедително доказва, че в основата
им лежат невробиологични мозъчни
механизми, което сякаш потвърждава имплицитно приетата пряка връзка между шизофренната психоза и болестния (шизофренен) процес в мозъка[5,6,7]. В същата посока е и първият опит за научно обяснение на тази евентуална връзка − класическата допаминова хипотеза за шизофренията, предложена от Arvid Carlsson (1967), който през 2000 г. е удостоен с Нобелова награда за медицина и фармакология[2,4]. Хипотезата му се базира на факта, че всички невролептици са допаминови антагонисти, а лечебният им ефект нерядко се съпътства от медикаментозен
паркинсонизъм, разглеждан като резултат от невролептично индуцирана хиподопаминергия в стриатума. Друг негов важен аргумент е наблюдението, че антипаркинсонови медикаменти (които са допаминови агонисти) могат да предизвикват шизофреноподобни психози при психично здрави лица или да провокират психотичен рецидив при шизофренно болни в ремисия. Оттук той извежда логически (ex juvantibus), че в основата на шизофренията лежи излишък на допамин в мозъка, който се потиска от допаминови антагонисти, но може да бъде предизвикан от допаминови агонисти. По-късно е уточнено, че хипердопаминергия е налице само в мезолимбичната система, която е и основният таргет на антипсихотиците[1,3,4]. Допълнително е установено, че след прекратяване на лечението й психозата в повечето случаи рецидивира и се налага то да бъде подновено, което подсказва, че терапевтичният му ефект е симптоматичен и без него психотичното симптомообразуване в крайна сметка се реактивира[3]. С натрупването на опит става ясно, че психотичните рецидиви оказват неблагоприятно въздействие върху протичането на заболяването, засилвайки персистиращите процесни дефицити[4]. От друга страна се оказва, че продължаването на антипсихотичната терапия по време на клинична ремисия има превантивен ефект по отношение на следващи психотични рецидиви[8.9]. Изследването на механизмите, които са в основата на тези емпирични находки, дава аргументи на нео-Крепелиновата концепция за невродегенерацията[7,9]. Според нея по време на шизофренна психоза се отключват абнормни неврохимични взаимодействия в мозъка, завършващи с ускорена програмирана клетъчна смърт (апоптоза) на корови неврони[10,11]. Тези субклетъчни и клетъчни патологични процеси предизвикват корова атрофия, която се засилва прогресивно след всеки пореден психотичен рецидив и се проявява клинично чрез постепенно задълбочаваща се апатико-абулична промя -
на на личността (dementia praecox по Kraepelin)[10,11]. Ето защо противорецидивното използване на антипсихотиците може да се разглежда и като метод за предотвратяване развитието на постпсихотични (Крепелинови) негативни симптоми[9] Макар все още да не е известно успешно лечение на тези симптоми, възможността за тяхната превенция всъщност разширява обхвата на доминиращата днес парадигма[1,5,6]. Тя разглежда шизофренията като психотично заболяване на мозъка, което може да доведе и до постпсихотична невродегенерация. По такъв начин са интегрирани подходите на Schneider и Kraepelin, но подходът на Bleuler продължава да бъде игнориран.
КРИЗА НА ДОМИНИРАЩАТА ПАРАДИГМА Терминът „ендогенна психоза“ би трябвало да означава, че първопричината за развитието на психотичните симптоми е генетично обусловена уязвимост на определени мозъчни структури и функции, която за известно време може да бъде компенсирана от паралелно активирани защитно-компенсаторни механизми, но рано или късно се стига до нейната декомпенсация и развитие на първи психотичен епизод. Ендогенната предразположеност в психиатрията по принцип предполага продължителен предклиничен (латентен) период, през който е налице компенсирана (клинично непроявена) мозъчна патология преди първите клинични прояви на болестния процес[2,3,7]. Доминиращата засега парадигма разглежда препсихотичният период като предболестен, тъй като приема, че първите болестни прояви на шизофренния процес са психотичните позитивни симптоми[5,6,7]. По тази причина предшестващите ги фундаментални (Блойлерови) негативни симптоми не се приемат за част от болестта, а за проява на ендогенната предразположеност към нея. По същата логика и останалите субклинични и клинични прояви на мозъчни дисфункции, предшестващи първия
[www.medmag.bg ] 27
психотичен епизод, се разглеждат
като маркери на уязвимост, а не като
маркери на заболяването[2,3,4]. Дъл -
гогодишното им изучаване все пак
послужи за основа на влиятелната
днес нео-Блойлерова концепция за
патологията в невроразвитието като
базисен мозъчен механизъм при шизофрения[2]. Според тази концепция
ендогенната предразположеност
(взаимодействайки с патогенни фактори на средата) нарушава нормал -
ната онтогенеза и обуславя най-ран -
ните (препсихотични) прояви на
болестния процес в мозъка, включ -
ващи и Блойлеровите негативни
симптоми, които са известни и като
„а“-симптоми, тъй като названията
им започват с „а“[1,10,11]. От съвремен -
на гледна точка най-важните от тях
са 5: апатия (афективно нивелиране), анхедония, амотивация (абулия, анергия, астения), аутизъм (асоциалност) и алогия (асоциативно блокиране). Наред с тях в препсихотичната
фаза при шизофрения са описвани и когнитивни дефицити, както и
по-редки и по-дискретни невропсихологични и неврологични дефицити (също „а“-симптоми) като: агнозия, апраксия, атаксия, афазия, амнезия, алекситимия, амимия, астазия-абазия, апросексия, апрагматизъм, аграматизъм, асинхронност, аритмичност и асиметрия[7,10,12]. Доколкото
тези експериментално разкрити или клинично проявени функционални дефицити предшестват началото на
първия психотичен епизод и персистират след него, обяснението им от гледна точка на доминиращата засега парадигма поражда сериозни проблеми[10,11,12]. Разглеждането им като
прояви на ендогенната предразположеност към шизофрения не може
да обясни защо и по какъв критерий
те се считат за предболестни, а пси -
хотичните и постпсихотичните симп -
томи − за болестни. Липсата на ясен
критерий за началните прояви на
шизофренния процес доведе до на -
растване влиянието на алтернативната (нео-Блойлерова) гледна точка, според която препсихотичните негативни, когнитивни и неврологични симптоми също са болестни про -
яви на шизофренния процес, които дори са по-близо до мозъчния му субстрат (следователно са по-фундаментални) в сравнение с психотичните[10,11,12]. С натрупването на опит в последните години става все по-ясно, че шизофренната психоза е само преходна и относително краткотрайна фаза от развитието на заболяването, а успешното й лечение в повечето случаи не е достатъчно за връщане на болните към нормален и пълноценен социален живот[5,7]. Вече е установено, че основна причина за тяхната трайна социална (семейна, битова и трудова) дезадаптация са персистиращите препсихотични и постпсихотични шизофренни „а“-симптоми[10,11,12]. Особено важно е откритието, че въпросните симптоми не просто не се подобряват от антипсихотична терапия, но дори се влошават от нея[11,12,13]. От такава гледна точка съвременното лечение на шизофренията не е антишизофренно, а остава фокусирано върху потискането на психотичните симптоми и превенцията на последствията от тях. Следователно, то не е насочено към първопричината − ендогенния болестен процес в мозъка и неговите препсихотични прояви[7,10,11,12]
НОВА ПАРАДИГМА ПРИ ЛЕЧЕНИЕ НА ШИЗОФРЕНИЯ Емпиричните и теоретичните проучвания, провеждани в рамките на концепцията за патология в невроразвитието при шизофрения, постепенно доведоха до преоценка на центрираната върху психозата парадигма. С напредването на технологиите за изследване на мозъчните структури и функции все повече се изяснява, че най-ранните нарушения предшестват първия психотичен епизод и са свързани със структурни и функционални дефицити в областта на челната кора (хипофронталност). Тези препсихотични обективни находки при лица с повишен генетичен и клиничен риск за развитие на шизофренна психоза стимулираха нови хипотези за мозъчните механизми на болестта. Направена беше радикална ревизия и на класическата допаминова хипотеза. Спо -
ред ревизираната й версия, хипердопаминергията в мезолимбичната
система е вторично следствие от първична хиподопаминергия в мезокортикалната система, която нормално упражнява инхибиторен контрол върху мезолимбичната[7]. Оттук следва, че болестният процес в мозъка пряко засяга структурата и функцията на челната кора, а хиперактивирането на подкорови кръгове (в основата на шизофренната психоза) не е пряко свързано с шизофренния процес, а е косвен резултат от преходната им дезинхибиция[4]. Самият Arvid Carlsson (2006) също ревизира хипотезата си и започна да разглежда първичното нарушение при шизофрения като резултат от ендогенно обусловена хиподопаминергия в мезокортикалната система[4]. Нашият екип разработи интегративна концепция, според която шизофренният процес пряко обуславя хиподопаминергия в мезокортикалната система, водеща до трайни препсихотични сензорни, моторни, когнитивни, афективни и социални дефицити („а“-симптоми), но от друга страна може да доведе и до дефицит на инхибиторен контрол върху мезолимбичната система, предизвиквайки в нея преходна хипердопаминергия, проявена чрез шизофренните психотични симптоми[4]. С течение на времето става все по-очевидно, че шизофренният процес пряко предизвиква трайни увреждания в челната кора (включващи и мезокортикална хиподопаминергия), които са в основата на препсихотичните „а“-симптоми, а изтъкваното досега преходно подкорово хиперактивиране (включващо и мезолимбична хипердопаминергия) е само вторично следствие от загубата на инхибиторен контрол от челната кора[4,7,10,11,12]. От своя страна, антипсихотичната терапия просто компенсира загубения инхибиторен контрол, но не лекува първичните процесни дефицити, тъй като не само не подобрява базисната хипофронталност, а дори я влошава[4,13]. Тази нова гледна точка радикално променя и парадигмата при лечение на заболяването. Логично е да се допусне, че щом антипсихотичната терапия
28 І Medical Magazine | юли 2023 ПСИХИАТРИЯ
А. Бешков1 , П. Въргов2 , К. Акабалиева3 ,
В. Акабалиев 4
1Катедра по психиатрия и ме-
дицинска психология, Меди-
цински университет - Пловдив 2магистър-психолог
3Катедра по психиатрия и ме-
дицинска психология, Меди-
цински университет – София
Психофармакотерапия:
крос-културални и етнически
съображения
Ключови думи: Фармакокинетика, фармакодинамика, фармакогеномика, психофармакотерапия, култура, етнос.
4без афилиация В настоящия текст подчертаваме някои ключови фактори, с които клиницистите трябва да са наясно, когато практикуват психиатрия в етнически различни популации – фармакокинетични и фармакодинамични принципи и тяхното приложение при фармакологичното лечение на психиатрични състояния. Обръщаме внимание на вариациите сред биологичните (фармакологични) фактори, определящи различните реакции при психофармакологичното лечение в различни етнически групи и култури. Поставяме акцент върху ценността и клиничната приложимост на компетентността в тази област в настоящата епоха на нарастващи глобализация, миграция и мултикултурализъм и в контекста на бурното развитие на фармакогеномиката и бъдещето на персонализираната медицина/психиатрия.
ВЪВЕДЕНИЕ
Въпреки че психиатричните лекар -
ства се използват по цял свят, из -
следванията за определяне на
точни фармакокинетични и фарма -
кодинамични профили сред различни етнически групи са ограничени.
Когато става въпрос за лекарстве -
на терапия, психиатрите често преминават към едноизмерен поглед върху пациента и прилагат категориен подход за предписване на лекарства (напр. диагностични подтипо -
ве на отговор, придържане/липса на
придържане към лечението, повлияващ се/неповлияващ се и т.н.). Поради „далтонисткия (сляп за цвета)“
подход, свързан с честото игнорира -
не на значителни и автентични ин -
дивидуални вариации, се счита, че
хората с различен етнически произ -
ход не се различават по своите био -
логични реакции или възприятия за медикаментозното лечение. Във връзка с това пациентите, които се оплакват от нежелани ефекти и же -
лаят промени в дозировката, звучат така, сякаш са „несътрудничещи“.
Поради все по-силно засилващите се глобализация и миграция клиницистите вече по-често лекуват пациенти с различен произход, поради което трябва да са наясно с културалните различия в отговора на лечението и с ролята на етническата принадлежност и културата в рутинната си практика. С доближаването до персонализиран медицински подход в съвременната епоха, разбирането на етническите и културалните фактори и техните взаимодействия с биологичните вариации е още по-важно.
ЕТНИЧЕСКА ПРИНАДЛЕЖНОСТ Етническата принадлежност и култура определят значително индивидуалните фармакологични реакции, които се оформят както от средови, така и от генетични фактори. Медицинската практика и изследвания разпознават комбинация от социал -
ни, културални и фенотипни прилики, а не генотипни различия. Точно връзката на фенотипното сходство с фармакогенетичните вариации в лекарствения метаболизъм съставлява клинично значимите етнофармакогенетични вариации.
ФАРМАКОКИНЕТИЧНИ ФАКТОРИ Лекарствата и други чужди субстанции (ксенобиотици) се метаболизират от редица ензими, чиито дейности, както по генетични, така и по свързани със средата причини, варират значително между индивидите и етническите групи. Метаболизмът на повечето психотропни лекарства включва основно фазата на оксидация, медиирана от изоензимите на цитохром Р-450 (CYP450). Има 57 CYP450 гени, 15 от които участват в лекарствения метаболизъм при хора. В психиатрията отговорни за метаболизма на повечето психотропни лекарства са CYP2D6, CYP2C19, CYP3A4, CYP1A2 и
30 І Medical Magazine | юли 2023
ПСИХИАТРИЯ
CYP2C9. Генетичните вариации в тези CYP450
гени могат да доведат до липсваща, намале -
на, нормална или повишена ензимна актив -
ност. Въз основа на тези генетични вариации
може да се предвиди метаболитният фено -
тип на индивида. Индивидите, които носят
два алела, кодиращи „нормалната“ ензим -
на функция, се класифицират като нормал -
ни метаболизатори (НМ), докато тези, кои -
то носят два алела, кодиращи неактивна
или липсваща ензимна функция, се опреде -
лят като слаби метаболизатори (СМ). Освен
това, индивиди, които носят един нормален и един неактивен/отсъстващ алел, се класифицират като междинни метаболизатори (ММ), а тези с генни дупликации или мултипликации се определят като ултра-бързи метаболизатори (УБМ). Разпространението на НМ, ММ, СМ и УБМ варира значително сред различните етнически популации (Ozawa et al., 2004; van Booven et al., 2010).
CYP2D6 е отговорен за метаболизма на 2030% от всички лекарства, включително всички трициклични антидепресанти (ТАД), повечето селективни инхибитори на серотониновия транспорт (СИСТ) и около полови -
ната от всички антипсихотици. CYP2D6 е силно полиморфен с над 100 алела, въпреки че само няколко от тях са обичайни. Тези общи алели варират значително между етносите. Всъщност 5–10% от кавказците и 1–2% от азиатците са СМ на базата на CYP2D6 генотип (Poolsup et al., 2000). По сходен начин, в различните етнически групи значително варират нивата на дублиране на гена на CYP2D6 и съответния фенотип на УБМ. Честотата варира от 1–2% при кавказците, 7–10% при средиземноморските популации, 19% при арабите и до 29% при популациите от Източна Африка (Teh and Bertilsson, 2012).
CYP2C19 е особено важен в метаболизма на СИСТ. Индивиди с два неактивни алела се считат за CYP2C19 СМ; докато носителите на алела CYP2C19*17 се счита, че имат УБМ метаболитен фенотип. Например, генетични изследвания на CYP2C19 са установили, че 15-30% от някои азиатски популации са СМ в сравнение с 3-6% от кавказците и 2-4% от африканците (Fricke-Galindo et al., 2016).
Цялостните генетични познания за фармакокинетиката предполагат необходимостта от коригиране на дозата в съответствие с генетичните вариации на CYP450, особено в CYP2D6 и CYP2C19, както и при гени, различ -
ни от CYP450, в
съответствие с междуиндивидуалните и междуетническите фармакокинетични вариации.
Консорциумът за внедряване на клинична фармакогенетика (CPIC - www.pharmgkb.org/ page/cpic) е разработил насоки за дозиране на СИСТ въз основа на генотипове CYP2D6 и CYP2C19 (Hicks et al., 2015).
ФАРМАКОДИНАМИЧНИ ФАКТОРИ Генетични полиморфизми на гени, кодиращи протеини/ензими, които участват в синтеза, рецепторите (брой, чувствителност, активност), транспорта и разграждането на невротрансмитери, са свързани с вариации в отговора на психотропните лекарства. Сред тях, полиморфизмът на свързаната с транспортера на серотонина област
(5-HTTLPR) показва, че притежаващите дългия алел на 5-HTTLPR депресивни пациенти имат по-силен отговор към СИСТ, отколкото тези с късия алел (Ng et al., 2013), въпреки че резултатите са противоречиви.
5-HTTLPR се свързва с ефикасността на СИСТ по начин, зависим от етническата принадлежност (Bousman et al., 2014). Кавказци с дълъг/дълъг алели, но не и дълъг/къс или къс/къс алели, имат по-силен отговор и нива на ремисия към есциталопрам, в сравнение с корейците. Прави впечатление, че 19–29% от източноазиатците носят дългия алел на 5-HTTLPR, в сравнение със 72% от африканците и 57% от кавказците (Goldman et al., 2010), така че има доказателства за междуиндивидуални и междуетнически различия в отговора на СИСТ в зависимост от 5-HTTLPR генотипа.
Честотите на алелите на касаещите фармакодинамиката полиморфизми се свързват с различна ефикасност на психофармакотерапията и/или нежелани ефекти сред различните етнически групи. Всъщност, почти всички полиморфизми, за които е доказано, че имат умерена или по-голяма връзка с отговора на психотропните лекарства и/или нежеланите ефекти, имат значително различаващи се алелни честоти в различните етноси.
Скорошните постижения в технологията за генотипизиране са полезни за прогнозиране на индивидуалните метаболитни фенотипове, рисковете от странични ефекти и вероят-
[www.medmag.bg ] 31
ността за лекарствен отговор. Използването на генотипизиране може да оптимизира клиничния отговор и да предотврати прекомерни неблагоприятни ефекти за отделни пациенти от различен произход. Чрез систематично характеризиране на естеството и функцията на полиморфизмите, генотипно ръководената фармакотерапия може значително да подобри терапевтичния режим за отделни пациенти в различни етнически и културални групи. В световен план вече има десетки касаещи психиатрията търговски фармакогенетични тестове, разработени и предлагани на пазара за тази цел. Повечето
от тези тестове обаче все още не са адекватно оценени, а оценените са ограничени до кавказките популации.
УСТАНОВЕНИ ЕТНИЧЕСКИ РАЗЛИЧИЯ В
ТЕРАПЕВТИЧНИТЕ ЕФЕКТИ
Открити са разлики между кавказки, азиатски и други етнически групи в дозирането и отговора спрямо трициклични антидепресанти и антипсихотични лекарства; данните като цяло са смесени. Поради методологичните слабости етно-психофармакологичните проучвания до голяма степен не са успели да изяснят дали наистина съществува различен отговор на психотропните лекарства между етническите групи и дали тези различия имат биологична основа или са резултат от социо-културални фактори. Тези ограничения включват несъответна дефиниция на етническа група, липса на интеграция с генетичните данни и липса на контролиране на физическите, хранителните и свързаните със средата променливи (Ng, 2008). Смята се, че допълнителни фактори като тютюнопушене, хранителни табута и навици играят роля при различните етнически групи.
Повечето от наличните данни идват от САЩ и най-обсъждани са антипсихотиците. Междурасовите различия в дозите на антипсихотиците, които предизвикват странични ефекти, са широко проучени при американци от азиатски произход (японски, корейски и китайски). Binder & Levy (1981) съобщават, че 95% от азиатските хора в тяхната извадка са развили екстрапирамидни странични ефекти в рамките на 2 седмици след започване на лечението, докато такива са имали само 60% от чернокожите и 67% от белите пациенти. При сравнение на еквивалентни дози на халоперидол при китайски и не-китайски пациенти, Jann et al. (1989) съ -
общават, че китайците са имали по-високи нива на екстрапирамидни странични ефекти и по-високи нива в кръвната плазма. В подобно проучване Chang et al. (1991) съобщават за намалени плазмени нива на халоперидол и като цяло по-ниски съотношения на халоперидол в стабилни нива при китайски пациенти, в сравнение с не-китайци, потвърждавайки своите по-ранни данни (Chang et al., 1987) и предполагайки, че е възможно да действат различни метаболитни фактори. Съобщава се, че азиатските американци имат значително по-високи серумни нива на халоперидол и по-изразен пролактинов отговор, в сравнение с белите пациенти, получаващи същата доза. Твърди се, че по-ниските намалени съотношения на халоперидола при американците от азиатски произход се дължат на по-бавна скорост на редукция и метаболизъм (Chang et al., 1987; Jann et al., 1989). Има хипотеза, че ензимът CYP2D6 играе решаваща роля в този метаболизъм.
Ключови разлики между различните етнически групи са посочени и за антидепресантите. Съобщава се за по-ниски плазмени нива на трициклични антидепресанти и по-късни плазмени пикове при белите, отколкото при азиатците (с произход от Далечния Изток и от индийския субконтинент) (Rudorfer et al., 1984). При изследване на кинетиката на нортриптилин при доброволци без депресия, Gaviria et al. (1986) отбелязват, че предполагаемата свръхчувствителност към лекарството при техните испаноговорящи доброволци се дължи на рецепторна свръхчувствителност, тъй като тази група реагира на по-ниски дози и има повече странични ефекти при приемане на трициклични антидепресанти. Има данни, че азиатски пациенти с тежка депресия реагират на по-ниски комбинирани концентрации на имипрамин и дезипрамин в сравнение с дозите, използвани за белите групи (Hu et al., 1983). Съобщава се, че афро-американците имат по-високи нива на неврологични странични ефекти, когато приемат антидепресанти (Escobar & Tuason, 1980), но механизмите на подобни действия не са изяснени. Вътрешногруповите вариации във фармакокинетиката на трициклиците значително надвишават междугруповите различия и бавното достигане на пикова концентрация при белите хора може да се дължи на по-бързо хидроксилиране в тази група. Възможно е ан -
32 І Medical Magazine | юли 2023
ПСИХИАТРИЯ
тидепресанти като моклобемид да покажат по-големи вариации в метаболизма, в сравнение с други антидепресанти, поради вариациите в моноаминооксидазната (МАО) активност между етническите групи. В заключение, дозите на антидепресантите трябва да бъдат внимателно индивидуализирани за продължителен период от време.
Сред японски пациенти литият се оказва ефективен при по-ниски нива в кръвната плазма. Тайванските па -
циенти биват поддържани на по-високи плазмени нива от японските,
но по-ниски от тези при америка -
нците от китайски произход (Chang et al., 1991). Тайванските пациенти
се поддържат при нива на литий от 0,5-0,79 mmol/l, докато китайските
пациенти имат нива от около 0,710,73 mmol/l, но при американците от китайски произход не са докладвани фармакокинетични различия. Фактори на средата като времето (горещо лято, което води до дехидратация) и индивидуалните фактори като диетата стават още по-важни при предписването и поддържащото лечение с литий при отделните пациенти.
Доказателствата относно отговора на бензодиазепините и техните дози
в различните етнически групи остават неубедителни. Едно проучване установява, че въпреки по-бавното изчистване от диазепам при американците от азиатски произход и по-високите серумни нива сред тях спрямо белите американци, лекарството не демонстрира значителни агонистични ефекти (Ghoneim et al., 1981). Други изследователи обаче показват фармакокинетични различия в две групи – американци от азиатски и от кавказки произход (Zhang et al., 1990).
ПЛАНИРАНЕ НА ФАРМАКОЛОГИЧНО ЛЕЧЕНИЕ ПРИ ПАЦИЕНТИ ОТ МАЛЦИНСТВЕНИ ЕТНИЧЕСКИ ГРУПИ Преди предписване: проверете диетата; проверете религиозните табута и ритуали; проверете за тютюнопушене, употреба на алкохол и наркотици и отношението към тях. Докато предписвате: започнете с по-ниска доза; придържайте
се към нисък праг за идентифициране на странични ефекти, базирано на доказателства; коригирайте редовно дозите, ако е необходимо; предоставяйте информация. След предписване: наблюдавайте страничните ефекти; проследявайте придържането; проверете факторите на околната среда/хранителния режим
ЗАКЛЮЧЕНИЕ Клиницистите трябва да са наясно с различната безопасност и ефикасност на фармакологичните агенти при хора от различни етнически групи. Крос-културалната психофармакотерапия остава недостатъчно проучена, особено по отношение
на новите психофармакологични агенти, които могат да имат потенциални междуетнически различия. Фармакогенетиката, която показва значителни етнически различия, може да помогне на клиницистите да вземат терапевтични решения. При все това, трябва да се вземат предвид и влиянието на диетата, начина на живот, системните и културалните променливи върху лекарствения отговор. Такова многостранно разнообразие във фармакотерапевтичния отговор може да бъде обединено в интегриран био-психо-социо-културален модел като основа за систематично изследване и клинично приложение. За да се даде възможност за гъвкаво индивидуализирано приспособяване на терапията с психотропни лекарства, основаната на доказателства психофармакотерапия трябва да бъде адаптирана съответно на биологичното и на социо-културалното многообразие на отделните пациенти.
1. Binder, E. & Levy, R. (1981). Extrapyramidal reactions in Asians. American Journal of Psychiatry, 138, 1243-1244.
2. Bousman, C. A., Sarris, J., Won, E. S. et al. (2014). Escitalopram efficacy in depression: a cross-ethnicity examination of the serotonin transporter promoter polymorphism. Journal of Clinical Psychopharmacology, 34(5), 645–648.
3. Chang, S. S., Chen, T.Y., Lee, C. A., et al. (1987). Lithium plasma reduced haloperidol/ haloperidol ratios in Chinese patients. Biological Psychiatry, 22, 1406-1408.
4. Chang, S. S., Jann, M., Hwu, H.-G., et al. (1991). Ethnic comparison of haloperidol and reduced haloperidol plasma levels: Taiwan Chinese versus American non-Chinese. Journal of the Formosan Medical Association, 90, 572-578.
5. Escobar, J. I. and Tuason, V. B. (1980).
Antidepressant agents – a cross-cultural study. Psychopharmacology Bulletin, 16(3), 49–52.
6. Fricke-Galindo, I., Cespedes-Garro, C., Rodrigues-Soares, F. et al. (2016). Inter-ethnic variation of CYP2C19 alleles, ‘predicted’ phenotypes and ‘measured’ metabolic phenotypes across world populations. The Pharmacogenomics Journal, 16(2), 113–123.
7. Gaviria, M., Gill, A. & Javaid, J. (1986). Nortriptyline kinetics in Hispanic and Anglo subjects. Journal of Clinical Psychopharmacology, 6, 227-231.
8. Ghoneim, M., Kortilla, K., Chiang, C.K., et al. (1981). Diazepam effects and kinetics in Caucasians and Orientals. Clinical Pharmacology and Therapeutics, 29, 749-756.
9. Goldman, N., Glei, D. A., Lin, Y-H. and Weinstein, M. (2010). The serotonin transporter
polymorphism (5-HTTLPR): allelic variation and links with depressive symptoms. Depression and Anxiety, 27(3), 260–269.
10. Hicks, J. K., Bishop, J. R., Sangkuhl, K. et al. (2015). Clinical Pharmacogenetics Implementation Consortium (CPIC) guideline for CYP2D6 and CYP2C19 genotypes and dosing of selective serotonin reuptake inhibitors. Clinical Pharmacology and Therapeutics, 98(2), 127–134.
11. Hu, W., Lee, C., Yang, Y., et al. (1983). Imipramine plasma levels and clinical response. Bulletin of the Chinese Society of Neurology and Psychiatry, 9, 40-49.
12. Jann, M., Chang, W., Davis, C., et al. (1989). Haloperidol and reduced haloperidol plasma levels in Chinese vs non-Chinese psychiatric patients. Psychiatry Research, 30, 45-52.
13. Ng, C. H. (2008). Research directions
in ethno-psychopharmacology. In EthnoPsychopharmacology: Advances in Current Practice, ed. C. H. Ng, K. M. Lin, B. Singh and E. Chiu. New York, Cambridge University Press, 169–176.
14. Ng, C., Sarris, J., Singh, A. et al. (2013). Pharmacogenetic polymorphisms and response to escitalopram and venlafaxine over 8 weeks in major depression. Human Psychopharmacology, 28(5), 516–522.
15. Ozawa, S., Soyama, A., Saeki, M. et al. (2004). Ethnic differences in genetic polymorphisms of CYP2D6, CYP2C19, CYP3As and MDR1/ABCB1. Drug Metabolism and Pharmacokinetics, 19(2), 83–95.
16. Poolsup, N., Li Wan Po, A. and Knight, T. (2000). Pharmacogenetics and psychopharmacotherapy. Journal of Clinical
Pharmacy and Therapeutics, 25(3), 197–220.
17. Rudorfer, E., Lam, E., Chang, W., et al. (1984). Desipramine pharmacokinetics in Chinese and Caucasian volunteers. British Journal of Clinical Pharmacology, 17, 433-440.
18. Teh, L. K. and Bertilsson, L. (2012). Pharmacogenomics of CYP2D6: molecular genetics, interethnic differences and clinical importance. Drug Metabolism and Pharmacokinetics, 27(1), 55–67.
19. Van Booven, D., Marsh, S., McLeod, H. et al. (2010). Cytochrome P450 2C9-CYP2C9. Pharmacogenetics and Genomics, 20(4), 277–281.
20. Zhang, Y., Reviriego, J., Lou, Y., et al. (1990). Diazepam metabolism in native Chinese poor and extensive hydroxylators of S-mephenytoin. Clinical Pharmacology and Therapeutics, 48, 496-502.
[www.medmag.bg ] 33
ИЗПОЛЗВАНА ЛИТЕРАТУРА:
М. Ганчев, амбулаторен психиатър
МЦ "Стимул" - София
Тревожният
срещаното, но и най-НЕспецифичното оплакване в
амбулаторната психиатрия
При възникване на по-сериозни предизвикателства, които налагат мобилизиране, концентриране, включително и на организма,
зически сблъсък за оцеляване, тревожността
защото включва адаптационните механизми, активира личността за справяне с важни проблеми.
От друга страна хронич -
ният стрес води до поддържане на високи нива на тревожност, а това е токсично за организма.
Отделят се високи нива стрес невро -
медиатори, които вместо да подпомагат организма, стават токсични за него. Окастрят се дори рецепторите
за молекулите, които ни балансират
и успокояват и човек не може да премине в състояние на почивка.
Някои хора са по-уязвими и сравни-
телно малка продължителност или
значимост на обстоятелствата водят
до отключване на т.нар. генерализирано тревожно разстройство. При
него има усещане за неясна застраше -
ност, усещане като че ли нещо лошо
предстои и може да се случи, като например здравословен проблем за тях
или за техни близки. Тази свободно
плаваща тревожност в днешно време
много често се допълва със т.нар. со -
матизации – телесни симптоми, които имат функционален характер и не
се открива потвърждение за тях при
множество медицински изследвания. Пациентите месеци наред посещават невролог, кардиолог, гастроентеролог, ендокринолог преди някой да се сети да ги насочи към психиатър. Най-често те са 3 групи – вегетатив-
ни, псевдоневрологични и свързани с храносмилателната система.
Вегетатичните симптоми най-често са сърцебине, ускорен пулс, играене на кръвното налягане, изпотяване, топли вълни.
Псевдоневрологичните са различни болкови оплаквания, изтръпвания, стягане в гърдите, буца в гърлото, замайване, стягане на челюстта, трудно преглъщане.
Гастроинтестиналният тракт почти винаги реагира – дали със забавен или ускорен пасаж, подуване, парене и др.
Генерализираното тревожно разстройство налага лечение, като често симптомите се поддават на пълно
излекуване, но след месеци и години могат отново да се завърнат.
Нелекуваното тревожно разстройство след време често води до спад в биотонуса. Пациентът става вял, появяват се виновностови идеи, и такива за безпреспективност, отчаяние. Когато спадне биотонуса, обаче не се лекува тревожния симптом, а депресията. Ако не се лекува депресията пациентите често намират фатален за тях изход.
Вариант на нормалпсихолоогичната тревожност е реакцията на скръб след загуба на близък. Няма утеха за майка загубила детето си, няма срок, в който да се очаква тези емоции да отшумят. Ако обаче месеци след събитието човек става все по-зле, вместо да се стабилизира е необходимо да се вземат мерки. Реакцията на скръб може да премине в генерализирано тревожно разстройство.
Хората са различни. Някой са по-чувствителни, по-реактивни на
34 І Medical Magazine | юли 2023
синдром - най-често
Тревожността като емоция вероятно е възникнала еволюционно във връзка с нуждата от по-добра адаптация на човека.
когато се налага фи -
полезна,
ПСИХИАТРИЯ
е
случващите се около отях събития, имат тревожна личностова структура. Други по-леко приемат дори неблагоприятните събития около тях. Съответно трябва да разграничаваме дали не се касае по-скоро за личностови, за невротични тенденции, а не за някое заболяване, което да трябва да се лекува. Водещо е разбира се страданието и нарушеното функциониране на индивида, не толкова мащабът на събитията. И тук обичайно се налага да се проведе лечение, но изисква и много повече усилия от страна на пациента за промяна.
Паник атаки – внезапни кризи, свързани със срах, бурна вегетативна симптоматика, пациантите често търсят помощ в спешния кабинет. Атаките продължават сравнително кратко. Разбира се, че фонът е тревожен, но те са

много
по-биологични, възникват при дезрегулация на нарадренергичната система, представляват изръсване на стрес медиатори. Налага се медикаментозно лечение.
Често пациентите идват в кабинета, като съобщават че са тревожни, но същевременно не могат да си намерят място, ходят напред-назад, изискват незабавно да им се помогне. Такова представяне на тревожността представлява всъщност ажитация, която налага съвсем друго лечение.
Тревожността често съпътства редица телесни заболявания. Че какъв друг да е емоционалния фон, когато си болен? При пациенти с тежки хронични заболявания не трябва да се отказва помощ, за да им се намали тревож-
[www.medmag.bg ] 35
ността, въпреки, че водещата причина е друго страдание.
Тревожността съпровожда и други състояния – например употребата на вещества. Един абстинентен пациент (който употребява например алкохол или хероин) се представя с тревожни оплаквания, сърцебиене и др., но външният вид и подробната анамнеза ще ни дадът информация какво да лекуваме – в случая зависимостта.
Тревожността е емоцията, която заедно със страха, е обичайното представяне на пациенти с психоза. Когато страховете извират не от реалността, има странни, често плашещи идеи, чувство за страшеност, усещане, че група лица искат твоето унищожение – страховете ръководят поведението на пациента и бързащият лекар може да определи пациента като тревожен, а не параноиден. Като заключение, тревожността е може би най-честото оплакване в амбулаторната практика. За да сме полезни на пациентите винаги трябва да се търси второ, трето оплакване, други симптоми. Ако са налице страхове, употреба на вещества, спад в биотонуса, странни идеи, личностова патология, пациентът трябва да се насочи към психиатър за комплексно
изследване и лечение.
ЛЕЧЕНИЕТО НА ТРЕВОЖНИЯ СИНДРОМ

МОЖЕ ДА СЕ РАЗГЛЕДА ПО СЛЕДНИЯ НАЧИН: Ако сме определили, че става въпрос за Генерализирано тревожно разстройство – обичайното лечение е медикаментозното - антидепресант, като според оплакванията за кратко се добавя анксиолитик, който да подобрява съня или по-бързо да намали тревожността.
Личностовите разстройства изискват много по-комплексни усилия, като освен избрана таргетна анксиолитична терапия се препоръчва психотерапия, която да подпомогне пациента да промени свои когнитивни и поведенчески схеми, за да може да се адаптира по-добре.
Нормалпсихологичната тревожност не е необходимо да се лекува. Тя подобрява адаптацията, подпомага човек да насочи вниманието и да се активира за да преодолее предизвикателствата, които предстоят. Реакцията при скръб, както и тревожността при възрастни и хронично болни пациен -
ти налага щадящ, но ефективен подход, който се определя индивидуално. Например при по-възрастни пациенти се избягват анксиолитици поради седацията, паметовите нарушения, ортостатичната хипотония.

Ажитацията, тревожността при зависимости, психози налагат друг вид терапия, който е насочена към ядрото на проблема и това е работа на психиатъра.
Психотерапията е важна и при генарализираното тревожно разстройство, като според мен тя винаги е необходима като допълваща медикаментозното лечение. Пациентът трябва да се научи на нови модели на поведение, така че стресът да не го поваля.
Друг немедикаментозен метод за тревожни състояния, който прилагаме в практиката е Неврофийдбек трейнингът (за по-кратко фийдбек или биофийдбек). Това е метод, при който променена (разстроена, абнормна) мозъчна активност се възстановява чрез специализирано трениране с цел възвръщане към нормалните показатели и премахване на оплакванията. Може да се прилага самостоятелно или допълващо по назначение на психиатър за пациенти, които предпочитат да не приемат медикаменти, когато имат лоша поносимост, при бременност, при напълняване или когато няма достатъчен ефект с конвенционална медикаментозна терапия.
Започва се с изследване на състоянието на мозъчните функции чрез ЕЕГ (електроенцефалографско) изследване. Проверява се дали има потиснатост, забавеност или обратното - свръхактивиране на мозъчната кора. Това са ключовите биологични причини, които се проявяват с тревожно-депресивни симптоми. Според установените резултати от ЕЕГ изследването се подготвя протокол (параметри), по който се извършва фийдбек трейнинг. Самият подход представлява трениране на мозъчната активност чрез компютърна програма и специална игра, която се играе единствено с мисълта. По този начин постепенно се тренира достигането на желаното състояние на мозъчна активност - което е било определено като цел. Пациентът
се научава да остава все по-дълго в това състояние, вече извън играта, извън медицинския кабинет и оплакванията постепенно отшумяват.
36 І Medical Magazine | юли 2023
ПСИХИАТРИЯ
250 mg сух екстракт от Hypericum perforatum L.



Депресия? Тревожност?





Неспокоен сън?
Лекарствен продукт за лечение на лека до умерена депресия, тревожност и състояния на напрегнатост.

За възрастни – 2 х 250 mg дневно. Търсете в аптеките. Без рецепта.

Растителен лекарствен продукт. Съдържа екстракт от жълт кантарион. Лекарство за възрастни над 18 годишна възраст. Лекарствен продукт, отпускан без лекарско предписание. Преди употреба прочетете листовката. Рег. No. 20030262. КХП: BG/MA/MP-59499/06.07.2022 г.

За допълнителна информация: Eвофарма ЕООД | 1618 София, ул. „Пирински проход“ 24, Tел.: (02) 962 12 00, info@ewopharma.bg www.ewopharma.bg



Информация, относно това как Евофарма събира, обработва и съхранява лични данни може да получите тук: https://www.ewopharma.bg/politika-za-poveritelnost/

Б. Борисов, д.м. Клиника по нефрология и диализа, Медицински университет, Плевен
Ключови думи:
Диализно лечение, мастно-разтворими витамини, заместителна витаминна терапия, хронично бъбречно заболяване.
Роля
на мастно-разтворимите витамини при пациенти на
диализно
лечение
пациенти водят до недостатъчност на редица витамини и микроелементи, които често изискват допълнително заместване. Цел на настоящия обзор е да представи тенденциите за променения прием и биологична наличност на мастно-разтворимите витамини при пациентите, лекувани с диализа и да покаже тенденциите, свързани с необходимостта от тяхното допълнително включване в лечението им.
Броят на болните, лекувани с диализни методи нараства в световен мащаб и тази тенденция ще се запази поне в близките 20 години. Хранителните ограничения при тези пациенти водят до недостатъчност на редица витамини и микроелементи, които често изисват допълнително заместване.
Цел на настоящият обзор е да представи тенденциите за променения прием и биологична наличност на
мастно-разтворимите витамини при пациентите, лекувани с диализа и да
покаже тенденциите, свързани с не -
обходимостта от тяхното допълнител-
но включване в лечението им.
ВИТАМИН А
Витамин А (ретинол, бета-каротин)
се среща в природата като водноразтворимата прекурсорна форма – бета-каротин или в липидоразтворимата форма – ретинол. Храните от
животински произход съдържат ретинол, а тези от растителен произход – бета-каротин. Витамин А е важен за функцията на ретиналните
клетки; има изразен антиоксидативен ефект, има значение за правилното функциониране на имунитета и участва в диференциацията на епителните клетки. Симптомите на хиповитаминоза А включват нощна слепота, ксерофталмия, кератинизация на клетките, анемия, камъни в бъбреците, забавен костен растеж и нарушено образуване на зъбния емайл. Хипервитаминозата се характеризира с: декалцификация на костите, хипокоагулация, аменорея, кожни обриви, гадене, повръщане, замъглено зрение и загуба на апетит. Максималната дневна доза витамин А е 900 mcg/ ден за възрастни мъже и 700 mcg/ден за възрастни жени. Съдържа се главно в черния дроб, млечните продукти и рибата. В плодовете и зеленчуците се намира под формата на бета-ка-
ротин. Ретинолът се свързва с ретинол-свързващ протеин-4 (RBP4) и се секретира от черния дроб в комплекс с преалбумин. Взаимодейства с тетрациклинови антибиотици (риск от интракраниална хипертония), антиациди (повишаване на ефикасността им), антикоагуланти (риск от кървене), секвестранти на жлъчните киселини холестирамин и колестипол (намаляване на абсорбцията на витамин А) и др.
При пациенти с хронично бъбречно заболяване катаболизмът на RBP4 е нарушен, което води до повишени нива на несвързан RBP4. Следователно не е необходимо да се предписват добавки, съдържащи ретинол, при тази група пациенти. В много проучвания е доказана тенденцията към хипервитаминоза А при пациенти на хемодиализа и перитонеална диализа[1] При пациенти на перитонеална диализа, серумните концентрации на ре -
38 І Medical Magazine | юли 2023
Броят на болните, лекувани с диализни методи нараства в световен мащаб и тази тенденция ще се запази поне в близките 20 години. Хранителните
тези
НЕФРОЛОГИЯ
ограничения при
тинол, алфа- и бета-каротин често са намале -
ни и са обратно пропорционални на нивата на
интерлевкин-6 и С-реактивен протеин[2]
ВИТАМИН Д
Витамин Д (калциферол) се синтезира нормално в човешкия организъм. Синтезата му започва в черния дроб, с образуването на холекалциферол, който трябва да премине двуетапно
хидроксилиране на 1-во и 25-то място в неговата молекула, за да се превърне в активен витамин. Основната, циркулираща в човешкия организъм прекурсорна форма е тази на 25(OH) vit. Д, като за оптимални се приемат нивата >30 ng/mL[4]
Ефектите му дълго време се заключаваха в поддържането на калциево-фосфорното равновесие в човешкия организъм, но напосле -
дък се установи, че този витамин участва
активно в различни процеси, като диабет, автоимунни, сърдечно-съдови и бъбречни заболявания, туберкулоза, депресия, невродегенеративни заболявания и неоплазии.
При пациенти с хронични бъбречни заболявания (ХБЗ), намалява активността на ензима 1α-хидроксилаза и това води до намалена продукция на активен витамин Д.
Двете големи научно-практически платформи, занимаващи се с аспектите на бъбречното
здраве – Инициативата за качество на резултатите при бъбречните заболявания (KDOQI), така и Глобални резултати за подобряване на бъбречните заболявания (KDIGO), препоръчват проверка и допълване при ниски серумни нива на 25(OH)D, при ХБН и пациенти на диализа.
Витамин Д взаимодейства с естрогени, изониазид, тиазиди (те повишават нивата на витамин Д в кръвта) или антиациди, блокери на калциевите канали, севеламер, холестирамин, фенобарбитал, фенитоин и други антиконвулсивни лекарства (може да ускорят използването на витамин Д от организма), минерално масло (пречи на усвояването) и доксорубицин (витамин Д засилва ефектите си)[5] Дефицитът на активен витамин Д се свързва с повешена инсулинова резистентност, повишен атеросклеротичен риск, лявовентрикулна хипертрофия, когнитивни разтройства, прогресия на бъбречното заболяване, риск от патологични костни фрактури, влошено качество на живота на тези болни и повишена смъртност[3]
Все още няма ясни правила за необходимата
доза витамин Д, която да е достатъчна при пациентите на диализно лечение. В последните години се препоръчвата предимно ежедневен
прием на холекалциферол и по-рядко – месечни болусни режими от 80,000, 100,000 или 200,000 IU[6,7] Прилагането на естествен или активен витамин Д е свързано с подобряване на анемията и намаляване на нуждите от еритропоетин стимулиращи агенти.
Що се отнася до режима на заместване, витамин Д(3) е по-ефективен от витамин Д(2) при осигуряване на адекватни серумни нива на 25(OH)D при пациенти на хемодиализа[1,8].
ВИТАМИН К Терминът витамин К или нафтохинон се отнася до семейство мастноразтворими молекули, които имат подобна структура, изградена от 2-метил-1,4-нафтохинонов пръстен, но с различен произход и функция. Понастоящем са по-известни три първични форми, наречени витамери, които се различават по страничните вериги, свързани с основния пръстен на молекулата. Това са: витамин К1 (филохинон), витамин К2 (менахинон) и витамин К3 (менадион). Основната позната биологична функция на витамин К1 е кръвосъсирването, тъй като той действа като кофактор, необходим за II, VII, IX, и X коагулационни каскадни фактори, и за естествените антикоагуланти протеини S и C[9]. Витамин К2 се синтезира основно от чревната микробиота и се обозначава като менахинон (МК). Според дължината на изопреновата верига, прикрепена към метилирания нафтохинонов пръстен, могат да бъдат идентифицирани няколко различни форми, номерирани от МК-4 до МК-13. MK-4 се получава от превръщането на филохинон или менадион и се намира главно в месото и животните чрез продукти като яйца, краве прясно и кисело мляко. От друга страна, MK-7 е дълговерижна форма, която също се произвежда от чревни бактерии
и се намира във ферментирали храни, като сирене и соя[10]. Пациентите с хронично бъбречно заболяване се характеризират с лош статус на витамин К. Множество фактори могат да окажат ефектвърху запасите от витамин К при пациенти с ХБЗ и основните причини за неговия дефицит включват ограничение на храната, уремийна дисбиоза и лекарства. Освен това, диетичните ограничения поради високото съдържание на калий в повечето зелени зеленчуци, богати на витамин К, допринасят за неговия дефицит[9]
Редица проучвания доказват, че витамин К участва пряко и особено активно в костния метаболизъм. Някои от тях демонстрират, че той
[www.medmag.bg ] 39
инхибира костната резорбция, вероятно посредством намаленото произ-
водство на костно-резорбиращи ве -
щества, включително простагландин
Е2 и интерлевкин-6. Доказано е също, че витамин К е в състояние да насърчи костната минерализация, явявайки
се кофактор за някои протеини, участващи в минерализацията на костите, а
именно остеокалцин (костен Gla про -
теин или BGP) и матричен Gla протеин
(MGP)[11]. В този ред на мисли, дефи-
цитът на витамин К се разглежда като
независим рисков фактор за изявата
на костни фрактури при болните ле -
кувани с хемодиализа. Недостатъчи-
те нива на фило- и менахинон също се
свързват с терапевтично-резистент-
на артериална хипетония, повишен
риск от сърдечно-съдови инциден-
ти и мозъчни инсулти при пациентите
с терминална бъбречна недостатъч-
ност[12,13,14]
Липсва съгласие в научните среди не
дали, а каква да бъде дозиравката на
витамин К, използван за суплемен-
тация при пациентите на хемодиали-
за. Всъщност, основната необходи-
мост при тях е от вит. К2, но достъпна
в практиката е формата, съдържаща
К1. Въпреки, че част от нея се метабо -
лизират в организма до К2, остава отворен въпроса за риска от хипервитамоноза К.
ВИТАМИН Е
Семейството на витамин Е съдържа
четири естествено срещащи се структурно-подобни вещества, наситени
хомолози, α-, β-, γ- и δ-токофероли.
Има два начина за изразяване на дозата и количеството мастноразтворими витамини в даден продукт: единият начин се основава на количеството, където мерната единица е mg/ден, а другият начин се основава на биологичната активност, където единицата измерването е международна единица (IU). Добавка от α-токоферол 400 IU/ден е еквивалентна на 268 mg/ден, а препоръчваната дневна доза е около 15 mg[16] Витамин Е (токоферол) е много мощен антиоксидант, който стабилизира клетъчните мембрани и регулира окислителните реакции. Дефицитът на витамин Е обикновено се свързва със заболявания, които причиняват малабсорбция на мазнини, като кистозна фиброза. Клиничните характеристики на неговия дефицит включват хемолиза, невромускулна дисфункция на гръбначния мозък и лезии на ретината. На клетъчно ниво той пречи на реакциите, свързани с прогресиата на атеросклерозата, като пролиферация на гладкомускулни клетки, тромбоцитна агрегация, адхезия на моноцити, усвояване на окислени липопротеини с ниска плътност и производство на цитокини. Той взаимодейства с циклоспорин (витамин Е повишава абсорбцията на циклоспорин), със субстрати на цитохром P450 3A4 (CYP3A4) (витамин Е намалява тяхната ефективност чрез ускоряване на разграждането им), антикоагуланти/антитромбоцитни лекарства (витамин Е засилва
НЕФРОЛОГИЯ
техните ефекти) и статини (витамин Е намалява тяхната ефективност)[1]
Използването на високи дневни дози вит. Е (800-1200 mg) проказват в някои проучвания благоприятни ефекти върху бъбречната функция, особено при диабетици, което включва
също снижаването на нивата на някои проинфламаторни биомаркери[17].
T. Nguyen и сътр. (2021 г.) представят метаанализ на рандомизирани проучвания и правят практическия извод, че приложението на вит. Е достоверно намалява редица маркери на оксидативния стрес и съдовата увреда при пациенти на хемодиализно лечение[18]
Съществуват редица съобщения за изпорзването на low−flux диализатори, натоварени с витамин Е, което подобрява тяхната биосъвместимост и намалява достоверно известното покачване на нивата на проинфламаторни биомаркери в хода на диализната сесия[19,20].
ЗАКЛЮЧЕНИЕ Познаването на биологичните ефекти на мастно-разтворимите витамини при здрави индивиди и промените в техните нива при пациенти на диализно лечение ще бъдат полезни в ежедневната практика на личиния лекар и нефролога, за предписването на допълващо витаминно лечение. То ще подпомогне адаптацията на болния, лекуван с диализни методи, ще подобри качеството и продължителността на неговия живот.
1. Kosmadakis G, Da Costa Correia E, Carceles O. et al. Vitamins in dialysis: who, when and how much? Ren Fail. 2014 May;36(4):638-50.
2. Sundl I, Roob JM, Meinitzer A, et al. Antioxidant status of patients on peritoneal dialysis: associations with inflammation and glycoxidative stress. Perit Dial Int. 2009;29(1):89–101.
3. Jean G, Souberbielle JC, Chazot C. Vitamin D in Chronic Kidney Disease and Dialysis Patients. Nutrients. 2017 Mar 25;9(4):328.
4. Souberbielle J.C., Body J.J., Lappe J.M. et al. Vitamin D and musculoskeletal health, cardiovascular disease, autoimmunity and cancer: Recommendations for clinical practice. Autoimmun Rev. 2010;9:709–715.
5. Yilmaz MI, Sonmez A, Saglam M, et al. Comparison of calcium acetate and sevelamer on vascular function and fibroblast growth factor 23
in CKD patients: a randomized clinical trial. Am J Kidney Dis. 2012;59(2):177–185.
6. Martineau A.R., Jolliffe D.A., Hooper R.L. et al. Vitamin D supplementation to prevent acute respiratory tract infections: Systematic review and meta-analysis of individual participant data. BMJ. 2017;356:i6583. doi: 10.1136/bmj.i6583.
7. Bischoff-Ferrari H.A., Dawson-Hughes B., Orav E.J. et al. Monthly High-Dose Vitamin D Treatment for the Prevention of Functional Decline: A Randomized Clinical Trial. JAMA Intern. Med. 2016;176:175–183.
8. Wetmore J.B., Kimber C., Mahnken J.D., Stubbs J.R. Cholecalciferol v. ergocalciferol for 25-hydroxyvitamin D (25(OH)D) repletion in chronic kidney disease: A randomised clinical trial. Br. J. Nutr. 2016;116:2074–2081.
9. Bellone F, Cinquegrani M, Nicotera R. et al. Role
of Vitamin K in Chronic Kidney Disease: A Focus on Bone and Cardiovascular Health. Int J Mol Sci. 2022 May 9;23(9):5282.
10. Beulens J.W., Booth S.L., van den Heuvel E.G. et al. The role of menaquinones (vitamin K2) in human health. Br. J. Nutr. 2013;110:1357–1368.
11. Fusaro M., Gallieni M., Porta C. Et al. Vitamin K effects in human health: New insights beyond bone and cardiovascular health. J. Nephrol. 2020;33:239–249.
12. Wasilewski G.B., Vervloet M.G., Schurgers L.J. The Bone—Vasculature Axis: Calcium Supplementation and the Role of Vitamin K. Front. Cardiovasc. Med. 2019;6
13. Popa D.-S., Bigman G., Rusu M. The Role of Vitamin K in Humans: Implication in Aging and Age-Associated Diseases. Antioxidants. 2021;10:566.
14. Provenzano M., Coppolino G., Faga T. Et al. Epidemiology of cardiovascular risk in chronic kidney disease patients: The real silent killer. Rev. Cardiovasc. Med. 2019;20:209–220.
15. Jensen G.S., Lenninger M., Ero M.P., Benson K.F. Consumption of nattokinase is associated with reduced blood pressure and von Willebrand factor, a cardiovascular risk marker: Results from a randomized, double-blind, placebo-controlled, multicenter North American clinical trial. Integr. Blood Press. Control. 2016;9:95–104.
16. Baltusnikiene A., I. Staneviciene, E. Jansen. Beneficial and adverse effects of vitamin E on the kidney. Front. Physiol., Sec. Renal Physiology and Pathophysiology, 2023;14.
17. Di Vincenzo A., Tana C., El Hadi H. Et al. Antioxidant, antiinflammatory, and metabolic properties of tocopherols and
tocotrienols: Clinical implications for vitamin E supplementation in diabetic kidney disease. Int. J. Mol. Sci. 2019;20, 5101.
18. Nguyen TTU, Yeom JH, Kim W. Beneficial Effects of Vitamin E Supplementation on Endothelial Dysfunction, Inflammation, and Oxidative Stress Biomarkers in Patients Receiving Hemodialysis: A Systematic Review and MetaAnalysis of Randomized Controlled Trials. Int J Mol Sci. 2021 Nov 3;22(21):11923.
19. Libetta C, Zucchi M, Gori E. et al. Vitamin E-loaded dialyzer resets PBMC-operated cytokine network in dialysis patients. Kidney Int. 2004;65(4):1473–81.
20. Sepe, V., Gregorini, M., Rampino, T. et al. Vitamin e-loaded membrane dialyzers reduce hemodialysis inflammaging. BMC Nephrol. 2019; 20, 412.
40 І Medical Magazine | юли 2023
ИЗПОЛЗВАНА ЛИТЕРАТУРА:

Г. Господинова, И. Даскалов, Л. Демиревска Клиника по Кардиология, ВМА - София
миокардит с благоприятен изход
след имуносупресивно лечение
Ключови думи: Фулминантен миокардит, сърдечна недостатъчност.
Фулминантният миокардит е рядко и прогресиращо заболяване,
недостатъчност и левокамерна систола дисфункция. След своевременното лечение с имуномодулираща терапия, състоянието на пациентката се подобри значително. Бързата диагноза и лечение са от изключително значение за добрата прогноза на такива пациенти.
Фулминантният миокардит
представлява остро прогресиращо възпаление на миокарда, най-често предизвикано от вирусна инфекция. Клиничните прояви могат да
варират от безсимптомно протичане до
животозастрашаващи аритмии, сърдечна или полиорганна недостатъчност с
кардиогенен шок и смърт[1].
КЛИНИЧЕН СЛУЧАЙ
Жена на 37 години без известни до
момента сърдечно-съдови заболява-
ния постъпи в клиниката с оплаквания
от ретростернална болка и прояви
на сърдечна недостатъчност от 2 дни
с прогресивно влошаване през по -
следните часове. Една седмица пре -
ди това е преболедувала левостранна
пневмония, която е лекувана с антибиотик в домашни условия. Неколкократно е хоспитализирана в миналото
по повод нефролитиаза.
При постъпването пациентката беше
в тежко общо състояние, заемаше ор -
топноично положение. От аускултаци-
ята на бял дроб се установи отслабе -
но везикуларно дишане до липсващо
с двете белодробни основи и дифуз-
но пръснати разнокалибрени влажни
хрипове. Сърдечната дейност беше
ускорена и ритмична. Не се аускулти-
раха сърдечни шумове. Измери се ар -
териално налягане 80/50 mmHg.
Лабораторните изследвания пока -
заха повишени високочувствителен тропонин I (hsTPI) 0,81 ng/ml и С-ре -
активен протеин (CRP) 21 mg/l. Вирусологичното изследване доказа преболедувана инфекция с грип А. Имунологичният анализ на отношението Тreg/Th17 демонстрира патологично ниска стойност. От електрокардиограмата (ЕКГ) при постъпването се установи ST-елевация с преход към отрицателни Т-вълни във V1-V4 (Фиг. 1). При проследяващи ЕКГ се регистрираха епизоди на надкамерна аритмия под формата на честа надкамерна екстрасистолия и надкамерни тахикардии. Ехокардиографията (ЕхоКГ) заедно с specke-tracking показа тежка левокамерна систолна дисфункция с левокамерна фракция на изтласкване (ФИ) 29% при дифузна хипокинезия с аневризмално разширение на сърдечния връх и редуциран лонгитудинален стрейн (global longitudinal strain, GLS) – 8.7% (Фиг. 2). Визуализираха се и дифузен малък перикарден излив и двустранни плеврални излива по около 600 мл. Рентгенографията демонстри -
ра белодробен оток с двустранни
плеврални изливи.
Проведе се селективна коронарография, която не показа коронарни стенози.
Във връзка с клиничните, лабораторните, инструменталните данни и наличието на преболедувана вирусна инфекция с грип А се обсъди с висока клинична вероятност наличието на миокардит. За доказване на тази диагноза се проведе сърдечен магнитен
резонанс (СМР), при който на Т2-образите се установи едем на миокарда антеросептално и в областта на сърдечния връх и малък перикарден излив (Фиг. 3). На 10-та минута след венозното контрастиране с гадолиний се визуализира късно постконтрастно усилване в същите зони, което потвърди диагнозата остър миоперикардит (Фиг. 4 и 5). След съпоставка
на данните от speckle-tracking ЕхоКГ и СМР се отчете значима корелация и до 70% съвпадение на засегнатите зони от възпалителния процес.
Поради тежкото общо състояние и развитието на белодробен оток се започна насочено лечение за овладяване на проявите на левостранна сърдечна недостатъчност с приложение на бримкови диуретици в инфузионни режими паралелно с двойна катехоламинова поддръжка с допамин и добутамин. Надкамерната тахикардия бързо бе овладяна с венозно приложение на амиодарон. Независимо от приложеното лечение, при проследяващи ЕхоКГ се регистрира влошаване на левокамерната систолна функция в рамките на 24 часа. Затова се взе решение за провеждане на допълнителна имуносупресивна терапия с кортикостероид. В хода на това лечение общото състояние се подобри значително и проявите на декомпенсация се овладяха напълно. Болната беше изписана с продължаващо в дома лечение с фуроземид,
42 І Medical Magazine | юли 2023
Клиничен случай на фулминантен
най-често с вирусна генеза. Представяме клиничен случай на пациентка с миокардит с прояви на тежка сър -
дечна
КАРДИОЛОГИЯ
спиронолактон, дапаглифлозин заедно
с метилпреднизолон
в постепенно намаляващи дози. Препоръчахме специален режим на физическа
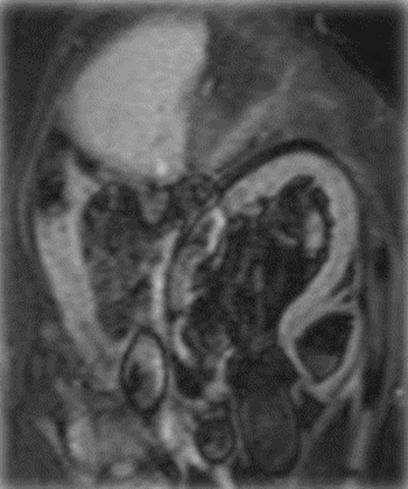
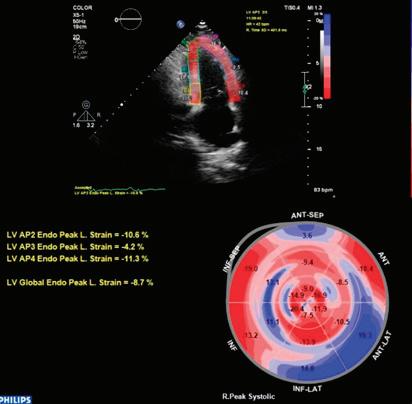
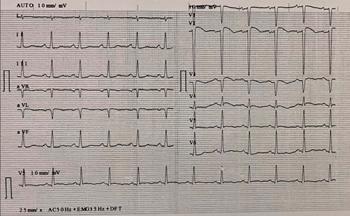
активност с постепенно увеличение на обхвата на натоварване и периодично проследяване.
При контролното
проследяване след 1 месец се отчете значително подобре -
ние на левокамерна -
та систола функция
с ФИ 45%, и липса на
прояви на сърдечна недостатъчност.
ОБСЪЖДАНЕ
Фулминантният мио -
кардит е тежко животозастрашаващо заболяване, при което
се развива оток и некроза на кардиомиоцитите. Честотата на вирусния миокардит е приблизително 10
до 20 клинични случая на 100 000 души годишно. Честотата на фулминантния миокардит не е ясно дефинирана, но е значително по-рядка[1] Фулминантният миокардит много често протича с прояви на тежка сърдечна недостатъчност с белодробен оток или кардиогенен шок. Заболяването няма
ференциална диа -
гноза с много други възможни сърдечни заболявания.
Във всеки етап на
развитието на остър
миокардит могат да
възникнат различни
ритъмно-проводни
нарушения - от живо -
тозастрашаващи ари -
тмии до тежки про -
водни нарушения с
развитие на внезап -
на сърдечна смърт (ВСС). Надкамерните
аритмии са по-чести
от камерните, а атрио-вентрикуларни -
ят блок се среща из -
ключително рядко[2]
Рискът от ВСС не ви -
наги е свързан с тежестта на миокардното възпаление и
може да персистира
и след острата фаза, поради което при
преживян миокар -
дит е необходимо
дългосрочно проследяване[3]. Освен ритъмно-проводни нарушения, ЕКГ може
да покаже и нисък
волтаж и промени в
ST-сегмента, които се
свързват с миокардния оток[4]. В нашия
клиничен случай се регистрираха както промени в ST-сегмента, така и надкамерни тахикардии. Установиха се и повишени маркери за миокардна некроза. Това наложи търсене на диференциална диагноза с остър миокар -
Фиг. 1
ЕКГ – синусов ритъм, сърдечна честота 109 уд./ мин., ST-елевация с пре -
ход към отрицателна Т-вълна във V1-V4
Фиг. 2
“Bull’s eye” изображение
в 18-сегментен модел на лява камера с редуциран GLS. Наблюдава се понижен стрейн в базалните долно-латерални, предно-латерални и предно-септални сегменти и средните долно-септални сегменти
Фиг. 3
T2-образ, демонстриращ
усилен интензитет на сигнала антеросептално и в областта на сърдечния връх, както при едем на миокарда
специфични клинични прояви, поради което се изисква провеждането на голям комплекс от лабораторни, ЕКГ и образни изследвания за потвърждаване на диагнозата и ди[www.medmag.bg ] 43
Фиг. 4 и 5
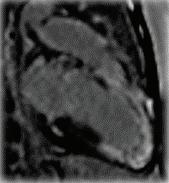
Т1 (LGE) – късно посткон-
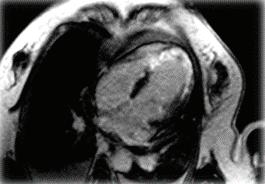
трастно усилване на 10-та
минута след контрасти-
ране с гадолиний. Нали-
це е усилване на сигнала
в резултат на задържане
на контрастната материя
в интерстициума поради
хиперемия
ден инфаркт. Лабораторните отклонения при тежък остър миокардит са свързани със загиването на множество кардиомиоцити и наличието на възпаление. Така че при това заболяване, освен маркерите за миокардна некроза, са налице и завишени възпалителни маркери (CRP).
Ехокардиографията е предпочитаният първоначален метод за оценка на миокардно увреждане, поради широката му достъпност и възможността му за извършване до леглото на болния[2]. Няколко ЕхоКГ белега могат да наклонят везната към диагноза остър миокардит вместо остър миокарден инфаркт. Такива са запазените теледиастолни левокамерни обеми при увеличена дебелина на стените (в резултат на миокардния оток), съпътстващо перикардно засягане и перикарден излив[5,6,7]. Важно значение тук има динамичното проследяване с ЕхоКГ на тези пациенти. Особеност на фулминантния миокардит е, че при него при успешно възстановяване се отчита подобрение на ФИ в по-голяма степен, отколкото при остър нефулминантен миокардит[8].
При наличие на повишени маркери за миокардна некроза и ЕКГ данни за ST-елевация все пак е необходимо извършването на селективна коронарна ангиография като част от диагностичния алгоритъм, за да се изключи исхемична коронарна генеза. Поради това извършихме това изследване и при нашата пациентка. За поставяне на диагнозата миокардит, обаче, е необходимо извършването на CMР. В клиничната практика СМР е неинвазивен метод за диагностика на клинично подозиран миокардит, благодарение на мултипараметричната си способност за характеризиране на тъканите. Параметрите, които той отчита са свързани с промени в извънклетъчния обем по време на възпаление, а именно едем, хи-
перемия, некроза и фиброза. Интензитетът на тези промени зависи от степента на възпаление. Поради това е необходимо СМР да се проведе през първите няколко седмици oт началото на заболяването[9,10]. Това направихме
и ние и въз основа на изпълнение на актуализираните критерии на Лейк Луис потвърдихме диагнозата остър миокардит.
Критериите на Лейк Луис за оценка на миокарднто възпаление са публикувани за първи път през 2009г и те включват: 1) едем на миокарда (количествено определено чрез регионално или глобално усилване на Т2); 2) белег или активно възпаление (чрез късно усилване след контрастиране с гадолиний - LGE); и 3) наличие на хиперемия (ранно усилване след контрастиране с гадолиний). Необходими са 2 от 3 критерия за потвърждение на диагнозата. Поради нарастващите данни за повишаване на диагностичната точност чрез Т2-картографирането, през 2018 г. критериите на Лейк Луис са актуализирани и включват един T2-базиран критерий (глобално или регионално увеличение на времето за T2 релаксация на миокарда или повишена интензивност на сигнала в T2-претеглени изображения), с поне един T1-базиран критерий (повишен миокарден T1, извънклетъчен обем или LGE) в острата фаза. При миокардит обикновено засегната зона се намира субепикардно, за разлика от субендокардното разположение при исхемична болест на сърцето[11,12,13,14,15]
Референтният стандарт за установяване на миокардит си остава ендомиокардната биопсия (ЕМБ), но нейните ограничения са свързани главно с нейния инвазивен характер и рядко извършване[11,16,17]
Миокардитът може да се разгледа като имуномедиирано заболяване, свързано с нарушение в толерантността към сърдечни антигени[18]. При остър вирусен миокардит може да
44 І Medical Magazine | юли 2023
КАРДИОЛОГИЯ
се промени имунният отговор на организма и да се развие автоимунна реакция[19,20,21,22]. При некроза с разрушаване на кардиомиоцитите в резултат на вирусна инфекция се освобождава големи количества сърдечен миозин и други клетъчни протеини. Освободеният сърдечен миозин при хората служи като мощен антиген.
Проучвания при мишки показват, че имунизирането със сърдечен миозин води до Т-хелперен 17 (Тh17) имунен отговор, характеризиращ се с ексцесивна мононуклеарна инфилтрация
и фиброза[23]. Установено е, че Тh17 са тясно свързани с автоимунитета при хората[24,25]. Критична роля в потискането на автимунитета имат T-регулаторните клетки (Тreg). Проучванията
показват, че при значимо намаляване на количеството на Treg в кръв-
та, се развива автоимунитет, в това чисто и миокардит с наличие на анти-сърдечни миозинови антитела[26].
При развитие на автоимунни процеси
се установява пролиферация на Th17 и подтискане на Тreg. Намаленото отношение Тreg/Th17 служи като имунологичен маркер за участието на автоимуния механизъм в патогенезата на миокардита[27]. Това може да има значение за преценка на лечение-
то и нуждата от включване на имуносупресивна терапия.
Според настоящите препоръки е желателно пациентите с миокардит с прояви на сърдечна недостатъчност, повишени стойности на тропонин и злокачествени аритмии да бъдат хоспитализирани за поне 48 часа. При наличие на левокамерна систолна
дисфункция в най-кратък срок трябва да се започне лечение за сърдечната недостатъчност. Това лечение трябва да продължи най-малко 6 месеца след възстановяването на сърдечната функция и нормализирането на тропонина и при липса на аритмии[28]. В определени случаи и само при наличие на клинични или ЕМБ данни за автоимунен процес може да се приложи имуносупресивно лечение[16]. При клинично подозрение за имуномедииран миокардит може да се започне емпирично терапия с кортикостероиди, особено при наличието на остра сърдечна недостатъчност, злокачествени аритмии и/или високостепенен AV блок[4,14]. С оглед на тези съображения наред със съобразената с международните препоръки терапия на сърдечната недостатъчност проведохме и имуносупресивна терапия с кортикостероид.
вишен тропонин и промени в ЕКГ за поне 6 месеца след пълното възстановяване[32]
В 20% от случаите острият миокардит може да доведе до развитието на дилатативна кардиомиопатия. Затова такива пациенти трябва да се проследяват ежегодно за поне 4 години с извършването на ЕКГ и ЕхоКГ[28].
1. Tschöpe C., Ammirati E., Bozkurt B., et al. Myocarditis and inflammatory cardiomyopathy: current evidence and future directions. Nat Rev Cardiol. 2021;18(3):169–193.
2. Baksi AJ, Kanaganayagam GS, Prasad SK. Arrhythmias in viral myocarditis and pericarditis. Card. Electrophysiol. Clin. 2015;7:269–281.
3. Maron BJ, et al. Eligibility and disqualification recommendations for competitive athletes with cardiovascular abnormalities: Task Force 3: Hypertrophic cardiomyopathy, arrhythmogenic right ventricular cardiomyopathy and other cardiomyopathies, and myocarditis: a scientific statement from the American Heart Association and American College of Cardiology. J. Am. Coll. Cardiol. 2015;66:2362–2371.
4. Kociol R.D., Cooper L.T., Fang J.C., et al. Recognition and initial management of fulminant myocarditis: a scientific statement from the
В момента клетъчно-базираната терапия (имуномодулираща терапия) е в етап на клинични проучвания. Тя се изразява в прилагането на Тreg или използването на мезенхимни стромални клетки и има за цел да повиши имуносупресията и така да подобри преживяемостта и прогнозата на пациентите с остър миокардит[29,30, 31]
Важен за възстановяването на пациентите с остър миокардит е режимът на физическо натоварване и затова ние изработихме специална програма за физическа активност съобразно състоянието на пациентката. Спортните дейности трябва да се избягват при наличие на симптоми, по -
ЗАКЛЮЧЕНИЕ Поставянето на диагнозата миокардит е трудна задача и изисква сбор от критерии. Клиничната характеристика и първоначалните резултати могат да насочат към диагнозата, но тя често може да се припокрива с други сърдечно-съдови заболявания. Използването на СМР като основен неинвазивен метод е от решаващо значение за ранната диагностика и започване на лечение. Лечението обикновено е поддържащо и насочено към овладяване на усложненията, най-тежкото от което е сърдечната недостатъчност. При развитие на автоимунна реакция е необходимо провеждането и на имуносупресивна терапия. От съществена важност е дългосрочното проследяване на преболедувалите миокардит. Пълно оздравяване се наблюдава при по-голямата част от случаите, но малка част развиват усложнения по формата на дилатативна кардиомиопатия с тежка сърдечна недостатъчност или животозастрашаващи аритмии. Своевременната диагноза и лечение могат да подобрят значително преживяемостта и прогнозата на тези пациенти. ИЗПОЛЗВАНА
American Heart Association. Circulation. 2020;141(6):e69–e92.
5. Skouri HN, Dec GW, Friedrich MG, Cooper LT. Noninvasive imaging in myocarditis.J Am Coll Cardiol. 2006; 48:2085–2093.
6. Shillcutt SK, Thomas WR, Sullivan JN, DuhachekStapelman A. Fulminant myocarditis: the role of perioperative echocardiography.Anesth Analg. 2015; 120:296–299.
7. Ammirati E, Cipriani M, Lilliu M, Sormani P, Varrenti M, Raineri C, Petrella D, Garascia A, Pedrotti P, Roghi A, et al. Survival and left ventricular function changes in fulminant versus nonfulminant acute myocarditis.Circulation. 2017; 136:529–545.
8. Felker GM, Boehmer JP, Hruban RH, Hutchins GM, Kasper EK, Baughman KL, Hare JM. Echocardiographic findings in fulminant and acute myocarditis.J Am Coll Cardiol. 2000; 36:227–232.
9. Lurz P., Luecke C., Eitel I., Fohrenbach F., Frank C., Grothoff M., de Waha S., Rommel K.P., Lurz J.A., Klingel K., et al. Comprehensive Cardiac Magnetic Resonance Imaging in Patients with Suspected Myocarditis: The MyoRacer-Trial. J. Am. Coll. Cardiol. 2016;67:1800–1811.
10. Luetkens J.A., Homsi R., Dabir D., Kuetting D.L., Marx C., Doerner J., Schlesinger-Irsch U., Andrie R., Sprinkart A.M., Schmeel F.C., et al. Comprehensive Cardiac Magnetic Resonance for Short-Term Follow-Up in Acute Myocarditis. J. Am. Heart Assoc. 2016;5:e003603.
11. Ferreira VM, Schulz-Menger J, Holmvang G, et al.. Cardiovascular Magnetic Resonance in Nonischemic Myocardial Inflammation: Expert Recommendations. J Am Coll Cardiol 2018;72(24):3158–3176.
12. Friedrich MG, Sechtem U, Schulz-Menger J, Holmvang G, Alakija P, Cooper LT, White JA, Abdel-
Aty H, Gutberlet M, Prasad S, et al; International Consensus Group on Cardiovascular Magnetic Resonance in Myocarditis. Cardiovascular magnetic resonance in myocarditis: a JACC white paper.J Am Coll Cardiol. 2009; 53:1475–1487.
13. Lurz P, Eitel I, Adam J, Steiner J, Grothoff M, Desch S, Fuernau G, de Waha S, Sareban M, Luecke C, et al. Diagnostic performance of CMR imaging compared with EMB in patients with suspected myocarditis.JACC Cardiovasc Imaging. 2012; 5:513–524.
14. Ammirati E, Frigerio M, Adler ED, Basso C, Birnie DH, Brambatti M, Friedrich MG, Klingel K, Lehtonen J, Moslehi JJ, Pedrotti P, Rimoldi OE, Schultheiss HP, Tschope C, Cooper LT, Jr., Camici PG. Management of acute myocarditis and chronic inflammatory cardiomyopathy: an expert consensus document. Circ Heart Fail 2020;13:e007405.
15. Abdel-Aty H, Boyé P, Zagrosek A, Wassmuth R, Kumar A, Messroghli D, Bock P, Dietz R, Friedrich MG, Schulz-Menger J. Diagnostic performance of cardiovascular magnetic resonance in patients with suspected acute myocarditis: comparison of different approaches.J Am Coll Cardiol. 2005; 45:1815–1822.
16. Caforio A.L., Pankuweit S., Arbustini E., Basso C., Gimeno-Blanes J., Felix S.B., Fu M., Helio T., Heymans S., Jahns R., et al. Current state of knowledge on aetiology, diagnosis, management, and therapy of myocarditis: A position statement of the European Society of Cardiology Working Group on Myocardial and Pericardial Diseases. Eur. Heart J. 2013;34:2636–2648.
Пълната библиографска справка съдържа 32 източника и ще бъде предоставена от редакцията при поискване.
[www.medmag.bg ] 45
ЛИТЕРАТУРА:
Л. Золумова, И. Желева, В. Гелев Клиника по кардиология, „Аджибадем Сити Клиник
УМБАЛ Токуда“ – София
Ключови думи: Артериална хипертония, фиксирани комбинации.
Артериална хипертония се дефинира като границата на артериалното налягане, над която ползите от лечението на АН надхвърлят рисковете. И докато това схващане не се променя в годините, то границите на систолното и диастолното налягане, при които поставяме диагноза артериална хипертония и се препоръчва иницииране на терапия постепенно намаляват на базата на редица клинични проучвания. Настоящите ръководства за лечение на артериална хипертония на Европейското дружество по кардиология и Европейското дружество по хипертония дефинират хипертонията като офисно систолно налягане >140 mmHg и диастолно налягане >90 mmHg[2]. За постигането на тези стойности се препоръчват както промени в начина на живот, така и медикаментозно лечение. Въпреки големия набор от доказано ефективни, добре поносими и достъпни антихипертензивни лекарства все още голям брой пациенти не се придържат към лечението и не постигат адекватен контрол на артериалното налягане. Непридържането към антихипертензивно лечение засяга около 50% от пациентите с АХ, като 83% от пациентите с лош контрол на АН не са съпричастни към препоръчаната терапията[3]. Облекченото и ненатоварващо антихипертензивно медикаментозно лечение, като комбинации на два или повече медикаменти в една таблетка, подобрява къмплайънса на пациента и ускорява процеса на достигане на таргетните стойности на АН. Не трябва да се забравя, че таргетните стойности на АН и типът медикаментозно лечение трябва да бъдат индивидуализирани в зависимост от съпътстващите заболявания, наличието на медииранa от хипертонията органнa увреда, сърдечно-съдови рискови фактори (вкл. напреднала възраст).
КОНТРОЛ НА АРТЕРИАЛНОТО
НАЛЯГАНЕ
За нaмаляване стойностите на арте -
риалното налягане се препоръчват
както промени в начина на живот, така и медикаментозно лечение. Ме -
та-анализи на рандомизирани клинични проучвания, включващи сто -
тици хиляди пациенти доказват, че редукция в САН >10 mmHg или ДАН
>5 mmHg водят до статистически значима редукция във всички големи сърдечно-съдови събития с близо 20%, в общата смъртност с 10-15%, в инсултите с 35%, коронарните съби -
тия с 20% и сърдечната недостатъч -
ност с близо 40%[4]. Промени в начи -
на на живот като редукция наприема
на сол <5 гр. дневно, преустановява -
не на тютюнопушенето, редукция в
телесното тегло и насърчаване към редовна физическа активност кате -
горично могат да доведат до намаляване на артериалното налягане, но повечето пациенти ще имат нужда и от медикаментозно лечение. Актуалните ръководства за лечение на артериална хипертония препоръчват пет основни класа медикаменти – АСЕ-инхибитори, ангиотензин-рецепторни блокери, б-блокери, калциеви антагонист и диуретици. Всеки от тези класове медикаменти е с доказан в рандомизирани клинични проучвания ефект върху редукцията в АН, както и върху редукцията в сърдечно-съдовите събития.
Мета-анализи, както и становището на Американския колеж по кардиология/Американската асоциация за сърдечни заболявания (АСС/ АНА) от 2017 г. относно лечението на АХ[5], глобалните практически насо -
ки за хипертония на Международното дружество по хипертония[6], както и на Европейското дружество по хипертония/Европейското кардиологично дружество (ESH/ESC) от 2018 г. относно управлението на хипертонията[2] стигат до заключението, че понижаването на стойностите на АН е основният определящ фактор за намаляване на сърдечно-съдовия риск както при по-млади, така и при по-възрастни пациенти с хипертония, а не вида на антихипертензивните медикаменти. Въпреки доказаните ползи артериалната хипертония е недобре контролирана в цял свят, както в развиващите се, така и в развитите страни. Не повече от 15-20% от пациентите достигат стойности на АН <140/90mmHg, а при намаляване на таргета на тези стойности, каквито са индикациите за някои гру-
46 І Medical Magazine | юли 2023
Лечение на артериалната хипертония: препоръки в практиката на специалиста кардиолог
КАРДИОЛОГИЯ
пи пациенти (например диабетици)
процентът става още по-нисък. Неконтролираните пациенти са с нарастващ риск от сърдечно-съдови
събития, като неоптималният кон -
трол на АН се смята за основна причина артериалната хипертония да
бъде водеща причина за смрътност.
Според Mancia et al, несъответствие -
то между препоръките и практиката
произтича от разликата между добре проектираните рандомизирани контролирани проучвания (RCT) и реал -
ната среда. В проучванията лекарите
следват стриктно протокола от из -
следването и пациентите трябва да
се придържат към лечението, докато
в действителност придържането към терапията на полиморбидните пациенти рядко надвишава 80%, а лекарите са по-загрижени за последици от свръхпонижаването на кръвното налягане[2]
В основата на неконтролираната
АХ се смята, че стоят т.нар. клинична „инерция“, субоптималното при -
държане към лечението и недостатъчната употреба на комбинирани
терапии, въпреки големия набор от доказателства за ползата от тях. Придържането се определя като степента, в която поведението на дадено лице като приемане на лекарства, спазване на диета или извършване на промени в начина на живот, съответства на препоръките от страна на лекуващия лекар[7]. Липсата на къмплайънс обикновено е в следствие на няколко фактора, които могат да бъдат свръзани с пациента, със състоянието му, с терапията, със системата на здравеопазване, както и социо-демографски особености. Сложни терапевтични схеми, свързани с прием на няколко медикамента в различни дозови режими е добре познато препядствие в придържането на пациентите към лечението. Множество проучвания демонстрират последователна обратна връзка между броя приемани медикаменти и степента на придържане[8]. Опростяването на дозовите режими е основна част от добрата терапия, пряко свързано с по-добър комплайънс на пациентите.
За предпочитане е еднократния прием на дългодействащи медикаменти и комбиниране на различни медикаменти в една таблетка (SPC – singlepill combination), каквито са и насоките в съвременните ръководства за лечение на артериална хипертония. АКТУАЛНИ ПРЕПОРЪКИ ЗА ЛЕЧЕНИЕ НА АРТЕРИАЛНА ХИПЕРТОНИЯ Актуалните ръководства за лечение на артериална хипертония на Европейското дружество по кардиология препоръчват започване на медикаментозно лечение наред с промени в начина на живот при пациент с първа стадий АХ и висок или много висок риск от ССС, бъбречно заболяване или таргетно органно увреждане, втори и трети стадий АХ. При пациенти с първи стадий АХ и нисък, интермедиерен риск от ССС без бъбречно заболяваен или таргетно органно увреждане се препоръчва промяна в начина на живот и при липса на адекватен контрол на АН след 3-6 месец започване на медикаментозно лечение[2]. Като първа цел на лечението се определя спад на АН < 140/90 mmHg и при добър толеранс
от страна на пациента последващо понижаване на АН <130/80 mHg. При пациенти над 65 г. таргетните стойности на САН са 130-139 mmHg. С малки изключения се препоръчва иницииране на терапия с два медикамента за предпочитане комбинирани в една таблетка. В ръководството на Американския колеж по кардиология/Американската асоциация за сърдечни заболявания (АСС/ АНА) за лечение на артериална хипертония начална терапия с два медикамента се препоръчва при пациенти с 2 стадий хипертония и АН >20/10 mmHg над таргетните стойности.
Всеки от известните антихипертензивни медикаменти е приблизително еднакво ефективен, предизвиквайки добър антихипертензивен отговор при 30 до 50% от пациентите, особено при тези с първа степен на АХ. Като пример, проучванията CAPPP, STOP-Hypertension-2, NORDIL,
UKPDS и INSIGHT откриват малка разлика в обобщените резултати между по-старите (диуретици и бета-блокери) и по-новите антихипертензивни медикаменти (ACE-инхибитори и калциевите антагонисти)[9,10]. От друга страна мета-анализи все пак показват разлики по отношение на някои сърдечно-съдови събития спрямо различните медикаменти, например по-малка редукция в честотата на инсултите при лечение с б-блокери или по-слаба превенция на СН при лечение с Са-антагонист. По тази причина и бета-блокерите рядко са първи избор на терапия, освен при наличие на специфични индикации. Така като първи линия терапия при липса на конкретна клинична причина за първоначална монотерапия се препоръчва използването на АСЕ-инхибитори, ангиотензин-рецепторни блокери, диуретици и Са-антагонисти.
МОНОТЕРАПИЯ
Към днешна дата монотерапия се препоръчва основно при пациенти с АХ първи стадий и нисък риск от сърдечно-съдови инциденти и САН <150 mmHg, много високо рискови пациенти с високо нормално АН или възрастни и немощни пациенти. Дори и при добър контрол на АН на фона на терапия с един медикамент с времето при повечето пациенти ще се наложи добавяне на втори. В проучването ALLHAT, например, делът на пациентите, лекувани с повече от едно лекарство, се увеличава от 26 на 33% на първата година и до 4043% на петата година[11].
В по-стари препоръки за лечение на АХ се е акцентирало на монотерапиите и увеличаване дозата на едно лекарство докато не се постигне максимален ефект и липса на допълнителна редукция в АН. Вече е добре известно, че след първоначалната доза, преминаването към по-високи дози на един медикамент води до сравнително по-малко по-нататъшно намаляване на АН с цената на нарастващ процент на нежеланите ефекти. Използването на по-високи дози може да доведе до по-нисък от-
[www.medmag.bg ] 47
КАРДИОЛОГИЯ
говор на кръвното налягане и по-го -
ляма токсичност сравнено с премина -
ването към второ лекарство. Добре
познат факт е, че нежеланите лекар -
ствени реакции са една от най-ва -
жните предпоставки за преустано -
вяване на провежданата терапия. Oт
друга страна данни от реалната кли -
нична практика показват, че голяма
част от пациентите, започващи анти -
хипертензивна терапия с един меди -
камент дълги години не преминават
към комбинирана терапия, въпреки
необходимостта от такава[12]. В дейст-
вителност и към момента антихипертензивното лечение е силно повлия -
но от интертно отношение, което се
противопоставя на адекватното ти -
триране на медикаментите.
Замяната на един медикамент с друг
или т.нар. секвенциална монотера -
пия е друга практика, която не е офи -
циално препоръчвана до момен -
та в ръководствата и рядко води до
по-добър контрол на АН, а от дру-
га страна се свърза и с по-слабо при -
държане на пациентите към лече -
нието. Препоръчва се основно при
изява на нежелани лекарствени реак-
ции към първоначално избраното ан -
тихипертензивно лекарство. Дори и
при тази стратегия на терапия отно -
сително малко пациенти преминават
от началната си терапия към друг медикамент. В действителност не прос-
то дълго време се отлага добавянето
на втори медикамент към терапия -
та, а много пациенти се придържат
към първоначално стартираното ле -
карство, независимо от липсата на достатъчно добър контрол на АН[12].
Затова и актуалните препоръки за
лечение на артериална хипертония
препоръчват при повечето пациенти
стартиране на терапия с два медикамента, комбинирани в една таблетна
форма[2]. На практика и петте класа
медикаменти могат да бъдат комби -
нирани помежду си с изключение на АСЕ-инхибиторите и ангиотензин-ре -
цепторните блокери, но се препо -
ръчват лечението да се базира на
комбинации АСЕ-инхибитори/ARB с
тиазидни диуретици или с калциеви антагонисти.
КОМБИНИРАНИ ТЕРАПИИ
Както вече бе споменато повечето пациенти в практиката имат нужда от терапия с повече от един медикамент. Само около 40% от пациентите имат адекватен контрол на АН на монотерапия, 75-80% постигат добър контрол на двойна терапия, а между 90% и 95% - на тройна терапия[13]. Необходимостта от лечение с повече от един медикамент е демонстрирана в множество рандомизирани проучвания в различни географски райони и население - The United Kingdom's Prospective Diabetes Study (UKPDS), the Hypertension Optimal Trial (HOT), the Antihypertensive and LipidLowering Treatment to Prevent Heart Attack Trial (ALLHAT), the Action to Control Cardiovascular Risk in Patients with Diabetes—Blood pressure trial (ACCORD), Heart Outcomes Prevention Evaluation (HOPE)-3 Trial, and the Systolic Blood Pressure Intervention Trial (SPRINT)[11,14,15,16,17].
Комбинира -
ни терапии, които влючват два или повече антихипертензивни медикамента имат възможността да елиминират част от предизвикателствата и ограниченията на терапията с един медикамент.
Осигуряват по-голямо действие върху понижаването на артериалното налягане, по-бързо достигане на таргетните нива на АН, по-добро придържане към терапията и едновременно намаляване честотата на страничните ефекти на лекарствата, наблюдавани при самостоятелно приложение. Oсновно предимство на комбинирата терапия е възможността да се преодолее клиничната инерция – пропускът на лекуващите лекари да увеличават дозите и броя медикаменти в терапията при пациенти с недобре контролиран рискови фактори, съобразено с ръководните препоръки. Този проблем става все по-актуален и е сред най-честите причина за неадекватен контрол на АН. Като причини за клиничната инерция могат да се разглеждат особености на пациента, особености на лекаря или особености в комуникацията лекар-пациент.
Патогенезата на артериалната хипер -
тония е многофакторна, което обяснява и многократното потенциране на антихипертензивния ефект на лекарствата при комбиниране на медикаменти от различни класове с различно действие. Повлияването на един от механизмите на АХ често води до компенсаторна засилена реакция на друг механизъм. Действайки върху различните патофизиологични явления комбинацията на лекарства води до 5 пъти по-голяма редукция в АН спрямо удвояване дозата на един медикамент[13]. Мета-анализ на 33 рандомизирани клинични проучвания, включващи 13 095 участници, показва по-добра редукция в АН и по-добър контрол на АН при ниски до стандартни дози комбинирани терапии в сравнение със стандартни доза монотерапия с приблизително еднакъв процент на преустановяване на терапиите[18]. Данни от реалната клинична практика демонстриат 18.5% по-бързо достигане на таргетните нива на АН при начална комбинирана терапия, корелиращо с 23% редукция в риска от ССС и смъртност[19]. Само по себе си бързото постигане на добър контрол на АН е предпоставка за по-добро придържане на пациента към предписаното лечение, което от своя страна води до по-добър дългосрочен контрол на АН и съответно по-значима редукция в сърдечно-съдовите събития. Резултатите показват, че комбинираните терапии подобряват прогнозата и чрез механизми, осъществяващи съдова и ренална протекция извън тази, която се постига с редукцията в артериалното налягане. Възможността за достигане на по-значимо намаляване на стойностите на АН при по-ниски дози медикамент от своя страна намалява честотата на нежеланите лекарствени реакции.
Кръстосани контролни изследвания демонстрират, че пациенти, отговарящи добре на един клас медикаменти могат да не отговарят на друг. Употребата на повече от един медикамент в лечението на АХ води и до преодоляване на хетерогенния отговор към монотерапията при различ -
48 І Medical Magazine | юли 2023
ни пациенти. По данни от клинично проучване с изключение на някои групи пациенти, като по-възрастни и немощните, рискът от прекомерна хипотония е само малко по-висок от този, придружаващ първоначалната монотерапия или плацебо, дори при пациенти с умерено първоначално повишаване на АН (хипертония степен 1).
Често срещани и използвани комбинации са АСЕ-инхибитор/АRB + калциев антагонист, АСЕ-инхибитори/АRB + тиазиден диуретик, б-блокер + тиазиден диуретик, Са-антагонист + тиазиден диуретик, както и тройни комбинации с АСЕ-инхибитор/ARB + Ca-aнтагонист + тиазиден диуретик. Като първа линия на терапия с препоръчват комбинациите АСЕ-инхибитор/АRB + Са-антагонист и АСЕ-инхибитор/ARB + тиазиден диуретик, подкрепено с многобройни проучвания и сигурни доказателства за ефективност и полза в редукцията на сърдечно-съдовите събития[20,21,22,23]
В проучването ACCOMPLISH комбинацията
АСЕ-инхибитор + Са-антагонист (беназеприл – амлодипин) превъзхожда комбинацията
АСЕ-инхибитор + тиазиден диуретик (беназеприл – хидрохлортиазид) по отношение намаляването на сърдечно-съдовите събития и
смъртност, без значима разлика в редукцията
на АН. В PROGRESS се изследва ефективност-
та на терапия с периндоприл с или без диуретик при пациенти с хипертония и пациенти
с нормално АН и анамнеза за преживян инсулт. Монотерапията с периндоприл не води до значима редукция в СС риск спрямо плацебо за разлика от комбинираната терапия периндропил + индапамид при значима разлика и в редукцията на АН[20]
Друг важен въпрос е под каква форма да се приема комбинирана терапия – фиксирани или свободни комбинации. От една страна фиксираните дози комбинирани лекарства правят титрирането на медикаментите по-трудно, но множество проучвания демонстрират, че намаляването на броя приемани таблетки подобрява придържането към терапията. Мета-анализ на проучвания, сравняващи фиксирани комбинации и съответните медикаменти, приемани в различни таблетки демонстрира статистичeски значимо подобрение в къмплайнса на пациента и нестатистически значима разлика в стойностите на АН при single-pill терапията[23]. Следва да се отбележе, че приема на фиксирани комбинации намалява вероятността от възникване на те -
рапевтични грешки. Ръководствоството за лечение на АХ на ESC препоръчва използването на комбинации от 2 или повече медикамента в една таблетка (single pill). Комбинацията от една таблетка облекчава както психологическото, така и финансовото обременяване при голямо натоварване с таблетки, което води до по-добро разбирателство и придържане.
В анализ на над 12 000 пациенти с атеросклероза стриктното спазване на терапията се свързва с по-ниски нива на големи нежелани сърдечни събития (MACE) и по-висока ефективност на разходите при двугодишно проследяване.
Въпреки изобилието от доказателства, все още много клиницисти не са склонни да предписват комбинация от две лекарства като терапия от първа линия. Докато две трети от пациентите се нуждаят от поне две лекарства за контрол в клиничните проучвания, реалните изследвания разкриват несъответствие в данните. От 125 635 пациенти с хипертония, на 80.4% е предписана монотерапия, 36% от които са преминали на комбинирана терапия след три години, в сравнение със 78% от първоначално лекуваните с комбинирани лекарства[12]. След като пациентите са започнали монотерапия, рядко са получавали допълнително лекарство, въпреки неадекватния контрол, което предполага, че първоначалната стратегия е решила окончателния план за лечение. Проучването илюстрира неуспеха на стъпаловидно лечение в клинична -
та практика, въпреки че е толкова често срещано и привидно радикално.
ВЪЗРАСТНИ Честотата на артериалната хипертония непрекъснато нараства като резултат от нарастващата продължителност на живота и експоненциалното увеличение на населението над 80 години. Загубата на самостоятелност, животът в старчески дом, значим когнитивен дефицит обичайно са изключващи критерии в големите проучвания за лечението на хронични заболявания. По тази причина и данните за отношението полза/риск от антихипертензивното лечение на тази група пациенти е отностително ограничено. Пациентите в напреднала и старческа възраст с хипертония често имат множество съпътстващи заболявания и поради това често получават полифармакотерапия, което може да доведе до нежелани събития и повишена заболеваемост. Възрастните хора чес -
[www.medmag.bg ] 49
то страдат от нарушение на хемо -
динамичната авторегулация, което
води до по-висок риск от хипотен -
зивни епизоди и последващи пада -
ния. Въпреки че възрастните хора са
с по-висок абсолютен риск от сери -
озни нежелани събития (SAE), свър -
зани с хипотония, синкоп и падане, относителният риск не се различава
значително между хората <75 и >75
години, с изключение на хората >85
години поради ограничени данни
за тази популация. В SPRINT интен -
зивното антихипертензивно лече -
ние води до повишен риск от сери -
озни нежелани събития, включващи
хипотония и вероятно синкоп, но не
и падания, което е в противоречие с
данни от реалната практика за пови -
шен брой хоспитализации за фрак-
тури на бедрената шийка до 30 дни
след започване на антихипертензив -
на терапия[17]
Няколко плацебо-контролирани
проучвания нееднозначно доказват ползата от редукция в артери -
алното налягане и при възрастни
хора. Средната възраст на пациентите в тях е между 70-76 г. с изключение на проучването HYVET [22] , където всички пациенти са над 80г. Освен това се наблюдава и добър толеранс към антихипертензивната терапия. Рost hoc анализ както на HYVET, така и на SPRINT не открива връзка между ползите от антихипертензивното лечение и слабостта на пациента. Следователно и двете проучвания стигат до извода, че стратегиите и целите на антихипертензивното лечение при немощни по-възрастни пациенти трябва да бъдат подобни на стратегиите за лечение, използвани в най-здравите подгрупи пациенти. На базата на това и актуалните ръководства за лечение на АХ препоръчват възрастните пациент (дефинирани като пациенти >65 г.) да бъдат лекувани спрямо общите препоръки, а при много възрастните (дефинирани като пациенти >80 г.) да се обмисли монотерапия или комбинирана терапия с минимални дози на избраните медикаменти.
ЗАКЛЮЧЕНИЕ
Режимите с две или повече лекарства е предпочитаната терапия в лечението на артериалната хипертония, като само няколко изключения изискват монотерапия и последващо надграждане на терапията. По-конкретно, комбинациите в една таблетка преодоляват клиничната
инерция и увеличават придържането на пациента чрез създаване на по-хомоложен отговор в хетероложната популация. При разпознаване на уязвим пациент трябва да се приложи по-предпазлив и индивидуализиран подход с по-голям акцент върху безопасността. Въпреки че базираната на ръководства медицинска терапия е принципът на лечението, все още са необходими индивидуализиран
подход към всеки пациент, съобразен с общото състояние, придружаващите заболявания и рискови фактори. В реалната практика обект на лечение е конкретен пациент с уникален сърдечно-съдов профил, а не статистически изведен такъв от клинични проучвания.
1. Kotseva K et al, "Lifestyle and impact on cardiovascular risk factor control in coronary patients across 27 countries: Results from the European Society of Cardiology ESC-EORP EUROASPIRE V registry.," European Journal of Preventive Cardiology., pp. 824-835, 2019.
2. Williams B, Mancia G, Spiering W, Agabiti Rosei E, Azizi M, Burnier M, Clement DL, Coca A, de Simone G, Dominiczak A, Kahan T, Mahfoud F, Redon J, Ruilope L, Zanchetti A, Kerins M, Kjeldsen SE, Kreutz R, Laurent S, Lip GYH, McManus R, Narkiewicz K, Ruschitzka F, Schmieder RE, Shlyakhto E, Tsioufis C, Aboyans V, Desormais I; ESC Scientific Document Group, "2018 ESC/ ESH Guidelines for the management of arterial hypertension: The Task Force for the management of arterial hypertension of the European Society of Cardiology (ESC) and the European Society of Hypertension (ESH)," European Heart Journal, p. 3021–3104, 2018.
3. Abegaz TM, Shehab A, Gebreyohannes EA, Bhagavathula AS, Elnour AA, "Nonadherence to antihypertensive drugs," Medicine, p. 5641, 2017.
4. Ettehad D, Emdin CA, Kiran A, Anderson SG, Callender T, Emberson J, Chalmers J, Rodgers A, Rahimi K, "Blood pressure
lowering for prevention of cardiovascular disease and death: a systematic review and meta-analysis.," Lancet, pp. 957-967, 2016.
5. Whelton PK, Carey RM, Aronow WS, Casey DE Jr, Collins KJ, Dennison Himmelfarb C, DePalma SM, Gidding S, Jamerson KA, Jones DW, MacLaughlin EJ, Muntner P, Ovbiagele B, Smith SC Jr, Spencer CC, Stafford RS, Taler SJ, Thomas RJ, Williams KA Sr, Williamson JD, Wright JT Jr, "ACC/AHA/AAPA/ABC/ ACPM/AGS/APhA/ASH/ASPC/NMA/PCNA Guideline for the Prevention, Detection, Evaluation, and Management of High Blood Pressure in Adults: A Report of the American College of Cardiology/American Heart Association Task Force on Clinical Practic," Hypertension, pp. 13-115, 2018.
6. Unger T, Borghi C, Charchar F, Khan NA, Poulter NR, Prabhakaran D, Ramirez A, Schlaich M, Stergiou GS, Tomaszewski M, Wainford RD, Williams B, Schutte AE, "2020 International Society of Hypertension Global Hypertension Practice Guidelines," Hypertension, pp. 1334-1357, 2020.
7. Burnier M, Egan BM, "Adherence in Hypertension," Circulation, pp. 1124-1140, 2019.
8. Claxton AJ, Cramer J, Pierce C., "A
systematic review of the associations between dose regimens and medication compliance," Clin Ther., 2001.
9. Staessen JA, Wang JG, Thijs L., "Cardiovascular prevention and blood pressure reduction: a quantitative overview," Hypertension, pp. 1055-1076, 2003.
10. Neal B, MacMahon S, Chapman N, "Effects of ACE inhibitors, calcium antagonists, and other blood-pressurelowering drugs: results of prospectively designed overviews of randomised trials. Blood Pressure Lowering Treatment Trialists' Collaboration," Lancet, pp. 19551964, 2000.
11. ALLHAT Officers and Coordinators for the ALLHAT Collaborative Research Group, "Major outcomes in high-risk hypertensive patients randomized to angiotensin-converting enzyme inhibitor or calcium channel blocker vs diuretic: The Antihypertensive and Lipid-Lowering Treatment to Prevent Heart Attack Trial (ALLHAT)," JAMA, pp. 2981-2997, 2002.
12. Rea F, Corrao G, Merlino L, Mancia G, "Initial Antihypertensive Treatment Strategies and Therapeutic Inertia," Hypertension, pp. 846-853, 2018.
13. Wald DS, Law M, Morris JK, Bestwick
JP, Wald NJ, "Combination therapy versus monotherapy in reducing blood pressure: meta-analysis on 11,000 participants from 42 trials.," The American Journal of Medicine, pp. 290-300, 2009.
14. King P, Peacock I, Donnelly R, "The UK prospective diabetes study (UKPDS): clinical and therapeutic implications for type 2 diabetes.," Br J Clin Pharmacol., pp. 643-8, 1999.
15. Kjeldsen SE, Hedner T, Jamerson K, Julius S, Haley WE, Zabalgoitia M, Butt AR, Rahman SN, Hansson L. Kjeldsen, "Hypertension Optimal Treatment (HOT) Study," Hypertension, pp. 1014-1020, 1998.
16. Salim Yusuf, DPhil, FACC; Eva M. Lonn, MD, FACC, "Heart Outcomes Prevention Evaluation–3 - HOPE-3," NEJM, 2016.
17. SPRINT Research Group; Wright JT Jr, Williamson JD et al, "A randomized trial of intensive versus standard blood-pressure control.," NYJM, pp. 2103-2116, 2015.
18. Salam A, Kanukula R, Atkins E, Wang X, Islam S, Kishore SP, Jaffe MG, Patel A, Rodgers A., "Efficacy and safety of dual combination therapy of blood pressurelowering drugs as initial treatment for hypertension: a systematic review and meta-analysis of randomized controlled
trials.," Hypertension, pp. 1768-1774, 2019.
19. Gradman AH, Parisé H, Lefebvre P, Falvey H, Lafeuille MH, Duh MS "Initial combination therapy reduces the risk of cardiovascular events in hypertensive patients: a matched cohort study.," Hypertension, pp. 309-318, 2013.
20. PROGRESS Collaborative Group.., "Randomised trial of a perindopril-based blood-pressure-lowering regimen among 6,105 individuals with previous stroke or transient ischaemic attack.," Lancet, pp. 1033-1041, 2001.
21. Anushka Patel, P Glasziou, ADVANCE Collaborative Group, "Effects of a fixed combination of perindopril and indapamide on macrovascular and microvascular outcomes in patients with type 2 diabetes mellitus (the ADVANCE trial): a randomised controlled trial.," Lancet, pp. 829-840, 2007.
22. Nigel S. Beckett et al, "Treatment of Hypertension in Patients 80 Years of Age or Older," NEJM, pp. 1887-1898, 2008.
13. Gupta AK, Arshad S, Poulter NR "Compliance, Safety, and Effectiveness of Fixed-Dose Combinations of Antihypertensive Agents," Hypertension, pp. 399-407, 2010.
50 І Medical Magazine | юли 2023
ИЗПОЛЗВАНА ЛИТЕРАТУРА:
КАРДИОЛОГИЯ

[www.medmag.bg ] 51
КАРДИОЛОГИЯ
Г. Костов, д.м. МЦ „Медконсулт“ - Плевен
Ритъмни и проводни
нарушения при сърдечна
недостатъчност
Ключови думи: Внезапна сърдечна смърт, камерна тахикардия, ляв бедрен блок, предсърдно мъждене, сърдечна недостатъчност, хоспитализация.
В световен аспект броят на хоспитализациите за сърдечна недостатъчност (СН) се увеличава, като голяма част от епизодите на декомпенсация са свързани с аритмии (предсърдно мъждене). ПМ и СН се изявяват съвместно. ПМ се документира при 44% от пациентите хоспитализирани за остра СН и при 37.6% от болните с хронична СН. Хроничната СН удвоява риска от сериозни камерни аритмии, 50% от смъртните случаи при СН се дължат на внезапната сърдечна смърт (ВСС), като най-честата причина e камерна тахикардия/камерно мъждене (KT/KM).
Над 15 милиона пациен -
ти в Европа са с прояви на
сърдечна недостатъчност
(СН). В общата популация
честотата на СН е в грани -
ците на 2-3%, като честотата на СН се
увеличава рязко при възраст над 75
години, достигайки до над 20% при
възраст на 80 и над 80 години[1]. Сър -
дечните аритмии са значим рисков фактор за заболеваемост и смъртност при пациентите със СН. Регистрира се и увеличаване броя на хоспитализациите на болните със СН, като голяма част от епизодите на декомпенсация са свързани с поява на аритмии[2].
Предсърдното мъждене (ПМ) е
най -честата аритмия при СН, независимо от съпътстващата левокамерна фракция на изтласкване (ФИ), като увеличава риска от тромбо-емболични усложнения (особено инсулт)
и може да наруши сърдечната функция, водейки до влошаване на симп -
томите на СН. Честотата на ПМ и СН
нараства константно през послед-
ните десетилетия, като често се изявяват едновременно и взаимно се потенцират. Скорошните Регистри
показват, че при около 40% от хос -
питализираните болни със СН вече има анамнестични данни за ПМ и при 20% се регистрира новопоявило се ПМ по време на хоспитализацията[3]. Инцидентната СН, провокирана от ПМ, е свързана с по-благоприятна прогноза, но новопоявилото се ПМ при пациент с установена СН е свързано с по-лоша прогноза, вероятно защото от една страна е маркер за по-тежка болест, а от друга страна нарушава сърдечната функция[4]. Sharma AK и съавтори обсъждат връзката между ПМ и застойна сърдечна недостатъчност (ЗСН) като разглеждат резултатите от Фрамингамското проучване[5]. В голяма кохорта от пациенти от Фрамингамското проучване, 26% от пациентите с диагностицирано за първи път ПМ имат данни за ЗСН като съпътстваща диагноза и 16% от останалия контингент развиват СН в период на проследяване от 5.6 години. Сред пациентите, които развиват ЗСН, 24% са имали предишна или съпътстваща диагноза на ПМ и 17% са развили ПМ през последващия период на проследяване от 4.2 години. Честотата на ЗСН е 3.3% годишно при пациентите с ПМ, а честотата на новопоявило се ПМ при пациенти със предхождаща ЗСН
е 5.4% годишно[6]. Sharma A. и съавтори, които анализират данните при над 200 000 пациенти със СН, включени в The Guidelines-Heart Failure Registry (GWTG-HF), по отношение на сърдечните коморбидности установяват тенденция към увеличаване честотата на ПМ от 32% на 37%[5,6] Според Sharma AK и съавтори, въпреки че познати генетични типове играят важна роля в развитието на ПМ и ЗСН при много индивиди, мнозинството от случаите с ПМ и ЗСН са вторични усложнения на други сърдечни състояния. Възрастта, мъжкият пол, артериалната хипертония (АХ), метаболитният синдром, захарният диабет (ЗД), алкохолната консумация, тютюнопушенето и неврохормоналната активация, възпалението, хипертиреоидизмът и хирургичните интервенции са най-честите фактори, които повишават риска за развитието на ПМ и ЗСН[7]. Сърдечните рискови фактори (РФ) включват: 1) исхемична болест на сърцето (ИБС) (с всички РФ за коронарна болест); 2) клапни сърдечни болести; 3) левокамерна систолна и диастолна дисфункция; 4) миокардит и инфилтративна кардиомиопатия. Независим РФ за ПМ са повишените нива на С-реактивен
52 І Medical Magazine | юли 2023
протеин[8] и повишените нива на хомоцистеина[9], както субклиничният
и клиничният хипертиреоидизъм[10]
и асимптомната ЛК дисфункция. ПМ
и ЗСН имат много общи РФ, които се простират далеч над предразполагащите състояния. Според Sharma AK
и съавтори, ПМ и ЗСН са много чести състояния, които предразполагат
едно към друго, имат общи РФ и са причина за заболеваемост и смъртност сред общата популация. Тези състояния имат обща патофизиология, която включва структурно и
електрическо ремоделиране, дисрегулация на вътреклетъчния калций и невроендокринни механизми, както
и обща генетична основа. Комплекс -
ни клетъчни, молекулярни, неврохормонални, структурни и електрофизиологични процеси са свързани
с повишаване риска за двете състояния. При болшинството от болните точното значение на ПМ и СН за клиничното състояние на пациента е трудно да се определи, тъй като ПМ
често е причина за изява на СН и от
друга страна СН може да е причина
за изява на ПМ. Пациенти с хронична СН и перманентно ПМ имат по-ло -
ша прогноза от тези в синусов ритъм, но това се обяснява до голяма сте -
пен с по-напредналата възраст и тежестта на СН[11]. Swedberg K и съавт.
също установяват, че пациентите с хронична СН и перманентно ПМ, които са в по-напредналата възраст и са със СН с намалена фракция на изтласкване, имат по-лоша прогноза от тези в синусов ритъм, което е свързано с възрастта и степента на СН[12]. Големите клинични проучвания доказват, че наличието на ПМ и СН заедно влошават симптомите и смъртността е по-висока, отколкото когато е налице само едно от двете състояния (SOLVD, V-HeFT)[13,14]. Данните от подгруповите анализи на големите клинични проучвания SOLVD (Studies of Left Ventricular Dysfunction), CHARM (Candesartan in Heart Failure Assessment of Reduction in Mortality and Morbidity) и V-HeFT (Valsartan in HF) за това, дали ПМ е независим предиктор за смъртност при пациентите със ЗСН са противоречиви[13,14,15].
Извършен е ретроспективен анализ на данните от 3-годишно проследяване на 6517 пациенти с ПМ от проучването SOLVD, които имат асимптомна или симптомна левокамерна дисфункция. В проучването SOLVD, ПМ се свързва със значително повишаване на общата смъртност (RR 1.34, 95% CI 1.12–1.62, p50.01), смъртността свързана със ЗСН (RR 1.42, 95% CI 1.09–1.85, p50.01) и смъртността и хоспитализаците за ЗСН (RR 1.26, 95% CI 1.03–1.42, p50.02). Това се дължи на повишената смъртност поради помпена недостатъчност (16.7 % срещу 9.4%). Проучването CHARM включва 7599 болни със симптомна ЗСН с редуцирана и със запазена ЛК ФИ, от които 18% имат и ПМ при включването им в проучването. След проследяване в продължение на 38 месеца се установява, че ПМ е свързано с повишен риск от обща смъртност, както при пациентите с ниска ЛК ФИ (40%) (RR 1.29, 95% CI 1.14–1.46, 37% срещу 28%), така и при пациентите със запазена ЛК ФИ (RR 1.72, CI 1.45–2.06, 24% срешу 14%)[16]. В V-HeFT I и II, в което са включени 1,427 болни със СН с NYHA клас II–III, от които 14% имат и ПМ, няма сигнификантна разлика в заболеваемостта или в смъртността, когато се сравняват пациентите с ПМ и тези без ПМ . Персистираща камерна честота >150 в мин. при болни с ПМ, може да причини СНзФИ, която претърпява обратно развитие след контрол на честотата или корекция на ритъма („тахикардиомиопатия”)[17]. Въпреки по-добрата преживяемост на пациентите с възстановен синусов ритъм в сравнение с пациентите, които остават с ПМ с контрол на честотата, стратегията за контрол на ритъма няма особени предимства пред стратегията за контрол на честотата[5,11]. Катетърната аблация и терапията с различни устройства – пейсмейкър и ресинхронизираща терапия, може да има благоприятни резултати при пациентите с ПМ и ЗСН. Пациенти с хронична СН и перманентно ПМ имат по-лоша прогноза от тези в синусов ритъм, но това се обяснява до голяма степен с по-напредналата възраст и тежест-
та на СН[11,18]. Според препоръките на Европейското кардиологично дружество за лечение на ПМ, ПМ трябва да бъде класифицирано (първи диагностициран епизод, пароксизмално, персистиращо, продължително персистиращо или перманентно), а подходът към него да съответства на настоящите препоръки за ПМ като си даваме сметка за несигурността относно действителната продължителност на епизода и за предшестващи неоткрити епизоди[19]. Според Европейското кардиологично дружество следните моменти трябва да се имат предвид при пациенти със СН представящи се с ПМ, независимо от ЛКФИ, особено с първи диагностициран епизод на ПМ или пароксизмално ПМ: идентификация на потенциално коригируеми причини (напр. хипертиреоидизъм, електролитни нарушения, неконтролирана хипертония, митрална клапна болест) и провокиращи фактори (напр. скорошна хирургия, инфекция в гръдния кош или обостряне на ХОББ/астма, остра миокардна исхемия, алкохолен запой), тъй като те могат да определят стратегията на поведение[19]
Ритъмните и проводни нарушения се срещат често при болните със сърдечна недостатъчност, като с амбулаторния електрокардиографски запис се регистрират камерни екстрасистоли при всички пациенти със СН. Епизодите на безсимптомна непродължителна камерна тахикардия (КТ) са чести, като честотата им се увеличава с прогресирането на СН и камерната дисфункция и са показател за неблагоприятна прогноза при пациенти със СН, но имат малка роля за разграничаване между внезапна сърдечна смърт (ВСС) и смърт поради прогресираща СН[19,20] Според Diseroti M. и съавтори ВСС е много честа при болните със сърдечна недостатъчност особено при пациентите с NYHA II и III ФК (съответно 50-80% и 30-50% от всички смъртни случаи). Механизмът за ВСС зависи от това дали СН е вторична като последствие на исхемична болест на сърцето (ИБС) или на дру -
[www.medmag.bg ] 53
го заболяване. При ИБС ВСС се дължи предимно на камерни аритмии:
камерна тахикардия (КТ), камерно
мъждене (КМ), които са причине -
ни от риентри механизъм в инфар -
ктната зона или от остри исхемич -
ни епизоди. При неисхемичните
сърдечни заболявания процентът
на ВСС причинена от аритмии из -
глежда е по-нисък. Голям процент
от случаите на ВСС при СН са свър -
зани с електромеханична дисоциа -
ция или белодробен или системен
емболизъм[21]. Според Parmley WW.
и съавтори аритмиите са много чес -
ти при пациенти със ЗСН, особено
при тези със съпътстващи ИБС. Спо -
ред авторите степента на левокамерната дисфункция е най-важният
индикатор за прогнозата при пациентите с тежка СН, като с най-висок
риск от ВСС са комплексните камер -
ни аритмии. Друг неблагоприятен
фактор е, че всички медикаменти,
които се използват за лечението на
аритмиите при ЗСН имат и потен -
циален проаритмичен ефект [22]. Бра -
дикардия и паузи също се наблю -
дават често, особено през нощта, когато симпатикусовата активност
е често по-ниска, а парасимпатикусовата активност по-висока; пусков механизъм може да бъде сънната апнея[23,24]. Паузите са свързани с лоша прогноза при пациенти с коронарна болест (КБ) и левокамерна дисфункция, като брадиаритмията може да има важен принос за ВСС при СН[25,26]. Според Zannand F. честотата на проводните нарушения и особено на левия бедрен блок (ЛББ) силно корелира с възрастта и с наличието на сърдечносъдово заболяване. ЛББ се среща при около 25% от пациентите със СН и има връзка с влошаването и прогресията на СН, което в клиничната практика често се подценява. Авторът обобщава данни от научната литература, които показват, че ЛББ чрез медииране на вътрекамерната асинхрония довежда до влошаване на сърдечната функция, сърдечно ремоделиране и СН[27]. Baldasseroni S и съавт., които анализират данните от италиянски регистър за СН установяват, че:
основната диагноза при 2512 болни (45.6%) е исхемична болест на сърцето (ИБС), при 1988 (36.0%) – дилатативна кардиомиопатия (ДКМП) и
хипертонична сърдечна болест при 714 (12.9%) от болните, останалите 303 болни (5.5%) са с друга причина за СН. ЛББ се установява при 1391 болни (25.2%). Според авторите ЛББ е предиктор на по-висока смъртност по всякаква причина (HR 1.70; 95%,CI 1.41 до 2.05), както и за ВСС (HR 1.58; 95% CI, 1.21 до 2.06)[27]. Според Baldasseroni S, и съавтори, ЛББ е предиктор за по-висока честота както на ВСС, така и на по-висока обща смъртност при болни със СН, според данните за 5517 болни от италиянски регистър за СН[27]
Ритъмните и проводни нарушения (ПМ, КТ, ЛББ) при болни със СН значително влошават прогнозата както при СН с намалена ФИ, така и при СН със запазена ФИ на лява камера. ВСС която най-често свързна с камерни аритмии е основната причина за смърт при болните със СН.
ИЗПОЛЗВАНА ЛИТЕРАТУРА:
1. Mosterd A, Hoes AW.Clinical epidemiology of heart failure. Heart 2007;93:1137–46.
2. LauYC, Lane DA, Lip GY. Atrial fibrillation and heart failure: a bad combination. Am J Cardiol 2014;113:1196–7).
3. 3.Ambrosy AP, FonarowG, Butler J, et al. The global health and economic burden of hospitalizations for heart failure: lessons learned from hospitalized heart failure registries. J Am Coll Cardiol. 2014 Apr 1;63(12):1123-1133.
4. Ponikowski P, Voors AA, Anker SD, Bueno H,et al.; Authors/Task Force Members. 2016 ESC Guidelines for the diagnosis and treatment of acute and chronic heart failure: the Task Force for the diagnosis and treatment of acute and chronic heart failure of the European Society of Cardiology (ESC) Developed with the special contribution of the Heart Failure Association (HFA) of the ESC. Eur Heart J. 2016; 37:2129–2200.
5. Sharma AK, Mansour M, Ruskin JM, Heist EK. Atrial Fibrillation and Congestive Heart Failure. Review Article. The Journal of Innovations in Cardiac Rhythm Management,2 (2011), 253-262.
6. Sharma A, Xin Zhao, B.G.Hammil et al. Patients Hospitalized for Heart Failure: Insights From the Get With The GuidelinesHeart Failure Registry. Critical Heart Failure.2018 Jun;11(6):e004646.
7. Anderson JL, Allen Maycock CA,
Lappe´ DL, et al. Frequency of elevation of C-reactive protein in atrial fibrillation. Am J Cardiol 2004; 94(10):1255–1259., 867 Deswal A, Petersen NJ, Feldman AM, et al. Cytokines and cytokine receptors in advanced heart failure: an analysis of the cytokine database from the Vesnarinone trial (VEST). Circulation 2001; 103(16):2055–2059.
8. Lund LH, Mancini D: Heart failure in women. Med Clin North Am 2004; 88:1321–1345.
9. Marcucci R, Betti I, Cecchi E, et al. Hyperhomocysteinemia and vitamin B6 deficiency: new risk markers for nonvalvular atrial fibrillation? Am Heart J 2004; 148(3):456–461.
10. Sawin CT, Geller A, Wolf PA, et al. Low serum thyrotropin concentrations as a risk factor for atrial fibrillation in older persons. N Engl J Med 1994; 331(19):1249–1252.
11. Hoppe UC, Casares JM, Eiskjaer H, et al. Effect of cardiac resynchronization on the incidence of atrial fibrillation in patients with severe heart failure. Circulation 2006;114:18–25.,15- 223
12. Swedberg K, Olsson LG, Charlesworth A, et al.Prognostic relevance of atrial fibrillation in patients with chronic heart failure on long-term treatment with betablockers:results from COMET. Eur Heart J 2005;26:1303–1308.
13. Carson PE, Johnson GR, Dunkman WB, et al. The influence of atrial fibrillation
on prognosis in mild to moderate heart failure. The V-HeFT Studies. The V-HeFT VA Cooperative Studies Group. Circulation 1993; 87(6 Suppl):VI102–110.
14. Dries DL, Exner DV, Gersh BJ, et al. Atrial fibrillation is associated with an increased risk for mortality and heart failure progression in patients with asymptomatic and symptomatic left ventricular systolic dysfunction: a retrospective analysis of the SOLVD trials. Studies of Left Ventricular Dysfunction. J Am Coll Cardiol 1998; 32(3):695–703.
15. Olsson LG, Swedberg K, Ducharme A, et al. Atrial fibrillation and risk of clinical events in chronic heart failure with and without left ventricular systolic dysfunction: results from the Candesartan in Heart failure-Assessment of Reduction in Mortality and morbidity (CHARM) program. J Am Coll Cardiol 2006; 47(10):1997–2004.).
16. Olsson LG, Swedberg K, Ducharme A, et al. Atrial fibrillation and risk of clinical events in chronic heart failure with and without left ventricular systolic dysfunction: results from the Candesartan in Heart failure-Assessment of Reduction in Mortality and morbidity (CHARM) program. J Am Coll Cardiol 2006; 47(10):1997–2004.
17. Calvo N, Bisbal F, Guiu E, et al. Impact of atrial fibrillation-induced tachycardiomyopathy in patients
undergoing pulmonary vein isolation. Int J Cardiol 2013;168:4093–4097.,18-157 Morris PD, Robinson T, Channer KS. Reversible heart failure: toxins, tachycardiomyopathy and mitochondrial abnormalities. Postgrad Med J 2012;88:706–712.
18. Swedberg K, Olsson LG, Charlesworth A, et al.Prognostic relevance of atrial fibrillation in patients with chronic heart failure on long-term treatment with betablockers:results from COMET. Eur Heart J 2005;26:1303–1308.
19. Kirchof P, Benussi S et al. 2016 ESC Guidelines for the management of atrial fibrillation developed in collaboration with EACTS. Eur Heart J. 2016. doi: 10.1093/ eurheartj/ehw210.
20. Camm AJ, Kirchhof P, Lip GYH, Schotten U, et al. Guidelines for the management of atrial fibrillation: the Task Force for the Management of Atrial Fibrillation of the European So- ciety of Cardiology (ESC). Eur Heart J 2010;31:2369–2429.
21. Diseroti M.,Dallafior D., Marini M.Arrhythmia risk stratification based on etiological and anatomo-structural factors. Ital Heart J Suppl 2001 Dec;2(12):1265-9.).
22. Parmley WW., Chatterjee K..Congestive heart failure and arrhythmias: An overview Am J Cardiol.1986, vol.57 (3),Jan.1986:B34-B37.
23. Cintra FD, Leite RP, Storti LJ, Bittencourt LA, Poyares D, Castro L
de S, Tufik S, Paola A de. Sleep apnea and nocturnal cardiac arrhythmia: a populational study. Arq Bras Cardiol 2014;103:368–374.
24. Gilat H, Vinker S, Buda I, Soudry E, Shani M, Bachar G. Obstructive sleep apnea and cardiovascular comorbidities: a large epidemiologic study. Medicine (Baltimore) 2014;93:e45.
25. Bloch Thomsen PE, Jons C, Raatikainen MJP, et all. Long-term recording of cardiac arrhythmias with an implantable cardiac monitor in patients with reduced ejection fraction after acute myocardial infarction: the Cardiac Arrhythmias and Risk Stratification After Acute Myocardial Infarction (CARISMA) study. Circulation 2010;122:1258–1264.
26. Faggiano P, D’Aloia A, Gualeni A, et al. Mechanisms and immediate outcome of in-hospital cardiac arrest in patients with advanced heart failure secondary to ischemic or idiopathic dilated cardiomyopathy. Am J Cardiol 2001;87:655–657, A10–A11.
27. Baldasseroni S, Opasich C, Gorini M, et al., Italian Network on Congestive Heart Failure Investigators Left bundlebranch block is associated with increased 1-year sudden and total mortality rate in 5517 outpatients with congestive heart failure: a report from the Italian network on congestive heart failure. Am Heart J. 2002;143(3):398
54 І Medical Magazine | юли 2023
КАРДИОЛОГИЯ
В. Янчева, А. Неутов, С. Казаков, С. Иванова, А. Келчев, д.м. Отделение по Кардиохирургия, УМБАЛ „Аджибадем Сити Клиник - Сърдечно-съдов център“ - София
Ключови думи: Артериални графтове, радиална артерия, две вътрегръдни артерии, тотална артериална реваскуларизация, аорто-коронарен байпас.
Аорто-коронарен байпас с повече от един артериален графт - опитът
на „Аджибадем Сити Клиник“ - София
В последните препоръки за миокардна реваскуларизация на европейските асоциации по кардио-торакална хирургия и кардиология се утвърждава нова насока в коронарната хирургияиндикация с клас I за използване на по-голям брой артериални графтове. Артериалните графтове, сравнени с венозните, увеличават продължителността и качеството на живот, намаляват риска от ОМИ и нуждата от реинтервенции. В настоящия материал са разгледани основните рандомизирани проучвания, доказващи предимствата на артериалните байпаси; показанията, противопоказанията и техниките за използването им; представен е опитът на отделението по Кардиохирургия на Аджибадем Сити Клиник София за период от две години. Поставянето на повече от един артериален байпас при пациенти с многоклонова коронарна болест се прилага рутинно от нашия екип с нисък периоперативен риск и отлични ранни резултати.
Съвместните препоръки[1] на EACTS и ESC за миокардна реваскуларизация от 2018 г. посочват Аорто-коронарния
байпас като най-доброто лечение на ИБС при пациенти: със захарен диабет, ФИ< 35%, стволова стеноза, умерен и висок SYNTAX Score*(>22), както и такива, подлежащи на клапна хирургия. За тези пациенти операцията носи преимущество, в сравнение със стентирането. В много други случаи двата метода на лечение са равностойни. Все повече се налага в практиката екипната работа на кардиохирурзи и инвазивни кардиолози и съвместното обсъждане на всеки конкретен пациент - т.нар. 'Heart Team'.
За пръв път в европейските препоръки бяха включени индикации с клас IB за използването на повече от един
артериален графт** - двете вътре -
гръдни артерии и артерия радиалис.
Нова препоръка с клас I вече е из -
ползването на радиалната артерия
вместо вена сафена магна при висо -
костепенни стенози на коронарните артерии. Все още основната маса
от пациенти, на които се извършва Аорто-коронарен байпас, получа -
ват един артериален (LAD-LITA) и няколко венозни графта. Във водещите кардиохирургични центрове по света има силна тенденция за увеличаване на процента артериални байпаси.
Коронарната реваскуларизация с няколко артериални графта доказано подобрява както краткосрочната, така и дългосрочната преживяемост на пациентите, в сравнение с тези, получили един артериален и венозни графтове. Наблюдава се по-ниска смъртност, нужда от повторна реваскуларизация, миокарден инфаркт и сърдечна недостатъчност; при същия оперативен риск за болния[3]. Най-често за тази цел се използват двете вътрегръдни артерии (BITA) –като in situ или като free graft. Радиалната артерия е другият най-широко използван артериален графт. Тя има дългосрочна проходимост, сходна с тази на дясната вътрегръдна артерия, и със своята дължина може да достигне всеки таргетен съд. При използването на RA и BITA може да се постигне оптимална артериална миокардна реваскуларизация, а това е основополагащо условие за добър резултат в лечението на ИБС.
* SYNTAX Score - точкова система за оценка ИБС според ангиографската находка - анатомична локализация и степен на стенозите, тортуозност и калциноза на съдовете, оклузия и тромбоза в лумена ** Графт - присадка; в сърдечната хирургия: кръвоносен съд от пациента - вена или артерия, който се използва за байпас
ДОКАЗАТЕЛСТВА И КЛИНИЧНИ ПРОУЧВАНИЯ
Съществува нарастваща база данни от доказателства, че колкото по-голям е броят на артериалните байпаси, особено в левия коронарен басейн[4], толкова е по-добра дългосрочната прогноза за пациента - продължителността и качеството му на живот. Добавянето на артерия радиалис като трети артериален байпас, в случаите когато ще се използват и двете вътрегръдни артерии, е свързано с допълнително подобряване на преживяемостта. При по-млади пациенти с голяма очаквана продължителност на живота хирурзите би трябвало да се стремят да постигнат Тотална Артериална Реваскуларизация (ТАР), използвайки BITA и RA[5]
ART проучването излезе през месец
56 І Medical Magazine | юли 2023
КАРДИОЛОГИЯ
октомври 2018 г. с резултати от рандомизирано сравняване на две групи пациенти - съответно получили една или две вътрегръдни артерии. Изненадващо, на десетата година не се откри разлика между двете групи. При по-задълбочен анализ обаче, се вижда, че близо 25% от пациентите в групата с една вътрегръдна артерия са получи -
ли и втори артериален графт - радиална артерия; голям е и процентът на прехвърляне
на пациенти от една група в друга в хода на лечението, което също повлиява на резултатите.
ROMA е най-мащабното проспективно рандомизирано проучване, правено някога в
Проучване Година Брой пациенти Сравнявани графтове Средно проследяване (години) Заключение
Без разлика в проходимостта
По-добра проходимост на RA
По-добра проходимост на RA
По-добра проходимост на RA с/у SVG, еднаква проходимост на RA и RITA
тази област, и включва реномирани болници в САЩ, Италия, Великобритания, Германия, Австрия, Канада, Китай, Русия, Япония и др. През 2018 г. То представлява сравнение на клиничния изход до десетата година от операцията при пациенти с Аорто-коронарен байпас с един, спрямо тези с няколко артериални графта. Големият брой пациенти (4300), дългият период на проследяване и стриктният протокол на проучването го правят и най-достоверно от научна и статистическа гледна точка. Финалният анализ на резултатите му е планиран да се публикува през 2030 г. Счита се, че то ще даде дефинитивно
доказателство за предимството на артериалните байпаси.
НАШИЯТ ОПИТ При извършване на Аорто-коронарен байпас с повече от един артериален графт се спазват всички правила на коронарната хирургия, както и специфичните показания и противопоказания за използване на BITA и RA. Пълнотата на миокардната реваскуларизация (байпас към всички коронарни артерии с големина >1 мм и стеноза >50% от диаметъра на съда) е основен принцип и независим рисков фактор за смъртност. Анастомозата LIТA-LAD е златен
Фиг. 1
Различни конфигурации
на артериалните графтове в зависимост от коронарната анатомия
Фиг. 2 Ендартеректомия на плака от дясна коронарна артерия с имплантиран в нея коронарен стент
Табл. 1 Основни рандомизирани проучвания, сравняващи проходимостта на артериални и венозни графтове
RA: radial artery, RAPCO: Radial artery patency and clinical outcomes study, interim results, final results presented at the 2016 AATS Annual Meeting (results unpublished to date) RA patency better than SVG (p=0.03) and free RITA (p=0.06), RAPS: Radial artery patency study, RITA: right internal thoracic artery, RSVP: Radial artery vs saphenous vein patency trial, SVG: saphenous vein graft, VA: Veteran’s Administration
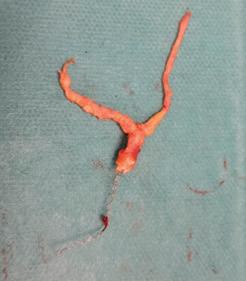

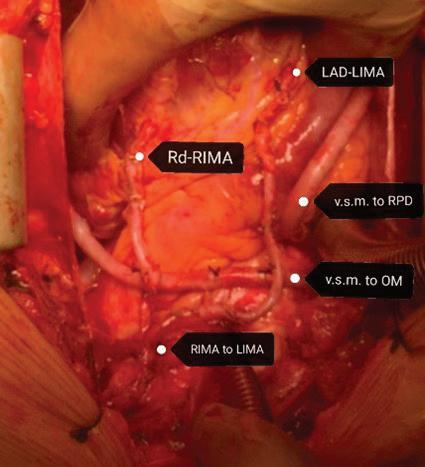
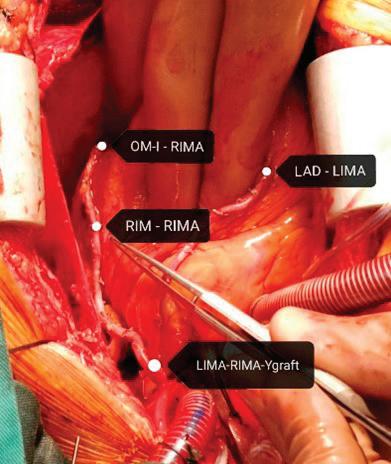
[www.medmag.bg ] 57
VA 2011 733 RA, SVG
RSVP 2008 142 RA, SVG 5
RAPS 2012 561 RA, SVG 7.7
RAPCO 2013
RA, SVG,
10
1
619
RITA
стандарт при този вид операции. Изборът на втори и трети артериален графт и планирането на конфигурацията им (композитни графтове, секвенциални анастомози) е важна част от предоперативната подготовка на пациента, но крайното решение се взима винаги интраоперативно.
За период от 2 години (05/201805/2020) в отделението по Кардиохирургия на Аджибадем Сити Клиник, София, са оперирани 266 пациенти с изолиран аорто-коронарен байпас.
LAD е реваскуларизирано с LITA във
всички случаи, освен тези с компро -
ментиран кръвоток и лошо качест-
во на графта. 94 са получили пове -
че от един артериален графт, което
представлява 35.4% от всички коро -
нарни пациенти. След изписването те
се проследяват според протокола на
клиниката на 1-та, 5-та и 10-та година
от операцията. В тази група 30-днев-
на смъртност и периоперативен МИ
не се наблюдават (0%). Дълбока стер -
нална ранева инфекция е настъпила
при 3 пациенти, като при двама от тях
са били отпрепарирани двете артерии
мамарии. Тези пациенти са третира-
ни с вакуум терапия за 7-14 дни след
което при всички се отдаде стернална
рефиксация и миопластика с пекторални мускули. Общият брой дистал-
ни анастомози с артериални графтове е 211 (средно 2,3 на пациент). Артерия
радиалис е поставена на 31 пациен-
та, а 14 са получили две вътрегръдни
артерии + радиална артерия. В случаите, в които използваме и двете вътрегръдни артерии, използваме техниката на скелетиране при тяхното отпрепариране. Средният постоперативен престой в болницата е 6,6 дни. Използването на мултиартериална реваскуларизация се използва както при изолиран аортокоронарен бай-пас, така и при комбинирани оперативни интервенции с реконструкция или протезиране на аортна или митрална клапи, без това да влияе върху ранните постоперативни резултати.
При пациенти под 75-годишна възраст, без противопоказания ( морбиден обезитет, или гликиран хемоглобин >7 mmol/l) се използват два или повече артериални графта: LITA към LAD като първи + RIТA и/или RA според коронарната анатомия, качеството на графтовете и преценката на оператора, като обичайната конфигурация е Y – графт, при който дясната артерия мамария се анастомозира за лявата по типа край – страна , а артерия радиис обикновено се анастомозира с асцендентната аорта. В общия случай допълнителните артериални байпаси преимуществено се използват към втория по значимост съд в левия коронарен басейн и PD. При пациенти с по-голяма очаквана продължителност на живота се стремим да постигнем тотална артериална реваскуларизация.
ПОКАЗАНИЯ И ХИРУРГИЧНИ
ТЕХНИКИ
- BITA - Скелетирането (отпрепариране без ламбо от тъкан и прилежащи вени) увеличава достъпната дължина на артерията, намалява деваскуларизацията на стернума, запазвайки неговото кръобращение и намалява риска от дълбока стернална ранева инфекция. Двете вътрегръдни артерии могат да се използват за байпас към коронарните съдове, без да се прекъсват в проксималния им край (in situ). По-честата конфигурация е т.нар. Y-graft: дясната вътрегръдна артерия се прекъсва в двата си края, след което се зашива за лявата по типа край-страна. Засягането на ITA от атеросклеротични плаки е казуистика. Все пак предоперативната ангиографска оценка на кръвотока през тях и интраоперативната инспекция на съдовата стена потвърждават доброто качество на графтовете.
- RA - Aртерия радиалис има силно изразена мускулна медия, пора -
ди което е склонна към спазъм в определени ситуации. Тя изисква повече технически умения и опит от страна на оператора, тъй като най-честите причини за спазъм са грубото манипулиране на артерията или зашиването и към съд с несигнификантна стеноза и голям конкурентен кръвоток. Радиалната артерия винаги се отпрепарира с прилежащите вени и се третира със специални вазодилатиращи
разтвори по протокола на съответната клиника. Предоперативната
и оценка е от изключително значение и включва: подробна анамнеза (професия, доминантна ръка, преживени травми), ехографско Doppler изследване и модифициран Allen тест*. Пациентите приемат Ca-антагонист 3-6 месеца постоперативно.
*Тестът е нормален при <6 секунди; граничен при 6-10 секунди и абнормен при >10 секунди. Всички пациенти с време под 10 секунди претърпяват харвестинг на радиалната артерия без исхемични усложнения на ръката. Задължително се използва пулс-оксиметър, винаги на I-ви пръст (той е с най-слаба колатерална мрежа), като се отчита времето до възстановяване на изходните пулсова крива и сатурация, а не единствено цвят на кожата.
ПРОТИВОПОКАЗАНИЯ Напредналата възраст (>80 г.), както и хронични съпътстващи заболявания, ограничаващи очакваната продължителност на живота са противопоказания за мултиартериална реваскуларизация. От голямо значение са степента на увреда и калибърът на коронарния съд. При значителни атеросклеротични промени, обхващащи дифузно цялото протежение на съда, дългосрочната прогноза не е добра както за артериалните, така и за венозните графтове. Извършването на ендартеректомия също е едно от относителните про -
58 І Medical Magazine | юли 2023 КАРДИОЛОГИЯ Брой чисти коронарни болни От тях с >1 артериален графт % общо 266 94 35,4%
тивопоказания за използване на артериален кондюит.
- BITA (Billateral Internal Thoracic Artery) - Из -
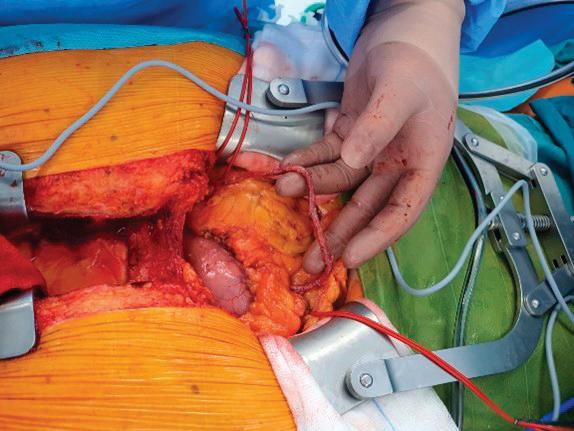
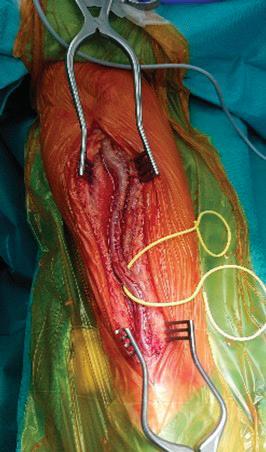
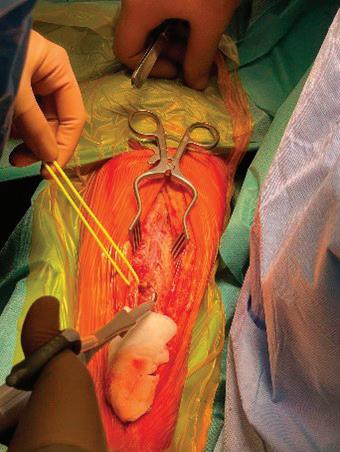
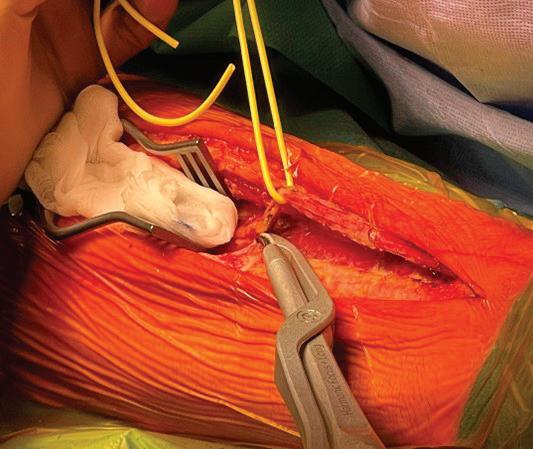
ползването на две вътрегръдни артерии
увеличава риска от стернална дехисцен -
ция и медиастинит при пациенти със захарен диабет, особено некомпенсиран. До -
пускат се болни с контролиран диабет +
нормални стойности на HbA1c. Също така
може да се компроментира зарастването на гръдната кост при пациенти с обезитет, при жени с голям бюст и при много въз -
растни пациенти. Тези рискове се минимализират със скелетирането на двете артерии при отпрепариране.
- RA (Radial Artery) - За неподходяща се счита радиална артерия с вътрешен диаметър <2 мм, такава с атеросклеротични плаки, или забавен кръвоток. Неудачни са и случаите с хипопластична улнарна артерия или вариации в палмарната съдова дъга, поради риск от исхемия на ръката. При пациенти с противопоказани за прием на Ca-антагонисти постоперативно (склонност към хи -
Фиг. 3
Отпрепариране на артерия радиалис с ултразвуков скалпел
Фиг. 4
Дясна артерия гастроепиплоика
[www.medmag.bg ] 59
потония, брадикардия, AV-блок, SSNS) RA следва да се използва с повишено внимание. Не са подходящи и пациентите с ХБН, които са потенциални кандидати за хрониодиализа, поради необходимостта от съдов достъп за А-В фистула.
- RGEA (Right gastroepiploic artery) –
Дясна артерия гастроепиплоика
е призната за подходящ и надежден кондюит за аорто коронарен байпас. От значителен брой про -
учвания знаем, че употребата на
тази артерия не увеличава по ни -
какъв начин хирургичният риск,
като не се появява нито чревна
или стомашна исхемия, нито друг
тип коремни усложнения. Артерия гастроепиплоика, се харвестира по скелетонизиран начин, кое -
то и придава дължина и позволява достигането на различни коронарни артерии, най-често това са клоновете на дясната коронарна артерия.
ЗАКЛЮЧЕНИЕ
В съвременната кардиоваскулар -
на медицина от ключово значение
за постигане на оптимални резулта -
ти има индивидуалният подход от т.нар. Heart Team. Всички пациенти, постъпващи за планова коронарна интервенция се обсъждат и всеки получава най-добрата за него индивидуализирана процедура, като се има предвид общото му състояние, съпътстващите заболявания, наличността и качеството на кондюитите за аортокоронарен байпас. Този подход е благодарение на активната колаборация между кардиолози, интервенционални кардиолози, кардиохирурзи, съдови хирурзи и анестезиолози и води до намаляване на перипроцедурните усложнения и осигуряване на оптимална дългосрочна прогноза при лечението на исхемичната болест на сърцето. Използването на няколко артериални байпаса при пациенти с многоклонова коронарна болест се прилага рутинно от нашия екип с нисък пе -
риоперативен риск и много добри ранни резултати. Развитието на мултиартериална коронарна реваскуларизация през последните години се базира на множеството натрупани доказателства за преимуществата на артериалните графтове и е в синхрон с последните европейски препоръки. Индивидуалният подход, предоперативната оценка на качеството на венозните и артериални графтове и планирането на хирургичната тактика ни позволяват да осигурим на своите пациенти оперативна интервенция, с възможно най-добра дългосрочна прогноза.
Използвани съкращения:
EACTS - European Association for Cardio Thoracic Surgery
ESC - European Society of Cardiology
LITA - Left Internal Thoracic Artery
RITA - Right Internal Thoracic Artery
BITA - Bilateral Internal Thoracic Artery
RA - Radial Artery
1. 2018 ESC/EACTS Guidelines on myocardial revascularization. FranzJosef Neumann Miguel Sousa-Uva
Anders Ahlsson Fernando AlfonsoAdrian
P Banning Umberto Benedetto Robert A
Byme Jean-Philippe ColletVolkmar Falk
Stuart J Head; Peter Juni Adnan Kastrati
Akos Koller Steen D Kristensen Josef
Niebauer Dimitrios j Richter Petar M Seferovic Dirk Sibbing Gulio G Stefanini
Stephan Windecker Rashmi Yadav Michael
O Zembala ESC Scientific Document Group.
European Heart Journal, 25 August 2018
2. Buxton BF, Shi WY, Tatoulis J, Fuller JA, Rosalion A, Hayward PA. Total arterial revascularization with internal thoracic and
radial artery grafts in triple-vessel coronary artery disease is associated with improved survival. J Thorac Cardiovasc Surg. 2014 Oct 3. Pu A, Ding L, Shin J, Price J, Skarsgard P, Wong DR, Bozinovski J, Fradet G, Abel JG Long-term Outcomes of Multiple Arterial Coronary Artery Bypass Grafting: A Population-Based Study of Patients in
British Columbia, Canada. JAMA Cardiol. 2017 Nov 1
4. Benedetto U, Raja SG, Albanese A, Amrani M, Biondi-Zoccai G, Frati G. Searching for the second best graft for coronary artery bypass surgery: A network meta-analysis of randomized controlled trials†. Eur J Cardiothorac Surg 2015
5. Shi WY, Tatoulis J, Newcomb AE, Rosalion A, Fuller JA, Buxton BF Is a third arterial conduit necessary? Comparison of the radial artery and saphenous vein in patients receiving bilateral internal thoracic arteries for triple vessel coronary disease. Eur J Cardiothorac Surg. 2016 Jul
60 І Medical Magazine | юли 2023
ЛИТЕРАТУРА:
ИЗПОЛЗВАНА
КАРДИОЛОГИЯ



























































































































Център за медицина на съня тел. 0878 67 98 98 www.inspiro.bg Полисомнография, Полиграфия, Актиграфия, СРАР титрация