

L ide L –edições técnicas



L ide L –edições técnicas
Autores VII Agradecimentos XI Prefácio ............................................................................................................................................... XIII Fausto J. Pinto Introdução XV
Parte III Anatomia e Fisiologia das Células Cardíacas e Introdução ao Eletrocacardiograma Normal .......................................................................... 1 1. Eletrofisiologia e Eletrocardiograma das Células Cardíacas 2 2. Obtenção do Eletrocardiograma 16 3. Ativação Elétrica das Diversas Estruturas Cardíacas ............................................................ 22 4. Ondas Eletrocardiográficas e sua Nomenclatura ................................................................... 33 5. Eixos Elétricos e sua Determinação 36 6. Rotações do Coração 56 7. O Eletrocardiograma Normal ................................................................................................... 62 8. Variações Eletrocardiográficas .................................................................................................. 80
Parte II Patologia da Onda P e Aumentos Ventriculares 85 9. Patologia das Aurículas 86 10. Patologia dos Ventrículos .......................................................................................................... 94
Parte III Bloqueios 111
11. Bloqueios Auriculoventriculares e Dissociação Auriculoventricular Isorrítmica 112 12. Bloqueios do Ramo Direito 120 13. Bloqueios do Ramo Esquerdo ................................................................................................... 130 14. Bloqueios Fasciculares do Ramo Esquerdo ............................................................................. 143 15. Associação de Bloqueios de Ramo 153 16. Paragens Sinusais versus Bloqueios Sinusais 167
Parte IV Síndromes de Pré-Excitação ................................................................................. 171 17. Síndromes de Pré-Excitação 172
Parte VI Cardiopatia Isquémica 193 18. Isquemia e Lesão 194 19. Necrose ......................................................................................................................................... 221 20. Necrose e Bloqueio de Ramo 229
Parte VI Eletrocardiograma em Situações Patológicas Especiais 239 21. Principais Alterações Iónicas com Repercussão no Eletrocardiograma 240 22. Síndromes Congénitas ............................................................................................................... 248
Parte VII Eletrocardiografia e Pacing ................................................................................. 273 23. Eletrocardiograma e Pacing 274
Parte VIII Eletrocardiografia de Esforço 305 24. Provas de Esforço ....................................................................................................................... 306
Parte IX Arritmias Cardíacas 321 25. Introdução às Arritmias – Conceitos e Mecanismos 322 26. Arritmias Supraventriculares .................................................................................................... 330 Nuno Cortez-Dias, J. C. Machado Rodrigues 27. Arritmias Ventriculares 366 Gustavo Lima da Silva, João de Sousa, J. C. Machado Rodrigues 28. Arritmias da Síndrome de Wolff-Parkinson-White ............................................................... 407 Manuel Nogueira da Silva, J. C. Machado Rodrigues
Parte X Eletrocardiografia Dinâmica (Holter)) 415
Introdução 416 29. A Importância da Eletrocardiografia Dinâmica (Holter/24 horas) no Diagnóstico das 29. Arritmias Supraventriculares .................................................................................................... 418 Manlio F. Márquez Murillo 30. A Eletrocardiografia Dinâmica (Sistema Holter) no Diagnóstico das Arritmias de QRS 29. Largo............................................................................................................................................. 434
Celso Salgado de Melo, Felipe Augusto de Oliveira Souza, J. C. Machado Rodrigues 31. O Holter na Avaliação da Variabilidade da Frequência Cardíaca 446 María José Romero Reyes 32. A Importância da Eletrocardiografia Dinâmica no Diagnóstico da Síncope 454 María José Romero Reyes, Ricardo Pavón Jiménez 33. Valor Diagnóstico e Prognóstico das Alterações da Repolarização Ventricular no 29. Eletrocardiograma Dinâmico de 24 Horas (Holter) 465 Arminda Veiga
Bibliografia Geral ............................................................................................................................... 475 Índice Remissivo 483
edições técnicas
JOsé CARlOs MAChADO RODRigUEs
Nasceu a 26 de janeiro de 1950 em Luanda, Angola.
Iniciou os estudos universitários na Faculdade de Medicina da Universidade de Luanda e terminou o último ano na Faculdade de Medicina da Universidade Clássica de Lisboa.
Internato Policlínico no Hospital de Santa Maria, Lisboa.
Foi médico Residente em Cardiologia no Instituto Nacional de Cardiología – Ignacio Chávez (México), altura em que trabalhou em eletrocardiografia clínica com Gustavo Medrano, Alfredo de Micheli e Abdo Bisteni (1978-1981).
Título Universitário de Cardiologia pela Universidad Nacional Autónoma do México (UNAM) (1978-1981).
Cardiologista pela Ordem dos Médicos Portuguesa. Assistente de Cardiologia pela Carreira Hospitalar (1980). Bolseiro do Instituto Nacional de Investigação Científica (1982).
Residente em Eletrofisiologia e Pacing Cardíaco na Clinique Saint Eloi (França) onde trabalhou com o Prof. Doutor Paul Puech (1982-1983).
Assistente da Faculdade de Medicina da Universidade Nova de Lisboa, de 1981 a 1984.
Foi Chefe de Serviço de Cardiologia da Carreira Hospitalar desde junho de 1995 (Hospital Pulido Valente – Lisboa) e do Serviço de Cardiologia do Centro Hospitalar Universitário Lisboa Norte, EPE, a partir de janeiro de 2008 (Centro Académico de Medicina de Lisboa/ /Centro Cardiovascular da Universidade de Lisboa).
Membro do Centro Académico de Medicina de Lisboa/Centro Cardiovascular da Universidade de Lisboa.
Fundador da Unidade de Pacing do Hospital Pulido Valente (Lisboa), em 1988, da qual foi responsável até 2006.
L
Responsável pelo Centro Universitário de Reabilitação Cardiovascular do Centro Hospitalar Universitário Lisboa Norte, EPE (Hospital Pulido Valente) até 2019.
Fundador e Diretor Clínico do Centro de Reabilitação Cardiovascular da Universidade de Lisboa (CRECUL) – Centro Académico de Medicina de Lisboa/Centro Cardiovascular da Universidade de Lisboa até 2019.
Fundador do Centro de Pacing do Hospital Militar/Instituto Superior de Luanda, República Popular de Angola.
Responsável pela Equipa que ministrou o 1.º Curso de Formação em Pacing no Hospital Militar/Instituto Superior de Luanda, República Popular de Angola.
Membro da equipa de investigação em Eletrocardiografia de Alta Resolução e Processamento Digital do Sinal do Instituto de Desenvolvimento de Novas Tecnologias (UNINOVA) da Faculdade de Ciências e Tecnologia da Universidade Nova de Lisboa.
Investigador do Instituto de Telecomunicações (Fundação para a Ciência e Tecnologia), na aplicabilidade de novas tecnologias na área do pacing cardíaco.
Membro da Sociedade Portuguesa de Cardiologia e da Sociedade Europeia de Cardiologia.
Membro da Sociedad Mexicana de Cardiología, da Sociedad Andaluza e Canária de Estimulación Cardíaca (SACEC) e Membro Honorário da Sociedad Internacional de Internos y Becários del Instituto de Cardiología (SIBIC Internacional).
Membro da APAPE (Associação Portuguesa de Arritmias, Pacing e Eletrofisiologia).
Publicou vários trabalhos na área de Cardiologia, dos quais dois livros: Recomendações Clínicas para Portadores de Pacemaker ou CDI e Electrocardiografia Clínica – Princípios Fundamentais, editados pela Lidel – Edições Técnicas, Lda. É um dos coautores da obra Temas de Marcapasso editado em 2011 pela Leitura Médica, Lda. – S. Paulo – Brasil.
ARMiNDA VEigA
Assistente Hospitalar de Cardiologia no Hospital de Santa Maria (Centro Hospitalar Universitário Lisboa Norte, EPE), Centro Académico de Medicina de Lisboa/Centro Cardiovascular da Universidade de Lisboa.
CElsO sAlgADO DE MElO
Chefe do Serviço de Estimulação Cardíaca Artificial da Universidade Federal do Triângulo Mineiro – Uberaba, MG – Brasil.
FElipE AUgUsTO DE OliVEiRA sOUzA
Mestre em Ciências da Saúde. Especialista em Cardiologia Clínica e em Eletrofisiologia Clinica Invasiva pela Universidade Federal de São Paulo (UNIFESP) – Brasil.
gUsTAVO liMA DA silVA
Assistente Hospitalar de Cardiologia no Serviço de Cardiologia do Hospital de Santa Maria (Centro Hospitalar Universitário Lisboa Norte, EPE), onde integra a equipa de Eletrofisiologia e Pacing da Unidade de Arritmologia Invasiva; Assistente Convidado de Cardiologia na Faculdade de Medicina da Universidade de Lisboa; Investigador no Centro Cardiovascular da Universidade de Lisboa.
edições técnicas
Assistente Hospitalar Graduado de Cardiologia; Coordenador da Unidade de Arritmologia do Centro Hospitalar Universitário de Lisboa Norte, EPE – Hospital de Santa Maria; Assistente Convidado da Faculdade de Medicina de Lisboa; Integra a Direção da Subespecialidade de Eletrofisiologia Cardíaca da Ordem dos Médicos; Consultor de Arritmologia do Hospital dos SAMS e do Hospital Lusíadas em Lisboa.
Subdiretor de Investigação Clínica no Instituto Nacional de Cardiología – Ignacio Chávez (México). Membro da Academia Nacional de Medicina de México. Diretor do Conselho de Electrocardiologia (ElectroSIAC) – Sociedade Interamericana de Cardiología. Secretário da Latin American Heart Rhythm Society.
Grau de Consultor de Cardiologia e Eletrofisiologista do Serviço de Cardiologia do Hospital Santa Marta (Centro Hospitalar Universitário Lisboa Central, EPE – CHULC). Membro da Sociedade Portuguesa de Cardiologia desde junho/1984 e sócio efetivo da Associação Portuguesa de Arritmologia, Pacing e Eletrofisiologia. Responsável pelo Sector de Eletrofisiologia do Serviço de Cardiologia do Hospital Santa Marta (CHULC) de outubro/1988 a fevereiro/2014. É autor e coautor de mais de 280 comunicações e preleções em congressos e reuniões científicas nacionais e internacionais e de 68 publicações em revistas da especialidade.
Licenciada em Medicina. Especialista em Cardiologia. Doutorada em Medicina pela Universidad de Sevilla – Espanha. Mestrados em Investigación en Medicina Clínica, em Diagnóstico por la Imagen en Cardiología, em Ecocardiografía transesofágica, em Cuidados Cardíacos Agudos. Facultativa Especialista em Cardiologia no Hospital Universitario de Valme, Sevilla – Espanha.
Cardiologista; Assistente Hospitalar Graduado do Serviço de Cardiologia do Centro Hospitalar Universitário de Lisboa Norte, EPE - Hospital de Santa Maria; Eletrofisiologista, Sub-coordenador da Unidade de Eletrofisiologia (HSM-CHLN); Consulta de Doenças Arritmogénicas Hereditárias (HSM-CHLN); Responsável do Curso de Introdução à Eletrocardiografia (no âmbito da disciplina de Introdução à Clínica) da Faculdade de Medicina da Universidade de Lisboa.
Licenciado em Medicina pela Universidad de Sevilla – Espanha. Especialista em Cardiologia. Mestrados em Electrofisiología Diagnóstica y Terapéutica pela Universidad Complutense de Madrid – Espanha. Acreditación en la Práctica de Electrofisiología Diagnóstica y Terapéutica pela Sección de Arritmias de la Sociedad Española de Cardiología. Facultativo Especialista em Cardiologia no Hospital Universitario de Valme, Sevilla – Espanha.
edições técnicas
A eletrocardiografia constitui uma das disciplinas mais antigas no âmbito da cardiologia moderna, tendo sido o resultado de uma evolução do conhecimento ao longo dos tempos, que alguns consideram que se iniciou em 1791, quando o médico e físico italiano Luigi Galvani publicou um trabalho relatando como conseguiu movimentar, através do estímulo elétrico, o músculo da perna da rã. Em 1820, o dinamarquês Hans Ørsted verificou que podia medir as pequenas variações da corrente elétrica através do movimento de uma agulha, batizando o aparelho de galvanómetro, em homenagem a Galvani. Em 1842, Carlo Matteucci demonstrou que o nervo da perna da rã, quando estimulado, poderia contrair o músculo abaixo dele. Em 1872, o físico francês Jonas Gabriel Lippmann criou um método revolucionário em que, através de um tubo de vidro fino preenchido com mercúrio e banhado com ácido sulfúrico – eletrómetro capilar –, podia medir a corrente elétrica pelo movimento da coluna de mercúrio; esse movimento era projetado num papel fotossensível, permitindo um registo permanente. Em 1908 recebeu o prémio Nobel da Física pela criação de um método para fazer fotografias coloridas sem utilizar pigmentos ou tinta. E foi em 1887 que Augustus Waller, um fisiologista britânico, criou o primeiro aparelho de eletrocardiograma, usando um eletrómetro capilar e elétrodos colocados no peito de um voluntário, demonstrando, pela primeira vez, que uma atividade elétrica precedia a contração do coração. O médico e fisiologista holandês Willem Einthoven pesquisou durante anos um método não-invasivo para estudar o funcionamento do coração. Em 1901, obteve registos eletrocardiográficos, ligando fios ao pé e mãos de um voluntário mergulhados num balde com uma solução de eletrólitos, ligando depois essas três derivações a uma máquina que, na altura, pesava quase 300 quilos, necessitando de cinco pessoas para operá-la. O seu objetivo era entender “… o funcionamento do coração em detalhe e a causa de uma grande variedade de anormalidades, o que permitirá aliviar o sofrimento de nossos doentes”. Em 1924, recebeu o prémio Nobel da Medicina.
Desde então o eletrocardiograma passou a ser um elemento essencial para o diagnóstico cardiológico, ao mesmo tempo que ajudou à melhor compreensão de muitos fenómenos a nível cardíaco.
Com o passar dos anos e o aparecimento de novas tecnologias, em particular as tecnologias de imagem, parecia que o eletrocardiograma iria perder a sua importância no diagnóstico cardiológico. Contudo, e apesar desses enormes avanços, continua a ter um
papel central na abordagem diagnóstica do doente com suspeita de patologia cardíaca, sendo mesmo crítico nalgumas circunstâncias, como, por exemplo, no diagnóstico de enfarte agudo do miocárdio.
Torna-se, assim, essencial que não se perca o conhecimento sobre tudo o que aprendemos sobre eletrocardiografia e se continue a dispor de ferramentas que ajudem a passar essa informação para as gerações futuras. É neste contexto que surge o presente livro, coordenado pelo meu querido colega e amigo, José Carlos Machado Rodrigues, que o construiu de forma extremamente cuidada e meticulosa, cobrindo, basicamente, todas as áreas da eletrocardiografia atual. Teve ainda o privilégio de se rodear de um conjunto de peritos, quer nacionais quer internacionais, que trouxeram o seu conhecimento e a sua experiência de forma a robustecer ainda mais esta obra. Trata-se, pois, de um trabalho que irá ser muito útil a todos aqueles que queiram saber um pouco mais sobre eletrocardiografia, independentemente do seu nível de conhecimento, pois o livro está feito de forma a poder ser usado tanto pelo estudante de medicina como pelo cardiologista.
É para mim um enorme prazer poder associar-me a esta obra que é também um tributo à cardiologia e, em particular, à eletrocardiografia, pelas mãos de um dos seus artífices que mais se dedicou a esta área e que, ainda hoje, continua a ser uma referência.
Desejo, pois, uma excelente leitura e, acima de tudo, que este livro possa ser de grande utilidade a quem o usar, a fim de poder contribuir para uma melhor prática cardiológica na abordagem do doente com suspeita de patologia cardíaca.
Fausto J. Pinto
Diretor do Departamento do Coração e Vasos do Centro Hospitalar Universitário Lisboa Norte, EPE Professor Catedrático de Cardiologia da Faculdade de Medicina da Universidade de Lisboa Presidente da World Heart Federation
edições técnicas
Este livro de eletrocardiologia clínica é dirigido a todos os profissionais de saúde, especialmente aos internos de cardiologia, cirurgia cardiovascular, cardiologistas e outros médicos que necessitem destes conhecimentos para o desempenho da sua atividade profissional diária.
Procurei escrevê-lo com uma linguagem simples e acessível sem, no entanto, deixar de ser científica. Este livro foi escrito com dificuldade crescente, de modo a facilitar a apreensão da mensagem transmitida, tentando não só fazer a descrição teórica, mas demonstrando através de figuras, esquemas e eletrocardiogramas, todas as situações descritas, de modo que o diagnóstico eletrocardiográfico fosse feito por compreensão lógica e sequencial e não por memorização de parâmetros.
Este livro é um agradecimento e uma homenagem sincera a todos com quem trabalhei e aprendi, muito especialmente à Escola Mexicana de Cardiologia e ao Instituto Nacional de Cardiología – Ignacio Chavez (México) onde fiz a minha especialização em cardiologia, aos meus mestres de eletrocardiografia com quem tive a honra de trabalhar e de criar amizade, sendo eles, entre outros, o Dr. Gustavo Medrano, Dr. Alfredo de Michelli, Dr. Abdo Bisteni e Dr. Manoel Cárdenas, para eles vai o meu muito obrigado e a minha especial homenagem. Não posso esquecer outro dos meus grandes mestres e a quem quero também homenagear – o Prof. Doutor Paul Puech com quem trabalhei durante um ano em eletrofisiologia e pacing na Clinique Saint Eloi em Montpellier – França.
Não posso deixar de referir duas pessoas que não conheci pessoalmente, mas que através dos seus trabalhos em eletrocardiografia criaram em mim paixão por este tema, são eles o Dr. Soddi Pallares, Dr. João Tranchesi e Dr. Bayés de Luna, o primeiro de nacionalidade mexicana, o segundo de nacionalidade brasileira e o terceiro de nacionalidade espanhola, com cujos livros de eletrocardiografia da sua autoria me iniciei.
Não quero deixar de agradecer e homenagear todo o pessoal do Serviço de Cardiologia do Hospital Pulido Valente com quem trabalhei desde 1988 até 2019, assim como toda a equipa do Serviço de Cardiologia do Hospital Santa Maria (Centro Académico de Medicina de Lisboa/Centro Cardiovascular da Universidade de Lisboa) e em especial ao seu diretor – Prof. Doutor Fausto Pinto – a quem agradeço a confiança, apoio e amizade.
Tenho ainda de dirigir uma palavra de agradecimento, à equipa de Reabilitação Cardiovascular do Centro Hospitalar Universitário Lisboa Norte pela qual fui responsável
e à equipa do Centro de Reabilitação Cardiovascular da Universidade de Lisboa (CRECUL), centro do qual fui fundador e diretor clínico até ao final de 2019.
Espero que este livro de eletrocardiografia seja digno da Escola Mexicana de Cardiologia e dos mestres e amigos com quem trabalhei.
J. C. Machado Rodrigues (Coordenador)
Anatomia e Fisiologia das Células Cardíacas e Introdução ao Eletrocardiograma Normal
Anatomia e Fisiologia das Células Cardíacas e Introdução ao Eletrocardiograma Normal Eletrofisiologia e Eletrocardiograma das Células Cardíacas
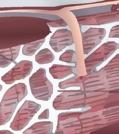

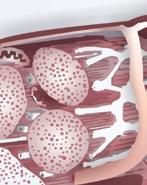
FigurA 1.1 – Principais células cardíacas. A. Célula contrátil (muscular) e seus constituintes: Membrana celular, sarcómero e sistema mitocondrial; B. Célula P (automática) e seus constituintes: Plana, de grande núcleo em relação ao citoplasma envolvente; C. Célula de Purkinje: De aspeto estriado, filiforme, de grande comprimento, de aspeto dendrítico nas suas extremidades; D. Inter-relação da célula de Purkinje com as células musculares cardíacas.
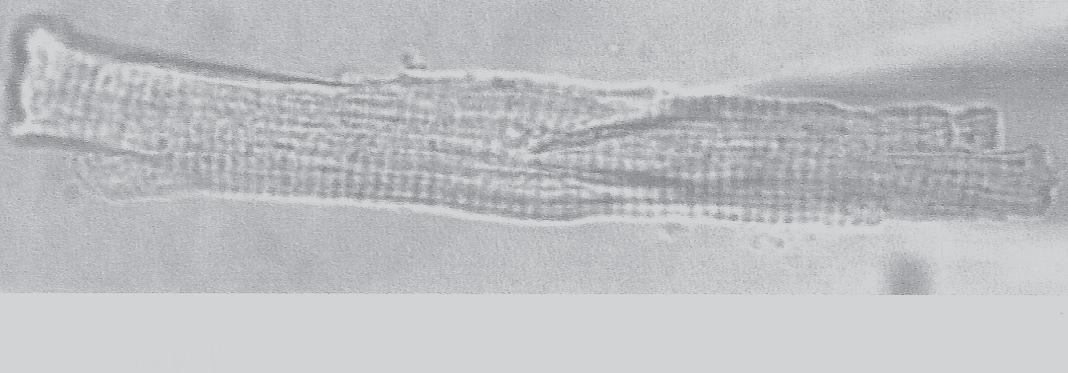
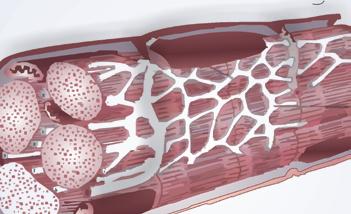
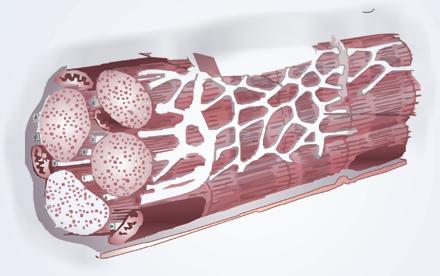
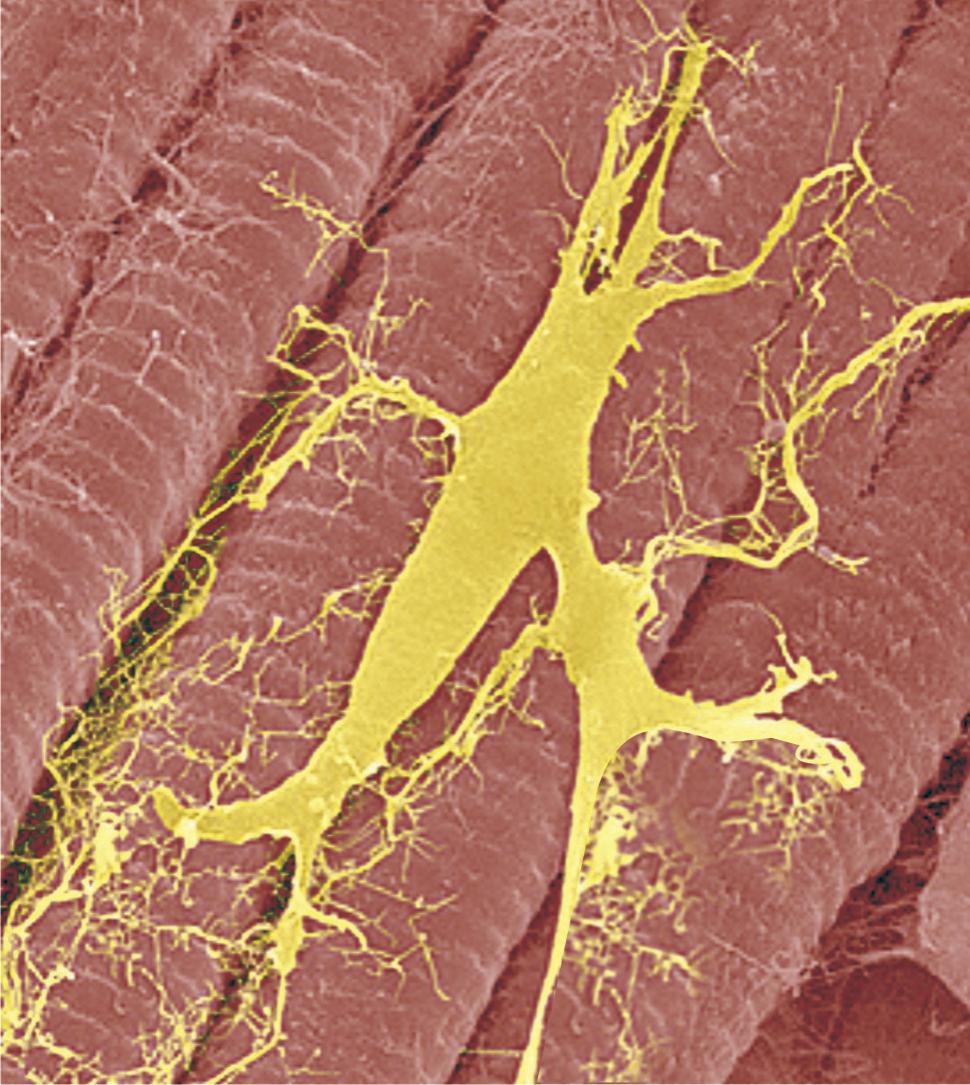
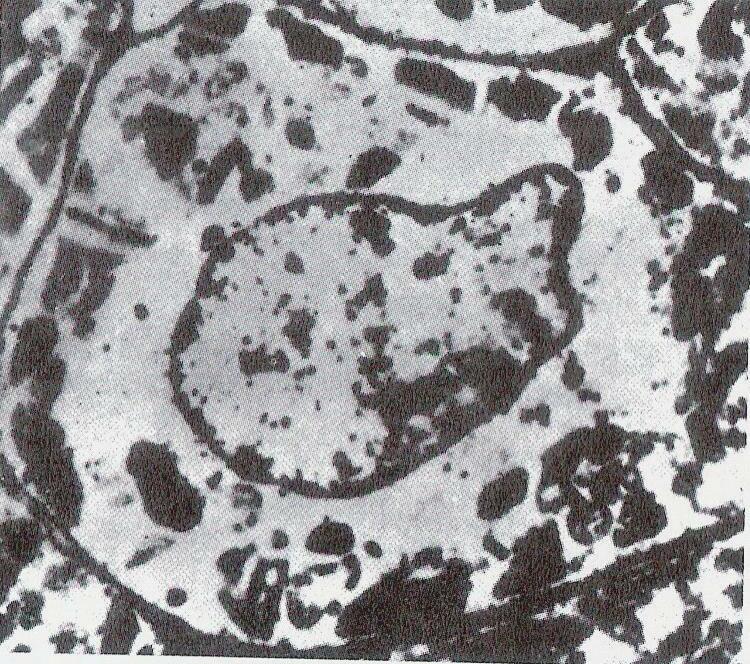
FigurA 1.2 – Diferenças morfológicas dos potenciais de ação de transmembrana. A. Potencial de ação de transmembrana (PAT) numa célula automática (sinusal). Observar a despolarização diastólica (Fase 4) que não se observa no potencial de ação (PA) de uma célula contrátil, como se mostra na figura B. O PA de uma célula de Purkinje é idêntico ao da célula contrátil, diferindo apenas por ter uma ligeira despolarização diastólica; B. Potencial de ação de transmembrana de uma célula contrátil. PL – potencial limiar.



Anatomia e Fisiologia das Células Cardíacas e Introdução ao Eletrocardiograma Normal Obtenção do Eletrocardiograma
aVR+
aVL+ aVR
-150° -30°
-120° -90° -60° aVL 0° - I +30°
aVF+
figuRa 2.4 – Obtenção dos potenciais absolutos das derivações unipolares dos membros (aVR, aVL e aVF).
180° +150° III aVF II
+120° +60° +90°
figuRa 2.5 – Sistema triaxial de Bailey. Disposição angular e a polaridade das derivações frontais.
As derivações precordiais são todas unipolares, em que os elétrodos exploradores (positivo) se colocam em determinados pontos definidos do tórax. Habi tualmente têm 6 localizações distintas no hemitórax esquerdo que se denominam V1, V2, V3, V4, V5 e V6. No entanto, estas derivações em determinadas situações poderão ser feitas até V9. De igual modo, por vezes são necessárias derivações direitas, em que V1 e V2 têm exatamente a mesma localização das esquerdas e as restantes chamadas R ( right) são V3R, V4R, V5R, V6R – podendo ir até V9R, a sua localização é idêntica às esquerdas apenas situadas no hemitórax direito. Assim as derivações precordiais esquerdas têm a seguinte localização ( Figura 2.6):
■ V1 – 4.º espaço intercostal, junto ao bordo direito do esterno;
■ V2 – 4.º espaço intercostal, junto ao bordo esquerdo do esterno;
■ V3 – Entre V2 e V4;
■ V4 – Cruzamento entre o 5.º espaço intercostal e a linha médio ‑clavicular esquerda.
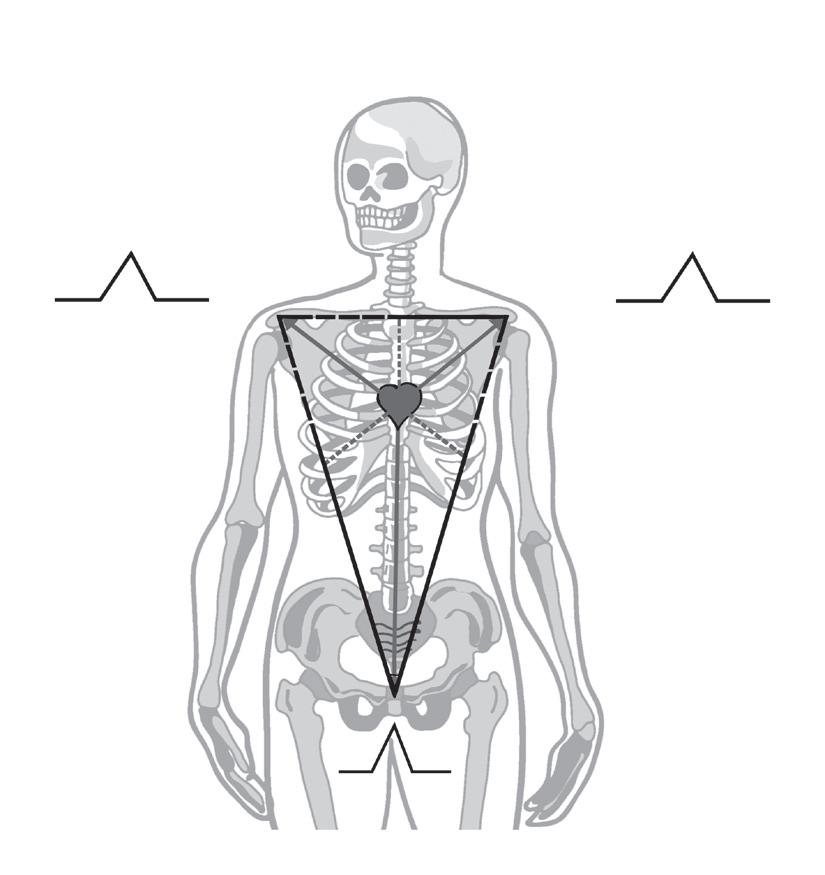
Depois de terem sido publicadas as novas guidelines da American Heart Association Electrocardiography and Arrhythmias Committee (Circulation 2007; 115; 1306‑1324. Part I) as derivações V5 e V6 passaram a ter novas localizações. Nos parágrafos que se seguem estão descritas estas novas localizações e entre parêntesis as que anteriormente eram usadas.
Assim:
Ângulo de Louis 2.º espaço intercostal
f igu R a 2.6 – Localização das derivações precordiais.
■ V5 – localizada no cruzamento do plano horizontal de V4 com a linha axilar anterior esquerda, ou, se esta for de localização ambígua, esta derivação ficará a meia distância entre V4 e V6 (anteriormente – cruzamento entre o 5.º espaço intercostal e a linha axilar anterior esquerda);
FigurA 3.7 – Angiografia da coronária direita. A e B. Obtida em oblíqua anterior direita (OAD) onde se observa a artéria do nódulo sinusal saindo da porção mais proximal da coronária direita e a artéria do NAV saindo junto à crux cardíaca; C e D . Obtida em OAD caudal onde se observa a artéria do NAV saindo da artéria coronária direita no momento em que dá origem à artéria descendente posterior (crux cardíaca). NS – artéria do nódulo sinusal; NAV – artéria do nódulo auriculoventricular.
FigurA 3.8 – Artéria coronária esquerda dominante onde se vê a artéria do nódulo sinusal (NS) emergindo do tronco comum.
anterior do septo interventricular (artérias septais) e para a parede ântero ‑lateral do ventrículo esquerdo (artérias diagonais), terminando em 80 a 90 % dos casos em artérias que rodeiam a ponta do coração e sobem pelo sulco interventricular posterior, anastemosando‑se com os ramos mais distais da artéria descendente posterior. A artéria circunflexa esquerda dirige ‑se
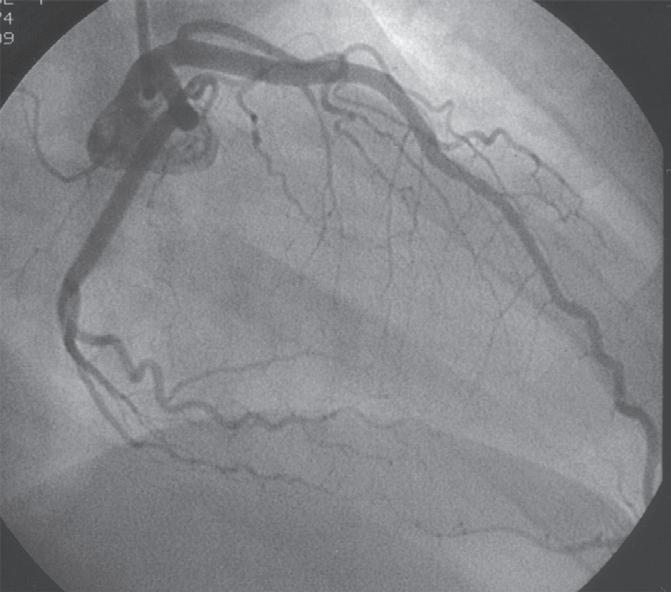
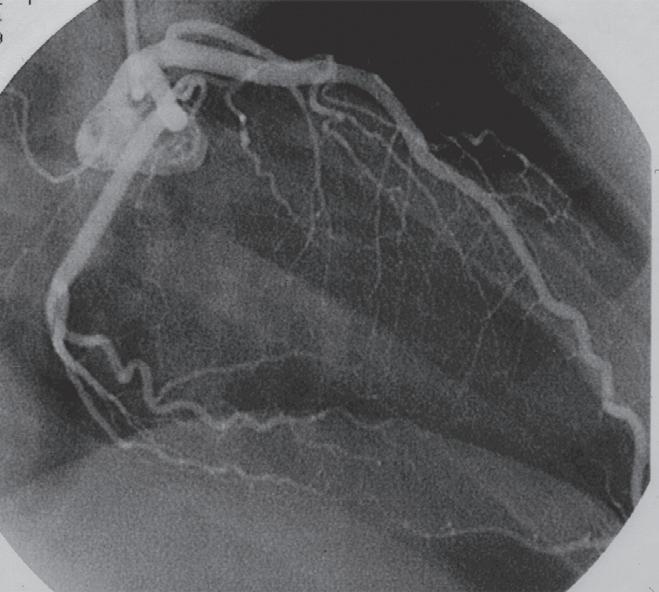
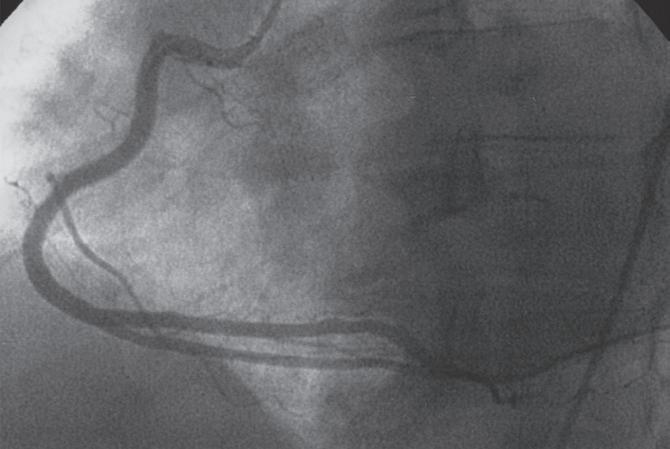
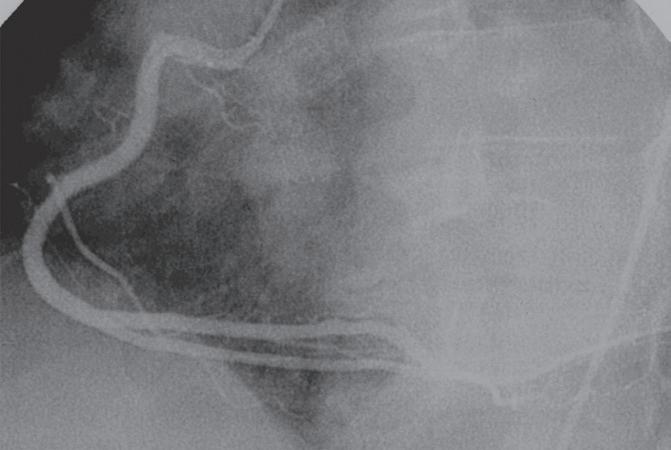
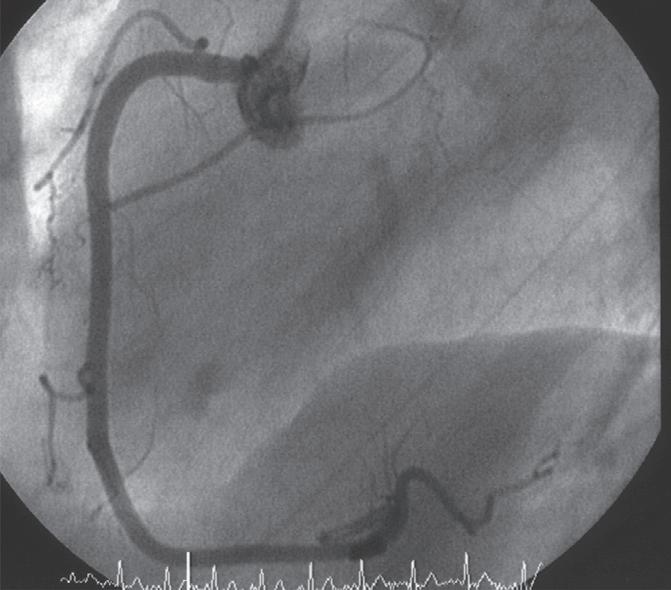
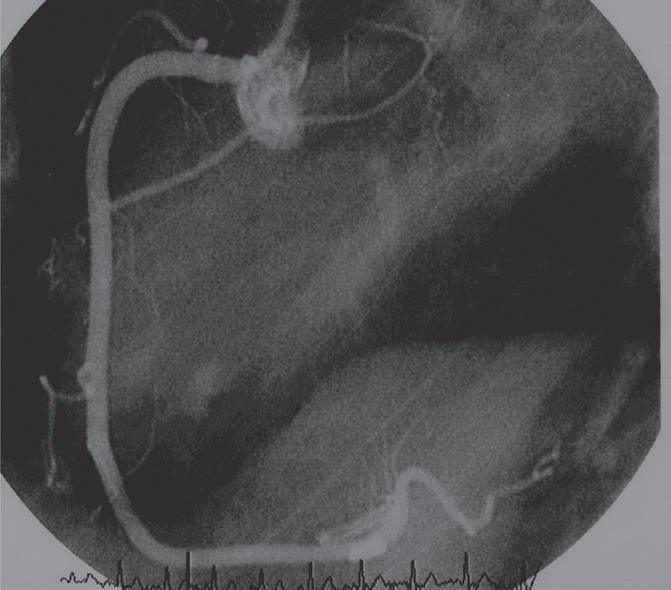
BloqueIo completo e IntermItente do ramo esquerdo do feIxe de HIs
Ver Figura 13.13
Por vezes, encontramos uma intermitência entre um QRS com morfologia normal e um QRS com morfologia de bloqueio completo de ramo. Quer este bloqueio de ramo intermitente quer o bloqueio intermédio de ramo evoluem, na grande maioria dos casos, para bloqueio completo do ramo correspondente.
PR constante de 0,14 seg. QRS de duração variável (entre 0,09 e 0,16 seg). Observe-se: o 1.º, o 2.º, o 6.º e o 7.º QRS com morfologia de bloqueio completo do feixe de His (QRS = 0,16 seg); o 3.º e o 4.º complexos QRS são normais (QRS = 0,09 seg); o 5.º complexo apresenta bloqueio intermédio do feixe de His (QRS = 0,115 seg).
fIgura 13.13 – Bloqueio completo e intermitente do ramo esquerdo do feixe de His.
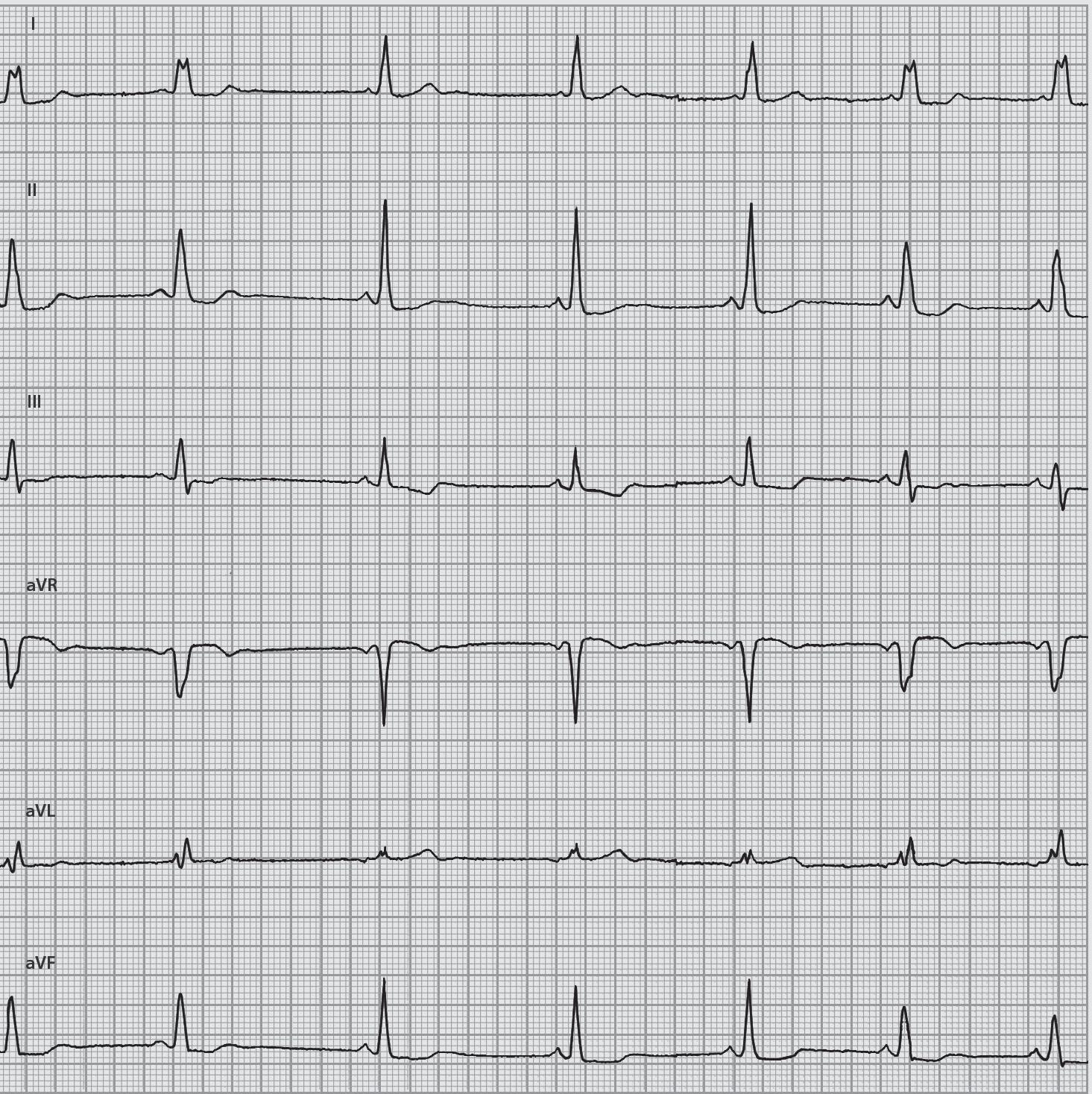
Doente em fibrilhação auricular. Quando a resposta ventricular é mais lenta, os complexos ventriculares são finos (QRS = 0,10 seg) (ver setas). 3.º complexo em I, II, III e 1.º complexo em aVR, aVL e aVF, mas com um ÂQRS = -40º e deflexão intrinsecoide em aVL = 0,06 seg e em aVF = 0,02 seg, (diferencial de 0,04 seg) que corresponde a um bloqueio do fascículo anterior do ramo esquerdo do feixe de His. Quando a resposta ventricular é mais rápida (restantes complexos ventriculares), associase simultaneamente um bloqueio do fascículo posterior do ramo esquerdo do feixe de His, motivo pelo qual observamos no ECG uma morfologia de bloqueio completo do ramo esquerdo (QRS = 0,17 seg) como consequência do bloqueio bifascicular esquerdo.
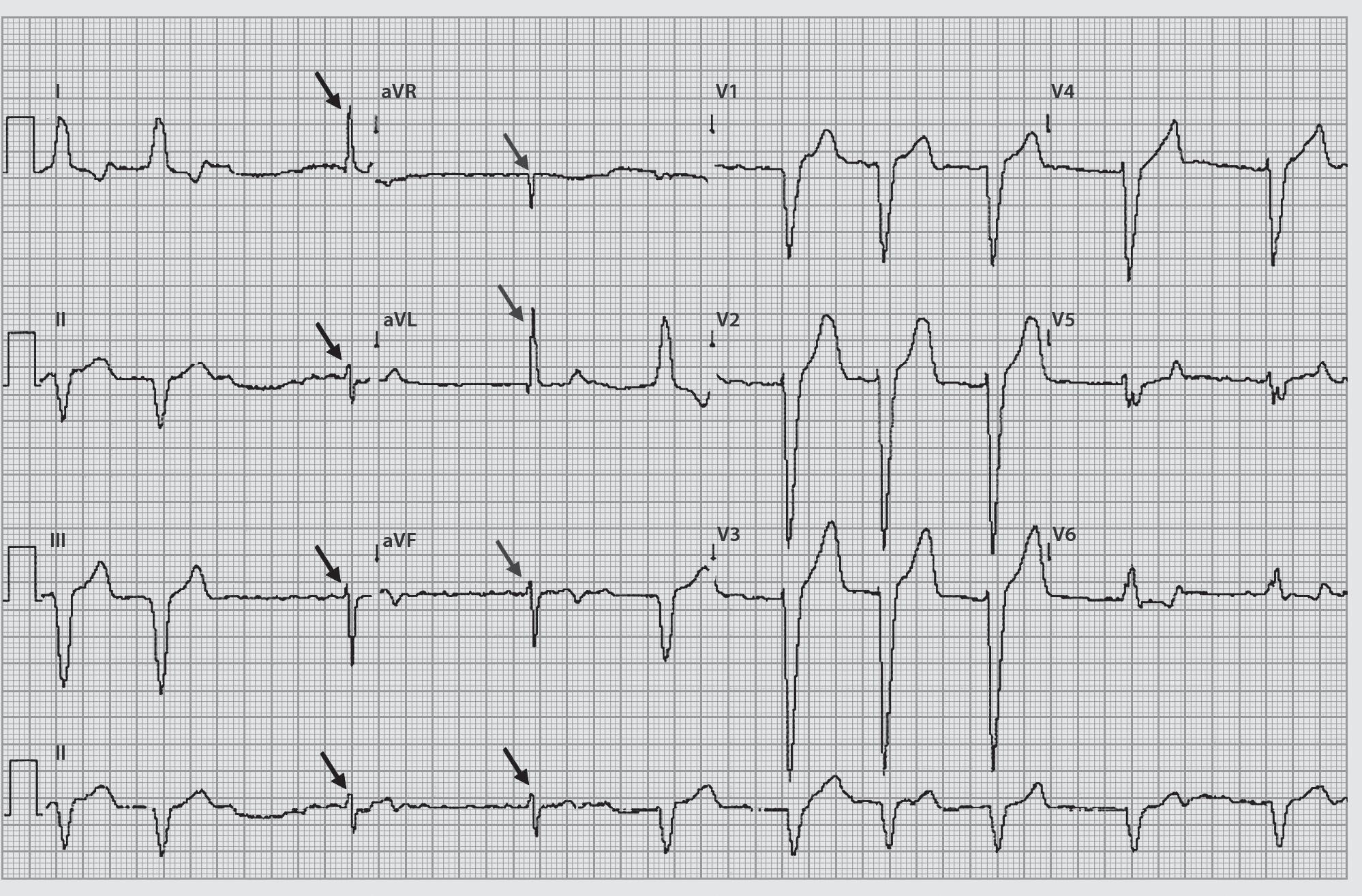
Figura 15.11 – Bloqueio bifascicular esquerdo.
Este bloqueio é devido à associação do bloqueio completo do ramo direito com bloqueio do fascículo anterior e bloqueio do fascículo posterior do ramo esquerdo. Como na associação dos bloqueios anteriormente referidos, estes bloqueios podem ser sincrónicos ou alternantes dos diversos ramos envolvidos.
Deve suspeitar‑se de bloqueio trifascicular quando há um bloqueio bifascicular associado a um bloqueio auriculoventricular ( Figuras 15.12 e 15.13 ), muito espe cialmente se existem modificações dos bloqueios ciclo a ciclo.
A forma mais comum de bloqueio trifascicular é denominada síndrome de Rosenbaum ( Figura 15.14 ), que consiste na presença de bloqueio de ramo direito com alter nância de bloqueio de fascículo anterior e bloqueio do fascículo posterior esquer dos. Esta alternância é acompanhada de modificações da condução auriculoventricular, que confirmam a afetação dos três feixes.
Quando o bloqueio dos três feixes é completo, dá origem a um BAV completo com QRS alargados.
de Bloqueios de Ramotécnicas
■ PR inferior a 0,12 segundos, com QRS normal (sem onda delta);
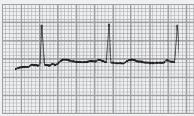
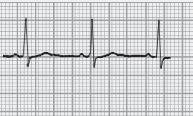
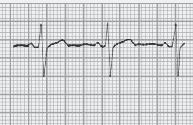
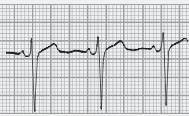
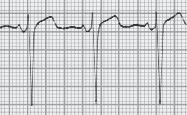
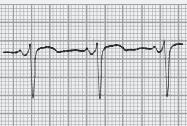
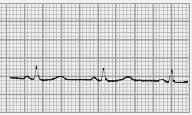
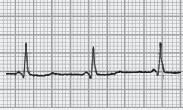
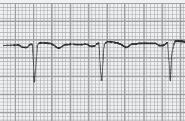
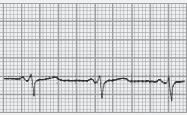
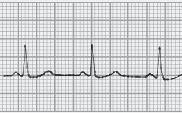
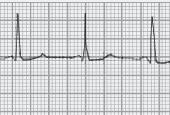
■ A repolarização ventricular é normal – porque a despolarização ventricular se faz com uma sequência normal, em virtude da condução do estímulo se continuar a fazer pelo feixe de His (o by‑pass é aurículo‑hissiano);
■ É frequente observarmos a porção terminal das ondas P sobrepostas com o início do QRS.
Nota: Quando encontramos um PR com duração inferior a 0,12 segundos, é importante que se meçam os PR em todas as outras derivações, pois poderão ter uma duração maior devido à projeção do PR no plano de cada uma das derivações. O PR válido é sempre aquele que tiver maior valor. Daqui se deduz que só poderemos considerar um PR curto se, em todas as derivações eletro cardiográficas, o PR for menor que 0,12 segundos.
Em condições normais, em que não haja pré‑excitação ventricular, o estímulo após ter che gado ao nódulo auriculoventricular (NAV) diminui a sua velocidade de condução (condução decremental), para em seguida chegar ao feixe de His, distribuindo ‑se pelos seus ramos, e, através da rede de Purkinje, despolarizar os ventrículos.
Na síndrome de WPW, a existência de uma via anómala de condução rápida e anterógrada, que liga a aurícula ao ventrículo, tem como consequência uma ativação precoce ventricular a partir do ponto ventricular, onde esta via anómala (feixe de Kent) se insere, levando por isso a um PR curto e a uma onda anómala no início do QRS a que se denomina onda delta (onda ∆).
PR = 0,11 seg com QRS de duração normal e sem onda delta. Observe-se que, em DI, a parte terminal da onda P dos 1.º e 2.º complexos se encontra sobreposta à porção inicial do QRS.
fiGura 17.1 – Síndrome de Lown-Ganong-Levine – PR: 0,11 segundos.
técnicas
Etiologia da síndrome de Wolff‑Parkinson‑White
Está, muitas vezes, associada a outras cardiopatias:
■ Prolapso da válvula mitral;
■ Em 25% dos casos da malformação de Ebstein da válvula tricúspide (WPW tipo B);
■ Em 4% dos casos de cardiomiopatia hipertrófica;
■ Aneurismas do seio coronário;
■ Em 6% dos doentes com hipertiroidismo.
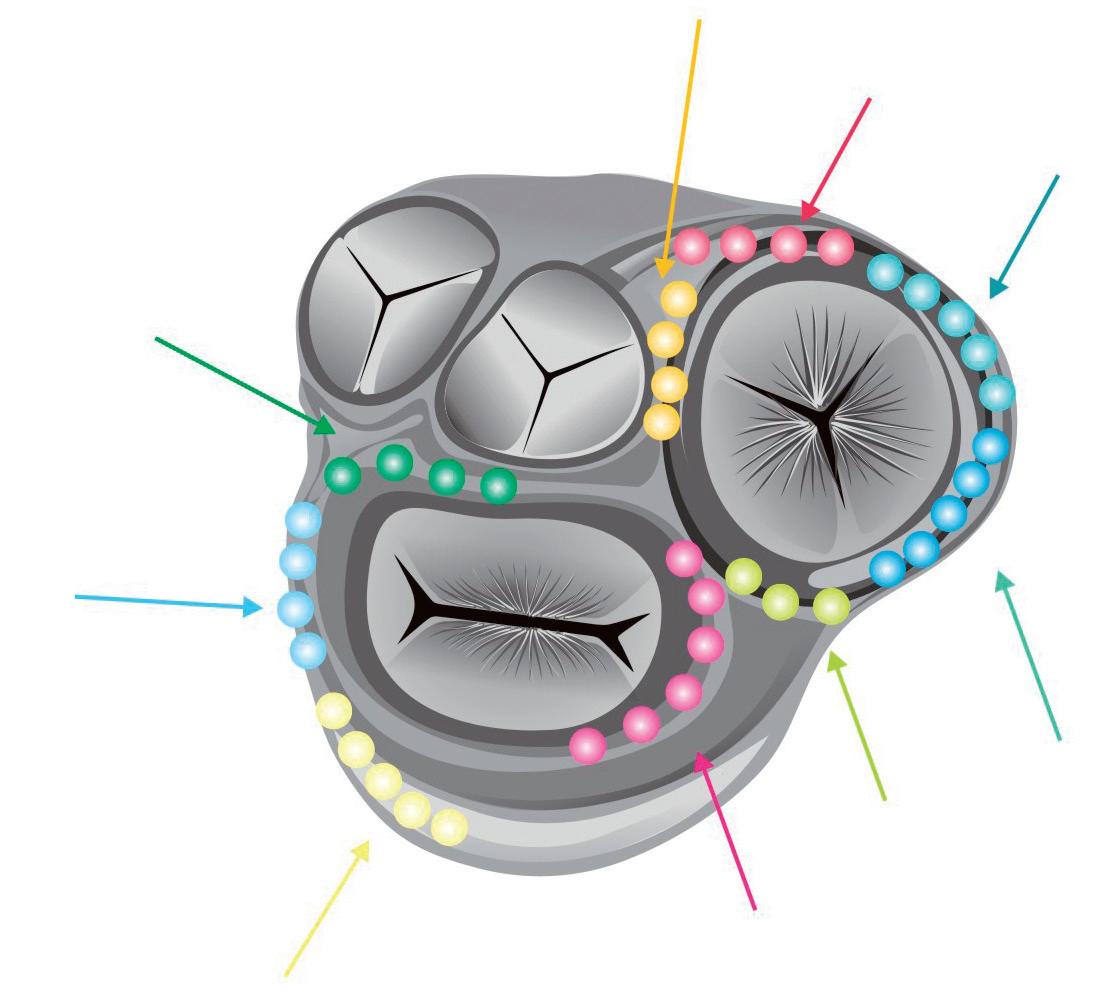
Na Figura 17.10 estão assinaladas as possíveis localizações do feixe de Kent.
Parasseptal anterior direito
Anterior direito Lateral direito
Lateral esquerdo P Ao His VT VM
Anterior esquerdo
Látero-posterior direito
Parasseptal posterior direito
Látero-posterior esquerdo
fiGura 17.10 – Localização anatómica dos feixes de Kent e sua correlação com as principais estruturas cardíacas. P – artéria pulmonar. Ao – aorta. VM – válvula mitral. VT – válvula tricúspide. His – feixe de His.
Nas Figuras 17.11 a 17.26 mostram‑se diversos ECG com as res petivas classificações da localização topográfica do feixe de Kent na síndrome de WPW.
A síndrome de WPW é uma entidade provocadora de arritmias potencialmente letais, mesmo no primeiro episódio. Estas arritmias são supra ventriculares, têm um mecanismo de reentrada que, por vezes (o mais frequente), o estímulo sobe pela via anómala (taquicardias ortodrómicas) e desce pela via normal – do qual resultam QRS estreitos, exceto se houver bloqueio funcional de um dos ramos do feixe de His em que os QRS são alargados. Outras vezes, o sentido ascendente da reentrada dá‑se pela via normal e o descendente pelo fei xe anómalo (taquicardias antidrómicas), dando sempre origem a QRS alargados. O flutter auricular e a fibrilhação auricular são particularmente graves na síndrome de WPW, por que a ausência de condução decremental na via anómala provoca respostas ventricula
Síndromes de Pré-Excitação
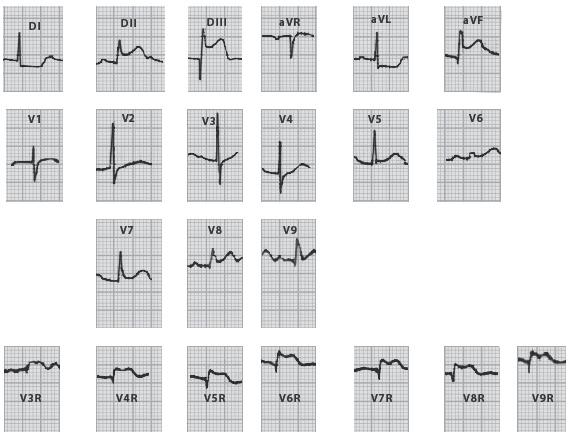
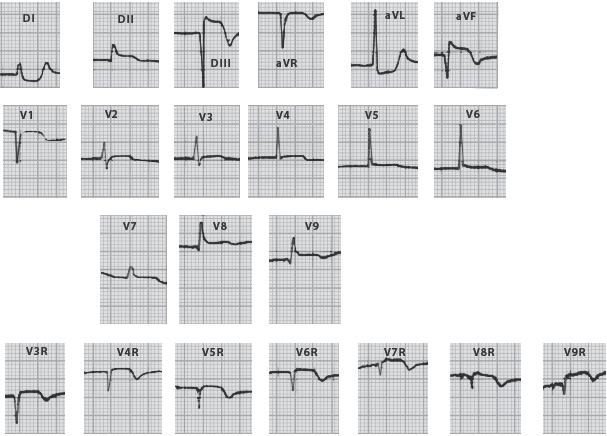
A. Enfarte agudo do miocárdio da parede inferior com um eixo da corrente de lesão de +120º (corrente de lesão em DIII > aVF > DII) o que faz suspeitar de extensão ao ventrículo direito. Nas derivações direitas, o supradesnivelamento de ST vai desde V3R até V9R, confirmando o diagnóstico de um enfarte extenso do ventrículo direito (grau IV).
Cardiopatia IsquémicaB. Os comentários são exatamente iguais aos da figura anterior (A). Trata-se de um enfarte agudo do miocárdio da parede inferior, com extensão ao ventrículo direito (grau IV).
técnicas
Figura 18.28 – Enfarte agudo do miocárdio da parede inferior com extensão ao ventrículo direito.
anatomia das artérias Coronárias
Ver Figuras 18.34 a 18.37
Não podemos terminar este capítulo de isquemia e lesão miocárdica sem abordar a ana tomia das artérias coronárias, a sua relação com as diversas estruturas cardíacas, a sua loca lização topográfica, assim como a correlação entre a obstrução da artéria e do local da artéria com as alterações agudas do segmento ST.
Na cardiopatia isquémica, não há qualquer correlação entre a depressão aguda do seg mento ST e a localização da artéria coronária envolvida, pelo contrário, quando há supra desnivelamento de ST (onda de lesão) verificamos que existe uma grande correlação entre, as respetivas derivações eletrocardiográficas onde está presente e a obstrução ou o sítio de obstrução da artéria coronária doente.
Artéria do cone da pulmonar
Artéria coronária direita
Artéria ventricular direita
Artéria marginal direita
Artéria do nódulo sinusal
Artéria do NAV Artéria septal inferior
Artéria descendente posterior
B
Artéria do nódulo sinusal
Artéria do cone da pulmonar
Artéria coronária direita
Artéria marginal direita
Artéria ventricular direita Artéria do NAV
Artérias septais inferiores
Figura 18.36 – Angiografia da artéria coronária direita. Visualização das diversas colaterais. A. Oblíqua anterior esquerda 45º caudal 15º; B. Oblíqua anterior direita 45º.
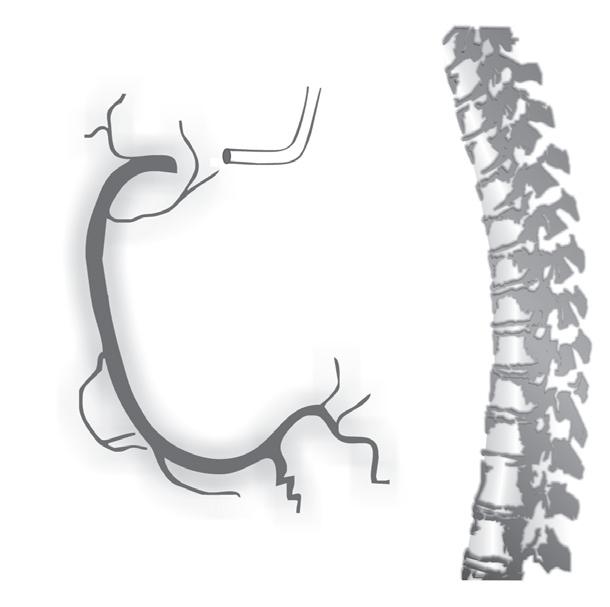
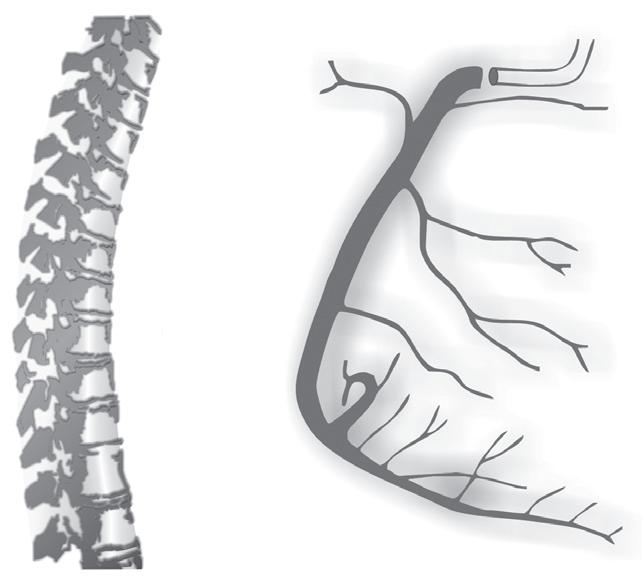
Figura 18.37 – Coronariografia da artéria coronária direita (dominante).
A artéria circunflexa (Cx) segue pelo sulco auriculoventricular esquerdo até ao sulco interventricular posterior. Esta artéria é dominante, isto é, ultrapassa este sulco e dá origem à descendente posterior em 15% dos casos.
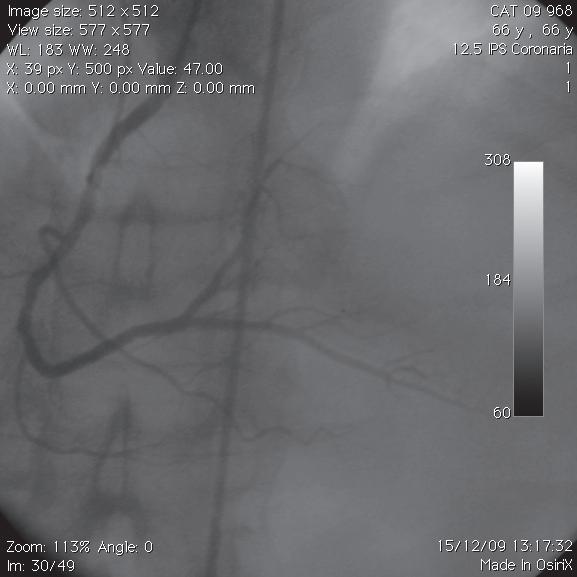
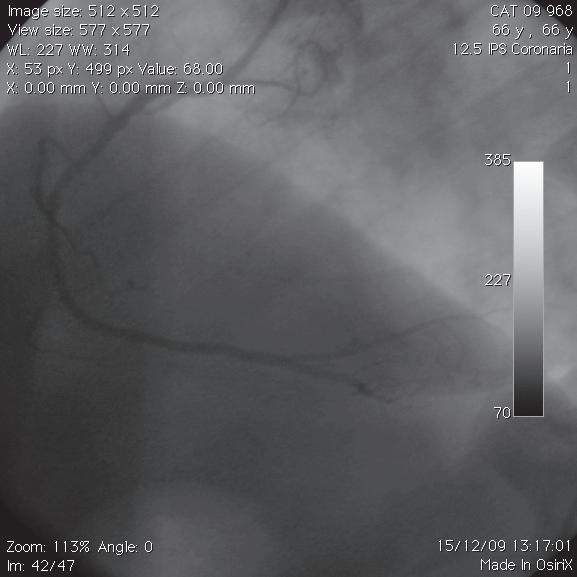
Da artéria circunflexa originam ‑se três grandes artérias que denominamos obtusas margi nais, sendo estas os principais ramos da artéria circunflexa, que vascularizam a parede livre do ventrículo esquerdo. Para além da origem destas artérias obtusas marginais, a artéria circunflexa tem calibre pequeno. Da artéria circunflexa emergem um ou dois ramos para a aurícula esquerda. Estes ramos vão suprir a parte lateral e posterior da aurícula esquerda.
O ostium da artéria coronária direita (CD) tem origem na parte superior e ligeiramente anterior do seio coronário direito, junto à união sino tubular da aorta, ficando, no entanto,
Bloqueio do ramo esquerdo e necrose da parede livre do ventrículo esquerdo
Como podemos ver na Figura 20.4 , o potencial intracavitário do ventrículo esquerdo no bloqueio completo do ramo esquerdo é do tipo RS, porque o vetor 1 e 2D ficam anulados pelo vetor 2E e pelo salto de onda, resultando um vetor 2 que se dirige para dentro da cavidade esquerda, assim como o vetor 3. O vetor 4 é o único que se afasta desta cavidade, dando origem à onda S intracavitária.
Quando se dá uma necrose da parede livre do ventrículo esquerdo, esta região deixa de ter atividade elétrica, abrindo ‑se, assim, nas derivações V5 e V6, como que uma janela para dentro da cavidade ventricular esquerda, fazendo com que estas derivações registem os potenciais intracavitários do ventrículo esquerdo. Deste modo, quando há uma necrose da parede livre do ventrículo esquerdo em presença de bloqueio completo do ramo esquerdo, o que se verifica não é o apa recimento de ondas Q, mas sim o aparecimento de com plexos RS em V5 e V6.
No entanto, a presença de onda S em V5 e V6 no bloqueio completo do ramo esquerdo pode acontecer noutras situações, como no bloqueio bifascicular esquerdo com predomínio de bloqueio do fascículo anterior e nas grandes dilatações do ventrículo direito.
Segundo a Escola Mexicana, podemos falar em necrose da parede livre do ventrículo esquerdo em presença de bloqueio completo do ramo esquerdo quando a onda S, em V5 e V6 ou só em V6, é empastada ou com entalhes, tem uma duração igual ou superior a 0,05 segundos e, muito especialmente, se for acompanhada de onda T negativa e simétrica.
Os critérios eletrocardiográficos de necrose em presença de bloqueio completo do ramo esquerdo são:
■ Se observamos qRs, qrs, Qrs ou QrS, em V5 e V6, a onda Q ou q é sinal de necrose septal esquerda e a onda S ou s é sinal de necrose da parede lateral ( Figura 20.5). No entanto, a presença de onda S isolada em V5 e V6 não é um sinal seguro de necrose da parede lateral do ventrículo esquerdo;
■ Ondas QS de V1 a V6, em presença de bloqueio completo do ramo esquerdo, são sempre sinal de necrose de todo o septo interventricular associada a necrose da parede lateral do ventrículo esquerdo ( Figura 20.6 );
■ Ondas Q em V5 e V6, em presença de bloqueio completo do ramo esquerdo, são sempre sinal de necrose septal esquerda, mesmo que sejam pequenas e de curta duração. Se forem acompanhadas de QS em V1 e V2, podemos afirmar que esta necrose também se estendeu à massa septal direita e, por isso, é uma necrose de todo o septo interven tricular ( Figuras 20.7 e 20.8).
edições técnicas
Síndromes Congénitas
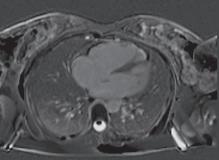
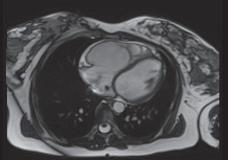
A. Ventrículo direito (VD) com volumes moderadamente aumentados e função sistólica diminuída (fração de ejeção em 3D = 33%), com hipocinesia da parede livre e da câmara de saída do ventrículo direito (CSVD), com pequenas zonas de discinesia (bulging) a nível da parede livre; B. RT a nível da parede livre do VD e CSVD, que pode corresponder a áreas de fibrose.
Ondas épsilon Padrão de Brugada
Ondas de Osborne
Figura 22.23 – Diagnóstico diferencial entre ondas épsilon, padrão de Brugada e ondas de Osborne. Figura amavelmente cedida pelo Dr. Nogueira da Silva (Serviço de Cardiologia do Hospital de Santa Marta, Centro Hospitalar de Lisboa Central).

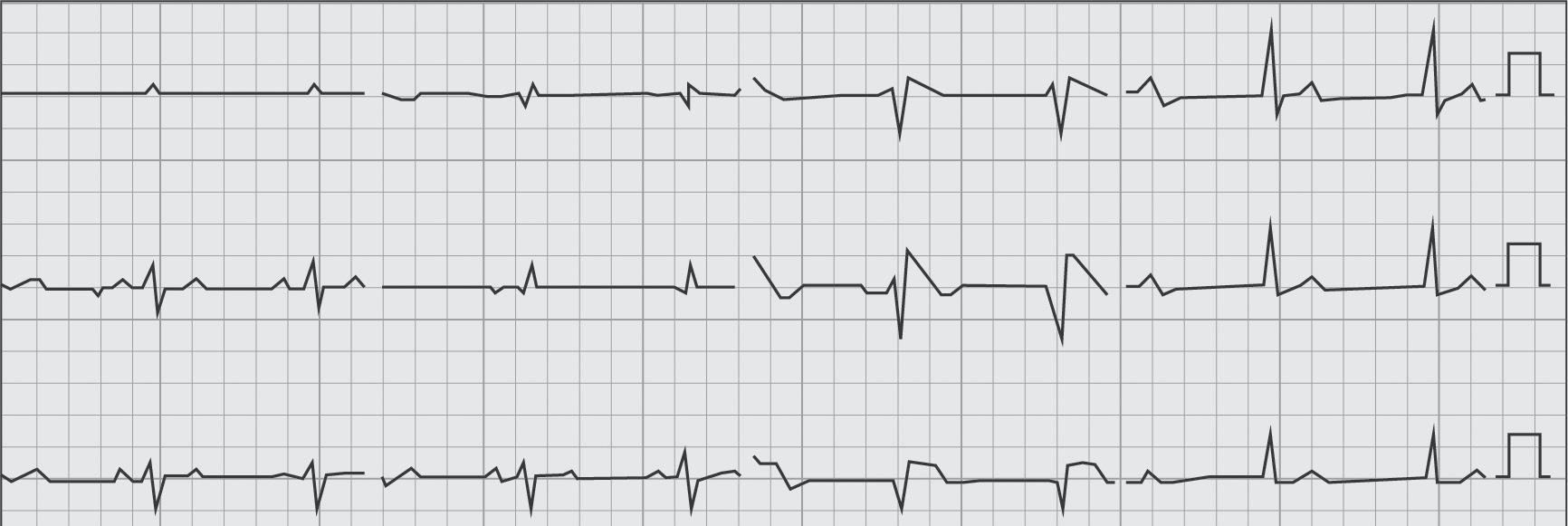
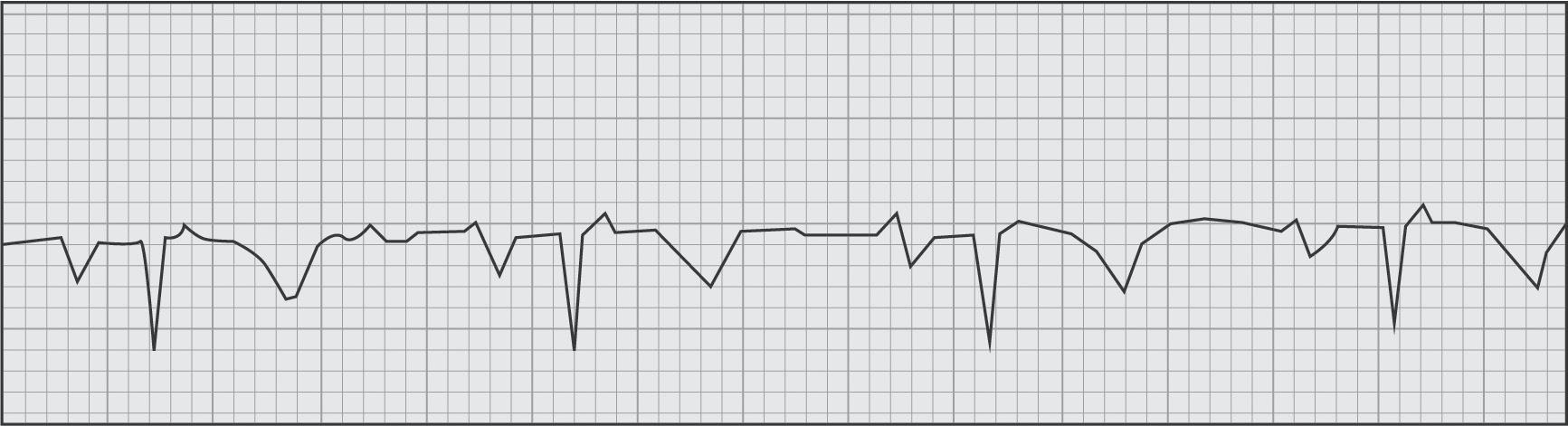
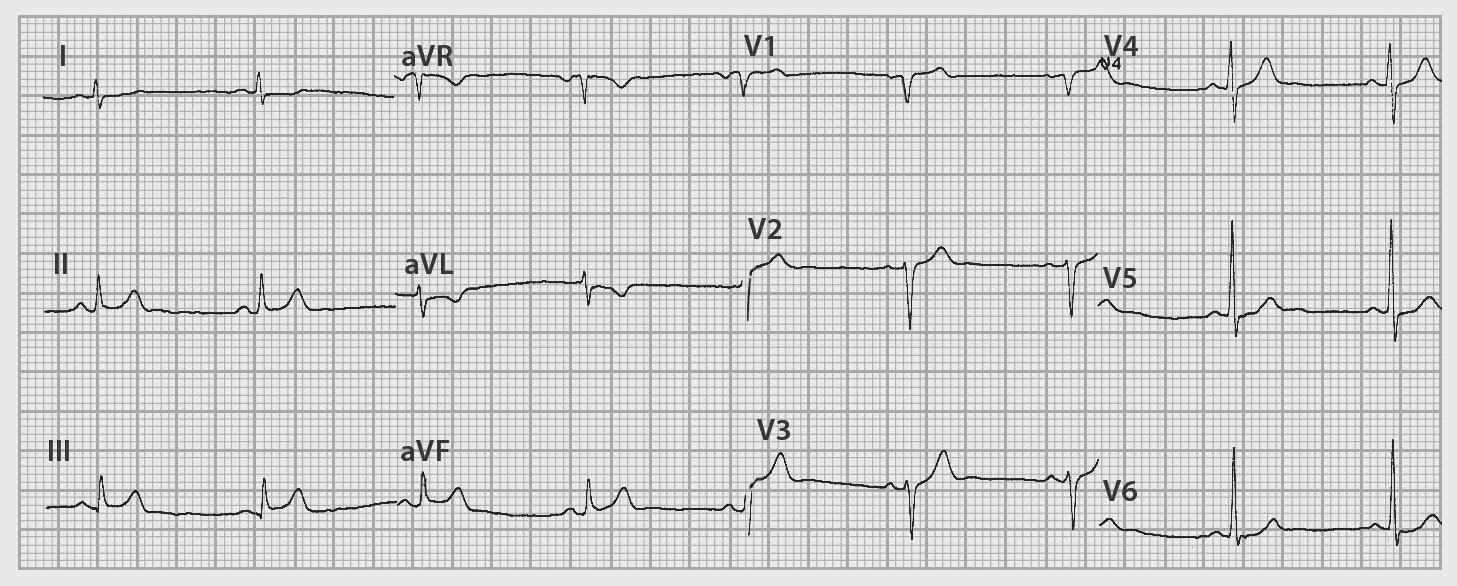
Nesta figura, observa-se a evolução da prova de esforço de um doente com uma coronariopatia grave. Prova de esforço (protocolo de Bruce).
A. O ECG feito em repouso e imediatamente antes da prova de esforço mostra um ritmo sinusal com frequência de 90/min e sem alterações dignas de nota.
B a I. Verifica-se que ao 3.º minuto de esforço nada há a salientar. A partir do 6.º min de prova, observa-se um supradesnivelamento do ponto J e do segmento ST de 3 mm em DII, DIII e aVF (mostrando uma lesão obstrutiva grave da artéria descendente posterior) e de V1 a V4 (por lesão obstrutiva grave da coronária descendente anterior) que se mantêm na recuperação, no pós-esforço imediato e no 1.º min da recuperação, e aos quais se agrega a imagem em espelho de ST-T em aVL. No 3.º min de recuperação e a partir do 2.º complexo há uma paragem sinusal de 3,2 seg (não há registo de complexos em aVR, aVL e aVF), ao que se segue um ritmo de escape hissiano com frequência de 37/min, retomando o ritmo sinusal normal apenas ao 5.º min de recuperação. Por este comportamento pode dizer-se que muito provavelmente há uma obstrução grave da coronária direita proximal (que dará posteriormente a artéria descendente posterior, como já foi dito) e antes da emergência da artéria sinusal, além de uma obstrução grave da artéria descendente anterior. A coronariografia mostrou uma lesão ostial de 90% da coronaria direita e uma lesão proximal de 90% da descendente anterior.
figura 24.4 – Positividade de prova de esforço por supradesnivelamento do ponto J e do segmento ST.
prova dE Esforço positiva E localização da obstrução coronária Numa prova de esforço positiva, o infradesnivelamento de ST, numa ou mais derivações, não nos permite afirmar em que coronária se encontra a lesão. No entanto, se essa positividade for dada por supradesnivelamento de ST, podemos afirmar com segurança que a lesão obstrutiva corresponde à coronária que vasculariza essa parede, como já foi referido no Capítulo 18. Por exemplo, o supradesnivelamento de ST em DII, DIII e aVF corresponde a uma lesão grave da descendente posterior, se, concomitantemente, se observarem arritmias supraventriculares, arritmias ou paragens sinusais, fibrilhações auriculares, etc. Pode, então, concluir se que a obstrução se situa na coronária direita proximal, antes da saída da artéria do nódulo sinusal (Figura 24.4). Se um supradesnivelamento de ST se observa de V1 a V3 ou V4, tal corresponde a uma lesão grave da artéria coronária descendente anterior (Figura 24.4). incompEtência (ou insuficiência) cronotrópica sinusal
Denomina‑se incompetência cronotrópica sinusal à incapacidade do nódulo sinusal de elevar eficazmente a frequência cardíaca com o esforço de modo a aumentar o débito cardíaco com o fim de o adequar às necessidades metabólicas do esforço. Durante a prova de esforço, estes doentes nunca chegam a atingir as frequências cardíacas máximas. Quando
técnicas
■ Frequentemente, ocorrem variações e oscilações do ciclo da taquicardia. Em alguns casos, poderá ser observada variação ventriculofásica, na qual duas ondas P com QRS a meio têm um ciclo mais curto do que duas ondas P sem QRS a meio. Em casos raros, detetam-se com aumentos e diminuições súbitas da frequência da taquicardia, múltiplas da frequência original, devidos a bloqueio de saída funcional;
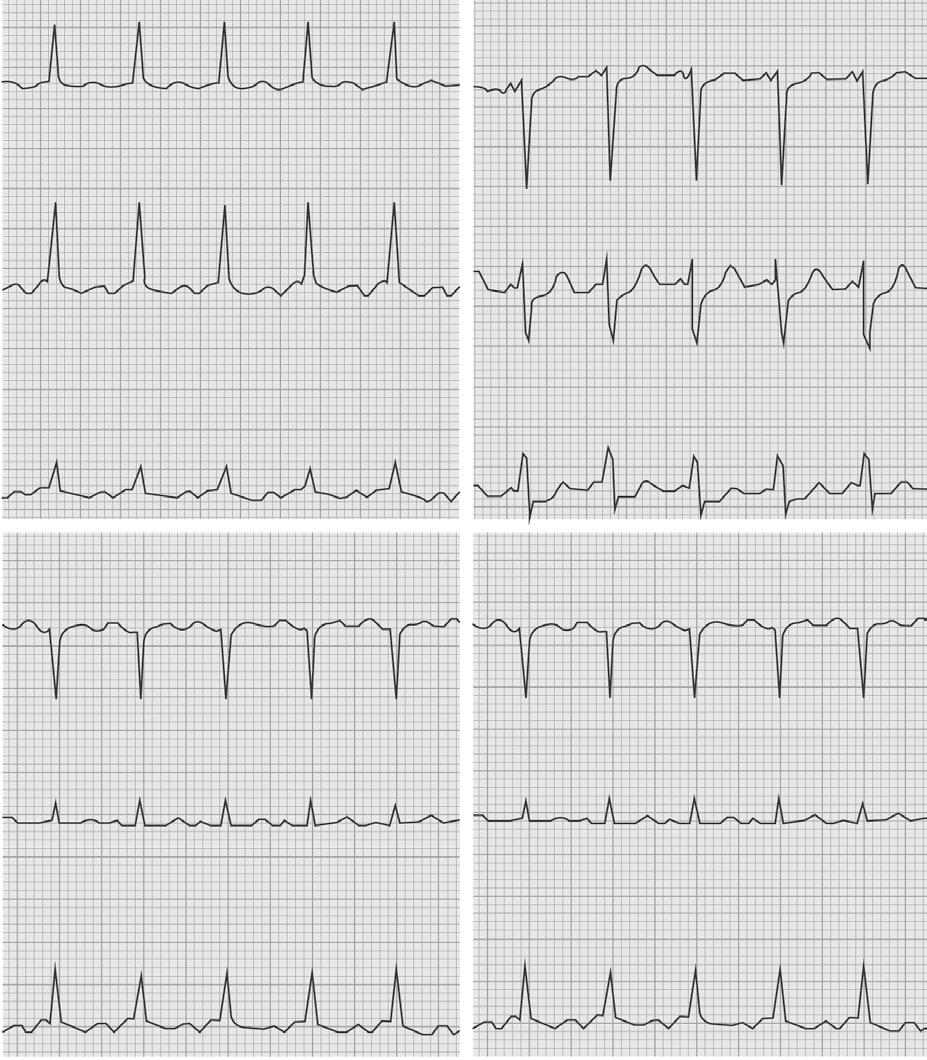
■ A frequência da atividade auricular durante a taquicardia é muito variável de doente para doente. Quando a atividade auricular é relativamente lenta, por exemplo, inferior a 150/ /minuto, poderá haver condução AV a 1:1 (Figura 26.19). Nos casos em que exista atividade auricular mais rápida (frequentemente 200-280/minuto) e nos doentes em quem exista diminuição da condução nodal AV (por exemplo, induzida por fármacos), poderá ocorrer condução ≥2:1 (bloqueio funcional fisiológico gerado por fenómeno de Wenckebach).
Para o tratamento das taquicardias auriculares focais podem ser úteis várias classes farmacológicas, incluindo os bloqueadores beta-adrenérgicos e os antiarrítmicos das classes I e III, tendo em vista, em particular, a supressão do excesso de automatismo subjacente. No entanto, a resposta à terapêutica farmacológica é pouco previsível, obriga a terapêutica de duração indefinida em doentes frequentemente jovens e apresenta taxa de sucesso a longo prazo muito limitada. Por conseguinte, seja por insucesso da terapêutica farmacológica, seja por preferência dos doentes, o tratamento passa frequentemente por mapeamento eletrofisiológico com ablação por cateter ( Figuras 26.19 e 26.20).
II III
aVR
aVL
aVF
V1 I V2 V3 V4 V5 V6
No traçado eletrocardiográfico é evidente a presença de uma taquicardia regular com complexos QRS estreitos, durante a qual são evidentes ondas P, com frequência de 145/minuto, com condução AV a 1:1 e intervalo RP longo (RP>>PR). O mapeamento eletrofisiológico confirmou dever-se a taquicardia auricular focal com origem no apêndice auricular esquerdo.
Figura 26.19 – Taquicardia auricular ectópica focal.
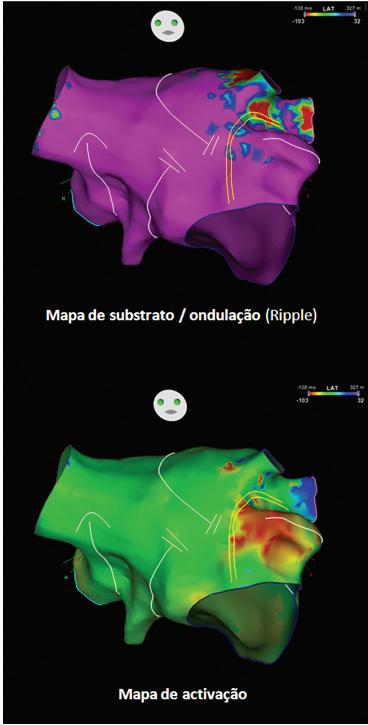
aurícula esquerda (Figuras 26.27 e 26.29). Os flutters atípicos são hoje muito frequentes, sendo pelo menos tão frequentes quanto os flutters típicos, e é previsível o aumento progressivo da sua incidência como resultado do envelhecimento progressivo da população e o aumento da frequência das condições predisponentes à fibrose auricular. De facto, o principal substrato para esta arritmia é a presença de áreas de fibrose nas aurículas, as quais suscitam a produção de zonas de atraso na propagação dos impulsos elétricos e linhas de bloqueio, favorecendo a formação dos circuitos de reentrada ( Figura 26.29 ).
Mapeamento eletroanatómico da aurícula esquerda durante flutter atípico numa doente com história prévia de valvuloplastia mitral cirúrgica (sistema Carto). São apresentados os mapas de ativação ( A a C) e de substrato (D a F). Os mapas de substrato revelaram múltiplas zonas de fibrose auricular (regiões coloridas com outras cores que não púrpura), particularmente na parede anterior (estendendo-se do anel mitral à veia pulmonar superior direita, D) e na parede posterior (nos antros venosos, E). Os mapas de ativação revelaram que o flutter atípico se devia a um mecanismo de macrorreentrada dual-loop, com um circuito a rodar em torno das veias direitas e outro circuito em torno do apêndice auricular esquerdo (A a C, encontrando-se os circuitos assinalados pelas setas), localizando-se o istmo partilhado pelos dois circuitos no teto da aurícula (A, região colorida a vermelho). A ablação no istmo partilhado terminou eficazmente o flutter
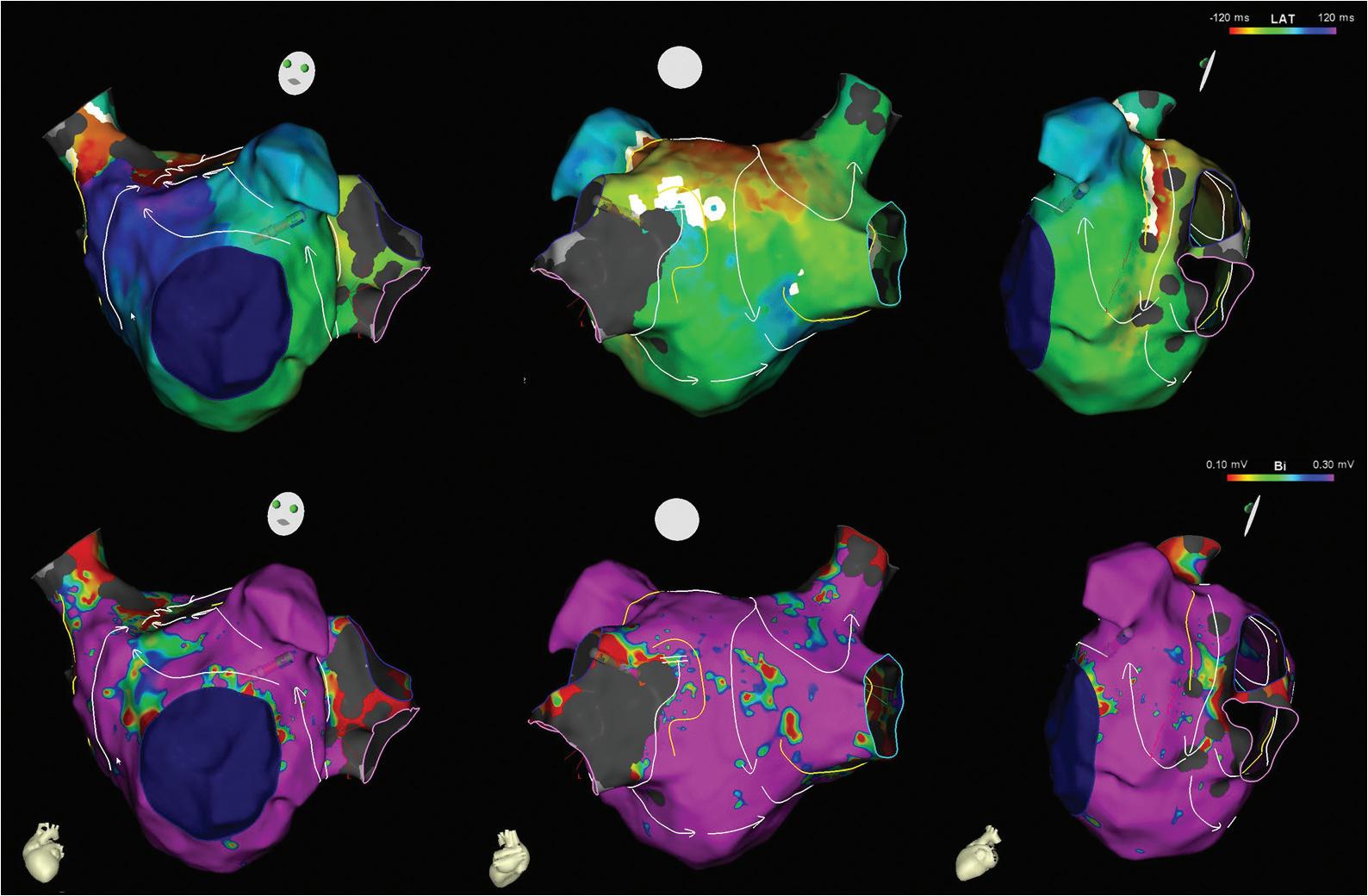
Figura 26.29 – Flutter auricular atípico com origem na aurícula esquerda.
A fibrilhação auricular (FA) é a arritmia mantida mais frequente, aumentando a sua prevalência com a idade, atingindo mais de 10% nos doentes com idade superior a 80 anos. A FA caracteriza-se pela ausência de atividade elétrica organizada e coordenada na aurícula, a qual se encontra substituída por atividade elétrica caótica auricular, sendo as aurículas percorridas por numerosas ondas elétricas aleatórias e desordenadas em simultâneo.
Do ponto de vista etiopatogénico, a FA compreende um conjunto muito heterogéneo de condições que poderão ser sistematizadas ao longo de um espectro, encontrando-se num
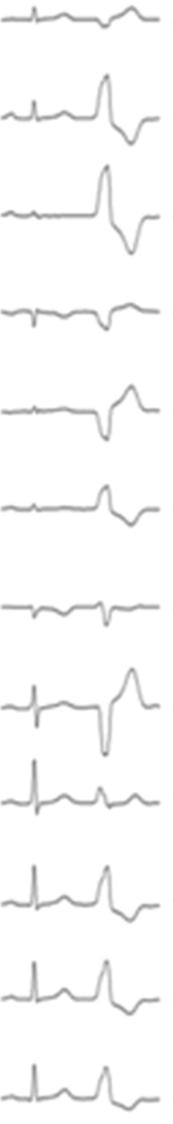

fIgura 27.37 – Eixo no plano frontal no diagnóstico diferencial de arritmias ventriculares com origem nas câmaras de saída ventriculares. Adaptado de Hutchinson, 2013.
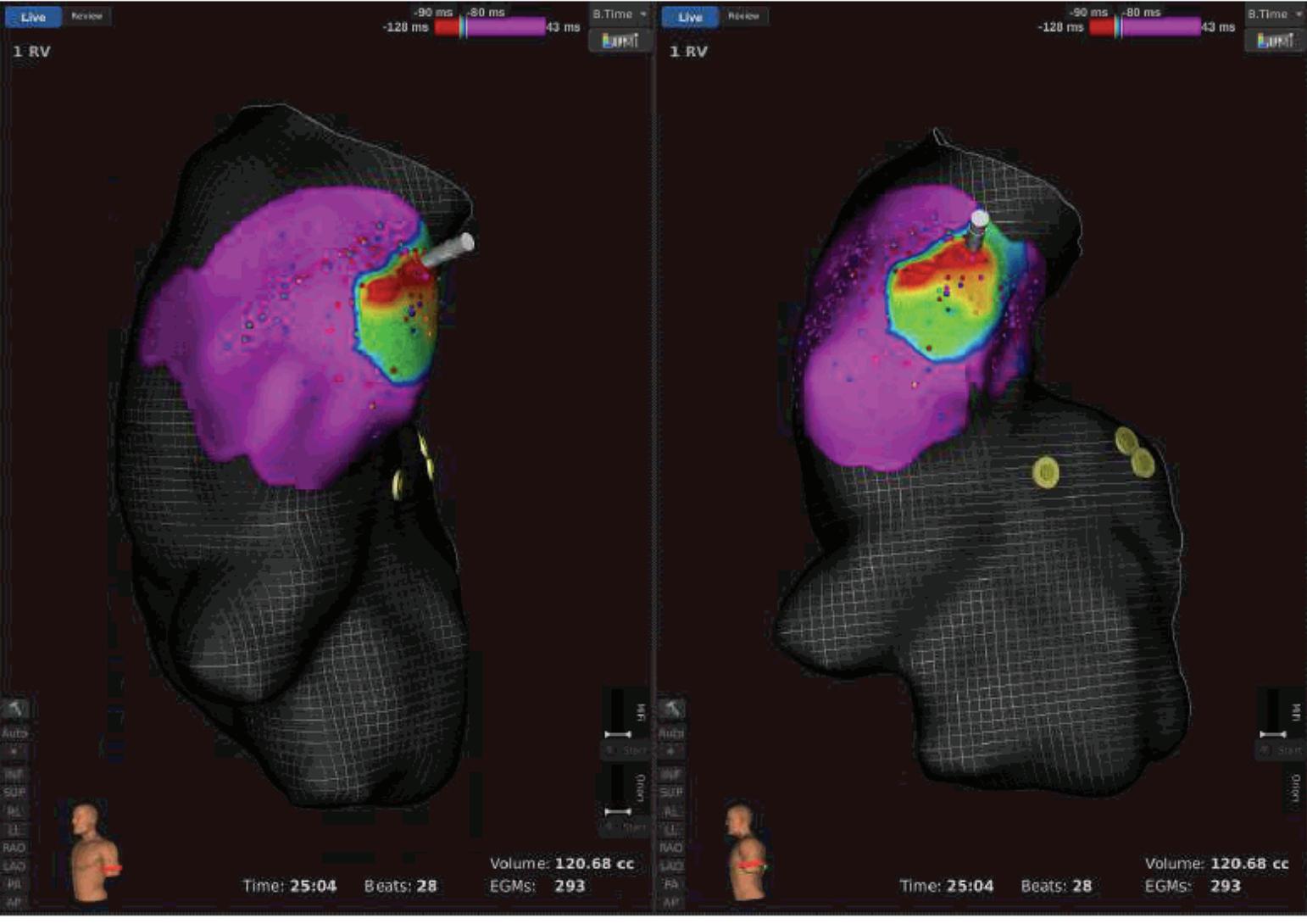
fIgura 27.38 – Exemplo de mapeamento eletrofisiológico em contexto de TV monomórfica da CSVD. A. Morfologia do QRS em ritmo sinusal e durante TV. Em TV, o QRS apresenta QRS com eixo inferior, morfologia em V1 do tipo rS e transição em V3. A transição em ritmo sinusal é mais precoce (V2) do que durante TV, sugerindo a sua origem na parede septal da CSVD. Adicionalmente, no plano frontal, a TV apresenta um eixo direito (D1 é negativo, R em D3 >D2 e S em avL >aVR), sugerindo origem na porção mais esquerda da CSVD; B. Mapa de ativação de TV em estudo eletrofisiológico demonstrando origem na porção esquerda da parede septal da CSVD.
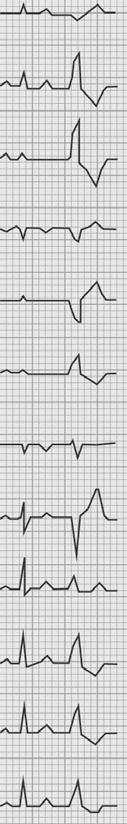
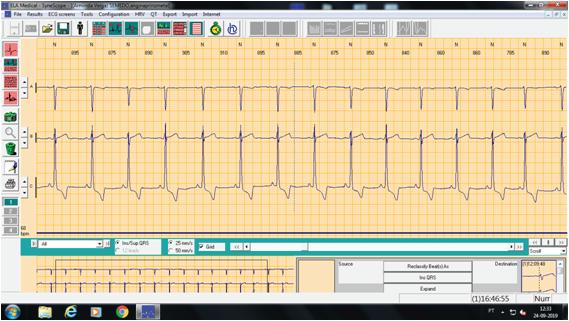
FIgura 29.14 – Flutter auricular com condução A:V fixa 2:1 – ver texto.
A Importância da Eletrocardiografia Dinâmica (Holter/24 horas) no Diagnóstico das Arritmias Supraventriculares
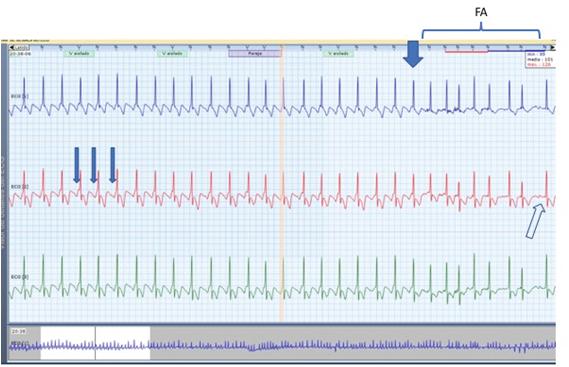
FIgura 29.15 – Flutter auricular com pseudo-pré-excitação.
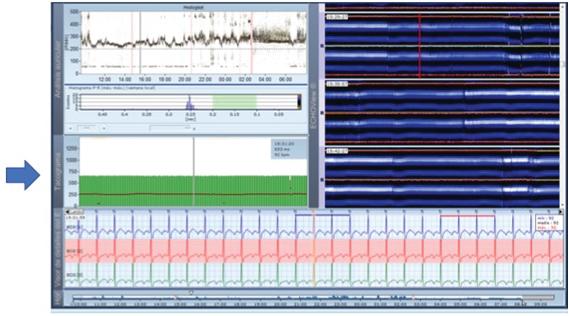
Compare‑se a Figura 29.16 com a anterior. Observam‑se ondas P sinusais, seguidas por um intervalo PR curto (a onda P termina onde começa o complexo ventricular). Ainda que no canal 1 não se veja a onda delta (onda delta isoelétrica), esta é claramente visível nos canais 2 e 3, com o que se estabelece o diagnóstico de pré‑excitação. Se, além disso, o doente tiver taquicardias paroxísticas supraventriculares, é estabelecido o diagnóstico de síndrome de WPW.
Valor Diagnóstico e Prognóstico das Alterações da Repolarização Ventricular no Eletrocardiograma Dinâmico de 24 Horas (Holter)
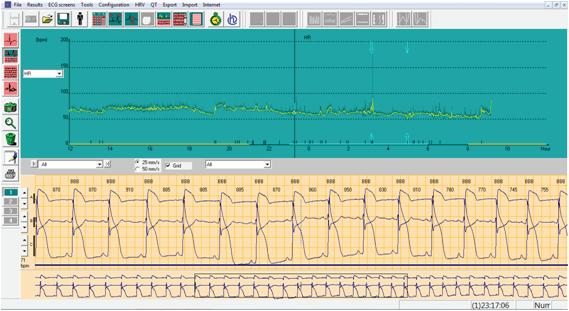
V5 like
FIgura 33.1 – A. Derivações V1 like, V3 like e V5 like traçado de Holter sem dor; B. As mesmas deriva ções de A e no mesmo Holter, agora com supradesnivelamento marcado do segmento ST (máximo 7 mm em V5 like), com início às 23h17, coincidindo com episódio de dor.
O prognóstico da angina de Prinzmetal a longo prazo é bom. Pacientes sem doença coronária ou doença coronária de um vaso têm bom prognóstico, com taxas de sobrevivência de 99% ao fim de um ano e de 94% ao fim de cinco anos. Por outro lado, as taxas de sobrevivência ao fim de um e cinco anos caem para 87% e 77%, respetivamente, em doentes com doença coronária aterosclerótica multivaso. Além da presença de doença coronária multivaso, são fatores que afe tam o prognóstico os espasmos multivasos, o tabagismo ativo e a intolerância aos antagonistas do cálcio. O score de risco da Japonese Coronary Spasm Association permite definir o risco de MACE (Major Adverse Cardiovascular Events) em doentes com angina vasoespástica de acordo com os seguintes critérios:
■ A: Paragem cardiorrespiratória fora do hospital (4 pontos);
■ B: 1. Tabagismo ativo; 2. Angina em repouso; 3. Doença coronária aterosclerótica; 4. Espas mo multivaso (2 pontos cada);
Este livro aborda toda a eletrocardiografia clássica. Nesta 3.ª edição revista e atualizada, destacamos a inclusão da técnica de Holter de 24 horas. Além das funções eletrofisiológicas das células do coração, faz a descrição das manifestações eletrocardiográficas das patologias cardíacas, incluindo alterações iónicas, síndromes congénitas, eletrocardiografia do pacing, eletrocardiografia de esforço, eletrocardiografia das arritmias cardíacas, a sua eletrofisiologia e avaliação das variações circadianas da frequência cardíaca.
Com uma linguagem simples e acessível, mas ao mesmo tempo rigorosa e científica, aborda os temas com uma dificuldade crescente, facilitando a apreensão dos conteúdos. As descrições teóricas são complementadas com um amplo leque de figuras, esquemas e eletrocardiogramas e, no caso das arritmias, com estudos eletrofisiológicos e respetivos registos para que o diagnóstico eletrocardiográfico seja feito por compreensão lógica e sequencial, e não por memorização de parâmetros.
Estamos perante uma obra de referência, dedicada ao estudo da eletrocardiografia clínica, excelente auxiliar de consulta e aprendizagem para médicos, enfermeiros, técnicos de cardiopneumologia, cardiologistas e cirurgiões cardiotorácicos, internos destas especialidades e para todos os profissionais de saúde que necessitem destes conhecimentos para o desempenho da sua atividade profissional diária.
3.ª EDIÇÃO Nesta
ISBN 978-989-752-437-0
