LA VOCE AICCER

RIVISTA SCIENTIFICA DI INFORMAZIONE
CHIRURGIA DELLA CATARATTA
Chirurgia della cataratta: quando e come interviene l’anestesista?
CHIRURGIA DELLA CATARATTA
Dinamica e fattori di rischio per la capsula posteriore durante femtocataratta
SUPERFICIE OCULARE
Antisepsi e rigenerazione della superficie oculare
CHIRURGIA DELLA CATARATTA
Edema maculare cistoide: come combatterlo La sinergia tra FANS e corticosteroidi è la formula vincente
DALLE AZIENDE
Dry Eye e chirurgia oftalmica, esperti a confronto per fare il punto su come la condizione di Dry Eye incide nel pre e post-chirurgico

2023 2 FGE S.r.l. - Reg. Rivelle 7/F - 14050 Moasca (AT) - Trimestrale nr. 2/23 - Anno XXV
ASSOCIAZIONE ITALIANA DI CHIRURGIA DELLA CATARATTA E REFRATTIVA







RIVISTA SCIENTIFICA DI INFORMAZIONE ASSOCIAZIONE ITALIANA DI CHIRURGIA DELLA CATARATTA E REFRATTIVA
22023
Responsabile Editoriale
Scipione Rossi
Vice-Direttore Editoriale
Dario Aureggi
Direttore Responsabile
Ferdinando Fabiano
Comitato Pubblicazioni AICCER
Giovanni Alessio, Roberto Bellucci, Vincenzo Orfeo, Riccardo Sciacca
Redazione Segreteria AICCER
AIM Group International - Milan Office
Via G. Ripamonti 129 - 20141 Milano
tel. 02 56601.1 - fax 02 70048578
e-mail: segreteriaaiccer@aimgroup.eu

Scipione Rossi
e-mail: scipione.rossi@gmail.com
Grafica e Stampa

FGE S.r.l.
Pubblicità
FGE S.r.l.
Reg. Rivelle 7/F - Moasca (AT)
tel. 0141 1706694
e-mail: info@fgeditore.it
ISSN 1973-9419
Registrazione presso il Tribunale di Asti n° 5/98 del 15/12/1998
Il contenuto degli articoli pubblicati è di esclusiva responsabilità degli autori.
La riproduzione di articoli o parte di essi deve essere autorizzata dall’Editore.
Inserzionisti:
Alcon II Cove, 6, 9
FB Vision 4
Fidia 27, 30

Strada 4 Milano Fiori, Palazzo Q7 – 20089 Rozzano (MI)
operativa: FGE srl − Regione Rivelle 7/F − 14050 Moasca (AT) – Tel. 0141 1706694 – Fax 0141 856013 e-mail: info@fgeditore.it − www.fgeditore.it LA VOCE AICCER RIVISTA SCIENTIFICA DI INFORMAZIONE 2023 2 FGE S.r.l. Reg. Rivelle 7/F 14050 Moasca (AT) Trimestrale nr. 2/23 Anno XXV ASSOCIAZIONE ITALIANA DI CHIRURGIA DELLA CATARATTA E REFRATTIVA CHIRURGIA DELLA CATARATTA Chirurgia della cataratta: quando e come interviene l’anestesista? CHIRURGIA DELLA CATARATTA Dinamica e fattori di rischio per la capsula posteriore durante femtocataratta SUPERFICIE OCULARE Antisepsi e rigenerazione della superficie oculare CHIRURGIA DELLA CATARATTA Edema maculare cistoide: come combatterlo La sinergia tra FANS e corticosteroidi è la formula vincente DALLE AZIENDE Dry Eye e chirurgia oftalmica, esperti a confronto per fare il punto su come la condizione di Dry Eye incide nel pre e post-chirurgico Disponibile anche su APP Scaricala gratuitamente
Redazione:
Sede
Case

Efficacia
OLIO OZONIZZATO IN LIPOSOMI: LA LETTERATURA SCIENTIFICA LA LINEA OZONO
NELLA PROFILASSI PREOPERATORIA E NELLE INFIAMMAZIONI DELLA SO ANCHE DI ORIGINE INFETTIVA
Efficacia antivirale in vitro su Sars-CoV-2 e riparativa sulla supe icie oculare



Translational Vision Science & Technology (2021)



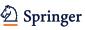


Microorganisms (2021)
















NELLA PROTEZIONE DELLE LESIONI DELLA SO
NELLE PATOLOGIE PALPEBRALI E NEL PRE E POST CHIRURGIA
NELLE PATOLOGIE PALPEBRALI (BLEFARITI, ORZAIOLO, CALAZIO)

Efficacia
Liposomal Ozonated Oil in Ocular Infections: A Review of Preclinical and Clinical Studies, Focusing on Its Antiseptic and Regenerative Properties 14
su congiuntiviti virali
STUDI PUBBLICATI
Reports in Ophthalmology (2018) Effe
supe
Use of Ozone-Based Eye Drops: A Series of Cases in Veterinary and Human Spontaneous Ocular Pathologies International Medical Case Report Journal (2021) Efficacia in casi corneali
EXPERIMENTAL EYE RESEARCH
o antise ico e riparativo su patologie spontanee della
icie oculare
complicati
Ozone-Based Eye Drops Activity on Ocular Epithelial Cells and Potential Pathogens Infecting the Front of the Eye Microbial Biotechnology (2021) Eliminazione
Antibiofilm and repair activity of ozonated oil in liposome Journal of Cataract & Refractive Surgey (2021)
antiba erica e antifungina in vitro e antiossidante sulla supe icie oculare
del biofilm ba erico e a ività riparativa
In vitro antimicrobial activity of ozonated oil in liposome eyedrop against multidrug-resistant bacteria OPEN MEDICINE
Medicine
Efficacia su ba eri multiresistenti
Open
(2022)
Inhibitory Effect of Ophthalmic Solutions against SARS-CoV-2: A Preventive Action to Block the Viral Transmission?
Effe o inibitorio su Sars-CoV-2
COVID-19
Ocular Prophylaxis: The Potential Role of Ozonated-Oils in Liposome Eyedrop Gel
Materiale riservato esclusivamente a Medici e Farmacisti. FBV-PGO25/2023
Per molto tempo, l’importanza della funzione del sistema della superficie oculare nella genesi delle problematiche corneali e dei processi riparativi post chirurgici è stata trascurata.
Negli ultimi anni la comprensione dei fenomeni che regolano le risposte della superficie oculare ai diversi stimoli e delle influenze che esse hanno sulle strutture e la trasparenza corneali, sulla funzione visiva e sulla qualità della vita è fortunatamente molto cresciuta.
Oggi per la qualità delle soluzioni chirurgiche e dei risultati da esse ottenibili, la conservazione dell’integrità dell’omeostasi della superficie oculare ha assunto un posto decisamente rilevante nella costruzione di un atto chirurgico percepito in tutto il suo valore dai nostri pazienti.
La combinazione di passione, sensibilità, intelligenza ed esperienza di Vincenzo Orfeo, sono alla base di questo testo, che rappresenta una informazione tanto agile quanto pratica per la gestione pre, intra e post operatoria delle problematiche della superficie oculare legate alla chirurgia della cataratta, ma in genere valida per qualsiasi tipo di chirurgia che venga in contatto con il sistema della superficie oculare.

Facile da leggere, corredato da immagini esplicative, potrà essere un compagno utile per molti di noi e potrà aiutarci a migliorare la percezione finale del nostro lavoro e soprattutto la qualità della vita dei nostri pazienti. Buona lettura.
Maurizio Rolando
Redazione: Strada 4 Milano Fiori, Palazzo Q7 – 20089 Rozzano (MI)
Sede operativa: FGE srl − Regione Rivelle 7/F − 14050 Moasca (AT) – Tel. 0141 1706694 – Fax 0141 856013
e-mail: info@fgeditore.it − www.fgeditore.it

SOMMARIO NOTIZIE DAL CONSIGLIO DIRETTIVO di Paolo Vinciguerra 7 CHIRURGIA DELLA CATARATTA Chirurgia della cataratta: quando e
interviene l’anestesista? 10
CHIRURGIA DELLA CATARATTA Dinamica e fattori di rischio per la capsula posteriore durante femtocataratta 14
SUPERFICIE OCULARE Antisepsi e rigenerazione della superficie oculare 20
come
Guerin
G.M., Guerin P.L., Verdimonti E., Iuri L., Tognetto D.
Carlo Bellucci, Paolo Mora, Salvatore Antonio Tedesco, Roberto Bellucci, Stefano Gandolfi
José Luis Güell
CATARATTA
CHIRURGIA DELLA
corticosteroidi è
formula vincente 24
DALLE AZIENDE Dry Eye e chirurgia oftalmica, esperti a confronto per fare il punto su come la condizione di Dry Eye incide nel pre e post-chirurgico 28
Edema maculare cistoide: come combatterlo - La sinergia tra FANS e
la
Alessandro David



Il nuovo SMART Educator di Alcon è disponibile adesso. Scopri il nuovo modo di presentare le opzioni di IOL ai pazienti. ©2023 Alcon Inc. 04/23 IT-SG-2300018 Password: 'Smart'
INTERAZIONI
NOTIZIE DAL CONSIGLIO DIRETTIVO di Vincenzo Orfeo

Cari amici dell’AICCER; molte sono le attività che costituiscono la vita e la mission di una società. Recentemente Aiccer si è impegnata per stilare un documento col metodo della Delphi, sulla terapia pre e postoperatoria dell’intervento di cataratta per aiutare la gestione di alcuni importanti momenti prima e dopo l’intervento.
Siamo partiti da una Survey cui hanno risposto più di 100 oculisti tra i maggiori esperti italiani di chirurgia della cataratta, volta a conoscere le abitudini prescrittive nel pre e nel postoperatorio.
Da questa survey (pubblicata su EJO1) sono emerse varie considerazioni sulla varietà di approcci diversi: alcuni condivisibili secondo le direttive della letteratura internazionale, altri meno condivisibili.
Chiamando a collaborare altri esperti oculisti e microbiologi, abbiamo creato un team per una valutazione della letteratura internazionale maggiormente accreditata e per stilare un documento base per una Delphi, che è strutturata in una serie di affermazioni (statements). Questi testi sono stati poi sottoposti ad altri 15 esperti individuati nel Direttivo e nel Comitato tecnico scientifico di Aiccer. Ogni statement è stato votato anonimamente; per ottenere l’approvazione ogni testo doveva avere almeno l’80% dei voti positivi. Dalla votazione dei 18 statements proposti, ben 16 hanno ottenuto una approvazione a grandissima maggioranza (14 di questi con più del 90%).
In breve si è voluto, con questo documento, puntualizzare che:
1) È assolutamente da evitare la terapia preoperatoria di alcuni giorni con antibiotico in collirio. Non c’è alcuna evidenza della sua utilità e, se condotta a dosi non congrue, può facilitare l’insorgenza di resistenze batteriche
2) La terapia antibiotica deve essere effettuata sempre a dose piena e per non più di 5-7 giorni; ciò per ottenere la massima efficacia e ridurre al minimo il rischio di indurre resistenze. Da dimenticare quindi, l’abitudine di ridurre progressivamente la posologia delle associazioni antibiotico - cortisone (il famigerato “Tapering”).
3) Da recenti lavori si è evidenziato come una terapia di associazione antibiotico-cortisone a dosi piene (quindi almeno 4 volte al giorno) per 7 giorni, sia sufficiente nella stragrande maggioranza dei casi a prevenire le infezioni e ad eliminare l’infiammazione evidente. Sappiamo che in 7 giorni otteniamo la guarigione epiteliale della ferita corneale (non ovviamente una chiusura ermetica stromale) per cui, se non intervengono traumi, si può considerare concluso il rischio di penetrazione intraoculare di germi.
4) Nel preoperatorio quindi mai più antibiotico di routine ma attenzione alle condizioni in cui arriva il paziente. Un paziente in buon compenso non è necessario che sia trattato con una terapia. Coloro che hanno alterazioni della Superficie legata a Dry Eye, e sono la maggioranza soprattutto delle donne, è utile che siano individuati e correttamente trattati con sostituti lacrimali adeguati. Chi presenta invece una blefarite deve essere trattato per un rischio infettivo. Può essere presa anche in considerazione una disinfezione con degli antisettici purché siano rispettosi della superficie oculare e non siano aggressivi.
5) Nell’immediato preoperatorio, subito prima dell’inizio della chirurgia, è ovviamente indispensabile lo Iodopovidone al 5% in soluzione acquosa per 3 minuti sulla cute perioculare e sulla congiuntiva
6) Nel postoperatorio una associazione antibiotico + cortisone a dosi piene per 7 giorni; dopo i 7 giorni iniziali, può essere utile continuare con un collirio cortisonico (senza antibiotico) a bassa potenza o comunque con una preparazione da poter dosare in relazione alla eventuale residua infiammazione postoperatoria (controllando sempre il Tono Oculare). Dopo un intervento senza complicazioni è presumibile un permanere di una situazione infiammatoria subclinica per diverse settimane.
7) Nel postoperatorio, sono utili i sostituti lacrimali anche per dei mesi, sia per il recupero dell’integrità della superficie ma anche per mitigare i sintomi da Discomfort postchirurgico che spesso disturbano il paziente.
8) Infine, vi riporto uno statement che pur avendo avuto molti consensi non è arrivato all’80% richiesto. Si conferma l’abitudine consolidata di utilizzare nel postoperatorio i Fans per la prevenzione dell’edema maculare cistoide. Sono considerati ottimi farmaci da usare però con attenzione in pazienti con alterazione severa della superficie da Dry Eye.
Questi, in breve, i principali concetti espressi in questa Delphi, Speriamo che, una volta pubblicati, possano essere di aiuto a tutti noi oculisti.
7 LA VOCE AICCER 2/2023
1. Orfeo V, Aragona P, Rossi S, Mastropasqua L, Alessio G, Vinciguerra P, Ciprandi G, Tognetto D. Management of patients undergoing cataract surgery: An Italian survey. Eur J Ophthalmol. 2022 Dec 12:11206721221145055




Redazione: Strada 4 Milano Fiori, Palazzo Q7 – 20089 Rozzano (MI) Sede operativa: FGE srl − Regione Rivelle 7/F − 14050 Moasca (AT) Tel. 0141 1706694 – Fax 0141 856013 e-mail: info@fgeditore.it − www.fgeditore.it Ordina la tua copia su www.fgeditore.it
DIAGNOSTICA OCULARE
alla interpretazione delle immagini: Ecografia, OCT, OCTA, Fluorangiografia
ATLANTE DI
Guida
Pierro
Luisa
1
Volume
2
Volume
S H OCKI N G L Y BRILLI A NT

D IS T A NCE V I S I ON , T IME A F T ER T I M E 1 -5
Le IOL CLAREON ® MONOFOCALI forniscono ai pazienti una visione intermedia funzionale, mantenendo un'eccezionale nitidezza nella visione d a lo ntano. 6-9

Ma ciò che vedranno potrebbe sorprenderli.
1. Clareon® IOL Directions for Use. 2. Lane S, Collins S, Das KK, Maass S, Thatthamla I, Schatz H, Van Noy S, Jain R. Evaluation of intraocular lens mechanical stability. J Cataract Refract Surg. 2019 Apr;45(4):501-506. 3. Alcon Data on File, 2017. 4. Lehmann R, Maxwell A, Lubeck DM, Fong R, Walters TR, Fakadej A. Effectiveness and Safety of the Clareon Monofocal Intraocular Lens: Outcomes from a 12-Month Single-Arm Clinical Study in a Large Sample. Clin Ophthalmol. 2021;15:1647-1657. 5. Oshika T, Fujita Y, Inamura M, Miyata K. Mid-term and long-term clinical assessments of a new 1-piece hydrophobic acrylic IOL with hydroxyethyl methacrylate. J Cataract Refract Surg. 2020 May;46(5):682-687. 6. AcrySof® IQ Vivity® Extended Vision IOL Directions for Use. 7. Bala, Chandra, et al. Multi-country clinical outcomes of a new nondiffractive presbyopia-correcting intraocular lens. JournalofCataractandRefractiveSurgery Publish Ahead of Print DOI:10.1097/j.jcrs.0000000000000712. 8. Varma, Devesh, et al. Clinical Outcomes of a New Non-Diffractive Presbyopia-Correcting Intraocular Lens From Two Large Confirmatory Studies. AmericanAcademyofOphthalmology. Abstract: PA005. 9. Alcon Data on File, 2022. [A01970-REP-211731] -Optical Equivalency of Clareon Monofocal and AcrySof IQ IOL Version 1.2 REF-15172. Based on Studies with AcrySof®; Clareon® and AcrySof® are optically equivalent with the same -0.2µm aspheric design resulting in improved depth of focus. Per la lista completa di indicazioni, controindicazioni e avvertenze fare riferimento alle istruzioni per l'uso o ai manuali di istruzioni d'uso dei rispettivi prodotti.
Visitate il sito Alcon
informazioni
©2023 Alcon Inc. 04/23 IT-CLI-2300007
https://ifu.alcon.com/ per importanti
di prodotto.
Clareon. Monofocal
Chirurgia della cataratta: quando e come interviene l’anestesista?
Introduzione
Negli ultimi anni si è assistito ad un forte incremento delle richieste di interventi chirurgici per quel che concerne l’estrazione di cataratta e, complice il progressivo invecchiamento della popolazione, si stima che nel 2050 il numero di pazienti affetti da cataratta aumenterà del 50-60 %.1
Come noto, le attuali linee guida italiane in materia raccomandano la presenza dell’anestesista in sala operatoria. “La scelta tra anestesia locale (topica o infiltrativa) e generale dipende dalle condizioni fisiche e mentali del paziente e deve essere definita in base alle necessità e preferenze del chirurgo, dell’anestesista e del paziente stesso. La sedazione endovenosa è comunemente associata per ottimizzare la collaborazione del paziente durante l’atto chirurgico.”2
Va però anche considerato il delicato periodo storico in cui viviamo, che ha richiesto al personale medico, sia durante sia dopo l’emergenza COVID-19, un profuso e maggiore impegno su più fronti. Pertanto, se da un lato risulta necessario riuscire ad indirizzare le risorse dei medici anestesisti laddove vi è maggior richiesta, dall’altro risulta mandatorio intervenire per ridurre le sempre più lunghe liste d’attesa per l’intervento di facoemulsificazione. In un recente articolo pubblicato sul BMJ, infatti, si stima che gli ospedali, per riuscire a far fronte all’aumento delle richieste, dovranno addirittura raddoppiare il volume degli interventi erogati.3 In questo senso, la French National Authority for Health (HAS) ha aperto la strada ad una semplificazione delle procedure per l’intervento di cataratta rilasciando, nel luglio del 2010, un report in cui si afferma che in Francia non solo la visita pre-anestesiologica è obbligatoria esclusivamente in caso di anestesia generale o locoregionale, ma anche che l’uso dell’anestesia topica non richiede la presenza di un medico rianimatore in

sala operatoria sebbene, per il comfort e la sicurezza del paziente è raccomandato che tale figura sia sempre disponibile in caso di necessità.4
Secondo un’analisi della Mayo Clinic, su 4000 pazienti operati di cataratta in regime di anestesia locale con associata sedazione endovenosa, è stato necessario l’intervento del medico solo nell’1,5% dei casi e quasi esclusivamente per l’insorgenza di crisi ipertensive che in più della metà degli eventi si sono risolte dopo semplice monitoraggio.5
Di fronte a questi dati, numerosi centri si sono posti il problema su come ridistribuire in modo ottimale le risorse a disposizione, mantenendo degli standard di cura elevati e garantendo la massima sicurezza e tutela del paziente. La questione in analisi è stata l’effettiva necessità della presenza dell’anestesista per tutta la durata dell’intervento di facoemulsificazione ed il profilo di sicurezza in caso di un eventuale monitoraggio da parte di figure qualificate ed adeguatamente formate, come l’infermiere di sala o, nei paesi in cui è presente, il terapista respiratorio.
Questi dati trovano conferma anche in numerosi altri articoli, come in quello di Zakrzewski e collaboratori, 6 che hanno analizzato le complicanze occorse in circa 2000 interventi di facoemulsificazione in regime di anestesia topica con monitoraggio del paziente da parte del terapista respiratorio e hanno concluso che l’impiego dell’anestesista è stato necessario solo nel 2.2% dei casi; questi numeri trovano conferma anche in un altro studio pubblicato su Journal of Cataract & Refractive Surgery 7 dove, su un totale di 1002 procedure chirurgiche eseguite in anestesia topica con premedicazione orale il rianimatore è intervenuto solo nel 2.9% dei casi.
Da tutti questi dati emerge chiaramente come l’intervento dell’anestesista sia significativamente più basso laddove l’intervento di cataratta viene eseguito in regime di anestesia topica o in anestesia locale
10 LA VOCE AICCER 2/2023
CHIRURGIA DELLA CATARATTA
di G.M. Guerin, P.L. Guerin, E. Verdimonti, L. Iuri, D. Tognetto
previa sedazione, come dimostrato in precedenza anche dallo studio di Katz.8
Alla luce di questi risultati e nell’ottica di ottimizzare le risorse a disposizione abbiamo condotto, presso la Clinica Oculistica Universitaria di Trieste, uno studio retrospettivo non randomizzato per valutare il ruolo dell’anestesista in sala operatoria durante l’intervento di facoemulsificazione.
Materiali e metodi
L’analisi in questione ha previsto l’arruolamento di 848 pazienti sottoposti a intervento di facoemulsificazione con anestesia topica presso la nostra Struttura nel periodo da aprile a ottobre 2022. Per ogni paziente sono state riportate tutte le caratteristiche demografiche e quelle inerenti all’esame obiettivo oftalmologico pre-operatorio (Tabella 1).
Prendendo in considerazione come variabile dipendente l’intervento dell’anestesista in sala operatoria, abbiamo dunque analizzato quali fossero le condizioni pre- e intraoperatorie maggiormente predisponenti a tale evenienza.
Sulla base di questi parametri abbiamo eseguito un’analisi statistica univariata utilizzando il test chi quadrato (χ2) e, successivamente, tutte le variabili risultate statisticamente significative (P < 0,05) sono state oggetto di un’analisi di regressione logistica multivariata (SPSS Inc., Chicago; IL; IBM), allo scopo di creare uno score apposito per stimare quali
VARIABILI OCULISTICHE
Età
PSX
Facodonesi
Opacità corneali
Gutte
Assunzione di alfa-bloccanti
Maculopatia, glaucoma, retinopatia diabetica
Opacità della cataratta
(evoluta, brunescente, totale)
Scarsa midriasi (diametro pupillare < 4,0 mm)
Scarsa compliance
Camera anteriore < 2,5 mm
AL > 26,0 mm o < 21,5 mm
Durata intervento
Tabella 1. Parametri predittori
pazienti siano a maggior rischio di intervento dell’anestesista durante l’atto chirurgico.
Risultati
Dai dati raccolti è emerso che il numero totale di interventi anestesiologici intraoperatori è stato del 18%. Tuttavia, analizzando nel dettaglio, in due terzi dei casi l’anestesista interveniva esclusivamente con farmaci sedativi (nella fattispecie benzodiazepine a breve durata d’azione) e solo un terzo delle volte per altre evenienze come crisi ipertensive, bradicardie, dolori articolari correlati ad artrosi o cifosi, etc. Va precisato, inoltre, che non si sono mai verificate situazioni estreme quali l’arresto cardiorespiratorio. Dall’analisi univariata è emerso che il fattore predittivo con il maggior odds ratio, e pertanto di maggior rilievo, per l’intervento dell’anestesista è la durata dell’operazione chirurgica (test chi quadrato, P < 0,05) e il valore cut-off, scelto sulla base della curva ROC (receiver operating characteristic) come il punto con la maggior area sotto la curva, con una sensibilità del 75% e una specificità del 70%, corrisponde ad una durata della chirurgia di 25 minuti (Figura 1). Da ciò possiamo dedurre che quando la chirurgia si protrae oltre i 25 minuti sussiste una elevata probabilità che l’anestesista debba provvedere alla somministrazione di farmaci per via endovenosa. La durata dell’intervento è una variabile intraoperatoria strettamente connessa con un’aumentata difficoltà dell’intervento e, di conseguenza, con lo sviluppo di complicanze che, come noto, prolungano le
11 LA VOCE AICCER 2/2023 CHIRURGIA DELLA CATARATTA
Figura 1. Curva ROC per stimare il valore cut-off della durata della chirurgia cui corrisponda, con massima sensibilità e specificità, l’intervento dell’anestesista.
CHIRURGIA DELLA CATARATTA
tempistiche operatorie. Essa, parimenti all’intervento anestesiologico in sala, correla con alcuni dei para metri preoperatori presi in esame. L’analisi fin qui eseguita, però, non teneva conto di un elemento fondamentale, ossia l’esperienza del chirurgo, che inficia notevolmente la durata dell’in tervento. Questo emerge chiaramente andando ad analizzare i dati relativi alle cataratte “di complessa esecuzione”, come ad esempio le cataratte totali le quali, stando all’analisi statistica, non costituireb bero un elemento determinante nel produrre tempi stiche operatorie dilatate; ciò è giustificato dal fatto che nella nostra struttura vengono eseguite, nella maggior parte dei casi, da chirurghi esperti. Pertan to, in questo studio abbiamo preso in considerazio
, nell’analisi univariata, significatività statistica sono state inserite nell’analisi di regressione 2). Questa ci ha fornito i valori di P – value di ogni variabile esponenziali dei coefficienti di regressione beta (EXP β) che ciascuna variabile nel determinare l’evento. A partire da questi la stratificazione del rischio di intervento anestesiologico (Tabella
IBM Chicago Illinois versione 25.0
Tabella 2: Analisi di regressione logistica multivariata Chicago
per la stratificazione del rischio di intervento anestesiologico nei pazienti operandi di estrazione di cataratta
12 LA VOCE AICCER 2/2023
VARIABILI Sig. (P) Exp (B) 95% C.I. for Exp (B) Età 0,05 2, 11 1,01 ± 4, 40 Alfa litici 0,10 0, 87 0,49± 1, 54 Scarsa compliance <0,05 1, 61 1,02 ± 2,54 Maculopatia / Glaucoma <0,05 2, 40 1,45 ± 3,96 Opacità corneali <0,05 3, 90 2,36 ± 6,43 Cataratta evoluta <0,05 3, 80 2,39 ± 6,27 Cataratta totale <0,05 8, 34 4,35 ± 15,97 Facodonesi + PSX <0,05 3, 56 1,37 ± 9,26 Scarsa midriasi <0,05 5, 97 3,16 ± 11,30 CA bassa <0,05 2, 12 1,16 ± 3,88
e impianto
VARIABILI Sig. (P) Età 0,05 Alfa litici 0,10 Scarsa compliance <0,05 Maculopatia / Glaucoma <0,05 Opacità corneali <0,05 Cataratta evoluta <0,05 Cataratta totale <0,05 Facodonesi + PSX <0,05 Scarsa midriasi <0,05 CA bassa <0,05
Tabella 2. Analisi di regressione logistica multivariata ottenuta con il software SPSS
one
Illinois versione
FATTORI DI RISCHIO PUNTEGGIO Età > 90 anni 1 Maculopatia, glaucoma o altre patologie retiniche 1 Densità della cataratta Evoluta Totale / Brunescente 2 4 Facodonesi / PSX 2 Scarsa compliance 1 Opacità corneali (in base a posizione e grado dell’opacità) 1 – 3 Scarsa midriasi (diametro pupillare < 4.0 mm) 3 Camera anteriore < 2.5 mm o SE > 5.0 D 1 Chirurgo principiante 2
25.0
Tabella 3. Score pre-operatorio
ne solo pazienti operati da chirurghi che avessero una media esperienza, definita come un numero di interventi di cataratta all’attivo compreso tra 100 e 800.
Le variabili indipendenti preoperatorie che, nell’analisi univariata, hanno dimostrato una significatività statistica sono state inserite nell’analisi di regressione logistica multivariata (Tabella 2). Questa ci ha fornito i valori di P – value di ogni variabile diagnostica e, soprattutto, gli esponenziali dei coefficienti di regressione beta (EXP β) che esprimono il rischio relativo di ciascuna variabile nel determinare l’evento. A partire da questi ultimi abbiamo creato uno score per la stratificazione del rischio di intervento anestesiologico (Tabella 3).
Inoltre, abbiamo notato che sussiste un significativo aumento di probabilità di intervento anestesiologico qualora la chirurgia sia eseguita da un chirurgo con un’esperienza inferiore ai 100 interventi.
Il valore cut-off definito grazie alla curva ROC è 4: un punteggio totale maggiore o uguale a 4 è associato ad un’aumentata probabilità di intervento da parte del rianimatore durante la chirurgia.
Conclusioni
Ad oggi, a seguito dell’emergenza COVID-19 che ha visto i medici anestesisti sempre più impegnati e in sofferenza per la carenza di organico, è necessario indirizzare le loro risorse verso dove vi è una maggior richiesta.
L’obiettivo è quello di un’ottimizzazione: ridurre, entro i ragionevoli limiti, l’attività del medico rianimatore in sala operatoria oculistica e, eventualmente, poter organizzare due sedute di chirurgia della cataratta contemporanee con la presenza di un solo anestesista.
In questo studio ci siamo limitati alla disamina esclusiva di parametri oculistici, per avere un’analisi completa occorre tenere in considerazione
anche lo stato di salute generale del paziente, in modo da potersi esprimere con maggiori sicurezze circa la necessità di presenza dell’anestesista in sala operatoria durante l’intervento di facoemulsificazione.
Per questo motivo, in fase preliminare sono stati raccolti dai colleghi rianimatori anche i parametri predittivi di natura sistemica; il passo successivo consisterà nell’andare ad integrare ed implementare il nostro score con i dati inerenti alle patologie internistiche concomitanti.
Bibliografia
1. Song P, Wang H, Theodoratou E, Chan KY, Rudan I. The national and subnational prevalence of cataract and cataract blindness in China: a systematic review and metaanalysis. 2018;8(1):10804. doi:10.7189/jogh.08.010804
2. Linee Guida CLiniCo orGanizzative SuLLa ChirurGia deLLa Cataratta. Accessed April 4, 2023. www.soiweb. com
3. Lin PF, Naveed H, Eleftheriadou M, Purbrick R, Zarei Ghanavati M, Liu C. Cataract service redesign in the post-COVID-19 era. Br J Ophthalmol. 2021;105(6):745750. doi:10.1136/BJOPHTHALMOL-2020-316917
4. Conditions de réalisation de la chirurgie de la cataracte: environnement technique—rapport d’évaluation. Haute Autorité de Santé.
5. Erie AJ, McHugh R, Warner M, Erie JC. Model of anesthesia care that combines anesthesiologists and registered nurses during cataract surgery. J Cataract Refract Surg. 2011 Mar;37(3):481-5. doi: 10.1016/j.jcrs.2010.09.021. Epub 2011 Jan 22. PMID: 21262560.
6. Zakrzewski PA, Friel T, Fox G, Braga-Mele R. Monitored anesthesia care provided by registered respiratory care practitioners during cataract surgery: a report of 1957 cases. Ophthalmology. 2005 Feb;112(2):272-7. doi: 10.1016/j.ophtha.2004.08.016. PMID: 15691563.
7. Jonas, J. B., Pakdaman, B., Sauder, G. & Bender, H.-J. Is intraoperative monitoring necessary in cataract surgery under topical anesthesia? J. Cataract Refract. Surg. 30, 2645-2646 (2004).
8. Katz J, Feldman MA, Bass EB, et al, Study of Medical Testing before Cataract Surgery. Adverse intraoperative medical events and their association with anesthesia man- agement strategies in cataract surgery. Ophthalmology 2001;108:1721– 6.
13 LA VOCE AICCER 2/2023 CHIRURGIA DELLA CATARATTA
Dinamica e fattori di rischio per la capsula posteriore durante femtocataratta
L’impiego del laser a femtosecondi per il moderno intervento di cataratta (Femtosecond-Laser-Assisted Cataract Surgery, FLACS) rappresenta uno dei maggiori progressi tecnologici degli ultimi anni nell’ambito dell’Oftalmologia1. Seppur tale tecnologia permetta attualmente solo di effettuare le prime fasi dell’intervento, ovvero la capsuloressi, la frammentazione della cataratta e le incisioni corneali, i sostenitori di questa tecnologia elogiano le maggiori qualità e precisione con le quali queste fasi vengono eseguite dal laser rispetto alla tecnica manuale2 . Il laser a femtosecondi agisce producendo delle microbolle all’interno di tessuti trasparenti, le quali nell’insieme producono il piano di taglio. Il volume delle microbolle dipende dall’energia e dalla spaziatura del laser ed un problema noto nell’impiego dei laser a femtosecondi è quello di determinare la quantità precisa di energia e di spaziatura dello spot per ottenere il taglio.

Poiché l’energia dello spot deve essere impostata prima dell’intervento in base alla presunta durezza della cataratta, è possibile venga selezionato un livello basso, o eccessivamente alto di energia. Un’energia inferiore a quella richiesta sarà inefficace nel produrre il taglio, mentre un’energia eccessiva darà luogo a grandi e confluenti bolle, con il rischio di danneggiare i tessuti circostanti. Un problema specifico della FLACS sta nel determinare la giusta distanza dalla capsula posteriore (PC) alla quale si può avere un’efficace frammentazione senza il rischio di danneggiarla.
I moderni femtolaser sono dotati inoltre di un dispositivo OCT (Optical Coherence Tomography) che in tempo reale ci permette di osservare la
procedura in tempo reale. Proprio osservando lo svolgersi della procedura di frammentazione mediante OCT in continuo abbiamo identificato quattro condizioni che possono mettere a rischio la capsula posteriore.
Dinamiche e possibilità di danno
Meccanismo 1
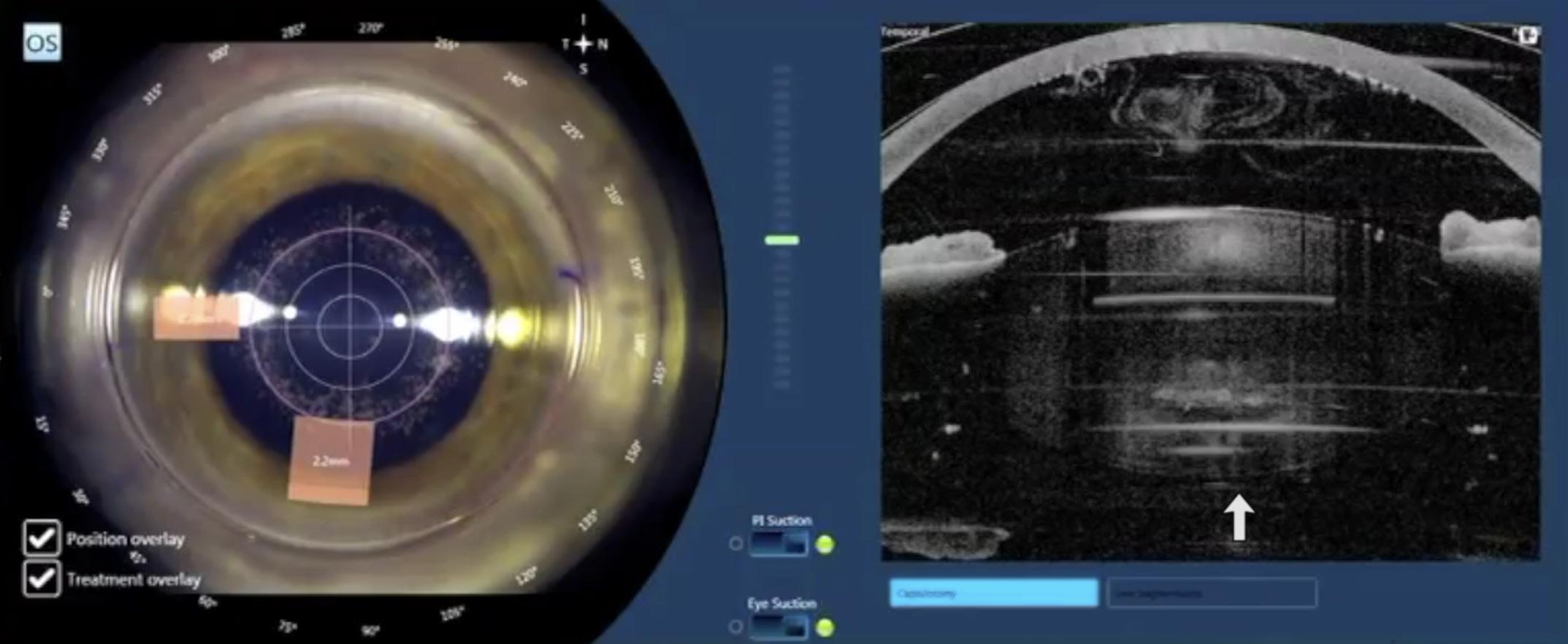
L’occhio si inclina (tilting) subito dopo la procedura di docking o dopo la capsulotomia. In questo caso il pericolo per la capsula posteriore è evidente, poiché il chirurgo può non rendersene conto e procedere comunque con la frammentazione laser che può tagliare la capsula posteriore. Particolare attenzione va riservata quando si sceglie una procedura di “soft docking”, la quale più facilmente permette che condizioni come questa si verifichino, in associazione a ridotta zona posteriore non trattata, ad esempio di soli 0.5 mm (Figura 1).
Meccanismo 2
In tutte le procedure FLACS eseguite in occhi con cataratta di una certa durezza si può quasi sempre osservare un minimo movimento della capsula posteriore, mentre per cataratte poco avanzate spesso tali movimenti non si osservano. Ciò è verosimilmente dovuto all’aumento di volume intralenticolare prodotto dalle microbolle. Poiché l’energia meccanica di espansione trova maggiore sfogo dove la resistenza è minore, cataratte molli assorbiranno l’energia di espansione a 360°, mentre cataratte con nucleo duro la assorbiranno meno e l’energia meccanica tenderà a sfogarsi nella direzione in cui la resistenza è minore, ovvero verso la capsula posteriore.
14 LA VOCE AICCER 2/2023
CHIRURGIA DELLA CATARATTA
di Carlo Bellucci, Paolo Mora, Salvatore Antonio Tedesco, Roberto Bellucci, Stefano Gandolfi
Meccanismo 3
Quando la durezza della cataratta è tale da non permettere in alcun modo l’assorbimento di questa energia di espansione dovuta alla formazione delle microbolle, tale energia verrà subito, e in maniera quasi completa, direzionata verso la capsula posteriore in quanto locus di minore resistenza, portando al verificarsi di una vera e propria concussione posteriore dell’intera capsula. Quando inizia la frammentazione, la grande bolla di gas potrà così espandersi rapidamente e il rischio di sfondamento della capsula posteriore diventa reale.
Meccanismo 4
La concussione della capsula posteriore può essere diffusa all’intera capsula, come mostrato in precedenza, o localizzata in una sua porzione. Questo fenomeno transitorio è solitamente localizzato nella porzione centrale della capsula posteriore, ma per i meccanismi esposti in precedenza, tale concussione può avvenire in maniera isolata anche in periferia. Ciò si può verificare ad esempio in quelle condizioni in cui la cataratta presenta durezza disomogenea e a condizione che la pupilla e l’area di frammentazione siano sufficientemente grandi (Figura 4).
15 LA VOCE AICCER 2/2023 CHIRURGIA DELLA CATARATTA
Figura 1. Occhio inclinato dopo procedura docking.
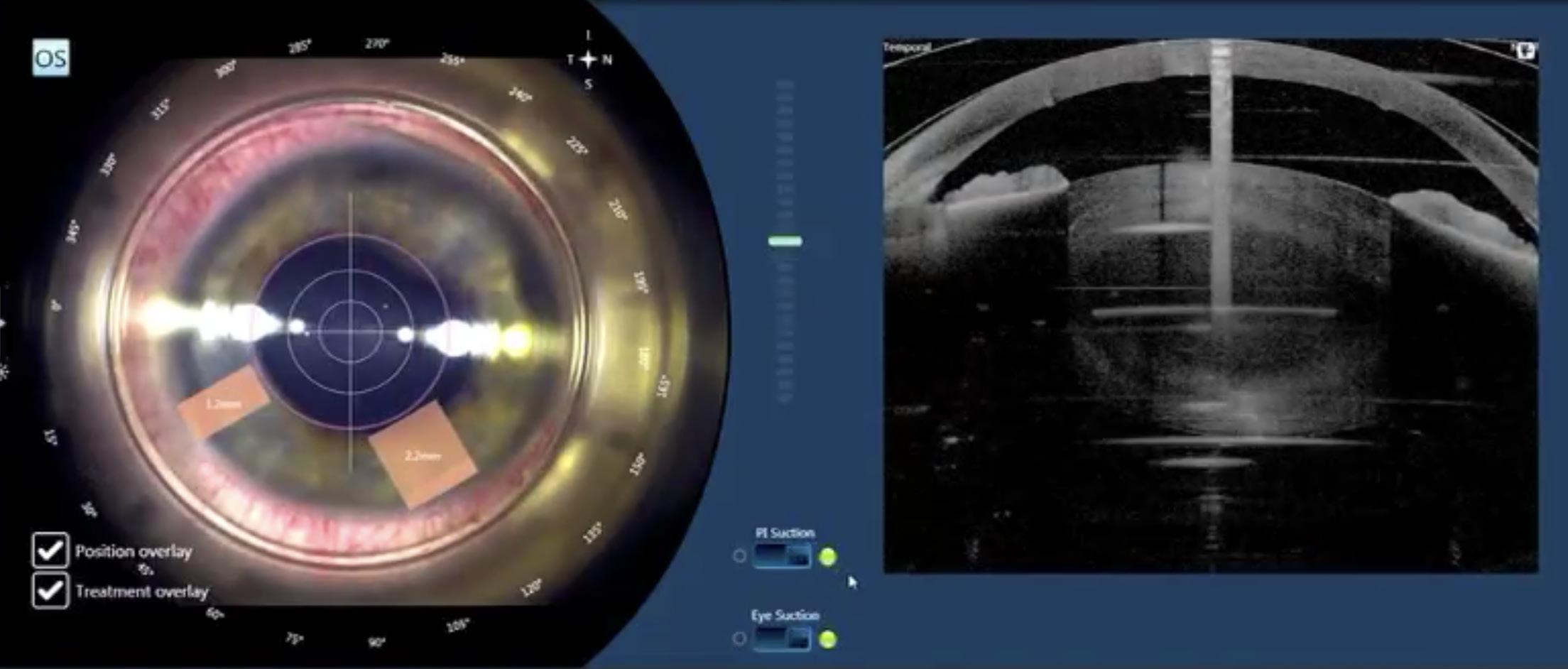
Figura 2. Piccoli movimenti della capsula posteriore si possono spesso osservare in corrispondenza del primo piano di applicazione del laser per frammentare la cataratta.
16 LA VOCE AICCER 2/2023
CHIRURGIA DELLA CATARATTA
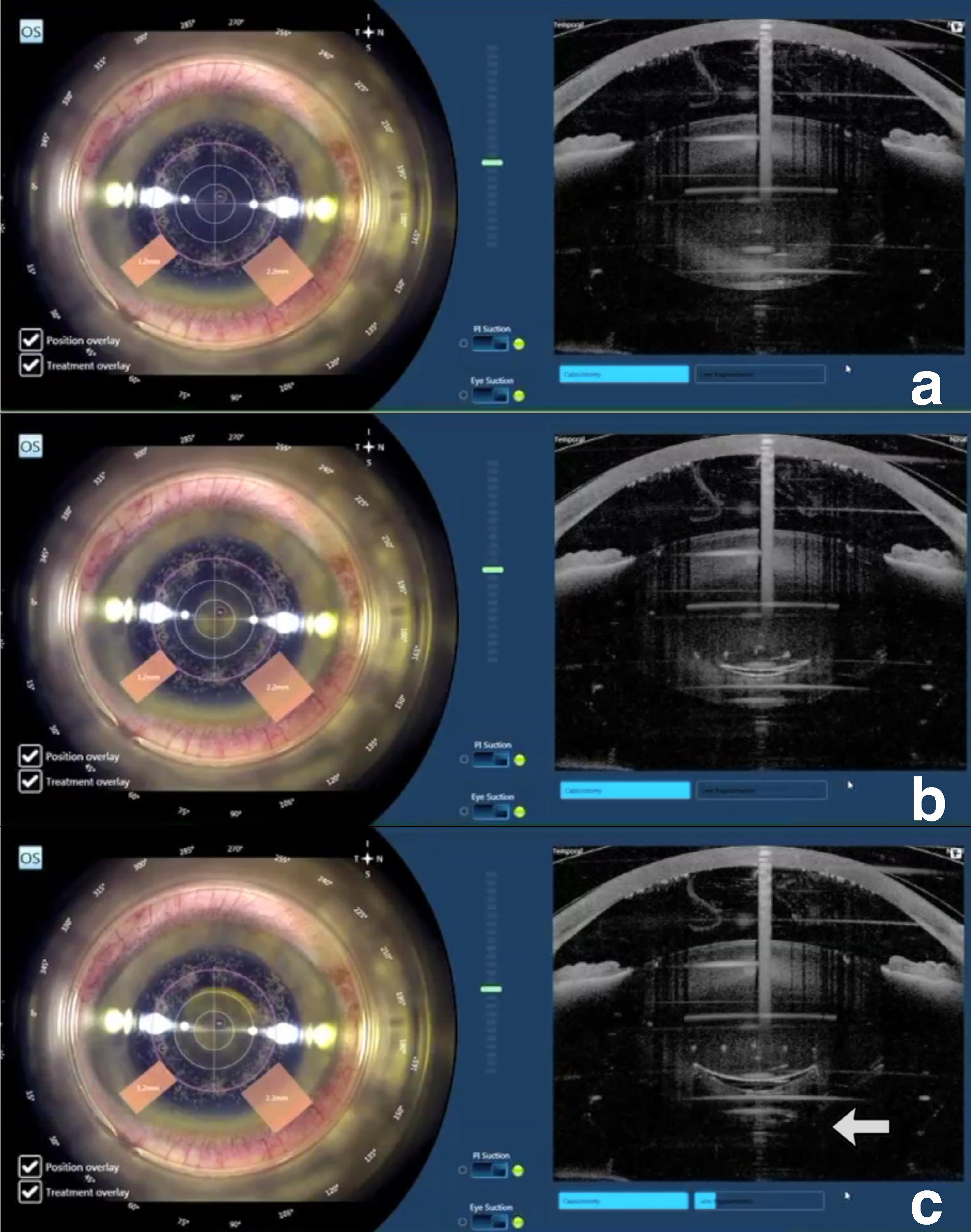
Figura 3. (a-c). Composita che mostra diversi momenti di applicazione del laser per frammentare una cataratta dura: a) preframmentazione; b) inizio della frammentazione; c) con l’avanzare della frammentazione l’energia di espansione si accumula e si sfoga posteriormente dislocando temporaneamente la capsula posteriore.
Discussione
Seppur il numero di lacerazioni della capsula posteriore della FLACS è simile a quello della facoemulsificazione o addirittura inferiore5-9, il perfezionamento delle nostre conoscenze riguardo questa procedura può aiutarci a capire meglio e migliorare la nostra tecnica.
L’azione del laser a femtosecondi comporta la formazione di bolle di gas, aumentando così il volume di qualsiasi tessuto trattato, e l’entità di questo aumento dipende dall’energia dello spot, dalla spaziatura e dalla densità del tessuto. Seppur sembri ragionevole
aumentare l’energia dello spot per tagliare i nuclei duri così come si aumenta la potenza degli ultrasuoni nella facoemulsificazione, questo concetto è discutibile. Infatti l’energia del laser a femtosecondi è completamente diversa da quella degli ultrasuoni: trattandosi di energia luminosa viene bloccata dalle opacità, ma risulta molto efficace in tessuti duri e trasparenti che possono richiedere un’energia inferiore rispetto ai tessuti opachi più morbidi.
Le grandi bolle che spostano posteriormente la capsula posteriore per alcuni secondi si sviluppano a causa dell’eccessiva energia applicata nella parte
17 LA VOCE AICCER 2/2023 CHIRURGIA DELLA CATARATTA
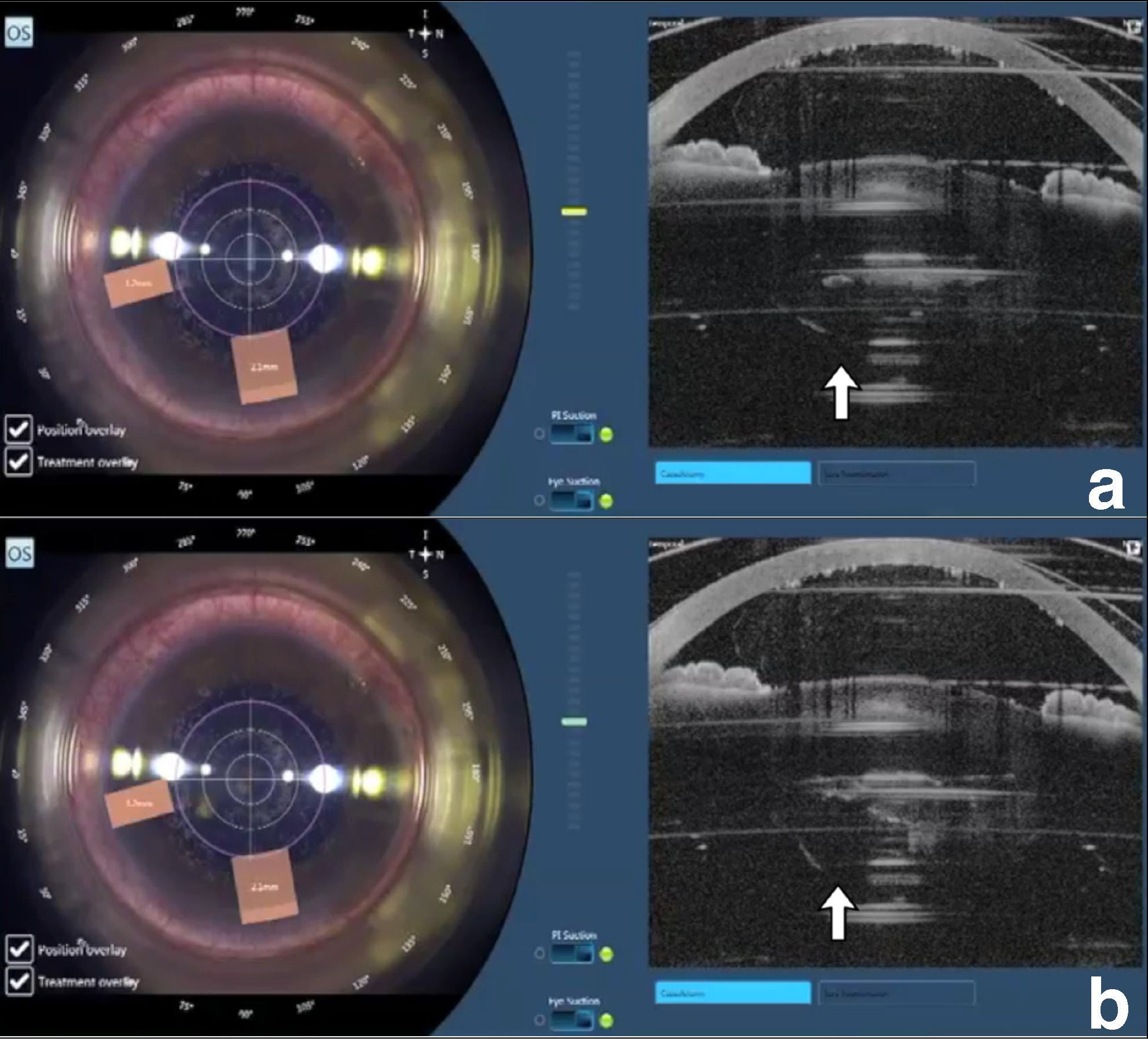
Figura 4. (a-b). Composita che mostra diversi momenti di applicazione del laser per frammentare una cataratta con consistenza disomogenea: a) inizio della frammentazione, la capsula posteriore rimane in sede; b) la freccia indica la porzione di capsula che si è dislocata posteriormente rimanendo integra.
CHIRURGIA DELLA CATARATTA
posteriore del nucleo di una lente dura. Possiamo limitare questo spostamento riducendo l’energia dello spot e aumentando la zona di sicurezza posteriore per avviare la frammentazione all’interno del nucleo della lente, anche se purtroppo questo ne limiterà l’efficacia. Riteniamo che una migliore comprensione delle dinamiche tissutali durante l’attività del laser a femtosecondi sia importante non solo per l’impostazione dei parametri da parte del chirurgo, ma anche per il miglioramento dell’interazione tra ingegneri e medici. Ad esempio, un’impostazione dell’energia dello spot che aumenta dalla corteccia posteriore del cristallino fino alla zona dell’equatore e successivamente diminuisce fino alla corteccia anteriore potrebbe ridurre il rischio per la capsula posteriore, pur mantenendo l’efficienza della frammentazione.
Bibliografia
1. Nagy Z, Takacs A, Filkorn T, Sarayba M. Initial clinical evaluation of an intraocular femtosecond laser in cataract surgery. J Refract Surg. 2009 Dec;25(12):1053-60. doi: 10.3928/1081597X-20091117-04. PMID: 20000286.
2. Nagy ZZ, McAlinden C. Femtosecond laser cataract surgery. Eye Vis (Lond). 2015 Jun 30;2:11. doi: 10.1186/ s40662-015-0021-7. PMID: 26605364; PMCID: PMC4655462.
3. Kanclerz P, Alio JL. The benefits and drawbacks of femtosecond laser-assisted cataract surgery. Eur J Ophthalmol. 2021 May;31(3):1021-1030. doi: 10.1177/1120672120922448. Epub 2020 Jun 7. PMID: 32508179.
4. Mayer WJ, Ohlmann A, Schuh A, Priglinger S, Kohnen T, Shajari M. Electron microscopy analysis of femtose-
cond laser-assisted capsulotomy before and after lens fragmentation. Sci Rep. 2021 Dec 24;11(1):24427. doi: 10.1038/s41598-021-04054-5. PMID: 34952916; PMCID: PMC8709839.
5. Kolb CM, Shajari M, Mathys L, Herrmann E, Petermann K, Mayer WJ, Priglinger S, Kohnen T. Comparison of femtosecond laser-assisted cataract surgery and conventional cataract surgery: a meta-analysis and systematic review. J Cataract Refract Surg. 2020 Aug;46(8):10751085. doi: 10.1097/j.jcrs.0000000000000228. PMID: 32358416.
6. Abell RG, Darian-Smith E, Kan JB, Allen PL, Ewe SY, Vote BJ. Femtosecond laser-assisted cataract surgery versus standard phacoemulsification cataract surgery: outcomes and safety in more than 4000 cases at a single center. J Cataract Refract Surg. 2015 Jan;41(1):4752. doi: 10.1016/j.jcrs.2014.06.025. Epub 2014 Nov 11. PMID: 25466483.
7. Song C, Baharozian CJ, Hatch KM, Grassett GC, Talamo JH. Rate of Unplanned Vitrectomies in Femtosecond Laser-Assisted Cataract Surgery Compared to Conventional Phacoemulsification. J Refract Surg. 2018 Sep 1;34(9):610-614. doi: 10.3928/1081597X-2018072601. PMID: 30199565.
8. Day AC, Burr JM, Bennett K, Doré CJ, Bunce C, Hunter R, Nanavaty MA, Balaggan KS, Wilkins MR; FACT trial group. Femtosecond laser-assisted cataract surgery compared with phacoemulsification cataract surgery: randomized noninferiority trial with 1-year outcomes. J Cataract Refract Surg. 2020 Oct;46(10):1360-1367. doi: 10.1097/j.jcrs.0000000000000257. Erratum in: J Cataract Refract Surg. 2021 Feb 1;47(2):286. PMID: 32773608.
9. Wang J, Su F, Wang Y, Chen Y, Chen Q, Li F. Intra and post-operative complications observed with femtosecond laser-assisted cataract surgery versus conventional phacoemulsification surgery: a systematic review and meta-analysis. BMC Ophthalmol. 2019 Aug 9;19(1):177. doi: 10.1186/s12886-019-1190-2. PMID: 31399070; PMCID: PMC6688351.
18 LA VOCE AICCER 2/2023
OCCHIO SECCO

Diagnosi e terapia


Giuseppe Di Meglio
Luigi Marino
Maria Luisa Verbelli
Lucio Buratto
VOLUME 3

Tel.
e-mail:
Ordina la tua copia su www.fgeditore.it
Redazione: Strada 4 Milano Fiori, Palazzo Q7 – 20089 Rozzano (MI) Sede operativa: FGE srl − Regione Rivelle 7/F − 14050 Moasca (AT)
0141 1706694 – Fax 0141 856013
info@fgeditore.it − www.fgeditore.it
ATLAS OF ANTERIOR SEGMENT OCT
di José Luis Güell*
Antisepsi e rigenerazione della superficie oculare
Review degli studi preclinici e clinici sull’olio ozonizzato in liposomi per la superficie oculare
Abstract
L’olio ozonizzato ha dimostrato proprietà antimicrobiche, antinfiammatorie e rigenerative, che lo rendono utile nella prevenzione delle patologie infettive, nonché come coadiuvante nella gestione della riparazione tissutale. Questa review della letteratura tratta la maggior parte degli aspetti relativi all’applicazione dell’olio ozonizzato in liposomi (OOL), relativamente ad infezioni oculari e rigenerazione della superficie oculare.
A seguito di una ricerca condotta sulle maggiori banche dati, sono state selezionate 25 pubblicazioni in merito a composizione, meccanismo d’azione, attività riparativa e studi pre-clinici e clinici. In pazienti con patologia corneale complicata, l’OOL ha mostrato di avere un effetto nel ripristino di ulcere corneali e di migliorare la cheratite. In pazienti con patologie oculari, infiammatorie o infettive, è stato riscontrato che l’OOL era in grado di migliorare e risanare quasi completamente i segni di congiuntivite Vernal, granulomatosa e adenovirale, ed ha dimostrato di essere efficace nel ridurre la flora microbica oculare. In conclusione, l’OOL è dotato di un effetto antisettico e riparativo sui tessuti corneocongiuntivali, ha mostrato un profilo di efficacia e sicurezza nella gestione di infezioni oculari e può essere considerato come una strategia di supporto, sia da solo che combinato con altri agenti antimicrobici.
Parole chiave: antifungino, antimicrobico, antivirale, olio ozonizzato in liposomi, effetto riparativo
Introduzione
L’olio ozonizzato in liposomi è il primo antisettico oculare a base di ozono destinato al supporto della prevenzione e del trattamento delle infezioni oculari1
L’ozono è un potente ossidante con proprietà antimicrobiche (contro batteri, virus e funghi), ed è dotato di attività di controllo dell’infiammazione e riparazione dei tessuti, ampiamente utilizzate in patologie dermatologiche e odontoiatriche2
L’olio ozonizzato, poi incapsulato in liposomi e disperso in una soluzione di ipromellosa, è ottenuto per reazione fra l’ozono gassoso e gli acidi grassi polinsaturi, e ne mantiene le proprietà1-3.
Le infezioni oculari, della superficie o riguardanti strutture interne, possono essere causate da un gran numero di microrganismi come batteri (fra cui Staphylococcus aureus, Stafilococchi coagulasinegativi, Pseudomonas aeruginosa), virus (come Adenovirus o, meno frequentemente, Herpes Simplex o Herpes Zoster), o funghi e lieviti (come Candida, Aspergillus o Fusarium)1
Generalmente le patologie oculari, traumatiche o infettive, sono gestite con diverse terapie volte a trattare e/o prevenire le infezioni e a promuovere la riepitelizzazione. L’uso eccessivo di antibiotici ha portato alla comparsa di ceppi batterici multi-

20 LA VOCE AICCER 2/2023
SUPERFICIE OCULARE
resistenti ai farmaci, pertanto vi è oggi la necessità di formulazioni antimicrobiche con nuovi meccanismi di azione per superare questo importante problema sanitario.
determinando, quindi, la distruzione del patogeno (Figura 1)1-2
Questa review riassume i dati rilevanti, preclinici e clinici, circa l’uso dell’OOL rigenerazione della superficie oculare1 .
Questa review riassume i dati rilevanti, preclinici e clinici, circa l’uso dell’OOL nelle infezioni oculari e nella rigenerazione della superficie oculare1
Venticinque articoli sono stati selezionati a seguito di una ricerca condotta sulle banche dati PubMed, Medline, Web of Science, and Cochrane Library1
Venticinque articoli sono stati selezionati a seguito di una ricerca condotta Medline, Web of Science, and Cochrane Library1 .
Risultati
Risultati
Composizione e Meccanismo d’azione
L’olio ozonizzato è un prodotto stabile generato dalla reazione dell’ozono gassoso con i doppi legami carbonio-carbonio degli acidi grassi insaturi contenuti nell’olio di girasole, attraverso intermedi chiamati ozonidi. La tollerabilità per i tessuti corneali è favorita dall’incapsulazione dell’olio ozonizzato in liposomi, che inoltre ne modula il rilascio e ne migliora la stabilità fisica, e dall’inserimento in una soluzione di ipromellosa2,4
Composizione e Meccanismo d’azione
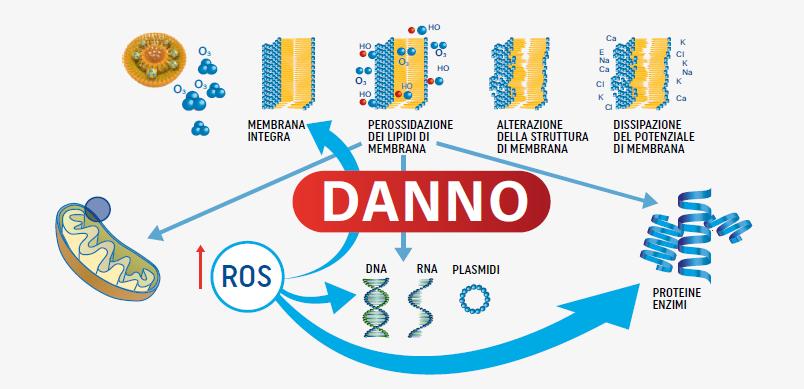
L’OOL è dotato di un doppio meccanismo d’azione: si lega alle strutture superficiali dei patogeni, danneggiandole per ozonolisi, e rilascia ozonidi che penetrano nel patogeno e generano composti ossigenati (come perossidi lipidici e specie reattive dell’ossigeno (ROS)) in grado di alterare macromolecole interne (proteine, lipidi, enzimi, DNA/RNA)
L'olio ozonizzato è un prodotto stabile generato dalla reazione dell’ozono carbonio-carbonio degli acidi grassi insaturi contenuti nell’olio di girasole ozonidi. La tollerabilità per i tessuti corneali è favorita dall’incapsulazione dell’olio fosfolipidi di soia, che inoltre ne modula il rilascio e ne migliora la stabilità soluzione di ipromellosa2,4 .
L’OOL non influisce negativamente sulle cellule epiteliali corneali e congiuntivali. L’ozono è un ossidante potente per le cellule umane ad alte concentrazioni ma, somministrato a dosi controllate, promuove l’adattamento cellulare allo stress ossidativo, attivando meccanismi antiossidanti ed antinfiammatori endogeni. Infatti, è naturalmente parte dell’immunità, innata ed acquisita; inoltre esercita attività di immunoeffettore, amplificando la risposta immunitaria attraverso la modulazione della produzione e dell’attività di molecole come NF-kB (nuclear factor kappa B) e TNFα (tumor necrosis factor alpha), interferone, citochine ed enzimi antiossidanti; inoltre regola i livelli di ossido nitrico, promuove la sintesi di collagene e stimola la produzione di fattori di crescita come il PDGF (platelet-derived growth factor) e il TGFβ (transforming growth factor-beta). L’effetto sui tessuti corneocongiuntivali comprende tre fasi: attività antimicrobica diretta; attivazione di difese antiossidanti locali con il rilascio di fattori di crescita ad effetto proliferativo; e promozione della guarigione delle ferite con effetto rimodellante1.
A dosi terapeutiche, non mostra tossicità su cellule epiteliali corneali e congiuntivali5-6.
L’effetto antimicrobico, unito a quello riparativo sui tessuti, offre un vantaggio rispetto ad altri antisettici disponibili1
L’OOL è dotato di un doppio meccanismo d’azione: si lega alle strutture danneggiandole per ozonolisi, e rilascia ozonidi che penetrano nel patogeno (come perossidi lipidici e specie reattive dell’os sigeno (ROS)) in grado di (proteine, lipidi, enzimi, DNA/RNA) determinando, quindi, la distruzione del
composti ossigenati, quali perossidi lipidici e ROS, che a loro volta alterano le strutture interne del patogeno portando alla sua distruzione.
21 LA VOCE AICCER 2/2023
Figura 1. Meccanismo d’ azione. I liposomi si legano alla superficie dell’agente patogeno danneggiandola per ozonolisi e rilasciando gli ozonidi, che penetrano nell’agente patogeno, si idrolizzano e formano
L'OOL non influisce negativamente sulle cellule epiteliali corneali e congiuntivali. potente per le cellule umane ad alte concentrazioni ma, somministrato SUPERFICIE OCULARE
Figura 1 Meccanismo d’ azione. I liposomi si legano alla superficie dell'agente patogeno danneggiandola e rilasciando gli ozonidi, che penetrano nell'agente patogeno, si idrolizzano e formano composti ossigenati volta alterano le strutture interne del patogeno portando alla sua distruzione.
SUPERFICIE OCULARE
Studi pre-clinici di efficacia
L’azione battericida dell’OOL è stata dimostrata in-vitro nei confronti di alcuni fra i più comuni patogeni oculari (Staphylococcus aureus e Pseudomonas aeruginosa), in grado di causare infezioni acute e croniche, con un effetto dose-dipendente5
Due studi hanno valutato e dimostrato l’attività antibatterica e l’effetto sul biofilm dell’OOL 0,5% (concentrazioni testate tra 250 e 0,25 μg/mL) su diversi ceppi fra cui S. aureus e P. aeruginosa, anche resistenti agli antibiotici6-7. L’OOL ha inoltre mostrato di inibire la formazione di biofilm da P. aeruginosa e S. aureus e di rimuovere il biofilm preformato su diversi supporti, come piastre di plastica e lenti a contatto7
Due studi hanno valutato e dimostrato l'attività antibatterica e l'effetto sul biofilm dell’OOL (concentrazioni testate tra 250 e 0,25 μg/mL) su diversi ceppi fra cui S. aureus e P. aeruginosa, resistenti agli antibiotici6-7 L’OOL ha inoltre mostrato di inibire la formazione di biofilm da P. aeruginosa aureus e di rimuovere il biofilm preformato su diversi supporti, come piastre di plastica e lenti a contatto Ha inoltre mostrato effetto fungicida su vari ceppi di Candida con MIC (minimum inhibitory concentration da 0.195% a 6.25%, ed il 70% delle cellule inattivate dopo 1 ora di esposizione2
o infettiva, come ulcere corneali, cheratiti o congiuntiviti, o con traumi corneali, sia da solo che in aggiunta ad altre terapie topiche o sistemiche10-12 Uno studio prospettico, singolo cieco, randomizzato, a gruppi paralleli, condotto su 80 pazienti con congiuntivite adenovirale, randomizzati a ricevere un’associazione di tobramicina 0,3%/desametasone 0,1% topico, da sola o in aggiunta ad OOL, quattro volte al giorno per sette giorni, ha mostrato una riduzione dei segni della congiuntivite (iperemia e chemosi) nei pazienti che avevano ricevuto OOL, nonché una riduzione della durata dell’infezione virale con un maggior numero di risultati PCR (polymerase chain reaction) negativi rispetto al controllo (82,3% vs 59,4%)13
L’effetto antivirale dell’ozono è stato mostrato su diverse specie (Herpes simplex virus-1, Adenovirus Influenza A, etc.), suggerendo un danno alle strutture lipidiche dell’envelope e proteiche del capside8 Studi in vivo su animale hanno mostrato l’efficacia dell’OOL su congiuntiviti ricorrenti ed ulcere corneali Inoltre, applicato nel sacco congiuntivale e sulla cute perioculare del cane, l’OOL 0,5%, ha mostrato effetto superiore all’ofloxacina e paragonabile allo iodopovidone 5%, nell’abbattimento della conta microbica totale3
Studi clinici di efficacia
Ha inoltre mostrato effetto fungicida su vari ceppi di Candida con MIC (minimum inhibitory concentration) da 0.195% a 6.25%, ed il 70% delle cellule inattivate dopo 1 ora di esposizione2 L’effetto antivirale dell’ozono è stato mostrato su diverse specie (Herpes simplex virus-1, Adenovirus-2, Influenza A, etc.), suggerendo un danno alle strutture lipidiche dell’envelope e proteiche del capside8 .
Studi in vivo su animale hanno mostrato l’efficacia dell’OOL su congiuntiviti ricorrenti ed ulcere corneali9. Inoltre, applicato nel sacco congiuntivale e sulla cute perioculare del cane, l’OOL 0,5%, ha mostrato effetto superiore all’ofloxacina e paragonabile allo iodopovidone 5%, nell’abbattimento della carica microbica totale3
Alcune serie di casi clinici pubblicati hanno evidenziato l’effetto del OOL in pazienti con patologie corneali complicate di origine infiammatoria o infettiva, come ulcere corneali, cheratiti o congiuntiviti, o con traumi corneali, sia da solo che in aggiunta ad altre terapie topiche o sistemiche10-12 .
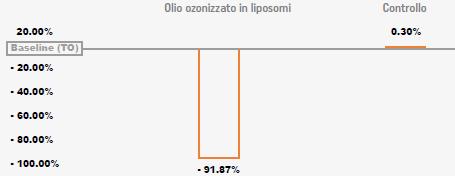
In uno studio interventistico di Fase IV, non randomizzato, ad occhi paralleli, 174 pazienti che dovevano sottoporsi ad un intervento di chirurgia della cataratta hanno ricevuto una soluzione allo 0,5% di OOL e soluzione salina all’occhio controlaterale, 2 gocce per 4 volte al giorno nei 3 giorni precedenti l’intervento. L’OOL ha determinato una riduzione >90% della flora microbica oculare, rimasta invece inalterata nel gruppo di controllo (p < 0.001) (Figura 2)14. Dunque, può essere utilizzato come profilassi pre-operatoria domiciliare, quale adiuvante della soluzione di iodopovidone utilizzata in sala operatoria1
Uno studio prospettico, singolo cieco, randomizzato, a gruppi paralleli, condotto su 80 pazienti congiuntivite adenovirale, randomizzati a ricevere tobramicina 0,3%/desametasone 0,1% topico, da solo aggiunta ad OOL, quattro volte al giorno per sette giorni, ha mostrato una riduzione dei segni congiuntivite (iperemia e chemosi ) nei pazienti che avevano ricevuto OOL, nonché una riduzione della durata dell’infezione virale con un maggior numero di risultati PCR (polymerase chain reaction) negativi rispetto controllo (82,3% vs 59,4%)13
Studi clinici di efficacia
Alcune serie di casi clinici pubblicati hanno evidenziato l’effetto del OOL in pazienti con patologie corneali complicate di origine infiammatoria
Sicurezza
Test oftalmici e dermatologici classificano l’olio ozonizzato come non-irritante, non-sensitizzante. Studi in vitro su linee cellulari umane, come cheratinociti epiteliali e cellule di epitelio congiuntivale e corneale, non hanno evidenziato inibizione della crescita o tossicità cellulare vs controllo,
In uno studio interventistico di Fase IV, non randomizzato, ad occhi paralleli, 174 pazienti che dovevano sottoporsi ad un intervento di chirurgia della cataratta hanno ricevuto una soluzione isotonica allo 0,5% OOL e soluzione salina all’occhio controlaterale, 2 gocce per 4 volte al giorno nei 3 giorni precedenti l’intervento L’OOL ha determinato una riduzione >90% della flora microbica oculare, rimasta inalterata nel gruppo di controllo (p < 0.001) (Figura 2)14 Dunque, può essere utilizzato come profilassi operatoria domiciliare, quale adiuvante della soluzione di iodopovidone utilizzata in sala operatoria1
Sicurezza
Test oftalmici e dermatologici classificano l’olio ozonizzato come non-irritante, non-sensitizzante Studi vitro su linee cellulari umane, come cheratinociti epiteliali e cellule di epitelio congiuntivale e corneale, hanno evidenziato inibizione della crescita o tossicità cellulare vs controllo, né alterazione dell’attività metabolica (1-3 ore di contatto con OOL)5-6
Gli studi clinici condotti su pazienti con congiuntivite adenovirale e su pazienti che dovevano sottoporsi
22 LA VOCE AICCER 2/2023
Figura 2. Riduzione del carico microbico con olio ozonizzato vs gruppo di controllo.
Figura 2 Riduzione del carico microbico con olio ozonizzato vs gruppo di controllo.
né alterazione dell’attività metabolica (1-3 ore di contatto con OOL)5-6
Gli studi clinici condotti su pazienti con congiuntivite adenovirale e su pazienti che dovevano sottoporsi a chirurgia della cataratta hanno mostrato che il trattamento era ben tollerato con solo 3 pazienti che mostravano tracce di iperemia congiuntivale e 7 pazienti che hanno riferito discomfort all’instillazione (6 lieve, 1 moderato)13-14
Discussione e Conclusioni
La review ha riassunto 25 articoli sull’olio ozonizzato, le sue proprietà e gli studi clinici e preclinici condotti, che hanno contribuito alla comprensione delle sue caratteristiche e proprietà nella gestione delle infezioni oculari.
L’abuso di antibiotici, e la conseguente emergenza di specie multi-resistenti, rappresenta una minaccia per la salute che andrà affrontata nel breve termine e sta portando allo studio di ulteriori agenti antimicrobici come gli antisettici. L’OOL è stato studiato in diverse patologie mostrando buone proprietà antimicrobiche e, finora, non è stata descritta alcuna resistenza batterica agli oli ozonizzati, rendendolo una valida alternativa nella prevenzione e nel trattamento di infezioni oculari, da solo o in combinazione ad altri antimicrobici.
Gli studi pre-clinici e clinici hanno confermato l’attività antimicrobica ad ampio spettro nonché l’effetto riparativo, e un basso tasso di eventi avversi. Inoltre, potrebbe rappresentare un interessante supplemento nell’equilibrio antiossidante ed infiammatorio della superficie oculare.
Pertanto, in ragione della sua sicurezza ed efficacia, l’OOL può essere considerato un nuovo strumento di contrasto alle infezioni oculari. Sono comunque raccomandati ulteriori studi con OOL, sia da solo che in combinazione con farmaci antinfettivi1
Bibliografia
1. Pérez-Santonja JJ, Güell JL, Gris O, Vázquez Dorrego XM, Pellicer E, Benítez-Del-Castillo JM. Liposomal Ozonated Oil in Ocular Infections: A Review of Preclinical and
SUPERFICIE OCULARE
Clinical Studies, Focusing on Its Antiseptic and Regenerative Properties. Clin Ophthalmol. 2022;16:1953-1962.
2. Celenza G, Iorio R, Cracchiolo S, et al. Antimycotic Activity of Ozonized Oil in Liposome Eye Drops against Candida spp. Transl Vis Sci Technol. 2020;9(8):4.
3. Marchegiani A, Magagnini M, Cerquetella M, et al. Preoperative topical liposomal ozone dispersion to reduce bacterial colonization in conjunctival sac and periocular skin: Preliminary study in dogs. Exp Eye Res. 2019;189:107848.
4. Ugazio E, Tullio V, Binello A, Tagliapietra S, Dosio F. Ozonated Oils as Antimicrobial Systems in Topical Applications. Their Characterization, Current Applications, and Advances in Improved Delivery Techniques. Molecules. 2020;25(2):334.
5. Cutarelli, A. , Carlini, G. , Sarno, F. , et al. The Role of Ozone Carried by Liposomes in the Therapy of Infectious and Skin-Regenerating Ocular Surface. Journal of Biomedical Science and Engineering. 2019 (12): 347-353.
6. Paduch R, Urbanik-Sypniewska T, Kutkowska J, et al. Ozone-Based Eye Drops Activity on Ocular Epithelial Cells and Potential Pathogens Infecting the Front of the Eye. Antioxidants (Basel). 2021;10(6):968.
7. Zerillo L, Polvere I, Varricchio R, et al. Antibiofilm and repair activity of ozonated oil in liposome. Microb Biotechnol. 2022;15(5):1422-1433.
8. Murray BK, Ohmine S, Tomer DP, et al. Virion disruption by ozone-mediated reactive oxygen species. J Virol Methods. 2008;153(1):74-77.
9. Marchegiani A, Spaterna A. Ozone-based eye drops in anterior segment pathologies: rationale and pre-clinical data. Ozone Ther. 2017;2(1):6743.
10. Passidomo F, Pignatelli F, Addabbo G, Costagliola C. Topical Liposomal Ozonated Oil in Complicated Corneal Disease: A Report on Three Clinical Cases. Int Med Case Rep J. 2021;14:327-332.
11. Spadea L, Tonti E, Spaterna A, Marchegiani A. Use of Ozone-Based Eye Drops: A Series of Cases in Veterinary and Human Spontaneous Ocular Pathologies. Case Rep Ophthalmol. 2018;9(2):287-298.
12. Basile AA, Cendali M, Mandelli G, Fioretto G. Antiinflammatory effect of an eye drops solution based on liposomal ozonated oil in different corneal and anterior segment human diseases. Ozone Ther. 2019;4(2):8377.
13. Cagini C, Mariniello M, Messina M, et al. The role of ozonized oil and a combination of tobramycin/dexamethasone eye drops in the treatment of viral conjunctivitis: a randomized clinical trial. Int Ophthalmol. 2020;40(12):3209-3215.
14. Spadea L, Zanotto E, Cavallo R, et al. Effectiveness of liposomal ozonized oil in reducing ocular microbial flora in patients undergoing cataract surgery. J Cataract Refract Surg. 2021;47(12):1548-1555.
23 LA VOCE AICCER 2/2023
*Dipartimento di Cornea e Chirurgia Refrattiva, Institut de Microcirurgia Ocular (IMO), Barcellona, Spagna. Past President ESCRS e EuCornea.
di Alessandro David

Edema maculare cistoide: come combatterlo
La sinergia tra FANS e corticosteroidi
è la formula vincente
Nonostante l’alto grado di standardizzazione e il profilo di sicurezza ed efficacia ottimale, la chirurgia della cataratta ancora oggi non è esente da problematiche post-operatorie di vario genere. Tra queste l’edema maculare cistoide pseudofachico (PCME), noto anche come Sindrome di Irvine-Gass (IGS), rimane una delle cause di maggiore compromissione della qualità visiva del paziente durante il recupero postoperatorio.
Per quanto l’introduzione della moderna facoemulsificazione, dei farmaci antinfiammatori non steroidei e dei colliri glucocorticoidi abbiano sensibilmente ridotto la sua incidenza, circa lo 0,18% dei pazienti presenta ancora manifestazioni cliniche significative di questa patologia. La patogenesi del PCME non è ancora del tutto chiara; tuttavia, il primo possibile fattore scatenante la cascata infiammatoria alla base della rottura della barriera emato-retinica è indicato nel trauma chirurgico dei tessuti intraoculari. Il danno iatrogeno alla barriera emato-acquosa potrebbe infatti essere responsabile di una diffusione nella cavità vitrea di prostaglandine (PG) ed altri mediatori dell’infiammazione con conseguente insorgenza di PCME in alcuni pazienti.
Intervenire tempestivamente sul processo infiammatorio in fase postoperatoria con un uso topico combinato di corticosteroidi e FANS è raccomandato per ridurre il rischio di sviluppare questa complicanza post-chirurgica.
L’utilizzo della terapia con FANS
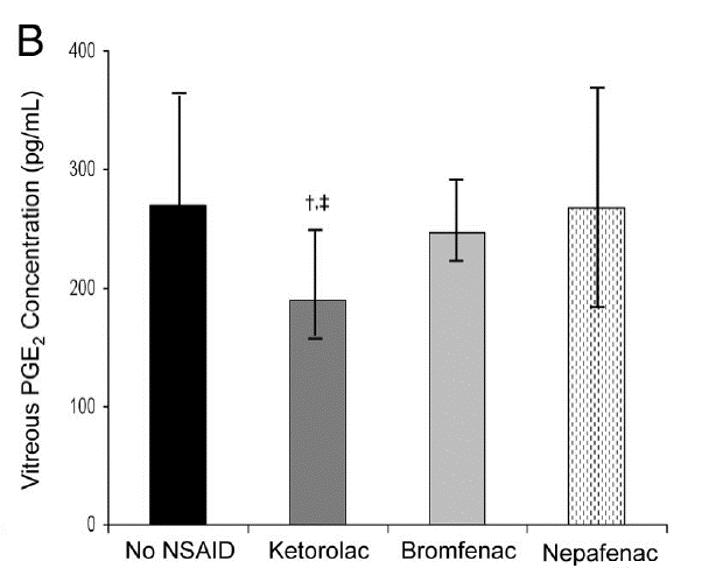
I farmaci antinfiammatori non steroidei (FANS) sono tra i più prescritti per le loro proprietà analgesiche, antipiretiche e antinfiammatorie. Sono infatti dei potenti inibitori degli enzimi cicloossigenasi (COX) poiché riducono la sintesi delle prostaglandine, coinvolte nei processi infiammatori. In oftalmologia, la somministrazione topica di farmaci FANS raggiunge facilmente livelli terapeutici nell’umore acqueo, riducendo la sintesi delle prostaglandine nel corpo ciliare e nell’iride. Tuttavia, tale effetto terapeutico è meno evidente a livello retinico e coroideale e attualmente pochi studi hanno misurato i livelli di FANS nella cavità vitrea umana dopo la somministrazione topica. Heier et all, in uno studio del 2009, hanno misurato i livelli vitreali di farmaco nei pazienti che hanno ricevuto ketorolac 0,4% quattro volte al giorno, bromfenac 0,09% due volte al giorno e nepafenac 0,1% tre volte al giorno nei tre giorni precedenti la vitrectomia. I livelli del farmaco antinfiammatorio non steroideo e dei livelli di PGE2 sono stati determinati tramite campioni di vitreo prelevati all’inizio della procedura chirurgica. I risultati hanno dimostrato che i livelli nel vitreo di ketorolac, bromfenac e amfenac erano rispettivamente 2,8 ng/mL, 0,96 ng/mL e 2,0 ng/mL, ma solo ketorolac ha dimostrato di abbassare i livelli di PGE2 nella cavità vitrea in maniera significativa rispetto al placebo.
Esistono convincenti prove cliniche nella lettera-
24 LA VOCE AICCER 2/2023 CHIRURGIA DELLA CATARATTA
tura peer-reviewed che attestano la capacità dei FANS topici di ridurre l’infiammazione nel postoperatorio di una chirurgia oculare. In studi clinici controllati randomizzati FANS come bromfenac 0,09%, nepafenac 0,1%, diclofenac 0,1%, flurbiprofene 0,03%, indometacina 1% e, ancora, ketorolac 0,5% hanno ampiamente dimostrato la loro capacità antinfiammatoria nel postoperatorio della cataratta.
I farmaci steroidei
La terapia topica con colliri a base di corticosteroidi ha dimostrato l’utilità nella riduzione dell’edema maculare cistoide. Anche i farmaci steroidei sono ampiamente utilizzati nel postoperatorio per ridurre l’infiammazione, pertanto sono stati condotti studi di confronto tra le due classi di farmaci.
I cortisonici perioculari sono stati proposti per il trattamento dell’edema maculare cistoide pseudofachico resistente ai farmaci topici. Diversi studi di confronto tra le iniezioni retrobulbari e subtenoniane non hanno mostrato differenze significative tra le due vie di somministrazione nel miglioramento della vista e l’innalzamento della IOP. L’utilizzo di corticosteroidi intraoculari si avvale sia del trattamento diretto con iniezione in-
travitreale, che tramite sistema di delivery a lento rilascio, come per il desametasone.
Nel caso del desametasone, diversi studi confermano che l’impianto a lento rilascio favorisce in modo significativo la riduzione dell’edema maculare cistoide, ma la necessità di monitoraggio costante, di iniezioni ripetute ed il prezzo elevato ne limitano l’applicazione clinica. Inoltre, il rischio di recidiva dell’edema maculare e di alta pressione intraoculare non può ancora essere evitato. Una buona alternativa è l’utilizzo del triamcinolone acetonide, un corticosteroide sintetico con lunga durata dell’azione antinfiammatoria ed effetto antiVEGF. Inoltre, è di difficile dissoluzione in acqua e si assorbe lentamente nelle applicazioni locali. Sia l’impianto di 0,7 mg di desametasone, come Ozurdex, che l’iniezione intravitreale di 4 mg di triamcinolone sono ugualmente efficaci nell’aumentare la BCVA nei pazienti con edema maculare cistoide a un follow-up di sei mesi; tuttavia, è risultato che l’edema maculare rispondesse più rapidamente e in modo significativamente superiore nel gruppo trattato con triamcinolone intravitreale, con il massimo effetto sulla riduzione dello spessore maculare centrale dopo solo una settimana dall’iniezione. Inoltre, un recente studio (Tariq, 2022) ha confrontato gli effetti visivi e morfologici tra l’iniezione intravitreale di triamcinolone 2 mg e ranibizumab 0,5 mg in pazienti con edema maculare cistoide pseudofachico, rilevando che il triamcinolone ha ottenuto un miglioramento della BCVA e una riduzione crescente dello spessore maculare centrale a partire da due settimane dopo l’iniezione, senza evidente aumento dell’IOP.
FANS e corticosteroidi in combinazione:
ancora più efficacia
Concentrazione media di PGE2 nel vitreo nello studio NSAID. Grafico estratto da Heier JS, et al, Vitreous nonsteroidal antiinflammatory drug concentrations and prostaglandin E2 levels in vitrectomy patients treated with ketorolac 0.4%, bromfenac 0.09%, and nepafenac 0.1%. Retina. 2009 Oct;29(9):1310-3. doi: 10.1097/IAE.0b013e3181b094e6. PMID: 19934822
Nonostante non siano state registrate differenze significative nella riduzione dell’infiammazione intraoculare dopo la chirurgia della cataratta tra le due classi di farmaci, i FANS si sono dimostrati più efficaci nel ristabilire la barriera emato-acqueo, come indicato dal bagliore misurato dalla lampada a fessura o dalla fluorofotometria. Dunque, l’evidenza collettiva suggerita dalla letteratura suggerisce che i FANS topici possono essere usati al posto dei corticosteroidi dopo l’intervento di cataratta o, ancora meglio, in combinazione con essi. A supporto di ciò, infatti, molti studi clinici hanno evidenziato l’effetto sinergico tra FANS e corticosteroidi quando questi vengono somministrati in combinazione.
25 LA VOCE AICCER 2/2023 CHIRURGIA DELLA CATARATTA
TITOLO SEZIONE
Bibliografia


1. Tariq F, Wang Y, Ma B, He Y, Zhang S, Bai L. Efficacy of Intravitreal Injection of Filtered Modified Low-Dose Triamcinolone Acetonide and Ranibizumab on Pseudophakic Cystoid Macular Edema. Front Med (Lausanne). 2022 Feb 16;9:777549. doi: 10.3389/fmed.2022.777549. PMID: 35252233; PMCID: PMC8888519.
2. Heier JS, Awh CC, Busbee BG, Waterbury LD, Daniel P, Stoller GL, Cleary TS. Vitreous nonsteroidal antiinflammatory drug concentrations and prostaglandin E2 levels in vitrectomy patients treated with ketorolac 0.4%, bromfenac 0.09%, and nepafenac 0.1%. Retina. 2009 Oct;29(9):1310-3. doi: 10.1097/IAE.0b013e3181b094e6. PMID: 19934822.

3. Russo A, Costagliola C, Delcassi L, Parmeggiani F, Romano MR, Dell’Omo R, Semeraro F. Topical nonsteroidal antiinflammatory drugs for macular edema. Mediators Inflamm. 2013;2013:476525. doi: 10.1155/2013/476525. Epub 2013 Oct 21. PMID: 24227908; PMCID: PMC3818914.

4. T. Ke, G. Graff, J. M. Spellman, and J. M. Yanni, “Nepafenac, a unique nonsteroidal prodrug with potential utility in the treatment of trauma-induced ocular inflammation: II. In vitro bioactivation and permeation of external ocular barriers,” Inflammation, vol. 24, no. 4, pp. 371–384, 2000

5. F.A. Bucci Jr., L.D. Waterbury, and L.M. Amico, “Prostaglandin E2 inhibition and aqueous concentration of ketorolac 0.4% (acular LS) and nepafenac 0.1% (nevanac) in patients undergoing phacoemulsification,” American Journal of Ophthalmology, vol. 144, no. 1, pp. 146–147, 2007
6. C. Hirneiss, A.S. Neubauer, A. Kampik, and C. Schonfeld, “Comparison of prednisolone 1%, rimexolone 1% and ketorolac tromethamine 0.5% after cataract extraction. A prospective, randomized, double-masked study,” Graefe’s Archive for Clinical and Experimental Ophthalmology, vol. 243, no. 8, pp. 768–773, 2005.


7. A.J. Flach, M.C. Kraff, D.R. Sanders, and L. Tanenbaum, “The quantitative effect of 0.5% ketorolac tromethamine solution and 0.1% dexamethasone sodium phosphate solution on postsurgical blood-aqueous barrier,” Archives of Ophthalmology, vol. 106, no. 4, pp. 480–483, 1988.
8. J.R. Wittpenn, S. Silverstein, J. Heier, K. R. Kenyon, J. D. Hunkeler, and M. Earl, “A randomized, masked comparison of topical ketorolac 0. 4% plus steroid vs steroid alone in low-risk cataract surgery patients,” American Journal of Ophthalmology, vol. 146, no. 4, pp. 554–560, 2008.
9. J.S. Heier, T.M. Topping, W. Baumann, M.S. Dirks, and S. Chern, “Ketorolac versus prednisolone versus combination therapy in the treatment of acute pseudophakic cystoid macular edema,” Ophthalmology, vol. 107, no. 11, pp. 2034–2039, 2000
10. Mylonas G, Georgopoulos M, Malamos P, Georgalas I, Koutsandrea C, Brouzas D, Sacu S, Perisanidis C, Schmidt-Erfurth U; Macula Study Group Vienna. Comparison of Dexamethasone Intravitreal Implant with Conventional Triamcinolone in Patients with Postoperative Cystoid Macular Edema. Curr Eye Res. 2017 Apr;42(4):648-652. doi: 10.1080/02713683.2016.1214968. Epub 2016 Sep 9. PMID: 27612922.

Ulrich Spandau Edizione Italiana a cura di Alfonso Anania
di Stanislao Rizzo
2/2023
Redazione: Strada 4 Milano Fiori, Palazzo Q7 – 20089 Rozzano (MI) Sede operativa: FGE srl − Regione Rivelle 7/F − 14050 Moasca (AT) Tel. 0141 1706694 – Fax 0141 856013 e-mail: info@fgeditore.it − www.fgeditore.it Ordina la tua copia su www.fgeditore.it Trocar Surgery per i chirurghi della cataratta
Prefazione


















www.fidiapharma.it Ketorolac trometamolo 5 mg/ml Cod. 99002543Dep. in data AIFA 01/12/2022 CLASSIFICAZIONE AI FINI DELLA RIMBORSABILITÀ, CLASSIFICAZIONE AI FINI DELLA FORNITURA E PREZZO KOMOREBI “5 mg/ml COLLIRIO, SOLUZIONE” 1 flacone contagocce in LDPE da 10 ml A.I.C. n. 047312018. Classificazione ai fini della rimborsabilità: C. Classificazione ai fini della fornitura: medicinale soggetto a prescrizione medica (RR). Prezzo al pubblico (IVA inclusa) in vigore dal 01/01/2023: € 21,00. PER LA GESTIONE DEL DOLORE E DELL’ INFIAMMAZIONE IN OFTALMOLOGIA
Report Symposium ALCON
In occasione del XXIV Congresso Nazionale AICCER - Associazione Italiana Chirurgia della Cataratta e Refrattiva, un panel di esperti ha fatto il punto sulla condizione di occhio secco pre e postchirurgia e ha presentato un importante progetto relativo al rapporto tra superficie e chirurgia oculare in occasione del simposio, promosso da Alcon, “La superficie oculare e la chirurgia oftalmica: more than meets the eye”.
Al confronto hanno preso parte Edoardo Villani, Professore Associato di Oftalmologia presso l’Università degli Studi di Milano, Dirigente Medico presso Eye Clinic Ospedale San Giuseppe Milano, Carlo Cagini, Professore Associato di Oculistica presso l’Università degli Studi di Perugia e Direttore della struttura complessa Clinica Oculistica presso l’Azienda Ospedaliera di Perugia e Chiara Posarelli, Professoressa Associata di Oculistica presso l’Università di Pisa. Nel corso del suo intervento Edoardo Villani ha presentato il progetto DROPS (Dry Eye Opportunity
Pre and post Surgery), un progetto di narrative review promosso da un board di oculisti chirurghi ed esperti di superficie oculare italiani, insieme ad un gruppo di opinion leader europei e realizzato con il contributo di Alcon. “L’iniziativa è nata dall’esigenza di fare un focus sull’evidenza scientifica relativa alle problematiche della superficie oculare in ambito chirurgico con l’obiettivo di accrescere la consapevolezza su questa tematica. Oggi sappiamo che il rapporto tra superficie oculare e chirurgia oculare
è un rapporto rilevante e complesso. Da una parte le varie tipologie di chirurgia oculare sono in grado di influenzare la superficie oculare e il suo stato di salute. Dall’altra la superficie oculare è in grado di condizionare gli outcome chirurgici. Questa è una consapevolezza che ormai abbiamo maturato sulla base dell’esperienza clinica quotidiana, ed è stata recepita da importanti società scientifiche internazionali come la Society for Clinical Research Sites (SCRS), ad esempio, che ha sviluppato un algoritmo che possa intercettare i pazienti più ad alto rischio per quanto riguarda la superficie oculare”.
E a proposito dei risultati attesi e dei benefici che ne potranno trarre i clinici “Il progetto DROPS ha comportato uno sforzo collegiale durato circa un anno e mezzo e ha coinvolto clinici e ricercatori italiani e alcuni esperti europei. Il primo traguardo sarà la pubblicazione di quattro paper, narrative review che al loro interno conterranno raccomandazioni per la gestione clinica pre, intra e post operatoria della superficie oculare. Da questi lavori c’è la volontà di sviluppare tools che gli specialisti possano utilizzare nella loro attività quotidiana, traendo vantaggi rispetto alla gestione della superficie oculare dei loro pazienti”.
Tra le cause che possono portare problematiche alla superficie oculare troviamo le iniezioni intravitreali. Carlo Cagini ha proposto alcune considerazioni sulle capacità di un sostituto lacrimale a base di Hp guar e acido ialuronico di mitigare questi danni.
dalle aziende 28 LA VOCE AICCER 2/2023
Dry Eye e chirurgia oftalmica, esperti a confronto per fare il punto su come la condizione di Dry Eye incide nel pre e post-chirurgico
“I trattamenti intravitreali possono indurre occhio secco post-operatorio. Situazione che si manifesta maggiormente nei pazienti che avevano già condizioni di occhio secco latente o evidente, che dopo la chirurgia denunciano un fastidio importante. La somministrazione in questa fase di un sostituto lacrimale a base di Hp guar e acido ialuronico, unito alla terapia già prevista, può migliorare in maniera significativa il discomfort che i pazienti riferiscono molto frequentemente durante le visite di follow up”.
La sindrome da occhio secco rappresenta una problematica anche per i pazienti con glaucoma. L’esposizione a lungo termine ai colliri antiglaucoma con conservanti può indurre un’importante problematica della superficie oculare e, quindi, un fallimento della chirurgia filtrante. Si stima che circa il 60%1-3 dei pazienti in terapia cronica per il glaucoma sia affetto da un problema di superficie oculare. E di questi una buona percentuale sviluppa anche un dry eye severo. Quindi in queste condizioni operare un paziente potrebbe notevolmente peggiorare gli outcome della chirurgia.
Chiara Posarelli ha evidenziato quali strategie applicare per migliorare e preparare la superficie

oculare dei pazienti in previsione della chirurgia del glaucoma. “Si può preparare la superficie oculare cercando di ridurre l’infiammazione. Questo può essere fatto riducendo il numero di gocce che i pazienti istillano, privilegiando combinazioni fisse oppure formulazioni senza conservanti, andando anche a somministrare, laddove ve ne sia il tempo, colliri antinfiammatori non steroidei e steroidi da 1 a 4 volte al giorno un mese prima della chirurgia. In questo modo è possibile portare ad un livello di infiammazione più basso per ottenere un miglior successo della chirurgia filtrante”.
Bibliografia
1. Leung EW, Medeiros FA & Weinreb RN (2008): Prevalence of ocular surface disease in glaucoma patients. J Glaucoma 17: 350–355.
2. Skalicky SE, Goldberg I & McCluskey P (2012): Ocular surface disease and quality of life in patients with glaucoma. Am J Ophthalmol 153: 1–9.e2.
3. Stewart WC, Stewart JA & Nelson LA (2011): Ocular surface disease in patients with ocular hypertension and glaucoma. Curr Eye Res 36:391–398.
dalle aziende 29 LA VOCE AICCER 2/2023
Ketorolac trometamolo 5 mg/ml
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE KOMOREBI 5 mg/ml, collirio, soluzione. 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ketorolac trometamolo 5 mg/ml. Eccipiente con effetti noti: Benzalconio cloruro - 0,05 mg/ml. Per l’elenco completo degli eccipienti, vedere paragrafo 6.1. 3. FORMA FARMACEUTICA Collirio, soluzione. Soluzione trasparente, incolore e inodore con pH compreso tra 6,50 e 7,50 e osmolalità compresa tra 280 e 320 mOsm/kg. 4. INFORMAZIONI CLINICHE 4.1 Indicazioni terapeutiche. Komorebi è indicato per: - il trattamento del dolore e dell’infiammazione conseguenti alla chirurgia della cataratta; - l’inibizione della miosi intraoperatoria durante la chirurgia della cataratta; - il sollievo a breve termine della congiuntivite allergica. 4.2 Posologia e modo di somministrazione Posologia Trattamento del dolore e dell’infiammazione conseguenti alla chirurgia della cataratta: la dose raccomandata è 1 goccia 4 volte al giorno per 2-4 settimane. Inibizione della miosi intraoperatoria durante la chirurgia della cataratta: la dose raccomandata è 1 goccia ogni 30 minuti, iniziando la somministrazione 2 ore prima dell’intervento chirurgico, per un totale di 4 gocce. L’ultima goccia deve essere somministrata 30 minuti prima della preparazione chirurgica. Sollievo a breve termine della congiuntivite allergica: la dose raccomandata è 1 goccia 4 volte al giorno per 1-2 settimane. Popolazione pediatrica. La posologia raccomandata è identica alla dose raccomandata per gli adulti. L’efficacia e la sicurezza di questo medicinale non sono state ancora studiate in pazienti pediatrici, di età inferiore ai 14 anni. Popolazione speciale. Anziani, pazienti con insufficienza renale e pazienti con insufficienza epatica. Non sono stati eseguiti studi su questi gruppi di pazienti. Modo di somministrazione. Applicare il collirio goccia a goccia nella dose raccomandata nella sacca congiuntivale dell’occhio da trattare, tirando con attenzione la palpebra inferiore verso il basso e guardando verso l’alto. I pazienti devono essere avvertiti di evitare di toccare l’occhio e le aree circostanti con la punta del contagocce. In caso di utilizzo di Komorebi in concomitanza con altri medicinali oftalmici per uso topico, si deve attendere almeno 5 minuti tra le somministrazioni di ciascun prodotto. Se si dimentica una dose, questa deve essere somministrata appena possibile. Successivamente, il trattamento deve essere seguito come previsto. 4.3 Controindicazioni. Ipersensibilità al principio attivo o a uno qualsiasi degli eccipienti elencati al paragrafo 6.1. È possibile che vi sia una sensibilità crociata con acido acetilsalicilico e altri farmaci antinfiammatori non steroidei. Komorebi è controindicato nei pazienti ipersensibili che hanno precedentemente mostrato sensibilità a questi farmaci. 4.4 Avvertenze speciali e precauzioni di impiego. Komorebi non deve essere utilizzato contemporaneamente alle lenti a contatto. Si consiglia di utilizzare Komorebi con cautela nei pazienti con tendenza emorragica o sottoposti a trattamento anticoagulante. Come per gli altri FANS, l’uso di ketorolac trometamolo collirio, soluzione può ritardare la cicatrizzazione delle ferite corneali, quindi il suo uso nei soggetti predisposti (con lesioni epiteliali persistenti, denervazione della cornea, diabete mellito, sindrome dell’occhio secco severa) deve essere valutato attentamente. L’uso prolungato di FANS può portare ad assottigliamento, erosione, ulcerazione o perforazione della cornea. I FANS topici devono essere utilizzati con cautela in pazienti che sono stati sottoposti a interventi chirurgici oculari complicati, che presentano denervazione della cornea, difetti dell’epitelio corneale, diabete mellito, patologie della superficie oculare (ad es. sindrome dell’occhio secco), artrite reumatoide oppure che sono stati sottoposti a ripetuti interventi chirurgici agli occhi in un breve lasso di tempo, perché possono essere maggiormente esposti al rischio di reazioni avverse a livello corneale che possono compromettere la capacità visiva. L’esperienza post-marketing con i FANS topici indica inoltre che l’uso oltre le 24 ore precedenti all’intervento chirurgico, oppure oltre 14 giorni dopo l’intervento, può aumentare il rischio di insorgenza e gravità di eventi avversi a livello corneale. L’uso concomitante di ketorolac trometamolo collirio, soluzione e dei corticosteroidi per uso topico deve essere attentamente monitorato nei pazienti predisposti alla rottura dell’epitelio corneale, a causa del ritardo nel processo di cicatrizzazione. Ogni ml di Komorebi contiene 0,05 mg di benzalconio cloruro. Il benzalconio cloruro può essere assorbito dalle lenti a contatto morbide e alterarne il colore. Le lenti a contatto devono essere rimosse prima di usare questo medicinale e riapplicate 15 minuti dopo. È stato riportato che il benzalconio cloruro causa irritazione agli occhi, sintomi di secchezza oculare e può influire sul film lacrimale e sulla superficie corneale. Deve essere usato con cautela in pazienti con occhio secco e in pazienti in cui la cornea può essere compromessa. I pazienti devono essere monitorati in caso di uso prolungato.4.5 Interazioni con altri medicinali ed altre forme di interazione. Non sono stati effettuati studi di interazione. Il ketorolac trometamolo collirio, soluzione si è dimostrato ben tollerato quando impiegato in associazione con medicinali oftalmici e sistemici quali antibiotici, sedativi, ialuronidasi e/o anestetici (bupivacaina HCl, lidocaina HCl e tetracaina HCl), betabloccanti, inibitori dell’anidrasi carbonica, miotici, midriatici e cicloplegici. Utilizzare sotto monitoraggio nei pazienti con tendenza alle emorragie o sottoposti a trattamento anticoagulante. L’uso concomitante di farmaci antinfiammatori non-steroidei e corticosteroidi per uso topico può incrementare il rischio di problemi di cicatrizzazione (vedere paragrafo 4.4). 4.6 Fertilità, gravidanza e allattamento. Gravidanza. La sicurezza dell’uso del medicinale in donne in gravidanza non è stata stabilita. I risultati degli studi condotti su animali non hanno evidenziato il rischio di tossicità riproduttiva (vedere il paragrafo 5.3). Ad oggi non esistono studi controllati sull’uso di ketorolac trometamolo collirio, soluzione in donne in gravidanza. Pertanto l’uso del medicinale in queste situazioni deve essere preso in considerazione solo se i benefici superano i rischi. A causa dei rischi noti associati all’uso di FANS durante il terzo trimestre di gravidanza (chiusura prematura del dotto arterioso), il ketorolac trometamolo collirio, soluzione non deve essere utilizzato in questa fase della gravidanza. Allattamento. L’uso di Komorebi non è raccomandato in donne che allattano al seno. Il ketorolac trometamolo viene escreto, dopo somministrazione sistemica, nel latte materno. Fertilità. Gli studi sugli animali non hanno mostrato reazioni avverse sulla fertilità. 4.7 Effetti sulla capacità di guidare veicoli e sull’uso di macchinari. Komorebi non altera la capacità di guidare veicoli e di usare macchinari. Tuttavia, immediatamente dopo la somministrazione, la visione può essere transitoriamente offuscata, pertanto i pazienti non devono guidare o usare macchinari fino a quando non si ristabilisce la normale visione. 4.8 Effetti indesiderati. Gli effetti collaterali sono elencati in base alla classificazione per sistemi e organi e alla frequenza. Le frequenze sono definite come: molto comune (≥1/10), comune (da ≥1/100 a <1/10), non comune (da ≥1/1.000 a <1/100), rara (da ≥1/10.000 a <1/1.000), molto rara (<1/10.000), non nota (la frequenza non può essere definita sulla base dei dati disponibili). Disturbi del sistema immunitario. Comune: reazioni allergiche. Patologie dell’occhio. Molto comune: irritazione oculare (compresa sensazione di bruciore), dolore oculare (compreso dolore pungente). Comune: cheratite superficiale, edema oculare e/o palpebrale, prurito oculare, iperemia congiuntivale, infezione oculare, infiammazione oculare. Non comune: ulcera corneale, infiltrati corneali, offuscamento e/o riduzione della vista, secchezza oculare, irite. Non nota: assottigliamento della cornea, erosione corneale, rottura dell’epitelio o perforazione della cornea. A causa della possibilità di assorbimento sistemico di ketorolac trometamolo collirio, soluzione somministrato per via topica, possono verificarsi, benché raramente, gli effetti collaterali riportati per l’uso sistemico, quali cefalee, sintomi simil-influenzali, nausea, vomito, emorragia e ulcera peptica. Segnalazione delle reazioni avverse sospette. La segnalazione delle reazioni avverse sospette che si verificano dopo l’autorizzazione del medicinale è importante, in quanto permette un monitoraggio continuo del rapporto beneficio/rischio del medicinale. Agli operatori sanitari è richiesto di segnalare qualsiasi reazione avversa sospetta tramite il sistema nazionale di segnalazione all’indirizzo https://www.aifa.gov.it/content/segnalazioni-reazioni-avverse 4.9 Sovradosaggio Non sono stati riportati casi di sovradosaggio con questa forma farmaceutica. 5. PROPRIETÀ FARMACOLOGICHE 5.1 Proprietà farmacodinamiche. Categoria farmacoterapeutica: 15.2.2 Farmaci antinfiammatori non-steroidei. Codice ATC: S01BC05 KETOROLAC. Il ketorolac trometamolo è un antinfiammatorio che mostra attività analgesica, antinfiammatoria e antipiretica quando somministrato per via sistemica. Il meccanismo che induce tali azioni è, in parte, dovuto alla capacità d’inibire la biosintesi delle prostaglandine. La somministrazione oftalmica di ketorolac trometamolo riduce i livelli della prostaglandina E2 nell’umore acqueo. Le prostaglandine inducono un certo tipo di infiammazione oculare, poiché la loro presenza causa vasodilatazione e aumento della permeabilità vascolare, leucotassia, aumento del tono intraoculare e rottura della barriera fluida sangue-umore acqueo. Favorendo la costrizione dello sfintere dell’iride, le prostaglandine sono responsabili della risposta pupillare miotica durante la chirurgia oculare. 5.2 Proprietà farmacocinetiche Assorbimento. L’assorbimento sistemico di ketorolac trometamolo collirio, soluzione dopo somministrazione per via topica non è chiaro, tuttavia le concentrazioni ematiche dopo applicazione per via topica sono minime, rispetto alla somministrazione orale o parenterale. In uno studio sulla tollerabilità con dosi multiple per 21 giorni su volontari sani, solo 1 dei 13 soggetti presentava una quantità valutabile nel plasma (0,021 μg/ml). In un altro gruppo di 13 soggetti, solo 4 presentavano concentrazioni molto basse di ketorolac trometamolo nel plasma (da 0,011 a 0,023 μg/ml) 15 minuti dopo la somministrazione oculare. Quindi, gli elevati livelli di ketorolac trometamolo nell’umore acqueo e i livelli molto bassi o non rilevabili dopo somministrazione oftalmica, suggeriscono che l’uso di ketorolac trometamolo per via oftalmica nel trattamento di patologie oculari determini un assorbimento sistemico molto basso nei pazienti. Distribuzione. La distribuzione del ketorolac trometamolo collirio, soluzione nei tessuti umani e nei fluidi oculari non è ben caratterizzata. Il ketorolac trometamolo attraversa la placenta. Oltre a ciò il ketorolac trometamolo è distribuito nel latte materno anche se a basse concentrazioni. Biotrasformazione. Il destino metabolico del ketorolac trometamolo dopo assorbimento sistemico non è ben stabilito, tuttavia il ketorolac trometamolo viene metabolizzato nel fegato mediante idrossilazione. Il ketorolac trometamolo assorbito per via sistemica viene coniugato con l’acido glucuronico. Eliminazione. Dopo uso orale, intramuscolare o intravenoso, il ketorolac trometamolo e i suoi metaboliti vengono principalmente escreti nelle urine; solo piccole quantità di medicinale e relativi metaboliti vengono escrete con le feci. 5.3 Dati preclinici di sicurezza I dati non-clinici non rivelano rischi particolari per l’uomo, basati sugli studi convenzionali di safety-pharmacology, tossicità a dosi ripetute, genotossicità, potenziale cancerogeno, tossicità della riproduzione e dello sviluppo. Studi relativi alla tossicità acuta, subacuta e cronica di KOMOREBI su animali hanno dimostrato la sicurezza del medicinale. Studi di tossicità riproduttiva hanno evidenziato distocia e aumento della mortalità neonatale nei topi ma solo a dosi eccessive rispetto ai dosaggi terapeutici. La somministrazione di KOMOREBI non è stata irritante per l’occhio del coniglio e non ha mostrato effetti anestetici locali, non ha influenzato la cicatrizzazione delle ferite corneali sperimentali nei conigli, non ha incrementato la diffusibilità di infezioni oculari da Candida albicans, Herpes simplex tipo 1 o Pseudomonas aeruginosa negli stessi animali e sempre nel coniglio sano non ha determinato un aumento della pressione oculare. Studi di tossicità oculare su cani, scimmie e ratti non hanno rivelato evidenza di irritazione locale a concentrazioni fino allo 0,5% di ketorolac trometamolo applicato per via topica. 6. INFORMAZIONI FARMACEUTICHE 6.1 Elenco degli eccipienti Sodio cloruro. Disodio edetato. Benzalconio cloruro. Acqua per preparazioni iniettabili. Acido cloridrico o sodio idrossido per l’aggiustamento del pH. 6.2 Incompatibilità Il benzalconio cloruro non è compatibile con alluminio, tensioattivo anionico, fluoresceina, perossido di idrogeno, idrossipropilmetilcellulosa, composti dello iodio, lanolina, nitrati, tensioattivi non ionici altamente concentrati, permanganati, proteine, salicilati, sali d’argento, sulfamidici, ossido di zinco, alcune mescole di gomma, alcuni composti plastici e lenti a contatto morbide. L’acqua per preparazioni iniettabili non è compatibile con sostanze che idrolizzano facilmente, metalli alcalini e rispettivi ossidi, diversi acetati di sali anidri e alcuni materiali organici. 6.3 Periodo di validità 30 mesi. Dopo prima apertura: 28 giorni. 6.4 Precauzioni particolari per la conservazione Non conservare a temperatura superiore a 25ºC. Tenere il flacone ben chiuso. Conservare il flacone nella confezione originale, per proteggere il medicinale dalla luce e dall’umidità. Tenere fuori dalla vista e dalla portata dei bambini. 6.5 Natura e contenuto del contenitore. Komorebi collirio viene fornito in un flacone di polietilene a bassa densità da 10 ml, con punta contagocce sigillata in polietilene a bassa densità e tappo di polietilene ad alta densità. Il tutto è precedentemente sterilizzato con raggi gamma. Una volta riempiti, i flaconi vengono confezionati in scatole di cartone debitamente stampate, insieme al rispettivo foglio illustrativo. 6.6 Precauzioni particolari per lo smaltimento e la manipolazione. Il medicinale non utilizzato e i rifiuti derivati da tale medicinale devono essere smaltiti in conformità alla normativa locale vigente. Aprire il tappo del contenitore e premerlo delicatamente, erogando il liquido goccia a goccia nel dosaggio raccomandato. 7. TITOLARE DELL’AUTORIZZAZIONE ALL’IMMISSIONE IN COMMERCIO Fidia Farmaceutici S.p.A., Via Ponte della Fabbrica, 3/A - 35031 Abano Terme (PD), Italia. 8. NUMERO(I) DELL’AUTORIZZAZIONE ALL’IMMISSIONE IN COMMERCIO A.I.C. n. 047312018 - “5 MG/ML COLLIRIO, SOLUZIONE” 1 FLACONE CONTAGOCCE IN LDPE DA 10 ML. 9. DATA DELLA PRIMA AUTORIZZAZIONE/ RINNOVO DELL’AUTORIZZAZIONE Determina AAM/A.I.C. n. 232/2019 del 10 dicembre 2019. 10. DATA DI REVISIONE DEL TESTO 12/2021. CLASSIFICAZIONE AI FINI DELLA RIMBORSABILITÀ, CLASSIFICAZIONE AI FINI DELLA FORNITURA E PREZZO KOMOREBI “5 MG/ML COLLIRIO, SOLUZIONE” 1 flacone contagocce in LDPE da 10 ml A.I.C. n. 047312018. Classificazione ai fini della rimborsabilità: C. Classificazione ai fini della fornitura: medicinale soggetto a prescrizione medica (RR). Prezzo al pubblico (IVA inclusa) in vigore dal 01/01/2023: € 21,00

PER LA GESTIONE DELL’INFIAMMAZIONE IN OFTALMOLOGIA

Cod. 99002543Dep. AIFA in data 01/12/2022
AGE-RELATED MACULAR DEGENERATION


Presidente
Marcella Nebbioso (Roma)
Vice presidente
Emilia Gallo (Catania)
Segretario scientifico

Maria Rosaria Franco (Lecce)
Sponsor management
Patrizia Costanzo
Coordinamento segreteria on-site
Motus Animi
Consiglieri
Federico Bartolomei (Bologna)
Rocco Di Lorenzo (Palermo)
Luigi Donato (Messina)
Federica Franzone (Roma)
Paolo Giuseppe Limoli (Milano)
Marco Ulisse Morales (Padova)
Erika Rigoni (Latina)
Sergio Zaccaria Scalinci (Bologna)
Lucia Scorolli (Bologna)
Antonella Sidoti (Messina)
Gianfrancesco Villani (Verona)
Enzo Maria Vingolo (Roma)
Updates in ambito riabilitativo e clinico-terapeutico XXII CONGRESSO NAZIONALE DI IPOVISIONE www.lowvisionacademy.org Segreteria organizzativa info@fgeditore.it SAVE THE DATE
settembre
LECCE HILTON GARDEN HOTEL Via Cosimo De Giorgi, 62 20 CREDITI ECM Acquisibili tramite corso FAD ECM
29-30
2023














SCOPRI PERCHÉ È IMPORTANTE CONTROLLARE GLI OCCHI SIN DAI PRIMI ANNI DI VITA! 10/10 9/10 8/10 Lions Clubs International MULTIDISTRETTO 108 - ITALY Campagna di prevenzione dell’ambliopia INIZIATIVA PROMOSSA DA Con il patrocinio di Una iniziativa Lions Clubs International MULTIDISTRETTO 108 ITALY LA VISIONE NEL istruzioniBAMBINO: per l’uso Manuale pratico per genitori consapevoli Puoi richiedere n. 50 copie gratuite da mettere a disposizione dei tuoi pazienti in sala d’attesa Con il sostegno di Richiedi gli opuscoli a: info@fgeditore.it ADERISCI ANCHE TU! www.sightforkids.it La soluzione oftalmica per la gestione della progressione miopica





























































































