
Curso continuo de actualización en Pediatría CCAP
Volumen 23 Número 2 Mayo - Agosto 2024




Curso continuo de actualización en Pediatría CCAP
Volumen 23 Número 2 Mayo - Agosto 2024


Junta Directiva Nacional 2024 - 2026
Presidente
Vicepresidente
Secretario
Vocal
Vocal
Vocal
Vocal
Vocal
Vocal
Vocal
Fiscal
Vocal Representante de Capítulos
Expresidente
Dra. Eliana Zemanate Pediatra Intensivista (Editora)
Dra. Nury Mancilla Pediatra Neuróloga
Dr. Víctor Mora Pediatra
Dr. Mauricio Javier Guerrero Román
Dra. Eliana Zemanate Zúñiga
Dr. Alberto José Esmeral Ojeda
Dra. Claudia Patricia Beltrán Arroyave
Dr. Jerónimo Zuluaga Vargas
Dra. Ángela María Giraldo Mejía
Dr. Víctor Manuel Mora Bautista
Dra. Liliam María Macías Lara
Dr. Mauricio Hernández Cadena
Dr. Iván Alejandro Villalobos Cano
Dra. Iliana Francineth Curiel Arizmendi
Dra. Nury Isabel Mancilla Gómez
Dra. Marcela María Fama Pereira
Comité Editorial
Dr. Mauricio Fernández Pediatra Intensivista (Editor Ejecutivo)
Dr. Jürg Niederbacher Pediatra Neumólogo
Sociedad Colombiana de Pediatría www.scp.com.co
Subdirección de Programas Dirigidos al Pediatra
Calle 83 n.o 16A-44, Oficina 701
Edificio Cima. Bogotá, D.C.
Teléfonos: (601) 6495352 - 7464706/07 precop@scp.com.co
Producción editorial
Grupo Distribuna Carrera 9 B # 117 A-05
Barrio Santa Bárbara Central Bogotá, D.C., Colombia
Teléfonos: (571) 6202294 - 2158335 (571) 2132379 www.libreriamedica.com
La circuncisión, realidades actuales. Mitos y realidades de la circuncisión neonatal
Francisco Javier Mejía Sarasti, MD
Ana María López Londoño, MD
Infección por citomegalovirus congénito. Enfoque práctico para el pediatra
Hernando Pinzón Redondo, MD
Sady David Roa Valdelamar, MD
María José Daniels García, MD
Paola Andrea Manjarrés Figueredo, MD
Ana Isabel Hernández Villadiego, MD
Síndrome del macrófago activado: desafíos actuales para el diagnóstico y enfoque del tratamiento
Cristina Del Carmen Muñoz Otero, MD
Carlota Valentina Ovalle Villadiego, MD
María Clara Vigna De La Hoz, MD
Valeria Vásquez Amell, MD
Estrategias para comprender y tratar la ansiedad en niños, niñas y adolescentes
Adolfo Álvarez Montañez, MD
Mauricio Guerrero Román, MD
Gennys Gutiérrez Ramírez, MD
Mónica Holguín Barrera, MD
Paula Herrera Revollo, MD
Estrategias para el abordaje integral de la salud oral en la infancia
Jorge Mario Luján Pinzón, MD
María Camila Niebles Ramírez, MD
Mauricio Guerrero Román, MD
Jaime Plazas Román, MD
Francisco Javier Mejía Sarasti, MD1
Ana María López Londoño, MD2
Para comenzar este artículo, se deben recordar apartes de la historia de la cirugía más antigua del mundo, que incluso se remonta a más de 15.000 años a. C., cuando en Egipto se realizaba la circuncisión, lo cual está evidenciado en representaciones gráficas y en momias bien conservadas de dicha cultura. También en la cultura católica se recuerda la circuncisión de Jesús, la cual según el rito judío se hizo a los 8 días, como lo ordenaba la ley de Abraham. Entonces se debe revisar por qué Abraham se circuncidó. Dicen las escrituras del Antiguo Testamento que Abraham se circuncidó a sí mismo y dejó claro que todos aquellos que estuvieran en su casa y, por ende, los elegidos de Israel deberían hacerlo como un mandato de Dios. Y de allí entonces se ubica el momento histórico: casi 2000 años a. C. nació Abraham y, según el relato del Génesis, solo a los 75 años de vida comenzó su trabajo profético y tuvo a su primer hijo a los 90 años, Isaac.
Para esa época, la religión era el motivo para reglamentar todo. Se puede suponer, por ejemplo, que los cerdos de la Antigüedad
tenían tal riesgo de tener cisticercosis y otras enfermedades por las cuales prohibían su consumo, debido a la costumbre de comer la carne cruda o poco cocida, y es sabido que la carne de cerdo requiere cocciones mayores que la de res y de pollo; entonces, se puede llegar a pensar que con esta ley del Antiguo Testamento pudieron cuidar a la población.
De regreso a Abraham, como ya se mencionó, tenía una edad avanzada cuando recibió la orden de establecer su vida de profeta, y él no estaba circuncidado; debía llenar la tierra con su descendencia junto con su esposa Sara, también anciana y estéril. Es posible que hubiesen tenido dificultades con el prepucio, razón por la que pudo haber decidido hacerse la circuncisión, que es un procedimiento muy molesto y doloroso en las personas mayores, y ante ese hecho pudo haber decidido que sus hijos y su estirpe no pasaran por la dificultad, dolor y malestar que él sufrió. ¿Acaso de ese evento personal, posiblemente muy molesto y doloroso, surgió la decisión de volverlo ley de Dios? Es una teoría para tener en cuenta y se debe agregar en este momento que ese es un motivo de consulta usual en cirugía pediátrica:
1. Cirujano pediátrico, Torre Médica Clínica Rosario Tesoro, Universidad de Antioquia. Medellín, Colombia.
2. Residente de segundo año, Universidad CES. Medellín, Colombia.
el padre que es sometido a la circuncisión de adulto lleva a su hijo para saber qué puede hacer al respecto, porque no desea que su hijo pase por ello.
Los judíos, descendientes de Abraham, tienen el rito por ley de hacer la circuncisión, pero también los musulmanes tienen a Abraham como padre de su religión y, entonces, también tienen dicho rito. ¿Pero entonces por qué los cristianos no se hacen la circuncisión como rito, ya que provienen de la misma estirpe? Una vez Jesús fue crucificado, los apóstoles habían recibido la orden de regar sus enseñanzas y convertir a los gentiles (que para ellos eran todos aquellos no judíos y, por tanto, no circuncidados) al cristianismo. Al parecer, en el Nuevo Testamento queda claro que hubo una discusión sobre si debían o no ser circuncidados, de lo que se deriva otra suposición: si tenían que convencer a los gentiles de convertirse al cristianismo, y esto implicaba la circuncisión, es posible que algunos decidieran no optar por ello pensando en el gran dolor de la circuncisión adulta. Fue entonces San Pablo, que en ese entonces solo era Pablo de Tarso, quien convenció a los apóstoles en el Concilio de Jerusalén de no obligar a la circuncisión, y considero que fue un éxito en el proceso, porque si no, la conversión sería intensamente dolorosa y generaría el rechazo de más de un hombre.
En Colombia, el conocimiento médico surgió primero por la relación convento-hospital, que enmarcaba la salud de la colonia española, pero luego de la independencia aparecieron el apoyo y conocimientos de los oficios como se daba en Francia; de allí que, para la segunda mitad del siglo XIX, los jóvenes se formaran en Europa para venir a expandir su profesión y formar universidades. Se debe recordar que en Europa hubo un segregacionismo intenso contra los judíos y este se trasladó hasta el proceso nazi a mediados del siglo XX. Entonces ser circuncidado casi era lo mismo que ser judío y eso podría traer dificultades. En la Europa que enseñó la academia y la medicina,
la circuncisión era un estigma, razón por la que posiblemente Latinoamérica esté entre las zonas geográficas con menos incidencia de circuncisión del mundo.
En Estados Unidos, la circuncisión es extensamente recomendada desde que fuera extendida como una práctica de prevención de enfermedades, y para la actualidad, es sabido que ese país es el segundo lugar con más población judía después de Israel. Por ello, la estadística confirma que más del 60 % de la población estadounidense y, en algunas partes de ese extenso país, hasta el 80 % tiene la circuncisión en los primeros años de su vida. En la actualidad, hay una disminución en las estadísticas estadounidenses de circuncisión neonatal, posiblemente porque los inmigrantes no acostumbrados a esta estrategia de cuidado de la salud no optan por ella, pero también hay un crecimiento en la solicitud de la circuncisión de la población que comienza la vida sexual y un deseo por parte de la población femenina de que sus parejas sean hombres circuncidados, como reportan en el portal www.urologicalcare.com
Todas estas anotaciones históricas y actuales, que para algún lector podrán parecer exageradas, pero que para otras podrán parecer interesantes, son la base de algunas de las ideas que se exponen en este artículo.
He estado practicando la cirugía pediátrica desde hace más de 20 años, y en nuestro medio, la circuncisión ha sido recomendada como un procedimiento que se le realiza a los niños cuando la necesitan. De allí surge una de las primeras preguntas: ¿cuándo se necesita la circuncisión? Para unos pediatras es después del primer año; para otros, el deseo es esperar a que el niño deje el pañal; otros, luego de las publicaciones de autismo asociado a los procedimientos anestésicos, decidieron diferirla para después de los 4 años, y para muchos, solo si hay dolor, inflamación o algún otro síntoma atribuible al prepucio cerrado. Esto hizo que muchos hombres fueran circuncidados en la
adolescencia o al principio de la edad adulta, cuando es un procedimiento intensamente molesto, principalmente mediado por las erecciones y el hecho de que es un órgano colgante y de mucho mayor tamaño a esa edad, con lo cual el dolor y la inflamación son mucho más graves que en los niños.
FISIOPATOLOGÍA E HISTOLOGÍA DEL PREPUCIO
Son relativamente pocos los datos estudiados de especímenes del prepucio, ya que la circuncisión suele hacerse en un tejido que, más allá de estar cicatrizado, no tiene realmente alteraciones que ameriten estudios anatomopatológicos en los pacientes. Pero se hizo una valoración histológica del prepucio comparándolo desde el periodo neonatal hasta la edad prepuberal y dicha valoración demostró que las fibras de colágeno tipo I necesarias para la cicatrización tienen tendencia a disminuir con la edad, y el periodo neonatal es en el cual se encontraban más fibras de este tipo. Además, se observó que había menos fibras nerviosas y los vasos sanguíneos eran más delgados, y por ello podría explicarse el hecho observado de una menor respuesta inflamatoria y una mejor evolución luego de la circuncisión de los niños más pequeños. Como se ha constatado en la práctica quirúrgica, la circuncisión es mucho más dolorosa y traumática cuanto mayor sea la edad del paciente.
El papel del prepucio en el recién nacido es cuidar el glande para que este no se lastime ni se deteriore. Podría considerarse de vital importancia para el mantenimiento de las especies de los mamíferos en la jungla, pues el trauma del glande podría llevar a la muerte por imposibilidad para la micción, o de otra parte a dificultades en la procreación si queda afectado el órgano genital para engendrar la especie. Sin embargo, para el bebé humano, este riesgo es de mínimo suceso, la gran mayoría de los humanos con acceso a la decisión de la
circuncisión están bajo un sinnúmero de cuidados de sus genitales y no se tiene ese temor, con o sin prepucio.
Tal vez este sea el punto de partida para el análisis y es que aún puede haber algunas recomendaciones en el vulgo sobre la retracción del prepucio del niño pequeño. El prepucio al nacer está en íntimo contacto con el glande y el proceso de descamación de la piel interna del prepucio y la acumulación del esmegma hacen la labor de separación y liberación del glande de una forma natural con el paso de los años. Un poco jocosamente, le digo a los padres que nunca se ha visto a una mamá gorila retrayendo el pene de un pequeño gorila en la jungla, con el fin de enfatizar en que es un proceso que está a cargo de la madre naturaleza y no de la madre biológica. La retracción del prepucio debe ser absolutamente ligera y tenue para limpiar las secreciones que salgan espontáneamente y muy posiblemente muchas de las circuncisiones que se deben hacer en niños mayores proceden del evento traumático de una retracción brusca hecha por cuidadores que buscan “evitar la circuncisión”. Cuando un niño es sometido a tracciones recurrentes donde se presentan pequeñas heridas, estas harán un proceso de cicatrización que confluye en el centro del prepucio y cierran el mismo; de esta manera, una cicatriz circular del prepucio será una indicación absoluta para una circuncisión en cualquier momento de la vida que esta sea detectada.
El baño de los niños debe incluir el uso de abundante agua y la retracción mínima necesaria; puede usarse agua jabonosa, pero parece no estar indicado el uso exclusivo de jabón en el pene, ya que restos de este pueden acumularse y generar irritaciones molestas y generadoras de síntomas que también lleven a la circuncisión por balanitis recurrentes. La retracción del prepucio puede suceder en diferentes
momentos del desarrollo de los niños, no hay una edad a la que se pueda señalar que este evento sucedió o no. Algunos han escrito que esto debe suceder en el primer año, otros que alrededor de los 4 años y hay quienes escriben que la cobertura del glande por el prepucio puede estar siendo fisiológica incluso hasta los 17 años en un 1 % de casos. Así que decir que una edad es la indicada para decidir la circuncisión está lejos de ceñirse a la realidad, es más bien la situación del paciente la que se debe considerar para decidir la circuncisión.
Se ha recomendado el uso de esteroides para el manejo de la fimosis en los niños escolares, y se han hecho múltiples estudios usando diferentes tipos de esteroides, como hidrocortisona, triamcinolona, entre otros, y con variados tiempos de uso: 4, 6, 8 y hasta 12 semanas. No se ha discutido tal vez de forma significativa el hecho de que los esteroides tópicos generan atrofia de la piel y los dermatólogos son muy prudentes en su uso, incluso ante situaciones posquirúrgicas con afección importante de la piel que podría ameritarlos. Estos estudios con esteroides tópicos muestran que son útiles para evitar un 35 % de las circuncisiones, pero otros han mostrado que la recaída después del uso de los esteroides no se ha medido y podría ser menos eficiente aún. El uso de esteroides hasta por 12 semanas mostró que en alrededor de un 60 % de los casos se descubrió el glande, pero es sabido que en muchos de esos niños posteriormente se vuelve a cerrar, por lo que requieren una cirugía más tardía y posiblemente más molesta.
Es una discusión de nunca acabar. Esta es una sentencia que definitivamente determina qué hacer al respecto. Y en el mundo entero hay una gran discusión en la consideración de la circuncisión neonatal frente a la circuncisión del paciente según la aparición de síntomas o
en edad de autodeterminación. La Academia Estadounidense de Pediatría ha generado al menos dos artículos de revisión y recomendaciones acerca del tema, y en el último de ellos dice textualmente: “La evaluación de la información actual indica que los beneficios para la salud de la circuncisión masculina del recién nacido son mayores que sus riesgos, y se justifica el acceso a este procedimiento para las familias que lo elijan. Se identificaron beneficios específicos de la circuncisión masculina para prevenir las infecciones del tracto urinario, la adquisición del VIH, la transmisión de algunas infecciones de transmisión sexual y el cáncer de pene (…). La circuncisión masculina no afecta negativamente a la función o sensibilidad sexual del pene ni la satisfacción sexual (…). Es imprescindible que las personas que practiquen la circuncisión utilicen técnicas estériles y un tratamiento eficaz del dolor (…). Los padres deben recibir la información necesaria para tomar la decisión libremente ceñidos a sus creencias y consideraciones culturales.”.
Si se consultan artículos de Canadá o del Norte de Europa, la conducta es más expectante y la discusión a propósito del tema ha sido en ocasiones de alto calibre y tenor. En una revisión presentada por médicos australianos, Morris y colaboradores hicieron una valoración ética del tema y describen que aquellos que están en contra de la circuncisión en la infancia generalmente tienen argumentos emotivos y lejos de un soporte científico. En dicho artículo hay una tabla que se comparte en esta publicación, con algunas modificaciones que permitan al lector de nuestra latitud entender mejor algunos aspectos ( Tabla 1).
Morris y colaboradores cuentan que: “En 2007, la destacada revista británica BMJ publicó dos breves artículos “cara a cara” en los que se debatía la circuncisión neonatal (CN). En el primero, el Dr. Geoff Hinchley, médico de urgencias, argumentó en contra de la circuncisión infantil de forma emotiva, unilateral y basada en falacias. En el segundo, se refirió
Tabla 1. Comparación de beneficios entre la circuncisión neonatal y la postergada hasta la edad de autodeterminación
Circuncisión neonatal/infantil
Procedimiento simple en manos entrenadas
Rápido, demora pocos minutos
Costos menores
Mínimos eventos adversos (0,4 %)
Cualquier sangrado es mínimo y para fácil
Con mínima manipulación
No necesita suturas
Conveniente porque el niño duerme más
Anestesia local hasta los 9 meses aprox.
Herida sana en menos de 2 semanas
Aspecto estético más controlado
Sin efectos psicológicos
Efecto inmediato en el control de ITU
Da una salud óptima toda la vida
Relación beneficios-riesgo de 100:1
Diferida a edad de autodeterminación
Procedimiento más complejo
Demora al menos 30 minutos
Suele ser más costoso
Más frecuentes efectos adversos (4 %-8 %)
Sangrado que amerite intervenir es más frecuente
Mayor manipulación
Se necesitan suturas
Inconveniente la incapacidad laboral o estudiantil
Anestesia general
Malestar de la herida por más tiempo
Se pueden ver saltos de suturas o requerir grandes resecciones del prepucio
Puede haber efectos psicológicos
Beneficios solo después de la intervención
Difieren los beneficios solo hasta después de la autodeterminación
Aumentan los riesgos, si se presentan problemas, exceden los beneficios
ITU: infección del tracto urinario. Modificada de: Morris B, et al. Cureus. 2024;16(2):e54772.
dos veces a la CN como “mutilación genital masculina”, un estudio desacreditado en el que se afirmaba que la circuncisión infantil provoca “una reducción de la sensibilidad del pene en la edad adulta para todos”, que la CN se realiza “a menudo sin anestesia”, y que no proporciona “ningún beneficio médico”. La Dra. Kirsten Patrick argumentó a favor de la práctica de la CN sobre la base de la “reciente fuerte evidencia” de que es “médicamente beneficioso” y “si es realizado de manera competente, la CN conlleva poco riesgo”, con el dolor “si se hace bajo anestesia local es comparable al de una inyección de inmunización, que también conlleva riesgos.”. Algunos han llegado a decir que la utilidad demostrada por la circuncisión tanto en la prevención de situaciones de salud en la infancia como en problemas relacionados
con el prepucio y las infecciones de transmisión sexual a mayor edad, como la infección por VIH, podría llegar a inclinar la balanza de tal forma que impedir la circuncisión infantil sería una falta a la ética.
Para algunos de los que debaten la utilidad de la CN, la referencia a las complicaciones de la circuncisión hace parte del arsenal de elementos para debatir, pero las publicaciones al respecto son muy significativas: eventos graves como la amputación del pene suelen ser menores, de 1 en 4 millones, y se han descrito en situaciones de circuncisiones rituales, principalmente en África. La frecuencia de eventos adversos para la circuncisión es 20 veces mayor en niños entre 1 y 10 años y 10 veces mayor en mayores de 10 años. El Dr. Khan, en el Reino
Unido, encontró que con el uso del dispositivo de Circumplast® para la circuncisión en 1000 casos, los eventos adversos fueron del 7 % en menores de 3 meses y del 14 % en mayores de dicha edad, lo que sugiere que la técnica en los primeros meses es más segura. Los eventos observados fueron: sangrado posoperatorio (1 %), adherencias prepuciales (1 %), pene atrapado (0,6 %), reintervención (0,7 %) y retención urinaria (0,01 %). No hubo ningún caso de parafimosis por el dispositivo que se ha encontrado en otros dispositivos similares de un diseño diferente hasta en un 17 %, lo que ha generado el rediseño de este dispositivo.
Otro de los argumentos para evitar la circuncisión se refiere a la satisfacción o el desempeño sexual. En la literatura se encuentran numerosas demostraciones científicas que descartan este hecho. La revista Sexual Medicine en 2020 publicó una revisión sistemática en la que se incluyeron medidas fisiológicas, análisis de la ubicación de los receptores sensoriales y metaanálisis de la disfunción sexual, y “concluyeron que la circuncisión, neonatal, infantil o del adulto, tiene efectos adversos mínimos o nulos sobre las funciones, la sensación, la satisfacción y el placer sexuales”.
Hay autores que han hecho una analogía con las vacunas. Con respecto a la circuncisión neonatal, esta última suele ser realizada una única vez, mientras que la inmunización requiere de repetición de dosis para lograr el objetivo de prevenir la enfermedad. Está estipulado que se requieren 39 circuncisiones para evitar una infección urinaria, mientras que se necesitan 50 vacunas de influenza para evitar un caso de esta. En cuanto al dolor y el requerimiento de analgésicos después del evento, estos son incluso semejantes, ya que el niño en cualquiera de las dos situaciones suele recibir un par de días de medicamentos como el acetaminofén para el manejo de sus síntomas asociados como dolor, febrícula y malestar general.
Tobías Hainz, de la Universidad de Hannover, Alemania, publicó en el 2005 un artículo en Bioética, llamado: The Enhancement of Children versus Circumcision: A Case of Double Moral Standards? y hace de nuevo un acercamiento de la circuncisión al símil de las vacunas, en el que menciona: “tal vez la circuncisión esté al mismo nivel que otras intervenciones que alteran la naturaleza de los humanos, pero que suelen considerarse permisibles o incluso recomendables, u obligatorias, como la vacunación (...)” y agrega: “ la circuncisión, éticamente hablando, por razones religiosas sería inaceptable si la forma de realizarla pusiera en riesgo a los niños, como algunas técnicas de succión utilizadas (…)”; en este punto se refiere a algunas tradiciones judías donde el rabino completa la resección del prepucio con su boca.
En cuanto al control de enfermedades de transmisión sexual, está claro que el uso del preservativo es un buen método, pero si a esto se le agrega que el hombre esté circuncidado, el valor de protección es aditivo. Las vacunas contra VPH no cubren todos los serotipos y está demostrado que dicha vacuna previene la infección del 28 %-34 %, que es un valor semejante al logrado por la circuncisión masculina, entre el 33 % y el 34 %.
La sugerencia de la AAP que indica que la CN supera por mucho sus riesgos y, por tanto, debe recomendarse está orientada a facilitar la decisión de los padres para optar por la circuncisión. Los detractores sugieren que esta decisión sea tomada por el paciente mayor de edad o cuando tenga libre autodeterminación; si esto fuera la acción más común, se perderían muchos de los beneficios que puede traer la circuncisión neonatal, ya que el CDC ha demostrado que la cantidad de adolescentes que cursan el último año de colegio y tienen actividad sexual que incluye el coito es más de la mitad y hasta una quinta parte habrá tenido más de cuatro compañeros sexuales. La Tabla 2 es una modificación
Tabla 2. Condición médica, reducción de riesgo y cantidad de casos prevenibles Condición médica
mayor de 18 años
riesgo de infección por VIH
Enfermedad de transmisión sexual, alto control*
*Úlcera genital, sífilis, tricomona y cancroide. **Micoplasma genital y herpes tipo 2. Modificada de: Modificada de: Morris B, et al. Cureus. 2024;16(2):e54772.
de la publicada por el metaanálisis australiano en la que se observan las referencias de este artículo y expresa las situaciones de salud que cambian por la realización de la CN, así como el riesgo de que estas sucedan y de allí el número de pacientes que se benefician con la CN; para esto usaron los datos de la recomendación realizada por el CDC y sus estadísticas. Según su análisis, más de 1 millón de personas se ven beneficiadas con la CN cada año.
Si no todos los niños requieren la circuncisión, ¿será que algunos sí tienen clara necesidad de ella? Para la infancia, lo que está más claro como utilidad de la circuncisión es el hecho de prevenir las infecciones urinarias en los primeros dos años de vida. Se sabe que, si un niño varón tiene una infección urinaria, se deberían hacer estudios de extensión, y no tener estas podría ser muy beneficioso.
Los artículos han demostrado que los niños que nacen con hidronefrosis de cualquier etiología se benefician de la circuncisión; desde el punto
de vista práctico, estos niños pueden necesitar una cistouretrografía miccional y dicho estudio radiológico es mucho más benevolente y fácil en niños circuncidados que en aquellos que no lo están. Además, se demostró en un metaanálisis publicado por Chan y colaboradores en el Journal of Pediatric Urology de 2023 que los niños con cualquier hidronefrosis tienen un riesgo menor de infección urinaria si son circuncidados (3,9 %) frente a los no circuncidados (16 %). Si se habla de niños con reflujo vesicoureteral (RVU), se encontró que había 518 niños circuncidados y 851 no circuncidados; en el grupo con circuncisión, el 18 % experimentó una infección de tracto urinario (ITU), mientras que los no circuncidados tuvieron 38,8 % de ITU. En niños con valvas de uretra posterior, los valores fueron más impresionantes: hubo 19 % de ITU en los niños circuncidados y casi 50 % de ITU en los no circuncidados. Una de las estrategias utilizadas para evitar las ITU en niños con RVU ha sido la administración de antibiótico profiláctico, y se revisó el uso de esta en relación con tener o no tener circuncisión, y se observó que el
efecto era aditivo; es decir, los niños con RVU y profilaxis antibiótica que eran circuncidados tuvieron 8 % de eventos de infección urinaria, mientras que los no circuncidados con profilaxis tuvieron 35 %. Esto quiere decir que los niños que nacen con hidronefrosis deberían estar circuncidados como estrategia de cuidado y prevención del daño renal. Un metaanálisis publicado desde 2005 en Australia menciona que el riesgo de sufrir una infección urinaria en el primer año de vida es del 1 % y mostró que, acumulando más de 400 000 niños, aquellos con infecciones urinarias recurrentes o con RVU que se sometían a la circuncisión neonatal tenían menor riesgo de ITU en un 10 %-30 %, además de que eventos adversos como la infección o el sangrado no superaron el 2 %. Por esto, dichos autores recomiendan siempre la circuncisión neonatal.
CIRCUNCISIÓN: DETALLES
INTERESANTES PARA UN PEDIATRA
No voy a hacer una descripción detallada de técnica quirúrgica, pues no es el objetivo de este artículo y del público usual de esta publicación, pero sí quiero hacer algunas anotaciones importantes que definen lo que se puede o no hacer.
No se podría saber cuándo se hizo la primera circuncisión en Colombia, pero siempre ha sido un procedimiento bajo anestesia general. Esta ha sido por siempre la limitación inicial para definir la edad a la cual se realiza la misma. Nuestra técnica usual consiste en un procedimiento en el cual se libera el prepucio del glande retirando todo el esmegma y dejando libre el surco balanoprepucial, luego se hace una incisión de la piel externa y una disección de la parte intermedia donde está el tejido vascularizado, generalmente haciendo uso de electrofulguración monopolar o bipolar; se logra la hemostasia a dicho nivel y luego se reseca la piel interna. Se procede a una sutura que para algunos especialistas es de
puntos separados y otros de puntos continuos para lograr la reconstrucción de los tejidos. La cantidad de resección de tejido tiene que ver con los hallazgos durante la cirugía de la piel afectada y luego con el deseo médico o familiar, pero siempre se debe tener en cuenta no dejar piel estrecha o dañada que pueda generar la necesidad posterior de una nueva intervención. El prepucio puede quedar detrás del surco balanoprepucial o cubriendo el glande. Como se puede inferir de la descripción de la técnica usual (sabiendo que muchos colegas podrán tener algunas variaciones propias de su experiencia o formación), esta forma de hacer la circuncisión obliga una anestesia general para el paciente, ya que la disección descrita no puede hacerse de forma segura si el niño llegara a moverse. Debido a esto, en nuestro medio, la discusión de la circuncisión neonatal o en los primeros meses de vida prácticamente no existió, ya que no se podía realizar.
Pido disculpas si hago una apelación en primera persona en este artículo, pero creo que la situación que me llevó a lo que quiero compartir a continuación con ustedes así lo amerita. En los últimos años mi consulta ha cambiado y me he enfrentado cada vez más a la solicitud de la circuncisión de los niños por motivos que anteriormente no me eran solicitados. Cuando un padre o una madre tienen acceso a un servicio médico privado, los motivos de consulta pueden cambiar y la influencia estadounidense de nuestra cultura en las últimas décadas es innegable. De allí surgió que alguna vez una madre llevara a su hijo de 3 meses a mi consultorio, y contaba que ella decidió que su hijo tenía que ser circuncidado y que le habían realizado la circuncisión con 1 mes de vida. Al interrogarle sobre la forma del procedimiento contó que la intervención la hizo un urólogo de adultos con anestesia general de forma ambulatoria. Allí surgieron las primeras alertas: ¿cómo era posible que un niño fuera sometido a una cirugía con anestesia general antes de sobrepasar el tiempo de riesgo de apnea posoperatoria y le dieran
manejo ambulatorio? Quienes estamos a cargo de la cirugía pediátrica tenemos un dogma: la cirugía del recién nacido está reservada para aquellas situaciones que amenazan la vida o un órgano, esto por el hecho conocido de que los menores de 60 semanas posconcepción que necesitan una anestesia general tienen un riesgo mayor de tener apneas posoperatorias y, por ello, deben quedarse hospitalizados en unidades con posibilidad de vigilar las apneas y darles manejo a tiempo, pues si esto sucede en casa, esos niños pueden tener muerte súbita o daños cerebrales irrecuperables.
Luego de este suceso me encontré cada día más siendo consultado en este tema, y aparecieron otras situaciones y es el hecho de que en nuestro medio ha estado creciendo la población cuya cultura indica la circuncisión en el periodo neonatal: judíos, musulmanes, entre otros, o hijos de padres de origen norteamericano que están acostumbrados a esta práctica. La respuesta fácil y que di durante 20 años fue: “para nosotros es una intervención que obliga una anestesia general, así que debemos esperar al menos que salga de ese rango de edad de alto riesgo”. Pero cuando me di cuenta de que las personas estaban convencidas de hacerlo y tomaban cualquier ruta ofrecida, así esta tuviera algún riesgo para sus niños, pero desconocido por ellos, consideré buscar alternativas, saber qué hacían en otras latitudes y ofrecerle algo seguro a los niños. Por esta razón surge esta revisión de la literatura y la posibilidad de tener otras maneras de enfrentar el tema y nuevas soluciones disponibles.
Fue entonces cuando me di a la tarea de conocer la técnica utilizada en otras partes del mundo y en otras culturas. La tarea de un cirujano pediátrico es cuidar de la salud de los niños que requieren cirugía y están en su entorno, y los padres encontraban quien les hiciera el procedimiento a sus hijos incluso corriendo riesgos. Los judíos de nuestras ciudades suelen ser intervenidos por médicos que practican su religión y utilizan unos dispositivos reutilizables que ellos han usado siempre.
El Gomco es un dispositivo muy utilizado en Norteamérica, el cual tiene dos partes, una campana que se coloca entre el glande y el prepucio y otra parte que comprime intensamente la piel contra la campana inicial durante 3 a 5 minutos, luego se reseca la piel sobrante y se retira el dispositivo. Las críticas para este dispositivo están centradas en los riesgos de sangrado que se puede presentar debido a que no hay ninguna sutura que asegure dicho evento adverso.
También hay dispositivos desechables. En Estados Unidos han desarrollado unos dispositivos desechables de fácil uso que colocan en los servicios neonatales y de obstetricia, algunos llegan a criticar que incluso no tienen ningún control posterior por parte de los médicos que le practican el procedimiento a sus pacientes. Con esos dispositivos se han descrito eventos adversos muy molestos y graves debido a su diseño, ya que tienen forma de campana y en ellos el glande puede deslizarse fuera del dispositivo, lo que lleva a una parafimosis con el dispositivo. También sucede que el diseño está hecho para retirar todo el prepucio, dejando completamente descubierto el glande en todos los casos.
SE PUEDE HACER EN COLOMBIA AL RESPECTO?
En la búsqueda realizada para entender la situación en Colombia con respecto a la circuncisión, encontré un dispositivo que, en mi opinión y experiencia local, corregía algunas cosas que podían ser importantes en nuestro medio: el Circumplast®. En primer lugar, su diseño corrige el riesgo de la parafimosis descrita con otros dispositivos semejantes y, en segundo lugar, permite definir la extensión de la resección del prepucio, lo que para nuestro medio me pareció muy positivo ya que lo esperado culturalmente es que parte del prepucio cubra el surco balanoprepucial, así que con este dispositivo se puede lograr un efecto estético más cercano a nuestra cultura.
Desde febrero de 2024, este dispositivo desechable está autorizado en Colombia por el Instituto Nacional de Vigilancia de Medicamentos y Alimentos (Invima) para su uso, con el cual se puede hacer la circuncisión con anestesia local durante el primer año de vida, obviando el requerimiento de anestesia general; es seguro y tiene un diseño que corrige los problemas de otros dispositivos usados en el mundo, además de que permite una circuncisión que deja una cobertura parcial del glande, lo cual está más cerca del aspecto usual que se le ha dado a nuestros pacientes con la técnica convencional.
Desde hace más de 30 años ha habido una evolución de la cirugía, conocida mundialmente como de mínima invasión; y en relación dicho término, quiero presentarles lo que he llamado circuncisión de mínima manipulación. Para esto se usa el dispositivo Circumplast®, un dispositivo estéril
y desechable que se inserta entre el glande y el prepucio del niño; esto se hace en cualquier niño, desde recién nacido hasta los 5 años en promedio, y este último valor se decide por el diámetro del pene del niño, ya que el dispositivo viene en 4 diámetros. Si se trata de un bebe pequeño, el control de sus movimientos es fácil y se realiza con anestesia local, así que el dolor será únicamente el relacionado con la aplicación de un bloqueo en la raíz del pene (Figura 1); una vez colocada la inyección de más o menos 2 mL, el niño regresa a los brazos de su madre y será alimentado para darle comodidad; a los 5 minutos regresa al sitio del procedimiento y se hace una incisión ventral (Figura 2) para acomodar el dispositivo (Figura 3) como se describió. Posteriormente, se decide el nivel al cual se realiza la circuncisión y allí se ata una sutura alrededor muy fuerte contra la copa del dispositivo (Figura 4), de tal manera que se detiene el flujo sanguíneo distal. Se secciona el resto de la piel (Figura 5) y se deja la copa protectora en su sitio, lo cual será muy tranquilizador en el posoperatorio, pues protege el glande de la ropa interior.
Figura 1. Bloqueo de la raíz del pene con anestesia local sin epinefrina. Modificada de: London Circumcision Centre.YouTube; 2014.
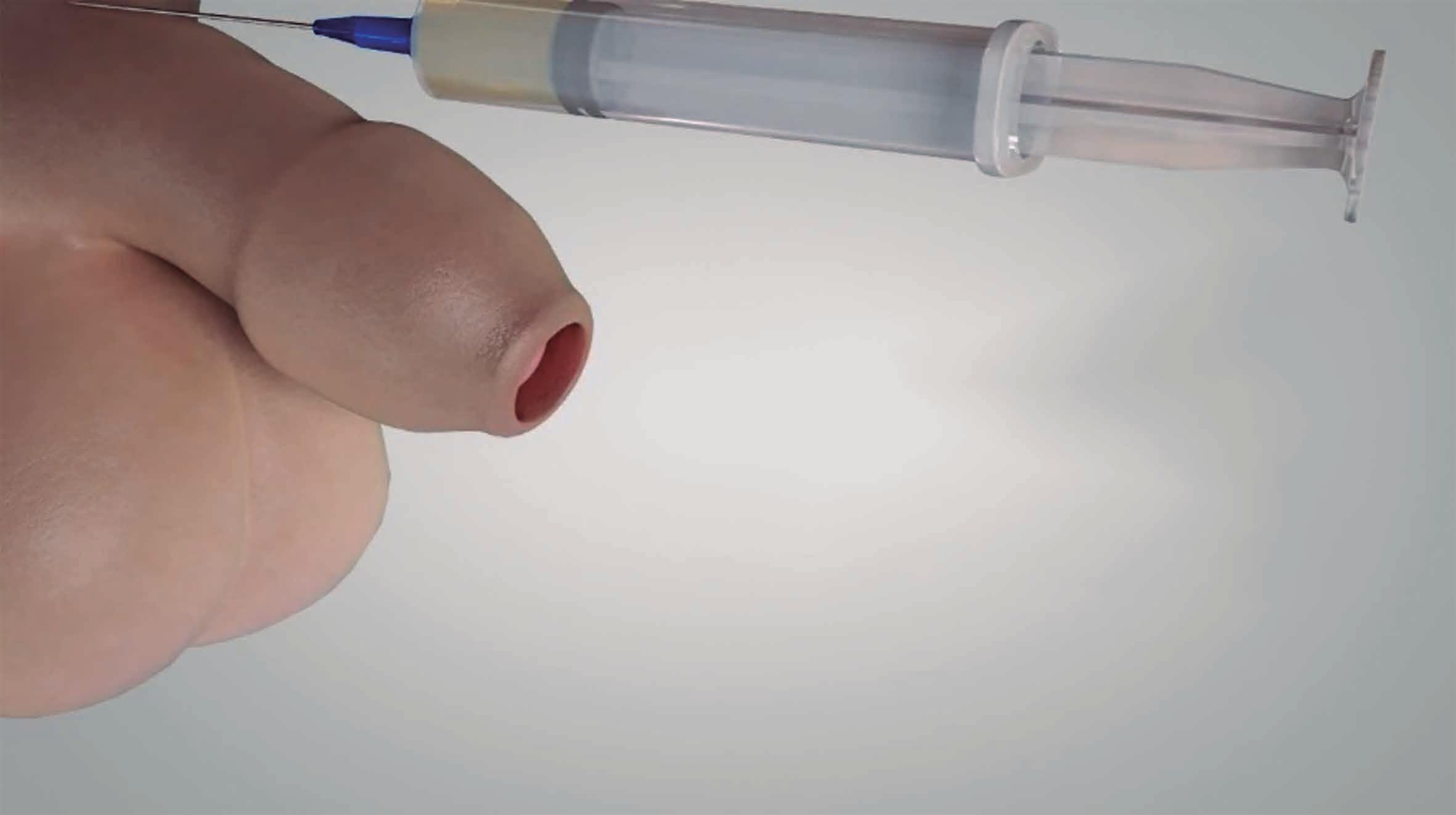
Se coloca un bloqueo de anestesia local en la raíz del pene sin epinefrina y se lleva al niño a los brazos de su madre mientras el bloqueo hace su efecto
Figura 2. Corte dorsal para ampliar el prepucio. Modificada de: London Circumcision Centre. YouTube; 2014.
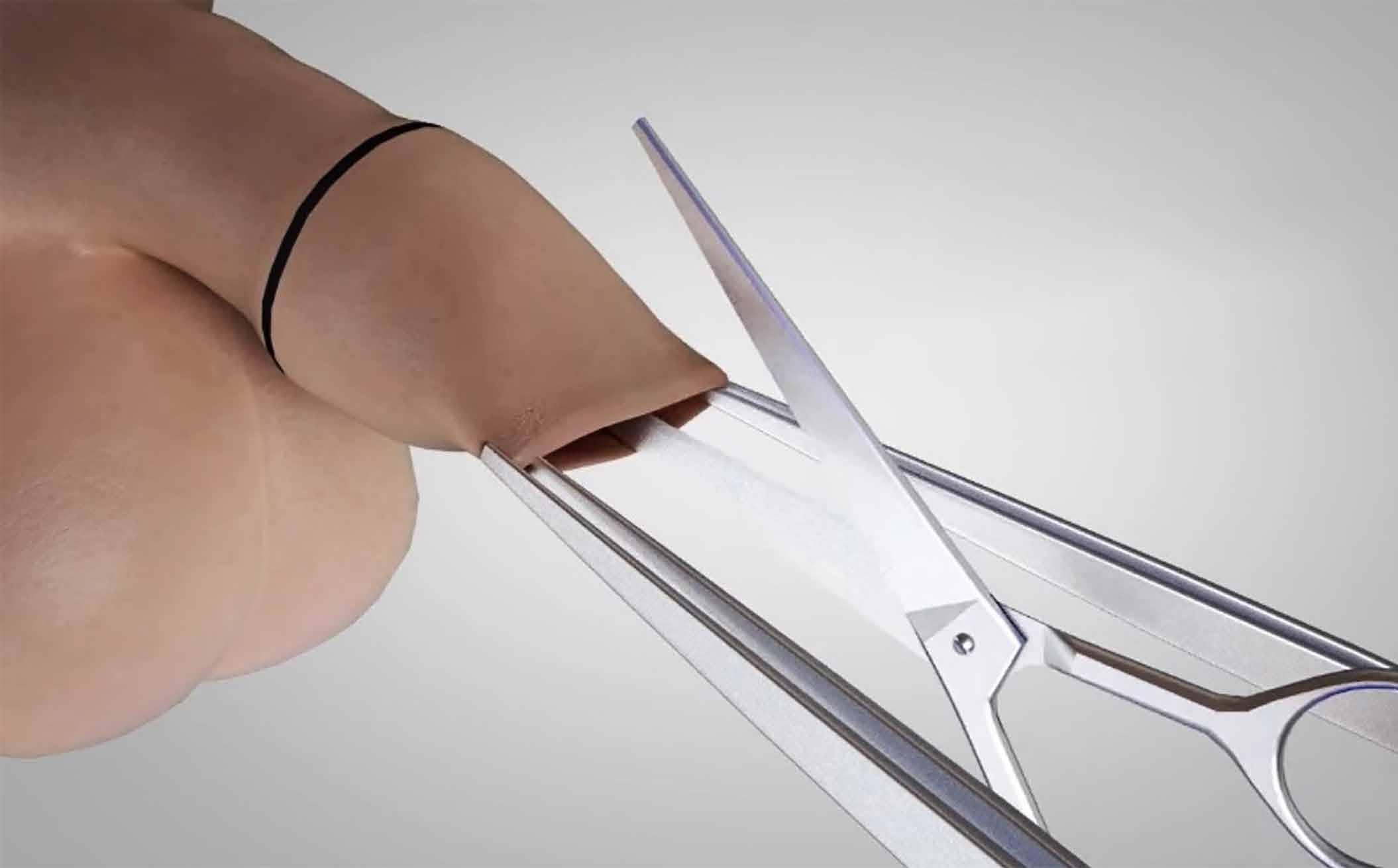
Se realiza un corte dorsal con el fin de lograr el espacio necesario para insertar la copa del Circumplast®
Figura 3. Inserción de la copa del Circumplast®. Modificada de: London Circumcision Centre. YouTube; 2014.

Se inserta la copa del Circumplast® entre el glande y el prepucio hasta el surco balanoprepucial
Figura 4. Colocación de la ligadura del Circumplast®. Modificada de: London Circumcision Centre.YouTube; 2014.
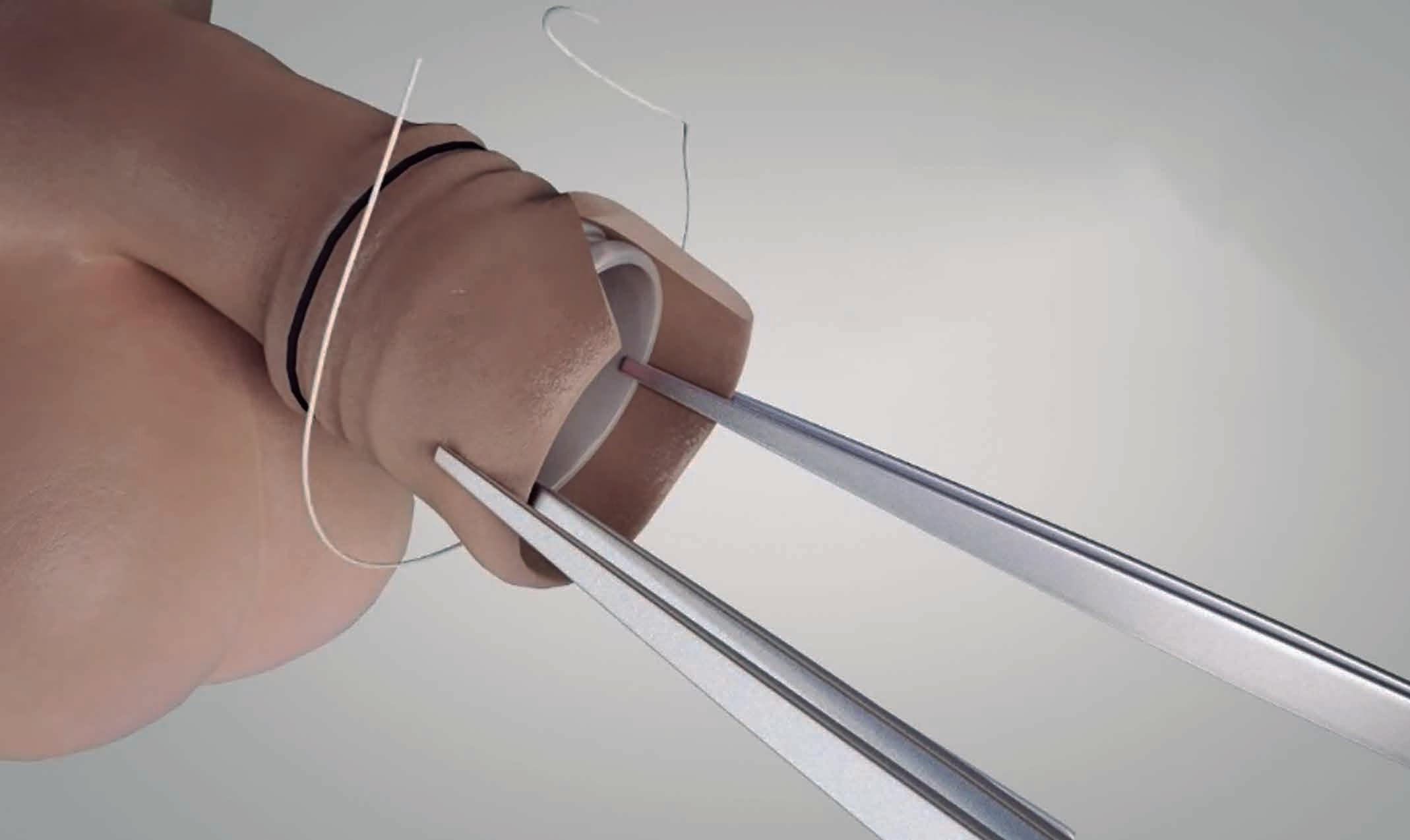
Se ata la ligadura incluida en el Circumplast® alrededor del prepucio en el nivel deseado, tan fuerte como sea posible para asegurar la hemostasia y que el dispositivo quede fijado
Figura 5. Resección de la piel distal. Modificada de: London Circumcision Centre.YouTube; 2014.
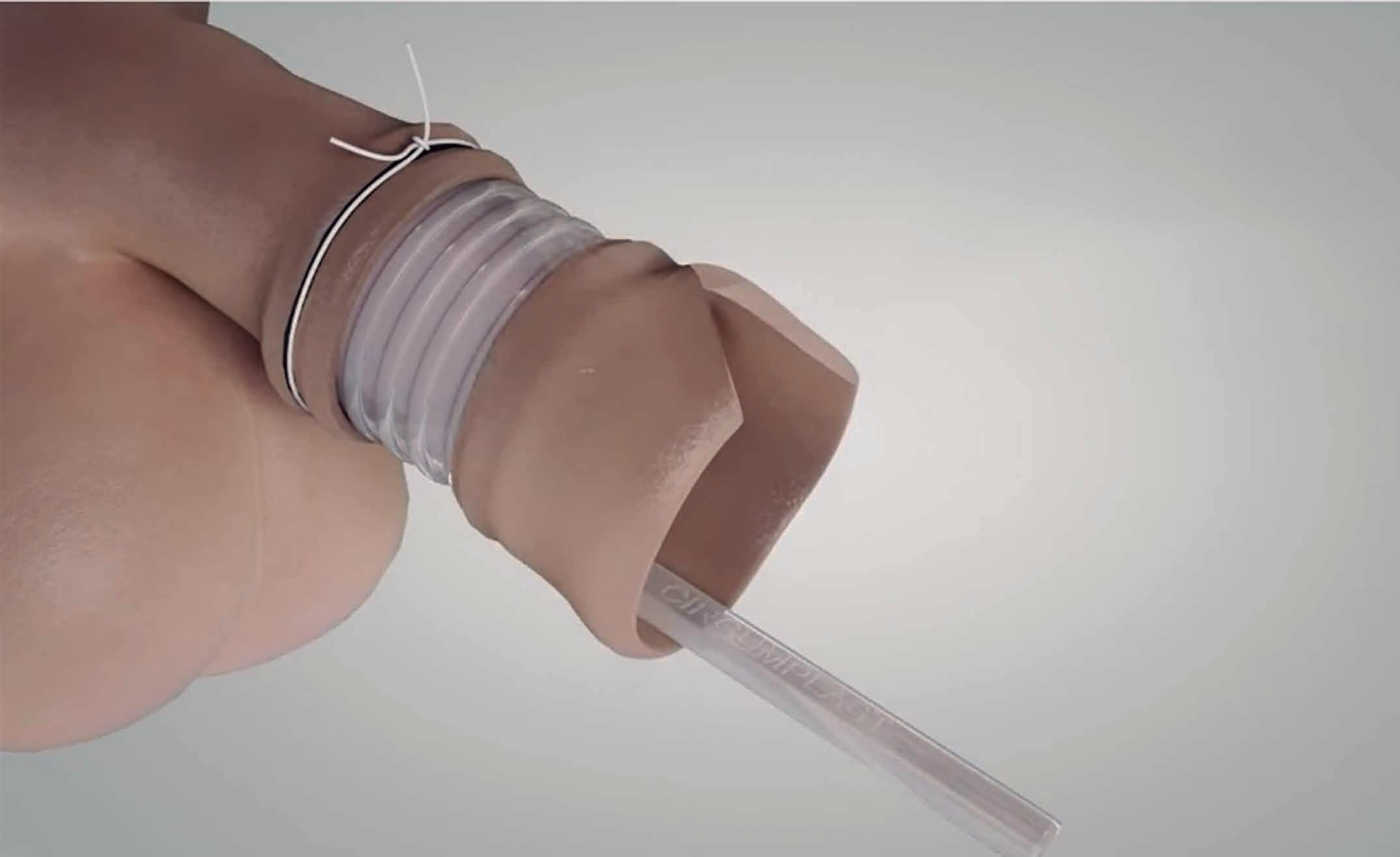
Se reseca el reborde de piel sobrante usando tijeras y se retira el exceso de piel y el fijador del Circumplast®
Figura 6. Momificación de la piel y caída de la copa. Modificada de: London Circumcision Centre.YouTube; 2014.

El prepucio distal a la ligadura se pondrá necrótico en los siguientes días, como sucede luego de la ligadura del ombligo. Habrá algunos cambios de edema y enrojecimiento con la manipulación y a veces equimosis en los sitios de punción del bloqueo anestésico.
Figura 7. Caída espontánea de la copa del Circumplast® en casa. Modificada de: London Circumcision Centre.YouTube; 2014.

La copa del Circumplast® se caerá espontáneamente entre 5 y 15 días después del procedimiento, y queda una circuncisión con bordes muy nítidos, el glande ya tolerará el roce y el edema y la congestión ceden rápidamente después de la caída del dispositivo.
Los cuidados posteriores son muy fáciles: se indica el uso de crema anestésica las primeras 24 horas para colocar en la piel expuesta, al día siguiente sigue el uso de un gel que ayude a la cicatrización y se administra analgésico oral usualmente por 2 a 3 días. Es normal que hacia el quinto día haya un enrojecimiento y este se mejora rápidamente después de la caída del dispositivo, sin necesidad de antibióticos.
1. American Academy of Pediatrics Task Force on Circumcision. Circumcision policy statement. Pediatrics. 2012;130(3):585-6.
2. Chan JY, Khondker A, Lee MJ, Kim JK, Chancy M, Chua ME, et al. The role of circumcision in preventing urinary tract infections in children with antenatal hydronephrosis: Systematic review and meta-analysis. J Pediatr Urol. 2023;19(6):766-777.
3. El Bcheraoui C, Zhang X, Cooper CS, Rose CE, Kilmarx PH, Chen RT. Rates of adverse events associated with male circumcision in U.S. medical settings, 2001 to 2010. JAMA Pediatr. 2014;168(7):625-34.
4. Hainz T. The Enhancement of Children versus Circumcision: A Case of Double Moral Standards? Bioethics. 2015;29(7):507-15.
5. London Circumcision Centre. Infant and Children Circumcsion by Circumplast ring [Internet]. YouTube;
Francisco Javier Mejía es un cirujano infantil de la ciudad de Medellín y quien logró el certificado del Invima para importar y vender Circumplast® en territorio colombiano. Puede ser contactado por correo electrónico: doctorfranciscomejia@gmail.com o conspacho@ gmail.com.
2014. Disponible en: https://www.youtube.com/ watch?v=QG29dTcdF18
6. Morris B, Rivin BE, Sheldon M, Krieger JN. Neonatal Male Circumcision: Clearly Beneficial for Public Health or an Ethical Dilemma? A Systematic Review. Cureus. 2024;16(2):e54772.
7. National Center for HIV/AIDS, Viral Hepatitis, STD, and TB Prevention (U.S.). Division of HIV/AIDS Prevention. Information for providers counseling male patients and parents regarding male circumcision and the prevention of HIV infection, STIs, and other health outcomes. Centers for Disease Control and Prevention; 2018. Disponible en: https://stacks.cdc.gov/view/cdc/58456
8. Saeed A, Gregory D, Amin R, Khanbhai M, Khan A. A novel disposable ring (Circumplast) showed no ring migration onto the shaft of the penis in first 1000 male children’s circumcisions in a community specialist clinic. J Pediatr Surg Case Rep. 2023; 92:102603.
Hernando Pinzón Redondo, MD1
Sady David Roa Valdelamar, MD2
María José Daniels García, MD3
Paola Andrea Manjarrés Figueredo, MD3
Ana Isabel Hernández Villadiego, MD3
Las infecciones de trasmisión vertical (ITV) hacen referencia a todas las infecciones que afectan al embrión, feto o recién nacido, y que se transmiten a través de la madre. Su contagio puede ocurrir durante la gestación (infecciones congénitas), periparto o en el periodo posnatal, a lo que hace referencia el acrónimo TORCH, que incluye toxoplasmosis, rubéola, citomegalovirus [CMV], virus del herpes simple y otros (paperas, virus de la inmunodeficiencia humana [VIH], parvovirus, sífilis, virus de la varicela). Dicho acrónimo puede ser confuso y hacer que el personal médico olvide incluir la sífilis dentro del abordaje etiológico, por lo que se sugiere hacer el cambio al acrónimo SCORTH (sífilis, CMV, otros como Zika, malaria, parvovirus,
VIH, hepatitis B y C, rubeola, toxoplasma y virus del herpes). Dentro de este gran espectro, la infección congénita por citomegalovirus (CMVc) es la más común de este grupo y representa una causa importante de mortalidad, secuelas neurológicas y discapacidad auditiva en la población pediátrica.
La infección por CMVc tiene una mayor incidencia, prevalencia y gravedad en los países con menos recursos; sin embargo, esta información es difícil de verificar debido a que en muchos de estos países no hay fácil acceso a pruebas diagnósticas y, por tal razón, ocurre un infradiagnóstico y escasa notificación de la enfermedad. En relación con la presentación clínica, solo el 10 % de los pacientes con CMVc presentan una infección sintomática al
1. Infectólogo pediatra, Hospital Infantil Napoleón Franco Pareja. Grupo de Investigación de Infectología Pediátrica, Universidad de Cartagena. Cartagena, Colombia.
2. Pediatra, Universidad de Cartagena, Hospital Infantil Napoleón Franco Pareja. Cartagena, Colombia.
3. Residente de Pediatría, Universidad de Cartagena. Cartagena, Colombia.
nacimiento, con una tasa de mortalidad del 40 % y, de los sobrevivientes, el 40 %-90 % desarrollan secuelas permanentes, de las cuales la más común es la pérdida auditiva. Además de los trastornos auditivos, estos pacientes pueden desarrollar un amplio espectro de manifestaciones que incluyen: trombocitopenia, hepatoesplenomegalia, hepatitis, miocarditis, microcefalia, malformaciones anatómicas del sistema nervioso central (polimicrogiria, calcificaciones, ventriculomegalia) y epilepsia; por estas razones es fundamental identificar los factores de riesgo sociales, maternos y gestacionales para realizar un seguimiento adecuado a la población de bebés vulnerables.
La infección congénita por CMV tiene una distribución de contagio universal, con una prevalencia en los recién nacidos del 0,58 % al 0,7 % en los países industrializados; aproximadamente, 40.000 bebés nacen con infección por CMV cada año en los Estados Unidos. Se ha reportado una diferencia en la prevalencia de CMVc según las características raciales o étnicas del neonato; en un estudio de cohorte retrospectivo publicado en Journal of Pediatrics que incluyó a 100 332 bebés de siete centros médicos se obtuvo una prevalencia de CMVc de 4,5 por cada 1000 nacidos vivos (NV), y es mayor en recién nacidos afroamericanos (9,5/1000 NV) frente a los bebés blancos no hispanos (2,7/1000 NV) y bebés blancos hispanos (3,0/1000 NV). Sin embargo, es importante tener en cuenta que los estudios estadísticos se realizan principalmente en países desarrollados y que los países de menos recursos suelen no tener acceso a los métodos diagnósticos correctos, lo que lleva a un subregistro de la enfermedad en esta población. Representa la causa más importante de pérdida auditiva neurosensorial no hereditaria, es la causa del 20 % de todas las pérdidas auditivas al nacer y del 25 % de todas las pérdidas auditivas a la edad de 4 años.
La infección por CMV puede presentarse en cualquier grupo etario, con un alto pico de incidencia en los niños, adolescentes y mujeres embarazadas. Hacia los 3 años de edad, el 80 % de los niños ya tendrán anticuerpos contra CMV y en la adultez se habla de hasta un 100 %. En mujeres embarazadas, la prevalencia de infección por CMV es de 0,2 %-2 %, con una frecuencia de seroconversión baja del 1 %-4 %, lo que explica por qué la mayoría al llegar a la gestación ya habrá presentado una infección por el virus. En Colombia no se cuenta con estadísticas específicas para infección por CMVc; sin embargo, existe una alta tasa de seropositividad en mujeres embarazadas, de un 66 %, y reportes de positividad del 1,5 % en recién nacidos de bajo peso para la edad.
El CMV humano, también conocido como herpesvirus humano 5, es un miembro de la familia de los virus del herpes (Herpesviridae), la subfamilia de los β -herpesvirus (Betaherpesvirinae) y el género Cytomegalovirus. Su genoma viral es de ADN de doble cadena con un tamaño entre 196 000 y 240 000 pb, y tiene el genoma más grande de los virus del herpes humanos. Además, es un patógeno que solo afecta a los humanos.
La transmisión de la infección por CMV puede ocurrir mediante varias vías:
• Horizontal: por contacto directo de persona a persona con secreciones que contienen virus.
• Verticalmente: de madre a hijo antes, durante o después del nacimiento.
• Transfusiones de sangre, plaquetas y glóbulos blancos, trasplante de órgano sólido o de células madre hematopoyéticas.
En relación con la infección congénita, puede darse de modo intrauterina (más común), intraparto o en la lactancia.
La transmisión al feto ocurre en alrededor del 32 % de estos casos y conduce a la enfermedad en alrededor del 13 % de los recién nacidos. Los estudios han demostrado que la transmisión de la infección materna al feto difiere según el estado infeccioso de la madre; por tanto, en la primoinfección, la tasa de transmisión se da en un 30 %-40 %, y en la reinfección o reactivación, solo en un 1 %-2 %, lo que evidencia que la inmunidad materna preexistente no previene la transmisión intrauterina o el desarrollo de la enfermedad.
Así mismo, el riesgo de la transmisión vertical de CMV se incrementa con el avance de la gestación. Para el primer trimestre, el riesgo se encuentra alrededor del 36 %; para el segundo trimestre, del 40 %, y, finalmente, para el tercer trimestre, del 66 %. Por el contrario, el riesgo de complicaciones fetales/neonatales es inversamente proporcional a la edad gestacional de la infección; por tanto, en pacientes con infección adquirida antes de la decimosegunda semana de gestación, la probabilidad de contagio es casi nula; en cambio, si la exposición materna es periconcepcional (entre 4 semanas previas a la concepción y 5 semanas posconcepción), el riesgo aumenta al 21 %.
En la infección por CMVc, la placenta tiene un rol importante y ha sido objeto de estudio. Diversas investigaciones han hallado la presencia de zonas de inflamación y necrosis. El virus puede infectar al endometrio, sincitiotrofoblasto, citotrofoblasto y las células endoteliales, lo que conlleva alteraciones en las funciones de estas células, sobre todo del citotrofoblasto, que es primordial en el primer trimestre en relación con la composición de la placenta, lo que se traduce en un aumento del riesgo de
presentar prematuridad, restricción de crecimiento intrauterino, infección placentaria y posteriormente fetal.
Los eventos moleculares resultantes son el efecto de múltiples interacciones entre las proteínas propias del virus y los procesos celulares del huésped; inicialmente se presenta la unión entre proteínas de la envoltura del virus y los proteoglicanos de heparán sulfato de la superficie celular del hospedador; posteriormente, se da la fusión completa de la envoltura viral con la membrana celular, lo que dará entrada a la nucleocápside, de modo que se garantiza la supervivencia y replicación del ADN a través del metabolismo celular del huésped. En particular, las células vasculares endoteliales son un sitio de intensa replicación y son protagonistas en el proceso de diseminación debido a las citocinas secretadas que generan la migración de los granulocitos y su posterior diseminación hacia las células de las glándulas salivales, riñones, pulmones, oído interno, vías biliares y neuronas.
Existen ciertas condiciones de la inmunidad en la etapa prenatal y neonatal, como la disminución de funciones de los neutrófilos, las células asesinas naturales (NK) y factores del complemento que permiten la multiplicación viral persistente, característica de la infección intrauterina y neonatal, además de la respuesta defectuosa de grupos celulares como los linfocitos T CD8+ y CD4+, que son claves en el control de replicación viral en las glándulas salivales. Estudios realizados evidencian una escasa respuesta de dichas células a los antígenos del virus, al igual que una disminución en la actividad de las células NK al momento de neutralizar a fibroblastos infectados por el virus.
La infección congénita por CMV tiene una presentación clínica espectral y varí a desde los cuadros asintomáticos hasta la enfermedad
diseminada con alto riesgo de mortalidad. Afortunadamente, solo el 10 % de los pacientes infectados presentan sintomatología. Sin embargo, del 15 % al 25 % de los pacientes asintomáticos podrían presentar secuelas a largo plazo, entre ellos alteraciones neurológicas y en el psicodesarrollo.
Las manifestaciones clínicas y hallazgos de laboratorio neonatales más prevalentes en la infección congénita por CMV se encuentran en la Tabla 1.
En la Figura 1 se observa la clasificación y características de acuerdo con la sintomatología en pacientes con infección congénita por CMV.
En relación con el compromiso neurosensorial, aproximadamente el 25 % de las hipoacusias en preescolares menores de 4 años están
relacionadas con la infección congénita por CMV. Dicha afección está presente en 35 %-50 % de los pacientes sintomáticos y aproximadamente en el 8 % de los pacientes asintomáticos. La pérdida de la audición es una de las complicaciones más temidas relacionadas con esta infección congénita; en ocasiones puede estar presente al momento del nacimiento o desarrollarse de manera tardía en los primeros años de vida, con un promedio de dos años y 9 meses en pacientes sintomáticos y de tres años y 8 meses en pacientes asintomáticos. En cuanto a las alteraciones oftalmológicas, alrededor del 10 % o menos de pacientes con CMV congénitos sintomáticos tienen alteraciones como coriorretinitis y atrofia óptica.
La convulsiones y epilepsias afectan aproximadamente al 40 % de los niños sintomáticos, con presentaciones neonatal o en primera infancia;
Tabla 1. Manifestaciones clínicas y hallazgos de laboratorio en neonatos con infección congénita por CMV
Adaptada y traducida de: Bale JF. En: Tselis AC, Booss J (editores). Elsevier; 2014. p. 319-26.
Figura 1. Definiciones y clasificaciones de infección congénita por CMV. Adaptada y traducida de: Rawlinson WD, et al. Lancet Infect Dis. 2017;17(6):e177-e188.
Enfermedad congénita por citomegalovirus moderada a gravemente sintomática
- Múltiples manifestaciones atribuibles a la infección congénita por citomegalovirus: trombocitopenia, petequias, hepatomegalia, esplenomegalia, crecimiento intrauterino restricción, hepatitis (transaminasas elevadas o bilirrubina).
- Compromiso del sistema nervioso central, como: microcefalia, anormalidades evidenciadas en radiografías consecuentes con afección del sistema nervioso central por citomegalovirus, índices anormales de líquido cefalorraquídeo para la edad, coriorretinitis, pérdida auditiva neurosensorial o la detección de ADN de citomegalovirus en el fluido cerebroespinal.
Infección congénita asintomática por citomegalovirus con neurosensorial aislado Pérdida de la audición
- Sin anomalías aparentes que sugieran enfermedad congénita por citomegalovirus, pero pérdida auditiva neurosensorial (= 21 decibelios).
Infección congénita asintomática por citomegalovirus
- Sin anomalías aparentes que sugieran enfermedad congénita por citomegalovirus, y con audición normal.
el síndrome de West es una presentación típicamente evidenciada entre los 3 y 10 meses de edad que consiste en espasmos, ipsiarritmias evidenciadas en electroencefalograma y retraso en el neurodesarrollo.
La infección por CMV congénito puede darse por una infección primaria y no primaria o reactivación de la madre durante el embarazo. El escenario de mayor riesgo es el de las madres seronegativas infectadas durante el embarazo. La transmisión al feto se produce en el 32 % de estos casos y conduce a la enfermedad en alrededor del 13 % de los recién nacidos infectados congénitamente. Entre las mujeres seropositivas, la reactivación de una cepa endógena o la
Enfermedad congénita por citomegalovirus levemente sintomática
- Puede ocurrir con una o dos manifestaciones aisladas de citomegalovirus congénito, en su mayoría son leves y transitorias (p. ej., hepatomegalia leve o una sola medición de recuento bajo de plaquetas o niveles elevados de alaninaaminotransferasa).
- Estos pueden superponerse con manifestaciones más graves. Sin embargo, la diferencia es que ocurren de forma aislada.
reinfección con una nueva cepa da lugar a una infección fetal en aproximadamente el 1 % de los embarazos. No obstante, la identificación y el riesgo de transmisión pueden ser un reto, y el diagnóstico de la enfermedad por CMV se ve dificultado por la ubicuidad del virus, la elevada tasa de excreción asintomática, la frecuencia de las infecciones reactivadas, el desarrollo de anticuerpos séricos específicos contra el CMV en algunos episodios de reactivación, la reinfección con diferentes cepas de CMV y la infección simultánea con otros patógenos.
Embarazo
El cribado universal del CMV en mujeres embarazadas no está recomendado en ningún país. Sin embargo, cuando se sospecha clínicamente de una infección materna primaria por CMV, las
pruebas serológicas pueden ayudar a determinar el riesgo de transmisión al feto. El diagnóstico de la infección materna primaria por CMV no se puede hacer sobre la base de los síntomas clínicos, ya que estos son inespecíficos, y la proporción de pacientes asintomáticas es de aproximadamente un 25 %-50 %.
Cuando se desconoce el estado inmunitario del CMV antes del embarazo, se recomienda la detección aislada con la técnica de avidez de anticuerpos IgG o la detección de anticuerpos IgM específicos especialmente antes de las 12-16 semanas de gestación, que indican un mayor riesgo de infección congénita sintomática.
Fetal
Invasivo
Se recomienda realizar una amniocentesis para la muestra de reacción en cadena de la polimerasa (PCR) a partir de la semana 21 de gestación debido a que se garantiza la excreción de orina al líquido amniótico en este periodo. Esta técnica tiene una sensibilidad del 90 %-98 % y una especificidad del 92 %-98 %.
Se han notificado casos de CMV con resultados negativos en el líquido amniótico, lo que puede reflejar sensibilidad de la PCR o que la transmisión se produjo después de la amniocentesis. Otro método podría ser la cordocentesis, que ofrece información pronóstica sobre los resultados en los bebés infectados, pero supone un riesgo para el feto y generalmente no se recomienda para el diagnóstico de la infección fetal por el CMV.
No invasivo
La sensibilidad de la ecografía para la detección de la infección por CMV es solo de aproximadamente el 15 %. Los hallazgos ecográficos incluyen la placentitis con calcificaciones que coexisten con áreas hipoecoicas, oligohidramnios, intestino hiperecogénico, íleo meconial,
hepatoesplenomegalia y posiblemente ascitis (debido a una hepatitis colestásica y a una insuficiencia hepática).
Recién nacido
El parámetro de referencia para la identificación de los bebés con CMV ha sido la detección del virus en muestras de saliva u orina obtenidas en las primeras 2-3 semanas de vida para distinguir la infección congénita de la posnatal.
Se puede realizar la identificación a través del cultivo viral o la prueba cuantitativa de amplificación de ácidos nucleicos. El desarrollo de nuevos métodos de recolección de muestras y la aplicación de métodos moleculares de alto rendimiento de alto rendimiento, como la reacción en cadena de la polimerasa (PCR) de alto rendimiento o la reacción en cadena de la polimerasa cuantitativa, han sustituido en gran medida a los métodos basados en los cultivos.
Se han realizado estudios que comparan la sensibilidad entre las muestras realizadas; sin embargo, la sensibilidad para la detección por PCR de CMV es de 99,7 % sin diferenciación del tipo de muestra de saliva o de orina; a pesar del riesgo de contaminación materna, es menos de 0,03 % y se recomienda recoger la muestra con hisopos antes de la alimentación o una hora después de esta.
Las muestras de sangre seca no se recomiendan, ya que la viremia es oscilante y pueden obtenerse falsos negativos con mayor frecuencia. Como parte complementaria de la evaluación general del paciente, se deben incluir algunos exámenes de laboratorio, como recuento hematológico, pruebas hepáticas, bilirrubinas, función renal y citoquímico de líquido cefalorraquídeo (LCR).
Los avances en la terapia antiviral neonatal contra la infección por CMV han sido significativos
en los últimos años; sin embargo, la indicación es bastante controversial por los riesgos mielotóxicos de los antivirales y el impacto en la hipoacusia neurosensorial a largo plazo.
Las recomendaciones actuales se refieren a tratar aquellos neonatos mayores de 32 semanas con síntomas moderados a graves de enfermedad congénita por CMV dentro del primer mes de vida. Los recién nacidos asintomáticos o con enfermedad sintomática leve o con hipoacusia neurosensorial aislada y sin otras manifestaciones de la enfermedad no deben recibir tratamiento antiviral de forma rutinaria debido a la falta de datos que sugieran beneficios en esta población menos gravemente afectada.
Opciones
Valganciclovir
Es un profármaco de ganciclovir. El valganciclovir de 16 mg/kg/dosis se administra por vía oral dos veces al día durante seis meses. La terapia de primera línea con valganciclovir durante seis meses mejora modestamente la audición y los resultados del desarrollo a largo plazo.
Ganciclovir
El ganciclovir a 6 mg/kg/dosis se administra por vía intravenosa dos veces al día por seis semanas en caso de un recién nacido con imposibilidad para absorber los medicamentos de forma fiable desde el tracto gastrointestinal (por ejemplo, debido a una enterocolitis necrotizante u otros trastornos intestinales).
Los recuentos absolutos de neutrófilos deben realizarse semanalmente durante seis semanas, luego a las ocho semanas y después mensualmente mientras dure el tratamiento
antiviral. La neutropenia significativa es menos frecuente con valganciclovir oral que con ganciclovir intravenoso y generalmente ocurre en el primer mes de tratamiento. Otros efectos secundarios observados son trombocitopenia y hepatotoxicidad, notificados hasta en un 30 % de los pacientes tratados con ganciclovir.
Foscarnet
El foscarnet a 180 mg/kg/día se administra por vía intravenosa en tres dosis por tres semanas. Los estudios son limitados, y su uso se reserva a casos de resistencia o toxicidad a la primera línea.
Inmunoglobulina intravenosa
La terapia con inmunoglobulina específica para CMV no se recomienda en la etapa neonatal.
Las ITV son un grupo de patologías muy heterogéneas, pero que pueden coexistir en un mismo paciente, y que comparten la característica de generar a corto, mediano y largo plazo una gran carga para el niño y la familia, debido a la elevada tasa de morbimortalidad. La infección congénita por CMV es la ITV de mayor frecuencia de presentación, cuyo diagnóstico en edades tempranas de la gestación puede ser difícil, por lo cual es importante realizar un arduo trabajo de prevención e identificación de los bebés en riesgo (madres con pobre control prenatal, en condiciones de hacinamiento, en contacto con niños pequeños), así como una evaluación ecográfica completa para identificar alteraciones anatómicas tempranas, con el fin de realizar una preparación del equipo de atención del parto y un eventual plan de seguimiento multidisciplinario para el neonato.
Hernando Pinzón Redondo, Sady David Roa Valdelamar, María José Daniels García, Paola Andrea Manjarrés Figueredo, Ana Isabel Hernández Villadiego
1. Bale JF. Congenital cytomegalovirus infection. En: Tselis AC, Booss J (editores). Handbook Of Clinical Neurology. Elsevier; 2014. p. 319-26.
2. Britt WJ. Maternal Immunity and the Natural History of Congenital Human Cytomegalovirus Infection. Viruses. 2018;10(8):405.
3. Cofré F, Delpiano L, Labraña Y, Reyes A, Sandoval A. Síndrome de TORCH: enfoque racional del diagnóstico y tratamiento pre y post natal. Recomendaciones del Comité Consultivo de Infecciones Neonatales Sociedad Chilena de Infectología. Rev Chil Infectol. 2016;2(33):191-216.
4. Chiopris G, Veronese P, Cusenza F, Procaccianti M, Perrone S, Daccò V, et al. Congenital cytomegalovirus infection: Update on diagnosis and treatment. Microorganisms. 2020;8(10):1516.
5. Fowler KB, Boppana SB. Congenital cytomegalovirus infection. Semin Perinatol. 2018;42(3):149-154.
6. Harrison GJ. Current controversies in diagnosis, management, and prevention of congenital cytomegalovirus: updates for the pediatric practitioner. Pediatr Ann. 2015;44(5):115-25.
7. Mareri A, Lasorella S, Iapadre G, Maresca M, Tambucci R, Nigro G. Anti-viral therapy for congenital
cytomegalovirus infection: Pharmacokinetics, efficacy and side effects. J Matern Fetal Neonatal Med. 2016;29(10):1657–64.
8. Rawlinson WD, Boppana SB, Fowler KB, Kimberlin DW, Lazzarotto T, Alain S, et al. Congenital cytomegalovirus infection in pregnancy and the neonate: consensus recommendations for prevention, diagnosis, and therapy. Lancet Infect Dis. 2017;17(6):e177-e188.
9. Razonable RR, Inoue N, Pinninti SG, Boppana SB, Lazzarotto T, Gabrielli L, et al. Clinical Diagnostic Testing for Human Cytomegalovirus Infections. J Infect Dis. 2020;221(1):74–85.
10. Sampedro Martínez A, Martínez LA, Teatino PM, Rodríguez-Granger J. Diagnóstico de infección congénita. Enferm Infecc Microbiol Clin. 2011;29 Suppl 5:15-20.
11. Ssentongo P, Hehnly C, Birungi P, Roach MA, Spady J, Fronterre C, et al. Congenital Cytomegalovirus Infection Burden and Epidemiologic Risk Factors in Countries With Universal Screening: A Systematic Review and Meta-analysis. JAMA Netw Open. 2021;4(8):e2120736.
12. Wang C, Zhang X, Bialek S, Cannon MJ. Attribution of congenital cytomegalovirus infection to primary versus non-primary maternal infection. Clin Infect Dis. 2011;52(2):e11-3.
Cristina Del Carmen Muñoz Otero, MD1
Carlota Valentina Ovalle Villadiego, MD2
María Clara Vigna De La Hoz, MD3
Valeria Vásquez Amell, MD4
El síndrome del macrófago activado (SMA) es un tipo de linfohistiocitosis hemofagocítica secundaria (LHH) asociada a complicaciones de trastornos inflamatorios sistémicos y considerada como una emergencia médica potencialmente letal que puede llevar a falla multiorgánica. La patología reumática más asociada es la artritis idiopática juvenil (AIJ) con una prevalencia del 10 %; sin embargo, el SMA subclínico puede estar presente hasta en un 30 % de los casos de AIJ. A su vez, se ha visto relacionada con enfermedad de Kawasaki, dermatomiositis juvenil (DMJ) y lupus eritematoso sistémico (LES).
Ha sido un desafío diagnosticar la enfermedad desde que se hicieron los primeros reportes
de caso alrededor de 1980; por eso, es de vital importancia conocer su presentación clínica con el fin de realizar un diagnóstico oportuno y un manejo adecuado, y de este modo mejorar los desenlaces de esta enfermedad en pediatría.
Aún no es muy bien conocido el motivo por el cual algunas patologías reumatológicas llegan a desarrollar el SMA; sin embargo, la hipótesis actual consiste en que un desorden autoinmunitario de las células asesinas naturales (NK) y los linfocitos T CD8, que genera una disfunción citolítica debido a una inhibición en la expresión de la perforina por mutaciones genéticas que bien pueden ser homocigotas o heterocigotas.
1. Medicina interna pediátrica, Hospital Universidad del Norte. Docente de posgrado, Universidad Libre y Universidad del Norte.
2. Residente de Pediatría, Universidad del Norte. ORCID: 0009-0000-2179-6034
3. Médica General, Universidad del Norte.
4- Médica General, Universidad del Norte.
Factores genéticos, proinflamatorios, infecciosos y medicamentos asociados
Normalmente, la perforina es empaquetada en gránulos citolíticos de las células NK y T CD8 para ser transportada por el citoesqueleto y así salir a la sinapsis inmunológica con el fin de llegar a la célula presentadora de antígeno (CPA) para formar un poro y permitir que la granzima B entre y genere apoptosis celular como mecanismo de defensa inmunológico. Al haber mutaciones en genes como LYST, RAB27A, UNCI13D, STXBP2, STX11, se da paso a una alteración en el proceso de tráfico y acoplamiento de gránulos citolíticos, para generar la posterior interrupción del proceso normal de citólisis en niños sanos, lo que finalmente da paso a que se genere una cascada proinflamatoria debido a la interacción prolongada entre la célula citolítica y la CPA.
Entre las citocinas inflamatorias más importantes descritas en la fisiopatología de la enfermedad se encuentra el interferón gamma (INF- γ), que se encarga de activar a los macrófagos para que estos fagociten las células infectadas y produzcan otras citocinas en grandes cantidades. Lo anterior terminaría generando una activación masiva de las células del sistema inmunitario, las cuales son responsables de generar las manifestaciones clínicas en los pacientes con SMA.
Otros factores que se han visto relacionados con la disminución de citólisis son los agentes infecciosos, de los cuales el virus de EpsteinBarr es el más relacionado, y fármacos como las sales de oro, la sulfasalazina y el sulfametoxazol.
Reconocer los signos y síntomas del SMA tempranamente mejora los resultados en los pacientes. La presencia de fiebre alta persistente en niños con enfermedades reumáticas debe
generar sospechas de SMA, especialmente en aquellos que no están inmunosuprimidos.
Otros síntomas acompañantes incluyen manifestaciones, como se detallan en la Tabla 1
Tabla 1. Manifestaciones clínicas que sugieren SMA
Manifestaciones clínicas
Fiebre alta y persistente
Hepatomegalia
Signos y síntomas
Esplenomegalia 38
%-70 %
Disfunción neurológica
Afectación cardiaca
%
Afectación pulmonar 14 %-22 %
Hemorragias 14 %-20 %
Afectación renal 9 %-15 %
Tomada de: Núñez Cuadros E, et al. Protoc Diagn Ter Pediatr. 2020; 2:89-100.
La activación masiva de células inmunitarias y la producción excesiva de citocinas inflamatorias resultan en una afectación multiorgánica. Además del compromiso de los órganos linfoides, el sistema nervioso central puede estar afectado, presentando síntomas como cefalea, confusión, convulsiones y coma, lo que agrava el pronóstico del paciente. En casos graves, también se pueden observar petequias, exantemas, hemorragias, sangrado gastrointestinal y coagulopatía. Sin un diagnóstico y tratamiento oportunos, los pacientes pueden experimentar falla multiorgánica, responsable de la mortalidad que oscila entre 10 % y 35 % en niños con SMA.
Para realizar el diagnóstico óptimo y oportuno de la enfermedad, es crucial la realización de una anamnesis adecuada. Esto permite identificar las enfermedades subyacentes que padece el
Tabla 2. Hallazgos de laboratorio encontrados en el SMA
Parámetro de Laboratorio Hallazgo en SMA
Hemograma
Función hepática
Albúmina sérica
Tiempos de coagulación
Ferritina sérica
Otros hallazgos
Biomarcadores adicionales
Pancitopenia.
Elevación de transaminasas y ocasionalmente aumento de la bilirrubina.
Hipoalbuminemia moderada.
Prolongación de los tiempos de protrombina y tromboplastina parcial, hipofibrinogenemia, productos de degradación de fibrina detectables y aumento en los niveles de dímero D.
Aumento al inicio de SMA, más de 5000 a 10 000 ng/dL.
Aumento de triglicéridos y de lactato deshidrogenasa.
Medición del receptor soluble de IL-2 α (también conocido como CD25 soluble) y CD163 soluble, que pueden reflejar el grado de activación y expansión de las células T y los macrófagos, respectivamente.
Modificada de: Ravelli A, et al. Hematol Oncol Clin North Am. 2015;29(5):927-41.
paciente, así como el tratamiento que recibe actualmente, lo que facilita la dirección de los estudios confirmatorios. En la Tabla 2 se presentan los hallazgos de laboratorio encontrados en los niños con SMA.
La ferritina sérica ha demostrado ser un excelente marcador para monitorizar la enfermedad, esto se debe a que son valores fundamentales para evaluar la respuesta al tratamiento y para prever su pronóstico. Por su parte, otros biomarcadores se han destacado en su diagnóstico óptimo de SMA con el limitante de que no se encuentran como pruebas de rutina en la mayoría de los centros hospitalarios.
Para determinar el diagnóstico de SMA, la Organización Internacional de Ensayos en Reumatología Pediátrica (PRINTO) llegó a un consenso en 2016 respecto a los criterios de laboratorio necesarios para sospechar esta entidad. Estos criterios, detallados en la Tabla 3, presentan una sensibilidad del 73 % y especificidad del 99%, y se han encontrado útiles en pacientes con AIJ, LES y enfermedad de Kawasaki, y recientemente se validaron para los pacientes
con SMA asociado a síndrome inflamatorio multisistémico a causado por covid-19.
Las recomendaciones enfatizan en la importancia de conocer sobre la enfermedad para que pueda ser sospechada en pacientes con fiebre, citopenia o coagulopatías que presenten niveles de ferritina > 10 000 ng/mL. De esta manera, se realizan estudios adicionales según la probabilidad diagnóstica de la entidad y el manejo por especialista.
Tabla 3. Criterios diagnósticos de SMA descritos en 2016 por la Organización Internacional de Ensayos en Reumatología Pediátrica (PRINTO)
Paciente febril con sospecha de o enfermedad conocida de AIJ, es clasificado con SMA si la ferritina sérica es > 698 ng/mL y ≥ 2 de los siguientes:
- Plaquetas ≤ 181 x 109/L
- AST > 48 U/L
- Triglicéridos > 156 mg/dL
- Fibrinógeno ≤ 360 mg/dL
AIJ: artritis idiopática juvenil; AST: aspartato-aminotransferasa; SMA: síndrome del macrófago activado. Tomada de: Bagri NK, et al. Indian Pediatr. 2021;58(12):1155-1161.
Teniendo en cuenta la alta mortalidad y agresividad en el curso clínico del SMA, es fundamental el inicio precoz e intensivo del tratamiento, aun cuando solo exista la sospecha clínica. De hecho, debido a la complejidad del cuadro, la mayoría de los pacientes requerirán manejo en una unidad de cuidados intensivos pediátrica y atención multidisciplinaria. El objetivo radica en mitigar la tormenta de citocinas a través de la instauración de una adecuada inmunosupresión y el control del factor desencadenante, siempre que esto sea posible.
El manejo inicial y de carácter urgente debe realizarse con altas dosis de glucocorticoides, y los pulsos de metilprednisolona intravenosa en dosis de 30 mg/kg (máximo 1 g) durante 3 a 5 días es el tratamiento de primera línea. Por su parte, los esteroides orales se inician a una dosis de 2 mg/kg/día, se titulan gradualmente según la evolución clínica y paraclínica, y continúan generalmente hasta la normalización de las alteraciones hematológicas.
En casos refractarios o en los que exista compromiso del sistema nervioso central, algunos autores han reportado con éxito la utilización de dexametasona palmitato a 7,5-10 mg/día, en vez de metilprednisolona, principalmente cuando se utiliza en terapia combinada con el inhibidor de la calcineurina, la ciclosporina A. Esto se debe fundamentalmente a una utilización más eficiente por parte de los macrófagos de los corticosteroides incorporados en emulsiones lipídicas en comparación con los corticosteroides libres, a través de fenómenos como la fagocitosis, los cuales a su vez conducen a una mayor retención de dexametasona palmitato en el citoplasma.
Aunque la remisión del cuadro se alcanza en un 70 % de los pacientes utilizando únicamente corticosteroides, en la actualidad se recomienda adicionar el inhibidor de la calcineurina, la ciclosporina A, a aquellos pacientes en los
que no se presente una respuesta adecuada en las primeras 24-48 horas. Su eficacia se demostró por primera vez en la década de los 90, al ser utilizada con excelentes resultados en pacientes con refractariedad a corticoides intravenosos en dosis altas. La ciclosporina A parece dirigirse preferentemente a los linfocitos, por medio de la inhibición de una familia de factores de transcripción fundamentales para la activación de genes de citocinas, de modo que se amortigua la tormenta de citocinas propia de esta condición. La duración adecuada no se ha establecido claramente en la literatura; de hecho, se ha utilizado de forma variable en un rango comprendido entre 3 meses y 2 años, y lo más recomendable es una dosis de 2-7 mg/kg/d durante 3-6 meses. Así mismo, debe continuarse hasta la consecución de la normalización de los parámetros de laboratorio, con una apropiada titulación para prevenir recaídas. Por su parte, aunque este fármaco reduce la utilización desmesurada de corticosteroides, debe ser administrado con precaución en pacientes con falla multiorgánica, considerando sus efectos neurotóxicos y nefrotóxicos.
Además de las opciones anteriores, la inmunoglobulina intravenosa es una opción de manejo y fue uno de los primeros fármacos biológicos en ser indicados dentro del tratamiento del SMA, y es administrada principalmente como un agente coadyuvante a la metilprednisolona intravenosa debido a la seguridad relativa y el perfil favorable en cuanto a efectos adversos. Cabe aclarar que el éxito de la inmunoglobulina depende en gran medida de su inicio temprano y generalmente se indica en el contexto en el que se sospeche un proceso infeccioso subyacente debido a sus propiedades inmunorreguladoras y su potencial efecto preventivo de complicaciones sépticas. En ocasiones se ha descrito un abordaje más agresivo utilizando la globulina antitimocítica; sin embargo, ante el alto riesgo de infecciones secundarias y las tasas de mortalidad elevadas, muchos autores no recomiendan su administración y prefieren la utilización de otros biológicos.
Los primeros inhibidores de citocinas utilizados en pacientes con SMA fueron los fármacos antifactor de necrosis tumoral (anti-TNF); no obstante, ante la posibilidad de desencadenar un SMA en pacientes en manejo con estos medicamentos, se relegó la utilización de los bloqueantes de TNF en el contexto del SMA, y se ha dirigido la terapia con bloqueantes de citocinas hacia los fármacos anti-IL-1 y los anti-IL-6.
El primer reporte de administración del antagonista del receptor de IL-1, anakinra, en el SMA se realizó en un paciente críticamente enfermo con una grave condición inflamatoria, y resultó en una rápida y favorable recuperación. Posteriormente, se evidenció una impresionante mejoría a nivel sistémico y en el componente artrítico de una cohorte de pacientes refractarios al tratamiento convencional de la artritis idiopática juvenil sistémica (AIJs). Además, Miettunen y colaboradores lograron tratar de forma exitosa a 12 pacientes pediátricos con SMA en el contexto de una enfermedad reumatológica con una respuesta inadecuada al tratamiento convencional. Cabe resaltar que una gran limitación en el uso de anakinra en la población pediátrica con SMA corresponde a que la mayoría de información proviene de estudios observacionales y reportes de casos. No obstante, tomando en consideración la alta efectividad del antagonista del receptor de IL-1 en la AIJs, este biológico se considera un tratamiento muy útil en el abordaje del SMA. La dosis de inicio suele ser de 2 mg/kg/d y en casos refractarios puede aumentarse a 8 mg/ Kg/d. Habitualmente, se considera un paso temprano en el manejo del SMA en caso de una inadecuada respuesta al tratamiento convencional, especialmente en ausencia de un desencadenante infeccioso. Algunos autores recomiendan la administración de una triple terapia consistente en anakinra, dexametasona y ciclosporina A en el manejo del SMA en el contexto de la AIJs. Cuando la condición clínica del paciente implique estados de choque y pobre absorción periférica, se podría recomendar la administración intravenosa. Aunque
se han descrito casos de hepatitis al parecer secundarios a anakinra en pacientes con AIJs, y se ha sugerido que podría desencadenar SMA en algunos pacientes, la literatura no es concluyente al respecto y, en términos generales, una vasta cantidad de publicaciones en las que se ha utilizado el antagonista del receptor de IL-1 en pacientes con SMA han dado resultados ampliamente favorables, por lo que se considera en la gran mayoría de ocasiones un fármaco seguro con una vida media corta y una amplia ventana terapéutica.
El anticuerpo monoclonal anti-IL-1β, canakinumab, es otra opción disponible; se ha utilizado con éxito en el tratamiento de SMA en pacientes con AIJs, a una dosis de 4 mg/kg subcutánea (SC).
A pesar de eso, se requieren estudios adicionales para definir con mayor certeza su eficacia. Por su parte, la administración del anticuerpo monoclonal dirigido al receptor de la IL-6, tocilizumab, ha sido altamente eficaz en el tratamiento de la AIJs; sin embargo, su utilización en el contexto del SMA es incierto, en especial, porque existe un caso reportado de SMA desencadenado por el bloqueo de la IL-6. Es importante tomar en consideración que, debido a la función bien definida en la promoción de la fase aguda de la respuesta inflamatoria y en la coordinación de reacciones inmunitarias por parte de la IL-6, los pacientes pediátricos con AIJs en tratamiento con tocilizumab pueden permanecer afebriles, con recuentos celulares y niveles de ferritina más bajos en caso de desarrollar SMA en comparación con aquellos que no reciben esta terapia, lo cual podría entorpecer el diagnóstico oportuno de estos pacientes.
Adicionalmente, se podría considerar la utilización del anticuerpo monoclonal específico para el antígeno CD20, rituximab, en el abordaje de pacientes con SMA secundario a infecciones por virus de Epstein-Barr, a una dosis de 375 mg/m2 semanalmente durante cuatro semanas debido principalmente al éxito en la administración de este fármaco en procesos linfoproliferativos inducidos por este virus.
Por otra parte, el SMA refractario al tratamiento inicial con pulsos de metilprednisolona y la ciclosporina se comporta como un verdadero desafío para los clínicos a pesar de su baja frecuencia. En estos casos, se ha considerado la administración de etopósido, pero se ha evidenciado una mayor incidencia en manifestaciones graves, admisiones a la unidad de cuidados intensivos (UCI), infecciones oportunistas y mielosupresión en los pacientes que reciben este fármaco, por lo que su indicación sigue siendo muy controvertida.
Adicionalmente, la citocina proinflamatoria IL-18 se ha encontrado desproporcionadamente elevada en el SMA asociado a AIJs; de hecho, Shimizu y colaboradores indicaron que el SMA se complicaba solamente en pacientes con AIJs cuyos niveles séricos de IL-18 eran extremadamente altos, especialmente en pacientes con valores de > 47 750 pg/mL, por lo que propuso la importancia de monitorizarla para predecir el desarrollo del SMA debido a su posible asociación con una disfunción de células NK. Además, la implicación de la IL-18 en la patogénesis del SMA fue ampliamente potenciada por la identificación de una enfermedad autoinflamatoria monogénica secundaria a la mutación del gen NLRC4, en la que se produce un SMA recurrente de inicio temprano, se desencadena la escisión constitutiva de la caspasa-1 y se genera una producción incrementada de IL-18. En pacientes con mutaciones en el gen NLRC4 se han utilizado fármacos anti-IL-1, los cuales han demostrado una mejoría clínica evidente. Actualmente, se está llevando a cabo un ensayo clínico con un fármaco anti-IL-18, tadekinig alfa en pacientes con mutaciones en el gen NLCR4 y deficiencia de XIAP.
Nuevos estudios han evidenciado la elevación del IFN- γ y las citocinas inducidas por este en el SMA, en comparación con pacientes con AIJs sin SMA; por tanto, algunos autores lo proponen como el principal mediador en el SMA secundario a infecciones y enfermedades reumáticas. Es por esto que la terapia de este síndrome se dirige hacia la utilización de un anticuerpo monoclonal IgG1 anti-INF- γ totalmente
humano, emapalumab, que hasta el momento ha brindado datos preliminares exitosos con respecto a su eficacia en SMA asociado a AIJs; sin embargo, se requieren estudios adicionales para aclarar su utilidad en SMA secundario a otras condiciones reumatológicas. Por su parte, los inhibidores de las JAK cinasas han evidenciado resultados experimentales prometedores en el abordaje del SMA al bloquear las vías de señalización de las citocinas implicadas en el cuadro clínico.
En casos refractarios o con recaídas frecuentes, se podría utilizar como último escalón el trasplante de células madre hematopoyéticas (TCMH); no obstante, ante la disponibilidad de terapias más específicas y dirigidas a citocinas con óptimos resultados y la alta incidencia de efectos adversos, muchos autores consideran que la utilización del TCMH para el tratamiento del SMA refractario es contradictorio y su indicación sigue siendo incierta.
Un algoritmo con el esquema de tratamiento se muestra en la Figura 1.
• Antes de iniciar el tratamiento antiinflamatorio, se debe valorar el tratamiento específico en caso de infecciones y la retirada de fármacos que hayan podido actuar como desencadenantes. Resultará imprescindible asociar el tratamiento de soporte en caso de falla hepática, coagulopatía o signos de choque.
• En caso de afectación del sistema nervioso central, se podrá sustituir la metilprednisolona por dexametasona intravenosa a 10-20 mg/m2 /día, en dosis única.
• La dosis de ciclosporina oral será 5 mg/kg/ día 2 dosis, y vía intravenosa 2-4 mg/kg/día 2 dosis. Se deben solicitar niveles séricos en caso de falla hepática. Niveles terapéuticos de 200 µg/mL.
• Después de las 2 primeras dosis, se administrará al menos una dosis más semanal.
• La globulina antitimocítica constituye una alternativa al etopósido en caso de insuficiencia hepática.
Figura 1. Algoritmo terapéutico propuesto de SMA. IV: intravenoso(a). Tomada de: Núñez Cuadros E, et al. Protoc Diagn Ter Pediatr. 2020;2:89-100.
Sospecha de SMA (a)
Metilprednisolona (b) IV. 20-30 mg/kg/día (máx. 1 g), 3-5 días
± Ciclosporina oral o IV (c)
¿Mejoría?
Metilprednisolona IV 2 mg/kg/día cada 8 h hasta la normalización analítica y estabilidad clínica
± Ciclosporina oral (c)
¿Mejoría?
Prednisona oral 1-2 mg/kg/día con reducción progresiva
± Ciclosporina oral con dosis decrecientes hasta valorar retirada en 2-3 meses
• El tratamiento con IGIV se puede considerar de forma concomitante con otros tratamientos en cualquier momento del proceso. En algoritmos de pacientes adultos con enfermedad de Still lo consideran como tratamiento inicial junto a los bolos de metilprednisolona.
• En caso de SAM secundario a AIJs y luego de descartar infecciones activas, se podría tratar la actividad de la enfermedad con fármacos biológicos (anti-IL-1/anti-IL-6) incluso antes del empleo de etopósido.
Finalmente, el SMA representa una entidad clínica compleja, con una condición inflamatoria
Mantener bolos IV de metilprednisolona 10-30 mg/kg/día, 2-3 días/semana hasta la normalización analítica/estabilidad clínica
± Ciclosporina oral o IV (c)
± Etopósido (d) 150 mg/m2, 2 veces/semana las 2 primeras semanas, posteriormente semanal
¿Mejoría?
Otras alternativas: globulina antitimocítica (e) 1-1,5 mg/kg/día Inmunoglobulina IV (f) 2 g/kg
Anti-IL-1 (g): anakinra o canakinumab Anti-IL-6 (g): tocilizumab
grave que puede llegar a falla multiorgánica o incluso a la muerte si no se sospecha y trata adecuadamente. La hiperactividad de la respuesta celular inmunológica y el aumento de la respuesta inflamatoria contribuyen a las manifestaciones clínicas y complicaciones. Comprender cómo se desarrolla el SMA puede ayudar a identificar tempranamente, diagnosticar y guiar el tratamiento, el cual deberá ser dirigido a la causa subyacente y la modulación del sistema inmunológico. Un enfoque multidisciplinario entre clínicos, investigadores y pacientes es fundamental para mejorar los resultados en los pacientes; sin embargo, aún se necesita desarrollar estrategias terapéuticas más precisas y efectivas.
1. Bagri NK, Gupta L, Sen ES, Ramanan AV. Macrophage Activation Syndrome in Children: Diagnosis and Management. Indian Pediatr. 2021;58(12):1155-1161.
2. Bruck N, Suttorp M, Kabus M, Heubner G, Gahr M, Pessler F. Rapid and sustained remission of systemic juvenile idiopathic arthritis-associated macrophage activation syndrome through treatment with anakinra and corticosteroids. J Clin Rheumatol. 2011;17(1):23-7.
3. Crayne CB, Albeituni S, Nichols KE, Cron RQ. The Immunology of Macrophage Activation Syndrome. Front Immunol. 2019;10:119. https://doi.org/10.3389/ fimmu.2019.00119
4. Lotfy H, Abu-Zaid MH, Salah S, El Gaafary M, Abdulhady H, Salah H, et al. Egyptian evidencebased consensus on clinical practice guidelines for the diagnosis and treat-to-target management of macrophage activation syndrome in children. Egypt Rheumatol Rehabil. 2022;49(1):36.
5. Miettunen PM, Narendran A, Jayanthan A, Behrens EM, Cron RQ. Successful treatment of severe paediatric rheumatic disease-associated macrophage activation syndrome with interleukin-1 inhibition following conventional immunosuppressive therapy: case series with 12 patients. Rheumatology (Oxford). 2011;50(2):417-9.
6. Minoia F, Davì S, Horne A, Demirkaya E, Bovis F, Li C, et al. Clinical features, treatment, and outcome of macrophage activation syndrome complicating
systemic juvenile idiopathic arthritis: a multinational, multicenter study of 362 patients. Arthritis Rheumatol. 2014;66(11):3160-9.
7. Nakagishi Y, Shimizu M, Kasai K, Miyoshi M, Yachie A. Successful therapy of macrophage activation syndrome with dexamethasone palmitate. Mod Rheumatol. 2016;26(4):617-20.
8. Núñez Cuadros E, Galindo Zavala R, Díaz-Cordovés Rego G. Síndrome de activación macrofágica. Protoc Diagn Ter Pediatr. 2020;2:89-100.
9. Ravelli A, Davì S, Minoia F, Martini A, Cron RQ. Macrophage Activation Syndrome. Hematol Oncol Clin North Am. 2015;29(5):927-41.
10. Ravelli A, Grom AA, Behrens EM, Cron RQ. Macrophage activation syndrome as part of systemic juvenile idiopathic arthritis: diagnosis, genetics, pathophysiology and treatment. Genes Immun. 2012;13(4):289-98.
11. Shimizu M, Nakagishi Y, Inoue N, Mizuta M, Ko G, Saikawa Y, et al. Interleukin-18 for predicting the development of macrophage activation syndrome in systemic juvenile idiopathic arthritis. Clin Immunol. 2015;160(2):277-81.Sönmez HE, Demir S, Bilginer Y, Özen S. Anakinra treatment in macrophage activation syndrome: a single center experience and systemic review of literature. Clin Rheumatol. 2018;37(12):3329-3335.
Adolfo Álvarez Montañez, MD1
Mauricio Guerrero Román, MD2
Gennys Gutiérrez Ramírez, MD3
Mónica Holguín Barrera, MD3
Paula Herrera Revollo, MD4
INTRODUCCIÓN
Intentar definir la ansiedad como una condición fisiológica y heterogénea es abarcar una temática amplia que involucra la educación integral en todas las etapas del ser humano; la identificación de hitos del neurodesarrollo; las reacciones frente a un estímulo externo en los lactantes; la separación de las figuras de apego y los miedos a figuras o fenómenos en preescolares; las fantasías, personajes, soledad, miedos persistentes y fobias en escolares; la falta de aceptación social y luchas hormonales en la difícil pubertad, y la búsqueda de identidad en la temida adolescencia. Sumado a lo anterior se identifican los traumas, las amenazas que se salen de control, el apego inseguro y la
sensación de peligro, que, en conjunto, pueden desencadenar los múltiples síntomas, que van desde los vegetativos hasta los conductuales, y pueden interpretarse de forma patológica hasta el grado de exteriorizarse de manera desproporcionada e inclusive en ausencia de un estímulo que la desencadene.
A nivel mundial se conoce que 10 a 15 de cada 100 niños, niñas y adolescentes presentan trastornos mentales asociados, mayormente, a problemáticas sociales; sin embargo, existe una prevalencia en Latinoamérica del 12,7 % al 15 % donde se añaden alteraciones nutricionales y perinatales. No obstante, en Colombia, el último boletín de salud mental arroja la ansiedad y la fobia social como trastornos mentales
1. Médico, neurólogo pediatra, Universidad Nacional. Docente de posgrado de Pediatría, Universidad del Sinú, Cartagena, y Universidad Simón Bolívar, Barranquilla, Colombia.
2. Presidente de la Sociedad Colombiana de Pediatría. Pediatra, servicio de hematooncología pediátrica, Fundación Hospital Infantil Napoleón Franco Pareja (HINFP). Cartagena, Colombia.
3. Residente de Pediatría, Universidad del Sinú. Cartagena, Colombia.
4. Residente de Pediatría, Universidad Simón Bolívar. Barranquilla, Colombia.
más frecuentes en la adolescencia, y la principal causa se le atribuye a la separación en la niñez.
Por otra parte, cabe aclarar que la preocupación excesiva, miedo, tensión y sensación de peligro/amenaza son algunos de los malestares que incluye este grupo de trastornos que han sido estudiados históricamente y considerados incluso como mecanismos de defensa para la supervivencia mediante funciones adaptativas, de modo que se obtienen desequilibrios en los sistemas neurobiológicos, serotoninérgicos y gabaérgicos, sin dejar a un lado la fundamental epigenética y con ella la importancia de identificar los factores de riesgo en la población pediátrica.
En términos generales, poder abordar esta enfermedad constituye un reto debido a todos los posibles precipitantes a los cuales se encuentran expuestos los niños y adolescentes que permiten que desarrollen estas condiciones, como nacer en un mundo globalizado, amplio acceso al mundo digital y redes sociales, la importancia de crear una identidad aceptada para los demás, las pautas de crianza no saludables, entre otras, y que han ido en aumento después de la exposición de la sociedad en general a una pandemia sin precedentes que reflejó un sinnúmero de factores y desenlaces psicosociales, afectivos, mentales, culturales y económicos que afectaron el comportamiento de la población global, incluida la población pediátrica. Todo esto es un desafío para los profesionales de la salud a trabajar e impactar en los niños y adolescentes por medio de una detección temprana de síntomas, prevención y abordaje integral.
FISIOPATOGENIA
Psicobiología
Neurológicamente, por un lado, existe una liberación al torrente de diversas hormonas por la activación de la alarma al reconocer o recuperar vivencias que son desencadenadas
por estímulos del mundo externo mediante el hipocampo y el córtex asociativo; simultáneamente, las vías eferentes llevan la información a la amígdala con la posterior activación del eje hipotálamo-hipófisis-glándula suprarrenal, y con ello se obtienen altos niveles de noradrenalina, adrenalina y glucocorticoides. Por otro lado, se presenta también la activación del sistema nervioso autónomo simpático, que es quien prepara la reacción a los músculos y otros órganos, lo que se ve representado en un aumento de la frecuencia cardiaca, la presión arterial, la frecuencia respiratoria, la vasoconstricción periférica, diaforesis, entre otros.
Aproximadamente, el 33 % de la transmisión de los trastornos de ansiedad son explicados genéticamente; sin embargo, no se discrimina entre angustia, fobia y ansiedad generalizada, por lo que se considera entonces que es la vía fisiopatológica común, y, en este orden de ideas, se ha demostrado que las condiciones del ambiente intrauterino pueden afectar los circuitos cerebrales del miedo, por ejemplo, por un exceso de glucocorticoides. Una vez se da el nacimiento, se observan y aprenden patrones y comportamientos parentales de sus cuidadores y se convierten en acontecimientos de amenaza estresantes que pueden generar inicialmente fobias sin condicionar una crisis de angustia, así como cambios en el tamaño de la amígdala.
Esta situación se repite evolutivamente con los miedos adquiridos en las diferentes edades que se originan en etapas diversas del neurodesarrollo, iniciando en la etapa de lactantes con ruidos desconocidos, apego, soledad, personajes de terror e incluso la muerte o falta de aceptación social en la etapa escolar y adolescencia, respectivamente.
Por otra parte, en condiciones fisiológicas, el cuerpo humano tiene la capacidad de mantener un estado de vigilia o alerta que modula y facilita la estimulación de la corteza y la forma de procesar cada sensación, y esto es gracias al sistema reticular activador ascendente, a
su vez, mediado por catecolaminas, neuronas colinérgicas y del núcleo paraventricular. Así mismo, es importante destacar el papel de la dopamina, el cortisol, la serotonina, los neuropéptidos y neurotransmisores en la génesis de la ansiedad, pues son estos sistemas (mesolímbico, mesocortical y dopaminérgicos) los que influyen en la mantención de las conductas.
Temperamento y personalidad
Algunos aspectos importantes que incluyen la personalidad (Figura 1) y el temperamento, que hasta el momento son considerados como supuestos, son de relevancia actualmente en el desarrollo de la ansiedad, y se consideran condiciones precursoras de aparición.
Debido a las vulnerabilidades del temperamento y de los rasgos de imposición de la personalidad
de los pacientes pediátricos, es común en muchos de los pacientes la presencia de inestabilidad emocional y la activación de mecanismos para exteriorizarla, de modo que se generan comportamientos ansiosos con presencia de malestar general e hiperexitación fisiológica frente a un estímulo, así como la afectividad negativa con limitación de reposicionarse de manera afectiva.
Por otro lado, la inhibición del comportamiento muestra la conducta frecuente de reflejar temor, miedo y retraimiento frente a condiciones de las cuales no se tiene conocimiento. Este tipo de comportamientos tienden a ser identificables a etapas tempranas con presencia de una estabilidad moderada, la cual es posible controlar por parte del paciente, y llaman la atención las manifestaciones de timidez tanto con las personas extrañas y con las situaciones desconocidas.
Figura 1. Interacción neurobiológica de los trastornos de la ansiedad. Modificada por los autores.
Interacción neurobiológica de los trastornos de la ansiedad
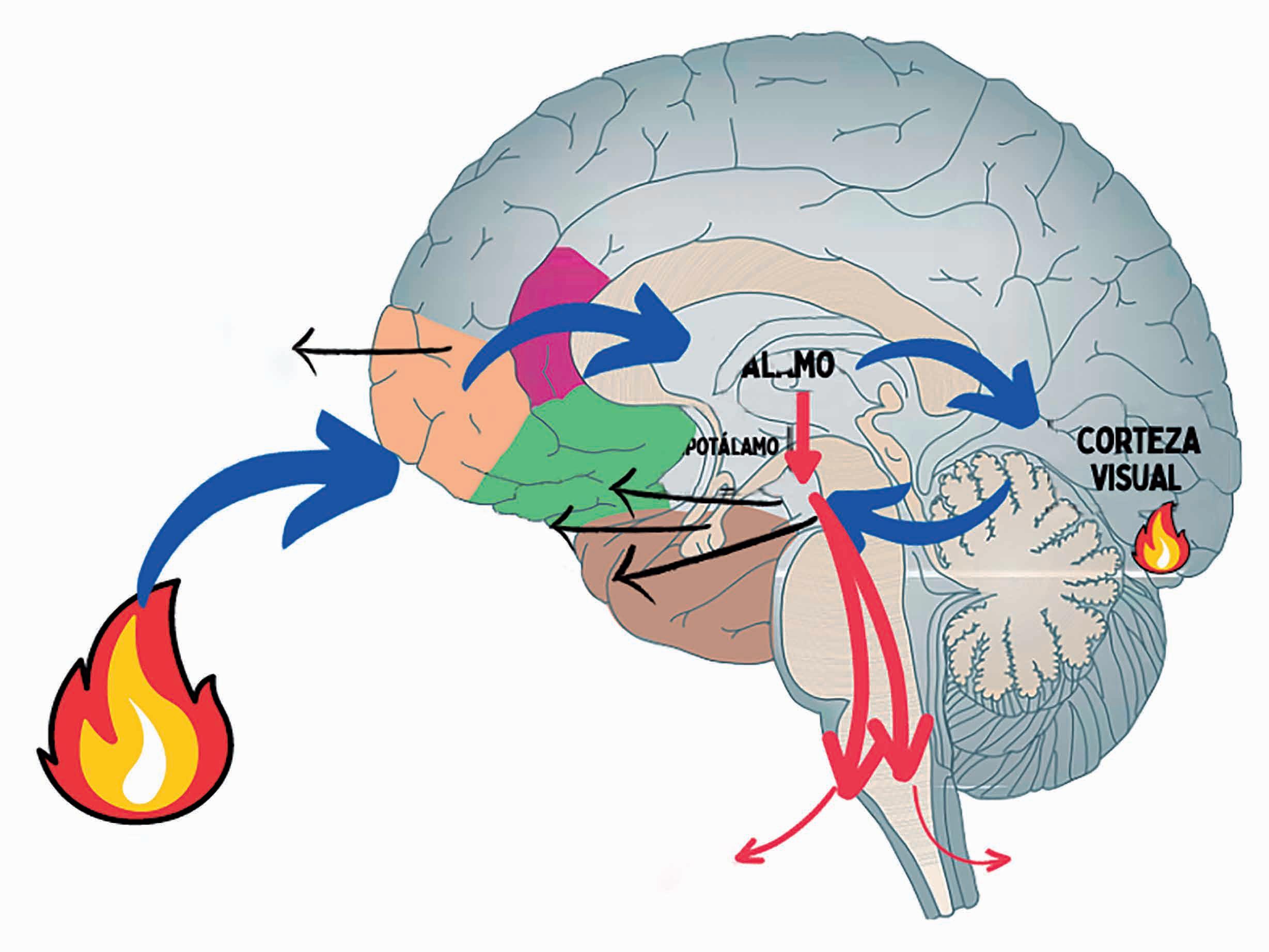
Situación de miedo
Hipotálamo Amígdala
Hipófisis
Hipocampo
Respuestas endocrinas secreciones hormonales
Excitación autónoma
Álvarez Montañez, Mauricio Guerrero Román, Gennys Gutiérrez Ramírez, Mónica Holguín Barrera, Paula Herrera Revollo
Las manifestaciones clínicas se pueden clasificar de acuerdo con el tipo de trastorno de ansiedad, como se muestra a continuación.
Ansiedad por separación
Desencadenada de forma excesiva e inapropiada al presentarse una separación de personas, situaciones o elementos que le generen apego al niño (hogar, padres, escuela, juguetes) en promedio entre los 6 y 18 años, se manifiesta durante al menos 4 semanas, con tres síntomas tales como:
• Preocupación persistente y excesiva por pérdida de figuras de apego o por si les pudiese pasar algo.
• Porque una situación pueda desencadenar esta separación descrita previamente.
• Desconfianza al asistir al colegio.
• Temor a estar sin figuras de apego.
• Negarse a dormir solo o fuera de casa por miedo.
• Pesadillas que se relacionen con la separación.
• Somatización cuando se genere una situación que separe al paciente de una de sus figuras de apego.
La ansiedad por separación se incluye en este grupo debido a la persistencia y recurrencia de un temor ante una situación puntual, un estímulo u objeto, los cuales la persona tiende a evitar, de modo que los asocia con un miedo que afecta diversas áreas de la vida. Para el diagnóstico, se considera que el problema lleve una duración mayor de 6 meses.
Trastorno de ansiedad social
Se desencadena al poner en contacto al paciente con personas desconocidas, pues esto lo obliga a desarrollar conductas evitativas ante la sociedad y el miedo a sentirse evaluado por otra persona. Se manifiesta con llanto, diaforesis, lenguaje no espontáneo, tartamudez y exceso
de preocupación por sus conductas. La edad promedio es los 13 años.
Mutismo selectivo
Entre los 4 y 8 años se puede evidenciar que el niño guarda absoluto silencio ante situaciones sociales que son muy estresantes; sin embargo, sucede lo contrario en ambientes que considere seguros, como su familia. Esta es una condición que no se puede justificar por falta de conocimiento del lenguaje. Para el diagnóstico, la duración debe ser al menos de un mes.
Trastorno de pánico
Sucede de manera inesperada, tanto en niños como en adolescentes, y consiste en el miedo intenso y súbito asociado a síntomas como disnea, temblor, dolor torácico, dolor abdominal, náuseas y miedo a perder el control; esto ocurre durante el trastorno y puede repercutir en el miedo de presentar nuevos episodios, lo que podría predisponer o anticipar las acciones con situaciones múltiples.
Agorafobia
Es el miedo significativo o ansiedad secundaria a exponerse o anticiparse a una situación, podrían presentarse síntomas parecidos a un ataque de pánico o expresar miedo relacionado con posibles escenarios (antes de que ocurran). Se produce en, por lo menos, 2 de los siguientes casos:
• uso de transporte público
• habitar en espacios abiertos
• estar en espacios cerrados
• encontrarse entre muchas personas
• estar solo y fuera de casa
Trastorno de ansiedad generalizada
Consiste en la excesiva preocupación por diferentes aspectos de la vida que pueden no estar relacionados entre sí y pueden
pertenecer a eventos pasados, presentes o futuros. Clínicamente se presenta dificultad para concentrarse, irritabilidad, inquietud motora, trastornos del sueño, tensión de la musculatura y nerviosismo constante.
Ansiedad inducida por medicamentos/sustancias
Síntomas similares a los ataques de pánico durante o después de abstenerse o usar excesivamente un medicamento/sustancia.
Trastorno de ansiedad debido a otra afección médica
No se ajusta con criterios de trastorno mental sino con uno fisiológico asociado, que condiciona clínicamente una ansiedad con predominio de ataques de pánico. Se ha identificado que hay diagnósticos diferenciales que pueden generar una clínica ansiosa; por ejemplo, ictus, accidente cerebrovascular (ACV), epilepsia, tumores del sistema nervioso central (SNC), hipotiroidismo, hipertiroidismo y anorexia nerviosa.
El diagnóstico de la ansiedad en niños y adolescentes es un proceso complejo que requiere una comprensión integral de los síntomas, la presentación clínica y el contexto de desarrollo. La identificación temprana y precisa de los trastornos de ansiedad en esta población es crucial para proporcionar intervenciones terapéuticas efectivas y promover resultados positivos a largo plazo. La discusión sobre el diagnóstico de la ansiedad en niños y adolescentes implica considerar una serie de factores importantes que pueden influir en la presentación clínica y el abordaje terapéutico.
Para la evaluación clínica integral, el diagnóstico requiere una evaluación clínica completa que abarque una amplia gama de síntomas
emocionales, cognitivos y conductuales. Se deben considerar los antecedentes familiares, el entorno social y la historia de desarrollo del paciente para comprender la etiología y el curso de la ansiedad en un contexto más amplio.
Por una parte, la detección de síntomas de ansiedad debe integrar la calificación de la gravedad de los mismos, el deterioro de las actividades funcionales del paciente y las asociaciones a patologías (como el hipertiroidismo), separándolos de aspectos fisiológicos y que causan preocupaciones presentes en el desarrollo. Por otra parte, también es relevante tener en cuenta los síntomas que acompañan a estas situaciones como la irritabilidad, el llanto, las rabietas, entre otras, que muchas veces puede ser malinterpretado como situaciones de desobediencia u oposición, y más bien pueden ser la forma de somatización de situaciones de angustia como respuesta a no desencadenar síntomas más claros de la ansiedad.
Es fundamental diferenciar la ansiedad de otros trastornos psiquiátricos y condiciones médicas que pueden presentar síntomas superpuestos, descartando las formas de manifestación de la ansiedad y miedos que son comunes y esperables durante la infancia y adolescencia según el grupo etario (Figura 2).
Por otra parte, para poder categorizar al paciente dentro de un trastorno, se hace necesario que los signos y síntomas se relacionen con algún diagnóstico al cumplir con los criterios de cada uno de ellos. El Manual Diagnóstico y Estadístico de los Trastornos Mentales- 5 edición (DSM- V) realiza una descripción dentro de los espectros de ansiedad al trastorno de ansiedad generalizada (TAG), la fobia específica, agorafobia, trastorno de pánico (TP) y la fobia social (FS) que, desde el punto de vista de identificación y diagnóstico en niños, niñas y adolescentes, presentan algunas anotaciones en ciertas descripciones de los hallazgos ( Tabla 1).
Álvarez Montañez, Mauricio Guerrero Román, Gennys Gutiérrez Ramírez, Mónica Holguín Barrera, Paula Herrera Revollo
Figura 2. Aspectos importantes de la personalidad implicados en la ansiedad en el paciente pediátrico. Imagen propiedad de los autores.
Aspectos importantes de la personalidad implicados en la ansiedad en el paciente pediátrico
Neuroticismo, según Hans Eysenck
El más alto grado de inestabilidad emocional caracterizado por la forma de reacción exagerada a un estímulo amenazante y les cuesta volver a un nivel normal de activación emocional. Aprenden a evitar las situaciones que le causan pánico muy rápida y bruscamente, o comportamientos particulares para controlar sus miedos.
Rasgo de ansiedad, según Jeffrey Gray
Inhibe la realización de conductas que provoquen aquellos tipos de señales, situaciones y estímulos desagradables; es decir, del castigo, ya que produce una activación biológica. La evitación conductual de estímulos que son percibidos como ansiógenos por parte del individuo.
Inhibición conductual, según Jerome Kagan
Es un miedo extremo frente a la novedad. Es una variable temperamental que genera timidez, retraimiento, evitación social, inquietud o malestar social, además de miedo ante personas, objetos o situaciones desconocidas.
Tabla 1. Anotaciones especiales en DSM-V en el diagnóstico de espectros de ansiedad en niños, niñas y adolescentes
Fobia social - (A) Se debe encontrar la forma de tener relaciones sociales apropiadas para su edad con personas conocidas y la ansiedad social debe ocurrir en entornos de pares, no solo en interacciones con adultos.
- (B) En los niños, la ansiedad puede expresarse mediante llanto, rabietas, paralización y alejamiento de situaciones sociales con personas desconocidas.
- (C) En los niños, reconocer el miedo de manera excesiva/irrazonable puede estar ausente.
- (F) En pacientes < 18 años, la duración de los síntomas es de al menos 6 meses.
- El miedo a sentirse avergonzado en algunos momentos de interacción social es frecuente, pero normalmente el grado de angustia o deterioro es insuficiente para justificar un diagnóstico.
- La ansiedad o evitación social transitoria se presenta de manera frecuente en la niñez y la adolescencia.
- Posiblemente los niños no tienen opción de evitar por completo las situaciones que produzcan temor y, por ende, identificar la naturaleza de su ansiedad.
Fobia específica (aislada)
- (B) La ansiedad la pueden manifestar por medio de llanto, rabietas, congelamiento o apego. En los niños, reconocer el miedo de manera excesiva/irrazonable puede estar ausente.
- (C) En pacientes < 18 años, la duración de los síntomas es de al menos 6 meses.
- (F) El miedo a los animales y otros objetos en el entorno natural puede ser común y está presente durante la infancia.
- El diagnóstico no es justificable a menos que los temores causen un deterioro clínico importante.
Tabla 1. Anotaciones especiales en DSM-V en el diagnóstico de espectros de ansiedad en niños, niñas y adolescentes (continuación)
Trastorno
Trastorno de ansiedad generalizada
Trastorno obsesivo compulsivo
Estrés postraumático
Aspectos en niños, niñas y adolescentes
- (C) Para su diagnóstico se requiere la presencia de 1 de los 6 síntomas propuestos por DSM-V.
- El concepto de ansiedades y preocupaciones son secundarias al desempeño escolar o actividades deportivas, así como la puntualidad.
- Pueden presentar preocupación excesiva por acontecimientos de tipo catastróficos.
- Pueden tornarse muy perfeccionistas, conformistas y con presencia de inseguridad con ellos mismos, por lo que es usual que rehagan las tareas por la sensación de insatisfacción.
- Por lo general, son demasiado entusiastas en la búsqueda de aprobación y requieren excesiva tranquilidad sobre su desempeño y sus preocupaciones.
- El trastorno puede diagnosticarse en niños, por lo que se debe realizar una evaluación exhaustiva de la presencia de otros trastornos de ansiedad infantiles para determinar si las preocupaciones pueden explicarse mejor por uno de estos trastornos.
- (B) Los criterios no aplican para los niños.
- Su presentación habitualmente es similar a la de los adultos.
- Es muy común identificar rituales de lavado, control y orden.
- Usualmente el menor no solicita ayuda y los síntomas pueden no ser egodistónicos.
- A menudo el problema es identificado por los padres.
- Se identifican disminuciones graduales en el desempeño escolar producto de menor capacidad de concentración.
- Usualmente participan en rituales en frente de sus compañeros, maestros o extraños, al igual que los adultos.
- El trastorno puede estar asociado a infección por estreptococos betahemolíticos del grupo A, en algún grupo de niños muy pequeño, y se caracteriza por inicio prepuberal, asociado a anormalidades neurológicas y un comienzo súbito de los síntomas o evolución de los síntomas de forma episódica en concomitancia con infección temporalmente.
- (A) El criterio en los niños puede expresarse mediante un comportamiento desorganizado o agitado.
- B (1) Puede ocurrir juego repetitivo en el que se expresan temas o aspectos del trauma en los niños más pequeños.
- B (2) Puede haber sueños que causen terror sin un contenido identificable.
- B (3) Se puede identificar un patrón de recreación del trauma en niños pequeños.
- Deben evaluarse los síntomas de disminución del interés en las actividades importantes y las limitaciones de afecto del niño por medio de informes de padres, maestros o cuidadores, ya que es difícil identificarlas.
Tabla modificada por los autores del DSM-V.
La utilización de escalas de evaluación validadas brinda una visión más clara de la gravedad de los síntomas y ayuda a guiar la planificación de intervenciones terapéuticas específicas, que, si bien no es una herramienta diagnóstica, permite complementar la evaluación del pediatra por medio de la identificación de puntuación alta en quien se sospecha, lo que
brinda un juicio clínico con validez, pero sin sustituir la entrevista clínica. Dentro de este grupo se encuentran la Escala de Ansiedad
Multidimensional para Niños, La Escala de Ansiedad Preescolar, la Pantalla de Ansiedad Infantil y Trastornos Emocionales Relacionados (SCARED) y la Escala de Ansiedad Infantil de Spence (SCAS) ( Tabla 2).
Álvarez Montañez, Mauricio Guerrero Román, Gennys Gutiérrez Ramírez, Mónica Holguín Barrera, Paula Herrera Revollo
Es esencial evaluar los factores de riesgo y protectores que pueden influir en el desarrollo y la manifestación de la ansiedad en niños y adolescentes.
Los factores de riesgo varían ligeramente según el tipo de trastorno de ansiedad, pero presentan características generales (Figura 3).
Tabla 2. Escalas más usadas para identificación de ansiedad en pediatría
Escalas para identificación de ansiedad en pediatría
Nombre
Escala de Ansiedad
Multidimensional para Niños, MASC2 (1997)
Pantalla de Trastornos relacionados con la ansiedad infantil (SCARED), Birmaher y colaboradores, 1997
Escala de ansiedad para niños de Spence (Spence Children’s Anxiety Scale, SCAS), Spence, 1997
Tabla elaborada por autores.
Aspectos importantes
Evaluar el rango y la gravedad de los síntomas relacionados con los trastornos de ansiedad en jóvenes de 8 a 19 años. Da una puntuación de probabilidad de ansiedad, una escala de trastorno obsesivo compulsivo.
Es adecuada para su aplicación en niños de edades comprendidas generalmente entre los 8 y los 18 años. Se enfoca en varios dominios específicos de la ansiedad y busca identificar la presencia y la gravedad de los síntomas en estas áreas: ansiedad generalizada, fobia específica, fobia social, trastorno de pánico y ansiedad por separación.
La SCAS está destinada a ser utilizada en niños y adolescentes de edades comprendidas entre los 8 y los 15 años. La SCAS evalúa múltiples dimensiones de la ansiedad en niños y adolescentes: ansiedad de separación, ansiedad social, ansiedad por rendimiento y ansiedad general.
Figura 3. Patrones de ansiedad clásica en la niñez y la adolescencia según DSM- V. Imagen modificada por los autores.
6-8 Meses de edad
Timidez/ansiedad con un extraño
DSM -V: Trastorno de ansiedad por separación
12-18 Años de edad
Rechazo de sus compañeros
Miedo a la evaluación negativa
DSM-V: Desorden de ansiedad social
5-7 Años de edad
Miedo a objetos específicos (animales, monstruos, fantasmas)
DSM-V: fobias específicas
Miedo a los gérmenes o a contraer una enfermedad grave
DSM-V: Trastorno obsesivo compulsivo
Miedo a los desastres naturales, miedo a eventos traumáticos
DSM-V: fobias específicas (subtipo ambiental), trastorno de estrés agudo
Patrones de ansiedad clásica en la niñez y adolescencia (DSM-V)
4-5 Años de edad
Miedo a la muerte o a los muertos
DSM-V: trastorno de ansiedad generalizada, ataques de pánico
8-12 Meses de edad
Ansiedad de separación, alteraciones del sueño, ataques de pánico nocturnos, comportamiento opositor.
DSM - V: trastorno de ansiedad por separación/ataques de pánico
8-18 Meses de edad
Trastorno de ansiedad por separación, ataques de pánico
DSM-V: ansiedad por separación, alteraciones del sueño, pánico nocturno
2-3 Años de edad
Llorar, aferrarse, retraerse, congelarse, fugarse, buscar seguridad y contacto físico, evitar estímulos destacados (p. ej., encender la luz), pavor nocturno, enuresis
DSM-V: fobias específicas (subtipo ambiental), trastorno de pánico. Miedos a los animales, fobias específicas (subtipo animal)
El tratamiento resulta ser un desafío por parte del pediatra y su correcto abordaje puede tener repercusiones significativas en el bienestar psicológico y el funcionamiento social y académico a lo largo de la vida.
El objetivo del tratamiento es reducir la ansiedad y el estrés en el niño o adolescente. Por tanto, se necesita un enfoque de tratamiento multidisciplinario y común dirigido a aliviar los síntomas, evitar complicaciones a largo plazo y prevenir el desarrollo de comorbilidad psiquiátrica y de trastornos de ansiedad en la edad adulta. Por tal motivo, se hace necesario que se establezca un plan terapéutico que integre lo siguiente:
• Gravedad de la discapacidad.
• Diagnóstico específico del trastorno de ansiedad.
• Momento de aparición del trastorno (inicio reciente, síntomas de larga duración con empeoramiento progresivo o fluctuante).
• Situaciones en las que aparecen los síntomas (como mientras se desplaza al colegio o mientras duerme).
• Comorbilidades (p. ej., trastorno por déficit de atención con hiperactividad [TDAH], trastorno del espectro autista, trastorno de conducta).
• La edad y el nivel de desarrollo del niño (cuanto más pequeño sea el niño, más intensivas deberían ser las intervenciones de formación de los padres).
• Situaciones sociales, familiares y escolares de niños y jóvenes.
• Características y psicopatología familiares. Sistema de atención de salud disponible y recursos familiares.
• Tratamientos anteriores que han funcionado o fracasado.
Con una comprensión más profunda de los factores subyacentes y los avances en el campo de la psicofarmacología y la psicoterapia, ha surgido
un conjunto diverso de enfoques terapéuticos para abordar esta condición.
La primera línea de tratamiento para los pacientes con ansiedad es la psicoeducación para los niños y sus padres. El papel de los pediatras en atención primaria es muy importante. En primer lugar, es un experto que conoce el entorno de cada niño y desde ese punto de vista puede, por ejemplo, identificar a niños con inhibición conductual y enseñarles estrategias para que se expongan a situaciones nuevas y evitar el miedo, porque se puede hacer prevención primaria. Se enseñan técnicas de afrontamiento centradas en el problema. Los ejemplos incluyen búsqueda activa de información, autodirección positiva, distracción, relajación y detención de los pensamientos negativos.
La terapia cognitivo-conductual (TCC) se ha establecido como el tratamiento de elección para la ansiedad en niños y adolescentes. Es el método de psicoterapia con mayor evidencia científica en ensayos controlados aleatorios para el tratamiento de los trastornos de ansiedad. En esta terapia se examinan las diversas modalidades, que incluyen técnicas de exposición gradual, reestructuración cognitiva y estrategias de manejo del estrés.
Los propósitos de estas intervenciones son enseñar al niño a manejar problemas, fortalecer su confianza en sí mismo, cambiar sus pensamientos negativos y adaptar sus acciones a través de la práctica de nuevas conductas, como técnicas de relajación y respiración, técnicas de estudio, entrenamiento en habilidades sociales, ejercicios de dramatización o role-play, y enfrentamiento gradual a situaciones que generan ansiedad. Además, ayuda a enfatizar en la adaptación a la edad y el desarrollo cognitivo de los pacientes.
Los inhibidores selectivos de la recaptación de serotonina (ISRS) son el tratamiento de elección para el manejo de los trastornos de ansiedad. Aunque no cuentan con la aprobación
de la Administración de Alimentos y Medicamentos (FDA) para tratar la ansiedad, diversos estudios han demostrado su efectividad
y tolerancia. Los ISRS cuya eficacia ha sido demostrada como superior al placebo se presentan en la Figura 4
Figura 4. Factores de riesgos asociados a trastornos de la ansiedad. Modificado de: Figueroa Quintana A, Díez Suárez A. Factores de riesgo de trastornos psiquiátricos en niños y adolescentes. En: Curso de psiquiatría del niño y del adolescente para pediatras; 2020. p. 21-51.
Factores de riesgo
Trastorno de ansiedad
Biológicos
Sexo
Edad
Temperamento
Más frecuente en mujeres. Se aumenta 2 veces a partir de los 6 años, y 3 veces a partir de la adolescencia.
Trastorno de ansiedad por separación y algunas fobias específicas, inicia antes de 12 años. La fobia social empieza al final de la edad escolar y al inicio de la adolescencia.
La inhibición conductual aumenta el riesgo de fobia social. La emocionalidad negativa incrementa el riesgo de fobia social, trastorno de pánico y trastorno de ansiedad generalizada.
Enfermedades
- Infecciones: víricas como mononucleosis infecciosa o por estreptococo, como síndrome pediátrico neuropsiquiátrico de inicio agudo o PANS (pediatric acute onset neuropsychiatric syndrome).
- Psiquiátricas: el diagnóstico de depresión aumenta el riesgo.
Ambientales
Antecedente de aborto, enfermedad grave en el primer año de vida del niño.
- Trauma temprano (aumenta el riesgo de trastorno de pánico, ansiedad generalizada y trastorno de estrés postraumático).
- Abuso (sexual).
- Acoso escolar.
- Catástrofes naturales.
- Padres con psicopatología.
- Estilo educativo hipercontrolador, sobreprotector.
- Disfunción familiar grave.
- Pérdida de uno de los padres.
- Depresión materna.
- Maltrato, negligencia o hipoestimulación.
Nivel educativo o económico bajo.
Perinatales
Estresantes
Familiares
Familiares
Se recomienda que la fluoxetina se tome a partir de los 7 años, la sertralina a partir de los 6 años, la fluvoxamina a partir de los 8 años y el escitalopram a partir de los 12 años. Para los demás no existen estudios suficientes que indiquen cuál es la edad adecuada para comenzar el tratamiento. Además, se ha comprobado que ciertos antidepresivos duales, como la venlafaxina (37,5-150 mg/día), la duloxetina (30-60 mg/día) y la mirtazapina (15-30 mg/día), también son efectivos en el tratamiento de la ansiedad. Sin embargo, se recomienda su uso solo en adolescentes y fuera de las indicaciones técnicas específicas ( Tabla 3).
En relación con los eventos adversos de los ISRS, se observan con mayor frecuencia síntomas gastrointestinales, alteraciones en el ciclo sueño-vigilia, inquietud, cefalea, acatisia, cambios en los hábitos de ingesta de alimentos y problemas sexuales. La venlafaxina puede causar un ligero aumento en la presión arterial, y los niños pueden experimentar un empeoramiento en su comportamiento, mostrando mayor impulsividad.
Respecto al uso de benzodiazepinas, no se ha demostrado que sean más efectivas que el placebo en ensayos clínicos controlados en niños
y adolescentes con trastornos de ansiedad, por lo que no se consideran psicofármacos de primera línea en estos casos. Sin embargo, suelen utilizarse en personas jóvenes con síntomas de ansiedad graves y deben limitarse a situaciones específicas o al inicio del tratamiento con ISRS hasta que surtan efecto. Las benzodiazepinas más utilizadas son las de vida media larga que se encuentran en Colombia, que son diazepam o lorazepam, por su mayor tolerabilidad y menor riesgo de recaída y dependencia, aunque también se puede usar clonazepam ( Tabla 4).
Algunos otros enfoques innovadores y complementarios integran terapias alternativas emergentes. Una de estas es mejor conocida como mindfulness. El entrenamiento en mindfulness ha demostrado ser benéfico en el tratamiento de la ansiedad en niños y adolescentes al promover la conciencia plena del momento presente y fomentar la regulación emocional. Las técnicas de mindfulness, como la meditación guiada, la atención plena al cuerpo y la respiración consciente, pueden ayudar a los niños y adolescentes a desarrollar habilidades de atención y a reducir la reactividad emocional frente a situaciones estresantes. La integración de prácticas de mindfulness en la vida cotidiana puede promover una mayor resiliencia emocional y mejorar el bienestar general (Anexo 1).
Tabla 3. Medicamentos inhibidores selectivos de la recaptación de serotonina (ISRS) para tratamiento de la ansiedad en niños y adolescentes
Inhibidores selectivos de la recaptación de serotonina (ISRS) para el tratamiento de la ansiedad en niños y adolescentes
5-10 mg/día 20
10-20 mg/día cada 7 a 14 días 60-80 mg/día Sertralina 12,5-25 mg/día 50-100 mg/día 25-50 mg/día cada 7 a 14 días 200 mg/día Citalopram 10 mg/día 20-30 mg/día 10 mg/día/semana 40 mg/día Escitalopram 5-10 mg/día 10-20 mg/día 10 mg/día/semana 20 mg
Paroxetina 5 mg/día 20 mg/día 5 mg/día/semana 60 mg
Fluvoxetina 10- 25 mg/día 50-100 mg/día 5 mg/día/semana 300 mg/día, o 15 mg/kg/día
Modificada de: Pérez M, et al. Pediatr Integral. 2022;26(1):40-7.
Tabla 4. Benzodiacepinas para el tratamiento de la ansiedad en niños y adolescentes de utilidad en Colombia
Benzodiacepinas para el tratamiento de la ansiedad en niños y adolescentes Medicamento Dosis inicial Dosis habitual Incremento gradual Dosis máxima
Clonazepam
0,01-0,03 mg/kg/día 0,5 mg (máximo 1,5 mg) cada 8-12 h
0,02-0,1 mg/kg/día 2-4 mg/día 0,25-0,5 mg cada 72 h 6 mg/día
Lorazepam 2,5-5 mg/día cada 6-8-12 h 10-40 mg/día 5 mg 40 mg/día
Diazepam 0,5-1 mg/día cada 8-12 h
0,02-0,1 mg/kg/día 1-5 mg/día 0,25-0,5 mg 20 mg/día
Modificada de: Pérez M, et al. Pediatr Integral. 2022;26(1):40-7.
Anexo 1. Dibujos realizados por adolescentes hospitalizados con trastorno de ansiedad en un pabellón psiquiátrico en Barranquilla, Colombia, al describir lo que sienten. Documentos originales escaneados tomados con permiso de los pacientes.




1. Beesdo K, Knappe S, Pine DS. Anxiety and anxiety disorders in children and adolescents: developmental issues and implications for DSM-V. Psychiatr Clin North Am. 2009;32(3):483-524.
2. Figueroa Quintana A, Díez Suárez A. Factores de riesgo de trastornos psiquiátricos en niños y adolescentes. En: Curso de psiquiatría del niño y del adolescente para pediatras; 2020. p. 21-51.
3. Guerrero F, Sánchez Mascaraque P. Trastornos por ansiedad y trastorno obsesivo-compulsivo en la infancia y la adolescencia. En: Hidalgo Vicario MI, Rodríguez Hernández PJ (editores). I Curso de psiquiatría del niño y del adolescente para pediatras. SEMA; 2019. p. 135-62.
4. Guía de Práctica Clínica para el Manejo de Pacientes con Trastornos de Ansiedad en Atención Primaria [Internet]. Madrid: Plan Nacional para el SNS del MSC, Unidad de Evaluación de Tecnologías Sanitarias; 2008.
5. Instituto Nacional De Salud. Salud mental: asunto de todos [Internet]. INS; 2022. Disponible en: https:// www.minsalud.gov.co/Paginas/Salud-mental-asuntode-todos.aspx
6. Palacio-Ortiz JD, Londoño-Herrera JP, NanclaresMárquez A, Robledo-Rengifo P, Quintero-Cadavid
CP. Psychiatric disorders in children and adolescents during the COVID-19 pandemic. Rev Colomb Psiquiatr (Engl Ed). 2020;49(4):279-288.
7. Pérez M, Sánchez P. Ansiedad en la infancia y adolescencia. Pediatr Integral. 2022;26(1):40-7.
8. Pettitt RM, Brown EA, Delashmitt JC, Pizzo MN. The Management of Anxiety and Depression in Pediatrics. Cureus. 2022;14(10):e30231.
9. Piqueras, JA, Martín-Vivar M, Sandín B, San Luis C, Pineda D. The Revised Child Anxiety and Depression Scale: A systematic review and reliability generalization meta-analysis. Journal of Affective Disorders. 2017:218(15), 153-169.
10. Silver G, Shapiro T, Milrod B. Treatment of anxiety in children and adolescents: using child and adolescent anxiety psychodynamic psychotherapy. Child Adolesc Psychiatr Clin N Am. 2013;22(1):83-96.
11. Wehry AM, Beesdo-Baum K, Hennelly MM, Connolly SD, Strawn JR. Assessment and treatment of anxiety disorders in children and adolescents. Curr Psychiatry Rep. 2015;17(7):52.
Jorge Mario Luján Pinzón, MD1
María Camila Niebles Ramírez, MD2
Mauricio Guerrero Román, MD3
Jaime Plazas Román, MD4
INTRODUCCIÓN
La atención dental preventiva hace parte del seguimiento del niño con el fin de mantener la salud oral, prevenir enfermedades y promover el bienestar físico, emocional y social de nuestros niños. Las temáticas referentes a la salud oral en la población pediátrica no son un tema frecuente a tratar en la literatura médica, ya que se tiene la falsa creencia de que la información referente a esta área debe estar limitada al odontólogo y al odontopediatra; sin embargo, el conocimiento acerca de la salud oral de los niños le concierne a todo aquel que se encuentre involucrado en el seguimiento del infante.
La prevalencia de caries dental ha disminuido desde el siglo pasado; sin embargo, aún representa una de las entidades crónicas que afectan con mayor frecuencia a los niños de todas las edades. En caso de no recibir tratamiento, pueden progresar y provocar enfermedades periodontales y pérdida de piezas dentales, lo que afecta aspectos esenciales de la vida diaria. Algunos de los hábitos más comunes durante la infancia, como la exposición a azúcares desde el embarazo, el uso prolongado del biberón o la succión digital, pueden tener efectos negativos para la salud oral de los niños, por lo cual su identificación debe realizarse de manera oportuna, dado que después de la infancia pueden afectar el crecimiento facial, la relación oclusal y la estética facial.
1. Residente del posgrado de Pediatría, Universidad del Sinú, seccional Cartagena. https://orcid.org/0000-00030147-0808
2. Residente del posgrado de Pediatría, Universidad del Sinú, seccional Cartagena. https://orcid.org/0009-00076944-5859
3. Médico, especialista en Pediatría, miembro de la Sociedad Colombiana de Pediatría. https://orcid.org/00090006-4850-2941
4. Odontólogo y especialista en Odontopediatría y Ortopedia Maxilar, Universidad de Cartagena. Magister en Bioinformática, Universidad Tecnológica de Bolívar. Docente, Universidad de Cartagena y Corporación Universitaria Rafael Núñez. https://orcid.org/0000-0002-5040-6899
La finalidad de la presente revisión es abordar las generalidades de la salud oral en la infancia, el proceso de formación de los dientes y las técnicas para realizar una adecuada higiene oral.
PRINCIPIOS BÁSICOS
SOBRE LOS DIENTES
Para empezar, cabe mencionar que el diente se compone de cuatro tejidos dentales: el esmalte,
la dentina y el cemento, que son tejidos duros, y la pulpa, que se encuentra ubicada en el centro de diente y contiene los nervios, la vasculatura y el tejido conjuntivo. La corona del diente está formada por el esmalte y la dentina, el cuello alberga la cavidad pulpar y la raíz contiene el canal radicular y tejido periodontal (Figura 1).
La dentina constituye el tejido mineralizado de la mayor parte de la estructura dental. Es un tejido conjuntivo vascular atravesado por
Figura 1. Partes del diente.Tomada de: Gómez de Ferraris ME, Campos Muñoz A. Histología, embriología e ingeniería tisular bucodental. 4.a edición. Editorial Médica Panamericana S. A.; 2019.
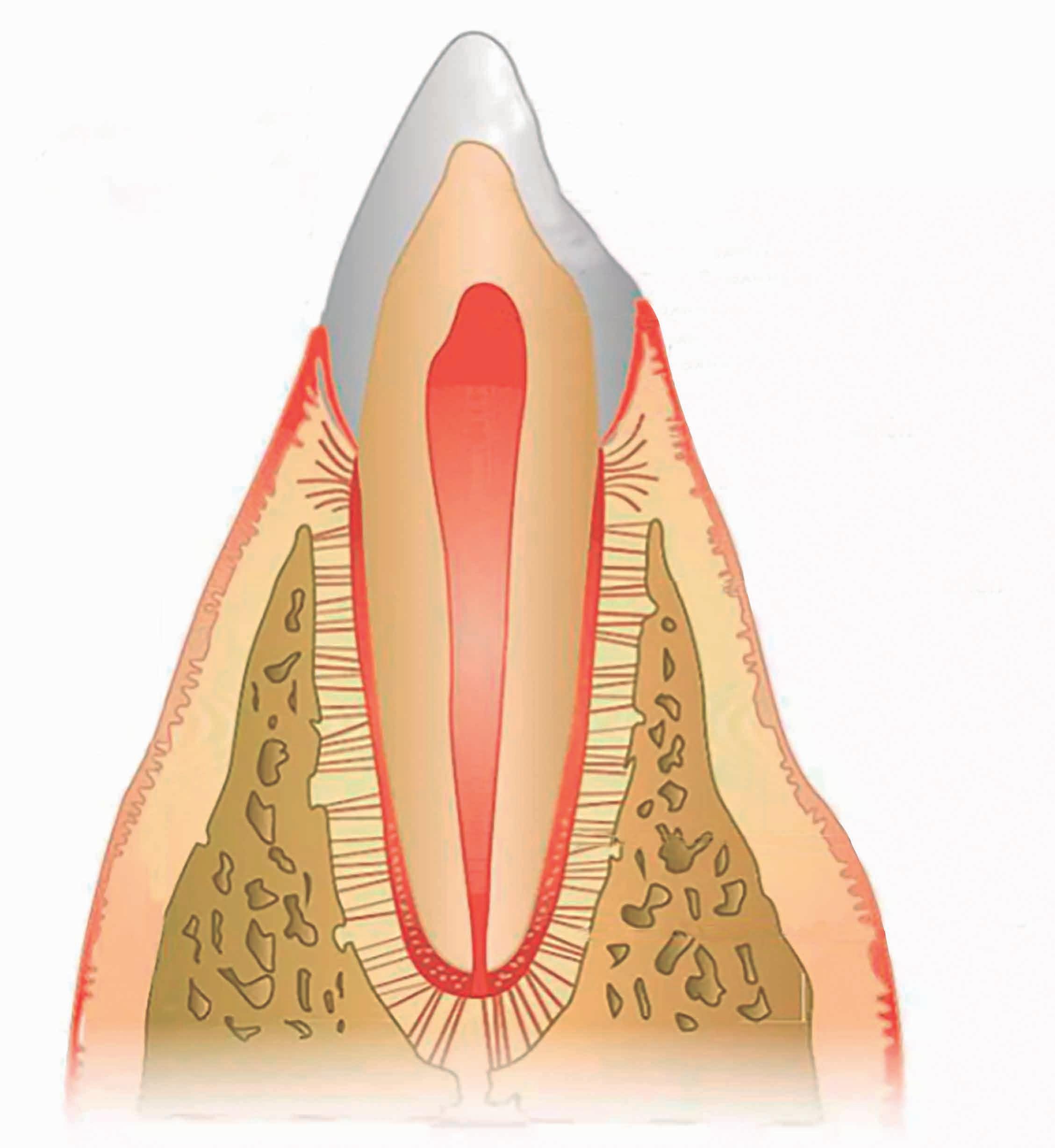
Corona clínica
Corona anatómica
Dentina
Conexión amelodentinaria
Pulpa
Encía
Epitelio de unión Hueso alveolar
Raíz
Cemento
Ligamento periodontal
los túbulos dentales, revestido por el esmalte en su porción coronal y por el cemento en su porción radicular, y por dentro contiene la cámara pulpar.
La pulpa es el tejido blando del diente que contiene los nervios, los vasos sanguíneos y el tejido conectivo; se extiende desde la corona del diente hasta la punta de las raíces y es la zona por la cual se le da vitalidad a la pieza dental. Al ser una zona tan importante, se encuentra cubierta por la dentina y el esmalte, que la protegen frente a amenazas externas. La pulpa tiene diferentes funciones: proporciona el suministro vascular, sustrato de las funciones metabólicas, y el mantenimiento de las células y de la matriz orgánica; tiene una función sensorial, ya que transmite la respuesta nociceptiva y la respuesta propioceptiva del diente, por lo cual es donde se origina el dolor, y también tiene una función protectora, ya que responde a estímulos inflamatorios y antigénicos removiendo sustancias perjudiciales a través de la circulación y el sistema linfático.
El esmalte es la parte externa que recubre el diente y es semitransparente, su función principal es proteger la dentina y la pulpa, y es la primera capa de defensa frente a elementos dañinos o perjudiciales, desde ácidos provenientes de los alimentos hasta el crecimiento de bacterias secundario a inadecuadas técnicas de cepillado.
El cemento es un tejido conectivo mineralizado que recubre las raíces anatómicas de los dientes, comienza en la región cervical del diente al nivel de la unión con el esmalte y continúa hasta el vértice, proporciona el medio para la unión de las fibras que unen al diente con las estructuras periodontales, no tiene capacidad de ser remodelado y es más resistente a la resorción que el hueso, no está vascularizado y carece de inervación.
La formación dental involucra dos capas germinativas principales: el ectodermo, responsable exclusivamente del esmalte, y el ectomesénquima, que origina el complejo dentinopulpar, el cemento, el ligamento periodontal y el hueso alveolar. Además, el hueso alveolar induce la proliferación del epitelio bucal que recubre la boca primitiva del embrión, lo que impulsa tanto la morfogénesis (formación de la corona dental) como la histogénesis (calcificación del diente). La morfogénesis dental se inicia durante la sexta semana de vida intrauterina, cuando las células basales de la membrana basal se adentran en el ectomesénquima, lo que da lugar a dos estructuras clave: la primera es la lámina vestibular, que eventualmente se transforma en el surco vestibular, y la segunda es la lámina dental, que para la octava semana de vida intrauterina forma diez crecimientos epiteliales dentro del ectomesénquima de cada maxilar. Posteriormente, durante el cuarto y quinto mes de vida intrauterina, se forman los gérmenes dentales de los dientes permanentes y comienza su desarrollo.
En el primer estadio, conocido como el estadio de brote o yema, las células basales del epitelio se proliferan para formar dos estructuras que darán origen al órgano del esmalte. En esta etapa, las células periféricas adoptan una forma cúbica, mientras que las células internas presentan una forma poligonal o cilíndrica. Este proceso marca el inicio del desarrollo del esmalte dental y es fundamental para la formación adecuada de los dientes.
En el segundo estadio, conocido como el estadio de casquete , se distinguen dos etapas. La etapa temprana, que ocurre aproximadamente en la novena semana de vida intrauterina, se caracteriza por la formación de una concavidad en la cara profunda del brote, adoptando la apariencia de un casquete, de donde proviene su
denominación. Además, se desarrolla la papila y el saco dentales, lo que marca un hito crucial en la morfogénesis dental.
El tercer estadio, conocido como estadio de campana, se desarrolla entre las 14 y 18 semanas de vida intrauterina. En este se desarrolla la trama vascular destinada a nutrir al órgano del esmalte. Se forma la primera capa de dentina, que constituye el primer tejido dental. Posteriormente, se da lugar al cemento, el ligamento periodontal y el hueso alveolar. Los odontoblastos producen la matriz orgánica de la dentina a partir de fibras colágenas tipo
I y glucosaminoglicanos, lo que contribuye a la formación de la pulpa dental.
En el cuarto estadio, denominado estadio posicional, comienza la deposición de matriz de esmalte sobre las capas de dentina en desarrollo y se observa la desintegración completa de la lámina dental. Durante este estadio ocurre tanto la histogénesis como la dentinogénesis. Cuando el diente erupciona se da lugar al epitelio de unión, formando el surco gingival. Posteriormente, se inicia la formación radicular, que da lugar al agujero apical primario para la erupción dental (Figura 2).
Epitelio bucal

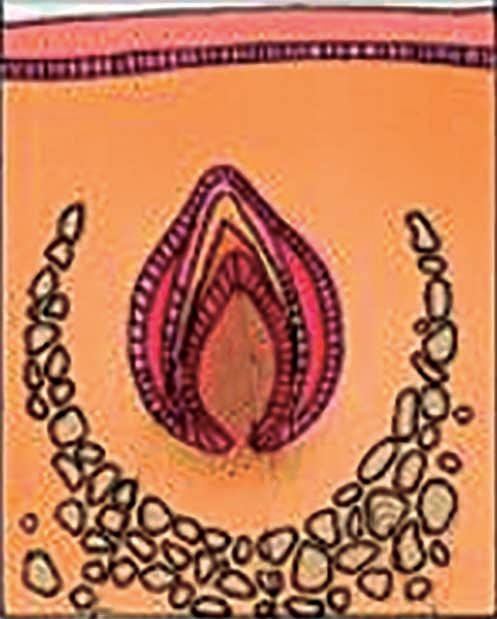
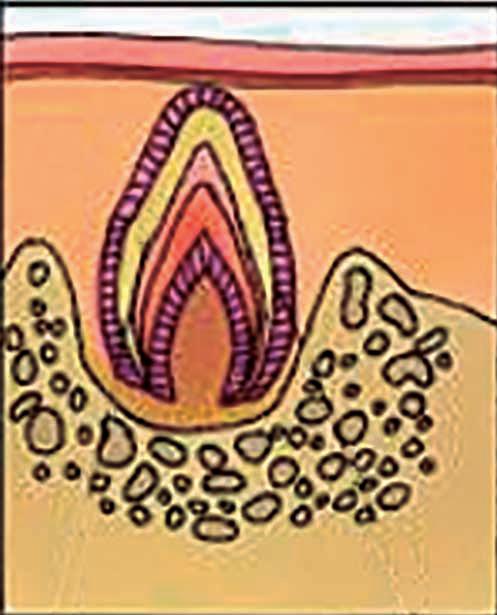
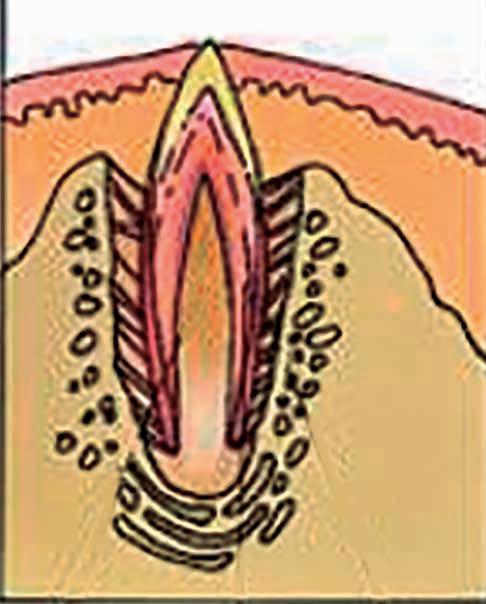
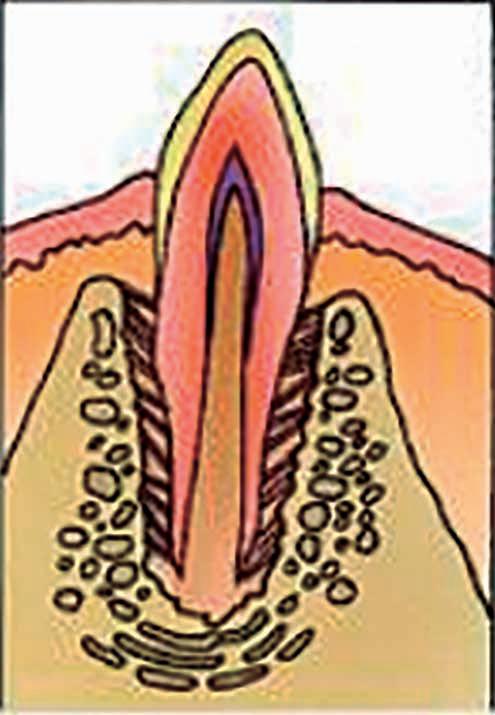
La secuenciación de la erupción dental ( Tabla 1) es el proceso en el que cada diente desarrollado en los maxilares ocupa su posición en la arcada dental, inicia alrededor de los seis meses de edad y culmina cerca de los tres años, momento en el cual el niño debería contar con un total de 20 dientes temporales. Durante el periodo de recambio dental, entre los 6 y los 12 años, esta dentición se exfolia y, a medida que los dientes permanentes reemplazan a los temporales, se observan 28 órganos dentales. Finalmente, la erupción de los terceros molares, también conocidos como muelas del juicio, suele ocurrir entre los 17 y 21 años; en este momento se completa la arcada compuesta por 32 piezas dentales del adulto.
Se distinguen dos tipos de dentición: la primaria (temporal, de decidua o de leche) y la secundaria (permanente):
• Dentición primaria: consta de 20 dientes, incluyendo un incisivo central, un incisivo lateral, un canino, un primer molar y un segundo molar. No se encuentran premolares en la dentición primaria.
• Dentición secundaria: Comprende un total de 32 piezas dentarias, que incluyen incisivos centrales y laterales, caninos, primeros y segundos premolares, primeros y segundos molares, y los terceros molares, también conocidos como muelas del juicio o cordales.
La función principal de cada pieza dentaria es:
• Incisivo: cortar.
• Canino: desgarrar.
• Premolar: desgarrar y triturar.
• Molar: triturar y moler los alimentos.
Es crucial resaltar que a los seis meses los maxilares son pequeños, lo que facilita una oclusión adecuada al momento de la erupción dental; sin embargo, a medida que los maxilares comienzan a crecer, pueden aparecer pequeños
espacios entre los dientes, conocidos como diastemas , especialmente notorios hacia los 3 o 4 años; estos se forman con el fin de compensar la longitud de los dientes permanentes que están por erupcionar. La ausencia de estos espacios puede indicar una patología y debería motivar una consulta con un especialista en odontopediatría.
Tabla 1. Cronología de la erupción primaria y permanente
Segundo premolar 10-11
Primer molar 6*
Segundo molar 12
Tercer molar 17-21
*La erupción y mantenimiento del primer molar controla la correcta ubicación de los demás dientes, evitando malposiciones. Adaptada de: Gómez de Ferraris ME, Campos Muñoz A. Histología, embriología e ingeniería tisular bucodental. 4.a edición. Editorial Médica Panamericana S. A.; 2019.
Se han propuesto diversas teorías para explicar la erupción dental y a continuación se describen las principales:
1. Formación y crecimiento radicular: se plantea que la erupción dental se produce debido al crecimiento y desarrollo de la raíz dental, que, al alargarse y desarrollarse, permite que el diente emerja gradualmente
hacia la superficie oclusal. Sin embargo, investigaciones señalan casos de dientes funcionales sin una raíz dental completa, así como dientes con raíces completas que no erupcionan correctamente según las radiografías. Estos hallazgos han motivado la exploración de otras teorías para comprender mejor los mecanismos implicados en la erupción dental.
2. Aposición de cemento apical: esta teoría sugiere que, además del crecimiento del cemento de la raíz dental, se produce un depósito óseo selectivo y crecimiento del hueso alveolar, lo que ejerce presión sobre el diente. Esta presión facilita el movimiento del diente hacia la superficie oclusal.
3. Presión vascular e hidrostática del conectivo periodontal: se plantea que la presión vascular de los tejidos periapicales genera la erupción del diente hacia arriba a través del hueso alveolar y hacia la cavidad bucal.
4. Tracción del colágeno del ligamento periodontal: esta teoría trata de que las fibras del ligamento periodontal, responsables de conectar el diente al hueso alveolar, generan fuerzas de tracción sobre el diente en proceso de erupción. Estas fuerzas de tracción promueven el movimiento del diente hacia la superficie oclusal.
Estas teorías tienen un factor en común: los movimientos que se deben dar para que el diente se logre ubicar en la arcada dental, los cuales se agrupan en tres grandes categorías, según el momento en que se producen en relación con la posición del diente en el hueso maxilar: preeruptivos, eruptivos y poseruptivos.
Movimientos preeruptivos
En la fase preeruptiva, los dientes en desarrollo se mueven dentro del hueso alveolar antes de que comiencen a erupcionar. Estos movimientos aseguran que los dientes se posicionen adecuadamente en la arcada dental en respuesta al crecimiento de los maxilares y la posición de los dientes vecinos.
• Movimientos de traslación: el diente se desplaza lateralmente dentro del hueso alveolar para alinearse con los dientes adyacentes y adaptarse a los cambios en el desarrollo óseo.
• Movimientos axiales: el diente se mueve en dirección vertical (hacia arriba o hacia abajo) dentro del hueso, lo que le permite adaptarse al crecimiento del hueso y prepararse para la erupción.
Estos movimientos preeruptivos son lentos y sutiles, pero esenciales para la correcta posición del diente en la arcada.
Movimientos eruptivos
Durante la fase eruptiva, el diente se mueve desde su posición dentro del hueso alveolar hacia la cavidad oral, pasando por la encía hasta emerger completamente.
• Movimientos oclusales: el diente se desplaza hacia la cavidad oral en dirección a la superficie oclusal, lo que permite su erupción a través de la encía.
• Movimientos rotacionales: a medida que el diente se mueve hacia la superficie, puede girar o rotar ligeramente para ajustarse mejor dentro del arco dental y alinearse correctamente con los dientes adyacentes.
Estos movimientos son fundamentales para que el diente alcance su posición funcional en la boca y establezca un contacto adecuado con los dientes opuestos.
Movimientos poseruptivos
Una vez que el diente ha erupcionado y alcanzado su posición funcional en la boca, continúan los movimientos poseruptivos. Estos movimientos son ajustes continuos que permiten que el diente se mantenga en su posición y funcione correctamente durante toda la vida.
• Movimientos oclusales: los dientes se desplazan lentamente en dirección oclusal para
compensar el desgaste dental natural, asegurando que se mantenga el contacto oclusal.
• Movimientos de traslación y rotación: son pequeños ajustes laterales y rotacionales para mantener la alineación y la estabilidad del diente en respuesta a los cambios en la estructura ósea o la pérdida de dientes vecinos.
• Movimientos axiales: los dientes pueden desplazarse en dirección vertical para adaptarse a los cambios en la mandíbula y el maxilar, especialmente durante el crecimiento o en respuesta a fuerzas masticatorias.
Estos movimientos poseruptivos son cruciales para preservar la función masticatoria y la estabilidad dental a lo largo del tiempo.
La semiología de la cavidad oral es de gran importancia en la práctica clínica de un pediatra y el uso adecuado de los términos semiológicos
Término
Enfermedad periodontal
Periodontitis
Caries dental
Piorrea
Asialia
Xerostomía
Ptialismo
Sialorrea
Halitosis
Odinofagia
Disfagia
es esencial tanto para lograr un diagnóstico correcto como para que el odontólogo pediatra planifique el tratamiento adecuado, estableciendo una comunicación clara y efectiva. A continuación, se realiza una disertación de los diferentes términos semiológicos asociados a la salud oral ( Tabla 2).
U ODONTOGRAMA
La secuenciación de los dientes, u odontograma, se basa en el método dígito-DOS (Figura 3), aceptado por la Federación Dental Internacional. Utiliza dos cifras: la primera indica el cuadrante y la segunda, el orden del diente dentro de ese cuadrante. Estos dos dígitos deben enumerarse por separado. Es importante tener en cuenta que el orden de los cuadrantes comienza en el sector superior derecho y progresa en sentido horario, desde la perspectiva del odontólogo mirando al paciente.
Tabla 2. Términos semiológicos en salud oral
Significado
Proceso que afecta la encía y los tejidos de soporte de los dientes.
Inflamación que compromete la encía, la membrana periodontal y el hueso alveolar.
Enfermedad infecciosa endógena de los dientes.
Exudado purulento en las encías.
Falta de saliva. Fugaz como en las emociones, o permanente por intoxicación atropínica.
Mucosas secas, acompañadas de dificultad para hablar, masticar y tragar.
Aumento en la cantidad de saliva.
Salida involuntaria de saliva por la boca resbalando por el mentón.
Mal olor del aliento debido fundamentalmente a mala higiene, en otros casos por la presencia de caries.
Dolor al deglutir, frecuente en procesos supraglóticos; es decir, infecciones localizadas en la faringe.
Dificultad para deglutir.
Término
Significado
Gingivorragia Hemorragia por las encías, aparece durante el cepillado de los dientes y se relaciona con la falta de uso de seda dental.
Ageusia Pérdida total del gusto.
Parageusia Percepción diferente de los distintos sabores.
Macroglosia Tamaño excesivamente grande de la lengua, se observa en acromegalia, mixedema y cretinismo.
Microglosia Tamaño pequeño de la lengua. Hipopituitarismo.
Odontalgia Dolor dental.
Macrostomia Tamaño excesivo de la boca. Es una anomalía congénita.
Microstomía Tamaño pequeño de la boca. Se observa en esclerodermia (boca de pescado).
Queilitis Inflamación de la mucosa de los labios.
Macroqueilia Labios grandes. En hipotiroidismo, acromegalia y raza negra.
Retroqueilia Labios dirigidos hacia atrás. Labio hendido. Hendidura del borde libre. Defecto congénito.
Queilopalatosquisis Fisura congénita alveolar o alvéolo palatina del labio superior que hace difícil la deglución. También llamado paladar hendido.
Glosodinia Lengua dolorosa y se manifiesta con la sensación de tensión, plenitud y pesadez. Acompaña con frecuencia la hipovitaminosis B y el déficit de hierro sérico en caso de anemia.
Gingivitis Inflamación de las encías con mucosa edematosa, con exudado y a veces con ulceraciones.
Estomatitis Proceso inflamatorio de los tejidos blandos de la boca, en enfermedades carenciales, metabólicas, endocrinas o infecciosas.
Glositis Inflamación de la lengua, hay sialorrea y rechazo a los condimentos.
Anodoncia Falta parcial o completa de los dientes. Rubeola congénita o retención dental.
Macrodoncia Dientes de tamaño grande. Acromegalia.
Microdoncia Dientes pequeños. En casos de raquitismo e hipopituitarismo.
Criptodoncia Dientes incluidos. Prótesis. Dentadura artificial.
Diastema Separación exagerada entre los incisivos centrales.
Tabla elaborada por los autores.
EXAMEN DE LA CAVIDAD ORAL
Labios
Son la estructura que protege la cavidad oral y se constituyen en su límite externo. Tienen una estructura triple (mucosa, muscular y
cutánea). Su exploración comienza con el cierre de la boca del paciente, la inspección y palpación de los labios, evaluando su simetría, coloración, presencia de edema y posibles anomalías superficiales. La simetría labial puede indicar un desarrollo normal o la presencia de asimetrías relacionadas con patologías
Figura 3. Odontograma. Adaptada de: Merán Gil J, Masgoret Palau E, Ramos Macías A. Semiología y exploración clínica de la cavidad oral y la faringe. En: Libro virtual de formación en otorrinolaringología. SEORL; 2015.
Derecha del paciente
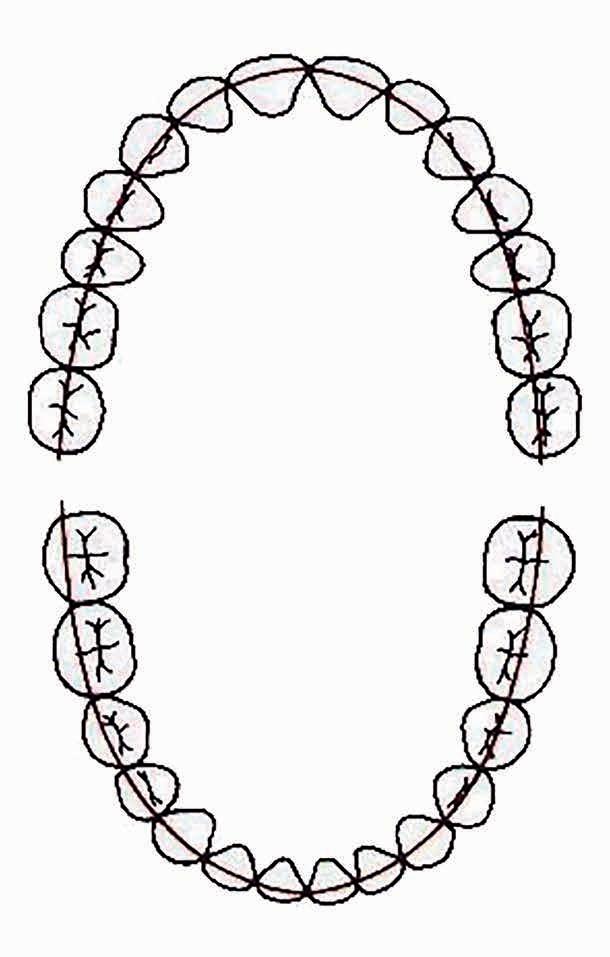
Izquierda del paciente
esencial para detectar signos de condiciones orales y sistémicas como infecciones, reacciones alérgicas o trastornos hematológicos. Esta inspección inicial proporciona información valiosa para la identificación temprana y el manejo adecuado de las condiciones de salud oral en los niños.
Mucosa oral
subyacentes. La coloración normal de los labios es rosada o rojiza, aunque pueden presentar variaciones dependiendo de la pigmentación de la piel del paciente. El edema puede ser indicativo de inflamación, trauma o reacciones alérgicas. Además, la presencia de anomalías en la superficie de los labios, como lesiones, úlceras o cambios en la textura, requiere una evaluación minuciosa para determinar su naturaleza y posible implicación clínica. Esta inspección inicial proporciona información vital para el diagnóstico y manejo adecuados de las condiciones orales del paciente.
Deben evaluarse en el niño con la cara relajada o con expresión neutral. Se busca que sean de color rosado, lisos, suaves, uniformes y simétricos. También se examina la comisura oral, donde se encuentran los labios superior e inferior con la piel facial. Cambios en la coloración, textura o simetría de los labios pueden indicar anomalías subyacentes. La evaluación de los labios es
Es el tejido de la parte interior de la cavidad oral que cubre la mejilla y los labios. El examen clínico debe ser realizado con la apertura parcial de la cavidad oral y con una adecuada fuente de luz, deben tener una consistencia uniforme y ser de color rojizo-rosado, con una superficie suave y húmeda. Una mucosa muy pigmentada puede indicar patología de origen endocrino. La existencia de una mancha roja en la mucosa bucal en la desembocadura del conducto de Stenon se relaciona con parotiditis. Las úlceras aftosas o aftas de la mucosa bucal aparecen en forma de lesiones blanquecinas, redondas u ovales, circundadas por un halo rojo, las cuales son muy molestas para los pacientes y son una de las causas de hiporexia en los niños.
Encías
Son el tejido que se encuentra en el interior de la cavidad oral, recubriendo los procesos alveolares de las mandíbulas y rodeando el cuello de las piezas dentales; su color es rosa, su superficie es generalmente suave y en ellas se debe observar si hay eritema, edema, ulceración, atrofia o sangrado.
Paladar duro y paladar blando
El paladar duro representa los dos tercios anteriores del techo de la boca, los cuales son óseos; esta estructura separa la cavidad nasal de la cavidad bucal. Está compuesto por el premaxilar, los procesos palatinos y el rafe palatino. Su examen se realiza primero mediante la visualización directa y la observación en busca de masas, edema y ulceración; posteriormente,
se procede a realizar la palpación rastreando imperfecciones. Es normal la presencia de una protuberancia de tejido blando que cubre el agujero incisivo, llamada papila incisiva, medial a ella se encuentra el rafe de la línea media y a los lados, posteriormente, se encuentran múltiples crestas onduladas que se irradian a los lados, llamadas rugas palatinas
El paladar blando o el velo del paladar hace referencia al tercio posterior del paladar, de color rojizo-rosado. Se examina mediante visión directa y normalmente no se palpa, a menos que sea necesario verificar la presencia de ulceraciones, engrosamientos, exudados o petequias. Esta estructura ayuda a controlar la deglución y a prevenir la regurgitación de alimentos hacia la cavidad nasal.
Dentro de los hallazgos patológicos que se pueden encontrar en el paladar duro están la fisura palatina (paladar hendido), el paladar ojival y la presencia de tumores. En el paladar blando es anormal la presencia de fisura palatina o leucoplasia del paladar blando.
Úvula
Es un tejido blando de forma cónica que se proyecta en dirección cefalocaudal desde la parte posterior del paladar blando. Se debe evaluar su posición centrada y su forma; es anormal el hallazgo de úvula bífida, edema uvular, quistes o tumores uvulares. La posición de la úvula puede estar desplazada por abscesos periamigdalinos o por parálisis del nervio craneal IX o X (glosofaríngeo o vago).
Lengua
Esta estructura está ligada al piso de la boca y es el órgano muscular de deglución, habla y gusto. Tiene una amplia variedad de funciones dentro las que se encuentran la deglución, la masticación, el habla y el gusto. Su superficie está cubierta de papilas gustativas filiformes, foliadas, fungiformes y caliciformes. Las filiformes son
las más numerosas y se ubican por todo el dorso de la lengua, pero no ofrecen percepción gustativa. Posteriormente, se encuentra un surco en forma de V, que se denomina surco terminal y separa los dos tercios anteriores de la base posterior de la lengua; adicionalmente, se encuentra el agujero ciego. También se puede apreciar la amígdala lingual, que es una masa redondeada de tejido linfoide en la línea media, ubicada en la superficie dorsal de la base de la lengua.
Para realizar una adecuada exploración de la lengua se debe sujetar la punta de la lengua con una gasa, moverla ligeramente hacia fuera y examinar todas sus caras. En la lengua se pueden evidenciar áreas sin papilas, que dan lugar a un patrón de manchas lisas y rojizas rodeadas por un borde blanco elevado conocido como glositis migratoria benigna o lengua geográfica; es necesario buscar placas blanquecinas o amarillentas en la superficie de la lengua que se desprenden con facilidad, puesto que pueden ser indicativas de candidiasis oral, lengua saburral, macroglosia, hiperplasia de las papilas o tumores.
Piso de boca
Es un espacio en forma de U, alineado horizontalmente y ubicado en la región sublingual de la cavidad bucal. Esta región constituye el límite inferior de la cavidad oral. En su parte más anterior, el frenillo lingual conecta los músculos de la lengua con los tejidos gingivales; en el borde medial de la glándula sublingual se encuentra el conducto de Wharton, y en una parte más posterior y justo debajo de la lengua se encuentran los pliegues sublinguales, donde se encuentran las respectivas glándulas sublinguales y sus conductos de drenaje.
Para su adecuada evaluación, se debe examinar mediante visualización directa, así como mediante la palpación bimanual. De forma sencilla, basta con solicitarle al niño que levante su lengua y la mueva de lado a lado, y anotar cualquier desviación o limitación de movimiento.
En cuanto a las patologías que se pueden observar en el piso de la boca, se pueden ver el mucocele, que es la acumulación de moco que bloquea un conducto salival; cuando este se presenta en el piso de la boca se denomina ránula. También se puede ver la formación de cálculos dentro de los conductos salivales, lo que se conoce como sialolitiasis; además, se pueden evidenciar quistes en el conducto de Wharton o signos inflamatorios en los espacios submandibular, sublingual y submentoniano propios de la angina de Ludwig. También se puede ver la presencia de un quiste congénito o quiste dermoide, o la presencia de placas blancas o manchas rojas, conocidas como leucoplasia y eritroplasia, respectivamente.
Frenillo bucal
Es un pliegue fino de tejido blando que va desde la superficie interna de la parte medial del labio superior o inferior hasta la encía del reborde alveolar medio anterior. Puede producir dolor en el pezón de la madre y trauma, dificultad para fijar el bebé en el pecho, alimentación frecuente y succión no coordinada. Esto es importante ya que puede ocasionar que la madre decida interrumpir la lactancia antes de tiempo, aumento de peso lento para el bebé e incluso deshidratación hipernatrémica, así como defectos del habla.
Frenillo lingual
Es un pliegue fino de tejido blando que se extiende desde el piso de la boca hasta la base de la lengua; la principal patología relacionada es la anquiloglosia, que es una anomalía congénita que limita los movimientos de la lengua a causa de la disminución de la longitud del frenillo lingual.
Dientes
Como ya se mencionó, la mayoría de los bebés nacen sin dientes y estos inician su erupción alrededor de los 5 a 7 meses. En la vida se cuenta
con dos denticiones, en los niños se encuentra la dentición primaria o decidua, que consta de 20 piezas dentales y se compone de 8 incisivos, 4 caninos y 8 molares. La muda de los dientes inicia alrededor de los 6 años.
Para una adecuada valoración de los dientes, se deben examinar todos los dientes e identificar el número por el método dígito-DOS, la posición, el color y la oclusión. Los dientes primarios influyen en gran medida al momento de comer y hablar, así como en el crecimiento de los maxilares. La caries dental y la pérdida prematura de los dientes temporales pueden conducir a patologías en la dentición permanente.
Para la evaluación de los dientes se debe prestar atención a las manchas blancas o marrones en el esmalte, el cual puede ser el indicio de la aparición de caries dental, así como también puede ser indicativo de hipoplasia del esmalte dental, y en algunos casos estas manchas también pueden ser indicativas de fluorosis dental. Es importante evaluar la oclusión de la mordida y la relación entre las arcadas dentales; un desalineamiento de los dientes puede indicar maloclusión dental.
Es esencial reconocer que los azúcares libres constituyen la principal causa de caries dental. La sacarosa, un azúcar fácilmente fermentable, perturba el equilibrio oral al adherirse a la superficie dental, lo que facilita la acción de bacterias cariogénicas presentes en la cavidad bucal y altera su composición. Cuando las bacterias de la placa metabolizan los carbohidratos adheridos a la superficie del diente, se producen residuos ácidos, por lo cual disminuye el pH de la cavidad bucal. Esto puede ser amortiguado por la saliva, pero solo hasta un pH por encima de 5,5; cuando el PH es inferior a este valor, empieza la desmineralización del esmalte dental, de la que resulta una textura calcárea, conocida como lesión de mancha blanca, que
sin intervención alguna conlleva a cavitación y aparición de caries.
CON LA CARIES
Múltiples estudios han demostrado que un elevado consumo de azúcares incrementa el riesgo de nuevas lesiones por caries a lo largo de la vida, independientemente del uso de flúor. En 2015, la Organización Mundial de la Salud (OMS) emitió directrices sobre el consumo de azúcar basadas en revisiones sistemáticas, las cuales revelaron una relación dependiente de la dosis entre el consumo de azúcares libres y el desarrollo de enfermedades como la caries dental, así como un mayor riesgo de aumento de peso y desarrollo de diabetes tipo 2. La Asociación Estadounidense del Corazón (AHA) recomienda que menos del 10 % de las calorías diarias provengan de azúcares libres, lo que para un niño de dos a tres años equivale a menos de 25 gramos, aproximadamente la cantidad presente en dos o tres galletas comerciales.
Aunque aún no se ha establecido una relación clara entre la obesidad y la caries en la dentición temporal, sí se ha asociado la obesidad con la caries en la dentición permanente, aunque los estudios al respecto aún no son concluyentes. Se ha intentado vincular el aumento de diferentes medidas antropométricas por encima de los rangos adecuados para la edad con la caries dental; sin embargo, estos estudios todavía no arrojan conclusiones definitivas.
Desde el inicio de la vida intrauterina, el bebé se familiariza con una variedad de sabores debido a la exposición temprana a diversos estímulos sensoriales durante el desarrollo de sus sistemas olfativo y gustativo. Esto se debe a las percepciones que recibe del líquido
amniótico y, más tarde, de la leche materna. Varios estudios han observado cambios en los patrones de respuesta gustativa ante diferentes estímulos, y destacan que los fetos a menudo muestran expresiones de placer durante ecografías obstétricas y aumentan la frecuencia de deglución en respuesta a ciertos sabores como el dulce en comparación con estímulos amargos.
Se ha documentado que el sabor de la leche materna varía según la alimentación materna, lo cual sugiere un posible impacto en las preferencias alimenticias y la selectividad del bebé en el futuro. La literatura sugiere que una mayor variedad de alimentos consumidos por la madre durante el embarazo aumenta la exposición del bebé a diferentes sabores, lo que potencialmente facilita una mayor aceptación de alimentos durante la introducción de la alimentación complementaria.
El uso de fórmulas infantiles se ha asociado con preferencias por sabores dulces, salados y ácidos de los alimentos artificiales; además, se ha relacionado con un aumento en el consumo de carbohidratos y una disminución en el consumo de frutas y verduras. Los niños que comienzan a recibir alimentación artificial antes de los cuatro meses de edad muestran preferencia por una alimentación alta en carbohidratos y una menor aceptación de las frutas y las verduras; este hallazgo sugiere que las preferencias alimenticias podrían estar influenciadas durante la alimentación del niño en los primeros 1000 días de vida.
ARTIFICIALES
Es muy importante aclarar que los términos chupete , biberón y tetina no corresponden al mismo objeto. La tetina o biberón se relaciona con un hábito de succión nutritiva y se asocia a la oferta de algún líquido como leche de fórmula, agua o incluso jugos. En cambio, el chupete hace referencia a una succión no nutritiva. Los
estudios nacionales e internacionales muestran que hay una alta prevalencia del uso de las tetinas artificiales en los lactantes menores de un año, se calcula que aproximadamente el 60 % de las madres se las ofrecen a sus hijos. Es muy importante aclarar que se desaconseja totalmente el uso de chupetes y tetinas, no solamente por la asociación a la interrupción de la lactancia materna exclusiva, sino también porque afectan la funcionalidad del individuo, como se explica a continuación.
• Funciones orales: durante la lactancia exclusiva, las estructuras que se encuentran dentro de la cavidad oral y a sus alrededores realizan una actividad muscular sinérgica y en conjunto para llevar a cabo esta función vital. Por eso se aconseja la oferta exclusiva de leche materna sin otros sólidos o líquidos hasta que el niño cumpla seis meses, ya que, además de suplir de manera adecuada los requerimientos nutricionales del bebé, también hace parte fundamental del desarrollo de las diferentes estructuras orofaciales.
- La succión es uno de los reflejos orales primitivos presentes en los recién nacidos a término. El posicionamiento y la función musculares que se dan para succionar durante la alimentación con biberón o chupete son completamente diferentes a las que ocurren en la alimentación en el seno materno: la succión por el biberón se da por fuerza y no por masaje, como naturalmente ocurre, por lo cual este patrón de alimentación sobrecarga los músculos orofaciales y producen una subsecuente disminución de la musculatura nasal, lo que puede llevar a problemas oclusales y respiratorios en un futuro para el recién nacido; mientras que el uso del chupete se asocia a succiones no nutritivas por largos periodos, lo cual con el tiempo puede llevar a una necesidad de mayor estimulación del reflejo de succión y limita el contacto físico madre-hijo, por lo que puede causar dificultades en el desarrollo de un apego seguro.
- Masticación y deglución: en la lactancia se produce una serie de movimientos musculares coordinados que se resumen en protrusión, restricción, elevación y cierre, y dan lugar al crecimiento armónico de la cara. Estudios han mostrado que la alimentación con biberón se asocia a un crecimiento vertical de la cara; adicionalmente, se ha visto que el uso de biberón por más de un año y el uso de chupete por más de seis meses impactan de manera contraproducente en la función masticatoria.
- Habla: el uso de tetina artificial está relacionado con la producción de algunas dificultades al momento de hablar. Los principales sonidos que se ven afectados son los representados por las letras T, D, N, L, S, Z.
• Dentición:
- Caries: se ha visto que los niños que usan biberón tienen una mayor incidencia de caries que los niños que son alimentados con la lactancia materna exclusiva.
- Maloclusión: en este punto hay evidencia contradictoria; sin embargo, algunos estudios apuntan a que el uso del biberón se asocia a una mordida cruzada posterior y mordida abierta anterior, aunque sin demostrar una relación estadísticamente significativa.
• Otitis media grave: se ha descrito que principalmente el uso del chupete es un factor de riesgo para la ocurrencia de otitis media aguda; se ha descrito hasta un riesgo 1,8 veces mayor por el uso del chupete.
• Inteligencia: se ha visto una asociación entre un menor coeficiente intelectual y el uso de chupetes en comparación con los bebés que recibieron lactancia materna exclusiva; algunos autores lo atribuyen a un menor estímulo social y ambiental.
• Vicios orales en la adultez: se ha visto que el uso de chupete más allá de los dos años se relaciona con hábitos como el cigarrillo, teniendo un importante componente ansiolítico en esta conducta.
O UN CHUPETE?
Es un tema muy controversial, lo cierto es que el retiro de un chupete no es para nada fácil, ya que el bebé cuenta con una necesidad neural de succión, que generalmente se satisface con el uso de un chupete, por lo cual los bebés pueden desarrollar algunos hábitos después de la remoción de los chupetes para suplir sus necesidades.
La succión del dedo comienza en la vida intrauterina alrededor de las 18-24 semanas de gestación; este acto prepara a los músculos orofaciales para la futura lactancia materna al momento del nacimiento, por lo cual puede ser considerada fisiológica y o benéfica para el bebé especialmente durante los primeros seis meses de vida.
RECOMENDACIONES EN SALUD E HIGIENE BUCAL
Cuidado dental
La preservación de una salud oral adecuada y el control de las enfermedades dentales son fundamentales para mantener el bienestar de la mujer durante el embarazo y su calidad de vida. Por tanto, la atención en salud oral y sus procedimientos son de suma importancia en la rutina de cuidado materno. Es crucial promover la adopción de hábitos saludables respaldados por la evidencia disponible. Además, es importante destacar que algunas enfermedades, como la periodontitis, se han vinculado con el parto prematuro. Aunque la caries dental también se ha relacionado con el parto prematuro, la evidencia más sólida apunta hacia la periodontitis.
La madre debe incorporar en su rutina de higiene oral el cepillado con pasta fluorada al menos dos veces al día, el uso diario de hilo dental, la reducción de la carga bacteriana mediante enjuagues de clorhexidina o el consumo de
chicles con xilitol, y una dieta equilibrada que limite el consumo de azúcares entre comidas.
La educación y el nivel socioeconómico también desempeñan un papel crucial en el desarrollo de enfermedades bucales en la infancia, como las caries. Factores sociales y ambientales, como el nivel educativo de los padres, el entorno socioeconómico, los hábitos alimenticios familiares, la higiene oral insuficiente y la falta de controles dentales regulares influyen directamente en la salud bucal de los niños. Por tanto, es fundamental implementar programas preventivos y educativos para fomentar una vida libre de enfermedades bucales desde una edad temprana.
Para lograr una óptima salud oral, es esencial centrarse en cambios en el estilo de vida, así como en el conocimiento, las actitudes y el comportamiento relacionados con la salud bucal. Por ello, el embarazo representa un momento clave para iniciar la educación del paciente, ya que muchas mujeres embarazadas desconocen las medidas preventivas para mantener una buena salud oral. Es más efectivo adoptar buenos hábitos antes del nacimiento del bebé que intentar cambiarlos una vez que el bebé ha nacido.
El uso de crema dental con flúor, adecuada al nivel de riesgo de caries de cada persona, representa un gran beneficio en el cepillado dental para mejorar la salud bucal de los niños. El odontopediatra es el experto idóneo para evaluar el riesgo de caries de cada paciente y recomendar la crema dental más apropiada. Es factible influir en los padres para que adopten e implementen estos hábitos dentales positivos. Al educar sobre la importancia del flúor y su impacto en la prevención de caries, se promueve una mejor salud bucal desde la infancia. Además, al adaptar el tipo de pasta dental al riesgo de caries específico de cada niño, se personaliza el cuidado dental y se optimizan los resultados.
Este enfoque integral, con la orientación del odontopediatra, garantiza una sonrisa sana y radiante para los menores.
Higiene bucal del bebé sin dientes
La higiene bucal desde los primeros meses de vida es esencial para el bienestar y desarrollo saludable de un bebé. Aunque aún no hayan brotado los dientes, es crucial mantener la boca limpia para prevenir la acumulación de bacterias y evitar posibles problemas dentales en el futuro. Se recomienda limpiar suavemente la mucosa bucal del bebé después de cada toma de líquidos, utilizando una gasa humedecida. Este hábito ayuda a eliminar los residuos de alimentos y la placa bacteriana, lo que contribuye a una salud oral óptima. Además, es importante fomentar este cuidado desde temprana edad para que el bebé se acostumbre a la rutina de higiene bucal y pueda disfrutar de una sonrisa saludable en su etapa adulta.
Higiene bucal del bebé con dientes
Una vez que los dientes del bebé comienzan a erupcionar, es fundamental establecer una rutina de higiene oral adecuada. Se recomienda el uso de un dedal de silicona o un cepillo dental infantil con cerdas extremadamente suaves y cabezales de goma para hacer del cepillado una experiencia menos dolorosa. Esta limpieza debe llevarse a cabo dos veces al día, por la mañana y por la noche, ya que durante la siesta aumenta el riesgo de caries debido a la disminución de la cantidad de saliva en la boca. Además, los padres deben introducir el uso de hilo dental tan pronto como haya contacto entre los dientes o los molares. Para facilitar este proceso, pueden emplear los portahílo, dispositivos diseñados específicamente para facilitar el uso del hilo dental y mejorar su manejo. Es esencial establecer estas prácticas de higiene oral desde una edad temprana para promover la salud bucal a lo largo de la vida del niño y prevenir enfermedades dentales futuras.
La atención y el cuidado dental adecuados desde la infancia sientan las bases para una salud oral óptima en el futuro. En la Tabla 3 se presentan cinco pasos para un correcto cepillado dental del bebé por parte de los padres.
Tabla 3. Cinco pasos para un correcto cepillado dental del bebé por parte de los padres
1. Controlar y supervisar la motricidad del cepillado del niño y la cantidad de pasta dental, de acuerdo con el nivel de riesgo de padecer lesiones cariosas.
2. El abordaje final del cepillado debe ser realizado por los padres.
3. Comenzar siempre por el mismo lado y realizar el mismo recorrido.
4. Limpiar todas las superficies externas, internas y masticatorias.
5. Cepillar la lengua y los carrillos suavemente.
Adaptada de: Cardoso AR. Odontol Activa Rev Cient. 2020;5(2):21-26.
¿Qué cantidad de pasta dental es suficiente?
Desde la salida del primer diente se debe realizar el cepillado con pastas dentales con flúor. Se debe realizar el cepillado de los dientes mínimo dos veces, aunque lo recomendable es tres veces al día con una adecuada técnica de cepillado. Se recomienda realizar el lavado de dientes en niños menores de 3 años con una pasta dental que tenga una concentración de flúor de alrededor de 500 partes por millón (ppm), mientras que para niños mayores de tres años se puede utilizar una pasta dental con una concentración de flúor entre 1000 y 1450 ppm. Los autores del Grupo Cochrane de Salud Oral realizaron en 2018 una revisión de 96 estudios publicados entre 1955 y 2014 sobre la comparación de los efectos de la crema dental fluorada de 450-2400 ppm, y concluyeron que la crema dental que contiene 1000-1250 ppm de flúor es más efectiva que la crema dental no fluorada. Para las otras concentraciones
de la crema dental comparadas entre sí o con la crema dental no fluorada, hay muy pocos estudios que además cuentan con muy pocos
1. Abanto J, Duarte D, Feres M. Primeros mil días del bebé y salud bucal. 1. a edición. Napole ão Quintessence; 2020.
2. Alvear MC. Recomendaciones en nutrición, dieta y salud bucal para los niños. Odontol Activa Rev Cient. 2016;1(1):76-79.
3. Alzate García F, Serrano Vargas L, Cortes López L, Torres EA, Rodríguez MJ. Cronología y secuencia de erupción en el primer periodo transicional. Rev CES Odont. 2016;29(1):57-69.
4. Avila WM, Pordeus IA, Paiva SM, Martins CC. Breast and Bottle Feeding as Risk Factors for Dental Caries: A Systematic Review and Meta-Analysis. PLoS One. 2015;10(11):e0142922.
5. Cardoso AR. Recomendaciones sobre salud bucal en infantes y preescolares. Revisión de literatura. Odontol Activa Rev Cient. 2020;5(2):21-26.
6. de la Luz Ayala C. Los pediatras en la prevención de enfermedades bucales. Arch Pediatr Urug. 2016;87(3):257-62.
7. Dye BA, Thornton-Evans G, Li X, Iafolla TJ. Dental caries and sealant prevalence in children and adolescents in the United States, 2011-2012. NCHS Data Brief. 2015;(191):1-8.
participantes para lograr claridad acerca de los efectos, por lo que se recomienda una concentración de 1000-1250 ppm de flúor.
8. Gartner LP. Texto de histología. Atlas a color. 5.a edición. Elsevier; 2021.
9. Gómez de Ferraris ME, Campos Muñoz A. Histología, embriología e ingeniería tisular bucodental. 4.a edición. Editorial Médica Panamericana S. A.; 2019.
10. Ibáñez Ng. Propedéutica y Semiología en Odontología. Barcelona, España: Elsevier; 2021.
11. Lin M, Griffin SO, Gooch BF, Espinoza L, Wei L, Li CH, et al. Oral Health Surveillance Report: Trends in Dental Caries and Sealants, Tooth Retention, and Edentulism, United States, 1999–2004 to 2011–2016. Atlanta, GA: Centers for Disease Control and Prevention, US Dept of Health and Human Services; 2019.
12. Mena Tudela D, Sánchez Reolid J. Uso del chupete y efectos sobre la salud: una revisión de la literatura. Rev ROL Enferm. 2019;42(2):34-42.
13. Merán Gil J, Masgoret Palau E, Ramos Macías A. Semiología y exploración clínica de la cavidad oral y la faringe. En: Libro virtual de formación en otorrinolaringología. SEORL; 2015.
14. Walsh T, Worthington HV, Glenny A, Marinho VCC, Jeroncic A. Fluoride toothpastes of different concentrations for preventing dental caries. Cochrane Database Syst Rev. 2019;3(3):CD007868.
1. La principal razón por la cual en nuestro medio no se realizaba la circuncisión antes de las 60 semanas posconcepción era porque:
a. La circuncisión nunca se necesita antes de esa edad.
b. El riesgo de apnea posoperatoria existe hasta la edad mencionada y, por tanto, ningún procedimiento que implique anestesia general debe hacerse antes, a menos que la situación esté amenazando la vida o un órgano.
c. La circuncisión es una mutilación y nunca debe hacerse.
d. La sensibilidad del pene no está preservada antes de esa edad.
e. En ningún país del mundo la realizan en recién nacidos.
2. A propósito del prepucio, cuál de las siguientes afirmaciones es cierta:
a. El prepucio no tiene ninguna utilidad diferente a ser circuncidado.
b. El prepucio debe retraerse completamente para el aseo desde los primeros días de vida, independiente de si se presentan heridas en su retracción, para poder mantenerlo limpio.
c. El prepucio se tiene que retirar completamente en todas las técnicas de circuncisión para que quede bien realizada.
d. El prepucio no resecado era la marca con la cual los primeros cristianos se identificaban.
e. En los animales es evidente que las madres no manipulan el prepucio y este tiene una evolución natural, cumpliendo su papel de proteger el pene.
3. La circuncisión de mínima manipulación se refiere a:
a. NO hacer nada con el prepucio para evitar problemas de fimosis.
b. Practicar la circuncisión con un dispositivo desechable que facilita la técnica y se puede hacer con anestesia local mientras el bebé sea fácil de sujetar o con sedación si es de mayor edad.
c. A cualquier edad los efectos adversos son igual de frecuentes.
d. NO es necesario colocar ninguna anestesia porque los niños no tienen receptores de dolor.
e. La inflamación depende de la técnica y no aumenta cuanto mayor sea el niño.
4. En la discusión ética de la circuncisión infantil frente a la edad de autodeterminación está claro que:
a. Los argumentos de quienes están en contra de la circuncisión infantil suelen estar apoyados por estadísticas de alto peso generadas por estudios de alta calidad.
b. La analogía con la vacunación muestra que la prevención de infecciones urinarias en la infancia NO ha podido demostrarse, como sí se ha logrado con vacunas como la influenza.
c. Las complicaciones de la circuncisión infantil superan por mucho sus beneficios.
d. La Academia Estadounidense de Pediatría cree que NO deben hacerse las circuncisiones infantiles y los médicos deberían convencer a los padres de estos niños de no hacer la intervención.
e. Los padres que deseen la circuncisión infantil para sus hijos pueden acceder a ella y sus hijos tienen beneficios como la prevención de infección urinaria, la reducción de las balanitis, la prevención de infecciones de transmisión sexual y menor incidencia de algunos tipos de cáncer del tracto urinario y genital tanto en la población de circuncidados como en sus parejas masculinas o femeninas.
5. ¿Qué tan frecuente es la presentación sintomática de la infección congénita por citomegalovirus al nacimiento?
a. 20 %.
b. 10 %.
c. 33 %.
d. 5 %.
6. ¿En qué trimestre del embarazo ocurre la mayor transmisión vertical de citomegalovirus?
a. Primero.
b. Segundo.
c. Tercero.
d. Todos por igual.
7. ¿A partir de qué edad posnatal se logra diferenciar entre la infección congénita y la adquirida por citomegalovirus?
a. 7 días.
b. 2-3 semanas.
c. 12 semanas.
d. 6 meses.
8. ¿Qué grupo de recién nacidos debería recibir tratamiento para la infección por citomegalovirus?
a. Menores de 32 semanas con síntomas moderados a graves de enfermedad congénita por citomegalovirus.
b. Todos los recién nacidos.
c. Ningún recién nacido debe recibir tratamiento.
d. Mayores de 32 semanas con síntomas de moderados a graves.
9. ¿Cuál patología autoinmune está asociada mayoritariamente al síndrome de monocito macrófago activado?
a. Lupus eritematoso sistémico.
b. Artritis idiopática juvenil.
c. Dermatomiositis juvenil.
d. Fiebre reumática.
10. ¿Cuál es el signo clínico más común o que se presenta con mayor frecuencia en el síndrome de monocito macrófago activado?
a. La fiebre alta.
b. La febrícula persistente.
c. La esplenomegalia.
d. Las linfadenopatías.
11. ¿Cuál es el biomarcador que mayor eficacia ha mostrado para el seguimiento del síndrome de monocito activado?
a. La medición del receptor soluble de IL-2 alfa
b. Ferritina sérica.
c. La proteína C-reactiva.
d. La lactato-deshidrogenasa.
12. ¿Cuál es el tratamiento más apropiado para el paciente con síndrome de monocito macrófago activado?
a. Inicio temprano de antibióticos (primeras horas) y el control de la temperatura con antipiréticos.
b. Los antirretrovirales han demostrado algún papel si se inician temprano.
c. Tratar la causa subyacente y la inmunomodulación del sistema inmune.
d. Dosis altas de esteroides (pulsos)
13. ¿Cuál(es) es(son) el(los) trastorno(s) mental(es) más frecuente(s) en la adolescencia en Colombia de acuerdo con el último boletín de salud mental?
a. Separación en la niñez y apego
b. Fobia social y ataque de pánico
c. Trastorno de ansiedad y fobia social
d. Ansiedad por consumo de sustancias psicoactivas
e. Agorafobia
14. ¿Qué sistema es el responsable de preparar a los órganos al reconocer alarmas de estímulos externos?
a. Sistema osteomuscular
b. Eje hipotálamo-hipófisis-suprarrenal
c. Hormonas adrenérgicas
d. Sistema nervioso autónomo simpático
e. Sistema parasimpático
15. Las siguientes sustancias participan en la génesis de la ansiedad, excepto:
a. Leptina
b. Cortisol
c. Serotonina
d. neurotransmisores
e. Adrenalina
16. La edad promedio en la que clínicamente se desencadena el trastorno de ansiedad social mediante el desarrollo de conductas evitativas sociales es:
a. 10-18 años.
b. 8 años.
c. 13 años.
d. 3-6 años.
e. 2 años.
17.¿Qué tejido dental protege al diente frente a amenazas externas?
a. Cemento.
b. Esmalte.
c. Pulpa.
d. Dentina.
18.¿A qué edad ocurre la erupción del incisivo central inferior en la dentición primaria?
a. 9 meses.
b. 7 meses.
c. 12 meses.
d. 6 meses.
19. ¿Qué concentración de flúor se recomienda en la pasta dental para niños menores de 3 años?
a. 1000-1450 ppm.
b. 500 ppm.
c. 2000 ppm.
d. 750 ppm.
20. ¿Qué concentración de flúor es recomendada para niños mayores de 3 años?
a. 1000-1450 ppm.
b. 500 ppm.
c. 750 ppm.
d. 2400 ppm.



